-
抗生素被广泛应用于医疗和畜牧业,其可随人类或动物的尿液或粪便排出,进入土壤、地表水、市政管网及污水处理设施,甚至地下水中[1]. 抗生素不仅具有一定的毒性,还会诱导微生物产生抗性基因. 因此,会造成生态环境和健康风险[2].
目前,处理抗生素废水的传统方法包括吸附法、臭氧氧化、电化学氧化以及生物法等[3]. 近年来,生物电化学系统(Bioelectrochemical systems, BES) 也被用于降解抗生素. 例如,Chen[4]等在MFC中,利用石墨烯修饰生物电极来降解土霉素,8 d后降解率达95%[5]. Liang[6]等报道,改良的BES在24 h内对氯霉素的去除率达96%. Wu[7]等报道,在基于碳棒和泡沫铜电极的BES中,可在36 h内对CAP(初始浓度为32 mg·L−1)完全去除. 然而,在BES中,难降解有机物在降解过程中产生的一些有毒且难以矿化中间体,使微生物活性降低. 为解决该问题,有研究者将BES与人工湿地[8]或光催化技术耦合起来以强化污染物的矿化. 其中,BES与光催化过程耦合,既可提高污染物的矿化效率,又可提高能源回收[9-10],因而备受关注. 本课题组前期的研究工作证实,通过构建基于生物阳极和光电阴极的生物光电化学系统(Biophotoelectro- chemical system, BPES)可促进染料、2,4-二氯苯酚以及抗生素的降解[10-13]. 然而,BPES中高效光电极材料的研发以及抗生素降解过程机理仍需进一步深入研究.
在BPES中,光电极的催化性能对体系降解污染物的影响很大,因此,设计和构筑性能优异的光催化剂至关重要. 溴氧化铋(BiOBr)是一种层状半导体,因其独特的电子结构、适中的能带位置和良好的光学特性而受关注[14]. 但是,BiOBr的禁带宽度较宽 (Eg≈2.90 eV),且其光生电子空穴对极易复合,导致光催化效率较低[15]. 研究表明,通过金属离子Cu掺杂可提高催化剂的光催化活性[16]. 因此,本文的研究目的是通过Cu离子掺杂优化BiOBr光阴极,分析其理化性质和光电化学特性,并将其与生物阳极耦合构建BPES,考察其对盐酸四环素(TC)、磺胺甲恶唑(SMX)和阿莫西林(AMX)的降解性能. 此外,考察不同操作条件对BPES降解抗生素性能的影响,推断AMX的降解路径,并解析BPES生物阳极上微生物群落结构的演变规律,为BPES处理抗生素废水提供一定的理论依据.
-
实验使用的试剂主要包括Bi(NO3)3·5H2O、Cu(NO3)2·3H2O、KBr、KH2PO4、甲醇(色谱纯)、乙腈(色谱纯)、Nafion、无水乙酸钠、TC、SMX和AMX等.
-
Cu掺杂的BiOBr通过溶剂热法制备. 首先分别将0.05、0.15 、0.25 mmol的Cu(NO3)2·3H2O溶解到80 mL的乙二醇溶液中,经充分搅拌溶解后向其中加入5 mmol的 Bi(NO3)3·5H2O 和5 mmol的KBr,剧烈搅拌1 h,随后超声分散20 min,形成均匀的悬浮液. 将得到的混合悬浮液分别转移到100 mL聚四氟乙烯内衬的反应釜中,在160 ℃下加热12 h,随后样品60 ℃下烘12 h,所得样品分别命名为5-Cu-BiOBr、15-Cu-BiOBr、25-Cu-BiOBr. BiOBr的制备同上. 光阴极材料由催化剂通过涂覆法负载在泡沫镍基底上得到. 首先将泡沫镍(5 cm×3 cm)浸没于硫酸(1 mol·L−1)和无水乙醇混合液中超声清洗30 min,再用去离子水多次冲洗,自然干燥备用;然后分别将60 mg的上述光催化剂加入到0.3 mL异丙醇和0.6 mL Nafion的混合溶液中,经超声混合后将悬浮液均匀涂在泡沫镍上,自然干燥备用.
通过扫描电子显微镜(SEM, Hitachi S-SU8020)及透射电镜(TEM)和高分辨率透射电镜(HR-TEM)(FEI Tecnai G2 F30)来观察光电极材料的微观形貌结构. 用X射线光电子能谱(XPS, ESCALAB 250XI+)分析光电极的化学成分. 采用傅里叶变换红外光谱(FT-IR, IRTracer-100)分析化学键. 利用UV-vis漫反射光谱(UV-vis DRS, UV-2600)检测其光吸收特性,并利用光致发光光谱(PL, ZLX-PL-I)分析光生载流子的分离效率. 此外,采用光电化学工作站(荷兰,Metrohm-Autolab,PGSTAT302N)三电极体系测试光阴极的光电化学性能,包括电化学阻抗谱(EIS), 线性扫描伏安曲线(LSV)和循环伏安曲线(CV)等测试,具体体系及操作参数与本课题组前期报道相同[12].
-
BPES反应器为石英玻璃单室瓶式反应器(设置2个平行反应器),有效容积为160 mL(直径为6 cm,高度为8 cm). 碳刷阳极的长度为4.0 cm,直径为2.5 cm. 以制备的BiOBr及Cu-BiOBr光电极为阴极,两电极(间距约2 cm)平行放置在BPES中,外接10 Ω电阻. 选用南宁市琅东污水处理厂的生活污水进行接种,在0.6 V外加电压下驯化挂膜. BPES的基质主要成分为(以1 L基质计):1.0 g无水乙酸钠,100 mL PBS缓冲液,2.5 mL微量元素溶液,0.2 mL维他命溶液,873.2 mL去离子水. 挂膜成功后,向上述基质中添加一定浓度(5 mg·L−1)的TC、SMX、AMX,驯化阳极微生物使之适应抗生素废水. 采用多通路电压数据采集器 (Model M2700, module M7708, Keithley Instruments,美国)采集电阻两端的电压. 采用300W的氙灯(λ >420 nm)作为可见光光源.
-
TC浓度采用紫外分光光度计测定,波长265 nm. SMX与AMX的浓度通过高效液相色谱仪(HPLC-20AD,岛津)测定,采用C18色谱柱(5 μm,4.6 mm×150 mm),SMX的流动相比例为10%甲醇/90%超纯水,流速为0.8 mL·min−1,检测波长为277 nm;AMX的流动相比例为2.5%甲醇/97.5% 5 mmol·L−1磷酸二氢钾,流速为1.0 mL·min−1,检测波长254 nm. 采用Waters Xevo G2-XS QTOF 液质联用仪(Waters ACQUITY UPLC BEH C18柱,1.7 μm)对AMX降解的中间产物进行鉴定,柱温为40 ℃,流动相比例为0.1%甲酸水/乙腈=95/5,流速为0.3 mL·min−1,进样量为2 μL.
-
从图1a-d可看出,Cu-BiOBr和BiOBr均为规整、均匀的层状纳米片组成的花瓣球体,且Cu掺杂减小了花瓣球体的直径(Cu-BiOBr 3 µm vs. BiOBr 6 µm),使材料比表面积及总孔体积均有所增加. Cu-BiOBr的TEM图中的晶格条纹间距0.282 nm、0.277 nm与0.229 nm分别对应{102}、{110}和{112}晶面,与标准卡片 (PDF#85-0862)相符合 (图1e-f),说明Cu-BiOBr的成功合成.
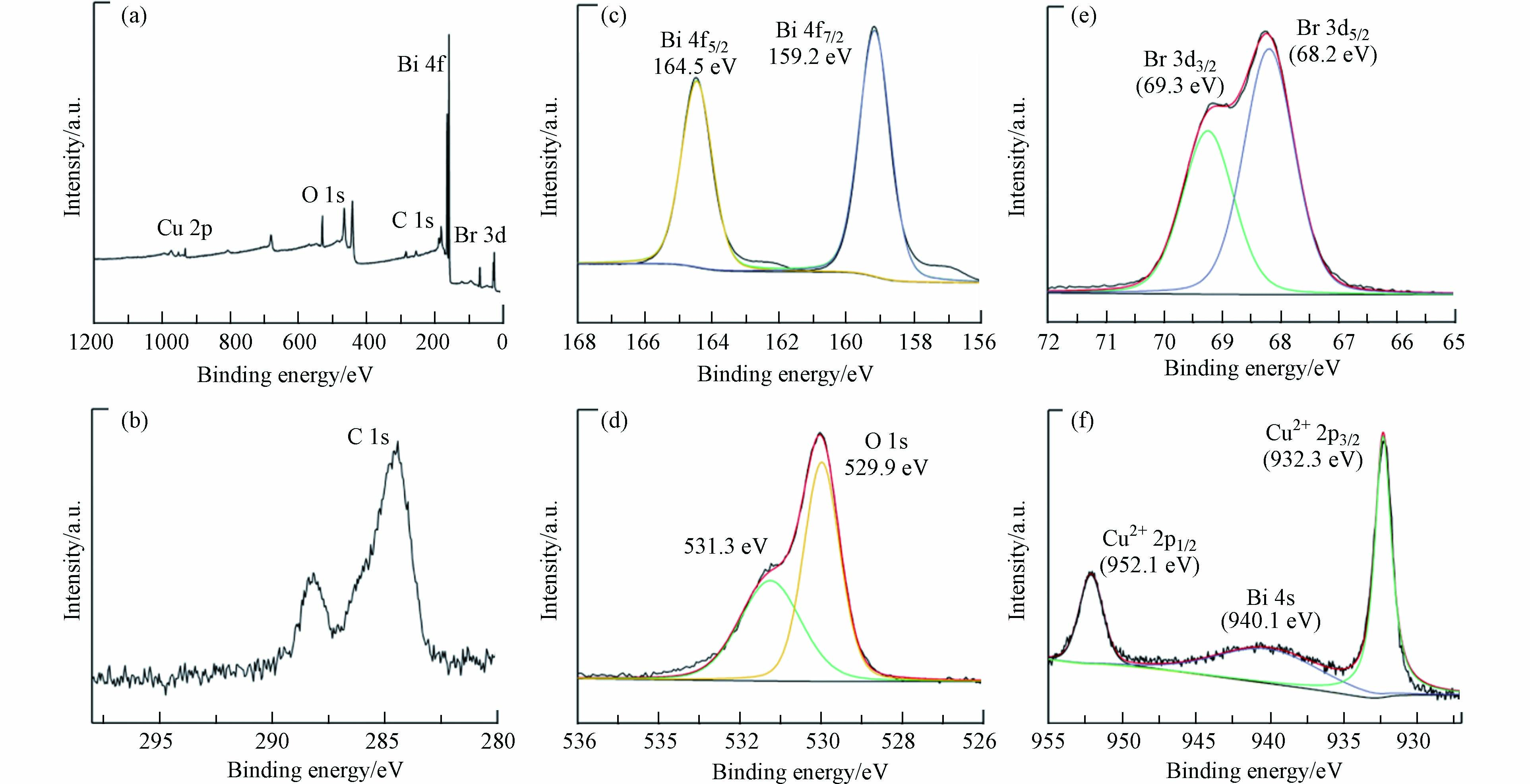
XPS全扫描光谱(图2a)可看出,15-Cu-BiOBr主要由C、Bi、O、Br和Cu组成. 结合能位于69.3 eV,68.2 eV处的峰对应着Br 3d3/2与Br 3d5/2,验证了BiOBr中Br的存在. Bi3+的结合能位于164.5 eV与159.2 eV处的峰对应着Bi 4f5/2 和Bi 4f5/2,说明Bi3+的存在. 而O 1s 的531.3 eV与529.9 eV的结合能峰值分别属于晶格氧 (O2-)与H2O的特征峰[17]. 对于Cu-BiOBr,结合能峰位于932.3 eV (Cu 2p3/2)和952.1 eV (Cu 2p1/2),表明Cu2+的存在. 结合能940.1 eV处的峰出现,可能是Bi 4s的峰,也可认为该峰与Cu 2p处的轨道峰发生重叠[18].
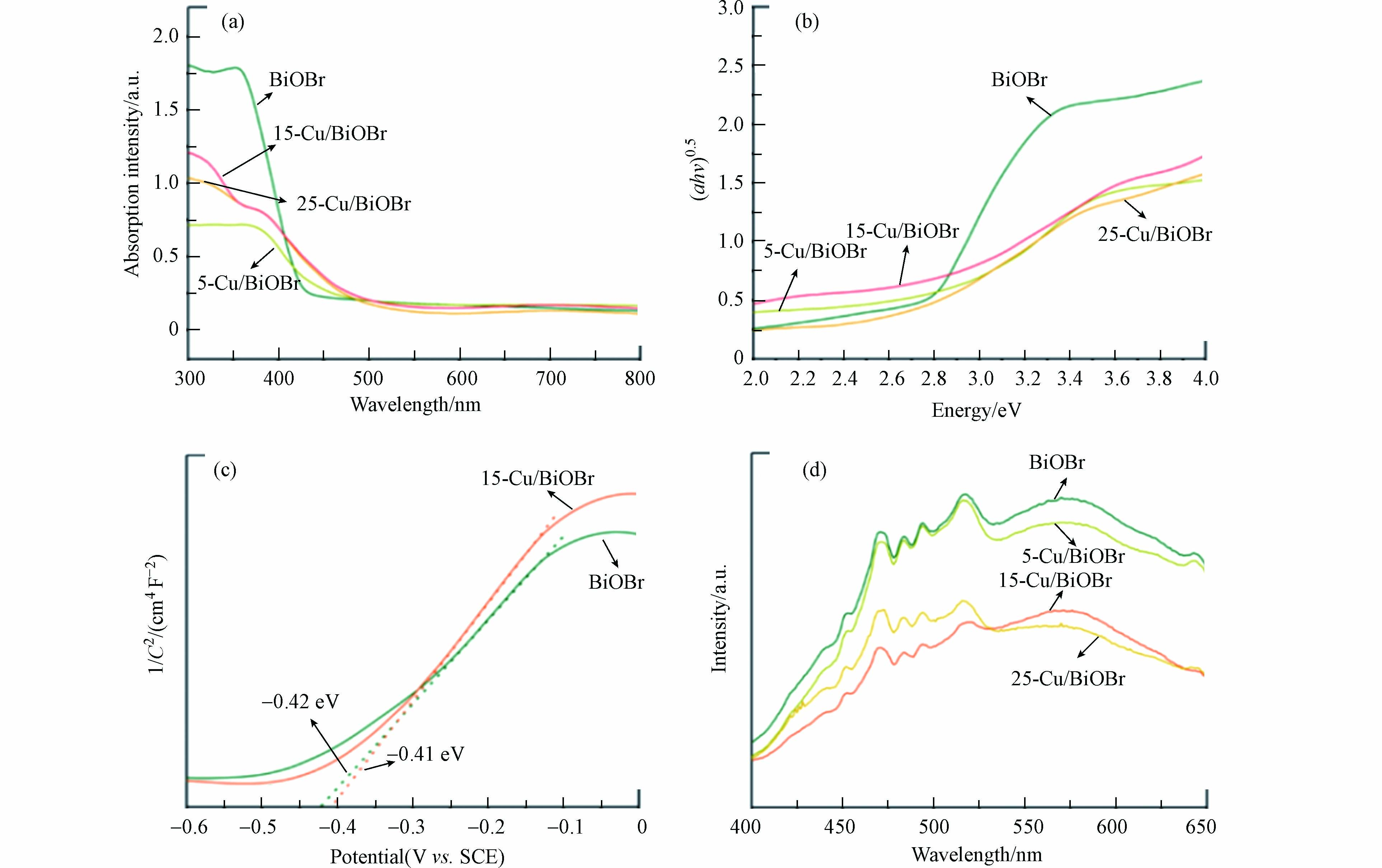
从UV-vis-DRS光谱(图3a)可看出,原始BiOBr的可见光吸收较差,其吸收边约为440 nm,而Cu-BiOBr最大吸收边有所拓宽. 从图3b可得出BiOBr和Cu-BiOBr的禁带宽度分别为2.70 eV和 2.60 eV. 由 Mott-Schottky曲线(图3c)可得BiOBr与15-Cu-BiOBr的平带势,通过计算可知BiOBr与15-Cu-BiOBr的导带位置分别为-0.18 eV和-0.17 eV,其价带位置分别在2.88 eV和2.77 eV. PL图谱(图3d)显示,所有材料在451、470、484、495、519nm处均有相同的发射峰,主要在于BiOBr具有不同的发射中心 [19]. 此外,Cu-BiOBr的发射峰强度低于BiOBr,说明Cu掺杂有助于提高BiOBr光生载流子的分离效率,且15-Cu-BiOBr的峰强度最低,说明其载流子分离效率最高.
-
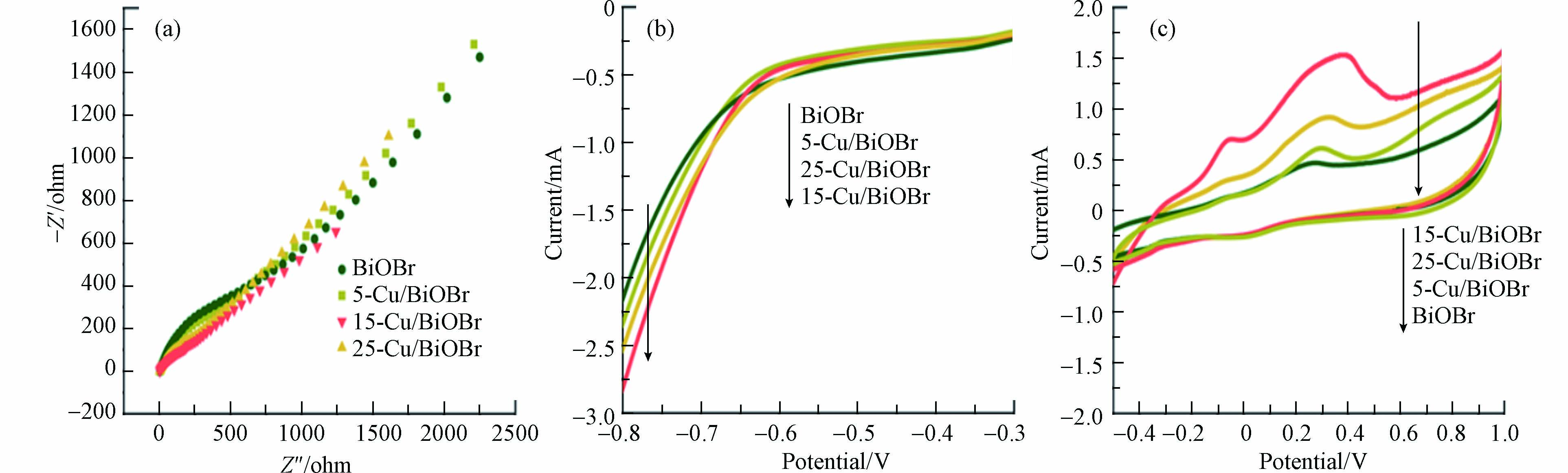
从EIS曲线拟合结果(表1)可知,Cu掺杂减少了BiOBr电荷转移电阻(R1),有利于加速电荷转移. LSV(图4b)显示,15-Cu-BiOBr的过电位最小,其末端电流最大(在-0.8 V,5-Cu-BiOBr、15-Cu-BiOBr和25-Cu-BiOBr的电流分别为2.33、2.52、2.81 mA,大于BiOBr的2.15 mA),说明15-Cu-BiOBr光阴极电化学性能最优. CV曲线(图4c)显示光电极材料在0.3-0.4 V电位附近均出现明显的氧化峰,且15-Cu-BiOBr比电容最大(由曲线面积的整体积分可得)[20]. 这些结果均表明,Cu的掺杂有助于提高BiOBr的电化学性能,使光生电子空穴对加速分离,且15-Cu-BiOBr光阴极最优.
-
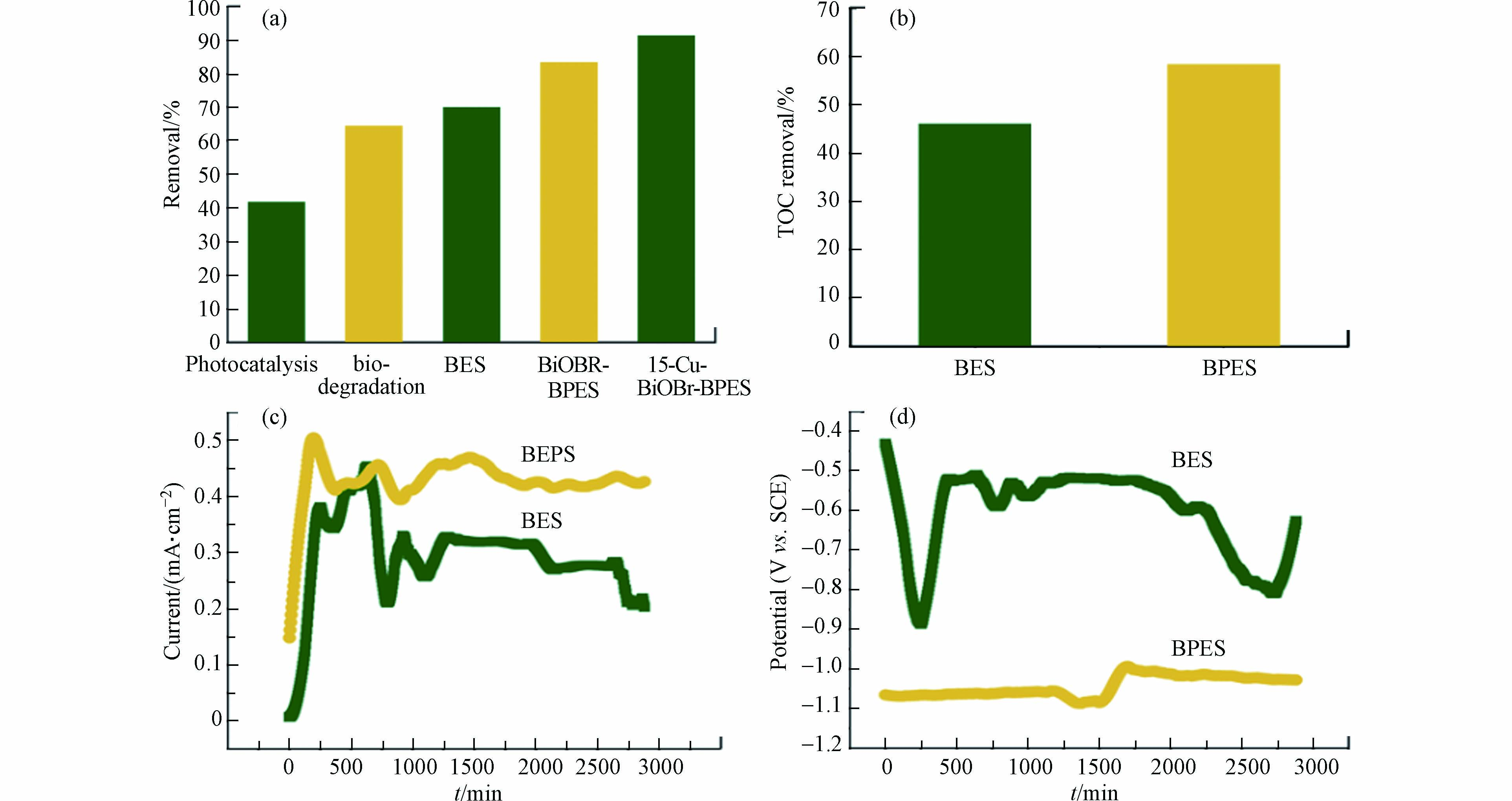
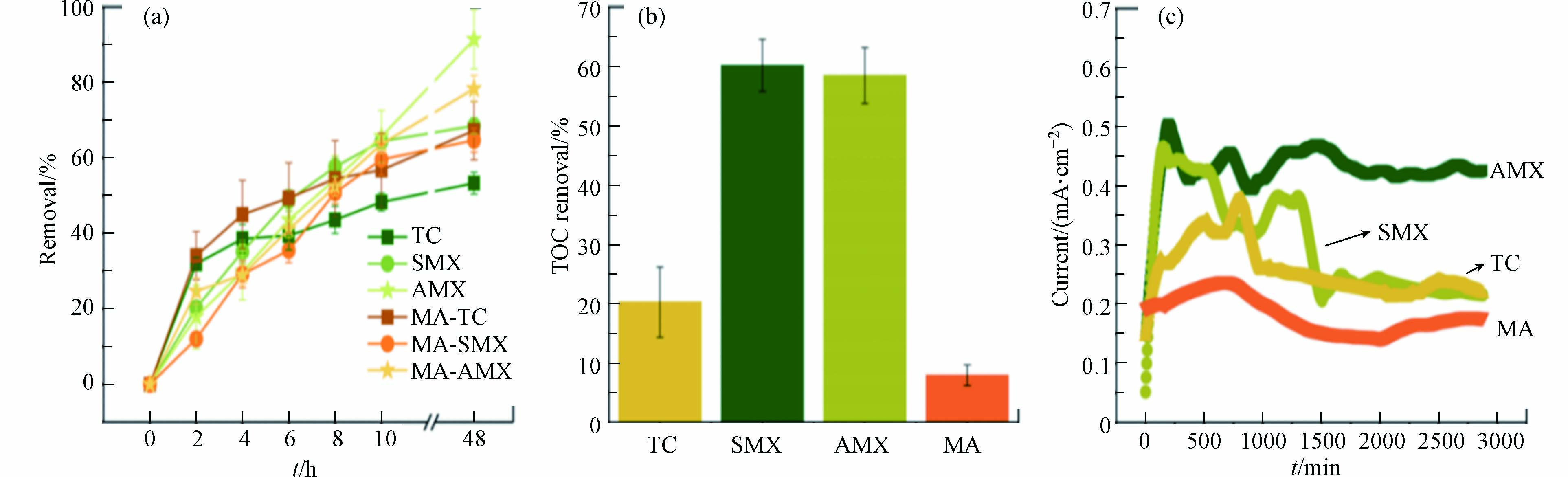
从图5a可知,经过48 h的运行,15-Cu-BiOBr 光阴极的BPES中AMX的降解率91.38%,高于BiOBr光阴极的BPES的降解率(83.52%),而光无光照的BES对AMX的去除率为70.10%. 此外,光催化降解、开路(即微生物降解过程)的去除率分别为41.81%、64.60%. 这些结果表明,在BPES中,微生物降解、光催化降解及电化学过程共同促进了AMX的分解,且微生物降解过程占主导. 由图5b可知,BPES中TOC去除率为58.43%,约为BES中TOC去除率(46.14%)的1.3倍. 这可归因于BPES中光催化产生活性基团,可作用于AMX及其中间产物,促进其降解为小分子物质,进而再被阳极微生物利用,微生物-光-电协同加速污染物的降解,这与前期研究结果一致[12]. 此外,光照还可提高BPES的电流输出(图5c),原因是光阴极表面产生的光生空穴能捕获生物阳极传递过来的电子,加速电子从阳极到阴极之间的转移,进而增加电流输出. 此外,BPES阴极电位比BES更低,与生物阳极形成更大的电势差,也有利于电子转移(图5d).
-
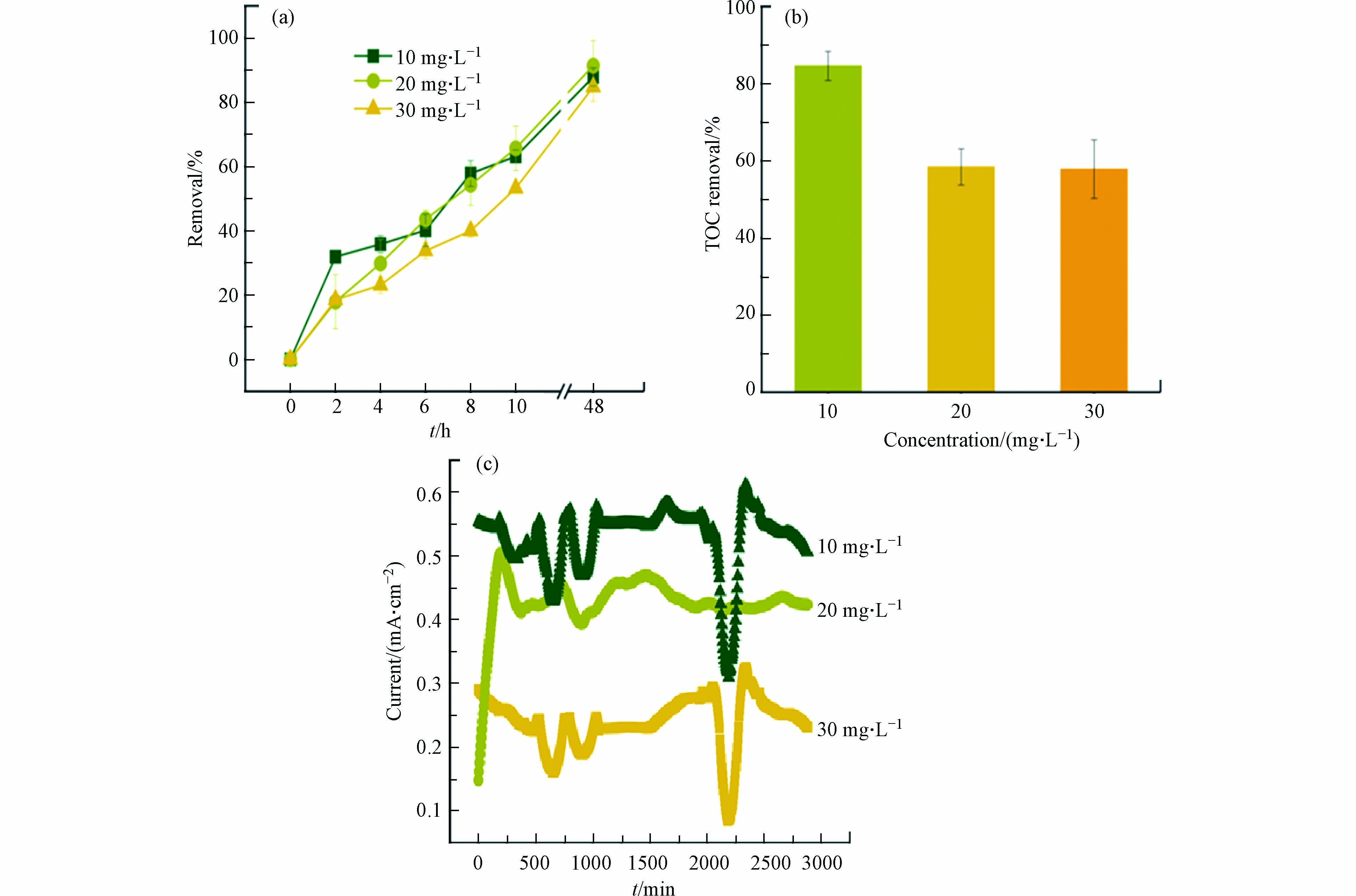
如图6a所示,在BPES中,当 AMX初始浓度从10 mg·L−1增加到20 mg·L−1时,AMX的去除无显著差异;当初始浓度增加至30 mg·L−1时,去除率下降. 然而,当初始浓度为10 mg·L−1时,TOC去除率达到84.60%,明显高于初始浓度为20 mg·L−1和30 mg·L−1的情况(图6b). BPES的电流输出则随着AMX的初始浓度的增加而降低(图6c),可能的原因是当AMX初始浓度增加时,会对阳极电活性微生物产生一定的抑制作用,从而抑制外电路的电流输出.
-
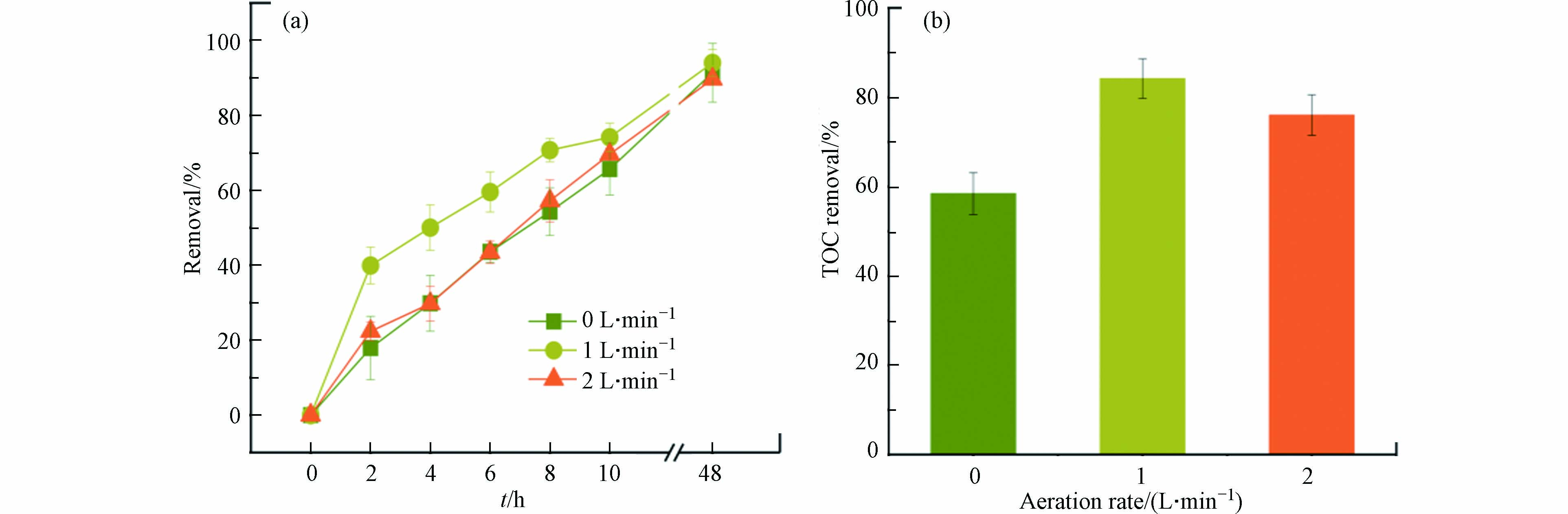
为提高BPES中光催化过程对AMX降解的贡献,对BPES进行微曝气. 当曝气速率为1 L·min−1时,前10 小时可显著加速AMX降解(74.16 %)(图7). TOC结果也验证了该结果:当曝气速率为1 L·min−1时,TOC去除率为84.17%,高于曝气速率为2 L·min−1的情况(76.01%)以及不曝气的情况(58.43%). 原因是适当曝气可增加溶解氧,有利于光阴极表面生成更多活性物种,促进AMX降解与矿化;当曝气速率较大时,则可能会对阳极微生物产生不利影响,影响AMX降解.
-
图8展示了TC,SMX与AMX在BPES中降解性能以及电能输出特性. 如图8a所示,BPES经过48 h的运行后,AMX的去除率最高,达到91.38%,SMX次之(68.49%),TC降解率最低(53.32%). 原因可能是AMX及其降解中间产物对阳极电活性菌的抑制作用较低,而TC降解的中间体则对微生物具有较大的抑制作用. 当BPES中加入混合抗生素(Mixed antibiotic,MA)(TC、SMX和AMX各10 mg·L−1),TC、SMX和AMX在10 h的降解率分别是56.81%、59.57%、63.67%,48 h后的降解率分别是67.22%、64.68%和78.33%,均低于单一降解性能. 图8b显示,SMX和AMX的TOC去除率分别为60.15%和58.43%,TC的TOC去除为20.26%,而MA的TOC去除率最低. 在混合抗生素体系中,由于BPES污染物的总浓度为30 mg·L−1,远高于单一降解的情形,且共存情况下3种抗生素降解过程相互竞争,再者,混合抗生素及其中间体也会抑制微生物的呼吸代谢,因此,共存情况下抗生素的降解效率和TOC去除率均最低. 如图8c所示,BPES电流输出性能与抗生素降解效果的趋势基本一致:处理AMX的BPES电流输出最高,处理SMX的BPES次之,再者是降解TC的BPES,电流输出最低的是处理MA的BPES. 这与抗生素及其降解中间产物对阳极电活性菌的抑制作用有密切关系.
-
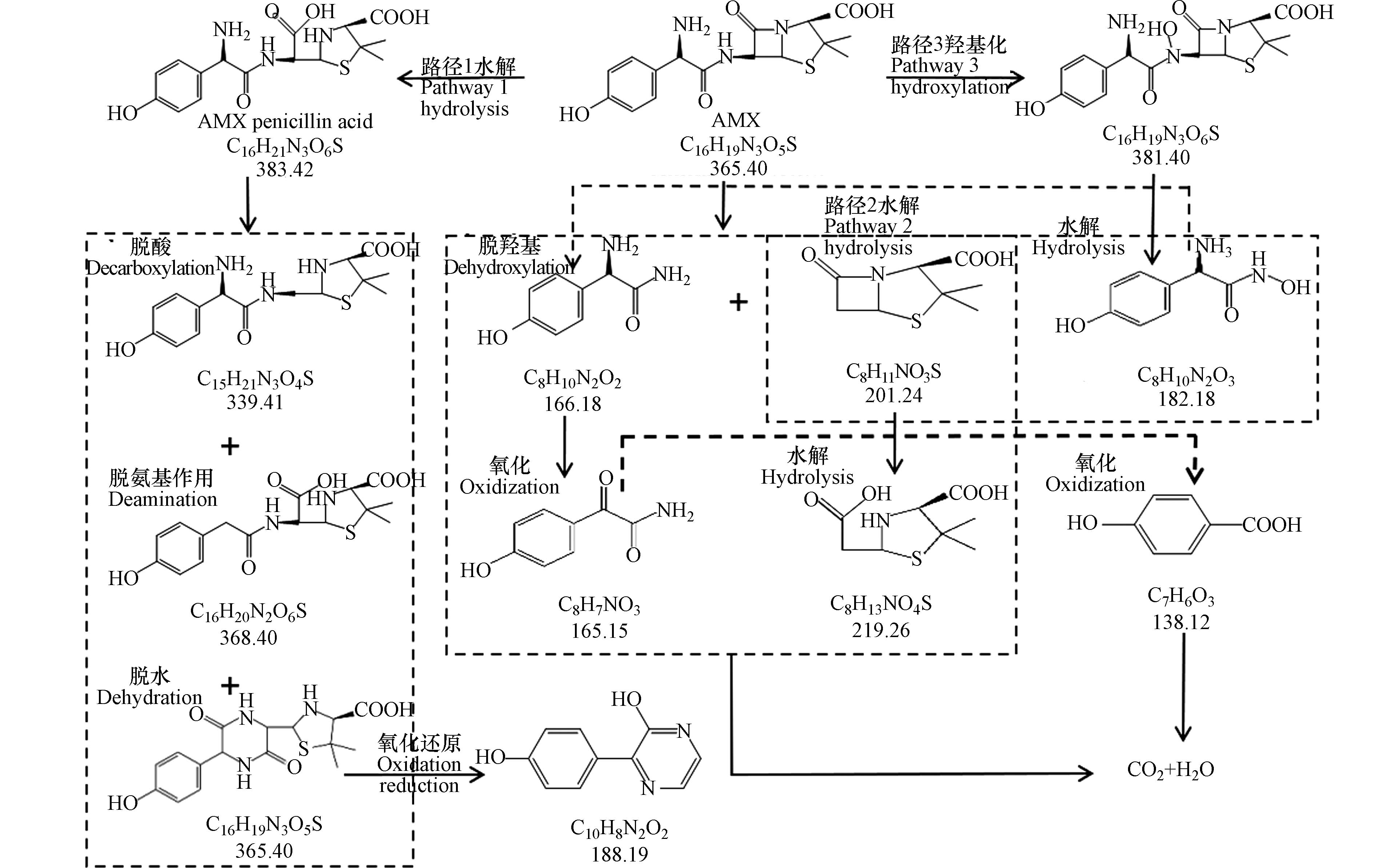
通过液质联用仪鉴定识别出来的AMX的中间产物主要为C16H19N3O5S (m/z=366.11)、C16H19N3O6S (m/z=382.12)、C16H21N3O6S (m/z=384.12)、C8H10N2O2 (m/z=166.98)、C8H11NO3S (m/z=202.22)、C8H9N2O3 (m/z=182.98)、C8H7NO3 (m/z=166.34)、C8H13NO4S (m/z=220.22)、C15H21N3O4S (m/z=340.39)、C16H20N2O6S (m/z=369.39)、C10H8N2O2 (m/z=188.95)、C7H6O3 (m/z=139.99). 由中间产物可推测,AMX主要发生了水解、氧化开环、自由基取代,以及脱氨和脱羧等反应过程,根据已知信息及相关文献报道推断,AMX在BPES中可能的降解路径主要有三条,如图9所示.
-
图10揭示了接种液、BES以及BPES生物阳极处理不同抗生素废水之后的微生物群落结构在种属水平上的演变规律. 经过BES和BPES的驯化以后,生物阳极上Geobacter的占比比接种液的显著增加,在处理AMX、SMX、TC和MA分别占细菌总数65.48%、40.6%、13.41%和12.46%. 这是因为Geobacter具有优良的细胞外电子转移能力和载体表面的附着生长能力[21]. 相比于BES,降解SMX和AMX的BPES阳极上的Geobacter的数量分别增加了12.5%和37.38%. 据报道,Geobacter广泛存在于磺胺类抗生素[22]和AMX[23]污染废水中,对抗生素的降解发挥着重要作用.
Dysgonomonas在TC样品中占比最大为26.42%,高于BES (0.86%)、SMX (0.3%)、AMX (3.01%)、MA (4.32%). Dysgonomonas属于Bacteroidetes,非运动性的兼性厌氧球菌[24],被认为是生物降解药物污染物的优势菌属,也常出现在抗生素废水中[25-27]. 此外,在TC样品的阳极生物膜中,Comamonas占细菌总数15.66%,而Acidovorax、Gordonia、Stenotrophomonas、Sphaerochaeta和Desulfovibrio等占比也较高..
在SMX和AMX的样品生物膜中,也含有少数的Comamonas、Acidovorax、Gordonia、Stenotrophomonas、Sphaerochaeta、Desulfovibrio等,均电活性细菌,为 BPES 的产电提供贡献. 在3种抗生素混合降解的BPES阳极中,Comamonas、Acidovorax、Gordonia、Stenotrophomonas、Sphaerochaeta、Desulfovibrio等细菌的数量都有所增加,说明微生物群落结构会随着共底物的类型及浓度变化进而发生改变.
-
(1) Cu的掺杂提高了BiOBr的光电化学性能;以最优的Cu-BiOBr为光阴极构建的BPES可高效降解AMX,且当曝气速率为1L·min−1时,AMX降解加速. BPES对SMX也有较好的去除效果,而对TC的降解则不太理想. AMX, TC和SMX共存情况下,其降解过程会出现相互竞争相互抑制现象,导致去除率降低.
(2) AMX在BPES中可能的降解路径主要有三条,降解主要通过水解、自由基的取代、氧化开环,以及脱氨和脱羧等反应过程.
(3) BPES生物阳极的微生物群落结构随着污染物的改变而发生演变,降解SMX和AMX的主要菌种为Geobacter,分别占比40.6%和65.48%. 另外, Dysgonomonas主要有助于降解TC,其占其细菌总数的26.42%. Comamonas则在MA中占有较大比例,表明Comamonas对不同抗生素均具有良好的耐受性.
基于Cu掺杂BiOBr光阴极的生物光电化学系统降解典型抗生素的特性及微生物群落响应
Degradation of typical antibiotics and microbial community response in a biophotoelectrochemical system with a Cu-doped BiOBr photocathode
-
摘要: 抗生素难以生物降解且会诱导产生抗性基因,对生态环境和人体健康均造成威胁,因此,抗生素废水的高效处理意义重大. 本研究制备了Cu掺杂的BiOBr光阴极,并与生物阳极耦合,构建生物光电化学系统(biophotoelectrochemical system,BPES),用于降解抗生素. 结果表明,Cu-BiOBr较BiOBr具有更优异的光电化学性能. 光照条件下的BPES在48 h内对初始浓度为20 mg·L−1的阿莫西林(AMX)的去除率达91.38%. 此外,适当曝气可提高BPES对AMX的去除. 当AMX与盐酸四环素(TC),磺胺甲恶唑(SMX)在BPES中共降解时,降解过程均受到不同程度的抑制. 根据鉴定的AMX的降解中间产物,推断了AMX的降解路径. BPES的阳极生物膜上的微生物主要以电活性细菌Geobacter为主,其对抗生素具有较高耐受性以及降解能力.
-
关键词:
- 生物光电化学系统 /
- Cu-BiOBr光阴极 /
- 抗生素 /
- 降解路径 /
- 微生物群落.
Abstract: Antibiotics are difficult to be biodegraded, and they can induce resistance genes; therefore, efficient treatment of antibiotics wastewater is of great significance. In this study, the Cu-doped BiOBr (Cu-BiOBr) photocathode was prepared and coupled with a bioanode to constructed a biophotoelectrochemical system (BPES) for antibiotics degradation. Results showed that the Cu-BiOBr exhibited superior photochemical performance as compared with the BiOBr. In the light-illuminated BPES, the removal of amoxicillin (AMX, initial concentrationof 20 mg·L−1) reached 91.38% within 48 h. In addition, providing suitable aeration in the BPES could promote AMX removal. When AMX, tetracycline hydrochloride (TC), and sulfamethoxazole (SMX) were co-existed in the BPES, degradation process of each antibiotic was inhibited to some extent. Possible degradation pathways of AMX in BPES were proposed according to the identified degradation intermediates. The dominated microorganisms on the anodic biofilm of the BPESs treating different antibiotic wastewater were electro-active bacteria--Geobacter, which showed relatively high resistance towards antibiotics and certain degradation ability. -
随着我国社会和经济发展,农业生产过程中过量使用磷肥及城市大量排放含磷污水导致我国水体富营养化问题突显. 近年来,我国的滇池、太湖和巢湖等内陆湖泊不断发生水华现象[1]. 根据2019年中国海洋灾害公报显示,我国赤潮暴发频率自70年代开始每10年增长3倍,截止2018年我国有明确暴发时间及地点等基本信息的赤潮次数为1780次. 大量未经处理的含磷污水的直接排入是造成水体总磷超标的主要原因,包括城市、工业和农业中大量含磷水的排放. 控制磷污染,保障生态系统安全已刻不容缓.
吸附法除磷因具有操作简便、适用范围广、效果好、运行费用低等优点而得到高度关注[2]. 稀土元素镧(La)对磷酸盐具有强亲和力,可与磷酸根形成稳定不可溶的LaPO4,展现出优异的除磷性能[3]. 然而镧的氧化物通常以粉末形式存在,易流失、堵塞,且流体力学性能差,吸附磷后会沉入水体难以回收,造成了资源的浪费和污泥污染,从而限制了镧氧化物在水体除磷中的应用. 将La固定在多孔颗粒材料的表面或孔道中是减少La组分流失和提高除磷性能的有效方式. 目前常采用多孔的天然黏土材料(如沸石、蛭石、硅藻土等)、碳基材料(如活性炭、黑炭、碳纳米管等)、离子交换树脂高分子材料负载La,得到La改性的多孔无机或有机复合吸附材料,如La-负载多孔沸石、La-负载碳纳米管、La-离子交换树脂等含La吸附剂[4 − 6].
不同于以上载体硬模板方式固定La,钛(Ti)基多孔材料可通过原位自生模板法原位转化为介孔毫米球同步固载La[7],得到具有丰富的孔道(孔径2—50 nm)、高比表面积的球形颗粒,具有优异的流体力学与传质性能,有望实现高选择性除磷性能[8 − 9]. 而且,Ti载体本身也可通过静电吸附、配体交换、Ti—P化学键等作用吸附磷[10 − 11],起到协同La除磷作用. 故以Ti为载体通过溶胶-凝胶法制备镧钛双金属氧化物介孔毫米球,提高对磷的吸附能力,减少吸附过程中La的流失,同时大大增强吸附剂流体力学性能,实现吸附材料的分离与回收利用.
为此,本文以镧和钛金属盐为原料,海藻酸钠为交联剂,采用沉淀凝胶法制备了镧钛双金属氧化物介孔毫米球LaxTi1-xO2,利用N2吸附-脱附、XRD、SEM、TEM等对制备的LaxTi1-xO2进行了表征,根据镧钛物质的量比、煅烧温度对LaxTi1-xO2除磷性能的影响,优选出400 ℃煅烧制得的La0.5Ti0.5O2. 考察了La0.5Ti0.5O2投加量、溶液pH等因素对吸附的影响,并利用准一级和二级动力学模型及Langmuir和Freundlich模型对La0.5Ti0.5O2除磷过程进行了动力学与热力学研究. 通过除磷性能测定并结合零电荷点、FT-IR、XPS等表征手段提出了La0.5Ti0.5O2除磷机制.
1. 材料与方法(Materials and methods)
1.1 实验试剂
实验过程中使用的试剂主要包括:LaN3O9·6H2O(AR,99%,麦克林)、TiOSO4·xH2SO4·xH2O(synthesis grade,阿拉丁)、尿素(AR,99%,阿拉丁)、海藻酸钠(AR,阿达丁)、磷酸二氢钾(AR,广东光华科技)、抗坏血酸(AR,西陇科学)、钼酸铵(AR,西陇科学)、酒石酸锑钾(AR,西陇科学)、硫酸(AR,中星化工),所有实验用水均为超纯水(Millipore,18.2 MΩ·cm).
1.2 吸附剂制备
镧钛金属氧化物制备是基于海藻酸钙凝胶球模板法和尿素沉淀法为基础并进行了改进和开发[12 − 13]. 制备具体步骤如下:将TiOSO4·xH2SO4·xH2O和LaN3O9·6H2O共15 mmol按照La占双金属元素物质的量比分别为0、2.5、5.0、7.5 mmol溶于80 mL去离子水中;将120 mL含有14.0 g尿素的水溶液加入到上述所得溶液中,500 r·min−1磁力搅拌并于90—95 ℃水浴锅中加热8 h;搅拌加热后,用去离子水将悬浊液离心清洗3次,得到高浓度金属氧化物前驱体悬浊液40 g,将0.4 g的海藻酸钠粉末加入到悬浊液中,在55 ℃水浴中高速磁力搅拌30 min预混合,静置30 min;利用蠕动泵将所得到的悬浊液滴入0.1 mol·L−1的LaN3O9·6H2O溶液中形成凝胶球,静置24 h后在60 ℃烘箱中烘干12 h;然后将烘干材料放入管式炉进行两段煅烧,先经氮气气氛下200 ℃预处理2 h后在空气气氛400 ℃下煅烧2 h,升温速度为5 ℃·min−1.
经过预实验后, LaN3O9·6H2O和TiOSO4·xH2SO4·xH2O共15 mmol分别按照La/Ti物质的量比1:1、2:1、3:1、1:3制备,其中La:Ti=2:1形成的球形形状不规范,故排除该物质的量比; La:Ti=3:1因过于黏稠无法成球,故也排除该物质的量比. 最终,制得3种不同物质的量比的小球材料,分别为:TiO2球、La:Ti=1:1(La0.5Ti0.5O2)、La:Ti=1:3(La0.25Ti0.75O2). 另外,为了探究煅烧温度的影响,在400 ℃和600 ℃两个不同的煅烧温度下制备了介孔毫米球.
1.3 吸附剂表征
通过测定ASAP2020HD88型比表面孔径测定仪(BET,中国,麦克默瑞提克)得到材料的比表面积和孔径. 通过JSM-6700F型扫描电子显微镜(SEM,日本,JEOL)分析介孔毫米球的表观形貌. 材料的微观结构通过JEM-2100F型透射电子显微镜/选区电子衍射(TEM/SAED,日本,JEOL)和D8ADVANCE型X射线衍射仪(XRD,美国,BRUKER)表征. 吸附剂中La含量采用6 mol·L−1硝酸消解后通过电感耦合等离子谱仪(ICP-OES, PerkinElmer,USA)测定.
1.4 吸附实验
用超纯水配制30 mg·L−1的KH2PO4溶液为初始磷溶液,取100 mL于150 mL三角烧瓶中. 用0.1 mol·L−1的NaOH溶液和0.1 mol·L−1的HCl溶液调节pH至7,温度为25 ℃,加入0.1 g吸附材料,振荡速率为150 r·min−1,在0、3、6、12、24、36、48、60、72 h分别取样测定,并用0.22 μm滤膜过滤,测定不同时间间隔下的磷浓度,水样中磷含量采用钼酸铵分光光度法(GB11893—89),并计算磷吸附量.
设置磷浓度为30 mg·L−1,溶液体积为100 mL,温度为25 ℃,振荡速率为150 r·min−1,通过改变溶液初始pH值(pH=3、5、7、9),介孔毫米球的投加量(投量为0.05、0.075、0.1、0.15、0.2 g)来探究对磷吸附效果的影响,同时选取水中常见阴离子Cl−、SO42−、NO3−和HCO3−(以钠盐形式存在)考察了共存离子的影响.
1.5 吸附等温线模型
吸附剂投量为1 g·L−1,设置初始磷酸盐浓度为1—70 mg·L−1,pH为3,在25 ℃条件下以150 r·min−1速度振荡72 h.采用Langmuir和Freundlich模型进行拟合.
Langmuir等温吸附方程:
stringUtils.convertMath(!{formula.content}) (1) Freundlich等温吸附方程:
stringUtils.convertMath(!{formula.content}) (2) 式中,qm为最大吸附量(mg·g−1);qe为吸附平衡时的磷酸盐吸附量(mg·g−1);Ce为吸附平衡时的磷酸盐浓度(mg·L−1);1/n为经验常数;KL和KF分别为Langmuir吸附模型和Freundlich吸附模型的吸附常数,代表吸附能力的强弱.
1.6 吸附动力学模型
吸附动力学参数决定了磷酸盐回收时间,在水处理过程中至关重要. 吸附剂投加量为1 g·L−1,初始磷酸盐浓度为30 mg·L−1,pH为7,温度为25 ℃,置于恒温振荡器内以150 r·min−1速度振荡72 h,设置时间段测定磷酸盐浓度. 实验数据由准一级动力学模型和准二级动力学模型进行拟合.
准一级动力学模型:
stringUtils.convertMath(!{formula.content}) (3) 准二级动力学模型:
stringUtils.convertMath(!{formula.content}) (4) 式中,k1为准一级动力学速率常数(min−1);k2为准二级动力学速率常数(g·(mg·min)−1);t为反应时间(min);qe为反应平衡时的吸附量(mg·g−1);qt为反应时间t时的吸附量(mg·g−1).
2. 结果与讨论(Results and discussion)
2.1 吸附剂表征
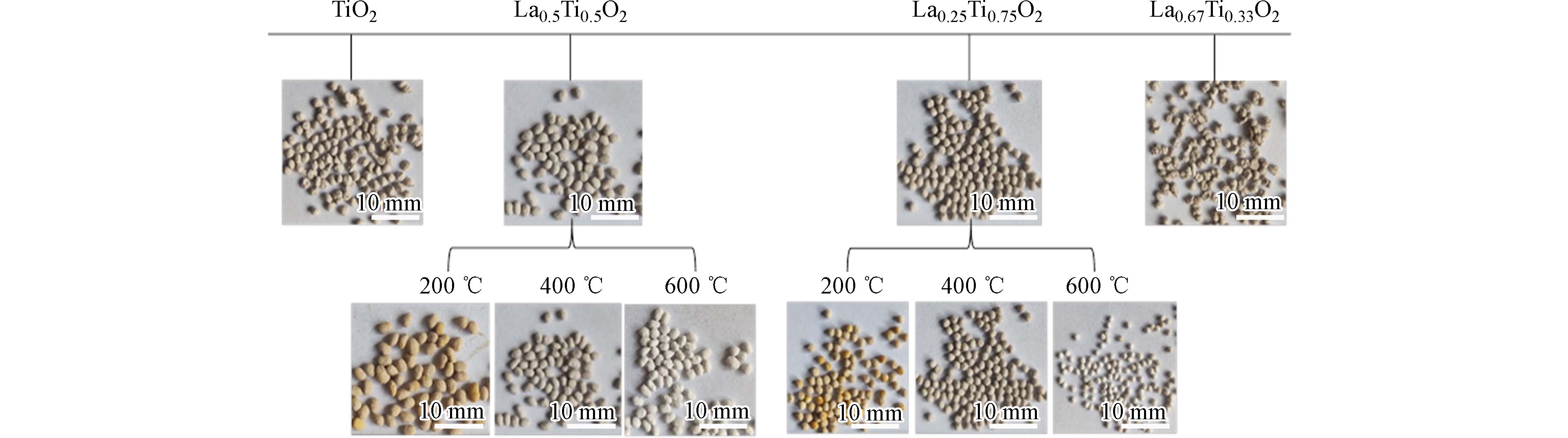
采用溶胶-凝胶模板法在不同煅烧温度下制备了不同La/Ti物质的量比的镧钛双金属氧化物介孔毫米球LaxTi1-xO2. 由图1可知,从宏观形貌上来看,随着煅烧温度的增加,LaxTi1-xO2的颜色由黄色逐渐变为灰白色,且通过吸附实验发现在200 ℃下煅烧制作的小球硬度不够,易碎成粉末,机械强度低,故舍弃该煅烧温度下制备的材料. 对比不同La/Ti物质的量比下制得的介孔毫米球发现,随着Ti含量增加,得到的毫米球球形变得更加规则,LaxTi1-xO2平均粒径为2—3 mm.
LaxTi1-xO2介孔毫米球的SEM图像如图2(a)所示,TiO2和La:Ti=1:3的LaxTi1-xO2颗粒外形均呈现球状且表面光滑,而La:Ti=1:1的LaxTi1-xO2颗粒外形均呈现棒状且互相黏集在一起,即随着La量的增加,介孔毫米球表面会形成褶皱而变得粗糙,这种形貌可有效增加吸附剂活性吸附位点,增强除磷性能. 类似的在负载La之后使得吸附剂表面呈条状褶皱的粗糙形态在其他研究中也有发现[14]. 为进一步探究材料的微观结构,对不同La/Ti物质的量比的LaxTi1-xO2介孔毫米球研磨制样进行了TEM和选区电子衍射(SAED)表征,结果如图2(b)所示. LaxTi1-xO2以纳米颗粒或纳米簇形式存在,且分散均匀,400 ℃和600 ℃下煅烧的Ti0.5La0.5O2球存在明显的晶格条纹,而400 ℃下煅烧的TiO2球与Ti0.75La0.25O2球未观测到晶格条纹. 400 ℃下煅烧的Ti0.5La0.5O2球和600 ℃下煅烧Ti0.75La0.25O2球存在明显的环状多晶衍射图样,而400 ℃下煅烧的Ti0.75La0.25O2球和600 ℃下煅烧Ti0.5La0.5O2球未观测到衍射图样,表明这两种金属氧化物球在微观尺度上依然保持无定形结构,这可能是因为La、Ti两种元素相互渗入对方氧化物晶格达到一定比例后造成明显的畸变和扭曲后,导致各自的周期性被破坏,形成了La—O—Ti键[15]. 以上结果说明, 控制La/Ti物质的量比和煅烧温度可以调控LaxTi1-xO2晶型和无定形两类结构的产生.
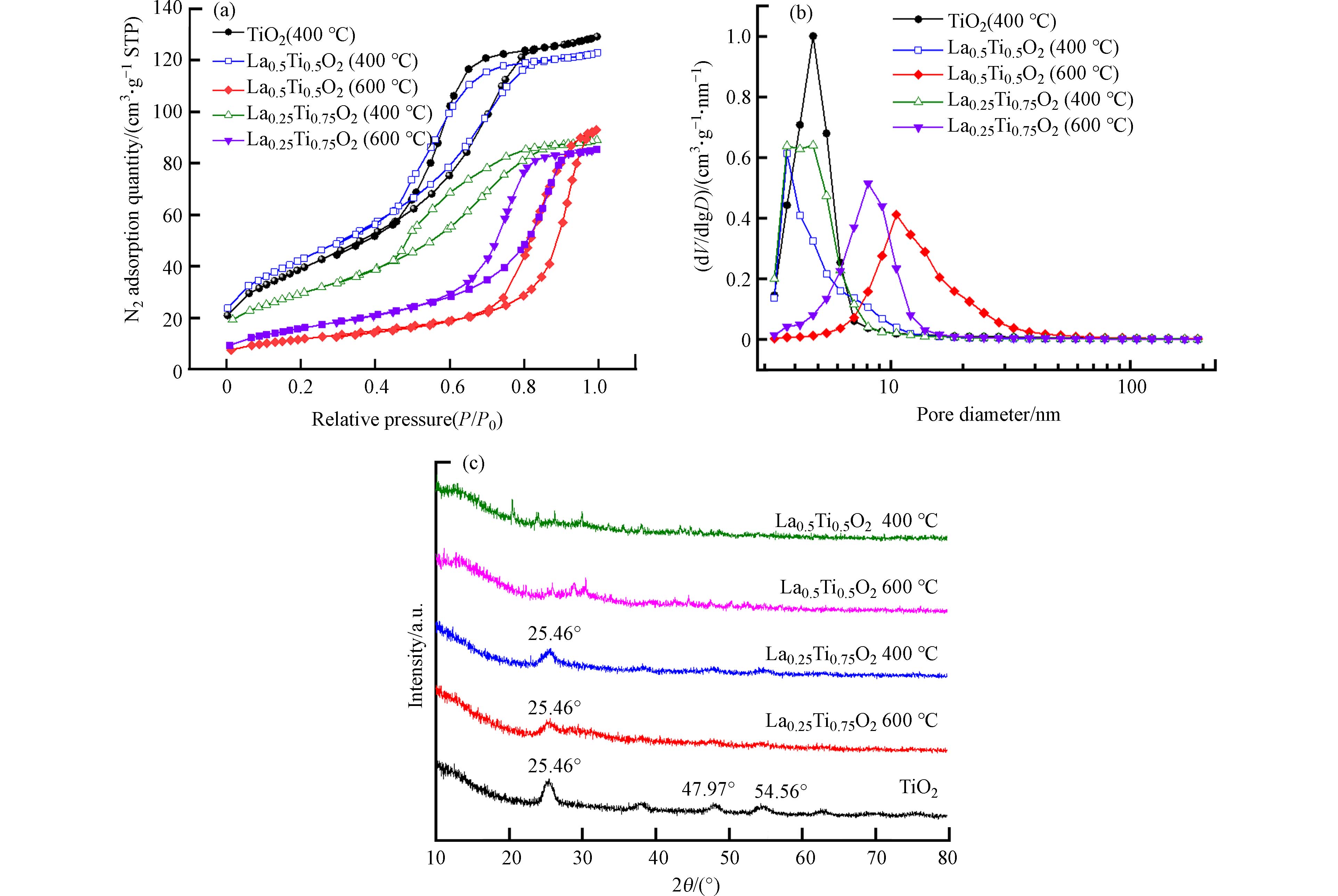
通过比表面积分析仪进一步测定了LaxTi1-xO2的孔结构. 根据国际纯粹与应用化学联合会(IUPAC)分类,LaxTi1-xO2的氮吸附-脱附等温线显示出“Ⅳ”型等温线(图3a),表明其孔结构主要是介孔,1—40 nm的孔径分布进一步证实了其介孔结构(图3b). 介孔毫米球LaxTi1-xO2的平均孔径和平均比表面积如表1所示,在不同的煅烧温度和La/Ti物质的量比下制备的材料的平均孔径和比表面积差别较大. 在400 ℃下煅烧LaxTi1-xO2平均孔径主要集中在3—5 nm;在600 ℃下煅烧LaxTi1-xO2平均孔径主要集中在8—10 nm. 由此可见,随着煅烧温度的增加,LaxTi1-xO2平均孔径有了明显的增加. 而在不同的煅烧温度下, LaxTi1-xO2介孔毫米球的比表面积也有不同程度的变化,其中在La:Ti=1:3时,400 ℃下煅烧的材料拥有最大的比表面积,为151 m2·g−1. 总体而言,在400 ℃下煅烧的材料的比表面积大于600 ℃下煅烧材料的比表面积. 综上,煅烧温度对LaxTi1-xO2比表面积影响较为显著,而La/Ti物质的量比对平均孔径和平均比表面积影响较小.
表 1 不同煅烧温度下LaxTi1-xO2介孔毫米球的基本性质Table 1. Basic properties of LaxTi1-xO2 mesoporous millispheresLaxTi1-xO2介孔毫米球 TiO2(400 ℃) La0.5Ti0.5O2 (400 ℃) La0.5Ti0.5O2 (600 ℃) La0.25Ti0.75O2 (400 ℃) La0.25Ti0.75O2 (600 ℃) 平均孔径/nm平均比表面积/(m2·g−1) 4.76140 3.71105 10.641.3 4.76151 8.0656.9 利用XRD谱图对LaxTi1-xO2的晶体结构特征进行了进一步分析,结果如图3(c)所示. TiO2的XRD谱图与锐钛矿标准谱图(PDF #21-1272)相符;对于La:Ti=1:3的两种LaxTi1-xO2,均在2θ=25.46°时出现了TiO2衍射峰,但是在特征峰处的衍射强度均有所减小,且经过改性后的LaxTi1-xO2的杂峰相较于TiO2有所减少,说明掺杂La之后的介孔材料和TiO2具有相似的结构特性[16]. 但是随着La量从La:Ti=1:3增加到La:Ti=1:1,TiO2特征峰逐渐消失,这表明LaxTi1-xO2中La含量增加会改变其晶形结构,使材料转变为无定形态[17 − 18]. 此外, LaxTi1-xO2的 XRD谱图中并没有出现明显的La相关衍射峰,谱图均表现为无定形特征,与SEAD和TEM结果一致,说明晶格周期性被完全破坏,形成了La—O—Ti键. 这与Ce—O—Ti破坏晶格周期性结构,形成无定型铈钛氧化物的结果一致[15 − 19].
2.2 除磷性能
2.2.1 吸附剂优选
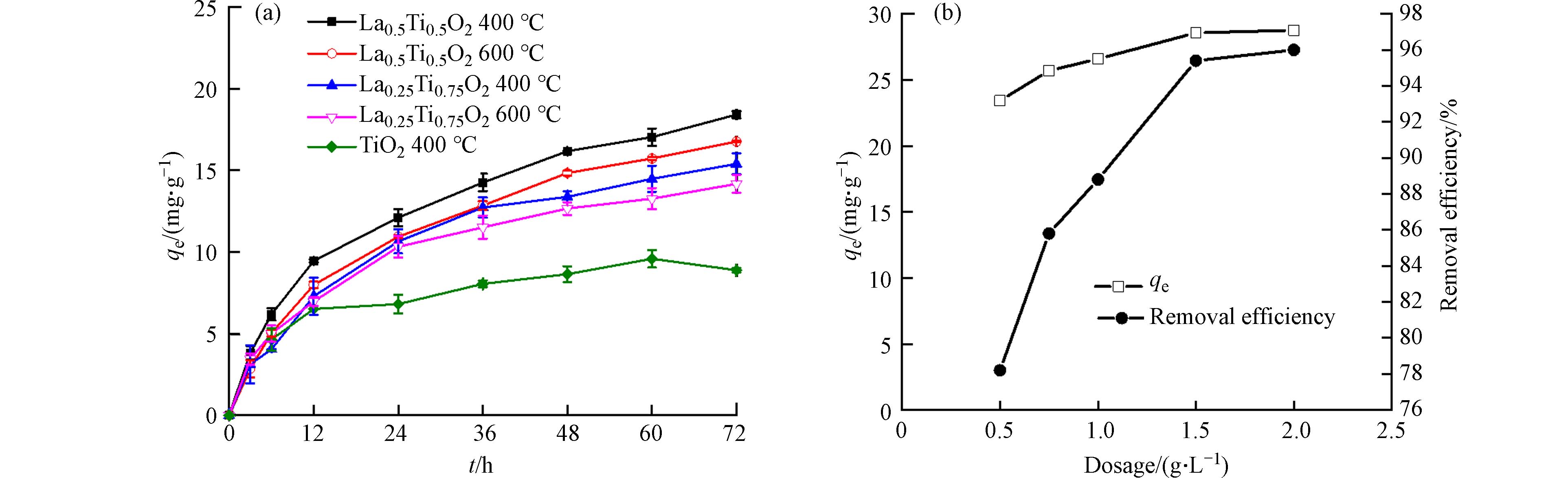
通过实验发现当La所占物质的量比过多时制备的吸附材料形状不规范甚至无法成球,因此选取了La:Ti=1:1、1:3的物质的量比条件下制备的LaxTi1-xO2介孔毫米球并探究其对磷酸盐的吸附性能. 如图4(a)所示,不管是La:Ti=1:1还是La:Ti=1:3的介孔毫米球,其对磷酸盐的吸附效果相较于TiO2球都有显著提高,TiO2对磷的吸附量仅为9 mg·g−1,而LaxTi1-xO2对磷的吸附量高达13—18 mg·g−1. 对比4种不同条件下制备的LaxTi1-xO2的吸附效果可知,煅烧温度由400 ℃升高至600 ℃,LaxTi1-xO2对磷的吸附量有一定下降. 400 ℃煅烧温度下La:Ti=1:1(La0.5Ti0.5O2)的介孔毫米球对磷的吸附量最大,为18.4 mg·g−1,是TiO2介孔毫米球的2倍. 故优选400 ℃下煅烧的La0.5Ti0.5O2介孔毫米球进行后续实验探究.
由图4(b)可以看出,在0.5 g·L−1到1.5 g·L−1范围内增加La0.5Ti0.5O2介孔毫米球的投加量,会提高对磷的吸附量和去除率,继续增加吸附剂投加量至2.0 g·L−1时对磷的吸附量和去除率趋于平缓. 尽管La0.5Ti0.5O2投加量为2.0 g·L−1时吸附量达到最大值28.76 mg·g−1,此时对磷的去除率达到96%,但当其投加量减少为1.0 g·L−1时其对磷的吸附量为26.59 mg·g−1,除磷率依然能够达到88.8%,因此本实验以磷的排放标准为基础,综合考虑吸附剂的吸附效果和经济成本,选用1.0 g·L−1 作为La0.5Ti0.5O2介孔毫米球最佳投加量.
2.2.2 pH和共存离子影响
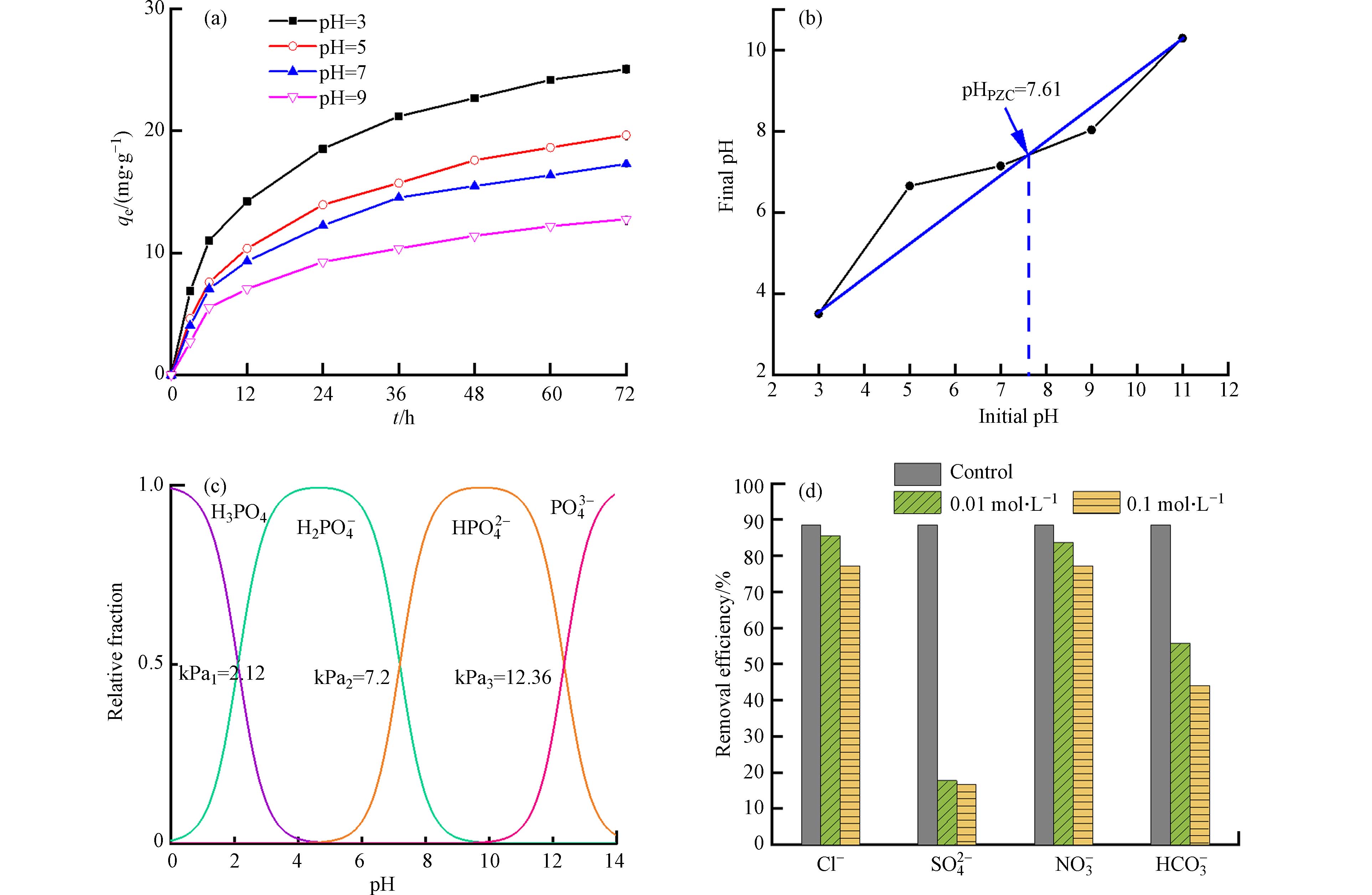
水体pH值是影响La0.5Ti0.5O2介孔毫米球吸附磷酸盐的重要影响因素,pH值既影响磷酸根在水体中的分布形态,又影响La0.5Ti0.5O2介孔毫米球的表面电荷[16]. 因此,实验通过改变溶液初始pH值,研究了其对La0.5Ti0.5O2介孔毫米球吸附磷酸盐的影响. 如图5(a)所示,La0.5Ti0.5O2介孔毫米球对磷酸盐的吸附效果随着溶液初始pH的增加而削弱,当pH值为3时,吸附量达到最大值26.15 mg·g−1. 这主要归因于La是原子半径较大的带正电荷原子,主要吸附阴离子,当溶液中的OH−逐渐增多时,会与磷酸根产生竞争吸附作用从而不利于La0.5Ti0.5O2吸附磷的进行[20 − 22]. 如图5(b)所示,通过pH漂移法获得La0.5Ti0.5O2的零电荷点(pHpzc)为7.61,表明La0.5Ti0.5O2在pH<7.61时容易携带正电荷(H+),导致La0.5Ti0.5O2和磷酸盐之间产生静电吸引,有利于对磷的吸附. 相反,La0.5Ti0.5O2在pH>7.61时倾向于携带负电荷(OH−),导致其与磷酸盐之间产生静电排斥,不利于对磷的吸附. 此外,pH值的增加也导致H2PO4−转化为HPO42−和PO43−(图5c),并且它们的吸附亲和力弱于H2PO4−,从而进一步削弱La0.5Ti0.5O2对磷的吸附. 综上,La0.5Ti0.5O2在酸性水质条件下对磷的去除性能表现更好.
如图5(d)所示,考察了湖泊或河流中常见的阴离子(Cl−、NO3−、SO42−和HCO3−)对La0.5Ti0.5O2去除磷的影响. 所有阴离子对磷的去除都表现出一定的抑制作用. 其中,Cl−和NO3−对磷去除的抑制作用不大,而SO42−和HCO3−对磷去除的抑制作用较强. 与空白组相比,当添加0.01—0.1 mol·L−1 Cl−和NO3−时,磷的去除率仅下降了3%—10%,表明La0.5Ti0.5O2主要以化学吸附的形式去除磷,因此其对磷的去除几乎不受Cl−和NO3−离子强度的影响[23]. SO42−和HCO3−对磷去除的强烈抑制作用可能是由于这些阴离子会与La3+反应形成La2(SO4)3和La2(CO3)3[24 − 25],从而减少了对磷的有效吸附位点. 此外,SO42−和HCO3−还可以提高水环境的pH值,从而增强磷酸盐与La0.5Ti0.5O2之间的静电排斥,抑制La0.5Ti0.5O2对磷的吸附.
2.2.3 吸附动力学和吸附等温线
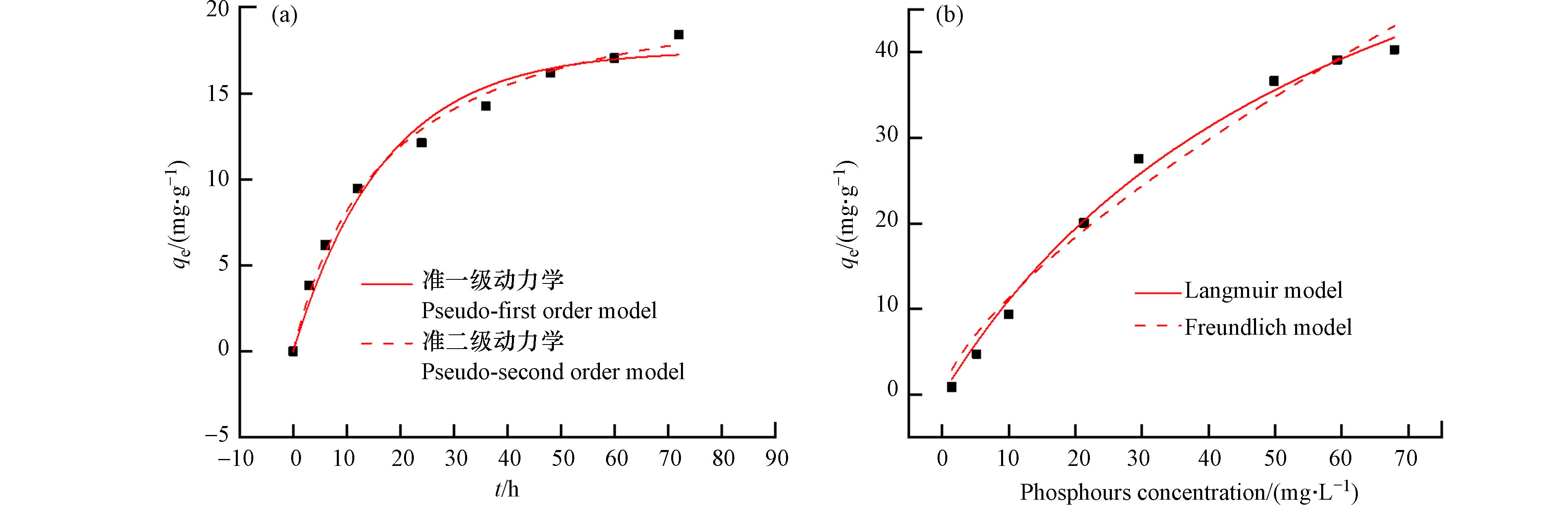
为了评估La0.5Ti0.5O2介孔毫米球对磷吸附的快慢程度,考察了该材料对磷的吸附动力学,结果如图6(a)和表2所示. 由表2可知,准二级动力学模型的R2=0.994,高于准一级动力学模型的R2=0.978,说明La0.5Ti0.5O2介孔毫米球对磷的吸附过程是以化学吸附为主的物理化学吸附过程. 图6(b)是La0.5Ti0.5O2介孔毫米球对磷酸盐的吸附等温线,得到的拟合参数见表3. La0.5Ti0.5O2介孔毫米球对磷的吸附量随着磷酸盐浓度的增加而逐渐增加,但增加速率逐渐变缓. 在低浓度磷酸盐溶液范围内的磷几乎被La0.5Ti0.5O2介孔毫米球完全吸附去除,这是因为在处理低浓度磷时,La0.5Ti0.5O2介孔毫米球吸附位点相对充足,可以足够吸附溶液中的磷. 但随着磷浓度的增加,吸附位点保持不变,La0.5Ti0.5O2介孔毫米球不能够完全吸附溶液中的磷,吸附量增加幅度随之变小,当吸附位点被占满后,吸附量几乎保持不变,从而吸附趋于饱和. 从拟合结果来看,两种模型均能较好地描述吸附过程,Freundlich模型的R2=0.974,Langmuir模型的R2=0.992,更接近于1. Langmuir模型更符合La0.5Ti0.5O2介孔毫米球对磷的吸附过程,说明La0.5Ti0.5O2介孔毫米球对于磷酸盐的吸附是单分子层吸附,这与已有报道的镧改性吸附剂一致[26 − 27]. La0.5Ti0.5O2介孔毫米球的理论最大磷吸附量为75.8 mg·g−1. 式(4)中的n值表示与吸附强度有关的常数,Freundlich模型得到的1/n小于1,表明磷易于吸附在La0.5Ti0.5O2介孔毫米球上[28]. 与其它含La吸附剂相比(表4), La0.5Ti0.5O2 表现出较好的磷吸附性能,磷的吸附量和P/La比(1.24)高于大多数含La吸附剂. 此外,La0.5Ti0.5O2对低浓度磷(<30 mg·L−1)的吸附能力明显强于其它含La吸附剂,这使其有望用于处理河流和湖泊的实际含磷水体治理.
表 2 La0.5Ti0.5O2介孔毫米球吸附磷的动力学参数Table 2. Kinetic parameters of phosphorus adsorption by LaxTi1-xO2 mesoporous millispheres温度/℃Temperature 准一级动力学Pseudo-first order model 准二级动力学Pseudo-second order model qe/(mg·g−1) k1 R2 qe/(mg·g−1) k2 R2 25 ℃ 17.5 6.25×10−2 0.978 22.1 2.74×10−3 0.994 表 3 Langmuir和Freundlich模型拟合参数Table 3. Fitting related parameters of Langmuir and Freundlich温度/℃Temperature Langmuir模型Langmuir model Freundlich模型Freundlich model qm/(mg·g−1) R2 KL/(L·mg−1) KF/(mg·g−1) 1/n R2 25 75.8 0.992 0.0176 2.49 0.671 0.974 表 4 吸附剂吸附性能对比Table 4. Comparation of adsorption capacity of adsorbents吸附剂Adsorbents 初始浓度/(mg ·L−1P)Initial concentration pH 投加量/(g·L−1)Dosage 比表面积/(m2·g−1)Specific surface area 吸附容量/(mg ·g−1P)Adsorption capacity 磷镧比P/La 参考文献References La-多孔沸石 5—60 7.02 2.0 52.75 14.8 0.95 [29] La(OH)3 5—500 11.3 12.5 153 107.5 0.84 [30] Fe3O4/50%-La(OH)3 1—10 7.0 0.1 190 52.7 0.68 [31] FeOOH/La-磁铁矿 2—120 6.8 1.0 85.8 44.8 1.30 [32] La-功能化SiO2气凝胶 10—120 5.0 1.0 192 69.4 0.85 [33] La(OH)3-改性蛭石 1—100 7.0 1.0 39.1 79.6 0.85 [27] La-介孔硅小球 5—80 6.0 0.5 67.4 44.8 0.67 [34] La(OH)3-改性硅藻石 10—100 6.8 0.5 74.1 58.7 2.39 [35] 沸石-氢氧化镧复合吸附剂 10—500 7.74 0.1 55.7 71.9 1.48 [6] 碳酸镧-阴离子交换树脂 5—60 7.0 0.5 — 77.4 0.73 [5] La-碳纳米管 0—100 12.0 0.2 — 96.3 — [4] LaOH-活性炭纤维 10—70 2.0 0.25 — 15.3 1.30 [36] LaFe-活性炭纤维 5—60 4.0 1.0 — 29.4 — [37] La0.5Ti0.5O2 1—70 3.0 1.0 105 75.8 1.24 本研究 2.3 吸附机理
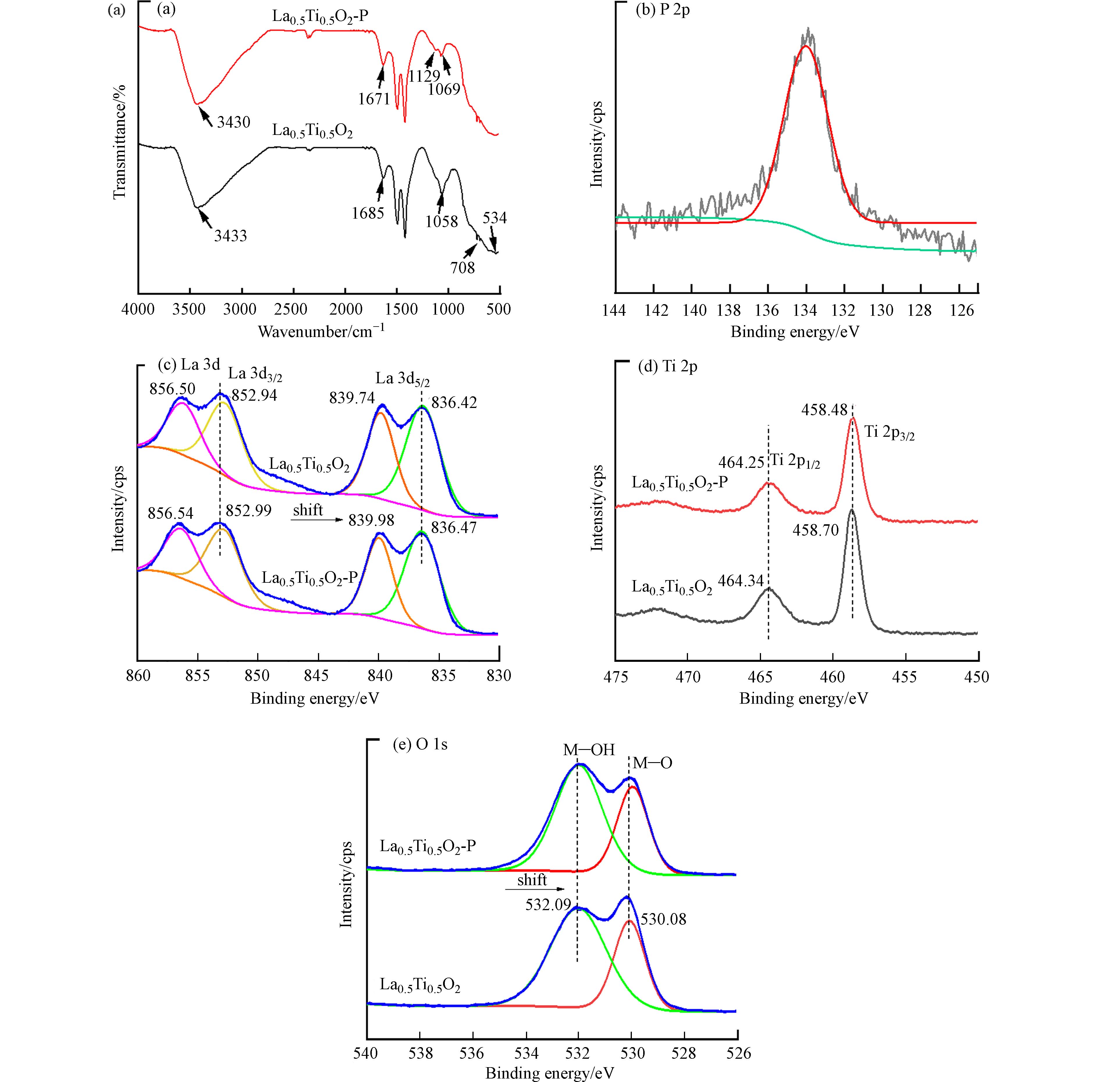
通过FR-IR谱图分析发现(图7a),在吸附磷的样品中检测到位于1129 cm−1处的P—O不对称拉伸振动[27]. La0.5Ti0.5O2吸附磷后,其位于534 cm−1处的特征峰消失,这是因为受到O—P—O的不对称拉伸振动影响. 此外,La0.5Ti0.5O2光谱中位于3433 cm−1和1685 cm−1处的O—H的拉伸和弯曲振动峰分别红移到3430 cm−1和1671 cm−1,表明La0.5Ti0.5O2表面的—OH参与了吸附磷过程,可能是由于La—OH中的—OH与部分磷酸盐发生了配体交换[29]. 为进一步探究La0.5Ti0.5O2与磷酸盐之间的相互作用,用XPS分析材料吸附磷酸盐前后结构变化,结果见图7(b)—(e). 吸附磷的La0.5Ti0.5O2样品的XPS光谱中检测到位于133.8 eV处的特征性P 2p峰(图7b),表明La0.5Ti0.5O2成功吸附了磷酸盐. 在吸附磷之前,在La 3d谱图中出现两特征峰(图7c),这两组峰分别是La 3d 3/2=856.50 eV、852.94 eV和La 3d 5/2=839.74 eV、83.42 eV. 在吸附磷之后,La 3d 3/2和La 3d 5/2的结合能移到较高的数值,分别为La 3d 3/2=856.54 eV、852.99 eV和La 3d 5/2=839.98 eV、836.47 eV,表明La价带上可能发生了电子转移且形成了La—O—P的内球络合物LaPO4[30]. 有研究表明P—O键具有强吸电子效应,其与镧(氢)氧化物结合后,导致镧电子密度降低,La 3d电子的结合能升高[38],这与本研究的现象一致. 此外,吸附后的La0.5Ti0.5O2的Ti 2p 2/3和Ti 2p 1/2也向较低的数值移动,在Ti 2p 2/3处的特征峰由458.70 eV移动到458.48 eV,在Ti 2p 1/2的特征峰由464.34 eV移动至464.25 eV(图7d),这可能是由于吸附剂表面的—OH键与磷酸盐之间发生了交换反应引起[31]. 由图5b可知,初始pH在零电荷点pHpzc=7.61以下,吸附稳定后的pH值均有一定程度的升高,进一步表明吸附过程表面-OH与磷酸盐发生配体交换反应. 吸附前,La0.5Ti0.5O2在532.09 eV和530.08 eV处出现了O 1s的两个特征峰(图7e),分别归属于La—OH和La—O[27]. 吸附后,532.09 eV处的特征峰强度增强,而530.08 eV处的特征峰强度减弱,进一步说明吸附的磷酸根形成了新的化学键La—O—P,改变了La—O键的化学环境. 结合文献报道和以上分析结果,La0.5Ti0.5O2通过配体交换吸附磷的过程可以表示如下[7, 29]:
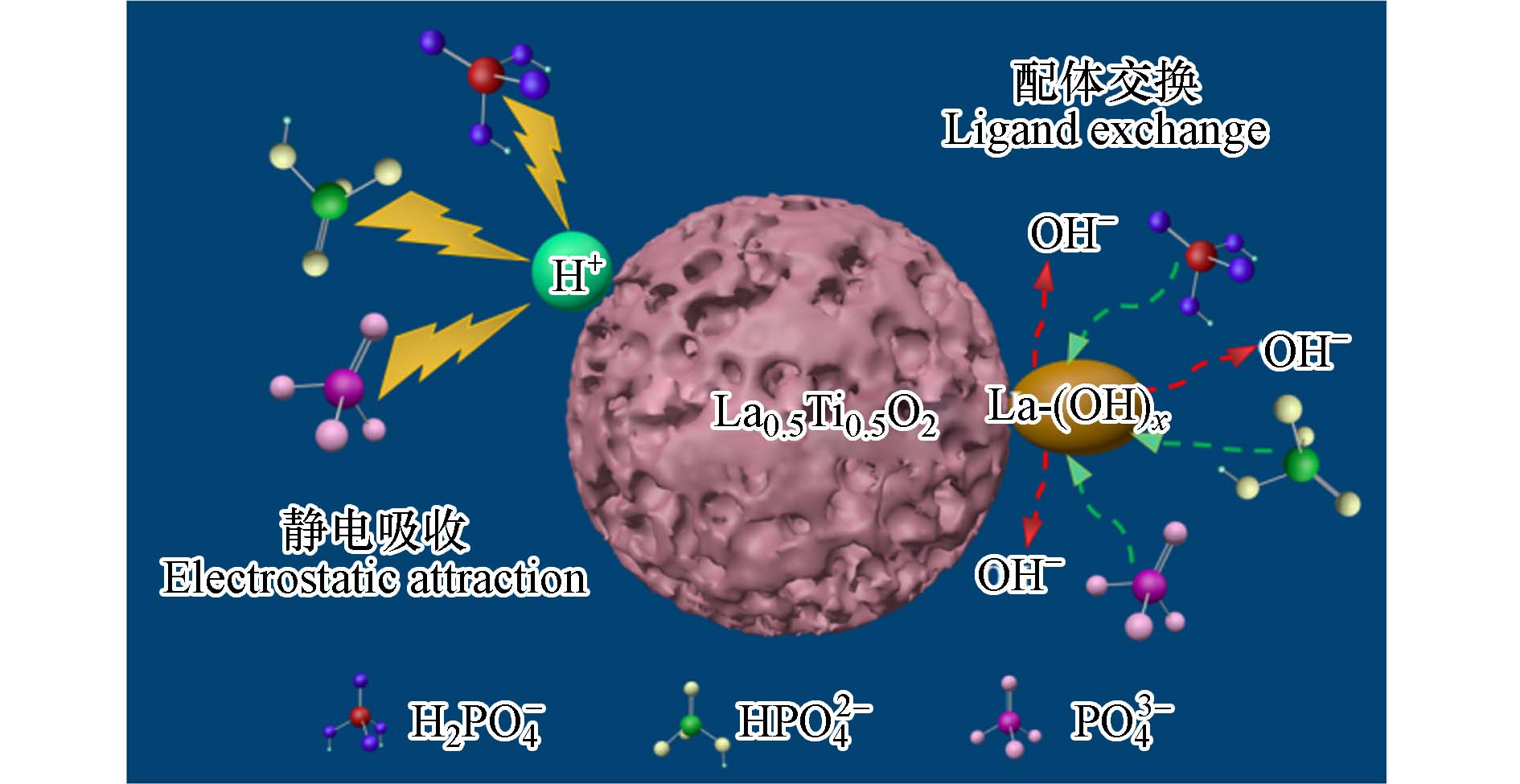
stringUtils.convertMath(!{formula.content}) (5) stringUtils.convertMath(!{formula.content}) (6) stringUtils.convertMath(!{formula.content}) (7) La0.5Ti0.5O2介孔毫米球对磷酸盐的吸附过程如图8所示. 在吸附过程中,静电吸引(物理吸附)和配体交换(化学吸附)都起着重要作用. 静电吸引受到溶液pH值的显著影响. 当pH<pHpzc时,La0.5Ti0.5O2表面发生质子化,H+浓度增加,吸附位点与磷酸盐之间的吸附力增强. 当pH>pHpzc时,La0.5Ti0.5O2表面脱质子化,OH−浓度增加,吸附位点与磷酸盐之间的排斥力增强. 配体交换过程[式(5)—(7)]也受到水溶液pH的极大影响. 提高pH值会大幅提高OH−的浓度,这不利于吸附剂与磷酸盐的配体交换过程. 配体交换机制也可以解释La0.5Ti0.5O2对磷酸盐的高选择性,与常见的阴离子Cl−、NO3−、SO42−和HCO3−等相比,配体交换反应为磷酸盐与La0.5Ti0.5O2结合提供了非常强的驱动力.
3. 结论(Conclusion)
(1) 本研究制备合成的介孔钛镧双金属氧化物毫米球,在La:Ti=1:1,煅烧温度为400 ℃时具有良好的吸附性能,其平均孔径为3.71 nm,具有丰富的孔结构、高比表面积,对磷酸根的吸附容量可以达到75.8 mg·g−1.
(2) 溶液pH的升高会抑制La0.5Ti0.5O2介孔毫米球的对磷的吸附性能;吸附除磷效果随着吸附剂投量的增加而增加,但投量为1.5 g·L−1之后,对磷去除效果提升较小;水体中常见的共存离子Cl−、NO3−对吸附除磷效果干扰不大,而SO42−和HCO3−对La0.5Ti0.5O2吸附除磷的抑制作用明显.
(3) La0.5Ti0.5O2介孔毫米球对磷的吸附过程符合Langmuir模型和准一、准二级动力学模型,说明La0.5Ti0.5O2介孔毫米球对磷酸盐的吸附是单分子层吸附,对磷酸盐吸附过程是物理化学吸附.
4) 静电吸附和配体交换反应共同决定了La0.5Ti0.5O2介孔毫米球对磷的吸附,两种作用机制均受pH值影响,pH值越低,吸附性能越好.
-
表 1 拟合不同光电阴极的EIS数据
Table 1. EIS data fitted by different photocathodes
光电阴极Photocathodes R0/Ω R1/Ω R2/Ω BiOBr 4.24 6.16×10−3 1.60×10−6 5-Cu-BiOBr 4.55 4.92×10−3 1.95×10−6 15-Cu-BiOBr 4.30 3.62×10−3 1.19×10−6 25-Cu-BiOBr 4.51 5.33×10−3 8.45×10−5 -
[1] LU N, WANG L Q, LV M, et al. Graphene-based nanomaterials in biosystems [J]. Nano Research, 2019, 12(2): 247-264. doi: 10.1007/s12274-018-2209-3 [2] 陶玥彤, 李茹莹. 生物电化学系统对河道沉积物中抗生素的强化去除 [J]. 环境科学学报, 2021, 41(4): 1383-1392. TAO Y T, LI R Y. Enhanced removal of antibiotics from the river sediments by bioelectrochemical systems [J]. Acta Scientiae Circumstantiae, 2021, 41(4): 1383-1392(in Chinese).
[3] 郑乐媚, 关亦玮, 文定, 等. BiOBr/GO复合纳米光催化剂的制备及可见光下降解环丙沙星废水 [J]. 环境化学, 2020, 39(8): 2137-2146. ZHENG L M, GUAN Y W, WEN D, et al. Preparation of BiOBr/GO composition nanocatalysts and application of degradation of ciprofloxacin wastewater in visible light [J]. Environmental Chemistry, 2020, 39(8): 2137-2146(in Chinese).
[4] CHEN J F, HU Y Y, HUANG W T, et al. Biodegradation of oxytetracycline and electricity generation in microbial fuel cell with in situ dual graphene modified bioelectrode [J]. Bioresource Technology, 2018, 270: 482-488. doi: 10.1016/j.biortech.2018.09.060 [5] CHEN J F, YANG Y W, LIU Y Y, et al. Bacterial community shift and antibiotics resistant genes analysis in response to biodegradation of oxytetracycline in dual graphene modified bioelectrode microbial fuel cell [J]. Bioresource Technology, 2019, 276: 236-243. doi: 10.1016/j.biortech.2019.01.006 [6] LIANG B, CHENG H Y, KONG D Y, et al. Accelerated reduction of chlorinated nitroaromatic antibiotic chloramphenicol by biocathode [J]. Environmental Science & Technology, 2013, 47(10): 5353-5361. [7] WU D, SUN F Q, ZHOU Y. Degradation of chloramphenicol with novel metal foam electrodes in bioelectrochemical systems [J]. Electrochimica Acta, 2017, 240: 136-145. doi: 10.1016/j.electacta.2017.04.059 [8] ZHANG S, YANG X L, LI H, et al. Degradation of sulfamethoxazole in bioelectrochemical system with power supplied by constructed wetland-coupled microbial fuel cells [J]. Bioresource Technology, 2017, 244: 345-352. doi: 10.1016/j.biortech.2017.07.143 [9] HOU Y P, LUO H P, LIU G L, et al. Improved hydrogen production in the microbial electrolysis cell by inhibiting methanogenesis using ultraviolet irradiation [J]. Environmental Science & Technology, 2014, 48(17): 10482-10488. [10] HOU Y P, YUAN G Y, QIN S M, et al. Photocathode optimization and microbial community in the solar-illuminated bio-photoelectrochemical system for nitrofurazone degradation [J]. Bioresource Technology, 2020, 302: 122761. doi: 10.1016/j.biortech.2020.122761 [11] HOU Y P, GAN Y Y, YU Z B, et al. Solar promoted azo dye degradation and energy production in the bio-photoelectrochemical system with a g-C3N4/BiOBr heterojunction photocathode [J]. Journal of Power Sources, 2017, 371: 26-34. doi: 10.1016/j.jpowsour.2017.10.033 [12] TU L L, HOU Y P, YUAN G Y, et al. Bio-photoelectrochemcial system constructed with BiVO4/RGO photocathode for 2, 4- dichlorophenol degradation: BiVO4/RGO optimization, degradation performance and mechanism [J]. Journal of Hazardous Materials, 2020, 389: 121917. doi: 10.1016/j.jhazmat.2019.121917 [13] QIN S M, HOU Y P, YUAN G Y, et al. Different refractory organic substances degradation and microbial community shift in the single-chamber bio-photoelectrochemical system [J]. Bioresource Technology, 2020, 307: 123176. doi: 10.1016/j.biortech.2020.123176 [14] 周奥, 曹新强, 顾彦, 等. 以生物炭为内核的BC@BiOBr催化剂的制备及可见光光催化性能 [J]. 环境化学, 2019, 38(2): 235-242. ZHOU A, CAO X Q, GU Y, et al. Preparation of BC@BiOBr catalyst with biochar as core and its visible light photocatalytic performance [J]. Environmental Chemistry, 2019, 38(2): 235-242(in Chinese).
[15] 李冬梅, 梁奕聪, 卓涌淇, 等. 铋修饰BiOBr/g-C3N4异质结光催化剂合成及其可见光催化性能研究 [J]. 环境科学学报, 2021, 41(3): 960-968. LI D M, LIANG Y C, ZHUO Y Q, et al. Synthesis of Bi-decorated BiOBr/g-C3N4 heterojunction photocatalyst and its visible light-driven photocatalytic performance [J]. Acta Scientiae Circumstantiae, 2021, 41(3): 960-968(in Chinese).
[16] 叶少琛, 徐向阳, 何光裕, 等. CuxZn1-xS/RGO复合材料的制备及其光催化降解环丙沙星性能研究[J]. 环境化学, 2020, 39(7): 1977-1984. YE S C, XU X Y, HE G Y, et al. Preparation and performance of CuxZn1-xS/RGO composite for photocatalytic degradation of CIP[J]. Environmental Chemistry, 2020, 39(7): 1977-1984(in Chinese). Environmental chemistry, 2020, 39(07): 1977-1984 (in Chinese).
[17] WANG H, YONG D Y, CHEN S C, et al. Oxygen-vacancy-mediated exciton dissociation in BiOBr for boosting charge-carrier-involved molecular oxygen activation [J]. Journal of the American Chemical Society, 2018, 140(5): 1760-1766. doi: 10.1021/jacs.7b10997 [18] HILL D M, MEYER H M 3rd, WEAVER J H, et al. Cu adatom interactions with single- and polycrystalline Bi2Ca1+xSr2-xCu2O8+y and YBa2Cu3O7-x [J]. Physical Review. B, Condensed Matter, 1988, 38(16): 11331-11336. doi: 10.1103/PhysRevB.38.11331 [19] LV X C, YAN D Y S, LAM F L Y, et al. Solvothermal synthesis of copper-doped BiOBr microflowers with enhanced adsorption and visible-light driven photocatalytic degradation of norfloxacin [J]. Chemical Engineering Journal, 2020, 401: 126012. doi: 10.1016/j.cej.2020.126012 [20] SENGOTTAIYAN C, KALAM N A, JAYAVEL R, et al. BiVO4/RGO hybrid nanostructure for high performance electrochemical supercapacitor [J]. Journal of Solid State Chemistry, 2019, 269: 409-418. doi: 10.1016/j.jssc.2018.10.011 [21] WANG L, LIU Y L, WANG C, et al. Anoxic biodegradation of triclosan and the removal of its antimicrobial effect in microbial fuel cells [J]. Journal of Hazardous Materials, 2018, 344: 669-678. doi: 10.1016/j.jhazmat.2017.10.021 [22] YAN W F, XIAO Y, YAN W D, et al. The effect of bioelectrochemical systems on antibiotics removal and antibiotic resistance genes: A review [J]. Chemical Engineering Journal, 2019, 358: 1421-1437. doi: 10.1016/j.cej.2018.10.128 [23] LV L Y, LI W G, WU C D, et al. Microbial community composition and function in a pilot-scale anaerobic-anoxic-aerobic combined process for the treatment of traditional Chinese medicine wastewater [J]. Bioresource Technology, 2017, 240: 84-93. doi: 10.1016/j.biortech.2017.01.053 [24] BRIDGES C M, GAGE D J. Development and application of aerobic, chemically defined media for Dysgonomonas [J]. Anaerobe, 2021, 67: 102302. doi: 10.1016/j.anaerobe.2020.102302 [25] 王思祺, 严伟富, 赵峰, 等. 基于微生物电化学技术的萘普生高盐废水处理 [J]. 环境化学, 2020, 39(4): 1137-1144. WANG S Q, YAN W F, ZHAO F, et al. Treatment of naproxen high-salt wastewater based on microbial electrochemical technology [J]. Environmental Chemistry, 2020, 39(4): 1137-1144(in Chinese).
[26] MORRIS J M, JIN S, CRIMI B, et al. Microbial fuel cell in enhancing anaerobic biodegradation of diesel [J]. Chemical Engineering Journal, 2009, 146(2): 161-167. doi: 10.1016/j.cej.2008.05.028 [27] ALEXANDRINO D A M, MUCHA A P, ALMEIDA C M R, et al. Biodegradation of the veterinary antibiotics enrofloxacin and ceftiofur and associated microbial community dynamics [J]. Science of the Total Environment, 2017, 581/582: 359-368. doi: 10.1016/j.scitotenv.2016.12.141 期刊类型引用(0)
其他类型引用(3)
-






 下载:
下载: