-
我国城市污水进水碳氮比(C/N)低的现象较为普遍,80%的污水处理厂BOD5/TN<3.6,仅有10%污水厂>4[1]。随着国家对污水出水总氮要求的日益提高,为达到稳定的脱氮效果,须通过外加碳源来弥补生物反硝化脱氮碳源的不足,因此增加了较多运营成本。葡萄糖、乙酸钠和甲醇作为主要碳源产品被投加于污水处理中,但也存在各自缺点:葡萄糖分子量大,冬季溶液黏度高,流动性差,污泥量较大;乙酸钠易结晶;甲醇属于易燃易爆品,对管理水平要求较高。
为降低外加碳源使用费用,研究和工程应用领域均开展了一些有益的尝试。通过对初沉和剩余污泥[2-6]、餐厨垃圾[7-9]等有机质进行机械破碎、厌氧发酵等方式处理后,对释放碳源进行回收再利用。但目前仍存在发酵液浓度低、溶解性COD与N、P元素分离、发酵液纯化与浓缩等问题,绝大多数工作仍止步于中试。在实际工作中,运营单位通过引入小股生化性优的果汁、甲醇等高浓度有机废水[10-11]用于补充主流废水处理中的碳源不足,获得了较好收益,但往往可遇不可求。此外,复合碳源[12-13]的开发亦为一个方向,张民权等[12]通过调整多种碳源配比,克服单一碳源劣势,同时在反硝化速率上可与乙酸钠相当。近2年,多种新型碳源的出现为水务行业提供了更多选择,其来源多为纯化后的工业副产品或复配品,主要成分为短链醇和糖类,目前来看,这类产品仍缺乏统一的行业规范,产品质量参差不齐,因此,在使用前对其进行小试评估非常关键。
本研究内容主要分为2部分:选取了3种新型碳源,BC5、BC6和BC8,以葡萄糖和乙酸钠为对比碳源,通过小试进行脱氮性能和经济性评估,优选出厂试碳源BC8;通过厂试评估BC8性能,以期达到污水运营“提质增效”之需求。
-
本试验共选取5种碳源,其中葡萄糖和乙酸钠为常规碳源,BC5、BC6和BC8为新型碳源。BC3为农业副产物短C3链醇类,主要成分为丙三醇;BC6为糖蜜经二次加工提纯产品,主要成分为多种糖类混合物;BC8为丙三醇和乙酸钠复配产品,详细参数见表1。所有碳源均稀释为10 000 mg/L COD液体碳源备用。
检测方法:总氮(TN):碱性过硫酸钾法消解紫外分光光度法;硝氮(NO3 −-N):麝香草酚分光光度法,TU-1810型紫外分光光度计;化学需氧量(COD):重铬酸钾法;溶解氧(DO)和pH:哈希HQ30D;污泥浓度:哈希HA16-TSS Portable。生物群落分析[14]:取厂试生化池末端污泥,采用高通量测序技术对生物膜污泥16S rRNA基因测序进行分析。采用Fast DNA spin试剂盒提取DNA, ETC Thermocycler进行PCR反应。采用Nobar_341F / Nobar_805R引物扩增16S rRNA基因的V3~V4区,所有扩增产物均采用测序系统测序(美吉生物,上海,中国)。
-
碳源优选小试:取生化池末端泥水混合物,取样检测硝氮和氨氮,氨氮需<1 mg/L,投加KNO3至硝氮达25~30 mg/L。缓慢搅拌释氧,待DO< 1 mg/L,将泥水混合物均匀分置于1 L烧杯内,按设定C/N值补充碳源(碳源稀释需至COD=10 000 mg/L取用),磁力搅拌均匀后,计时、取样。本试验最大反应时长240 min。污泥MLSS≈2.5 g/L(MLVSS/MLSS≈0.7),试验期内控制室温约20 ℃,每组设3个平行样。检测指标为COD、硝氮和总氮,水样经滤纸过滤后进行检测分析。
污泥反硝化速率测定方法:样品取自间歇式反硝化反应器,一次性投加基质后,从0时开始间隔一定的时间取样,直至设定反应时间结束,根据单位时间、单位体积去除硝氮量计算反硝化速率[15]。
厂试:本次厂试项目为某工业园区污水处理厂,设计规模5 000 m3/d,2组并联运行,工艺为AOAO,停留时间分别为5.5、10、3和1.5 h,投加碳源为葡萄糖(液体,55万 mg/L COD当量)。厂试选用新型碳源为BC8,对比组碳源为葡萄糖,碳源投加点为1 A,检测出水COD、氨氮、TN和TP。88 d厂试期内,室外气温−19~16 ℃,水温约20 ℃,污泥浓度范围4.2~6.0 g/L,MLVSS/MLSS范围0.4~0.6。
-
由于生化池污泥原投加碳源为葡萄糖,投加新型碳源后污泥存在适应期。不同投加C/N比对出水硝氮的影响,见图1。为使污泥稳定利用新碳源,在进行C/N比优选试验前,对待试验活性污泥采用新碳源培养7 d。图1可知,在投加C/N比为3~7时,所有碳源均随C/N比上升,出水中
NO−3 -N值呈逐步下降趋势。若以出水NO−3 -N≤10 mg/L为控制目标,不同碳源C/N比各异,乙酸钠和BC8的C/N比最小,为4.5;其次为BC5,C/N比为5;葡萄糖、BC6的C/N比最大,为7,该值与文献所述相近[7]。C/N越小则意味着去除单位硝氮所需外加碳源量越少,相应的脱氮成本更低。当要求极低出水硝氮值时,可进一步提高碳源C/N比,以乙酸钠、BC8为例,当投加C/N比达到6,出水硝氮值可降低至1 mg/L左右。但在实际运行中,如此低的出水硝氮值并无必要,此处将出水NO−3 -N≤10 mg/L所需C/N作为较优值并用于后续碳源评估试验中。 -
图2可知,在进水硝氮约30 mg/L时,较优C/N比条件下(乙酸钠、BC8为4.5, BC5为5,葡萄糖、BC6为7),出水硝氮和TN浓度随运行时间的延长逐步降低,经各自反应期后,最终出水硝氮和TN浓度呈如下排序:葡萄糖>BC6>BC5>BC8≈乙酸钠。其中,乙酸钠及其复配类碳源(BC8)反硝化脱氮效果较优,反应160 min后,出水TN可低至5~7 mg/L,C3醇类(BC5)居中,反应180 min后,出水TN<9 mg/L,糖类碳源(BC6和葡萄糖)反硝化效果相对较差,反应240 min后,出水TN约为12 mg/L,基本可满足一级A排放标准。
图3可知,反硝化速率随时间增加呈逐步下降趋势。乙酸盐类碳源(乙酸钠、BC8)的反硝化速率最快,最大值约21.6 mg
NO−3 -N/(L·h),丙三醇类(BC5)其次,最大值约15 mgNO−3 -N/(L·h)。糖类碳源的反硝化速率值相对较低,但BC6表现更佳,最大值可达11.5 mgNO−3 -N/(L·h),约为C6H12O6的1倍,这可能与BC6为多种糖的混合物有关。HAGMAN et al[16]研究发现,碳源多样性往往会导致污泥微生物种群多样性,如甲醇/乙酸钠复合型碳源脱氮性能会优于单一组分碳源。因此,复配碳源的开发对脱氮性能的提高是较好的切入点。 -
为评估投加碳源后可能造成的COD超标风险,测得污水中COD随时间的变化结果,见图4。随着运行时间增加,COD均呈逐步下降趋势。受不同碳源反硝化速率差异的影响,COD下降速率呈如下趋势: BC8≈乙酸钠>BC5>葡萄糖>BC6。常规碳源葡萄糖、乙酸钠在反应分别进行至180和100 min后,COD即可降至<50 mg/L。新型碳源中,BC8和BC5在反应分别进行至100和140 min后,COD亦可降至<50 mg/L,但新型碳源BC6,反应进行至240 min,COD达59 mg/L,且静置1夜,上清液COD值仍可达53 mg/L,高于一级A排放限值,这可能与BC6中存在部分难生物降解的COD有关。因此,新型碳源BC5、BC8均可用于反硝化生物过程,但需警惕BC6造成的COD超标风险。
-
通过小试研究可知,BC8除具备较优脱氮性能外,经济性上同样具备一定优势,较优投加C/N比下,BC8可较葡萄糖使用成本降低12%左右。因此, BC8将作为厂试碳源进行进一步评估,相关工作论述如下。
生化系统进出水COD、氨氮和TN等指标,见表2。由于进水COD可生化性差,主要由后段Fenton系统处理,生化单元主要功能表现为脱氮。厂试初期,活性污泥对BC8表现出不适应性,与葡萄糖对照组相比,生化出水COD和TN分别提高约14和3.33 mg/L,增加幅度达10%和66%,同时氨氮和TP也略有增加,分别提高约0.12和0.02 mg/L。经过约15 d适应期, BC8投加组与葡萄糖对比组出水水质已基本相当,出水TN可控制在5 mg/L左右。稳定期内,BC8日均用量为350 kg(总COD=301.22 kg),仅为葡萄糖日均用量的38.2%(总COD=419.83 kg)。图5可知,稳定期内新型碳源投加费用均值约为葡萄糖的92%,表现出较佳经济性。随着近期化工原材料价格的大幅上涨,BC8的经济性将进一步凸显。值得一提的是,尽管运行期内室外温度最低至−19 ℃,但BC8依旧表现出较好流动性,投加稳定。
-
为对比BC8与葡萄糖碳源对活性污泥菌种的影响,门水平微生物群落多样性分析结果,见图6。以葡萄糖、BC8为碳源时,微生物中优势菌门主要有绿弯菌门(Chloroflexi)、变形菌门(Proteobacteria)、放线菌门(Patescibacteria和Actinobacteria)和酸杆菌门(Acidobacteria),其值分别为32.17%/34.88%、21.94%/18.52%、19.75%/18.16%、11.69%/16.05%和4.99%/4.41%。变形菌门是参与脱氮除磷和有机物降解的主要菌种,绿弯菌门是微生物反硝化脱氮过程中主要参与菌种,另有研究发现[17-18],Patescibacteria是厌氧氨氧化耦合反硝化启动的主要菌门之一,据认为适应厌氧发酵代谢和潜在共生生化方式,生物膜内层的厌氧层为其提供了适宜生产环境,起着重要的反硝化作用。为更加详细地分析系统中的微生物,图7将相对丰度>1%的属进行了对比, Saccharimonadales、Ardenticatenales和Hyphomicrobium为优势菌属,分属于Patescibacteria门[19]、绿弯菌门和变形菌门,在以葡萄糖和BC8为碳源条件下,占比分别为17.16%/16.26%、10.08%/11.53%和6.88%/6.54%,结合高效反硝化菌群[20-21] Pseudomonas、Comamonas在BC8污泥中的丰度分别为1.91%和1.85%,较葡萄糖为碳源时高约1倍,这或可解释BC8具有更高脱氮效率。
-
(1)在小试环节,所有碳源出水TN均可满足一级A标准,其中NaAc和BC8最优,160 min后出水TN可低至5~7 mg/L。反应期内最大反硝化速率值相比,呈如下趋势:BC8≈乙酸钠>BC5>BC6>葡萄糖,BC8最大值约为21.6 mg
NO−3 -N/(L·h)。各碳源较优投加C/N比:乙酸钠和BC8为4.5, BC5为5,葡萄糖和BC6为7,BC8相对使用成本最低。除BC6存在COD超标风险外,其余碳源无超标风险。综合上述结果,BC8作为优选碳源用于厂试评估。(2)在88 d厂试期内,生化池活性污泥对BC8的适应期约15 d,保证系统出水COD、氨氮和TN等关键指标与葡萄糖对比组的相关指标基本相当的前提下,BC8日均用量仅为350 kg,为葡萄糖同期日均用量的38.2%,综合使用成本约为葡萄糖的92%。此外,考虑到BC8与NaAc的反硝化速率相当,后期亦将尝试BC8用于反硝化滤池工艺的评价。
(3)对厂试活性污泥微生物群落多样性分析表明,碳源类型对微生物优势菌门类影响不大,但有助于增加Pseudomonas、Comamonas等反硝化菌群丰度,提高系统反硝化能力。
新型碳源用于脱氮的经济性对比及生物群落分析
Economic comparison and microbial community analysis of nitrogen removal with new carbon sources
-
摘要: 以淄博某污水厂生化出水为原水,通过活性污泥法反硝化小试试验,重点考察了3种新型碳源(农产品副产物BC5、制糖副产物二次加工品BC6和乙酸盐复配产品BC8)和2种常规碳源(C6H12O6、NaAc)的反硝化脱氮效果,以确定较优厂试新型碳源。小试结果表明,BC8在较优投加C/N为4.5时,可在160 min内将进水总氮由32.4降至<7 mg/L,最大反硝化速率达21.6 mg
NO−3 -N/(L·h)。在88 d厂试期内,在TN约5 mg/L同等出水水质条件下,BC8日均用量和使用成本仅为葡萄糖的38.2%和92%,经济性良好。对厂试活性污泥微生物群落多样性分析表明,碳源类型对微生物优势菌门类影响不大,但有助于提高Pseudomonas、Comamonas等反硝化菌群丰度。Abstract: A laboratory denitrification test was performed for the biological treatment of the secondary biochemical effluent of a wastewater treatment plant in Zibo. Five external carbon sources, including conventional carbon sources (glucose, sodium acetate) and new carbon sources (BC5, BC6 and BC8), were investigated through batch denitrification experiments by the activated sludge process. The results of the laboratory test showed that BC8 performed best synthetically. When the carbon source changed from glucose to BC8, the influent TN could be reduced from 32.4 mg/L to <7 mg/L within 160 minutes when the C/N ratio was 4.5 and the maximum value of denitrification rate was 21.6 mg NO3--N/(L·h). Furthermore, during 88 days’ plant test, the average daily dose and cost of BC8 were only 38.2 % and 92 % of glucose. Analysis of microbial community diversity in activated sludge showed that carbon source type had little effect on the dominant microbial bacteria. However, it was helpful to increase the abundance of denitrifying bacteria such as Pseudomonas and Comamonas.-
Key words:
- new carbon source /
- activated sludge process /
- denitrification /
- plant test /
- microbial community
-
我国在过去的几十年里,由于金属的大量开采和冶炼[1]、污水灌溉[2]、化肥的不合理施用[3],镉砷在农田土壤中不断地积累。镉砷是毒性较大的重金属,农田土壤中重金属总量超标现象会通过食物链对生态系统和人类的健康构成威胁。根据原环境保护部和国土资源部2014年4月公布的《全国土壤污染状况调查公报》[4],全国镉污染物点位超标率为7.0%,位居重金属污染物榜首;砷污染物点位超标率为2.7%,砷超标的问题也不容忽视。因此,土壤镉、砷超标的环境问题亟待解决。
修复重金属污染农田有多种修复技术,其中使用修复材料将农田土壤的重金属钝化的技术因其具有成本低廉、修复时间短、效果显著的优点[5],具有广泛的应用前景。然而,GONG等[6]认为,这些钝化技术的研究大多停留在条件容易控制的实验室研究阶段,实际应用条件的复杂性可能会影响修复效果及可行性。近年来,针对镉污染土壤现场修复有效的钝化材料包括生物炭材料[7]、磷酸盐材料[8]、黏土矿物[9]等,黏土矿物因其来源丰富、成本低廉、效果显著等特点已被广泛研究[6]。TAHERVAND等[10]发现,黏土矿物具有很强的吸附重金属的能力,但黏土矿物对重金属的吸附存在选择性。目前,研究用黏土矿物进行砷的固定修复的研究比较少,砷污染土壤的修复材料以铁基材料为主[11]。
镉砷是2种性质极不相同的元素,农田重金属污染大多是复合污染,适合镉单一污染修复的材料和适合砷单一污染修复的材料能否用于农田镉、砷复合污染修复尚有待研究。国内外的学者们普遍研究单一修复材料对农田重金属的钝化效果,而不同修复材料之间的修复效果缺乏比较。因此,本研究比较分析了不同修复材料(硅藻土、膨润土、海泡石、人造沸石)和农田调理剂对农田土壤镉、砷的钝化效果,探究了修复材料处理后土壤中的镉、砷的形态以及土壤理化性质的变化,通过种植水稻并检测水稻内的镉、砷含量来检验修复效果,从而为镉砷污染农田土壤现场修复提供参考。
1. 材料与方法
1.1 供试土壤与供试材料
供试土壤场地位于中国广东省佛山市三水区,农田大小约为6 660 m2,黄棕色黏质土,选取其中的42个点对农田的基本情况进行分析,土壤的基本理化性质如下:总镉0.95~1.50 mg·kg−1,总砷11.41~17.06 mg·kg−1,总铅30.92~42.82 mg·kg−1,总锌39.35~69.70 mg·kg−1,速效磷16.9~86.1 mg·kg−1,碱解氮73.2~117 mg·kg−1,有机质25.7~95.4 g·kg−1,阳离子交换量4.33~7.12 cmol·kg−1,pH为5.22~5.70。供试的修复材料有硅藻土、膨润土、海泡石、人造沸石和农田调理剂,均为化学纯,粒径均在微米级;农田调理剂是由硅、镁、磷等元素构成的复合材料。供试的水稻品种为油牙占。
1.2 实验设计与样品采集
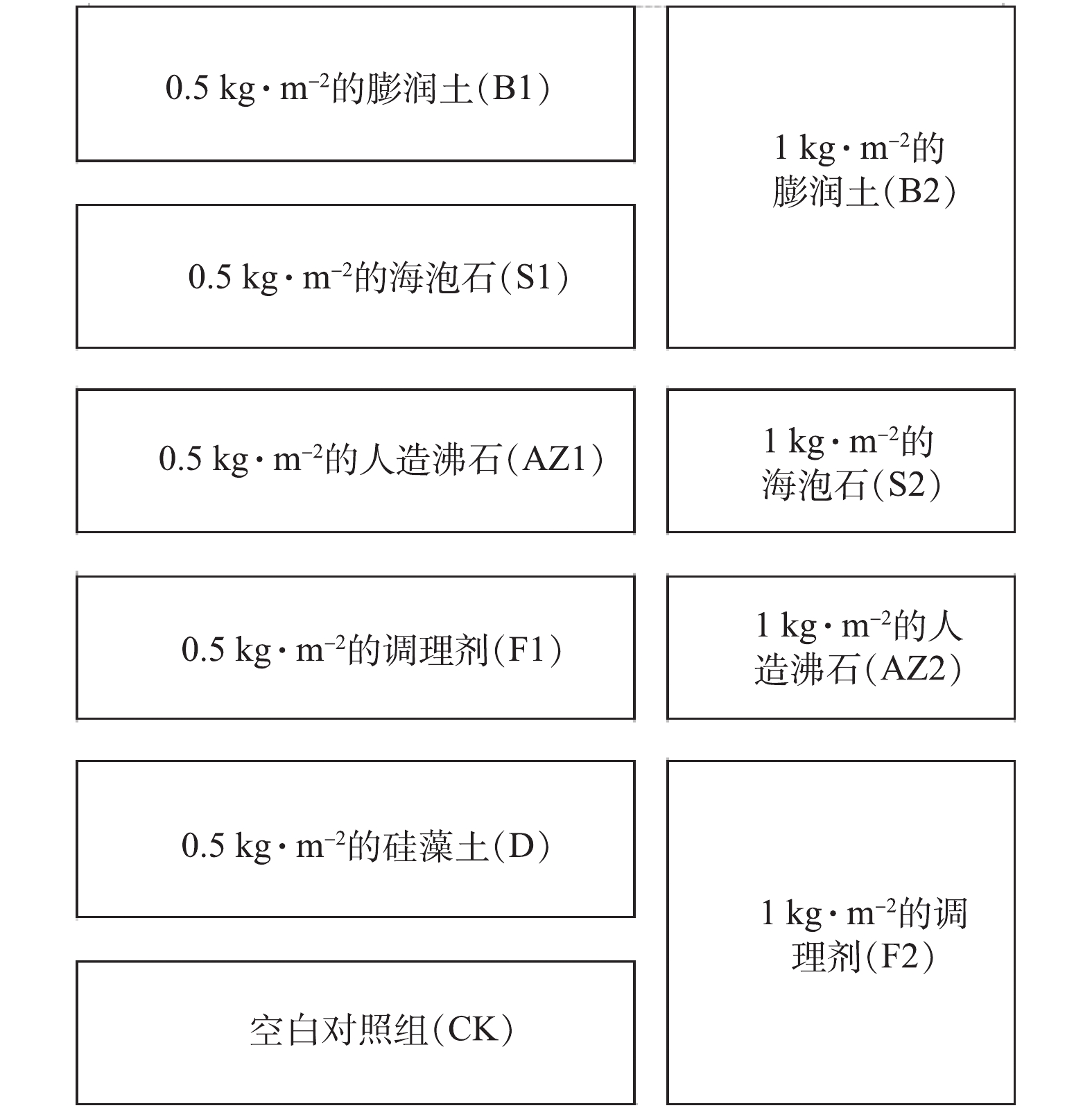
修复材料处理方法如图1所示。育苗工作完成后,投加修复材料7 d后插秧,修复材料处理10 d后(插秧3 d后)施加尿素,修复材料处理17 d和24 d后施加氮磷复合肥。从插秧前到水稻分蘖期期间都是淹水处理,保证田间持水量达到60%~80%,到水稻分蘖数足够的时候开始晒田。
在修复材料处理30 d(水稻秧苗期)、60 d(分蘖期)、100 d(成熟期)时按蛇形取样法随机采集每块实验田的土壤样品,然后进行风干处理,在水稻成熟后按蛇形取样法随机采集水稻样品,每块实验田采集20株水稻。
1.3 分析方法
土壤重金属总量的测定参考电感耦合等离子体质谱法[12];土壤重金属有效形态含量的测定参考电感耦合等离子体质谱法[13];Cd和As形态分布的测定参考Tessier提出的顺序提取程序(SEP)[14];参考钼锑抗分光光度法[15]检测土壤速效磷含量;参考《森林土壤氮的测定》[16]检测土壤碱解氮含量;参考分光光度法[17]检测土壤有机质含量;参考分光光度法[18]检测土壤阳离子交换量;参考《土壤pH的测定》[19]检测土壤的pH;参考《食品中镉的测定》[20]和《食品中总砷及无机砷的测定》[21]测定水稻中Cd和As的含量。
2. 结果与讨论
2.1 实验田各时期重金属总量
表1为实验田各时期Cd和As总量的平均值,总Cd含量高于风险筛选值,低于风险管控值,可能存在食用农产品不符合质量安全标准等土壤污染风险[22]。理论上,钝化材料的投加不会影响重金属在土壤中的总量,经检验,各组别的总Cd和总As的含量之间无显著差异(P<0.05)。土壤重金属总量在秧苗期、分蘖期、成熟期之间也无显著差异(P<0.05)。
表 1 实验田各时期Cd和As总量Table 1. Total cadmium and arsenic content in paddy field during different periodsmg·kg−1 样品 总Cd浓度 总As浓度 秧苗期 分蘖期 成熟期 秧苗期 分蘖期 成熟期 CK 1.22 1.13 1.16 14.10 14.05 14.28 D 1.16 1.13 1.13 13.20 13.62 14.01 F1 1.06 1.08 1.15 17.06 14.06 14.15 AZ1 1.06 1.09 1.07 16.84 13.49 13.83 S1 1.12 1.11 1.01 15.66 13.25 13.37 B1 1.10 1.09 0.99 15.19 13.24 13.32 F2 1.09 1.12 1.02 15.76 13.07 13.94 AZ2 1.07 1.12 1.00 13.96 12.81 12.85 S2 1.05 1.11 0.97 14.02 12.77 11.44 B2 0.99 1.10 0.95 16.76 11.41 11.17 2.2 钝化材料对DTPA提取重金属有效性的影响
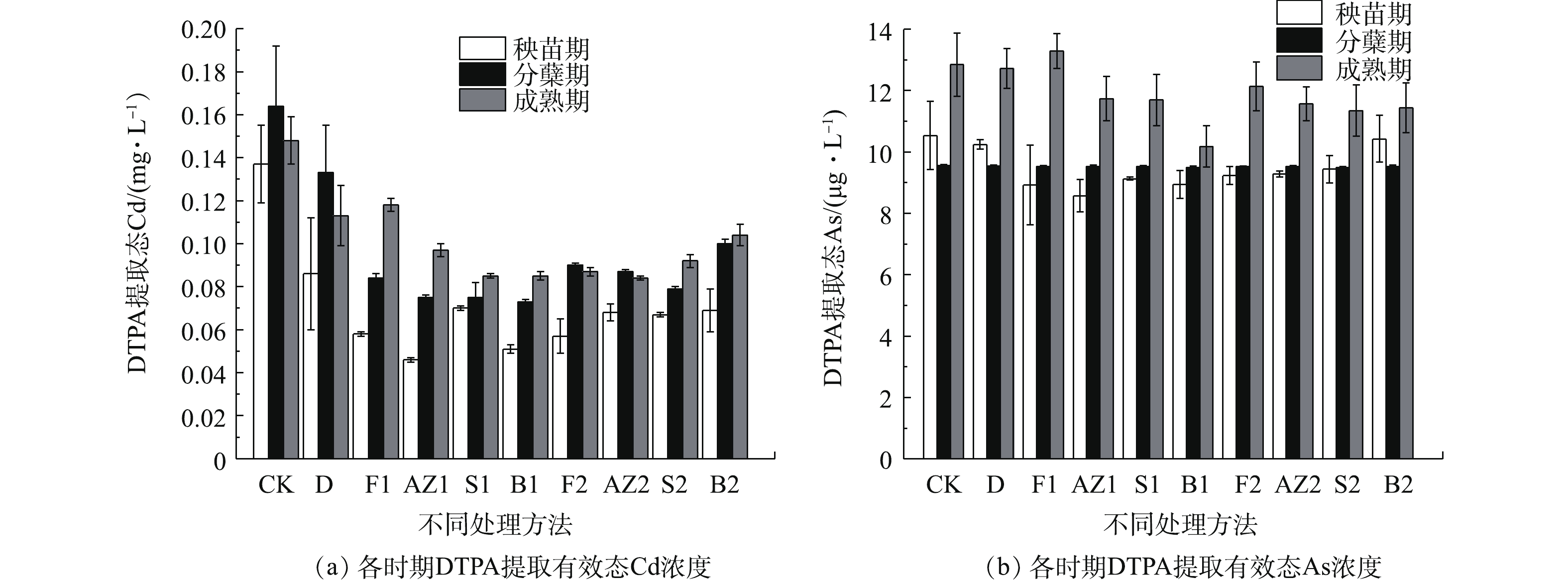
1)钝化材料对DTPA提取Cd有效性的影响。水稻的秧苗期、分蘖期、成熟期的DTPA浸出的平均Cd浓度如图2(a)所示,从秧苗期到分蘖期浸出液的平均Cd浓度有所提升,其原因可能是秧苗期水稻淹水程度较高,分蘖期水稻淹水程度较低,淹水程度高可以降低水稻吸收重金属Cd的效率[23-24]。跟CK对比,各种材料的浸出Cd浓度下降了20.3%~43.2%,S1、S2在处理初期就有较好的钝化效果,而F1和F2在成熟期的钝化效果最好,其原因可能是海泡石处理后迅速提高了土壤的pH和土壤中酶的活性[24],从而提高土壤中Cd的稳定性,而调理剂可能是通过与Cd形成磷酸盐沉淀,所以反应时间更长。
2)钝化材料对DTPA提取As有效性的影响。水稻的秧苗期、分蘖期、成熟期的DTPA浸出的平均As浓度如图2(b)所示,空白对照组浸出液的平均As浓度没有随时间发生显著变化,其他修复材料处理后浸出液的平均As浓度变化趋势与CK保持一致。跟CK相比,各组修复材料对砷都没有明显的修复效果,但维持着土壤中有效形态的As含量,没有造成有效态As显著提升的副作用。修复材料的种类和投加量对As的有效形态含量的改变无显著影响,因此,可以认为本研究中的硅藻土、调理剂、海泡石、人造沸石、膨润土等修复材料能显著降低土壤中DTPA提取Cd有效性的效果。
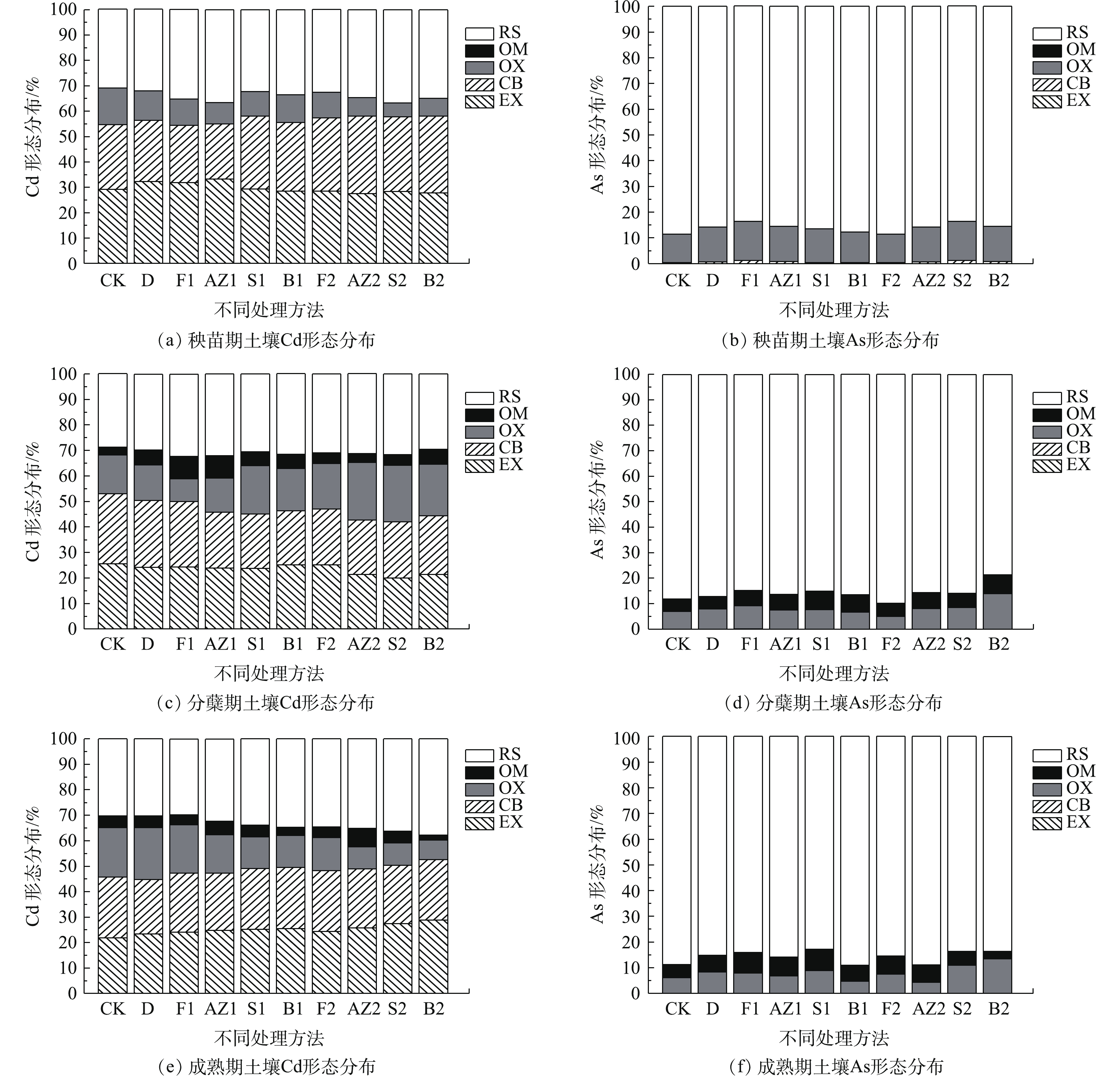
2.3 钝化材料对重金属SEP形态分布的影响
通过SEP连续提取法估算土壤中真实的重金属形态分布和机理[25-26]。在SEP连续提取法中,土壤中的重金属可以根据其在土壤中的稳定性划分为可交换态(EX)、碳酸盐结合态(CB)、铁锰氧化态(OX)、有机结合态(OM)和残余态(RS),各种形态的稳定性顺序为EX<CB<OX<OM<RS。结合图3(a)、图3(c)、图3(e)来看,CK从秧苗期到成熟期的OM形态上升可能是秧苗期后给农田中的水稻追肥所致,修复材料处理后RS形态与CK相比有所提高,其中AZ2、S2、B2的提高幅度比较明显,这说明人造沸石、海泡石、膨润土可能主要以沉淀的方式固定Cd。结合图3(b)、图3(d)、图3(f)来看,空白对照组的OM形态的As含量有所上升,这说明可能是秧苗期前后投加的肥料使OX形态的砷转化为OM形态,或者是由其他农艺因素引起的。其余修复材料处理后,As的各种形态变化趋势与CK相似,这说明修复材料对土壤中As的形态变化无显著影响。
2.4 土壤理化性质的变化
不同修复材料处理后土壤的pH如表2所示。在秧苗期,pH提高的幅度依次为人造沸石粉>海泡石粉>调理剂>膨润土,投加硅藻土后农田土壤的pH反而略有下降。在分蘖期和成熟期,经修复材料处理后农田土壤的pH的变化趋势基本与秧苗期的一致,硅藻土的pH与CK基本一致,其余修复材料处理后的土壤pH均有不同程度地提高,提高的幅度依次为人造沸石粉>海泡石粉>膨润土>调理剂。
表 2 土壤理化性质的变化Table 2. Changes of basic physical and chemical properties of soil阶段 样品 pH 速效磷/(mg·kg−1) 碱解氮/(mg·kg−1) 有机质/(g·kg−1) 阳离子交换量/(cmol·kg−1) 秧苗期 CK 6.02±0.01 33.9±10.2 148±6 32.1±0.8 7.53±0.01 D 5.91±0.07 29.3±2.2 165±0 30.5±0.3 7.74±0.07 F1 6.93±0.04 42.0±4.2 142±25 28.3±5.6 9.16±0.03 AZ1 7.61±0.01 25.1±9.1 137±10 27.6±4.5 7.66±0.30 S1 6.99±0.05 27.4±6.0 204±4 22.8±2.7 8.41±0.64 B1 6.19±0.13 28.7±6.0 164±15 24.0±0.1 8.75±0.01 F2 6.95±0.01 119±27.5 170±5 27.1±4.2 9.38±0.13 AZ2 7.30±0.25 31.1±4.7 292±4 23.7±1.1 8.42±0.55 S2 7.36±0.13 38.3±0.5 320±4 20.0±1.1 9.71±0.02 B2 6.23±0.08 28.4±6.4 330±3 26.1±0.1 8.92±0.13 分蘖期 CK 5.60±0.03 15.9±1.0 88.6±0.2 36.9±0.2 6.10±0.30 D 5.40±0.12 17.3±3.3 81.8±4.8 27.6±5.2 7.70±1.30 F1 5.93±0.04 26.9±1.8 84.7±3.9 30.1±5.3 7.04±1.16 AZ1 6.86±0.02 14.8±0.3 85.5±1.1 38.2±2.3 7.60±0.20 S1 6.49±0.11 14.7±1.8 86.6±9.6 29.3±0.5 9.80±0.20 B1 6.55±0.00 17.2±0.1 77.1±0.1 34.3±0.6 7.14±0.74 F2 6.35±0.01 35.0±4.7 85.6±8.4 22.8±6.9 5.00±0.40 AZ2 6.47±0.03 33.0±2.3 74.0±0.2 14.8±7.4 5.30±0.10 S2 6.38±0.02 22.1±0.1 96.5±7.4 33.9±1.0 5.50±0.30 B2 5.92±0.01 34.1±0.4 73.7±3.0 34.1±8.9 6.64±0.04 成熟期 CK 5.89±0.01 21.3±5.9 95.8±14.9 21.9±3.8 5.88±0.04 D 5.62±0.02 20.7±0.3 106±4.2 33.1±1.8 6.24±0.04 F1 6.18±0.02 45.5±3.4 86.0±3.5 34.4±2.0 7.74±1.30 AZ1 6.64±0.01 21.5±0.9 89.0±0.1 35.7±4.8 6.14±0.30 S1 6.33±0.21 19.5±0.4 95.4±3.3 35.8±0.9 6.27±0.19 B1 6.29±0.02 9.90±0.6 94.4±11.8 30.2±4.5 6.27±0.19 F2 6.27±0.04 41.5±2.7 87.8±1.7 31.3±0.2 5.11±0.19 AZ2 7.07±0.02 26.1±0.7 98.2±8.7 23.4±6.4 5.11±0.19 S2 6.93±0.08 23.6±1.0 101±5.4 22.2±1.5 6.76±0.10 B2 6.59±0.06 29.6±0.8 76.9±0.2 15.0±3.6 8.32±0.49 土壤溶液中的氮、磷元素是植物的主要氮源和磷源,也是衡量土壤肥力的重要指标[24];同时,还有研究表明,速效磷有利于土壤中的Cd形成沉淀[27]。不同修复材料处理后土壤的速效磷含量如表2所示,在秧苗期,经F2处理后,速效磷含量有所提高,与CK存在显著差异,其余修复材料处理后与CK没有较大差异;在成熟期,F1和F2处理后土壤的速效磷含量与CK相比,提升幅度最大,这说明使用调理剂能在较短时间内大幅度提高土壤速效磷含量,其余修复材料处理后,速效磷与CK一致。
不同修复材料处理后,土壤的碱解氮含量如表2所示,在秧苗期,土壤碱解氮的含量高于分蘖期和成熟期,其原因可能是秧苗期前后施加了尿素和复合肥。在秧苗期,经修复材料S1、AZ2、S2、B2处理后,农田土壤的碱解氮含量与CK相比明显提高。在分蘖期和成熟期,各种修复材料处理后,农田土壤的碱解氮含量与空白对照组相比没有显著性差异,这说明修复材料投加后的短时间内,土壤的碱解氮含量会有所提升,经过一段时间后,会恢复到空白对照组的水平。
土壤有机质是土壤肥力的物质基础,其对土壤肥力有多方面的作用[28]。不同修复材料处理后土壤的有机质含量如表2所示,在秧苗期,经修复材料S1和S2处理后,农田的有机质含量与CK相比有所下降,这说明海泡石粉使用初期容易使土壤的有机质减少。在分蘖期,各组实验田的有机质含量与CK相比基本上没有显著差异;在成熟期,除B2处理后农田的有机质含量与CK相比有所下降,其余修复材料处理后农田的有机质含量与CK相比没有显著差异。
阳离子交换量可以用来估算土壤吸收、保留和交换阳离子的能力。不同修复材料处理后土壤的阳离子交换量如表2所示。在秧苗期和分蘖期,部分修复材料处理后的阳离子交换量有所提高,与CK存在显著差异;在成熟期,只有B2处理后的阳离子交换量与CK相比存在较大差异,其原因可能是膨润土富含大量的阳离子,阳离子与土壤中的重金属离子发生交换[29]。这说明修复材料投加后的短时间内土壤的阳离子交换量会有所提升,经过一段时间后,阳离子交换量基本上会恢复到没有修复材料处理过的空白对照组的水平。
2.5 水稻产量
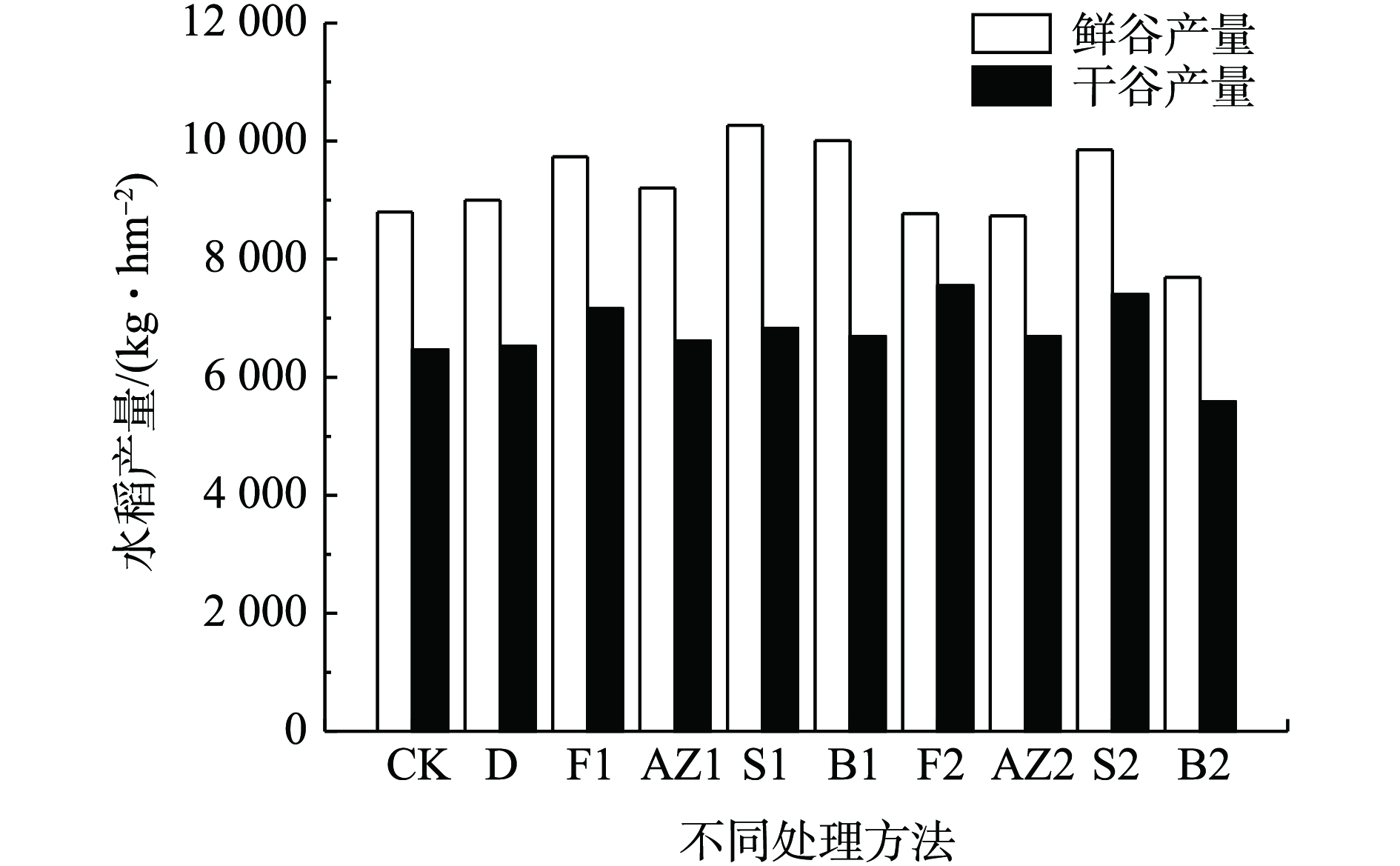
水稻的产量是评价修复材料是否适合农田修复的重要指标,水稻的产量因品种不同、气候不同等因素存在差异。不同修复材料处理后水稻的收成情况如图4所示,各组的水稻产量存在差异,空白对照组的鲜谷产量为8 800 kg·hm−2。经修复材料处理后,水稻的鲜谷产量均有不同程度地增加,其中S1、B1、S2和F1处理后的鲜谷产量最高。空白对照组的干谷产量为6 466 kg·hm−2,除B2外,经修复材料处理后,水稻的干谷产量均有不同程度地增加,其中F2、S2和F1处理后的干谷产量最高,分别为7 549、7 400、7 160 kg·hm−2,分别增产16.74%、14.43%、10.72%。水稻增产的原因可能是因为修复材料缓解了Cd抑制水稻生长的不良影响[30],提高土壤pH从而提高植物的酶活性;同时,磷是作物生长的必需元素,结合土壤速效磷含量的数据可知,调理剂提高了土壤速效磷浓度,有利于水稻的光合作用、碳水化合物运输、氮元素的代谢和脂肪生成,从而提高水稻的产量[31]。
2.6 水稻重金属含量
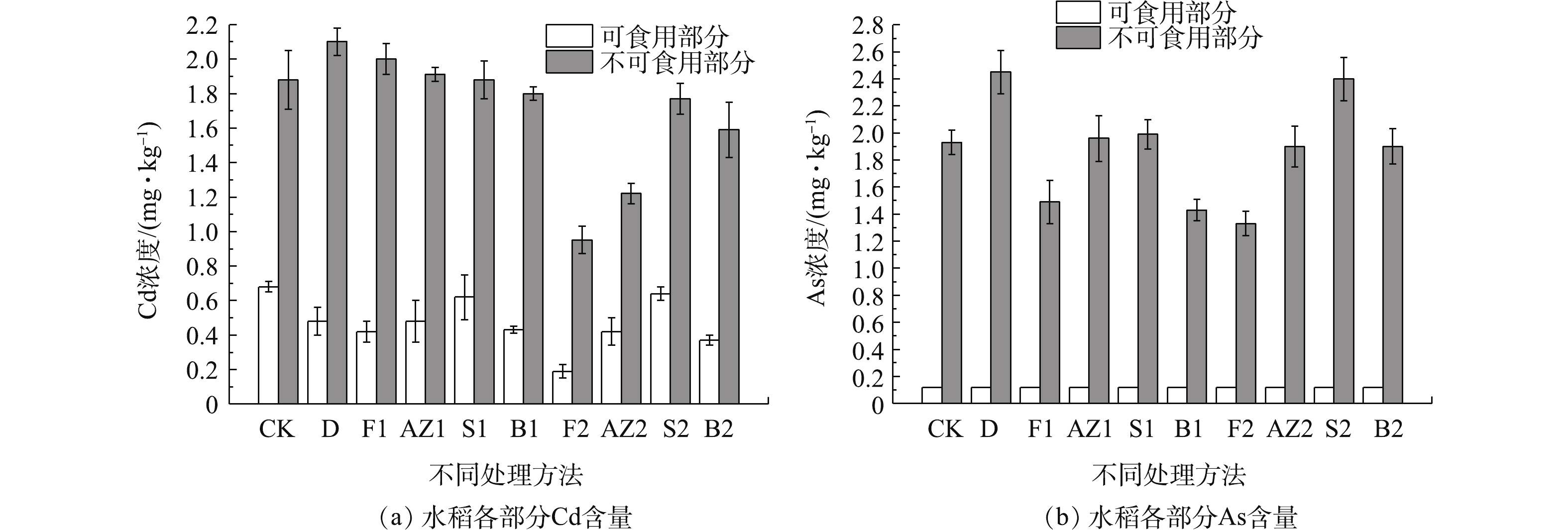
农田修复最关键的是让水稻可食用部分的重金属含量可以满足人体健康食用。水稻可食用部分的Cd含量如图5(a)所示,空白对照组水稻可食用部分的平均Cd含量为《食品中污染物限量》[32]中标准值(0.20 mg·kg−1)的3.4倍。F2处理后水稻可食用部分的Cd含量最低,平均含量为0.19 mg·kg−1,符合《食品中污染物限量》[32]的食用标准值,其他修复材料处理后的平均Cd含量均超出相关标准[32],F2处理后水稻可食用部分的Cd含量与CK相比下降了72%,与MENG等[33]使用的碱性修复材料的修复效果相似,F2处理后速效磷含量和Cd残余态含量均有所提高,因此,调理剂的修复机理可能是调理剂以磷酸盐沉淀固定Cd[27]。B2和AZ2处理后水稻可食用部分与CK相比分别下降了46%和38%,效果没有调理剂明显,膨润土可能是通过离子交换抑制水稻吸收Cd,人造沸石可能是通过表面吸附和沉淀来钝化重金属[34]。F1处理后,水稻可食用部分的Cd含量为0.42 mg·kg−1,与F2存在显著差异,其余修复材料也有相似的规律。这说明在一定范围内,投加量越高,修复材料的修复效果越好,修复材料的投加量和修复材料的种类相比,修复材料的投加量对修复材料修复效果的影响更大。
水稻可食用部分的As含量如图5(b)所示,空白对照组水稻可食用部分的As含量为0.12 mg·kg−1,未超过《食品中污染物限量》的标准值(0.20 mg·kg−1)[32]。修复材料处理后,水稻可食用部分的As含量均是0.12 mg·kg−1,As含量也未超过标准值。
水稻不可食用部分的Cd含量如图5(a)所示,空白对照组的不可食用部分Cd的平均浓度为1.88 mg·kg−1,F2、AZ2和B2处理后水稻的不可食用部分Cd的平均浓度与CK存在显著差异,其中F2与CK相比下降了49.5%,下降幅度最大。其余的修复材料处理后,水稻的不可食用部分Cd与CK没有太大的差异。
水稻不可食用部分的As含量如图5(b)所示,F2与CK相比下降了31.1%,B1和F1与CK相比下降了25.9%和22.8%。其余的修复材料处理后,与CK没有显著差异。海泡石粉、膨润土的投加量对阻止As进入水稻不可食用部分有显著的影响,海泡石粉、膨润土的投加量越高,则会促进As进入水稻的不可食用部分,原因可能是海泡石粉、膨润土的投加量越高,土壤的pH提升越显著,导致含砷沉淀物中的As得到释放,As的迁移能力得到提高[35]。
3. 结论
1)跟其他修复材料相比,调理剂的修复效果最好,既能有效地阻止Cd进入水稻的可食用部分和不可食用部分,也能提升水稻干谷产量,且提升幅度比其他修复材料更高。因此,调理剂具有修复Cd和As污染农田的应用前景。1 kg·m−2投加量的调理剂修复效果比0.5 kg·m−2的调理剂更好。
2)膨润土具备修复Cd污染农田的能力。0.5 kg·m−2投加量的膨润土能有效地阻止Cd进入水稻的可食用部分和不可食用部分,提升水稻干谷产量。但1 kg·m−2投加量的膨润土会减少水稻干谷产量,故膨润土的投加量要根据实际情况考虑。
3)人造沸石具备修复Cd污染农田的能力,能有效地阻止Cd进入水稻的可食用部分。投加人造沸石粉对水稻产量没有较大的影响。1 kg·m−2投加量的人造沸石修复效果比0.5 kg·m−2的人造沸石更好。
4)海泡石粉可以降低农田土壤中Cd的迁移能力,但无法有效地阻止Cd和As进入水稻的可食用部分和不可食用部分。海泡石粉处理后能提高水稻干谷产量。
5)硅藻土能抑制Cd进入水稻的可食用部分,促进Cd和As进入水稻的不可食用部分。因此,这种情况下建议不要将水稻的不可食用部分还田,以减少农田中重金属的总量。投加硅藻土对水稻产量没有较大的影响。
-
表 1 试验碳源性能表
碳源种类 主要成分 比重 pH 粘度/cP( 20 ℃) 凝固点 COD/×104 mg·L−1 葡萄糖 C6H12O6 (50 wt%) 1.20 4~6 2 500 0 55 乙酸钠 NaAc (25 wt%) 1.06 7~9 100 - 20 BC5 C3醇类混合物 1.20 6~7 25 −35 110 BC6 糖类混合物 1.25 6~7 2 200 −18 80 BC8 NaAc复配物 1.22 5~7 70 −20 105 表 2 厂试进出水指标记录表
mg·L−1 试验日期 投加碳源 COD 氨氮 TN TP 2020-12-01~2020-12-15 进水 192±27 5.71±3.70 18.62±2.56 1.72±1.10 出水 碳源-BC8 156±17 0.87±0.38 8.33±4.53 0.70±0.32 碳源-葡萄糖 142±15 0.75±0.26 5.03±1.72 0.68±0.30 2020-12-16~2021-2-26 进水 164±17 7.64±3.20 19.72±4.09 2.78±1.49 出水 碳源-BC8 112±18 0.82±0.23 5.50±1.54 0.56±0.29 碳源-葡萄糖 110±16 0.80±0.24 5.15±1.34 0.53±0.23 -
[1] 郭泓利, 李鑫玮, 任钦毅, 等. 全国典型城市污水处理厂进水水质特征分析[J]. 给水排水, 2018, 54(6): 12 − 15. doi: 10.3969/j.issn.1002-8471.2018.06.003 [2] 王先宝, 亓雪菲, 费骄, 等. 剩余污泥机械破碎碳源快速释放与回收技术[J]. 中国给水排水, 2018, 34(19): 12 − 16. doi: 10.19853/j.zgjsps.1000-4602.2018.19.003 [3] WEN L, HUAN Y, YE J J, et al. Short-chain fatty acids recovery from sewage sludge via acidogenic fermentation as a carbon source for denitrification: A review[J]. Bioresource Technology, 2020, 311: 123446. doi: 10.1016/j.biortech.2020.123446 [4] SERENA S, AGUS S, CLAUDIA F M, etal. Product concentration, yield and productivity inanaerobic digestion to produce short chain organicacids: acritical analysis of literature data[J]. Processes, 2020, 8: 1538. doi: 10.3390/pr8121538 [5] 李健弟, 张伟, 张小玲, 等. 超声预处理污泥发酵液作为反硝化聚磷补充碳源研究[J]. 中国给水排水, 2019, 35(9): 9 − 15. doi: 10.19853/j.zgjsps.1000-4602.2019.09.002 [6] 刘智晓, 季民, 郝赟, 等. 利用活性污泥水解发酵补充碳源优化脱氮除磷[J]. 中国给水排水, 2013, 29(4): 12 − 16. doi: 10.3969/j.issn.1000-4602.2013.04.004 [7] VIDAL A C, PEREZ E N, ASTALS S, et al. Assessing the potential of waste activated sludge and food wasteco-fermentation for carboxylic acids production[J]. Science of the Total Environment, 2021, 757: 143763. doi: 10.1016/j.scitotenv.2020.143763 [8] QI S S, YUAN S J, WANG W, et al. Effect of solid-liquid separation on food waste fermentation productsas external carbon source for denitrification[J]. Journal of Cleaner Production, 2021, 284: 124687. doi: 10.1016/j.jclepro.2020.124687 [9] 吴亚南, 王晓昌, 唐嘉陵, 等. 以厨余发酵液为A/O-DMBR碳源处理生活污水[J]. 中国给水排水, 2017, 33(19): 68 − 72. doi: 10.19853/j.zgjsps.1000-4602.2017.19.015 [10] 申世峰, 熊会斌, 郭兴芳, 等. 果汁废液作为碳源强化生物脱氮效果的研究[J]. 工业水处理, 2020, 40(5): 81 − 83. doi: 10.11894/iwt.2019-0417 [11] 张乐乐, 刘兵, 杨号, 等. 副产甲醇作为外加碳源时脱氮效果的应用研究[J]. 中国资源综合利用, 2018, 36(11): 33 − 35. doi: 10.3969/j.issn.1008-9500.2018.11.011 [12] 张民权, 刘永, 范杰, 等. 新型高效复合碳源的制备及其在反硝化脱氮中的应用[J]. 给水排水, 2019, 55(S1): 153 − 155. doi: 10.13789/j.cnki.wwe1964.2019.S1.40 [13] 邓林, 王庆, 潘倩, 等. 新型复合碳源去除工业综合园区废水中硝酸盐试验研究[J]. 天津科技, 2020, 47(4): 43 − 46. doi: 10.3969/j.issn.1006-8945.2020.04.014 [14] GUOQ M, YANG Z H, ZHAO Q, et al. A pilot-scale study of a novel two-stage denitrification filter[J]. Journal of Water Process Engineering, 2021, 39: 101873. doi: 10.1016/j.jwpe.2020.101873 [15] 张仲玲. 反硝化脱氮外加碳源的选择[D]. 哈尔滨: 哈尔滨工业大学, 2010. [16] HAGMAN M, NIELSEN J L, NIELSEN P H et al. Mixed carbon sources for nitrate reduction in activated sludge-identification of bacteria and process activity studies[J]. Water Research, 2008, 42: 1539 − 1546. doi: 10.1016/j.watres.2007.10.034 [17] 宋壮壮, 吕爽, 刘哲, 等. 厌氧氨氧化耦合反硝化工艺的启动及微生物群落变化特征[J]. 环境科学, 2019, 40(11): 5057 − 5065. doi: 10.13227/j.hjkx.201905223 [18] 赵远哲, 杨永哲, 王海燕, 等. 新型填料 A/O 生物滤池处理低碳氮比农村污水脱氮[J]. 环境科学, 2020, 41(5): 2329 − 2338. [19] 刘文蓉. SBR与生物接触氧化法对对硝基苯酚的降解研究[D]. 泰安: 山东农业大学, 2020. [20] WU W Z, YANG L H, WANG J L. Denitrification using PBS as carbon source and biofilm support in a packed-bed bioreactor[J]. Environmental Science and Pollution Research, 2013, 20(1): 333 − 339. doi: 10.1007/s11356-012-0926-9 [21] SUN H H, WU Q, YU P, et al. Denitrification using excess activated sludge as carbon source: performance and the microbial community dynamics[J]. Bioresource Technology, 2017, 238: 624 − 632. doi: 10.1016/j.biortech.2017.04.105 -







 下载:
下载: