-
化学镀铜工艺是指在无外加电流的条件下,利用合适的还原剂(常用次磷酸盐),使溶液中的铜离子在具有催化活性的基体表面还原沉积出金属铜,形成铜镀层的一种工艺[1-3]。近年来,化学镀铜工艺在表面处理行业中所占的地位在不断上升,在机械工业、航空航天、电子工业等各行各业都有着越来越广泛的应用[4]。在化学镀铜工艺中,会产生大量的化学镀铜废水,将这些废水进行处理和回收,对保护生态环境,变废为宝,提高经济效益,尤为重要[5]。
化学镀铜废水主要来源于清洗零部件时所产生的清洗废水,因此,也可以称为化学镀铜清洗废水,其中主要含有铜离子和次磷酸盐等污染物[6]。过量的铜会刺激人类的消化系统,引起腹痛、呕吐等,严重时可造成中毒。而含铜废水进入水体后,成为持久性污染物,危机植物生长,影响水产养殖。当进入土壤时,会在土壤和作物中富集,经过一系列的环境迁移转化最终进入食物链,对人类健康产生威胁[7]。与正磷酸盐比,次磷酸盐由于其溶解度大且难与沉淀剂反应形成沉淀,导致水体富营养化严重的同时亦造成磷资源的流失[8]。故次磷的去除通常需氧化成正磷,再加入沉淀剂将正磷彻底去除或回收[9]。因此,对化学镀铜清洗废水的处理并回收磷和铜成为当前研究热点之一。
目前,含铜废水处理方法有很多,例如物化沉淀法、膜分离法、吸附法、混凝法和电解法等[10-11]。其中电解法可以使铜离子以金属铜的形式沉积在阴极上,实现了金属铜的回收[12]。除电解法外,其他方法只改变了铜离子存在形态,使铜离子发生迁移,但污染并没有彻底消除。而采用电解法时,当溶液为偏碱性条件下,铜离子很容易水解生成铜的氧化物,累积在阳极或生成沉淀物,使其难以在阴极进行电化学沉积回收[13]。因此,在电解法沉积铜离子实现阴极回收金属铜时,控制溶液的pH较为重要。
光电催化法是一种将光化学和电化学法相结合的方法,通过对半导体光催化剂施加外加偏压作用实现光生电子和光生空穴的有效分离,有效促进自由基的生成,提升污染物的降解效果[14]。光电催化作为高级氧化技术研究热点之一,是一种不仅能产生强氧化性活性物种实现污染物氧化降解,同时也能利用光生电子的还原能力实现阴极还原回收重金属的有效方法[15]。具有运行成本较低、温度和压力适应范围广、可实现有机物矿化且无二次污染等优点,在环境保护水处理领域越来受到关注[16]。二氧化钛(TiO2)纳米管光电极具有高度有序、比表面积大、电池容量高及量子化学效应强等优点,被广泛应用于纳米微电子、光伏器件、水分解产氢、环境污染物降解等领域[17-19]。有研究[20]表明,利用TiO2纳米管电极作为光阳极可有效实现铜氰络合物的氧化破络合同时电还原回收金属铜。
本研究采用电化学阳极氧化法制得的TiO2纳米管电极为光阳极和钛片(Ti)为阴极,在模拟太阳光(AM 1.5)照射进行光电催化处理次磷酸根离子(H2PO2−)和重金属铜离子(Cu2+)同时回收金属铜(Cu)。对TiO2纳米管电极进行了表征分析;对比分析了光电催化(PEC)、电催化(EC)和光催化(PC)体系对次磷氧化和Cu回收效果;考察了电压、初始PH、电解质种类对PEC体系下次磷氧化和Cu回收效率的影响,并进一步探讨该体系的反应机理。本研究结果可为含次磷和重金属铜的工业废水资源化处理提供参考。
-
电极材料钛片购自北京恒力钛工贸公司。实验用次磷酸钠(NaH2PO2·H2O)、亚磷酸钠(Na2HPO3·5H2O)、硫酸铵((NH4)2SO4)、氟化铵(NH4F)、丙三醇(C3H8O3)、硫酸铜(CuSO4)、硝酸(HNO3)、氢氟酸 (HF)、氢氧化钠(NaOH)、硫酸(H2SO4)、过硫酸钾(K2S2O8)、抗坏血酸(C6H8O6)、钼酸铵((NH4)6Mo7O24·4H2O)、酒石酸锑钾(KSbC4H4O7·1/2H2O)、硫酸钠(Na2SO4)、高氯酸钠(NaClO4)、氯化钠(NaCl)、叔丁醇(C4H10O)等均购自国药集团化学试剂公司,均为分析纯。
-
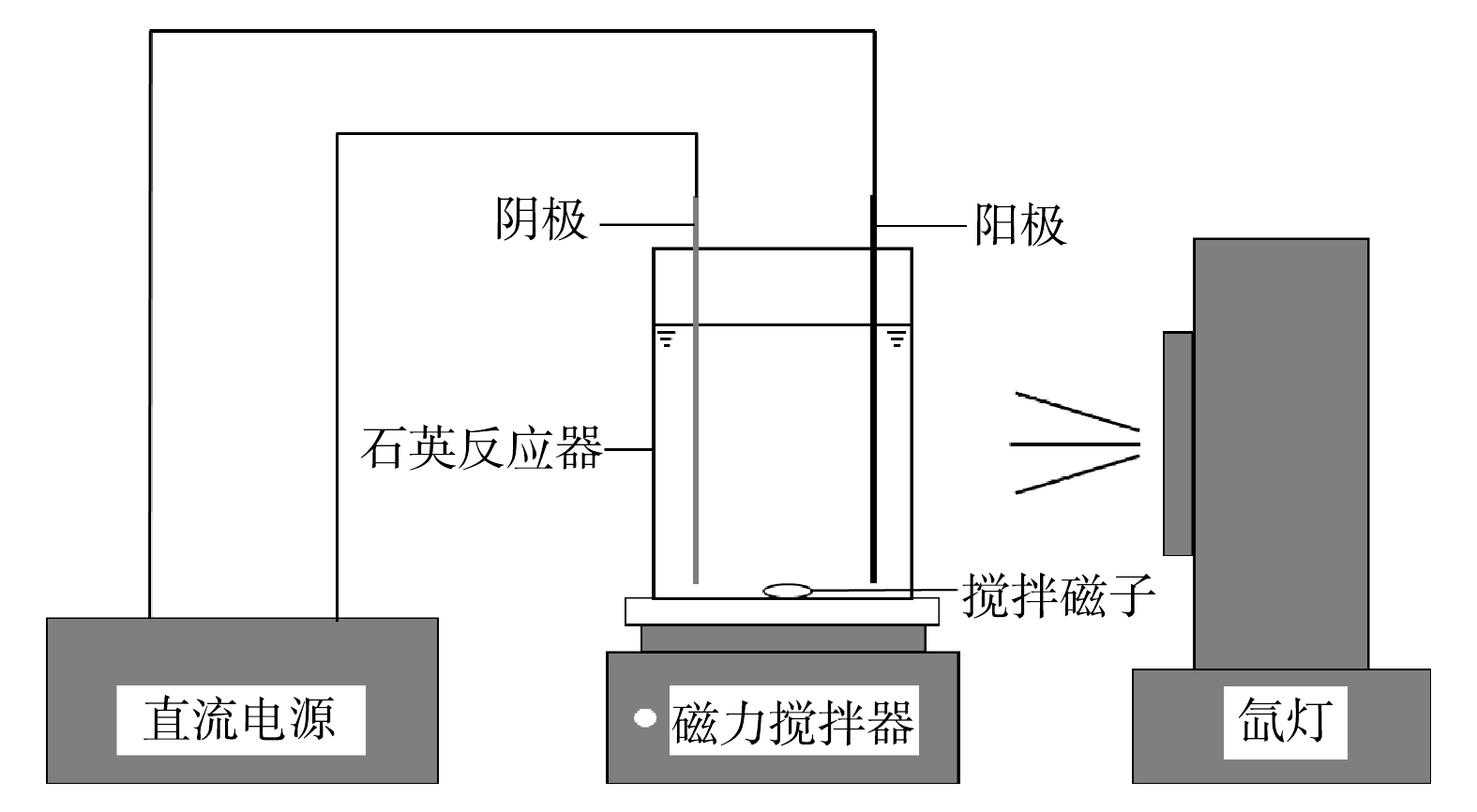
光电催化氧化装置如图1所示,其中包括石英反应器(长5.0 cm,宽5.0 cm,高6.0 cm),150 W的氙灯(Zolix instruments Co,China),直流电源(DH1718E-4,北京大华仪器公司,中国),磁力搅拌器(MS-H380-Pro,北京大龙兴创实验仪器有限公司,中国)。在氙灯光源处安装了一个AM 1.5滤光片,使其照射到反应器内阳极的光为模拟的太阳光。阳极为TiO2纳米管电极,阴极为钛片(长5.0 cm,宽3.0 cm,厚0.2 mm)。
-
1) TiO2纳米管电极的制备。采用阳极氧化法制备电极,制备方法参考文献[20]。钛片预处理:将钛片分别在无水乙醇和丙酮中超声清洗,后用不同目数金相砂纸(200、400、600、1000 目)依次打磨,去离子水清洗,将清洗后的钛片置于HF/HNO3/H2O体积比为1∶4∶5 的混合溶液中浸泡1 min,使钛片化学抛光。电解质制备方法:配制100 g质量比为0.5% NH4F + 1% (NH4)2SO4+ 90% C3H8O3的混合水溶液,即为所需电解质电解质溶液。TiO2纳米管电极制备方法:阳极为预处理钛片,阴极为铂丝,两级间距为20 mm,垂直插入电解质中,电压为20 V,室温下阳极氧化10 h,将氧化后的电极放入马弗炉中450 ºC热处理2 h,升温程序为5 ºC·min−1。
2)降解实验。含次磷酸根离子和重金属铜离子的化学镀铜模拟废水制备方法如下:配制1.0 mmol·L−1的NaH2PO2溶液;将CuSO4溶于其中使Cu2+浓度为0.5 mmol·L−1,即为所需化学镀铜模拟废水。取上述溶液120 mL置于反应器中,开启直流电源在两极间施以一定的电压,同时开启氙灯,反应时间为180 min,取样时间为0、30、60、90、120、150、180 min。反应液以10 mmol·L−1的Na2SO4为电解质。光催化反应时只开启氙灯,两极之间不施加电压。电化学反应时只开启直流电源。
3)表征及分析方法。电极表面形态通过场发射扫描电镜(SEM,SU-8010,日本日立公司)进行观察;晶体结构通过X射线衍射(XRD,XPert Pro MPD,荷兰帕纳科分析仪器有限公司)进行表征,所用的仪器是配有石墨晶体单色器的Rigaku D/max-B衍射仪,2θ扫描范围为10°~90°,扫描速率为0.5°·min−1,加速电压和工作电流分别为30 kV和30 mA;阴极回收Cu价态通过X射线光电子能谱仪(XPS,PHI Quantera SXM,日本ULVAC-PHI 公司)进行测定;电子自旋共振波谱仪(ESR,A300−10/12,德国布鲁克有限公司)用来检测自由基的生成。总磷的测定方法为采用国标过硫酸钾氧化-钼酸铵分光光度法;正磷的测定方法为采用国标钼酸铵分光光度法;次磷和亚磷采用离子色谱(IC,ICS-1500,美国戴安公司)测定,所用色谱柱为AS23分析柱和AG23保护住,淋洗液为4.5 mmol·L−1的Na2CO3和0.8 mmol·L−1的NaHCO3溶液,流速为1.0 mL·min−1;重金属Cu含量采用电感耦合等离子体发射光谱仪(ICP-OES,P700,美国安捷伦科技公司)来测定。
-
图2(a)和图2(b)分别是Ti基底和TiO2纳米管电极的SEM正面图像。可见,Ti基底表面平整,经阳极氧化法制备的TiO2纳米管电极上,纳米管阵列高度有序、管径均匀、排列整齐的在Ti基底上呈现。图2(c)是TiO2纳米管电极的SEM截面图像,可以发现电极截面呈现明显的管状结构。由图2(d)可见,TiO2纳米管电极在2θ在25.3°和48°处出现明显的衍射峰。这表明TiO2呈现锐钛矿结构。
-
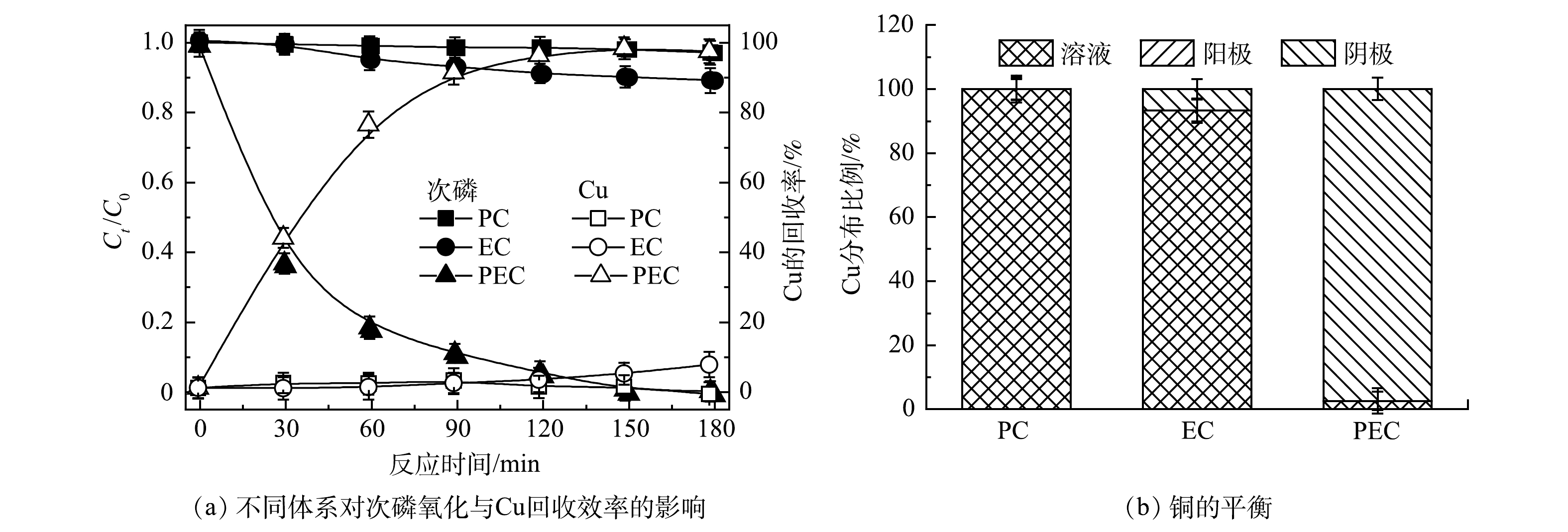
图3(a)分别对比了光电催化(PEC)、电催化(EC)和光催化(PC)体系对次磷氧化和Cu回收效果的影响。结果表明:PEC体系效果最好,当电压为2.0 V,反应时间180 min,PEC、EC、PC 3个体系对次磷的氧化率分别为100%、11%和0,Cu的回收率分别是97%、7%和0。图3(b)反映了反应180 min时Cu在溶液、阳极、阴极的分布情况。结果证明,回收的Cu均沉积在阴极上。通过对不同体系进行比较,单独EC或者单独PC均不能实现高效率的次磷氧化和Cu回收;当电化学作用和光催化作用联合即PEC体系时,可以产生很好的协同作用。这是因为通过光激发TiO2半导体产生光生空穴与电子,外加偏压促进了空穴和电子的高效分离,大大提高了反应的氧化还原作用。
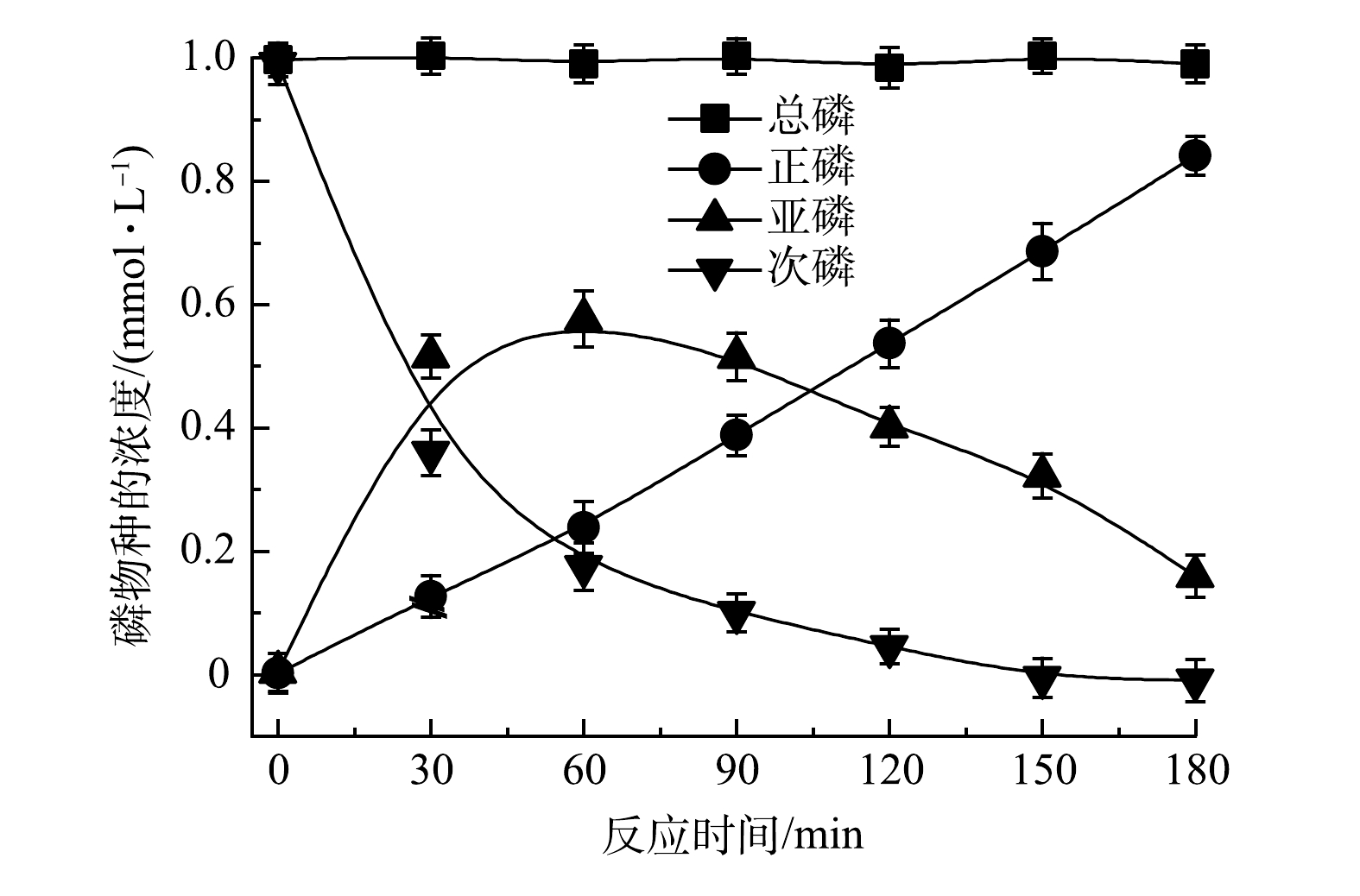
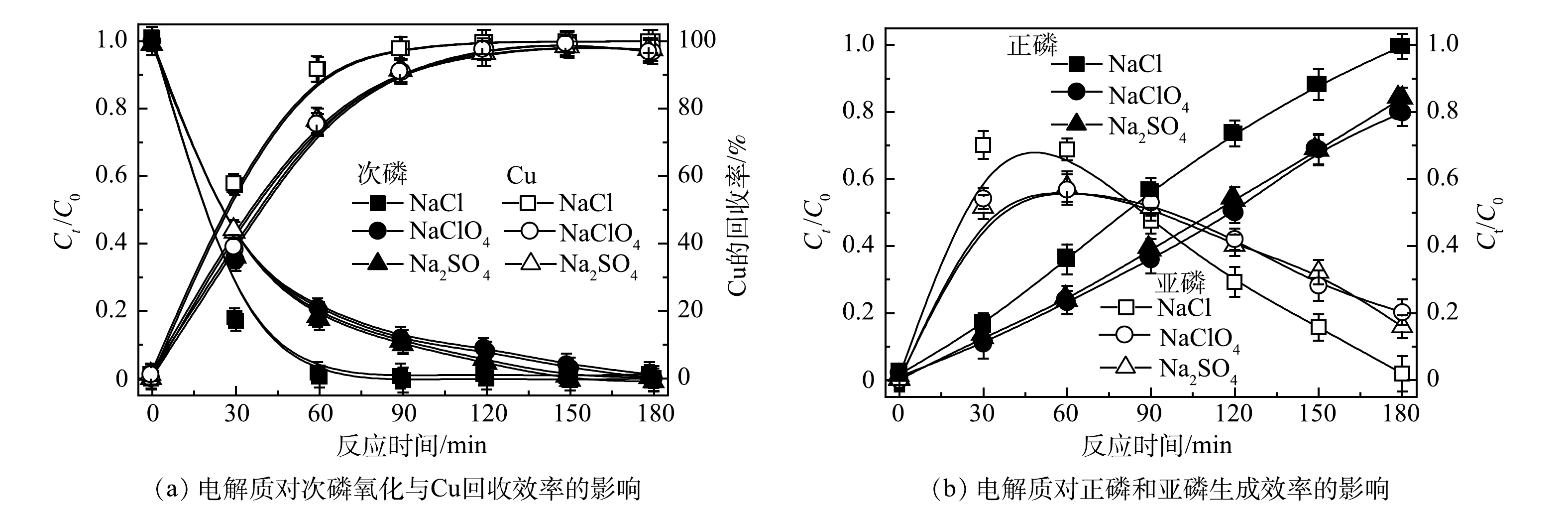
图4反映了TiO2纳米管电极作为光阳极在2.0 V下PEC体系次磷氧化过程中间产物的生成和P元素的平衡过程。可以看出,随着反应的进行,总磷的浓度基本保持不变,而亚磷酸盐的浓度随反应时间延长先升高后降低,正磷酸盐的浓度则一直呈现升高的趋势。由此可见,在次磷氧化过程中,次磷(P为+1价)先被氧化成为亚磷(P为+3价),进而最终被氧化成为正磷(P为+5价),且随着反应的进行,总磷浓度基本不变。
-
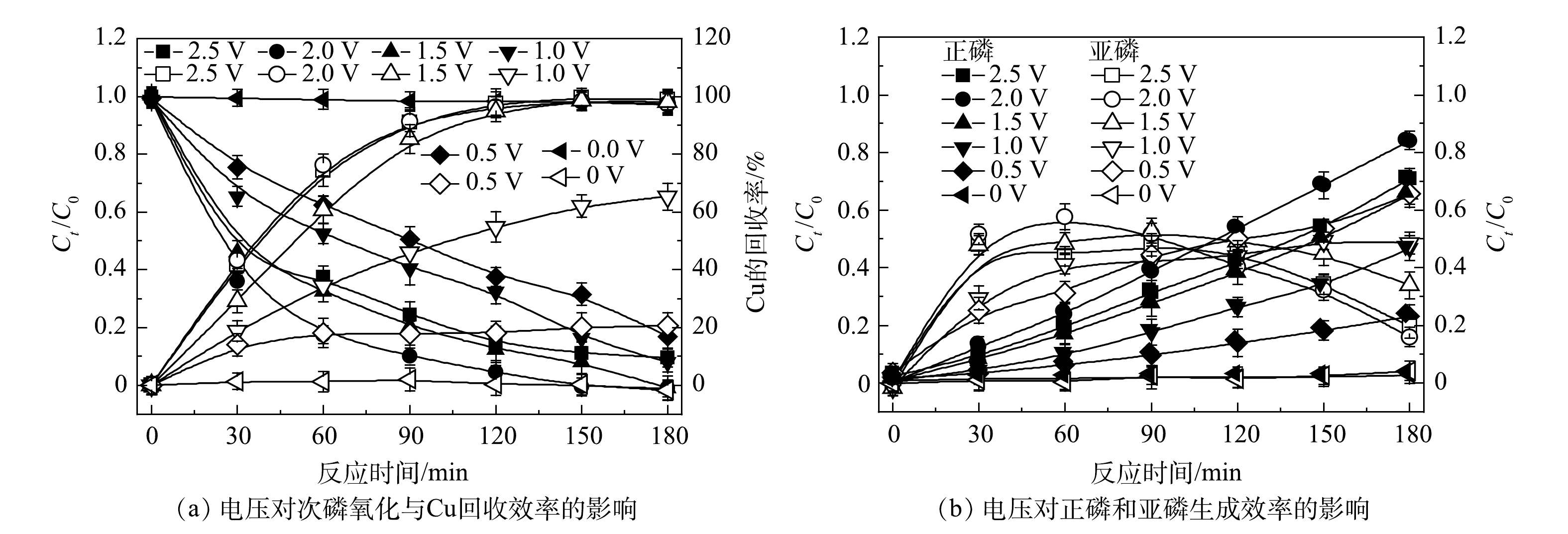
不同电压条件下TiO2纳米管电极作为光阳极的PEC体系对次磷氧化和Cu回收效率的影响如图5所示。随着电压的增大及反应时间的延长,次磷氧化和Cu回收的效率逐渐升高。当电压为2.0 V、反应时间为180 min时,1 mmol·L−1的次磷全部被氧化,其中,84%以正磷形式存在,剩下的16%以亚磷形式存在并且呈现继续下降趋势,同时0.5 mmol·L−1的Cu 全部以金属形式在阴极沉积回收。而当电压增加至2.5 V时,效果反而变差。其原因可能是,随着电压的增加,阳极析氧和阴极析氢等副反应越来越剧烈,从而抑制了污染物在电极表面的迁移,导致电极表面电流效率的降低以及能量的大量损耗[21]。
-
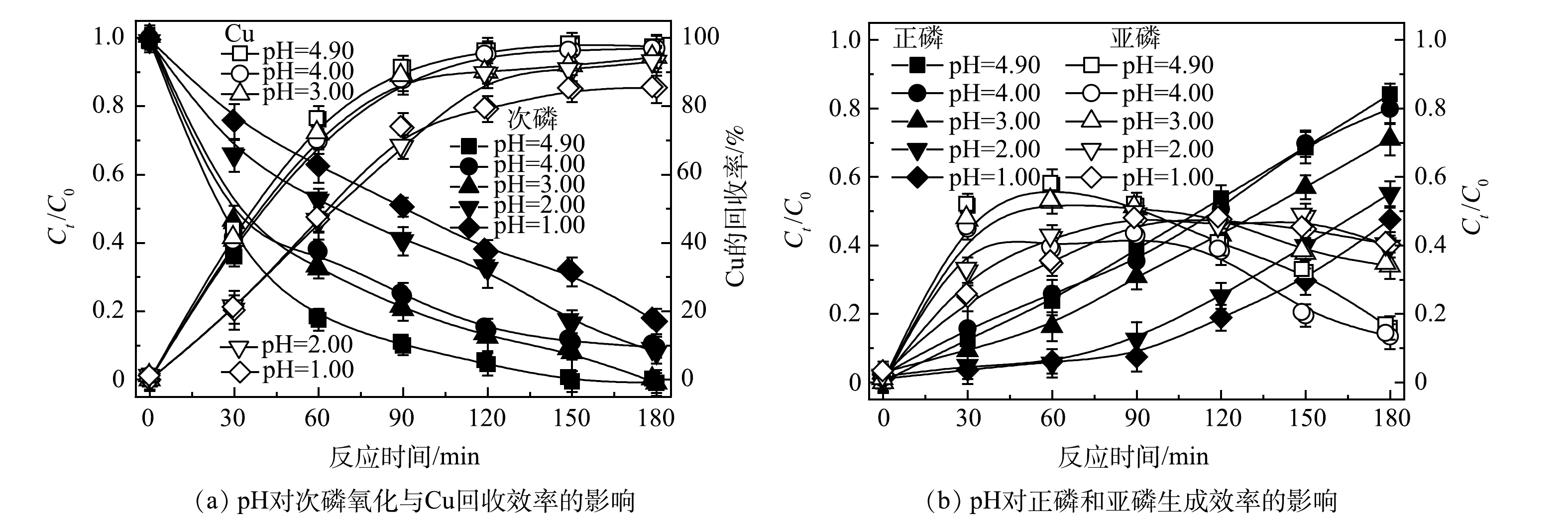
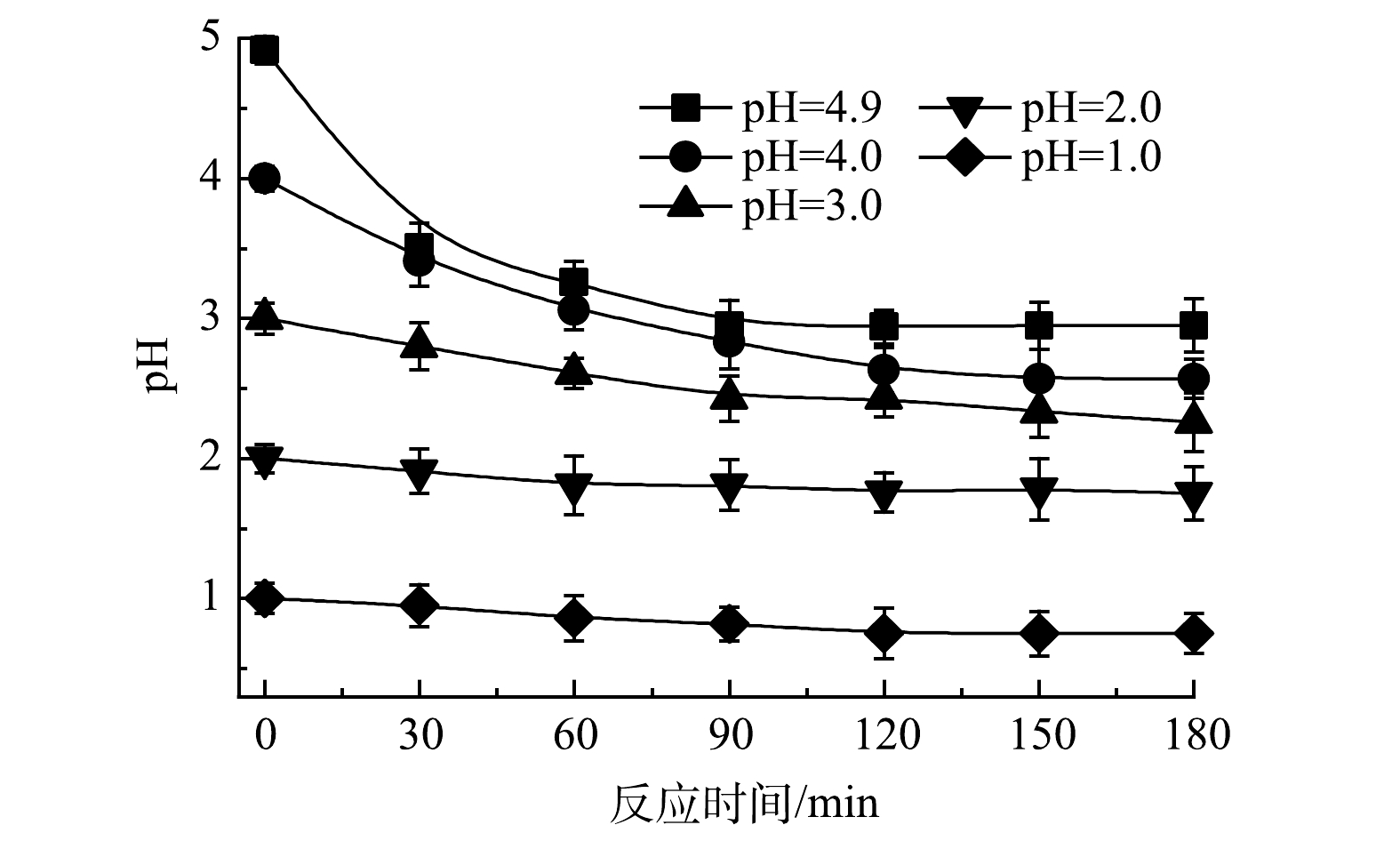
反应溶液的初始pH为4.9,由于Cu2+存在,Cu(OH)2的溶度积为2.2×10−20,由此计算得出,在本研究中pH大于5.8后会产生Cu(OH)2沉淀。因此,本研究利用H2SO4的稀释溶液调节溶液的初始pH为4.0、3.0、2.0、1.0进行对比实验。如图6所示,当溶液初始pH为4.9,即不用H2SO4调节时,对次磷氧化和Cu回收效果最好;当溶液初始pH降低后,次磷氧化和Cu回收效果均受到明显的抑制,同时,次磷氧化过程中生成的亚磷以及正磷也受到了抑制。由图7可以看出,随着反应的进行,pH均会下降。这说明反应过程中有大量氢离子释放,推测是因为在次磷最终氧化成为正磷的过程中,均会有氢离子释放[8]。pH能影响水中溶解氧(DO)含量[22],随着pH降低,DO含量减少,从而影响了·OH的生成,且在酸性条件下,·OH更易反应生成活性较弱的·OOH[23],因此,会影响体系次磷氧化的效率。此外,在单独电沉积Cu2+时由于阴极析发生氢反应造成溶液偏碱性,Cu2+水解生成铜的氧化物在阳极沉积生成沉淀物[13],而次磷氧化的同时在溶液中释放氢离子可以降低溶液pH,克服了Cu2+难以在阴极进行电化学沉积回收金属Cu的问题,使Cu2+有效沉积在阴极回收为金属Cu。
-
如图8所示,溶液采用的电解质不同时对次磷氧化和Cu回收效果也有影响。当电解质为Na2SO4和NaClO4时,反应效率基本无明显差异,但当电解质为NaCl时,反应效率明显提高,1 mmol·L−1次磷全部被氧化为正磷。进一步详细探讨了NaCl电解质在反应中的作用。如图9所示,在不同浓度NaCl对次磷氧化和Cu回收效果影响实验中,NaCl浓度越高,效果越高。其原因为,在PEC体系中,反应中的氯离子可以通过一系列反应生成活性氯(式(1)~式(3))[24]。在阳极表面生成的活性氯以氯气(Cl2)、次氯酸(HClO)和次氯酸根(ClO−)等形式在溶液中存在。图10是在不同NaCl浓度反应体系中,活性氯浓度的测定结果,NaCl浓度越高时,活性氯生成量越多。此外,有文献报道,在紫外光照射下,活性氯有利于进一步产生羟基自由基(·OH)和氯自由基(Cl·)(式(4))[25-26]。因此,当采用NaCl作为电解质时,氯离子的加入最终会促进以上自由基的产生,强化了反应效率。
-
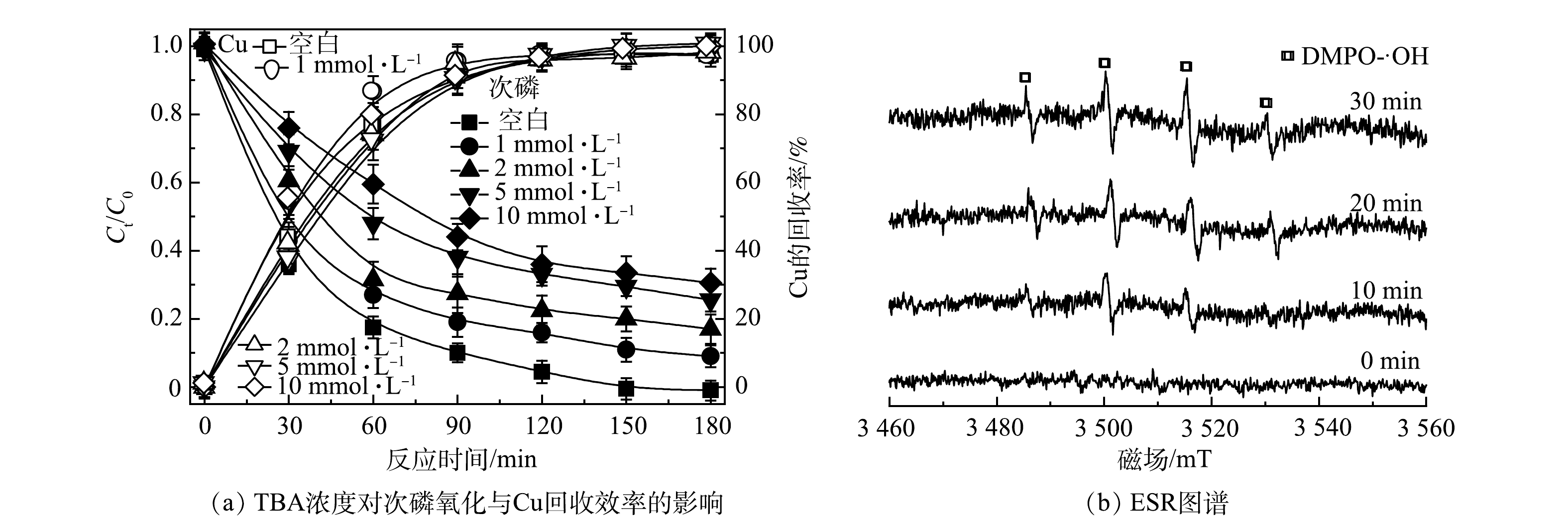
为了探究反应过程中PEC体系下存在的主要活性物种,通过加入不同浓度的·OH自由基淬灭剂叔丁醇(TBA)来探究·OH对次磷氧化的作用。如图11(a)所示,考察了TBA对TiO2纳米管电极作为光阳极下PEC对次磷氧化与Cu回收效率的影响。结果表明:TBA对PEC体系中次磷氧化有明显的抑制作用,当TBA浓度为10 mmol·L−1时,次磷的去除率降低到60%,而TBA的加入对Cu回收无明显影响。这一结果表明,·OH 自由基对次磷氧化起重要作用。ESR检测结果也进一步验证了这一结果。如图11(b)所示,使用DMPO为捕获剂,在反应过程中观测到了特征的 DMPO-·OH络合物的信号,并随反应时间的延长而显著增强。以上结果表明,·OH自由基是次磷氧化的主要活性物种。
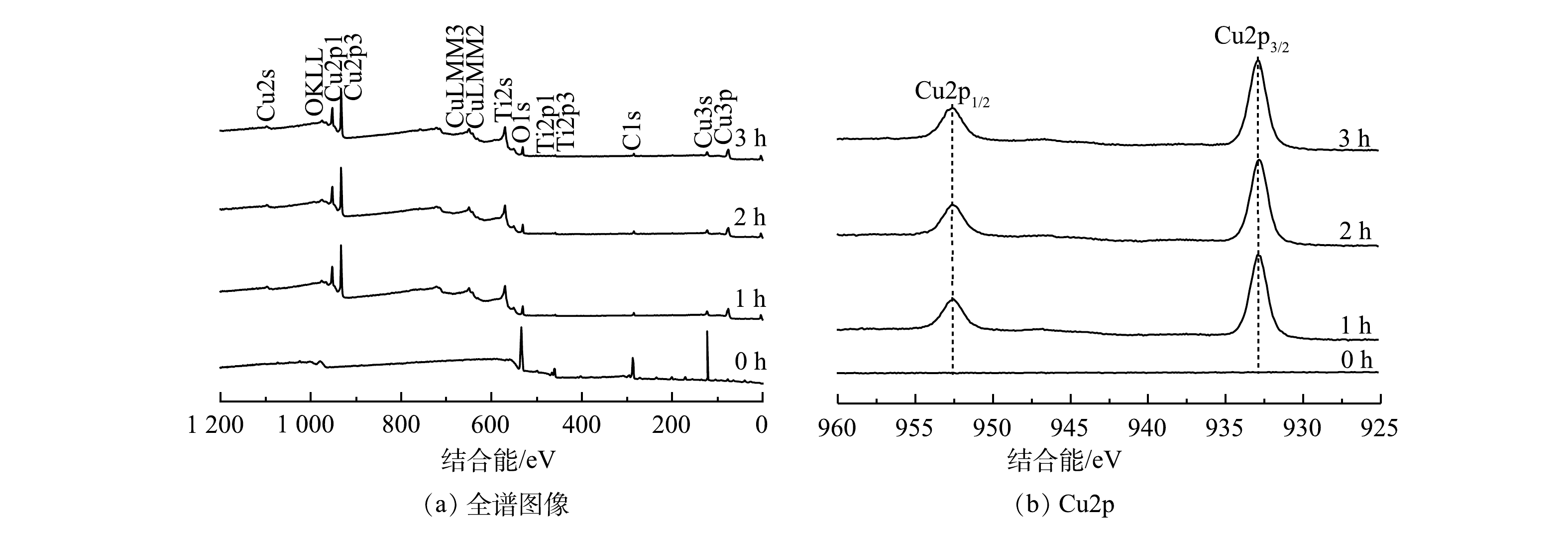
图12是反应过程中阴极钛片上Cu沉积物的XPS谱图。当反应时间分别为1、2、3 h时,Cu2p3/2的峰值在932.68 eV处出现,主要对应金属Cu的特征峰,且随反应的进行峰值强度有所增强,且并未检测到其他价态的Cu。由此证明在本研究中阴极钛片上回收的是金属Cu。
-
1)通过PEC、EC、PC 3个体系对次磷氧化和Cu回收效率比较,发现单独EC或者PC均不能实现高效率的次磷氧化和Cu回收,当电化学和光催化联合(PEC体系)时,可以产生很好的协同效果。
2)对于PEC体系中次磷氧化和Cu的回收效果,在电压为2.0 V、反应时间为180 min时1 mmol·L−1的次磷全部被氧化且84%以正磷形式存在,另外16%以亚磷形式存在并且呈现继续下降趋势,同时0.5 mmol·L−1的Cu 100%以金属形式在阴极沉积回收。当溶液初始pH为4.9时,采用NaCl作为电解质,可促进·OH的产生,1 mmol·L−1次磷全部被氧化为正磷,提高了反应效率。
3)在单独电沉积Cu2+时,由于阴极发生析氢反应造成溶液偏碱性,Cu2+水解生成铜的氧化物在阳极沉积生成沉淀物,而次磷氧化的同时在溶液中释放氢离子可以降低溶液pH,克服了Cu2+难以在阴极进行电化学沉积回收金属Cu的问题,使Cu2+有效沉积在阴极回收为金属Cu。
4) TBA对PEC体系中次磷的氧化有明显的抑制作用,且对Cu回收无明显影响,表明·OH为实现次磷氧化的主要活性物种。
5)采用光电催化技术处理含次磷和重金属铜废水,废水中的Cu2+在阴极电沉积生成金属Cu回收,而废水中次磷氧化后形成正磷,然后加入钙盐或铁盐等与正磷反应生成沉淀将磷在废水中去除同时回收磷。
TiO2纳米管阳极光电催化氧化次磷酸盐同时阴极回收金属铜
Photoelectrocatalytic oxidation of hypophosphite with TiO2 nanotube arrays anode and simultaneous recovery of copper on the cathode
-
摘要: 采用电化学阳极氧化法制备了高度有序阵列的二氧化钛(TiO2)纳米管电极,采用此电极作为光阳极在模拟太阳光(AM 1.5)照射下进行了光电催化氧化次磷酸盐且同时回收金属铜(Cu)的研究,比较了光电催化、电催化和光催化体系对次磷氧化和Cu回收效率的差异,详细探究了电压、初始pH、电解质种类对光电催化体系下次磷氧化和Cu回收效率的影响。结果表明,当电压为2.0 V,初始pH为4.9,电解质为10 mmol·L−1 NaCl,在180 min内,1 mmol·L−1次磷全部被氧化为正磷,同时0.5 mmol·L−1的Cu 100%以金属形式在阴极沉积回收。在该光电催化体系中,在一定范围内,外加偏压的增加、溶液初始pH的升高和NaCl浓度的提高有利于次磷氧化和Cu回收。自由基淬灭实验和电子自旋共振实验结果证明,该体系中羟基自由基为氧化次磷的主要活性物种。以上研究结果可为含次磷和重金属铜废水的资源化处理提供参考。Abstract: Highly ordered TiO2 nanotube arrays electrode fabricated using Ti plate by electrochemical anodization method was used as a photoanode under simulated sunlight (AM 1.5G, 100 mW cm−2) irradiation for hypophosphite (H2PO2−) oxidation and Cu recovery. The performance for H2PO2− oxidation and Cu recovery in the photoelectrocatalytic (PEC) process was evaluated compared with the individual electrocatalytic (EC) or photocatalytic (PC) process. The effects of applied bias, initial solution pH and electrolyte type were investigated in detail. The results show that for 1 mmol·L−1 H2PO2− and 0.5 mmol·L−1 Cu2+, 100 % H2PO2− was oxidized to PO43−, 100 % Cu2+ was recovered as metallic Cu within 180 min at an applied bias of 2.0 V, initial solution pH of 4.9 and electrolyte of 10 mmol·L−1 NaCl. In this constructed PEC system, the increase of applied bias, initial solution pH or NaCl concentration within a certain range was proved to be favorable in the efficiency of H2PO2− oxidation and Cu recovery. The radical quenching experiments and electron spin resonance results indicated that hydroxyl (·OH) radicals were the major active species for H2PO− oxidation. This study can provide a reference for the resource treatment of wastewater containing H2PO2− and heavy metal Cu2+ ions.
-
纺织行业中棉织物活性印花工艺一般包括印花、洗网、洗筒、水洗、皂洗等工序,生产过程中会产生大量的工艺废水[1-2]。活性印花废水具有浆料浓度高、活性染料残留多、可生化性相对较好等特点[3]。除此之外,印花废水中残留大量尿素,使印花废水含氮量非常高,从而导致碳氮比失调的问题[4-5]。一般的生化工艺经过厌氧反应器处理,可去除印花废水中部分COD,同时也会将有机氮转化为氨氮,加剧碳氮失调比例,增加了后续的生物脱氮难度。为了解决活性印花废水中高氮问题,行业迫切需要开发一种既高效又经济的生物脱氮技术[6]。
近年来开发出的厌氧氨氧化技术(anaerobic ammonium oxidation, ANAMMOX)为低碳高氮废水提供了高效经济的方法[7]。与传统硝化反硝化相比,ANAMMOX工艺具有节省曝气量和碳源、脱氮效率高、剩余污泥泥少等优点[8]。目前,ANAMMOX工艺已经成功应用于实验室处理高氨氮(>300 mg·L−1)废水,如垃圾渗滤液[9]等。由于厌氧氨氧化工艺以氨氮和亚硝态氮为基质,因此,工艺前段须匹配短程亚硝化工艺来提供亚硝态氮[10-11]。在此基础上,开发出二阶段厌氧氨氧化工艺(如短程硝化-厌氧氨氧化(SHARON-ANAMMOX)工艺[12-13])和平阶段厌氧氨氧化工艺(如完全自养脱氮(completely autotrophic nitrogen removal over nitrite, CANON)工艺[14-15])。
由于工业废水中存在大量化学品或其中间产物(如染料)可能会抑制厌氧氨氧化菌的生长,因此,目前主流厌氧氨氧化工艺应用于处理印花废水方面的研究未见报导。本研究旨在探讨厌氧氨氧化工艺处理高氨氮工业废水的实验应用可行性,以典型的高氮印花废水作为处理目标,将UASB工艺和主流厌氧氨氧化MBR-CANON工艺进行串联,来处理活性印花废水,考察了UASB/MBR-CANON工艺对印染废水COD、高氮和色度去除的效率,验证了该工艺处理高氮活性印花废水的可行性。
1. 材料与方法
1.1 实验材料与装置
UASB/MBR-CANON工艺通过前置的UASB反应器去除废水中浆料等可生化降解的有机物,同时实现尿素的氨化,为后续的MBR-CANON提供适合的反应条件。CANON采用MBR工艺,反应器内置填料可以通过截留生物量来提高污泥浓度,但生物膜的脱落仍会造成部分污泥流失,因此,本研究采用MBR工艺以加强污泥截留,增加污泥浓度,同时可以过滤悬浮颗粒,优化出水水质。
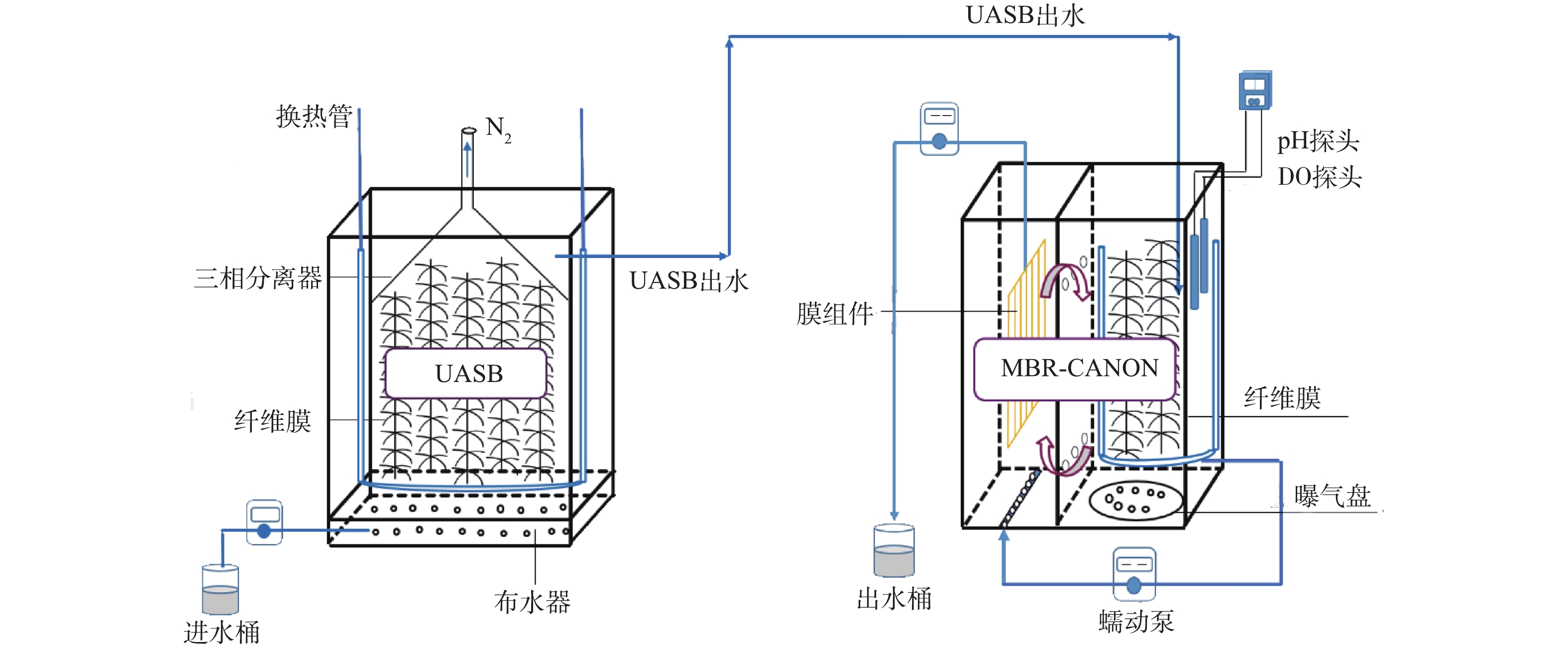
实验装置系统由厌氧反应器和脱氮反应器组成,分别采用UASB和MBR-CANON反应器形式,如图1所示。其中UASB反应器有效体积为36 L,内部填充软性纤维填料,顶端封闭并设置排气口。MBR-CANON反应器有效体积为12 L,使用隔板平分为左右2部分,左边装填中空纤维膜组件(PVDF膜面积0.144 m2),右边填充软性纤维填料,底部设置曝气盘为微生物提供溶解氧,并放置溶解氧探头和pH计进行实时监测。通过蠕动泵抽取右侧混合液循环至左侧实现膜组件冲刷,使其达到减轻膜污染的目的。当跨膜压力达到−10 kPa时进行膜组件反冲洗。2个反应器均采用连续运行方式,并通过恒温水浴锅和加热管控制反应器内环境温度。
1.2 接种污泥
UASB反应器接种污泥来自本实验室印染废水的中试厌氧反应器[16],接种污泥浓度为15.6 g·L−1,污泥体积为15 L。MBR-CANON反应器接种污泥来自正在运行的河北某畜牧场厌氧氨氧化污泥,其污泥浓度为10.0 g·L−1,污泥体积为0.5 L。
1.3 实验运行方法
系统运行共200 d,分为2个阶段。UASB反应器和MBR-CANON反应器的独立启动阶段:UASB反应器启动运行共40 d,在此阶段中,水力停留时间为72 h,pH为7.0~8.5,温度为(25±1) ℃。淀粉是活性印花工艺中常用的浆料之一[17],通过将进水中淀粉浓度由500 mg·L−1增加到1 000 mg·L−1,使COD容积负荷由0.17 kg·(m3·d)−1逐渐提高至0.34 kg·(m3·d)−1。染料为活性黄,分子式为C28H20ClN9O16S5·4Na。进水尿素浓度保持在1 070 mg·L−1,其总氮浓度为500 mg·L−1,总氮容积负荷为0.17 kg·(m3·d)−1。MBR-CANON反应器启动共140 d,在此阶段中,水力停留时间为24 h,水力循环中出水与回流比为1∶100。通过将氯化铵浓度由191 mg·L−1依次提高至382、573、764、1 146 mg·L−1的方式,使氨氮容积负荷由0.05 kg·(m3·d)−1逐渐提高至0.10、0.15、0.20、0.30 kg·(m3·d)−1。控制pH为7.5~8.5,温度为(35±1)℃,溶解氧为0.1~0.5 mg·L−1;系统运行140 d后,UASB反应器和MBR-CANON反应器均启动成功并运行稳定,此时将UASB反应器出水逐步添加进入MBR-CANON反应器的进水中进行串联,其他条件保持不变。2个反应器在启动和串联运行中均不排泥。本研究中UASB反应器和MBR-CANON反应器均配制与实际废水相仿的模拟印花废水,具体如表1和表2所示,并添加适量磷、钙镁离子及微量元素[18]。
表 1 UASB进水水质及成分Table 1. Wastewater quality and compositions of UASB influentmg·L−1 基质 启动阶段浓度 140 d后浓度 TN 1 000 1 000 COD 500~1 000 1 000 活性黄 100~150 150 P 5.70 5.70 表 2 MBR-CANON进水水质及成分Table 2. Wastewater compositions of MBR-CANON influentmg·L−1 基质 启动阶段浓度 140 d后浓度  -N
-N50~300 1 146~1 337 COD 0~100 100~200 活性黄 0 20~30 HCO3− 580~1 815 1 815 P 1.42 1.42 1.4 分析项目与测试方法
实验在线监测并记录DO和pH(LDO101,Hach,可在线监测并记录数据)。COD采用微波消解法,氨氮采用纳氏试剂分光光度法,亚硝态氮采用N-(1-萘基)-乙二胺分光光度法,硝态氮采用氨基磺酸紫外分光光度法,总氮采用碱性过硫酸钾分光光度法,以上均采用文献中的方法[19]进行测定。
活性黄染料浓度采用分光光度法:取一定量染料溶于去离子水中,在波长200~800 nm范围内,进行紫外-可见全波段扫描,确定染料最大吸收波长。配制梯度浓度的染料标准溶液,在最大吸收波长下测定其吸光度,并绘制吸光度与染料浓度标准曲线。测得水样吸光度,根据标准曲线计算水样染料浓度,染料脱色率计算如式(1)和式(2)所示。
R1=C(NO−2-Neff)C(NO−2-Neff)+C(NO−3-Neff)×100% (1) R2=C(Dyeinf)−C(Dyeeff)C(Dyeinf)×100% (2) 式中:R1为亚硝酸盐积累率;R2为染料脱色率;C为浓度,mg·L−1。
1.5 膜污染分析方法
在本实验中,膜污染分析测试指标包括膜通量和膜表面滤饼层EPS中的多糖和蛋白质。EPS采用热提取法[20]:将膜表面滤饼层刮至50 mL离心管后,放入摇床中至污泥完全溶解并提取EPS,通过改进Lowry法和蒽酮-硫酸法测定其蛋白质和多糖。
2. 结果与讨论
2.1 UASB/MBR-CANON反应器的启动
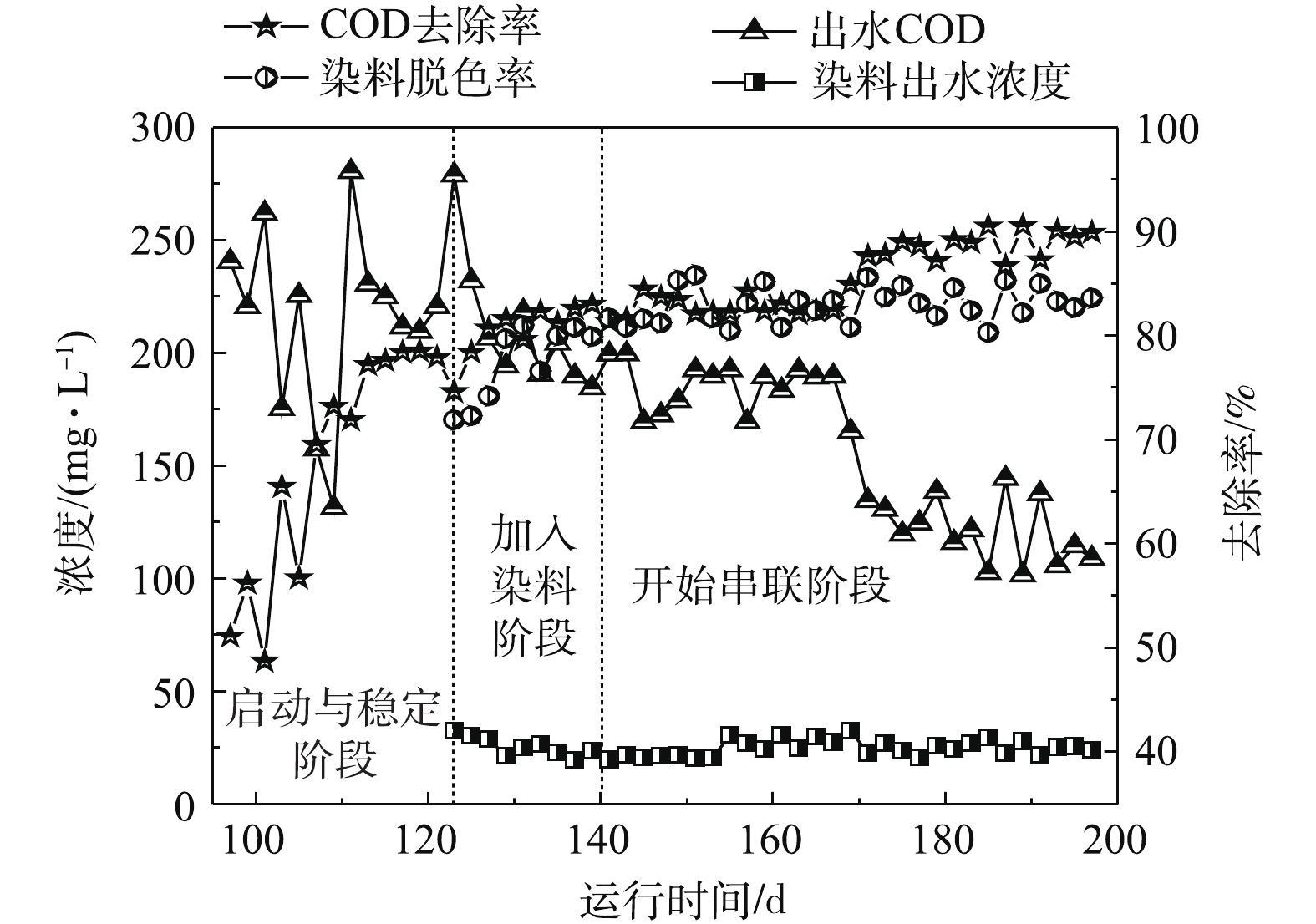
1) UASB反应器启动与运行。UASB反应器可将模拟印花废水中的尿素水解为氨氮,降解大部分淀粉,分解染料,从而降低色度。当MBR-CANON反应器运行至97 d时,开始启动UASB反应器。UASB反应器启动运行结果如图2所示。由图2可知,在UASB反应器运行的第97~109天中,出水COD值平均为201 mg·L−1左右,COD去除率接近60%。当进水继续提高淀粉浓度至1 000 mg·L−1左右时,反应器内微生物浓度与活性不断提高,COD去除率逐渐上升至78%左右。从第123天开始向反应器中加入100 mg·L−1活性黄染料,由图2可知,随着反应器的运行,染料不断被降解,到第140天时,出水染料浓度为25 mg·L−1左右,染料的脱色率缓慢升高至80%左右,此时认为UASB启动成功。由于反应器内接种污泥为处理印染废水中试装置中的污泥,因此,反应器启动所需时间较短。
随着UASB反应器的运行,微生物不断增殖,出水COD去除率和染料脱色率均在80%以上,最高分别可达到85%和86%。运行15 d左右后,提高UASB反应器进水染料浓度至150 mg·L−1,此时出水染料浓度为30 mg·L−1左右,染料的脱色率为80%左右。从第171天开始,反应器出水COD由189 mg·L−1逐渐降低至109 mg·L−1左右,COD去除率平均值为89%,同时,此阶段UASB反应器的染料降解效果相对比较稳定,出水染料浓度和染料脱色率分别为25 mg·L−1和84%左右。以上研究结果表明,UASB反应器对印花废水中COD和活性黄染料均有较好的去除效果。
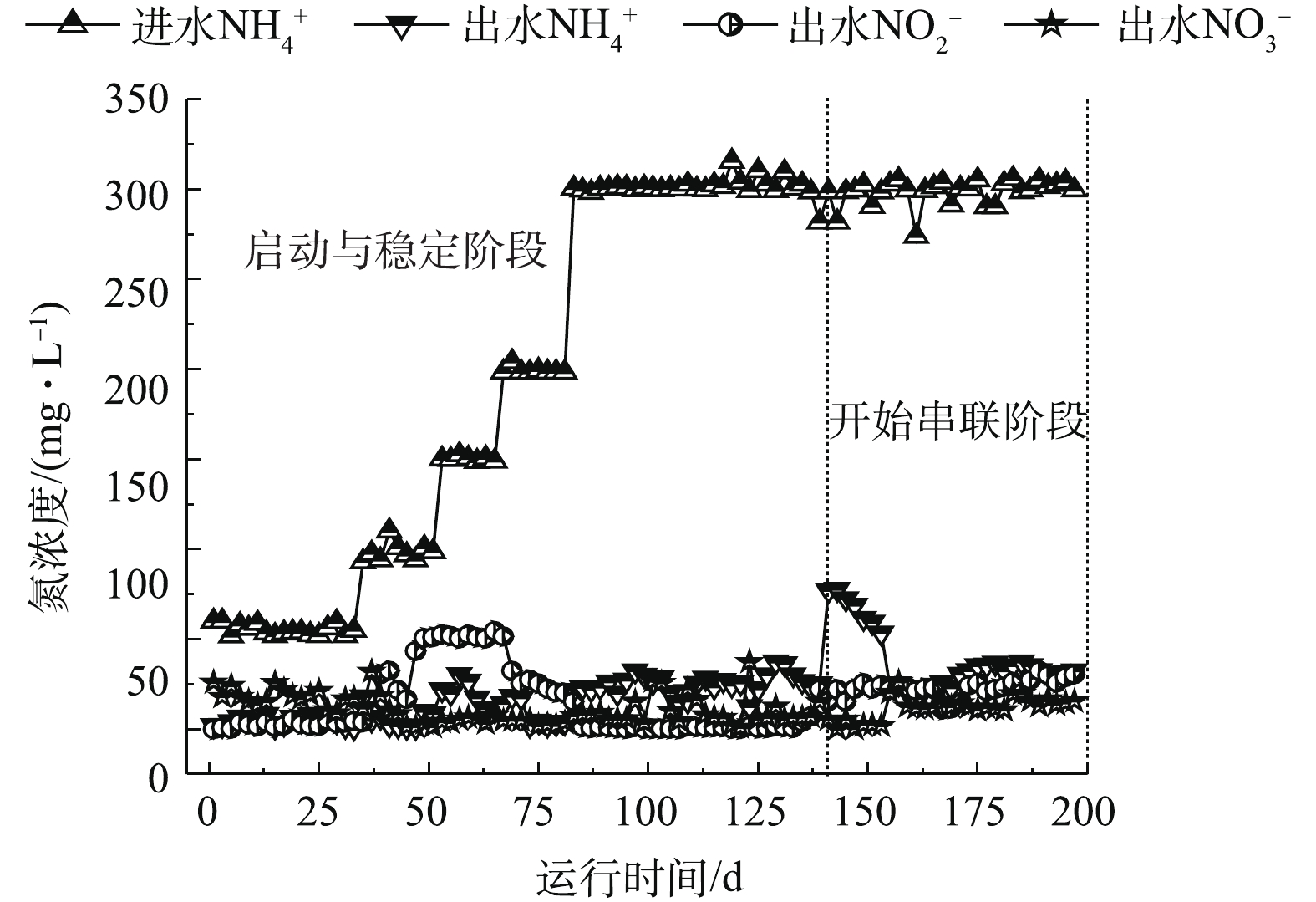
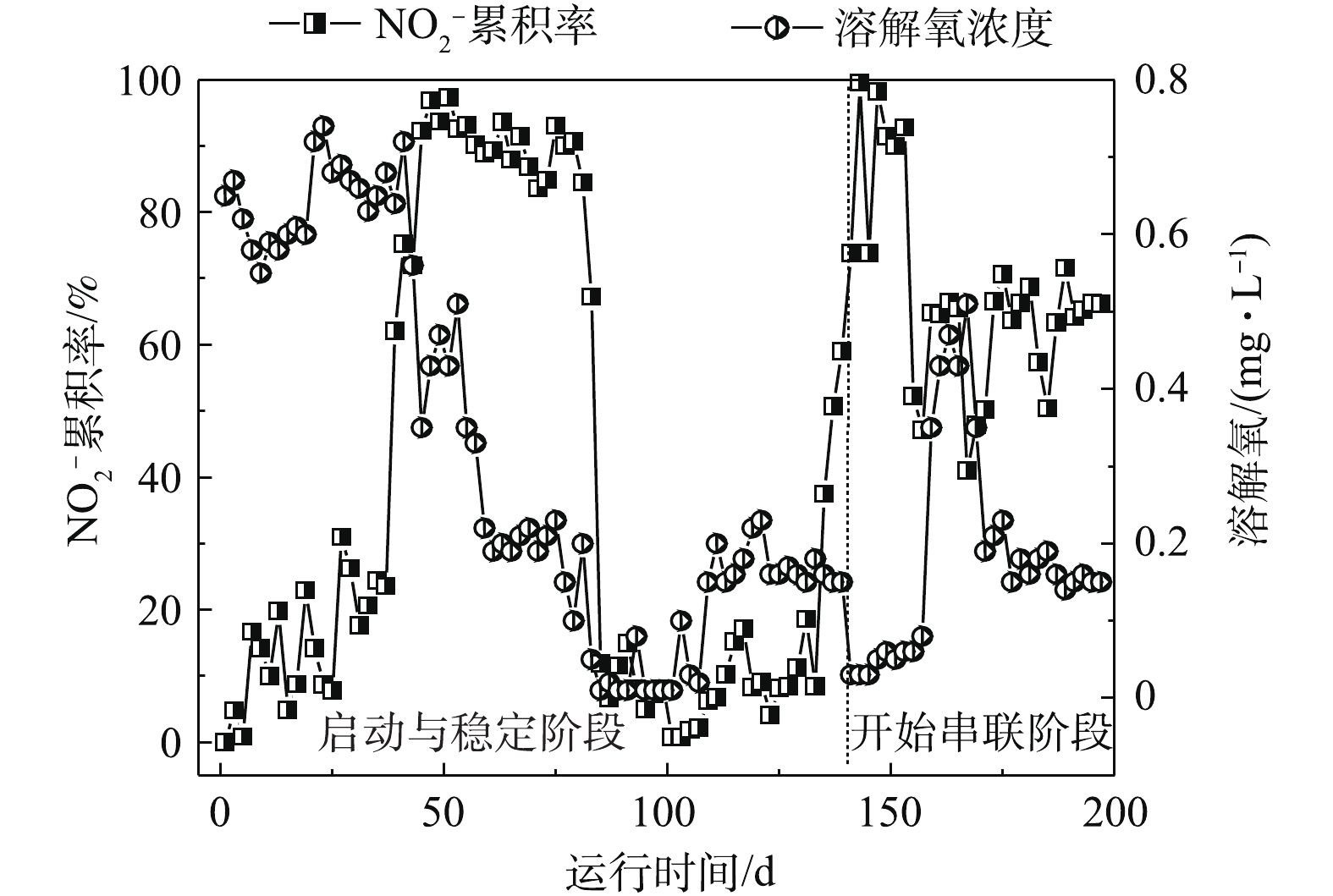
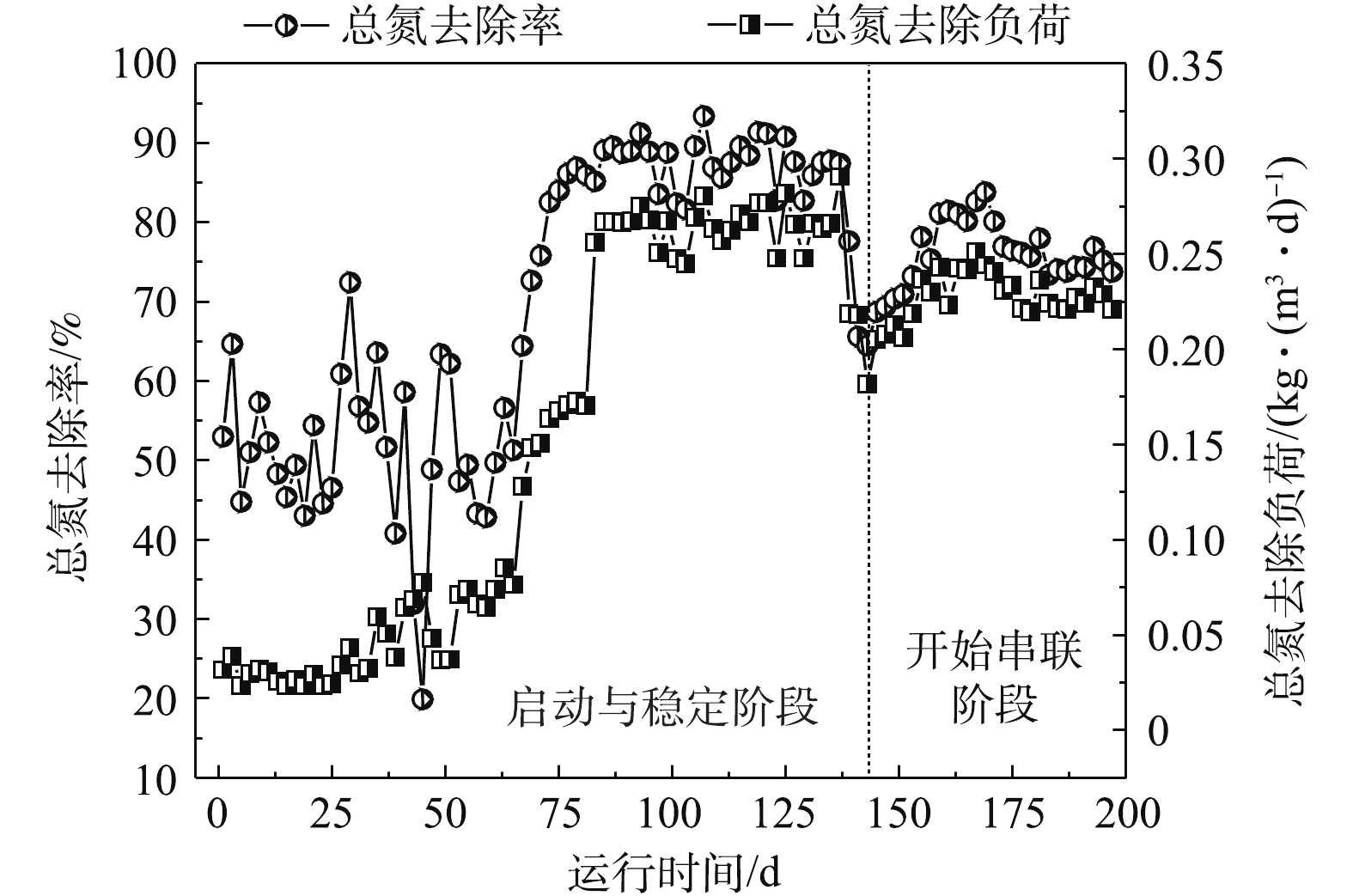
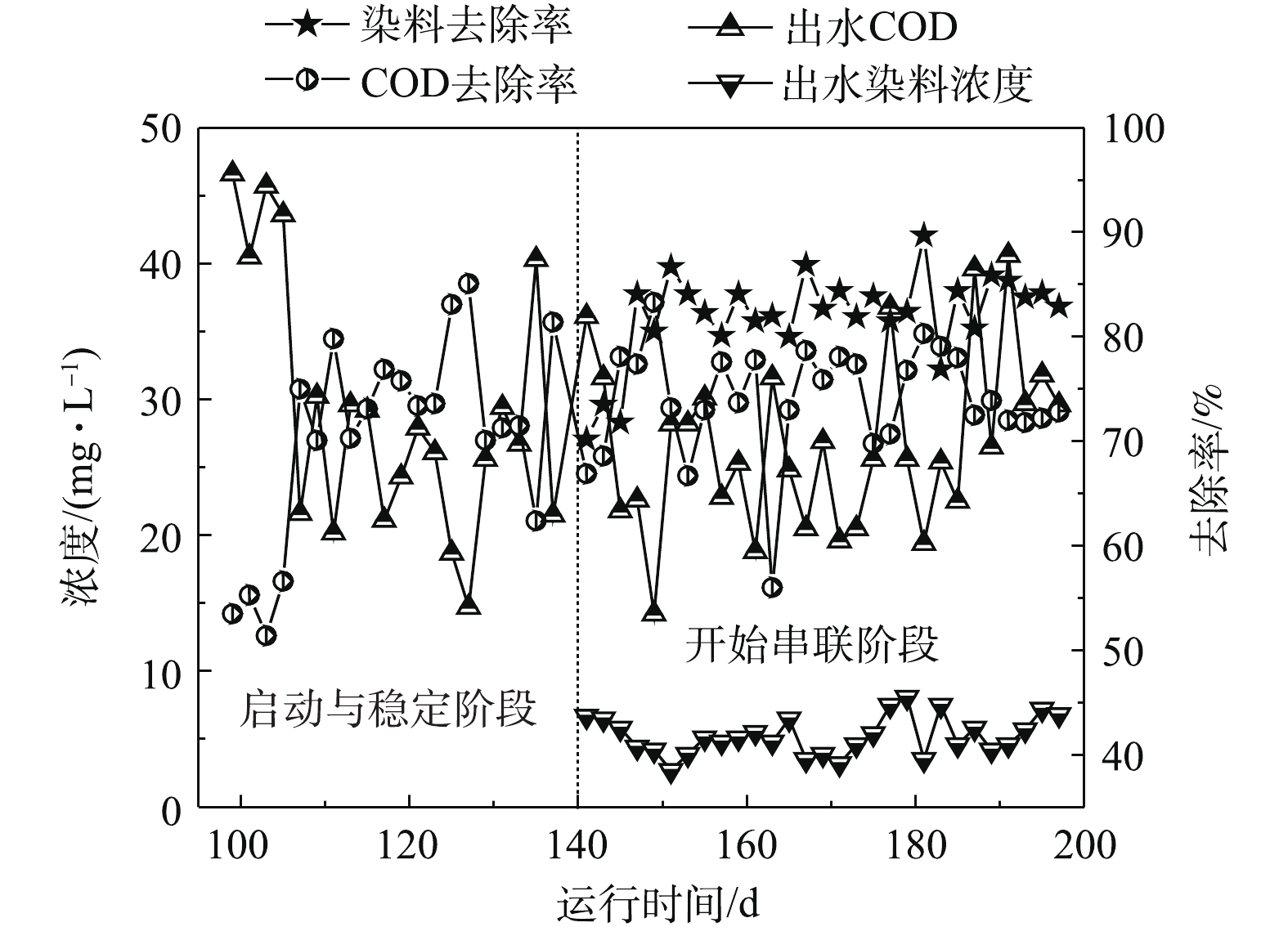
2) MBR-CANON反应器启动与运行。MBR-CANON反应器运行分为2个阶段。第1阶段为启动与稳定阶段,共运行140 d;第2阶段为与UASB串联阶段,共运行60 d,处理效果如图3~图6所示。在MBR-CANON反应器启动与稳定阶段,逐渐将反应器进水氨氮浓度由50 mg·L−1提高至100 mg·L−1,系统中生物量逐渐增多并且微生物逐渐适应水质。在第49天时,亚硝酸盐累积率增长至97%左右,此时亚硝化阶段出现并且趋于稳定。AOB比NOB的氧半饱和常数大,因此,在较低的溶解氧水平下,NOB难以和AOB竞争有限的氧气,从而抑制NOB活性。将反应器进水氨氮浓度提高为200 mg·L−1,此时反应器内溶解氧为0.2 mg·L−1左右,亚硝酸盐累积率逐渐下降,出水氨氮浓度持续降低,厌氧氨氧化反应逐渐出现,在第69天时,反应器总氮去除负荷达到0.15 kg·(m3·d)−1(大于0.10 kg·(m3·d)−1),标志着MBR-CANON反应器正式启动成功[21]。为了提高氨氮容积负荷,继续将反应器进水氨氮浓度提升至300 mg·L−1,反应器总氮去除率不断增高,到第140天时,总氮去除率最高达到91%,总氮去除负荷最高达到了0.29 kg·(m3·d)−1。为了强化MBR-CANON反应器去除COD的能力,在第99天时,开始向MBR-CANON反应器进水中加入100 mg·L−1淀粉。有研究[22]表明,加入少量COD并不会抑制AOB的活性,是因为反应器内COD过低或者溶解氧充足并未引起AOB和NOB对基质的竞争。而当C/N比为1.8~3.5时,AOB的活性将下降70%[23],本实验中也发现COD的加入并未抑制MBR-CANON反应器内AOB的活性。经过40 d运行后,反应器出水COD为29 mg·L−1左右,COD平均去除率最高达到85%以上。
MBR-CANON反应器运行140 d后,将UASB出水逐步添加至MBR-CANON进水中,正式进入UASB与MBR-CANON串联运行阶段。由图3可知,在第140天时,UASB出水接入MBR-CANON反应器后,微生物无法立刻适应进水水质的变化,导致其活性下降,反应器中总氮去除率和总氮去除负荷分别降到了约57%和0.18 kg·(m3·d)−1。在运行30 d后,增大反应器曝气量,使溶解氧升高,反应器内微生物逐渐适应进水水质条件,总氮去除率逐渐上升至82%以上。由图6可知,随着MBR-CANON反应器的不断运行,反应器出水COD平均值为26 mg·L−1左右,COD去除率缓慢上升并稳定在73%。MBR-CANON反应器对染料去除效果相对比较稳定,出水染料浓度平均为5 mg·L−1,染料的脱色率最高达到87%以上。
综上所述,在本实验条件下,接种厌氧氨氧化污泥的MBR-CANON反应器可在69 d内启动成功,并在140 d内达到稳定运行的状态,同时说明UASB/MBR-CANON串联工艺对高氮活性印花废水有良好的降解作用。
2.2 微生物多样性分析
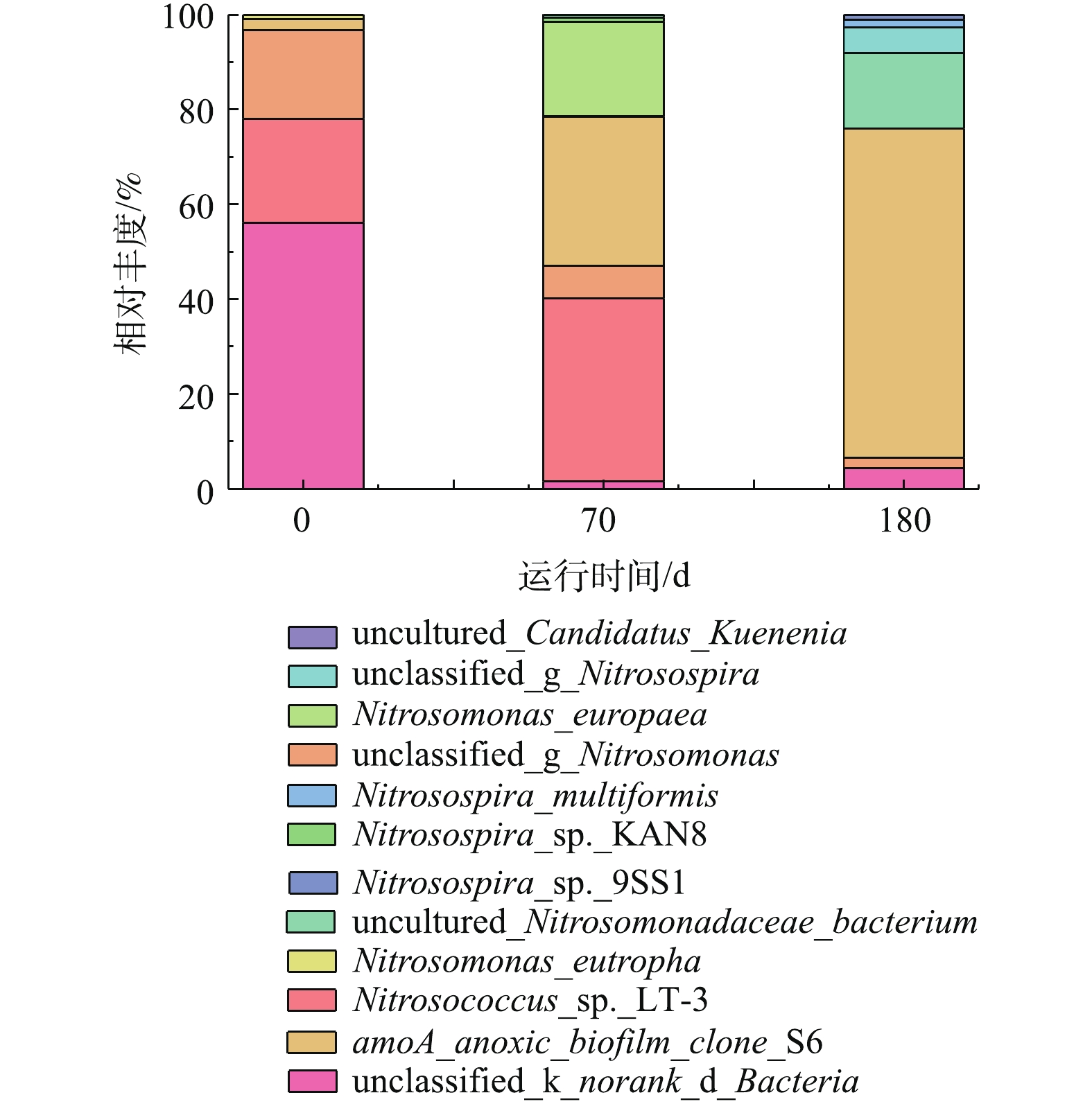
为了考察UASB/MBR-CANON串联工艺处理印花废水过程中MBR-CANON反应器中功能菌的种类及丰度变化情况,分别对反应器接种污泥、第70天和第180天污泥进行高通量测序,分析结果如图7所示。由图7可知,当MBR-CANON反应器启动成功后,亚硝化球菌的丰度由接种时的21.96%增长为38.54%,亚硝化单胞菌(Nitrosomonas_eutropha)的丰度由18.68%降为6.83%,同时出现了一种新的亚硝化单胞菌(Nitrosomonas_europaea,20%),说明随着反应器的运行,系统内亚硝化细菌种类和总相对丰度逐渐增多。此外,缺氧氨氧化菌[24](AmoA_anoxic_biofilm_clone_S6)的丰度由2.34%迅速增长到31.52%,同时出现了厌氧氨氧化菌(Candidatus_Kuenenia,0.001 9%),此时MBR-CANON反应器的脱氮效率在85%左右。这说明2种功能菌在脱氮中起着重要的作用,并且随着反应器的运行,功能菌种类也发生了变化。当UASB和MBR-CANON反应器串联运行稳定后,在第180天,测得系统内出现了大量的亚硝化螺旋菌,而亚硝化菌的总相对丰度逐渐降低。此外生物膜上生长的菌群中缺氧氨氧化菌(AmoA_anoxic_biofilm_clone_S6)和厌氧氨氧化菌(Candidatus_Kuenenia)的相对丰度分别增长至69.48%和0.32%,说明系统中起脱氮作用的氨氧化菌得到了增长。综上研究结果可知,在本研究条件下,印花废水中的污染物并未对系统内脱氮微生物的生长造成严重抑制。
2.3 全波段扫描分析
为了进一步探究活性黄染料的降解途径,本研究对活性黄染料、UASB反应器出水和MBR-CANON反应器出水进行紫外-可见全波段(UV-vis)扫描,扫描结果如图8所示。由图8可知,活性黄染料有4个特征吸收峰,其中224 nm处为苯环结构吸收峰,254 nm处为三嗪吸收峰,288 nm处为萘环吸收峰,而424 nm处为偶氮双键吸收峰,偶氮双键是形成发色体的主要基团[25]。经过UASB反应器厌氧降解后,位于424、254和288 nm的吸收峰基本消失,说明提供色度的偶氮双键被打开,同时三嗪结构和萘环结构可能被破坏。位于224 nm的苯环吸收峰只是降低但并未消失,可能是由于染料本身结构中的苯环已经被破坏,但三嗪和萘环在厌氧条件下可降解为含有苯环结构的物质,因此,苯环吸收峰仍然存在。接着经过MBR-CANON反应器处理之后,吸收峰位置基本未发生变化但吸光度降低,其原因可能是因为MBR-CANON反应器内生物膜的吸附作用和膜组件的过滤作用使染料进一步截留。
2.4 MBR-CANON反应器膜污染分析
图9反映了MBR-CANON反应器中胞外聚合物(extracellular polymeric substances, EPS)中多糖和蛋白质浓度变化及膜通量的衰减情况。由图9可知,膜表面滤饼层EPS中多糖和蛋白质含量在第40天时分别为30.53 mg·L−1和3.70 mg·L−1,第80天为15.30 mg·L−1和6.06 mg·L−1,第180天时为52.14 mg·L−1和17.40 mg·L−1。以上结果表明,多糖和蛋白质含量在膜清洗后有所下降,但总体呈现上升趋势,这可能是因为EPS作为形成生物膜的重要组成部分[26],混合液中的浓度与污泥浓度成正相关关系,随着反应器中微生物的浓度不断升高,污泥混合液中多糖和蛋白质含量不断增加,分离过程中被膜表面截留并不断累积。
膜表面的EPS累积会造成膜通量的衰减[27],MBR-CANON反应器运行200 d期间,膜通量由最初5.79 L·(m2·h)−1衰减至0.96 L·(m2·h)−1,经过清洗后,膜通量可迅速恢复初始通量的80%~90%。同时由于较大的膜出水通量会加速膜污染,污泥容易堵塞膜孔,从而造成更严重的膜污染[28],因此,经过分析验证,本实验中将膜通量控制在6 L·(m2·h)−1以下,此时过滤阻力较小,可有效减缓膜污染。
3. 结论
1) 采用逐渐提高COD容积负荷的方式启动UASB反应器,其在运行40 d后成功启动,印花废水中COD去除率最高可达到90%,染料的脱色率最高可达到88%;采用逐渐提高进水氨氮容积负荷的方式启动MBR-CANON反应器,其在运行69 d后成功启动,总氮去除率最高达到90%以上,总氮去除负荷最高达到0.29 kg·(m3·d)−1。
2) UASB/MBR-CANON串联运行后,该工艺处理活性印花废水总氮去除率达到70%以上,COD去除率和染料脱色率均达到90%以上。
3) 在MBR-CANON反应器处理活性印花废水过程中,功能菌AmoA_anoxic_biofilm_clone_S6的相对丰度由2.34%逐渐增高至69.48%,并且培养出了Candidatus_Kuenenia,其相对丰度增长至0.32%。
4) UASB/MBR-CANON反应器采用水力循环方式连续冲刷膜组件,经过清洗后,膜通量可恢复至原始通量的80%~90%,可有效减缓膜污染。
-
-
[1] 赵大伟, 张鹏. 化学镀铜的应用与发展[J]. 黑龙江冶金, 2010, 31(1): 38-39. [2] 田庆华, 闫剑锋, 郭雪益. 化学镀铜的应用与发展概况[J]. 电镀与涂饰, 2007, 26(4): 38-41. doi: 10.3969/j.issn.1004-227X.2007.04.012 [3] LIN Y M, YEN S C. Effects of additives and chelating agents on electroless copper plating[J]. Applied Surface Science, 2001, 178(1-4): 116-126. doi: 10.1016/S0169-4332(01)00306-3 [4] YUAN X L, GAO J, YANG Z F, et al. New electroless copper plating bath using sodium hypophosphite as reductant[J]. Surface Engineering, 2012, 28(5): 377-381. doi: 10.1179/1743294411Y.0000000049 [5] 黄万抚, 胡昌顺, 曹明帅, 等. 难处理含铜废水处理技术研究[J]. 应用化工, 2018, 47(10): 2248-2253. doi: 10.3969/j.issn.1671-3206.2018.10.047 [6] 李立清, 冯罗, 吴盼旺, 等. 新型次磷酸钠体系化学镀铜添加剂及其对镀液和镀层性能的影响[J]. 表面技术, 2020, 49(7): 329-337. [7] CHANG Y, DENG L, MENG X Y, et al. Closed-loop electrochemical recycling of spent copper(II) from etchant wastewater using a carbon nanotube modified graphite felt anode[J]. Environmental Science & Technology, 2018, 52: 5940-5948. [8] LIU P, LI C L, LIANG X G, et al. Advanced oxidation of hypophosphite and phosphite using a UV/H2O2 process[J]. Environmental Technology, 2013, 34(15): 2231-2239. doi: 10.1080/09593330.2013.765917 [9] LIU P, Li C, LIANG X, et al. Recovery of high purity ferric phosphate from a spent electroless nickel plating bath[J]. Green Chemistry, 2014, 16(3): 1217-1224. doi: 10.1039/C3GC41779D [10] 郭燕妮, 方增坤, 胡杰华, 等. 化学沉淀法处理含重金属废水的研究进展[J]. 工业水处理, 2011, 31(12): 9-12. doi: 10.11894/1005-829x.2011.31(12).9 [11] 王蓬勃, 李金花, 周保学, 等. 电镀含铜废水的资源化回收利用[J]. 环境科学与技术, 2020, 43(S2): 184-187. [12] 张惠灵, 杨瑾, 吴健, 等. 电沉积法回收离子交换再生液中Cu2+的研究[J]. 电镀与精饰, 2014, 36(3): 43-46. doi: 10.3969/j.issn.1001-3849.2014.03.011 [13] ZHAO X, ZHANG J J, QIAO M, et al. Enhanced photoelectrocatalytic decomposition of copper cyanide complexes and simultaneous recovery of copper with a Bi2MoO6 electrode under visible light by EDTA/K4P2O7[J]. Environmental Science & Technology, 2015, 49(7): 4567-4574. [14] 陈佩仪, 李彦旭, 孙楹煌, 等. 光电催化水处理技术研究进展[J]. 工业水处理, 2005, 25(12): 13-17. doi: 10.3969/j.issn.1005-829X.2005.12.004 [15] JEON T H, KOO M S, KIM H, et al. Dual-functional photocatalytic and photoelectrocatalytic systems for energy- and resource-recovering water treatment[J]. ACS Catalysis, 2018, 8(12): 11542-11563. doi: 10.1021/acscatal.8b03521 [16] PARK H, PARK Y, KIM W, et al. Surface modification of TiO2 photocatalyst for environmental applications[J]. Journal of Photochemistry and Photobiology C-Photochemistry Reviews, 2013, 15: 1-20. doi: 10.1016/j.jphotochemrev.2012.10.001 [17] MACAK J M, TSUCHIYA H, TAVEIRA L, et al. Smooth anodic TiO2 nanotube[J]. Angewandte Chemie International Edition, 2005, 44: 7463-7465. doi: 10.1002/anie.200502781 [18] MOR G K, SHANKAR K, PAULOSE M, et al. Use of highly-ordered TiO2 nanotube arrays in dye-sensitized solar cells[J]. Nano Letters, 2006, 6: 215-218. doi: 10.1021/nl052099j [19] WANG J, LIN ZQ. Anodic Formation of Ordered TiO2 Nanotube Arrays: Effects of electrolyte temperature and anodization potential[J]. Journal of Physical Chemistry C, 2009, 113: 4026-4030. doi: 10.1021/jp811201x [20] ZHAO X, ZHANG J J, QU J H. Photoelectrocatalytic oxidation of Cu-cyanides and Cu-EDTA at TiO2 nanotube electrode[J]. Electrochimica Acta, 2015, 180: 129-137. doi: 10.1016/j.electacta.2015.08.103 [21] ÖĞÜTVEREN Ü B, TÖRÜ E, KOPARAL S. Removal of cyanide by anodic oxidation for wastewater treatment[J]. Water Research, 1999,33(8): 1851-1856. [22] CHEN W S, HUANHG C P. Mineralization of aniline in aqueous solution by electrochemical activation of per-sulfate[J]. Chemosphere, 2015, 125: 175-181. doi: 10.1016/j.chemosphere.2014.12.053 [23] MILLER J S, OLEJNIK D. Photolysis of polycyclic aromatic hydrocarbons in water[J]. Water Research, 2001, 35(1): 233-243. doi: 10.1016/S0043-1354(00)00230-X [24] HERNLEM B J, Electrolytic destruction of urea in dilute chloride solution using DSA electrodes in a recycled batch cell[J]. Water Research, 2005, 39(11): 2245-2252. [25] NAM S W, YOON Y, CHOI D J, et al. Degradation characteristics of metoprolol during UV/chlorination reaction and a factorial design optimization[J]. Journal of Hazardous Materials, 2015, 285: 453-463. doi: 10.1016/j.jhazmat.2014.11.052 [26] XIAO S, QU J, ZHAO X, LIU H, et al. Electrochemical process combined with UV light irradiation for synergistic degradation of ammonia in chloride-containing solutions[J]. Water Research, 2009, 43(5): 1432-1440. doi: 10.1016/j.watres.2008.12.023 期刊类型引用(3)
1. 张晓晶,张志,裘思谦,王江龙,赵唯. 基于UASB+MBR乳制品废水处理系统的研制及运行效果. 中国现代教育装备. 2021(15): 59-62 .  百度学术
百度学术
2. 赵阁阁,孙婧,张运波,王洪波,吴俊森. 高级氧化技术处理印染废水的研究进展. 应用化工. 2021(09): 2550-2554+2558 .  百度学术
百度学术
3. 马慧婕,沈忱思,章耀鹏,徐晨烨,马春燕,刘艳彪,石磊,李方. 纺织工业产排污特征与水污染治理技术进展. 环境科学研究. 2020(11): 2529-2539 .  百度学术
百度学术
其他类型引用(12)
-






 下载:
下载: