-
肼(N2H4)又称联氨,是实验室常用化学品,具有较强的腐蚀性和还原性,应用广泛,在航空航天、工业生产、农业生产领域发挥重要作用[1 − 2]. 然而,肼有毒性,泄露会对环境造成巨大危害[3]. 研究表明,肼可以透过表层皮肤和呼吸粘膜进入生物体[4],对机体造成不可逆损坏[5]. 多数国家将一水合肼(N2H4·H2O)列为可致癌物质严格管控[6],我国明令禁止肼超标,规定生活饮用水源中的肼浓度严格控制在0.02 mg·L−1 (0.62 μmol·L−1)以内[7],地表水中肼的浓度严格控制在0.01 mg·L−1 (0.31 μmol·L−1)以内[8]. 肼检测的传统分析方法有滴定法[9]、伏安法[10]、电化学[11]和高效液相色谱法(HPLC)[12]等,但这些方法在不同程度上存在着缺陷,如检测仪器昂贵、样品制备繁琐、检测环境严格和实验条件复杂等. 因此,开发对肼高效便捷定性定量荧光检测方法具有重要意义.
肼的荧光检测技术最早出现在2011年[13]. 已报道肼探针的设计原理大致可以分为“反应型”和“材料型”的两种. “反应型”传感器的识别基团通常与荧光基团相连,荧光探针专一地与肼发生化学反应,反应类型包括去保护[14]、基团转化[15]、环化[16]和开环反应[17]等,探针与肼反应后荧光信号的变化表明肼的存在,并且基本与肼的浓度直接相关. “材料型”传感器利用肼的碱性、还原性和可成氢键性来设计. 金属有机框架(MOFs)[18]、聚合物泡囊(Polymersome)[19]、银纳米颗粒(AgNPs)[20]、金纳米颗拉(AuNPS)[21]和AIEens材料(AIE Enhancers)[22]被巧妙地用作这种设计的载体,从而实现了肼的荧光检测. 肼荧光检测追求更精确的机制、更高效的光源、更准确的数据反馈和更扩展的实用功能[23]已成为研究的热点. 3-羟基黄酮母核具有良好的光化学和光物理性质,常用作荧光探针的光源,其发光原理是激发态分子内质子转移(Excited-state intramolecularproton transfer,ESIPT)[24 − 26]. 氟对生命科学十分重要,由于氟原子电负性很强,药物分子上的氢被氟取代后可明显降低分子区域电子云密度,增强分子的抗氧化能力,可改变溶解度、酸碱度、构象以及生物利用度,常用作提高药物代谢稳定性的有效策略.
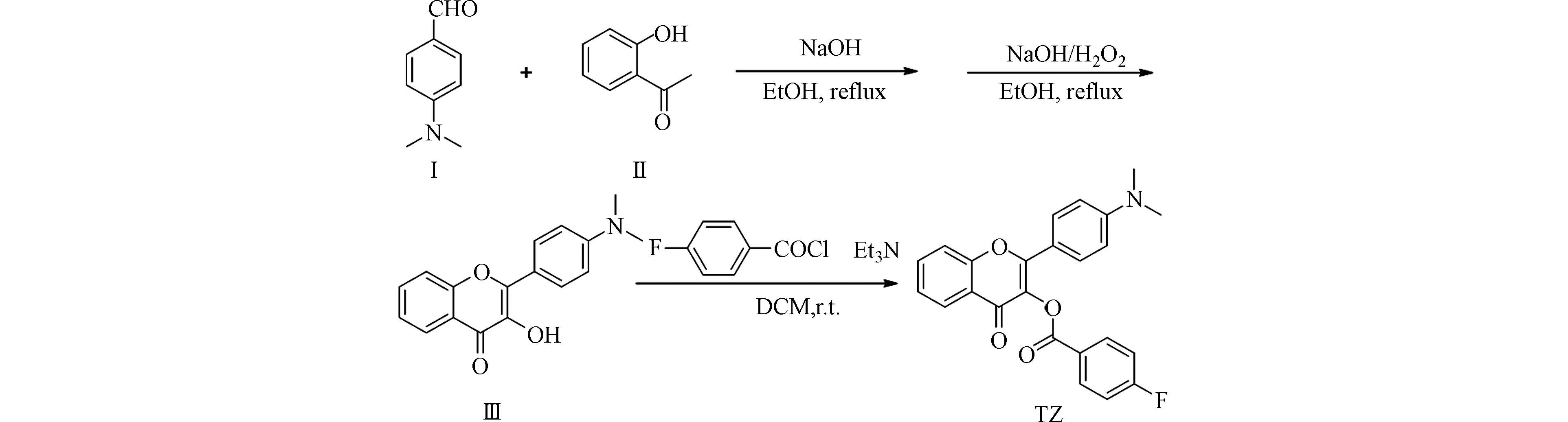
本研究以3-羟基黄酮为荧光团,对氟苯甲酰基为羟基保护基团,设计一种全新引入氟原子、可用于检测肼的荧光探针,为建立具有较好的响应性、选择性、灵敏度和潜在生物活性的肼检测方法提供依据. 具体合成方法如图1所示.
-
对二甲氨基苯甲醛,分析纯,天津市致远化学试剂有限公司;羟基苯乙酮、对氟苯甲酸,分析纯,阿拉丁试剂(上海)有限公司. 碳酸钠,氯化钠、溴化钠、碘化钠、氟化钾、磷酸钠、硫酸钠、亚硫酸氢钠、硫酸钠、碳酸钠、硝酸钠、氨水、硫氰酸钠、硝酸铜、硫酸铁、氯化钙、碳酸镁、碳酰胺、肼、盐酸均为分析纯,采购于上海振企化学试剂有限公司、天津大茂化学试剂有限公司、阿拉丁试剂(上海)有限公司等. 所用溶剂均为分析纯. 薄层层析硅胶GF254购自青岛海洋化工厂.
Bruker Advance 300 MHz型核磁共振仪,美国Bruker公司;Hitachi F-4500荧光分光光度计,日本HITACHI公司;HP-5989型质谱仪,美国HP公司.
-
依次将化合物I(对二甲氨基苯甲醛,0.1491 g,0.001 mol)、化合物II(羟基苯乙酮,0.1633 g,0.0012 mol)、氢氧化钠(0.4 g,0.010 mol)、无水乙醇(10 mL)加入至圆底烧瓶(100 mL)中,80 ℃下搅拌3 h后,加入氢氧化钠溶液(10 mL,1 mol·L−1)、过氧化氢(8 mL,质量分数35%),在室温下继续反应3 h后,调节pH=8—9(1 mol·L−1的盐酸),有固体析出,抽滤,石油醚打浆后,得到化合物 Ⅲ(2-(4-(二甲基氨基)苯)-3-羟基黄酮,黄色固体,0.1212 g,0.43 mmol),产率为60.32%,液相色谱纯度为96.40%. 1H NMR (CDCl3, 300 MHz), δ: 8.23 (d, J=8.8 Hz, 2H), 8.07 (d, J=7.6 Hz, 1H), 7.77—7.60 (m, 2H), 7.40 (td, J=5.4 Hz, J=2.3Hz, 1H), 6.75 (d, J=8.8 Hz, 2H), 3.10 (s, 6H). 13C NMR (75 MHz, CDCl3), δ:172.5, 155.1, 151.4, 141.2, 136.9, 132.9, 129.2, 125.3, 124.2, 120.9, 118.0, 111.5, 97.2, 40.1. MS, m/Z:[M+H]+理论值282.11;测试值282.10.
将4-氟苯甲酸(0.1411 g,0.001 mol)溶于二氯甲烷(10 mL),氮气保护下冷却至0℃,滴入草酰乙酸(0.5076 g,0.004 mol,0.338 mL),滴完后升至室温,加热至回流,反应2 h. 旋转蒸发除去溶剂,得到对氟苯甲酰氯,直接下一步反应.
称取化合物Ⅲ(0.2000 g,0.7100 mmol),溶于10 mL的二氯甲烷中,随后加入三乙胺0.25 mL(液体,1.8 mmol),向其中逐滴加入对氟苯甲酰氯溶液2 mL(液体,0.7100 mmol),室温条件下搅拌反应2 h后,经薄层硅胶板(V石油醚:V乙酸乙酯=3:1)点样检测. 待反应完成后,加入20 mL的蒸馏水,分液漏斗分液弃去水相,有机相使用10 mL的饱和食盐水洗涤两次,将其转移至锥形瓶,加入无水硫酸镁干燥. 旋转蒸发除去溶剂,得到探针TZ [2-(4-(二甲基氨基)苯基)-3-(4-氟苯甲酸酯)-4-氧代苯并吡喃,淡黄色固体,0.1779 g,0.46 mmol],产率为64.92%. 液相色谱纯度为95.26%. 1H NMR (DMSO-d6, 300 MHz) δ 8.27 (dd, J=8.9, 5.5 Hz, 2H), 8.07 (dd, J=7.9, 1.4 Hz, 1H), 7.90–7.82 (m, 4H), 7.50 (dd, J=16.7, 7.8 Hz, 3H), 6.83–6.78 (m, 2H), 2.99 (s, 6H). 13C NMR (DMSO-d6, 75 MHz) δ 170.42, 164.06, 162.36, 156.41, 154.87, 152.15, 134.36, 133.18, 133.04, 131.23, 129.42, 125.49, 124.98, 124.78, 124.74, 122.74, 118.50, 116.63, 116.34, 115.01, 111.52, 109.56, 39.78, 39.65. MS, m/Z:[M+H]+理论值404.13;测试值404.10.
-
准确称取探针TZ 10.08 mg (25.0 µmol)于乙醇(2 mL)溶液,在25 ℃环境下,采用50 Hz频率,超声(10 min)至完全溶解. 转移至25 mL容量瓶,水定容,浓度为1.0×10−3 mol·L−1. 移取所得母液5.0 mL至25 mL容量瓶,水定容至刻度线,摇匀,得到待测液(2.0×10−4 mol·L−1). 相同方法配制2.0×10−4 mol·L−1的F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3、N2H4储备液(溶剂为水).
-
探针TZ在激发波长为405 nm时,探针无荧光. 将探针TZ溶液和待测溶液混合于10 mL比色管,摇匀,定容. 充分振荡,10min后,测定探针化合物的荧光发射光谱. 仪器设置参数:激发狭缝宽度2.5 nm,发射狭缝宽度5.0 nm,灵敏度为1,响应时间0.5 s,于400—700 nm内检测荧光. 样品池为1.0 cm×1.0 cm×4.0 cm石英比色皿.
-
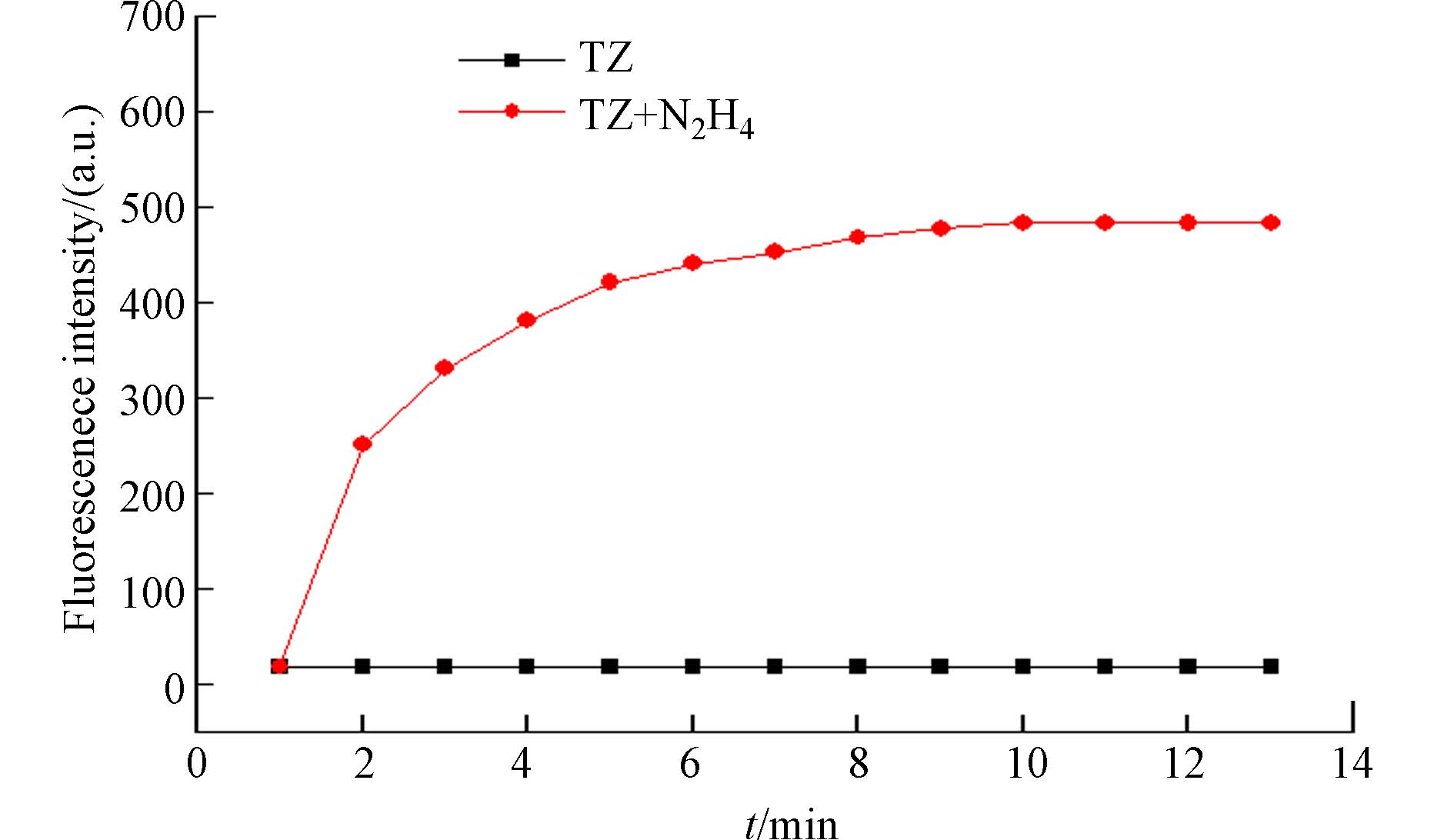
如图2所示,探针TZ本身在发射波长为530 nm处无荧光,当肼加入之后,在波长为530 nm处的发射光谱的荧光强度迅速增强,10 min后,达到最大值,且保持稳定,持续延长反应时间不再增强荧光强度. 由此可知,探针TZ对肼的检测具有很好的灵敏性,响应时间为10 min,低于一些已报道的肼检测荧光探针[17,27 − 30].
-
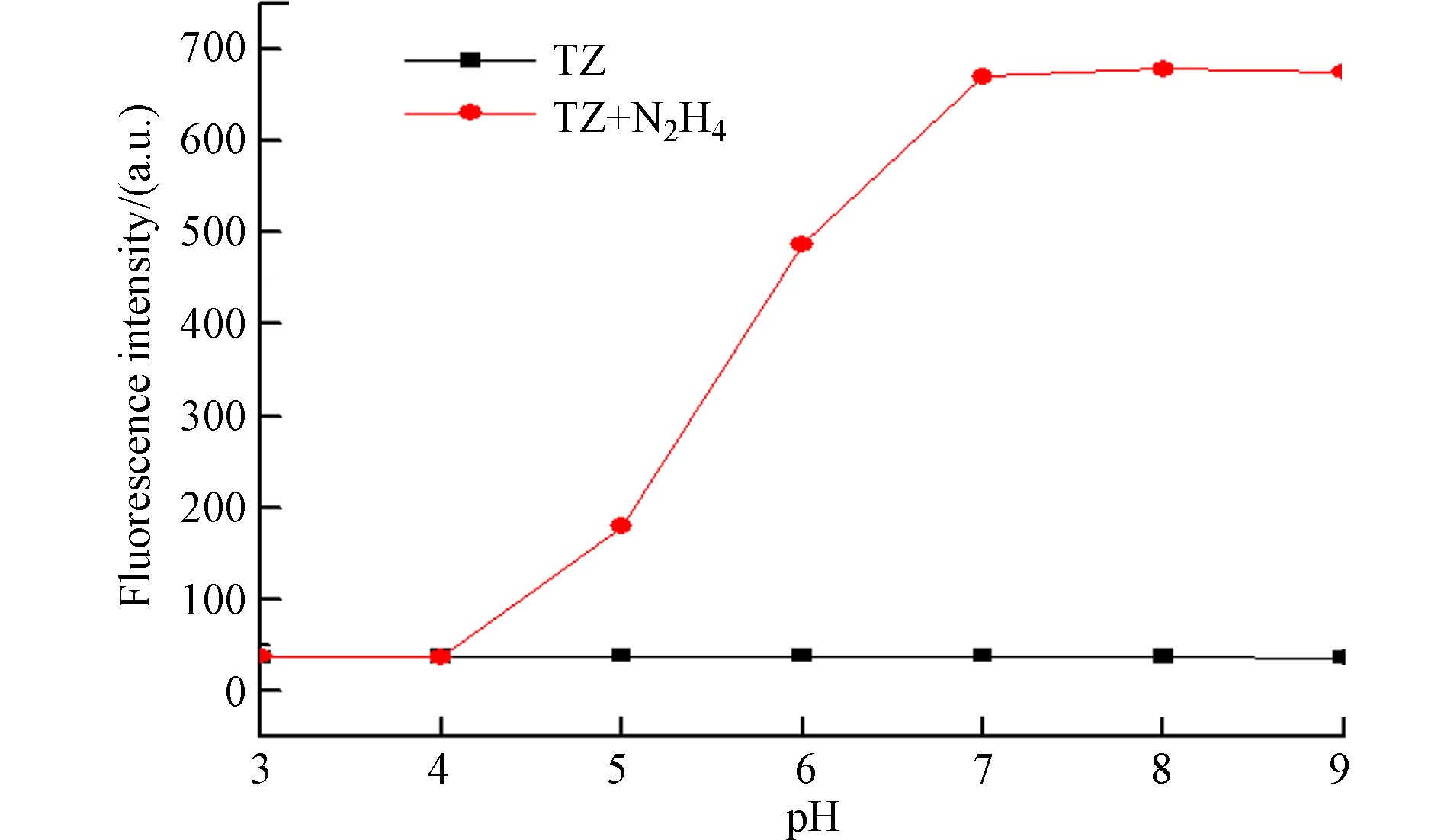
考察pH对检测效果的影响对探针普适性应用有重要意义. 如图3所示,pH对探针TZ与肼的化学反应有很大影响,体系的荧光强度随着pH的增大而增大. 可能是肼优先与水溶液中的酸结合,生成酸碱中和反应产物,影响与探针分子的反应. 实验表明,pH大于7以后的发射强度都不受溶液pH的干扰,可作为可靠的检测肼浓度的探针.
-
如图4所示,在探针TZ (10 μmol·L−1)的Tris-HCl /乙醇(9:1,V /V,pH=7.40)溶液中,加入2倍量的各种物质(F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3、N2H4)溶液,测量其荧光发射光谱(λex=530 nm). 结果表明,加入N2H4的探针溶液荧光强度明显增强,其余对照组加入其它物质后探针溶液荧光强度几乎未改变,表明探针TZ对N2H4具有较好的选择性识别能力,且不受其他物质干扰.
-
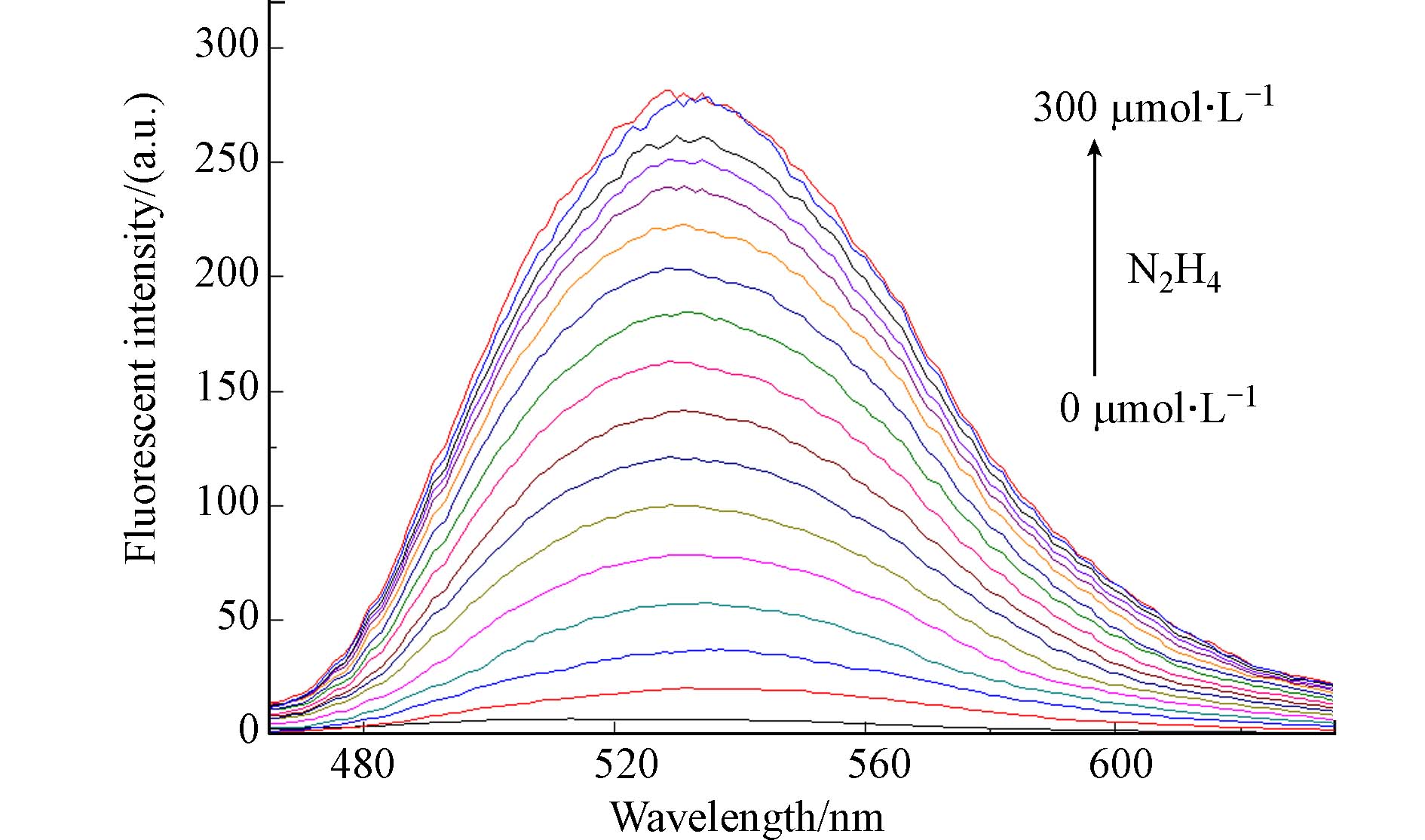
为进一步考察探针TZ在不同量肼加入后荧光强度变化的具体情况,通过控制N2H4的加入量,检测探针TZ体系荧光强度的变化. 结果如图5所示,探针TZ对肼具有很好的灵敏度,随着肼的加入量越来越多,体系的荧光强度不断增强(λem=530 nm),直至达到最大值,累计增强约43倍,此时探针与肼的反应达到平衡.
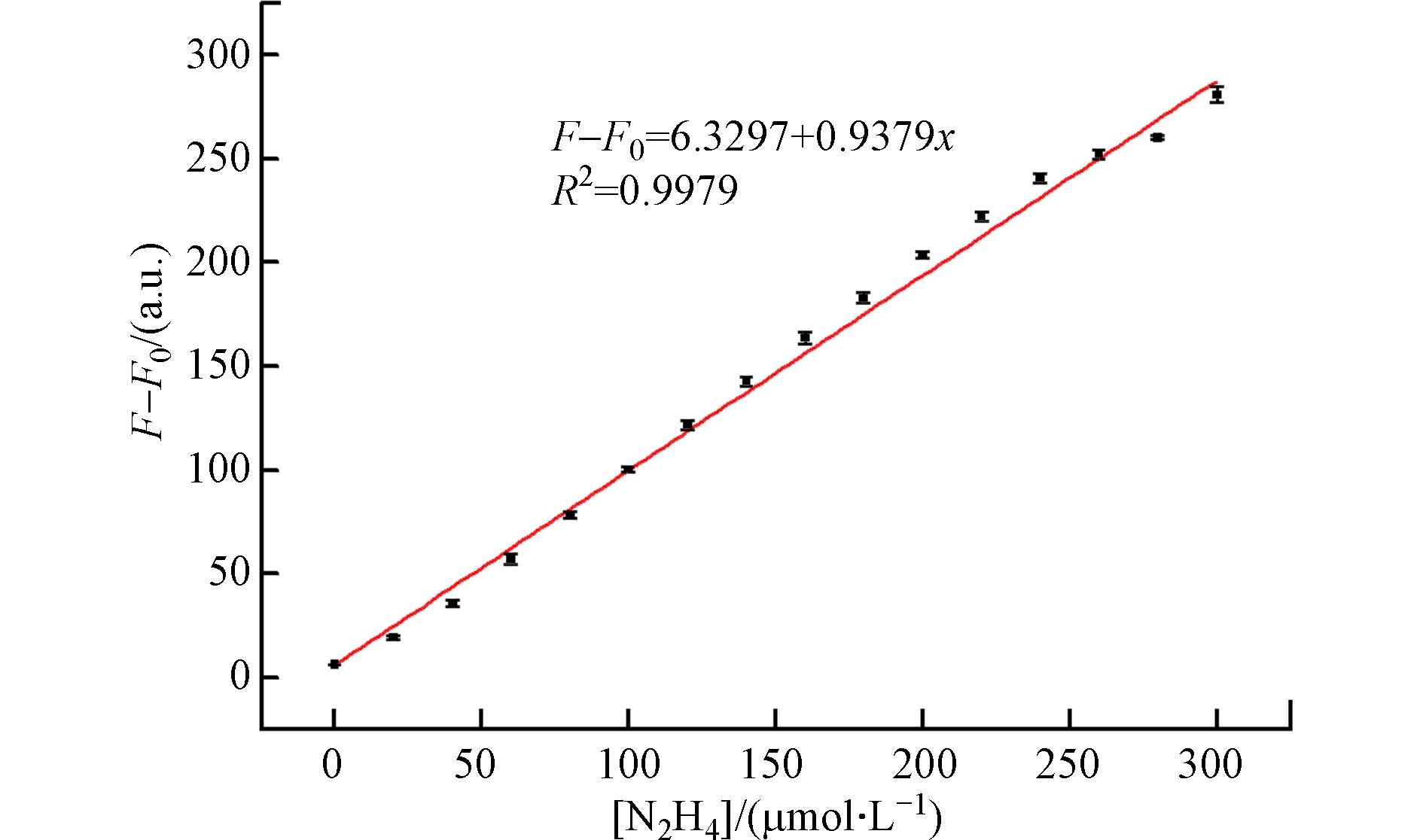
对不同量的肼加入后探针TZ体系在发射光谱为530 nm处的荧光强度进行线性拟合. 如图6所示,肼浓度在20—300 μmol·L−1,探针体系的荧光强度呈现良好线性关系,经拟合得到线性回归方程.
式中: F为测试荧光强度,F0为空白对照荧光强度,C为肼浓度,单位为μmol·L−1. 相关系数R2=0.9979.
根据检出率计算公式“LOD=3σ/k(LOD为检出限、σ为空白样本检出荧光强度5次检测值标准偏差、k为荧光强度与肼浓度线性回归曲线的斜率)”,计算出探针TZ检测肼的检出限为0.1103 μmol·L−1. 与一些已报道的肼检测荧光探针[17,27 − 30]相比,探针TZ的检出限更低.
-
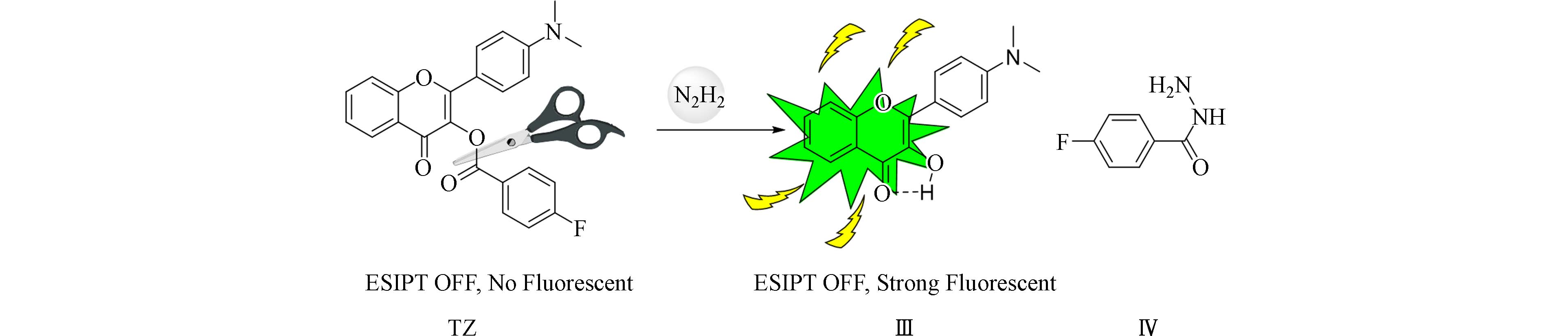
探针分子作用机制是肼的亲核加成反应. 待测物肼是亲核性很强的一类化合物,肼分子氮原子上有孤对电子,可以对酯基官能团中处于缺电子状态的羰基碳作用,引发碳氮新键生成,碳氧旧键断裂的盖布瑞尔反应. 受自身电子效应影响,探针TZ本身在溶液体系中具有微弱荧光性质,当遇到体系中游离的肼后,会发生酯的肼解反应,探针TZ分子3位酯基被肼解离,原则上可以生成3位为裸露的羟基的黄酮醇化合物和酰基肼类化合物,如图7所示. 已有研究显示,黄酮醇化合物III具有较强荧光,原因是分子中与3位羟基相连的氢原子4位羰基的氧原子的距离为0.21 nm[31],可以形成分子内氢键稳定形态,与黄酮母环共同构成相对稳定的5元环,发生激发态分子内质子转移(ESIPT).
如图8所示,当肼加入到探针体系后,探针分子迅速与肼反生反应,在反应检测的核磁中发现,在低场区出现一个新的单峰(δ 9.22 ppm)见a区,b区的一组dd峰随着反应的进行逐渐消失了,c区、d区、e区、f区则在裂分和位移上均明显发生了变化.
对反应进行HPLC色谱分析发现,探针分子原本的保留时间为6.107min. 当肼加入后,在保留时间5.367 min处,出现一个新的产物吸收峰,当反应结束后,体系中仅在保留时间1.773 min、5.367 min两处有吸收峰,保留时间为6.107 min探针分子的吸收峰则完全消失. 需要说明的是黄酮醇化合物在相同条件下保留时间为5.367 min. 经过质谱确认,保留时间1.773 min、5.367 min两个吸收峰,所对应的质谱值分别为155.1,282.1,与机理预测中化合物IV(对氟苯甲酰肼)和黄酮醇化合物Ⅲ理论质谱值一致. 经验证,反应结束后的生成化合物核磁裂分与黄酮醇化合物Ⅲ一致,进一步确认探针TZ对N2H4的识别机理.
-
如表1所示,探针TZ可用于实际水样中肼的检测. 采用加标回收实验[32-33]验证黄酮类肼探针的对实际环境中肼检测的情况. 取实验室自来水、去离子水(实验室自制)、丹江自然流水(采样点为陕西省商洛市商州区段),3次测量取平均值,检测样品中的肼. 3种样品中均未检测出肼存在. 回收率在97.00%—102.67%范围之间,测试样品的相对标准偏差RSD值在3%以内.
-
(1)利用黄酮醇合成方法优化的“一锅法”合成工艺,合成黄酮醇化合物,以此为母核,在黄酮醇3位羟基上引入对氟苯甲酰基酯,合成未见报道的一种引入氟原子的新型肼探针.
(2)在pH = 7.4的条件下,进入探针体系的肼与探针分子发生盖布瑞尔反应,导致探针分子酯基结构被破坏,生成黄酮醇母环,探针分子的电子环境被破坏,生成物黄酮分子3位羟基与母核4位羰基形成氢键,构成相对稳定的5元环,化合物发生激发态分子内质子转移(ESIPT),释放出很强的荧光. 探针TZ检测肼的检出限为0.1103 μmol·L−1,在20—300 μmol·L−1呈现良好的线性关系,达到定性、定量检测肼的效果,为肼的化学检测提供了一种选择方法,实测样品回收率在97.00%—102.67%范围之间.
(3)利用核磁、色谱和质谱技术验证了该类型荧光探针与肼作用机制. 肼的强亲核作用使探针分子酯基断裂,解离成黄黄酮醇中间体(2-(4-(二甲基氨基)苯)-3-羟基黄酮)和对氟苯甲酰肼.
新型黄酮醇类肼探针的设计、合成与应用
Design and synthesis of a novel flavone-based fluorescent probe for hydrazine detection and its application
-
摘要: 以黄酮醇[2-(4-(二甲基氨基)苯)-3-4-氧代苯并吡喃]为荧光母核,设计合成一种新型黄酮醇类肼(N2H4)探针[2-(4-(二甲基氨基)苯基)-3-(4-氟苯甲酸酯)-4-氧代苯并吡喃,TZ],并利用核磁共振(1H NMR、13C NMR )和质谱(MS)确证其结构. 通过测定探针TZ的选择性、竞争性、浓度梯度、Job’s曲线和pH对探针分子荧光强度的影响,发现在pH=7.4的条件下,当肼加入探针体系后,探针溶液荧光显著增强,探针对F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3、N2H4,具有非常强的抗干扰性. 机理验证表明,进入探针体系的肼与探针TZ发生盖布瑞尔反应,生成的2-(4-(二甲基氨基)苯)-3-羟基黄酮具有较强荧光. 探针TZ检测肼的检出限为0.1103 μmol·L−1,在肼浓度为20—300 μmol·L−1 时呈现良好的线性关系,实测水样品肼回收率在97.00%—102.67%范围之间. 该探针具备定性、定量检测生物机体或者环境中痕量肼的潜力,为肼的荧光检测提供了一种新的选择方法.Abstract: A novel Flavonol-based Fluorescent Probe [2-(4-(dimethylamino)phenyl)-4-oxo-4H-chromen-3-yl-4-fluorobenzoate, TZ] was designed and synthesized with the Flavonol [2-(4-(dimethylamino) phenyl)-3-hydroxy-4H-chromen-4-one] as fluorescent parent nucleus, and the structure was characterized by 1H NMR, 13C NMR and mass spectrometer (MS). Then, we measured the selectivity, competition, concentration gradient, Job’s curve, and pH on the fluorescence intensity. The results demonstrated a significant enhancement in the fluorescence intensity of the probe solution when the hydrazine sample was introduced into the pH 7.4 probe system. The probe exhibited robust resistance to F−, Cl−, Br−, I−, PO43−, Ac−, SO42−, HSO3−, SO32−, CO32−, NO3−, SCN−, Ca2+, Mg2+, Cu2+, Fe3+, NH2CONH2, NH3 and N2H4, which was demonstrated the strong anti-interference capability of probe TZ. The mechanism verification revealed that the main source of strong fluorescence was 2-(4-(dimethylamino) benzene)-3-hydroxyflavone produced by the Gabriel reaction upon hydrazine introducted into the probe system. The probe exhibited a strong linear correlation within the concentration range of 20—300 μmol·L−1 and the detection limit for hydrazine is 0.1103 μmol·L−1, with hydrazine recovery ranging from 97.00% to 102.67%. The probe possesses the potential for qualitative and quantitative detection of trace hydrazine in organisms or the environment, thereby offering an new alternative approach for chemical detection of hydrazine.
-
Key words:
- probe /
- hydrazine /
- flavonol /
- detection /
- functional molecules
-
肼(N2H4)又称联氨,是实验室常用化学品,具有较强的腐蚀性和还原性,应用广泛,在航空航天、工业生产、农业生产领域发挥重要作用[1 − 2]. 然而,肼有毒性,泄露会对环境造成巨大危害[3]. 研究表明,肼可以透过表层皮肤和呼吸粘膜进入生物体[4],对机体造成不可逆损坏[5]. 多数国家将一水合肼(N2H4·H2O)列为可致癌物质严格管控[6],我国明令禁止肼超标,规定生活饮用水源中的肼浓度严格控制在0.02 mg·L−1 (0.62 μmol·L−1)以内[7],地表水中肼的浓度严格控制在0.01 mg·L−1 (0.31 μmol·L−1)以内[8]. 肼检测的传统分析方法有滴定法[9]、伏安法[10]、电化学[11]和高效液相色谱法(HPLC)[12]等,但这些方法在不同程度上存在着缺陷,如检测仪器昂贵、样品制备繁琐、检测环境严格和实验条件复杂等. 因此,开发对肼高效便捷定性定量荧光检测方法具有重要意义.
肼的荧光检测技术最早出现在2011年[13]. 已报道肼探针的设计原理大致可以分为“反应型”和“材料型”的两种. “反应型”传感器的识别基团通常与荧光基团相连,荧光探针专一地与肼发生化学反应,反应类型包括去保护[14]、基团转化[15]、环化[16]和开环反应[17]等,探针与肼反应后荧光信号的变化表明肼的存在,并且基本与肼的浓度直接相关. “材料型”传感器利用肼的碱性、还原性和可成氢键性来设计. 金属有机框架(MOFs)[18]、聚合物泡囊(Polymersome)[19]、银纳米颗粒(AgNPs)[20]、金纳米颗拉(AuNPS)[21]和AIEens材料(AIE Enhancers)[22]被巧妙地用作这种设计的载体,从而实现了肼的荧光检测. 肼荧光检测追求更精确的机制、更高效的光源、更准确的数据反馈和更扩展的实用功能[23]已成为研究的热点. 3-羟基黄酮母核具有良好的光化学和光物理性质,常用作荧光探针的光源,其发光原理是激发态分子内质子转移(Excited-state intramolecularproton transfer,ESIPT)[24 − 26]. 氟对生命科学十分重要,由于氟原子电负性很强,药物分子上的氢被氟取代后可明显降低分子区域电子云密度,增强分子的抗氧化能力,可改变溶解度、酸碱度、构象以及生物利用度,常用作提高药物代谢稳定性的有效策略.
本研究以3-羟基黄酮为荧光团,对氟苯甲酰基为羟基保护基团,设计一种全新引入氟原子、可用于检测肼的荧光探针,为建立具有较好的响应性、选择性、灵敏度和潜在生物活性的肼检测方法提供依据. 具体合成方法如图1所示.
1. 材料与方法(Materials and methods)
1.1 试剂与仪器
对二甲氨基苯甲醛,分析纯,天津市致远化学试剂有限公司;羟基苯乙酮、对氟苯甲酸,分析纯,阿拉丁试剂(上海)有限公司. 碳酸钠,氯化钠、溴化钠、碘化钠、氟化钾、磷酸钠、硫酸钠、亚硫酸氢钠、硫酸钠、碳酸钠、硝酸钠、氨水、硫氰酸钠、硝酸铜、硫酸铁、氯化钙、碳酸镁、碳酰胺、肼、盐酸均为分析纯,采购于上海振企化学试剂有限公司、天津大茂化学试剂有限公司、阿拉丁试剂(上海)有限公司等. 所用溶剂均为分析纯. 薄层层析硅胶GF254购自青岛海洋化工厂.
Bruker Advance 300 MHz型核磁共振仪,美国Bruker公司;Hitachi F-4500荧光分光光度计,日本HITACHI公司;HP-5989型质谱仪,美国HP公司.
1.2 探针TZ的合成
依次将化合物I(对二甲氨基苯甲醛,0.1491 g,0.001 mol)、化合物II(羟基苯乙酮,0.1633 g,0.0012 mol)、氢氧化钠(0.4 g,0.010 mol)、无水乙醇(10 mL)加入至圆底烧瓶(100 mL)中,80 ℃下搅拌3 h后,加入氢氧化钠溶液(10 mL,1 mol·L−1)、过氧化氢(8 mL,质量分数35%),在室温下继续反应3 h后,调节pH=8—9(1 mol·L−1的盐酸),有固体析出,抽滤,石油醚打浆后,得到化合物 Ⅲ(2-(4-(二甲基氨基)苯)-3-羟基黄酮,黄色固体,0.1212 g,0.43 mmol),产率为60.32%,液相色谱纯度为96.40%. 1H NMR (CDCl3, 300 MHz), δ: 8.23 (d, J=8.8 Hz, 2H), 8.07 (d, J=7.6 Hz, 1H), 7.77—7.60 (m, 2H), 7.40 (td, J=5.4 Hz, J=2.3Hz, 1H), 6.75 (d, J=8.8 Hz, 2H), 3.10 (s, 6H). 13C NMR (75 MHz, CDCl3), δ:172.5, 155.1, 151.4, 141.2, 136.9, 132.9, 129.2, 125.3, 124.2, 120.9, 118.0, 111.5, 97.2, 40.1. MS, m/Z:[M+H]+理论值282.11;测试值282.10.
将4-氟苯甲酸(0.1411 g,0.001 mol)溶于二氯甲烷(10 mL),氮气保护下冷却至0℃,滴入草酰乙酸(0.5076 g,0.004 mol,0.338 mL),滴完后升至室温,加热至回流,反应2 h. 旋转蒸发除去溶剂,得到对氟苯甲酰氯,直接下一步反应.
称取化合物Ⅲ(0.2000 g,0.7100 mmol),溶于10 mL的二氯甲烷中,随后加入三乙胺0.25 mL(液体,1.8 mmol),向其中逐滴加入对氟苯甲酰氯溶液2 mL(液体,0.7100 mmol),室温条件下搅拌反应2 h后,经薄层硅胶板(V石油醚:V乙酸乙酯=3:1)点样检测. 待反应完成后,加入20 mL的蒸馏水,分液漏斗分液弃去水相,有机相使用10 mL的饱和食盐水洗涤两次,将其转移至锥形瓶,加入无水硫酸镁干燥. 旋转蒸发除去溶剂,得到探针TZ [2-(4-(二甲基氨基)苯基)-3-(4-氟苯甲酸酯)-4-氧代苯并吡喃,淡黄色固体,0.1779 g,0.46 mmol],产率为64.92%. 液相色谱纯度为95.26%. 1H NMR (DMSO-d6, 300 MHz) δ 8.27 (dd, J=8.9, 5.5 Hz, 2H), 8.07 (dd, J=7.9, 1.4 Hz, 1H), 7.90–7.82 (m, 4H), 7.50 (dd, J=16.7, 7.8 Hz, 3H), 6.83–6.78 (m, 2H), 2.99 (s, 6H). 13C NMR (DMSO-d6, 75 MHz) δ 170.42, 164.06, 162.36, 156.41, 154.87, 152.15, 134.36, 133.18, 133.04, 131.23, 129.42, 125.49, 124.98, 124.78, 124.74, 122.74, 118.50, 116.63, 116.34, 115.01, 111.52, 109.56, 39.78, 39.65. MS, m/Z:[M+H]+理论值404.13;测试值404.10.
1.3 待测液的配制
准确称取探针TZ 10.08 mg (25.0 µmol)于乙醇(2 mL)溶液,在25 ℃环境下,采用50 Hz频率,超声(10 min)至完全溶解. 转移至25 mL容量瓶,水定容,浓度为1.0×10−3 mol·L−1. 移取所得母液5.0 mL至25 mL容量瓶,水定容至刻度线,摇匀,得到待测液(2.0×10−4 mol·L−1). 相同方法配制2.0×10−4 mol·L−1的F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3、N2H4储备液(溶剂为水).
1.4 探针TZ荧光光谱测定
探针TZ在激发波长为405 nm时,探针无荧光. 将探针TZ溶液和待测溶液混合于10 mL比色管,摇匀,定容. 充分振荡,10min后,测定探针化合物的荧光发射光谱. 仪器设置参数:激发狭缝宽度2.5 nm,发射狭缝宽度5.0 nm,灵敏度为1,响应时间0.5 s,于400—700 nm内检测荧光. 样品池为1.0 cm×1.0 cm×4.0 cm石英比色皿.
2. 结果与讨论(Result and disscussion)
2.1 反应时间对探针TZ荧光强度的影响
如图2所示,探针TZ本身在发射波长为530 nm处无荧光,当肼加入之后,在波长为530 nm处的发射光谱的荧光强度迅速增强,10 min后,达到最大值,且保持稳定,持续延长反应时间不再增强荧光强度. 由此可知,探针TZ对肼的检测具有很好的灵敏性,响应时间为10 min,低于一些已报道的肼检测荧光探针[17,27 − 30].
2.2 pH值对探针TZ荧光强度的影响
考察pH对检测效果的影响对探针普适性应用有重要意义. 如图3所示,pH对探针TZ与肼的化学反应有很大影响,体系的荧光强度随着pH的增大而增大. 可能是肼优先与水溶液中的酸结合,生成酸碱中和反应产物,影响与探针分子的反应. 实验表明,pH大于7以后的发射强度都不受溶液pH的干扰,可作为可靠的检测肼浓度的探针.
2.3 探针TZ对N2H4的选择性识别
如图4所示,在探针TZ (10 μmol·L−1)的Tris-HCl /乙醇(9:1,V /V,pH=7.40)溶液中,加入2倍量的各种物质(F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3、N2H4)溶液,测量其荧光发射光谱(λex=530 nm). 结果表明,加入N2H4的探针溶液荧光强度明显增强,其余对照组加入其它物质后探针溶液荧光强度几乎未改变,表明探针TZ对N2H4具有较好的选择性识别能力,且不受其他物质干扰.
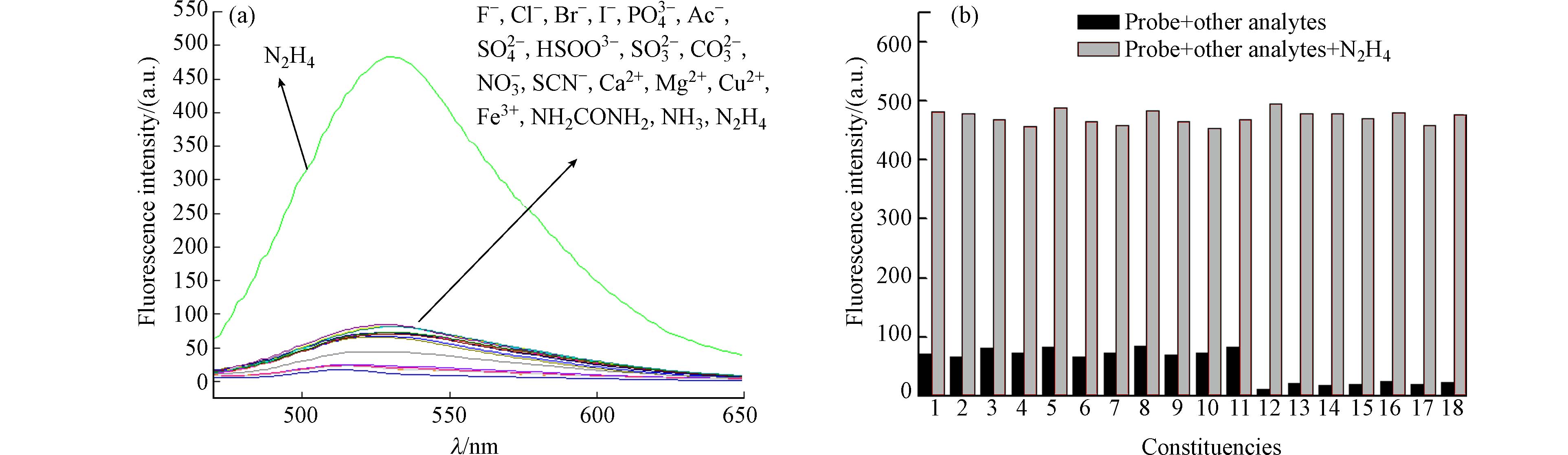 图 4 (a)探针TZ对测试离子的选择性;(b)测试离子与肼共存时探针TZ荧光发射光谱的变化Figure 4. (a) Selectivity of probe TZ for the tested ions; (b) The change of probe TZ fluorescence emission spectra when ions and hydrazine coexist was tested(1—18测序依次为:F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3) (λex=405 nm, λem=530 nm)(sequence 1—18 was F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3 ) (λex=405 nm, λem=530 nm)
图 4 (a)探针TZ对测试离子的选择性;(b)测试离子与肼共存时探针TZ荧光发射光谱的变化Figure 4. (a) Selectivity of probe TZ for the tested ions; (b) The change of probe TZ fluorescence emission spectra when ions and hydrazine coexist was tested(1—18测序依次为:F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3) (λex=405 nm, λem=530 nm)(sequence 1—18 was F−、Cl−、Br−、I−、PO43−、Ac−、SO42−、HSO3−、SO32−、CO32−、NO3−、SCN−、Ca2+、Mg2+、Cu2+、Fe3+、NH2CONH2、NH3 ) (λex=405 nm, λem=530 nm)2.4 探针TZ对N2H4的检测的荧光滴定
为进一步考察探针TZ在不同量肼加入后荧光强度变化的具体情况,通过控制N2H4的加入量,检测探针TZ体系荧光强度的变化. 结果如图5所示,探针TZ对肼具有很好的灵敏度,随着肼的加入量越来越多,体系的荧光强度不断增强(λem=530 nm),直至达到最大值,累计增强约43倍,此时探针与肼的反应达到平衡.
对不同量的肼加入后探针TZ体系在发射光谱为530 nm处的荧光强度进行线性拟合. 如图6所示,肼浓度在20—300 μmol·L−1,探针体系的荧光强度呈现良好线性关系,经拟合得到线性回归方程.
stringUtils.convertMath(!{formula.content}) 式中: F为测试荧光强度,F0为空白对照荧光强度,C为肼浓度,单位为μmol·L−1. 相关系数R2=0.9979.
根据检出率计算公式“LOD=3σ/k(LOD为检出限、σ为空白样本检出荧光强度5次检测值标准偏差、k为荧光强度与肼浓度线性回归曲线的斜率)”,计算出探针TZ检测肼的检出限为0.1103 μmol·L−1. 与一些已报道的肼检测荧光探针[17,27 − 30]相比,探针TZ的检出限更低.
2.5 探针TZ对N2H4的识别机理
探针分子作用机制是肼的亲核加成反应. 待测物肼是亲核性很强的一类化合物,肼分子氮原子上有孤对电子,可以对酯基官能团中处于缺电子状态的羰基碳作用,引发碳氮新键生成,碳氧旧键断裂的盖布瑞尔反应. 受自身电子效应影响,探针TZ本身在溶液体系中具有微弱荧光性质,当遇到体系中游离的肼后,会发生酯的肼解反应,探针TZ分子3位酯基被肼解离,原则上可以生成3位为裸露的羟基的黄酮醇化合物和酰基肼类化合物,如图7所示. 已有研究显示,黄酮醇化合物III具有较强荧光,原因是分子中与3位羟基相连的氢原子4位羰基的氧原子的距离为0.21 nm[31],可以形成分子内氢键稳定形态,与黄酮母环共同构成相对稳定的5元环,发生激发态分子内质子转移(ESIPT).
如图8所示,当肼加入到探针体系后,探针分子迅速与肼反生反应,在反应检测的核磁中发现,在低场区出现一个新的单峰(δ 9.22 ppm)见a区,b区的一组dd峰随着反应的进行逐渐消失了,c区、d区、e区、f区则在裂分和位移上均明显发生了变化.
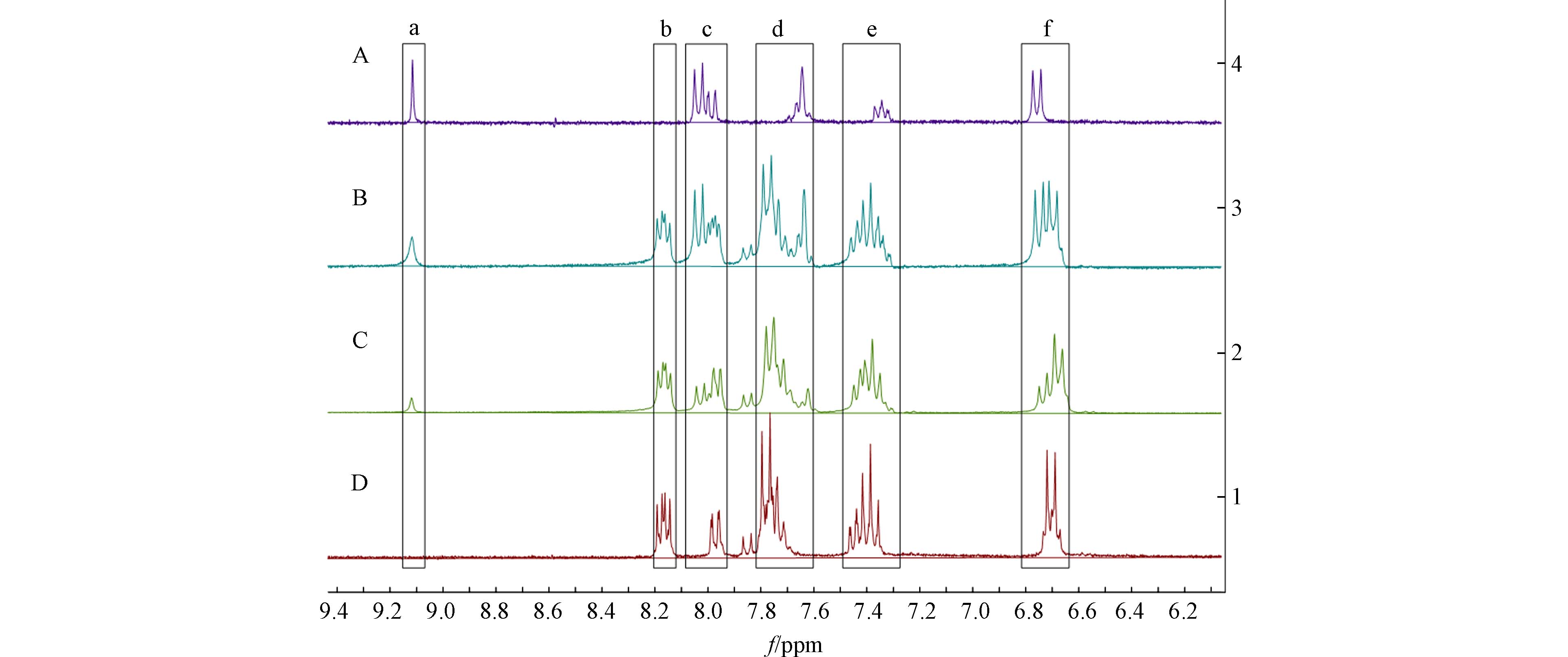 图 8 探针TZ与肼反应体系1H NMR谱图Figure 8. 1H NMR spectra of the reaction system between probe TZ and hydrazine(A)探针TZ与肼(2倍量)(反应10 min);(B)探针TZ与肼(2倍量)(反应5 min);(C)探针TZ与肼(2倍量)(反应2 min);(D)探针TZ(A) Probe TZ was combined with 2-fold hydrazine for 10 min; (B) Probe TZ was combined with 2-fold hydrazine for 5 min; (C) Probe TZ was combined with 2-fold hydrazine for 2 min; (D) Probe TZ
图 8 探针TZ与肼反应体系1H NMR谱图Figure 8. 1H NMR spectra of the reaction system between probe TZ and hydrazine(A)探针TZ与肼(2倍量)(反应10 min);(B)探针TZ与肼(2倍量)(反应5 min);(C)探针TZ与肼(2倍量)(反应2 min);(D)探针TZ(A) Probe TZ was combined with 2-fold hydrazine for 10 min; (B) Probe TZ was combined with 2-fold hydrazine for 5 min; (C) Probe TZ was combined with 2-fold hydrazine for 2 min; (D) Probe TZ对反应进行HPLC色谱分析发现,探针分子原本的保留时间为6.107min. 当肼加入后,在保留时间5.367 min处,出现一个新的产物吸收峰,当反应结束后,体系中仅在保留时间1.773 min、5.367 min两处有吸收峰,保留时间为6.107 min探针分子的吸收峰则完全消失. 需要说明的是黄酮醇化合物在相同条件下保留时间为5.367 min. 经过质谱确认,保留时间1.773 min、5.367 min两个吸收峰,所对应的质谱值分别为155.1,282.1,与机理预测中化合物IV(对氟苯甲酰肼)和黄酮醇化合物Ⅲ理论质谱值一致. 经验证,反应结束后的生成化合物核磁裂分与黄酮醇化合物Ⅲ一致,进一步确认探针TZ对N2H4的识别机理.
2.6 应用研究
如表1所示,探针TZ可用于实际水样中肼的检测. 采用加标回收实验[32-33]验证黄酮类肼探针的对实际环境中肼检测的情况. 取实验室自来水、去离子水(实验室自制)、丹江自然流水(采样点为陕西省商洛市商州区段),3次测量取平均值,检测样品中的肼. 3种样品中均未检测出肼存在. 回收率在97.00%—102.67%范围之间,测试样品的相对标准偏差RSD值在3%以内.
表 1 探针TZ对实际水样品中肼的检测Table 1. Detection of hydrazine in actual water samples by probe TZ样品Sample 加标量理论值/(μmol·L−1)Add scalar theoretical values 实测值/(μmol·L−1)Measured value 加标回收率Standard recovery 相对标准偏差Relative standard deviationRSD 自来水Tap-water 20.00 19.60 98.00% 1.29% 30.00 30.10 100.33% 40.00 40.40 101.00% 去离子水Deionized water 20.00 19.40 97.00% 2.51% 30.00 30.80 102.67% 40.00 39.10 97.75% 丹江水Danjiang River water 20.00 20.10 100.50% 0.44% 30.00 30.40 101.33% 40.00 40.60 101.50% 3. 结论(Conclusion)
(1)利用黄酮醇合成方法优化的“一锅法”合成工艺,合成黄酮醇化合物,以此为母核,在黄酮醇3位羟基上引入对氟苯甲酰基酯,合成未见报道的一种引入氟原子的新型肼探针.
(2)在pH = 7.4的条件下,进入探针体系的肼与探针分子发生盖布瑞尔反应,导致探针分子酯基结构被破坏,生成黄酮醇母环,探针分子的电子环境被破坏,生成物黄酮分子3位羟基与母核4位羰基形成氢键,构成相对稳定的5元环,化合物发生激发态分子内质子转移(ESIPT),释放出很强的荧光. 探针TZ检测肼的检出限为0.1103 μmol·L−1,在20—300 μmol·L−1呈现良好的线性关系,达到定性、定量检测肼的效果,为肼的化学检测提供了一种选择方法,实测样品回收率在97.00%—102.67%范围之间.
(3)利用核磁、色谱和质谱技术验证了该类型荧光探针与肼作用机制. 肼的强亲核作用使探针分子酯基断裂,解离成黄黄酮醇中间体(2-(4-(二甲基氨基)苯)-3-羟基黄酮)和对氟苯甲酰肼.
-
表 1 探针TZ对实际水样品中肼的检测
Table 1. Detection of hydrazine in actual water samples by probe TZ
样品Sample 加标量理论值/(μmol·L−1)Add scalar theoretical values 实测值/(μmol·L−1)Measured value 加标回收率Standard recovery 相对标准偏差Relative standard deviationRSD 自来水Tap-water 20.00 19.60 98.00% 1.29% 30.00 30.10 100.33% 40.00 40.40 101.00% 去离子水Deionized water 20.00 19.40 97.00% 2.51% 30.00 30.80 102.67% 40.00 39.10 97.75% 丹江水Danjiang River water 20.00 20.10 100.50% 0.44% 30.00 30.40 101.33% 40.00 40.60 101.50% -
[1] LAN R, IRVINE J T S, TAO S W. Ammonia and related chemicals as potential indirect hydrogen storage materials[J]. International Journal of Hydrogen Energy, 2012, 37(2): 1482-1494. [2] RAGNARSSON U. Synthetic methodology for alkyl substituted hydrazines[J]. Chemical Society Reviews, 2001, 30(4): 205-213. [3] GARROD S, BOLLARD M E, NICHOLLS A W, et al. Integrated metabonomic analysis of the multiorgan effects of hydrazine toxicity in the rat[J]. Chemical Research in Toxicology, 2005, 18(2): 115-122. [4] NGUYEN H N, CHENOWETH J A, BEBARTA V S, et al. The toxicity, pathophysiology, and treatment of acute hydrazine propellant exposure: A systematic review[J]. Military Medicine, 2021, 186(3/4): e319-e326. [5] MU S, GAO H, LI C, et al. A dual-response fluorescent probe for detection and bioimaging of hydrazine and cyanide with different fluorescence signals[J]. Talanta, 2021, 221: 121606. [6] MA J H, FAN J L, LI H D, et al. Probing hydrazine with a near-infrared fluorescent chemodosimeter[J]. Dyes and Pigments, 2017, 138: 39-46. [7] Health standard for hydrazine in source water. National standard of the People’s Republic of China. GB 18061-2000[S]. Beijing: China Standard Press, 2000: 4-10. [8] Environmental quality standards for surface water. National standard of the People’s Republic of China. GB 3838-2002[S]. Beijing: China Standard Press, 2002: 4-26. [9] RADUSHEV A V, CHEKANOVA L G, GUSEV V Y, et al. Determination of hydrazides and 1, 2-diacylhydrazines of aliphatic carboxylic acids by conductometric titration[J]. Journal of Analytical Chemistry, 2000, 55(5): 445-448. [10] PINTER J S, BROWN K L, DeYOUNG P A, et al. Amperometric detection of hydrazine by cyclic voltammetry and flow injection analysis using ruthenium modified glassy carbon electrodes[J]. Talanta, 2007, 71(3): 1219-1225. [11] WANG C, ZHANG L, GUO Z H, et al. A novel hydrazine electrochemical sensor based on the high specific surface area graphene[J]. Microchimica Acta, 2010, 169(1): 1-6. [12] ELIAS G, BAUER W F. Hydrazine determination in sludge samples by high-performance liquid chromatography[J]. Journal of Separation Science, 2006, 29(3): 460-464. [13] CHOI M G, HWANG J, MOON J O, et al. Hydrazine-selective chromogenic and fluorogenic probe based on levulinated coumarin[J]. Organic Letters, 2011, 13(19): 5260-5263. [14] TIENSOMJITR K, NOORAT R, CHOMNGAM S, et al. A chromogenic and fluorogenic rhodol-based chemosensor for hydrazine detection and its application in live cell bioimaging[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2018, 195: 136-141. [15] WU J J, PAN J, YE Z, et al. A smart fluorescent probe for discriminative detection of hydrazine and bisulfite from different emission channels[J]. Sensors and Actuators B: Chemical, 2018, 274: 274-284. [16] ZHANG Y B, HUANG Y F, YUE Y K, et al. A compact fluorescent probe based on o-phthalaldehyde for ultrasensitive detection of hydrazine in gas and solution phases[J]. Sensors and Actuators B: Chemical, 2018, 273: 944-950. [17] YU G Q, CAO Y P, LIU H M, et al. A spirobenzopyran-based multifunctional chemosensor for the chromogenic sensing of Cu2+ and fluorescent sensing of hydrazine with practical applications[J]. Sensors and Actuators B: Chemical, 2017, 245: 803-814. [18] SK M, KHAN M R U Z, DAS A, et al. A phthalimide-functionalized UiO-66 metal-organic framework for the fluorogenic detection of hydrazine in live cells[J]. Dalton Transactions, 2019, 48(33): 12615-12621. [19] NABEEL F, RASHEED T. Rhodol-conjugated polymersome sensor for visual and highly-sensitive detection of hydrazine in aqueous media[J]. Journal of Hazardous Materials, 2020, 388: 121757. [20] ZHAO Z L, ZHANG G, GAO Y, et al. A novel detection technique of hydrazine hydrate: Modality change of hydrogen bonding-induced rapid and ultrasensitive colorimetric assay[J]. Chemical Communications, 2011, 47(48): 12816-12818. [21] GU X, CAMDEN J P. Surface-enhanced Raman spectroscopy-based approach for ultrasensitive and selective detection of hydrazine[J]. Analytical Chemistry, 2015, 87(13): 6460-6464. [22] PUROHIT D, SHARMA C P, RAGHUVANSHI A, et al. First dual responsive “turn-on” and “ratiometric” AIEgen probe for selective detection of hydrazine both in solution and the vapour phase[J]. Chemistry, 2019, 25(18): 4660-4664. [23] ZHANG X Y, YANG Y S, WANG W, et al. Fluorescent sensors for the detection of hydrazine in environmental and biological systems: Recent advances and future prospects[J]. Coordination Chemistry Reviews, 2020, 417: 213367. [24] 曾碧涛, 钟学芳, 赵志刚, 等. 基于黄酮醇的新型荧光探针的合成及应用研究[J]. 现代化工, 2023, 43(10): 251-256. ZENG B T, ZHONG X F, ZHAO Z G, et al. Synthesis and application of novel fluorescent probes based on flavonol[J]. Modern Chemical Industry, 2023, 43(10): 251-256 (in Chinese).
[25] 周思仪, 丁旭, 赵永梅, 等. 基于黄酮的长波长荧光探针用于检测体外和体内生物硫醇[J]. 有机化学, 2023, 43(1): 178-185. ZHOU S Y, DING X, ZHAO Y M, et al. A Flavone-Based Long-Wavelength Fluorescent Probe to Detect Biothiols in vitro and in vivo[J]. Chinese Journal of Organic Chemistry, 2023, 43(1): 178-185(in Chinese).
[26] 曹小燕, 路宏朝, 张强, 等. 基于黄酮醇类半胱氨酸荧光探针的设计、合成及性能研究[J]. 分析化学, 2020, 48(8): 1033-1049. CAO X Y, LU H Z, ZHANG Q, et al. Design and synthesis of flavone-based fluorescent probe for cysteine detection and its application in living cells imaging[J]. Chinese Journal of Analytical Chemistry, 2020, 48(8): 1033-1049 (in Chinese).
[27] LI K, XU H R, YU K K, et al. A coumarin-based chromogenic and ratiometric probe for hydrazine[J]. Analytical Methods, 2013, 5(11): 2653-2656. [28] QIAN Y, LIN J, HAN L J, et al. A resorufin-based colorimetric and fluorescent probe for live-cell monitoring of hydrazine[J]. Biosensors and Bioelectronics, 2014, 58: 282-286. [29] LI B, HE Z S, ZHOU H X, et al. Reaction based colorimetric and fluorescence probes for selective detection of hydrazine[J]. Dyes and Pigments, 2017, 146: 300-304. [30] ZHENG X X, WANG S Q, WANG H Y, et al. Novel pyrazoline-based selective fluorescent probe for the detection of hydrazine[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2015, 138: 247-251. [31] TIAN M G, SUN J, TANG Y H, et al. Discriminating live and dead cells in dual-color mode with a two-photon fluorescent probe based on ESIPT mechanism[J]. Analytical Chemistry, 2018, 90(1): 998-1005. [32] 郝伟, 李丽, 张京, 等. 地下水中砷和汞的不同测试方法[J]. 环境化学, 2024, 43(2): 689-692. HAO W, LI L, ZHANG J, et al. Study on different test methods of arsenic and mercury in groundwater[J]. Environmental Chemistry, 2024, 43(2): 689-692 (in Chinese).
[33] 熊力, 王金成, 陈吉平. 超分子溶剂微萃取-高效液相色谱法快速测定土壤中氯代多环芳烃及多环芳烃[J]. 环境化学, 2022, 41(10): 3159-3166. doi: 10.7524/j.issn.0254-6108.2021060103 XIONG L, WANG J C, CHEN J P. Rapid determination of chlorinated polycyclic aromatic hydrocarbons and polycyclic aromatic hydrocarbons in soil by supramolecular solvent microextraction-high performance liquid chromatography[J]. Environmental Chemistry, 2022, 41(10): 3159-3166(in Chinese). doi: 10.7524/j.issn.0254-6108.2021060103
-






 下载:
下载: