-
随着人类生产活动的加剧、臭氧层破坏日益严重,生活在地球表面的生物可能遭受紫外线的过度辐射,由此所导致的皮肤晒伤、老化、甚至癌变等问题越来越受到人们的关注[1]. 为了缓解这一问题,紫外防晒剂被广泛应用,通常被添加到个人护理品如防晒霜、沐浴露、身体乳等日用护肤品中[2],同时紫外防晒剂也常被添加在塑料、橡胶、油漆等长期暴露在阳光直射环境的工业产品中以延缓老化. 据统计,全球防晒剂的年消耗量由2016年的4.4万吨增长至2021年的5.2万吨,年均增长率约4%. 随着这些个人护理品和工业产品的大量使用及逐渐老化,添加于其中的防晒剂逐渐被释放进入环境,成为一类新污染物,广受关注. Casas-Beltran等[3]的研究预估了2007年至2025年间当地居民和游客使用防晒霜将给墨西哥金塔纳罗奥水体排入近
4367.25 吨的化学物质.二苯甲酮类(BPs)化合物是有机防晒剂家族中的重要成员,由于其防晒谱广、致敏性低、价格便宜,在实际生产生活中应用广泛. 二苯甲酮的骨架结构是由羰基相连的两个苯环. 苯环上取代基种类、数量、位置的不同,衍生出一系列二苯甲酮类防晒剂,常见二苯甲酮类防晒剂的分子结构如表1所示.
随着二苯甲酮类化合物的广泛使用,排入环境的量也在逐年增加. 目前已经在几乎所有的环境介质中发现了BPs类防晒剂的残留,甚至在部分居民尿液、乳汁、血液中检测出了BPs,其含量水平大致在0.08 ng·mL−1至1.9 ng·mL-1[4]. 环境中BPs的来源广泛,如防晒霜生产企业的废水排放、居民日常洗漱和娱乐活动的排放等[5]. 由于BPs类化合物的化学性质相对稳定,进入水环境后不容易被降解去除,导致其在水环境中的残留水平呈逐渐升高的趋势[6]. 在中国香港某热门海滩水体中2-羟基-4-甲氧基二苯甲酮的检出浓度超过
1000 ng·L−1,汕头和潮州的地表水中浓度为50 ng·L−1[7]. 特别是在美国圣约翰岛的夏季海水中2-羟基-4-甲氧基二苯甲酮的浓度高达1.395 mg·L−1[8]. BPs的污染问题逐步成为国内外环境领域的研究热点之一.环境中BPs类化合物备受关注的主要原因是其潜在的内分泌干扰效应. 调查结果表明人精液中BPs的检出限为0.22—2.35 ng·mL−1. 其中二苯甲酮、2,4-二羟基二苯甲酮和2-羟基-4-甲氧基二苯甲酮的检出率分别为17.8%、18.5%和27.3%,它们会导致精子数量减少和前向运动精子比例降低[9 − 11]. 体外毒性实验结果表明,BPs表现出雌激素效应、抗雌激素效应、抗孕激素效应和抗雄激素效应等多种负面生物效应[12]. 此外,BPs还具有一定的急性毒性、亚急性及慢性毒性、生长发育毒性和光致毒性. 2022年发表于Science的研究揭示了2-羟基-4-甲氧基二苯甲酮的糖基化代谢产物是导致珊瑚漂白和死亡的主要毒性物质[13]. 毒理学实验结果表明,即使防晒霜的暴露剂量低至 10 μL·L−1,也能导致硬珊瑚在96 h内完全白化[14]. 已有一些研究者对BPs类防晒剂在水处理相关过程中的转化行为进行了探讨,但多数研究仅关注单个二苯甲酮化合物在实验条件下的降解动力学以及降解产物,对于该类化合物的转化机理缺乏系统的认知. 因此,本文主要梳理二苯甲酮类化合物在氧化/消毒等水处理相关过程中的转化反应机理,为其风险评价和控制管理提供理论支持.
-
氧化反应是指氧化剂与还原性底物之间发生的化学反应,在氧化反应中氧化剂将部分还原性官能团转化为氧化性官能团. 除了传统的氧化反应外,高级氧化技术近年来在水处理领域应用较广,主要借助光、声、电、磁等物理和化学过程中所产生的具有强氧化作用的活性氧自由基与底物发生反应. 羟基自由基(·OH)是活性氧自由基中的一种,具有高的电负性和电极电位(2.8 V),其氧化能力远远超过普通的化学氧化剂. 利用·OH作为氧化剂可以与大多数有机污染物及晶体材料发生氧化还原反应,可将水中的有机物降解成小分子有机物或完全矿化成CO2和H2O,实现污染物的高效去除[15 − 17].
Wang等研究了紫外防晒剂2,2´,4,4´-四羟基二苯甲酮在臭氧氧化处理中的转化特征[18]. 由于臭氧(O3)分子是由O2分子携带一个O原子构成,是一种性质活泼的暂存状态. 臭氧本身也是一种氧化还原电位很高的氧化剂(2.07 V),其氧化反应有两种方式,一种是O3分子直接进攻有机物形成臭氧化中间产物,并进一步分解;另一种是O3在紫外光诱导下,生成更为活泼的·OH.
Wang等发现2,2´,4,4´-四羟基二苯甲酮的氧化转化主要涉及两条转化路径[18]. 路径Ⅰ:由于2,2´,4,4´-四羟基二苯甲酮分子中C(7)原子的电子云密度较低,C(1)—C(7)和C(1´)—C(7)键容易断裂生成中间产物P1和P2,在O3和·OH存在的情况下,·OH攻击并取代羧基,P1也可以转化为P2. P2的苯环上有3个羟基官能团,很容易被臭氧继续氧化导致C(4)—C(5)键断裂,生成新的中间产物P3. P3的C(2)—C(3)键断裂被进一步氧化生成P4(草酸),是臭氧氧化过程的最终产物.
路径Ⅱ:BPs分子中与C(3´)相连的氢质子被·OH取代生成P6,由于P6具有与2,2´,4,4´-四羟基二苯甲酮相似的结构,其中C(1´)—C(7)键也可以被O3和·OH破坏而生成P7,但实验中发现中间产物P7的浓度始终低于其他产物,进一步研究发现P7可以继续与臭氧发生反应,转化为含氧杂环化合物(P9)和一些有机羧酸(P8, P10). 由于在整个实验过程中不断补充臭氧,中间产物有机羧酸(P8和P10)可以进一步氧化为更小分子的酸,如P11和P4. 另外,与P2相似,P6苯环上的3个羟基也很容易被继续氧化生成P12,并进一步发生苯环断裂生成羧酸类化合物(P13). 若反应体系中有羟基自由基,将进一步进攻P13发生脱羧反应生成P14,其C(1)—C(7)和C(1´)—C(7)键可以被O3和·OH继续进攻,在反应开始的4 min内大量生成P11和P4,而P11也会被羟基自由基进攻导致C—C断裂最终生成P4(图1a)[18].
过硫酸盐活化氧化也是近年研究较多的一种高级氧化处理技术,过硫酸盐可以诱导产生多种强氧化性自由基,如硫酸根自由基、羟基自由基等,利用这些自由基实现对污染物的高效降解甚至矿化. Pan等在光活化过硫酸盐降解2-羟基-4-甲氧基二苯甲酮的研究中提出了两条主要反应路线[19],如图1b所示. 其中路线Ⅰ是由诱导产生的·OH攻击2-羟基-4-甲氧基二苯甲酮分子中的C(1)—C(7)键一侧的苯环,生成键裂解产物P1. 途径Ⅱ主要涉及羟基化反应,生成了一系列连续羟基化产物2-羟基-4-甲氧基二苯甲酮→P2→P6→P7. 在这个过程中,中间产物P2还可以发生去甲基化生成P5. 此外,P2还可以通过直接氧化进一步转化为P3和P4. 除臭氧氧化、过硫酸盐氧化法外,高级氧化法还有光催化氧化法[20]、芬顿氧化法[21]、超声氧化法[22]等,这些方法都能生成·OH,可以降解水体中难以被普通氧化剂氧化的污染物.
在水的消毒处理中,需要向水中投加氧化性消毒剂(如次氯酸钠、臭氧等)以杀灭病原微生物,但这些消毒剂不仅仅和病原微生物反应,还可以和水中的还原性化学物质发生氧化还原反应. Zhang等所在的研究团队系统研究了多种BPs类防晒剂在氯化消毒过程中的转化反应[23],发现BPs类化合物在氯化消毒中大多会发生Baeyer-Villiger氧化反应[24]. 具体而言,在强氧化剂次氯酸的作用下,可以将BPs分子中的酮羰基氧化生成酯基衍生物,即Baeyer-Villiger氧化反应. 这些生成的酯基化合物还可以继续发生一系列反应生成氯代苯酚类产物,其在次氯酸体系中还可以继续发生氧化反应,生成苯醌类化合物,经过氧化开环,最后生成氯代乙酸、三氯甲烷类小分子高毒性消毒副产物. 一般而言,BPs防晒剂分子中羰基的化学性质比较稳定,但正是由于发生了Baeyer-Villiger氧化反应,改变了羰基的稳定性,才导致后续一系列反应的发生. 由此可见,Baeyer-Villiger氧化反应是BPs和其他含有酮羰基芳香族化合物氯化过程中形成氯仿等高毒性消毒副产物的关键环节(图1c)[25].
在2-羟基-4-甲氧基二苯甲酮的氧化、消毒等处理过程中发现,无论在酸性条件还是碱性条件下2-羟基-4-甲氧基二苯甲酮分子中的甲氧基都会被·OH攻击发生脱甲基反应,转化为新产物2,4-二羟基二苯甲酮(图1d)[26 − 28]
在氧化、消毒处理过程中,BPs转化主要涉及的氧化反应分为普通的分子氧化反应和高级的自由基氧化反应. 普通氧化反应主要在臭氧氧化过程中发生,臭氧分子会直接和BPs发生反应使其转化. 而高级氧化反应存在于多种处理方式中,诱导生成的羟基自由基、硫酸根自由基等强氧化性自由基参与反应. 此外, Baeyer-Villiger氧化反应可高效的将酮类化合物转化为酯类化合物,这对氯消毒至关重要,可将BPs转化为相对分子质量较小的产物.
-
取代反应是指化合物分子中某原子或原子团被试剂中相似类型的其它原子或原子团所替代的反应[29],可用通式表示为:
式中R-L为反应基质,A为进攻试剂,R-A为取代产物,L为离去基团.
芳香族化合物的取代反应从机理上可分为亲电取代、亲核取代以及自由基取代. 芳环亲电取代是指芳环上的氢原子被亲电试剂所取代的反应,如硝化、卤化、磺化、烷基化和酰基化等. 如果与芳环反应的试剂为亲核试剂,则发生芳环亲核取代. 从BPs类化合物的分子结构出发,其在氧化、消毒过程中可能发生亲电卤代反应和亲核水解反应.
-
在氯化消毒处理中,投加的消毒剂次氯酸分子容易在水中发生极化形成Clδ+和OHδ−,其中带部分正电荷的Clδ+扮演亲电试剂的角色,容易进攻BPs分子中电子云密度更高的原子而发生亲电取代反应. 由于BPs类化合物分子中有多个电子云密度较高的区域,在氯化消毒处理中可生成多种氯代产物(图2a).
在4-羟基二苯甲酮的氯化消毒过程中发现,无论是在酸性、中性、还是碱性条件下,苯环上的多个氢原子能被Clδ+连续取代,生成单氯取代、二氯取代、三氯取代产物(图2b)[30]. 在另一项紫外-氯联合处理2,3,4-三羟基二苯甲酮的研究中发现底物有两条可能的转化途径(图2c)[31]. 途径1中,氯取代首先发生在2,3,4-三羟基二苯甲酮的芳环上,形成单氯代产物TP1. 除了次氯酸作为消毒剂之外,氯胺也是在实际水消毒处理中常用的消毒剂,研究表明,2-羟基-4-甲氧基二苯甲酮和2-羟基-4-甲氧基二苯甲酮-5-磺酸被氯或者氯胺消毒时都可以被Clδ+进攻发生氯取代反应,且2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化和氯胺化过程中遵循相似的反应途径,生成了氯代产物. 由于次氯酸的反应活性高于氯胺,氯化反应比氯胺化反应更快. 另外,由于2-羟基-4-甲氧基二苯甲酮-5-磺酸分子中含有吸电子官能团磺酸基,其与氯、氯胺的反应活性低于2-羟基-4-甲氧基二苯甲酮(图2d)[32].
卤素离子是水体中,特别是沿海地区水体中常见无机离子,除了含量最高的氯离子外(约数十至数百 mg·L−1),溴离子和碘离子的浓度也可以达到ng·L−1—μg·L−1水平. 当向含有Br−、I−的水中投加次氯酸钠进行消毒处理时,可以将它们氧化为次溴酸、次碘酸,它们的性质与次氯酸相似,也能快速地与底物发生卤代反应[33]. 研究发现溴离子存在时,2-羟基-4-甲氧基二苯甲酮-5-磺酸的氯化消毒处理过程中生成了12种溴代化产物[34]. 相似地,若碘离子存在时,检出了4种碘代产物[35]. 溴离子、碘离子的存在增加了氯化体系中的竞争反应,消耗了部分次氯酸,抑制了2-羟基-4-甲氧基二苯甲酮-5-磺酸的转化效率. 但是,研究表明溴代产物、碘代产物往往具有比氯代产物更高的毒性,其所导致的健康风险更高.
-
水解反应是指水分子作为亲核试剂,攻击化合物中的原子或原子团形成新物质的过程[36 − 37]. 通过水解反应,羟基(·OH)被引入化合物中,羟基属于供电子官能团,使化合物更容易进一步转化[38]. 如前所述,BPs属于酮类化合物,经过Baeyer-Villiger反应转化为酯类中间体,其与水分子发生亲核水解,形成苯酚类和苯甲酸类产物.
此外,就消毒处理中所投加的消毒剂次氯酸钠而言,属于弱酸强碱盐,其在不同pH条件下也会发生水解. 比如在较强酸性条件下,次氯酸钠将水解为次氯酸. 图3a中4-羟基二苯甲酮生成二氯取代产物后,发生Baeyer-Villiger氧化反应后生成酯类化合物,经水解反应生成了酚类产物P3 [30].
如前所述,次氯酸钠在较强酸性pH条件下的主要赋存形态为次氯酸,在中性、碱性pH条件下次氯酸电离生成次氯酸根离子,是一种强亲核试剂,可使2-羟基-4-甲氧基二苯甲酮-5-磺酸的Baeyer-Villiger氧化所得的酯产物(P4和P8)继续发生亲核水解,生成酚类产物(P1和P5)和苯甲酸(P15)(图3b)[25].
由于2-羟基-4-甲氧基二苯甲酮-5-磺酸分子中既含有甲氧基又含有磺酸基官能团,在活化过硫酸盐氧化降解中发现由于水解反应的发生,生成了脱磺基、脱甲氧基的羟基取代产物[39]. 并且发现2-羟基-4-甲氧基二苯甲酮-5-磺酸分子在溴离子、碘离子存在下的氯化体系中会发生卤代反应生成卤化产物. 再发生Baeyer-Villiger氧化反应生成酯,进水解反应[34 − 35]. 大量研究表明,BPs的降解过程中,Baeyer-Villiger氧化是水解反应发生的重要前提.
-
脱羧反应是指羧酸分子中失去羧基放出二氧化碳的反应,该反应广泛应用于化工、医药等领域,是一种非常重要的化学转化,常用来构建新的C—C键和 C—X键,可以制备许多反应中间体[40]. 其反应通式为:
由于羧酸分子中的羧基为吸电子取代基,化学性质较为稳定,一般情况下不易发生脱羧反应,但在特殊条件下,羧酸能脱去羧基(失去二氧化碳)而生成烃. 脱羧反应通常不需要特殊的催化剂,在加热、碱性条件及光照等条件下即可发生. 当反应体系中有光催化剂存在时,催化诱导产生的活性自由基在脱羧过程中发挥关键作用[41]. 比如在紫外活化过硫酸盐处理2-羟基-4-甲氧基二苯甲酮-5-磺酸时,其中间产物会被·OH、SO4−·进攻氧化脱去羧基形成新的转化产物(图4a)[39]. 研究发现单独紫外[42]或紫外-过氧化物[43]降解BPs时也会发生脱羧反应,但紫外活化过硫酸盐对2-羟基-4-甲氧基二苯甲酮-5-磺酸的降解速率远远大于其他两种,这说明可能是因为诱导产生的SO4−·加速了脱羧反应.
在BPs的氯化处理过程中,也发现了脱羧反应形成酚类产物,比如,2,2´,4,4´-四羟基二苯甲酮在氯化处理中发生Baeyer-Villiger氧化反应生成苯甲酸苯酯类衍生物,进而发生亲核水解反应生成苯甲酸类产物,其在次氯酸作用下继续发生氯代脱羧反应. 值得注意的是,氯代脱羧反应促进了酚类产物的不断形成[23]. 酚类产物的生成促进了氯仿的大量生成(图4b). 而且在Larson和Rockwell等的研究中也发现取代苯甲酸在氯化过程中可发生脱羧并形成氯酚[44].
除上述常见的几种反应外,在氧化、消毒处理过程中BPs还会发生其他一些反应. 比如,2-羟基-4-甲氧基二苯甲酮被过硫酸盐氧化时·OH进攻苯环,导致形成羟基化产物P5A,进而通过羟基缩合反应转化为P1(图5a)[45]. 2,4-二羟基二苯甲酮及羟基化产物P229和P245在紫外和TiO2存在下发生Norrish Ⅰ反应,化合物中羰基的α-碳键被破坏形成只含有一个苯环的P94、P109和P122(图5b)[46]. 2-羟基-4-甲氧基二苯甲酮-5-磺酸在酸性的氯化处理过程中,先经过连续的氯化反应生成二氯代产物P11. 随着Baeyer-Villiger反应的发生转化为酯化产物P8,进一步水解为酚类产物P5. 类儿茶酚水解产物P5在酸性氯化体系中进一步氧化缩合,形成五元杂环类呋喃产物P6(图5c)[25].
由于这些反应的相关研究报道较少,本文没有展开详细论述. 但需要特别说明的是,在氧化、消毒处理过程中由于反应复杂,研究者所提出的转化反应路径中的中间产物并非全部检出,导致很难完整描述某化合物的转化路径. 加之,由于转化的中间产物产率低、生成量少,难以分离获得纯净的产物,很多研究者往往只是通过质谱信息推测产物的结构,进而推断可能的反应机理. 众所周知,质谱信息只能给出准确的相对分子质量,不能确定官能团(如羟基、氯离子、甲氧基等)在化合物分子中的确切取代位置,难以确定产物的绝对分子结构. 因此,在实验研究过程中需要密切观察不同反应阶段中间产物的生成规律,并且分离或制备相应的产物,借助高分辨质谱、核磁共振等多种方式确定产物的绝对分子结构. 确切的产物分子结构为科学准确地揭示底物在氧化、消毒处理中的转化机理提供支撑.
-
BPs类紫外防晒剂应用广泛,其潜在的负面生物学效应备受关注,因此研究它们在水处理过程中的转化特征非常必要. 氧化和消毒是最常用的水处理技术,本文总结了BPs类防晒剂在氧化和消毒处理中的转化机理,为该类污染物的风险管理和控制提供科学依据.
BPs的分子中含有不饱和的芳香苯环、酮羰基、羟基、甲氧基等官能团,其在氧化、消毒等水处理过程中最主要的转化机制是氧化反应,羟基自由基、硫酸根自由基等是最主要的活性氧化物种,可以促进BPs类物质的快速转化[47]. 此外,氯化消毒处理中的Baeyer-Villiger氧化反应可高效地将酮类化合物转化为酯类化合物,为后续的水解反应、脱羧反应、以及氧化开环提供了可能,大大促进了小分子高毒性消毒副产物的生成.
也正是由于BPs的分子中含有羰基、磺酸基等吸电子取代基,以及羟基、甲氧基等供电子取代基,BPs在氯化消毒处理中非常容易发生亲电取代反应,生成一系列单卤代、二卤代、三卤代产物,由于卤代产物的显著毒性效应,其潜在的生态与健康风险值得关注. 此外,BPs类化合物的Baeyer-Villiger氧化的酯类中间产物在次氯酸消毒体系中也容易发生亲核水解反应生成苯甲酸类产物,进一步与次氯酸发生取代脱羧反应.
由此可见,现有关于BPs类防晒剂在水处理中的转化主要涉及氧化反应、取代反应、脱羧反应等,虽然处理的方法不尽相同,但所涉及的反应类型大体相似. 因此,从反应机理出发,选择适当的处理方法,实现提高处理效率的目标,为该类污染物的风险管控提供科学依据.
氧化/消毒处理中二苯甲酮的转化反应机理
Transformation mechanisms of benzophenones during oxidation/disinfection treatments
-
摘要: 随着二苯甲酮类紫外防晒剂的大量使用,其在水体中频繁检出. 已有大量研究表明二苯甲酮类化合物在自然环境过程和人工水处理过程中可发生多种转化,其潜在的生态与健康风险值得关注. 近年来,针对二苯甲酮类化合物的转化研究逐渐增多,发现其在不同条件下的转化行为复杂,且存在较大差异. 本文从转化的化学反应机理出发,着重对二苯甲酮类化合物在氧化/消毒处理相关过程中的转化特征进行了梳理. 结果表明二苯甲酮类化合物在氧化/消毒过程中主要发生氧化反应、取代反应、脱羧反应等,多数转化产物具有较高毒性,其潜在的生态与健康风险不容忽视.Abstract: With the widespread use of benzophenone-type ultraviolet filters, they are frequently detected in aquatic environments. Numerous studies have indicated that benzophenone-type compounds can undergo various transformations in natural environmental processes and artificial water treatment processes, raising concerns about their potential ecological and health risks. In recent years, research on the transformation of benzophenone-type compounds has increased, revealing that their transformation behavior under different conditions is complex and exhibits significant variations. The present study reviews the transformation characteristics of benzophenone-type compounds in oxidation/disinfection-related processes from the perspective of chemical reaction mechanisms of these transformations. The results indicate that benzophenone-type compounds primarily undergo oxidation reactions, substitution reactions, decarboxylation reactions during oxidation/disinfection processes. Most of the transformation products exhibit relatively higher toxicity than the parent compounds, underscoring the importance of considering the potential ecological and health risks of benzophenone-type compounds.
-
Key words:
- benzophenone /
- sunscreen /
- transformation reactions /
- mechanism.
-
随着人类生产活动的加剧、臭氧层破坏日益严重,生活在地球表面的生物可能遭受紫外线的过度辐射,由此所导致的皮肤晒伤、老化、甚至癌变等问题越来越受到人们的关注[1]. 为了缓解这一问题,紫外防晒剂被广泛应用,通常被添加到个人护理品如防晒霜、沐浴露、身体乳等日用护肤品中[2],同时紫外防晒剂也常被添加在塑料、橡胶、油漆等长期暴露在阳光直射环境的工业产品中以延缓老化. 据统计,全球防晒剂的年消耗量由2016年的4.4万吨增长至2021年的5.2万吨,年均增长率约4%. 随着这些个人护理品和工业产品的大量使用及逐渐老化,添加于其中的防晒剂逐渐被释放进入环境,成为一类新污染物,广受关注. Casas-Beltran等[3]的研究预估了2007年至2025年间当地居民和游客使用防晒霜将给墨西哥金塔纳罗奥水体排入近
4367.25 吨的化学物质.二苯甲酮类(BPs)化合物是有机防晒剂家族中的重要成员,由于其防晒谱广、致敏性低、价格便宜,在实际生产生活中应用广泛. 二苯甲酮的骨架结构是由羰基相连的两个苯环. 苯环上取代基种类、数量、位置的不同,衍生出一系列二苯甲酮类防晒剂,常见二苯甲酮类防晒剂的分子结构如表1所示.
表 1 常见二苯甲酮类化合物Table 1. Common benzophenone compounds名称Name 化学式Chemical formula 名称Name 化学式Chemical formula 二苯甲酮(Benzophenone) 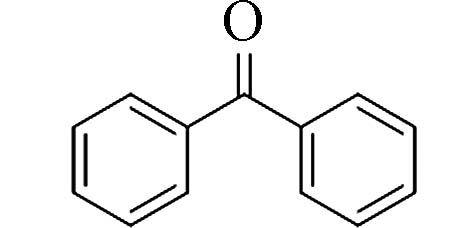
2-羟基二苯甲酮(2-Hydroxy-benzophenone) 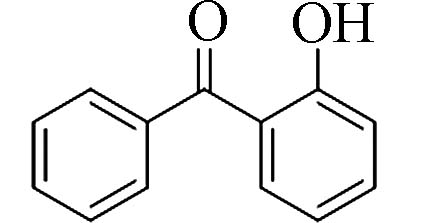
3-羟基二苯甲酮(3-Hydroxy-benzophenone) 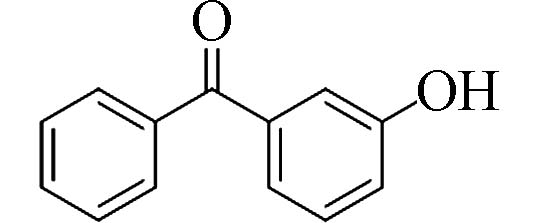
4-羟基二苯甲酮(4-Hydroxy-benzophenone) 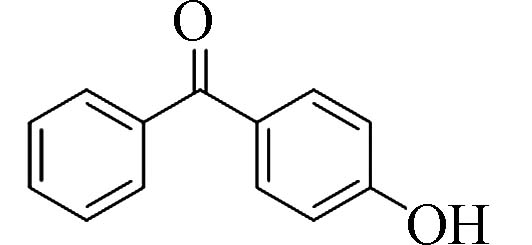
2,2´-二羟基二苯甲酮(2,2´-Dihydroxy-benzophenone) 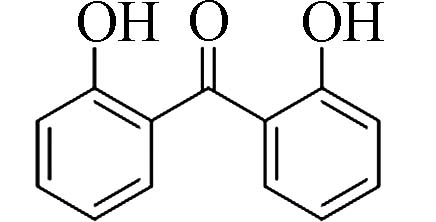
4,4´-二羟基二苯甲酮(4,4´-Dihydroxy-benzophenone) 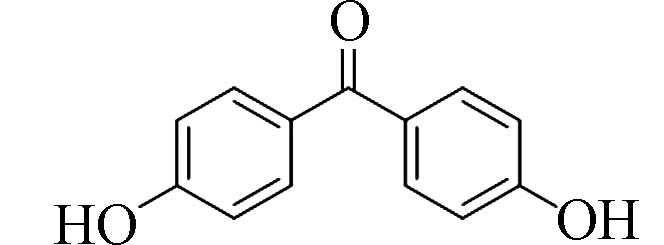
2,4-二羟基二苯甲酮(2,4-Dihydroxy-benzophenone) 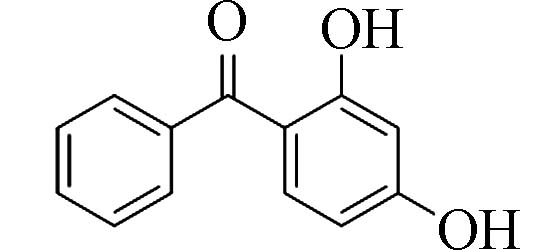
2,4,4´-三羟基二苯甲酮(2,4,4-Trihydroxy-benzophenone) 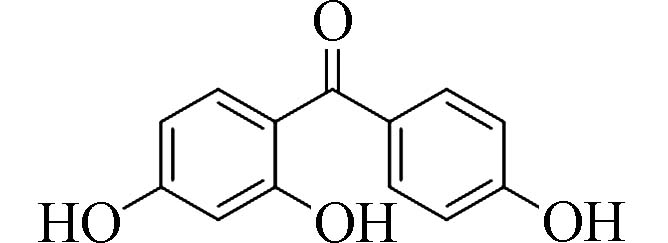
2,3,4-三羟基二苯甲酮(2,3,4-Trihydroxy-benzophenone) 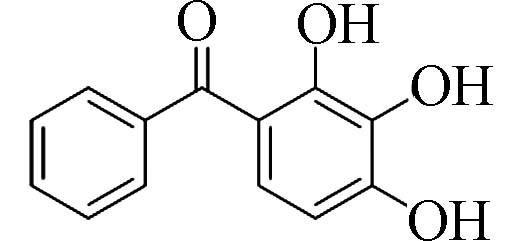
2,2´,4,4´-四羟基二苯甲酮(2,2 ́,4,4 ́-Tetrahydroxy-benzophenone) 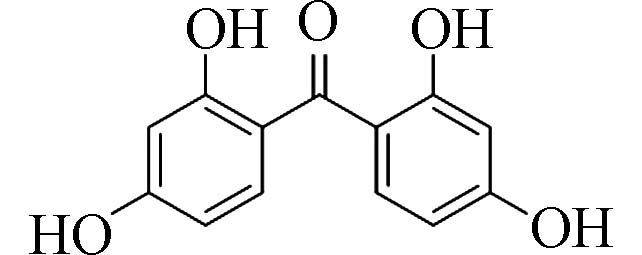
2-羟基-4-甲氧基二苯甲酮(2-Hydroxy-4-methoxy-benzophenone) 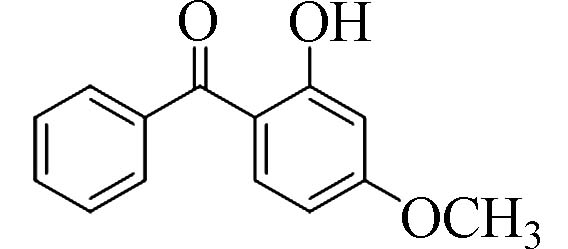
2-羟基-4-辛氧基二苯甲酮(2-Hydroxy-4-octyloxy-benzophenone) 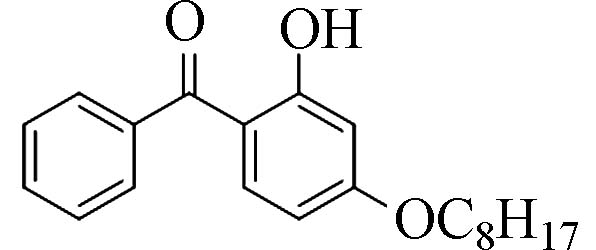
2-羟基-4-甲氧基二苯甲酮-5-磺酸(2-Hydroxy-4-methoxy-benzophenone-5-sulfonic acid) 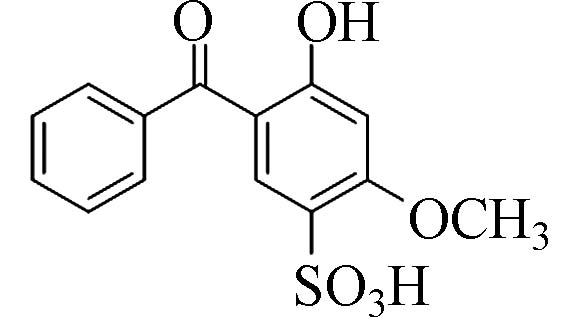
2,2´-二羟基-4,4´-二甲氧基二苯甲酮(2,2 ́-Dihydroxy-4,4 ́-dimethoxy-benzophenone) 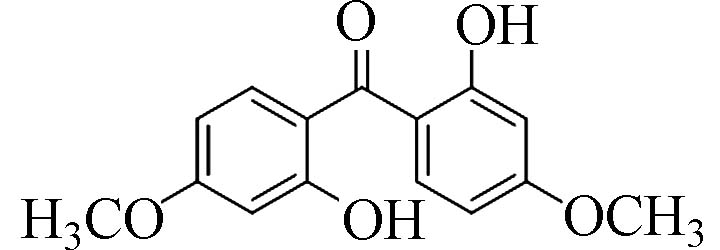
2-羟基-5-氯二苯甲酮(2-Hydroxy-5-chloro-benzophenone) 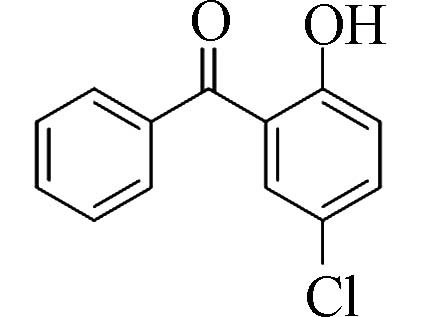
2,2´-二羟基-4-甲氧基二苯甲酮(2,2 ́-Dihydroxy-4-methoxy-benzophenone) 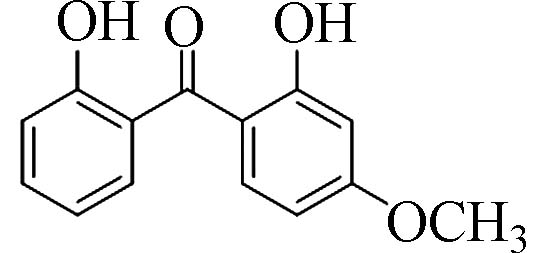
2,2'-二羟基-4,4'-二甲氧基苯甲酮-5,5'-二磺酸(2,2'-Dihydroxy-4,4'-dimethoxy-benzophenone-5,5'-disulfonic acid) 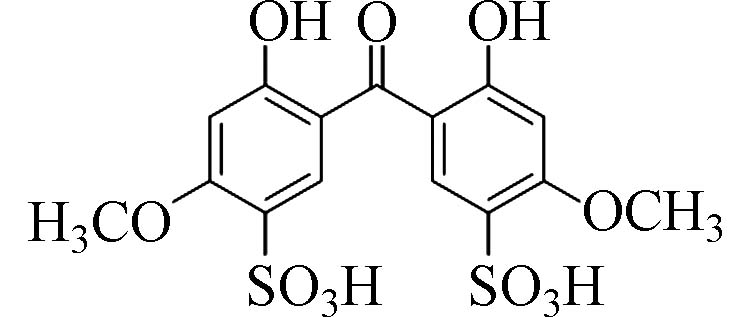
2,2´-羟基-4-甲氧基-4'-甲基二苯甲酮(2,2 ́-Hydroxy-4-methoxy-4'-methyl-benzophenone) 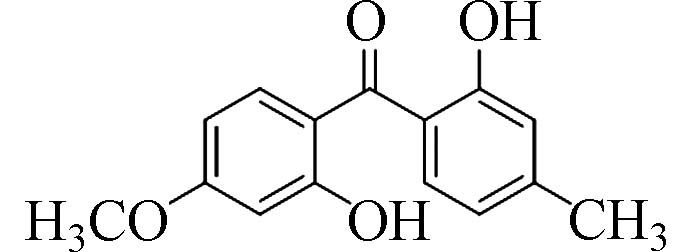
随着二苯甲酮类化合物的广泛使用,排入环境的量也在逐年增加. 目前已经在几乎所有的环境介质中发现了BPs类防晒剂的残留,甚至在部分居民尿液、乳汁、血液中检测出了BPs,其含量水平大致在0.08 ng·mL−1至1.9 ng·mL-1[4]. 环境中BPs的来源广泛,如防晒霜生产企业的废水排放、居民日常洗漱和娱乐活动的排放等[5]. 由于BPs类化合物的化学性质相对稳定,进入水环境后不容易被降解去除,导致其在水环境中的残留水平呈逐渐升高的趋势[6]. 在中国香港某热门海滩水体中2-羟基-4-甲氧基二苯甲酮的检出浓度超过
1000 ng·L−1,汕头和潮州的地表水中浓度为50 ng·L−1[7]. 特别是在美国圣约翰岛的夏季海水中2-羟基-4-甲氧基二苯甲酮的浓度高达1.395 mg·L−1[8]. BPs的污染问题逐步成为国内外环境领域的研究热点之一.环境中BPs类化合物备受关注的主要原因是其潜在的内分泌干扰效应. 调查结果表明人精液中BPs的检出限为0.22—2.35 ng·mL−1. 其中二苯甲酮、2,4-二羟基二苯甲酮和2-羟基-4-甲氧基二苯甲酮的检出率分别为17.8%、18.5%和27.3%,它们会导致精子数量减少和前向运动精子比例降低[9 − 11]. 体外毒性实验结果表明,BPs表现出雌激素效应、抗雌激素效应、抗孕激素效应和抗雄激素效应等多种负面生物效应[12]. 此外,BPs还具有一定的急性毒性、亚急性及慢性毒性、生长发育毒性和光致毒性. 2022年发表于Science的研究揭示了2-羟基-4-甲氧基二苯甲酮的糖基化代谢产物是导致珊瑚漂白和死亡的主要毒性物质[13]. 毒理学实验结果表明,即使防晒霜的暴露剂量低至 10 μL·L−1,也能导致硬珊瑚在96 h内完全白化[14]. 已有一些研究者对BPs类防晒剂在水处理相关过程中的转化行为进行了探讨,但多数研究仅关注单个二苯甲酮化合物在实验条件下的降解动力学以及降解产物,对于该类化合物的转化机理缺乏系统的认知. 因此,本文主要梳理二苯甲酮类化合物在氧化/消毒等水处理相关过程中的转化反应机理,为其风险评价和控制管理提供理论支持.
1. 氧化反应(Oxidation reactions)
氧化反应是指氧化剂与还原性底物之间发生的化学反应,在氧化反应中氧化剂将部分还原性官能团转化为氧化性官能团. 除了传统的氧化反应外,高级氧化技术近年来在水处理领域应用较广,主要借助光、声、电、磁等物理和化学过程中所产生的具有强氧化作用的活性氧自由基与底物发生反应. 羟基自由基(·OH)是活性氧自由基中的一种,具有高的电负性和电极电位(2.8 V),其氧化能力远远超过普通的化学氧化剂. 利用·OH作为氧化剂可以与大多数有机污染物及晶体材料发生氧化还原反应,可将水中的有机物降解成小分子有机物或完全矿化成CO2和H2O,实现污染物的高效去除[15 − 17].
Wang等研究了紫外防晒剂2,2´,4,4´-四羟基二苯甲酮在臭氧氧化处理中的转化特征[18]. 由于臭氧(O3)分子是由O2分子携带一个O原子构成,是一种性质活泼的暂存状态. 臭氧本身也是一种氧化还原电位很高的氧化剂(2.07 V),其氧化反应有两种方式,一种是O3分子直接进攻有机物形成臭氧化中间产物,并进一步分解;另一种是O3在紫外光诱导下,生成更为活泼的·OH.
stringUtils.convertMath(!{formula.content}) (1) stringUtils.convertMath(!{formula.content}) (2) Wang等发现2,2´,4,4´-四羟基二苯甲酮的氧化转化主要涉及两条转化路径[18]. 路径Ⅰ:由于2,2´,4,4´-四羟基二苯甲酮分子中C(7)原子的电子云密度较低,C(1)—C(7)和C(1´)—C(7)键容易断裂生成中间产物P1和P2,在O3和·OH存在的情况下,·OH攻击并取代羧基,P1也可以转化为P2. P2的苯环上有3个羟基官能团,很容易被臭氧继续氧化导致C(4)—C(5)键断裂,生成新的中间产物P3. P3的C(2)—C(3)键断裂被进一步氧化生成P4(草酸),是臭氧氧化过程的最终产物.
路径Ⅱ:BPs分子中与C(3´)相连的氢质子被·OH取代生成P6,由于P6具有与2,2´,4,4´-四羟基二苯甲酮相似的结构,其中C(1´)—C(7)键也可以被O3和·OH破坏而生成P7,但实验中发现中间产物P7的浓度始终低于其他产物,进一步研究发现P7可以继续与臭氧发生反应,转化为含氧杂环化合物(P9)和一些有机羧酸(P8, P10). 由于在整个实验过程中不断补充臭氧,中间产物有机羧酸(P8和P10)可以进一步氧化为更小分子的酸,如P11和P4. 另外,与P2相似,P6苯环上的3个羟基也很容易被继续氧化生成P12,并进一步发生苯环断裂生成羧酸类化合物(P13). 若反应体系中有羟基自由基,将进一步进攻P13发生脱羧反应生成P14,其C(1)—C(7)和C(1´)—C(7)键可以被O3和·OH继续进攻,在反应开始的4 min内大量生成P11和P4,而P11也会被羟基自由基进攻导致C—C断裂最终生成P4(图1a)[18].
 图 1 BPs类化合物的氧化反应途径Figure 1. Oxidation pathways of BPsa. 2,2´,4,4´-四羟基二苯甲酮的臭氧氧化过程;b. 2-羟基-4-甲氧基二苯甲酮的过硫酸盐活化转化过程;c. 氯代2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化体系中的Baeyer-Villiger氧化机理;d. 2-羟基-4-甲氧基二苯甲酮氧化为2,4-二羟基二苯甲酮的过程(Ox:氧化反应)a. Ozone oxidation of 2,2 ́,4,4 ́-tetrahydroxy-benzophenone; b. Persulfate activation oxidation of 2-hydroxy-4-methoxy-benzophenone; c. Baeyer-Villiger oxidation of chloro-2-hydroxy-4-methoxybenzophenone-5-sulfonic acid in a chlorinated system; d. The oxidation of 2-hydroxy-4-methoxy-benzophenone to 2,4-dihydroxy-benzophenone(Ox:Oxidation)
图 1 BPs类化合物的氧化反应途径Figure 1. Oxidation pathways of BPsa. 2,2´,4,4´-四羟基二苯甲酮的臭氧氧化过程;b. 2-羟基-4-甲氧基二苯甲酮的过硫酸盐活化转化过程;c. 氯代2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化体系中的Baeyer-Villiger氧化机理;d. 2-羟基-4-甲氧基二苯甲酮氧化为2,4-二羟基二苯甲酮的过程(Ox:氧化反应)a. Ozone oxidation of 2,2 ́,4,4 ́-tetrahydroxy-benzophenone; b. Persulfate activation oxidation of 2-hydroxy-4-methoxy-benzophenone; c. Baeyer-Villiger oxidation of chloro-2-hydroxy-4-methoxybenzophenone-5-sulfonic acid in a chlorinated system; d. The oxidation of 2-hydroxy-4-methoxy-benzophenone to 2,4-dihydroxy-benzophenone(Ox:Oxidation)过硫酸盐活化氧化也是近年研究较多的一种高级氧化处理技术,过硫酸盐可以诱导产生多种强氧化性自由基,如硫酸根自由基、羟基自由基等,利用这些自由基实现对污染物的高效降解甚至矿化. Pan等在光活化过硫酸盐降解2-羟基-4-甲氧基二苯甲酮的研究中提出了两条主要反应路线[19],如图1b所示. 其中路线Ⅰ是由诱导产生的·OH攻击2-羟基-4-甲氧基二苯甲酮分子中的C(1)—C(7)键一侧的苯环,生成键裂解产物P1. 途径Ⅱ主要涉及羟基化反应,生成了一系列连续羟基化产物2-羟基-4-甲氧基二苯甲酮→P2→P6→P7. 在这个过程中,中间产物P2还可以发生去甲基化生成P5. 此外,P2还可以通过直接氧化进一步转化为P3和P4. 除臭氧氧化、过硫酸盐氧化法外,高级氧化法还有光催化氧化法[20]、芬顿氧化法[21]、超声氧化法[22]等,这些方法都能生成·OH,可以降解水体中难以被普通氧化剂氧化的污染物.
在水的消毒处理中,需要向水中投加氧化性消毒剂(如次氯酸钠、臭氧等)以杀灭病原微生物,但这些消毒剂不仅仅和病原微生物反应,还可以和水中的还原性化学物质发生氧化还原反应. Zhang等所在的研究团队系统研究了多种BPs类防晒剂在氯化消毒过程中的转化反应[23],发现BPs类化合物在氯化消毒中大多会发生Baeyer-Villiger氧化反应[24]. 具体而言,在强氧化剂次氯酸的作用下,可以将BPs分子中的酮羰基氧化生成酯基衍生物,即Baeyer-Villiger氧化反应. 这些生成的酯基化合物还可以继续发生一系列反应生成氯代苯酚类产物,其在次氯酸体系中还可以继续发生氧化反应,生成苯醌类化合物,经过氧化开环,最后生成氯代乙酸、三氯甲烷类小分子高毒性消毒副产物. 一般而言,BPs防晒剂分子中羰基的化学性质比较稳定,但正是由于发生了Baeyer-Villiger氧化反应,改变了羰基的稳定性,才导致后续一系列反应的发生. 由此可见,Baeyer-Villiger氧化反应是BPs和其他含有酮羰基芳香族化合物氯化过程中形成氯仿等高毒性消毒副产物的关键环节(图1c)[25].
在2-羟基-4-甲氧基二苯甲酮的氧化、消毒等处理过程中发现,无论在酸性条件还是碱性条件下2-羟基-4-甲氧基二苯甲酮分子中的甲氧基都会被·OH攻击发生脱甲基反应,转化为新产物2,4-二羟基二苯甲酮(图1d)[26 − 28]
在氧化、消毒处理过程中,BPs转化主要涉及的氧化反应分为普通的分子氧化反应和高级的自由基氧化反应. 普通氧化反应主要在臭氧氧化过程中发生,臭氧分子会直接和BPs发生反应使其转化. 而高级氧化反应存在于多种处理方式中,诱导生成的羟基自由基、硫酸根自由基等强氧化性自由基参与反应. 此外, Baeyer-Villiger氧化反应可高效的将酮类化合物转化为酯类化合物,这对氯消毒至关重要,可将BPs转化为相对分子质量较小的产物.
2. 取代反应(Substitution reactions)
取代反应是指化合物分子中某原子或原子团被试剂中相似类型的其它原子或原子团所替代的反应[29],可用通式表示为:
stringUtils.convertMath(!{formula.content}) (3) 式中R-L为反应基质,A为进攻试剂,R-A为取代产物,L为离去基团.
芳香族化合物的取代反应从机理上可分为亲电取代、亲核取代以及自由基取代. 芳环亲电取代是指芳环上的氢原子被亲电试剂所取代的反应,如硝化、卤化、磺化、烷基化和酰基化等. 如果与芳环反应的试剂为亲核试剂,则发生芳环亲核取代. 从BPs类化合物的分子结构出发,其在氧化、消毒过程中可能发生亲电卤代反应和亲核水解反应.
2.1 亲电卤代反应
在氯化消毒处理中,投加的消毒剂次氯酸分子容易在水中发生极化形成Clδ+和OHδ−,其中带部分正电荷的Clδ+扮演亲电试剂的角色,容易进攻BPs分子中电子云密度更高的原子而发生亲电取代反应. 由于BPs类化合物分子中有多个电子云密度较高的区域,在氯化消毒处理中可生成多种氯代产物(图2a).
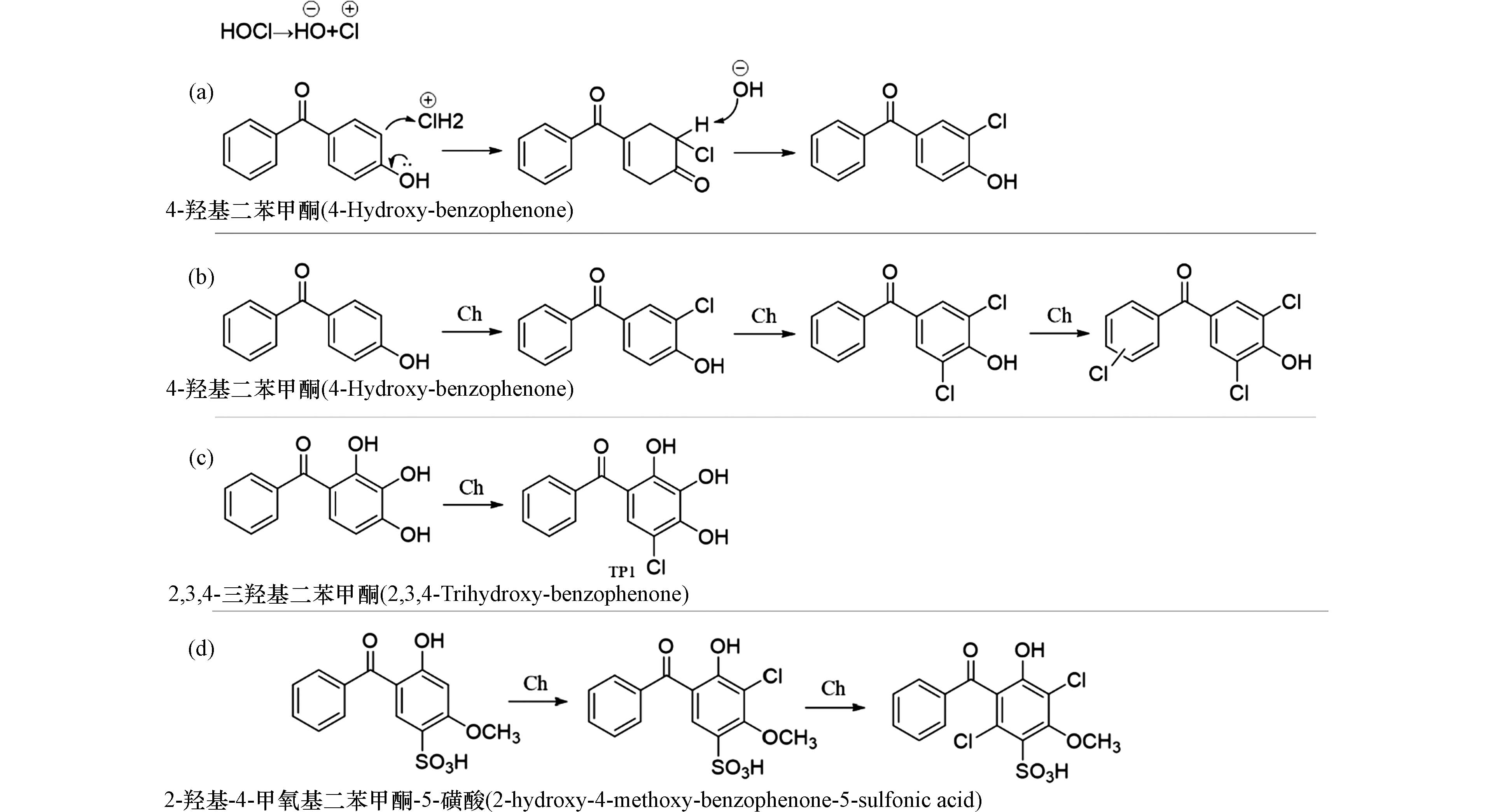 图 2 BPs类化合物的氯化转化途径Figure 2. Chlorination transformation pathways of BPsa. 4-羟基二苯甲酮的亲电氯化反应机理;b. 4-羟基二苯甲酮在氯化体系中的转化机理;c. 2,3,4-三羟基二苯甲酮在紫外-氯化体系中的转化机理;d. 2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化体系中的转化机理(Ch:氯化反应)a. Electrophilic chlorination mechanisms of 4-hydroxy-benzophenone; b. Transformation mechanisms of 4-hydroxy-benzophenone in chlorinated system; c. Transformation mechanisms of 2,3,4-trihydroxy-benzophenone in UV-chlorinated systems; d. Transformation mechanisms of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in chlorinated system(Ch:Chlorination)
图 2 BPs类化合物的氯化转化途径Figure 2. Chlorination transformation pathways of BPsa. 4-羟基二苯甲酮的亲电氯化反应机理;b. 4-羟基二苯甲酮在氯化体系中的转化机理;c. 2,3,4-三羟基二苯甲酮在紫外-氯化体系中的转化机理;d. 2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化体系中的转化机理(Ch:氯化反应)a. Electrophilic chlorination mechanisms of 4-hydroxy-benzophenone; b. Transformation mechanisms of 4-hydroxy-benzophenone in chlorinated system; c. Transformation mechanisms of 2,3,4-trihydroxy-benzophenone in UV-chlorinated systems; d. Transformation mechanisms of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in chlorinated system(Ch:Chlorination)在4-羟基二苯甲酮的氯化消毒过程中发现,无论是在酸性、中性、还是碱性条件下,苯环上的多个氢原子能被Clδ+连续取代,生成单氯取代、二氯取代、三氯取代产物(图2b)[30]. 在另一项紫外-氯联合处理2,3,4-三羟基二苯甲酮的研究中发现底物有两条可能的转化途径(图2c)[31]. 途径1中,氯取代首先发生在2,3,4-三羟基二苯甲酮的芳环上,形成单氯代产物TP1. 除了次氯酸作为消毒剂之外,氯胺也是在实际水消毒处理中常用的消毒剂,研究表明,2-羟基-4-甲氧基二苯甲酮和2-羟基-4-甲氧基二苯甲酮-5-磺酸被氯或者氯胺消毒时都可以被Clδ+进攻发生氯取代反应,且2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化和氯胺化过程中遵循相似的反应途径,生成了氯代产物. 由于次氯酸的反应活性高于氯胺,氯化反应比氯胺化反应更快. 另外,由于2-羟基-4-甲氧基二苯甲酮-5-磺酸分子中含有吸电子官能团磺酸基,其与氯、氯胺的反应活性低于2-羟基-4-甲氧基二苯甲酮(图2d)[32].
卤素离子是水体中,特别是沿海地区水体中常见无机离子,除了含量最高的氯离子外(约数十至数百 mg·L−1),溴离子和碘离子的浓度也可以达到ng·L−1—μg·L−1水平. 当向含有Br−、I−的水中投加次氯酸钠进行消毒处理时,可以将它们氧化为次溴酸、次碘酸,它们的性质与次氯酸相似,也能快速地与底物发生卤代反应[33]. 研究发现溴离子存在时,2-羟基-4-甲氧基二苯甲酮-5-磺酸的氯化消毒处理过程中生成了12种溴代化产物[34]. 相似地,若碘离子存在时,检出了4种碘代产物[35]. 溴离子、碘离子的存在增加了氯化体系中的竞争反应,消耗了部分次氯酸,抑制了2-羟基-4-甲氧基二苯甲酮-5-磺酸的转化效率. 但是,研究表明溴代产物、碘代产物往往具有比氯代产物更高的毒性,其所导致的健康风险更高.
2.2 水解反应
水解反应是指水分子作为亲核试剂,攻击化合物中的原子或原子团形成新物质的过程[36 − 37]. 通过水解反应,羟基(·OH)被引入化合物中,羟基属于供电子官能团,使化合物更容易进一步转化[38]. 如前所述,BPs属于酮类化合物,经过Baeyer-Villiger反应转化为酯类中间体,其与水分子发生亲核水解,形成苯酚类和苯甲酸类产物.
此外,就消毒处理中所投加的消毒剂次氯酸钠而言,属于弱酸强碱盐,其在不同pH条件下也会发生水解. 比如在较强酸性条件下,次氯酸钠将水解为次氯酸. 图3a中4-羟基二苯甲酮生成二氯取代产物后,发生Baeyer-Villiger氧化反应后生成酯类化合物,经水解反应生成了酚类产物P3 [30].
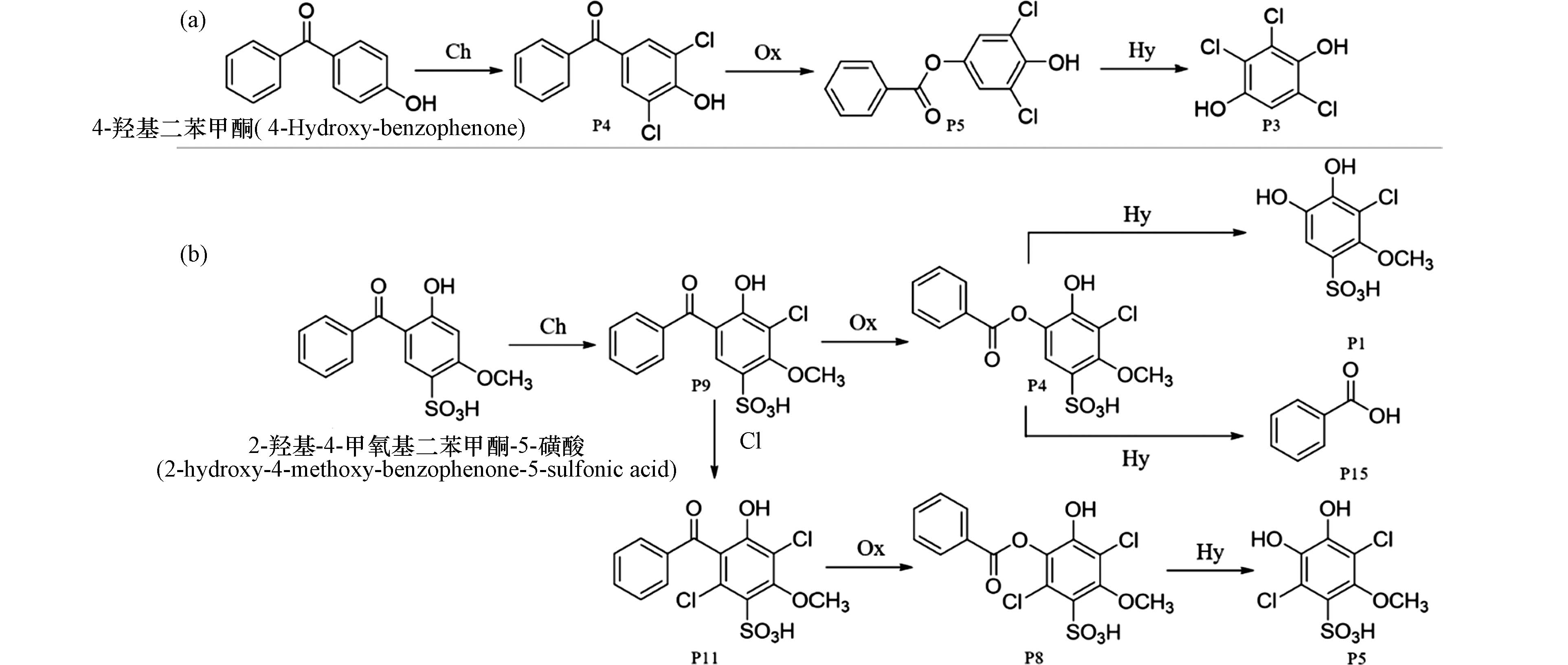 图 3 BPs类化合物的氧化及水解反应途径Figure 3. Oxidation and hydrolysis reaction pathways of BPsa. 4-羟基二苯甲酮在氯化体系中的转化机理;b. 2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化体系中的转化机理(Ch:氯化反应;Ox:氧化反应;Hy:水解反应)a. Transformation pathways of 4-hydroxy-benzophenone in chlorinated system; b. Transformation pathways of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in chlorinated system(Ch:Chlorination;Ox:Oxidation;Hy:Hydrolysis)
图 3 BPs类化合物的氧化及水解反应途径Figure 3. Oxidation and hydrolysis reaction pathways of BPsa. 4-羟基二苯甲酮在氯化体系中的转化机理;b. 2-羟基-4-甲氧基二苯甲酮-5-磺酸在氯化体系中的转化机理(Ch:氯化反应;Ox:氧化反应;Hy:水解反应)a. Transformation pathways of 4-hydroxy-benzophenone in chlorinated system; b. Transformation pathways of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in chlorinated system(Ch:Chlorination;Ox:Oxidation;Hy:Hydrolysis)如前所述,次氯酸钠在较强酸性pH条件下的主要赋存形态为次氯酸,在中性、碱性pH条件下次氯酸电离生成次氯酸根离子,是一种强亲核试剂,可使2-羟基-4-甲氧基二苯甲酮-5-磺酸的Baeyer-Villiger氧化所得的酯产物(P4和P8)继续发生亲核水解,生成酚类产物(P1和P5)和苯甲酸(P15)(图3b)[25].
由于2-羟基-4-甲氧基二苯甲酮-5-磺酸分子中既含有甲氧基又含有磺酸基官能团,在活化过硫酸盐氧化降解中发现由于水解反应的发生,生成了脱磺基、脱甲氧基的羟基取代产物[39]. 并且发现2-羟基-4-甲氧基二苯甲酮-5-磺酸分子在溴离子、碘离子存在下的氯化体系中会发生卤代反应生成卤化产物. 再发生Baeyer-Villiger氧化反应生成酯,进水解反应[34 − 35]. 大量研究表明,BPs的降解过程中,Baeyer-Villiger氧化是水解反应发生的重要前提.
3. 脱羧反应(Decarboxylation reactions)
脱羧反应是指羧酸分子中失去羧基放出二氧化碳的反应,该反应广泛应用于化工、医药等领域,是一种非常重要的化学转化,常用来构建新的C—C键和 C—X键,可以制备许多反应中间体[40]. 其反应通式为:
stringUtils.convertMath(!{formula.content}) (4) 由于羧酸分子中的羧基为吸电子取代基,化学性质较为稳定,一般情况下不易发生脱羧反应,但在特殊条件下,羧酸能脱去羧基(失去二氧化碳)而生成烃. 脱羧反应通常不需要特殊的催化剂,在加热、碱性条件及光照等条件下即可发生. 当反应体系中有光催化剂存在时,催化诱导产生的活性自由基在脱羧过程中发挥关键作用[41]. 比如在紫外活化过硫酸盐处理2-羟基-4-甲氧基二苯甲酮-5-磺酸时,其中间产物会被·OH、SO4−·进攻氧化脱去羧基形成新的转化产物(图4a)[39]. 研究发现单独紫外[42]或紫外-过氧化物[43]降解BPs时也会发生脱羧反应,但紫外活化过硫酸盐对2-羟基-4-甲氧基二苯甲酮-5-磺酸的降解速率远远大于其他两种,这说明可能是因为诱导产生的SO4−·加速了脱羧反应.
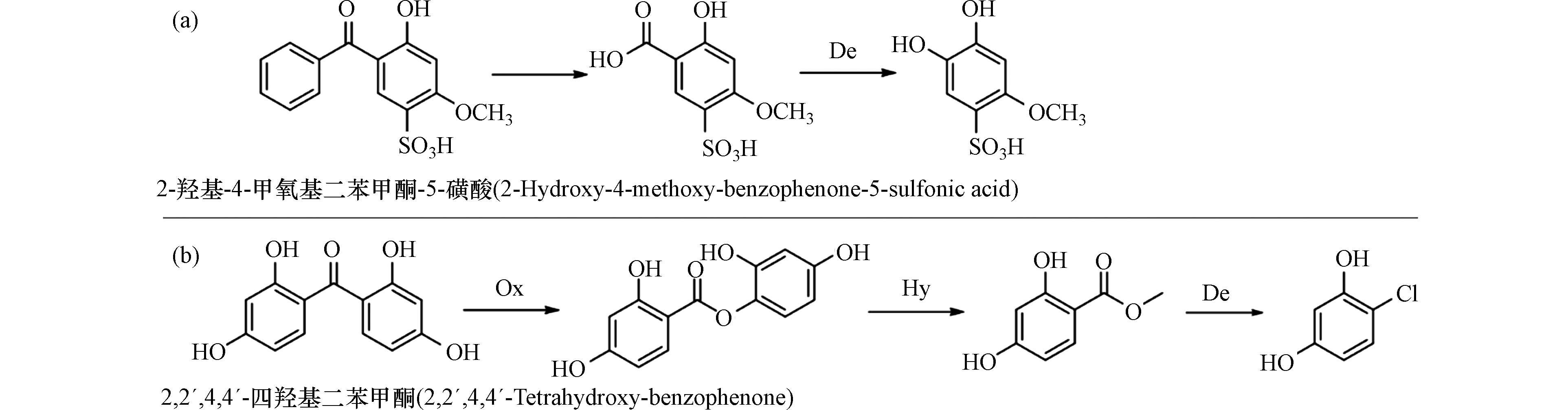 图 4 BPs类化合物转化中间产物的脱羧反应途径Figure 4. Decarboxylation pathway of BPs conversion intermediatesa. 紫外/过硫酸盐活化体系中2-羟基-4-甲氧基二苯甲酮-5-磺酸的转化机理;b. 2,2´,4,4´-四羟基二苯甲酮在氯化体系中的转化机理(Ch:氯化反应;Ox:氧化反应;Hy:水解反应;De:脱羧反应)a. Transformation mechanisms of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in UV/persulfate-activated system; b. Transformation mechanisms of 2,2 ́,4,4 ́-tetrahydroxy-benzophenone in a chlorinated system (Ch:Chlorination;Ox:Oxidation;Hy:Hydrolysis;De:Decarboxylation)
图 4 BPs类化合物转化中间产物的脱羧反应途径Figure 4. Decarboxylation pathway of BPs conversion intermediatesa. 紫外/过硫酸盐活化体系中2-羟基-4-甲氧基二苯甲酮-5-磺酸的转化机理;b. 2,2´,4,4´-四羟基二苯甲酮在氯化体系中的转化机理(Ch:氯化反应;Ox:氧化反应;Hy:水解反应;De:脱羧反应)a. Transformation mechanisms of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in UV/persulfate-activated system; b. Transformation mechanisms of 2,2 ́,4,4 ́-tetrahydroxy-benzophenone in a chlorinated system (Ch:Chlorination;Ox:Oxidation;Hy:Hydrolysis;De:Decarboxylation)在BPs的氯化处理过程中,也发现了脱羧反应形成酚类产物,比如,2,2´,4,4´-四羟基二苯甲酮在氯化处理中发生Baeyer-Villiger氧化反应生成苯甲酸苯酯类衍生物,进而发生亲核水解反应生成苯甲酸类产物,其在次氯酸作用下继续发生氯代脱羧反应. 值得注意的是,氯代脱羧反应促进了酚类产物的不断形成[23]. 酚类产物的生成促进了氯仿的大量生成(图4b). 而且在Larson和Rockwell等的研究中也发现取代苯甲酸在氯化过程中可发生脱羧并形成氯酚[44].
除上述常见的几种反应外,在氧化、消毒处理过程中BPs还会发生其他一些反应. 比如,2-羟基-4-甲氧基二苯甲酮被过硫酸盐氧化时·OH进攻苯环,导致形成羟基化产物P5A,进而通过羟基缩合反应转化为P1(图5a)[45]. 2,4-二羟基二苯甲酮及羟基化产物P229和P245在紫外和TiO2存在下发生Norrish Ⅰ反应,化合物中羰基的α-碳键被破坏形成只含有一个苯环的P94、P109和P122(图5b)[46]. 2-羟基-4-甲氧基二苯甲酮-5-磺酸在酸性的氯化处理过程中,先经过连续的氯化反应生成二氯代产物P11. 随着Baeyer-Villiger反应的发生转化为酯化产物P8,进一步水解为酚类产物P5. 类儿茶酚水解产物P5在酸性氯化体系中进一步氧化缩合,形成五元杂环类呋喃产物P6(图5c)[25].
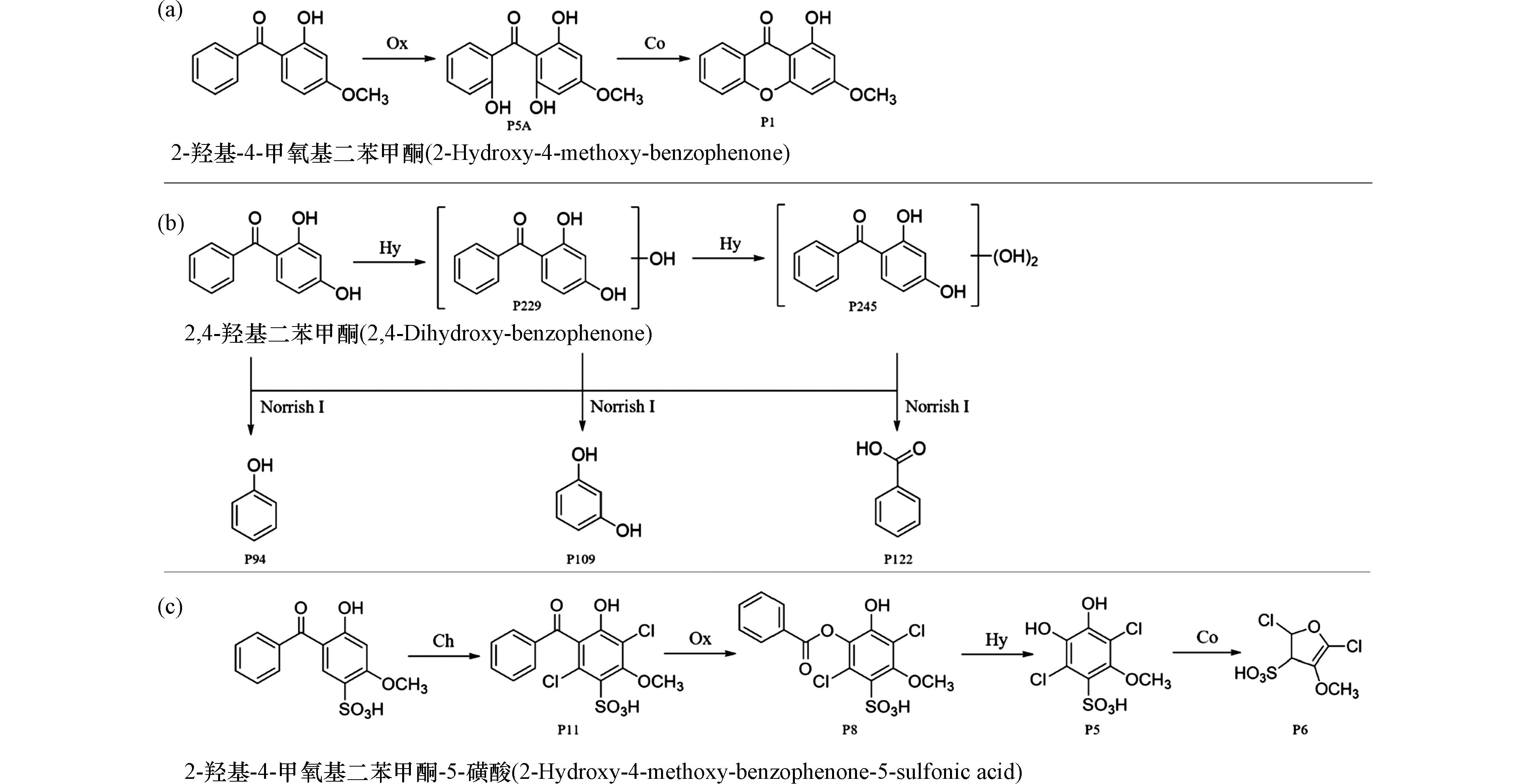 图 5 BPs类化合物其他反应的反应途径Figure 5. Some other transformation pathways of BPsa. 过硫酸盐活化体系中2-羟基-4-甲氧基二苯甲酮的转化机理;b. 紫外/TiO2氧化体系中2,4-二羟基二苯甲酮的转化机理;c. 氯化体系中2-羟基-4-甲氧基二苯甲酮-5-磺酸的转化机理(Ox:氧化反应;Hy:水解反应;Co:缩合反应)a. Transformation pathways of 2-hydroxy-4-methoxy-benzophenone in persulfate activation system; b. Transformation pathways of 2,4-dihydroxy-benzophenone in UV/TiO2 oxidation; c. Transformation pathways of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in chlorinated system(Ox:Oxidation;Hy:Hydrolysis;Co:Condensation)
图 5 BPs类化合物其他反应的反应途径Figure 5. Some other transformation pathways of BPsa. 过硫酸盐活化体系中2-羟基-4-甲氧基二苯甲酮的转化机理;b. 紫外/TiO2氧化体系中2,4-二羟基二苯甲酮的转化机理;c. 氯化体系中2-羟基-4-甲氧基二苯甲酮-5-磺酸的转化机理(Ox:氧化反应;Hy:水解反应;Co:缩合反应)a. Transformation pathways of 2-hydroxy-4-methoxy-benzophenone in persulfate activation system; b. Transformation pathways of 2,4-dihydroxy-benzophenone in UV/TiO2 oxidation; c. Transformation pathways of 2-hydroxy-4-methoxy-benzophenone-5-sulfonic acid in chlorinated system(Ox:Oxidation;Hy:Hydrolysis;Co:Condensation)由于这些反应的相关研究报道较少,本文没有展开详细论述. 但需要特别说明的是,在氧化、消毒处理过程中由于反应复杂,研究者所提出的转化反应路径中的中间产物并非全部检出,导致很难完整描述某化合物的转化路径. 加之,由于转化的中间产物产率低、生成量少,难以分离获得纯净的产物,很多研究者往往只是通过质谱信息推测产物的结构,进而推断可能的反应机理. 众所周知,质谱信息只能给出准确的相对分子质量,不能确定官能团(如羟基、氯离子、甲氧基等)在化合物分子中的确切取代位置,难以确定产物的绝对分子结构. 因此,在实验研究过程中需要密切观察不同反应阶段中间产物的生成规律,并且分离或制备相应的产物,借助高分辨质谱、核磁共振等多种方式确定产物的绝对分子结构. 确切的产物分子结构为科学准确地揭示底物在氧化、消毒处理中的转化机理提供支撑.
4. 结论(Conclusion)
BPs类紫外防晒剂应用广泛,其潜在的负面生物学效应备受关注,因此研究它们在水处理过程中的转化特征非常必要. 氧化和消毒是最常用的水处理技术,本文总结了BPs类防晒剂在氧化和消毒处理中的转化机理,为该类污染物的风险管理和控制提供科学依据.
BPs的分子中含有不饱和的芳香苯环、酮羰基、羟基、甲氧基等官能团,其在氧化、消毒等水处理过程中最主要的转化机制是氧化反应,羟基自由基、硫酸根自由基等是最主要的活性氧化物种,可以促进BPs类物质的快速转化[47]. 此外,氯化消毒处理中的Baeyer-Villiger氧化反应可高效地将酮类化合物转化为酯类化合物,为后续的水解反应、脱羧反应、以及氧化开环提供了可能,大大促进了小分子高毒性消毒副产物的生成.
也正是由于BPs的分子中含有羰基、磺酸基等吸电子取代基,以及羟基、甲氧基等供电子取代基,BPs在氯化消毒处理中非常容易发生亲电取代反应,生成一系列单卤代、二卤代、三卤代产物,由于卤代产物的显著毒性效应,其潜在的生态与健康风险值得关注. 此外,BPs类化合物的Baeyer-Villiger氧化的酯类中间产物在次氯酸消毒体系中也容易发生亲核水解反应生成苯甲酸类产物,进一步与次氯酸发生取代脱羧反应.
由此可见,现有关于BPs类防晒剂在水处理中的转化主要涉及氧化反应、取代反应、脱羧反应等,虽然处理的方法不尽相同,但所涉及的反应类型大体相似. 因此,从反应机理出发,选择适当的处理方法,实现提高处理效率的目标,为该类污染物的风险管控提供科学依据.
-
表 1 常见二苯甲酮类化合物
Table 1. Common benzophenone compounds
名称Name 化学式Chemical formula 名称Name 化学式Chemical formula 二苯甲酮(Benzophenone) 2-羟基二苯甲酮(2-Hydroxy-benzophenone) 3-羟基二苯甲酮(3-Hydroxy-benzophenone) 4-羟基二苯甲酮(4-Hydroxy-benzophenone) 2,2´-二羟基二苯甲酮(2,2´-Dihydroxy-benzophenone) 4,4´-二羟基二苯甲酮(4,4´-Dihydroxy-benzophenone) 2,4-二羟基二苯甲酮(2,4-Dihydroxy-benzophenone) 2,4,4´-三羟基二苯甲酮(2,4,4-Trihydroxy-benzophenone) 2,3,4-三羟基二苯甲酮(2,3,4-Trihydroxy-benzophenone) 2,2´,4,4´-四羟基二苯甲酮(2,2 ́,4,4 ́-Tetrahydroxy-benzophenone) 2-羟基-4-甲氧基二苯甲酮(2-Hydroxy-4-methoxy-benzophenone) 2-羟基-4-辛氧基二苯甲酮(2-Hydroxy-4-octyloxy-benzophenone) 2-羟基-4-甲氧基二苯甲酮-5-磺酸(2-Hydroxy-4-methoxy-benzophenone-5-sulfonic acid) 2,2´-二羟基-4,4´-二甲氧基二苯甲酮(2,2 ́-Dihydroxy-4,4 ́-dimethoxy-benzophenone) 2-羟基-5-氯二苯甲酮(2-Hydroxy-5-chloro-benzophenone) 2,2´-二羟基-4-甲氧基二苯甲酮(2,2 ́-Dihydroxy-4-methoxy-benzophenone) 2,2'-二羟基-4,4'-二甲氧基苯甲酮-5,5'-二磺酸(2,2'-Dihydroxy-4,4'-dimethoxy-benzophenone-5,5'-disulfonic acid) 2,2´-羟基-4-甲氧基-4'-甲基二苯甲酮(2,2 ́-Hydroxy-4-methoxy-4'-methyl-benzophenone) -
[1] 金锡鹏, 帕它木, 吴玉霞. 紫外辐射对人体健康的不良影响[J]. 环境与职业医学, 2002, 19(1): 44-45,48. JIN X P, PA T M, WU Y X. Adverse effects of ultraviolet radiation(UVR) on human being[J]. Journal of Labour Medicine, 2002, 19(1): 44-45,48 (in Chinese).
[2] 张英锋, 范林, 马子川. 防晒剂防晒机理及其应用[J]. 化学世界, 2007, 48(12): 762-765. ZHANG Y F, FAN L, MA Z C. Sunscreen mechanism and application of sunscreen[J]. Chemical World, 2007, 48(12): 762-765 (in Chinese).
[3] CASAS-BELTRAN D A, HERNÁNDEZ-PEDRAZA M, ALVARADO-FLORES J. Estimation of the discharge of sunscreens in aquatic environments of the Mexican Caribbean[J]. Environments, 2020, 7(2): 15. doi: 10.3390/environments7020015 [4] ZHANG H, LI J X, AN Y L, et al. Concentrations of bisphenols, benzophenone-type ultraviolet filters, triclosan, and triclocarban in the paired urine and blood samples from young adults: Partitioning between urine and blood[J]. Chemosphere, 2022, 288(Pt 2): 132563. [5] GIOKAS D L, SALVADOR A, CHISVERT A. UV filters: From sunscreens to human body and the environment[J]. TrAC Trends in Analytical Chemistry, 2007, 26(5): 360-374. doi: 10.1016/j.trac.2007.02.012 [6] EKPEGHERE K I, KIM U J, SUNG-HEE O, et al. Distribution and seasonal occurrence of UV filters in rivers and wastewater treatment plants in Korea[J]. Science of the Total Environment, 2016, 542: 121-128. doi: 10.1016/j.scitotenv.2015.10.033 [7] TSUI M M P, LEUNG H W, WAI T C, et al. Occurrence, distribution and ecological risk assessment of multiple classes of UV filters in surface waters from different countries[J]. Water Research, 2014, 67: 55-65. doi: 10.1016/j.watres.2014.09.013 [8] CADENA-AIZAGA M I, MONTESDEOCA-ESPONDA S, TORRES-PADRÓN M E, et al. Organic UV filters in marine environments: An update of analytical methodologies, occurrence and distribution[J]. Trends in Environmental Analytical Chemistry, 2020, 25: e00079. doi: 10.1016/j.teac.2019.e00079 [9] BRONIOWSKA Ż, TOMCZYK I, GRZMIL P, et al. Benzophenone-2 exerts reproductive toxicity in male rats[J]. Reproductive Toxicology, 2023, 120: 108450. doi: 10.1016/j.reprotox.2023.108450 [10] BUCK LOUIS G M, KANNAN K, SAPRA K J, et al. Urinary concentrations of benzophenone-type ultraviolet radiation filters and couples' fecundity[J]. American Journal of Epidemiology, 2014, 180(12): 1168-1175. doi: 10.1093/aje/kwu285 [11] MA J C, WANG Z M, QIN C, et al. Safety of benzophenone-type UV filters: A mini review focusing on carcinogenicity, reproductive and developmental toxicity[J]. Chemosphere, 2023, 326: 138455. doi: 10.1016/j.chemosphere.2023.138455 [12] KIM S, CHOI K. Occurrences, toxicities, and ecological risks of benzophenone-3, a common component of organic sunscreen products: A mini-review[J]. Environment International, 2014, 70: 143-157. doi: 10.1016/j.envint.2014.05.015 [13] VUCKOVIC D, TINOCO A I, LING L, et al. Conversion of oxybenzone sunscreen to phototoxic glucoside conjugates by sea anemones and corals[J]. Science, 2022, 376(6593): 644-648. doi: 10.1126/science.abn2600 [14] DANOVARO R, BONGIORNI L, CORINALDESI C, et al. Sunscreens cause coral bleaching by promoting viral infections[J]. Environmental Health Perspectives, 2008, 116(4): 441-447. doi: 10.1289/ehp.10966 [15] RIZZO L, MALATO S, ANTAKYALI D, et al. Consolidated vs new advanced treatment methods for the removal of contaminants of emerging concern from urban wastewater[J]. Science of the Total Environment, 2019, 655: 986-1008. doi: 10.1016/j.scitotenv.2018.11.265 [16] WANG J L, ZHUAN R. Degradation of antibiotics by advanced oxidation processes: An overview[J]. Science of the Total Environment, 2020, 701: 135023. doi: 10.1016/j.scitotenv.2019.135023 [17] 潘继生, 邓家云, 张棋翔, 等. 羟基自由基高级氧化技术应用进展综述[J]. 广东工业大学学报, 2019, 36(2): 70-77,85. PAN J S, DENG J Y, ZHANG Q X, et al. A review of the application of advanced oxidation technology of hydroxyl radicals[J]. Journal of Guangdong University of Technology, 2019, 36(2): 70-77,85 (in Chinese).
[18] WANG S Y, WANG X H, CHEN J, et al. Removal of the UV filter benzophenone-2 in aqueous solution by ozonation: Kinetics, intermediates, pathways and toxicity[J]. Ozone:Science & Engineering, 2018, 40(2): 122-132. [19] PAN X X, YAN L Q, QU R J, et al. Degradation of the UV-filter benzophenone-3 in aqueous solution using persulfate activated by heat, metal ions and light[J]. Chemosphere, 2018, 196: 95-104. doi: 10.1016/j.chemosphere.2017.12.152 [20] ZÚÑIGA-BENÍTEZ H, ARISTIZÁBAL-CIRO C, PEÑUELA G A. Heterogeneous photocatalytic degradation of the endocrine-disrupting chemical Benzophenone-3: Parameters optimization and by-products identification[J]. Journal of Environmental Management, 2016, 167: 246-258. doi: 10.1016/j.jenvman.2015.11.047 [21] ZÚÑIGA-BENÍTEZ H, ARISTIZÁBAL-CIRO C, PEÑUELA G A. Photodegradation of the endocrine-disrupting chemicals benzophenone-3 and methylparaben using Fenton reagent: Optimization of factors and mineralization/biodegradability studies[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 59: 380-388. doi: 10.1016/j.jtice.2015.09.004 [22] VEGA GARZÓN L P, ZÚÑIGA-BENÍTEZ H, PEÑUELA G A. Elimination of benzophenone-1 in water by high-frequency ultrasound[J]. Water, Air, & Soil Pollution, 2021, 232(12): 1-10. [23] ZHANG X Y, WEI D B, SUN X F, et al. Free available chlorine initiated Baeyer-Villiger oxidation: A key mechanism for chloroform formation during aqueous chlorination of benzophenone UV filters[J]. Environmental Pollution, 2021, 268(Pt A): 115737. [24] BAEYER A, VILLIGER V. Einwirkung des caro'schen reagens auf ketone[J]. Berichte Der Deutschen Chemischen Gesellschaft, 1899, 32(3): 3625-3633. doi: 10.1002/cber.189903203151 [25] XIAO M, WEI D B, YIN J X, et al. Transformation mechanism of benzophenone-4 in free chlorine promoted chlorination disinfection[J]. Water Research, 2013, 47(16): 6223-6233. doi: 10.1016/j.watres.2013.07.043 [26] GAGO-FERRERO P, DEMEESTERE K, SILVIA DÍAZ-CRUZ M, et al. Ozonation and peroxone oxidation of benzophenone-3 in water: Effect of operational parameters and identification of intermediate products[J]. Science of the Total Environment, 2013, 443: 209-217. doi: 10.1016/j.scitotenv.2012.10.006 [27] GONG P, YUAN H X, ZHAI P P, et al. Investigation on the degradation of benzophenone-3 by UV/H2O2 in aqueous solution[J]. Chemical Engineering Journal, 2015, 277: 97-103. doi: 10.1016/j.cej.2015.04.078 [28] 徐彬焜, 余韵, 潘志刚, 等. 紫外活化过硫酸盐工艺降解二苯甲酮-3效果研究[J]. 中国给水排水, 2020, 36(23): 69-74,80. XU B K, YU Y, PAN Z G, et al. Degradation of benzophenone-3 by UV-activated persulfate process[J]. China Water & Wastewater, 2020, 36(23): 69-74,80 (in Chinese).
[29] BRODSKY A M, LEVICH V G. Theory of the simplest substitution reactions[J]. The Journal of Chemical Physics, 1973, 58(7): 3065-3081. doi: 10.1063/1.1679618 [30] LIU W, WEI D B, LIU Q, et al. Transformation pathways and acute toxicity variation of 4-hydroxyl benzophenone in chlorination disinfection process[J]. Chemosphere, 2016, 154: 491-498. doi: 10.1016/j.chemosphere.2016.04.005 [31] ZHANG X Y, WEI D B, YU Q, et al. Characterization of UV and chlorine contributions to transformation of 2,3,4-trihydroxybenzophenone under combined UV-chlorine treatment[J]. Chemosphere, 2021, 263: 128310. doi: 10.1016/j.chemosphere.2020.128310 [32] YANG P Z, KONG D Y, JI Y F, et al. Chlorination and chloramination of benzophenone-3 and benzophenone-4 UV filters[J]. Ecotoxicology and Environmental Safety, 2018, 163: 528-535. doi: 10.1016/j.ecoenv.2018.07.111 [33] DEBORDE M, von GUNTEN U. Reactions of chlorine with inorganic and organic compounds during water treatment—Kinetics and mechanisms: A critical review[J]. Water Research, 2008, 42(1/2): 13-51. [34] XIAO M, WEI D B, LI L P, et al. Formation pathways of brominated products from benzophenone-4 chlorination in the presence of bromide ions[J]. Journal of Environmental Sciences, 2014, 26(12): 2387-2396. doi: 10.1016/j.jes.2014.03.001 [35] YANG F, WEI D B, XIAO M, et al. The chlorination transformation characteristics of benzophenone-4 in the presence of iodide ions[J]. Journal of Environmental Sciences, 2017, 58: 93-101. doi: 10.1016/j.jes.2017.04.023 [36] Peijnenburg W J G M. The use of quantitative structure-activity relationships for predicting rates of environmental hydrolysis processes[J]. Pure and Applied Chemistry, 1991, 63(11): 1667-1676. doi: 10.1351/pac199163111667 [37] SMITHM, MARCH J. Substitution Reactions: Free radicals. march's advanced organic chemistry: reactions, mechanisms, and structure[M]. HobokenJohn: Wiley & Sons, Inc, Sixth Edition 2006, 14: 934-998. [38] 贾娜, 施海燕, 王鸣华. 2, 4-D丁酯的水解与光解特性研究[J]. 农业环境科学学报, 2011, 30(6): 1082-1086. JIA N, SHI H Y, WANG M H. Hydrolysis and photolysis of 2, 4-D butylate[J]. Journal of Agro-Environment Science, 2011, 30(6): 1082-1086 (in Chinese).
[39] 沈一君, 彭明国, 徐彬焜, 等. 紫外活化过硫酸盐降解二苯甲酮-4的动力学影响及降解机理与风险评价[J]. 环境科学研究, 2019, 32(1): 174-182. SHEN Y J, PENG M G, XU B K, et al. Degradation of BP4 by UV-activated persulfate process: Kinetic, mechanism and risk[J]. Research of Environmental Sciences, 2019, 32(1): 174-182 (in Chinese).
[40] 关保川, 许孝良, 王红, 等. 可见光催化脱羧偶联反应研究进展[J]. 有机化学, 2016, 36(7): 1564-1571. doi: 10.6023/cjoc201601012 GUAN B C, XU X L, WANG H, et al. Progress on the decarboxylation coupling reaction mediated by visible light[J]. Chinese Journal of Organic Chemistry, 2016, 36(7): 1564-1571 (in Chinese). doi: 10.6023/cjoc201601012
[41] LI T, ZHANG X C, ZHANG C M, et al. Thermodynamic and kinetic studies on OH-involved photo-decarboxylation mechanism for waste cooking oils to biofuels[J]. Fuel, 2019, 254: 115665. doi: 10.1016/j.fuel.2019.115665 [42] ZHANG T, JI Y F, CHOVELON J M, et al. Self-accelerated photodegradation of 2, 4-dihydroxybenzophenone in water: Formation of photoactive products and implications for the transformation of coexisting organic contaminants[J]. ACS ES& T Water, 2022, 2(6): 1065-1072. [43] PENG M G, DU E D, LI Z H, et al. Transformation and toxicity assessment of two UV filters using UV/H2O2 process[J]. Science of the Total Environment, 2017, 603/604: 361-369. doi: 10.1016/j.scitotenv.2017.06.059 [44] LARSON R A, ROCKWELL A L. Chloroform and chlorophenol production by decarboxylation of natural acids during aqueous chlorination[J]. Environmental Science & Technology, 1979, 13(3): 325-329. [45] PAN X X, YAN L Q, LI C G, et al. Degradation of UV-filter benzophenone-3 in aqueous solution using persulfate catalyzed by cobalt ferrite[J]. Chemical Engineering Journal, 2017, 326: 1197-1209. doi: 10.1016/j.cej.2017.06.068 [46] GUO Q R, WEI D B, ZHAO C F, et al. Physical UV-blocker TiO2 nanocomposites elevated toxicity of chemical sunscreen BP-1 under UV irradiation[J]. Chemical Engineering Journal, 2023, 469: 143899. doi: 10.1016/j.cej.2023.143899 [47] ZÚÑIGA-BENÍTEZ H, PEÑUELA G A. Application of solar photo-Fenton for benzophenone-type UV filters removal[J]. Journal of Environmental Management, 2018, 217: 929-938. -






 DownLoad:
DownLoad:

