-
溶解性有机质(Dissolved organic matter,DOM)是指能溶解于水且能透过0.45 μm滤膜的复杂有机混合物[1-2],其广泛存在于天然水体、土壤和大气等生态系统中,对于维持全球碳循环具有十分重要的意义[3-5]. 近年来,傅里叶变换离子回旋共振质谱(Fourier transform ion cyclotron resonance mass spectrometry,FT-ICR MS)因其超高的分辨率(分辨率大于
200000 )和质量精确度(质量误差小于10−6)而广泛应用于分子水平的DOM化学多样性研究[1, 3, 6]. DOM的FT-ICR MS谱图中通常含有数千乃至上万个离子峰,各个离子峰的分子式匹配和单双电荷状态的确定是DOM超高分辨质谱(Ultrahigh-resolution mass spectrometry,UHR-MS)峰数据分析的难点. 针对DOM分子式匹配的难题,目前有一系列工具可用于分子式自动匹配,包括仪器软件(如DataAnalysis和Composer)、自动化程序(Formularity[7]、UltraMassExplorer[8]和TMDS[9]等)以及脚本(MFassignR[10]、CIA[11]、SQ[12]和 TRFu[13]等).DOM质谱峰电荷状态的确定使得DOM的高分辨质谱峰更加复杂. DOM分子中通常含有大量的含氧官能团,如羧基和羟基[14, 15],这使得DOM在电离过程中易形成多电荷离子,因此确定峰的电荷状态也成为了一大困扰[16]. 针对DOM的UHR-MS离子峰电荷状态的确定,早在1995年Senko等[17]就根据单同位素峰(12Cn峰)和13C同位素峰(13C112Cn−1峰)确定了质谱中的物质都带单个电荷. Brown等[18]根据12Cn峰和13C112Cn−1峰确定了单电荷离子,发现所观察到的离子均为单电荷离子并提出无法排出多电荷离子的存在. Leenheer等[19]在质谱上观察到的单个腐殖质离子被认为是带多个电荷,而据其它文献报道,电喷雾离子源(Electrospray ionization,ESI)质谱中DOM离子只带一个电荷[20, 21]. Kujawinski等[22, 23]认为在电喷雾正电荷模式[ESI(+)]质谱中只有极少数腐殖质离子带多个电荷,而在电喷雾负电荷模式[ESI(−)]质谱中可能包含多个多电荷离子. Stenson等[20]认为低分子量腐殖酸在ESI(−)质谱中更容易电离形成多电荷离子,高分子量离子大多带一个电荷. 在处理多电荷离子的问题上,大多数学者直接将质谱中的离子峰默认为单电荷离子峰[18, 22, 24, 25],而部分学者以12Cn峰和13C112Cn−1峰之间的质量差来判断多电荷离子的存在[2, 9, 26]. 这就导致双电荷离子的存在与13C同位素峰存在因果关系,然而当不存在13C112Cn−1峰时,12Cn峰也有可能是以双电荷离子峰的形式存在. 此外,传统方法没有考虑含N的双电荷离子的情况. 根据氮规则和ESI(-)模式下由天然有机质离子峰的经验规则(即天然有机质的离子峰常位于名义质量至名义质量+0.3范围内)[27]可知:含有奇数个N的双电荷离子12Cn峰会出现在质谱图上名义质量+0.5 Da的位置,而13C112Cn−1峰则会出现在质谱图上名义质量+1 Da的位置. 因此含有奇数个N的双电荷离子将会使双电荷离子的确定更加复杂化,这也给传统13C同位素方法带来了新的挑战.
基于此,本研究结合FT-ICR MS技术,提出了一种基于单电荷离子前体的双电荷离子分子式匹配方法,并进一步探讨了该方法对DOM的UHR-MS谱图中双电荷离子峰的识别效果以及不同类型DOM中多电荷离子的性质,加深了对DOM化学多样性的认识.
-
本研究所使用的玻璃瓶均在稀盐酸溶液(体积比为5%)中浸泡24 h后,然后用超纯水和甲醇(LC-MS纯)反复清洗[28]. 实验步骤:(1)用电子天平(购自波兰RADWAG,AS 60/220.R2)准确称取10.0 mg SRNOM标准品(购自国际腐殖质学会,2R101N),将其溶解在50 mL超纯水中制备成200 mg·L−1的储备液;(2)取5 mL SRNOM储备液,采用0.45 μm的纤维滤膜过滤;(3)将上述SRNOM储备液与甲醇溶液(LC-MS纯,购自Fisher Scientific公司)等体积混合.
此外,本研究还获取了127个样品谱图,数据来源于文献[29]. 该127个样品由5个不同类型的来源组成,分别为海水DOM(包含16个海洋水和23个海岸带海水样品)、自然淡水DOM(包含24个淡水、15个地下水、5个农田水、14个SRNOM和2个SRFA样品)、土壤DOM(20个样品)、废水DOM(6个样品)以及其它类型DOM(包含1个木质素和1个树叶浸提液样品).
-
本研究利用FT-ICR MS仪(型号为Solarix 2XR 7T,德国Bruker Daltonik公司),采用手动直接进样的方式,电荷模式为ESI(-),进样流速为120 μL·h−1,离子源喷针电压设置为5.0 kV,样品采用负离子宽谱扫描模式,质量(mass-to-charge ratio,m/z)扫描范围为100—
1100 ,离子累积时间为0.025 s,扫描次数为1000 次,数据容量为4 megaword. 在样品谱图采集前,先用100 mg·L−1三氟乙酸钠标准液(50%甲醇水溶液)对m/z值进行外标校准. 所有FT-ICR MS谱图以淡水天然有机质的CHO同系化合物为内标物质,采用Data Analysis软件(Bruker Daltonik,version 5.0)对谱图进行校准[13]. -
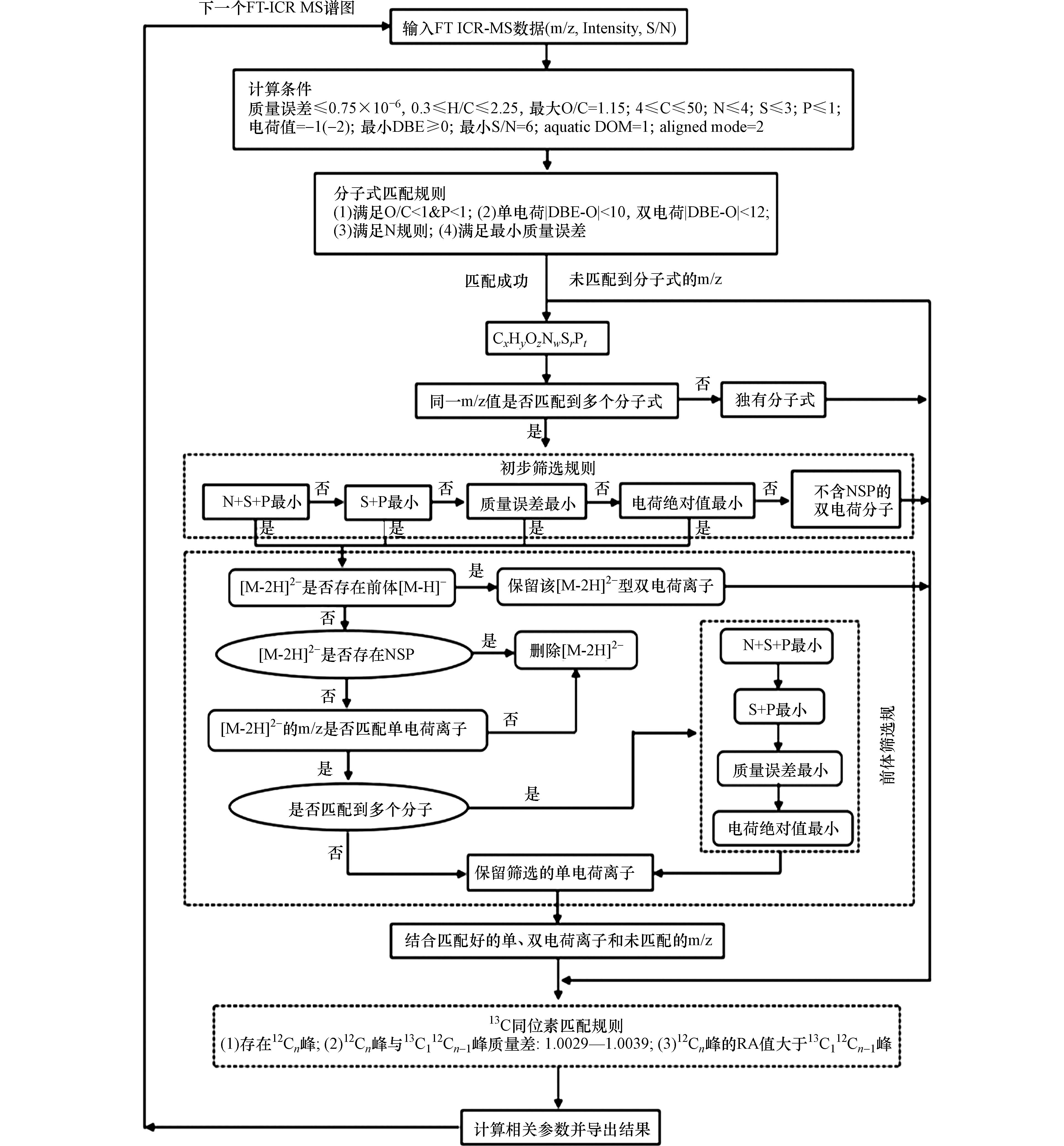
本研究采用TRFu代码[29]进行分子式匹配. TRFu代码运行流程图见图1,首先将质荷比(m/z)、强度(Intensity)和信噪比(Signal-to-noise ratio,S/N)输入到MATLAB中(必须确保m/z、Intensity和S/N的顺序一致). 计算条件如下:确认S/N大于等于6的峰,测量质量误差小于等于0.75×10−6;仅考虑C、H、O、N、P和S等6种元素,元素个数及比例设置如下:C(4—50)、N(0—5)、S(0—3)、P(0—1);氢碳比(H/C)范围:0.3≤H/C≤2.25,氧碳比(O/C)范围:0≤O/C≤1.15. 双键当量(Double-bond equivalence,DBE)大于等于0,电荷值为-1和-2. 进一步采用如下规则对得到的分子式进行过滤:设定单电荷离子的双键当量减氧[25](DBE-O)范围为-10≤DBE-O≤10;双电荷离子的DBE-O范围进一步扩大为-12≤DBE-O≤12且同时满足N+S+P原子个数总数最小和N规则.
由于DOM分子中非氧杂原子含量较低[30],同一m/z值下可能存在的多个分子式,通过最佳分子式筛选规则进行筛选. 最佳分子式筛选规则主要分为三个部分:初步筛选、前体筛选和13C同位素筛选. 初步筛选规则如下:(1)N+S+P原子个数之和最小;(2)S+P原子个数之和最小;(3)最小质量误差. 在初步筛选规则下得到的[M-2H]2−型分子式还需要进行前体筛选,规则如下:(a)当[M1-2H]2−型分子存在[M1-H]−型分子时,则保留该m/z值(m/z值为[M1-2H]2−型分子的质荷比,同下)所匹配的分子式;(b)当[M1-2H]2−型分子式不存在[M1-H]−型分子且含有非氧杂原子时,则删除该m/z值所匹配的分子式;(c)当[M1-2H]2−型分子式不存在[M1-H]−型分子和非氧杂原子时,则判断该m/z值是否匹配了[M2-H]−型分子式(M1、M2为不同的分子式). 判断条件如下:①如果未匹配到[M2-H]−型分子式,则删除该m/z值所匹配的分子式;②如果匹配到单个[M2-H]−型分子时,则将该m/z值匹配为[M2-H]−型分子式;③如果匹配到多个[M2-H]−型分子时,则将所有匹配到的[M2-H]−型分子继续按照以下顺序进行筛选:(i)N+S+P原子个数之和最小;(ii)S+P原子个数之和最小;(iii)最小质量误差. 最后将上述未匹配的峰、确定的峰以及选定的最佳峰组合后进行13C同位素筛选. 规则如下:(1)存在单同位素峰(12Cn峰);(2)存在13C同位素峰(13C112Cn−1峰),且13C112Cn−1峰与12Cn峰之间的m/z值相差
1.0031 Da至1.0035 Da;(3)满足12Cn峰的相对丰度(Relative abundance,RA)大于等于5%或13C112Cn−1峰的RA值小于12Cn峰且12Cn峰的RA值小于5%. -
本研究根据每个离子峰所属的化学式,采用以下方程分别计算DBE、修正的芳香性指数(Modified aromaticity index,AImod)和碳名义氧化态(Nominal oxidation state of carbon,NOSC). 其中DBE是指分子中双键和脂环总数;AImod被用来确定DOM中是否存在芳香结构(AImod>0.5)或缩合芳香结构(AImod≥0.67)[31-32];NOSC指数与有机化合物的生物地球化学反应性和生物利用度有关[33]. 功能多样性指数DF是以FT-ICR MS数据计算为距离函数(Rao的二次熵)[34],DF可理解为两个分子之间相对于所选DOM分子性质的预期差异值. 分子式CxHyOzNwSrPt的相关参数(包括DBE、AImod、NOSC和DF)计算公式分别如下式(1)—式(4)所示:
公式(1)、(2)和(3)中的x、y、z、w、r和t分别指每个分子式中的碳、氢、氧、氮、硫和磷原子的化学计量数. 公式(4)中n为样品匹配的分子式总数,pi和pj分别是分子式i和j的RA值,ci和cj分别是分子式i和j的特定参数(如O/C、H/C、DBE、AImod、和NOSC等).
单个13C同位素的13C112Cn−1峰的峰强度偏差的计算公式如下(式(5)和式(6)):
式(6)中,
0.010816 为13C与12C同位素的自然丰度比;nC是12Cn峰分子式中的碳原子数. 当样本数据通过Kolmogorov-Smirnov正态性检验时,使用单因素方差分析(One-way analysis of variance,ANOVA)在0.05的显著性水平上检验比较组之间的显著性差异;否则采用非参数Kruskal-Wallis单因素方差分析. -
实验中一共找到410个双电荷12Cn峰(对应410个双电荷13C112Cn−1峰,统称为A类峰)和116个单、双电荷同m/z值的12Cn峰(对应116个单电荷13C112Cn−1峰和116个双单电荷13C112Cn−1峰,统称为B类峰). 为验证双电荷DOM分子([M-2H]2−型分子,[M-H]2−型分子为单电荷DOM分子)的准确性,本实验将从质量误差和峰强度偏差两个角度进行13C同位素验证.
从质量误差的角度来看,A类12Cn峰与13C112Cn−1峰的m/z差值为(
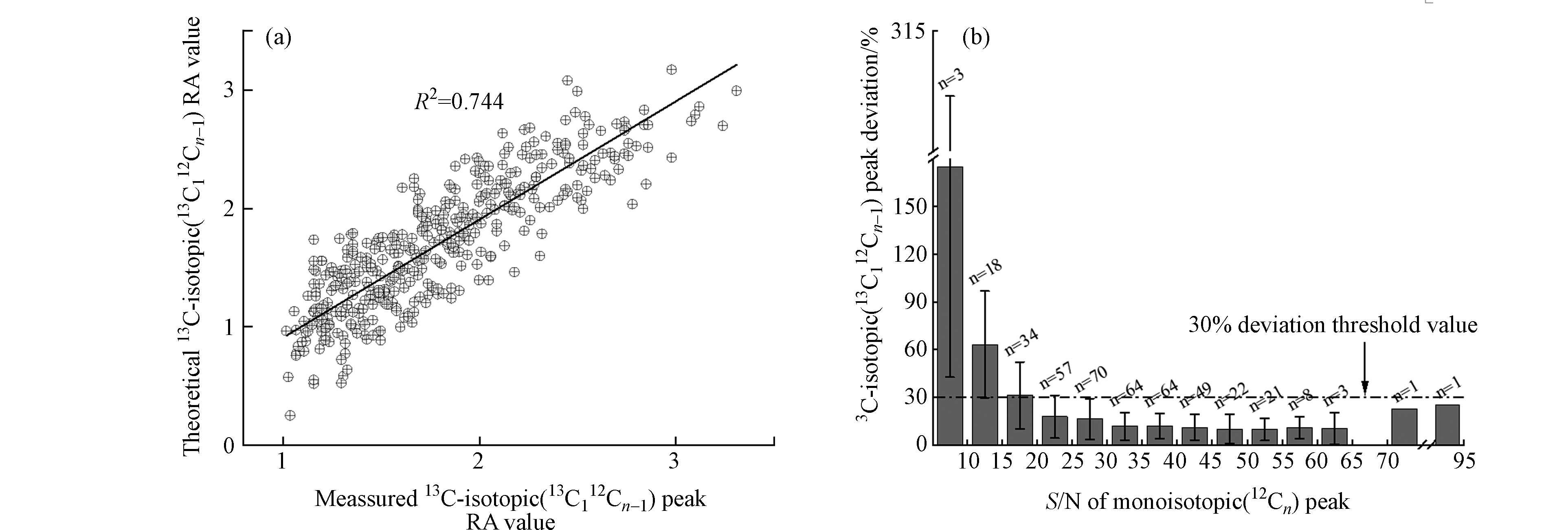
0.5016704 ±0.00007) Da,这与其理论值0.5016775 高度接近,说明双电荷DOM的12Cn峰和13C112Cn−1峰分子式均匹配正确. 假设A类12Cn峰和13C112Cn−1峰所匹配的分子式是假阳性的,结合A类峰的m/z值在质谱图中的位置来看,所有12Cn峰(13C112Cn−1峰)匹配的分子式将包含偶(奇)数个N或奇(偶)数个N加单个13C. 进一步,在初始分子式匹配条件下(如最小质量误差0.75×10−6,0.3≤ H/C ≤2.25,0≤ O/C ≤1.15,-12≤ DBE-O ≤12),A类12Cn峰和13C112Cn−1峰的m/z值分别匹配到2144 和1955个双电荷分子式. 其中12Cn峰匹配到的双电荷分子式类型包括X、13C1N1、N2、13C1N3、N4和13C1N5型分子式(X表示不含13C和N元素的CHO类分子式,其他元素未给出);13C112Cn−1峰匹配到的双电荷分子式类型包括13C1、N1、13C1N2、N3、13C1N4和N5型分子式. 12Cn峰和13C112Cn−1峰各自匹配的5类分子式的质量误差如图2a和图2b所示,结果显示:12Cn峰所匹配的分子式中X型与其它4类分子式均存在显著相关性(P<0.05);13C112Cn−1峰所匹配的分子式中13C1型与N1、13C1N2、N3和13C1N4型分子式存在显著性差异(P<0.05),与N5型无显著性差异. 以上结果表明,12Cn峰和13C112Cn−1峰所匹配的分子式中CHO类的质量误差最低,分别为(0.087±0.084)×10−6和(0.142±0.114)×10−6. 进一步从非氧杂原子的角度来看,由于DOM中非氧杂原子含量较低[30],12Cn峰和13C112Cn−1峰的分子式匹配为CHO类的准确性更高.从峰强度偏差来看,A类峰中13C112Cn−1峰的测量RA值与理论RA值(由公式(6)得出)的分布如图3a所示. 13C112Cn−1峰的理论RA值与测量RA值的比值为0.94±0.17,二者的相关系数(R2)为0.744,这表明由A类12Cn峰预测的理论13C112Cn−1峰与实际13C112Cn−1峰基本符合. 从±30%的偏差阈值来看[35],存在347个(约占A类双电荷离子峰总数的84.63%)A类12Cn峰满足13C同位素偏差验证. 而在±30%偏差阈值之外,通过13C同位素偏差验证时产生了较大的偏差(如图3b中6≤S/N≤20的区域). 如m/z值为
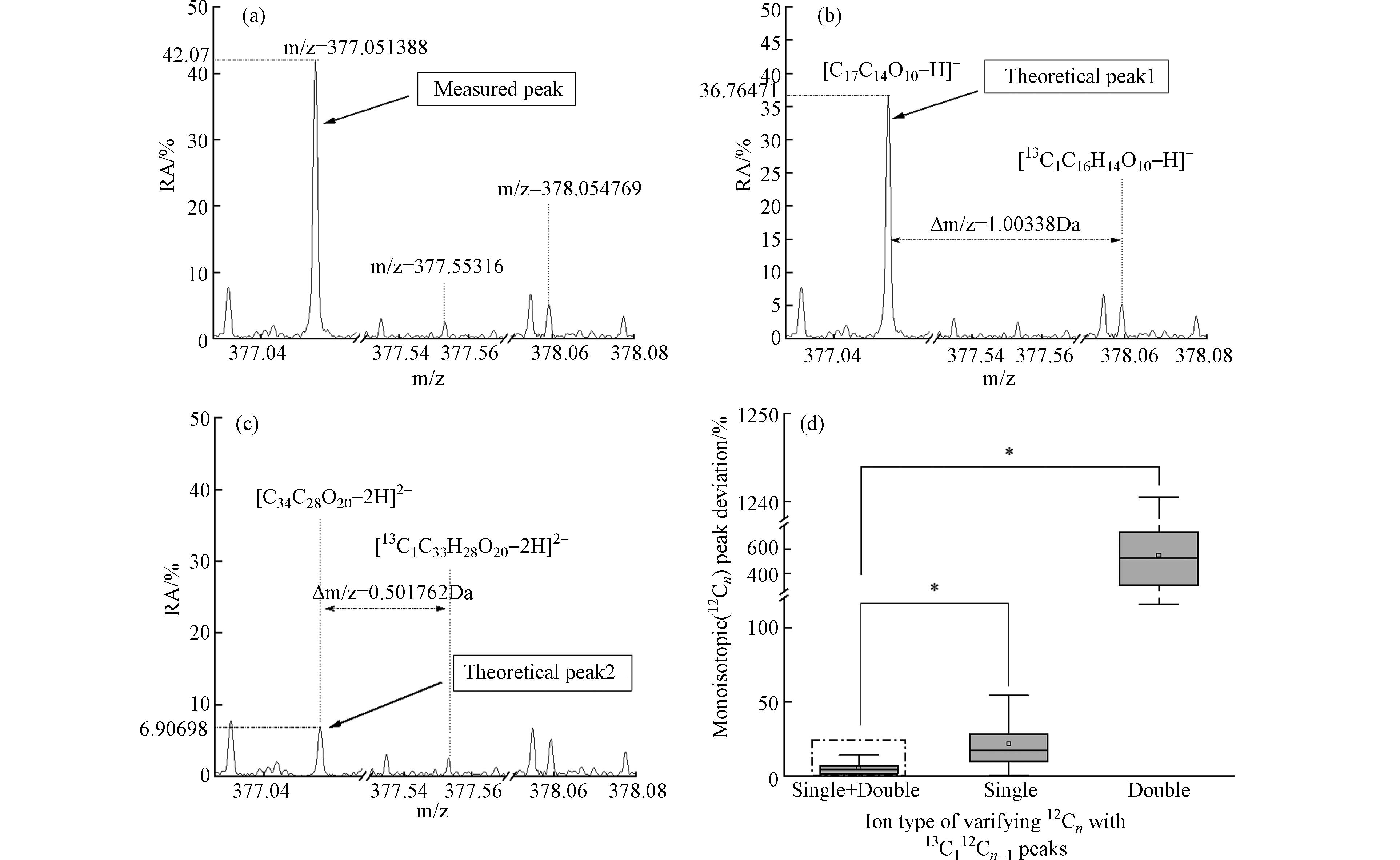
228.064009 的12Cn峰[C20H24O12]2−,其RA值和S/N值分别为1.15和7.2;以及m/z值为228.565737 的13C112Cn−1峰[13C1C19H24O12]2−,其RA值和S/N值为分别为1.04和6.3,通过公式(5)计算将会产生3.18的偏差值. 产生这个结果原因并不是分子式匹配错误,因为所有分子式赋值都满足严格的匹配条件,这可能是由于[C20H24O12]2−峰的S/N值过低(仅为7.2)从而差生较大的偏差. 因此,部分A类峰的13C同位素偏差较大可归结为S/N值过低(6≤S/N≤20)从而导致检测到的RA值偏低.质谱图上相同m/z值处的峰信号强度是由多个离子的信号叠加而成,这些离子可能来自多种不同的电荷态. 因此,对于B类12Cn峰的峰强度偏差验证,这里采用单、双电荷13C112Cn−1峰的RA值反向验证12Cn峰. 如图4a—图4c所示,在m/z值为
377.051388 的位置存在单电荷[C17H13O10]−和双电荷离子[C34H26O20]2−,同时分别在约为M + 1和M + 0.5的m/z差值处检测到13C同位素峰[13C1C16H13O10]−和[13C1C33H26O20]2−. 单、双电荷12Cn峰的理论RA值可由13C112Cn−1峰的RA值经过公式(6)分别反向推求出,结果分别为36.76%和6.91%. 因此,m/z值为377.051388 的理论RA值为43.67%,峰强度偏差为−3.67%. 若验证峰强度偏差时只考虑单电荷(或双电荷)13C112Cn−1的RA值,实验将会产生更大的偏差. 如图4d所示,采用单、双电荷13C112Cn−1峰相结合的验证方式与只采用单电荷(或双电荷)13C112Cn−1峰的验证方式之间存在显著性差异(P<0.05),采用单、双电荷13C112Cn−1峰相结合的所得到的分子式具有更低的强度偏差值(5.37%±5.254%).以上结果表明,A类峰中大部分双电荷离子(约占84.63%)通过了13C同位素偏差验证,少数双电荷离子存在较大偏差可归结为部分12Cn峰的S/N值过低(大约小于20);由13C112Cn−1峰反向验证12Cn峰的峰强度偏差结果表明:B类峰的信号强度是由相同m/z值的单、双电荷12Cn峰信号叠加而成,采用单、双电荷13C112Cn−1峰相结合的验证方式准确度更高,这也进一步表明B类双电荷离子有效的通过了13C同位素偏差验证.
-
对整个质谱数据进行分子式匹配和筛选后,DOM的FT-ICR MS谱图中双电荷离子峰总共
2097 个,其中以前体离子方法筛选得到的双电荷离目为1762 个(约占双电荷离子总数的84.02%). 以图5a中名义质量325和651为例,1号到9号峰均包含双电荷离子峰,其中2号、6号和9号峰为单、双电荷共存的离子峰([CxHyOz]−和[C2xH2yO2z]2−具有相同的m/z),同时存在强度较高的1'号到9'号单电荷离子峰前体. 从DOM分子中羧基的数量和间距来看[19],1号到9号双电荷离子峰的出现可能受到羧基的影响. 传统13C同位素方法是以分子式之间的质量差(∆m/z=13C112Cn−1-12Cn)来判断单、双电荷离子,如图5b(峰1和峰1'为单电荷离子峰;峰2和峰2'为双电荷离子峰)所示,该方法得到的双电荷离子数目为1216 个(约占双电荷离子总数的57.99%),这其中还包含27个含N的双电荷离子. 值得一提的是,传统13C同位素方法确认的双电荷12Cn峰(m/z值对应名义质量)和13C112Cn−1峰(m/z值对应名义质量+0.5 Da)如图5b中的峰2和峰2'所示,但该方法寻找的双电荷离子并不全面,这是因为传统13C同位素方法并没有考虑含N的双电荷离子. 如图5b中的峰3和峰3'所示,含奇数个N原子的双电荷12Cn峰(m/z值对应名义质量+0.5 Da)和13C112Cn−1峰(m/z值对应名义质量+1 Da)与传统13C同位素方法确认的双电荷12Cn峰和13C112Cn−1峰的在谱图上的位置不同,这也是传统13C同位素方法所未考虑的. 其中峰3的m/z为334.530568 ,离子化学式为[C29H19O18N1]2−;峰3'的m/z为335.032374 ,离子化学式为[13C1C28H19O18N1]2−(峰3'的S/N值仅为5.5,这里仅为说明传统13C同位素方法的不足). 此外,当强度较低或者不存在13C同位素峰时,传统13C同位素方法则不能判断12Cn峰的电荷状态. 如图5c所示,可以看到在m/z值相差约0.5 Da的范围内,识别了双电荷12Cn峰(峰a到峰d)以及对应的13C112Cn−1峰(峰a'到峰d'). 同时存在6个双电荷12Cn峰(峰f到峰k)没有匹配到13C112Cn−1峰,而峰f到峰k均满足严格的赋值条件[13],这说明以传统13C同位素方法来寻找双电荷离子并不可靠. 对比两种方法可知,传统13C同位素方法并没有考虑单电荷离子前体是否存在[16, 19, 20, 36],以名义m/z 323和m/z 647为例(图5d). 在m/z为323和647的质量窗口上验证了双电荷12Cn峰[C31H18O16]2−和双电荷13C112Cn−1峰[13C1C30H18O16]2−(分别对应图5d中峰a和峰a'),其中峰a存在单电荷离子峰前体[C31H19O16]−,但峰a'却并未找到单电荷离子峰前体. 在该样品中总共发现335个双电荷离子(约占双电荷离子总数的15.98%)不存在单电荷离子前体,出现这种结果可能是多个羧基的存在使DOM更易电离形成双电荷离子[19]. 以上结果表明,相比传统13C同位素方法,单电荷离子前体方法能够有效识别DOM的FT-ICR MS谱图中双电荷离子峰,可以进一步提高(提高44.90%)双电荷离子的个数. -
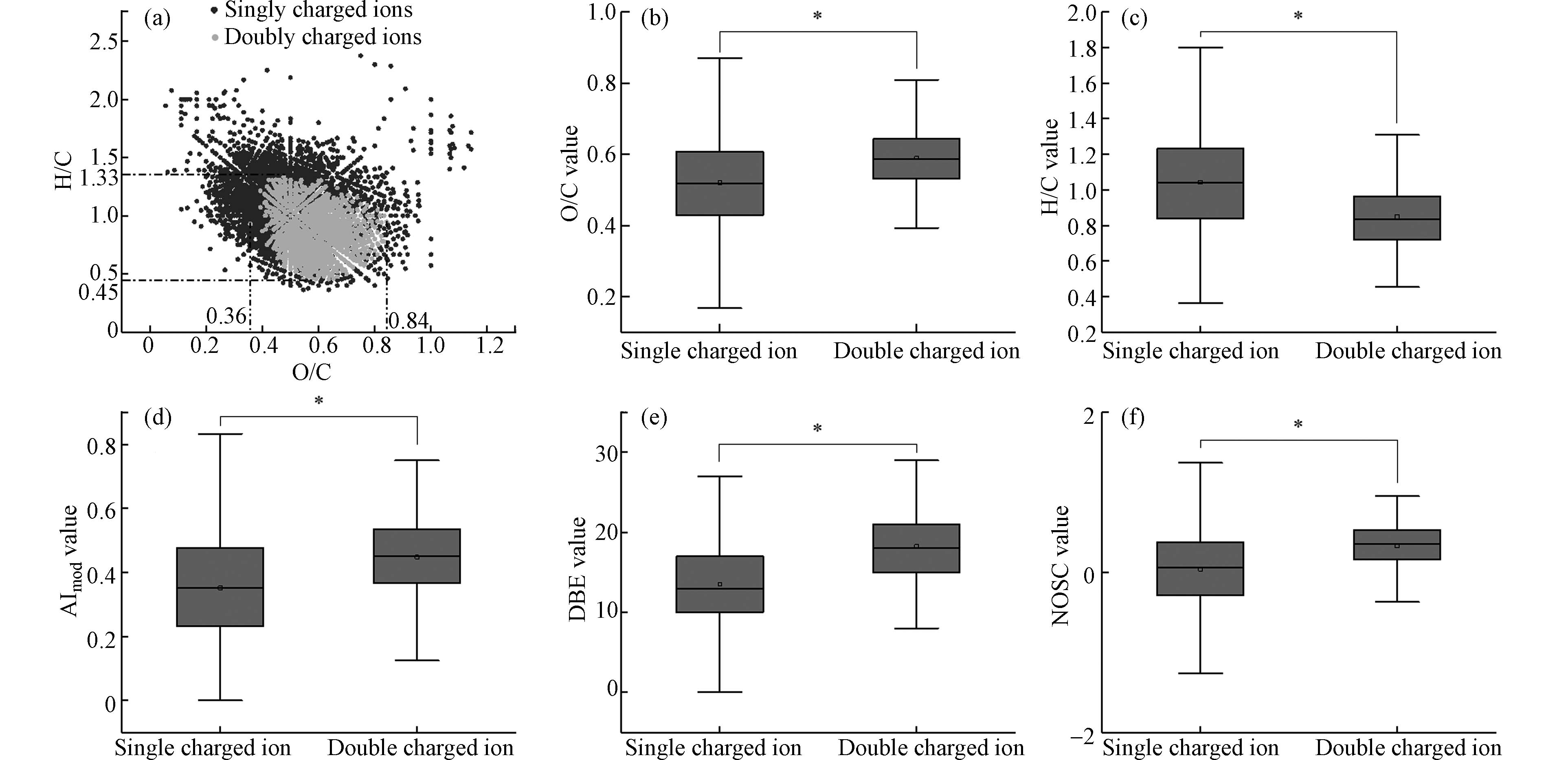
从单、双电荷DOM分子的van Krevelen[14]可知(图6a),大部分双电荷DOM分子(约占比双电荷离子总数的99.80%)具有较高的O/C值(0.39—0.84)和较低的H/C值(0.45—1.33),这意味着双电荷DOM分子具有较高的不饱和度,说明双电荷DOM分子经历了更多的氧化过程从而具有较高的氧化态(NOSC)[37]. 从单、双电荷DOM分子的5个参数箱线图(图6b—图6f)可以看到,5个参数值在单、双电荷DOM分子之间存在显著性差异(P<0.05). 其中O/C、DBE、AImod和NOSC值在双电荷DOM分子中均值更高,而H/C值更低. 以上结果表明双电荷DOM分子具有更高的芳香性、不饱和度和氧化态,这可能与双电荷DOM分子中存在较多的羧基有关[38].
-
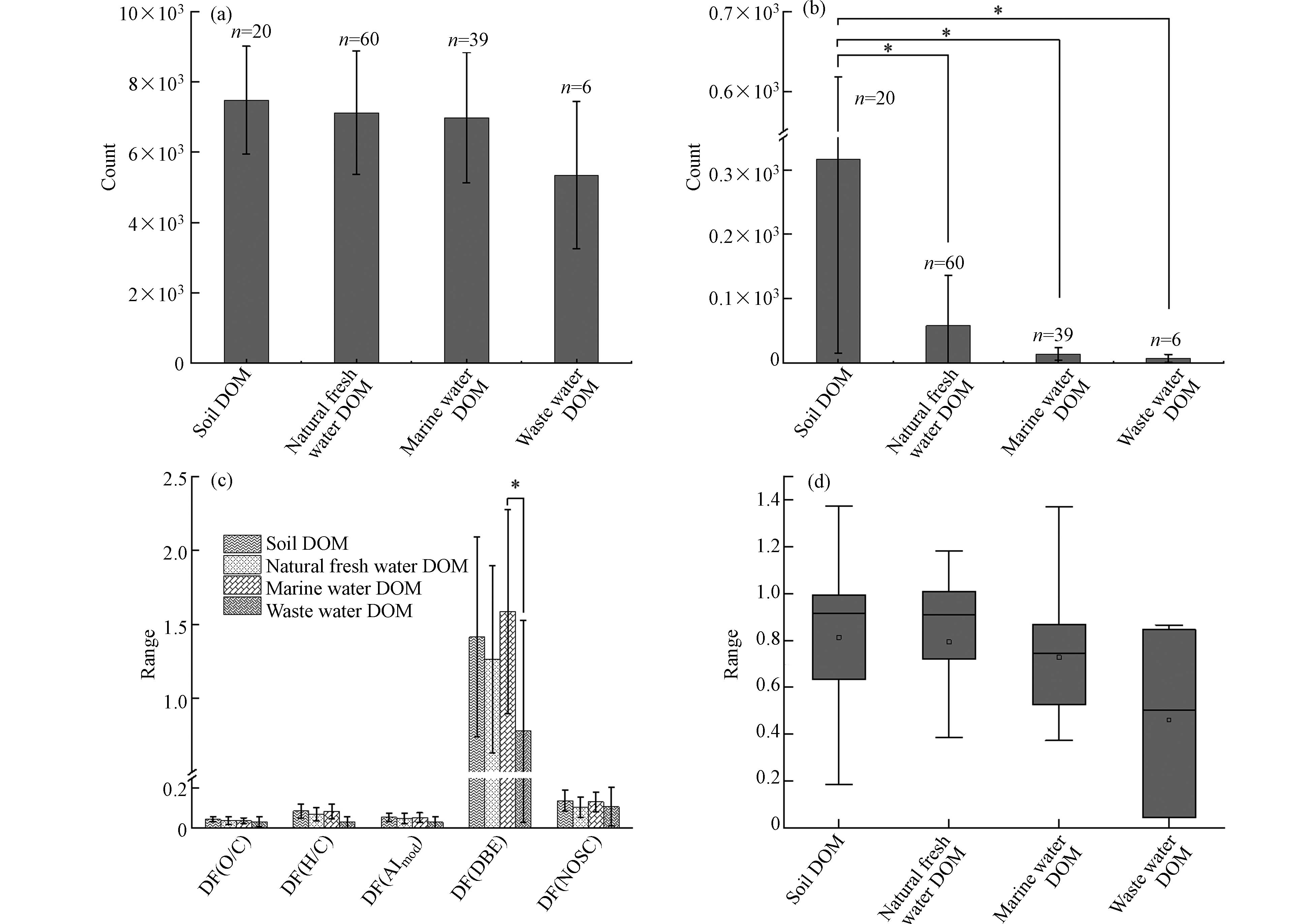
对4类样品(土壤、自然淡水、海水和废水)进行显著性分析(ANOVA,P<0.05)可知(图7a和图7b),单电荷DOM分子的数量在不同类型样品之间没有显著性差异. 相反,双电荷DOM分子的数量在不同类型样品之间存在显著性差异,土壤双电荷DOM分子与海水、自然淡水和废水双电荷DOM分子之间存在显著性差异(P<0.05). 以上结果表明双电荷DOM分子的数量在不同类型样品中存在显著性差异,土壤DOM中的双电荷离子更丰富.
根据分子式中O/C和H/C值,可将DOM分子的van Krevelen图划分为7类[13],4类样品的双电荷DOM分子的van Krevelen分类结果如表1所示. 可以看到,所有样品均以丰富的木质素为主,其中在土壤、自然淡水、海水和废水的双电荷DOM中分别占比76.71%、79.00%、88.15%和85.36%. 此外丹宁在四类样品中也有少量占比,分别为4.91%、11.04%和3.33%和7.32%. 这表明与大多数DOM的来源相似,不同类型的双电荷DOM分子可能来自植物源[39].
进一步结合四类样品不同性质参数的DF值来看(图7c),DF(O/C)、DF(H/C)、DF(AImod)和DF(NOSC)值在四类样品中均无显著性差异. 土壤、自然淡水和海水DOM中双电荷的DF(DBE)值与废水DOM存在显著性差异(P<0.05),废水双电荷DOM的DBE值更低,这可能与废水属于难降解的稳定化合物有关[40]. 从范围来看,四类样品的DF(O/C)值相差不大,这与图6a所述的双电荷DOM分子的高O/C值一致. 海水双电荷DOM有着更高的DF(DBE)和DF(NOSC)值,这说明海水DOM在生物地球化学反应中有更高的活性[37]. 从DF(H/C)和DF(AImod)可知,相比废水双电荷DOM分子,土壤、自然淡水和海水双电荷DOM的H/C和AImod值均更高,表明它们的生物可利用度更高[40]且有着更高的芳香程度. 综合分子式中所有性质参数的期望值来看(图7d),土壤双电荷DOM分子的综合功能多样性指数均值更高,其次是自然淡水、海水和废水双电荷DOM分子. 自然淡水和海水双电荷DOM分子的综合功能多样性指数分布更集中,而土壤和废水双电荷DOM分子则更分散,这可能与不同地区的土壤DOM分子性质相差较大以及不同来源的废水有关. 以上结果表明不同类型样品的双电荷DOM分子的多样性指数受到样品类型的影响,土壤双电荷DOM分子具有更高的芳香程度和不饱和度.
-
根据“1.3”节前体筛选规则可知:[M-H]−型分子和[M-2H]2−型分子最终匹配的分子式是相同的,因此对于分子式匹配而言,存在前体单电荷DOM分子的双电荷DOM分子的UHR-MS数据可以不考虑,并且不存在前体单电荷DOM分子的双电荷DOM分子的数量较少(约占单、双电荷离子总数的15.98%). 此外,由5类样品中单、双电荷DOM分子的元素组成上可知,如表2所示. 结果显示,单电荷DOM分子包含的8类化合物中以丰富的CHO类化合物为主(51.98%),其次为CHON类化合物(18.72%)和CHOS类化合物(12.25%). 而双电荷DOM分子仅包含4类化合物,其中CHO类化合物最为丰富(1.07%),其次为CHON类化合物(0.06%)、CHOS类化合物(0.02%)和CHOP类化合物(0.01%). 以上结果表明:相比双电荷DOM分子,单电荷DOM分子在元素组成和化合物类别上更复杂,在数量上也更多. 在FT-ICR MS谱图上成千上万个离子峰中,单电荷离子峰是主要的离子峰,而在双电荷离子中不存在单电荷离子前体的少之又少,其对谱图中成千上万个离子峰而言微不足道. 因此,在分子式匹配过程中,往往可以默认为只考虑单电荷离子而忽略双电荷离子,双电荷离子对质谱数据分析的影响十分有限.
-
本研究首次提出了单电荷离子前体确认双电荷离子的方法,该方法相比传统13C同位素方法能够有效提高DOM的FT-ICR MS谱图中双电荷离子峰的识别,双电荷离子比例提高44.90%. 同时该方法能确认不存在13C112Cn−1峰的12Cn峰是否为双电荷离子峰以及含N双电荷离子. 从单、双电荷离子的角度来看,相比单电荷离子,双电荷离子通常具有更高的O/C、DBE、AImod和NOSC值以及更低的H/C值,表明大部分双电荷DOM是富羧基的脂环分子,它们有着更高的芳香性、不饱和度和氧化态. 从样品类型的角度来看,不同类型的样品中双电荷DOM分子数量显著不同,土壤DOM样品中的双电荷离子数量更丰富. 进一步,结合功能多样性指数来看,土壤双电荷DOM分子的综合多样性指数最高,说明其具有更高的芳香程度和不饱和度,这与样品的类型以及样品来源有关.
此外,鉴于大多数双电荷离子存在单电荷离子前体以及质谱图中成千上万个单电荷离子峰,在不同类型DOM的分子式匹配过程中,往往可以默认为单电荷离子而忽略双电荷离子,双电荷离子对质谱数据分析的影响相对有限. 该方法为解析质谱图仅考虑单电荷离子提供了依据,同时也为UHR-MS数据分析提供了一个全新的视角.
基于超高分辨率质谱技术的溶解性有机质双电荷离子研究
Elucidation of doubly charged ions in DOM by ultrahigh-resolution mass spectrometry
-
摘要: 溶解性有机质(DOM)是各类环境介质中广泛存在的有机混合物,参与了表生地球系统的诸多生物地球化学和环境化学过程. DOM的傅里叶变换离子回旋共振质谱(FT-ICR MS)谱图仅考虑单电荷离子峰,但对双电荷离子峰的研究十分有限. 本研究结合FT-ICR MS技术,提出基于单电荷离子前体的双电荷离子筛选方法,并将其应用于各类环境介质中DOM的FT-ICR MS谱图中多电荷离子的化学多样性分析. 结果表明,相比传统仅考虑13C同位素峰的方法,基于单电荷离子前体的双电荷离子方法能够有效提高DOM的FT-ICR MS谱图中双电荷离子峰的识别(提高44.90%). 相比单电荷离子,双电荷离子拥有更高的O/C、DBE(最小双键当量)、AImod(修正芳香性指数)和NOSC(碳的名义氧化态)值以及更低的H/C值,表明大部分双电荷DOM是富羧基的脂环分子. 同时,双电荷离子的数量与样品类型有关,土壤DOM中的双电荷离子数量更高. 具体来说,各类样品中双电荷离子的数量和占比如下:海洋水DOM(540,0.18%)、天然淡水DOM(
3486 ,0.81%)、土壤DOM(6334 ,4.06%)和废水DOM(41,0.13%). 这表明单电荷离子峰是各类环境介质DOM的FT-ICR MS谱图中的主要离子峰. 本研究为DOM的化学多样性研究提供了一种新的数据分析方法,首次系统性地揭示了不同类型DOM中多荷离子的性质,并证实了双电荷离子对不同类型DOM的超高分辨质谱(UHR-MS)数据分析的影响相对有限.-
关键词:
- 双电荷离子 /
- 傅里叶变换离子回旋共振质谱 /
- 天然有机质 /
- 前体离子.
Abstract: Dissolved organic matter(DOM)is a heterogeneous organic mixture ubiquitous in various environmental media, participating in many biogeochemistry and environmental chemical processes in the supergene earth system. Despite the extensive occurrence of single-charged ion peaks in the mass spectra of DOM by Fourier transform ion cyclotron resonance mass spectrometry (FT-ICR MS), information regarding their double-charged ion peaks is very limited. In this study, a doubly charged ions algorithm based on their singly charged precursors was developed to characterize the chemodiversity of multiply charged ions in the FT-ICR MS spectra of DOM in various environmental media. Results showed that compared with the traditional method only considering 13C isotopic peaks, the doubly charged ions method based on singly charged precursors could effectively improve 44.90% number of doubly charged ion peaks in the FT-ICR MS spectra of DOM. The doubly charged ions had higher values of O/C, minimum double-bond equivalence (DBE), modified aromaticity index (AImod), nominal oxidation state of carbon (NOSC) and lower values of H/C than those for singly charged ions, indicating that most of the doubly charged DOM were carboxyl-rich alicyclic molecules. Moreover, the number of doubly charged ions was dependent on sample type. Soil DOM was most abundant in the doubly charged ions. The number and percentage of doubly charged ions in various samples were in the order of: marine DOM (540, 0.18%), natural fresh water DOM (3486 , 0.81%), soil DOM (6334 , 4.06%) and waste water DOM (41, 0.13%). These results suggested that the singly charged ion peaks were dominant in the FT-ICR MS spectra of DOM for various environmental matrices. In addition to providing a novel data analysis method for FT-ICR MS data analysis, for the first time, this study reveals the properties of multiply charged ions in different types of DOM and confirms the neglectable effect of doubly charged ions on ultrahigh-resolution mass spectrometry data analysis for different types of DOM.-
Key words:
- doubly charged ions /
- FT-ICR MS /
- natural organic matter /
- precursor ions.
-
矿山开发过程中会产生大量的固体废弃矿物,在自然环境中风化和微生物的氧化过程中伴随着有毒有害元素的释放,并逐渐形成了高硫酸根、高铁浓度的极端酸性矿山废水 (acid mine drainage,AMD) ,造成了矿区附近流域水体及土壤重金属的污染,严重威胁矿区生态系统安全及人群健康[1-4]。因此,AMD所引起的环境污染已成为国内外研究热点。
以广东省韶关市大宝山金属硫化物矿区为例,ZHUANG等[5]发现,受矿区酸性废水的长期影响,大宝山矿区附近土壤的pH多低于5,土壤中铜、铅、锌和镉的平均质量分数分别为502 mg·kg−1、278 mg·kg−1、498 mg·kg−1和3.92 mg·kg−1,远超过国家标准 (GB15618-2018) 限值。而AMD表层沉积物中的重 (类) 金属,如Pb、As和Cr的质量分数高达3 100、1 896和170 mg·kg−1[6-7]。据沉积物矿物学特征调查可知,AMD污染的流域中易形成大量特征性的含铁羟基硫酸盐次生矿物[8-10]。例如,当pH为2.8~4.5时,AMD环境中的三价铁和硫酸根离子共沉淀形成典型的施氏矿物 (schwertmannite) ;当体系中存在一价阳离子且pH为1.5~3时,易形成以黄铁矾类为主的矿物;当pH>5时,Fe3+水解产生的矿物主要为水铁矿[11-12]。由于类质同象作用,这些含铁羟基硫酸盐次生矿物容易吸持AMD中的重 (类) 金属离子,使其演变成为重 (类) 金属离子的沉淀库。同时,含铁硫酸盐次生矿物容易在环境因子 (pH、还原性物质、溶解性有机质 (dissolved organic matter,DOM) 和共存离子浓度等) 改变时,发生溶解重结晶,使其吸附和共沉淀的重 (类) 金属再次释放到相应的水体流域中,造成二次生态风险[13-16]。然而,目前关于大宝山矿区环境中重金属环境风险的研究主要针对矿区土壤中重金属的迁移。
在AMD环境中,可溶性S(-II)可由硫酸盐还原菌还原硫酸根产生,并通过还原、沉淀和络合等途径对矿区中重 (类) 金属的迁移转化起制约作用[17]。例如,在厌氧环境下,S(-II)可还原溶解铁 (氢) 氧化物等矿物且自身形态发生改变,亦引起了所吸持的重 (类) 金属再次释放[18-20]。然而,关于可溶性S(-II)与矿区沉积物中次生矿物的稳定性及重 (类) 金属的迁移转化动态关系的报道还甚少。
基于此,本研究围绕大宝山矿区拦泥库沉积物,采用流动柱进行模拟淋溶实验,模拟还原大宝山矿区拦泥库沉积物中的重 (类) 金属在还原性S(-II)介导下的垂直迁移特征,以探究S(-II)对拦泥库沉积物次生矿物的稳定性影响与重金属环境行为的关系,以期为金属硫化物矿区的环境修复与污染防治提供参考。
1. 材料与方法
1.1 实验主要试剂
主要试剂或药品:硫化钠 (Na2S,GR) 购自上海阿拉丁生化科技有限公司,硝酸 (HNO3,AR) 和氢氧化钠 (NaOH,AR) 购买于西陇科学股份有限公司;重 (类) 金属标准溶液购自于国家有色金属及电子材料分析测试中心,以5%的硝酸定容;实验用水为去离子水。
1.2 沉积物样品的采集与预处理
沉积物样品于2018年8月采集于大宝山矿区拦泥库 (经度:113°43′4.75″E,纬度:24°31′27.57″N) ,沉积物样品采集的深度为10 cm,沉积物样品呈现赭黄色。重金属质量分数分别为Pb 2 450 mg kg−1,Zn 1 009 mg kg−1,Mn 1 211 mg kg−1,Cu 680 mg kg−1,Cr 95 mg kg−1,Cd 16 mg kg−1,Mo 68 mg kg−1,以及As 760 mg kg−1。经采集的样品于干燥后压碎并混匀研磨过100目筛后进行密封保存,供沉积物流动柱实验和样品表征。
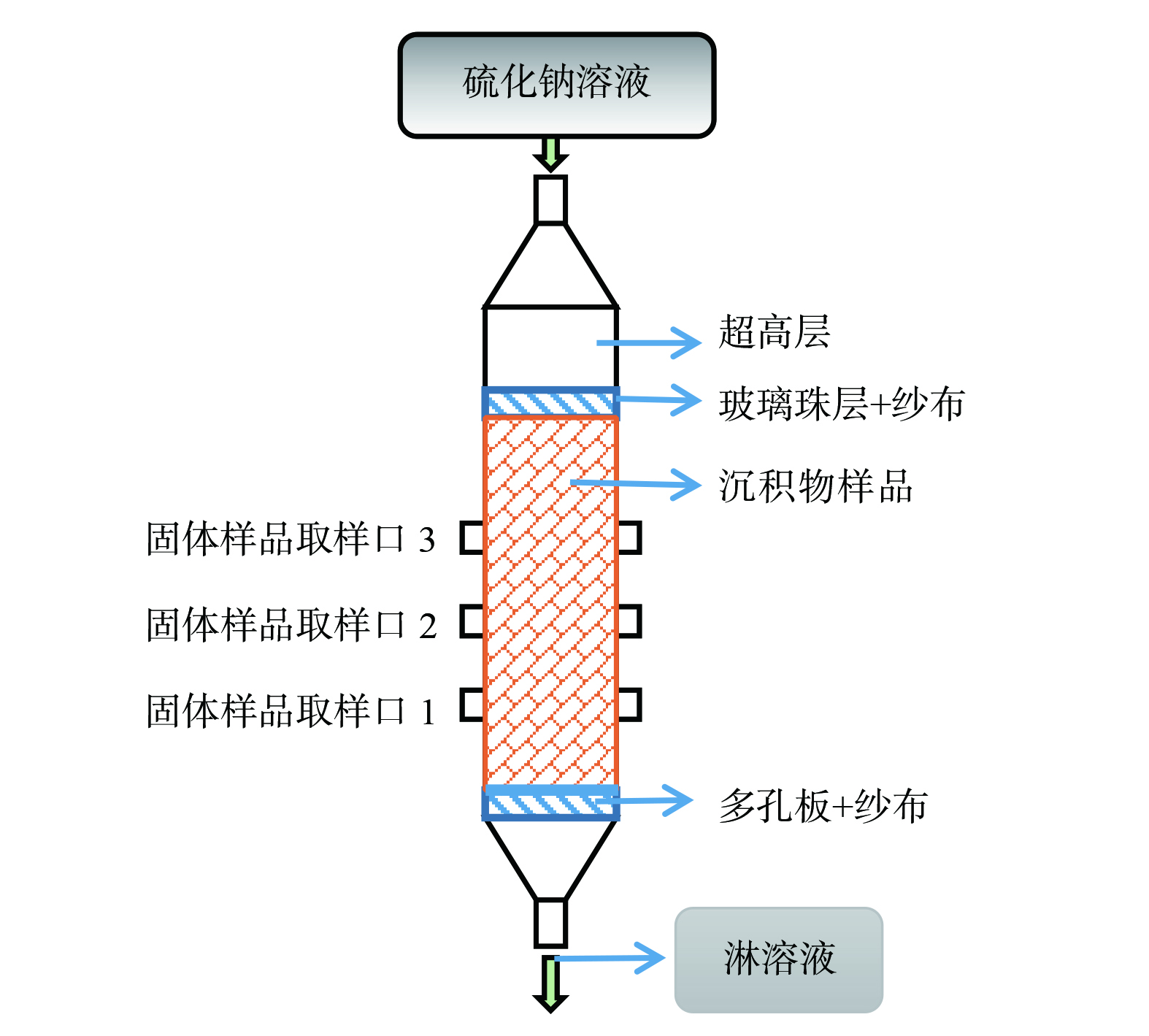
1.3 沉积物柱实验模拟研究实验及装置
实验装置如图1所示。淋滤柱体由有机玻璃制作而成,其内径为50 mm,高度为200 mm,在两侧各有3个直径10 mm的取样孔,其间距均为20 mm。在柱体底部放置一张滤网,然后平铺一层粒径为2 mm的石英砂。将粉末状样品填入柱体中,填充高度约为15 cm,轻微震荡后依靠重力使样品压实。在样品顶层放置一张滤网,并平铺一层粒径为2 mm的石英砂,避免水力作用对样品产生冲刷,模拟自然条件下的重力渗透过程。组装其他部件,将柱体固定在铁架上。所填沉积物样品的质量约为258.61 g。先向柱体通入初始pH为2.5的模拟AMD溶液以充分润湿沉积物并使孔隙饱和。其中,AMD溶液中各类重 (类) 金属的质量浓度分别约为SO42− 540.000 mg·L−1、Zn2+ 101.290 mg·L−1、Cu2+ 3.355 mg·L−1、AsO42− 0.024 mg·L−1、Cd2+ 0.170 mg·L−1、Pb2+ 0.349 mg·L−1、CrO42− 0.022 mg·L−1、MoO42− 0.011 mg·L−1及Mn2+ 80.620 mg·L−1。然后,每隔24 h分别添加30 mL质量浓度分别为10 mg·L−1和100 mg·L−1的Na2S溶液进行淋滤,空白对照组为去离子水。每日收集淋出液,约30 mL。实验周期为31 d。
1.4 样品收集及测定
液体样品用一次性取样针进行采集。经0.45 μm的水系滤膜过滤后,用pH计 (上海雷磁,PHS-3C) 测定样品pH,随后滴加1滴5%硝酸进行酸化,置于4 ℃下保存。使用电感耦合等离子体发射光谱仪 (ICP,日本岛津) 测定溶液中重金属离子浓度,并使用Origin 2018软件进行绘图。ICP测定过程中通过标准样品的回收率 (< 5%) 进行质量控制。
当淋溶实验结束后,在柱体3个取样口的沉积物分别混合均匀后各取约2 g沉积物样品。另取2 g未进行淋溶实验的沉积物样品作为对照,烘干后用聚乙烯离心管密封保存。使用X射线衍射仪 (XRD,德国布鲁克,D8 Advance) 分析样品的晶型结构。X射线为Cu靶Kα射线 (λ= 0.154 18 nm) ,管电压和管电流分别为40 V和40 mA,扫描区域为10°~80°,扫描速度为10°·min−1。利用场发射扫描电镜 (SEM,FEI Nova Nano SEM 450) 检测反应前后的固体颗粒样品的形貌。同时,采用0.2 mol·L−1草酸铵 (pH=3) 对固体样品进行避光萃取4 h,以验证重金属在还原态矿物相中的相对含量。
2. 结果与讨论
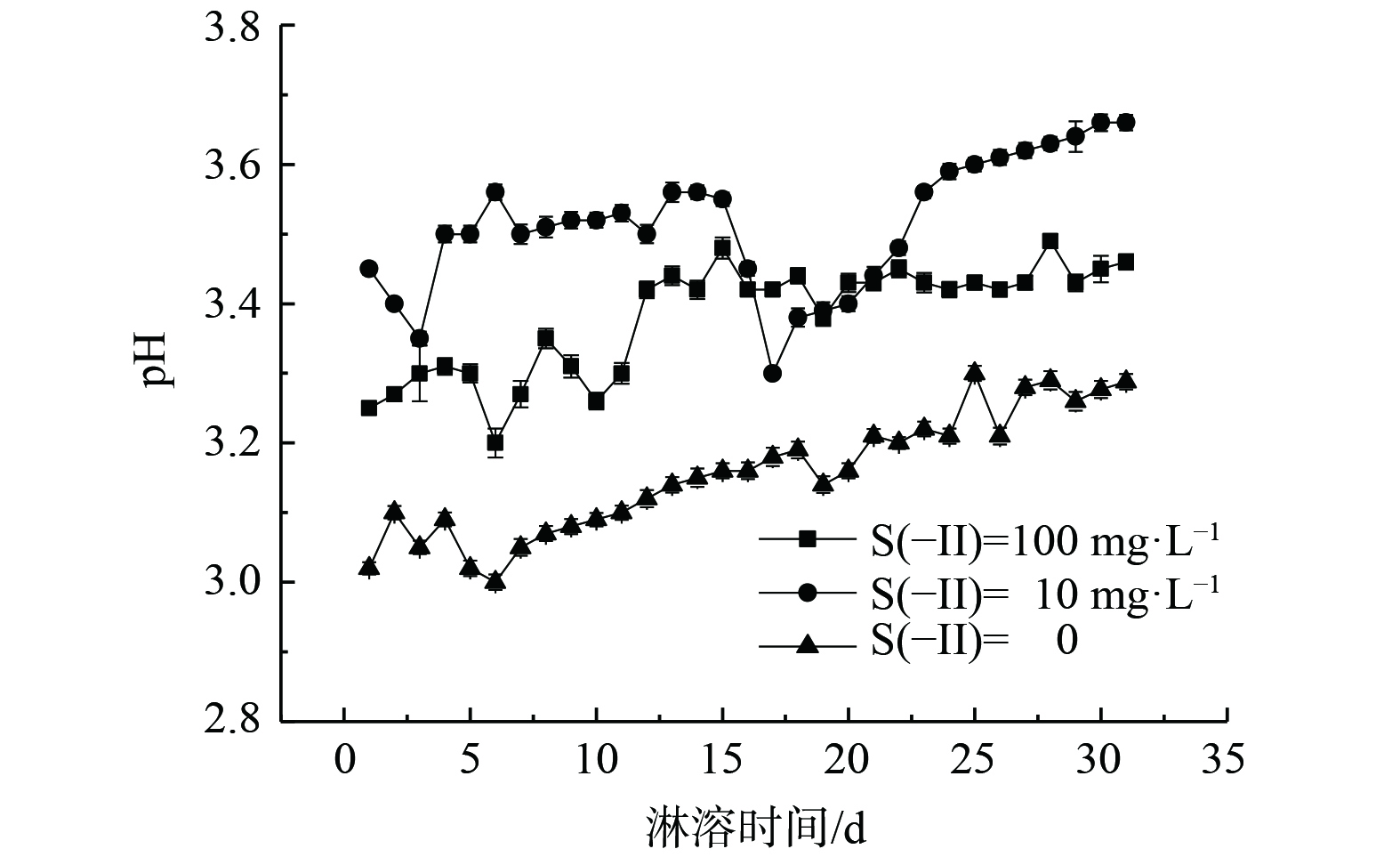
2.1 淋滤液pH的变化规律
如图2所示,在整个淋滤实验过程中,各组淋出液pH总体略呈上升趋势。其中,空白对照组的pH从最低3.00增至最高3.30,增幅最大,在7~18 d时,表现出稳步上升,前期和后期均出现一定波动。可见在没有S(-II)影响下,沉积物中的淋滤液pH呈现酸性且略为上升。质量浓度为10 mg·L−1的Na2S处理组pH从初始3.45增至最终的3.68,而质量浓度为100 mg·L−1 Na2S处理组的pH从最低3.20增至最高3.49。Na2S溶液呈碱性,沉积物本身为强酸性 (pH约为2.55) ,然而在通过沉积物淋溶后的淋溶液却呈现酸性,且质量浓度较高的S(-II)反而总体pH较低。原因可能是由于碱性溶液通过沉积物而使得沉积物中介稳定的矿物如施氏矿物溶解[6] (如式 (1) ) ,部分重金属和硫酸根的释放溶出,引起H+释放,从而使pH降低。然而,整个实验过程中3个实验组的pH变化较小,呈现酸性,其有利于重金属从结构态转变为游离态[21]并促进其迁移能力。
stringUtils.convertMath(!{formula.content}) (1) 2.2 淋滤液中重金属含量的变化
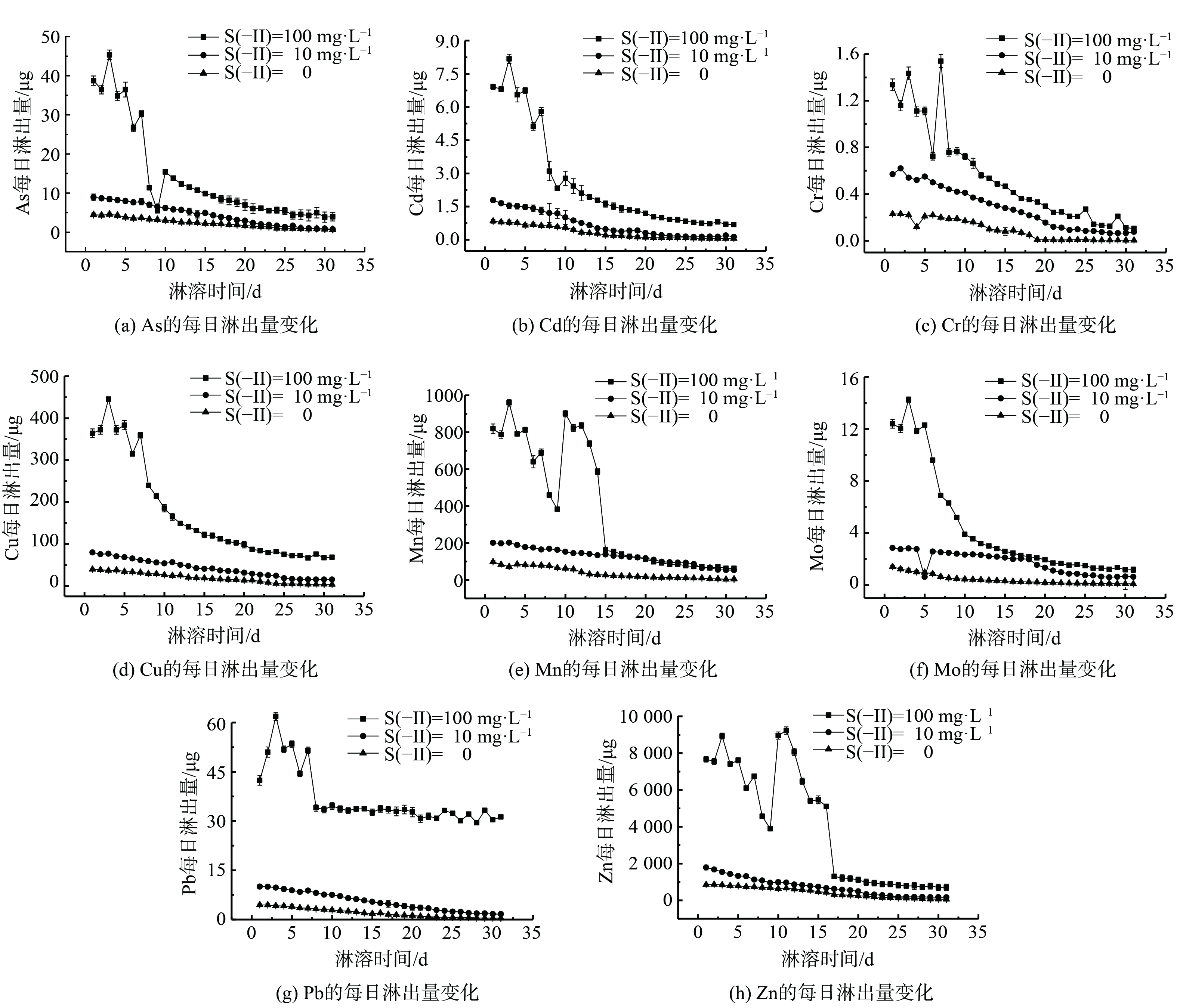
重金属每日淋出量随淋溶时间的变化趋势如图3所示。在本实验条件下,S(-II)的淋溶对于沉积物中重金属的释放有相对的促进作用。质量浓度为10 mg·L−1 Na2S处理组第1天的淋滤液中重 (类) 金属As、Cd、Cr、Cu、Mn、Mo、Pb和Zn的淋出量分别比空白高了约1.993、2.131、2.478、2.027、2.051、2.028、2.247、和2.095倍,且随着硫离子质量浓度的增加,重金属的释放量增加。
8种重金属元素的释放规律类似。1~3 d为重金属快速释放时期,各元素每日淋出量较高,且出现了一定的上升。但在此后5~10 d,各元素淋出量迅速下降。如Mo的每日淋出量从12.29 μg降至3.91 μg,降幅最大,为68.20 %。在10 d之后,各元素淋出量开始缓慢而稳定地下降,各元素的最终淋出量均小于2.09 μg·L−1。其中,Pb元素的变化趋势略有不同,每日淋出量虽在1~3 d时出现上升后下降,但其淋出量在8 d时便降至平稳阶段,其降幅相比As、Cu、Cr、Cd和Mo较小,此后一直稳定在约33.50 μg。从整体上看,Pb的每日淋出量从最高值61.88 μg降至最低值29.48 μg,变化幅度较小,但持续淋出量较高。这可能是由于拦泥库沉积物中Pb的质量分数最高 (2 450 mg·kg−1) ,这与文献[22]报道的结果一致。
Cu、Mn、Zn与Cd等其他元素在1~5 d时,同样呈现出先增长后回落的形势。Cu在7 d后稳步平滑下降。而Mn、Zn同时在第9天出现大幅异常增长后呈阶梯快速下降,最后分别于15 d和17 d转为平滑下降。从总体上看,Cu、Mn和Zn初始淋出量较高,分别为364.00、819.00 和7 670.00 μg,且Zn淋出量较Cu和Mn高出1个数量级。大宝山矿床主体为钼矿、褐铁矿、铜硫矿和铅锌矿等多金属共生或伴生矿体[23],矿区长期采矿和洗矿过程中产生的大量重金属污染,且研究区域的沉积物中重金属含量顺序为Zn>Mn>Cu>Cd。其中,Cd和As在9~11 d出现每日淋出量的大幅度快速增长。这表明各元素间可能具有一定的相互促进或抑制迁移作用。除了与沉积物中重金属的存在形态有关之外,也与淋滤液中硫离子的作用有关。研究表明,S2−离子的还原性会影响沉积物中矿物的稳定性,进而影响被沉积物固定的重金属,影响重金属的二次释放[24-26]。此外,S2−又会与重金属反应结合,生成较为稳定不易迁移的硫化物等沉淀[18, 27]。因此,S2−在整个淋滤过程中表现出前期促进而后期缓解抑制的作用。但Cu、Mn、Zn在淋滤过程中每日淋出量下降较快,或受到S2−的抑制作用。各重金属的淋溶特点均表明沉积物对环境造成的污染具有持续性特点,对于生态环境具有潜在影响[28]。
2.3 沉积物中重金属的释放动力学
沉积物中重金属的迁移过程受到水分、温度、氧化还原电位等多重因素的影响,是一个多因素相互作用的动态变化反应过程。为进一步研究这一过程,借助化学动力学和数学模型进行分析,通过拟合S(-II)介导下的实验结果以了解重金属迁移过程中的影响因素和各类重金属的迁移特点[29]。通过文献调研选取了一级动力学方程、双常数方程和Elovich方程 (式 (2)~(5) ) 。其中,Elovich方程是一个经验式,其主要描述一系列反应机制的过程,如溶质的本体、界面扩散、表面的活化与去活化作用等[30],其对重金属在土壤或沉积物界面上的迁移过程较为适用。而反应条件和反应过程较复杂的化学动力学过程则适合用双常数方程进行描述。其中,各类重金属累积释放量曲线如图4所示,拟合分析结果如表1所示。
表 1 各重金属元素拟合结果Table 1. Fitting results of each heavy metal elements重 (类) 金属元素种类 决定系数R2 一级动力学方程 双常数方程 Elovich方程 低浓度 高浓度 低浓度 高浓度 低浓度 高浓度 As 0.915 6 0.875 9 0.968 4 0.968 4 0.713 3 0.991 9 Cd 0.854 3 0.852 5 0.948 9 0.957 0 0.977 2 0.991 7 Cr 0.906 1 0.892 7 0.967 2 0.967 2 0.965 1 0.977 4 Cu 0.950 0 0.905 1 0.985 4 0.974 9 0.948 7 0.982 4 Mn 0.978 4 0.840 4 0.994 1 0.927 4 0.920 1 0.954 5 Mo 0.959 1 0.842 3 0.981 3 0.953 7 0.921 2 0.992 7 Pb 0.941 7 0.993 5 0.981 5 0.999 1 0.952 5 0.898 3 Zn 0.911 3 0.864 8 0.972 6 0.934 8 0.966 7 0.946 7 淋出液中重金属累积释放量的计算公式见式 (2) ,其一级动力学方程为式 (3) ,双常数方程为式 (4) ,Elovich方程为式 (5) 。
stringUtils.convertMath(!{formula.content}) (2) stringUtils.convertMath(!{formula.content}) (3) stringUtils.convertMath(!{formula.content}) (4) stringUtils.convertMath(!{formula.content}) (5) 式中:q为沉积物样品中重金属的累积释放量,μg·kg−1;t为淋溶时间,d;a, b为常数;
Ci为第i次采样的淋溶液中重金属浓度,μg·L−1;V为第i次采样的淋溶液体积,L;m为沉积物样品质量,kg。
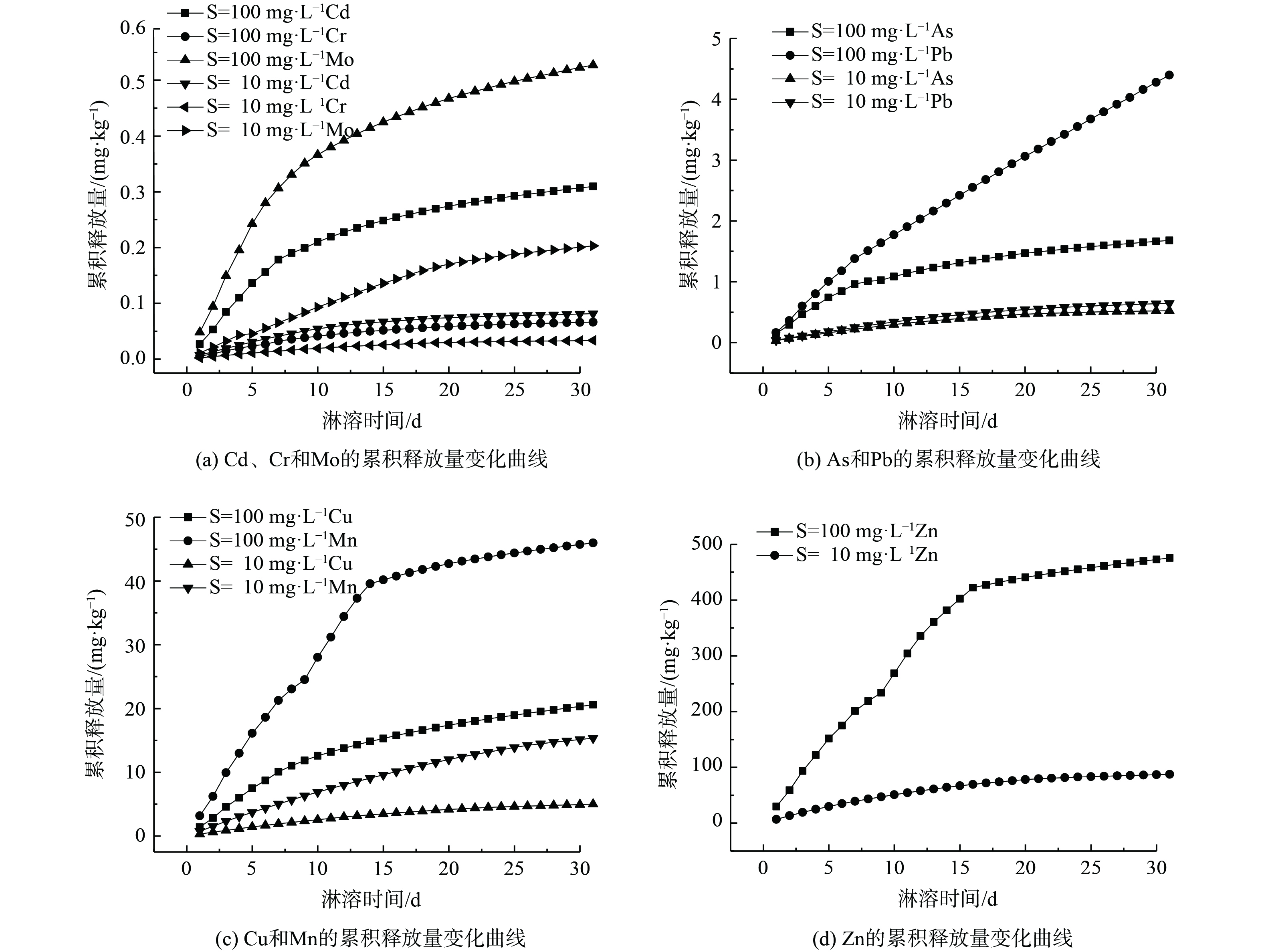
如图4所示,高浓度处理组中Cd、Mo、As和Cu的累积释放量在1~8 d增长较快,在9 d之后的增长趋于平缓;Pb的增长则呈现斜直线;Mn和Zn在1~14 d快速增长,在14 d后趋于平缓,Pb、Mn和Zn大致呈线性增长。而Cr的增长幅度不大,趋势不明显。而对于低浓度处理组,除Mn,Cd、Mo、Cr、Zn、Cu、As和Pb的累积释放量在20 d后趋于缓和,相比于高浓度处理组,累积释放量均在一定程度上下降了。
由表1拟合结果可知,对于一级动力学方程,在高浓度处理组中除Pb和Cu外,其他重金属的决定系数在0.85~0.90。这表明一级动力学对多数重金属元素拟合效果较为一般。一级动力学方程能体现出反应物浓度与反应速率之间的线性关系。这说明重金属在沉积物中吸附和分布并不是理想中的均匀状态,各吸附点位对于重金属的亲和力并不相等。但从个体来看,一级动力学方程对于Pb的拟合效果较好。而在低浓度处理组中,除了Cd,其他的决定系数都高于0.90。对于双常数方程而言,所有重金属决定系数均大于0.90。这表明双常数方程对于多数重金属拟合效果较好,且低浓度处理组的决定系数均高于0.94。其中,Pb的决定系数分别为0.98和0.99,这表明Pb的释放过程适合用双常数方程进行描述。对于Elovich方程而言,高浓度处理组中除Pb外,其余重金属决定系数均在0.95以上。这说明该方程具有较好的拟合效果。而在低浓度处理组中除As外,其余重金属决定系数均在0.92以上。这表明Elovich方程的拟合效果比双常数方程更好。
上述分析表明,低浓度处理组中所有重金属的双常数方程拟合度最优。而高浓度处理组中双常数方程能较好地描述Pb的迁移过程,这表明Pb在沉积物颗粒中的吸附和分布可能相对较为均匀,亦可能受到的影响因素较为单一。其他重金属As、Cd、Cr、Cu、Mn、Mo和Zn的Elovich方程拟合度最优。这表明多数重金属在沉积物中的吸附和解吸过程受到多种因素的制约和影响[31],如DOM、还原性物质、共存离子和pH等。
2.4 固体样品的分析
2.4.1 对重金属的萃取
通过对高浓度S(-II)处理组反应前后沉积物中水溶态、吸附和可交换态及易还原矿物相中重金属的萃取结果可知,被淋滤下来的重金属主要来源于沉积物中的水溶态、吸附和可交换态及易还原矿物相。其中,Zn和Mn的释放量为8种重金属中最高(见表2)。这可能是Zn和Mn在实验所测的8种重金属中含量较高,且其金属硫化物溶解度相对较高。此外,Zn所累积的释放量高于反应前水溶态、吸附和可交换态,以及易还原矿物相中Zn的含量。这说明淋滤的部分Zn来源较为稳定的矿物相。此外,Cd、Mo和Cr的累积释放量较低,源于其在沉积物中相对含量较低。而Pb和As在沉积物中的相对含量较高,但是被淋滤所累积的释放量却相反。这可能是由于Pb和As的硫化物溶解度较低,在一定程度上抑制了Pb和As的释放。因此,在AMD体系中,重金属的迁移转化受控于还原性物质等环境因子。
表 2 重金属萃取前后的对比Table 2. Comparison of heavy metals before and after extraction重金属种类 累积释放量/ (mg·kg−1) 重金属的质量分数/ (mg·kg−1) 反应前 反应后 Pb 4.40 544.55 540.20 Zn 475.53 268.43 23.49 Mn 45.97 215.12 206.15 Cu 20.60 174.40 153.70 Cr 0.07 45.32 45.26 Cd 0.31 3.93 3.64 Mo 0.53 44.01 43.52 As 1.68 540.11 538.58 注:反应前后重金属质量分数数据为水溶性、吸附和可交换态及易还原矿物相中重金属之和。 2.4.2 XRD表征
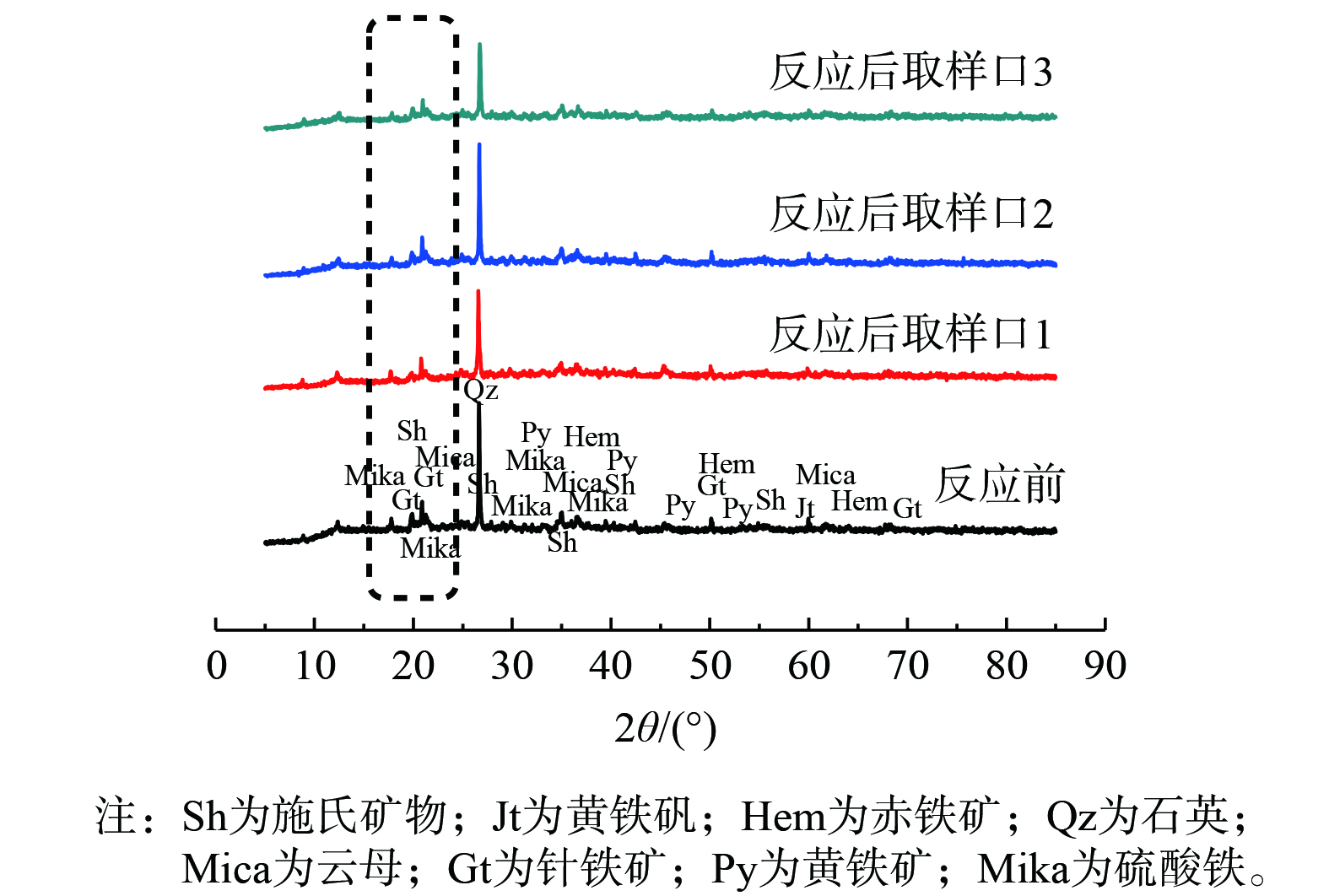
为进一步确定重金属的来源,采用了XRD对质量浓度为100 mg·L−1 Na2S处理组反应前后矿物组成进行分析,结果如图5所示。沉积物中主要矿物成分为:施氏矿物、黄铁矾、赤铁矿、石英、云母、针铁矿、黄铁矿、硫酸铁等含铁 (硫) 矿物及一些重金属与矿物形成的复合体。图5可观察到反应前后相对的区别,在峰位约20°可看到峰型的相对改变,即反应前峰型较宽,衍射强度更大,反应后衍射强度减弱,且在采样口3的位置处,无定型的矿物峰减弱最多。分析其原因,可能是S(-II)最先接触采样口3的沉积物,故采样口3的位置接触到的硫离子浓度最高。随着深度的增加,介稳定性矿物受淋溶液的影响较小,此时接触的硫离子质量浓度也低、厌氧程度加大,故出现了硫酸亚铁的峰位。因此,XRD结果表明沉积物中介稳定的矿物相对含量的变化,即淋溶液中重金属可能主要来源于沉积物中可还原态的矿物,如介稳定的施氏矿物和黄铁矾类矿物,淋溶后剩下了较为稳定的矿物相如针铁矿等。
2.4.3 SEM表征
采用SEM观察高浓度S(-II)处理组反应前后沉积物表观形貌,结果如图6所示。未淋溶前沉积物样品 (图6(a)) 表面相对较为光滑完整,且附着有页状形貌矿物。经过硫化钠溶液淋滤之后,柱体上层的沉积物 (图6(b)) 表面呈现附着有较多叠加的薄片状和少数杆状形貌的物质。柱体中层的沉积物 (图6(c)) ,颗粒表面较为粗糙,附着较小的片状、球状和少数米粒状的矿物。而柱体底层的沉积物 (图6(d)) 样品显示其表面附着的细小片状、针状矿物增多。这些片状、球状、针状的物质可能对应为施氏矿物、黄铁矾、赤铁矿、针铁矿等[32]。这表明在硫化钠溶液的淋溶作用下的沉积物中,从柱体上层至下层呈现不同的形貌变化,结合重金属萃取和XRD结果可知,沉积物中垂直迁移的重金属主要来源于沉积物相中可还原的矿物相,其迁移过程表现为“迁移—稳定”的模式[33]。
2.5 沉积物中重金属的可能释放机理
可溶性的二价硫离子具有还原、络合和沉淀重金属的作用,因此,在一定程度上制约着酸性矿山废水中重金属的迁移转化。本研究中的沉积物样品采集于大宝山拦泥库,含有的羟基含铁硫酸盐次生矿物质量分数约为24% [6],在环境因子pH改变和还原性物质存在时会导致矿物溶解重结晶的过程中吸附和共沉淀的重金属再次释放到环境中。在本研究的条件下,S(-II)可能会使环境中原有的铁矿物发生还原溶解,产生的内源二价铁对矿物具有催化作用,能加速含铁矿物的溶解重结晶。如ZHANG等[34]的研究结果,在S(-II)作用下,体系产生Fe(II)引发催化作用下,使得As(V)-施氏矿物会转化为Magnetite等次生矿物;但同时硫离子会与重金属离子形成硫化物沉淀;其次,硫化钠溶液本身呈现碱性,对矿物的溶解有促进作用。在复杂的反应过程中,矿物的溶解占据一定优势,故可观察到前期重金属的释放量相对较大。在反应的后期,由于S(-II)被氧化后或与沉积物中的重金属或Fe形成沉淀或新的矿物,使得被淋出的重金属再次被共沉淀和吸附,导致后期重金属淋出量减少。
2.6 对环境治理的意义
金属硫化物矿区AMD污染流域中的沉积物是矿区有毒有害金属元素的主要汇,且沉积物中存在大量的含铁硫酸盐次生矿物。这些次生矿物处于介稳定的状态,一旦环境条件改变 (还原性物质和共存离子等) 时,很容易发生溶解和相转变,从而引起沉积物中重金属的二次释放和再次分配,存在一定的环境风险。因此,基于以上的研究结果,在进行矿区AMD污染流域环境原位修复治理时,可对沉积物底泥进行清淤或者采用重金属吸附剂或钝化剂进行固定,但应避免选用还原性的吸附剂或钝化剂,并规避因流域pH变化引起固持的重金属存在二次释放的风险。
3. 结论
1) 在S(-II)介导,即在硫化钠溶液的淋滤作用下,大宝山拦泥库沉积物中重金属的垂直迁移特征,即沉积物中各重金属元素释放量的大小顺序为:Zn>Mn>Cu>Pb>As>Mo>Cd>Cr。
2) S(-II)在反应前期对重金属的释放具有较明显的促进作用,且释放的部分重金属主要来源于沉积物中的易还原矿物相,其释放过程可用双常数和Elovich模型进行描述拟合。
3) 在AMD环境下,沉积物中重金属的环境行为与介稳态矿物相的溶解-重结晶有关,存在着释放的潜在生态风险。因此,在AMD污染流域环境修复治理时应注意重金属的再次释放。
-
图 3 A类双电荷13C112Cn−1峰的理论RA值与测量RA值之间的散点图(a),A类12Cn峰的S/N值与13C112Cn−1峰的峰强度偏差的直方图(b)
Figure 3. Scatter plot between theoretical RA value and measured RA value of doubly charged 13C112Cn−1 peak in class A (a),histogram of peak intensity deviation between S/N value of 12Cn peak and 13C112Cn−1 peak in class A (b)n is the sample number of each method. The values and error bars represent average and ±SD, respectively
图 4 待验证的单、双电荷12Cn峰(a),单电荷13C112Cn−1峰预测12Cn峰(b),双电荷13C112Cn−1峰预测12Cn峰(c)和B类峰的峰强度偏差验证(单电荷+双电荷13C112Cn−1峰、单电荷13C112Cn−1峰和双电荷13C112Cn−1峰验证)(d)
Figure 4. The singly and doubly charged 12Cn peak to be verified(a),the singly charged 13C112Cn−1 peak is predicted to be 12Cn peak(b),the doubly charged 13C112Cn−1 peak prediction 12Cn peak(c)and class B peak intensity deviation verification(singly charged + doubly charged 13C112Cn−1 peak,singly charged 13C112Cn−1 peak and doubly charged 13C112Cn−1 peak verification)(d) The significant differences at P < 0.05 are indicated by the star symbol(*)
图 5 在名义m/z 325和651质量窗口处用利用单电荷离子前体确定双电荷离子(a),传统13C同位素确定单(双)电荷离子以及含N双电荷离子示例(b),在名义m/z 324质量窗口利用13C同位素确定的双电荷离子(c)和名义m/z 320和641质量窗口处[13C1C24H20O20]2−无单电荷离子前体(d)
Figure 5. Determination of doubly charged ions by singly charged precursor ions at the nominal m/z 325 and 651 mass windows(a),examples of determining singly(doubly)charged ions with 13C isotopes and containing N doubly charged ions(b),determination of doubly charged ions by 13C isotopes at the nominal m/z 324 mass window(c)and [13C1C24H20O20]2− without precursor singly charged ions at the nominal m/z 320 and 641 mass windows(d)
图 7 不同类型样品中单(a)、双(b)电荷DOM分子数量的显著性,不同类型样品间的功能多样性指数(DF)(c)和综合功能多样性指数分布箱线图(d).
Figure 7. Significance of the number of singly(a)、doubly(b)charged DOM molecules in different types of samples,significance of different functional diversity indices(DF)(c)and distribution box diagram of comprehensive function diversity index(d)
表 1 不同类型样品中双电荷DOM分子的van Krevelen分类结果
Table 1. Results of van Krevelen classification of double-charged DOM molecules in different types of samples
样品类型Sample types 木质素Lignin 丹宁Tannins 稠环芳烃Condensed aromatic 饱和化合物Saturated compounds 氨基糖Aminosugars 不饱和碳氢化合物Unsaturated hydrocarbons 碳氢化合物Carbo-hydrates 占比1)Percentage 总计2)Total 土壤 76.71% 4.91% 16.06% 2.00% 0.25% 0.01% 0.05% 4.06% 155947 自然淡水 79.00% 11.04% 9.75% 0.14% 0.06% 0 0 0.81% 430608 海洋水 88.15% 3.33% 2.30% 2.40% 0.74% 0 0 0.18% 304919 废水 85.36% 7.32% 0 7.32% 0 0 0 0.13% 32080 注:1)代表双电荷离子与离子总数(单电荷离子数目和双电荷离子数目总和)的占比;2)代表离子总数. Note: 1) represents the ratio of doubly charged ions to the total number of ions (the summed number of singly and doubly charged ions); 2) represents the total number of ions. 表 2 不同类型样品中所有单、双电荷离子的元素组成及占比
Table 2. Element composition and proportion of singly and doubly charged ions in different types of samples
离子类型Ion types 化合物类型Type of compound 总计*Total CHO CHON CHOS CHOP CHONS CHONP CHOSP CHONSP 单电荷离子(single charged ions) 51.98% 18.72% 12.25% 3.03% 6.56% 2.83% 1.57% 1.88% 890383 双电荷离子(double charged ions) 1.07% 0.06% 0.02% 0.01% 0 0 0 0 10497 注:*代表离子总数(单电荷离子数目和双电荷离子数目总和). Note: * represents the number of ions (the summed number of singly and doubly charged ions). -
[1] QI Y L, XIE Q R, WANG J J, et al. Deciphering dissolved organic matter by Fourier transform ion cyclotron resonance mass spectrometry (FT-ICR MS): From bulk to fractions and individuals[J]. Carbon Research, 2022, 1(1): 3. doi: 10.1007/s44246-022-00002-8 [2] D'ANDRILLI J, FISCHER S J, ROSARIO-ORTIZ F L. Advancing critical applications of high resolution mass spectrometry for DOM assessments: Re-engaging with mass spectral principles, limitations, and data analysis[J]. Environmental Science & Technology, 2020, 54(19): 11654-11656. [3] McDONOUGH L K, ANDERSEN M S, BEHNKE M I, et al. A new conceptual framework for the transformation of groundwater dissolved organic matter[J]. Nature Communications, 2022, 13: 2153. doi: 10.1038/s41467-022-29711-9 [4] van der WAL A, de BOER W. Dinner in the dark: Illuminating drivers of soil organic matter decomposition[J]. Soil Biology and Biochemistry, 2017, 105: 45-48. doi: 10.1016/j.soilbio.2016.11.006 [5] HAN R X, LV J T, LUO L, et al. Molecular-scale investigation of soil fulvic acid and water-extractable organic matter by high-resolution mass spectrometry and 1H NMR spectroscopy[J]. Environmental Chemistry, 2019, 16(2): 92. doi: 10.1071/EN18124 [6] SMITH D F, PODGORSKI D C, RODGERS R P, et al. 21 tesla FT-ICR mass spectrometer for ultrahigh-resolution analysis of complex organic mixtures[J]. Analytical Chemistry, 2018, 90(3): 2041-2047. doi: 10.1021/acs.analchem.7b04159 [7] TOLIĆ N, LIU Y N, LIYU A, et al. Formularity: Software for automated formula assignment of natural and other organic matter from ultrahigh-resolution mass spectra[J]. Analytical Chemistry, 2017, 89(23): 12659-12665. doi: 10.1021/acs.analchem.7b03318 [8] LEEFMANN T, FRICKENHAUS S, KOCH B P. UltraMassExplorer: A browser-based application for the evaluation of high-resolution mass spectrometric data[J]. Rapid Communications in Mass Spectrometry, 2019, 33(2): 193-202. doi: 10.1002/rcm.8315 [9] KUNENKOV E V, KONONIKHIN A S, PERMINOVA I V, et al. Total mass difference statistics algorithm: A new approach to identification of high-mass building blocks in electrospray ionization Fourier transform ion cyclotron mass spectrometry data of natural organic matter[J]. Analytical Chemistry, 2009, 81(24): 10106-10115. doi: 10.1021/ac901476u [10] SCHUM S K, BROWN L E, MAZZOLENI L R. MFAssignR: Molecular formula assignment software for ultrahigh resolution mass spectrometry analysis of environmental complex mixtures[J]. Environmental Research, 2020, 191: 110114. doi: 10.1016/j.envres.2020.110114 [11] KUJAWINSKI E B, BEHN M D. Automated analysis of electrospray ionization Fourier transform ion cyclotron resonance mass spectra of natural organic matter[J]. Analytical Chemistry, 2006, 78(13): 4363-4373. doi: 10.1021/ac0600306 [12] LI P H, TAO J C, LIN J, et al. Stratification of dissolved organic matter in the upper 2000 m water column at the Mariana Trench[J]. Science of the Total Environment, 2019, 668: 1222-1231. doi: 10.1016/j.scitotenv.2019.03.094 [13] FU Q L, FUJII M, RIEDEL T. Development and comparison of formula assignment algorithms for ultrahigh-resolution mass spectra of natural organic matter[J]. Analytica Chimica Acta, 2020, 1125: 247-257. doi: 10.1016/j.aca.2020.05.048 [14] 曹冬, 耿方兰, 饶子渔, 等. 傅里叶变换离子回旋共振质谱分子表征15N同位素标记羟胺衍生化天然有机质[J]. 环境化学, 2023, 42(4): 1118-1127. doi: 10.7524/j.issn.0254-6108.2022101902 CAO D, GENG F L, RAO Z Y, et al. Molecular characterization of 15N-labelled hydroxylamine-derivatized natural organic matter by FTICR-MS[J]. Environmental Chemistry, 2023, 42(4): 1118-1127 (in Chinese). doi: 10.7524/j.issn.0254-6108.2022101902
[15] STEVENSON F J. Humus chemistry: genesis, composition, reactions[M]. 2nd ed. New York: Wiley, 1994. [16] KIM S, RODGERS R P, MARSHALL A G. Truly “exact” mass: Elemental composition can be determined uniquely from molecular mass measurement at ~0.1 mDa accuracy for molecules up to ~500 Da[J]. International Journal of Mass Spectrometry, 2006, 251(2/3): 260-265. [17] SENKO M W, BEU S C, McLAFFERTY F W. Automated assignment of charge states from resolved isotopic peaks for multiply charged ions[J]. Journal of the American Society for Mass Spectrometry, 1995, 6(1): 52-56. doi: 10.1016/1044-0305(94)00091-D [18] BROWN T L, RICE J A. Effect of experimental parameters on the ESI FT-ICR mass spectrum of fulvic acid[J]. Analytical Chemistry, 2000, 72(2): 384-390. doi: 10.1021/ac9902087 [19] LEENHEER J A, ROSTAD C E, GATES P M, et al. Molecular resolution and fragmentation of fulvic acid by electrospray ionization/multistage tandem mass spectrometry[J]. Analytical Chemistry, 2001, 73(7): 1461-1471. doi: 10.1021/ac0012593 [20] STENSON A C, LANDING W M, MARSHALL A G, et al. Ionization and fragmentation of humic substances in electrospray ionization Fourier transform-ion cyclotron resonance mass spectrometry[J]. Analytical Chemistry, 2002, 74(17): 4397-4409. doi: 10.1021/ac020019f [21] LEENHEER J A, FERRER I, FURLONG E T, et al. Charge characteristics and fragmentation of polycarboxylic acids by electrospray ionization—Multistage tandem mass spectrometry[M]//ACS Symposium Series. Washington, DC: American Chemical Society, 2003: 312-324. [22] KUJAWINSKI E B, HATCHER P G, FREITAS M A. High-resolution Fourier transform ion cyclotron resonance mass spectrometry of humic and fulvic acids: Improvements and comparisons[J]. Analytical Chemistry, 2002, 74(2): 413-419. doi: 10.1021/ac0108313 [23] KUJAWINSKI E B, FREITAS M A, ZANG X, et al. The application of electrospray ionization mass spectrometry (ESI MS) to the structural characterization of natural organic matter[J]. Organic Geochemistry, 2002, 33(3): 171-180. doi: 10.1016/S0146-6380(01)00149-8 [24] NOVOTNY N R, CAPLEY E N, STENSON A C. Fact or artifact: The representativeness of ESI-MS for complex natural organic mixtures[J]. Journal of Mass Spectrometry:JMS, 2014, 49(4): 316-326. doi: 10.1002/jms.3345 [25] D’ANDRILLI J, CHANTON J P, GLASER P H, et al. Characterization of dissolved organic matter in northern peatland soil porewaters by ultra high resolution mass spectrometry[J]. Organic Geochemistry, 2010, 41(8): 791-799. doi: 10.1016/j.orggeochem.2010.05.009 [26] STENSON A C, MARSHALL A G, COOPER W T. Exact masses and chemical formulas of individual Suwannee River fulvic acids from ultrahigh resolution electrospray ionization Fourier transform ion cyclotron resonance mass spectra[J]. Analytical Chemistry, 2003, 75(6): 1275-1284. doi: 10.1021/ac026106p [27] FU Q L, FUJII M, WATANABE A, et al. Formula assignment algorithm for deuterium-labeled ultrahigh-resolution mass spectrometry: Implications of the formation mechanism of halogenated disinfection byproducts[J]. Analytical Chemistry, 2022, 94(3): 1717-1725. doi: 10.1021/acs.analchem.1c04298 [28] ZHANG H F, ZHANG Y H, SHI Q, et al. Study on transformation of natural organic matter in source water during chlorination and its chlorinated products using ultrahigh resolution mass spectrometry[J]. Environmental Science & Technology, 2012, 46(8): 4396-4402. [29] FU Q L, FUJII M, MA R. Development of a gaussian-based alignment algorithm for the ultrahigh-resolution mass spectra of dissolved organic matter[J]. Analytical Chemistry, 2023, 95(5): 2796-2803. doi: 10.1021/acs.analchem.2c04113 [30] KOCH B P, DITTMAR T, WITT M, et al. Fundamentals of molecular formula assignment to ultrahigh resolution mass data of natural organic matter[J]. Analytical Chemistry, 2007, 79(4): 1758-1763. doi: 10.1021/ac061949s [31] KOCH B P, DITTMAR T. From mass to structure: An aromaticity index for high-resolution mass data of natural organic matter[J]. Rapid Communications in Mass Spectrometry, 2006, 20(5): 926-932. doi: 10.1002/rcm.2386 [32] KELLERMAN A M, DITTMAR T, KOTHAWALA D N, et al. Chemodiversity of dissolved organic matter in lakes driven by climate and hydrology[J]. Nature Communications, 2014, 5: 3804. doi: 10.1038/ncomms4804 [33] LaROWE D E, van CAPPELLEN P. Degradation of natural organic matter: A thermodynamic analysis[J]. Geochimica et Cosmochimica Acta, 2011, 75(8): 2030-2042. doi: 10.1016/j.gca.2011.01.020 [34] KIDA M, MERDER J, FUJITAKE N, et al. Determinants of microbial-derived dissolved organic matter diversity in Antarctic Lakes[J]. Environmental Science & Technology, 2023, 57(13): 5464-5473. [35] FU Q L, FUJII M, KWON E. Development and application of a high-precision algorithm for nontarget identification of organohalogens based on ultrahigh-resolution mass spectrometry[J]. Analytical Chemistry, 2020, 92(20): 13989-13996. doi: 10.1021/acs.analchem.0c02899 [36] GASPAR A, KUNENKOV E V, LOCK R, et al. Combined utilization of ion mobility and ultra-high-resolution mass spectrometry to identify multiply charged constituents in natural organic matter[J]. Rapid Communications in Mass Spectrometry:RCM, 2009, 23(5): 683-688. doi: 10.1002/rcm.3924 [37] CHEN S, XIE Q R, SU S H, et al. Source and formation process impact the chemodiversity of rainwater dissolved organic matter along the Yangtze River Basin in summer[J]. Water Research, 2022, 211: 118024. doi: 10.1016/j.watres.2021.118024 [38] BAE E, YEO I J, JEONG B, et al. Study of double bond equivalents and the numbers of carbon and oxygen atom distribution of dissolved organic matter with negative-mode FT-ICR MS[J]. Analytical Chemistry, 2011, 83(11): 4193-4199. doi: 10.1021/ac200464q [39] YU K, DUAN Y H, GAN Y Q, et al. Anthropogenic influences on dissolved organic matter transport in high arsenic groundwater: Insights from stable carbon isotope analysis and electrospray ionization Fourier transform ion cyclotron resonance mass spectrometry[J]. The Science of the Total Environment, 2020, 708: 135162. doi: 10.1016/j.scitotenv.2019.135162 [40] CHEN X, LIU J H, CHEN J F, et al. Oxygen availability driven trends in DOM molecular composition and reactivity in a seasonally stratified fjord[J]. Water Research, 2022, 220: 118690. doi: 10.1016/j.watres.2022.118690 -




 下载:
下载: