-
羰基化合物, 即醛类和酮类化合物, 广泛存在于日常生活环境中, 对人体健康有重要影响. 研究发现, 空气中的羰基化合物不仅对人体的嗅觉产生影响, 还会刺激人体免疫系统, 长时间接触羰基化合物可能会出现不良健康影响. 另外羰基化合物还会引起染色体分裂而造成遗传物质损害或断裂, 如姐妹染色体交换及染色体变异等, 使羰基化合物具有致癌性和致突变性[1-4]. 人们在室内生活工作的时间超过80%, 室内成为越来越多的人最直接和最经常接触的环境[5]. 室内空气中大多数装饰和装修材料包括建筑材料[6]、新家具(尤其是由胶合板制成的家具[7]、木地板[8])、家居用品(如胶水、油漆和涂料[9])、香烟烟雾[10]、室内烹饪[3]以及一些生活用品(如消毒剂、化妆品和空气清新剂)等都会向室内空气环境直接释放羰基化合物[11-13]. 越来越密闭的建筑结构往往又会使室内产生的化学污染物不断积累[14]. 还有些羰基化合物作为一些污染物与臭氧反应的次级产物出现在室内空气环境中[15]. 比如, 臭氧与头发和衣服上残留的人体皮肤油反应也可作为室内空气中羰基化合物的来源[16-17]. 此外, 城区的车辆尾气和工业厂房的燃料燃烧也会产生羰基化合物, 然后通过空气渗透和自然通风进入室内环境中[18-19].
许多国内学者对室内羰基化合物的污染特征、来源情况以及健康影响开展相关研究工作. 黄晓影[20]研究发现, 包头市城区住宅羰基化合物采暖季污染更严重, 其中甲醛和乙醛浓度均与换气次数呈负相关, 较高的相对湿度是甲醛、乙醛和丙醛暴露的危险因素. Pu 等[21]研究发现, 北京城区住宅12种羰基化合物中甲醛污染最严重, 乙醛、丙酮和己醛次之, 其中甲醛受沙发材料、吸烟情况、家庭位置影响, 乙醛受吸烟情况和厨房结构影响, 丙酮受厨房结构和盆栽植物影响, 己醛受盆栽植物影响. Huang 等[22]研究发现, 室内甲醛暴露可能会增加儿童患普通感冒的风险. 由于环境中气态羰基化合物的分析方法比较繁琐以及相对较高的分析费用, 多数文献针对少数几种羰基化合物展开研究, 很少关注气味污染严重的高分子量醛(己醛、庚醛、辛醛、壬醛和癸醛)以及能够诱导细胞损伤和产生晚期糖基化终产物的乙二醛和甲基乙二醛等其它羰基化合物的污染情况及其对人体健康的影响, 这不足以充分了解我国城市住宅室内外空气中羰基化合物的污染特征及健康效应. 本研究旨在通过供暖季与非供暖季在城市居民住宅开展室内外同步观测, 分析季节变化对不同羰基污染物的影响,并评估室内羰基污染物对人群的健康风险及其对嗅觉的污染情况, 以期为进一步研究住宅室内痕量羰基污染物特征及其影响提供一定的科学依据.
-
本研究于2016 年供暖季(1月28日—30日)和非供暖季(9月23日—26日)在西安市雁塔区某住宅区5户住宅开展室内羰基化合物的同步观测, 为便于比较, 另选一住宅的露天阳台同步采集了室外样品. 采样点周围无明显工业污染源, 属于城市住宅区, 各住户家庭信息如表1所示. 采样期间, 所有仪器均放置在客厅中心位置(离地面1.0—1.5 m), 避开通风口. 采样头选用Sep-Pak DNPH(2,4-二硝基苯肼)-silica Gel cartridge + Ozone scrubber (Waters Corporation, USA), 流量为0.6—0.8 L·min−1的真空泵(Thomas)进行主动采样, 采集时间为 8 h(9:30—17:30), 采集后的DNPH样品用铝箔包裹后, 置于4 ℃以下冰箱保存, 防止样品被污染. 供暖季共采集DNPH样品18个(室内每户3个+室外3个), 均为工作日2个+周末1个; 非供暖季共采集24个(室内每户4个+室外4个), 均为工作日2个+周末2个. 此外, 采用 CO2分析仪(LI-820, LI-COR, USA)监测室内通风换气次数.
-
DNPH样品经乙腈洗提, 利用高效液相色谱仪(HPLC, Aglient 1200 LC)分析. 在25 ℃柱温、流速2.0 mL·min−1、检测波长为360 nm、390 nm和420 nm、进样量为20 μL的条件下, 利用梯度洗脱程序进行分析, 可定量检测20种羰基化合物, 分别为甲醛(C1)、乙醛(C2)、丙酮(A3K)、丙醛(n-C3)、2-丁酮(MEK)、丁醛(i,n-C4)、苯甲醛(Benz)、异戊醛(i-C5)、正戊醛(n-C5)、邻甲苯甲醛(o-tol)、间甲苯甲醛(m-tol)、对甲苯甲醛(p-tol)、2,5-二甲基苯甲醛(2,5-DB)、己醛(C6)、庚醛(C7)、辛醛(C8)、壬醛(C9)、癸醛(C10)、乙二醛(Gly)和甲基乙二醛(mGly), 其中己醛、庚醛、辛醛、壬醛和癸醛, 统称为高分子量羰基化合物(C6—C10), 各物质的方法检出限如表2所示. 本方法其他的详细介绍及质量控制参见文献[23].
-
绘图使用Origin 9.0软件, 统计分析用SPSS 26和 Excel 2021 软件. 样本正态性检验采用 Kolmogorov-Smirnov 检验. 若研究变量为非正态分布, 则进行非参数双样本Mann-Whitney U检验和多样本Kruskal-Wallis H检验, 比较不同住户的羰基化合物浓度差异. 所有统计分析结果在 P <0.05 时,被认为具有统计学意义.
-
与成人相比, 儿童因更高的呼吸频率、更多的脆弱性和更长的暴露时间[24-25], 更易受到环境污染物的影响, 因此有必要了解室内空气中羰基化合物污染对儿童健康的影响. 本研究采用美国环境保护署(U.S. Environmental Protection Agency, EPA)提出的个人吸入暴露的计算方法评估0—6岁儿童健康风险[26], 计算公式如下:
式中, Eij 为微环境 (j) 中污染物(i) 的日吸入剂量, μg·d−1; Cij为微环境 (j) 中污染物 (i) 的浓度, 即室内羰基化合物的实测浓度, μg·m−3; IRj 是微环境中的吸入率 (j) , m3·h−1, 2岁以下儿童IRj为0.22 m3·h−1, 2—6岁儿童为0.33 m3·h−1; tj 是在微环境 (j) 中的暴露时间, 即儿童每天在室内度过的时间, h·d−1, 2岁以下儿童tj为21.37 h·d−1 , 2—6岁儿童为20.15 h·d−1. IRj和tj 数据均来源于中国人群暴露参数手册(儿童卷)概要[27].
根据最近的研究中采用的方法[26, 28], 对儿童而言, 需要调整无显著风险水平(no significant risk levels, NSRLs) [26] , 调整后的儿童特定NSRLs: 2 岁以下儿童, 甲醛、乙醛分别为 0.52 μg·d−1、1.16 μg·d−1; 2—6岁儿童, 甲醛、乙醛分别为 3.15 μg·d−1、7.08 μg·d−1. 此外, 用风险商(risk quotients, RQ)来表示健康风险, RQ 的计算方法是将儿童每日吸入剂量除以儿童特定的 NSRLs. RQ >1 表明儿童吸入剂量超过了 10−5 终生致癌风险阈值, 即儿童面临潜在的癌症风险.
-
除了对人体健康造成影响外, 羰基化合物还会产生气味污染. 羰基化合物的质量浓度高并不意味着其气味强度也大, 而是与气味阈值共同呈比例地影响人体对气味的感知. 为了将污染物的浓度和气味强度联系起来, 需要对其气味进行污染评价. 气味污染评价中羰基化合物的气味强度用气味活性值(odor activity value, OAV)表示[13, 29]:
式中, OAVi 为污染物 i 的气味活性值, 无量纲; Cmi为污染物 i 的质量浓度, μg·m−3; Cti为污染物 i 的气味阈值, μg·m−3, 其取自日本环境卫生中心对有害气体污染物气味阈值的研究结果[30].
污染物的气味活性值以大多数正常人的感官为准, OAVi ≤1 表示一般人无法感知到污染物 i 的气味; OAVi >1可感知到污染物 i 所散发的气味, 且 OAVi 越大, 能感知到的气味越大, 即其气味强度越大.
-
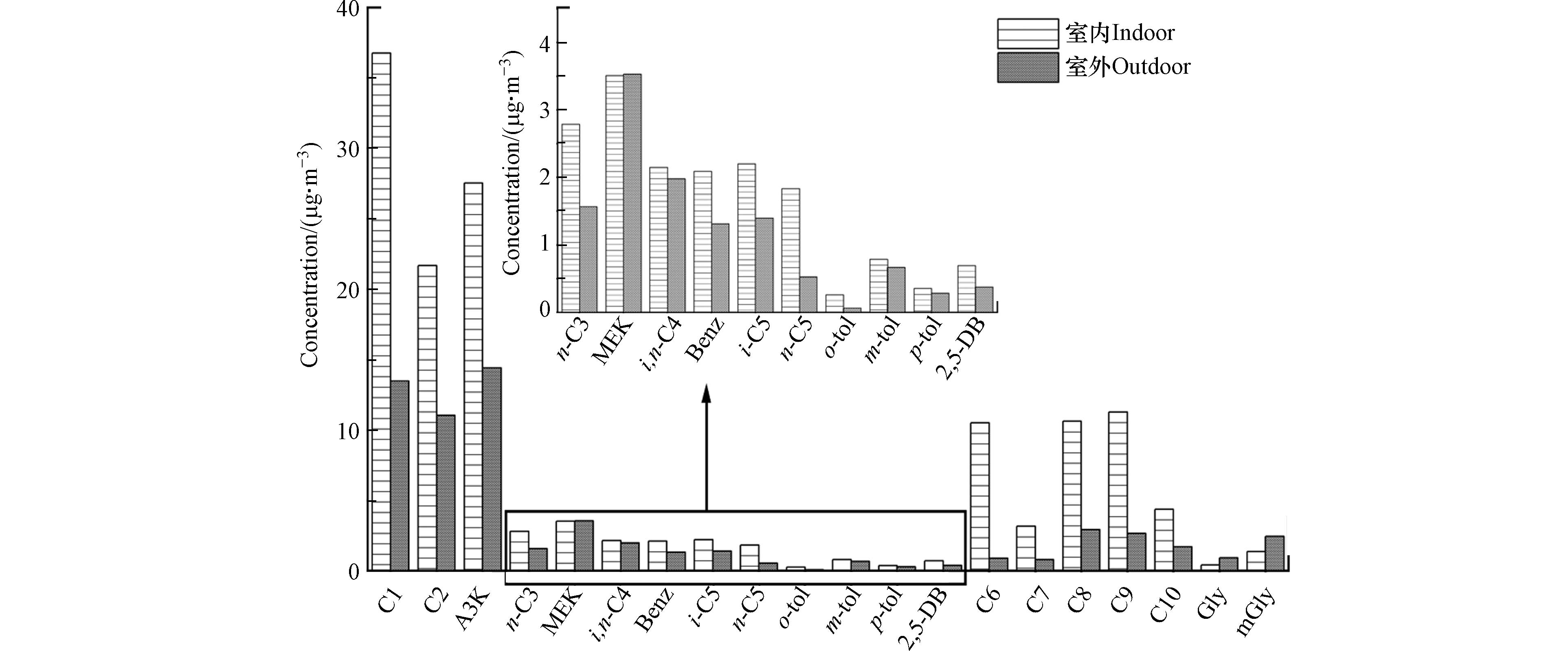
室内环境中羰基化合物的质量浓度为(144.3±56.2) μg·m−3, 其中甲醛(25.5%)、丙酮(19.1%)和乙醛(15.0%)是含量最高的3种物质, 其平均浓度分别为(36.8±21.0) μg·m−3、(27.5±14.3) μg·m−3、(21.7±14.4) μg·m−3, 均明显高于室外浓度(图1). 这3类羰基化合物的来源与居住者的生活息息相关, 可从建筑材料、环境烟草烟雾、烹饪油烟、香味消费品、个人护理产品、清洁等人为活动或通过室内VOCs(尤其是萜烯)的氧化排放[31-33]. 室内高分子量羰基化合物(C6—C10)占比也比较大, 约27.7%(15.9%—45.9%), C6—C10平均浓度(39.9 μg·m−3)是室外(9.0 μg·m−3)的4.4倍. 研究表明, 己醛不仅包含在香料和香精中, 还存在于含有植物化学物质的食物和办公家具[34]. 辛醛有很强的水果香味, 可用作食用香料, 也可作肥皂洗涤剂的香料使用. 壬醛具有玫瑰、柑橘等香气, 存在于红茶、绿茶中. 室外大气环境中羰基化合物的质量浓度为(63.0±21.8) μg·m−3, 其中丙酮浓度最高((14.4±4.8) μg·m−3), 其次是甲醛((13.5±6.8) μg·m−3)和乙醛((11.0±4.3) μg·m−3), 这3类化合物约占室外总羰基化合物浓度的61.8%. I/O 比值(室内/室外)能更好地推断室内羰基化合物的可能影响因素(室内源或室外渗透). 由图1可知, 乙二醛(Gly)和甲基乙二醛(mGly)的I/O 比值均低于1.0, 表明这两类典型的α-二羰基物质可能更多的来自室外环境的渗透. 研究发现, 室外大气环境中乙二醛和甲基乙二醛主要来源于生物质燃烧和挥发性有机化合物(如异戊二烯、芳烃和烯烃)的氧化[35-36]. 值得注意的是,低分子量的羰基化合物甲醛、乙醛、丙酮和高分子量羰基化合物(C6—C10)的 I/O 比值明显较高(1.9—11.8),说明室内排放源对这些羰基化合物有显著贡献.
从表2和表3中可以看出, 室内环境中非供暖季浓度最高的5种羰基化合物为甲醛、丙酮、辛醛、乙醛和壬醛, 其浓度范围分别为(17.6—49.9) μg·m−3、(13.1—18.3) μg·m−3、(8.3—19.3) μg·m−3、(7.6—12.9) μg·m−3和(4.0—8.8) μg·m−3. 而供暖季则为甲醛、丙酮、乙醛、壬醛和己醛, 其浓度范围分别为(23.2—86.7) μg·m−3、(31.2—47.8) μg·m−3、(24.1—48.5) μg·m−3、(14.9—18.9) μg·m−3和(10.8—30.0) μg·m−3, 均明显高于非供暖季. 该结果与有关包头市城区住宅羰基化合物污染水平的研究结果一致, 可能与供暖季住宅内温湿度、通风换气次数以及室外环境状况等因素有关[20]. 整体来看,无论供暖季还是非供暖季, 住宅室内环境中最丰富的3类羰基化合物均为甲醛、乙醛和丙酮, 这与国内其它城市(北京、大连、上海、武汉和长沙等)的研究结果一致[26]. 另外, 本文所关注的3类高分子量羰基化合物(己醛、辛醛和壬醛)占比也较高(14.4%—33.0%)(图2). Feng 等[37]研究发现,餐饮油烟可能是造成空气中高分子量羰基化合物浓度偏高的原因之一. 由此可见, 室内高分子量的羰基化合物可能来源于住户的烹饪活动. 室外大气环境中羰基化合物浓度表现为非供暖季(68.9±28.2) μg·m−3明显高于供暖季(55.3±9.4) μg·m−3, 其中甲醛浓度增量最大(6.6 μg·m−3), 其次是辛醛(3.5 μg·m−3)和甲基乙二醛(2.5 μg·m−3), 这归因于非供暖季温度偏高, 太阳辐射较强, 有利于大气有机物发生光化学反应, 同时非供暖季植物排放对羰基化合物有重要的贡献.
室内环境中甲醛、乙醛、丙酮的浓度范围分别为(17.6—86.7) μg·m−3、(7.6—48.5) μg·m−3、(13.1—47.8) μg·m−3, 不同住户室内羰基化合物浓度差异明显, 这可能与不同的生活习惯以及装修样式等因素有关[20-21]. 具体来看, 供暖季QJ-1室内甲醛平均浓度((86.7±10.8) μg·m−3)明显超过2022年7月11日国家市场监督管理总局(国家标准化管理委员会)批准发布的新版标准(GB/T 18883—2022) [38]中提到的室内甲醛1小时平均浓度(80 μg·m−3), 可能与该住宅在采样前期新增家具(床和衣柜)有关. QJ-3供暖季室内乙醛浓度((48.5±8.9) μg·m−3)比日本厚生劳动省出台的室内乙醛浓度限值(48 μg·m−3)略高[39]; 整体来看, QJ-1—QJ-5室内丙醛浓度均未超过加拿大卫生部报道的暴露限值(8 μg·m−3), 丙醛达到该限值的临界效应表现为嗅觉上皮萎缩[40].
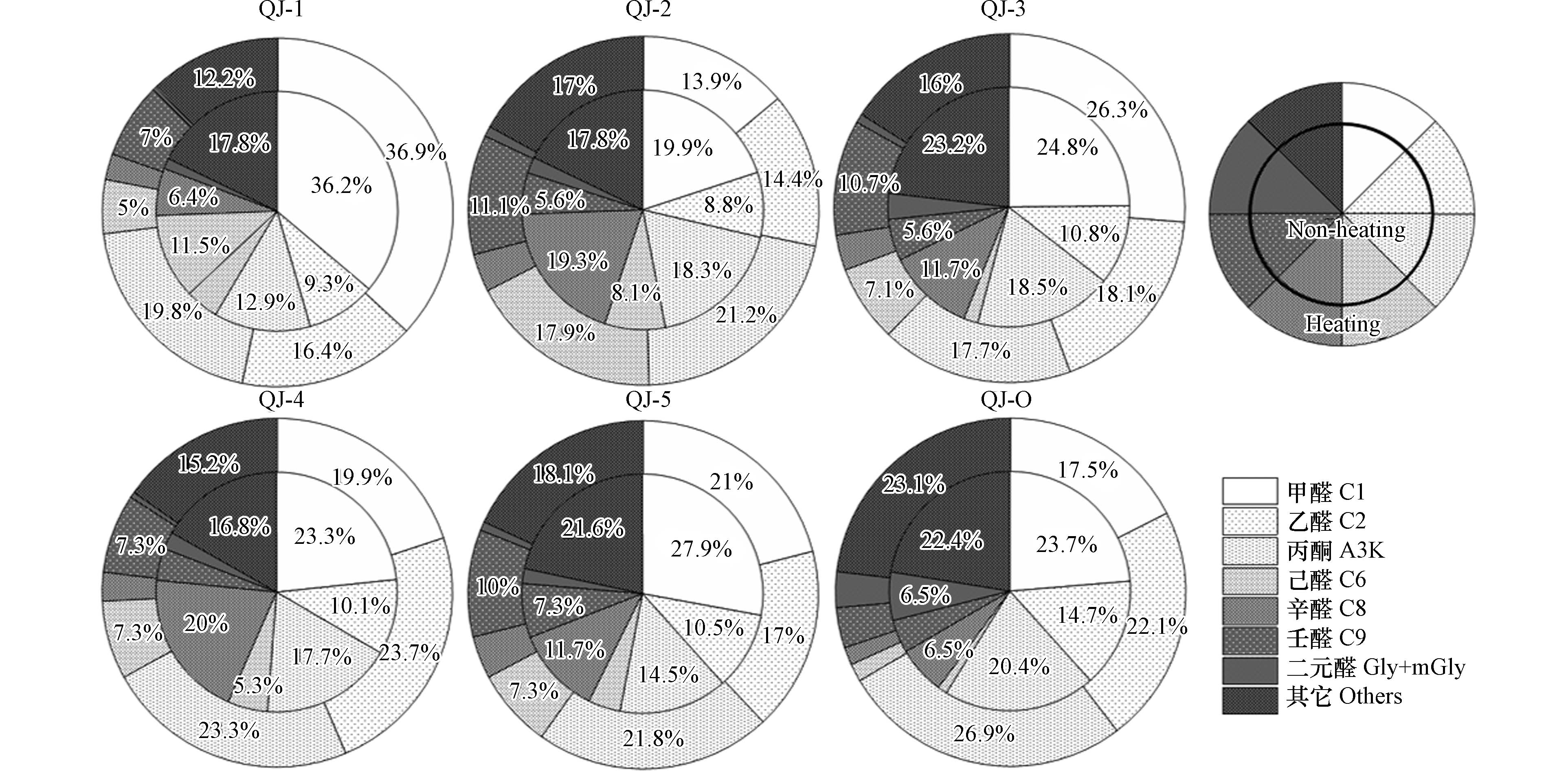
图2为供暖季与非供暖季住宅室内外空气中羰基化合物的浓度占比. 从图2可以看出, 低分子量的甲醛、乙醛和丙酮对室内外空气中羰基化合物的贡献较大, 占总羰基化合物浓度的47.0%—73.0%, 且供暖季的占比显著高于非供暖季, 其中乙醛占比全部表现为供暖季 > 非供暖季; 结合表2和表3浓度数据发现, 室内外环境中的乙醛浓度也均表现为供暖季 > 非供暖季. 值得注意的是, QJ-2无论是供暖季还是非供暖季, 己醛、辛醛和壬醛这3类羰基化合物的占比之和都超过 30%, 而甲醛、乙醛和丙酮占比之和较其它住宅偏低,推测是因为该住宅内选择瓷砖铺设且家具量较少. 此外, 与其它住户相比, QJ-2选用液化石油气作为烹饪燃料可能对室内羰基化合物的污染情况也有影响,需进一步研究.
-
诸多研究表明, 通风换气次数越大, 室内污染物浓度越小[20,29]. 为了解室内的通风状况, 本研究采用CO2示踪气体衰减法[29,41]计算得到各住宅供暖季和非供暖季的通风换气次数(表4). 该方法以CO2为示踪气体, 当室内CO2浓度比室外高时, 由于室内外的空气交换,室内CO2浓度会呈指数衰减, 式(3)为该过程中的质量守恒方程, 经推导可将CO2浓度与换气次数的关系写成式(4), 再通过线性回归计算, 即可求得室内的换气次数[29].
式中, Cin为室内CO2实时浓度, mg·m−3; Cout为室外CO2浓度, mg·m−3; G为通风量, m3·h−1; ACH为每小时换气次数, h−1; τ为时间, h; Cin,0表示室内CO2初始浓度, mg·m−3.
如表4所示, 供暖季室内通风换气次数为(0.1—0.8) h−1, 非供暖季为(2.6—48.6) h−1, 非供暖季换气次数比供暖季高1—2个数量级. 显然, 高频率的通风换气次数是非供暖季室内环境中羰基化合物浓度显著低于供暖季的原因. 但是, 室内羰基化合物的浓度还受室内温湿度、烹饪活动、人员情况(人员数量、人员类型等)、生活习性(个人护理产品、卫浴产品使用等)以及室外污染状况等其它诸多因素影响[31-33,37]. 此外, 室内外环境中二元醛(Gly+mGly)浓度则表现为非供暖季高于供暖季, 而且室内二元醛浓度随着室外浓度的增加而增加, 进一步表明室外源对室内贡献明显.
-
“周末效应”的概念在 1974 年被Cleveland 等[42]首次提出. 研究表明, 大气污染物质量浓度变化在工作日和周末存在明显差异, 这种变化被称为“周末效应”[43-44]. 周末效应源于工作和休息模式的节律性, 与人类活动密切相关. 本文采用如下方式量化周末效应(ΔWE)[44-46]:
式中, C工作日 表示工作日的浓度均值, C周末 表示周末的浓度均值. 为保持数据一致性, 本研究中C工作日 采用周五的污染物浓度, C周末 采用周六的污染物浓度.
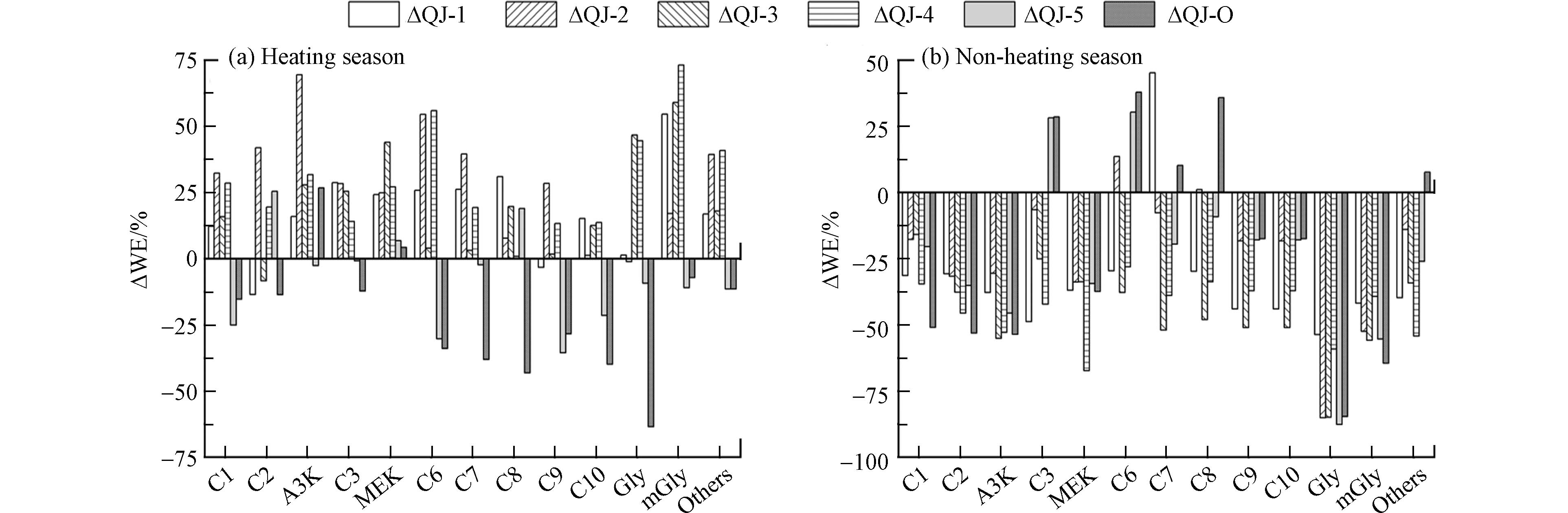
图3绘制了供暖季(a)和非供暖季(b)住宅室内外空气中羰基化合物浓度的相对偏差. 从图3可以看出, 供暖季, 不同住宅室内环境中羰基化合物的周末效应并不一致, 除QJ-5外, 其余4户住宅室内甲醛和丙酮浓度周末相比工作日增加, 分别增加了12.3%—32.3%、15.9%—69.4%; 高分子量羰基化合物(C6—C10)也表现出周末浓度高于工作日的“周末效应”. 室外大气环境中甲醛和乙醛浓度周末相比工作日减少, 分别减少了15.3% 和13.7%, 而丙酮则增加了26.7%; 高分子量的羰基化合物(C6—C10)浓度降幅超过30%. 非供暖季, “周末效应”更明显, 无论室内环境还是室外大气, 甲醛、乙醛、丙酮、壬醛、癸醛、乙二醛和甲基乙二醛均表现出工作日浓度高于周末的“周末效应”. 室内环境中甲醛、乙醛和丙酮周末浓度相较于工作日分别减少了15.9%—34.6%、30.7%—45.6%、30.6%—55.1%; 室外大气中这三类污染物浓度同样是周末低于工作日, 分别减少了51.0%、53.1%和53.6%.
综上所述, 住宅室内环境中, 供暖季多数羰基化合物呈周末高于工作日的“周末效应”, 非供暖季则呈工作日高于周末的“周末效应”; 这归因于供暖季室外较低的温度, 居民周末更多选择室内活动以及低频的通风换气次数导致室内环境中多数羰基化合浓度周末高于工作日; 而非供暖季相对较好的通风条件使室内外羰基化合物浓度的“周末效应”变化一致, 均表现为周末低于工作日. 室外环境中羰基化合物浓度不受季节变化影响, 均呈现工作日高于周末的“周末效应”. 研究发现, 在典型的城市地区PM2.5具有明显的工作日偏高, 周末偏低的“周末效应”[46]. 由此可见, 室外羰基化合物受到人类活动、污染排放和气象等各种因素的综合影响.
-
表5总结了各住户室内儿童每日吸入甲醛和乙醛的剂量. 2岁以下儿童的甲醛和乙醛日吸入量最高值分别为313.9 μg·d−1和121.1 μg·d−1, 2—6岁的儿童甲醛和乙醛日最高吸入量分别为457.5 μg·d−1和176.5 μg·d−1. 可发现随着年龄的增长, 身体不断发育, 儿童羰基污染物吸入剂量增加. 供暖季室内甲醛、乙醛浓度高于非供暖季, 因此供暖季节室内羰基化合物污染情况更值得关注.
儿童特定的无显著风险水平用于表征儿童在家中接触甲醛和乙醛的健康风险[26]. 如表5所示,每户儿童接触甲醛和乙醛的风险商均远大于1, 表明各住户儿童皆面临潜在的癌症风险. 2岁以下儿童甲醛暴露RQ值为192.4—609.0, 2—6岁儿童甲醛暴露RQ值为45.9—145.4, 即儿童的甲醛暴露量是“安全限”水平的数十至数百倍. 2岁以下儿童乙醛暴露RQ值为65.1—104.4, 2—6岁儿童乙醛暴露RQ值为15.5—24.9. 与乙醛相比, 儿童在家接触甲醛对其健康的影响相对更大. 这与Bradman 等[28]研究中甲醛暴露的 RQ 值(12.0—51.7)高于乙醛暴露的 RQ 值(2.3—9.8)的结果一致.
需指出, 在计算儿童吸入甲醛和乙醛的剂量时, 只考虑了儿童在住宅中接触羰基化合物的情况, 如果还考虑到儿童在学校等其它室内环境接触羰基化合物, 患癌风险会更大. 因此, 室内羰基化合物污染对儿童健康的影响, 需要居民和标准制定者高度重视. 此外, 由于缺乏指南和风险指数, 其它含量较高的羰基化合物(例如己醛和壬醛)的化学危害潜力或癌症风险无法系统地评估.
-
各住户室内环境中不同污染物对应的气味活性值如表6所示. 在分析各住宅所散发的羰基化合物成分时, 检测到较高浓度的甲醛、乙醛和丙酮, 但由于甲醛和丙酮的气味阈值相对较高, 因此这两种高浓度污染物的气味活性要低得多, 只有乙醛的气味活性更明显, 其气味活性值均大于5. 各住宅室内环境中高分子量的己醛、庚醛、辛醛、壬醛和癸醛的气味活性值均大于1, 尤其是辛醛最大, 均大于100, 其次是己醛. 对于广泛用作装修和家居的木质材料释放的气味物质——辛醛具有肥皂和柑橘味, 己醛具有香草味. 吴可[29]研究发现, 装修完工后室内环境中的气味污染主要来自于庚醛、辛醛、壬醛和己醛等醛类污染物. 而且这些高分子量的醛类污染物释放量在臭氧的影响下还会随时间而增加[47]. 因此, 室内环境中羰基化合物的气味污染更多应关注高分子量羰基化合物. 已有研究表明, 室内不良的气味感知是病态建筑综合征(sick building syndrome, SBS)的危险因素, 高分子量的羰基化合物对SBS的影响相当明显, 己醛对SBS的一般症状的危险性达到了显著性水平, 癸醛和辛醛对SBS的皮肤症状的危险性也达到了显著性水平[48]. 所以, 考虑针对室内环境中高分子量羰基化合物规定限值亦十分必要.
-
本研究选择5户城市住宅进行同步观测, 对室内外空气环境中痕量羰基化合物的浓度水平、影响因素、健康风险及气味污染展开研究. 通过分析, 得出以下结论:
(1)居民住宅室内外环境中总羰基化合物浓度变化表现为: 室内 > 室外; 室内供暖季 > 室内非供暖季; 室外供暖季 < 室外非供暖季; 室内外空气中甲醛、乙醛和丙酮3类羰基化合物比重高(47.0%—73.0%), 室内高分子量的羰基化合物(C6—C10)总浓度(39.9 μg·m−3)是室外(9.0 μg·m−3)的4倍多. 季节变化表明, 通风换气次数对室内环境中羰基化合物污染影响显著.
(2)供暖季室内多数羰基化合物呈周末高于工作日的“周末效应”, 非供暖季则呈工作日高于周末的“周末效应”. 室外环境中羰基化合物浓度不受季节影响均呈现工作日高于周末的“周末效应”.
(3)健康风险评估显示各住户儿童甲醛和乙醛的吸入剂量均远超过OEHHA 给出的暴露剂量安全限值, 表明各家庭的儿童都面临潜在的癌症风险. 住宅室内环境中主要气味污染来自于气味阈值较低的高分子量羰基化合物, 包括己醛、庚醛、辛醛、壬醛和癸醛.
需指出, 本研究中样本量并不是很充足, 但室内外同步观测结果也能反映城市住宅室内外空气中痕量羰基化合物不同季节的污染情况; 此外, 不同住户家庭成员的数量以及不同的生活习惯等因素对室内羰基污染物的影响各不相同, 关于这部分讨论还有待于进一步的研究. 尽管如此, 这些痕量羰基化合物的测定对我国室内空气质量监管的来源分配和数据保存仍具有价值.
住宅室内空气羰基化合物的污染特征及健康影响
Pollution characteristics and health effects of carbonyl compounds in residential indoors
-
摘要: 为研究住宅室内空气中羰基化合物污染水平及健康影响,于2016年采集西安市城区住宅5户家庭室内空气中20种羰基化合物,利用高效液相色谱仪进行检测和分析. 结果表明,室内羰基化合物浓度((144.3±56.2) μg·m−3)显著高于室外((63.0±21.8) μg·m−3). 甲醛、乙醛和丙酮是室内外环境中相对贡献比较丰富的化合物,占总羰基化合物浓度的47.0%—73.0%. 通风换气次数对室内环境中羰基化合物污染影响显著. 室内羰基化合物浓度变化呈现显著的“周末效应”,具体表现为供暖季多数羰基化合物周末高于工作日,非供暖季工作日高于周末. 健康风险评估表明各住宅儿童每日吸入甲醛和乙醛的剂量均超过儿童终生致癌风险阈值1—2个数量级,因此面临显著的潜在癌症风险. 室内气味污染则主要来自于气味阈值较低的高分子量羰基化合物,包括己醛、庚醛、辛醛、壬醛和癸醛. 其中辛醛贡献最大,其气味活性值均大于100. 本研究结果为城市住宅室内痕量羰基污染物特征及健康影响提供了基础数据和科学依据.Abstract: Twenty carbonyl compounds of the indoor air from five households in Xi'an were analyzed by high performance liquid chromatography coupled with DAD, to investigate the pollution level and health effect of indoor air. Higher concentration of carbonyl compounds were founded in indoor air ((144.3±56.2) μg·m-3) than outdoor ((63.0±21.8) μg·m-3). Formaldehyde, acetaldehyde and acetone were the most abundant carbonyl compounds in indoor and outdoor air, accounting for 47.0%—73.0% to the total carbonyl compounds. The air exchange rate had a major effect on indoor carbonyl compounds pollution. The “weekend effect” was significant with higher carbonyl compounds concentration on weekends than weekdays in heating season. In contrast, higher carbonyl compounds concentration was founded on weekdays than weekends in non-heating seasons. Health risk assessment showed that the daily inhaled doses of formaldehyde and acetaldehyde for children exceed the lifetime cancer risk threshold by 1—2 orders of magnitude, indicating significant potential cancer risk. Odor pollution were mainly from high molecular weight carbonyl compounds with lower odor threshold, including hexanal, heptanal, octanal, nonanal and decanal.
-
Key words:
- Indoor air /
- carbonyl compounds /
- pollution characteristics /
- influencing factors /
- health effects.
-
羰基化合物, 即醛类和酮类化合物, 广泛存在于日常生活环境中, 对人体健康有重要影响. 研究发现, 空气中的羰基化合物不仅对人体的嗅觉产生影响, 还会刺激人体免疫系统, 长时间接触羰基化合物可能会出现不良健康影响. 另外羰基化合物还会引起染色体分裂而造成遗传物质损害或断裂, 如姐妹染色体交换及染色体变异等, 使羰基化合物具有致癌性和致突变性[1-4]. 人们在室内生活工作的时间超过80%, 室内成为越来越多的人最直接和最经常接触的环境[5]. 室内空气中大多数装饰和装修材料包括建筑材料[6]、新家具(尤其是由胶合板制成的家具[7]、木地板[8])、家居用品(如胶水、油漆和涂料[9])、香烟烟雾[10]、室内烹饪[3]以及一些生活用品(如消毒剂、化妆品和空气清新剂)等都会向室内空气环境直接释放羰基化合物[11-13]. 越来越密闭的建筑结构往往又会使室内产生的化学污染物不断积累[14]. 还有些羰基化合物作为一些污染物与臭氧反应的次级产物出现在室内空气环境中[15]. 比如, 臭氧与头发和衣服上残留的人体皮肤油反应也可作为室内空气中羰基化合物的来源[16-17]. 此外, 城区的车辆尾气和工业厂房的燃料燃烧也会产生羰基化合物, 然后通过空气渗透和自然通风进入室内环境中[18-19].
许多国内学者对室内羰基化合物的污染特征、来源情况以及健康影响开展相关研究工作. 黄晓影[20]研究发现, 包头市城区住宅羰基化合物采暖季污染更严重, 其中甲醛和乙醛浓度均与换气次数呈负相关, 较高的相对湿度是甲醛、乙醛和丙醛暴露的危险因素. Pu 等[21]研究发现, 北京城区住宅12种羰基化合物中甲醛污染最严重, 乙醛、丙酮和己醛次之, 其中甲醛受沙发材料、吸烟情况、家庭位置影响, 乙醛受吸烟情况和厨房结构影响, 丙酮受厨房结构和盆栽植物影响, 己醛受盆栽植物影响. Huang 等[22]研究发现, 室内甲醛暴露可能会增加儿童患普通感冒的风险. 由于环境中气态羰基化合物的分析方法比较繁琐以及相对较高的分析费用, 多数文献针对少数几种羰基化合物展开研究, 很少关注气味污染严重的高分子量醛(己醛、庚醛、辛醛、壬醛和癸醛)以及能够诱导细胞损伤和产生晚期糖基化终产物的乙二醛和甲基乙二醛等其它羰基化合物的污染情况及其对人体健康的影响, 这不足以充分了解我国城市住宅室内外空气中羰基化合物的污染特征及健康效应. 本研究旨在通过供暖季与非供暖季在城市居民住宅开展室内外同步观测, 分析季节变化对不同羰基污染物的影响,并评估室内羰基污染物对人群的健康风险及其对嗅觉的污染情况, 以期为进一步研究住宅室内痕量羰基污染物特征及其影响提供一定的科学依据.
1. 材料与方法(Materials and methods)
1.1 样品采集
本研究于2016 年供暖季(1月28日—30日)和非供暖季(9月23日—26日)在西安市雁塔区某住宅区5户住宅开展室内羰基化合物的同步观测, 为便于比较, 另选一住宅的露天阳台同步采集了室外样品. 采样点周围无明显工业污染源, 属于城市住宅区, 各住户家庭信息如表1所示. 采样期间, 所有仪器均放置在客厅中心位置(离地面1.0—1.5 m), 避开通风口. 采样头选用Sep-Pak DNPH(2,4-二硝基苯肼)-silica Gel cartridge + Ozone scrubber (Waters Corporation, USA), 流量为0.6—0.8 L·min−1的真空泵(Thomas)进行主动采样, 采集时间为 8 h(9:30—17:30), 采集后的DNPH样品用铝箔包裹后, 置于4 ℃以下冰箱保存, 防止样品被污染. 供暖季共采集DNPH样品18个(室内每户3个+室外3个), 均为工作日2个+周末1个; 非供暖季共采集24个(室内每户4个+室外4个), 均为工作日2个+周末2个. 此外, 采用 CO2分析仪(LI-820, LI-COR, USA)监测室内通风换气次数.
表 1 各采样住户家庭信息Table 1. Household information of each sampled household采样点Site 房屋年龄/aAge of house 面积/m2Area 装修后放置时间/monthStorage time after decoration 地板材质Floor material 壁纸Wall-paper 取暖燃料Fuel for heating 烹饪燃料Fuel for cooking 每天烹饪次数Cooking frequency 通风方式Ventilation 吸烟Smoking QJ-1 5 100 6—12 客厅+卧室复合木地板 是 天然气 天然气 > 3 半开 否 > 1 h QJ-2 5 100 6—12 客厅+卧室瓷砖 否 天然气 液化石油气 > 3 半开 否 > 1 h QJ-3 5 102 6—12 客厅+卧室复合木地板 否 天然气 天然气 1 半开 否 电 < 1 h QJ-4 5 100 3—6 客厅+卧室复合竹地板 是 天然气 天然气 3 半开 否 < 1 h QJ-5 5 148 3—6 客厅瓷砖卧室复合木地板 否 天然气 天然气 3 全开 否 < 1 h 1.2 样品分析及质控
DNPH样品经乙腈洗提, 利用高效液相色谱仪(HPLC, Aglient 1200 LC)分析. 在25 ℃柱温、流速2.0 mL·min−1、检测波长为360 nm、390 nm和420 nm、进样量为20 μL的条件下, 利用梯度洗脱程序进行分析, 可定量检测20种羰基化合物, 分别为甲醛(C1)、乙醛(C2)、丙酮(A3K)、丙醛(n-C3)、2-丁酮(MEK)、丁醛(i,n-C4)、苯甲醛(Benz)、异戊醛(i-C5)、正戊醛(n-C5)、邻甲苯甲醛(o-tol)、间甲苯甲醛(m-tol)、对甲苯甲醛(p-tol)、2,5-二甲基苯甲醛(2,5-DB)、己醛(C6)、庚醛(C7)、辛醛(C8)、壬醛(C9)、癸醛(C10)、乙二醛(Gly)和甲基乙二醛(mGly), 其中己醛、庚醛、辛醛、壬醛和癸醛, 统称为高分子量羰基化合物(C6—C10), 各物质的方法检出限如表2所示. 本方法其他的详细介绍及质量控制参见文献[23].
表 2 供暖季室内外环境中羰基化合物浓度Table 2. Concentrations of carbonyl compounds in indoor and outdoor environments in heating season羰基化合物Carbonyl compounds 方法检测限/(µg·mL−1)Method detection limit 平均值±标准偏差 (AVG±SD)/( μg·m−3) QJ-1 QJ-2 QJ-3 QJ-4 QJ-5 QJ-O 甲醛(C1) 0.002 86.7 ± 10.8 23.2 ± 5.1 40.7 ± 2.8 30.9 ± 6.4 46.3 ± 6.9 9.7 ± 1.3 乙醛(C2) 0.004 38.4 ± 6.1 24.1 ± 5.7 48.5 ± 8.9 25.1 ± 5.0 31.9 ± 7.9 12.2 ± 2.6 丙酮(A3K) 0.006 46.5 ± 11.9 35.5 ± 13.9 47.8 ± 5.9 32.2 ± 10.3 31.2 ± 4.5 14.9 ± 4.4 丙醛(C3) 0.004 4.9 ± 0.7 3.5 ± 1.0 4.6 ± 0.5 3.1 ± 0.8 4.3 ± 0.2 2.3 ± 0.4 2-丁酮(MEK) 0.005 3.5 ± 0.6 3.2 ± 0.9 5.3 ± 1.0 3.3 ± 1.1 4.5 ± 0.3 3.1 ± 0.6 丁醛(i,n-C4) 0.003 2.9 ± 0.4 2.4 ± 0.7 3.0 ± 0.3 2.4 ± 0.6 2.5 ± 0.1 1.4 ± 0.3 苯甲醛(Benz) 0.007 1.9 ± 0.2 1.8 ± 0.4 2.9 ± 0.3 2.2 ± 0.7 1.9 ± 0.2 1.0 ± 0.2 异戊醛(i-C5) 0.004 3.4 ± 0.6 2.7 ± 0.7 3.0 ± 0.3 2.6 ± 0.6 3.6 ± 0.3 1.7 ± 0.4 正戊醛(n-C5) 0.005 2.4 ± 0.4 4.5 ± 1.4 3.0 ± 0.3 2.2 ± 0.7 2.1 ± 0.3 0.6 ± 0.2 邻甲苯甲醛(o-tol) 0.006 0.5 ± 0.1 0.6 ± 0.3 0.4 ± 0.1 0.5 ± 0.4 0.7 ± 0.2 0.1 ± 0.1 间甲苯甲醛(m-tol) 0.004 0.5 ± 0.1 0.5 ± 0.1 0.5 ± 0.2 0.5 ± 0.2 0.5 ± 0.2 0.5 ± 0.1 对甲苯甲醛(p-tol) 0.003 0.3 ± 0.1 0.6 ± 0.2 0.5 ± 0.2 0.3 ± 0.2 0.4 ± 0.2 0.2 ± 0.0 2,5-二甲基苯甲醛(2,5-DB) 0.003 0.6 ± 0.1 0.7 ± 0.2 0.6 ± 0.2 0.6 ± 0.1 0.5 ± 0.2 0.5 ± 0.2 己醛(C6) 0.007 11.8 ± 2.5 30.0 ± 7.7 14.9 ± 1.6 10.8 ± 4.6 12.6 ± 2.5 0.9 ± 0.2 庚醛(C7) 0.011 4.7 ± 1.0 4.5 ± 1.2 4.6 ± 0.1 3.6 ± 0.7 3.9 ± 0.8 0.8 ± 0.3 辛醛(C8) 0.016 5.6 ± 1.0 5.9 ± 1.5 5.5 ± 0.5 5.8 ± 1.7 5.8 ± 1.5 0.9 ± 0.3 壬醛(C9) 0.017 16.4 ± 2.8 18.6 ± 5.1 15.0 ± 1.1 14.7 ± 3.2 18.9 ± 5.9 2.1 ± 0.5 癸醛(C10) 0.001 2.9 ± 0.5 3.5 ± 2.2 2.8 ± 0.8 5.4 ± 0.8 3.3 ± 0.9 0.6 ± 0.2 乙二醛(Gly) 0.001 0.4 ± 0.1 0.7 ± 0.1 0.4 ± 0.1 0.4 ± 0.1 0.4 ± 0.1 0.8 ± 0.4 甲基乙二醛(mGly) 0.001 0.6 ± 0.2 0.9 ± 0.2 0.7 ± 0.2 0.8 ± 0.2 1.1 ± 0.2 1.0 ± 0.2 总和(SUM) 235.1±33.9 167.3 ± 38.7 204.7 ± 11.6 147.2 ± 33.1 176.3 ± 25.7 55.3 ± 9.4 1.3 数据分析
绘图使用Origin 9.0软件, 统计分析用SPSS 26和 Excel 2021 软件. 样本正态性检验采用 Kolmogorov-Smirnov 检验. 若研究变量为非正态分布, 则进行非参数双样本Mann-Whitney U检验和多样本Kruskal-Wallis H检验, 比较不同住户的羰基化合物浓度差异. 所有统计分析结果在 P <0.05 时,被认为具有统计学意义.
1.4 健康风险评价方法
与成人相比, 儿童因更高的呼吸频率、更多的脆弱性和更长的暴露时间[24-25], 更易受到环境污染物的影响, 因此有必要了解室内空气中羰基化合物污染对儿童健康的影响. 本研究采用美国环境保护署(U.S. Environmental Protection Agency, EPA)提出的个人吸入暴露的计算方法评估0—6岁儿童健康风险[26], 计算公式如下:
Eij=Cij×IRj×tj (1) 式中, Eij 为微环境 (j) 中污染物(i) 的日吸入剂量, μg·d−1; Cij为微环境 (j) 中污染物 (i) 的浓度, 即室内羰基化合物的实测浓度, μg·m−3; IRj 是微环境中的吸入率 (j) , m3·h−1, 2岁以下儿童IRj为0.22 m3·h−1, 2—6岁儿童为0.33 m3·h−1; tj 是在微环境 (j) 中的暴露时间, 即儿童每天在室内度过的时间, h·d−1, 2岁以下儿童tj为21.37 h·d−1 , 2—6岁儿童为20.15 h·d−1. IRj和tj 数据均来源于中国人群暴露参数手册(儿童卷)概要[27].
根据最近的研究中采用的方法[26, 28], 对儿童而言, 需要调整无显著风险水平(no significant risk levels, NSRLs) [26] , 调整后的儿童特定NSRLs: 2 岁以下儿童, 甲醛、乙醛分别为 0.52 μg·d−1、1.16 μg·d−1; 2—6岁儿童, 甲醛、乙醛分别为 3.15 μg·d−1、7.08 μg·d−1. 此外, 用风险商(risk quotients, RQ)来表示健康风险, RQ 的计算方法是将儿童每日吸入剂量除以儿童特定的 NSRLs. RQ >1 表明儿童吸入剂量超过了 10−5 终生致癌风险阈值, 即儿童面临潜在的癌症风险.
1.5 气味污染评价方法
除了对人体健康造成影响外, 羰基化合物还会产生气味污染. 羰基化合物的质量浓度高并不意味着其气味强度也大, 而是与气味阈值共同呈比例地影响人体对气味的感知. 为了将污染物的浓度和气味强度联系起来, 需要对其气味进行污染评价. 气味污染评价中羰基化合物的气味强度用气味活性值(odor activity value, OAV)表示[13, 29]:
OAVi=CmiCti (2) 式中, OAVi 为污染物 i 的气味活性值, 无量纲; Cmi为污染物 i 的质量浓度, μg·m−3; Cti为污染物 i 的气味阈值, μg·m−3, 其取自日本环境卫生中心对有害气体污染物气味阈值的研究结果[30].
污染物的气味活性值以大多数正常人的感官为准, OAVi ≤1 表示一般人无法感知到污染物 i 的气味; OAVi >1可感知到污染物 i 所散发的气味, 且 OAVi 越大, 能感知到的气味越大, 即其气味强度越大.
2. 结果与讨论 (Results and discussion)
2.1 羰基化合物的浓度水平
室内环境中羰基化合物的质量浓度为(144.3±56.2) μg·m−3, 其中甲醛(25.5%)、丙酮(19.1%)和乙醛(15.0%)是含量最高的3种物质, 其平均浓度分别为(36.8±21.0) μg·m−3、(27.5±14.3) μg·m−3、(21.7±14.4) μg·m−3, 均明显高于室外浓度(图1). 这3类羰基化合物的来源与居住者的生活息息相关, 可从建筑材料、环境烟草烟雾、烹饪油烟、香味消费品、个人护理产品、清洁等人为活动或通过室内VOCs(尤其是萜烯)的氧化排放[31-33]. 室内高分子量羰基化合物(C6—C10)占比也比较大, 约27.7%(15.9%—45.9%), C6—C10平均浓度(39.9 μg·m−3)是室外(9.0 μg·m−3)的4.4倍. 研究表明, 己醛不仅包含在香料和香精中, 还存在于含有植物化学物质的食物和办公家具[34]. 辛醛有很强的水果香味, 可用作食用香料, 也可作肥皂洗涤剂的香料使用. 壬醛具有玫瑰、柑橘等香气, 存在于红茶、绿茶中. 室外大气环境中羰基化合物的质量浓度为(63.0±21.8) μg·m−3, 其中丙酮浓度最高((14.4±4.8) μg·m−3), 其次是甲醛((13.5±6.8) μg·m−3)和乙醛((11.0±4.3) μg·m−3), 这3类化合物约占室外总羰基化合物浓度的61.8%. I/O 比值(室内/室外)能更好地推断室内羰基化合物的可能影响因素(室内源或室外渗透). 由图1可知, 乙二醛(Gly)和甲基乙二醛(mGly)的I/O 比值均低于1.0, 表明这两类典型的α-二羰基物质可能更多的来自室外环境的渗透. 研究发现, 室外大气环境中乙二醛和甲基乙二醛主要来源于生物质燃烧和挥发性有机化合物(如异戊二烯、芳烃和烯烃)的氧化[35-36]. 值得注意的是,低分子量的羰基化合物甲醛、乙醛、丙酮和高分子量羰基化合物(C6—C10)的 I/O 比值明显较高(1.9—11.8),说明室内排放源对这些羰基化合物有显著贡献.
从表2和表3中可以看出, 室内环境中非供暖季浓度最高的5种羰基化合物为甲醛、丙酮、辛醛、乙醛和壬醛, 其浓度范围分别为(17.6—49.9) μg·m−3、(13.1—18.3) μg·m−3、(8.3—19.3) μg·m−3、(7.6—12.9) μg·m−3和(4.0—8.8) μg·m−3. 而供暖季则为甲醛、丙酮、乙醛、壬醛和己醛, 其浓度范围分别为(23.2—86.7) μg·m−3、(31.2—47.8) μg·m−3、(24.1—48.5) μg·m−3、(14.9—18.9) μg·m−3和(10.8—30.0) μg·m−3, 均明显高于非供暖季. 该结果与有关包头市城区住宅羰基化合物污染水平的研究结果一致, 可能与供暖季住宅内温湿度、通风换气次数以及室外环境状况等因素有关[20]. 整体来看,无论供暖季还是非供暖季, 住宅室内环境中最丰富的3类羰基化合物均为甲醛、乙醛和丙酮, 这与国内其它城市(北京、大连、上海、武汉和长沙等)的研究结果一致[26]. 另外, 本文所关注的3类高分子量羰基化合物(己醛、辛醛和壬醛)占比也较高(14.4%—33.0%)(图2). Feng 等[37]研究发现,餐饮油烟可能是造成空气中高分子量羰基化合物浓度偏高的原因之一. 由此可见, 室内高分子量的羰基化合物可能来源于住户的烹饪活动. 室外大气环境中羰基化合物浓度表现为非供暖季(68.9±28.2) μg·m−3明显高于供暖季(55.3±9.4) μg·m−3, 其中甲醛浓度增量最大(6.6 μg·m−3), 其次是辛醛(3.5 μg·m−3)和甲基乙二醛(2.5 μg·m−3), 这归因于非供暖季温度偏高, 太阳辐射较强, 有利于大气有机物发生光化学反应, 同时非供暖季植物排放对羰基化合物有重要的贡献.
表 3 非供暖季室内外环境中羰基化合物浓度Table 3. Concentrations of carbonyl compounds in indoor and outdoor environments in non-heating season羰基化合物Carbonyl compounds 平均值±标准偏差 (AVG±SD)/(μg·m−3) QJ-1 QJ-2 QJ-3 QJ-4 QJ-5 QJ-O 甲醛(C1) 49.9 ± 11.1 19.9 ± 2.3 22.4 ± 3.1 32.2 ± 7.9 17.6 ± 2.1 16.3 ± 8.2 乙醛(C2) 12.9 ± 2.8 8.7 ± 1.5 9.7 ± 2.9 12.1 ± 4.1 7.6 ± 1.9 10.1 ± 5.4 丙酮(A3K) 17.8 ± 4.1 18.3 ± 3.9 17.0 ± 6.7 16.8 ± 6.2 13.1 ± 3.6 14.1 ± 5.7 丙醛(C3) 2.1 ± 0.7 1.3 ± 0.0 1.4 ± 0.4 2.1 ± 0.6 0.9 ± 0.2 1.0 ± 0.2 2-丁酮(MEK) 2.8 ± 0.7 2.4 ± 0.4 2.5 ± 0.5 3.7 ± 2.1 4.0 ± 2.7 3.9 ± 1.4 丁醛(i,n-C4) 1.3 ± 0.2 1.1 ± 0.1 1.4 ± 0.1 1.5 ± 0.5 3.1 ± 4.1 2.5 ± 2.3 苯甲醛(Benz) 2.3 ± 0.6 2.1 ± 0.8 1.9 ± 0.8 2.7 ± 1.1 1.2 ± 0.2 1.5 ± 1.0 异戊醛(i-C5) 1.7 ± 0.4 1.2 ± 0.3 0.9 ± 0.1 2.3 ± 1.8 1.0 ± 0.2 1.2 ± 0.3 正戊醛(n-C5) 0.9 ± 0.3 1.1 ± 0.3 0.8 ± 0.3 1.0 ± 0.5 0.4 ± 0.2 0.5 ± 0.1 邻甲苯甲醛(o-tol) bda bd bd bd bd bd 间甲苯甲醛(m-tol) 1.1 ± 0.4 1.1 ± 0.5 1.1 ± 0.6 0.9 ± 0.2 1.0 ± 0.5 0.8 ± 0.5 对甲苯甲醛(p-tol) 0.4 ± 0.0 0.2 ± 0.0 0.3 ± 0.1 0.2 ± 0.0 0.3 ± 0.2 0.4 ± 0.2 2,5-二甲基苯甲醛(2,5-DB) 1.2 ± 0.7 0.7 ± 0.2 0.8 ± 0.4 0.9 ± 0.2 0.4 ± 0.1 0.3 ± 0.1 己醛(C6) 6.1 ± 1.9 8.1 ± 2.4 5.1 ± 2.4 5.0 ± 1.7 1.4 ± 0.2 0.9 ± 0.2 庚醛(C7) 3.5 ± 1.6 1.9 ± 0.5 1.6 ± 0.7 2.7 ± 1.1 0.9 ± 0.2 0.8 ± 0.3 辛醛(C8) 15.8 ± 5.0 19.3 ± 5.6 19.2 ± 10.4 13.6 ± 4.5 8.3 ± 2.1 4.4 ± 1.2 壬醛(C9) 8.8 ± 3.4 5.6 ± 1.1 4.2 ± 1.9 8.4 ± 3.0 4.0 ± 0.9 3.1 ± 1.5 癸醛(C10) 7.2 ± 2.8 4.6 ± 0.9 3.4 ± 1.6 7.0 ± 2.5 3.3 ± 0.7 2.5 ± 1.3 乙二醛(Gly) 0.3 ± 0.1 0.3 ± 0.2 0.4 ± 0.4 0.3 ± 0.2 0.5 ± 0.5 1.0 ± 0.9 甲基乙二醛(mGly) 1.7 ± 0.5 1.9 ± 0.7 1.9 ± 1.0 2.0 ± 0.6 2.0 ± 0.9 3.5 ± 2.2 总和 137.7 ± 35.0 100.0 ± 17.2 95.8 ± 29.5 115.4 ± 37.6 70.9 ± 10.8 68.9 ± 28.2 注: a bd 低于检测下限。represents below limit of detection. 室内环境中甲醛、乙醛、丙酮的浓度范围分别为(17.6—86.7) μg·m−3、(7.6—48.5) μg·m−3、(13.1—47.8) μg·m−3, 不同住户室内羰基化合物浓度差异明显, 这可能与不同的生活习惯以及装修样式等因素有关[20-21]. 具体来看, 供暖季QJ-1室内甲醛平均浓度((86.7±10.8) μg·m−3)明显超过2022年7月11日国家市场监督管理总局(国家标准化管理委员会)批准发布的新版标准(GB/T 18883—2022) [38]中提到的室内甲醛1小时平均浓度(80 μg·m−3), 可能与该住宅在采样前期新增家具(床和衣柜)有关. QJ-3供暖季室内乙醛浓度((48.5±8.9) μg·m−3)比日本厚生劳动省出台的室内乙醛浓度限值(48 μg·m−3)略高[39]; 整体来看, QJ-1—QJ-5室内丙醛浓度均未超过加拿大卫生部报道的暴露限值(8 μg·m−3), 丙醛达到该限值的临界效应表现为嗅觉上皮萎缩[40].
图2为供暖季与非供暖季住宅室内外空气中羰基化合物的浓度占比. 从图2可以看出, 低分子量的甲醛、乙醛和丙酮对室内外空气中羰基化合物的贡献较大, 占总羰基化合物浓度的47.0%—73.0%, 且供暖季的占比显著高于非供暖季, 其中乙醛占比全部表现为供暖季 > 非供暖季; 结合表2和表3浓度数据发现, 室内外环境中的乙醛浓度也均表现为供暖季 > 非供暖季. 值得注意的是, QJ-2无论是供暖季还是非供暖季, 己醛、辛醛和壬醛这3类羰基化合物的占比之和都超过 30%, 而甲醛、乙醛和丙酮占比之和较其它住宅偏低,推测是因为该住宅内选择瓷砖铺设且家具量较少. 此外, 与其它住户相比, QJ-2选用液化石油气作为烹饪燃料可能对室内羰基化合物的污染情况也有影响,需进一步研究.
2.2 羰基化合物的影响因素
2.2.1 通风换气次数
诸多研究表明, 通风换气次数越大, 室内污染物浓度越小[20,29]. 为了解室内的通风状况, 本研究采用CO2示踪气体衰减法[29,41]计算得到各住宅供暖季和非供暖季的通风换气次数(表4). 该方法以CO2为示踪气体, 当室内CO2浓度比室外高时, 由于室内外的空气交换,室内CO2浓度会呈指数衰减, 式(3)为该过程中的质量守恒方程, 经推导可将CO2浓度与换气次数的关系写成式(4), 再通过线性回归计算, 即可求得室内的换气次数[29].
表 4 供暖季与非供暖季住户通风换气次数Table 4. The air exchange rate of households in heating season and non-heating season采样点Site 供暖季Heating season 非供暖季Non-Heating season 范围/h−1Range 平均值±标准偏差/h−1Mean±SD 范围/h−1Range 平均值±标准偏差/h−1Mean±SD QJ-1 0.1—0.7 0.3 ± 0.2 2.6—23.5 8.5 ± 8.6 QJ-2 0.4—0.8 0.6 ± 0.2 4.2—13.4 7.0 ± 3.8 QJ-3 0.2—0.6 0.4 ± 0.2 3.2—34.5 12.1 ± 15.0 QJ-4 0.2—0.5 0.4 ± 0.1 3.0—21.6 10.3 ± 8.8 QJ-5 0.1—0.6 0.3 ± 0.2 5.8—48.6 16.7 ± 18.0 VdCindτ=G(Cout−Cin) (3) ln(Cin−Cout)=ln(Cin,0−Cout)−ACHτ (4) 式中, Cin为室内CO2实时浓度, mg·m−3; Cout为室外CO2浓度, mg·m−3; G为通风量, m3·h−1; ACH为每小时换气次数, h−1; τ为时间, h; Cin,0表示室内CO2初始浓度, mg·m−3.
如表4所示, 供暖季室内通风换气次数为(0.1—0.8) h−1, 非供暖季为(2.6—48.6) h−1, 非供暖季换气次数比供暖季高1—2个数量级. 显然, 高频率的通风换气次数是非供暖季室内环境中羰基化合物浓度显著低于供暖季的原因. 但是, 室内羰基化合物的浓度还受室内温湿度、烹饪活动、人员情况(人员数量、人员类型等)、生活习性(个人护理产品、卫浴产品使用等)以及室外污染状况等其它诸多因素影响[31-33,37]. 此外, 室内外环境中二元醛(Gly+mGly)浓度则表现为非供暖季高于供暖季, 而且室内二元醛浓度随着室外浓度的增加而增加, 进一步表明室外源对室内贡献明显.
2.2.2 周末效应
“周末效应”的概念在 1974 年被Cleveland 等[42]首次提出. 研究表明, 大气污染物质量浓度变化在工作日和周末存在明显差异, 这种变化被称为“周末效应”[43-44]. 周末效应源于工作和休息模式的节律性, 与人类活动密切相关. 本文采用如下方式量化周末效应(ΔWE)[44-46]:
ΔWE=[(C周末−C工作日)/C工作日] (5) 式中, C工作日 表示工作日的浓度均值, C周末 表示周末的浓度均值. 为保持数据一致性, 本研究中C工作日 采用周五的污染物浓度, C周末 采用周六的污染物浓度.
图3绘制了供暖季(a)和非供暖季(b)住宅室内外空气中羰基化合物浓度的相对偏差. 从图3可以看出, 供暖季, 不同住宅室内环境中羰基化合物的周末效应并不一致, 除QJ-5外, 其余4户住宅室内甲醛和丙酮浓度周末相比工作日增加, 分别增加了12.3%—32.3%、15.9%—69.4%; 高分子量羰基化合物(C6—C10)也表现出周末浓度高于工作日的“周末效应”. 室外大气环境中甲醛和乙醛浓度周末相比工作日减少, 分别减少了15.3% 和13.7%, 而丙酮则增加了26.7%; 高分子量的羰基化合物(C6—C10)浓度降幅超过30%. 非供暖季, “周末效应”更明显, 无论室内环境还是室外大气, 甲醛、乙醛、丙酮、壬醛、癸醛、乙二醛和甲基乙二醛均表现出工作日浓度高于周末的“周末效应”. 室内环境中甲醛、乙醛和丙酮周末浓度相较于工作日分别减少了15.9%—34.6%、30.7%—45.6%、30.6%—55.1%; 室外大气中这三类污染物浓度同样是周末低于工作日, 分别减少了51.0%、53.1%和53.6%.
综上所述, 住宅室内环境中, 供暖季多数羰基化合物呈周末高于工作日的“周末效应”, 非供暖季则呈工作日高于周末的“周末效应”; 这归因于供暖季室外较低的温度, 居民周末更多选择室内活动以及低频的通风换气次数导致室内环境中多数羰基化合浓度周末高于工作日; 而非供暖季相对较好的通风条件使室内外羰基化合物浓度的“周末效应”变化一致, 均表现为周末低于工作日. 室外环境中羰基化合物浓度不受季节变化影响, 均呈现工作日高于周末的“周末效应”. 研究发现, 在典型的城市地区PM2.5具有明显的工作日偏高, 周末偏低的“周末效应”[46]. 由此可见, 室外羰基化合物受到人类活动、污染排放和气象等各种因素的综合影响.
2.3 健康风险评估
表5总结了各住户室内儿童每日吸入甲醛和乙醛的剂量. 2岁以下儿童的甲醛和乙醛日吸入量最高值分别为313.9 μg·d−1和121.1 μg·d−1, 2—6岁的儿童甲醛和乙醛日最高吸入量分别为457.5 μg·d−1和176.5 μg·d−1. 可发现随着年龄的增长, 身体不断发育, 儿童羰基污染物吸入剂量增加. 供暖季室内甲醛、乙醛浓度高于非供暖季, 因此供暖季节室内羰基化合物污染情况更值得关注.
表 5 各住户室内儿童每日吸入的甲醛和乙醛剂量及风险商Table 5. Daily inhalation doses and risk quotients of formaldehyde and acetaldehyde by children in each household甲醛Formaldehyde 乙醛Acetaldehyde 采样点Site 2岁以下Birth to < 2 years 2—6 岁2 years to < 6 years 2岁以下Birth to < 2 years 2—6 岁2 years to < 6 years 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients QJ-1 313.9 609.0 457.5 145.4 117.9 101.6 171.9 24.3 QJ-2 99.2 192.4 144.5 45.9 75.4 65.1 109.9 15.5 QJ-3 140.2 272.1 204.4 64.9 121.1 104.4 176.5 24.9 QJ-4 145.0 281.3 211.3 67.1 85.5 73.7 124.6 17.6 QJ-5 137.4 266.6 200.3 63.6 82.9 71.5 120.9 17.1 儿童特定的无显著风险水平用于表征儿童在家中接触甲醛和乙醛的健康风险[26]. 如表5所示,每户儿童接触甲醛和乙醛的风险商均远大于1, 表明各住户儿童皆面临潜在的癌症风险. 2岁以下儿童甲醛暴露RQ值为192.4—609.0, 2—6岁儿童甲醛暴露RQ值为45.9—145.4, 即儿童的甲醛暴露量是“安全限”水平的数十至数百倍. 2岁以下儿童乙醛暴露RQ值为65.1—104.4, 2—6岁儿童乙醛暴露RQ值为15.5—24.9. 与乙醛相比, 儿童在家接触甲醛对其健康的影响相对更大. 这与Bradman 等[28]研究中甲醛暴露的 RQ 值(12.0—51.7)高于乙醛暴露的 RQ 值(2.3—9.8)的结果一致.
需指出, 在计算儿童吸入甲醛和乙醛的剂量时, 只考虑了儿童在住宅中接触羰基化合物的情况, 如果还考虑到儿童在学校等其它室内环境接触羰基化合物, 患癌风险会更大. 因此, 室内羰基化合物污染对儿童健康的影响, 需要居民和标准制定者高度重视. 此外, 由于缺乏指南和风险指数, 其它含量较高的羰基化合物(例如己醛和壬醛)的化学危害潜力或癌症风险无法系统地评估.
2.4 气味污染评价
各住户室内环境中不同污染物对应的气味活性值如表6所示. 在分析各住宅所散发的羰基化合物成分时, 检测到较高浓度的甲醛、乙醛和丙酮, 但由于甲醛和丙酮的气味阈值相对较高, 因此这两种高浓度污染物的气味活性要低得多, 只有乙醛的气味活性更明显, 其气味活性值均大于5. 各住宅室内环境中高分子量的己醛、庚醛、辛醛、壬醛和癸醛的气味活性值均大于1, 尤其是辛醛最大, 均大于100, 其次是己醛. 对于广泛用作装修和家居的木质材料释放的气味物质——辛醛具有肥皂和柑橘味, 己醛具有香草味. 吴可[29]研究发现, 装修完工后室内环境中的气味污染主要来自于庚醛、辛醛、壬醛和己醛等醛类污染物. 而且这些高分子量的醛类污染物释放量在臭氧的影响下还会随时间而增加[47]. 因此, 室内环境中羰基化合物的气味污染更多应关注高分子量羰基化合物. 已有研究表明, 室内不良的气味感知是病态建筑综合征(sick building syndrome, SBS)的危险因素, 高分子量的羰基化合物对SBS的影响相当明显, 己醛对SBS的一般症状的危险性达到了显著性水平, 癸醛和辛醛对SBS的皮肤症状的危险性也达到了显著性水平[48]. 所以, 考虑针对室内环境中高分子量羰基化合物规定限值亦十分必要.
表 6 各住宅室内污染物的气味活性值Table 6. Odor activity values of indoor pollutants in various residences羰基化合物Carbonyl compounds 气味阈值/(μg·m−3)Odor threshold 气味活性值Odor activity value QJ-1 QJ-2 QJ-3 QJ-4 QJ-5 甲醛 670.3 0.10 0.03 0.05 0.05 0.04 乙醛 3.0 8.7 5.6 8.9 6.3 6.1 丙酮 108900.0 <0.01 <0.01 <0.01 <0.01 <0.01 丙醛 2.6 1.4 0.9 1.1 1.0 0.9 2-丁酮 1416.4 <0.01 <0.01 <0.01 <0.01 <0.01 丁醛 1.6 1.3 1.1 1.3 1.2 1.7 异戊醛 0.4 6.7 5.1 4.7 6.3 5.4 正戊醛 1.6 1.1 1.8 1.1 1.0 0.7 己醛 1.3 7.1 15.2 7.4 6.3 4.9 庚醛 0.8 5.1 4.0 3.5 3.9 2.7 辛醛 0.06 187.8 220.4 232.1 169.1 126.3 壬醛 2.2 5.8 5.6 4.0 5.4 4.8 癸醛 2.8 1.8 1.5 1.1 2.2 1.2 3. 结论(Conclusion)
本研究选择5户城市住宅进行同步观测, 对室内外空气环境中痕量羰基化合物的浓度水平、影响因素、健康风险及气味污染展开研究. 通过分析, 得出以下结论:
(1)居民住宅室内外环境中总羰基化合物浓度变化表现为: 室内 > 室外; 室内供暖季 > 室内非供暖季; 室外供暖季 < 室外非供暖季; 室内外空气中甲醛、乙醛和丙酮3类羰基化合物比重高(47.0%—73.0%), 室内高分子量的羰基化合物(C6—C10)总浓度(39.9 μg·m−3)是室外(9.0 μg·m−3)的4倍多. 季节变化表明, 通风换气次数对室内环境中羰基化合物污染影响显著.
(2)供暖季室内多数羰基化合物呈周末高于工作日的“周末效应”, 非供暖季则呈工作日高于周末的“周末效应”. 室外环境中羰基化合物浓度不受季节影响均呈现工作日高于周末的“周末效应”.
(3)健康风险评估显示各住户儿童甲醛和乙醛的吸入剂量均远超过OEHHA 给出的暴露剂量安全限值, 表明各家庭的儿童都面临潜在的癌症风险. 住宅室内环境中主要气味污染来自于气味阈值较低的高分子量羰基化合物, 包括己醛、庚醛、辛醛、壬醛和癸醛.
需指出, 本研究中样本量并不是很充足, 但室内外同步观测结果也能反映城市住宅室内外空气中痕量羰基化合物不同季节的污染情况; 此外, 不同住户家庭成员的数量以及不同的生活习惯等因素对室内羰基污染物的影响各不相同, 关于这部分讨论还有待于进一步的研究. 尽管如此, 这些痕量羰基化合物的测定对我国室内空气质量监管的来源分配和数据保存仍具有价值.
-
表 1 各采样住户家庭信息
Table 1. Household information of each sampled household
采样点Site 房屋年龄/aAge of house 面积/m2Area 装修后放置时间/monthStorage time after decoration 地板材质Floor material 壁纸Wall-paper 取暖燃料Fuel for heating 烹饪燃料Fuel for cooking 每天烹饪次数Cooking frequency 通风方式Ventilation 吸烟Smoking QJ-1 5 100 6—12 客厅+卧室复合木地板 是 天然气 天然气 > 3 半开 否 > 1 h QJ-2 5 100 6—12 客厅+卧室瓷砖 否 天然气 液化石油气 > 3 半开 否 > 1 h QJ-3 5 102 6—12 客厅+卧室复合木地板 否 天然气 天然气 1 半开 否 电 < 1 h QJ-4 5 100 3—6 客厅+卧室复合竹地板 是 天然气 天然气 3 半开 否 < 1 h QJ-5 5 148 3—6 客厅瓷砖卧室复合木地板 否 天然气 天然气 3 全开 否 < 1 h 表 2 供暖季室内外环境中羰基化合物浓度
Table 2. Concentrations of carbonyl compounds in indoor and outdoor environments in heating season
羰基化合物Carbonyl compounds 方法检测限/(µg·mL−1)Method detection limit 平均值±标准偏差 (AVG±SD)/( μg·m−3) QJ-1 QJ-2 QJ-3 QJ-4 QJ-5 QJ-O 甲醛(C1) 0.002 86.7 ± 10.8 23.2 ± 5.1 40.7 ± 2.8 30.9 ± 6.4 46.3 ± 6.9 9.7 ± 1.3 乙醛(C2) 0.004 38.4 ± 6.1 24.1 ± 5.7 48.5 ± 8.9 25.1 ± 5.0 31.9 ± 7.9 12.2 ± 2.6 丙酮(A3K) 0.006 46.5 ± 11.9 35.5 ± 13.9 47.8 ± 5.9 32.2 ± 10.3 31.2 ± 4.5 14.9 ± 4.4 丙醛(C3) 0.004 4.9 ± 0.7 3.5 ± 1.0 4.6 ± 0.5 3.1 ± 0.8 4.3 ± 0.2 2.3 ± 0.4 2-丁酮(MEK) 0.005 3.5 ± 0.6 3.2 ± 0.9 5.3 ± 1.0 3.3 ± 1.1 4.5 ± 0.3 3.1 ± 0.6 丁醛(i,n-C4) 0.003 2.9 ± 0.4 2.4 ± 0.7 3.0 ± 0.3 2.4 ± 0.6 2.5 ± 0.1 1.4 ± 0.3 苯甲醛(Benz) 0.007 1.9 ± 0.2 1.8 ± 0.4 2.9 ± 0.3 2.2 ± 0.7 1.9 ± 0.2 1.0 ± 0.2 异戊醛(i-C5) 0.004 3.4 ± 0.6 2.7 ± 0.7 3.0 ± 0.3 2.6 ± 0.6 3.6 ± 0.3 1.7 ± 0.4 正戊醛(n-C5) 0.005 2.4 ± 0.4 4.5 ± 1.4 3.0 ± 0.3 2.2 ± 0.7 2.1 ± 0.3 0.6 ± 0.2 邻甲苯甲醛(o-tol) 0.006 0.5 ± 0.1 0.6 ± 0.3 0.4 ± 0.1 0.5 ± 0.4 0.7 ± 0.2 0.1 ± 0.1 间甲苯甲醛(m-tol) 0.004 0.5 ± 0.1 0.5 ± 0.1 0.5 ± 0.2 0.5 ± 0.2 0.5 ± 0.2 0.5 ± 0.1 对甲苯甲醛(p-tol) 0.003 0.3 ± 0.1 0.6 ± 0.2 0.5 ± 0.2 0.3 ± 0.2 0.4 ± 0.2 0.2 ± 0.0 2,5-二甲基苯甲醛(2,5-DB) 0.003 0.6 ± 0.1 0.7 ± 0.2 0.6 ± 0.2 0.6 ± 0.1 0.5 ± 0.2 0.5 ± 0.2 己醛(C6) 0.007 11.8 ± 2.5 30.0 ± 7.7 14.9 ± 1.6 10.8 ± 4.6 12.6 ± 2.5 0.9 ± 0.2 庚醛(C7) 0.011 4.7 ± 1.0 4.5 ± 1.2 4.6 ± 0.1 3.6 ± 0.7 3.9 ± 0.8 0.8 ± 0.3 辛醛(C8) 0.016 5.6 ± 1.0 5.9 ± 1.5 5.5 ± 0.5 5.8 ± 1.7 5.8 ± 1.5 0.9 ± 0.3 壬醛(C9) 0.017 16.4 ± 2.8 18.6 ± 5.1 15.0 ± 1.1 14.7 ± 3.2 18.9 ± 5.9 2.1 ± 0.5 癸醛(C10) 0.001 2.9 ± 0.5 3.5 ± 2.2 2.8 ± 0.8 5.4 ± 0.8 3.3 ± 0.9 0.6 ± 0.2 乙二醛(Gly) 0.001 0.4 ± 0.1 0.7 ± 0.1 0.4 ± 0.1 0.4 ± 0.1 0.4 ± 0.1 0.8 ± 0.4 甲基乙二醛(mGly) 0.001 0.6 ± 0.2 0.9 ± 0.2 0.7 ± 0.2 0.8 ± 0.2 1.1 ± 0.2 1.0 ± 0.2 总和(SUM) 235.1±33.9 167.3 ± 38.7 204.7 ± 11.6 147.2 ± 33.1 176.3 ± 25.7 55.3 ± 9.4 表 3 非供暖季室内外环境中羰基化合物浓度
Table 3. Concentrations of carbonyl compounds in indoor and outdoor environments in non-heating season
羰基化合物Carbonyl compounds 平均值±标准偏差 (AVG±SD)/(μg·m−3) QJ-1 QJ-2 QJ-3 QJ-4 QJ-5 QJ-O 甲醛(C1) 49.9 ± 11.1 19.9 ± 2.3 22.4 ± 3.1 32.2 ± 7.9 17.6 ± 2.1 16.3 ± 8.2 乙醛(C2) 12.9 ± 2.8 8.7 ± 1.5 9.7 ± 2.9 12.1 ± 4.1 7.6 ± 1.9 10.1 ± 5.4 丙酮(A3K) 17.8 ± 4.1 18.3 ± 3.9 17.0 ± 6.7 16.8 ± 6.2 13.1 ± 3.6 14.1 ± 5.7 丙醛(C3) 2.1 ± 0.7 1.3 ± 0.0 1.4 ± 0.4 2.1 ± 0.6 0.9 ± 0.2 1.0 ± 0.2 2-丁酮(MEK) 2.8 ± 0.7 2.4 ± 0.4 2.5 ± 0.5 3.7 ± 2.1 4.0 ± 2.7 3.9 ± 1.4 丁醛(i,n-C4) 1.3 ± 0.2 1.1 ± 0.1 1.4 ± 0.1 1.5 ± 0.5 3.1 ± 4.1 2.5 ± 2.3 苯甲醛(Benz) 2.3 ± 0.6 2.1 ± 0.8 1.9 ± 0.8 2.7 ± 1.1 1.2 ± 0.2 1.5 ± 1.0 异戊醛(i-C5) 1.7 ± 0.4 1.2 ± 0.3 0.9 ± 0.1 2.3 ± 1.8 1.0 ± 0.2 1.2 ± 0.3 正戊醛(n-C5) 0.9 ± 0.3 1.1 ± 0.3 0.8 ± 0.3 1.0 ± 0.5 0.4 ± 0.2 0.5 ± 0.1 邻甲苯甲醛(o-tol) bda bd bd bd bd bd 间甲苯甲醛(m-tol) 1.1 ± 0.4 1.1 ± 0.5 1.1 ± 0.6 0.9 ± 0.2 1.0 ± 0.5 0.8 ± 0.5 对甲苯甲醛(p-tol) 0.4 ± 0.0 0.2 ± 0.0 0.3 ± 0.1 0.2 ± 0.0 0.3 ± 0.2 0.4 ± 0.2 2,5-二甲基苯甲醛(2,5-DB) 1.2 ± 0.7 0.7 ± 0.2 0.8 ± 0.4 0.9 ± 0.2 0.4 ± 0.1 0.3 ± 0.1 己醛(C6) 6.1 ± 1.9 8.1 ± 2.4 5.1 ± 2.4 5.0 ± 1.7 1.4 ± 0.2 0.9 ± 0.2 庚醛(C7) 3.5 ± 1.6 1.9 ± 0.5 1.6 ± 0.7 2.7 ± 1.1 0.9 ± 0.2 0.8 ± 0.3 辛醛(C8) 15.8 ± 5.0 19.3 ± 5.6 19.2 ± 10.4 13.6 ± 4.5 8.3 ± 2.1 4.4 ± 1.2 壬醛(C9) 8.8 ± 3.4 5.6 ± 1.1 4.2 ± 1.9 8.4 ± 3.0 4.0 ± 0.9 3.1 ± 1.5 癸醛(C10) 7.2 ± 2.8 4.6 ± 0.9 3.4 ± 1.6 7.0 ± 2.5 3.3 ± 0.7 2.5 ± 1.3 乙二醛(Gly) 0.3 ± 0.1 0.3 ± 0.2 0.4 ± 0.4 0.3 ± 0.2 0.5 ± 0.5 1.0 ± 0.9 甲基乙二醛(mGly) 1.7 ± 0.5 1.9 ± 0.7 1.9 ± 1.0 2.0 ± 0.6 2.0 ± 0.9 3.5 ± 2.2 总和 137.7 ± 35.0 100.0 ± 17.2 95.8 ± 29.5 115.4 ± 37.6 70.9 ± 10.8 68.9 ± 28.2 注: a bd 低于检测下限。represents below limit of detection. 表 4 供暖季与非供暖季住户通风换气次数
Table 4. The air exchange rate of households in heating season and non-heating season
采样点Site 供暖季Heating season 非供暖季Non-Heating season 范围/h−1Range 平均值±标准偏差/h−1Mean±SD 范围/h−1Range 平均值±标准偏差/h−1Mean±SD QJ-1 0.1—0.7 0.3 ± 0.2 2.6—23.5 8.5 ± 8.6 QJ-2 0.4—0.8 0.6 ± 0.2 4.2—13.4 7.0 ± 3.8 QJ-3 0.2—0.6 0.4 ± 0.2 3.2—34.5 12.1 ± 15.0 QJ-4 0.2—0.5 0.4 ± 0.1 3.0—21.6 10.3 ± 8.8 QJ-5 0.1—0.6 0.3 ± 0.2 5.8—48.6 16.7 ± 18.0 表 5 各住户室内儿童每日吸入的甲醛和乙醛剂量及风险商
Table 5. Daily inhalation doses and risk quotients of formaldehyde and acetaldehyde by children in each household
甲醛Formaldehyde 乙醛Acetaldehyde 采样点Site 2岁以下Birth to < 2 years 2—6 岁2 years to < 6 years 2岁以下Birth to < 2 years 2—6 岁2 years to < 6 years 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients 吸入剂量/(μg·d−1) Daily inhalation dose 风险商Risk Quotients QJ-1 313.9 609.0 457.5 145.4 117.9 101.6 171.9 24.3 QJ-2 99.2 192.4 144.5 45.9 75.4 65.1 109.9 15.5 QJ-3 140.2 272.1 204.4 64.9 121.1 104.4 176.5 24.9 QJ-4 145.0 281.3 211.3 67.1 85.5 73.7 124.6 17.6 QJ-5 137.4 266.6 200.3 63.6 82.9 71.5 120.9 17.1 表 6 各住宅室内污染物的气味活性值
Table 6. Odor activity values of indoor pollutants in various residences
羰基化合物Carbonyl compounds 气味阈值/(μg·m−3)Odor threshold 气味活性值Odor activity value QJ-1 QJ-2 QJ-3 QJ-4 QJ-5 甲醛 670.3 0.10 0.03 0.05 0.05 0.04 乙醛 3.0 8.7 5.6 8.9 6.3 6.1 丙酮 108900.0 <0.01 <0.01 <0.01 <0.01 <0.01 丙醛 2.6 1.4 0.9 1.1 1.0 0.9 2-丁酮 1416.4 <0.01 <0.01 <0.01 <0.01 <0.01 丁醛 1.6 1.3 1.1 1.3 1.2 1.7 异戊醛 0.4 6.7 5.1 4.7 6.3 5.4 正戊醛 1.6 1.1 1.8 1.1 1.0 0.7 己醛 1.3 7.1 15.2 7.4 6.3 4.9 庚醛 0.8 5.1 4.0 3.5 3.9 2.7 辛醛 0.06 187.8 220.4 232.1 169.1 126.3 壬醛 2.2 5.8 5.6 4.0 5.4 4.8 癸醛 2.8 1.8 1.5 1.1 2.2 1.2 -
[1] TANG X J, BAI Y, DUONG A, et al. Formaldehyde in China: Production, consumption, exposure levels, and health effects [J]. Environment International, 2009, 35(8): 1210-1224. doi: 10.1016/j.envint.2009.06.002 [2] MCGWIN G, LIENERT J, KENNEDY J I. Formaldehyde exposure and asthma in children: A systematic review [J]. Environmental Health Perspectives, 2010, 118(3): 313-317. doi: 10.1289/ehp.0901143 [3] DAI W T, ZHONG H B, LI L J, et al. Characterization and health risk assessment of airborne pollutants in commercial restaurants in northwestern China: Under a low ventilation condition in wintertime [J]. Science of the Total Environment, 2018, 633: 308-316. doi: 10.1016/j.scitotenv.2018.03.124 [4] VILLANUEVA F, LARA S, NOTARIO A, et al. Formaldehyde, acrolein and other carbonyls in dwellings of university students. Levels and source characterization [J]. Chemosphere, 2022, 288: 132429. doi: 10.1016/j.chemosphere.2021.132429 [5] WU C, XU B, SHI S S, et al. Time-activity pattern observatory from mobile web logs [J]. International Journal of Embedded Systems, 2015, 7(1): 71. doi: 10.1504/IJES.2015.066144 [6] ZHOU X J, LIU Y F, LIU J P. Alternately airtight/ventilated emission method: A universal experimental method for determining the VOC emission characteristic parameters of building materials [J]. Building and Environment, 2018, 130: 179-189. doi: 10.1016/j.buildenv.2017.12.025 [7] LIANG W H, YANG X D. Indoor formaldehyde in real buildings: Emission source identification, overall emission rate estimation, concentration increase and decay patterns [J]. Building and Environment, 2013, 69: 114-120. doi: 10.1016/j.buildenv.2013.08.009 [8] SALEM M Z M, BÖHM M, SRBA J, et al. Evaluation of formaldehyde emission from different types of wood-based panels and flooring materials using different standard test methods [J]. Building and Environment, 2012, 49: 86-96. doi: 10.1016/j.buildenv.2011.09.011 [9] KIM J A, KIM S, KIM H J, et al. Evaluation of formaldehyde and VOCs emission factors from paints in a small chamber: The effects of preconditioning time and coating weight [J]. Journal of Hazardous Materials, 2011, 187(1/2/3): 52-57. [10] REINGRUBER H, PONTEL L B. Formaldehyde metabolism and its impact on human health [J]. Current Opinion in Toxicology, 2018, 9: 28-34. doi: 10.1016/j.cotox.2018.07.001 [11] BORAN S, USTA M, GÜMÜŞKAYA E. Decreasing formaldehyde emission from medium density fiberboard panels produced by adding different amine compounds to urea formaldehyde resin [J]. International Journal of Adhesion and Adhesives, 2011, 31(7): 674-678. doi: 10.1016/j.ijadhadh.2011.06.011 [12] CHAN C S, RANASINGHE R S A, HO S S H, et al. Evaluation of hazardous airborne carbonyls in five urban roadside dwellings: A comprehensive indoor air assessment in Sri Lanka [J]. Atmospheric Pollution Research, 2018, 9(2): 270-277. doi: 10.1016/j.apr.2017.10.002 [13] JIANG C J, LI D D, ZHANG P Y, et al. Formaldehyde and volatile organic compound (VOC) emissions from particleboard: Identification of odorous compounds and effects of heat treatment [J]. Building and Environment, 2017, 117: 118-126. doi: 10.1016/j.buildenv.2017.03.004 [14] SHI S S, CHEN C, ZHAO B. Air infiltration rate distributions of residences in Beijing [J]. Building and Environment, 2015, 92: 528-537. doi: 10.1016/j.buildenv.2015.05.027 [15] STEINEMANN A. Ten questions concerning air fresheners and indoor built environments [J]. Building and Environment, 2017, 111: 279-284. doi: 10.1016/j.buildenv.2016.11.009 [16] GAO K, XIE J R, YANG X D. Estimation of the contribution of human skin and ozone reaction to volatile organic compounds (VOC) concentration in aircraft cabins [J]. Building and Environment, 2015, 94: 12-20. doi: 10.1016/j.buildenv.2015.07.022 [17] XIONG J Y, HE Z C, TANG X C, et al. Modeling the time-dependent concentrations of primary and secondary reaction products of ozone with squalene in a university classroom [J]. Environmental Science & Technology, 2019, 53(14): 8262-8270. [18] LUI K H, HO S S H, LOUIE P K K, et al. Seasonal behavior of carbonyls and source characterization of formaldehyde (HCHO) in ambient air [J]. Atmospheric Environment, 2017, 152: 51-60. doi: 10.1016/j.atmosenv.2016.12.004 [19] LV Y, ZHOU Y W, CHEN X, et al. Study on indoor and outdoor permeability coefficients and bacterial components, sources of fine particles in severe cold region of China [J]. Sustainable Cities and Society, 2020, 55: 102020. doi: 10.1016/j.scs.2020.102020 [20] 黄晓影. 包头市城区住宅醛酮污染水平及其影响因素分析[D]. 包头: 内蒙古科技大学, 2017. HUANG X Y. Characteristics of carbonyls in Baotou urban residences: Levels and factor[D]. Baotou: Inner Mongolia University of Science and Technology, 2017(in Chinese).
[21] PU Z N, HUANG L H, YUE Y, et al. Characteristics of carbonyls in Beijing urban residences: Concentrations, source strengths and influential factors [J]. Procedia Engineering, 2015, 121: 2052-2059. doi: 10.1016/j.proeng.2015.09.206 [22] HUANG C, LIU W, CAI J, et al. Household formaldehyde exposure and its associations with dwelling characteristics, lifestyle behaviours, and childhood health outcomes in Shanghai, China [J]. Building and Environment, 2017, 125: 143-152. doi: 10.1016/j.buildenv.2017.08.042 [23] 戴文婷. 关中含氧挥发性有机物对臭氧和二次有机气溶胶形成影响[D]. 西安: 中国科学院地球环境研究所, 2020. DAI W T. Distribution of oxygenated volatile organic compunds in the Guanzhong basin and their impacts on ozone and secondary organic aerosols formation[D]. Xi'an: Institute of Earth Environment, Chinese Academy of Sciences, 2020(in Chinese).
[24] LANDRIGAN P J. Children as a vulnerable population [J]. Human and Ecological Risk Assessment:An International Journal, 2005, 11(1): 235-238. doi: 10.1080/10807030590920051 [25] MATZ C J, STIEB D M, DAVIS K, et al. Effects of age, season, gender and urban-rural status on time-activity: Canadian Human Activity Pattern Survey 2 (CHAPS 2) [J]. International Journal of Environmental Research and Public Health, 2014, 11(2): 2108-2124. doi: 10.3390/ijerph110202108 [26] FAN G T, XIE J C, YOSHINO H, et al. Concentration characteristics of gaseous carbonyl compounds in urban houses in two different climatic zones of China and health risk assessment for schoolchildren [J]. Sustainable Cities and Society, 2020, 60: 102270. doi: 10.1016/j.scs.2020.102270 [27] 段小丽. 中国人群暴露参数手册(儿童卷)概要[M]. 北京: 中国环境科学出版社, 2016. DUAN X L. Highlight of Chinese children's exposure factors handbook [M]. Beijing: China Environmental Science Press, 2016(in Chinese).
[28] BRADMAN A, GASPAR F, CASTORINA R, et al. Formaldehyde and acetaldehyde exposure and risk characterization in California early childhood education environments [J]. Indoor Air, 2017, 27(1): 104-113. doi: 10.1111/ina.12283 [29] 吴可. 新装修住宅室内VOCs及其污染影响的长期变化特征研究[D]. 南京: 南京理工大学, 2020. WU K. Study on the long-term variation characteristics of indoor VOCs and pollution impact in newly decorated buildings[D]. Nanjing: Nanjing University of Science and Technology, 2020(in Chinese).
[30] NAGATA Y. Measurement of odor threshold value of odor substances by triangle odor bag method[R]. Meeting of the Japan Society of Air Pollution, 1988. [31] SALTHAMMER T. Formaldehyde sources, formaldehyde concentrations and air exchange rates in European housings [J]. Building and Environment, 2019, 150: 219-232. doi: 10.1016/j.buildenv.2018.12.042 [32] YAMASHITA S, KUME K, HORIIKE T, et al. A simple method for screening emission sources of carbonyl compounds in indoor air [J]. Journal of Hazardous Materials, 2010, 178(1/2/3): 370-376. [33] MISHRA N, BARTSCH J, AYOKO G A, et al. Volatile organic compounds: Characteristics, distribution and sources in urban schools [J]. Atmospheric Environment, 2015, 106: 485-491. doi: 10.1016/j.atmosenv.2014.10.052 [34] UENO H, SHIMADA A, SUEMITSU S, et al. Hexanal inhalation affects cognition and anxiety-like behavior in mice [J]. Zeitschrift Fur Naturforschung C, Journal of Biosciences, 2020, 75(11/12): 409-415. [35] LIU J W, LI X, YANG Y M, et al. An IBBCEAS system for atmospheric measurements of glyoxal and methylglyoxal in the presence of high NO2 concentrations [J]. Atmospheric Measurement Techniques, 2019, 12: 4439-4453. doi: 10.5194/amt-12-4439-2019 [36] ZOGKA A, ROMANIAS M, THEVENET F. Formaldehyde and glyoxal measurement deploying a selected ion flow tube mass spectrometer (SIFT-MS) [J]. Atmospheric Measurement Techniques, 2022, 15(7): 2001-2019. doi: 10.5194/amt-15-2001-2022 [37] FENG Y L, WEN S, CHEN Y J, et al. Ambient levels of carbonyl compounds and their sources in Guangzhou, China [J]. Atmospheric Environment, 2005, 39(10): 1789-1800. doi: 10.1016/j.atmosenv.2004.10.009 [38] 国家市场监督管理总局, 国家标准化管理委员会. 室内空气质量标准: GB/T 18883—2022[S]. 2022. State Administration for Market Regulation, Standardization Administration of the People's Republic of China. Standards for indoor air quality: GB/T 18883—2022[S]. 2022(in Chinese).
[39] AZUMA K, UCHIYAMA I, UCHIYAMA S, et al. Assessment of inhalation exposure to indoor air pollutants: Screening for health risks of multiple pollutants in Japanese dwellings [J]. Environmental Research, 2016, 145: 39-49. doi: 10.1016/j.envres.2015.11.015 [40] HEALTH CANADA. Residential indoor air quality guidelines [EB/OL]. [2022-8-16]. [41] YOU Y, NIU C, ZHOU J, et al. Measurement of air exchange rates in different indoor environments using continuous CO2 sensors [J]. Journal of Environmental Sciences, 2012, 24(4): 657-664. doi: 10.1016/S1001-0742(11)60812-7 [42] CLEVELAND W S, GRAEDEL T E, KLEINER B, et al. Sunday and workday variations in photochemical air pollutants in new jersey and New York [J]. Science, 1974, 186(4168): 1037-1038. doi: 10.1126/science.186.4168.1037 [43] KOO B, JUNG J, POLLACK A K, et al. Impact of meteorology and anthropogenic emissions on the local and regional ozone weekend effect in Midwestern US [J]. Atmospheric Environment, 2012, 57: 13-21. doi: 10.1016/j.atmosenv.2012.04.043 [44] 王俊秀. 南京北郊大气污染物对局地臭氧生成效率的影响[D]. 南京: 南京信息工程大学, 2017. WANG J X. The effect of atmospheric pollutants on local ozone production efficiency in northern suburb of Nanjing[D]. Nanjing: Nanjing University of Information Science & Technology, 2017(in Chinese).
[45] 楚芳婕, 孙爽, 李令军, 等. 2018—2020年北京市交通监测站点大气污染特征分析 [J]. 中国环境科学, 2021, 41(12): 5548-5560. doi: 10.3969/j.issn.1000-6923.2021.12.010 CHU F J, SUN S, LI L J, et al. Characteristics of the atmospheric pollutants at traffic monitoring sites in Beijing during 2018—2020 [J]. China Environmental Science, 2021, 41(12): 5548-5560(in Chinese). doi: 10.3969/j.issn.1000-6923.2021.12.010
[46] 李建东. 上海大气污染的季节特征及周末效应的研究[D]. 西安: 中国科学院研究生院(地球环境研究所), 2015. LI J D. Seasonal characteristics of air pollution and weekend effect in Shanghai[D]. Xi'an: Institute of Earth Environment, Chinese Academy of Sciences, 2015(in Chinese).
[47] NICOLAS M, RAMALHO O, MAUPETIT F. Reactions between ozone and building products: Impact on primary and secondary emissions [J]. Atmospheric Environment, 2007, 41(15): 3129-3138. doi: 10.1016/j.atmosenv.2006.06.062 [48] 刘雨晴. 家庭环境中挥发性有机污染物暴露特征及风险评估[D]. 天津: 天津大学, 2019. LIU Y Q. Exposure characteristics and risk assessment of volatile organic compounds in household environment[D]. Tianjin: Tianjin University, 2019(in Chinese).
期刊类型引用(1)
1. 崔敏,刘劲毅,侯筱筱,韩缘欣,张帆,李嘉. 生物柴油机械羰基化合物排放特征及环境效应研究. 实验技术与管理. 2024(11): 52-57 .  百度学术
百度学术
其他类型引用(0)
-






 DownLoad:
DownLoad: