-
塑料自出现以来极大地方便了人们的生活,其需求量和使用量不断增加,因此大量塑料垃圾进入并积累于环境中,在光照、热解、机械磨损以及生物作用下破碎形成粒径更小的塑料颗粒,其中直径小于5 mm的被定义为微塑料(microplastics,MPs)[1-2]. 微塑料作为一种新型污染物,广泛分布于水体、土壤、大气等环境介质中,在太平洋、大西洋、印度洋沿岸和深海地区,土壤及生物体内都能够检测到大量的微塑料[3-4],对生态环境安全及生物生存造成了严重的威胁[1]. 微塑料具有较大的比表面积,能够吸附大量的环境污染物,因此能够成为重金属、有机污染物等环境污染物质的运输载体,进一步增加其他环境污染物的风险[5]. 近期,重金属与微塑料之间的相互作用已成为环境领域关注的热点. 由于工业开采、金属冶炼、污泥回用等导致大量的重金属镉(Cd)进入土壤,造成严重的镉污染[6]. 据统计,我国Cd污染耕地土壤面积达2×105 km2,约占全国耕地总量的1/6,严重影响农业生产和粮食安全[7]. 重金属Cd具有高稳定性、不易降解、且易在生物体内累积的特点[8-9],严重威胁着人体健康和环境安全[10]. 同时,农业生产使用的大量农膜被遗留在环境中能够逐渐破碎形成微塑料,与重金属Cd形成复合污染[11]. 已有研究表明微塑料对水体环境中的重金属具有一定的富集作用[12],如海滩上微塑料表面镉、铬、铜、铁、锰、镍、铅、锌等重金属含量比周边海域中的重金属浓度高[13-14]. 然而,关于微塑料对Cd环境行为影响的研究仍存在不足.
微塑料吸附重金属还能影响其迁移特性与生物毒性,Boucher等[15]研究发现在潮汐带沉积物中,微塑料能够吸附重金属,而生物摄入微塑料后,重金属也随之进入食物链. 研究表明,微塑料吸附的重金属可能会在水体和肠道中被重新释放,从而使其生物毒性增加[16]. 镉与微塑料的复合污染对鲤鱼血浆中的酶活性、生化指标及免疫等具有明显的生物毒性效应,且二者表现出明显的协同作用[17]. 微塑料与重金属联合作用可导致海水青鳉肠道污染负荷增加,特定肠道微生物及肠道功能发生变化,免疫系统抵抗力受到明显抑制[18]. 目前,尚未有统一的方法对重金属与微塑料联合毒性进行测定. 研究发现,发光细菌毒性测定法具有高灵敏度、强相关性、快速、高自动化程度等特点,在重金属、有机物污染环境中的综合毒性分析中已得到广泛的应用[19]. 利用发光菌对取代苯酚和镉的混合物进行生物毒性测定,结果表明二者之间存在微弱的加成作用或近似加成作用的弱协同效应[19].
此外,环境中的微塑料在多种因素作用下逐渐发生老化,导致微塑料表面的氧化结合位点增多,对重金属及其他污染物的吸附能力增强[20],因此老化微塑料的吸附能力通常高于原始微塑料. 研究自然环境中老化微塑料对其他污染物环境行为的影响具有现实意义. 尽管已有国内外学者对实验室条件下微塑料与其他环境污染物的吸附进行了研究,但对于老化微塑料的研究仍不充分,且尚无一致定论.
微塑料高级氧化过程与自然老化过程中的氧化途径及老化产物具有极高的相似性[21],可克服自然环境中微塑料的老化速率极低的问题. 因此本研究采用热活化K2S2O8高级氧化法加速微塑料老化以获取不同老化程度的微塑料. 通过室内模拟实验,研究不同老化程度的微塑料对重金属的吸附动力学和吸附等温线的影响,以及在不同pH、微塑料浓度下对重金属的吸附,进一步探讨不同老化程度微塑料吸附行为的差异和作用机理. 采用发光菌毒性测试法对微塑料与重金属的复合污染的生物毒性进行测定,为复合污染的生物毒性评价提供科学依据.
-
微塑料聚乙烯(PE)、聚丙烯(PP)购于东莞市特塑朗化工原料,平均粒径约100 µm;镉标准溶液(1 mg·mL−1)购于北京北方伟业计量技术研究院;过硫酸钾(K2S2O8)购于天津市风船化学试剂科技有限公司,纯度为99%;明亮发光杆菌T3(Photobacterium phosphoreum T3)由中国科学院南京土壤研究所提供.
-
将微塑料用甲醇超声3次,每次20 min,再以超纯水洗涤3次于40 ℃干燥,密封保存、备用. 采用热活化K2S2O8高级氧化法进行微塑料老化[21],将1.0 g微塑料(PE、PP)加入到40 mL 100 mmol·L−1新鲜制备的pH 7.0的K2S2O8溶液中,于70 ℃恒温搅拌. 每12 h添加等量K2S2O8溶液,每2 天更换新鲜溶液以避免K2SO4积累. 分别于5、10、20 d取出老化的微塑料样品,清洗后于45 ℃烘干避光保存. 将老化微塑料分别记为PE5、PE10、PE20和PP5、PP10、PP20,初始微塑料分别记为PE0和PP0.
利用傅里叶红外光谱仪(FTIR)在分辨率4 cm−1条件下检测500—4000 cm−1区域老化前后微塑料的表面官能团变化,并利用扫描电镜(SEM)表征微塑料的表面形貌变化.
-
将镉标准溶液稀释至10 mg·L−1作为镉贮存液,并于4 ℃避光保存. 随后,进一步稀释成1 mg·L−1的镉吸附液. 在摇瓶中加入100 mL的镉吸附液,再分别加入0.2 g初始微塑料及不同老化程度的PE、PP微塑料,置于恒温摇床((25±2)°C、180 r·min−1)避光振荡72 h. 每处理重复3次,同时设置不添加微塑料的空白对照. 分别于0.5、1、3、6、12、24、36、48、60 h进行取样,过0.45 µm滤膜并稀释,采用火焰原子吸收分光光度计测定镉含量.
-
将镉贮存液准确地稀释至0.1、0.5、1、3、5、10 mg·L−1作为镉吸附液进行吸附等温线实验. 每100 mL镉吸附液添加0.2 g初始微塑料和老化20 d的微塑料,每处理重复3次,同时设置不添加微塑料的空白对照,于25 ℃,180 r·min−1振荡培养,并于24、48、72 h时取样. 将样品过0.45 µm滤膜并稀释,采用火焰原子吸收分光光度计对镉含量进行测定.
-
准确将镉贮存液稀释至1 mg·L−1,并用0.01 mol·L−1的NaOH和HNO3调节该溶液的pH,在不同pH(4、5、6、7、8)环境条件下进行微塑料对Cd的吸附,实验方法同1.4节.
将加入的微塑料浓度设为0.1、0.2、0.4、0.6 g·(100 mL) -1 以探究不同微塑料浓度对Cd吸附的影响,其实验方法同1.4节.
-
将达到吸附平衡的微塑料于40 ℃干燥,准确称取0.2 g吸附镉的微塑料,并向其中加入100 mL 3% 的NaCl溶液,并超声使微塑料均匀分散,于摇床中恒温振荡24 h过滤后以浸出液作为待测液,用于发光菌毒性测定. 将明亮发光杆菌T3接种于高温灭菌的专用培养基,其中每100 mL水中酵母浸出粉0.5 g,胰蛋白胨0.5 g,NaCl 3 g,Na2HPO4 0.5 g,KH2PO4 0.1 g,甘油0.3 g,pH值6.5,25 ℃避光培养20 h,于10000 r·min−1离心收集菌体并重悬于3% NaCl溶液以获得合适的菌体浓度. 取待测液180 μL于96孔板,随后加入20 µL重悬后的菌液,每样品重复3次. 同时,按照不同的微塑料吸附量,将镉贮存液稀释至与其相当,测定镉的生物毒性;按照0.2 g·100 mL−1测定微塑料的生物毒性,在微孔板上添加200 μL 3% 的NaCl溶液作为空白对照,于25 ℃下静置15 min,在450—490 nm波长下测定明亮发光杆菌的发光强度,并计算不同处理的发光强度抑制率.
-
数据统计和分析采用 Excel 2010,图表使用 Origin 2018;用 SPSS进行统计分析.
-
由图1可见,初始微塑料 PE、PP表面较光滑,而老化后微塑料表面的粗糙程度增加,并产生裂纹和孔隙,表面形貌更为破碎. 这一现象与以往的研究结果相似,即在老化过程中,微塑料表面的裂纹数目会增多,且裂缝深度会逐步扩展,会呈现碎片化现象[20]. 在老化作用下,微塑料的表面形态会发生变化,其比表面积、孔隙率可能增加,因此可能对其吸附性能造成一定的影响.
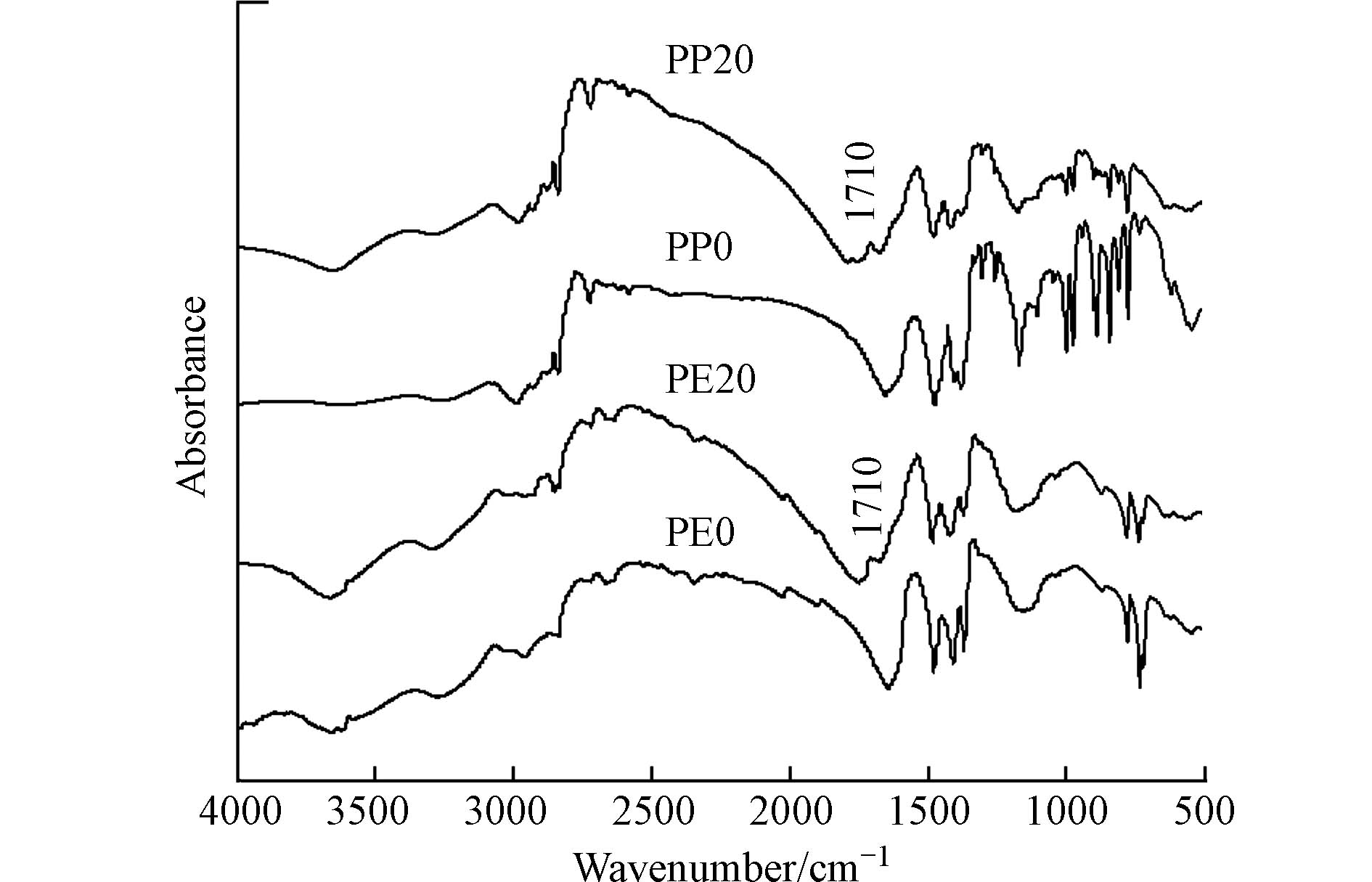
采用FTIR对老化前后的微塑料PE和PP表面官能进行表征. 由图2可见,老化后微塑料PE和PP在1710 cm−1出现新的红外吸收峰,其特征峰为甲酸/乙酸等羧酸基团(−CH2COOH),这表明老化能够使微塑料PE、PP表面发生官能团的氧化. 这一结果与Liu等[20]的研究结果一致,微塑料表面的含氧官能团的出现可能会使微塑料的亲水性得到改善[21],进而影响微塑料对重金属的吸附性能.
-
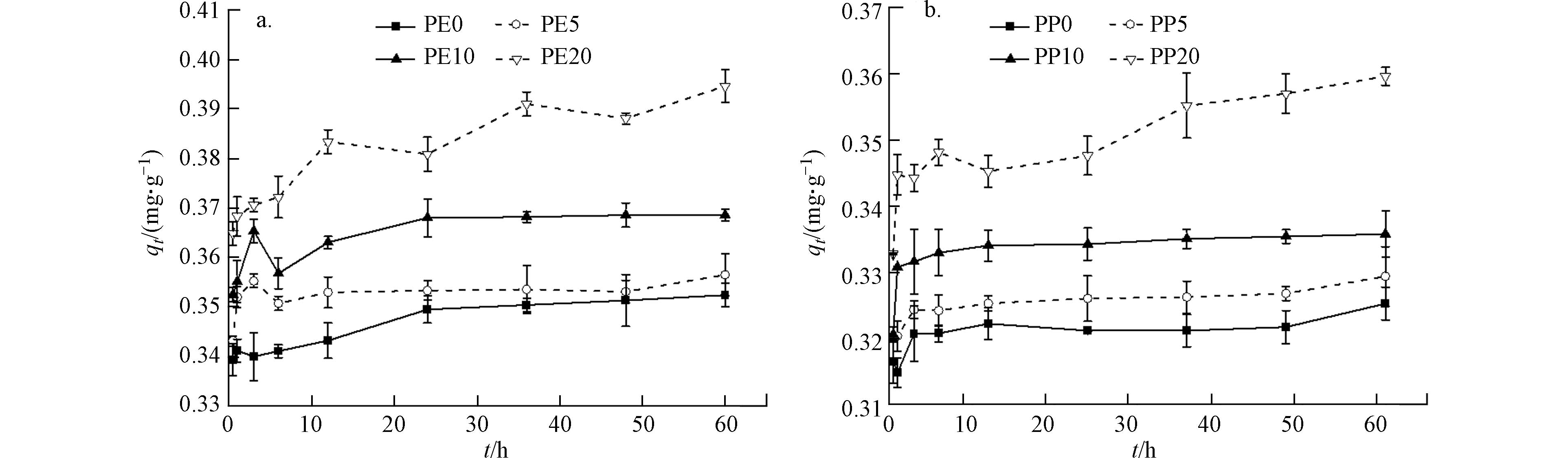
由图3可见,在不同的吸附时间下,微塑料PE、PP对重金属镉离子的吸附出现类似的变化,即随吸附时间延长,微塑料PE、PP对镉离子的吸附量都是增加的,而吸附速率均呈现先增加后减小的趋势. 由图3可见,吸附过程大致可分为3个阶段:0—10 h为快速吸附阶段,此时镉离子在微塑料上的吸附量约为其总量的1/2;10—30 h为第二阶段,微塑料PE、PP对镉离子的吸附速率逐步下降,此时微塑料上仍然有镉离子的吸附,但吸附速率逐渐降低;第三个阶段是30 h之后,吸附达到平衡. 这说明镉离子在微塑料上的吸附并不是瞬间完成的,而是一个由快速到缓慢的平衡过程.
通过微塑料的吸附实验,发现镉离子在微塑料上的吸附量依次为:PE20>PE10>PE5>PE0,PP20 >PP10 >PP5 >PP0. 由此可见,镉离子在老化微塑料的吸附量比初始微塑料的吸附量大,且随老化时间延长其吸附量增加,即微塑料吸附能力与老化时间具有正相关性. 这一发现与已有的研究结论一致,随着老化时间的推移,微塑料表面变得粗糙,其比表面积会增大,同时微塑料表面氧化结合位点、含氧官能团增多,这些都能导致微塑料表面负电性增大,与镉离子的络合作用增加,从而提高微塑料吸附镉离子的能力[22-23].
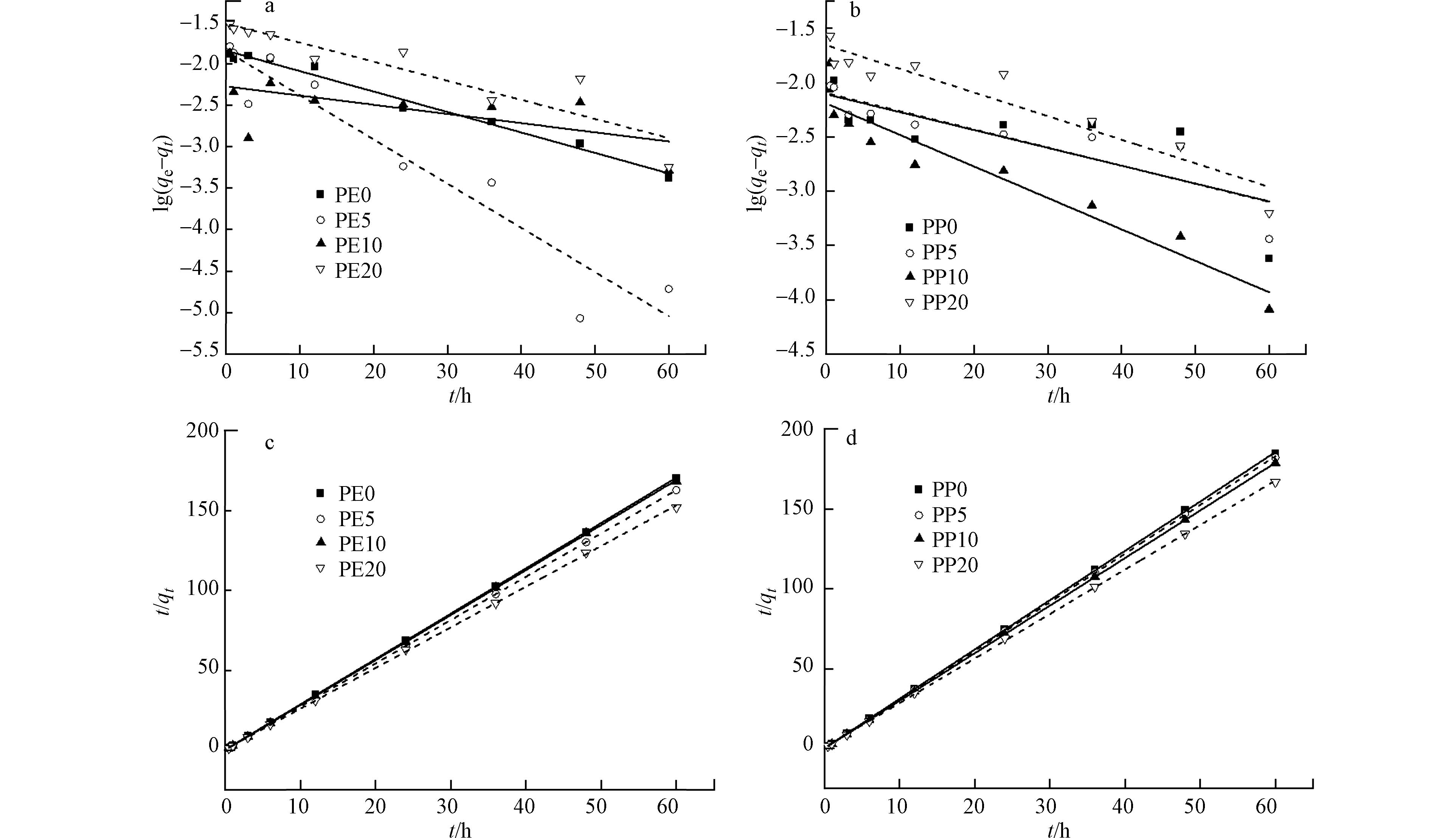
分别按照准一级动力学方程表达式(1)和准二级动力学方程表达式(2)对吸附动力学进行线性拟合,结果如图4所示. 由图4可见,按照准二级动力学方程表达式进行拟合时线性较好.
准一级动力学方程表达式:
其中,k1(h−1)一级吸附速率常数,qt(mg·g−1)为t时刻吸附量;qe(mg·g−1)为平衡时吸附量;t(h)为时间.
准二级动力学方程表达式为:
其中,k2(g·mg−1·h−1)为二级吸附速率常数.
同时,表1列出了相关的动力学模型参数,其中按照准二级动力学方程表达式计算获得的相关系数R2在0.9994—0.9999之间,而按照准一级动力学方程表达拟合获得的相关系数R2在0.3788—0.9971之间. 由此可见,准二级模型对于微塑料对镉离子的吸附动态特性拟合效果更佳,而准一级模型则不能很好地拟合. 这表明镉离子在微塑料上的吸附行为符合准二级动力学方程,微塑料对镉离子的吸附存在多个吸附阶段,物理吸附和化学吸附同时存在,其中以化学吸附为主.
-
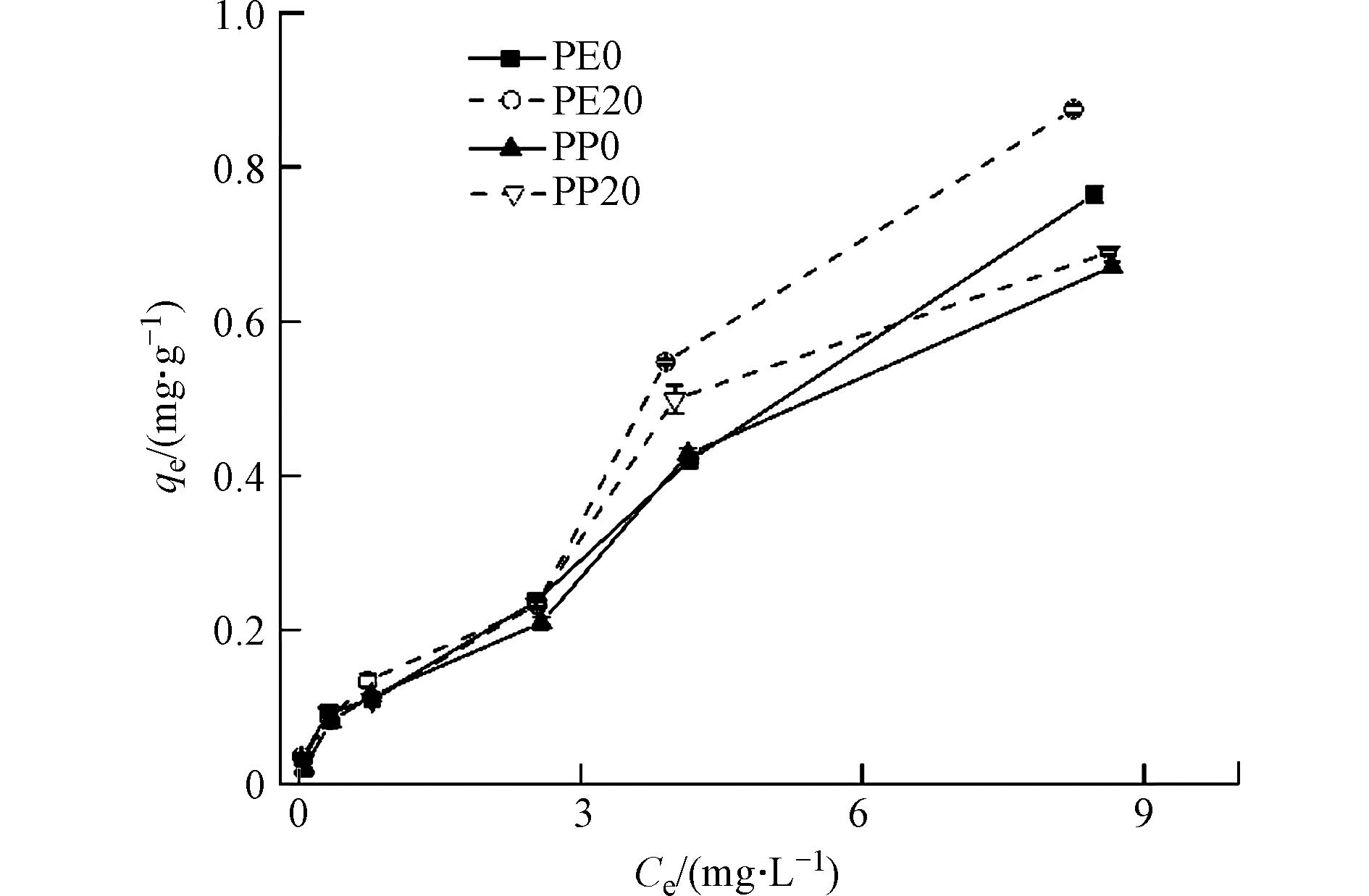
在25 ℃下,镉离子在微塑料PE、PP表面吸附达到平衡后,以平衡时溶液中镉离子浓度(Ce)为横坐标,以微塑料对镉离子的平衡吸附量为纵坐标绘图. 如图5所示,随着镉离子浓度增加,镉离子在微塑料PE、PP上的平衡吸附量也随之增加,但曲线的斜率却在不断降低. 这表明在镉离子浓度增加的同时微塑料表面镉的吸附量也逐渐增加,但其吸附速率却在逐渐降低. 这是由于微塑料与镉离子的吸附存在一定的定位性,即在较低浓度的镉离子溶液中,微塑料的表面存在大量的吸附位点,能够迅速吸附镉. 但随着镉离子浓度的升高,微塑料表面被占据的吸附点位也越来越多,吸附逐渐趋于饱和,进而影响吸附速率. 这表明镉离子的平衡吸附量与老化程度也存在一定的相关性,老化微塑料表面镉吸附量大于初始微塑料,即PE20 >PE0,PP20 >PP0. 由此可见,老化微塑料比初始微塑料具有更好的吸附性能,这也与老化微塑料表面形貌和官能团变化相关.
进一步利用Freundlich和Langmuir等温吸附模型对微塑料吸附等温线进行拟合,结果如图6和 表2所示. Freundlich和Langmuir模型拟合线性方程分别如公式(3)和(4)所示:
其中,KF为吸附平衡常数,n为吸附过程中的支持力.
其中,KL为平衡常数.
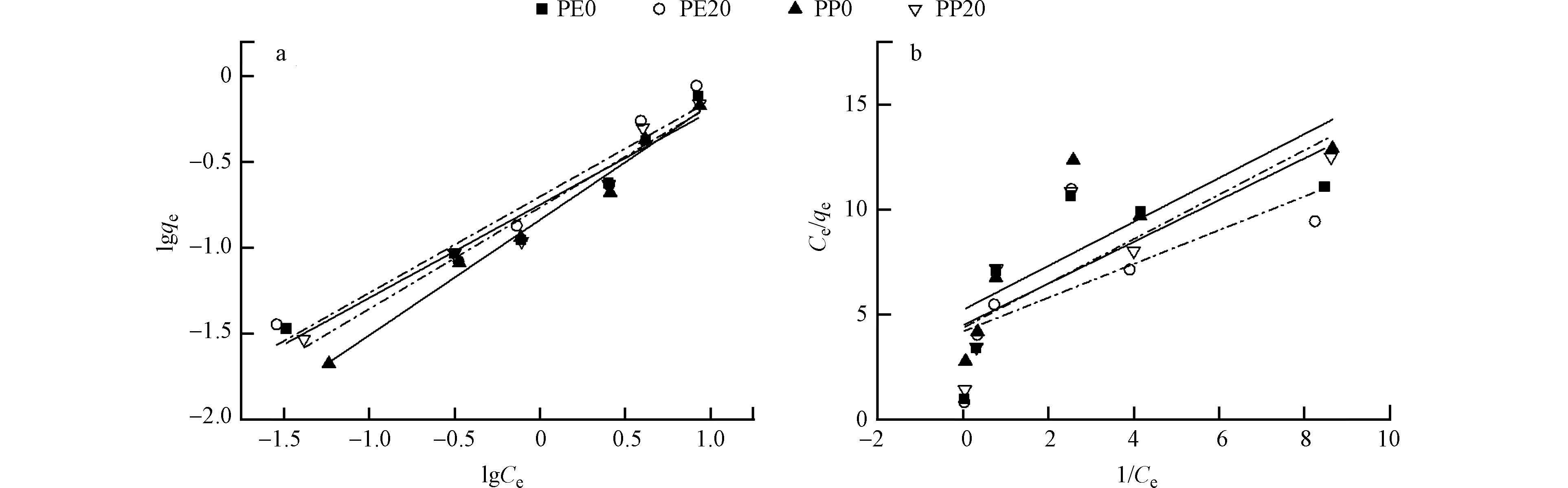
由表2中两种模型拟合的吸附等温线相关系数R2可以看出,Freundlich吸附模型R2的值在0.9694—0.9886之间,而Langmuir吸附模型R2的值在0.4516—0.6592之间,因此Freundlich等温模型能够较好地反映出镉离子在微塑料PE、PP上的吸附行为,即吸附等温线数据符合Freundlich吸附模型. 这一结果表明镉离子在微塑料 PE、PP上的吸附是非线性的,且其吸附过程具有不均匀性. 这与前人的研究结果相吻合[24],即镉离子先在微塑料表面的高能吸附点上进行吸附,再在低能吸附点上进行吸附. 这也进一步表明微塑料表面吸附镉的过程是由表面络合和静电引力共同控制的.
-
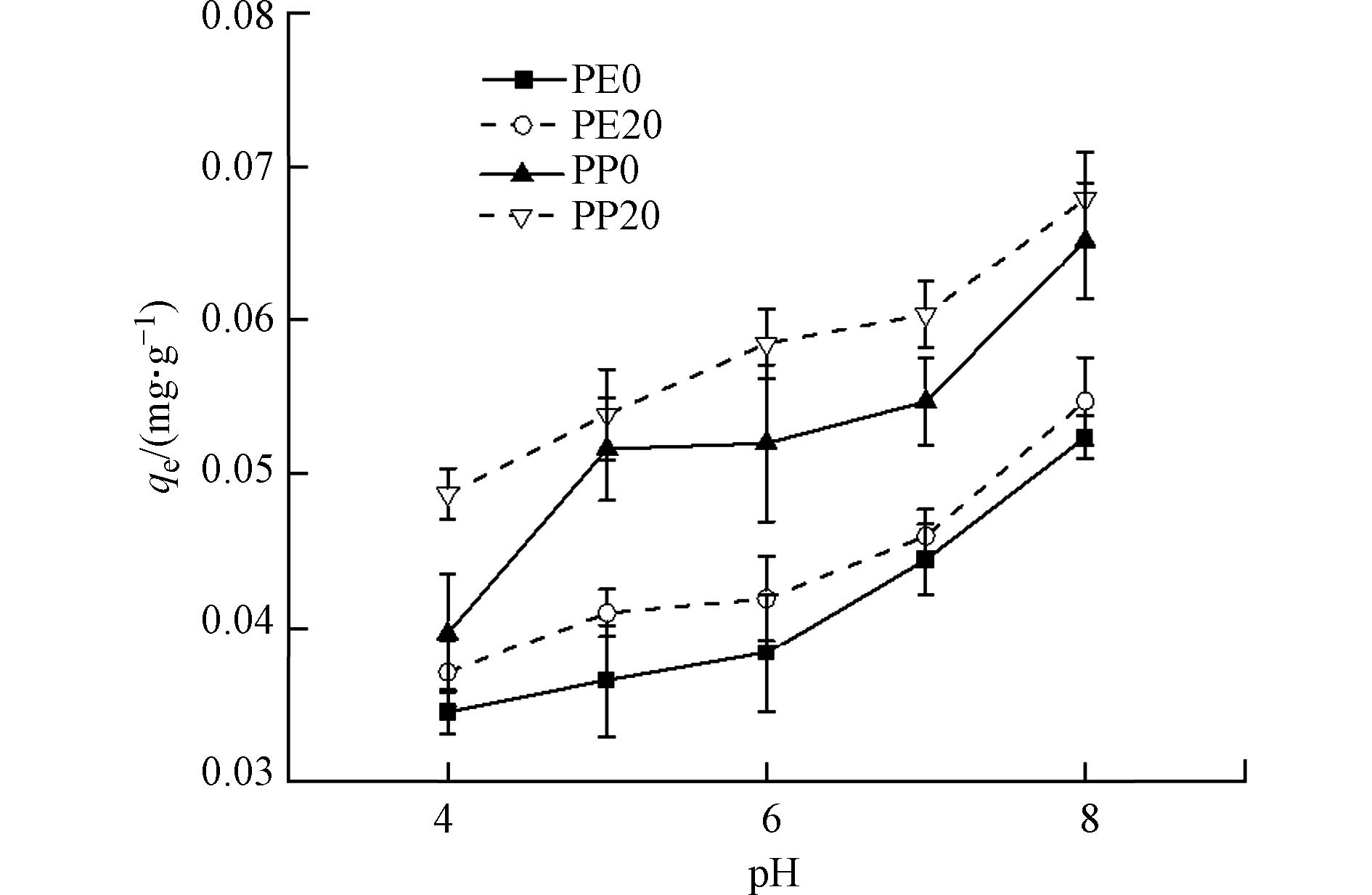
如图7所示,微塑料在不同pH值下对镉离子的吸附能力有所不同,随着 pH值的增加其吸附量增加,且老化微塑料对镉离子的吸附量大于初始微塑料. Brennecke等[25]研究发现,pH值对微塑料吸附镉离子的性能有很大影响,在低 pH值时,H+与镉离子能够竞争吸附点位导致微塑料对镉离子的吸附性能下降;而随着 pH值的增加,微塑料表面的官能团被去质子化,微塑料的负电性会增加,因此微塑料和镉离子间的静电作用会加强,微塑料吸附镉离子的能力则相应增加[25]. 这也进一步说明了静电作用对微塑料的吸附性能有很大的促进作用,微塑料吸附镉离子的主要机理可能是静电作用. 此外,受pH值的影响,老化及初始微塑料PP对镉离子的吸附量均高于PE,这可能与微塑料材质有关.
-
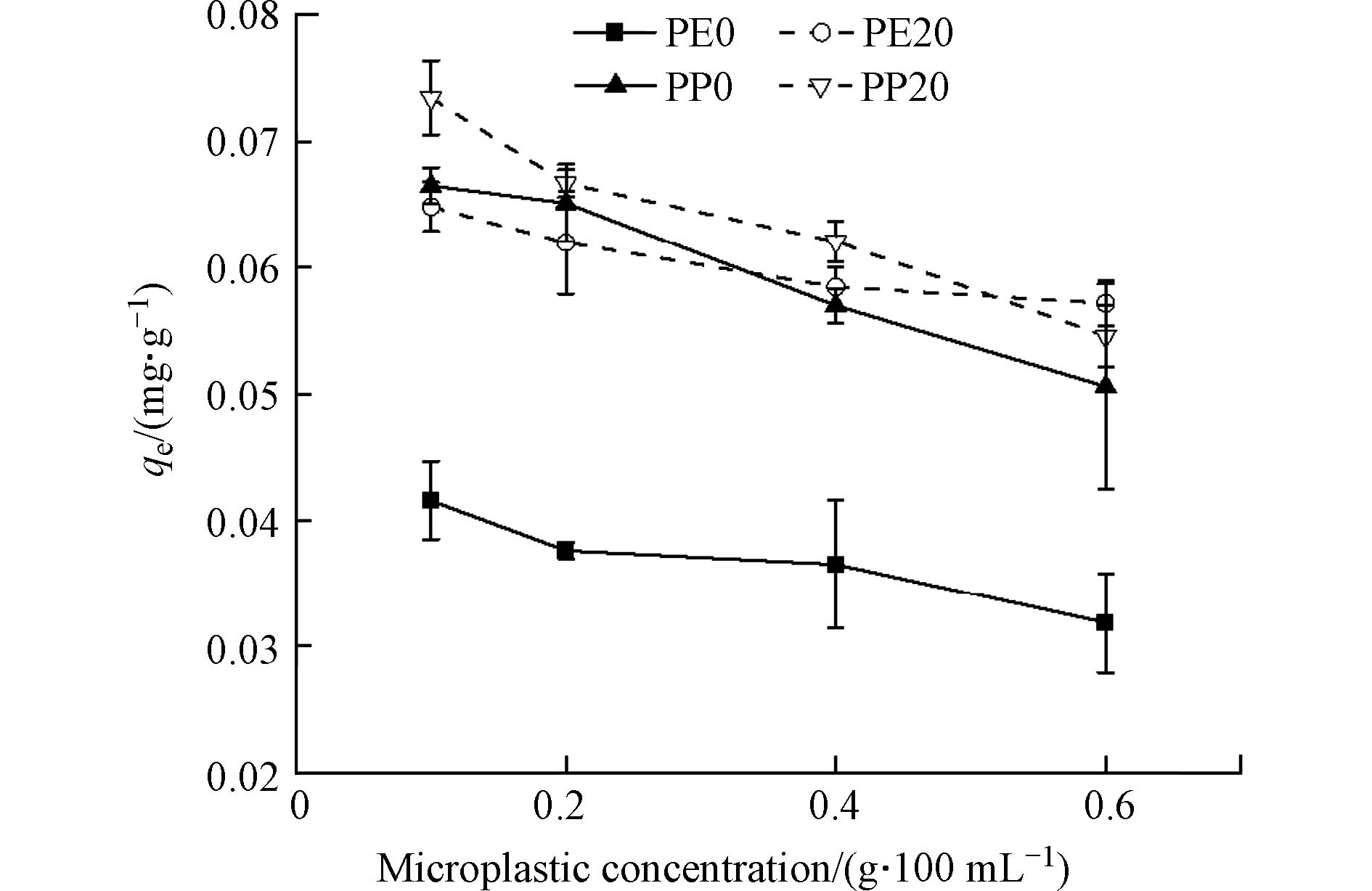
图8比较了不同微塑料浓度对镉离子的吸附量的影响. 由图8可见,在保持其它条件不变的情况下,随着微塑料浓度增加,两种类型微塑料对镉离子的吸附量皆会相应地下降. 但老化微塑料对镉离子的吸附量仍比初始微塑料大,这一研究结果与以往的研究结果相符,即当微塑料浓度较低时,微塑料在水中的分布比较均匀,可以很好地与水中的镉离子相结合[9]. 当微塑料的浓度升高时,微塑料的吸附点位会增多,使得微塑料颗粒间发生相互竞争,并且微塑料之间会发生相互黏合,使得在水中分散不均匀,与水中的镉离子接触不足,导致单位吸附量下降[9].
-
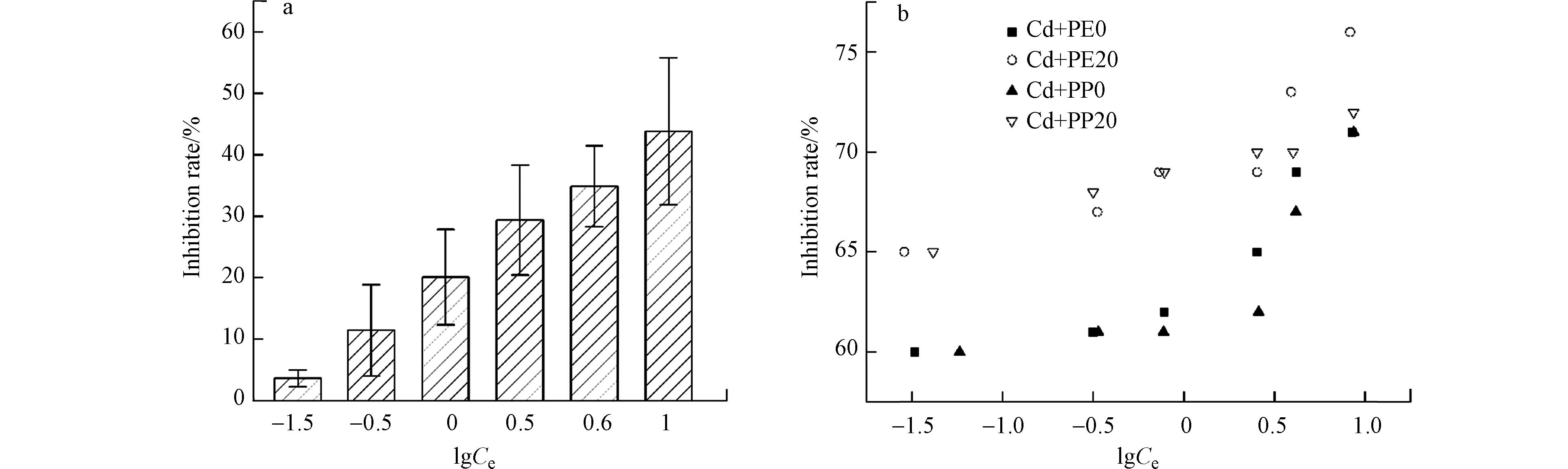
利用明亮发光杆菌T3对镉、微塑料及其二者的联合生物毒性进行测定,结果如图9所示. 初始微塑料对T3的发光强度几乎没有影响,而老化微塑料对T3的发光强度有轻微抑制,其中PE20抑制了4.5%的发光强度,PP20对T3发光抑制率约为6.6%. 这可能是老化微塑料在溶液中释放出了一些有毒物质,对发光菌产生了生物毒性. 此外,不同镉离子浓度下,T3发光强度也受到了抑制,且随着镉离子浓度的升高发光强度逐渐降低,即发光强度抑制率随镉离子浓度升高而升高(图9a). 这是由于重金属可以改变细胞膜的渗透率,阻碍氧气的透过,从而能够影响到细胞的呼吸,影响到发光[26]. 另外,由于发光菌的呼吸链位于细胞膜中,所以能影响细胞膜的因素都会影响到细胞的正常代谢,从而影响到发光.
由图9b可见,镉与微塑料的联合生物毒性大于二者单独作用时的生物毒性,对T3发光强度的抑制率均在60%以上. 随着微塑料吸附镉量的增加其联合生物毒性逐渐增强,这表明重金属镉与微塑料复合污染存在较强的生物毒性,其对发光强度的抑制程度与吸附的镉离子量之间存在着正相关关系. 由此可见,微塑料与镉对发光菌的生物毒性存在协同效应,且老化微塑料与镉的联合生物毒性较强. 这一结论与以往的研究相符合,即有毒物质如重金属、微塑料等,会抑制发光菌体内的核酸、蛋白质等的合成,从而抑制其新陈代谢,使得发光菌的正常代谢受到胁迫,而发光菌发光所依赖的荧光酶是其呼吸作用代谢过程中不可或缺的物质,因而镉离子与微塑料都会影响到发光菌的正常发光,而其复合形态的胁迫下,其对于发光强度抑制进一步加强,表现为协同作用[27].
-
(1)微塑料老化会使微塑料的表面结构发生变化,其孔隙率和比表面积增大并出现含氧官能团. 老化微塑料对重金属镉的吸附量大于初始微塑料,且与老化时间呈正相关.
(2)微塑料对重金属镉的吸附过程大致分成3个阶段:短时间内的快速吸附,较长时期的缓慢吸附,及达到吸附平衡后逐渐稳定. 吸附动力学数据符合准二级动力学模型,吸附等温线数据符合Freundlich模式,且吸附作用主要受表面络合和静电引力的影响.
(3)微塑料对镉离子的吸附量易受到外界环境因素影响. 随着pH值升高,由于微塑料表面的去质子化作用其对Cd的吸附量升高;随着微塑料浓度升高,由于微塑料表面结合位点的竞争作用其对Cd的吸附量下降.
(4)微塑料复合镉污染对发光菌的生物毒性表现出协同效应,且随吸附镉离子量的增加其生物毒性增强,其中老化微塑料复合镉表现出更强的生物毒性.
老化微塑料吸附重金属镉及其毒性效应
Impact of ageing microplastics on heavy metal cadmium adsorption and its combined toxicity effect
-
摘要: 微塑料广泛存在于各种环境介质中,且能够作为载体影响其他污染物环境行为. 本文主要探究了不同老化程度的微塑料PE和 PP对重金属镉(Cd)的吸附特性及生物毒性. 结果表明,微塑料颗粒随老化程度的增加其对Cd的吸附能力逐渐增强. 通过模型拟合发现,初始微塑料和老化微塑料对重金属Cd的吸附动力学符合准二级模型,热力学符合Freundlich吸附模型. 实验结果表明,微塑料吸附Cd的量与环境pH值及微塑料浓度密切相关. 随pH值升高,由于微塑料表面的去质子化作用Cd的吸附量逐渐增加. 然而,随着微塑料浓度升高,微塑料颗粒表面吸附位点的竞争作用则导致Cd吸附量的降低. 微塑料吸附Cd后其复合污染的生物毒性有所增加,二者的复合生物毒性与微塑料老化程度、Cd吸附量正相关,存在明显的协同效应. 本研究为充分认识微塑料及老化微塑料在环境中的行为作用提供理论依据,为准确评估微塑料与其他污染物复合污染的生态风险提供参考.Abstract: Microplastics widely exist in various environment, which can be served as a carrier to affect the environmental behavior of other pollutants. In the present study, the cadmium adsorption characteristics on different aged microplastics PE and PP were explored, and the combined biological toxicity were also investigated using Photobacterium phosphoreum T3. The adsorption capacity of Cd increased with the aging degree of microplastics increases. And the sorption kinetics was in accord with the pseudo second-order rate equation the thermodynamics was in accord with the Freundlich sorption model. In addition, the results showed that the adsorption of Cd by microplastics was strongly associated with the environmental pH and concentration of microplastics. The adsorption of Cd is positively associated with pH value, which should be attribute to the deprotonation on the surface of microplastics. On the contrary, the adsorption amount of Cd decreased with the concentration of microplastics increases, due to the competition of adsorption sites on the surface of microplastics. The toxicity of microplastics adsorbed by Cd was also determined using Photobacterium phosphoreum T3. The result showed that the biological toxicity of microplastics combined with Cd is positively associated with the ageing degree and the amount of Cd adsorbed, which indicated that there was a synergy between microplastics and cadmium. The present study provides a scientific reference for accurately assessing the ecological risk of microplastics combined with other pollutants.
-
Key words:
- microplastics /
- cadmium /
- environmental behavior /
- biotoxicity.
-
塑料自出现以来极大地方便了人们的生活,其需求量和使用量不断增加,因此大量塑料垃圾进入并积累于环境中,在光照、热解、机械磨损以及生物作用下破碎形成粒径更小的塑料颗粒,其中直径小于5 mm的被定义为微塑料(microplastics,MPs)[1-2]. 微塑料作为一种新型污染物,广泛分布于水体、土壤、大气等环境介质中,在太平洋、大西洋、印度洋沿岸和深海地区,土壤及生物体内都能够检测到大量的微塑料[3-4],对生态环境安全及生物生存造成了严重的威胁[1]. 微塑料具有较大的比表面积,能够吸附大量的环境污染物,因此能够成为重金属、有机污染物等环境污染物质的运输载体,进一步增加其他环境污染物的风险[5]. 近期,重金属与微塑料之间的相互作用已成为环境领域关注的热点. 由于工业开采、金属冶炼、污泥回用等导致大量的重金属镉(Cd)进入土壤,造成严重的镉污染[6]. 据统计,我国Cd污染耕地土壤面积达2×105 km2,约占全国耕地总量的1/6,严重影响农业生产和粮食安全[7]. 重金属Cd具有高稳定性、不易降解、且易在生物体内累积的特点[8-9],严重威胁着人体健康和环境安全[10]. 同时,农业生产使用的大量农膜被遗留在环境中能够逐渐破碎形成微塑料,与重金属Cd形成复合污染[11]. 已有研究表明微塑料对水体环境中的重金属具有一定的富集作用[12],如海滩上微塑料表面镉、铬、铜、铁、锰、镍、铅、锌等重金属含量比周边海域中的重金属浓度高[13-14]. 然而,关于微塑料对Cd环境行为影响的研究仍存在不足.
微塑料吸附重金属还能影响其迁移特性与生物毒性,Boucher等[15]研究发现在潮汐带沉积物中,微塑料能够吸附重金属,而生物摄入微塑料后,重金属也随之进入食物链. 研究表明,微塑料吸附的重金属可能会在水体和肠道中被重新释放,从而使其生物毒性增加[16]. 镉与微塑料的复合污染对鲤鱼血浆中的酶活性、生化指标及免疫等具有明显的生物毒性效应,且二者表现出明显的协同作用[17]. 微塑料与重金属联合作用可导致海水青鳉肠道污染负荷增加,特定肠道微生物及肠道功能发生变化,免疫系统抵抗力受到明显抑制[18]. 目前,尚未有统一的方法对重金属与微塑料联合毒性进行测定. 研究发现,发光细菌毒性测定法具有高灵敏度、强相关性、快速、高自动化程度等特点,在重金属、有机物污染环境中的综合毒性分析中已得到广泛的应用[19]. 利用发光菌对取代苯酚和镉的混合物进行生物毒性测定,结果表明二者之间存在微弱的加成作用或近似加成作用的弱协同效应[19].
此外,环境中的微塑料在多种因素作用下逐渐发生老化,导致微塑料表面的氧化结合位点增多,对重金属及其他污染物的吸附能力增强[20],因此老化微塑料的吸附能力通常高于原始微塑料. 研究自然环境中老化微塑料对其他污染物环境行为的影响具有现实意义. 尽管已有国内外学者对实验室条件下微塑料与其他环境污染物的吸附进行了研究,但对于老化微塑料的研究仍不充分,且尚无一致定论.
微塑料高级氧化过程与自然老化过程中的氧化途径及老化产物具有极高的相似性[21],可克服自然环境中微塑料的老化速率极低的问题. 因此本研究采用热活化K2S2O8高级氧化法加速微塑料老化以获取不同老化程度的微塑料. 通过室内模拟实验,研究不同老化程度的微塑料对重金属的吸附动力学和吸附等温线的影响,以及在不同pH、微塑料浓度下对重金属的吸附,进一步探讨不同老化程度微塑料吸附行为的差异和作用机理. 采用发光菌毒性测试法对微塑料与重金属的复合污染的生物毒性进行测定,为复合污染的生物毒性评价提供科学依据.
1. 材料与方法 (Materials and methods)
1.1 实验材料
微塑料聚乙烯(PE)、聚丙烯(PP)购于东莞市特塑朗化工原料,平均粒径约100 µm;镉标准溶液(1 mg·mL−1)购于北京北方伟业计量技术研究院;过硫酸钾(K2S2O8)购于天津市风船化学试剂科技有限公司,纯度为99%;明亮发光杆菌T3(Photobacterium phosphoreum T3)由中国科学院南京土壤研究所提供.
1.2 微塑料老化与表征
将微塑料用甲醇超声3次,每次20 min,再以超纯水洗涤3次于40 ℃干燥,密封保存、备用. 采用热活化K2S2O8高级氧化法进行微塑料老化[21],将1.0 g微塑料(PE、PP)加入到40 mL 100 mmol·L−1新鲜制备的pH 7.0的K2S2O8溶液中,于70 ℃恒温搅拌. 每12 h添加等量K2S2O8溶液,每2 天更换新鲜溶液以避免K2SO4积累. 分别于5、10、20 d取出老化的微塑料样品,清洗后于45 ℃烘干避光保存. 将老化微塑料分别记为PE5、PE10、PE20和PP5、PP10、PP20,初始微塑料分别记为PE0和PP0.
利用傅里叶红外光谱仪(FTIR)在分辨率4 cm−1条件下检测500—4000 cm−1区域老化前后微塑料的表面官能团变化,并利用扫描电镜(SEM)表征微塑料的表面形貌变化.
1.3 镉吸附动力学
将镉标准溶液稀释至10 mg·L−1作为镉贮存液,并于4 ℃避光保存. 随后,进一步稀释成1 mg·L−1的镉吸附液. 在摇瓶中加入100 mL的镉吸附液,再分别加入0.2 g初始微塑料及不同老化程度的PE、PP微塑料,置于恒温摇床((25±2)°C、180 r·min−1)避光振荡72 h. 每处理重复3次,同时设置不添加微塑料的空白对照. 分别于0.5、1、3、6、12、24、36、48、60 h进行取样,过0.45 µm滤膜并稀释,采用火焰原子吸收分光光度计测定镉含量.
1.4 镉的吸附等温线
将镉贮存液准确地稀释至0.1、0.5、1、3、5、10 mg·L−1作为镉吸附液进行吸附等温线实验. 每100 mL镉吸附液添加0.2 g初始微塑料和老化20 d的微塑料,每处理重复3次,同时设置不添加微塑料的空白对照,于25 ℃,180 r·min−1振荡培养,并于24、48、72 h时取样. 将样品过0.45 µm滤膜并稀释,采用火焰原子吸收分光光度计对镉含量进行测定.
1.5 不同因素对镉吸附的影响
准确将镉贮存液稀释至1 mg·L−1,并用0.01 mol·L−1的NaOH和HNO3调节该溶液的pH,在不同pH(4、5、6、7、8)环境条件下进行微塑料对Cd的吸附,实验方法同1.4节.
将加入的微塑料浓度设为0.1、0.2、0.4、0.6 g·(100 mL) -1 以探究不同微塑料浓度对Cd吸附的影响,其实验方法同1.4节.
1.6 明亮发光杆菌毒性测定
将达到吸附平衡的微塑料于40 ℃干燥,准确称取0.2 g吸附镉的微塑料,并向其中加入100 mL 3% 的NaCl溶液,并超声使微塑料均匀分散,于摇床中恒温振荡24 h过滤后以浸出液作为待测液,用于发光菌毒性测定. 将明亮发光杆菌T3接种于高温灭菌的专用培养基,其中每100 mL水中酵母浸出粉0.5 g,胰蛋白胨0.5 g,NaCl 3 g,Na2HPO4 0.5 g,KH2PO4 0.1 g,甘油0.3 g,pH值6.5,25 ℃避光培养20 h,于10000 r·min−1离心收集菌体并重悬于3% NaCl溶液以获得合适的菌体浓度. 取待测液180 μL于96孔板,随后加入20 µL重悬后的菌液,每样品重复3次. 同时,按照不同的微塑料吸附量,将镉贮存液稀释至与其相当,测定镉的生物毒性;按照0.2 g·100 mL−1测定微塑料的生物毒性,在微孔板上添加200 μL 3% 的NaCl溶液作为空白对照,于25 ℃下静置15 min,在450—490 nm波长下测定明亮发光杆菌的发光强度,并计算不同处理的发光强度抑制率.
1.7 数据处理与分析
数据统计和分析采用 Excel 2010,图表使用 Origin 2018;用 SPSS进行统计分析.
2. 结果与讨论 (Results and discussion)
2.1 老化前后的微塑料特征
由图1可见,初始微塑料 PE、PP表面较光滑,而老化后微塑料表面的粗糙程度增加,并产生裂纹和孔隙,表面形貌更为破碎. 这一现象与以往的研究结果相似,即在老化过程中,微塑料表面的裂纹数目会增多,且裂缝深度会逐步扩展,会呈现碎片化现象[20]. 在老化作用下,微塑料的表面形态会发生变化,其比表面积、孔隙率可能增加,因此可能对其吸附性能造成一定的影响.
采用FTIR对老化前后的微塑料PE和PP表面官能进行表征. 由图2可见,老化后微塑料PE和PP在1710 cm−1出现新的红外吸收峰,其特征峰为甲酸/乙酸等羧酸基团(−CH2COOH),这表明老化能够使微塑料PE、PP表面发生官能团的氧化. 这一结果与Liu等[20]的研究结果一致,微塑料表面的含氧官能团的出现可能会使微塑料的亲水性得到改善[21],进而影响微塑料对重金属的吸附性能.
2.2 镉的吸附动力学
由图3可见,在不同的吸附时间下,微塑料PE、PP对重金属镉离子的吸附出现类似的变化,即随吸附时间延长,微塑料PE、PP对镉离子的吸附量都是增加的,而吸附速率均呈现先增加后减小的趋势. 由图3可见,吸附过程大致可分为3个阶段:0—10 h为快速吸附阶段,此时镉离子在微塑料上的吸附量约为其总量的1/2;10—30 h为第二阶段,微塑料PE、PP对镉离子的吸附速率逐步下降,此时微塑料上仍然有镉离子的吸附,但吸附速率逐渐降低;第三个阶段是30 h之后,吸附达到平衡. 这说明镉离子在微塑料上的吸附并不是瞬间完成的,而是一个由快速到缓慢的平衡过程.
通过微塑料的吸附实验,发现镉离子在微塑料上的吸附量依次为:PE20>PE10>PE5>PE0,PP20 >PP10 >PP5 >PP0. 由此可见,镉离子在老化微塑料的吸附量比初始微塑料的吸附量大,且随老化时间延长其吸附量增加,即微塑料吸附能力与老化时间具有正相关性. 这一发现与已有的研究结论一致,随着老化时间的推移,微塑料表面变得粗糙,其比表面积会增大,同时微塑料表面氧化结合位点、含氧官能团增多,这些都能导致微塑料表面负电性增大,与镉离子的络合作用增加,从而提高微塑料吸附镉离子的能力[22-23].
分别按照准一级动力学方程表达式(1)和准二级动力学方程表达式(2)对吸附动力学进行线性拟合,结果如图4所示. 由图4可见,按照准二级动力学方程表达式进行拟合时线性较好.
准一级动力学方程表达式:
lg(qe−qt)=lgqe−k12.303t (1) 其中,k1(h−1)一级吸附速率常数,qt(mg·g−1)为t时刻吸附量;qe(mg·g−1)为平衡时吸附量;t(h)为时间.
准二级动力学方程表达式为:
tqt=1k2qe2+1qet (2) 其中,k2(g·mg−1·h−1)为二级吸附速率常数.
同时,表1列出了相关的动力学模型参数,其中按照准二级动力学方程表达式计算获得的相关系数R2在0.9994—0.9999之间,而按照准一级动力学方程表达拟合获得的相关系数R2在0.3788—0.9971之间. 由此可见,准二级模型对于微塑料对镉离子的吸附动态特性拟合效果更佳,而准一级模型则不能很好地拟合. 这表明镉离子在微塑料上的吸附行为符合准二级动力学方程,微塑料对镉离子的吸附存在多个吸附阶段,物理吸附和化学吸附同时存在,其中以化学吸附为主.
表 1 由准一级模型和准二级模型得到的吸附动力学参数Table 1. Adsorption kinetic parameters obtained from the quasi-first-order model and the quasi-second-order model微塑料Microplastics 准一级动力学方程Quasi-first-order model 准二级动力学方程Quasi-second-order model k1 qe/ (mg·g−1) R2 k2 qe/(mg·g−1) R2 PE0 14.4378 0.3496 0.9840 8.3893 0.3452 0.9999 PE5 6.5974 0.3652 0.9161 7.3099 0.3698 0.9999 PE10 6.8295 0.3547 0.3788 7.8927 0.3560 0.9996 PE20 6.1482 0.3813 0.8410 6.4735 0.3931 0.9998 PP0 8.5874 0.3207 0.6000 9.6525 0.3219 0.9994 PP5 10.1068 0.3250 0.7847 9.4340 0.3256 0.9997 PP10 7.6493 0.3337 0.9124 8.8810 0.3355 0.9996 PP20 5.9236 0.3504 0.9971 7.7520 0.3590 0.9998 2.3 镉的吸附等温线研究
在25 ℃下,镉离子在微塑料PE、PP表面吸附达到平衡后,以平衡时溶液中镉离子浓度(Ce)为横坐标,以微塑料对镉离子的平衡吸附量为纵坐标绘图. 如图5所示,随着镉离子浓度增加,镉离子在微塑料PE、PP上的平衡吸附量也随之增加,但曲线的斜率却在不断降低. 这表明在镉离子浓度增加的同时微塑料表面镉的吸附量也逐渐增加,但其吸附速率却在逐渐降低. 这是由于微塑料与镉离子的吸附存在一定的定位性,即在较低浓度的镉离子溶液中,微塑料的表面存在大量的吸附位点,能够迅速吸附镉. 但随着镉离子浓度的升高,微塑料表面被占据的吸附点位也越来越多,吸附逐渐趋于饱和,进而影响吸附速率. 这表明镉离子的平衡吸附量与老化程度也存在一定的相关性,老化微塑料表面镉吸附量大于初始微塑料,即PE20 >PE0,PP20 >PP0. 由此可见,老化微塑料比初始微塑料具有更好的吸附性能,这也与老化微塑料表面形貌和官能团变化相关.
进一步利用Freundlich和Langmuir等温吸附模型对微塑料吸附等温线进行拟合,结果如图6和 表2所示. Freundlich和Langmuir模型拟合线性方程分别如公式(3)和(4)所示:
表 2 由Freundlich模型和Langmuir模型得到的镉离子在微塑料上的吸附等温线参数Table 2. Adsorption isotherm parameters of Cd on microplastics obtained by Freundlich model and Langmuir model微塑料Microplastics 温度/℃Temperature Freundlich Langmuir KF n R2 KL Qmax R2 PE0 25 0.0301 0.6621 0.9783 0.1562 1.178 0.5861 PE20 25 0.0300 0.6958 0.9694 0.1626 1.5196 0.4516 PP0 25 0.0216 0.7354 0.9886 0.1402 1.0987 0.6591 PP20 25 0.0275 0.6887 0.9791 0.1600 1.0959 0.6592 Freundlich:lgqe=lgKF+nlgCe (3) 其中,KF为吸附平衡常数,n为吸附过程中的支持力.
Langmuir:Ceqe=αKLCe+1KL (4) 其中,KL为平衡常数.
由表2中两种模型拟合的吸附等温线相关系数R2可以看出,Freundlich吸附模型R2的值在0.9694—0.9886之间,而Langmuir吸附模型R2的值在0.4516—0.6592之间,因此Freundlich等温模型能够较好地反映出镉离子在微塑料PE、PP上的吸附行为,即吸附等温线数据符合Freundlich吸附模型. 这一结果表明镉离子在微塑料 PE、PP上的吸附是非线性的,且其吸附过程具有不均匀性. 这与前人的研究结果相吻合[24],即镉离子先在微塑料表面的高能吸附点上进行吸附,再在低能吸附点上进行吸附. 这也进一步表明微塑料表面吸附镉的过程是由表面络合和静电引力共同控制的.
2.4 不同因素对镉在微塑料上吸附的影响
2.4.1 pH对微塑料吸附镉的影响
如图7所示,微塑料在不同pH值下对镉离子的吸附能力有所不同,随着 pH值的增加其吸附量增加,且老化微塑料对镉离子的吸附量大于初始微塑料. Brennecke等[25]研究发现,pH值对微塑料吸附镉离子的性能有很大影响,在低 pH值时,H+与镉离子能够竞争吸附点位导致微塑料对镉离子的吸附性能下降;而随着 pH值的增加,微塑料表面的官能团被去质子化,微塑料的负电性会增加,因此微塑料和镉离子间的静电作用会加强,微塑料吸附镉离子的能力则相应增加[25]. 这也进一步说明了静电作用对微塑料的吸附性能有很大的促进作用,微塑料吸附镉离子的主要机理可能是静电作用. 此外,受pH值的影响,老化及初始微塑料PP对镉离子的吸附量均高于PE,这可能与微塑料材质有关.
2.4.2 不同微塑料浓度对镉吸附的影响
图8比较了不同微塑料浓度对镉离子的吸附量的影响. 由图8可见,在保持其它条件不变的情况下,随着微塑料浓度增加,两种类型微塑料对镉离子的吸附量皆会相应地下降. 但老化微塑料对镉离子的吸附量仍比初始微塑料大,这一研究结果与以往的研究结果相符,即当微塑料浓度较低时,微塑料在水中的分布比较均匀,可以很好地与水中的镉离子相结合[9]. 当微塑料的浓度升高时,微塑料的吸附点位会增多,使得微塑料颗粒间发生相互竞争,并且微塑料之间会发生相互黏合,使得在水中分散不均匀,与水中的镉离子接触不足,导致单位吸附量下降[9].
2.5 微塑料与镉的联合生物毒性
利用明亮发光杆菌T3对镉、微塑料及其二者的联合生物毒性进行测定,结果如图9所示. 初始微塑料对T3的发光强度几乎没有影响,而老化微塑料对T3的发光强度有轻微抑制,其中PE20抑制了4.5%的发光强度,PP20对T3发光抑制率约为6.6%. 这可能是老化微塑料在溶液中释放出了一些有毒物质,对发光菌产生了生物毒性. 此外,不同镉离子浓度下,T3发光强度也受到了抑制,且随着镉离子浓度的升高发光强度逐渐降低,即发光强度抑制率随镉离子浓度升高而升高(图9a). 这是由于重金属可以改变细胞膜的渗透率,阻碍氧气的透过,从而能够影响到细胞的呼吸,影响到发光[26]. 另外,由于发光菌的呼吸链位于细胞膜中,所以能影响细胞膜的因素都会影响到细胞的正常代谢,从而影响到发光.
由图9b可见,镉与微塑料的联合生物毒性大于二者单独作用时的生物毒性,对T3发光强度的抑制率均在60%以上. 随着微塑料吸附镉量的增加其联合生物毒性逐渐增强,这表明重金属镉与微塑料复合污染存在较强的生物毒性,其对发光强度的抑制程度与吸附的镉离子量之间存在着正相关关系. 由此可见,微塑料与镉对发光菌的生物毒性存在协同效应,且老化微塑料与镉的联合生物毒性较强. 这一结论与以往的研究相符合,即有毒物质如重金属、微塑料等,会抑制发光菌体内的核酸、蛋白质等的合成,从而抑制其新陈代谢,使得发光菌的正常代谢受到胁迫,而发光菌发光所依赖的荧光酶是其呼吸作用代谢过程中不可或缺的物质,因而镉离子与微塑料都会影响到发光菌的正常发光,而其复合形态的胁迫下,其对于发光强度抑制进一步加强,表现为协同作用[27].
3. 结论 (Conclusion)
(1)微塑料老化会使微塑料的表面结构发生变化,其孔隙率和比表面积增大并出现含氧官能团. 老化微塑料对重金属镉的吸附量大于初始微塑料,且与老化时间呈正相关.
(2)微塑料对重金属镉的吸附过程大致分成3个阶段:短时间内的快速吸附,较长时期的缓慢吸附,及达到吸附平衡后逐渐稳定. 吸附动力学数据符合准二级动力学模型,吸附等温线数据符合Freundlich模式,且吸附作用主要受表面络合和静电引力的影响.
(3)微塑料对镉离子的吸附量易受到外界环境因素影响. 随着pH值升高,由于微塑料表面的去质子化作用其对Cd的吸附量升高;随着微塑料浓度升高,由于微塑料表面结合位点的竞争作用其对Cd的吸附量下降.
(4)微塑料复合镉污染对发光菌的生物毒性表现出协同效应,且随吸附镉离子量的增加其生物毒性增强,其中老化微塑料复合镉表现出更强的生物毒性.
-
表 1 由准一级模型和准二级模型得到的吸附动力学参数
Table 1. Adsorption kinetic parameters obtained from the quasi-first-order model and the quasi-second-order model
微塑料Microplastics 准一级动力学方程Quasi-first-order model 准二级动力学方程Quasi-second-order model k1 qe/ (mg·g−1) R2 k2 qe/(mg·g−1) R2 PE0 14.4378 0.3496 0.9840 8.3893 0.3452 0.9999 PE5 6.5974 0.3652 0.9161 7.3099 0.3698 0.9999 PE10 6.8295 0.3547 0.3788 7.8927 0.3560 0.9996 PE20 6.1482 0.3813 0.8410 6.4735 0.3931 0.9998 PP0 8.5874 0.3207 0.6000 9.6525 0.3219 0.9994 PP5 10.1068 0.3250 0.7847 9.4340 0.3256 0.9997 PP10 7.6493 0.3337 0.9124 8.8810 0.3355 0.9996 PP20 5.9236 0.3504 0.9971 7.7520 0.3590 0.9998 表 2 由Freundlich模型和Langmuir模型得到的镉离子在微塑料上的吸附等温线参数
Table 2. Adsorption isotherm parameters of Cd on microplastics obtained by Freundlich model and Langmuir model
微塑料Microplastics 温度/℃Temperature Freundlich Langmuir KF n R2 KL Qmax R2 PE0 25 0.0301 0.6621 0.9783 0.1562 1.178 0.5861 PE20 25 0.0300 0.6958 0.9694 0.1626 1.5196 0.4516 PP0 25 0.0216 0.7354 0.9886 0.1402 1.0987 0.6591 PP20 25 0.0275 0.6887 0.9791 0.1600 1.0959 0.6592 -
[1] 李昇昇, 李良忠, 李敏, 等. 环境样品中微塑料及其结合污染物鉴别分析研究进展 [J]. 环境化学, 2020, 39(4): 960-974. doi: 10.7524/j.issn.0254-6108.2019102304 LI S S, LI L Z, LI M, et al. Study on identification of microplastics and the combined pollutants in environmental samples [J]. Environmental Chemistry, 2020, 39(4): 960-974(in Chinese). doi: 10.7524/j.issn.0254-6108.2019102304
[2] 白璐, 刘宪华, 陈燕珍, 等. 天津近岸海域微塑料污染现状分析 [J]. 环境化学, 2020, 39(5): 1161-1168. doi: 10.7524/j.issn.0254-6108.2019062901 BAI L, LIU X H, CHEN Y Z, et al. Current status of microplastics pollution in Tianjin coastal waters [J]. Environmental Chemistry, 2020, 39(5): 1161-1168(in Chinese). doi: 10.7524/j.issn.0254-6108.2019062901
[3] CLARK J R, COLE M, LINDEQUE P K, et al. Marine microplastic debris: A targeted plan for understanding and quantifying interactions with marine life [J]. Frontiers in Ecology and the Environment, 2016, 14(6): 317-324. doi: 10.1002/fee.1297 [4] COLE M, LINDEQUE P, FILEMAN E, et al. Microplastic ingestion by zooplankton [J]. Environmental Science & Technology, 2013, 47(12): 6646-6655. [5] 张伟平. 农田土壤微塑料的分离及其对污染物的吸附特征研究[D]. 开封: 河南大学, 2020. ZHANG W P. Study on the isolation of microplastics in farmland soil and adsorption behavior of contaminant onto microplastics[D]. Kaifeng: Henan University, 2020.
[6] CONRAD C F, FUGATE D, DAUS J, et al. Assessment of the historical trace metal contamination of sediments in the Elizabeth River, Virginia [J]. Marine Pollution Bulletin, 2007, 54(4): 385-395. doi: 10.1016/j.marpolbul.2006.11.005 [7] 宋玉婷, 雷泞菲. 我国土壤镉污染的现状及修复措施 [J]. 西昌学院学报(自然科学版), 2018, 32(3): 79-83. doi: 10.16104/j.issn.1673-1891.2018.03.018 SONG Y T, LEI N F. China's cadmium pollution land status and restoration measures [J]. Journal of Xichang University (Natural Science Edition), 2018, 32(3): 79-83(in Chinese). doi: 10.16104/j.issn.1673-1891.2018.03.018
[8] HUANG H G, YU N, WANG L J, et al. The phytoremediation potential of bioenergy crop Ricinus communis for DDTs and cadmium co-contaminated soil [J]. Bioresource Technology, 2011, 102(23): 11034-11038. doi: 10.1016/j.biortech.2011.09.067 [9] 张金彪, 黄维南. 镉对植物的生理生态效应的研究进展 [J]. 生态学报, 2000, 20(3): 514-523. doi: 10.3321/j.issn:1000-0933.2000.03.030 ZHANG J B, HUANG W N. Advances on physiological and ecological effects of cadmium on plants [J]. Acta Ecologica Sinica, 2000, 20(3): 514-523(in Chinese). doi: 10.3321/j.issn:1000-0933.2000.03.030
[10] JOHRI N, JACQUILLET G, UNWIN R. Heavy metal poisoning: The effects of cadmium on the kidney [J]. BioMetals, 2010, 23(5): 783-792. doi: 10.1007/s10534-010-9328-y [11] KUMAR R, IVY N, BHATTACHARYA S, et al. Coupled effects of microplastics and heavy metals on plants: Uptake, bioaccumulation, and environmental health perspectives [J]. Science of the Total Environment, 2022, 836: 155619. doi: 10.1016/j.scitotenv.2022.155619 [12] 祁锟. 湖库水体中微塑料对重金属的吸附机理研究[D]. 长春: 东北师范大学, 2021. QI K. Study on mechanism of heavy metals adsorption onto microplastics in lake and reservoir waters[D]. Changchun: Northeast Normal University, 2021.
[13] ZHOU Y F, LIU X N, WANG J. Characterization of microplastics and the association of heavy metals with microplastics in suburban soil of central China [J]. Science of the Total Environment, 2019, 694: 133798. doi: 10.1016/j.scitotenv.2019.133798 [14] MARŠIĆ-LUČIĆ J, LUŠIĆ J, TUTMAN P, et al. Levels of trace metals on microplastic particles in beach sediments of the island of Vis, Adriatic Sea, Croatia [J]. Marine Pollution Bulletin, 2018, 137: 231-236. doi: 10.1016/j.marpolbul.2018.10.027 [15] BOUCHER C, MORIN M, BENDELL L I. The influence of cosmetic microbeads on the sorptive behavior of cadmium and lead within intertidal sediments: A laboratory study [J]. Regional Studies in Marine Science, 2016, 3: 1-7. [16] 赵美静, 夏斌, 朱琳, 等. 微塑料与有毒污染物相互作用及联合毒性作用研究进展 [J]. 生态毒理学报, 2021, 16(5): 168-185. ZHAO M J, XIA B, ZHU L, et al. Research progress on interaction and joint toxicity of microplastics with toxic pollutants [J]. Asian Journal of Ecotoxicology, 2021, 16(5): 168-185(in Chinese).
[17] BANAEE M, SOLTANIAN S, SUREDA A, et al. Evaluation of single and combined effects of cadmium and micro-plastic particles on biochemical and immunological parameters of common carp (Cyprinus carpio) [J]. Chemosphere, 2019, 236: 124335. doi: 10.1016/j.chemosphere.2019.07.066 [18] 王燕. 微塑料与重金属(Cd、Pb、Zn)对海水青鳉复合毒性研究[D]. 重庆: 中国科学院大学(中国科学院重庆绿色智能技术研究院), 2020. WANG Y. Combined toxic effect of microplastics and heavy metals(Cd, Pb, Zn)on marine medaka[D]. Chongqing: Chongqing Institute of Green and Intelligent Technology, Chinese Academy of Sciences, 2020.
[19] 苏丽敏. 部分取代芳烃与重金属对发光菌联合毒性及构效关系研究[D]. 长春: 东北师范大学, 2008: 52-56. SU L M. Evaluation and quantitative structure-activity relationships of joint toxicity of substituted aromatic compounds and heavy metals to Photobacterium phosphoreum[D]. Changchun: Northeast Normal University, 2008: 52-56.
[20] DAVRANCHE M, VECLIN C, PIERSON-WICKMANN A C, et al. Are nanoplastics able to bind significant amount of metals?The lead example [J]. Environmental Pollution, 2019, 249: 940-948. doi: 10.1016/j.envpol.2019.03.087 [21] LIU P, QIAN L, WANG H Y, et al. New insights into the aging behavior of microplastics accelerated by advanced oxidation processes [J]. Environmental Science & Technology, 2019, 53(7): 3579-3588. [22] 徐鹏程, 郭健, 马东, 等. 新制和老化微塑料对多溴联苯醚的吸附 [J]. 环境科学, 2020, 41(3): 1329-1337. doi: 10.13227/j.hjkx.201908029 XU P C, GUO J, MA D, et al. Sorption of polybrominated diphenyl ethers by virgin and aged microplastics [J]. Environmental Science, 2020, 41(3): 1329-1337(in Chinese). doi: 10.13227/j.hjkx.201908029
[23] FAN X L, ZOU Y F, GENG N, et al. Investigation on the adsorption and desorption behaviors of antibiotics by degradable MPs with or without UV ageing process [J]. Journal of Hazardous Materials, 2021, 401: 123363. doi: 10.1016/j.jhazmat.2020.123363 [24] WANG Q J, ZHANG Y, WANGJIN X X, et al. The adsorption behavior of metals in aqueous solution by microplastics effected by UV radiation [J]. Journal of Environmental Sciences, 2020, 87: 272-280. doi: 10.1016/j.jes.2019.07.006 [25] BRENNECKE D, DUARTE B, PAIVA F, et al. Microplastics as vector for heavy metal contamination from the marine environment [J]. Estuarine, Coastal and Shelf Science, 2016, 178: 189-195. doi: 10.1016/j.ecss.2015.12.003 [26] CHU S, HE Y, XU X. Determination of acute toxicity of polychlorinated biphenyls to Photobacterium phosphoreum [J]. Bulletin of Environmental Contamination and Toxicology, 1997, 58(2): 263-267. doi: 10.1007/s001289900329 [27] 邹继颖. 微塑料对典型有机污染物和重金属离子的吸附及机理研究[D]. 长春: 东北师范大学, 2021. ZOU J Y. Research on sorption and mechanism of typical organic pollutants and heavy metal ions by microplastics[D]. Changchun: Northeast Normal University, 2021.
-





 下载:
下载: