-
微生物-矿物间的相互作用几乎无处不在,即使在深海热液喷口、酸性矿山排水、盐湖、油藏这样的极端环境中,仍发现了微生物的踪迹[1]. 复杂的地质环境下,矿物的成分、种类与存在形式不尽相同,研究手段与方法自然种类繁多. 但对微生物-矿物相互作用的研究将二者串联起来,并受到了地质微生物学、环境矿物学等新兴领域的重点关注. 同时,越来越多的研究表明,尽管微生物-矿物相互作用多发生在微观尺度下,但其影响深远,在地表环境改造、元素地球化学循环和矿床的形成等宏观行为上也发挥着重要作用.
目前国内外研究主要集中在以下几个方面:(1)微生物对矿物类别的适应性与机制. 矿物为微生物提供保护(物理遮蔽、矿质营养以及能量)的同时,微生物生长繁殖导致的矿物溶解、转化和沉淀可能释放出矿物中原本相对稳定的重金属离子,并诱导氧化应激反应,从而对生物体产生一定的毒害作用,这种利弊兼有的方式使得微生物与矿物结成了特殊的盟友,不同类型矿物上定殖的微生物往往具有其独特鲜明的特征[2]. Uroz等提出了“矿物圈”的概念,探讨了细菌群落在矿物表面的分布,和矿物相关细菌在酸性及贫营养环境下对矿物的风化和土壤元素循环的重要作用,认为矿物的物理化学性质是驱动微生物群落改变的重要因素[3]. Kleber等也指出矿物能吸附有机物尤其是生物源有机物,形成独特的微聚体以占据更多资源和生态位,进而容纳更丰富的微生物群落,还能充当界面反应的催化剂,促进有机碳在土壤中的稳定化[4]. (2)微生物-矿物相互作用机制. 原核生物(细菌)主要通过分泌有机酸、铁载体以及氧化还原作用改造矿物;除化学作用外,一些真核生物(真菌)、地衣(藻菌共生体)还能直接利用菌丝对矿物进行机械破坏(详见第2节). (3)微生物-矿物作用组合的功能效应. 随着研究的深入,“微生物-矿物”这一特殊组合全方位、多角度的应用也吸引了越来越多研究者们的注意,尤其是在二氧化碳固定、新能源开发以及环境净化等领域. 一些矿物在形成过程中能够直接将CO2固定,生成稳定的碳酸盐矿物,如方解石(CaCO3)、白云石(Ca0.5Mg0.5CO3)、菱镁石(MgCO3)和菱铁矿(FeCO3)[5],然而该自然形成过程十分缓慢. 在微生物的催化下,速度得到大幅提升. 有研究报道,蓝藻+假单胞菌组合能将橄榄石溶解后,以生物质和次生碳酸盐矿物形式高效固定CO2,且周期缩短为21 d[6]. Salek等定量评估了产酸(如硝化反应和厌氧发酵)和产碱(如反硝化和产甲烷反应)过程中矿物碳酸化对CO2的封存潜力,并指出优化这些过程有助于缓解全球气候变化[7]. 在能源方面,对部分功能微生物及其代谢产物的利用,为低品位矿产资源的绿色高效开发,稀、贵金属资源的循环利用等提供了新的理论依据与实践途径[8-10]. 此外,鲁安怀课题组提出一些非光合作用微生物能通过半导体矿物日光催化获得太阳能,细菌生物量与光的波长及强度显著相关,且生长模式与矿物的吸收光谱相匹配,生物量光能转化效率为0.13‰—1.90‰[11]. 诸多研究表明,氧化亚铁硫杆菌、粪产碱杆菌和异化金属还原菌等可与赤铁矿、针铁矿、锰钾矿、闪锌矿和磁黄铁矿等半导体矿物发生协同作用,有效强化微生物和矿物原本各自拥有的某些环境功能[12-14]. 微生物-矿物作用下的生物地球化学过程及其在环境修复中的应用也顺势成为了近些年的研究热点[15-16]. Naidu课题组研究了黏土矿物和微生物相互作用后微生物生长状况及矿物结构与理化性质变化,对黏土矿物介导的疏水性有机污染物(PAHs、VOCs)生物修复具有一定的指导意义[17-18]. 黄巧云课题组对细菌及其胞外产物与土壤矿物相互作用类型、机理及环境效应进行了探究,揭示了土壤矿物介导下细菌对重金属胁迫的响应以及土壤矿物-细菌-有机物等多元复合体的形成方式和重金属在复合体表面的微观吸附机制与络合模型[19-22]. 董海良课题组探究了在黏土矿物-溶解铁-微生物的复杂体系中,厌氧微生物对不同含铁量矿物结构中Fe(Ⅲ)的还原,发现富铁黏土矿物与铁还原菌共同作用下可最大程度地提高Cr(Ⅵ)、U(Ⅵ)的还原速率和还原量[23-24]. 陆现彩课题组以矿山背景下的微生物-金属硫化物相互作用为切入点,揭示了二者的相互作用机理及电子传递行为,为酸性矿山废水的治理和铁、硫元素地球化学循环提供了新思路[25-26]. (4)微生物-矿物对地表矿物多样性的改造. 在漫长的地球演化历史中,微生物与矿物相互影响、相互依存、共同进化. 大氧化事件(great oxidation event, GOE)后,大气中的氧气浓度升高,许多元素开始以氧化物形式出现在地表,矿物的种类得到极大丰富,从约1500种增加到4000余种. 随着真核生物的诞生,矿物种类进一步增加,达到了现在的5000余种[2, 27]. 微生物活动还可使岩石矿物的风化速度提升1个数量级. 在没有微生物作用的情况下,硅酸盐矿物的风化顺序大致遵循鲍文反应系列(结晶温度),如橄榄石→长石→石英,然而微生物加入后,矿物的风化顺序几乎颠倒了,这是因为橄榄石通常不含有生物生长所需的磷元素而长石含有. 微生物介导的矿物溶解,沉淀,转化过程使得矿物变化类型纷繁复杂,并常常伴随着新矿物的产生,许多氧化物、硫化物和碳酸盐就是生物矿化的结果[28-29].
众多研究结果揭示了微生物-矿物相互作用过程并提出了相关作用机制;同时,研究证实了矿物-微生物的相互作用显著影响着污染物的环境行为,尤其是土壤重金属的迁移与形态转化,在环境修复中具有深远意义. 为此,本文拟总结现阶段所报道的地表关键带中主要微生物-矿物相互作用机制以及微生物-矿物相互作用净化重金属污染的作用机制,希望本文对该领域的研究人员起到一定的指导作用,进一步推进该领域的研究发展.
-
微生物无处不在,作为地球上最早出现、数量最多的生命形式,驱动着物质循环和能量流动. 在微生物诸多特性中,最令人惊叹的是它们系统发育的多样性和代谢广泛性,能够通过形成生物膜使自身在环境中占据有利生态位,适应其他生物无法忍受的极端环境如干旱,高盐度,营养匮乏及重金属污染等[30]. 因此,它们普遍渗透于土壤各个组分之中,表1对近年来文献报道的微生物-矿物相互作用中涉及的细菌进行了汇总. 细菌与矿物类型的多样充分说明了其相互作用的广泛性和复杂性,也从侧面印证了细菌超强的环境适应能力. 在贫营养环境下,细菌通过风化矿物获取无机营养与能量,同时影响着矿物的分解、转化与和周围污染物的环境行为.
国内外众多学者发现土壤矿物对微生物具有巨大的吸引力[31-33];按照结合程度可分为以下两种:1)初始黏附,微生物借助鞭毛、菌毛等接触矿物并粘附在其表面;朱等将胶质芽孢杆菌和膨润土混合培养,发现与纯培养对照相比,细菌在膨润土的刺激下长出了鞭毛,膨润土的存在为细菌鞭毛的组装提供了适宜环境,同时鞭毛的生成也有利于游离态细菌移动并黏附在矿物表面[34]. 2)紧密黏附,微生物通过分泌多糖、蛋白质等胞外聚合物改变自身的理化性质,与矿物表面发生紧密结合. 在这过程中,矿物的物理化学性质如电负性和沉降能力,微生物种类,分泌物EPS的组成及性质,均能影响其与细菌的黏附强弱[35]. 在此之后,相互接触的矿物-微生物发生一系列复杂的物理化学反应,进而影响着细菌的生长和生物膜的形成等,以及矿物的演化(分解、氧化还原与新矿物形成等)[21]. 微生物与矿物之间的作用机制较为复杂(图1),概括起来主要有以下两个方面:生物力学作用和生物化学作用. 大多数原核生物(细菌)能通过分泌无/有机酸、铁载体以及氧化还原作用对矿物进行浸出,并以生物膜形式在矿物周围形成金属元素的汇(metal sink),从而实现对矿物的破坏. 除化学作用外,真菌、放线菌能利用菌丝沿着岩石中的晶面、解理、裂缝和晶界进行生长和渗透,在纳米尺度上对矿物进行穿插以及机械剥蚀作用,甚至形成所谓的矿物隧道化[36].
-
Welch曾发现,在相同pH值条件下,微生物产酸诱导的长石风化的速度是非生物处理风化速率的50—100倍,即与无机酸相比,有机酸对矿物的破坏作用更强[71]. 而微生物能够分泌多种有机酸,其电离出的H+以自由离子形式存在于水体中,有机酸浓度越高,相应的H+浓度也越高. 一方面,游离的H+能与矿物中氧化还原能力较弱的元素发生置换从而溶出其中的元素(Na、K、Ca等碱金属和碱土金属离子). 另一方面,有机酸发生电离后,基团中余下的—COOH、—OH等官能团能络合矿物中的高价金属离子(Fe3+、Al3+、 Si4+、 Cu2+、 Zn2+和Mn2+/3+/4+等),破坏矿物的晶体结构,从而释放矿物中的离子. 且微生物在该产酸过程中的效率远比想象中的要高,很多细菌仅需要1 d甚至12 h,就能将反应液pH值由中性7.5降低至4[34, 72]. 不同细菌分泌的不同种类有机酸对矿物的作用效果也存在差异. 以硅酸盐细菌、金黄色葡萄球菌和大肠杆菌为试验对象,发现这3种细菌的主要胞外有机酸为草酸、乳酸、柠檬酸和琥珀酸;它们对方解石的溶解效果也不同,其中草酸、乳酸和琥珀酸使方解石颗粒发生了不同程度的溶解,具体表现为颗粒失重,而柠檬酸溶解方解石后又发生了重结晶行为,且残余固体呈纤维状[73-74]. 除质子交换和络合作用以外,有机酸还可以通过改变溶液化学环境使矿物溶解. 如有机酸电离后的基团以配体的形式与溶液中的金属离子形成配合物,从而降低溶液中金属离子的浓度,改变难溶金属化合物的溶解平衡,提高难溶性金属化合物的溶解度,进一步加速矿质元素的溶出[53]. 此外,由微生物呼吸所产生的CO2形成的碳酸或硝化细菌产生的硝酸/亚硝酸等也能诱导矿物发生一定程度的溶解[75]. 在缺铁胁迫下,部分微生物可分泌低分子量(200—2000 Da)、高亲和力的铁载体来获取铁,铁载体作为一类特异性的铁离子螯合剂,其本质为非核糖体肽,按其化学结构可分为儿茶酚盐型、氧肟酸盐型和羧酸盐型3大类[76]. 铁载体的作用主要是螯合铁,但它也能非特异性地与环境介质中其他金属元素如Co、Cr、Mn、Mo、Ni、Zn螯合,促进矿物的溶解[77].
-
自然环境中,生活在矿物表面的微生物常常面临营养匮乏,阳光直射等恶劣环境,为了生存,微生物可通过分泌胞外聚合物(extracellular polymeric substance, EPS)使其附着于矿物表面形成凝胶层或生物膜[78]. 生物膜的成分和结构特殊,主要由蛋白质、多糖、核酸、糖醛酸、腐殖酸等生物大分子聚合物组成,其中蛋白质和多糖占总量的80%左右. 生物膜作为连接生物圈和土壤圈的关键微区,不仅能强化微生物和矿物的接触帮助其获取营养元素,还能为微生物自身的生长营造有利微环境. 例如,Glowa等在低钾培养基中添加黑云母,发现Piloderma sp.能高效利用黑云母的层间钾来维持其正常生命活动,并在培养时间长达110 d的时候仍处于对数生长期[79]. Grant等探究在缺铁/富铁培养基中,细菌在黑云母(富铁矿物)和玻璃表面的生长情况,进一步揭示了细菌能通过调控生物膜中多糖的相对含量来增强风化作用,从黑云母中获取铁以应对缺铁胁迫,其多糖/蛋白质的比值是含铁培养时的两倍;生物膜中Fe3+、K+、Mg2+等离子浓度也显著高于外围培养基,成为了细菌生长过程中提供阳离子营养盐的库[47]. Xu等将Serratia marcescens S14和黏土矿物(蒙脱石、高岭石、针铁矿)进行混合培养,发现加入黏土矿物后,细菌与黏附相关基因fimA、bsmA及EPS生成相关基因eps的表达均发生显著上调,促进了细菌生物膜的形成和对重金属镉的吸附[22]. 与游离细菌相比,以生物膜形式存在的细菌对重金属的抗性可提升2—600倍[80].
膜中各组分对细菌-矿物复合体的形成也有着不同程度的影响. 生物膜中的多糖—一种线性绕曲的高分子聚合体,能有效吸附矿物和土壤颗粒,链上存在大量—OH基,可与黏土矿物晶面上的氧原子结合形成氢键[81]. 生物膜中的蛋白质,包括酶蛋白和结构蛋白,不仅能分解生物膜中的物质为细菌生长提供养分,还关系着生物膜在非生物表面的吸附及形成;在这过程中,氢键和静电相互作用是影响矿物表面吸附蛋白质的主要因素[82-83]. 以枯草芽孢杆菌为例,其EPS主要成分为多糖和蛋白质,含有羧基、羟基、氨基、磷酰基、磷酸基、硫酸酯基等多种官能团,来源于蛋白质含EPS-N的基团会优先选择性吸附在蒙脱石和高岭石表面,而来源于核酸含EPS-P的基团则优先选择性吸附在针铁矿表面[84]. 生物膜所具有的络合及联结功能极大地促进了微生物-矿物复合体的形成,微生物营养的获取效率、重金属抗性、矿物溶蚀能力也得到显著提升[30, 85].
-
微生物的呼吸作用本质上即是氧化还原反应,不同于真核生物消耗氧气来进行呼吸,许多细菌可以利用矿物中的金属元素作为电子受体来实现自身的能量和代谢需求[86]. 其中最为典型的便是铁元素. 环境中的Fe(Ⅱ)常常被氧化为Fe(Ⅲ),自然pH下易沉淀,生物不便利用. 但由于铁的氧化还原特性,能参与电子传递(呼吸链、光合作用和Fe-S蛋白等),使其成为许多生物的必需元素. 铁常以二价或三价状态存在于矿物中,使得含铁矿物,如针铁矿(α-FeOOH)、赤铁矿(Fe2O3)、水铁矿(5Fe2O3·9H2O)、磁铁矿(Fe3O4)及纤铁矿(γ-FeOOH)等成为自然界中最常见的氧化还原活性矿物. 微生物为了从矿物中获得足够的铁满足其营养需求,亦进化出了多种铁氧化还原途径. 其中,通过氧化电子供体还原胞外不溶性铁氧化物并产生能量的过程称为异化铁还原或铁呼吸[87]. 与同化作用不同,异化铁还原过程中的还原产物Fe(Ⅱ)积聚在细胞外,其本质是呼吸链上的电子传递过程. 异化铁还原主要有4种机制[88]:(1)微生物通过细胞外膜蛋白直接接触铁矿物并发生电子转移,Fe(Ⅲ)氧化物被还原为Fe(Ⅱ);(2)微生物分泌铁载体等螯合剂促进铁溶解,增加微生物与矿物的接触从而提升还原速率;(3)微生物利用土壤中广泛存在的导电介质如腐殖质,或自身分泌黄素、醌类等物质充当电子载体加速铁还原过程;(4)微生物与铁矿物通过纤毛(纳米导线)进行胞外电子传递. Liu等以细胞色素c (c-Cyts)为切入点,发现光照条件下半导体赤铁矿产生的导带电子能直接还原c-Cyts. 而在黑暗厌氧条件下,由于Fe(Ⅱ)/c-Cyts存在,微生物先将代谢产生的电子由胞内穿过赤铁矿的导带传递给c-Cyts将其还原,然后还原态的c-Cyts再将电子转移至Fe(Ⅲ),在完成铁还原过程的同时细胞色素自身恢复至氧化态,并继续参与新一轮的电子传递作用,如此循环往复地进行下去[89]. 当微生物还原高价态的铁氧化物时,不仅干扰了重金属的生物地球化学循环,还影响了有机污染物和重金属在环境中的迁移、转化能力和生态效应,因此受到了人们的密切关注.
除了铁元素外,锰元素价态多变(Mn2+/Mn3+/Mn4+),含锰氧化物种类繁多,自然界中锰氧化物的形成很大程度上也依赖于微生物驱动,例如中性pH下,微生物氧化Mn(Ⅱ)主要形成水钠锰矿或二氧化锰[90]. 与人工合成相比,生物成因锰氧化物晶粒尺寸更小,比表面积更大,具有更高的反应活性,受周围环境介质的影响易发生相转化及老化,导致更多结晶性锰矿物的形成,如钡镁锰矿和六方水锰矿等. 这些变价金属矿物亦可跟微生物发生氧化还原作用,从而促进矿物的分解、元素的循环、污染物的消除以及微生物的生命活动[91-92].
-
近年来,随着电镜技术与分子生物学技术的飞速发展,研究者们在探寻微生物-矿物相互作用机理时也有了很多新的发现. 一些蓝藻、真菌、放线菌能沿着矿物孔隙对矿物进行穿插、挤压、剥蚀等生物力学行为,以协同矿物的分解. Burghelea等量化了与矿物结合的微量元素在微生物-植物复合体系的流动情况,发现丛枝菌根真菌的菌丝活性与界面pH值的降低及溶解性有机碳通量增加呈显著正相关关系,菌丝生长对矿物溶解、微量元素的获取及植物营养吸收具有明显地促进作用[93]. Mendes等选取3株风化能力较强的真菌,探究其对磷矿的转化机制,发现黑曲霉分泌的草酸能促进磷灰石的溶解和次生矿物水合草酸钙(CaC2O4·H2O)的形成,且菌丝与磷酸盐矿物颗粒直接作用能刺激菌丝发生形态变化并提供新的成核位点,低温SEM可清晰观察到菌丝穿透矿物并在其内部形成隧道[94]. 在真菌-铁矿物纳米颗粒体系中,晶格氧和氧空位的分子权衡关系是驱动铁矿物纳米酶活性的关键因子,真菌能借助生物矿化将纳米颗粒镶嵌进菌丝周围的EPS里,从而形成类金属-有机框架(MOF)结构的外壳,该结构不仅能对菌丝起到物理保护作用,还具有较强的催化活性[95]. Krause、Sun等通过实验室模拟及功能基因分析证实了微生物碳酸酐酶能促进CO2水合形成HCO3-直接攻击矿物,参与硅酸盐及碳酸盐的风化[96-97],刷新了一直以来酶通过参与合成代谢产物间接促进风化的认识,拓宽了微生物与矿物相互作用的范围[98]. 也有部分文献报道微生物能通过分泌氨基与胺类物质对硅酸盐矿物进行碱溶[99].
-
在自然环境中,微生物与矿物在任何时间、空间尺度上都能发生相互作用,改变矿物的表面性质及微生物活性,从而影响土壤中重金属的形态分布和生物有效性[2]. 对微生物代谢相关指标例如酶活性、呼吸速率进行监测,发现土壤矿物能够刺激或抑制微生物的生长及部分生理功能,影响土壤微生物群落的组成[100]. 大量研究表明,微生物与土壤矿物相互作用可以形成一种互利共赢的关系. 例如,土壤矿物中含量丰富的黏土矿物能为微生物的生长提供能源、营养元素以及代谢所需的电子受体,微生物的生长也反过来影响着黏土矿物的溶解与沉淀. 利用微生物-矿物这一体系协同效应治理重金属污染成为了当下的研究热点. 在微生物-矿物作用体系中,硅酸盐矿物、铁氧/硫化物矿物等受到重点关注,它们均是土壤的主要矿物. 硅酸盐矿物主要含铝、镁、硅等元素,同时含有铁、铜、锰、钾、钙、锌等一种或多种元素. 铁氧/硫化物矿物研究较多的主要包括水铁矿、针铁矿、赤铁矿、磁铁矿、纤铁矿、黄铁矿、磁黄铁矿等. 众多研究表明,在微生物-硅酸盐矿物以及微生物-铁矿物体系作用过程中,均发现了积极的重金属固定效应[20, 101]. 为此,本部分将首先简单概述矿物和微生物主要的重金属固定机制,并进一步重点介绍微生物-硅酸盐矿物、微生物-铁矿物两个作用体系中,微生物和矿物的协同作用对重金属的固定作用和机制.
-
微生物与矿物作为土壤中主要的活性组分,它们本身在重金属污染修复中具有积极的作用. 对于活性矿物而言,硅酸盐矿物、铁/锰氧化物矿物是其中的典型代表. 例如,土壤中的硅酸盐矿物主要为原生硅酸盐矿物如长石等风化后产生的次生硅酸盐矿物,其中以黏土矿物为主,它们孔隙丰富、比表面积大,离子交换性、吸附性和极性都很强. 因此,土壤硅酸盐矿物本身在污染治理尤其是重金属污染修复方面有着独特的优势. 土壤矿物主要通过吸附(物理吸附、化学吸附、离子交换吸附等)、界面沉淀、类质同象替换以及配体交换作用(如重金属离子与表面羟基中氢离子交换)等机制实现重金属固定[102-103],本文对分子尺度上矿物对重金属离子的固定方式进行了总结(图2).
对于微生物,根据微生物对重金属作用方式的不同,其固定机理可分为生物吸附、生物转化以及生物矿化. 微生物对重金属的吸附主要有胞外吸附、细胞表面吸附以及胞内累积(见图3,该图使用Figdraw在线绘制). 胞外吸附指微生物在生长代谢过程中分泌出多聚化合物,其表面含有大量能与金属离子相互作用的官能团,进而吸附或螯合重金属离子,阻止其进入细胞体内. Cao等研究发现希瓦氏菌HRCR-1的胞外聚合物(EPS)能通过吸附和还原作用实现U6+的固定化,其中紧密型EPS (tightly bound EPS)对U6+的固定效果显著,尤其是针对低浓度的U6+;并提出EPS中的多糖组分强化了细菌对U6+的整体吸附且对松散型EPS (loosely associated EPS)的反应活性起决定性作用[104]. 细胞表面吸附是因为细胞壁表面富含羟基、羧基、巯基和磷酸基等活性基团,使得细菌表面具有阴离子的性质,很容易与重金属发生有机结合. 胞内积累则是指进入细胞内的重金属通过区域化作用被分配至细胞内线粒体、液泡等不同部位,并与金属硫蛋白、多肽等结合形成沉淀,转化为低毒甚至是无毒的形式,最终实现重金属的固定. Lin等将Pseudomonas putida CZ1的生物膜细分为胶体EPS、荚膜EPS、细胞壁细胞膜和细胞内,探究各组分间重金属Cu2+的分布趋势,发现60%—67%的Cu2+位于胞外聚合物,以荚膜EPS占比最高;15.5%—20.1%的Cu2+与磷酰基反应生成了磷酸铜固定在细胞壁及细胞膜,17.2%—21.2%的Cu2+与巯基结合在细胞内部,实现了铜的有效区隔与积累[105]. 微生物对重金属的转化主要指微生物通过氧化/还原反应、甲基化/去甲基化、溶解以及有机络合配位降解等作用使其朝着无毒或低毒形态转变. 常见的有将Cr6+还原为Cr3+,Hg2+还原为易挥发的单质Hg、砷的甲基化等[106-107]. 生物矿化的机理较为复杂,根据微生物对矿化产物调控程度的不同可分为诱导矿化和控制矿化两类. 诱导矿化指微生物通过代谢活动引起局部微环境的改变,营造出有利于矿物沉淀的物理化学条件,从而在胞外诱导形成矿物的过程;控制矿化则是细胞自身调控下使摄入的金属离子与阴离子发生反应,从而得到具有特殊组装方式和多级结构的矿物. 人们关注较多的有分布广泛且易于获得的碳酸盐矿化菌、磷酸盐矿化菌、铁细菌和锰氧化细菌等[108-110]. 例如,Li等研究Cd2+对一株耐镉蜡样芽胞杆菌的作用,发现在高浓度Cd2+ (1 mmol·L−1)胁迫下,该菌胞内与细胞壁上能观察到高密度黑色矿化颗粒,XPS表征证实其为Cd2+的硫酸盐、磷酸盐和氢氧化物,且存在明显的混合晶型结构,具有较好的环境稳定性[111].
-
在微生物与硅酸盐矿物的协同作用下,重金属固定效果通常能得到明显强化. 在过去的10多年间人们就重金属离子在矿物-细菌二元复合体甚至多元复合体的结合机制与吸附性能上开展了各类研究. 同时,微生物-矿物复合方式、比例、环境介质等因素对重金属吸附速率、吸附容量和产物类别的影响也得到了广泛关注[20, 112-114].
微生物-硅酸盐矿物相互作用体系相比于微生物和矿物单体系,主要通过以下6种方式影响对周围重金属污染物的净化作用:(1)提高固有活性位点利用率. 细菌组分的引入能显著提升矿物和土壤颗粒的重金属吸附容量. Huang等将从矿区污染土壤中分离得到的一株产气肠杆菌(Enterobacter aerogenes)与高岭石胶体复合,发现复合体系比表面积增加了8.8%,Cd吸附量也由38.9 mmol·kg−1提高至63.8 mmol·kg−1,并进一步提出,细菌-矿物复合体黏附区内新生成的细胞壁-矿物界面能将一些原本被掩蔽的活性位点暴露出来,二者相互作用下引起的表面性质改变是造成重金属吸附量显著提升的重要原因[115]. Du等利用假单胞菌(Pseudomonas putida X4)、蒙脱石以及腐殖酸(HA)构建二元/三元复合体时,发现二元复合体Mt-Bacteria对Cd2+的吸附容量最大,最大理论吸附值为14.15 mg·g−1,比原蒙脱石增加了71.29%;而调整复合体组分构成及矿物-细菌复合方式后,三元复合体Mt-HA-Bacteria吸附量仅为9.80 mg·g−1,说明多元复合体的组成、菌-矿复合体的形成方式以及环境介质等因素均能影响其吸附性能[112]. (2)增加额外吸附位点(如羟基、羧基、巯基、磷酰基). Tan等将微藻与蒙脱石进行复合,实验表明pH值为5.5、藻矿比为1:5时,复合体对Cd2+的吸附量达到最大值65.25 mg·g−1,虽低于微藻的83.20 mg·g−1,但与纯蒙脱石的40.57 mg·g−1,相比提升了60.83%;复合体中蒙脱石的存在能有效促进微藻细胞的分散,从而暴露出更多的羧基和磷酰基位点供Cd2+在微藻表面发生结合,EXAFS结果进一步表明,复合体镉吸附性能的提升源于Cd2+在微藻与蒙脱石之间起到了桥接作用,其中单齿羧基-Cd与磷酰基-Cd配合物的形成使得Cd2+处于更稳定的状态[113]. (3)改变重金属与矿物的作用方式(如形成三元桥键结构). Qu等利用蒙脱石和假单胞菌按不同质量比进行复合并开展铅吸附实验,发现蒙脱石-细菌复合体与Pb2+作用可形成三元桥键复合物,即重金属离子充当阳离子桥连接复合体系中的矿物和有机组分,虽然桥键结构并未提升复合体对Pb2+的吸附量,但细菌源有机质的存在可藉由桥键结构增加重金属在矿物组分上的分配,从而有效促进Pb2+在矿物组分上的分布,在蒙脱石边面上形成双齿共边内圈络合物[19]. (4)影响矿物或微生物内部分散性或团聚性. Zhou等将海洋蓝细菌(聚球菌属,Synechococcus sp.)与3种常见黏土矿物(蒙脱石、高岭石、伊利石)相互作用,发现蓝细菌吸附聚集在矿物表面以形成更大的微团聚体,同时,相比于矿物,重金属Cd优先吸附在复合体中的蓝细菌表面[116]. (5)破坏矿物的原先结构(如层状矿物层堆积结构的剥离). 细菌的细胞壁或其胞外聚合物EPS作为细菌与土壤矿物或环境污染物如重金属离子接触的第一道屏障,其巨大的比表面积和丰富的表面官能团也引起了人们的注意. Yan等将芽孢杆菌(Bacillus sp. NT10)的EPS提取后与蒙脱石按5:50、1:50、0.5:50 (W/W)的3个比例进行复合,结果表明低质量比复合体对Cd2+吸附效果最佳,最大吸附量可达74.8 mg·g−1,;EPS能借助氢键作用和C=O、C—N、COO-官能团与层间阳离子的化学反应插入蒙脱石层间,促进蒙脱石片层的剥离,提升其镉吸附性能[65]. (6)改变微生物的分泌活动(如受所接触矿物的刺激改变分泌物种类与含量). Xu等将沙雷氏菌(Serratia marcescens S14)与黏土矿物(蒙脱石、高岭石)进行混合培养,发现加入黏土矿物后,细菌与黏附相关基因fimA、bsmA及EPS生成相关基因eps的表达均发生显著上调,其中“矿物+镉”处理的基因相对表达量较空白对照增加了2.8—17.8倍,表明复合体能通过促进细菌生物膜的形成强化对重金属镉的吸附[22].
-
金属离子在微生物-铁矿物复合界面的吸附行为,尤其是铁氧化/还原细菌与铁矿物之间的相互作用同样受到广泛关注. 自然环境中铁能够以离子,或无定型、结晶态铁氧化物形式存在,而微生物既能在有氧或缺氧条件下催化Fe2+的氧化,又能厌氧下将Fe3+还原;且微生物参与下铁的转化速度远大于其相应的化学反应速度,该过程往往伴随产生大量生物-铁氧化物混合物,形成微生物-铁矿物复合体.
自然界中许多水生植物就巧妙利用了微生物-铁矿物这一复合体系来增强营养吸收和抵御胁迫. 以水稻为例,稻田土壤中的铁、锰氧化细菌能够在水稻根表生成一层黄棕色的铁锰氧化物胶膜,简称铁膜,主要成分为水铁矿、纤铁矿、针铁矿等无定形铁氧化物. 铁膜既能充当动态营养库改善植物营养,又能通过物理吸附、共沉淀和竞争结合位点等方式来降低重金属吸收,可谓天然屏障[117]. 与单一的铁矿物体系相比,微生物更易与组成多元的铁矿物-有机物复合体(Fe-OM)发生氧化或还原反应. Copper等选取铁还原模式微生物——希瓦氏菌为研究对象,探究水铁矿表面吸附或共沉淀有机物对希瓦氏菌铁还原速率的影响,结果发现增加有机物含量能显著提升希瓦氏菌的铁还原速率[118]. 由于铁氧化物和微生物对重金属均具有较高的亲和力和吸附能力,二者形成的复合体对重金属迁移转化的影响也是研究者们关注的焦点. Wang等通过比较不同种类的希瓦氏菌对含砷铁矿物(黄铁矿和臭葱石)中As、Fe的释放行为,揭示了实验室条件下富铁砷污染土壤中微生物活化砷的潜在机制,认为体系中的次生矿物与新增的微生物的生物量有关,细胞表面含有丰富的活性基团,不仅能强化金属吸附,促进生物矿化沉淀,微生物还能根据周围环境改变而调整自身代谢,进一步为微生物群落生长和重金属吸附提供理想的吸附界面[119].
微生物在铁矿物表面的电子传递过程,以及该过程对重金属尤其是As、Cr、U等变价重金属(类金属)元素之间的氧化还原作用也至关重要. 微生物-铁矿物相互作用主要通过加速电子转移的方式加速促进变价金属/类金属污染物向低毒或无毒形态转变. 不少研究者选择人工构建复合体来强化其吸附性能. 例如,Mohamed等利用细菌-针铁矿-腐殖酸体系对铬进行吸附,发现与单独处理相比,三元复合体能显著提高Cr6+还原率(从56%到79%);XPS结果表明还原后的Cr3+以Cr(OH)3和Cr2O3形式沉淀在细菌表面;腐殖酸在反应过程中充当电子穿梭体,强化了电子传递过程,从而促进铬还原[120]. 酸性矿山废水中的富铁次生矿物如施氏矿物、黄钾铁钒等,能通过配位反应吸附水中的重金属Cr6+,缩短体系中细菌与铬酸盐之间的电子转移距离,因此Cr6+的生物还原速率得到显著提高[121]. 由于自然界中大部分铁、硫氧化物都属于半导体矿物,光照带来的矿物活性变化和对共存微生物的影响也不可忽视. 一些铁氧化物如赤铁矿、针铁矿、纤铁矿能通过日光催化为非光合作用微生物以及电活性细菌捕获太阳能,促进复合体系中微生物生长的同时缓解周边环境中重金属对微生物的毒害作用,利用该复合体系进行环境污染治理也成了重要的研究内容[13]. Cheng等研究了黑暗和光照条件下赤铁矿与希瓦氏菌对Cr6+去除的影响,发现黑暗条件下,赤铁矿能将细菌与铬富集在矿物表面,促进铬的微生物还原以减轻其对细菌的毒害;然而,随着反应的进行,矿物本身以及微生物作用产生的次生矿物对细菌的包裹将阻碍其与铬的进一步作用. 相反,光照触发了一条新的电子传递途径,将赤铁矿光催化反应与希瓦氏菌胞外电子传递联结起来,促进微生物生长代谢的同时提高铬的去除效率,且该过程中赤铁矿与希瓦氏菌的协同作用并不受矿物与细菌比例或电子传递抑制剂的影响[14].
-
近年来,随着研究的不断深入与拓展,新的研究成果不断涌现,对微生物与矿物间的相互作用也有了进一步的认识与了解,同时,利用该过程进行矿物的提纯、改性以及功能化应用,修复污染水体与土壤也成了研究热点. 然而,微生物-矿物相互作用研究整体仍处于初级阶段,还存在很多不足与空白领域,亟待去探索和实践.
(1)微生物数量巨大,种类繁多,但只有部分常见种属和模式微生物与矿物间的相互作用被研究者们所关注,同时,研究对象的选取大多局限于少数典型黏土矿物与铁、锰氧化物矿物等,其他矿物相关的研究则有待进一步深入完善. 此外,许多研究结果都基于实验室中小型的简化实验,使用的多为纯矿物与纯微生物培养物,在常压、室温条件下,缓冲液或成分固定的培养基中进行. 而自然界中微生物大都以群落形式存在,与矿物的相互作用除了互利共生还存在其它方式,因此研究结果并不能很好地准确反映自然生态系统中的状况. 微生物在风化、矿化与矿物转化等过程中所扮演的角色远比看到的要复杂.
(2)虽然目前学界已提出了较为全面的微生物-矿物作用方式与机理,研究者们也从微生物基因组、代谢产物、矿物形貌、物相转变等多角度入手,揭示了微生物作用下矿物的微观与亚微观形态和结构变化,但分子或原子水平上详细的作用机制与概念模型,以及微生物与矿物间互作的表象背后的驱动力还留有很多谜团.
(3)关于微生物-土壤矿物-重金属三者的研究还很缺乏. 微生物对重金属胁迫的解毒(防御)机制及相应的调控措施,如金属抗性相关基因的转录与表达,代谢产物种类与含量的变化等;与单一的重金属胁迫或矿物刺激相比,“微生物-矿物”二元/多元复合体的结合方式与表面反应活性(官能团类型、浓度与电荷分布等),重金属在该系统表面的分配与固定规律等,仍需进一步探究.
面对这些挑战,需要更多跨学科科研工作者们密切协作、联合攻关,明晰土壤矿物与微生物之间的相互作用,共同揭示“微生物-矿物”体系与环境净化机制的内在联系,为微生物-矿物联合修复重金属污染提供更坚实的理论基础与科学依据.
微生物-矿物相互作用:机制与重金属固定效应
Microbe-mineral interactions: Mechanisms and immobilization effect toward heavy metals
-
摘要: 微生物-矿物相互作用是地表中最基本的地球化学过程,影响着重金属的迁移转化与生态效应. 重金属胁迫下,微生物演化出了一系列适应机制,改变着矿物的表面反应活性,而矿物反过来刺激着微生物的分泌活动. 在两者的协同作用下实现了对重金属的钝化. 本文综述了微生物-矿物相互作用机制,并重点总结了微生物-硅酸盐矿物、微生物-铁矿物体系中微生物和矿物的协同作用对重金属的固定机制. 微生物与矿物之间的作用机制主要包括生物力学和生物化学作用. 一些真菌、放线菌能利用菌丝沿着矿物晶面、解理、裂缝和晶界,在纳米尺度上对矿物进行穿插、挤压、剥蚀等生物力学作用,甚至形成矿物隧道化. 而大多数微生物主要通过分泌铁载体、有机酸以及氧化还原作用改造矿物. 两者相互作用改变着矿物表面及微生物活性,影响着重金属的形态. 微生物-硅酸盐矿物体系主要通过提高固有活性位点利用率,增加额外吸附位点,改变与重金属的作用方式,影响矿物或微生物内部分散性,破坏矿物的结构,改变微生物的分泌活动等方式实现重金属的钝化. 而微生物-铁矿物体系则主要通过加速电子转移的方式促进变价金属向低毒或无毒形态转变. 期望本综述能为微生物-矿物联合修复重金属污染提供理论支持.
-
关键词:
- 微生物 /
- 矿物 /
- 重金属 /
- 环境修复 /
- 微生物-矿物相互作用.
Abstract: Microbial-mineral interactions have recently demonstrated to play a critical role in affecting the migration, transformation characteristics and environmental impacts of heavy metals, via formation of “microbial-mineral” binary complexes or “microbial-mineral-organic matter” multiple complexes. Microbes have evolved a series of adaptation mechanisms and survival strategies under heavy metal stress, during which minerals are modified and heavy metals immobilized. In such situation, minerals not only provide nutrients for microbial growth, but could also act as an important protective umbrella for microbes against toxicity of heavy metals or other pollutants. In this review paper, the interaction mechanisms between microorganisms and minerals were first introduced. Subsequently, the synergistic effect and mechanisms of microbe and mineral in heavy metal immobilization were highlighted via microbial-silicate mineral and microbial-iron mineral systems. Mechanisms of microbial interaction with minerals are quite complex, and there are two synergistic actions by which microorganisms can decompose mineral substrates: physical and biochemical. Biophysical weathering of minerals commonly occurs in the interaction of fungi and actinomycetes with minerals. Fungi and actinomycetes can break minerals through fungal hyphae penetration and growth along crystal planes, cleavage, cracks and grain boundaries, mechanically boring and denudating the rocks at the nanoscale, leaving the cracks and tunnels inside. As for the majority of heterotrophic microorganisms, the biochemical route for mineral dissolution is dominated by leaching, which is enforced by three main mechanisms. That is, the secretion of siderophores, organic/inorganic acids and redox actions. These mechanisms strongly accelerate dissolution of mineral, causing the formation of “metal sink” around the microbial biomass. The “metal sink” in return, works as nutrient sources to promote the growth of microorganisms. Importantly, the intimate interaction between microbial and soil mineral significantly alters the surface reactivity of mineral and microbial activity, and therefore leads to the immobilization and changes of speciation and bioavailability of heavy metals. Microbial-silicate mineral and microbial-iron mineral systems were employed to ascertain why microbe-mineral systems possess such merits in heavy metals remediation than single microbe or mineral system. In microbial-silicate mineral system, the interaction of microbe and silicate promotes heavy metal remediation depends primarily upon the following mechanisms: 1) provide additional adsorption sites such as hydroxyl, carboxyl, sulfhydryl, phosphorus acyl. 2) increase the utilization rate of inherent active sites. 3) change the binding characteristics of heavy metals with minerals, for example, negatively charged microorganisms can act as intermediates to bridge heavy metal ions with minerals, forming stabilized monodentate or multidentate complexes. 4) affect the dispersion or agglomeration status of mineral particles and microorganisms. 5) change the original structure of mineral, like the exfoliation of silicate layers of 2D silicate minerals, or even destroy the lattice structure. 6) make adjustments on the type and content of secretion and excretion products to regulate the microbial activities under the stimulation of direct contact with minerals. While the microbial-iron mineral systems tend to promote the metal or nonmetallic pollutants with variable valence states from toxic forms to less toxic ones by accelerating the electron transfer. This paper aims to provide a solid theoretical and scientific basis for microbial-mineral remediation of heavy metal pollution.-
Key words:
- microbe /
- mineral /
- heavy metal /
- environmental remediation /
- microbe-mineral interactions.
-
近些年,随着我国工业固废产生量的逐渐上升,工业固废减量化、无害化和资源化问题受到越来越多的关注[1-2]。其中,水泥窑协同处置工业固废和危废的方式和比例逐年上升,利用工业固废与传统硅酸盐水泥原料化学成分相近的特点替代天然矿物生产水泥,有助于解决大宗工业固废的消纳与资源化的问题[3]。例如,新疆天业水泥厂以煤化工电石渣作为钙质原料,粉煤灰和炉渣作为硅质原料,煤矸石作为铝制原料,硫酸渣、铜渣和铁质尾矿作为铁质原料,柠檬酸渣作为水泥缓凝原料,粉煤灰、煤矸石等作为拌合材原料,制备出符合国家标准的硅酸盐水泥[3-4]。在水泥生产的过程中,煤化工电石渣的氯元素质量分数较高[5],远高于传统硅酸盐水泥原料,不仅影响水泥熟料的性能[6],还会对水泥窑况产生着一定影响[7-8]。
有不少学者对氯元素在水泥窑中的行为规律进行了研究。崔育东等[9]开展了外掺CaCl2的水泥烧制实验,结果表明,生料中适量的氯离子可在水泥烧成反应中充当矿化剂的作用,生成低熔点含氯矿物相(C11A7·CaCl2)。施慧生等[10]认为,在含有CaCl2的CaO-SiO2-Al2O3-Fe2O3-MgO体系中,还可能发生CaO+SiO2+CaCl2+C12A7+MgO→Alinite的反应,生成化学组成为Ca10Mg1-x/2Vx/2[(SiO4)3+x(AlO4)1-x]O2Cl(V:晶格空位,0.35<x<0.45)的Alinite相。WANG[11]等的研究发现,随着生料中氯质量分数的上升,水泥窑中生成的低熔点含氯组分会随烟气循环富集,致使分解炉和回转窑窑尾处形成结皮堵塞。ZHU等[12]从整体工艺层面分析传统水泥生产过程中氯元素的流动途径和质量分配,对水泥品质的保证和窑设备的维护具有一定指导作用。就天然原料制备硅酸盐水泥工艺而言,已知氯质量分数低于0.03%时对熟料的形成有积极影响,但对氯质量分数为0.04%或更高的高氯原料的研究意义不大[13]。KWON等[14]在研究以污泥为水泥原料时指出,即使生料中的氯化物质量分数最高为0.04%,但窑炉中的氯化物质量分数仍可达1.5%,继而开展了掺氯量为0~2%的生料掺杂NH4Cl水泥烧制实验,并得出熟料的主要矿物相C3S、C2S、C3A和C4AF的质量分数变化规律,但仅从实验角度给出这一结论,并未继续监测水泥强度性能变化。
目前,有关水泥中氯元素行为规律的研究主要集中在低氯质量分数生料的传统硅酸盐水泥工艺上,且涉及到水泥强度性能方面的实验研究较少。为了探究电石渣中高质量分数的氯元素对熟料物相组成和水泥性能的影响规律,本研究以某水泥厂全废渣生料为原料,借助热力学计算方法模拟不同掺氯量CaO-Al2O3-SiO2-Fe2O3-MgO-Cl体系的高温煅烧反应相图[15],揭示不同氯质量分数下该体系高温煅烧过程中的物相转化,并结合不同掺氯质量分数水泥烧制实验,综合分析氯元素对矿物相组成变化规律和由此引起的水泥物理性能变化,最后对完整工艺中氯元素的物质流进行计算分析。本研究结果可为全废渣水泥生产生料中氯质量分数的控制提供参考。
1. 材料与方法
1.1 实验试剂及设备
实验试剂。氯元素标准溶液,硝酸(HNO3,65%~68%),氟化钙(CaF2),氯化钙(CaCl2),三乙醇胺(C6H15NO3),二水硫酸钙(CaSO4·2H2O)等,均为分析纯;纯水为实验室自制。
实验设备。实验电炉(HTF-1600型,武汉亚华);离子色谱仪(DX-120型,美国DIONEX);XRD衍射仪(XRD-7000型,日本Shimadzu);行星式球磨机(QM-3SP4型,南京南大);水泥砼恒温恒湿标准养护箱(HBY-40B型,上海康路);微机伺服水泥抗折抗压试验机(DYE-300B型,无锡新建)。
1.2 实验原料
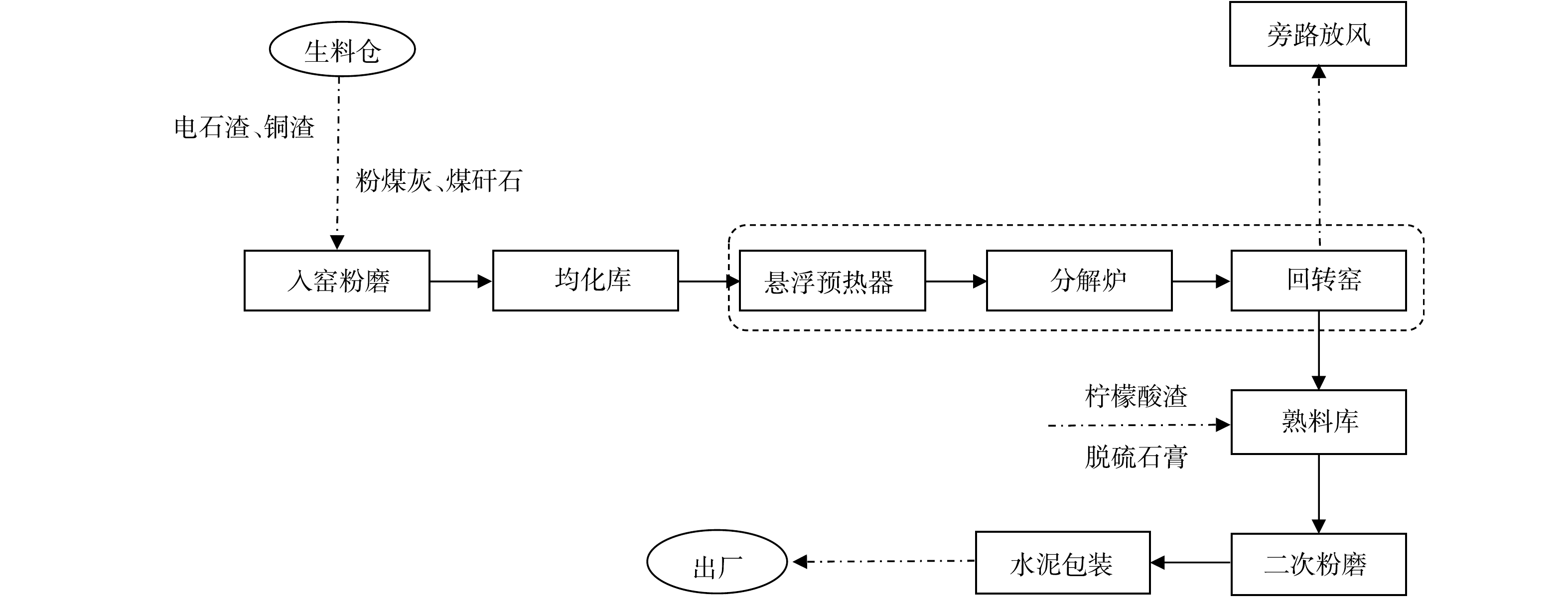
原料取自新疆天业水泥厂(以下简称T水泥厂)其中1条规模为4 000 t·d–1的水泥熟料生产线。其生产工艺流程如图1所示,采用电石渣、钢渣、粉煤灰和硅粉等10余种固废为生产水泥的原料,在经过原料预处理和生料配伍计算后,按照硅酸盐水泥正常生产流程生产符合国家标准要求的水泥产品。本研究所取原料为T水泥厂生料均化库中的生料。其中,生料的烧失量为13.99%;各组分的质量分数比例为,54.90%CaO、18.60%SiO2、4.45%Al2O3、3.33%Fe2O3、2.56%MgO、0.10%Cl−。熟料三率值,即石灰饱和系数(Lime Saturation Factor,LSF或KH)、硅率(Silica Modulus,SM)和铝率(Alumina Modulus,IM),分别为KH=0.84、SM=2.53、IM=1.31。
1.3 实验设计
鉴于生料中氯元素基本上以Cl−形式存在,参考相关文献[16-18],拟用CaCl2作为掺氯剂,利用T水泥厂生料均化库生料,开展氯(Cl−)质量分数为0.1%~0.5%的生料煅烧实验制备熟料和水泥,并以熟料矿物相组分的质量分数和水泥3和28 d强度性能作为分析指标。外掺CaCl2水泥烧制实验设计如表1所示,S-1~S-5组生料的化学组分除了氯质量分数外,其余(氧化物组分和三率值)视为不变。
表 1 外掺CaCl2水泥烧制实验设计表Table 1. Design of experimental table for calcination of CaCl2 containing cement实验编号 氯(Cl−)掺量/% 氯(Cl−)质量分数/% CaCl2掺量/g 生料原料/g 总生料/g S-1 0 0.1 0 1 350.00 1 350.00 S-2 0.1 0.2 2.11 1 347.89 1 350.00 S-3 0.2 0.3 4.22 1 345.78 1 350.00 S-4 0.3 0.4 6.33 1 343.67 1 350.00 S-5 0.4 0.5 8.44 1 341.56 1 350.00 1.4 实验方法
1)生料制备。根据实验设计,精准称量好不同掺氯质量分数的CaCl2粉末和生料,放置在橡胶球磨罐中,用球磨机混合均匀后过190目筛至筛余率为12%~14%。准确称取筛下生料粉末450.00 g,加入50 mL纯水,用电液式压力试验机压制成Φ50 mm×20 mm的生料饼,放置在105 ℃的烘箱内12 h至恒重。
2)熟料烧制。烘干的生料饼盛放在石墨坩埚中,移至高温电炉中进行煅烧。高温电炉的升温程序设置依次为:0~300 ℃,升温速率6 ℃·min–1,升温时间50 min;300~900 ℃,升温速率10 ℃·min–1,升温时间60 min;900 ℃,保温50 min;900~1 450 ℃,升温速率10 ℃·min–1,升温时间110 min;1 450 ℃,保温时间90 min。将烧制好的熟料块从炉中取出急冷至室温,准确称量熟料块质量并记录。
3)水泥制备。依照GB 175-2007《通用硅酸盐水泥》标准[19],在熟料块粉磨过程中加入质量分数为0.3%的三乙醇胺试剂,粉磨后过80目筛至筛余率20%以下,制得熟料粉末,取5.00 g粉末留样(XRD表征备用)。按照m(剩余熟料)∶m(CaSO4·2H2O)=95∶5的比例掺入CaSO4·2H2O粉末,放置在橡胶球磨罐中,用球磨机混合均匀后过190目筛至筛余率20%以下制得水泥。
4)净浆实验。取适量质量的水泥粉末,按照0.30的水灰质量比加入对应质量的纯水,放在水泥净浆搅拌机上低速搅拌30 s,高速搅拌90 s。搅拌均匀的水泥浆体放入20 mm×20 mm×20 mm的水泥模具内(每个配方6个平行样),并放置在振动台上震动(120±5) s,用水平刮尺将模具表面的多余浆体刮掉,保持试块与模具表面的高度齐平,置于标准养护箱内养护24 h后脱模,制得抗压强度测定用的水泥净浆试块。脱模后的试件在养护箱中继续养护至指定龄期,等待3和28 d强度测定[20]。同上述实验步骤,将搅拌均匀的净浆水泥浆体也另外放入20 mm×40 mm×80 mm的水泥模具内(每个配方3个平行样)制备抗折强度测定用的水泥净浆试块,后续养护步骤同上。
1.5 分析方法
1)熟料XRD表征。采用XRD衍射仪定性分析水泥熟料矿物相组成;按照m(熟料)∶m(CaF2)=9∶1的比例掺入CaF2粉末作为内标物质,利用Rietveld全谱拟合分析法对熟料各矿物相的质量分数进行半定量分析[21]。XRD仪器采用CuKα靶,步长2θ=0.02(°)·step-1,扫描速度10 (°)·min–1(定量分析时采用4 (°)·min–1,电压30 kV,电流40 mA,石墨单色器。
2)热力学相图模拟。采用FactSage软件的Equilib模块模拟生料在800~1 500 ℃高温煅烧的物相转化过程[21]。输入T水泥厂生料均化库中的生料化学组分(质量分数),并将氯的质量分数设置在0.1%~0.5%的梯度内,继而模拟不同氯质量分数下,CaO-Al2O3-SiO2-Fe2O3-MgO-Cl体系的高温反应相变化历程。
2. 结果与讨论
2.1 热力学模拟分析
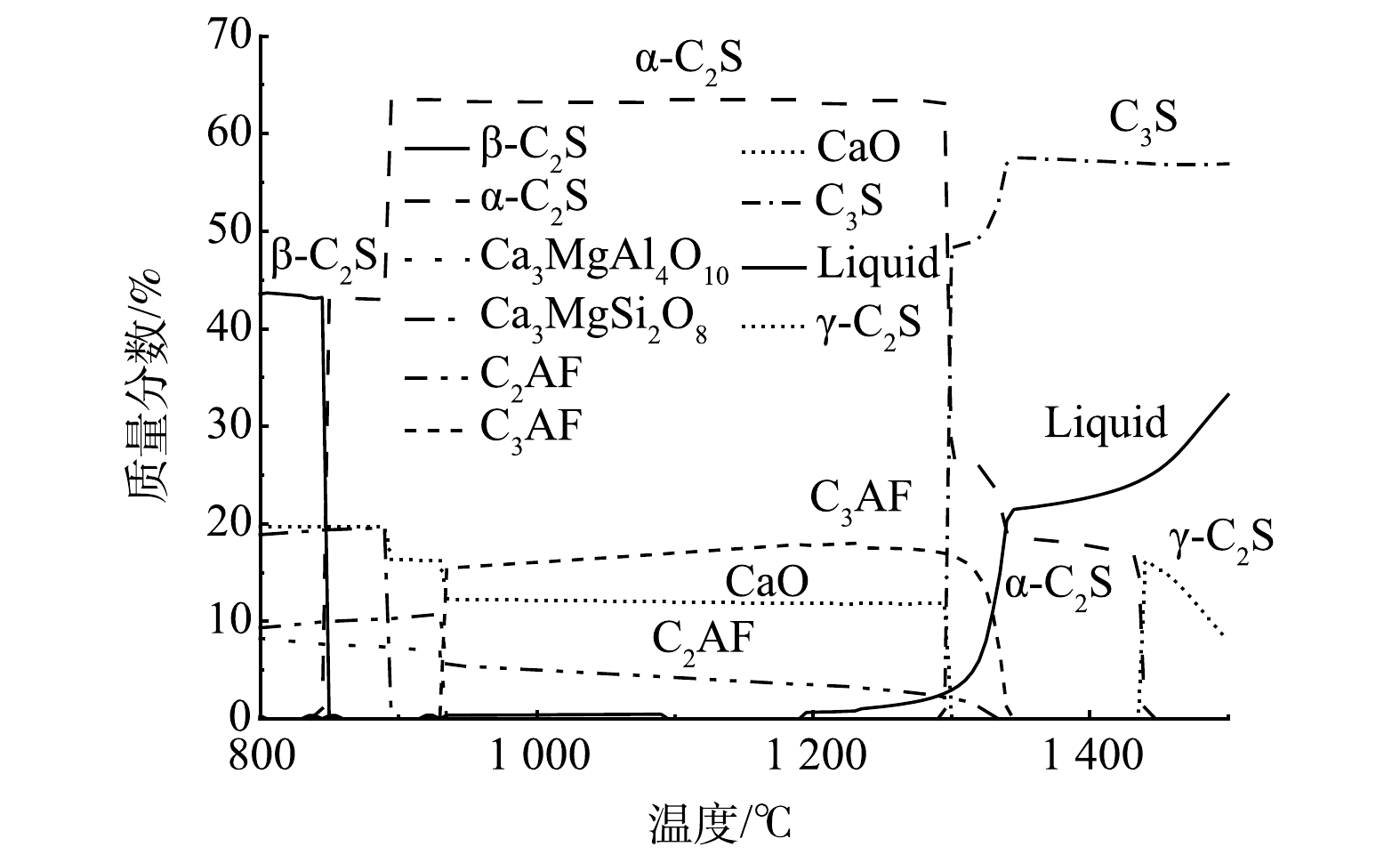
1)全废渣生料反应相图模拟。利用FactSage热力学软件,按照表1中第一行的生料各氧化物的质量分数比54.90%CaO∶18.60%SiO2∶4.45%Al2O3∶3.33%Fe2O3∶2.56%MgO∶0.10%Cl−模拟计算800~1 500 ℃温度区间内体系中各氧化物的反应历程,并绘制反应相图如图2所示。由图2可知,体系中的β-C2S在800 ℃前就已大量存在,伴随着铁相固溶体C2AF、钙镁铝盐中间矿物相Ca3MgSi2O8和Ca3MgAl4O10的生成。850 ℃后C2S由β型向α型转化,这与C2S在高温下的主要存在类型为α型的规律[22]是一致的。900~940 ℃,中间矿物Ca3MgSi2O8分解,进一步消耗体系中的CaO生成α-C2S,使得C2S质量分数骤增,并在900 ℃时达到最大值63%;同时,C2AF质量分数也有缓慢上升。940~1 300 ℃,Ca3MgAl4O10中间相全部分解,各矿物相相互转化,质量分数基本保持稳定,铁相固溶体中C2AF质量分数不断下降,C3AF组分占得优势[23];1 200 ℃后,体系中开始生成液相,为α-C2S与CaO结合生成C3S创造有利环境。1 300 ℃时,C2S大量转化为C3S,CaO的质量分数骤减为0。据此推测,熟料烧成实际温度对应热力学反应相图的1 300 ℃。1 300~1 340 ℃,热力学模拟的反应体系中除C3S以外的矿物如C3AF,倾向于分解成CaO、Al2O3、Fe2O3并熔融成液相,体系中的液相量持续上升,并进一步与C2S结合生成C3S。1 340 ℃后,C3S的生成量已达到稳定并呈轻微下降趋势。此时,C2S倾向于熔融生成液相,直至1 400 ℃后体系中的C2S由β型开始向γ型转化。热力学模拟相图图2反映出,体系中的C3S在1 300 ℃瞬时生成,f-CaO也在1 300 ℃时瞬间全部消耗。由此推断,热力学计算得到的CaO-SiO2-Al2O3-Fe2O3-MgO-Cl体系熟料烧成温度为1 300 ℃。
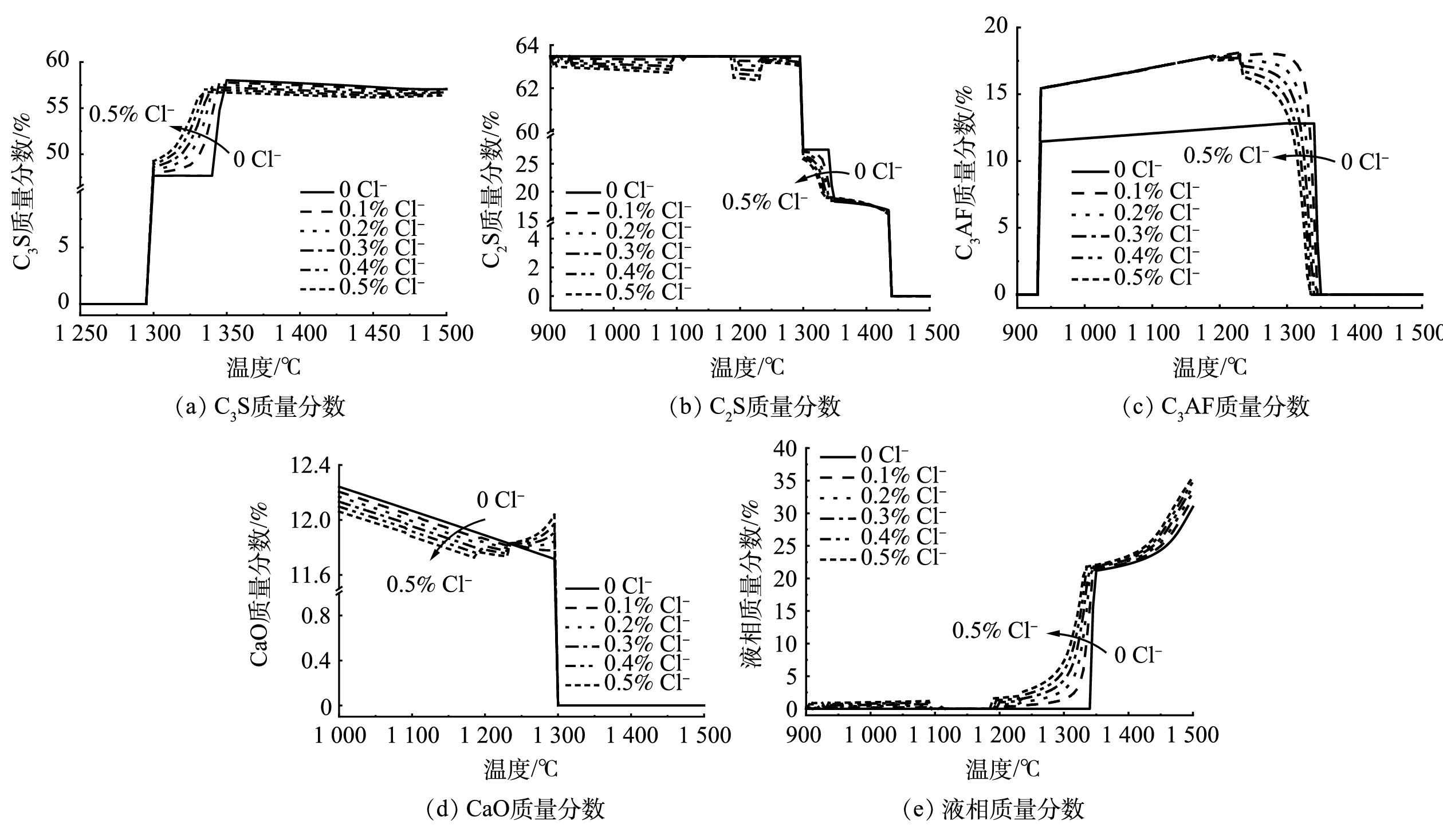
2)不同氯质量分数体系热力学相图模拟。进一步从热力学计算角度探索氯(Cl−)质量分数在0.1%~0.5%的范围内,CaO-SiO2-Al2O3-Fe2O3-MgO-Cl体系高温煅烧反应过程中的液相及各矿物相质量分数的生成变化规律,并与不含氯体系进行对比,着重关注1 300 ℃时各物相及液相的质量分数变化趋势。绘制不同氯质量分数下C3S、C2S、C3AF、CaO、液相的质量分数随温度变化图,如图3所示。由图3(a)可发现,随着氯质量分数的上升,1 300 ℃时体系中的C3S质量分数逐渐增加,氯质量分数从0.1%上升至0.5%时,C3S的质量分数由48%增加至49.5%。对照图3(b)和图3(d)可知,1 300 ℃时随着氯质量分数的上升,体系中的C2S质量分数呈现出不断下降的趋势,当氯质量分数由0.1%上升至0.5%时,C3S的质量分数从27.5%增加至25.5%;同时,体系中CaO的消耗量也随着氯质量分数上升不断增大。C3S、C2S和CaO的质量分数变化趋势与C3S的生成规律是一致的,即氯元素可以促进C2S结合CaO生成C3S的反应速率,并增加C3S生成量[17]。熟料中的铁相固溶体组成形式包括C2AF~C6AF[23],C3AF是其中的1种。由图3(c)可知,氯质量分数由0.1%上升至0.5%时,体系中C3AF的质量分数在1 300 ℃时从18%下降至13%,但均高于不含氯的体系。可见,氯元素的升高对于C3AF的生成起到了抑制作用。结合图3(e)可发现,液相量在1 300 ℃时随着氯质量分数的上升逐渐增加,但不含氯体系中液相量为0。因此,氯元素的存在促进了液相量的生成[6]。液相的形成主要依靠Al2O3、Fe2O3等氧化物组分[22]。可见,在热力学模拟的1 300 ℃时氯质量分数较高的体系中,Al2O3、Fe2O3等氧化物组分倾向于熔融成液相,因此C3AF的生成量逐渐降低。
结合热力学模拟CaO-SiO2-Al2O3-Fe2O3-MgO-Cl体系反应相图可知,熟料烧成温度为1 300 ℃。不同氯质量分数体系反应相图中各物相和液相量在1 300 ℃处的生成转化规律表明,氯元素可以促进C2S消耗CaO生成C3S,并促进液相量的生成。随着氯质量分数由0.1%上升至0.5%时,1 300 ℃时体系中的C3S质量分数从48%上升至49.5%;C2S质量分数由27.5%下降至25.5%,C3AF的质量分数从18%下降至13%。在不考虑动力学反应速率和时间限制的条件下,热力学相图模拟结果很好地反映了0.1%~0.5%氯质量分数生料体系高温煅烧反应过程中,主要矿物相C3S、C2S、C3AF及CaO和液相质量分数的变化趋势,这对水泥生产尤其是高氯质量分数的水泥生产工艺具有一定的理论指导价值。然而,热力学软件模拟有其局限性。一是未能考虑动力学方面的影响。这是因为,在实际生产中不可能达到理想的传质条件和无限的反应时间,如各物相的生成均在某温度处瞬时完成。二是FactSage软件数据库不含C3A组分,无法准确反映C3A的质量分数生成规律。因此,相图模拟的不同氯质量分数体系中各物相的质量分数变化规律,还有待开展不同的掺氯生料水泥烧制实验来进一步验证。
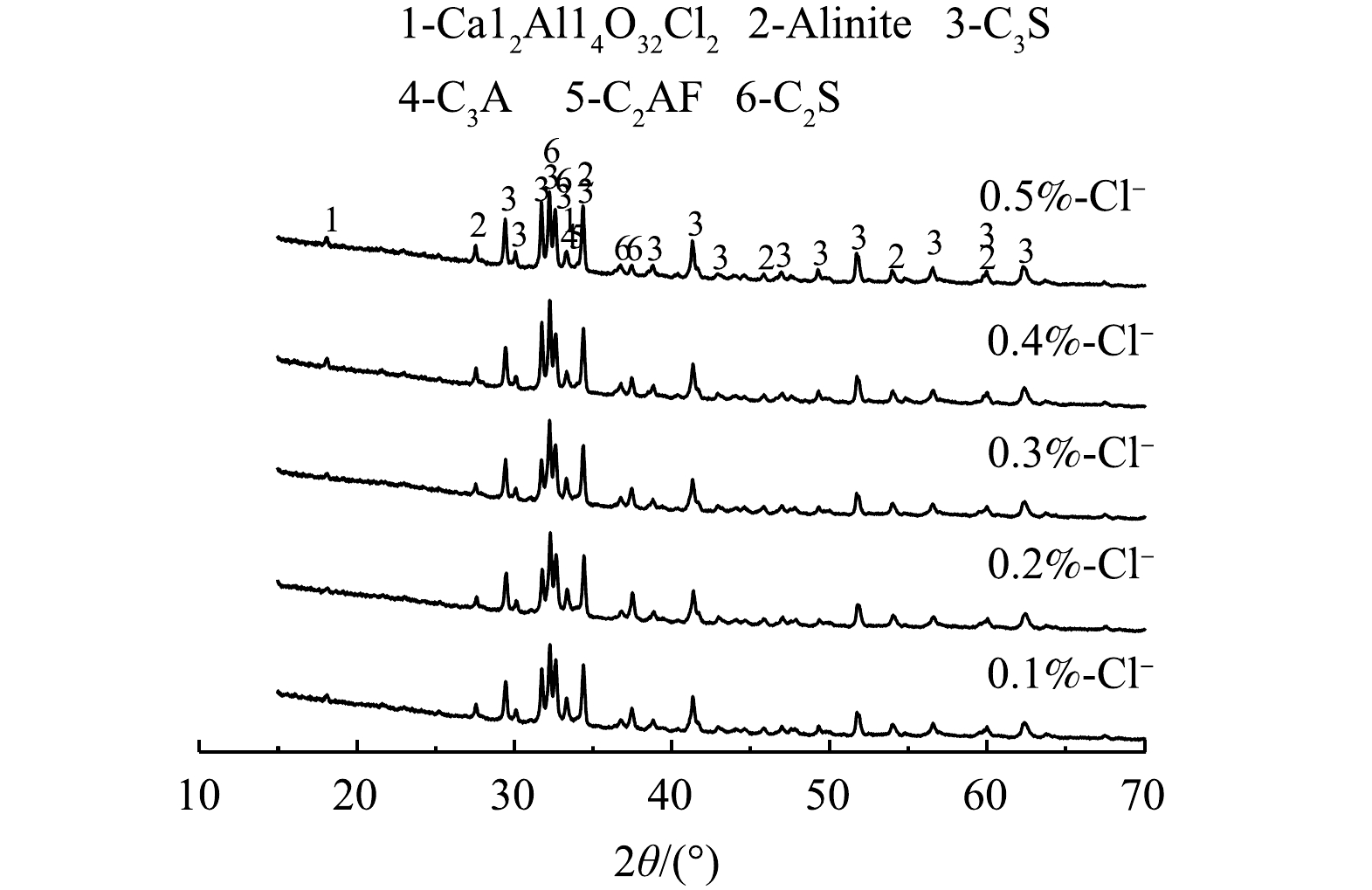
2.2 熟料XRD分析
对熟料进行XRD表征分析,结果如图4所示。全废渣水泥熟料中除了常见的C3S、C2S、C2AF、C3A矿物相之外,还发现了Alinite相和Ca12Al14O32Cl2相2个新相[10]。采用Rietveld全谱拟合分析法并借助MDI Jade 6.0软件对内掺CaF2熟料XRD图谱中各物相的质量分数进行精修[24]。精修过程中发现,由于Alinite相是通式为Ca10Mg1-x/2Vx/2[(SiO4)3+x(AlO4)1-x]O2Cl(V:晶格空位,0.35<x<0.45)[25-27]的一类混合物,难以得到其准确分子式并进行精修,但由于其结构与C3S类似且质量分数较少,将Alinite相质量分数纳入到C3S相中计算。主要对C3S、C2S、C3A、C2AF、Ca12Al14O32Cl2相、f-CaO和无定型相(Amorphous)的质量分数进行半定量分析,结果如表2所示。主要矿物相组分C3S、C2S、C3A、C2AF和Ca12Al14O32Cl2的质量分数变化如图5(a)和图5(b)所示。由表2中的精修参数可知,S-1~S-5组内掺CaF2熟料XRD图谱的精修结果均满足E≤R≤2E。这表明,精修结果在置信区间内。熟料中存在一部分无定型态物质。这可能是因为,冷却过程中液相来不及结晶形成玻璃体相,其中含有少量氧化物如Fe2O3、MgO等[22]。由氯质量分数为0.1%时Ca12Al14O32Cl2的质量分数为2.44%计算得到氯的质量分数为0.12%,此结果超过了生料中氯的质量分数。这说明,精修结果存在着一定的误差。但在相同的工艺条件和精修参数背景下,仍可借助XRD精修结果对熟料中主要矿物相质量分数的变化趋势进行半定量分析。
表 2 S-1~S-5组内掺CaF2熟料物相组分精修质量分数表Table 2. Phase content of S-1~S-5 clinker after Rietveld refinement with addition of CaF2 within group编号 矿物相组分质量分数/% 精修参数 C3S C2S C3A C2AF Ca12Al14O32Cl2 f-CaO Amorphous R/% E/% S-1 48.44 34.67 4.94 5.28 2.44 4.22 0.00 2.18 1.62 S-2 55.74 26.38 5.52 5.74 1.77 3.86 1.00 2.43 1.69 S-3 59.49 22.51 4.39 4.18 2.36 2.79 4.29 2.31 1.68 S-4 63.70 19.36 3.08 2.87 5.74 1.84 3.40 2.12 1.70 S-5 65.02 20.89 2.45 2.13 4.37 1.20 3.94 2.34 1.68 表2反映出,熟料的主要矿物相为C3S和C2S。随着氯质量分数的上升,熟料中f-CaO的质量分数逐渐减少。这表明,氯元素增强了熟料的易烧性。由图5(a)可观察到,氯质量分数由0.1%上升至0.5%时,C3S质量分数由48.44%增加至65.02%,其中包含着少量Alinite相;C2S质量分数则由34.67%下降至19.36%,且在氯质量分数为0.4%时达到最低值,当氯质量分数上升至0.5%后,C2S的质量分数有所增加。熟料中C3S、C2S和f-CaO质量分数的变化趋势表明,氯元素促进了体系中的C2S相向C3S相的转化,但在氯质量分数超过0.4%后,促进作用减弱。图5(b)表明,熟料中的C3A和C2AF组分受氯质量分数影响较大,当生料掺氯量上升至0.2%后,C3A和C2AF质量分数均呈下降趋势。其中,氯质量分数从0.2%上升至0.5%的过程中,C3A和C2AF的质量分数分别由5.52%下降至2.45%和5.74%下降至2.13%;同时,体系中的Ca12Al14O32Cl2相作为产生C3A的中间相,其质量分数不断上升,直至超过C3A和C2AF组分。从Al元素的质量守恒角度来说,部分Al元素还可能参与了Alinite相的形成。这表明,在氯质量分数较高的高温煅烧反应过程中,较多的Al2O3倾向于与CaO、SiO2、MgO和含氯组分等结合生成Ca12Al14O32Cl2相和Alinite相。由图5可以发现,氯质量分数由0.4%上升至0.5%时,体系中的C2S质量分数由19.36%上升至20.89%;同时,Ca12Al14O32Cl2的质量分数由5.74%下降至4.37%,而C3S质量分数仍增长了1.32%。结合Ca、Al、Si和Cl元素的质量守恒和Alinite相的化学组成可知,氯质量分数为0.5%时C3S质量分数的微弱增长可能主要来源于Alinite相。此时,氯元素促进C2S向C3S转化的作用较弱;相对地,体系中Alinite相的生成速率变大。
不同掺氯量熟料的各矿物相质量分数变化趋势表明,氯元素可增加高温体系中CaO的消耗量,促进C2S向C3S的转化,并显著增加C3S的生成量。同时,在氯质量分数较高的高温反应体系中,CaO、SiO2和Al2O3倾向于与MgO和含氯物质等结合生成Alinite相和Ca12Al14O32Cl2相;相应地,熟料中的C2S、C3A和C2AF相质量分数随着氯质量分数的上升均呈现明显下降趋势,这与上文热力学模拟不同氯质量分数体系C3S、C2S和C3AF的质量分数变化规律是符合的。值得注意的是,当生料中的氯质量分数超过0.4%后,体系中的C2S组分质量分数有所增加。可推测,此时氯元素促进C2S相向C3S相转化的作用变弱,而Alinite相的增长速率变大。
2.3 水泥强度性能测定
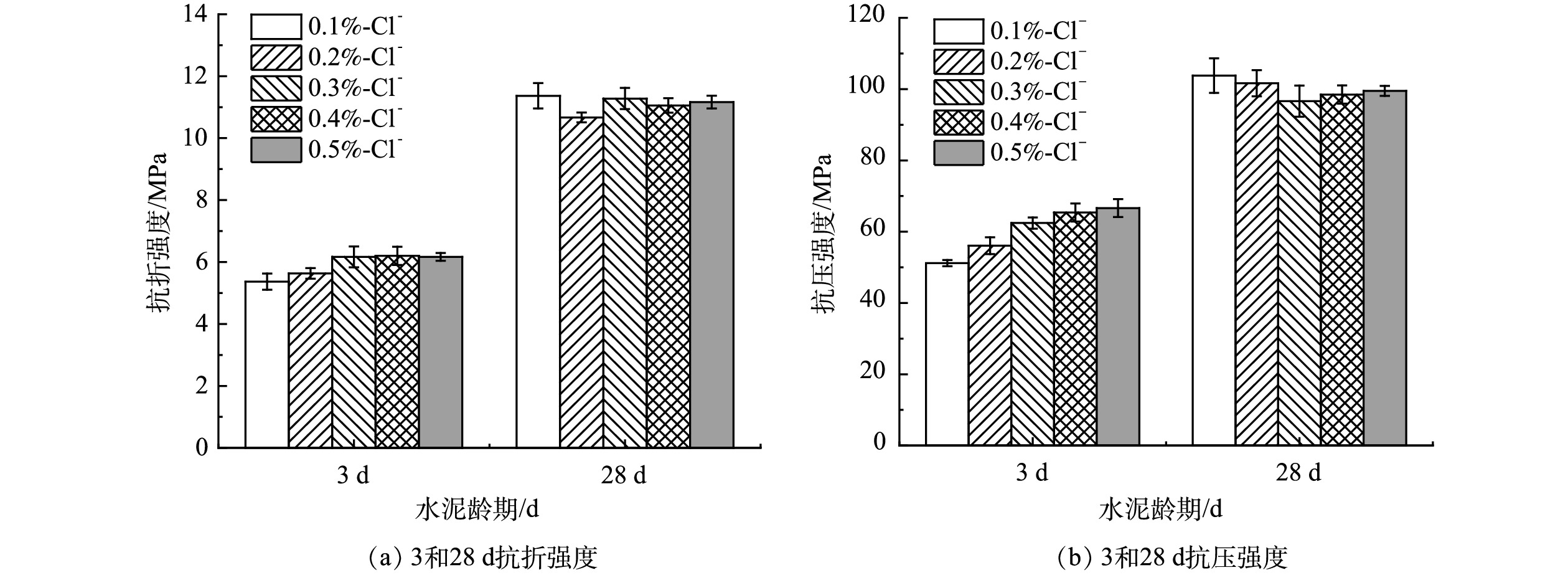
水泥3和28 d抗折、抗压强度数值如图6所示,结合上文熟料矿物相XRD精修半定量分析结果表2可知,影响水泥早期强度的C3S相在熟料中占比较大,可达50%~65%,其中包含的少量Alinite相也对3 d强度的增长有利,且随着氯质量分数的上升,C3S质量分数占比逐步上升,因此水泥3 d强度增长速率较快。使用SPSS软件进行相关性分析可知,氯离子质量分数与28 d抗折强度皮尔逊相关系数为0.972,表现为强正相关;氯离子质量分数与28天抗压强度皮尔逊相关系数为−0.666,表现为负相关。其中,氯质量分数为0.3%时,28 d抗压强度达96.6 MPa,相比氯质量分数为0.1%时的28 d抗压强度103.8 MPa降低了7%。实际上,水泥28 d强度受到多种矿物的综合影响,但主要是C3S和C2S质量分数的影响。熟料XRD矿物相质量分数精修结果表2表明,当生料掺氯质量分数上升时,熟料中C3S相质量分数不断上升的同时,C2S和C4AF质量分数却呈现下降趋势,C3S和C2S质量分数随掺氯量的变化趋势使得2者对水泥28 d强度的增长产生拮抗作用。因此,28 d抗压强度的增长空间不如3 d抗压强度,且总体呈现轻微下降的趋势。
对于附有旁路除氯系统的高氯原料水泥生产工艺而言,熟料中含有部分Alinite组分可使水泥具有易磨的特性,有利于水泥粉磨环节节省能耗[28-29]。结合S-1组~S-5组熟料XRD表征和水泥强度性能测定结果,为了极大程度地促进熟料中C3S相的生成,同时保证熟料中适宜的C2S质量分数和水泥优良的3 d和28 d性能,将生料氯元素质量分数控制在0.4%以下是较好的选择。
2.4 氯元素物质流分析
取流水线上某24 h工作周期内水泥烧制物料投入量和输出量数据,并根据GB/T 176-2017《水泥化学分析方法》[30]离子色谱法测定各样品中的氯元素质量分数,结果如表3所示。
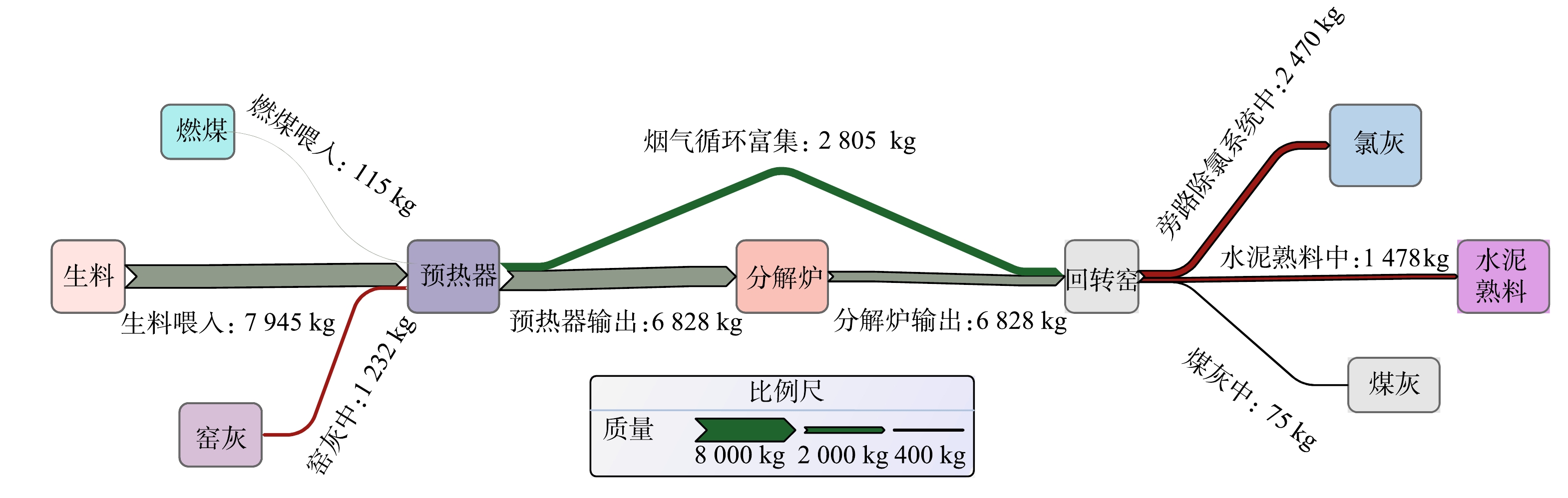
表 3 某24 h工作周期内各物料氯元素质量分数及物料喂入量和输出量数据Table 3. Chlorine content of each material as well as material feeding and output data in 24 h含氯物料 氯质量分数/% 物料消耗量/(t·d–1) 生料 0.112 7 094.000 燃煤 0.022 522.000 熟料 0.025 5 912.000 旁路除氯氯灰 21.900 11.280 窑灰 0.196 628.760 煤灰 0.084 88.840 结合图1的T水泥厂全废渣水泥工艺流程得知,整体工艺中的氯元素来源于电石渣、粉煤灰等工业废渣原料,在生料均化环节其质量分数得到均化。随着生料进料,熟料煅烧至1 100 ℃时,氯元素与生料中其他碱性金属组分如钠、钾形成低熔点的氯盐挥发到预热器、分解炉和回转窑中。当窑中煅烧温度进一步上升至1 300 ℃后,体系中的氯组分已大部分挥发至烟气中,只有小部分掺杂在熟料矿物相中被带出。一部分烟气中的挥发性氯组分随烟气至窑头处被新进的生料裹挟,随后在回转窑中循环富集;另一部分随烟气被抽取至旁路除氯系统中,被迅速冷凝除尘作为捕集的氯灰进行离线处理。随着窑尾处的烟气回到预热器后经过降温与除尘器收集到的窑灰被回喂进生料系统中,部分窑尾处烟气在温度适宜区的预热器和分解炉处富集形成结皮堵塞。根据图1工艺流程和表3的数据对氯元素的物质流动进行质量平衡计算。氯元素有2个来源,通过计算得到,来自生料的氯为7.945 t,来自燃料携带的氯为0.115 t,总量为8.060 t。氯元素有4个去向,其中,进入熟料中的氯的质量为1.478 t,进入旁路除氯系统收尘灰中的氯为2.470 t,去往窑灰中的氯为1.232 t,进入煤灰中的氯为0.075 t。根据质量守恒的原则进行计算得到随窑尾结皮、随烟气循环富集中的氯的质量为2.805 t。因此,系统旁路除氯的效率为47%。
由氯元素的质量平衡分析计算和工艺流程图1绘制氯元素的物质流分析Sankey图,如图7所示。氯元素的总量达8.060 t,其中随烟气循环富集的量为2.805 t,占氯元素总量的34.80%;熟料中氯元素的质量分数达1.478 t,占氯元素总质量分数的18.34%。可见,回转窑工艺下高氯全废渣生料在高温煅烧过程中氯元素的循环富集情况较为普遍,应特别注重水泥氯元素质量分数的指标。全废渣工艺的旁路除氯系统效率达47.00%,而普通水泥窑的旁路除氯效率可达70%以上[31],与普通硅酸盐水泥工艺相比,该除氯系统设备的效率仍有很大提升潜力。
3. 结论
1)掺氯质量分数为0.1%~0.5%的CaO-SiO2-Al2O3-Fe2O3-MgO-Cl体系热力学相图计算和水泥烧制实验均反映出,氯元素可促进C2S结合f-CaO转化生成C3S,并使得熟料中C3S质量分数上升,C2S、C3A和C4AF质量分数下降。
2)在氯质量分数较高的高温反应体系中,CaO、SiO2和Al2O3倾向于与MgO和含氯物质结合生成Alinite相和Ca12Al14O32Cl2相。当氯质量分数超过0.4%后,促进C2S结合CaO转化生成C3S的作用变弱,此时Alinite相的增长速率变大。
3)氯质量分数由0.1%上升至0.5%时,水泥3 d抗压强度从51.2 MPa上升至66.6 Mpa,呈上升趋势;C3S和C2S质量分数随氯质量分数变化趋势表明2者对水泥28 d强度的增长产生了拮抗作用,28 d强度增长空间较小。
4)在附有旁路除氯系统的高氯原料水泥生产实际中,建议生料中氯质量分数控制在0.4%以下,可极大程度地促进熟料中C3S的生成,并保证适宜的C2S质量分数和较为优良的3 d和28 d强度性能。
-
表 1 常见矿物-微生物相互作用中的细菌汇总
Table 1. Summary of some bacteria involved in mineral–microbe interactions
菌属Bacteria species 作用矿物Mineral 研究内容Research contents 参考文献Reference 革兰氏阴性菌 金黄杆菌hryseobacterium 蒙脱石 矿物介导下细菌重金属抗性调控机制 [37] 鞘氨醇单胞菌Sphingomonas 细菌在矿物表面的黏附及对有机污染物降解的影响 [38-39] 肠杆菌Enterobacter 产生草酸、酒石酸等溶解释放蛭石中的Fe、K、Si元素 [40] 沙雷氏菌Serratia 促进菌-矿复合体生物膜形成,强化Cd2+吸附 [22] 希瓦氏菌Shewanella 含铁黏土矿物-有机配体-希瓦氏菌复合体系生物还原铀 [23] 希瓦氏菌Shewanella 铁氧化物 “砷-微生物-铁氧化物体系”耦合反应动力学模型 [41] 地杆菌Geobacter 微生物驱动二价铁和高活性羟基自由基的形成 [42] 产碱杆菌Alcaligenes 粪产碱杆菌与铁矿物协同作用加速原油降解 [43] 伯克氏菌Burkholderia 钾长石 分泌葡萄糖酸和EPS促进矿物风化,溶出Al、Fe元素 [44] 根瘤菌Rhizobium 细菌肥料,酸解、络合作用释放Si、K、Al元素 [45] 戴氏菌Dyella 黑云母 贫瘠土壤中风化黑云母释放Al、Fe元素 [46] 假单胞菌Pseudomonas 增加多糖分泌量以风化黑云母获取Fe、Mg、K元素 [47] 弗拉托氏菌Frateuria 含钾矿物 解钾从而促进植物生长 [48] 水生拉恩菌Rhanella 金云母 风化矿物溶出Mg、Si元素 [49] 紫色杆菌Janthinobacterium 钾铝硅酸盐 低温仍能风化矿物释放K元素 [50] 色杆菌Chromobacterium 硅酸盐矿物 黏土矿物对紫色杆菌群体感应的影响 [51] 柠檬酸杆菌Citrobacter 碳酸盐矿物 生物成因碳酸盐矿物种类和形态 [52] 根瘤菌Rhizobium 水铁矿 微生物驱动的亚铁氧化过程中碳固定机制与砷转化规律 [53] 地杆菌Geobacter 蓝铁矿 分泌黄腐酸催化异化铁还原反应实现蓝铁矿资源回收 [54] 希瓦氏菌Shewanella 黄钾铁矾 以乳酸为电子供体还原黄钾铁矾生成菱铁矿与磁铁矿 [25] 硫杆菌Acidithiobacillus 铁尾矿 形成"cell-EPS-mineral"复合结构单元促进细菌定殖和矿物转化 [55] 硫杆菌Acidithiobacillus 金红石、闪锌矿 通过生物电化学作用参与半导体矿物的日光催化作用过程 [11] 脱硫弧菌Desulfurivibrio 硫化汞 硫化汞颗粒的表面结构及其生物甲基化潜能 [56] 土壤杆菌Agrobacterium 锰氧化物 细菌与矿物协同促进亚砷酸盐氧化 [57] 地杆菌Geobacter 锑矿物 利用呼吸性砷酸盐、锑酸盐还原酶还原锑 [58] 极地单胞菌Polaromonas 钒尾矿 微生物介导的钒尾矿中钒还原过程 [59] 脱硫弧菌Desulfurivibrio 锑尾矿 脱硫弧菌介导的硫氧化与锑还原耦合过程 [60] 不动杆菌Acinetobacter 含金矿物 细菌介导的金的生物地球化学循环 [61] 假单胞菌Pseudomonas 岩石漆 “水钠锰矿-假单胞菌”复合体系的电子传递过程 [62] 革兰氏阳性菌 芽孢杆菌Bacillus 蒙脱石 细菌-蒙脱石相互作用对蒙脱石结构的影响;提取细菌EPS构建EPS-蒙脱石复合体强化Cd2+吸附;微生物代谢对蒙脱石层间有机质保存的影响 [63][64][65] 类芽孢杆菌Paenibacillus 蒙脱石 微生物风化蒙脱石使其向伊利石转化 [66] 类芽孢杆菌Paenibacillus 钙长石、钾长石 细菌粘附促进钙长石溶解释放Si、Al、Ca元素;风化钾长石释放钾离子等促进植物生长; [67][68] 节杆菌Arthrobacter 黑云母 分泌葡萄糖酸促进黑云母风化释放Al、Fe元素 [69] 葡萄球菌Staphylococcus 砷黄铁矿 微生物作用下砷黄铁矿中砷的迁移转化 [70] -
[1] ROTHSCHILD L J, MANCINELLI R L. Life in extreme environments [J]. Nature, 2001, 409(6823): 1092-1101. doi: 10.1038/35059215 [2] DONG H L, HUANG L Q, ZHAO L D, et al. A critical review of mineral-microbe interaction and co-evolution: Mechanisms and applications[J]. National Science Review, 2022, [3] UROZ S, KELLY L C, TURPAULT M P, et al. The mineralosphere concept: Mineralogical control of the distribution and function of mineral-associated bacterial communities [J]. Trends in Microbiology, 2015, 23(12): 751-762. doi: 10.1016/j.tim.2015.10.004 [4] KLEBER M, BOURG I C, COWARD E K, et al. Dynamic interactions at the mineral–organic matter interface [J]. Nature Reviews Earth & Environment, 2021, 2(6): 402-421. [5] OELKERS E, GÍSLASON S, MATTER J. Mineral carbonation of CO2 [J]. Elements, 2008, 4: 333-337. doi: 10.2113/gselements.4.5.333 [6] LAMÉRAND C, SHIROKOVA L S, BÉNÉZETH P, et al. Olivine dissolution and hydrous Mg carbonate and silicate precipitation in the presence of microbial consortium of photo-autotrophic and heterotrophic bacteria [J]. Geochimica et Cosmochimica Acta, 2020, 268: 123-141. doi: 10.1016/j.gca.2019.09.040 [7] SALEK S S, KLEEREBEZEM R, JONKERS H M, et al. Mineral CO2 sequestration by environmental biotechnological processes [J]. Trends in Biotechnology, 2013, 31(3): 139-146. doi: 10.1016/j.tibtech.2013.01.005 [8] WANG Y, CAI Z L, ZHANG Y M, et al. Green recovery of vanadium from vanadium-bearing shale under the biological action by Bacillus mucilaginosus and its effect on mineral dissolution [J]. Journal of Environmental Chemical Engineering, 2022, 10(1): 107048. doi: 10.1016/j.jece.2021.107048 [9] FATHOLLAHZADEH H, HACKETT M J, KHALEQUE H N, et al. Better together: Potential of co-culture microorganisms to enhance bioleaching of rare earth elements from monazite [J]. Bioresource Technology Reports, 2018, 3: 109-118. doi: 10.1016/j.biteb.2018.07.003 [10] SUN Q B, FU Z Y, FINLAY R, et al. Transcriptome analysis provides novel insights into the capacity of the ectomycorrhizal fungus Amanita pantherina to weather K-containing feldspar and apatite [J]. Applied and Environmental Microbiology, 2019, 85(15): e00719-e00719. [11] LU A H, LI Y, JIN S, et al. Growth of non-phototrophic microorganisms using solar energy through mineral photocatalysis [J]. Nature Communications, 2012, 3: 768. doi: 10.1038/ncomms1768 [12] 鲁安怀, 李艳, 丁竑瑞, 等. 地表“矿物膜”: 地球“新圈层” [J]. 岩石学报, 2019, 35(1): 119-128. doi: 10.18654/1000-0569/2019.01.08 LU A H, LI Y, DING H R, et al. “Mineral membrane” of the surface: “New sphere” of the Earth [J]. Acta Petrologica Sinica, 2019, 35(1): 119-128(in Chinese). doi: 10.18654/1000-0569/2019.01.08
[13] 贾昊凝, 李艳, 黎晏彰, 等. 矿物电子能量协同微生物胞外电子传递与生长代谢 [J]. 微生物学报, 2020, 60(9): 2084-2105. doi: 10.13343/j.cnki.wsxb.20200314 JIA H N, LI Y, LI Y Z, et al. Mineral electronic energy cooperates with microbial extracellular electron transfer and growth metabolism [J]. Acta Microbiologica Sinica, 2020, 60(9): 2084-2105(in Chinese). doi: 10.13343/j.cnki.wsxb.20200314
[14] CHENG H, JING Z H, YANG L, et al. Sunlight-triggered synergy of hematite and Shewanella oneidensis MR-1 in Cr(Ⅵ) removal [J]. Geochimica et Cosmochimica Acta, 2021, 305: 19-32. doi: 10.1016/j.gca.2021.04.034 [15] GADD G M. Metals, minerals and microbes: Geomicrobiology and bioremediation[J]. Microbiology, 2010, 156(Pt 3): 609-643. [16] ZHANG L, GADD G M, LI Z. Microbial biomodification of clay minerals [J]. Advances in Applied Microbiology, 2021, 114: 111-139. [17] BISWAS B, CHAKRABORTY A, SARKAR B, et al. Structural changes in smectite due to interaction with a biosurfactant-producing bacterium Pseudoxanthomonas kaohsiungensis [J]. Applied Clay Science, 2017, 136: 51-57. doi: 10.1016/j.clay.2016.11.008 [18] BISWAS B, SARKAR B, RUSMIN R, et al. Bioremediation of PAHs and VOCs: Advances in clay mineral-microbial interaction [J]. Environment International, 2015, 85: 168-181. doi: 10.1016/j.envint.2015.09.017 [19] QU C C, DU H H, MA M K, et al. Pb sorption on montmorillonite-bacteria composites: A combination study by XAFS, ITC and SCM [J]. Chemosphere, 2018, 200: 427-436. doi: 10.1016/j.chemosphere.2018.02.136 [20] QU C C, CHEN W L, HU X P, et al. Heavy metal behaviour at mineral-organo interfaces: Mechanisms, modelling and influence factors [J]. Environment International, 2019, 131: 104995. doi: 10.1016/j.envint.2019.104995 [21] MA W T, PENG D H, WALKER S L, et al. Bacillus subtilis biofilm development in the presence of soil clay minerals and iron oxides [J]. NPJ Biofilms and Microbiomes, 2017, 3: 4. doi: 10.1038/s41522-017-0013-6 [22] XU S Z, XING Y H, LIU S, et al. Co-effect of minerals and Cd(Ⅱ) promoted the formation of bacterial biofilm and consequently enhanced the sorption of Cd(II) [J]. Environmental Pollution, 2020, 258: 113774. doi: 10.1016/j.envpol.2019.113774 [23] ZHANG L M, CHEN Y, XIA Q Y, et al. Combined effects of Fe(Ⅲ)-bearing clay minerals and organic ligands on U(Ⅵ) bioreduction and U(Ⅳ) speciation [J]. Environmental Science & Technology, 2021, 55(9): 5929-5938. [24] BISHOP M E, DONG H L, GLASSER P, et al. Reactivity of redox cycled Fe-bearing subsurface sediments towards hexavalent chromium reduction [J]. Geochimica et Cosmochimica Acta, 2019, 252: 88-106. doi: 10.1016/j.gca.2019.02.039 [25] OUYANG B J, LU X C, LIU H, et al. Reduction of jarosite by Shewanella oneidensis MR-1 and secondary mineralization [J]. Geochimica et Cosmochimica Acta, 2014, 124: 54-71. doi: 10.1016/j.gca.2013.09.020 [26] 陆现彩, 李娟, 刘欢, 等. 金属硫化物微生物氧化的机制和效应 [J]. 岩石学报, 2019, 35(1): 153-163. doi: 10.18654/1000-0569/2019.01.12 LU X C, LI J, LIU H, et al. Microbial oxidation of metal sulfides and its consequences [J]. Acta Petrologica Sinica, 2019, 35(1): 153-163(in Chinese). doi: 10.18654/1000-0569/2019.01.12
[27] DONG H, LU A. Mineral-microbe interactions and implications for remediation [J]. Elements, 2012, 8(2): 95-100. doi: 10.2113/gselements.8.2.95 [28] DONG H L. Mineral-microbe interactions: A review [J]. Frontiers of Earth Science in China, 2010, 4(2): 127-147. doi: 10.1007/s11707-010-0022-8 [29] BENNETT P C, ROGERS J R, CHOI W J, et al. Silicates, silicate weathering, and microbial ecology [J]. Geomicrobiology Journal, 2001, 18(1): 3-19. doi: 10.1080/01490450151079734 [30] COSTA O Y A, RAAIJMAKERS J M, KURAMAE E E. Microbial extracellular polymeric substances: Ecological function and impact on soil aggregation [J]. Frontiers in Microbiology, 2018, 9: 1636. doi: 10.3389/fmicb.2018.01636 [31] KLEBER M, EUSTERHUES K, KEILUWEIT M, et al. Mineral-organic associations: Formation, properties, and relevance in soil environments [J]. Advances in Agronomy, 2015, 130: 1-140. [32] SMALL T D, WARREN L A, RODEN E E, et al. Sorption of strontium by bacteria, Fe(Ⅲ) oxide, and Bacteria−Fe(Ⅲ) oxide composites [J]. Environmental Science & Technology, 1999, 33(24): 4465-4470. [33] DU H H, HUANG Q Y, PEACOCK C L, et al. Competitive binding of Cd, Ni and Cu on goethite organo-mineral composites made with soil bacteria [J]. Environmental Pollution, 2018, 243: 444-452. doi: 10.1016/j.envpol.2018.08.087 [34] ZHU Y, LI Y, LU A H, et al. Study of the interaction between bentonite and a strain of Bacillus mucilaginosus [J]. Clays and Clay Minerals, 2011, 59(5): 538-545. doi: 10.1346/CCMN.2011.0590511 [35] CAI P, LIN D, PEACOCK C L, et al. EPS adsorption to goethite: Molecular level adsorption mechanisms using 2D correlation spectroscopy [J]. Chemical Geology, 2018, 494: 127-135. doi: 10.1016/j.chemgeo.2018.07.028 [36] GADD G M. Geomicrobiology of the built environment [J]. Nature Microbiology, 2017, 2: 16275. doi: 10.1038/nmicrobiol.2016.275 [37] WANG H M, WU P X, LIU J, et al. The regulatory mechanism of Chryseobacterium sp. resistance mediated by montmorillonite upon cadmium stress [J]. Chemosphere, 2020, 240: 124851. doi: 10.1016/j.chemosphere.2019.124851 [38] RUAN B, WU P X, LIU J, et al. Adhesion of Sphingomonas sp. GY2B onto montmorillonite: A combination study by thermodynamics and the extended DLVO theory [J]. Colloids and Surfaces. B, Biointerfaces, 2020, 192: 111085. doi: 10.1016/j.colsurfb.2020.111085 [39] RUAN B, WU P X, WANG H M, et al. Effects of interaction between montmorillonite and Sphingomonas sp. GY2B on the physical and chemical properties of montmorillonite in the clay-modulated biodegradation of phenanthrene [J]. Environmental Chemistry, 2018, 15: 296-305. doi: 10.1071/EN18001 [40] POURJASEM L, LANDI A, ENAYATIZAMIR N, et al. The release of some elements from vermiculite during the short periods of incubation by heterotrophic bacteria [J]. Eurasian Soil Science, 2020, 53(2): 223-229. doi: 10.1134/S106422932002009X [41] LIN J Y, HU S W, LIU T X, et al. Coupled kinetics model for microbially mediated arsenic reduction and adsorption/desorption on iron oxides: Role of arsenic desorption induced by microbes [J]. Environmental Science & Technology, 2019, 53(15): 8892-8902. [42] YU G H, KUZYAKOV Y, LUO Y, et al. Molybdenum bioavailability and asymbiotic nitrogen fixation in soils are raised by iron (oxyhydr)oxide-mediated free radical production [J]. Environmental Science & Technology, 2021, 55(21): 14979-14989. [43] OYEWOLE O A, RAJI R O, MUSA I O, et al. Enhanced degradation of crude oil with Alcaligenes faecalis ADY25 and iron oxide nanoparticle [J]. International Journal of Applied Biological Research, 2019, 10(2): 62-72. [44] WANG Q, GAO S, MA X, et al. Distinct mineral weathering effectiveness and metabolic activity between mineral-weathering bacteria Burkholderia metallica F22 and Burkholderia phytofirmans G34 [J]. Chemical Geology, 2018, 489: 38-45. doi: 10.1016/j.chemgeo.2018.05.016 [45] CHEN W, LUO L, HE L Y, et al. Distinct mineral weathering behaviors of the novel mineral-weathering strains Rhizobium yantingense H66 and Rhizobium etli CFN42 [J]. Applied and Environmental Microbiology, 2016, 82(14): 4090-4099. doi: 10.1128/AEM.00918-16 [46] BAO Y Y, KWOK A H, HE L Y, et al. Complete genome sequence of Dyella jiangningensis strain SBZ3-12, isolated from the surfaces of weathered rock [J]. Genome Announcements, 2014, 2(3): e00416-e00414. [47] GRANT M R, TYMON L S, HELMS G L, et al. Biofilm adaptation to iron availability in the presence of biotite and consequences for chemical weathering [J]. Geobiology, 2016, 14(6): 588-598. doi: 10.1111/gbi.12187 [48] SAHA M, MAURYA B R, BAHADUR I, et al. Can potassium-solubilising bacteria mitigate the potassium problems in India?//Potassium solubilizing microorganisms for sustainable agriculture[M]. New Delhi: Springer, 2016: 127-136. [49] BALLAND-BOLOU-BI C, BOLOU-BI E B, VIGIER N, et al. Increased Mg release rates and related Mg isotopic signatures during bacteria-phlogopite interactions [J]. Chemical Geology, 2019, 506: 17-28. doi: 10.1016/j.chemgeo.2018.12.020 [50] RAJAWAT M V S, SINGH R, SINGH D, et al. Psychrotrophs of the genus Janthinobacterium with potential to weather potassium aluminosilicate mineral [J]. Biotech, 2019, 9(4): 142. doi: 10.1007/s13205-019-1672-1 [51] YANG S S, QU C C, MUKHERJEE M, et al. Soil phyllosilicate and iron oxide inhibit the quorum sensing of Chromobacterium violaceum [J]. Soil Ecology Letters, 2021, 3(1): 22-31. doi: 10.1007/s42832-020-0051-5 [52] GUO W W, MA H, LI F C, et al. Citrobacter sp. strain GW-M mediates the coexistence of carbonate minerals with various morphologies [J]. Geomicrobiology Journal, 2013, 30(8): 749-757. doi: 10.1080/01490451.2013.769650 [53] TONG H, ZHENG C J, LI B, et al. Microaerophilic oxidation of Fe(II) coupled with simultaneous carbon fixation and as(III) oxidation and sequestration in karstic paddy soil [J]. Environmental Science & Technology, 2021, 55(6): 3634-3644. [54] WANG S, WU Y, AN J K, et al. Geobacter autogenically secretes fulvic acid to facilitate the dissimilated iron reduction and vivianite recovery [J]. Environmental Science & Technology, 2020, 54(17): 10850-10858. [55] YI Q, WU S L, SOUTHAM G, et al. Acidophilic iron- and sulfur-oxidizing bacteria, Acidithiobacillus ferrooxidans, drives alkaline pH neutralization and mineral weathering in Fe ore tailings [J]. Environmental Science & Technology, 2021, 55(12): 8020-8034. [56] TIAN L, GUAN W Y, JI Y Y, et al. Microbial methylation potential of mercury sulfide particles dictated by surface structure [J]. Nature Geoscience, 2021, 14(6): 409-416. doi: 10.1038/s41561-021-00735-y [57] JONES L C, LAFFERTY B J, SPARKS D L. Additive and competitive effects of bacteria and Mn oxides on arsenite oxidation kinetics [J]. Environmental Science & Technology, 2012, 46(12): 6548-6555. [58] SUN W M, SUN X X, HÄGGBLOM M M, et al. Identification of antimonate reducing bacteria and their potential metabolic traits by the combination of stable isotope probing and metagenomic-pangenomic analysis [J]. Environmental Science & Technology, 2021, 55(20): 13902-13912. [59] SUN X X, QIU L, KOLTON M, et al. VⅤ reduction by Polaromonas spp. in vanadium mine tailings [J]. Environmental Science & Technology, 2020, 54(22): 14442-14454. [60] SUN X X, KONG T L, LI F B, et al. Desulfurivibrio spp. mediate sulfur-oxidation coupled to Sb(V) reduction, a novel biogeochemical process [J]. The ISME Journal, 2022, 16(6): 1547-1556. doi: 10.1038/s41396-022-01201-2 [61] SANYAL S K, SHUSTER J. Gold particle geomicrobiology: Using viable bacteria as a model for understanding microbe–mineral interactions [J]. Mineralogical Magazine, 2021, 85(1): 117-124. doi: 10.1180/mgm.2021.19 [62] REN G P, YAN Y C, NIE Y, et al. Natural extracellular electron transfer between semiconducting minerals and electroactive bacterial communities occurred on the rock varnish [J]. Frontiers in Microbiology, 2019, 10: 293. doi: 10.3389/fmicb.2019.00293 [63] YANG X X, LI Y, LU A H, et al. Effect of Bacillus mucilaginosus D4B1 on the structure and soil-conservation-related properties of montmorillonite [J]. Applied Clay Science, 2016, 119: 141-145. doi: 10.1016/j.clay.2015.08.033 [64] YAN S J, CAI Y G, LI H Q, et al. Enhancement of cadmium adsorption by EPS-montmorillonite composites [J]. Environmental Pollution, 2019, 252: 1509-1518. doi: 10.1016/j.envpol.2019.06.071 [65] ZHAO Y L, DONG F Q, DAI Q W, et al. Variation of preserving organic matter bound in interlayer of montmorillonite induced by microbial metabolic process [J]. Environmental Science and Pollution Research International, 2018, 25(23): 22348-22355. doi: 10.1007/s11356-017-9806-7 [66] REN X Y, LI F C, CAI Y F, et al. Paenibacillus sp. strain SB-6 induces weathering of Ca-montmorillonite: Illitization and formation of calcite [J]. Geomicrobiology Journal, 2017, 34(1): 1-10. doi: 10.1080/01490451.2015.1129472 [67] LIU D F, LIAN B, DONG H L. Isolation of Paenibacillus sp. and assessment of its potential for enhancing mineral weathering [J]. Geomicrobiology Journal, 2012, 29(5): 413-421. doi: 10.1080/01490451.2011.576602 [68] ZHOU Y F, WANG R C, LU X C. Anorthite dissolution promoted by bacterial adhesion: Direct evidence from dialytic experiment [J]. Science China Earth Sciences, 2011, 54(2): 204-211. doi: 10.1007/s11430-010-4068-y [69] SUN Y, WANG Y L, LI L, et al. Distinct biotite-weathering activities of Arthrobacter pascens F74 under different contact conditions [J]. Journal of Basic Microbiology, 2020, 60(4): 362-371. doi: 10.1002/jobm.201900518 [70] RATHOD J, JEAN J S, JIANG W T, et al. Micro-colonization of arsenic-resistant Staphylococcus sp. As-3 on arsenopyrite (FeAsS) drives arsenic mobilization under anoxic sub-surface mimicking conditions [J]. Science of the Total Environment, 2019, 669: 527-539. doi: 10.1016/j.scitotenv.2019.03.084 [71] WELCH S A, BARKER W W, BANFIELD J F. Microbial extracellular polysaccharides and plagioclase dissolution [J]. Geochimica et Cosmochimica Acta, 1999, 63(9): 1405-1419. doi: 10.1016/S0016-7037(99)00031-9 [72] DONG Y B, LIU Y, LIN H, et al. Improving vanadium extraction from stone coal via combination of blank roasting and bioleaching by ARTP-mutated Bacillus mucilaginosus [J]. Transactions of Nonferrous Metals Society of China, 2019, 29(4): 849-858. doi: 10.1016/S1003-6326(19)64995-2 [73] LI Q F, DONG F Q, DAI Q W, et al. Surface properties of PM2.5 calcite fine particulate matter in the presence of same size bacterial cells and exocellular polymeric substances (EPS) of Bacillus mucitaginosus [J]. Environmental Science and Pollution Research International, 2018, 25(23): 22429-22436. doi: 10.1007/s11356-017-0829-x [74] 王建萍, 李琼芳, 董发勤, 等. 3种常见细菌胞外特征有机酸对方解石的溶蚀研究 [J]. 岩石矿物学杂志, 2015, 34(3): 387-392. WANG J P, LI Q F, DONG F Q, et al. A study of the dissolution of calcite by three common bacterial typical extracellular organic acids [J]. Acta Petrologica et Mineralogica, 2015, 34(3): 387-392(in Chinese).
[75] EHRLICH H L. Geomicrobiology: relative roles of bacteria and fungi as geomicrobial agents//Fungi in Biogeochemical Cycles[M]. Cambridge: Cambridge University Press, 2006: 1-27. [76] 董子阳, 胡佳杰, 胡宝兰. 微生物铁载体转运调控机制及其在环境污染修复中的应用 [J]. 生物工程学报, 2019, 35(11): 2189-2200. DONG Z Y, HU J J, HU B L. Regulation of microbial siderophore transport and its application in environmental remediation [J]. Chinese Journal of Biotechnology, 2019, 35(11): 2189-2200(in Chinese).
[77] RIBEIRO I D A, VOLPIANO C G, VARGAS L K, et al. Use of mineral weathering bacteria to enhance nutrient availability in crops: A review [J]. Frontiers in Plant Science, 2020, 11: 590774. doi: 10.3389/fpls.2020.590774 [78] FLEMMING H C, WINGENDER J, SZEWZYK U, et al. Biofilms: an emergent form of bacterial life [J]. Nature Reviews Microbiology, 2016, 14(9): 563-575. doi: 10.1038/nrmicro.2016.94 [79] GLOWA K R, AROCENA J M, MASSICOTTE H B. Extraction of potassium and/or magnesium from selected soil minerals by Piloderma [J]. Geomicrobiology Journal, 2003, 20(2): 99-111. [80] TEITZEL G M, PARSEK M R. Heavy metal resistance of biofilm and planktonic Pseudomonas aeruginosa [J]. Applied and Environmental Microbiology, 2003, 69(4): 2313-2320. doi: 10.1128/AEM.69.4.2313-2320.2003 [81] JUCKER B A, HARMS H, HUG S J, et al. Adsorption of bacterial surface polysaccharides on mineral oxides is mediated by hydrogen bonds [J]. Colloids and Surfaces B:Biointerfaces, 1997, 9(6): 331-343. doi: 10.1016/S0927-7765(97)00038-6 [82] YU W H, LI N, TONG D S, et al. Adsorption of proteins and nucleic acids on clay minerals and their interactions: A review [J]. Applied Clay Science, 2013, 80/81: 443-452. doi: 10.1016/j.clay.2013.06.003 [83] ZHOU X Y, HUANG Q Y, CHEN S W, et al. Adsorption of the insecticidal protein of Bacillus thuringiensis on montmorillonite, kaolinite, silica, goethite and Red soil [J]. Applied Clay Science, 2005, 30(2): 87-93. doi: 10.1016/j.clay.2005.04.003 [84] CAO Y Y, WEI X, CAI P, et al. Preferential adsorption of extracellular polymeric substances from bacteria on clay minerals and iron oxide [J]. Colloids and Surfaces B:Biointerfaces, 2011, 83(1): 122-127. doi: 10.1016/j.colsurfb.2010.11.018 [85] WU Y C, CAI P, JING X X, et al. Soil biofilm formation enhances microbial community diversity and metabolic activity [J]. Environment International, 2019, 132: 105116. doi: 10.1016/j.envint.2019.105116 [86] 朱永官, 段桂兰, 陈保冬, 等. 土壤-微生物-植物系统中矿物风化与元素循环 [J]. 中国科学:地球科学, 2014, 44(6): 1107-1116. doi: 10.1360/zd-2014-44-6-1107 ZHU Y G, DUAN G L, CHEN B D, et al. Mineral weathering and element cycling in soil-microorganism-plant system [J]. Scientia Sinica (Terrae), 2014, 44(6): 1107-1116(in Chinese). doi: 10.1360/zd-2014-44-6-1107
[87] LOVLEY D R, COATES J D, BLUNT-HARRIS E L, et al. Humic substances as electron acceptors for microbial respiration [J]. Nature, 1996, 382(6590): 445-448. doi: 10.1038/382445a0 [88] ESTHER J, SUKLA L B, PRADHAN N, et al. Fe (Ⅲ) reduction strategies of dissimilatory iron reducing bacteria [J]. Korean Journal of Chemical Engineering, 2015, 32(1): 1-14. doi: 10.1007/s11814-014-0286-x [89] LIU T X, WANG Y, LIU C X, et al. Conduction band of hematite can mediate cytochrome reduction by Fe(Ⅱ) under dark and anoxic conditions [J]. Environmental Science & Technology, 2020, 54(8): 4810-4819. [90] SANTELLI C M, WEBB S M, DOHNALKOVA A C, et al. Diversity of Mn oxides produced by Mn(Ⅱ)-oxidizing fungi [J]. Geochimica et Cosmochimica Acta, 2011, 75(10): 2762-2776. doi: 10.1016/j.gca.2011.02.022 [91] SPIRO T G, BARGAR J R, SPOSITO G, et al. Bacteriogenic manganese oxides [J]. Accounts of Chemical Research, 2010, 43(1): 2-9. doi: 10.1021/ar800232a [92] WEI Z, HILLIER S, GADD G M. Biotransformation of manganese oxides by fungi: Solubilization and production of manganese oxalate biominerals [J]. Environmental Microbiology, 2012, 14(7): 1744-1753. doi: 10.1111/j.1462-2920.2012.02776.x [93] BURGHELEA C I, DONTSOVA K, ZAHARESCU D G, et al. Trace element mobilization during incipient bioweathering of four rock types [J]. Geochimica et Cosmochimica Acta, 2018, 234: 98-114. doi: 10.1016/j.gca.2018.05.011 [94] MENDES G O, BAHRI-ESFAHANI J, CSETENYI L, et al. Chemical and physical mechanisms of fungal bioweathering of rock phosphate [J]. Geomicrobiology Journal, 2021, 38(5): 384-394. doi: 10.1080/01490451.2020.1863525 [95] CHI Z L, YU G H, KAPPLER A, et al. Fungal-mineral interactions modulating intrinsic peroxidase-like activity of iron nanoparticles: Implications for the biogeochemical cycles of nutrient elements and attenuation of contaminants [J]. Environmental Science & Technology, 2022, 56(1): 672-680. [96] SUN Q B, LIAN B. The different roles of Aspergillus nidulans carbonic anhydrases in wollastonite weathering accompanied by carbonation [J]. Geochimica et Cosmochimica Acta, 2019, 244: 437-450. doi: 10.1016/j.gca.2018.10.022 [97] KRAUSE S, LIEBETRAU V, LÖSCHER C R, et al. Marine ammonification and carbonic anhydrase activity induce rapid calcium carbonate precipitation [J]. Geochimica et Cosmochimica Acta, 2018, 243: 116-132. doi: 10.1016/j.gca.2018.09.018 [98] POWER I M, HARRISON A L, DIPPLE G M. Accelerating mineral carbonation using carbonic anhydrase [J]. Environmental Science & Technology, 2016, 50(5): 2610-2618. [99] FOMINA M, SKOROCHOD I. Microbial interaction with clay minerals and its environmental and biotechnological implications [J]. Minerals, 2020, 10(10): 861. doi: 10.3390/min10100861 [100] SU M, HAN F Y, WU Y L, et al. Effects of phosphate-solubilizing bacteria on phosphorous release and sorption on montmorillonite [J]. Applied Clay Science, 2019, 181: 105227. doi: 10.1016/j.clay.2019.105227 [101] LI G L, ZHOU C H, FIORE S, et al. Interactions between microorganisms and clay minerals: New insights and broader applications [J]. Applied Clay Science, 2019, 177: 91-113. doi: 10.1016/j.clay.2019.04.025 [102] YUAN G D, THENG B K G, CHURCHMAN G J, et al. Clays and clay minerals for pollution control//Handbook of clay science [M]. Amsterdam: Elsevier, 2013: 587-644. [103] O'DAY P A, VLASSOPOULOS D. Mineral-based amendments for remediation [J]. Elements (Quebec, Quebec), 2010, 6(6): 375-381. doi: 10.2113/gselements.6.6.375 [104] CAO B, SHI L, BROWN R N, et al. Extracellular polymeric substances from Shewanella sp. HRCR-1 biofilms: Characterization by infrared spectroscopy and proteomics [J]. Environmental Microbiology, 2011, 13(4): 1018-1031. doi: 10.1111/j.1462-2920.2010.02407.x [105] LIN H R, WANG C Y, ZHAO H M, et al. A subcellular level study of copper speciation reveals the synergistic mechanism of microbial cells and EPS involved in copper binding in bacterial biofilms [J]. Environmental Pollution, 2020, 263: 114485. doi: 10.1016/j.envpol.2020.114485 [106] MISHRA J, SINGH R, ARORA N K. Alleviation of heavy metal stress in plants and remediation of soil by rhizosphere microorganisms [J]. Frontiers in Microbiology, 2017, 8: 1706. doi: 10.3389/fmicb.2017.01706 [107] CHEN R Q, TU H J, CHEN T T. Potential application of living microorganisms in the detoxification of heavy metals [J]. Foods (Basel, Switzerland), 2022, 11(13): 1905. [108] DHAMI N K, REDDY M S, MUKHERJEE A. Biomineralization of calcium carbonates and their engineered applications: A review [J]. Frontiers in Microbiology, 2013, 4: 314. [109] SINHA A, SINGH A, KUMAR S, et al. Microbial mineralization of struvite: A promising process to overcome phosphate sequestering crisis [J]. Water Research, 2014, 54: 33-43. doi: 10.1016/j.watres.2014.01.039 [110] TEBO B M, HE L M. Microbially mediated oxidative precipitation reactions //Mineral-water interfacial reactions [M]. Washington, DC: Americal Chemical Society. 1999: 393-414 [111] LI F, WANG W, LI C C, et al. Self-mediated pH changes in culture medium affecting biosorption and biomineralization of Cd2+ by Bacillus cereus Cd01 [J]. Journal of Hazardous Materials, 2018, 358: 178-186. doi: 10.1016/j.jhazmat.2018.06.066 [112] DU H H, CHEN W L, CAI P, et al. Cd(Ⅱ) sorption on montmorillonite-humic acid-bacteria composites [J]. Scientific Reports, 2016, 6: 19499. doi: 10.1038/srep19499 [113] TAN J Q, LI Y T, XIA L, et al. Enhancement of Cd(Ⅱ) adsorption on microalgae–montmorillonite composite [J]. Arabian Journal for Science and Engineering, 2022, 47(6): 6715-6727. doi: 10.1007/s13369-021-06063-y [114] ZENG Q, HUANG L Q, MA J Y, et al. Bio-reduction of ferrihydrite-montmorillonite-organic matter complexes: Effect of montmorillonite and fate of organic matter [J]. Geochimica et Cosmochimica Acta, 2020, 276: 327-344. doi: 10.1016/j.gca.2020.03.011 [115] HUANG Q Y, CHEN W L, XU L H. Adsorption of copper and cadmium by Cu- and Cd-resistant bacteria and their composites with soil colloids and kaolinite [J]. Geomicrobiology Journal, 2005, 22(5): 227-236. doi: 10.1080/01490450590947779 [116] ZHOU Q X, LIU Y X, LI T, et al. Cadmium adsorption to clay-microbe aggregates: Implications for marine heavy metals cycling [J]. Geochimica et Cosmochimica Acta, 2020, 290: 124-136. doi: 10.1016/j.gca.2020.09.002 [117] WEI T, LIU X, DONG M F, et al. Rhizosphere iron and manganese-oxidizing bacteria stimulate root iron plaque formation and regulate Cd uptake of rice plants (Oryza sativa L. ) [J]. Journal of Environmental Management, 2021, 278: 111533. doi: 10.1016/j.jenvman.2020.111533 [118] COOPER R, EUSTERHUES K, WEGNER C E, et al. Ferrihydrite associated organic matter (OM) stimulates reduction by Shewanella oneidensis MR-1 and a complex microbial consortia [J]. Biogeosciences Discussions, 2017, 14(22): 1-32. [119] WANG Y, LIU X H, SI Y B, et al. Release and transformation of arsenic from As-bearing iron minerals by Fe-reducing bacteria [J]. Chemical Engineering Journal, 2016, 295: 29-38. doi: 10.1016/j.cej.2016.03.027 [120] MOHAMED A, YU L, FANG Y, et al. Iron mineral-humic acid complex enhanced Cr(Ⅵ) reduction by Shewanella oneidensis MR-1 [J]. Chemosphere, 2020, 247: 125902. doi: 10.1016/j.chemosphere.2020.125902 [121] ZHANG K, LI N, LIAO P, et al. Conductive property of secondary minerals triggered Cr(Ⅵ) bioreduction by dissimilatory iron reducing bacteria [J]. Environmental Pollution, 2021, 286: 117227. doi: 10.1016/j.envpol.2021.117227 -





 下载:
下载: