-
草甘膦是一种非选择性的广谱除草剂,因其具有与土壤快速结合、不挥发、不易光解等特性[1],在全世界范围内被广泛应用。有研究[2-3]表明:每生产1 t草甘膦原药,要至少排放4倍的高浓度废水,其中的草甘膦含量约为0.9%,该废水可生化性差、治理难度大。当农田施加草甘膦以后,其通过介质迁移而进入到水体中。张石云等[4]在哈尼梯田采集水源水库及梯田汇水处水样,草甘膦检出率为100%;王静等[5]和陈界江等[6]分别在浙江省饮用水源、太湖及阳澄湖水源地水样中检测到少量草甘膦。MESNAGE等[7]的研究表明,即使浓度低于监管限值,商业制剂中的草甘膦也会对肝肾有致癌、致畸和致瘤作用。鉴于草甘膦在饮用水源地的高检出和潜在毒理效应,《生活饮用水卫生标准》(GB 5749-2006)中规定草甘膦浓度限值为0.7 mg L−1。因此,草甘膦的去除也成为近年的水处理领域的热点问题[1, 8]。
在草甘膦的去除技术中,吸附法[9-10]被证明是一种高效廉价的技术。草甘膦作为阴离子型有机磷化合物,带有正电荷的吸附材料可以通过静电吸附作用实现对其的高效吸附。2016年以来,DONG等[11]制备了以季铵基团(-N+(CH3)3)为核心的高正电荷水凝胶吸附剂:MGO-CH[12]、MCH-La[13]和载有La3+(ion)/La(OH)3-W/La(OH)3-EW的MCH,其与AR88、F−和
PO3−4 之间存在显著的静电吸附作用,但目前尚未使用此类水凝胶吸附剂对草甘膦进行吸附研究。近年来,环糊精作为聚合物的单体而受到关注[14-17],环糊精具有疏水性内腔和亲水性外表面的特定截锥形结构,可用于与各种具有适当大小和极性的分子相互作用形成可逆的主-客体包含物[15]。同时,环糊精内部和外部的高密度羟基可以通过各种官能团进行修饰,使环糊精具有额外的特殊性能[18]。以β-环糊精为单体制备的新型环糊精基聚合物(EA-CDP)[16]和两亲性高交联多孔环糊精聚合物(PBCD-B-D)[17]在有机污染物的吸附中发挥了环糊精包合作用及疏水性和氢键等其他作用,取得了良好的吸附效果,然而其对草甘膦的吸附性能尚需验证。
基于上述研究,本研究以阳离子化的β-环糊精为单体,通过自由基接枝共聚,制备了环氧丙基三甲基氯化铵-β-环糊精复合水凝胶(MGTA-CDCH),耦合季胺基团的正电荷特征与β-环糊精的氢键专属吸附作用,进行了草甘膦的吸附研究;通过静态吸附实验,评价了MGTA-CDCH对草甘膦的吸附效果、探讨其吸附特征,并分析相应的吸附机制,以期为草甘膦的高效去除提供技术支撑。
全文HTML
-
β-环糊精、2, 3-环氧丙基三甲基氯化铵(GTA)、氢氧化钠、过硫酸钾、磷酸二氢钾、氯化钠、无水乙醇、腐殖酸和纳米Fe3O4均为分析纯,购于国药基团化学试剂有限公司;另外,N, N'-亚甲基双丙烯酰胺(MBA)、N, N, N', N'-四甲基乙二胺(TEMED)及草甘膦试剂均购于上海麦克林生化科技有限公司,且均为分析纯试剂。甲醇为色谱纯,购于上海阿拉丁生化科技股份有限公司。高效液相色谱测试实验用水为超纯水。相关试剂的主要结构参数见表1。
草甘膦废水的配置。称取0.2 g草甘膦试剂置于烧杯中加入去离子水溶解后,将其定容到1 L容量瓶中,制备成浓度为200 mg·L−1的草甘膦标准溶液。在后续吸附实验中,从标准液中移取相应体积的溶液稀释至定容刻度,即可得到相应浓度的草甘膦溶液。
-
磁性阳离子环糊精基复合水凝胶(MGTA-CDCH)的制备。称取2.5 g的β-环糊精于质量分数为40%的NaOH溶液中,再加入3.5 g GTA、2 mL无水乙醇和5 mL去离子水,在70 ℃下反应4 h,将pH调至7后,真空干燥24 h至恒重,获得阳离子化环糊精(GTA-CD)。准确称取5 g GTA-CD,向其中加入0.05 g交联剂MBA。待交联剂MBA全部溶解后(搅拌均匀后),加入加速剂0.02 mL TEMED和0.2 g纳米Fe3O4。当以上物质混合均匀后,加0.6 mL饱和过硫酸钾(KPS)溶液作为引发剂。在60 ℃水浴中搅拌反应15 min。将生成的MGTA-CDCH转移到玻璃瓶中,浸没在纯水里,每8 h换一次水,然后将磁性水凝胶冷冻干燥,磨成颗粒备用。
在进行吸附动力学实验时,取1 000 mL浓度为20 mg·L−1的草甘膦水样,采用0.1 mol·L−1的HCl或NaOH溶液调节水样pH后,按投加量加入0.2 g·L−1的MGTA-CDCH。在恒温((25±1) ℃)振荡箱中,在pH=7.0±0.2和转速为150 r·min−1的条件下振荡。在不同反应时间点取样,经0.45 μm膜过滤,所得样品存放于(4±0.5) ℃冰箱内备用。此外,所使用的进行动力学模拟的模型方程[12]如式(1)~式(3)所示。准一级动力学模型见式(1),准二级动力学模型见式(2),Weber-Morris方程见式(3)。
式中:qe和qt分别为草甘膦的平衡吸附量和t时刻的吸附量,mg·g−1;k1为准一级动力学模型的平衡常数,h−1;k2为准二级动力学模型的平衡常数,g∙(mg·h)−1;kp为Weber-Morris方程的平衡常数,h−1。
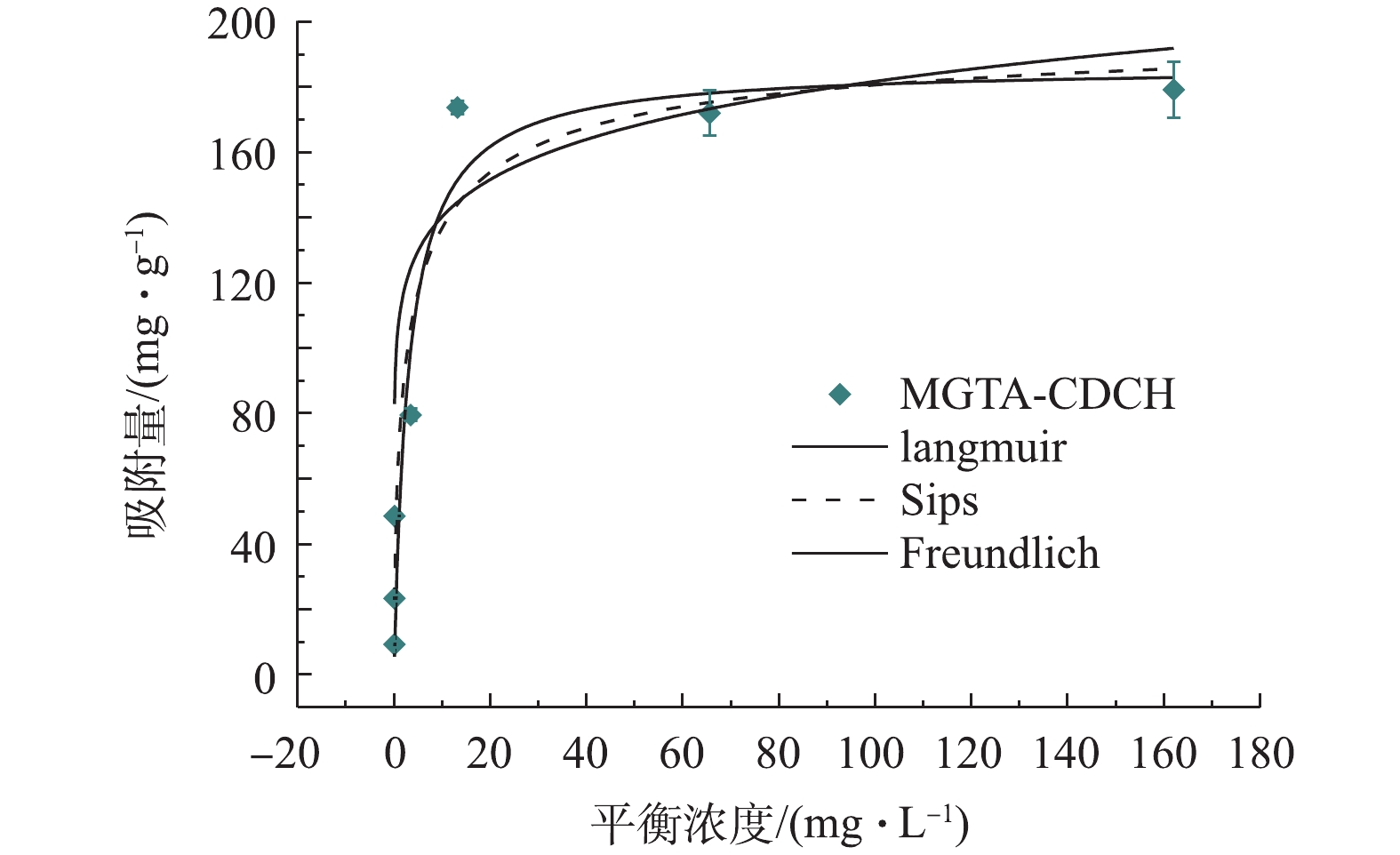
在进行吸附等温线实验时,取一系列不同浓度的草甘膦水样,向其中分别加入0.2 g·L−1 MGTA-CDCH,其余测定条件同上。此外,进行等温线拟合的模型方程[12]如式(4)~式(6)所示。Langmuir方程见式(4),Freundlich方程见式(5),Sips方程见式(6)。
式中:qe和qm分别为吸附平衡时草甘膦的吸附量和最大吸附量,mg·g−1;kL、kF和ks分别为Langmuir、Freundlich和Sips模型常数;Ce为平衡浓度,mg·L−1;RL为Langmuir模型中的分离系数;n为Freundlich吸附指数;αs为平衡常数;βs为吸附平衡分解常数。
pH、共存有机物对吸附量的影响实验。取一系列20 mg·L−1的草甘膦水样加入0.2 g·L−1 MGTA-CDCH,使用0.1 mol·L−1的HCl或NaOH溶液调节初始pH,共存有机物浓度为0~200 mg·L−1,待吸附平衡后,取样测定不同条件下草甘膦的吸附量。
在进行吸附再生实验时,吸附实验方法同上,在吸附结束后,在磁场下进行固液分离,直接在固体样品中加入配制好的脱附液进行脱附,在一定时间后,同样固液分离并进行下一次的吸附实验,一共重复5次。脱附率按脱附量与吸附量的比值进行计算。
-
为表征样品表面形貌,采用蔡司Merlin扫描电子显微镜(SEM)对样品进行观察分析。为了解样品的相关物理化学性质如荷电特性、比表面积和孔径分布、磁强度特征等性质,其中,Zeta电位测试测定使用Zetasizer Nano Z分析仪(英国马尔文)测量吸附剂的表面电荷;BET比表面积使用美国麦克公司ASAP-2460全自动比表面积与孔隙度仪分析测定。
草甘膦浓度的测定使用高效液相色谱法测定(GB/T 20684-2017),以pH=1.9的磷酸二氢钾水溶液和甲醇为流动相,使用色谱柱Agilent ZORBAX Eclipse Plus C18 (150 mm×2.1 mm,2.6 μm),紫外检测器波长195 nm,对样品中草甘膦进行高效液相色谱的分离与测定。流速0.8 mL·min−1,柱温为室温,进样体积20 μL。
1.1. 试剂
1.2. 实验方法
1.3. 分析测试方法
-
图1为MGTA-CDCH的SEM图。由图1可知,在MGTA-CDCH表面有明显的褶皱和不同的球状聚集体,球形直径分布在10~50 nm。
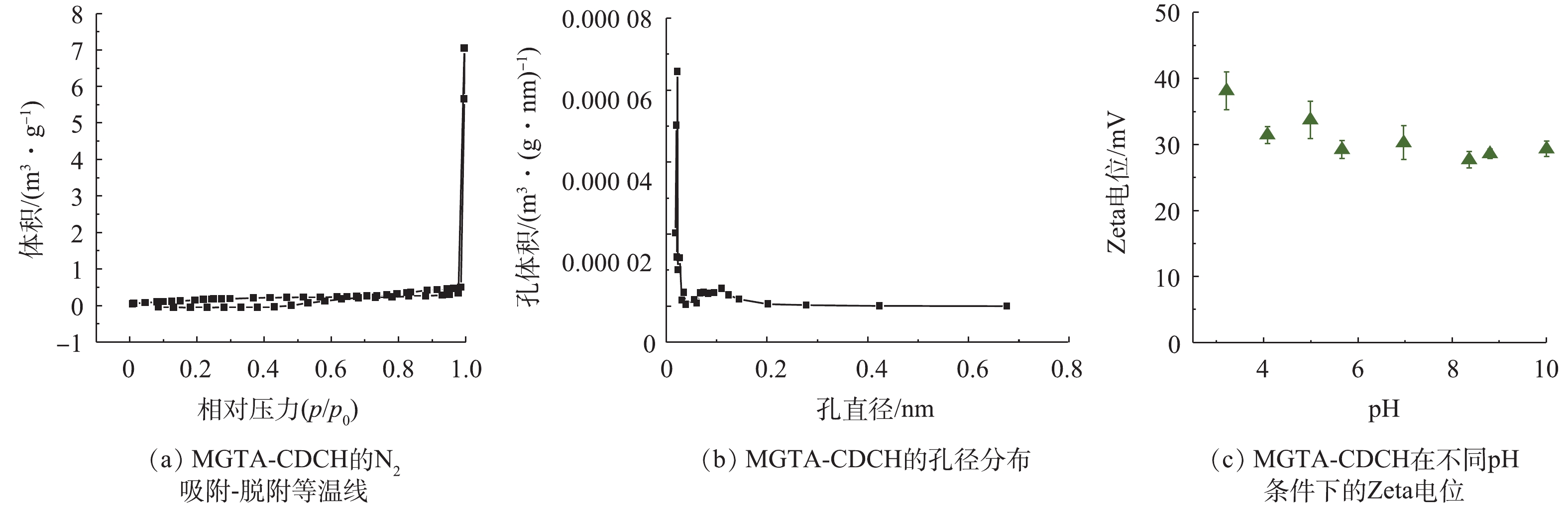
图2为MGTA-CDCH的N2吸附-脱附等温线、孔径分布及其在不同pH条件下Zeta电位的变化情况。如图2(a)所示,MGTA-CDCH的吸附等温线为Ⅰ型[19],这说明材料中存在大量微孔,这类等温线在接近饱和蒸汽压时,由于微粒之间存在缝隙,会发生类似于大孔的吸附,等温线会迅速上升。MGTA-CDCH的比表面积和平均孔径(图2(b))分别为0.67 m2·g−1和0.52 nm。传统水凝胶常具有较小(0.47~4.46 m2·g−1)的比表面积[11, 20],结合扫描电镜图与BET所得参数可知,MGTA-CHCH脱水所得的颗粒间发生团聚,粒径较大,比表面积和孔体积相对较小。此外,MGTA-CDCH的平均孔径(0.52 nm)小于β-环糊精的空腔尺寸(0.65 nm),有研究[21]表明,β-环糊精在强碱条件下易形成6号位羟基取代物,此时仅有2、3号位羟基可形成分子内氢键,这可能导致β-环糊精本身的空腔结构缩小,同时,在凝胶的合成过程中,可能在环糊精空腔内部发生了聚合而导致孔径降低。
Zeta电位是影响吸附剂与吸附质之间静电作用的关键影响因素。实验测定了pH为3~10.5下MGTA-CDCH的Zeta电位,结果如图2(c)所示。MGTA-CDCH的Zeta电位在整个测试区间内均保持在27 mV以上,其主要原因是,MGTA-CDCH表面的季胺基团使吸附剂具有较高的表面正电荷[11]。当pH为3.0~4.0时,MGTA-CDCH的Zeta电位从38.1 mV降低至30.3 mV;当pH为4.0~7.0时,MGTA-CDCH的Zeta电位基本稳定在30.3 mV左右;当pH在7.0~8.3时,MGTA-CDCH的Zeta电位缓慢下降至28.0 mV左右,并在此后随pH的升高,Zeta电位保持稳定。MGTA-CDCH中的环糊精中含有羟基基团,在强酸性条件下其会发生质子化,从而增强MGTA-CDCH的正电性;随着pH的升高,在弱酸和中性条件下羟基质子化程度有所减弱、在碱性条件下发生氢离子离解,产生氧负离子,从而在一定程度上降低了MGTA-CDCH的正电性。在碱性条件下,OH−对MGTA-CDCH表面正电荷的屏蔽作用似乎并不明显。
-
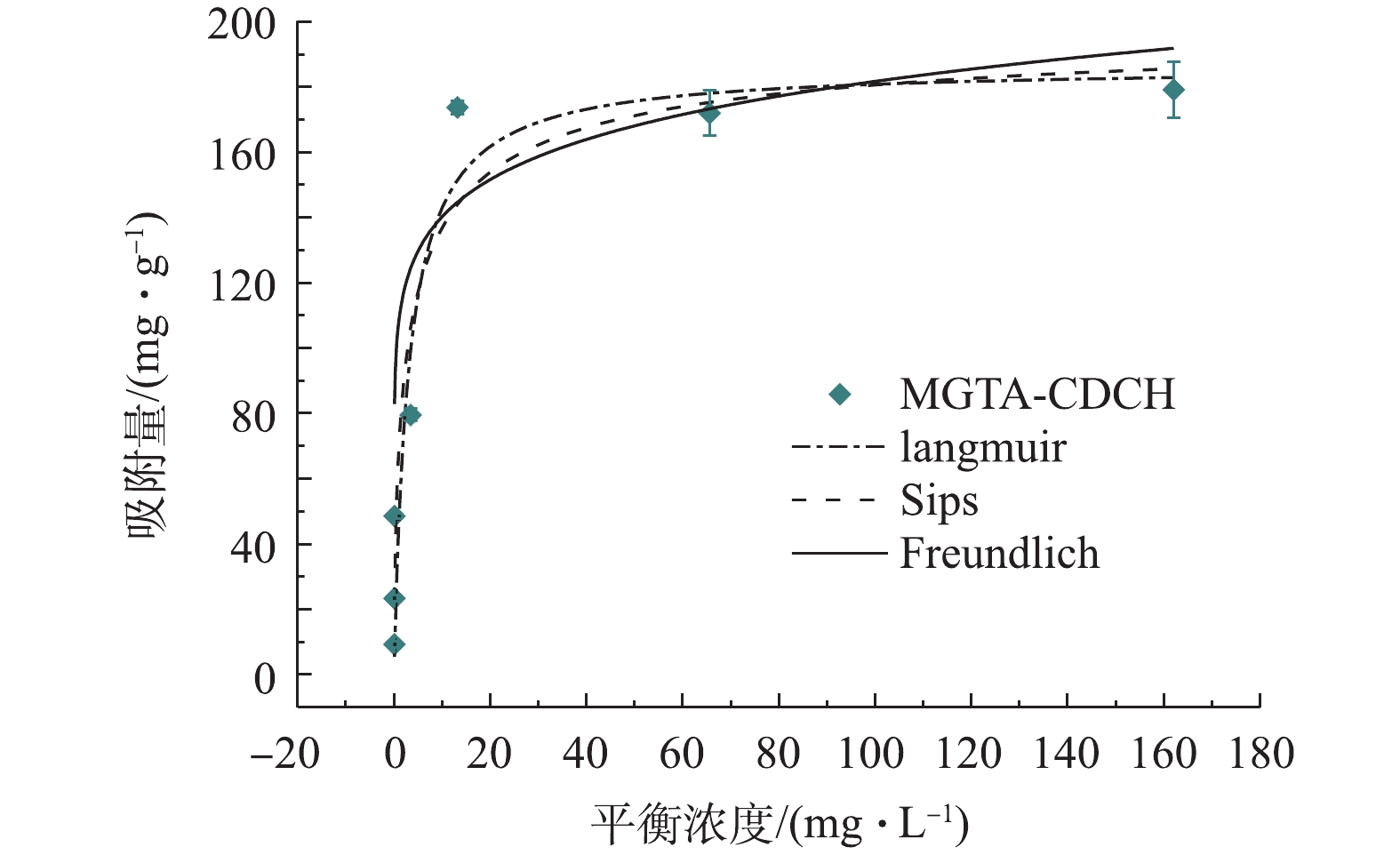
图3显示了草甘膦的初始浓度为0~200 mg·L−1时,MGTA-CDCH对草甘膦的吸附等温线。由图3可知,吸附量随草甘膦平衡浓度从0~15 mg·L−1的增加而急剧增加。在草甘膦平衡浓度为13.1 mg·L−1时,MGTA-CDCH的吸附容量接近179.2 mg·g−1的稳定值,如表2所示,与相关研究[8-9, 22, 27]报道的吸附剂相比,MGTA-CDCH对草甘膦的吸附能力最高。MGTA-CDCH对草甘膦废水的吸附等温线由Langmuir、Freundlich和Sips模型拟合,相应的拟合结果见表3。Sips模型具有最高的拟合系数(R2=0.927),拟合效果最好。这些结果证明,草甘膦在MGTA-CDCH上的吸附可以同时用单层和多层协同吸附模型来描述[28]。
-
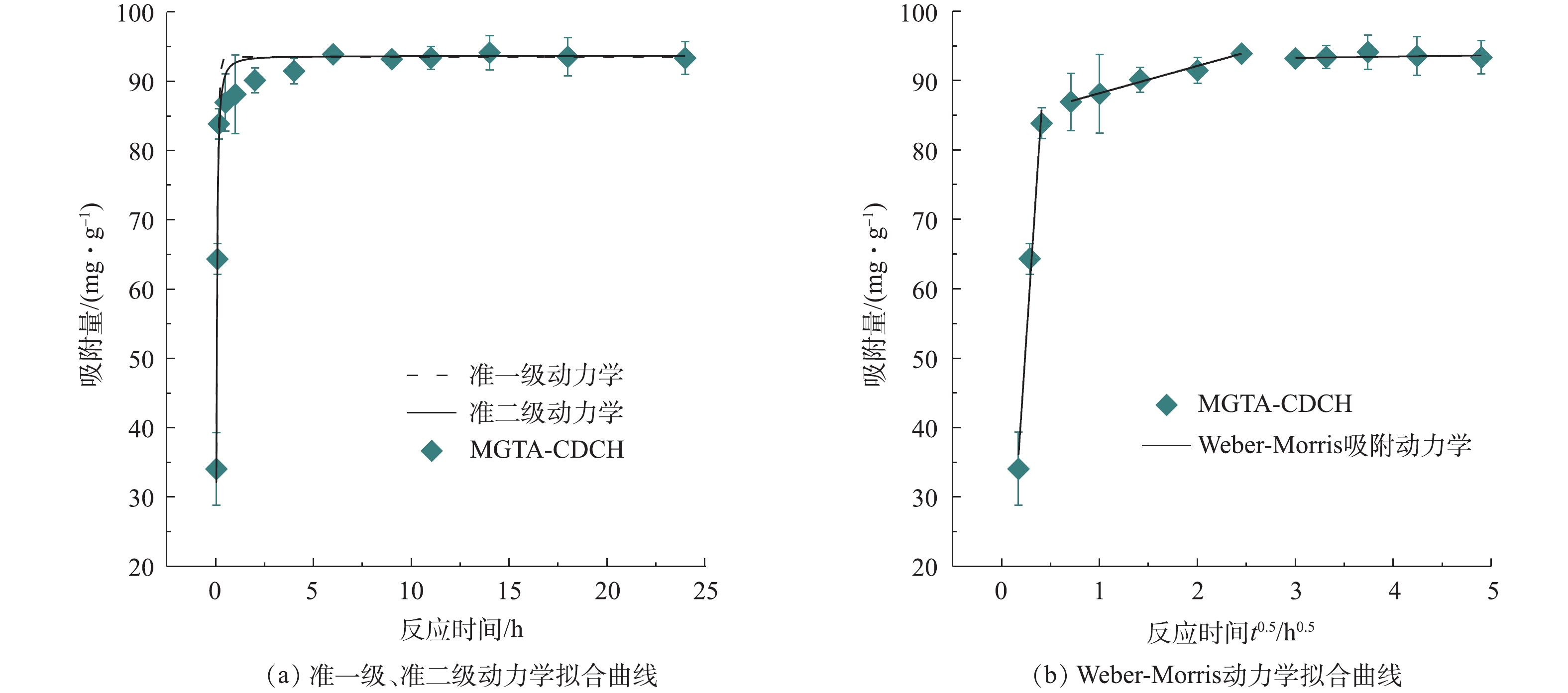
图4为初始浓度为20 mg·L−1草甘膦在MGTA-CDCH上的吸附动力学拟合结果。如图4(a)所示,吸附容量在1 h内迅速增加,达到最大吸附容量的96.6%。拟一级动力学模型(R2=0.970)和拟二级动力学模型(R2=0.973)均能描述草甘膦在MGTA-CDCH上的吸附过程,且计算得到的平衡吸附量(93.53 mg·g−1和93.65 mg·g−1)与实验测得的平衡吸附量(94.10 mg·g−1)接近,这表明MGTA-CDCH吸附草甘膦吸附过程主要以物理吸附作用和化合键力的化学吸附作用为主导[12, 29]。Weber-Morris吸附动力学模型的拟合结果如图4(b)所示,存在3个线性区域,斜率分别为211.39、3.93和0.17,这意味着在上述吸附过程中发生了3个连续的传质速率控制步骤:液膜或外部扩散、颗粒内或内部扩散,以及进入内表面活性中心的过程[27]。由图4(b)可知,第1个线性部分具有最陡的斜率,对应于初始快速动力学特征。在这个扩散阶段,草甘膦从溶液迁移到MGTA-CDCH粒子周围的边界层,或穿过边界层迁移到MGTA-CDCH的外表面与其外表面结合。第2直线段坡度较低,草甘膦连续从外表面迁移到内表面[28, 30],由于MGTA-CDCH的孔容孔径较小,导致颗粒内或内部扩散受到限制。第3个线性部分是最后阶段,草甘膦进入MGTA-CDCH内表面的活性位点,完成吸附。在这一阶段,缓慢的吸附动力学是由速率限制的扩散传质引起的。如图4(b)所示,该曲线未穿过原点,这意味着边界层扩散和粒子内扩散对速率控制均有贡献[29]。
-
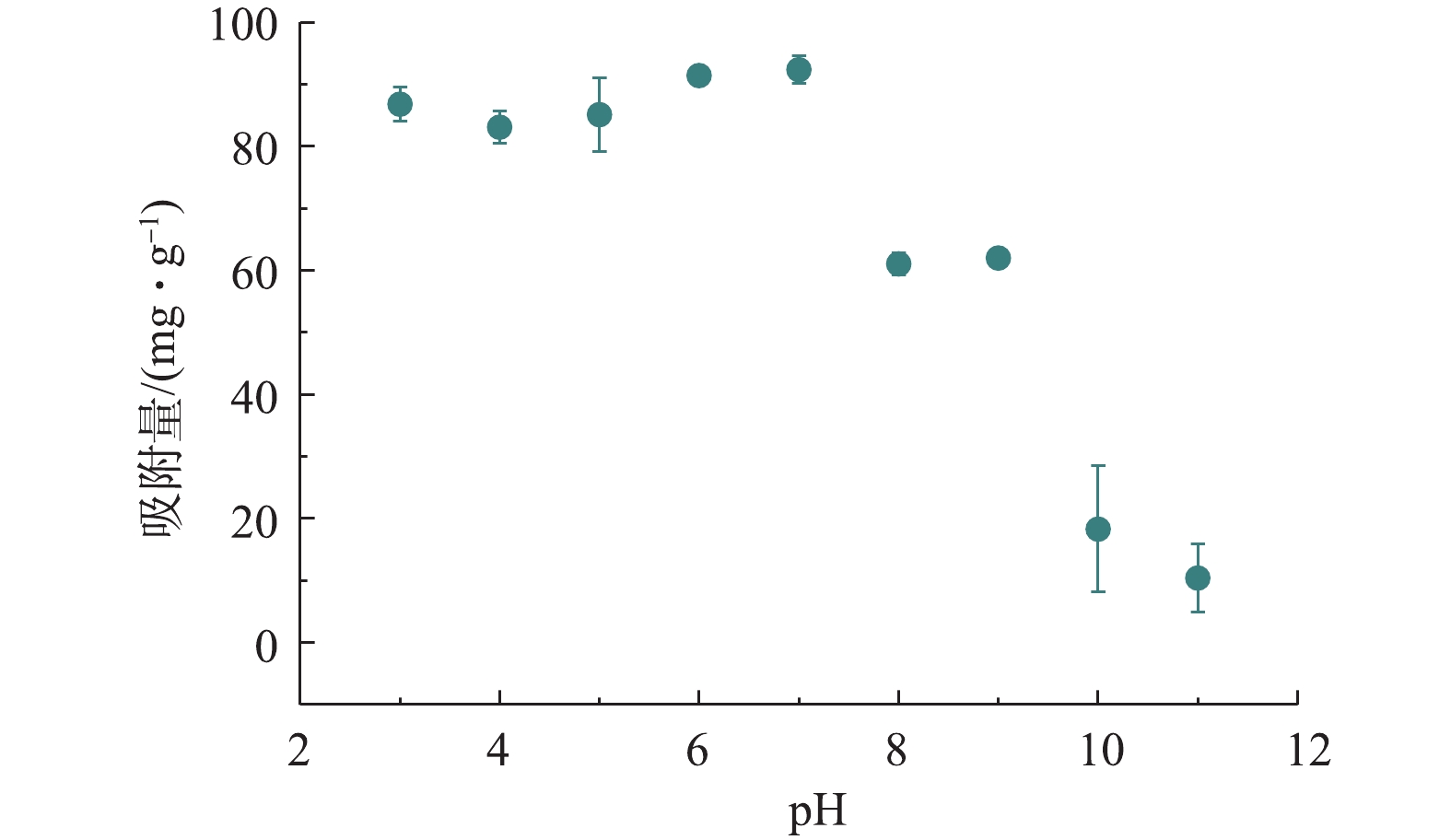
MGTA-CDCH对草甘膦的吸附量随pH的变化情况如图5所示。当pH为3.0~5.0时,MGTA-CDCH对草甘膦的吸附量保持在85.1 mg·g−1;当pH为5.0~7.0时,草甘膦的吸附量略有增加,达到最大值(92.3 mg·g−1);当pH≥8时,吸附量逐渐下降到61.1 mg·g−1;当pH≥10时,吸附量急剧下降。
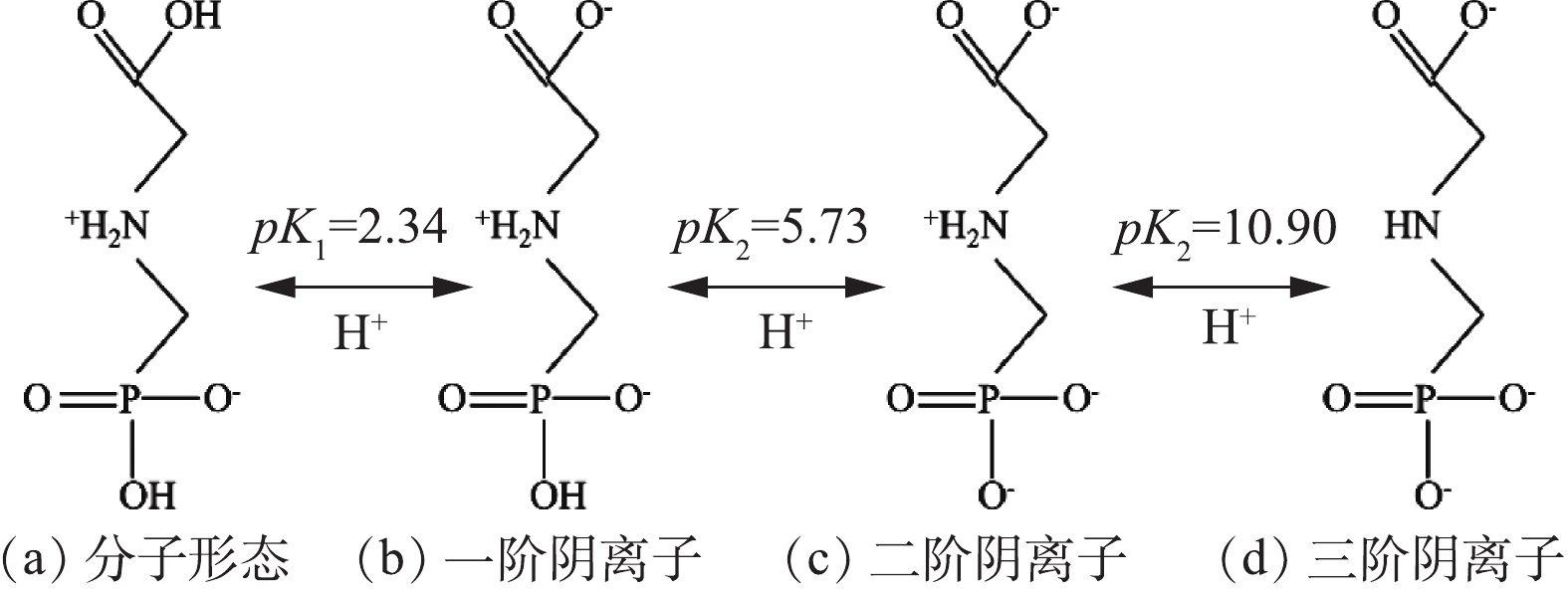
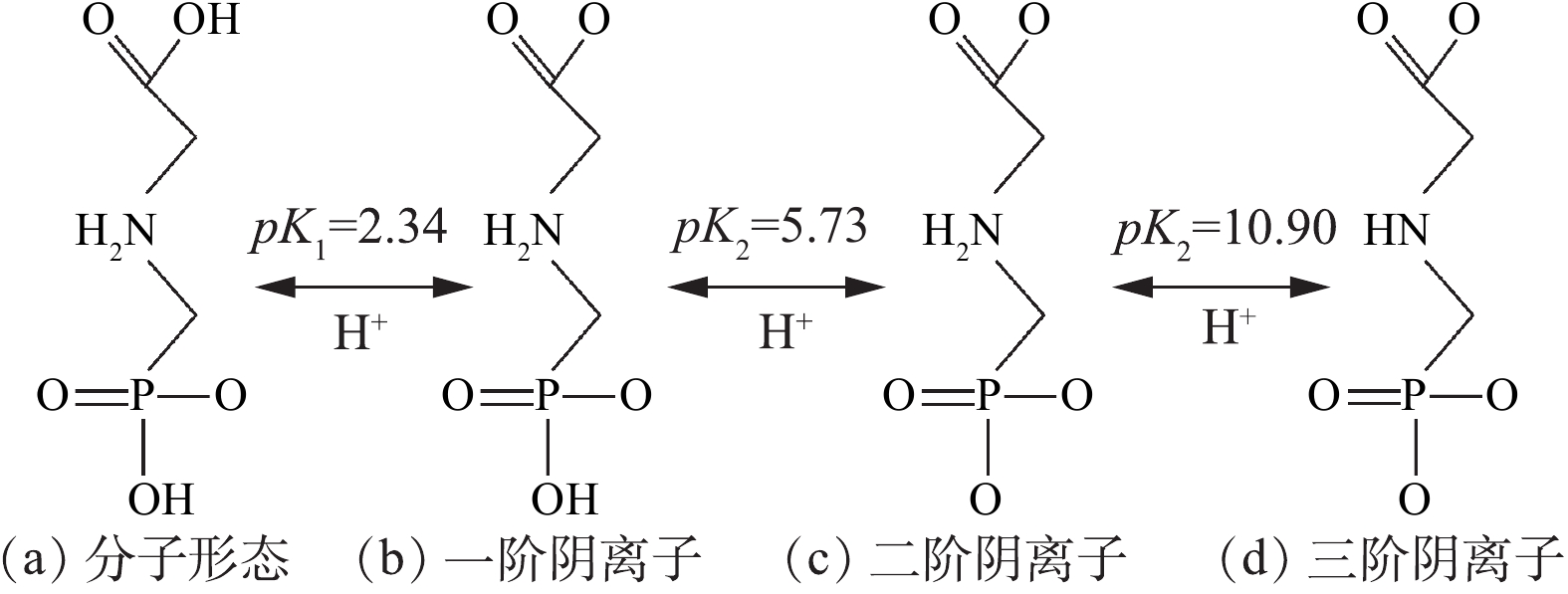
图6为草甘膦的酸解离方程式[31],有3个氢离子在不同pH下可以发生相应的离解;因此,溶液pH的变化会对MGTA-CDCH表面电荷(图2(b))和草甘膦解离形态造成影响,从而导致MGTA-CDCH对草甘膦吸附性能的差异。当pH<pK1=2.20时,草甘膦以分子形态所示,磷酸根上羟基氢离子的离解而带上了1个负电荷,
NH+2 基团带有1个正电荷,分子形态中净的电荷为零;当pH为3.0~4.1时,草甘膦以一阶阴离子为主,而且其比例越来越多,该形态为草甘膦分子上的羧酸基团上羟基氢离子的离解而带上了1个净的负电荷,但此时MGTA-CDCH表面正电荷的下降程度相对较大,导致其与草甘膦一阶阴离子之间的静电吸引力下降,从而降低了吸附量;当pH=4.1~7.0时,MGTA-CDCH表面正电荷基本保持稳定,草甘膦一阶阴离子由100%的比例(pH=(pK1+ pK2)/2=4.03)开始逐渐降低,而其二阶阴离子的比例逐渐升高,其中二阶阴离子为一阶阴离子进一步发生磷酸根上羟基氢离子的离解而带上了2个净的负电荷,因此,MGTA-CDCH与草甘膦之间的静电作用逐渐增强;此外,随着pH向中性变化,MGTA-CDCH与草甘膦之间的氢键数量会增加;这些均导致草甘膦在MGTA-CDCH上的吸附量在该pH范围内逐渐上升。当pH继续上升至碱性条件时,草甘膦二阶阴离子的比例上升至100%(pH=(pK2+ pK3)/2=8.31)后再下降,草甘膦三阶阴离子的比例逐渐上升,其中三阶阴离子为二阶阴离子进一步发生NH+2 基团上氢离子的离解而带上了3个净的负电荷;MGTA-CDCH的正电荷在该范围内发生了一定程度的降低;因此,MGTA-CDCH与草甘膦二阶阴离子之间的静电吸引力下降;随着pH向碱性变化,MGTA-CDCH与草甘膦二阶阴离子和三阶阴离子之间的氢键数量也减少了;这些变化均导致草甘膦在MGTA-CDCH上的吸附量大幅度下降[15, 32]。 -
HA实验浓度为0~200 mg·L−1,实验结果如图7所示。HA对草甘膦的吸附存在负面影响,但随着HA浓度的升高,吸附量逐渐回升,MGTA-CDCH对草甘膦的吸附量仍然能保持在118 mg·g−1以上。HA相比于草甘膦具有更多的苯基和含氧基团,并且其尺寸较大,因此,在低浓度的情况下,HA的部分结构能够被环糊精的疏水空腔包络[29]。此时腐殖酸分子为长链结构,优先接触MGTA-CDCH的活性位点,草甘膦和HA发生竞争吸附,导致吸附量的下降。随着HA浓度的逐渐升高,HA分子链呈团缩状,使分子链中的羧基等官能团被屏蔽而导致反应活性降低,削减其在MGTA-CDCH上的吸附作用[33]。同时,溶液中HA的剩余浓度增加,HA含有的羟基、羧基及疏水官能团会与草甘膦通过氢键、范德华力相互作用[34]。因此,草甘膦与HA单独形成新的复合物导致草甘膦剩余浓度下降,表现为吸附量回升。
-
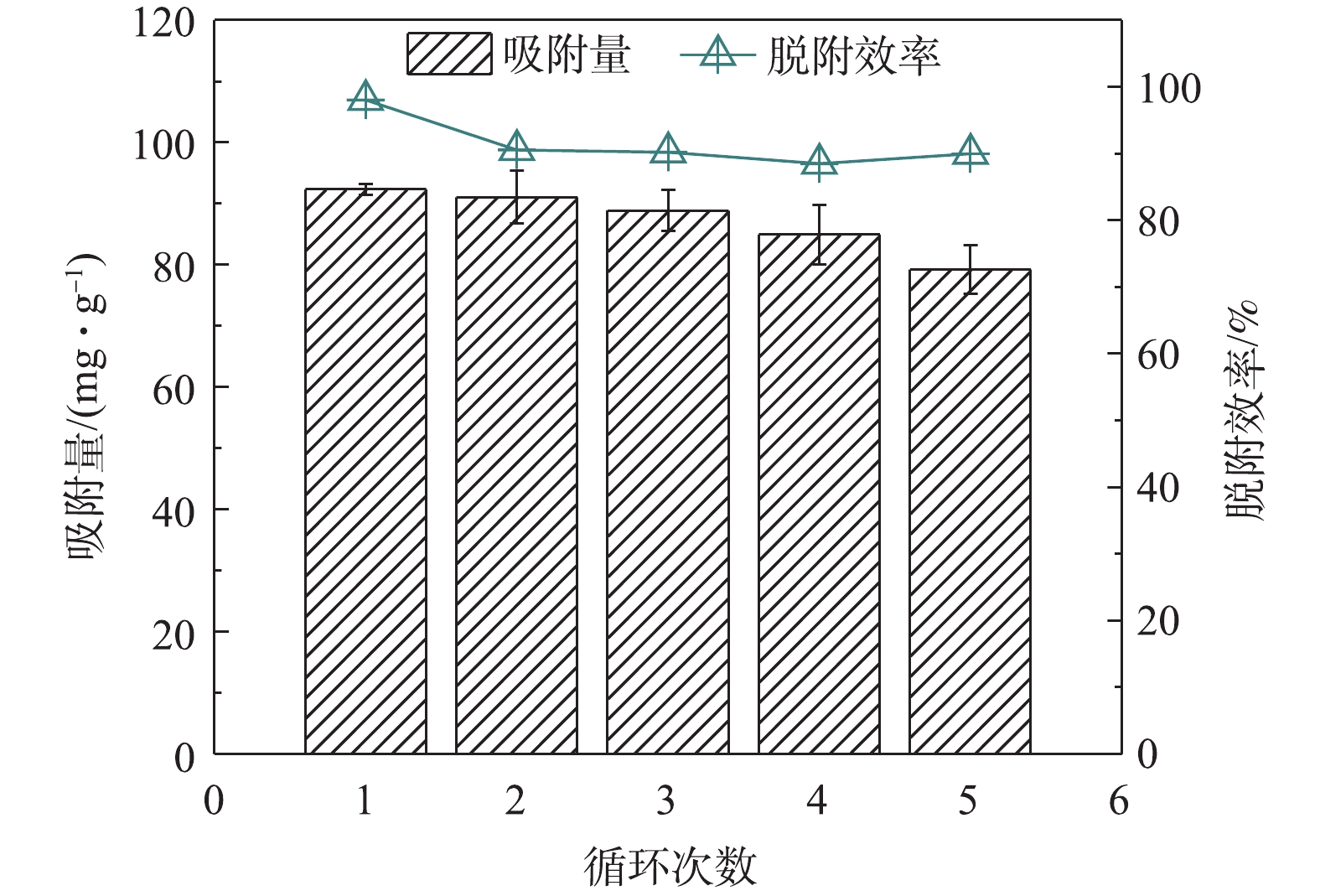
本研究采用0.5 mol·L−1 NaCl、1 mol·L−1 NaOH和无水乙醇混合溶液作为脱附剂,并对MGTA-CDCH进行5次吸脱附再生回用实验,结果如图8所示。在20 mg·L−1草甘膦初始浓度下,经过5个吸附-解吸循环后,再生后保持新鲜MGTA-CDCH的85.8%吸附能力。在前2次循环中,被吸附的草甘膦仅占据表面活性吸附位点,该位点很容易被NaCl-NaOH-乙醇解吸;随着循环使用次数增加,部分草甘膦以静电吸引和氢键的双重作用而与固体表面紧密结合,同时内部扩散阻力也可以抑制NaCl-NaOH-乙醇的解吸作用,导致吸附量下降,但吸附量的损失率不到初始饱和吸附量的15%。
-
本研究中所用实际水样取自北京市地表水,水样经0.45 μm滤膜过滤后进行测定,相应的草甘膦浓度由后续实验室添加获得,具体的水质参数为1.93 mg·L−1草甘膦、pH=7.12、9.03 mg·L−1 COD、
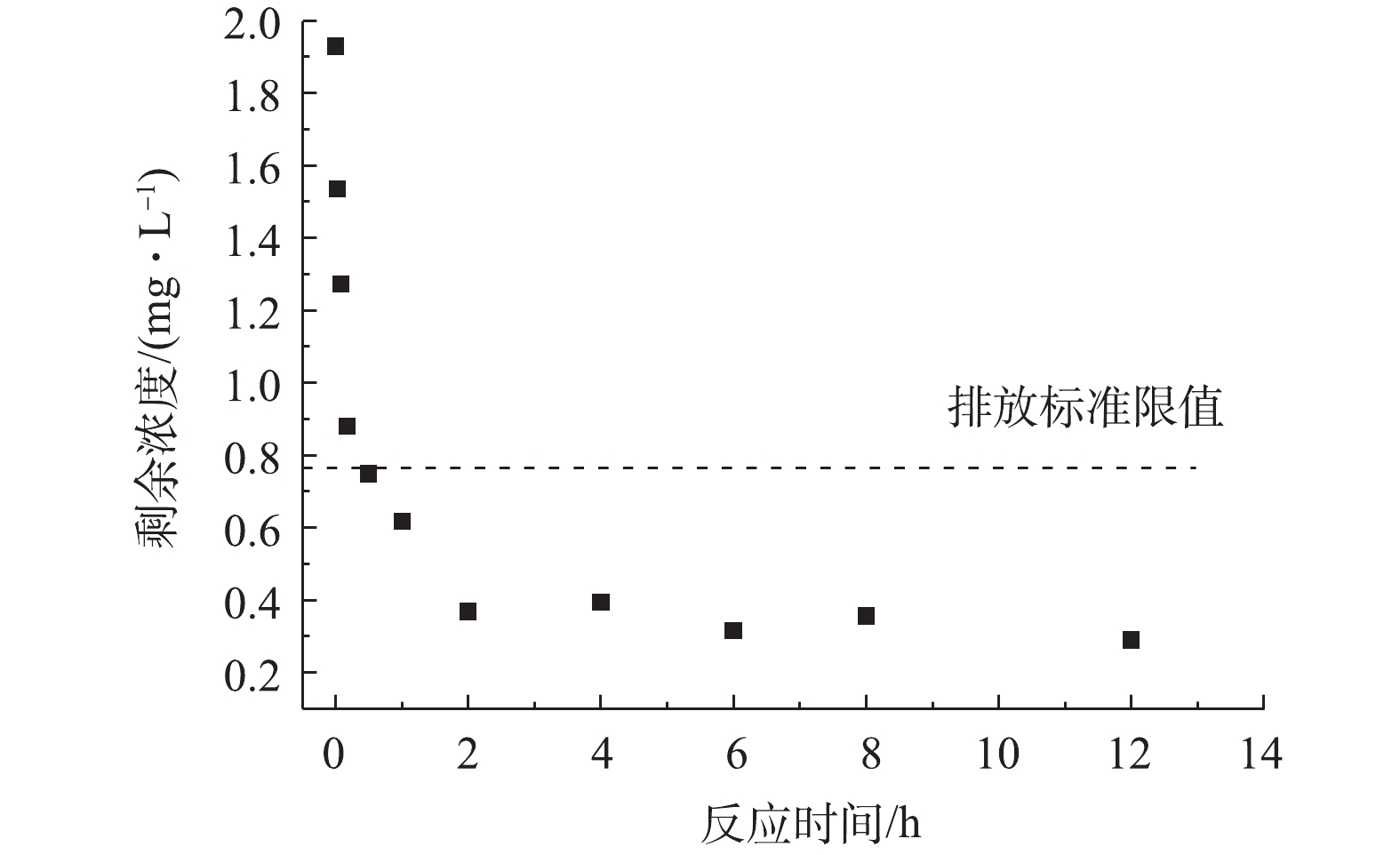
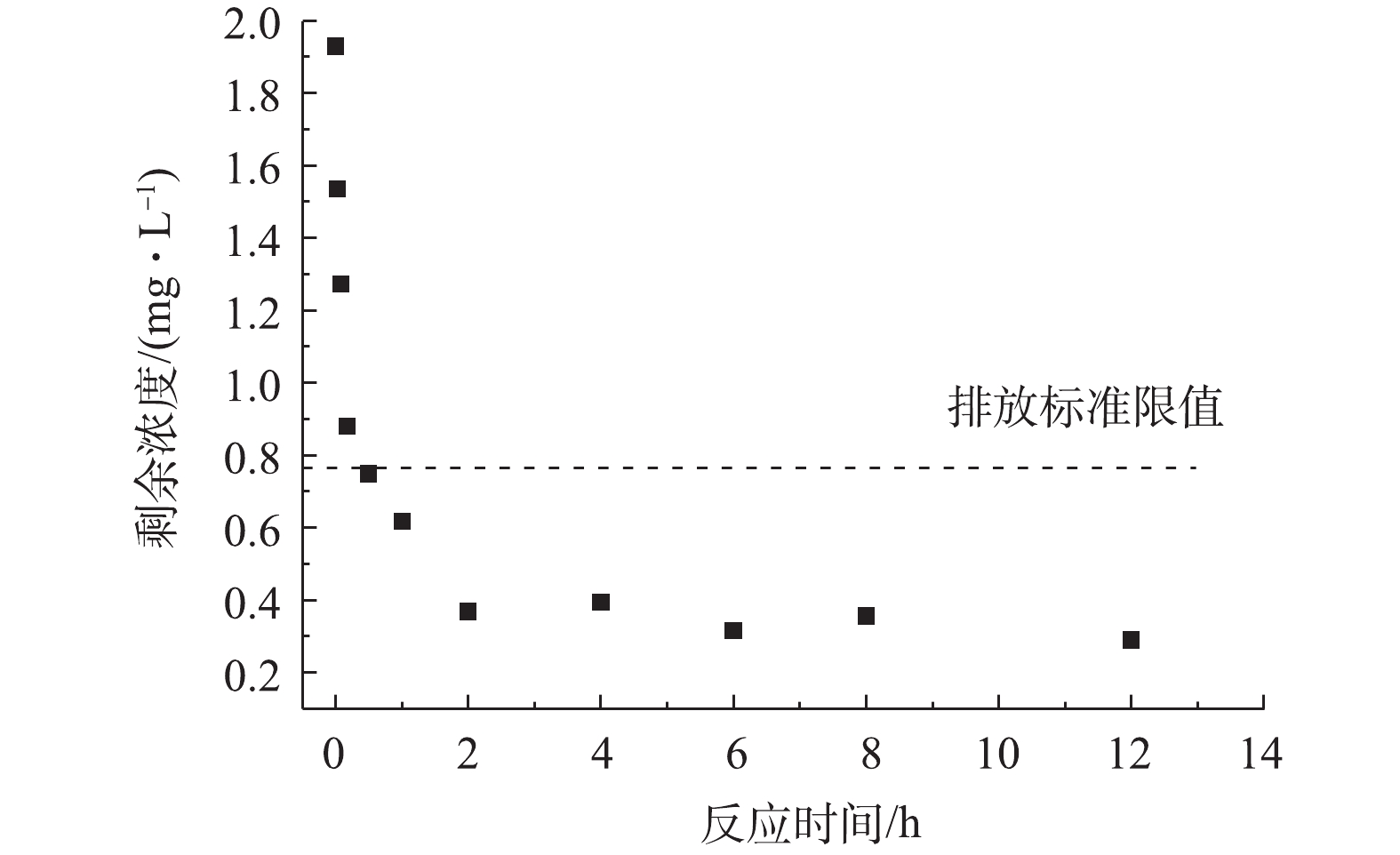
PO3−4 -P <0.051 mg·L−1、10.08 mg·L−1NO−3 、86 mg·L−1 Cl−、57.4 mg·L−1SO2−4 。可见该废水中的草甘膦浓度大约为2 mg·L−1,并且存在着数倍于草甘膦浓度的各种共存离子和一定有机物,水质参数较模拟水样更为复杂。MGTA-CDCH对实际污染水体的草甘膦吸附能力如图9所示,在投加量为0.2 g·L−1时,2 h内剩余草甘膦浓度远低于《生活饮用水卫生标准》(GB 5749-2006)中规定草甘膦浓度限值(0.7 mg·L−1)。此时,MGTA-CDCH对草甘膦的吸附量为8.30 mg·g−1,仍能保持草甘膦模拟水样吸附量的89.7%。结果表明,在复杂的实际污染水体中,MGTA-CDCH仍能保持对草甘膦的吸附能力。
2.1. 材料的制备与表征
2.2. 吸附等温线
2.3. 吸附动力学
2.4. pH对草甘膦吸附的影响
2.5. 共存有机物对草甘膦吸附的影响
2.6. 吸附再生实验
2.7. MGTA-CDCH在实际废水中的应用
-
1)利用阳离子化和自由基聚合法成功合成了一种可再生且易于磁分离的复合水凝胶MGTA-CDCH,表征结果表明,该材料中存在大量微孔结构,且Zeta电位在整个测试区间(pH=3~10.5)均保持在27 mV以上,这说明该材料具有永久正电荷。
2) MGTA-CDCH对草甘膦吸附过程符合Sips等温线模型,饱和吸附量为186.3 mg·g−1。吸附动力学拟合结果表明,吸附量在1 h内迅速增加,可达饱和吸附量的96.6%。pH=3~7为该吸附过程的适用范围,在腐殖酸存在下,MGTA-CDCH同样具有较好的草甘膦吸附性能。吸附后经NaOH-NaCl-乙醇脱附液处理后的MGTA-CDCH脱附率可达90%以上,在5次循环后仍保持86%的吸附容量,这说明该材料具有可重复使用性。
3)针对阴离子有机物草甘膦,MGTA-CDCH中起主要活性作用为阳离子基团–[N+(CH3)3]和环糊精主体结构,该吸附过程依赖于静电吸引和氢键的双重作用。






 DownLoad:
DownLoad: