-
铜绿微囊藻是产生藻华的主要藻种之一,高藻水会给自来水厂水质处理带来困难,藻细胞在新陈代谢过程中会释放有机物至水体中,其中包括嗅味物质,并在消毒工艺过程中产生消毒副产物[1-2]。目前,常用的除藻方法有生物去除法、化学去除法和物理去除法3种[3]。物理法包括超滤膜法、气浮法和活性炭吸附法。超滤膜法对水中藻细胞和胞外聚合物(extracellular organic matters,EOM)有良好的去除效果,但是藻及藻源有机物极易堵塞膜孔,造成严重的膜污染。气浮法只适合高藻低浊度的水处理,同时水厂须新建的构筑物及新增加的水泵增大了能耗,使水厂处理成本增加。生物法处理采用能溶解藻的细菌破坏藻细胞壁,但藻破裂死亡后会将细胞内有机物的释放,消耗水体中溶解氧,增加水体中总有机碳的浓度,破坏水生生物的生态平衡[4]。
与上述技术相比,化学法特别是混凝沉淀法依旧是最好的除藻方法之一,铝系混凝剂因其经济高效成为目前水厂使用最广泛的混凝剂。CHRISTOPHER等[5]通过研究发现,混凝前后钾离子浓度没有明显变化,证明铝系混凝剂没有杀死藻细胞,没有破坏藻细胞细胞壁结构。通过Ferron逐级络合比色法可将铝系絮凝剂的形态分成3种:单体形态Ala、中等聚和形态Alb、胶体及固体形态Alc[6]。YAN等[7]认为这3种形态去除有机物(nature organic matter, NOM)的机理分别为络合、电中和、吸附。分子式为[AlO4Al12(OH)24(H2O)12]7+的Al13带有很高的正电荷及很强的架桥能力,是Alb的主要活性成分。WANG等[8]和ISHIFUJI等[9]发现,低浓度的EOM能促进混凝,高浓度的EOM却抑制混凝过程。虽然很多学者研究了不同混凝剂对藻细胞的去除效果,但是混凝除藻过程中胞外聚合物对不同混凝剂混凝效果的影响研究并不充分,对于哪种铝系混凝剂去除藻的EOM效果最优及作用机理也没有达成共识[2-4]。
混凝剂的选取是除藻的关键因素之一,AlCl3为传统铝盐絮凝剂,其特点是制备工艺简单。PACl的特点是除浊效果好、成本适中、污泥产量少。本研究对比了2种最常见的铝系混凝剂对藻细胞的去除效果,分析了溶出有机物和形成絮体的特征,讨论了胞外有机物在混凝过程中和铝形态的相互作用,研究了EOM对混凝除藻的影响,为水厂优化混凝处理富藻水提供参考。
-
实验试剂均为国药集团生产优级纯试剂,包括NaOH、AlCl3·6H2O、NaHCO3以及BG11藻培养基。该培养基包括NaNO3、K2HPO4、MgSO4·7H2O、CaCl2·2H2O、EDTANa2、Na2CO3、柠檬酸、柠檬酸铁铵、H3BO3、MnCl2·4H2O、ZnSO4·7H2O、Na2MoO4、CuSO4·5H2O、Co(NO3)2·6H2O。实验仪器包括pH计(FE, METTLER TOLEDO, Switzerland),浊度仪(2100N, HACH, USA),紫外/可见光分光光度计(UH5300, HITACHI, Japan),马尔文激光粒度分析仪(3000, MALVERN, UK),梅宇六联搅拌仪(MY3000-6F, MEIYU, China),高效排阻测定仪(WATERS1525液相色谱仪)连接东曹凝胶色谱柱(Shoko Corporation, Japan)。
-
铜绿微囊藻(蓝藻)购于中国科学院武汉水生生物研究所,藻种接种至120 ℃灭菌15 min的BG11培养基中,并放入人工培养箱,人工培养箱的设置参数为:温度25 ℃,光照强度2 000 lx,光暗比12 h∶12 h[10]。
藻细胞的密度与悬浮藻液在680 nm处的吸光度具有良好的线性关系,因此,本研究以含藻水在680 nm的吸光度值作为藻细胞密度的度量标准。在实验中,将处于初始稳定期的铜绿微囊藻溶液用去离子水稀释至680 nm处,吸光度值为0.3,加入5 mmol·L−1 NaNO3和4 mmol·L−1 NaHCO3以提供离子强度和碱度。
-
本实验采用AlCl3和PACl 2种混凝剂,PACl采用慢速滴碱法[11]制备。采用Al-Ferron逐时络合比色法测定铝形态:反应时间<1 min的形态为单体态Ala,反应时间为1~120 min的形态为Alb,不反应的形态为Alc。实验所用混凝剂的Ferron表征结果见表1。可以看出,AlCl3主要以Ala为主(92.53%),PACl以Alb为主(79.18%)。
使用六联搅拌机进行实验,加入混凝剂后,进行0.5 min的250 r·min−1快速搅拌,促进混凝剂的均匀分散,40 r·min−1慢速搅拌10 min,促进絮体形成,沉淀30 min后,取液面下2 cm的样品进行OD680及浊度检测。
三维荧光主要用于描绘水中有机物的特征。本实验使用F-7000三维荧光分析(Hitachi,Japan),采用氘灯,设置发射波长(Em)为220~550 nm,设置激发波长(Ex)为200~400 nm。用高效体积排阻色谱仪(HPSEC)测定混凝前后溶液中有机物的表观分子质量。HPSEC应用的是Waters的液相分析系统,主要包括Waters 2487双波长检测器和Waters1525双泵系统。选用凝胶色谱柱(Shoko Corporation, Japan)对样品进行分离。配置含有0.02 mol·L−1磷酸盐缓冲液及 0.01 mol·L−1 NaCl的流动相,流动相用0.22 µm滤膜过滤,在使用前,超声15 min,排出流动相中的微气泡。样品测定前,用0.22 µm滤膜过滤。测试时,流动相流速为 0.8 mL·min−1,进样体积为200 μL,在紫外波长254 nm处检测样品。
采用马尔文激光粒度仪对混凝过程中形成的絮体进行连续监测[12]。投加混凝剂后,用蠕动泵将溶液引入样品池,以光散色确定絮体生长的平均粒径[13](用D50表示)。投加混凝剂慢速搅拌约10 min后,以 200 r·min−1快速搅拌5 min,模拟絮体与水厂构筑物的碰撞过程。为了描述絮体的强度及再生长能力,可使用强度因子和恢复因子2个指标,絮凝过程中的强度因子(Rs)和恢复因子(Rf)计算方法[14]见式(1)和式(2)。
式中:d1为慢速搅拌时的絮体平均粒径,μm;d2为絮体破碎时的平均粒径,μm;d3为再重组絮凝的平均粒径。
将混凝后絮体进行24 h冷冻干燥,将少量絮体粘贴至样品盘导电胶表面上,然后对样品进行喷金,采用日立SU8020扫描电子显微镜对其表面形貌进行分析。
-
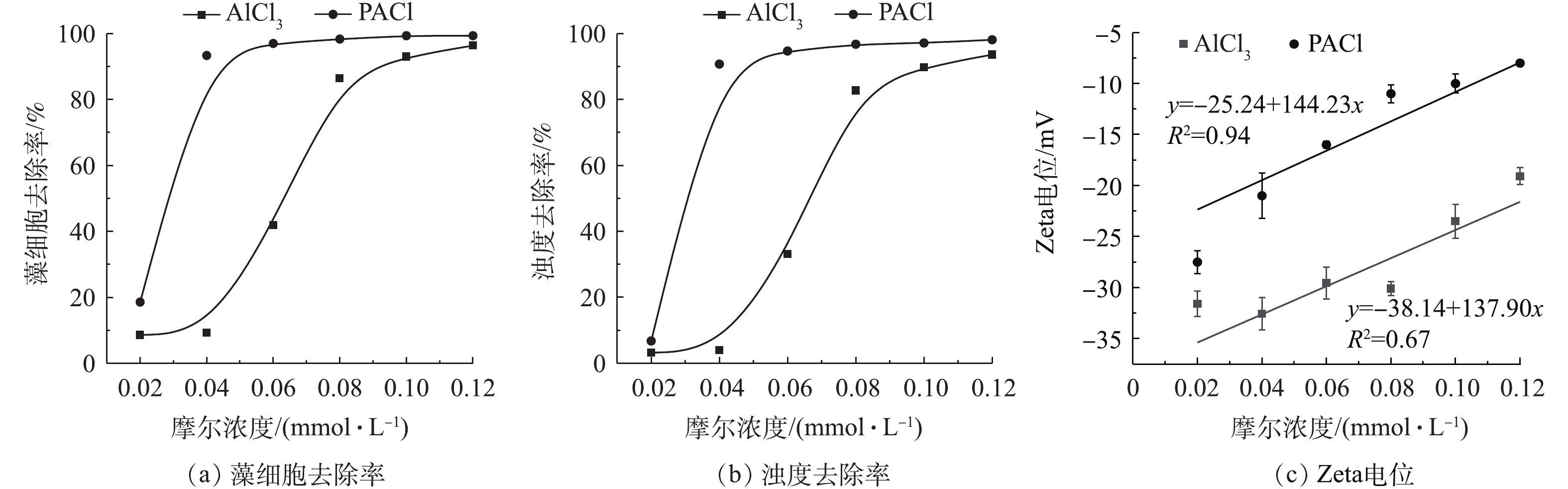
投加不同摩尔浓度混凝剂,考察单体铝和聚合铝2种混凝剂对藻细胞以及浊度的去除率。由图1可以看出,对于这2种铝盐混凝剂,浊度去除率和藻细胞的去除率都随着混凝剂摩尔浓度的增加而增加,但是相同投加量下PAC对藻的去除效果优于AlCl3。在摩尔浓度为0.04 mmol·L−1时,投加PACl对藻细胞的去除率能达到93%,而投加AlCl3的藻细胞去除率只有9%;投加PACl和AlCl3对浊度去除率分别为91%和4%。这是因为PACl中存在大量高电量且稳定的多核预水解产物(Alb),中和水中带负电的dEOM及藻细胞。含有较低正电荷的AlCl3只有不断增大投加量,才达到与高聚合态混凝剂 PACl相同的混凝效果,因此,AlCl3在摩尔浓度为0.08 mmol·L−1时才能达到85%的藻细胞去除率[15]。由图1(c)可知,PACl和AlCl3的Zeta电位均随着投加量的升高而增大,这是因为投加带正电的混凝剂压缩了胶体的双电层。将Zeta电位和混凝剂投加量线性拟合,PAC的R2为0.94,可以看出,Zeta电位随PAC投加量成正比增加,因此,PAC中的Alb电中和藻表面负电荷是混凝除藻的主要机理。而AlCl3的R2为0.67,说明在较低混凝投加量下(0.02、0.04、0.06 mmoL·L−1)为电中和,随着投加量的增加,氯化铝的架桥网捕作用得以有效发挥[16-17]。
-
pH是水化学的一个很重要的指标,为了考察pH对混凝的影响,调节水样的pH为6.0、6.5、7、7.5、8、8.5。2种混凝剂的投加量为0.08 mmol·L−1时,藻细胞去除率为80%以上。由图2可知,在弱酸性及中性条件下,AlCl3和PACl都有着较高的藻细胞去除率。在pH为6时,AlCl3对藻细胞的去除率为95%,PACl对藻细胞的去除率甚至达到了98%,这与本研究的结果一致。CLASEN等[18]研究表明,铝系混凝剂的最佳pH为6~6.5。随着pH的升高,2种混凝剂对藻细胞的去除率均降低,但是AlCl3下降更为显著。pH从6.5上升至7时,AlCl3对藻细胞的去除率从95%下降至68%;当pH为7时,水溶液中主要存在的是单体态的铝,此时对藻细胞的去除率低于酸性条件下的去除率。对于PACl,pH从6上升至7.5时,藻细胞去除率一直保持在95%左右;pH上升至8.5,藻细胞去除率降至85%。这是因为PACl中预水解生成的Alb为Al13聚体,化学性质较为稳定,受pH的影响较小[19]。如图2所示,在混凝时,相同pH下PAC的Zeta电位高于AlCl3,这说明AlCl3体系更稳定,絮体沉降性低于PAC。
-
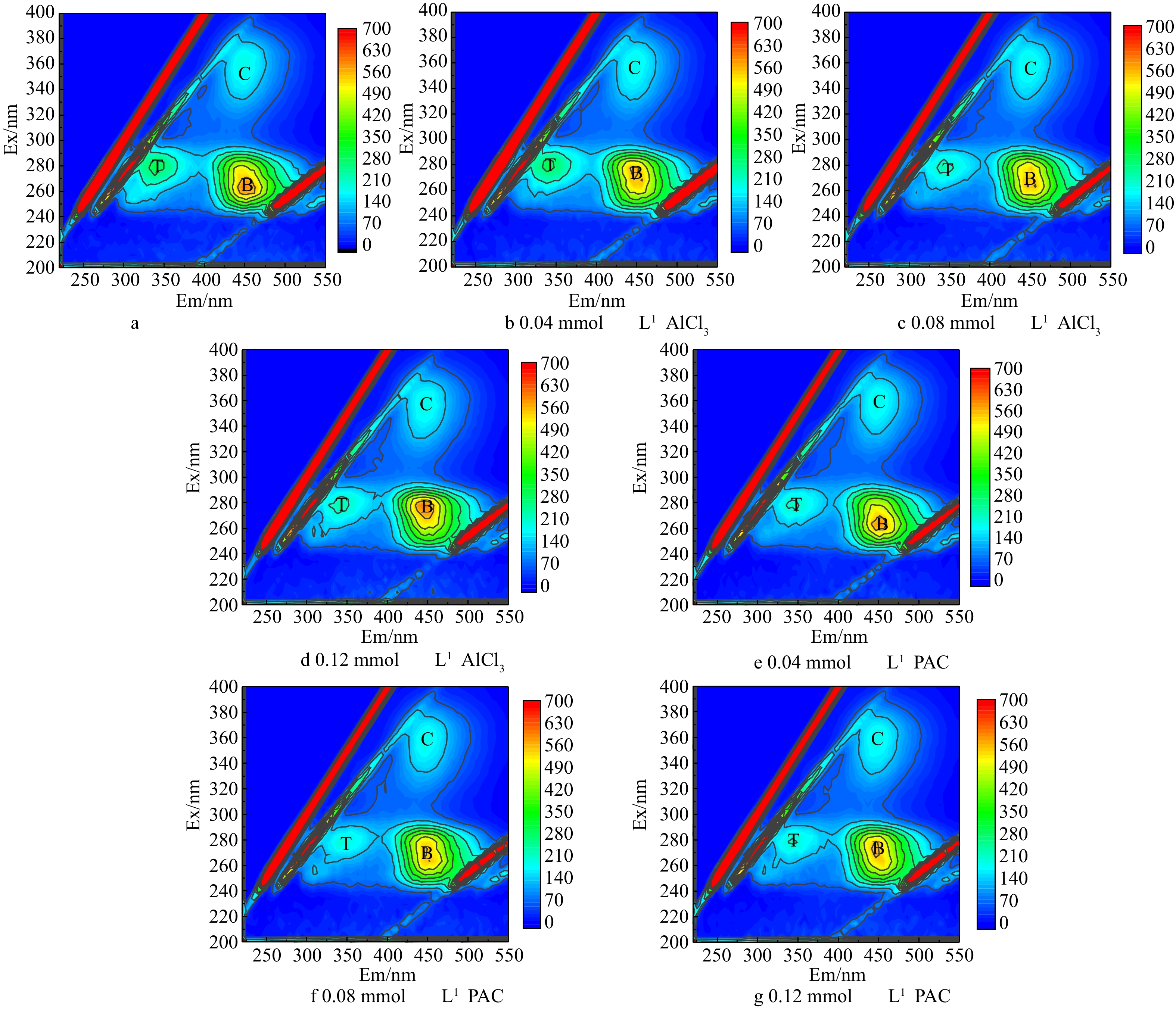
为研究混凝过程中胞外有机物的去除情况,取混凝剂摩尔浓度为0.04、0.08、0.12 mmol·L−1的沉后水,过0.45 μm滤膜后进行EEM测试,结果见图3。可以看出,藻混凝前后都有T、B和C 3个峰,分别代表微生物代谢产物、富里酸和腐殖酸[20]。有研究[8]表明,芳香类蛋白质的降解会导致发射及激发波长的蓝移。而图3中的2种混凝剂荧光图的特征峰位置均没有发生变化,只是强度发生了变化,这说明AlCl3及PACl在混凝过程中仅导致了蛋白质的聚集沉淀。
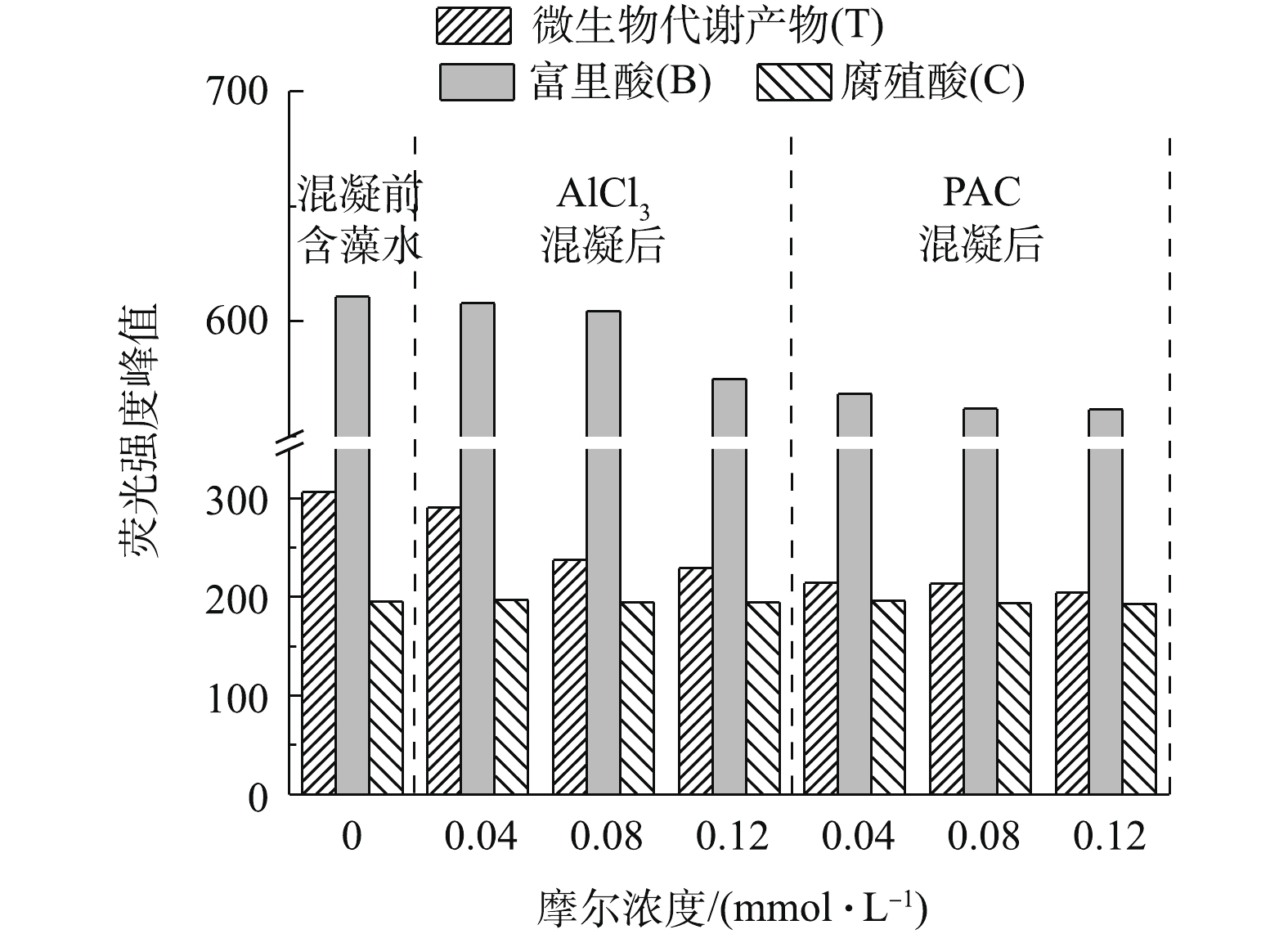
为了进一步分析三维荧光图中各组分随摩尔浓度的变化,选出T、B和C 3个峰强最大值(见图4)。首先,AlCl3和PACl在本实验的摩尔浓度下对腐殖酸基本无去除效果。与原水对比,0.04 mmol·L−1 AlCl3摩尔浓度下的T、B和C 3个峰值未发生明显变化,这说明Ala在此摩尔浓度下对EOM的3种组分几乎无去除。当AlCl3摩尔浓度上升到0.08 mmol·L−1时,腐殖酸没有去除效果,微生物代谢产物的荧光强度从306降低到237,去除率为22%。当AlCl3的摩尔浓度上升至0.12 mmol·L−1时,富里酸开始去除,峰强从611下降至575,去除率为5.8%。当PACl为0.04、0.08、0.12 mmol·L−1时,3个摩尔浓度下3种胞外有机物的去除率接近,当PACl浓度为0.08 mmol·L−1时,对微生物代谢产物的去除率为30.3%左右,PACl对微生物代谢产物的去除率比AlCl3高7.7%。
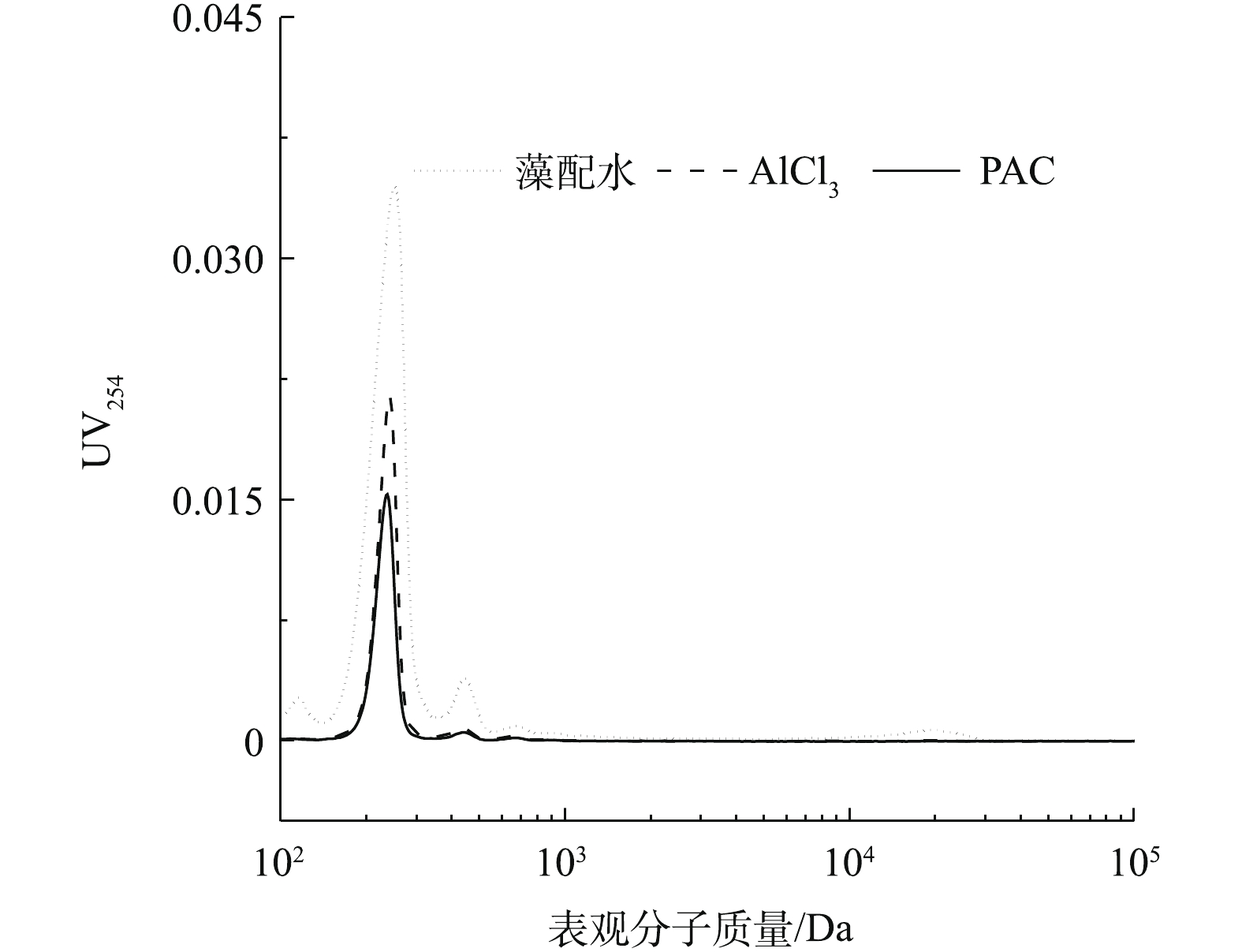
为进一步分析2种铝形态混凝对溶液体系中藻胞外有机物的影响,采用高效液相排阻色谱分析了藻配水、PACl和AlCl3摩尔浓度为0.08 mmol·L−1沉后水有机物的表观分子质量分布情况,结果见图5。可以看出,在表观分子质量为200~300 Da处有1个强峰,表观分子质量为400~500 Da处有1个次强峰,在分子质量为20 000 Da处有1个小峰。2种混凝剂混凝静置后,表观分子质量为400~500 Da和20 000 Da这2个峰几乎消失,这说明AlCl3和PACl都能沉降表观分子质量为400~500 Da和20 000 Da的有机物,这符合马敏等[21]的研究结果,表观分子质量较大或芳香度较高的胞外聚合物在铝盐混凝中可被优先去除。结合三维荧光分析可知,这2个峰可能为憎水性的蛋白质或多糖。但是对于200~300 Da处的最强峰,PACl对其的去除率明显高于AlCl3,这和三维荧光得出的结论相符。结合图1可以看出,在摩尔浓度为0.08 mmol·L−1时,PACl比AlCl3多去除了表观分子质量为200~300 Da的胞外有机物,造成PACl对藻细胞的去除率比AlCl3的高10%。
-
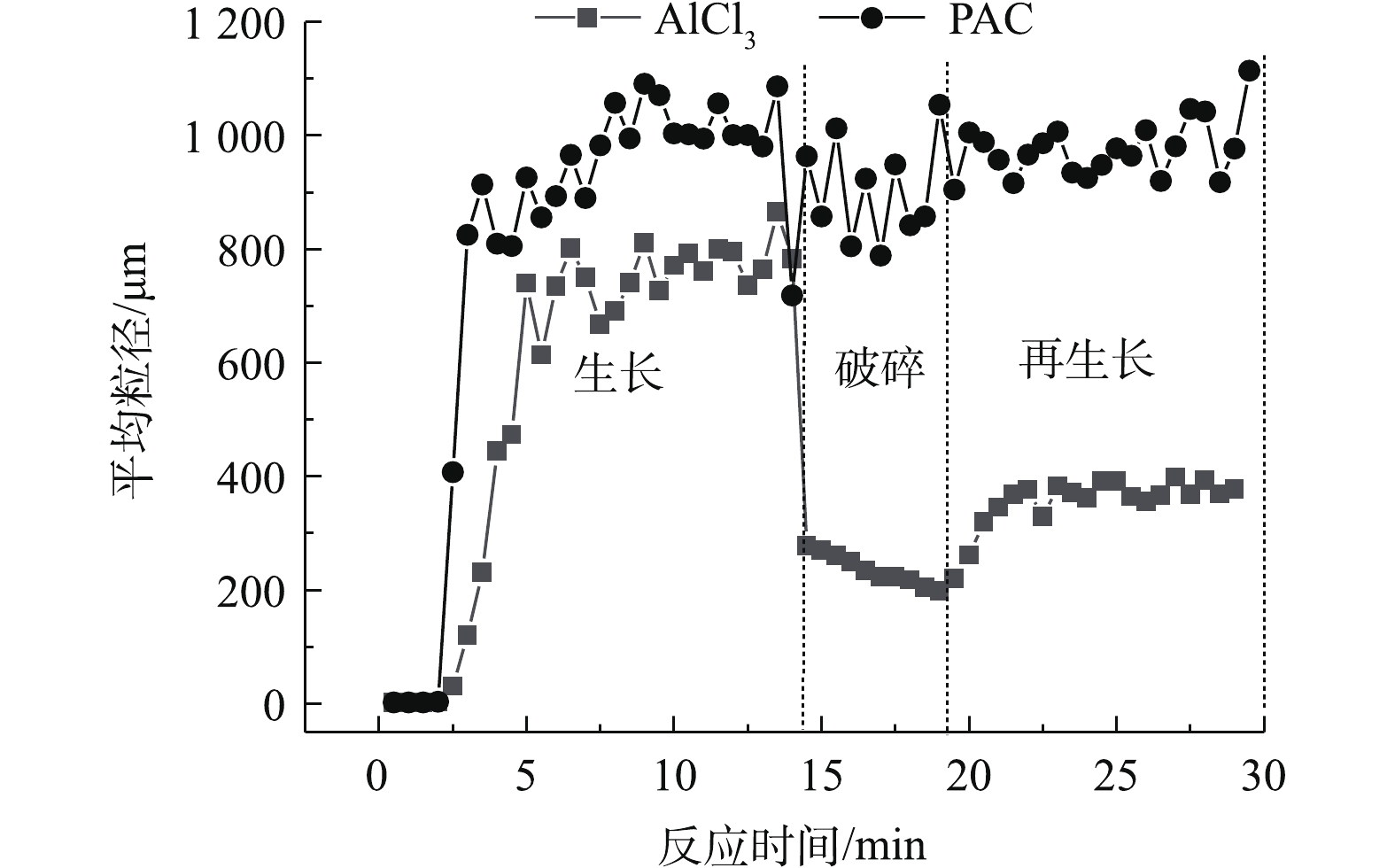
当摩尔浓度为0.08 mmol·L−1时,用马尔文激光粒度仪监测投加不同混凝剂生成絮体的特征,结果见图6。可以看出,待絮体粒径达到稳定时,投加AlCl3的藻配水中絮体的平均粒径可增加至800 μm,投加PACl的藻配水中絮体的平均粒径可增加至1 000 μm。但到了破碎期,2种混凝剂投加下形成的絮体表现出不同的强度。在剪切力的作用下,投加AlCl3生成的絮体迅速破裂至200 μm,而投加PACl形成的絮体粒径能保持在9 000 μm左右。这从表2中的强度因子可以证明,强度因子越大,絮体结构越紧密结实,PACl的强度因子86.28%远大于AlCl3的强度因子31.82%。分形维数[22-24]是用来确定絮体形态及强度的一个常用指标,分型维数为3时表示该颗粒为球形,PACl絮体的分形维数为2.17,大于AlCl3絮体的分形维数1.76,这也能证明PACl产生的絮体更密实。在絮体再生长期,投加PACl的絮体经过碰撞再链接,又能生长至1 000 μm,而投加AlCl3的絮体再生长后只能达到400 μm,为生长期的一半。这也可从表2得到验证,PACl的恢复因子49.52%大于AlCl3的29.6%。
为了直观地观察絮体的形貌,采用扫描电子显微镜观察摩尔浓度为0.08 mmol·L−1 PACl和AlCl3冷冻干燥后的絮体,见图7。
由图7(a)可以看出,绝大多数藻细胞相互紧贴,主要是由于Alb中和了藻细胞表面的负电荷,这些抱团的藻细胞聚集体再通过片状Al(OH)3卷扫网捕形成更大的絮体。由图7(b)可以看出,藻细胞和片状Al(OH)3近似均匀混合,因此可以确定主要混凝机理为卷扫网捕。可以看出,PACl絮体的密集性高于AlCl3的密集性,这与PACl絮体分形维数大于AlCl3的结论相吻合。
-
1)在常规混凝条件下,PACl比AlCl3具有更好的藻细胞和藻源有机物去除率。当投加量为0.08 mmol·L−1时,对藻的去除率分别为96%和82%。
2)当pH为6~8时,PACl均可保持95%以上的藻细胞去除率,AlCl3只能在pH为6~6.5狭小的范围内保持相同的去除率。
3)三维荧光结果表明,最佳投加量为0.08 mmol·L−1 时,PAC可去除30.3%的微生物代谢产物,AlCl3去除22.6%的微生物代谢产物。PACl中含有的Alb对提高微生物代谢产物和富里酸的去除发挥了重要作用。
4)在摩尔浓度为0.08 mmol·L−1时,PACl比AlCl3多去除了分子量为200~300 Da的胞外有机物。PACl的强度因子和恢复因子均大于AlCl3,且絮体的分形维数2.17大于AlCl3的1.76,因此,PACl形成絮体的密实程度大于AlCl3的絮体。
铜绿微囊藻的胞外有机物对不同混凝剂除藻效果的影响
Effects of extracellular organic matters of Microcystis aeruginosa on algal removal by different coagulants
-
摘要: 为了保证水厂在高藻条件下的安全清洁供水,以分布较为广泛的铜绿微囊藻(Microcystis aeruginosa)为研究对象,采用2种铝系混凝剂AlCl3和聚合氯化铝(polyaluminum chloride,PACl)进行烧杯混凝实验,考察混凝过程中铝形态对除藻的影响,分析铜绿微囊藻的胞外有机物(extracellular organic matters,EOM)对藻去除的影响机制。结果表明:在PACl浓度为0.04 mmol·L−1时,对藻细胞及浊度的去除率均为90%,而AlCl3摩尔浓度为0.08 mmol·L−1时,藻细胞及浊度去除率才达到90%;在制备PAC时,会水解产生大量中等聚合形态、性质稳定的Alb,在弱酸性到弱碱性的范围(pH为6~8)内,Alb对藻细胞去除率均可达到95%以上;而AlCl3只有在比较窄的pH范围内形成原位Alb,AlCl3只能在较窄的pH范围内(pH为6~6.5)保持95%藻细胞去除率。与AlCl3相比,PACl可去除更多表观分子质量为200~300 Da的胞外聚合物,同时PACl混凝后得到的絮体密实度大于AlCl3。以上结果为研究铝系混凝剂强化去除藻的胞外有机物提供了参考。Abstract: In order to guarantee the safety of tape water under high algae level conditions, the widespread Microcystis aeruginosa was taken as targeted object in this study. Two kinds of coagulants (AlCl3 and polyaluminum chloride) were used to evaluate the effects of Al species on algae removal through jar test, and identify the effect mechanism of extracellular organic matters of Microcystis aeruginosa on algal removal. The results showed that at PACl dosage of 0.04 mmol·L−1, the removal rates of both algae and turbidity reached 90%, while at AlCl3 dosage of 0.08 mmol·L−1, the removal rates of both algae and turbidity reached 90%. During the preparation of PAC, large amount of intermediate polymer species (Alb) with high stability were produced through hydrolysis, which could achieve 95% algae removal within the weak acid and alkaline pH range of 6 to 8. However, Alb could only be in situ formed after AlCl3 dosing into water for hydrolysis within a narrow pH range of 6 to 6.5 and maintain 95% algae removal within it. Compared with AlCl3, PACl could remove more extracellular polymers with apparent molecular mass of 200~300 Da, and the formed flocs through PACl coagulation were more dense than through AlCl3 coagulation. The research results provide reference for study the enhanced removal of algal extracellular organic matters by aluminum coagulants.
-
Key words:
- coagulation /
- Microcystis aeruginosa /
- extracellular organic matters /
- Al species
-
表 1 2种混凝剂铝形态的分布
Table 1. Al species distribution of two coagulants
% 混凝剂种类 Ala Alb Alc AlCl3 92.53 3.92 3.55 PACl 11.47 76.18 12.35 表 2 混凝后絮体的强度因子、恢复因子与分形维数
Table 2. Strength factor, recovery factor and fractal dimensions of flocs formed after coagulation
混凝剂 强度因子/% 恢复因子/% 分形维数 AlCl3 31.82 29.60 1.76 PACl 86.28 49.52 2.17 -
[1] 吴昊澜, 杨晓芳, 沈敏丽, 等. 钙离子对混凝去除水体中铜绿微囊藻的影响[J]. 环境工程学报, 2018, 12(3): 839-847. doi: 10.12030/j.cjee.201708138 [2] GENG C X, CAO N, XU W, et al. Molecular characterization of organics removed by a covalently bound inorganic-organic hybrid coagulant for advanced treatment of municipal sewage[J]. Environmental Science & Technology, 2018, 52(21): 12642-12648. [3] 何晓梅, 古宇力. 给水厂中处理高藻水常用的方法[J]. 能源与环境, 2016(4): 84-85. doi: 10.3969/j.issn.1672-9064.2016.04.042 [4] 张利. 水处理过程中常见的混凝除藻方法综述[J]. 中国资源综合利用, 2019, 37(4): 69-72. doi: 10.3969/j.issn.1008-9500.2019.04.021 [5] CHRISTOPHER W K C, DRIKAS M, HOUSE J, et al. The impact of conventional water treatment processes on cells of the cyanobacterium Microcystis aeruginosa[J]. Water Research, 1999, 33(15): 3253-3262. doi: 10.1016/S0043-1354(99)00051-2 [6] 汤鸿霄. 无极高分子絮凝理论与絮凝剂[M]. 北京: 中国建筑工业出版社, 2006. [7] YAN M Q, WANG D S, NIA J, et al. Mechanism of natural organic matter removal by polyaluminum chloride: Effect of coagulant particle size and hydrolysis kinetics[J]. Water Research, 2008, 42(13): 3361-3370. doi: 10.1016/j.watres.2008.04.017 [8] WANG L, LIANG W, YU J, et al. Flocculation of Microcystis aeruginosa using modified larch tannin[J]. Environmental Science & Technology, 2013, 47(11): 5771-5777. [9] ISHIFUJI S, SATO Y, IMAE H, et al. Identification of coagulation inhibitor proteins from Microcystis aeruginosa[J]. Journal of Japan Society on Water Environment, 2010, 33(6): 73-79. doi: 10.2965/jswe.33.73 [10] 张大为, 徐慧, 王希. 藻形态及混凝剂组成对混凝-超滤过程的影响[J]. 环境科学, 2017, 38(8): 3281-3289. [11] YAN M, WANG D, QU J, et al. Relative importance of hydrolyzed Al(III) species (Ala, Alb, and Alc) during coagulation with polyaluminum chloride: A case study with the typical micro-polluted source waters[J]. Journal of Colloid and Interface Science, 2007, 316(2): 482-489. doi: 10.1016/j.jcis.2007.08.036 [12] 焦茹媛. 水质特征对铝盐混凝剂混凝过程的影响-残余铝生成及沉后水过滤特性[D]. 北京: 中国科学院大学, 2016. [13] 唐立朋, 魏群山, 刘亚男. 对位芳纶纤维对印染废水中染料的吸附行为研究[J]. 水处理技术, 2018, 44(6): 28-33. [14] JARVIS P, JEFFERSON B, PARSONS S A. Breakage, regrowth, and fractal nature of natural organic matter flocs[J]. Environmental Science & Technology, 2005, 39(7): 2307-2314. [15] YAN M Q, WANG D S, QU J H, et al. Enhanced coagulation for high alkalinity and micro-polluted water: The third way through coagulant optimization[J]. Water Research, 2008, 42(8/9): 2278-2286. [16] SHI B, LI G, WANG D, et al. Removal of direct dyes by coagulation: The performance of preformed polymeric aluminum species[J]. Journal of Hazardous Materials, 2007, 143(1): 567-574. [17] SU Z Y, LIU T, YU W Z, et al. Coagulation of surface water: Observations on the significance of biopolymers[J]. Water Research, 2017, 126(2): 144-152. [18] CLASEN J, MISCHKE U, DRIKAS M, et al. An improved method for detecting electrophoretic mobility of algae during the destabilisation process of flocculation: Flocculant demand of different species and the impact of DOC[J]. Journal of Water Supply Research and Technology, 2000, 49(2): 89-101. doi: 10.2166/aqua.2000.0008 [19] WANG D S, SUN W, XU Y, et al. Speciation stability of inorganic polymer flocculant-PACl[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2004, 243(1/2/3): 1-10. [20] CHEN W, WESTERHOFF P, LEENHEER J A, et al. Fluorescence Excitation-Emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(24): 5701-5710. [21] 马敏, 刘锐平, 刘会娟. 预氯化对铝盐混凝铜绿微囊藻过程中溶解性有机物和残余铝的影响[J]. 环境科学学报, 2014, 5(1): 73-78. [22] FICEK D, DERA J, WOZNIAK B. UV absorption reveals mycosporine-like amino acids (MAAs) in Tatra mountain lake phytoplankton[J]. Oceanologia, 2013, 55(3): 599-609. doi: 10.5697/oc.55-3.599 [23] XU H, ZHANG D W, XU Z Z, et al. Study on the effects of organic matter characteristics on the residual aluminum and flocs in coagulation processes[J]. Journal of Environmental Sciences, 2018, 63(5): 307-317. [24] 王东升, 汤鸿霄, 栾兆坤. 分形理论及其研究方法[J]. 环境科学学报, 2001, 24(1): 10-16. -




 下载:
下载: