-
含高浓度磷酸盐的废水排放到地表水中,可造成各种水体污染问题,如水体富营养化[1]。水中磷酸盐、硝酸盐等无机阴离子刺激蓝藻过度生长,破坏生物多样性[2]。如果大量含氮、磷的废水排入湖泊、河口、水库等缓流水体,这些营养物质会使藻类等水生生物过量繁殖,进而导致水体透明度下降、水质恶化等一系列问题[3]。水体富营养化给人们的生产生活带已成为迫切需要解决的问题[4]。为了控制水体富营养化、进一步减少排入水体中的磷,自从上个世纪年代开始,研发人员对水体中磷的去除技术进行了大量的探索[5]。
吸附法作为一种成本低、操作简便、效率高的方法受到了不同研究者的广泛关注[6]。层状双金属氢氧化物(layered double hydroxides, LDHs)是一种层状材料,俗称水滑石,属于阴离子型层状化合物,由带正电荷的金属氢氧化物层和带负电荷的层间阴离子以及水分子构成[7-8],基于LDHs的无机吸附剂可以从水中去除氧化阴离子,如砷酸盐、铬酸盐和磷酸盐[9]。由于其特殊的层状结构和高比表面积,LDHs比大多数常见的氧阴离子吸附剂具有更强的吸附能力[10]。与其他吸附剂相比,LDHs的合成工艺相对简单,成本较低。但一般的二元LDHs材料的吸附能力相对较低,作为除磷吸附剂仍存在元素组成需进一步优化、吸附速率和吸附选择性需进一步提高等问题[11],而三元、四元LDHs材料与二元LDHs材料有类似的结构,却有更优越的物化性质和吸附能力,对于作为吸附法除磷的除磷剂有很大的应用前景[12]。JIAN等[13]用氧化共沉淀法制备了Fe、Al、Mn摩尔比为3∶3∶1的纳米铁铝锰三元金属氧化物吸附剂,该吸附剂对磷酸盐的最大吸附容量约为48.3 mg·g−1,高于文献报道的单组分氧化物铁铝锰三金属氧化物。
本研究对三元(Mg-Al-Zn)LDHs和四元(Mg-Al-Zn-Fe)LDHs吸附剂进行了制备,考察了LDHs基吸附剂对磷酸盐的吸附性能,探讨了吸附机理,利用响应曲面法(RSM)数学模型优化了吸附过程的相关参数。
-
六水合氯化镁(MgCl2·6H2O),六水合氯化铝(AlCl3·6H2O),氯化锌(ZnCl2),氯化铁(FeCl3),磷酸二氢钾(KH2PO4),氢氧化钠(NaOH),盐酸(HCl),均为分析纯,以上药剂均购于国药集团化学试剂有限公司。
-
本实验采用水热法制备多元LDHs材料[14],首先制备10%(质量分数)的NaOH溶液标记为溶液A,按照Mg∶Zn∶Al(∶Fe)摩尔比为1∶3∶1(∶0.5),称取一定量的AlCl3·6H2O、MgCl2·6H2O、ZnCl2(和FeCl3)于烧杯中,加20 mL去离子水溶解,记为B溶液。在转速300 r·min−1,温度80 ℃下将A、B溶液同时缓慢加入含20 mL纯水的烧杯中,并控制其pH在11左右,反应0.5 h,然后80 ℃陈化过夜,将得到的陈化产物离心、洗涤至中性、干燥、研磨,即得到MgZnAl-LDHs和MgZnAlFe-LDHs。
-
本实验中所使用的磷酸盐按照国标(GB 11893-1989)配制,吸附实验操作步骤:取(0.030 g±0.005) g的样品于150 mL锥形瓶中,加入30 mL 100 mg·L−1的磷酸盐溶液(pH=2),25 ℃,160 r·min−1振荡6 h,过滤后根据国标(GB 11893-1989)进行测定剩余磷酸盐的浓度(以P计),并根据式(1)计算平衡吸附量qe。
式中:qe为平衡吸附容量,mg·g−1;C0为溶液起始质量浓度,mg·L−1;Ce为溶液平衡质量浓度,mg·L−1;V为吸附溶液体积,L;m为吸附剂质量,g。
1)吸附等温线。分别称量(0.030±0.005) g的MgZnAl-LDHs和MgZnAlFe-LDHs加入到30 mL不同质量浓度(60~400 mg·L−1)的磷酸盐溶液中,调节pH=2,在25 ℃,160 r·min−1的条件下,于旋转式恒温振荡器中振荡6 h,吸附完成后,分别测定磷酸盐溶液浓度并计算磷酸盐的平衡吸附量。采用Langmuir(式(2))、Freundlich(式(3))和 Sips吸附等温模型(式(4))对吸附数据进行拟合。
式中:qe、qm分别为平衡吸附容量、吸附剂的吸附容量,mg·g−1;KL为Langmuir 吸附常数,L·mg−1;Ce为溶液平衡质量浓度,mg·L−1;KF为Freundlich 等温吸附常数,(mg·g−1) ·(mg·L−1)−n;n为吸附常数;qms为拟合最大平衡吸附量,mg·g−1;Ks为Sips吸附参数,(L·mg−1)ms;ms为非均一系数。
2)吸附动力学。分别称量(0.030±0.005) g的MgZnAl-LDHs和MgZnAlFe-LDHs加入锥形瓶中,加入30 mL 100 mg·L−1的磷酸盐溶液(pH=2),在25 ℃,160 r·min−1的条件下,于旋转式恒温振荡器中振荡,在0~300 min内测定磷酸盐浓度,并计算磷酸盐的吸附量。采用准一级(式(5))、准二级(式(6))和Elovich吸附动力学模型(式(7))对此动力学过程进行拟合。
式中:qe为平衡吸附容量,mg·g−1;qt为时间为t时的吸附容量,mg·g−1;t为吸附时间,min;k1为准一级动力学方程常数,min−1;k2为准一级动力学方程常数,g·(mg·min)−1;α为代表初始吸附速率的常数,g·(g·min)−1;β为解吸速率平衡常数,mg·g−1。
3) pH对吸附性能的影响。分别称量(0.030±0.005) g的MgZnAl-LDHs和MgZnAlFe-LDHs加入到30 mL 100 mg·L−1磷酸盐溶液中,用NaOH和HCl调节pH为2、3、4、5、6、7、8、9,在25 ℃,160 r·min−1的条件下,于旋转式恒温振荡器中振荡6 h,吸附完成后分别测定磷酸盐溶液浓度并计算磷酸盐的平衡吸附量。
4)共存离子对吸附性能影响。称量(0.030±0.005) g的MgZnAl-LDHs和MgZnAlFe-LDHs加入到30 mL 100 mg·L−1磷酸盐溶液中,分别加入0.1 mol·L−1的Cl−、
SO2−4 NO−3 HCO−3 5)响应面法优化实验设计。在上述实验的基础上,跟据Box-Behnken Design的原理,以pH(X1)、温度(X2)、初始质量浓度(X3) 3个因子为自变量, 以磷酸盐平衡吸附量(Y)为响应值,设计17组优化实验,对MgZnAlFe-LDHs的吸附实验建立响应回归模型,并采用Design Expert 12软件对实验结果进行统计分析,分析各影响因子间的交互作用及对响应值的影响。
-
1) SEM分析。多元LDHs的SEM图如图1所示。图1(a)、图1(b)为MgZnAl-LDHs的SEM图,图1(c)、图1(d)为MgZnAlFe-LDHs的SEM表征图。由图1可以看出,MgZnAl-LDHs和MgZnAlFe-LDHs材料均具有清晰的片层结构。图1(a)、图1(b)显示MgZnAl-LDHs表面较为光滑,并有较多的孔隙,结构较疏松,而图1(c)、图1(d)显示的MgZnAlFe-LDHs较MgZnAl-LDHs而言有更多的孔隙,结构变得更加紧密。
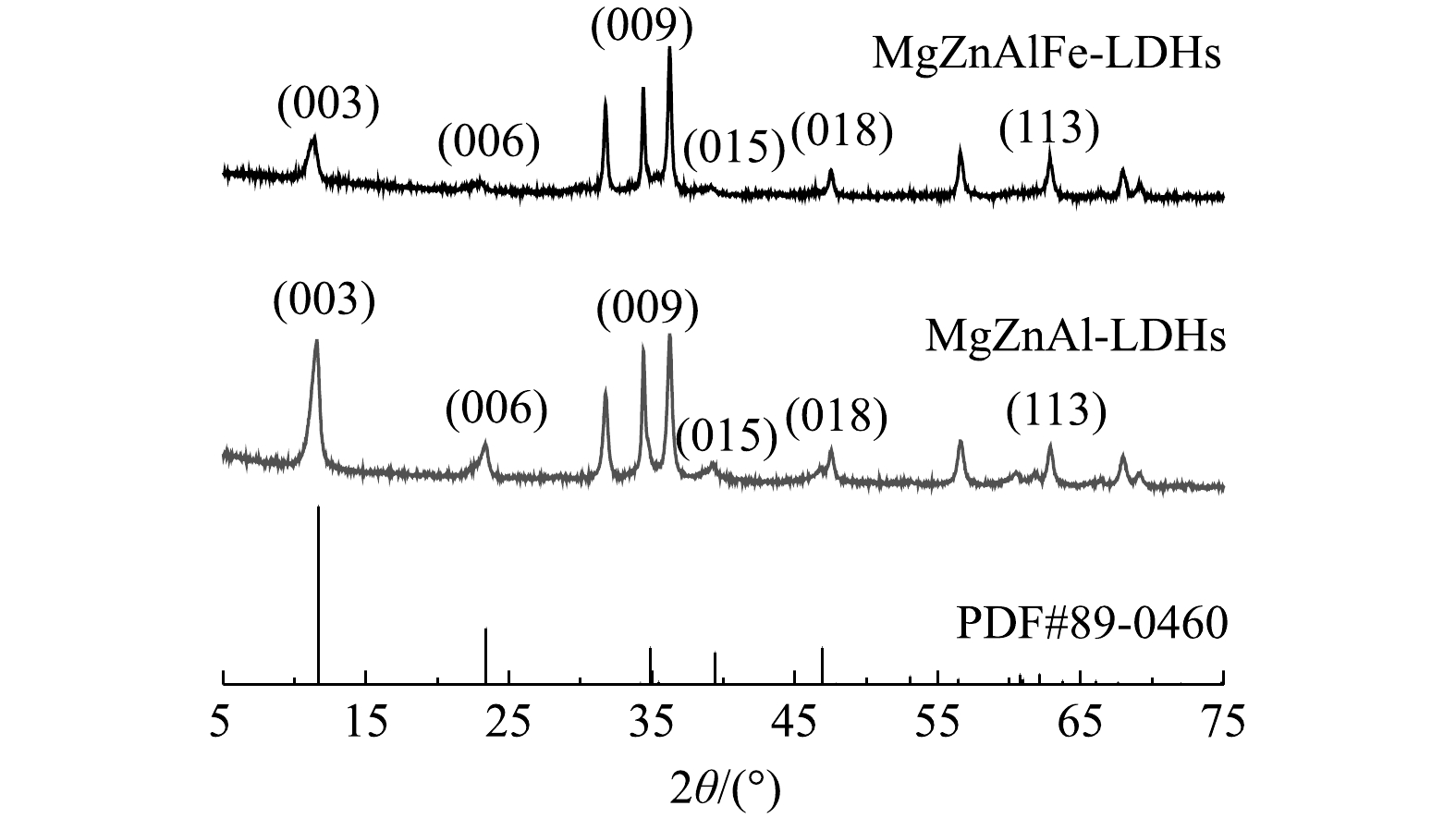
2) XRD分析。采用XRD对制备的吸附剂的晶体结构进行了研究。图2为MgZnAl-LDHs和MgZnAlFe-LDHs的XRD图谱。根据无机晶体结构数据库(ICSD)[15],图中XRD光谱均是典型的LDH相(与LDHs标准卡片PDF#89-0460高度符合),在(003)、(006)和(009)平面上有强烈的反射峰,在(015)、(018)和(113)平面上有宽的不对称峰,表明本实验制备的材料具有LDHs的结构特征。由图2可以看出,制备的MgZnAlFe-LDHs的峰与MgZnAl-LDHs相比发生了轻微的偏移,2θ分别为11.36°和11.55°,根据布拉格公式[16]计算层间距分别为0.778 nm和0.765 nm,可见四元LDHs相比三元LDHs层间通道有所增大。
-
1)吸附等温线。图3为MgZnAl-LDHs和MgZnAlFe-LDHs的吸附平衡等温线拟合结果,拟合参数如表1所示。由表1可知,MgZnAl-LDHs和MgZnAlFe-LDHs对磷酸盐的吸附等温模型符合Sips等温模型和Freundlich等温吸附模型,R2均大于0.9,这表明Sips模型和Freundlich等温吸附模型能够很好的解释MgZnAl-LDHs和MgZnAlFe-LDHs的等温吸附行为。MgZnAl-LDHs和MgZnAlFe-LDHs对磷酸盐的吸附符合Freundlich等温吸附模型方程说明两者可能是多层化学吸附[17],且其1/n值均小于1,说明两者均易吸附磷酸盐;KF值代表吸附剂的吸附能力,KF值越大,表明吸附剂对磷酸盐的吸附容量越大[18],MgZnAlFe-LDHs的KF值大于MgZnAl-LDHs,说明MgZnAlFe-LDHs较MgZnAl-LDHs吸附容量更大。同时,Sips拟合模型显示MgZnAl-LDHs和MgZnAlFe-LDHs对磷酸盐的最大拟合吸附量分别可达172.00 mg·g−1和189.62 mg·g−1。与MgAl-LDHs(76.8 mg·g−1)[19]相比,吸附量增大和吸附性能有所提高,同时MgZnAlFe-LDHs较MgZnAl-LDHs对磷酸盐的吸附量有所提高,这可能由于四元LDHs的层间通道宽于三元LDHs,同时吸附位点增多,使得磷酸盐吸附量增加。
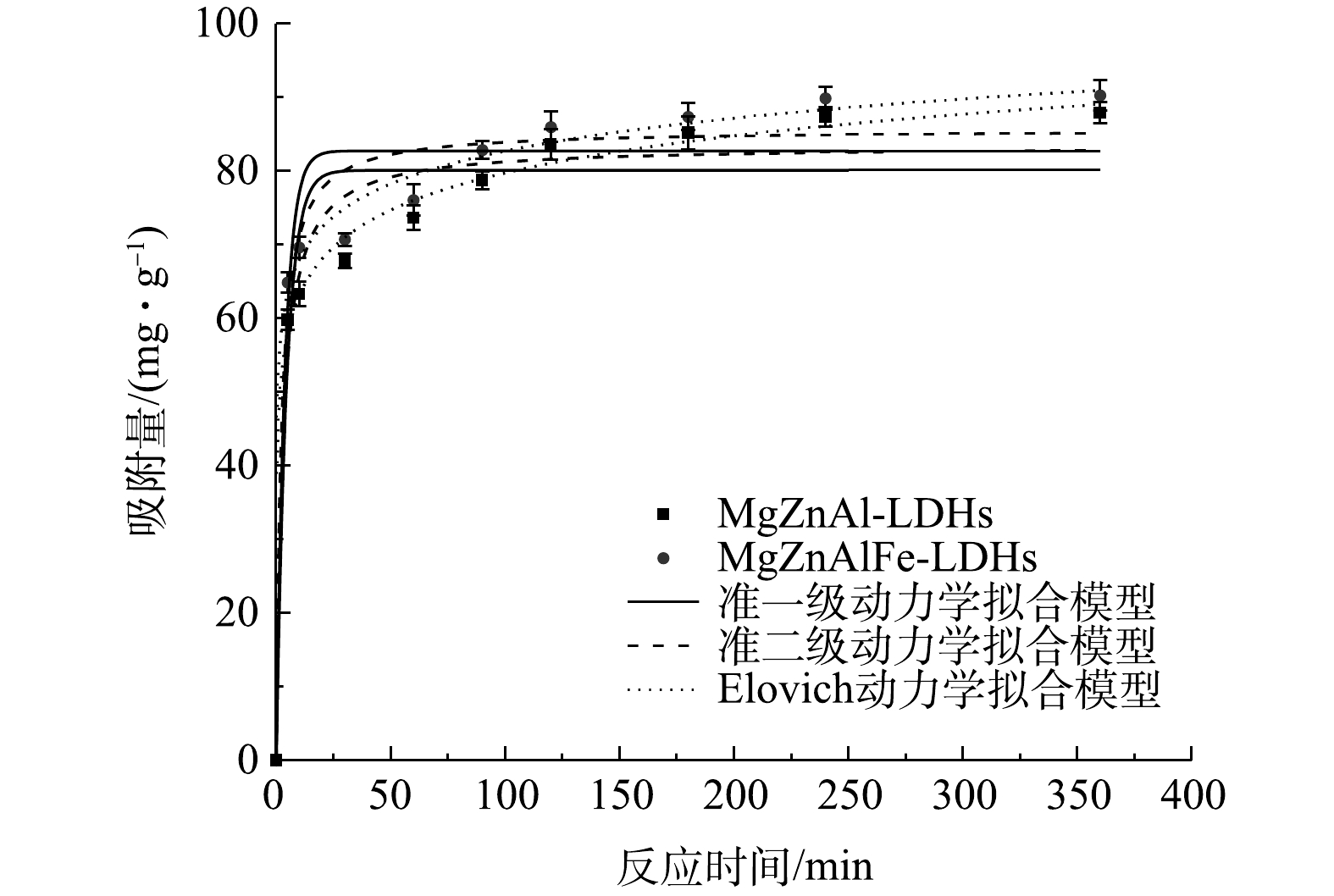
2)吸附动力学。如图4所示,本实验使用准一级动力学、准二级动力学和Elovich模型对吸附过程进行拟合,结果如表2所示。结果表明,MgZnAl-LDHs和MgZnAlFe-LDHs对磷酸盐的吸附动力学拟合符合准二级动力学吸附模型,拟合系数R2分别为0.968和0.963,且其计算吸附容量与实际吸附容量更加接近。同时,Elovich模型拟合系数R2均在0.99以上,说明MgZnAl-LDHs和MgZnAlFe-LDHs对磷酸盐的吸附动力学拟合也符合Elovich模型,吸附过程以化学吸附为主[20]。准二级动力学方程常数k2以及Elovich方程的α值反映了反应速率[21]。由表2可知,MgZnAlFe-LDHs对磷酸盐的吸附速率大于MgZnAl-LDHs的吸附速率,这可能是因为四元LDHs比三元的LDHs层间通道大,在吸附过程中磷酸盐可以更加快速地进入层间,这与XRD分析结果相一致。
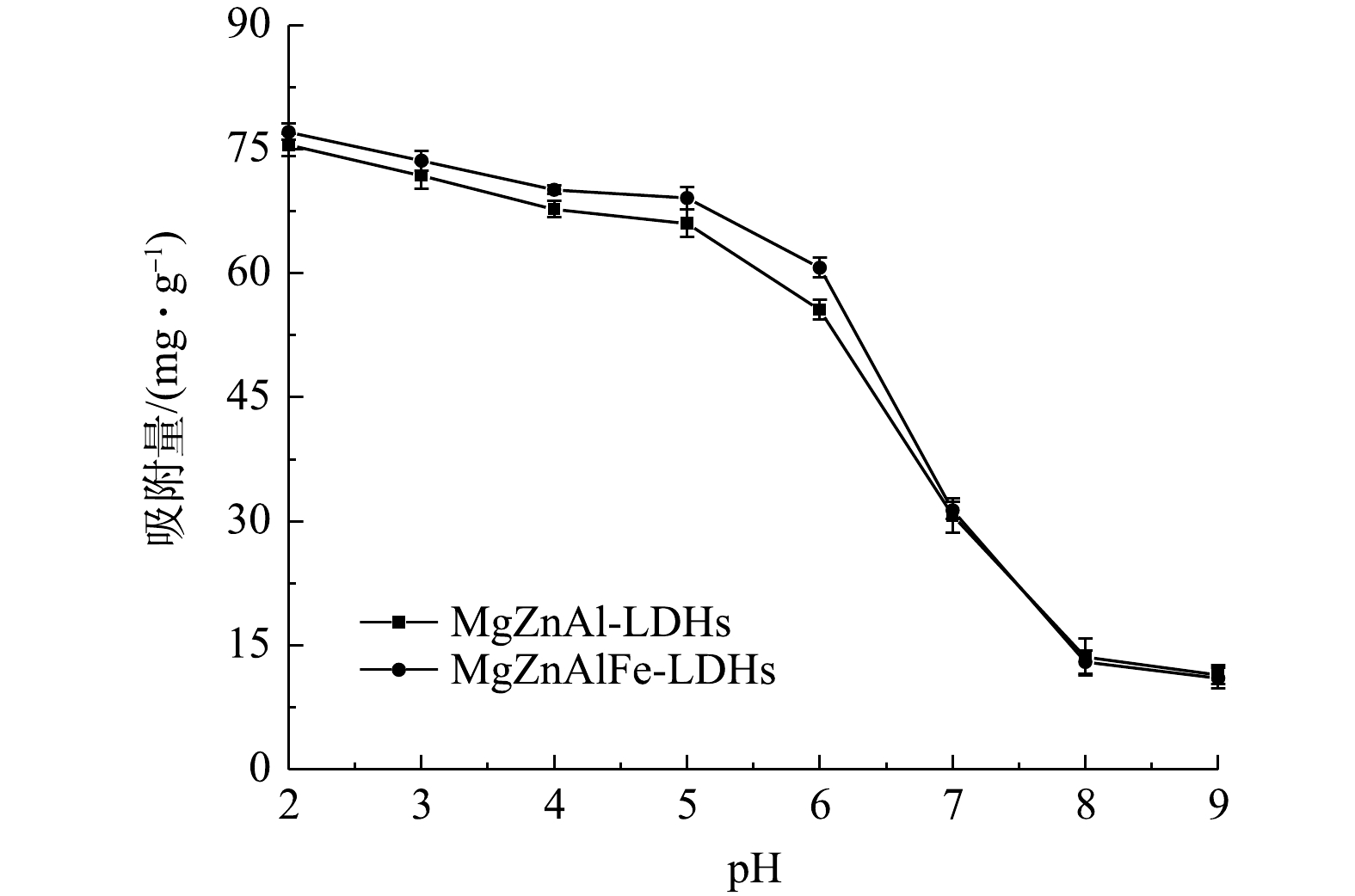
3) pH对吸附的影响。磷酸根在水溶液中的存在形式主要由pH决定[9],在酸性条件下,P离子主要以
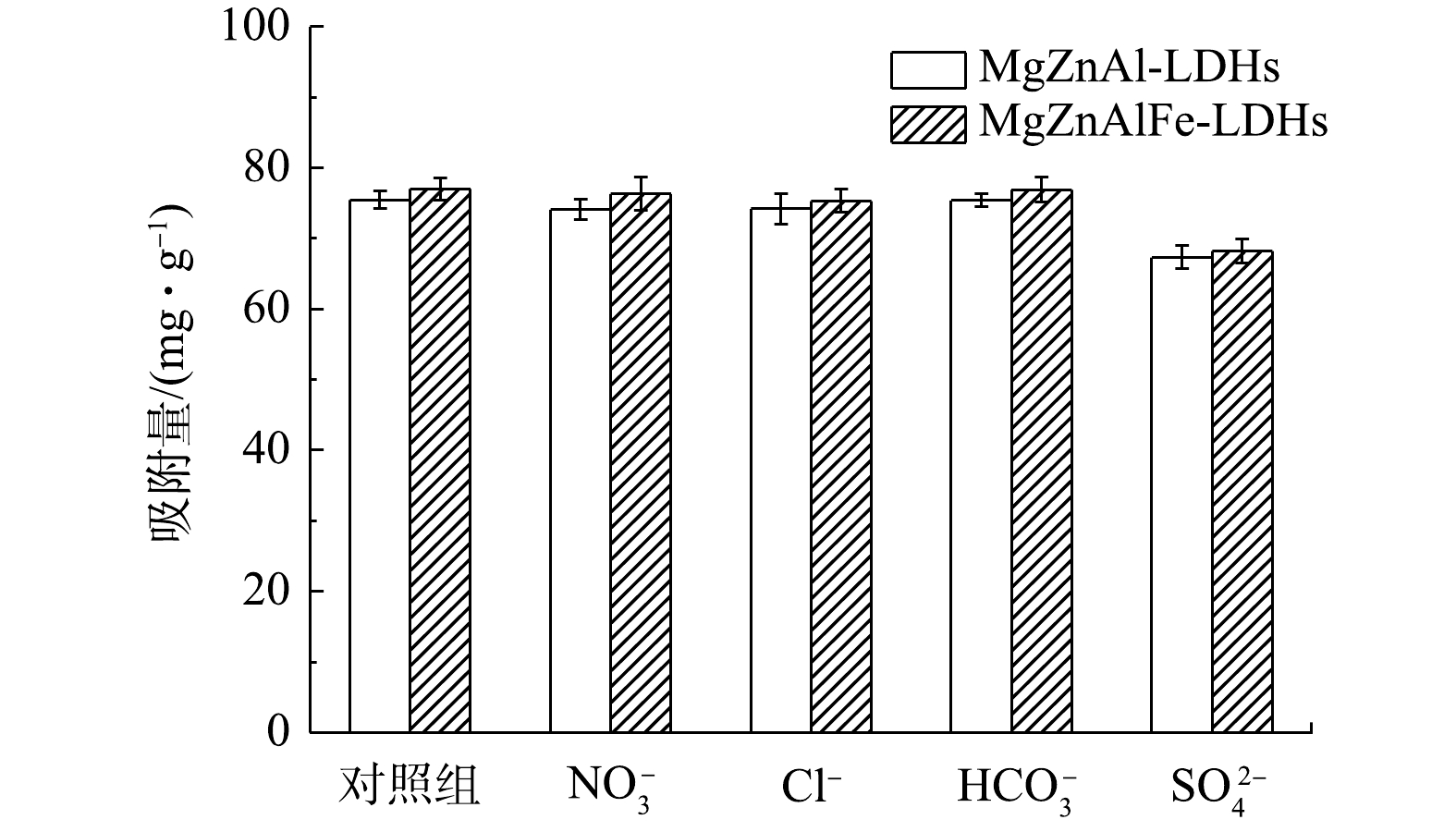
H2PO−4 HPO2−4 PO3−4 HPO2−4 PO3−4 H2PO−4 4)共存离子对吸附性能影响。图6为常见的阴离子对MgZnAl-LDHs和MgZnAlFe-LDHs吸附磷酸盐的影响。可以看出,
HCO−3 HCO−3 NO−3 SO2−4 NO−3 SO2−4 -
本实验通过设计软件 Design-Expert 12进行响应面分析实验设计及分析,采用Box-Behnken (BBD)方法,实验设计见表3。由表3可得,MgZnAlFe-LDHs响应面编码形式二次回归方程如式(8)所示。
由式(8)可以看出,pH、反应温度以及初始质量浓度这3个影响因子对于磷酸盐的吸附性能的影响不是简单的线性关系,而是交互影响的关系,因此,简单的单因素的影响分析会对结果造成误差。表4为对MgZnAlFe-LDHs二次模型的方差分析(ANONA)。由表4可知,在对MgZnAlFe-LDHs的响应面分析实验中,模型F值为74.07,P<0.000 1,说明回归模型拟合是显著的[24];模型失拟项P=0.060 9>0.05,说明失拟项不显著,无失拟因素存在;模型的校正决定系数
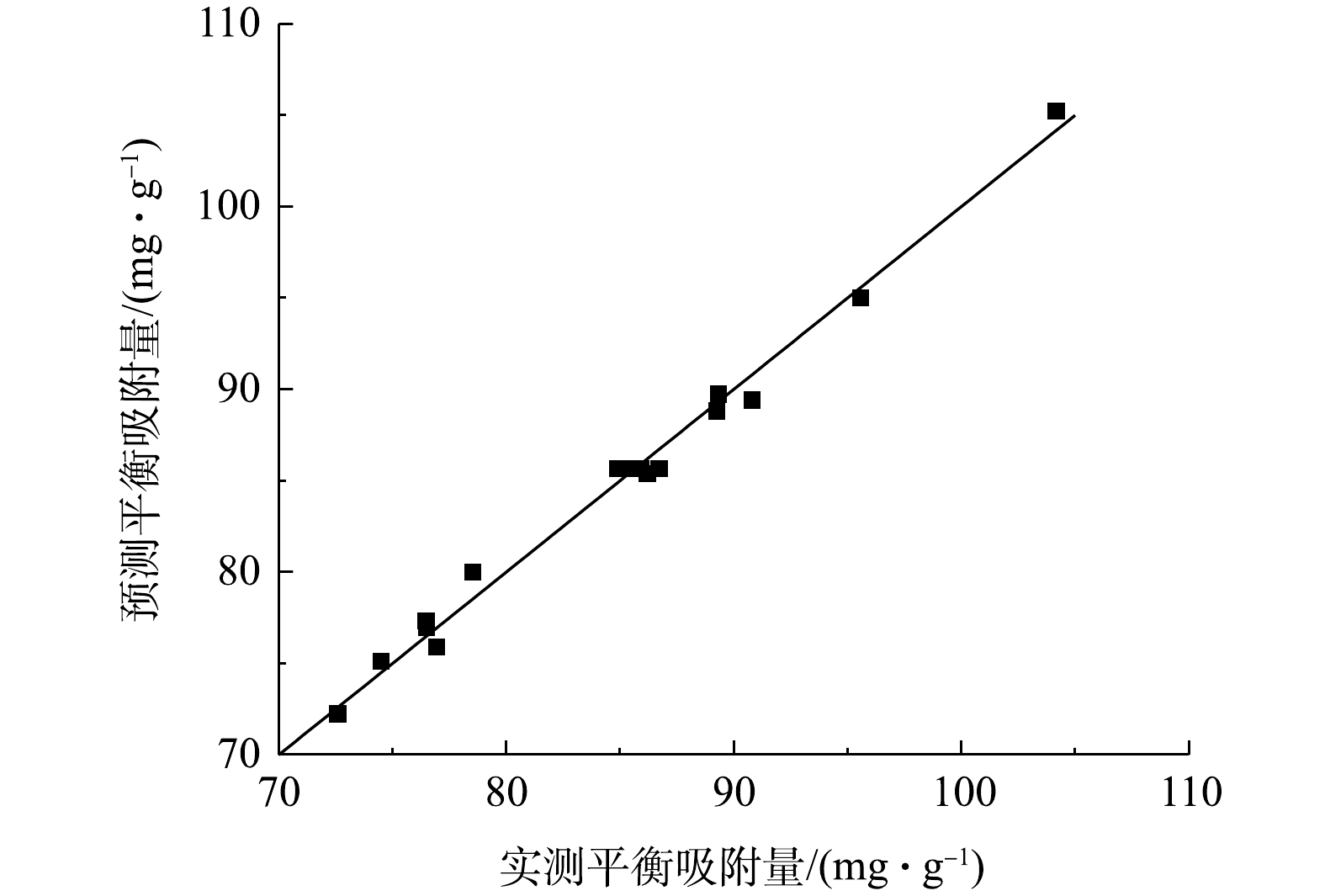
R2adj=0.9962 由表4可知,pH和初始质量浓度的F值分别为142.33、440.23,P <0.000 1,表明pH和初始质量浓度对响应值的影响为显著,影响因子中温度的F值为1.84,P=0.216 6>0.05,表明温度对响应值的影响不显著;在交互项中,pH与初始质量浓度的交互项以及温度与初始质量浓度的交互项对响应值影响均为显著(P<0.05)。图7为平衡吸附量预测值与实测值对比。可以看出,直线斜率接近于1,说明该模型预测结果较好。
响应面图可以反映出3个因素交互作用对响应值的影响[26]。图8为MgZnAlFe-LDHs吸附磷酸盐过程中各因素的交互作用。当初始质量浓度在中心值(100 mg·L−1)时(图8(a)),响应曲面坡度较缓,pH与温度对平衡吸附量的交互作用不显著,平衡吸附量随着温度的增加呈先增大后较小趋势,随着pH的增大呈减小趋势;当温度在中心值(30 ℃)时(图8(b)),pH与初始质量浓度对平衡吸附量的交互作用显著,响应曲面坡度较大,平衡吸附量随着初始质量浓度的增加而增大,随着pH的增加而减小;当pH在中心值(pH=3)时(图8(c)),温度与初始质量浓度对平衡吸附量的交互作用显著,从响应曲面可以看出,响应曲面坡度较大,平衡吸附量随着初始质量浓度的增加而增大,随着温度的增加而呈先增大后减小的趋势。
通过模型拟合可知,最佳平衡吸附量的条件为:pH为2,反应温度为30 ℃,初始质量浓度为120 mg·L−1,此条件下平衡吸附量为104.18 mg·g−1,与预测值105.23 mg·g−1基本一致,说明该模型能够用来预测吸附效果,对实际应用于酸性高磷废水的吸附中有一定的指导作用。
-
1) MgZnAlFe-LDHs较MgZnAl-LDHs在结构上层间距增大,孔隙增多,吸附位点增加,更有利于磷酸盐的吸附。
2) MgZnAl-LDHs和MgZnAlFe-LDHs符合Sips等温吸附模型,最大拟合吸附量分别可达172.00 mg·g−1和189.62 mg·g−1,可见MgZnAlFe-LDHs较MgZnAl-LDHs对磷酸盐的吸附量有所提高。MgZnAl-LDHs和MgZnAlFe-LDHs对磷酸盐的吸附动力学拟合符合准二级动力学吸附模型及Elovich模型,以化学吸附为主,且MgZnAlFe-LDHs对磷酸盐的吸附速率大于MgZnAl-LDHs的吸附速率。
3)通过Box-Behnken响应面分析法建立的回归模型显著,失拟项不明显,99.62%以上的响应值可以用模型解释,说明模型较为准确可靠,可以用于磷酸盐吸附条件优化。








 下载:
下载: