-
砷(As)是一种广泛分布在水体、土壤和岩石等中的有毒致癌物质. 高砷地下水是指As浓度大于10 µg·L−1的地下水(世界卫生组织(WHO)规定的饮用水标准)[1],长期饮用高砷地下水会导致慢性砷中毒,严重威胁人体健康. 目前,高砷地下水广泛分布在世界各地,超过1.5亿人的饮水安全受到了威胁[2],据Rodriguez-Lado等的统计风险预测模型,中国受高砷地下水影响的人口约1960万[3]. 高砷地下水多是原生自然成因造成的,不同区域的原生高砷水成因存在一定差异.
微生物参与铁氧化物的还原性溶解被认为是高砷地下水形成的关键过程[4-5],在此过程中,溶解性有机碳(DOC)作为微生物代谢活动的主要碳源和能量来源,在一定程度上影响着元素的氧化还原反应和迁移转化[6-10]. DOC的同位素δ13CDOC可指示地下水中有机碳的来源,并反应微生物代谢活动. 溶解性无机碳(DIC)是微生物作用下有机质降解的重要产物,其稳定同位素δ13CDIC可用于判断地下水DIC的来源,揭示地下水中微生物对有机质的降解过程. 碳同位素在高砷地下水中主要用于地下水有机质来源的判别和有机质的微生物代谢指示两方面[11]. 因此,利用地下水稳定碳同位素表征微生物作用下有机质降解过程及其对砷富集的影响具有一定指示意义. 例如,周殷竹对河套盆地[12]和Guo等[13]对松嫩盆地的高砷地下水中δ13CDIC和δ13CDOC特征研究表明,铁氧化物还原性溶解过程中均有微生物参与并伴随着DOC的氧化分解共同导致地下水中砷的迁移和富集.
新疆奎屯地区是中国西北干旱区典型原生高砷水分布区,高砷地下水多分布在深层承压水层,同其他地区高砷地下水埋深在潜水层、浅层承压水层不同. 前期研究表明[14-16],该地区地下水多为碱性和还原性环境,铁氧化物矿物的还原性溶解是高砷地下水形成的主要机制,但微生物在该成因机制中起到的作用还不清楚. 因此,本研究以奎屯地区深层承压地下水为研究对象、地表水为对照并结合地下水水化学特征和稳定碳同位素分析,旨在查明研究区高砷地下水中微生物作用下有机质降解过程对砷富集的影响,进一步加深对新疆奎屯原生高砷地下水成因机制的认识,为地下水的保护及有效利用提供理论指导.
-
奎屯地区位于新疆天山山坡中段和准噶尔盆地西南部的奎屯河流域,深处于亚欧大陆内部,属于温带大陆性干旱荒漠气候,多年平均气温(7.3 ℃)较低,年平均降水量为165 mm,而蒸发量高达2080 mm,蒸发量远大于降水量. 奎屯河流域的地质范围从南部山区的古生代岩层延伸至南盆地中更新统的冰水沉积层,再到第四系松散沉积层的平原区[17]. 平原区地下水沉积物厚度在800—1400 m之间,含水层结构由单一的卵砂砾石潜水层逐渐转变为以黄灰色粉质黏土夹薄层砂、青灰色的砂和砂砾石、浅黄的粉细砂夹粘性土为主的多层承压水结构[18]. 南部山区以卵砾石区为主,以侏罗系、第三系与平原第四系接触,颗粒粒径大,平均厚度约为26 m. 地下水径流方向自南向北由上游山区流向下游平原区[19]. 地下水由单一结构潜水层过渡到多层结构潜水—承压水层,且水位埋深呈逐渐增加的趋势. 研究区地下水集中在深层承压水层,砷浓度分布极不均匀.
-
根据前期研究,奎屯地区126团和128团地下水中As浓度含量较高[20-21],本研究于2019年8月对奎屯河流域地表水(2组)和地下水(15组)共17组水样进行采集分析(如图1). 地表水采自距奎屯河源头流出后约3 km的位置,地下水水样中6组采集于126团,其余9组采集于128团(表1). 采集水样前清洗井孔,用清澈地下水润洗采样瓶3次后再采集水样. 地表水和地下水采样封存后分别用K(1—2)和C(1—15)进行标记分类.
用于阳离子分析(常量元素和微量元素)和总As测定的水样用浓硝酸(优级纯)将其酸化至pH<2并避光保存;阴离子、DIC和DOC分析的水样过滤后直接分装保存;无机碳及有机碳稳定同位素测试的样品分别加入HgCl2饱和溶液灭菌处理和浓磷酸(优级纯)酸化至pH<2密封保存[22]. 所有采集水样的样品瓶中不留气泡,并在低温4 ℃条件下冷藏保存. 同时现场记录采样点经纬度和井深,现场使用多参数便携式仪器(HI 8424,HANNA)测定水温、pH和Eh.
-
Na+和K+用火焰光度法测定;Ca2+和Mg2+采用EDTA间接络合滴定法测定;HCO3−和CO32−用双指示剂-中和滴定法测定;SO42−采用BaCl2滴定法测定;Cl−用硝酸银滴定法测定;Fe用TAS-990原子吸收分光光度计测定;总As用PF3-原子荧光光度计(北京普析)测定(标准曲线R2=0.999),仪器参数为温度200 ℃,载气气压为0.25—0.3 MPa.
DIC和DOC采用总有机碳分析仪1030(美国)测定,碳稳定同位素使用稳定同位素质谱仪(MAT 253)进行测定,测定工作由上海复昕化工技术服务有限公司完成. DIC碳稳定同位素测定方法采用准确度较高的气体逸出法. 首先,加入0.5 mL 85%H3PO4到进样瓶,用高纯氩气吹扫1 h去除CO2,再用1 mL注射器取0.8 mL样品注入进样瓶,然后进行60 ℃水浴加热1 h充分反应生成CO2,测定顶部CO2气体的无机13C. DOC稳定同位素测定采用湿法氧化法,首先将进样瓶使用马弗炉500 ℃燃烧5 h,冷却后加入0.5 mL水样,取50 µL 0.1 mol·L−1 AgNO3(催化剂)和0.5 mL 85%H3PO4加入进样瓶盖紧,用高纯氦气吹扫进样瓶1 h. 同时60 ℃水浴加热1 h,将吹扫气排除,以去除瓶中的残留气体,之后加入1 mL氧化剂,并在100 ℃水浴加热1 h,使DOC充分反应,测定进样瓶顶部CO2气体的有机13C.
DIC和DOC同位素测试精度可达0.04‰. DOC稳定同位素样品的标准样品采用美国国家标准技术研究所(NIST)认证的同位素标准物质USGS40(左旋谷氨酸,真值有机13C=−26.39‰±0.09‰)和USGS41(左旋谷氨酸,真值有机13C=+37.63‰±0.1‰)对未知样品进行较正,测试采用标准标准物质线性校正方法对测量值进行较正,每3至5个样品后分别加入所选的两种标准物质,选取有机碳13C值相差较大的两个标准物质,在相同参考条件下,将所选标准物质和待测样品采用相同的预处理流程处理,对其同位素比值进行测定,最终将标准物质的测量值与真值进行对比校正,根据线性回归,对样品的测量值进行校正.
-
采用ArcMap 10.7绘制研究区及采样点分布图;SPSS 25 进行数据统计和分析;Origin 2021 绘制散点图和箱线图.
-
由水样主要水化学指标统计表(表2)可知,研究区地表水pH值呈中性和氧化性环境;地下水的pH范围介于7.59—9.42之间,均值为8.63,整体呈弱碱性-碱性;Eh范围为−96—−7.5 mV,均值为−55.08 mV,地下水均处于还原性环境.
地下水中优势阳离子为Ca2+,其次为Mg2+和Na+,K+含量较低,阳离子的变异系数均大于1,说明地下水中阳离子浓度变化范围较大;阴离子Cl−含量占比最大,其次为SO42−和HCO3−,CO32−浓度最低,其中Cl−变异系数大于1,属于强变异. 地下水HCO3−质量浓度为49.44—125.52 mg·L−1,平均值为72.06 mg·L−1,地下水的HCO3−质量浓度小于地表水. 地下水中HCO3−和砷酸根离子均会吸附在铁氧化物矿物表面,矿物表面有限的吸附位置会使两种离子发生竞争吸附作用,当HCO3−形成碳酸盐复合物吸附在矿物表面时,As就会被释放到地下水中,导致地下水中As含量增加,HCO3−浓度也会降低[23],其次河流水体与大气CO2的交换作用也会使地表水HCO3−质量浓度高于地下水.
地表水As浓度均低于10 µg·L−1,为低砷水. 地下水As含量范围在2.45—460.38 µg·L−1之间,平均值为60.60 µg·L−1,73%的地下水As浓度大于10 µg·L−1,为高砷水. 126团地下水采样点As浓度范围在3.89—460.38 µg·L−1之间,平均值为120.81 µg·L−1,6组地下水样品中4组为高砷水;128团地下水采样点As浓度范围在2.45—48.77 µg·L−1之间,平均值为20.47 µg·L−1,9组地下水样品中7组为高砷水,2个团场高砷地下水检出率均较高. 整体看来,126团地下水样点As含量高于128团. 126团位于整个奎屯河流域地下水排泄区,径流条件更弱,更有利于地下水As的富集. 地下水中As的变异系数为1.83,大于1,属于强变异,表明该区域地下水中As的浓度变化较大. 奎屯高砷地下水主要分布在深层承压含水层中[14],本研究中约82%的高砷地下水分布在100 m以上的深层承压水中,与大同盆地(19—100 m)、河套平原(15—80 m)和江汉平原(15—40 m)的3个地区高砷地下水埋深分布在潜水、浅层承压水[10,24-25]有明显差异,不同采样点同一井深的地下水砷浓度可能相差很大. 这一原因主要是研究区地下水位埋深由南部山区到北部平原区呈现逐渐增加的趋势,由单一结构潜水层过渡到多层结构潜水—承压水层,即该地区奎屯河上游、中游和下游同一井深的地下水,赋存的含水层可能不同,不同含水层的地下水砷浓度变化较大.
-
地表水和地下水中DIC和DOC含量如图2所示,地表水和地下水DIC浓度均大于DOC浓度,地下水DIC和DOC浓度大多高于地表水. 地表水DIC的浓度范围为12.16—15.99 mg·L−1,平均值为14.08 mg·L−1,DOC的浓度范围在1.26—2.56 mg·L−1之间,平均值为1.91 mg·L−1;地下水的DIC浓度范围为10.84—45.28 mg·L−1,平均浓度为23.39 mg·L−1,DOC的浓度相比DIC较低,范围介于0.73—6.25 mg·L−1之间,均值为2.55 mg·L−1.
地表水DIC主要来源包括土壤中CO2、岩石风化溶解作用、水体与大气CO2的交换作用、大气降水的直接输入以及水中动植物的呼吸作用等[26];地下水DIC主要来源于微生物作用下有机质的代谢分解活动、空气中CO2的补偿以及碳酸盐矿物的溶解[27-30]. 前人研究表明,当[HCO3−]/[Ca2++Mg2+]≥2时,认为水体中的HCO3−主要来自碳酸盐岩的风化作用,当[HCO3−]/[Ca2++Mg2+]<2时,则水体的HCO3−存在多个潜在来源[31]. 在本研究中,根据所测得的离子数据计算出地表水[HCO3−]/[Ca2++Mg2+]的值均大于2,说明地表水中DIC主要来自碳酸盐岩风化作用的影响;地下水[HCO3−]/[Ca2++Mg2+]的值约60%小于2,表明地下水DIC受多种来源的共同影响. 地表水DOC值可反应水体的污染程度与人类活动对流域地表水体的影响[32],全球天然水体DOC平均含量为5 mg·L−1左右[33],若因人类生活污水和废水汇入,地表水DOC浓度会大于5 mg·L−1. 本研究地表水DOC的浓度范围在1.26—2.56 mg·L−1之间(图2),说明地表水并未受人为活动污染的影响.
-
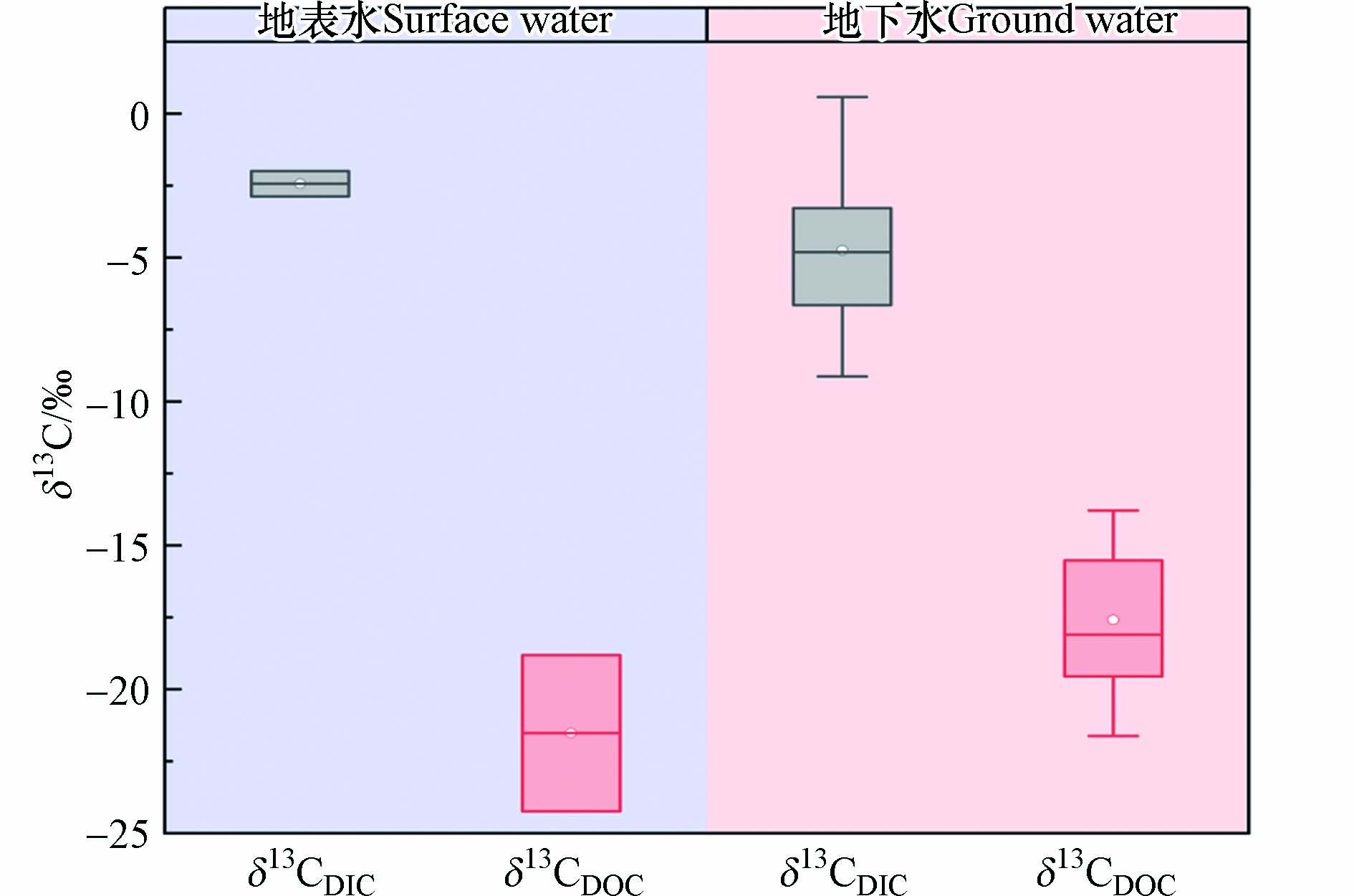
由地表水和地下水中δ13CDIC和δ13CDOC关系图(图3)可知,研究区地表水δ13CDIC值范围为−2.88‰—−1.99‰(平均值为−2.44‰);地下水δ13CDIC值范围介于−9.13‰—0.58‰之间,平均值为−4.74‰. 与地表水相比,地下水中12个样点(80%)的δ13CDIC值偏负于−2.88‰,范围介于−9.13‰—−3.28‰之间,1个样点的δ13CDIC值大于−1.99‰,为0.58‰,接近0,另外2个样点的δ13CDIC值位于地表水δ13CDIC值范围内. 不同来源的DIC,其碳同位素具有不同的特征范围. 来源于碳酸盐岩溶解的DIC具有较大的δ13C值,而含水层中有机质的微生物降解过程,优先趋向利用较轻的12C,从而使产物中富集较轻的12C并导致13C发生分馏,其反应物中富集较大的13C,因此微生物对有机质的降解作用相对碳酸盐岩溶解的δ13CDIC值更偏负. 相关研究已证实有机质的生物降解过程会使δ13CDIC值负向移动[34],与地表水主要来源于碳酸盐岩溶解的DIC同位素δ13CDIC值范围相比,地下水有80%的δ13CDIC值更贫化,说明地下水DIC来源除受碳酸盐岩溶解的影响外,还存在微生物对有机质的降解作用. 微生物分解有机质释放的DIC,其δ13C值范围为−25‰—−18‰[35],而研究区地下水δ13CDIC值范围同微生物对有机质降解产生的δ13CDIC值范围相比偏正. 一方面,该区域地下水HCO3−受到含水层碳酸盐岩溶解的影响[36],会导致δ13CDIC值偏正;另外,已有研究表明在地下水缺氧的强还原环境中,产甲烷过程会使有机碳降解产生的CO2中富集13C,继而产生更多的DIC,所以产甲烷过程导致的碳同位素分馏所生成的DIC的δ13CDIC值会更偏正[37],研究区地下水氧化还原点位均小于0,深层承压水的还原缺氧环境,为产甲烷过程提供了有利条件,因此,研究区地下水中微生物作用下有机质降解产生的无机碳δ13C值不仅受到碳酸盐岩溶解的影响,还可能存在产甲烷的过程使δ13CDIC值偏正.
研究区地表水δ13CDOC值范围为−24.24‰—−18.81‰(平均值为−21.53‰),地下水δ13CDOC值范围介于−21.62‰—−13.79‰之间,平均值为−17.59‰,地表水的δ13CDOC值与地下水相比更贫化(图3). 地质来源碳和微生物活动产生的内源碳是地下水中DOC的主要碳源,此外,还存在从地表水通过地下径流过程进入到地下水的外源有机碳[25]. 不同碳源的DOC,其碳同位素具有不同的特征. C3植物(如树木、小麦、棉花等)的δ13CDOC值范围在−35‰—−20‰之间,C4植物(如玉米、高粱和甘蔗等)的δ13CDOC值介于−19‰—−8‰之间[34,38],景天酸代谢(CAM)植物的δ13CDOC值范围为−22‰—−10‰[39],CAM植物的同位素组成通常为中间值分布在C3和C4植物δ13CDOC值范围内. 土壤腐殖质中的δ13C值与该区域的植被类型有关,浅层地下水的DOC会受到人为活动和地表径流携带土壤有机质的影响. 奎屯地区经历多次地质运动中,垂直升降过程使得地表植被形成变迁,并在第四纪时期一直处于沉积地带的中心区域,形成了以泥质、黏土质和腐殖质为主的深厚沉积层地质条件[14,40],长期以微生物为媒介得生物地球化学过程演化成如今地下水中的沉积物. 地下水中δ13CDOC值分布于C3植物、C4植物和CAM植物的δ13CDOC值范围之间,埋深在浅层的地下水会受到地表入渗携带土壤有机质的影响,奎屯地区高砷地下水主要分布在100—200 m左右的深层承压水,相对封闭的水文地质条件使承压水受外源有机碳的影响可能性很小,因此,影响地下水δ13CDOC值大小的因素主要取决于地质条件造成地下水中沉积物富含的内源有机质,和微生物利用沉积物中有机质产生的内源碳以及通过地下径流汇入到浅层地下水的外源有机碳.
-
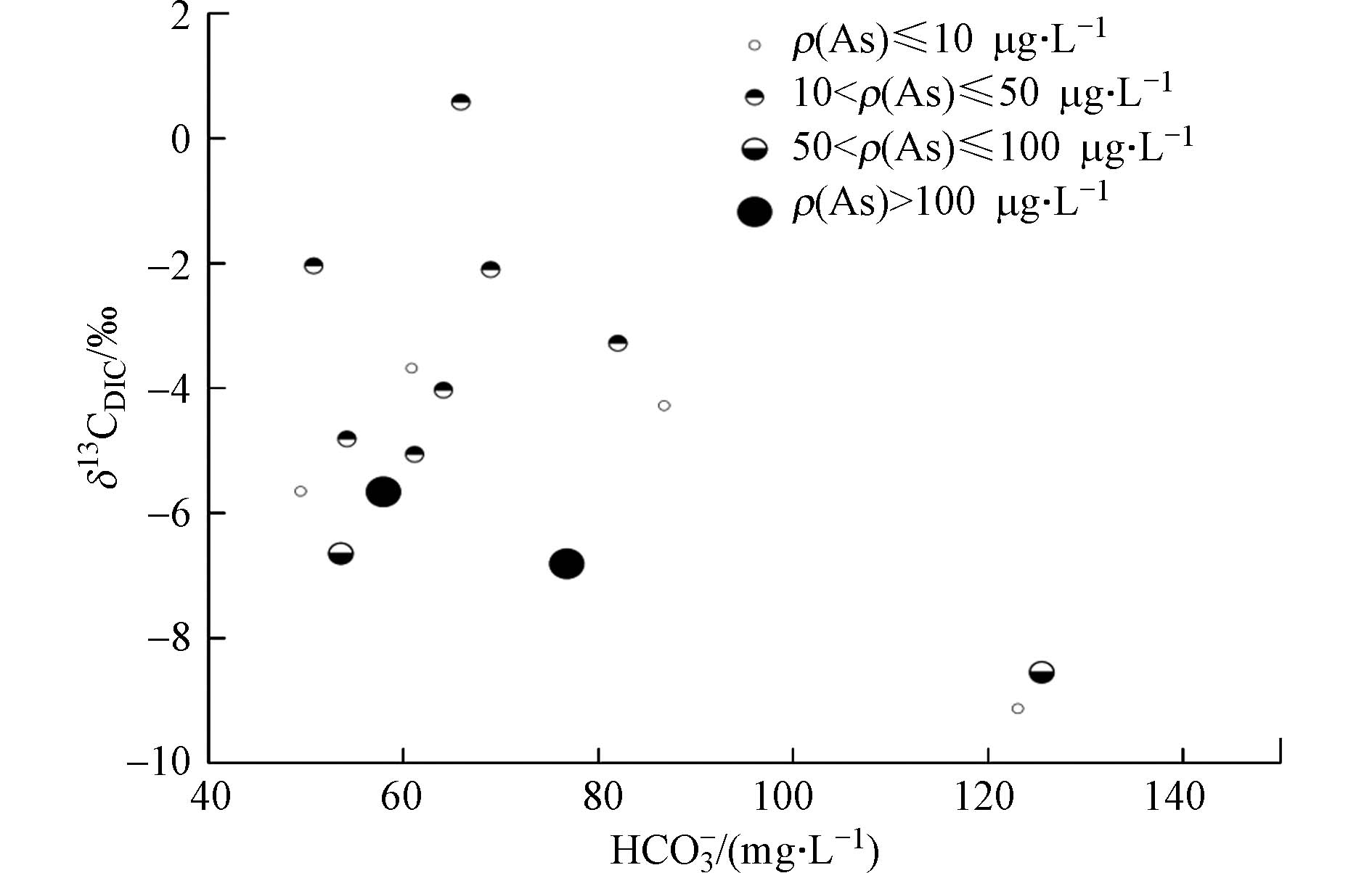
由地下水δ13CDIC值与ρ(HCO3−)呈显著负相关性(r=−0.541,P=0.037)的关系可知,δ13CDIC值越偏负,微生物活动越强,ρ(HCO3−)的浓度越高,说明微生物作用下有机质降解产生的HCO3−是地下水中DIC的重要来源之一. 由地下水δ13CDIC值与HCO3−关系图(图4)可以看出,高砷水主要分布在左侧区域,整体看来,砷浓度越高,δ13CDIC值越贫化,表示微生物作用下的有机质降解对地下水中As的富集具有重要意义.
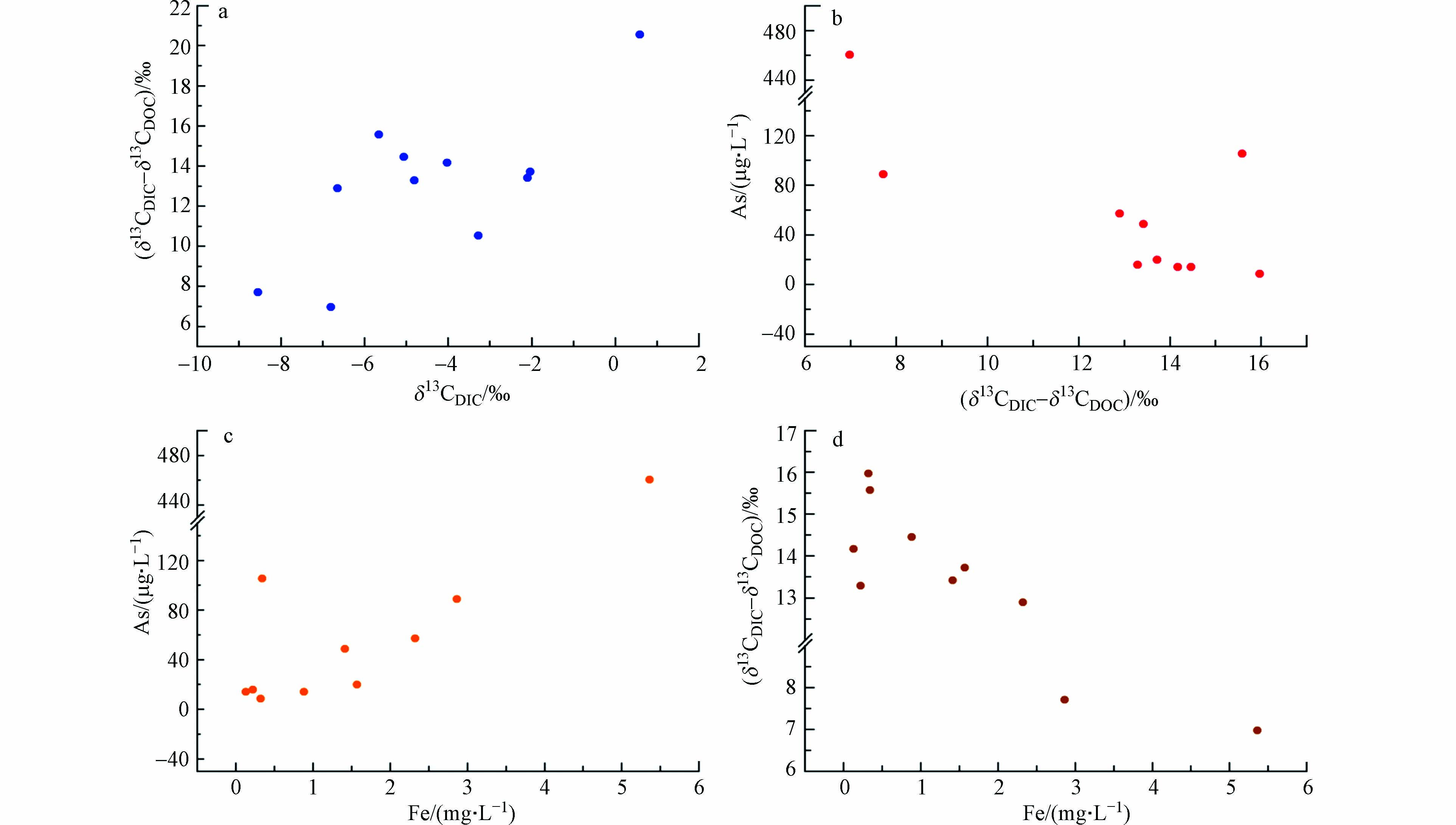
研究区高砷地下水中δ13CDIC-δ13CDOC差值与δ13CDIC具有极显著正相关关系(r=0.729,P=0.013)(图5a),表明在δ13CDIC不断贫化过程中,DOC的氧化分解起一定作用. 当δ13CDIC-δ13CDOC值较大时,说明碳酸盐岩的溶解是DIC的主要来源;相反如果δ13CDIC-δ13CDOC值越小,则表明无机碳多来源于有机物的氧化分解越多,微生物活动越强烈. 由地下水中As含量可知,高砷水井深主要集中在100—200 m范围内,因此选取地下水(井深≥100 m)分析稳定碳同位素对砷富集的影响. 地下水(井深≥100 m)中As浓度与δ13CDIC-δ13CDOC的差值呈显著负相关关系(r=−0.726,P=0.017),随着砷浓度逐渐升高,δ13CDIC-δ13CDOC差值呈降低趋势(图5b),即砷浓度越高,δ13CDIC值越贫化,微生物活动越强烈,说明微生物对有机质的降解促进了地下水中As的富集.
研究区地下水所处的环境为还原性-弱碱性,地下水(井深≥100 m)中As与Fe具有极显著正相关关系(r=0.858,P=0.001)(图5c),随着地下水中Fe的浓度升高,As浓度也逐渐增加,说明在强还原环境下,铁氧化物表面高价态迁移性较差的Fe(Ⅲ)还原为溶解态和迁移性较强的Fe(Ⅱ),进而吸附在Fe(Ⅲ)上的砷被释放,使地下水中砷含量增加,这和前人的研究[14,21,23,41]一致. 地下水(井深≥100 m)中δ13CDIC-δ13CDOC的差值与Fe的浓度呈极显著负相关关系(r=−0.887,P=0.001)(图5d),结合图5(b、c),随着δ13CDIC-δ13CDOC差值的减小,Fe浓度越高且As的浓度也逐渐升高,说明微生物活动参与了含水层中铁氧化物的还原及砷的释放这一过程. 在这一生物地球化学过程中,溶解性有机碳和沉积物中有机质为微生物的代谢活动提供主要碳源和能量来源,有机碳在微生物的作用下被分解为无机碳形成碳的转化和分馏. 当微生物可利用的碳源增加时,可促进异养微生物的代谢,并消耗氧气,形成更有利于地下水As富集的还原环境.
我国北方典型高砷地下水分布区和南方典型高砷地下水分布区的地下水DIC与DOC同位素δ13C值、As和Fe质量浓度范围及埋深见表3. 研究区地下水中δ13CDIC值范围介于−9.13‰—0.58‰之间,整体变化范围同河套平原δ13CDIC值较接近,而比大同盆地和江汉平原更富集13C,最大值(0.58‰)和其他3个地区相比较正. 已有研究表明,在含水层中有丰富的有机质来源,微生物活动强烈,当O2、NO3−、Fe3+、SO42−等电子受体消耗殆尽时可能会进入到产甲烷阶段,该过程中发生明显的碳同位素分馏[42],地下水中的各项反应共同影响着体系内的无机碳和δ13C值的组成,因此,可能会导致砷、铁质量浓度较高的地下水中碳同位素δ13CDIC值更大. 铁氧化物矿物的还原性溶解均是这4个典型高砷水分布区砷释放的重要成因,微生物在此过程中发挥着重要作用. 其他3个地区地下水中均存在微生物对有机质的降解作用使δ13CDIC值偏负,新疆奎屯地区除了微生物对有机质降解作用和碳酸盐岩的溶解会影响外,还可能存在含水层相对封闭的水文地质条件下的产甲烷过程对δ13CDIC值的影响. 研究区地下水中δ13CDOC值范围为−21.62‰—−13.79‰,同河套平原(−22.9‰—−19.20‰)和江汉平原(−28.5‰—−19.60‰)相比偏正. 在强还原环境地下水中,微生物对有机质作用较强时,微生物优先利用更多的12C转化到降解产物DIC中,使得有机碳中更富集13C,推测新疆奎屯地区地下水中微生物活动较强.
-
(1)地下水中As浓度分布不均匀,平均值为60.60 µg·L−1,73%的地下水为高砷水,处于还原-弱碱性环境. 地下水中优势阴阳离子分别为Cl−和Ca2+. 地表水As浓度均为低于10 μg·L−1的低砷水,处于中性和氧化环境.
(2)地下水DIC浓度范围为10.84—45.28 mg·L−1,DOC浓度范围介于0.73—6.25 mg·L−1之间. 地下水DIC受多种来源的共同影响,地表水DIC主要来自碳酸盐岩风化作用的影响.
(3)地下水δ13CDIC值的范围在−9.13‰—0.58‰之间,80%的δ13CDIC值比地表水更贫化,δ13CDOC值的范围为−21.62‰—−13.79‰. 地下水中除了微生物作用下有机质降解,还存在碳酸盐岩溶解影响δ13CDIC值.
(4)地下水δ13CDIC-δ13CDOC差值与δ13CDIC呈正相关关系,有机碳的氧化分解对无机碳稳定同位素贫化过程起一定作用. 地下水中δ13CDIC-δ13CDOC差值与ρ(As)、ρ(Fe)均呈显著负相关关系,微生物参与了铁氧化物的还原性溶解并促进了As的富集.
新疆奎屯地区高砷地下水稳定碳同位素特征及其指示意义
Stable carbon isotope signatures of high arsenic groundwater and their indicative significancein in Kuitun area of Xinjiang
-
摘要: 地下水稳定碳同位素可以指示微生物作用下有机质降解过程对砷富集的影响. 新疆奎屯地区是中国西北干旱区典型原生高砷水分布区,本研究以地下水为研究对象,奎屯河地表水为对照,通过野外采样,并借助原子荧光、稳定同位素分析等技术手段,对地下水的水化学指标、溶解性无机碳(DIC)、溶解性有机碳(DOC)和碳稳定同位素进行测定与分析. 结果表明,研究区73%的地下水为高砷水,平均值为60.60 μg·L−1,呈还原-弱碱性环境,地表水均为低砷水,呈中性和氧化环境. 地下水中优势阴阳离子分别为Cl−和Ca2+. 地下水DIC受多种来源的共同影响,地表水DIC主要来自碳酸盐岩风化作用的影响. 地下水δ13CDIC值的范围为−9.13‰—0.58‰,δ13CDOC值的范围在−21.62‰ — −13.79‰之间. 地下水中除了微生物作用下有机质降解和碳酸盐岩溶解的影响外,还可能存在产甲烷过程对δ13CDIC值的影响. 地下水中δ13CDIC-δ13CDOC差值与ρ(As)、ρ(Fe)均呈显著负相关关系,表明微生物参与了铁氧化物的还原性溶解并促进了As的富集.Abstract: The stable carbon isotope of groundwater can indicate the influence of organic matter degradation process under the action of microorganisms on arsenic enrichment. Kuitun area of Xinjiang is a typical primary high arsenic water distribution area in the arid region of northwest China. In this study, the groundwater was taken as the research object, and the surface water of Kuitun River was taken as the control. The hydrochemical indicators, dissolved inorganic carbon (DIC), dissolved organic carbon (DOC) and carbon stable isotope of the groundwater were determined and analyzed. The results show that 73% of groundwater in the study area was high arsenic water, with an average value of 60.60 μg·L−1, presenting a reduction-weak alkaline environment, while the surface water was low arsenic water, presenting a neutral and oxidizing environment. The dominant anions in the groundwater were Cl− and Ca2+, respectively. The DIC of the groundwater was commonly influenced by various sources, and the DIC of the surface water mainly came from the influence of carbonate weathering.The value of δ13CDIC ranged from −9.13‰ to 0.58‰ and the values of δ13CDOC ranged from −21.62‰ to −13.79‰ in the groundwater. In addition to the degradation of organic matter and the dissolution of carbonate karst under the action of microorganisms, methanogenesis may also affect the δ13CDIC value in the groundwater. There was a negative correlation between δ13CDIC—δ13CDOC and As concentration also between δ13CDIC—δ13CDOC and Fe concentration in the groundwater, indicating that microorganisms participated in the reductive dissolution of iron oxides and promoted the enrichment of As.
-
室内污染源/危险源的定位在提升室内空气品质、防控流行病疫情、处置危险气体泄漏和应对生化恐怖袭击等方面均能发挥重要作用[1-4]。迄今为止,研究者们针对室内通风环境中的源定位问题已经开展了大量研究[5]。然而,针对未通风或通风不良的室内弱气流环境中的源定位问题,除了多年前的个别探索,鲜有研究报道[6]。在实际应用中,室内弱气流环境对应的场景十分普遍,如在过渡季节室内未通风的场景,通风空调系统发生故障的场景,在事故和灾害中通风空调系统受损的场景以及受建筑结构或家具影响形成室内风影区的场景等。在上述场景中,由于通风量不足且缺乏主导气流的输运作用,污染物或危险物质更容易积聚并达到有害或危险浓度。现有研究的不足与实际应用需求之间的矛盾凸显了在室内弱气流环境下开展源定位研究的必要性。
目前,对室内污染源/危险源进行定位的方法主要分为固定传感器网络(SSN)方法和移动机器人嗅觉(MRO)方法。SSN方法通常利用传感器读数,通过正向或反向求解室内流场和污染物扩散的基本模型(如计算流体动力学(CFD)模型和多区模型)来定位室内污染源/危险源[7-9]。由于只有当污染物/危险物扩散到监测位置,传感器才能获得其浓度读数,SSN方法也被视作为被动式方法。迄今为止,尽管SSN方法在室内通风环境的源定位研究中已经有大量报道,但尚未见有此类方法应用在室内弱气流环境中进行源定位的研究报道。近年来,尽管SSN方法的研究已经取得了很大的进展,但该类方法仍存在需要提前布置传感器,边界条件难以确定,模型求解难度大等局限。另外,室内弱气流环境由于其特殊性,也对SSN方法的研究提出了一些新挑战。例如,由于缺少主导气流且受湍流主控,污染物扩散过程的建模和求解会更加困难。此外,污染物可能需要更长的时间才能扩散到传感器所在位置,因此,也难以对突发污染作出快速响应。
与SSN方法相比,因为移动机器人具有在空间中主动搜索的能力,MRO方法也被视作为主动式方法。此类方法通常是受动物的觅食、求偶和避敌等行为启发而发展而来,因而在方法中通常会体现出仿生学原理[10-12]。与SSN方法相比,MRO方法主要有以下3点优势:机器人通过主动搜索可以更快地探测到目标污染物;MRO方法通常不需要对复杂的室内污染物扩散过程进行建模和求解;机器人可以执行多重任务,如源头控制、疏散引导、医疗救助等。综上所述,针对室内弱气流环境中的源定位问题,本文开展基于MRO方法的研究。
现有的基于MRO方法的源定位研究主要针对有主导气流的室内通风环境[5,13-24]。相比之下,只有少数研究考虑了未通风或通风不良的室内弱气流环境[6,25-30]。与室内通风环境相比,室内弱气流环境对MRO方法的挑战主要有2点:没有主导气流信息可以指导机器人连续跟踪污染物烟羽;污染物的扩散受湍流的影响更大,其浓度的波动往往会更加剧烈和频繁,从而无法形成持续指向源的浓度梯度,并由此增加机器人溯源的难度。
针对室内弱气流环境的MRO方法溯源研究,根据使用机器人的数量可分为单机器人嗅觉方法和多机器人嗅觉方法。在早期研究中,单机器人嗅觉方法因其成本低、易于实现而受到青睐。LILIENTHAL团队[22]提出了Braitenberg-type方法,FERRI团队受飞蛾等生物启发提出了Spiral方法[25]。2个团队皆通过实验验证了其所提方法在室内弱气流环境中的有效性。从这2个团队的单机器人溯源实验来看,均采用二维溯源方式,即假设源高度已知,且机器人所携带的传感器也固定在源高度上。然而,在实际应用中还普遍存在源高度未知的场景,此时二维溯源能否适用则有待于验证。
为了进一步提升源定位的成功率和效率,研究者们尝试着用多机器人嗅觉方法来解决室内弱气流环境中的源定位问题。FERRI[30]提出了1种基于家蚕行为的多机器人嗅觉方法,通过模拟室内弱气流环境对该方法进行了测试,结果表明,该方法在成功率和效率方面明显优于单机器人嗅觉方法。在这项研究之后,FERRI[27]进一步提出了1种基于粒子群优化算法的多机器人嗅觉方法(EPSO),该方法进一步加强了机器人之间的协作。尽管上述研究取得了一定进展,但是这些研究均是基于模拟的污染物浓度场开展的仿真研究,因此,不可避免地存在以下局限:在真实的室内弱气流环境中,受湍流影响,污染物的浓度会呈现出剧烈和频繁的波动,这是难以通过时均化的数值模型模拟得出的;在仿真研究中也没有充分考虑传感器的实际特性,如响应/恢复时间和检测误差;在仿真研究中也很难体现机器人之间的碰撞以及机器人运动对流场的干扰。
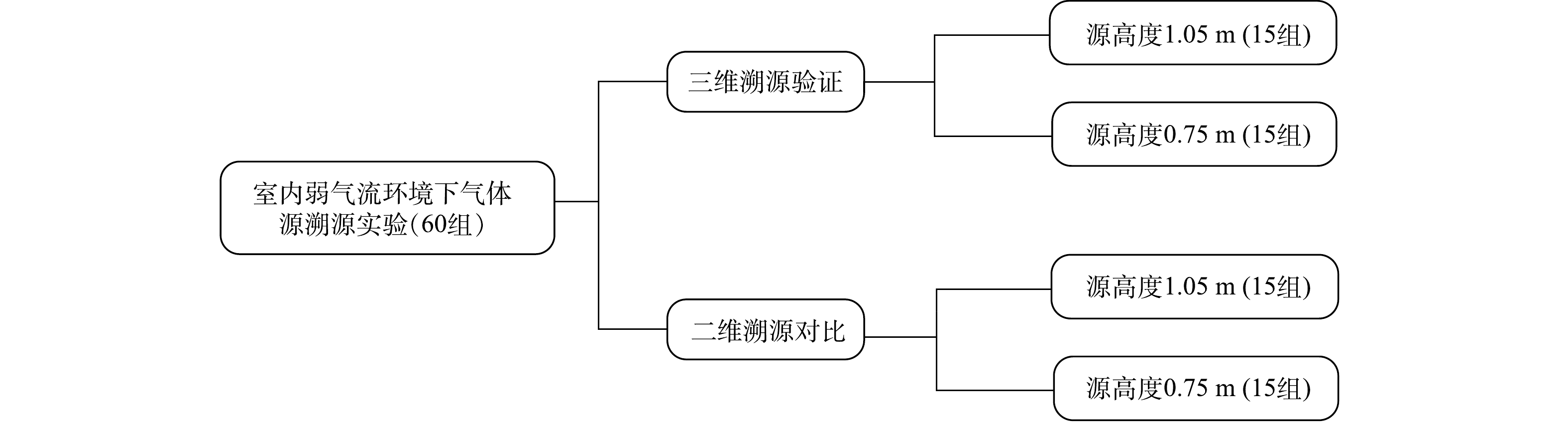
本研究的目标是在真实的室内弱气流环境下,利用基于标准粒子群算法(SPSO)的多机器人嗅觉方法(SPSO方法)来实现对源高度未知的气体污染物的溯源。虽然OSÓRIO[32]等建立了一种能够检测不同高度气味浓度和风向的机器人,但其机器人上仅是在垂直方向3个高度上携带了传感器,其传感器是固定不可受控移动的[32],而本研究中我们开发了多机器人三维溯源系统,该系统由3台传感器可以在高度方向上受控移动的三维溯源机器人组成,并且能够执行SPSO方法。在本研究中,设置了1.05 m和0.75 m 2种源高度,并在每种源高度下均开展了15组三维和二维溯源(传感器高度为1.05 m)实验,以验证三维溯源的有效性,并对比三维溯源和二维溯源的性能。
1. 方法原理
1.1 源定位流程
如图1所示,多机器人在源定位过程中包括3个阶段:烟羽发现、烟羽跟踪和源确认阶段。烟羽发现是源定位的开始,在此阶段机器人通过烟羽发现算法以相同的速度向各个方向发散,直到其中某个机器人检测到目标气体浓度高于烟羽发现预设浓度阈值Cmin,则所有机器人进入烟羽跟踪阶段;在烟羽跟踪阶段,机器人结合烟羽跟踪算法和获得的传感器信息去规划路径,从而接近污染源。烟羽跟踪阶段根据功能还可细分为烟羽跟踪和烟羽再发现,当机器人在跟踪烟羽的过程中丢失烟羽时,便可根据烟羽再发现重新寻回烟羽;在源确认阶段,机器人利用源确认算法判断是否到达源附近,或是陷入了局部浓度极值区域(源不在其中但浓度比周围高的区域)。如果陷入了局部浓度极值区域,则需要利用烟羽发现算法逃离,机器人逃离出局部浓度极值区后,则切换到烟羽跟踪阶段来重新寻找源。在这3个阶段中,每台机器人行进一步后,均要停留一段时间来采集浓度信息,信息采集完成后机器人会共享各自的位置和浓度信息,并根据源定位方法计算出各自下一步的目标位置。
1.2 源定位方法
本研究采用的SPSO方法主要包括3个核心算法,即烟羽发现算法、烟羽跟踪算法、源确认算法。此外,在现实的应用场景中进行多机器人源定位研究时,需考虑机器人本身以及周围障碍物的存在,所以在源定位过程中还加入了1种已知障碍物的机器人避障算法[28]。
1)烟羽发现算法。本研究所采用的烟羽发现算法为1种简单的发散搜索策略[33],通过多台机器人以相同速度向不同方向并行直线运动的形式快速捕获实验场地里目标气体的烟羽。在烟羽发现过程中,如果机器人碰到场地边界,则根据反射定律[34]改变移动轨迹。当机器人检测到的气体浓度超过Cmin,则切换到烟羽跟踪模式。
2)烟羽跟踪算法。为了进一步理解烟羽跟踪算法的实现,需要引入2个重要的概念,即全局最优值和全局最优位置。全局最优值C*(t)为到当前时刻t,机器人群检测到的最大浓度;全局最优位置
P∗g(t) 本研究所采用的烟羽跟踪算法是标准粒子群算法(SPSO),该算法是1种模仿鸟群、鱼群觅食行为发展起来的1种进化算法。该算法易于编程实现、运行效率高、参数相对较少,在源定位领域中得到了广泛的应用[5,15,27,31,35]。SPSO算法一般使用第i个机器人
Ri(i=1,2,3,⋯,N) Vi(t+1)=wVi(t)+l1r1(P∗i(t)−Pi(t))+l2r2(P∗g(t)−Pi(t)) (1) 式中:Vi(t+1)为Ri在t+1时刻的速度向量;
wVi(t) Vi(t) l1r1(P∗i(t)−Pi(t)) P∗i(t) C∗i(t) l2r2(P∗g(t)−Pi(t)) P∗g(t) Ri的位置更新如式(2)所示。机器人自身的局部最优位置更新如式(3)所示。机器人群的全局最优位置更新如式(4)所示。
Pi(t+1)=Pi(t)+Vi(t+1) (2) P∗i(t+1)={Pi(t+1)Ci(t+1)>Ci(t)P∗i(t)Ci(t+1)⩽Ci(t) (3) P∗g(t+1)={P∗i(t+1)Ci(t+1)>C∗i(t)P∗g(t)Ci(t+1)⩽C∗i(t) (4) 3)源确认算法。源确认是指通过获取气味特征来确认源在机器人附近的定位过程。本研究中使用浓度极大值方法来进行源确认和结束源定位过程,即当机器人在全局最优位置
P∗g(t) 2. 实验设计
2.1 实验方案设计
如图2所示,为了验证在室内弱气流环境下三维溯源的有效性以及对比三维和二维溯源的性能,在实验开始前设置了1.05 m和0.75 m 2种源高度。在每种源高度下,分别计划开展15组三维和二维溯源实验,共计60组实验。实验过程中,二维溯源机器人传感器固定在1.05 m高度。
2.2 多机器人溯源系统
本研究基于课题组之前开发的多机器人二维溯源系统新开发了1套多机器人三维溯源系统,该系统机器人上的传感器可在0.5~1.5 m内受控移动。每台二维溯源机器人(图3(a))均配备1种用于搭载和移动的机器人底盘(Kobuki Turtlebot2),用于定位和导航机器人的激光测距雷达(RPlidarA2),用于监测和收集气流速度与方向的超声波风速风向仪(Windsonic, Gill,传感器精度:风速(12±0.24) m·s−1,风向±3 °),以及用于监测和收集乙醇蒸汽浓度的气体传感器MICS-5524((267±8) mg·m−3,响应时间小于2 s)。
三维溯源机器人(图3(b))的基础配置跟二维溯源机器人类似,包括机器人底盘,激光测距雷达,超声波风速风向仪和气体传感器。三维机器人与二维机器人的显著区别是设计了可以使传感器在高度上受控移动的三维运载模组。三维运载模组用于控制风速风向仪与气体传感器在垂直高度方向上的移动。三维运载模组的运行逻辑为:首先启动并初始化机器人,待气体传感器将收集到的浓度信息传送给工控机,工控机根据相应的运行策略计算出下一步传感器要到达的目标高度;然后根据此刻激光测距传感器测得的传感器的高度来计算出需要上下移动的距离;最后换算出直流电机需要的转向和圈数,如此迭代更新,不断控制传感器在不同高度上的移动。
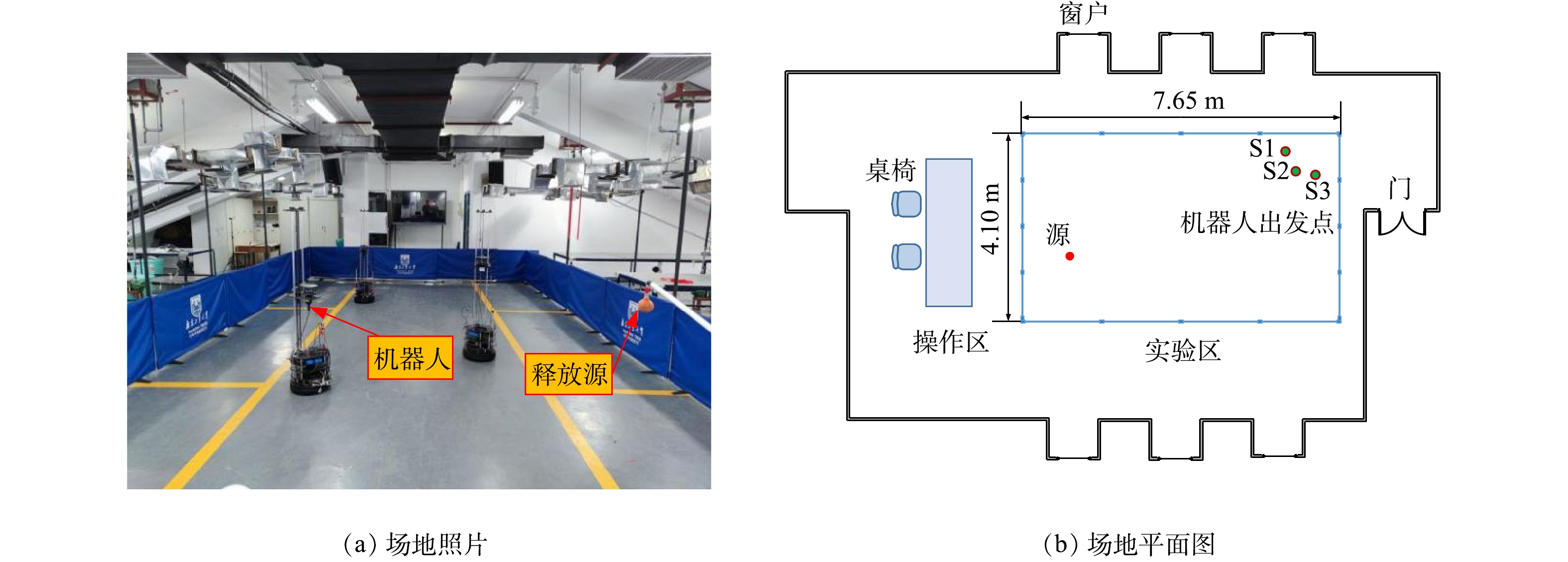
2.3 实验场地及源设置
本研究的溯源实验在城市建设学院生产实训基地(图4(a))开展,其中机器人活动范围限定为7.65 m×4.1 m(图4(b))。在本研究中,由于乙醇无毒、易挥发、易获取、价格低廉等特性被选来作为示踪气体。在实验过程中使用水浴箱(保持65 °C恒温)加热含有乙醇液体的烧瓶,生成的乙醇蒸汽通过与气泵相连的橡胶管输送到源位置。实验过程中乙醇以12.5 mg·s−1的速率恒定释放。
2.4 实验流程
在每次源定位实验前,将门窗打开进行通风,直至室内乙醇浓度低于10.3 mg·m−3,以保证每次实验开始前的情况基本一致。在实验过程中,室内通风设备全部关闭,门窗也均呈关闭状态,以营造1个无主导气流的室内弱气流环境。在实验开始时,3个机器人分别从起始位置S1、S2、S3出发(图4(b)),机器人采用“走-停-走”的行进策略,即机器人每向前走1步,均需要停留一段时间,以便收集浓度信息,机器人每移动1步均会共享各自的位置信息和浓度信息,然后根据共享的信息代入各阶段的算法计算出各机器人下一步所需抵达的位置。在烟羽发现阶段,各机器人以烟羽发现算法更新自己的位置,一旦某个机器人测得的烟羽浓度超过所设的烟羽发现的阈值,各机器人则进入烟羽追踪阶段,在该阶段,3台机器人的位置信息和浓度信息每行进一步都会带入式(1)~式(4)来计算更新局部最优位置和全局最优位置,以此来规划机器人的路径。
三维溯源与二维溯源不同的是,机器人每次停留,其三维运载模组均在高度上移动一段距离(0~0.08 m),以采集不同高度上的浓度信息,其中在烟羽发现阶段固定移动0.08 m,在烟羽追踪和源确认阶段,每一步将根据3台机器人所处位置的高度和浓度通过标准粒子群算法计算出下一步在高度上移动的最优距离。在机器人溯源过程中,如果浓度最大值在5步内保持不变,则视为自己被困在了局部浓度极值区域,此时转为源确认算法。当实验结束时,如果定位误差小于或等于0.5 m,则视为实验成功。此外,为控制每次实验的耗时和保障溯源过程的效率,若机器人在50步(二维溯源约为15 min,三维溯源约为20 min)内无法找到源位置,则溯源实验终止,并宣布实验失败。
3. 结果与讨论
3.1 实验结果分析
为了验证三维溯源的有效性,以及在源高度未知的场景中二维溯源是否仍然适用,在室内弱气流环境下,本研究利用SPSO方法进行源定位实验。针对1.05 m和0.75 m 2种源高度,共开展了60组溯源实验,结果如表1所示。由表1可见,对于2种源高度,三维溯源的实验结果差别很小。在源高度为1.05 m和0.75 m时,三维溯源实验分别成功完成了9组和8组,成功率分别为60%和53.3%。上述实验结果验证了三维溯源的有效性,同时表现出三维溯源对不同源高度的较好适应性。此外,以上研究结果也表明,在弱气流环境中三维溯源的成功率仍不是很理想,还有待进一步提高。
表 1 源在不同高度释放时二维溯源和三维溯源实验结果统计Table 1. Statistics of two-dimensional and three-dimensional source localization experiment results when the source was released at different heights溯源类型 源高度/m 成功组数/总组数 成功率/% 平均定位步数/步 平均定位时长/s 三维溯源 1.05 9/15 60.0 30.0 762 0.75 8/15 53.3 32.8 815 二维溯源 1.05 12/15 80.0 16.0 318 0.75 4/15 26.7 42.0 734 对比三维溯源和二维溯源实验结果可以发现,当源高度为1.05 m时,即源高度与二维溯源传感器高度相同时,二维溯源不仅成功率(80%)明显高于三维溯源的成功率(60%),而且平均定位步数(16步)和平均定位时长(318 s)也明显低于三维溯源的平均定位步数(30步)和平均定位时长(762 s)。当源高度为0.75 m时,即源高度与二维溯源传感器高度不同时,从成功率和平均定位步数以及平均定位时间来看,三维溯源性能仅略有降低,但二维溯源的性能却显著下降,尤其是成功率已从80%陡降至26.7%,虽然此工况下二维溯源平均定位时长要低于三维溯源,但如此低的成功率已经不能满足实际应用需求。上述对比进一步说明,对于源高度未知的场景,三维溯源具有较高的适应性,而二维溯源却不具备类似的适应性。
由表2可见,二维溯源和三维溯源的失败实验多是由于定位误差超过了0.5 m,主要因为室内弱气流环境缺少主导气流且受湍流主控,实验区域内很容易形成多个浓度局部极值区域,导致机器人难以跳出,以至于最后在远离源的位置宣告了源的存在。对于源高度为0.75 m的二维溯源失败实验多是因为机器人传感器高度为1.05 m固定不变,以至于难以在这一高度上持续追踪从源处释放的酒精蒸汽的烟羽。
表 2 源在不同高度释放时二维溯源和三维溯源失败实验结果统计Table 2. Statistics of two-dimensional and three-dimensional source localization failure experiment results when the source was released at different heights溯源类型 源高度/m 总失败组数/组 定位偏差超0.5 m组数/组 定位步数超50步组数/组 三维溯源 1.05 6 4 2 0.75 7 4 3 二维溯源 1.05 3 2 1 0.75 11 3 8 3.2 源定位过程分析
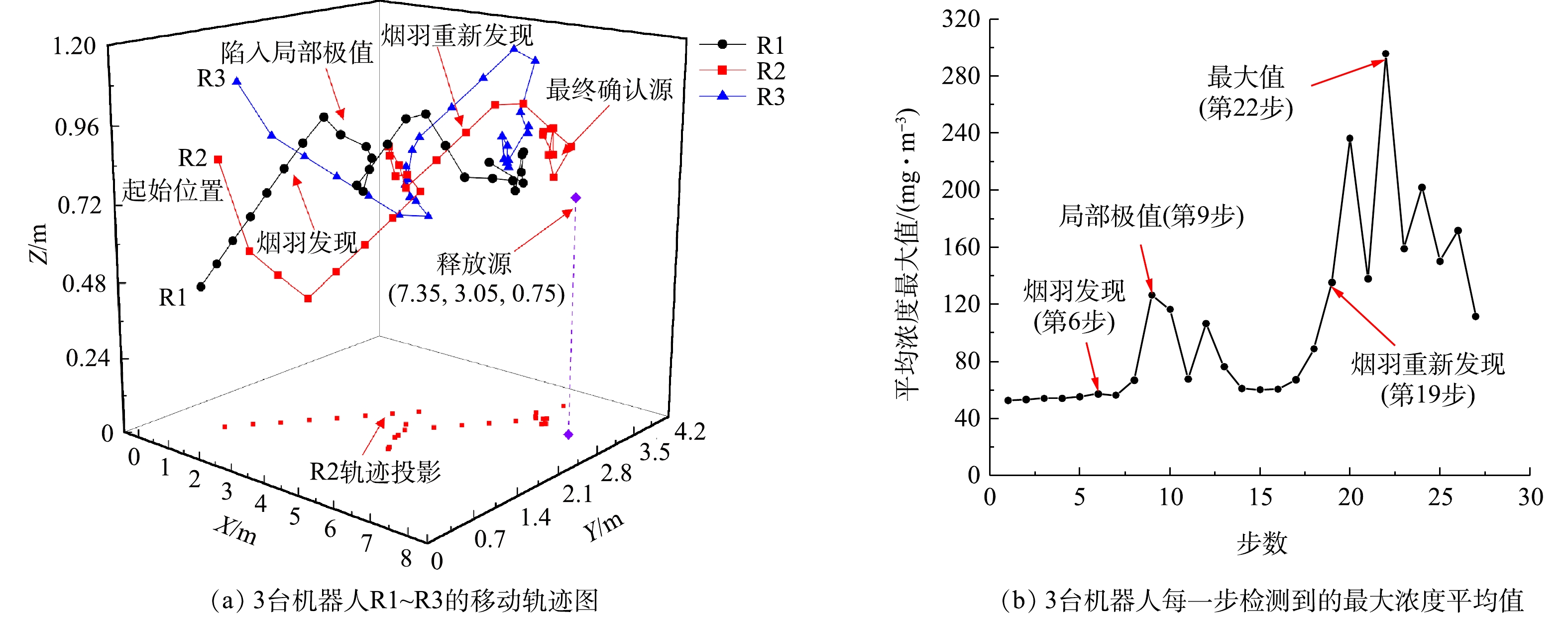
1)在源高度0.75 m时成功的三维溯源实验。图5展示了1组利用3台三维溯源机器人在实训中心三楼实验区域中,使用SPSO方法进行三维溯源并成功定位恒定源的实验过程以及机器人每1步检测到的最大浓度平均值。在实验过程中,从起始点出发到最终定位目标源,机器人主要经历了烟羽发现、烟羽追踪、第1次陷入并逃离局部极值区域、烟羽重发现以及源确认阶段,共用了27步。
实验开始前,3台机器人首先进行初始化,机器人移动到预先设置的出发位置。实验开始后,机器人从起始位置采用发现搜索策略出发,烟羽是由R1在第6步发现的,此时R1的信息采集模块高度为0.76 m。在此组实验过程中,R1第6步发现烟羽后,整个机器人群便切换到烟羽追踪阶段,开始执行SPSO算法。开始烟羽追踪后,第9步时,R1在0.81 m高度检测到1个较大的浓度平均值,接着R1开始在附近继续移动搜索以找到更高的浓度值,R2和R3则开始不断向R1靠近。在接下来的5步中,3台机器人均未检测到更高的浓度均值,表明此时机器人已经陷入了局部浓度极值区,并采用浓度极大值方法进行源确认。但R1在第9步检测到的较高浓度平均值小于之前设定的源确认浓度阈值Cmax,根据浓度极大值方法,机器人判定找到了1个局部浓度极值区。为了更好地逃离局部浓度极值区并再次搜索到更高的浓度,机器人再次采用发散搜索策略去移动探索。在第19步时,R2检测到了1个更高的浓度值,3台机器人再次进入烟羽追踪阶段。在第21步时,R2检测到1个较高的浓度平均值,并已经到达了源位置附近。然后R2对其周边领域进行搜索,试图找到1个更高的浓度均值,R1和R3则不断向R2靠近,直到第27步时,机器人群均未找到1个更高的浓度均值。机器人立即开始采用浓度极大值方法进行源确认,判断出第22步测得的浓度大于设定的Cmax,故判定机器人已经成功定位到了释放源,终止源定位过程。此时,机器人确定的源位置(全局最优位置)与真实源位置之间的距离为0.32 m(小于0.5 m),表明这组源定位实验成功完成。
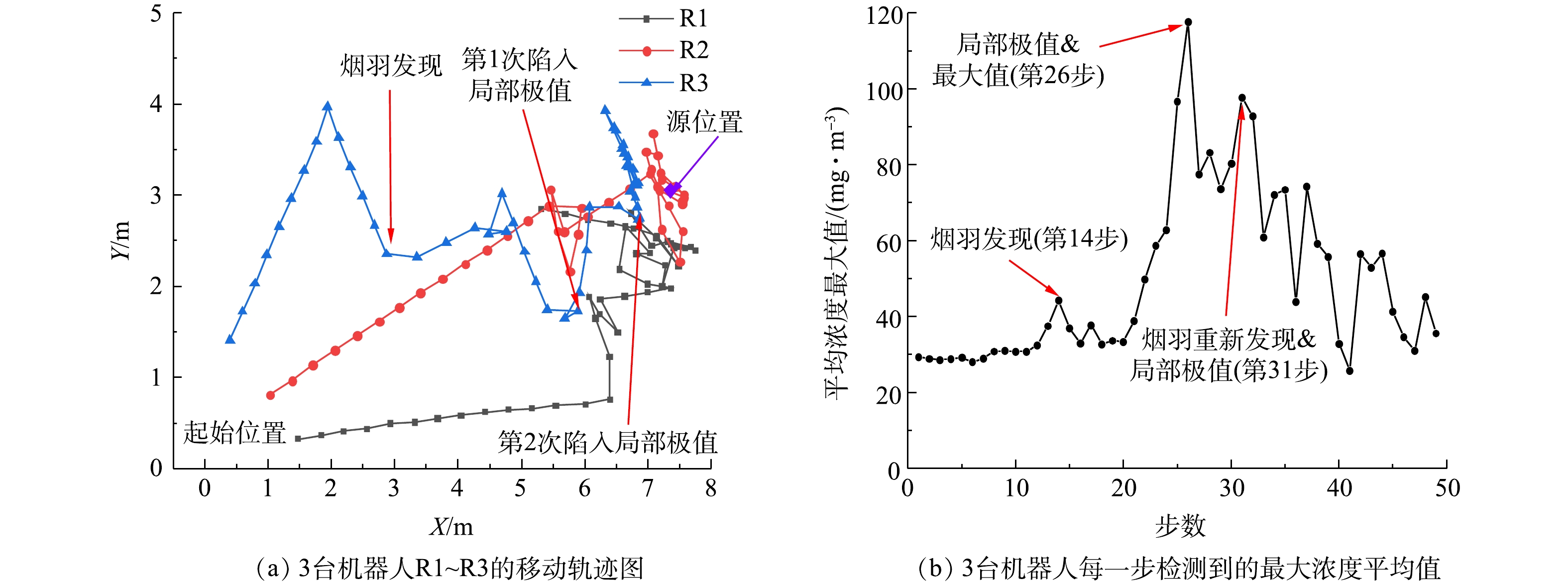
2)在源高度0.75 m时失败的二维溯源实验。在源释放高度为0.75 m时,机器人从预先设定的起始位置按固定角度出发,按直线发散搜索策略前进。第14步时,R3发现烟羽,随后进入烟羽追踪阶段;第26步时,机器人群找到了1个局部浓度极值区,并根据浓度极大值方法判定机器人已经陷入该区域,随后采用发散搜索策略跳出,进入烟羽再发现阶段;第31步时,机器人重新检测到1个较高的浓度均值,开始进行烟羽追踪,但在接下来直到源定位过程结束均未找到更高的浓度值,又因第31步的浓度值未到达源确认的阈值,故判定此组源定位实验失败(图6)。
进一步分析这组失败的实验案例可以发现,在二维溯源机器人上的传感器高度低于源释放高度时,即使机器人与源的距离会很近甚至是小于0.5 m,但在该位置不能检测到更高的浓度均值来取代已测得的较高的浓度均值,从而导致机器人接下来朝远离源的方向行进,最后终止了源定位过程。这说明,室内弱气流环境下风速风向无规律变化会使源附近的流场和气体浓度出现较大的波动,让机器人有时检测不到较高的浓度均值。此外,由于乙醇蒸汽的密度较大而发生下沉,可能使机器人在高于源释放高度上难以持续追踪其烟羽,从而导致源定位失败。
4. 结论
1)在源高度为1.05 m和0.75 m时各开展了15组三维溯源实验。结果表明,SPSO方法能够适用于室内弱气流环境下的三维溯源,并且对不同的源高度具有良好的适应性,故其能够应用于源高度未知的场景;此外,在室内弱气流环境中三维溯源的成功率还有待提高。
2)当三维溯源的源高度(1.05 m)与二维溯源的传感器高度相同时,二维溯源的性能明显优于三维溯源;但当源高度(0.75 m)与二维溯源传感器高度不同时,二维溯源的成功率(26.7%)已不能满足现实需求,说明二维溯源并不能适应不同的源高度,因而也难以将其应用于源高度未知的场景中。
3)当源高度(0.75 m)低于二维溯源的传感器高度时,三维和二维溯源的源定位过程显示,三维溯源通过主动调节传感器高度更易于检测到乙醇蒸汽,而二维溯源则因为传感器的高度固定而难以检测到乙醇蒸汽,这也说明在室内弱气流环境中三维溯源比二维溯源更能够适应源高度未知的场景。
-
表 1 研究区采样点信息
Table 1. Information on sampling sites in the study area
采样点编号Sampling number 经度Longitude 纬度Latitude 井深/m Well depth 采样地点Location of sampling K1 84.7277 44.1247 — 奎屯河 K2 84.7519 44.1605 — 奎屯河 C1 84.0812 45.0314 200 126团 C2 84.0641 45.0257 180 126团 C3 84.1032 45.0210 200 126团 C4 84.0825 45.0215 180 126团 C5 84.0808 45.0222 160 126团 C6 84.1322 45.0230 70 126团 C7 84.3551 45.0217 130 128团 C8 84.3553 45.0221 80 128团 C9 84.3747 44.5852 60 128团 C10 84.3739 44.5848 60 128团 C11 84.3659 44.5905 200 128团 C12 84.4051 44.5836 100 128团 C13 84.4038 44.5558 80 128团 C14 84.4004 44.5723 120 128团 C15 84.3508 45.0513 100 128团 表 2 水样主要水化学指标统计表
Table 2. Statistical table of main water chemical indicators of water samples
指标 Index pH K+/(mg·L−1) Na+/(mg·L−1) Ca2+/(mg·L−1) Mg2+/(mg·L−1) 地表水 6.66—7.06(6.86) 1.18 273.50—280.41(276.96) 47.33 10.67—32.80(21.73) 地下水 7.59—9.42(8.63) 0.02—1.25(0.46) 4.58—503.07(107.62) 5.01—544.42(151.57) 1.37—467.36(110.11) 指标 Index Eh/mV CO32−/(mg·L−1) HCO3−/(mg·L−1) Cl−/(mg·L−1) SO42−/(mg·L−1) As/(μg·L−1) 地表水 21.3—28.5(24.90) — 157—179(168) 24.69—50.07(37.38) 536—640(588) 6.27—6.76(6.52) 地下水 −96— −7.5(−55.08) 2.45—9.81(5.19) 49.44—125.52(72.06) 18.88—1829.43(527.35) 0—1415.70(506.56) 2.45—460.38(60.60) 注:括号内为平均值. Note: Average values in brackets 表 3 不同地区地下水中δ13CDIC与δ13CDOC值、As和Fe质量浓度及井深范围
Table 3. δ13CDIC and δ13CDOC values, As and Fe mass concentrations and well depth ranges in groundwater from different regions
-
[1] 贾永锋, 郭华明. 高砷地下水研究的热点及发展趋势 [J]. 地球科学进展, 2013, 28(1): 51-61. doi: 10.11867/j.issn.1001-8166.2013.01.0051 JIA Y F, GUO H M. Hot topics and trends in the study of high arsenic groundwater [J]. Advances in Earth Science, 2013, 28(1): 51-61(in Chinese). doi: 10.11867/j.issn.1001-8166.2013.01.0051
[2] GILLISPIE E C, ANDUJAR E, POLIZZOTTO M L. Chemical controls on abiotic and biotic release of geogenic arsenic from Pleistocene aquifer sediments to groundwater [J]. Environmental Science. Processes & Impacts, 2016, 18(8): 1090-1103. [3] RODRÍGUEZ-LADO L, SUN G F, BERG M, et al. Groundwater arsenic contamination throughout China [J]. Science, 2013, 341(6148): 866-868. doi: 10.1126/science.1237484 [4] AHMED K M, BHATTACHARYA P, HASAN M A, et al. Arsenic enrichment in groundwater of the alluvial aquifers in Bangladesh: An overview [J]. Applied Geochemistry, 2004, 19(2): 181-200. doi: 10.1016/j.apgeochem.2003.09.006 [5] SMEDLEY P L, KINNIBURGH D G. A review of the source, behaviour and distribution of arsenic in natural waters [J]. Applied Geochemistry, 2002, 17(5): 517-568. doi: 10.1016/S0883-2927(02)00018-5 [6] 于凯. 高砷地下水系统中有机质来源及其对砷动态变化的影响研究: 以江汉平原为例[D]. 武汉: 中国地质大学, 2016. YU K. The sources and influences of dissolved organic matter on temporal variations of groundwater arsenic concentrations— a case study in Jianghan plain[D]. Wuhan: China University of Geosciences, 2016 (in Chinese).
[7] 周殷竹. 基于碳、铁稳定同位素的高砷地下水生物地球化学研究[D]. 北京: 中国地质大学(北京), 2018. ZHOU Y Z. Biogeochemical processes in high arsenic groundwater in the northwestern Hetao Basin, Inner Mongolia: Evidences from hydrogeochemistry and stable isotopes[D]. Beijing: China University of Geosciences, 2018 (in Chinese).
[8] YU K, GAN Y Q, ZHOU A G, et al. Organic carbon sources and controlling processes on aquifer arsenic cycling in the Jianghan Plain, central China [J]. Chemosphere, 2018, 208: 773-781. doi: 10.1016/j.chemosphere.2018.05.188 [9] 韩莉, 甘义群, 于凯. 江汉平原高砷地下水中溶解性有机质来源的稳定碳同位素示踪研究[J]. 地质学报, 2015, 89(S1): 266-268. HAN L, GAN Y Q, YU K. Stable carbon isotope tracing study on the source of dissolved organic matter in high arsenic groundwater in Jianghan plain[J]. Acta Geologica Sinica, 2015, 89(Sup 1): 266-268 (in Chinese).
[10] XIE X J, WANG Y X, ELLIS A, et al. Multiple isotope (O, S and C) approach elucidates the enrichment of arsenic in the groundwater from the Datong Basin, Northern China [J]. Journal of Hydrology, 2013, 498: 103-112. doi: 10.1016/j.jhydrol.2013.06.024 [11] 张亚男. 江汉平原含水层铁还原砷释放过程中有机质转化机制研究[D]. 武汉: 中国地质大学, 2021. ZHANG Y N. Mechanisms of organic matter transformation during dissimilated iron reduction and arsenic mobilization in aquifer of Jianghan plain[D]. Wuhan: China University of Geosciences, 2021 (in Chinese).
[12] 周殷竹. 内蒙古河套盆地地下水碳同位素特征及生物地球化学意义[D]. 北京: 中国地质大学(北京), 2014. ZHOU Y Z. Characteristics of C isotopes and its biogeochemistry significance in high as groundwater system in the Hetao Basin, Inner Mongolia[D]. Beijing: China University of Geosciences, 2014 (in Chinese).
[13] GUO H M, ZHANG D, WEN D G, et al. Arsenic mobilization in aquifers of the southwest Songnen Basin, P. R. China: Evidences from chemical and isotopic characteristics [J]. Science of the Total Environment, 2014, 490: 590-602. doi: 10.1016/j.scitotenv.2014.05.050 [14] 罗艳丽, 李晶, 蒋平安, 等. 新疆奎屯原生高砷地下水的分布、类型及成因分析 [J]. 环境科学学报, 2017, 37(8): 2897-2903. LUO Y L, LI J, JIANG P A, et al. Distribution, classification and cause analysis of geogenic high-arsenic groundwater in Kuitun, Xinjiang [J]. Acta Scientiae Circumstantiae, 2017, 37(8): 2897-2903(in Chinese).
[15] 罗艳丽, 李晶, 蒋平安, 等. 新疆高砷地区地下水水化学特征及其成因分析 [J]. 干旱区资源与环境, 2017, 31(8): 116-121. doi: 10.13448/j.cnki.jalre.2017.256 LUO Y L, LI J, JIANG P A, et al. Hydro-chemical characteristics and the formations for groundwater in Kuitun, Xinjiang [J]. Journal of Arid Land Resources and Environment, 2017, 31(8): 116-121(in Chinese). doi: 10.13448/j.cnki.jalre.2017.256
[16] 邓雯文, 罗艳丽, 王翔, 等. 新疆奎屯地区地下水中砷和盐的分布特征及成因分析 [J]. 环境污染与防治, 2021, 43(11): 1404-1409. DENG W W, LUO Y L, WANG X, et al. Distribution characteristics and cause analysis of arsenic and salinity in groundwater of Kuitun area, Xinjiang [J]. Environmental Pollution & Control, 2021, 43(11): 1404-1409(in Chinese).
[17] 张慧. 基于RS与GIS的天山奎屯河流域冰川变化研究[D]. 兰州: 西北师范大学, 2015. ZHANG H. Research of glacier change based on RS and GIS in the Kuytun River Basin, Tianshan mountains[D]. Lanzhou: Northwest Normal University, 2015 (in Chinese).
[18] 南峰, 李有利, 邱祝礼. 新疆奎屯河流域山前河流地貌特征及演化 [J]. 水土保持研究, 2005, 12(4): 10-13. doi: 10.3969/j.issn.1005-3409.2005.04.004 NAN F, LI Y L, QIU Z L. Characteristics and evolutions of fluvial geomorphology in foreland of the Kuitun River valley [J]. Research of Soil and Water Conservation, 2005, 12(4): 10-13(in Chinese). doi: 10.3969/j.issn.1005-3409.2005.04.004
[19] 王丽娟, 王文科, 王哲, 等. 奎屯河流域包气带盐分分布特征与影响因素 [J]. 地球科学与环境学报, 2008, 30(4): 429-433. WANG L J, WANG W K, WANG Z, et al. Distribution regularity and the formative factor soil salt of the Kuitun River Basin [J]. Journal of Earth Sciences and Environment, 2008, 30(4): 429-433(in Chinese).
[20] 王翔, 罗艳丽, 邓雯文, 等. 新疆奎屯地区高砷地下水DOM三维荧光特征 [J]. 中国环境科学, 2020, 40(11): 4974-4981. WANG X, LUO Y L, DENG W W, et al. The 3D-EEM characteristics of DOM in high arsenic groundwater of Kuitun, XinjiangFull text replacement [J]. China Environmental Science, 2020, 40(11): 4974-4981(in Chinese).
[21] 王翔. 奎屯河下游区域地下水中砷的释放过程研究[D]. 乌鲁木齐: 新疆农业大学, 2021. WANG X. Mobilization processes of arsenic in groundwater of Kuitun River downsteam[D]. Urumqi: Xinjiang Agricultural University, 2021 (in Chinese).
[22] 周殷竹, 郭华明, 逯海. 高砷地下水中溶解性有机碳和无机碳稳定同位素特征 [J]. 现代地质, 2015, 29(2): 252-259. ZHOU Y Z, GUO H M, LU H. Stable isotope characteristics of dissolved organic carbon and inorganic carbon in high arsenic groundwater [J]. Geoscience, 2015, 29(2): 252-259(in Chinese).
[23] 袁翰卿, 李巧, 陶洪飞, 等. 新疆奎屯河流域地下水砷富集因素 [J]. 环境化学, 2020, 39(2): 524-530. doi: 10.7524/j.issn.0254-6108.2019051403 YUAN H Q, LI Q, TAO H F, et al. Groundwater arsenic enrichment factors of Kuitun River Basin, Xinjiang [J]. Environmental Chemistry, 2020, 39(2): 524-530(in Chinese). doi: 10.7524/j.issn.0254-6108.2019051403
[24] FONYUY E W, ATEKWANA E A. Dissolved inorganic carbon evolution and stable carbon isotope fractionation in acid mine drainage contaminated streams: Insights from a laboratory study [J]. Applied Geochemistry, 2008, 23(9): 2634-2648. doi: 10.1016/j.apgeochem.2008.05.012 [25] 袁晓芳, 邓娅敏, 杜尧, 等. 江汉平原高砷地下水稳定碳同位素特征及其指示意义 [J]. 地质科技通报, 2020, 39(5): 156-163. YUAN X F, DENG Y M, DU Y, et al. Characteristics of stable carbon isotopes and its implications on arsenic enrichment in shallow groundwater of the Jianghan Plain [J]. Bulletin of Geological Science and Technology, 2020, 39(5): 156-163(in Chinese).
[26] 史婷婷. 岩溶流域水循环过程碳汇效应研究: 以湖北香溪河流域为例[D]. 武汉: 中国地质大学, 2012. SHI T T. The carbon sequestration effect of water cycle in a Karst Basin— a case study of Xiangxi River Basin, Hubei[D]. Wuhan: China University of Geosciences, 2012 (in Chinese).
[27] YANG C, TELMER K, VEIZER J. Chemical dynamics of the “St. Lawrence” riverine system: δDH2O, δ18OH2O, δ13CDIC, δ34Ssulfate, and dissolved 87Sr/86Sr [J]. Geochimica et Cosmochimica Acta, 1996, 60(5): 851-866. doi: 10.1016/0016-7037(95)00445-9 [28] BARTH J A C, CRONIN A A, DUNLOP J, et al. Influence of carbonates on the riverine carbon cycle in an anthropogenically dominated catchment basin: Evidence from major elements and stable carbon isotopes in the Lagan River (N. Ireland) [J]. Chemical Geology, 2003, 200(3/4): 203-216. [29] 邹君宇, 韩贵琳. 河流中碳、硫稳定同位素的研究进展 [J]. 地球与环境, 2015, 43(1): 111-122. doi: 10.14050/j.cnki.1672-9250.2015.01.016 ZOU J Y, HAN G L. Research review on carbon and sulfur stable isotopes in rivers [J]. Earth and Environment, 2015, 43(1): 111-122(in Chinese). doi: 10.14050/j.cnki.1672-9250.2015.01.016
[30] ZHOU Y Z, GUO H M, ZHANG Z, et al. Characteristics and implication of stable carbon isotope in high arsenic groundwater systems in the northwest Hetao Basin, Inner Mongolia, China [J]. Journal of Asian Earth Sciences, 2018, 163: 70-79. doi: 10.1016/j.jseaes.2018.05.018 [31] 姚冠荣, 高全洲. 河流碳循环对全球变化的响应与反馈 [J]. 地理科学进展, 2005, 24(5): 50-60. doi: 10.11820/dlkxjz.2005.05.006 YAO G R, GAO Q Z. The feedback and response of the riverine carbon cycle to global changes [J]. Progress in Geography, 2005, 24(5): 50-60(in Chinese). doi: 10.11820/dlkxjz.2005.05.006
[32] 丁薇. 河流水体有机碳研究综述 [J]. 安徽农学通报, 2017, 23(9): 28-29,71. doi: 10.3969/j.issn.1007-7731.2017.09.010 DING W. The review of the riverine organic carbon [J]. Anhui Agricultural Science Bulletin, 2017, 23(9): 28-29,71(in Chinese). doi: 10.3969/j.issn.1007-7731.2017.09.010
[33] 魏秀国. 河流有机质生物地球化学研究进展 [J]. 生态环境, 2007, 16(3): 1063-1067. WEI X G. Progress in the study of biogeochemistry of riverine organic matter [J]. Ecology and Environment, 2007, 16(3): 1063-1067(in Chinese).
[34] CLARK I D, FRITZ P. Environmental Isotopes in Hydrogeology[M].New York: Lewis Publishing House, 1997. [35] TRUESDELL A H, HULSTON J R. Isotopic evidence on environments of geothermal systems[M]//The Terrestrial Environment, A. Amsterdam: Elsevier, 1980: 179-226. [36] 江军, 鲜虎胜, 李巧, 等. 奎屯河流域地下水地球化学特征及其对砷运移的影响 [J]. 环境化学, 2021, 40(6): 1775-1786. doi: 10.7524/j.issn.0254-6108.2020062702 JIANG J, XIAN H S, LI Q, et al. Groundwater geochemistry and its implications for arsenic mobilization in Kuitun River Basin, Xinjiang [J]. Environmental Chemistry, 2021, 40(6): 1775-1786(in Chinese). doi: 10.7524/j.issn.0254-6108.2020062702
[37] 吕航. 地下水中石油烃生物降解的同位素地球化学研究[D]. 长春: 吉林大学, 2011. (LÜ/LV/LU/LYU) H. Isotope geochemistry of biodegradation processes in a petroleum hydrocarbon-contaminated aquifer[D]. Changchun: Jilin University, 2011 (in Chinese).
[38] 郑永飞, 陈江峰. 稳定同位素地球化学[M]. 北京: 科学出版社, 2000. ZHENG Y F, CHEN J F. Isotopic geochemistry[M]. Beijing: Science Press, 2000(in Chinese).
[39] 陈世苹, 白永飞, 韩兴国. 稳定性碳同位素技术在生态学研究中的应用 [J]. 植物生态学报, 2002, 26(5): 549-560. doi: 10.3321/j.issn:1005-264X.2002.05.007 CHEN S P, BAI Y F, HAN X G. Applications of stable carbon isotope techniques to ecological research [J]. Acta Phytoecologica Sinica, 2002, 26(5): 549-560(in Chinese). doi: 10.3321/j.issn:1005-264X.2002.05.007
[40] 洪里. 新疆奎屯北部车排子地区高氟、高砷水的病害与形成环境的初步研究 [J]. 新疆环境保护, 1983, 5(1): 22-28. HONG L. Preliminary study on diseases and formation environment of high fluorine and high arsenic water in Chepaizi area of northern Kuitun, Xinjiang [J]. Environmental Protection of Xinjiang, 1983, 5(1): 22-28(in Chinese).
[41] 宿彦鹏, 李巧, 陶洪飞, 等. 新疆奎屯河流域地下水砷超标原因分析 [J]. 长江科学院院报, 2022, 39(3): 54-59. doi: 10.11988/ckyyb.20201188 SU Y P, LI Q, TAO H F, et al. Causes of excessive arsenic in groundwater of Kuitun River Basin in Xinjiang [J]. Journal of Yangtze River Scientific Research Institute, 2022, 39(3): 54-59(in Chinese). doi: 10.11988/ckyyb.20201188
[42] HUANG S B, WANG Y X, MA T, et al. Lin1 dissolved organic matter to sedimentary organic matter from a fluvio-lacustrine aquifer at Jianghan Plain, China by EEM-PARAFAC and hydrochemical analyses [J]. Science of the Total Environment, 2015, 529: 131-139. doi: 10.1016/j.scitotenv.2015.05.051 期刊类型引用(1)
1. 贺凯凯,朱峰,王彦堂,郝春明. 湖南锡矿山高锑地下水稳定碳同位素特征及其富锑意义. 科学技术与工程. 2024(22): 9672-9680 .  百度学术
百度学术
其他类型引用(0)
-






 下载:
下载: