-
臭氧混凝耦合工艺(hybrid ozonation-coagulation,HOC)是基于传统污水深度处理工艺“混凝-沉淀-过滤”处理流程长、溶解性有机物去除效果差的问题提出并构建的,具有臭氧氧化与混凝同时进行、溶解性有机物去除率高的特点[1-3]。然而在进行高Br−浓度废水处理时,例如工业盐水、肥料废水等[4-5],HOC工艺中的臭氧和由于臭氧与混凝剂的互促增效反应产生的·OH[6]会将Br−氧化为潜在致癌物质溴酸盐(BrO3−)[7-9],而我国《生活饮用水卫生标准》(GB 5749-2022)规定,饮用水中BrO3−含量不能高于0.01 mg·L−1。
近年来,臭氧氧化过程的BrO3−消毒副产物的控制方法受到国内外相关研究领域学者的广泛重视[10-13]。在臭氧氧化体系中,BrO3−的生成途径主要分为2种[14-15]:臭氧直接氧化和·OH间接氧化,2种氧化途径均伴随着中间产物HBrO/BrO−的生成,因此,HBrO/BrO−的继续氧化是控制Br−转化为BrO3−的重要限制反应[16]。而有研究表明,H2O2能通过与HBrO/BrO−反应阻碍其继续氧化为BrO3−,从而有效地延缓溴酸盐消毒副产物的生成[13]。此外,H2O2能加速臭氧分解生成·OH,控制BrO3−生成的同时可提高有机物的去除效果,但·OH的间接氧化也会促进BrO3−的生成[11, 17]。目前HOC工艺中H2O2控制下的溴酸盐消毒副产物的抑制效能尚未探讨,抑制原理也有待进一步探究。
基于以上研究结果,本研究探究在不同臭氧投加量下HOC工艺的有机物处理效果和BrO3−生成情况,考察H2O2投加量对HOC工艺中BrO3−生成的抑制效能,通过对BrO3−生成贡献率和Br−消耗动力学的分析,明确HOC体系中BrO3−的主要生成途径和H2O2抑制原理。
-
实验用水为外加KBr(Br−质量浓度为500 μg·L−1)的二级出水,二级出水来自西安某城市污水处理厂的二沉池,主要水质指标参数如下:pH为7.56±0.23,TOC为(5.43±1.66) mg·L−1,Br−为 (117±8) μg·L−1。
-
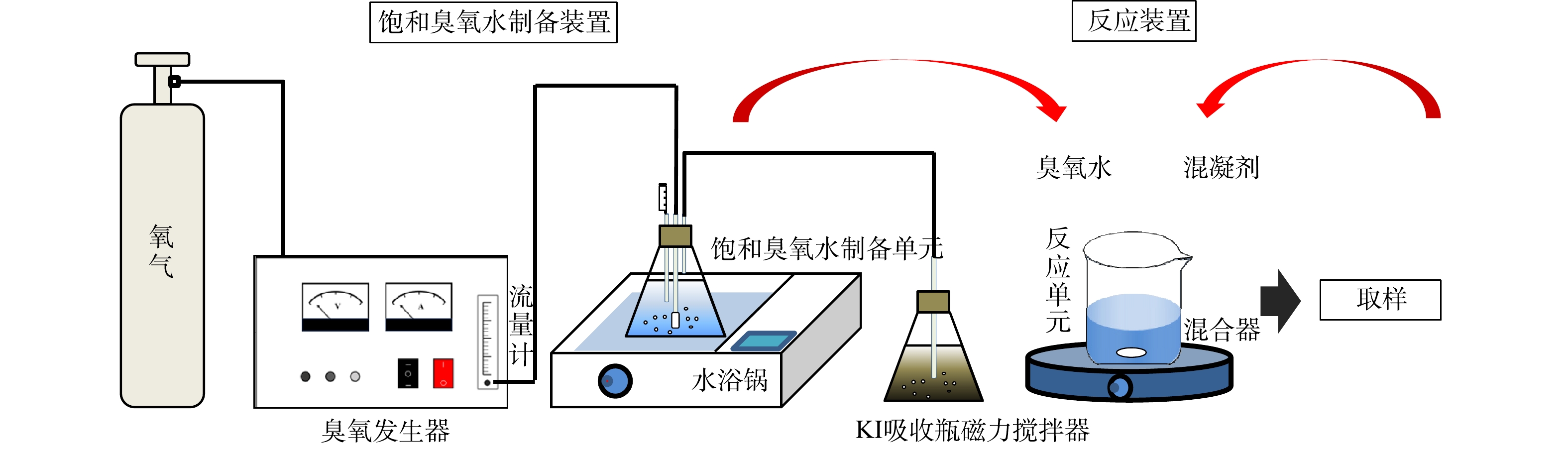
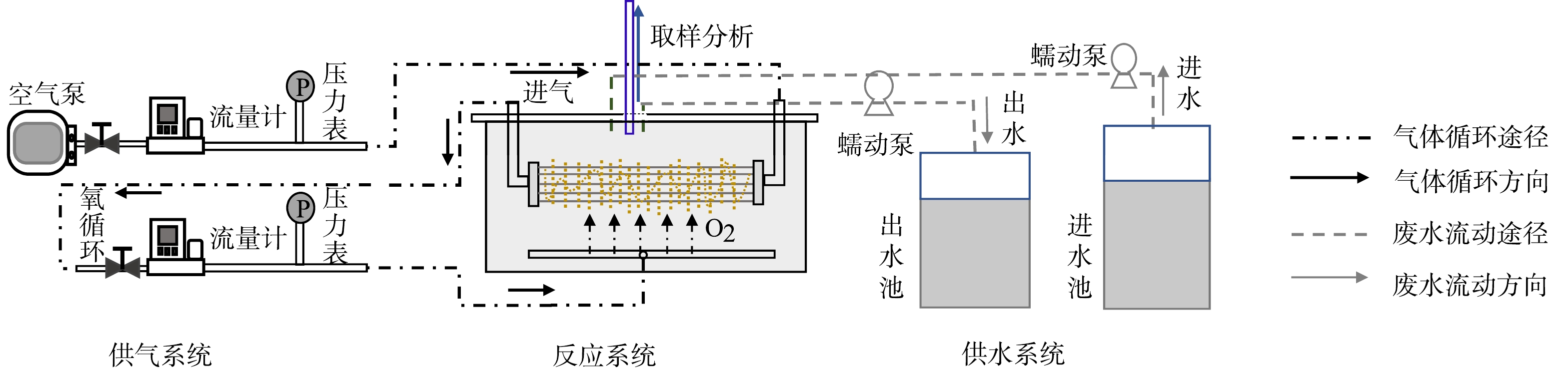
饱和臭氧水制备装置和HOC反应装置如图1所示,由气体流量计控制氧气源臭氧发生器(济南三康,SK-CFQ-3P)的出口流量为16 L·h−1,整个装置在0~4 ℃的水浴温度下持续曝气2 h后臭氧达饱和状态,本研究所投加的臭氧质量浓度为4.5、8.0、11.3 mg·L−1。HOC实验在外加Br−的100 mL二级出水中进行,混凝剂AlCl3·6H2O的投加量为15 mg·L−1。实验前使用0.2 mmol·L−1的磷酸缓冲溶液和1 mol·L−1的H2SO4溶液调节pH在7±0.2左右,然后加入混凝剂快搅1 min (转速300 r·min−1),饱和臭氧水和过氧化氢(n(H2O2):n(O3) = 0、0.5、1.0、1.5、2.0)在快搅结束后迅速加入体系,继而慢搅25 min (转速100 r·min−1),取不同反应时间的水样进行总有机碳(TOC)、溴离子(Br−)、溴酸根(BrO3−)、次溴酸(HBrO/BrO−)等指标的测定。
在探究HOC体系中BrO3−的生成贡献率时,取不同反应时间的水样经0.45 μm滤头过滤后快速测定臭氧质量浓度。由于对氯苯甲酸(pCBA)与·OH的反应速率k·OH,pCBA=5.0×109 L·(mol·s)−1远高于与O3的反应速率kO3,pCBA<0.15 L·(mol·s)−1[18],因此采用pCBA作为·OH的探针间接测定·OH的浓度。实验前向反应体系中加入0.5 μmol·L−1的pCBA,水样中pCBA的浓度测定前使用Na2S2O3淬灭·OH。
-
样品经0.45 μm滤头过滤、H2SO4酸化、N2吹脱3 min处理后,使用岛津TOC-VCPH分析仪测定TOC。饱和臭氧水质量浓度采用靛蓝比色法测定[19],气态臭氧采用碘量法测定[20]。Br−和BrO3−的质量浓度由热电阴离子色谱(ICS-1100 Dionex)测定,色谱柱为Dionex IonPacTM AS23(4×250 mm)。样品经固相萃取装置进行预处理:首先使用Bond Elut-C18小柱去除有机物;再使用Dionex OnGuardTM Ⅱ Ag/H小柱去除过渡金属离子和氯离子。HBrO/BrO−的质量浓度由苯酚衍生法测定[21],样品在pH为3、70 ℃的水浴条件下与苯酚反应1 h,反应后使用高效液相色谱法测定4-溴苯酚的质量浓度[22]。·OH浓度由pCBA探针法间接测定,pCBA浓度采用高效液相色谱法测定[23]。
-
Rct为某段时间内·OH暴露量与O3暴露量的比值(式(1))[24],Rct值通过式(2)计算。HOC体系中臭氧直接氧化和·OH间接氧化对BrO3−生成的贡献f(O3)和f(·OH)由式(3)~(5)[25-26]计算。
式中:C(·OH)为·OH的浓度,mol·L−1;C(O3)为O3的浓度,mol·L−1;C(pCBA)0和C(pCBA)分别为pCBA的初始浓度和反应后浓度,mol·L−1;k·OH,pCBA为pCBA与·OH的反应速率常数,5.0×109 L·(mol·s)−1。
式中:fBr−,·OH为·OH间接氧化的贡献率f(·OH);fBr−,O3为臭氧直接氧化的贡献率f(O3);C(Br−)为Br−的浓度,mol·L−1;C(·OH)为·OH的浓度,mol·L−1;kBr−,·OH为Br−与·OH的反应速率常数,1.1×109 L·(mol·s)−1[13];kBr−,O3为Br−与O3的反应速率常数,160 L·(mol·s)−1;C(O3)为O3的浓度,mol·L−1[13]。
-
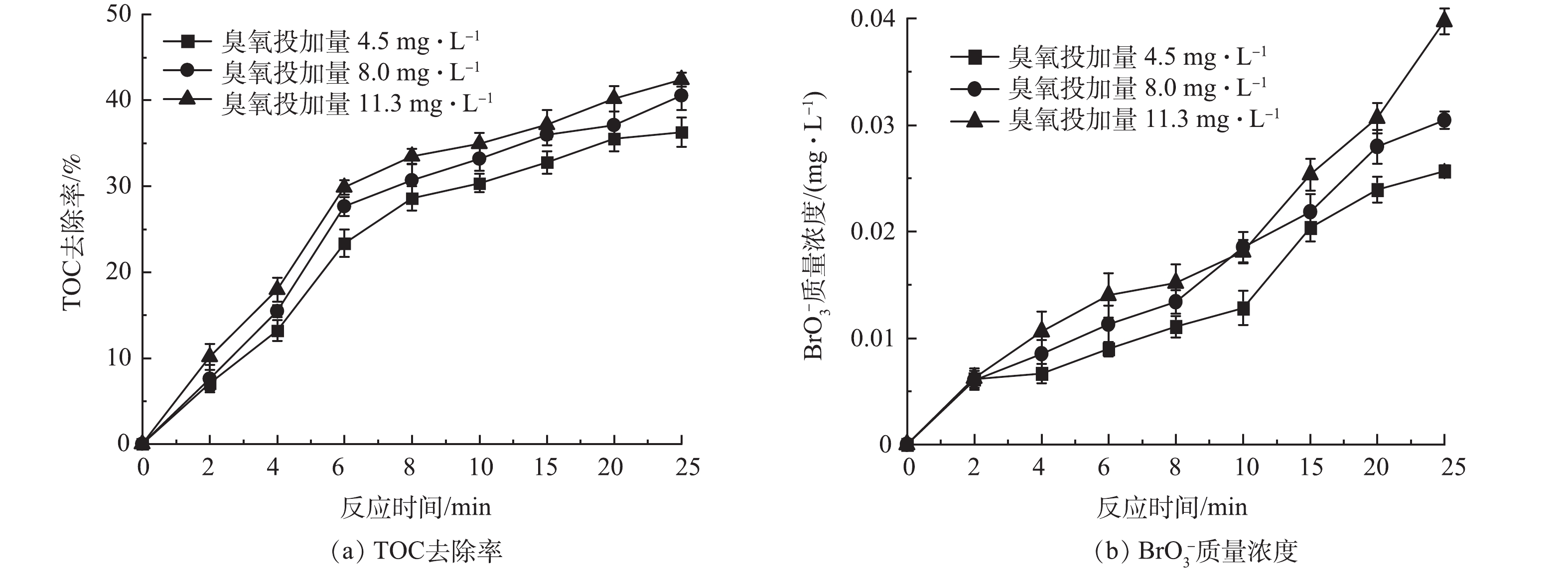
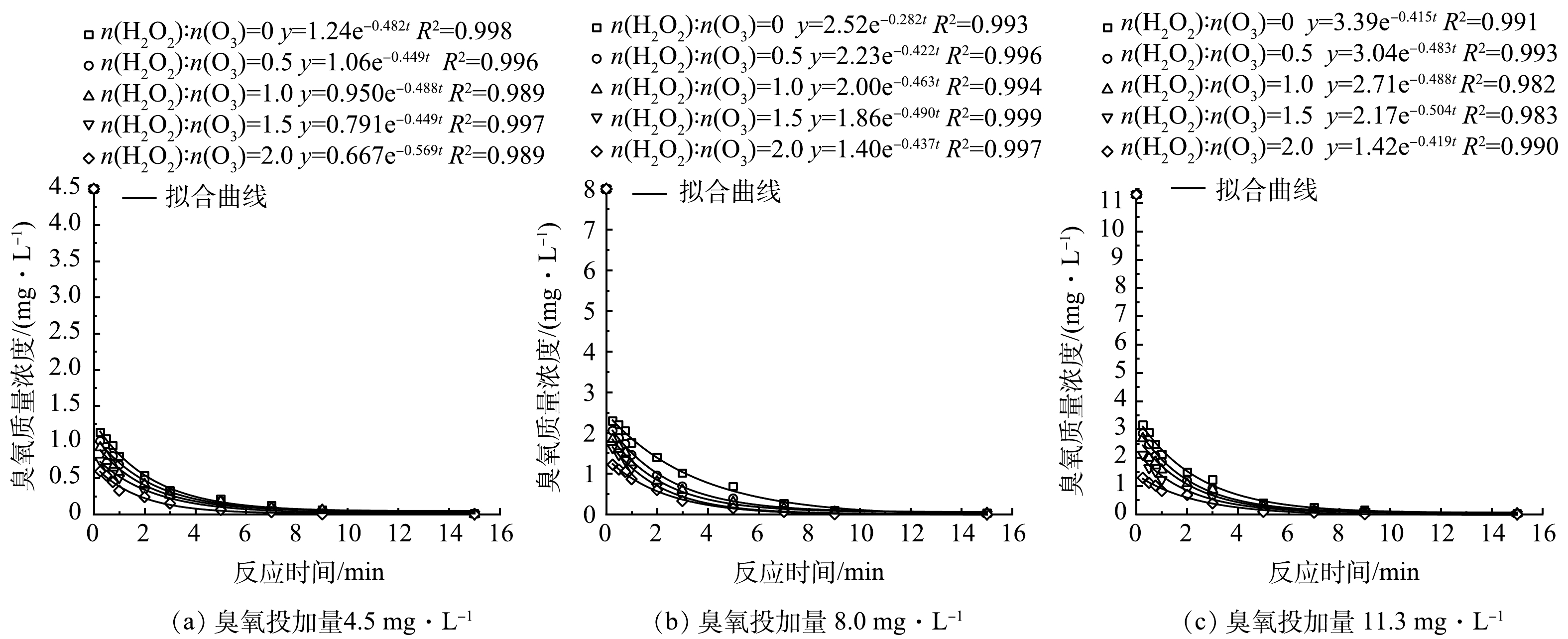
图2为不同臭氧投加量下HOC体系对二级出水中有机物的处理效果和生成的BrO3−质量浓度的变化。当臭氧投加量为4.5、8.0、11.3 mg·L−1时,反应25 min后HOC体系对TOC的去除率分别达到36.29%、40.56%和42.41%,BrO3−的生成量分别为0.026、0.030和0.040 mg·L−1,有机物的去除率和BrO3−质量浓度均随着臭氧投加量的增大而增加。这是因为在HOC体系中混凝剂既可以作为混凝剂发挥混凝作用,又可以作为催化剂催化臭氧产生·OH[1-3, 6],随着臭氧投加量的增加,O3和·OH的含量增大,体系的氧化能力增强,强化了有机物去除的同时使更多的Br−被O3直接或·OH间接氧化为BrO3−[14-15]。同时,由图2(b)可以看到,在3种臭氧投加量下,反应8 min后HOC体系中的BrO3−质量浓度均已经超过0.01 mg·L−1,即国家饮用水标准规范(GB 5749-2022)的BrO3−质量浓度限值,因此需对HOC体系中溴酸盐的生成进行控制。
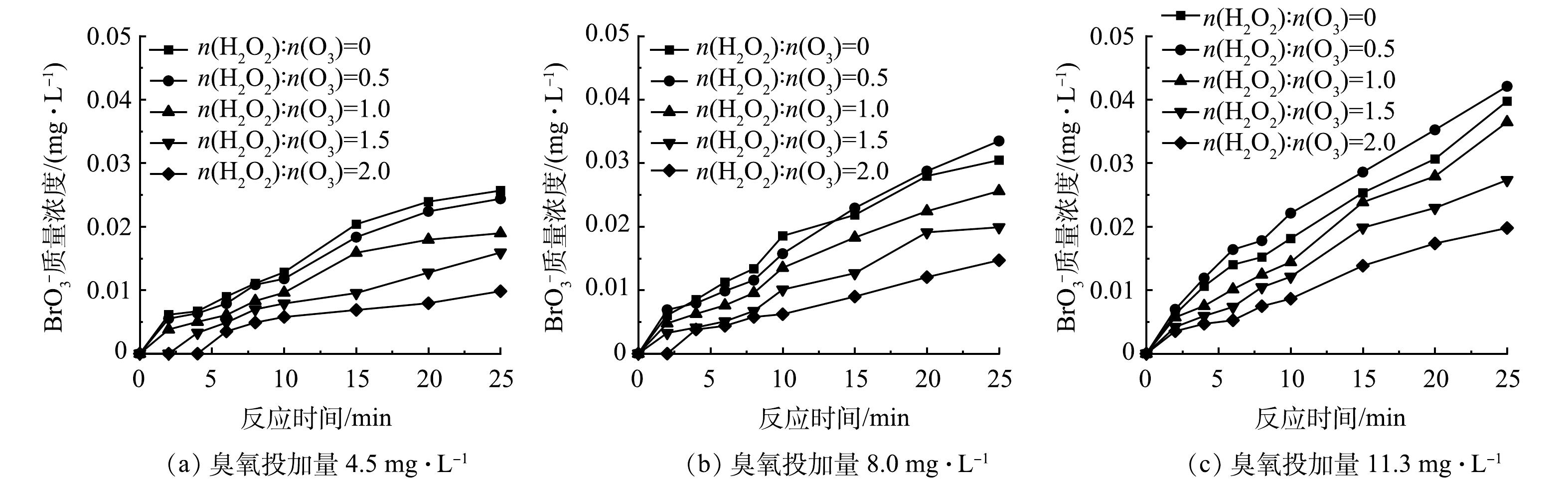
图3为不同H2O2投加量(n(H2O2):n(O3)=0.5、1、1.5和2)下HOC体系BrO3−质量浓度的变化。对于不同臭氧投加量的HOC体系,当n(H2O2):n(O3)>0.5时,H2O2对体系中BrO3−的生成具有明显的抑制作用,并且抑制作用随着H2O2投加量的增大而增强,其中当臭氧投加量为4.5 mg·L−1、n(H2O2):n(O3)=2时(图3(a)),H2O2对BrO3−的抑制率可达60%,BrO3−的生成量略低于0.01 mg·L−1。这与MIZUNO等[27]的研究结果一致,即n(H2O2):n(O3)超过1.25时能将BrO3−质量浓度控制在0.01 mg·L−1以下。这是因为过量的H2O2与生成BrO3−的重要中间产物HBrO/BrO−反应,将其还原回Br−,阻断了BrO3−的生成路径[28],同时H2O2的投加还会促进O3分解,降低了O3的暴露量,减少了HBrO/BrO−的生成,进而抑制了BrO3−的产生[11]。
由图3还可以看出,随着臭氧投加量的增加,H2O2对HOC体系中BrO3−生成的抑制效果变差,在臭氧投加量分别为4.5、8.0和11.3 mg·L−1时,当n(H2O2):n(O3)=2时对BrO3−的最大抑制率分别为60%、52%和42%,说明随着臭氧投加量的增大,O3暴露量升高,BrO3−生成量也随之增加[29]。因此,在较高臭氧投加量下投加相同摩尔比的H2O2难以达到低臭氧投加量时较好的抑制效果[30],但H2O2的投加延缓了HOC体系中BrO3−的生成。
-
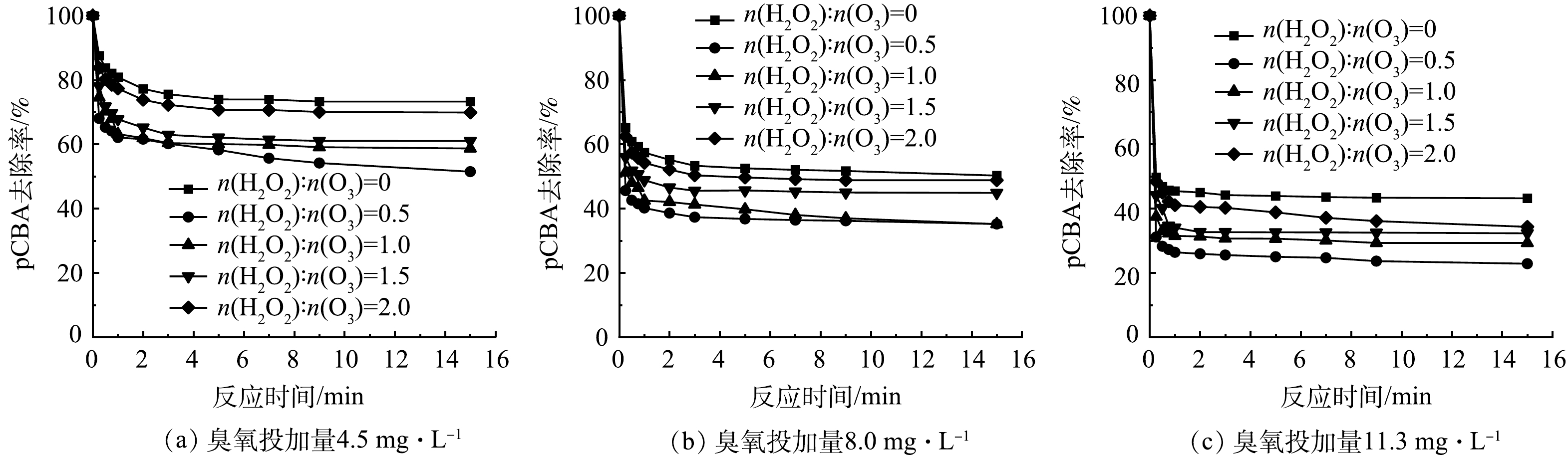
在HOC工艺中,BrO3−由Br−经臭氧直接氧化和·OH间接氧化2种途径生成[14-15],实验探究了不同臭氧投加量下投加H2O2时2种途径对BrO3−生成的贡献率。H2O2抑制条件下不同臭氧投加量的HOC体系中pCBA去除曲线(·OH的含量变化)如图4所示。随着臭氧投加量的增大,pCBA去除量增加,说明HOC体系中生成了更多的·OH。在同一臭氧投加量下,随着H2O2投加量的增大,pCBA去除量减少,说明HOC体系中的·OH浓度降低,这归因于低浓度的H2O2能促进O3分解产生·OH,而高浓度的H2O2不仅促进·OH的产生还会与·OH反应,消耗体系中的·OH[31-32]。
臭氧自分解反应一级动力学方程拟合曲线如图5所示,随着H2O2投加量的增大,HOC体系中臭氧分解前15 s的瞬时臭氧需求量(instantaneous O3 demand,IOD)增大,说明H2O2促进了臭氧的分解,降低了臭氧的质量浓度,进而抑制了BrO3−的臭氧直接氧化产生过程[33]。
H2O2抑制条件下的不同臭氧投加量的Rct值如图6所示,在HOC的反应初始阶段Rct值快速下降,中后期保持恒定。当臭氧投加量相同时,随着H2O2投加量的增大,Rct值增大,说明H2O2促进了O3的分解,使单位臭氧产生的·OH量增加;而随着臭氧投加量的增大,H2O2投加量相同时,Rct降低,说明O3的暴露量随着臭氧投加量的增加而增大。
HOC体系中·OH间接氧化和臭氧直接氧化对BrO3−生成的贡献f(·OH)和f(O3)如表1所示,结果表明,未投加H2O2时HOC体系中臭氧直接氧化对BrO3−的生成起主要作用,在不同臭氧投加量下,臭氧直接氧化的贡献率f(O3)均维持在80%以上。随着臭氧投加量的增加,HOC体系中O3的暴露量增大,臭氧直接氧化的贡献率增大,当臭氧投加量为11.3 mg·L−1时f(O3)可达到98%。
随着H2O2投加量的增大,·OH对BrO3−生成的贡献率f(·OH)增大,f(O3)相应降低,臭氧投加量为4.5 mg·L−1时,投加n(H2O2):n(O3)=2的H2O2相较于未投加H2O2使反应初始阶段f(·OH)由15.83%增加至34.44%,反应后期f(·OH)由7.90%增加至16.88%。在H2O2的抑制条件下,反应时间在0~5 min内f(·OH)逐渐减少,f(O3)逐渐增加且均在60%以上;在5~15 min的反应时间内臭氧与·OH的贡献率基本保持稳定,且f(O3)保持在80%以上。因此,在H2O2抑制条件下臭氧直接氧化仍是HOC体系中BrO3−生成的主要途径。
-
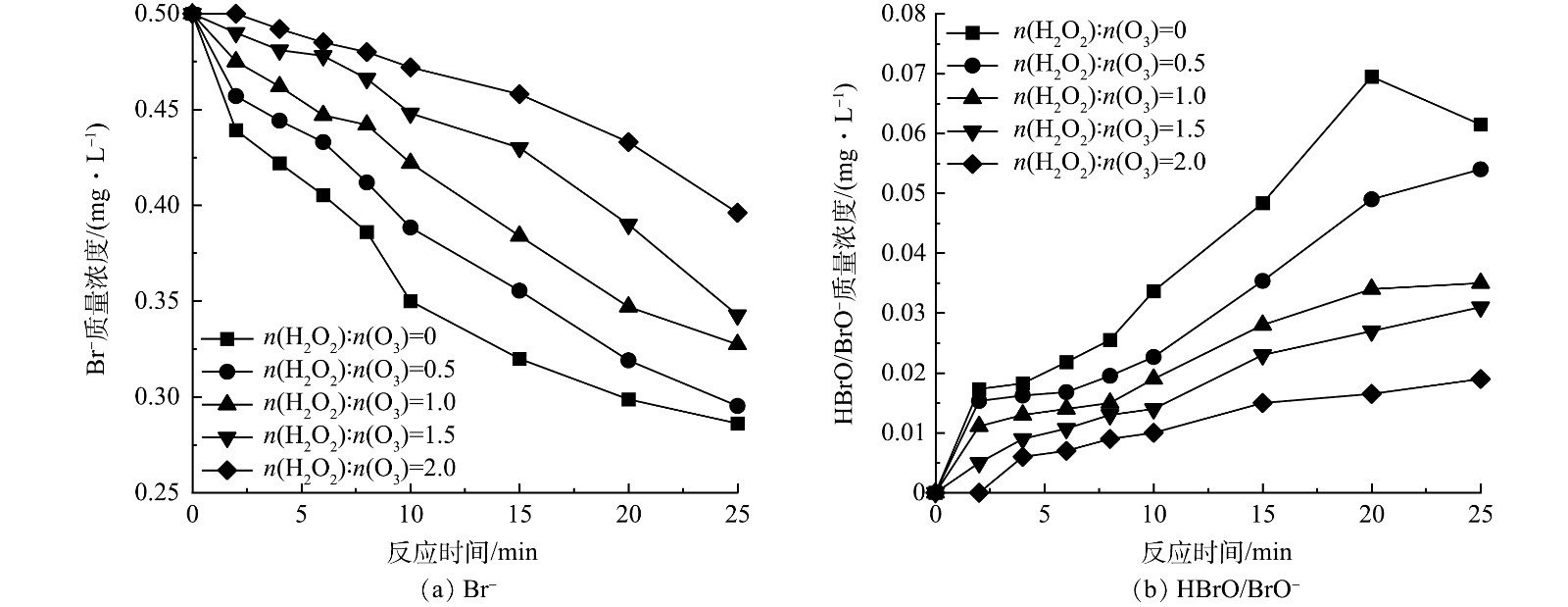
为探究HOC体系中H2O2对BrO3−生成的抑制原理,测定了臭氧投加量为4.5 mg·L−1时H2O2抑制条件下的Br−和HBrO/BrO−质量浓度变化如图7所示,BrO3−质量浓度变化如图3(a)所示。反应前期,由于H2O2的抑制,体系中HBrO/BrO−质量浓度保持在较低水平,Br−的消耗和BrO3−的生成都较为缓慢;在反应中后期,随着H2O2的消耗,其抑制作用减弱,难以继续抑制Br−的氧化,HBrO/BrO−开始积累,BrO3−生成速度加快。H2O2投加量越大,HBrO/BrO−维持低质量浓度的时间越长,BrO3−的最终生成量越低,当n(H2O2):n(O3)=2时,HBrO/BrO−在反应前10 min的质量浓度均在0.01 mg·L−1以下,BrO3−最终生成量也在0.01 mg·L−1以下。
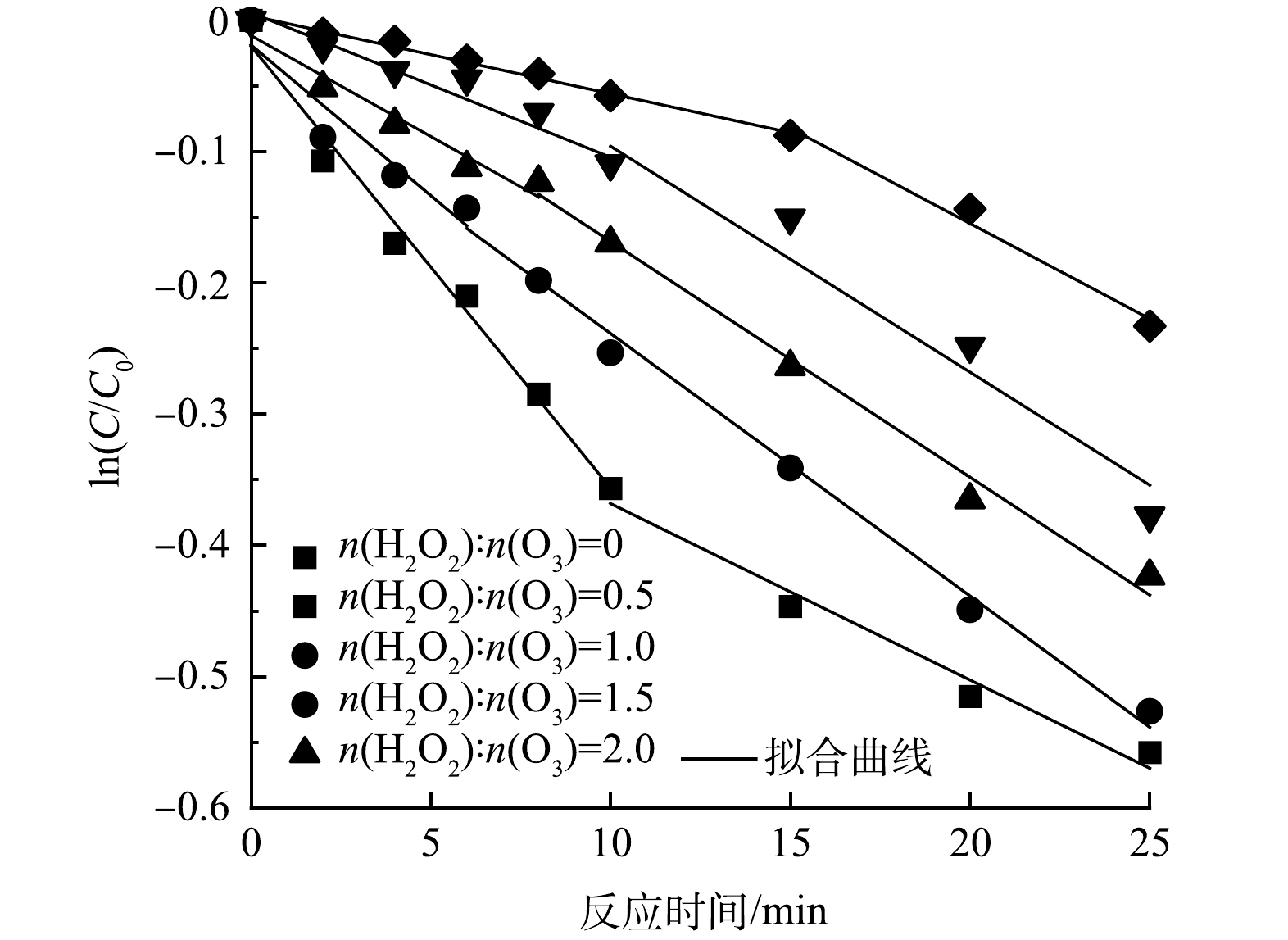
Br−的ln(C/C0)-t散点图如图8所示,可将Br−质量浓度的消耗过程分为快速阶段和慢速阶段,对两消耗阶段进行拟合,得到了不同H2O2投加量下的Br−拟一级反应速率常数kobs,具体拟合结果见表2。
根据表2,在H2O2抑制条件下的HOC体系中,当n(H2O2):n(O3)>0.5时,Br−的消耗由原本的先快速消耗后慢速消耗[34]变成了先慢速消耗后快速消耗。在反应前期,由于H2O2的抑制作用,Br−的消耗速率常数降低,且H2O2投加量越大,消耗速率常数越低,当n(H2O2):n(O3)=2时,Br−的消耗速率常数低至0.005 9 min−1。同时,H2O2投加量越大,Br−的慢速消耗时间越长,相同反应时间下BrO3−的生成量越低,说明H2O2的投加有效延缓了HOC体系中Br−的消耗和BrO3−的生成[11, 17]。在反应后期,H2O2被消耗,抑制能力减弱,Br−的消耗速率常数开始增大,BrO3−质量浓度逐渐增大。随着H2O2投加量的增大,反应后期剩余H2O2增多,促进了臭氧自分解以及·OH和H2O2的反应,快速消耗阶段的kobs减小,有效的降低了反应后期BrO3−的生成量。
因此,在HOC体系中,H2O2对BrO3−消毒副产物的抑制主要通过两个阶段进行:在反应前期,H2O2阻断了HBrO/BrO−被氧化为BrO3−的反应,有效抑制了Br−的消耗和BrO3−的生成;在反应后期,残留的H2O2加速了体系中臭氧的分解,当H2O2足够时还会与·OH反应,使反应后期体系中活性氧物质含量降低,有效减少了BrO3−的生成。在HOC体系中使用H2O2控制BrO3−的生成时,可以在保证有机物去除效果的同时通过控制反应时间处于慢速反应阶段控制BrO3−的生成。
-
在HOC体系中,H2O2对BrO3−消毒副产物的抑制主要通过慢速反应前期和快速反应后期进行,而慢速反应前期充分的H2O2能迅速地与HBrO/BrO−反应,减少BrO3−的生成,是抑制BrO3−的生成的主要阶段。
TOC去除结果表明,8.0 mg·L−1和11.3 mg·L−1的臭氧投加量对TOC的去除效果并未显著优于4.5 mg·L−1臭氧投加量,因此,控制臭氧投加量在4.5 mg·L−1,可在源头上降低BrO3−的生成量。同时,控制HOC工艺反应时间不超过15 min可以保证HOC工艺具有30%以上的有机物去除率;当n(H2O2):n(O3)=2时,可以将HOC工艺中的慢速反应前期的反应时间延长至15 min,进而控制BrO3−的生成量在0.01 mg·L−1以下。
-
1) HOC体系中随着臭氧投加量增大,TOC去除率升高, BrO3−质量浓度增大。当臭氧投加量为11.3 mg·L−1时,TOC去除率可达42.41%,但生成的BrO3−质量浓度达0.04 mg·L−1,远超国家饮用水标准规范(GB 5749-2022)。当n(H2O2):n(O3)>0.5时,H2O2能有效的抑制HOC体系中BrO3−的生成。
2) HOC体系中臭氧直接氧化是BrO3−生成的主要途径,f(O3)维持在80%以上,随着臭氧投加量增大,O3暴露量增大,f(O3)增大。在H2O2抑制条件下,反应前期f(·OH)增大,最大可达35.77%,而f(O3)均在60%以上,臭氧氧化仍是HOC体系中BrO3−生成的主要途径。
3)在H2O2抑制条件下的HOC体系中,Br−的消耗反应为先慢速反应后快速反应。反应前期H2O2抑制了Br−的氧化,且随着H2O2投加量增大,慢速反应时间增长,有效延缓了BrO3−的生成;反应后期H2O2被消耗,Br−消耗速率增大,BrO3−浓度增大,而随着H2O2投加量的增大,体系中活性氧物质减少,抑制了BrO3−的生成。
4)通过控制臭氧投加量为4.5 mg·L−1、反应时间不超过15 min以及n(H2O2):n(O3)=2可以保证HOC体系的有机物去除率在30%以上,同时控制BrO3−的生成量在0.01 mg·L−1以下。
臭氧混凝耦合体系中H2O2对溴酸盐生成的抑制效果及相关机理
Inhibitory effect and mechanism of bromate formation by H2O2 in the hybrid ozonation-coagulation process
-
摘要: 探究了臭氧混凝耦合体系(hybrid ozonation-coagulation,HOC)中H2O2对溴酸盐消毒副产物(BrO3−)的抑制效能,明确了BrO3−的主要生成途径和H2O2对BrO3−生成的抑制原理。结果表明,当n(H2O2):n(O3)>0.5时,H2O2能有效延缓BrO3−的生成。当臭氧投加量为4.5 mg·L−1、n(H2O2):n(O3)=2时,能有效的将BrO3−生成量控制在0.01 mg·L−1以下。通过对BrO3−生成贡献率和Br−消耗动力学的分析,臭氧直接氧化是HOC工艺中BrO3−生成的主要途径,贡献率维持在80%以上。在H2O2抑制条件下,•OH间接氧化贡献率有所提高,但臭氧直接氧化仍然是HOC工艺中BrO3−生成的主要途径,贡献率在60%以上。在H2O2抑制条件下,Br−的消耗反应为先慢速后快速,前期慢速反应阶段Br−的氧化过程被抑制,后期快速反应阶段中残余H2O2的存在减少了体系中活性氧物质的浓度,进而有效抑制了BrO3−的生成。
-
关键词:
- 臭氧混凝耦合工艺(HOC) /
- 溴酸盐 /
- 消毒副产物 /
- 动力学分析
Abstract: In this study, the inhibitory effect of H2O2 on bromate disinfection byproducts (BrO3−) formation in the hybrid ozonation-coagulation (HOC) process was investigated, and the main generation pathway of BrO3− and the inhibitory mechanism of BrO3− generation by H2O2 addition were clarified. The results showed that when n(H2O2):n(O3)>0.5, BrO3− formation could be effectively mitigated. When the ozone dosage was 4.5 mg·L−1 and n(H2O2):n(O3)=2, BrO3− production could be effectively controlled below 0.01 mg·L−1. Through the analysis of BrO3− generation contribution rate and Br− consumption kinetics, direct ozone oxidation was the main pathway of BrO3− generation in the HOC process, and the contribution rate maintained above than 80%. With the addition of H2O2, the contribution rate of •OH indirect oxidation increased, while ozone direct oxidation was still the main pathway for BrO3− generation with the contribution rate above 60%. With the addition of H2O2, the consumption reaction of Br− was slow at first and then became fast. The oxidation process of Br− was inhibited during slow reaction at the early stage, and the presence of residual H2O2 during fast reaction at the later stage reduced the concentration of oxidizing substances in the process, thus effectively inhibited the formation of BrO3−. -
食品加工、制药工业、皮革工业、垃圾渗滤液等废水不仅氨氮 (NH4+-N) 浓度高,还含有大量盐分[1-3]。生物法虽然作为一种经济有效的废水处理方法,但是高盐分可抑制微生物酶活,甚至引起细胞质壁分离导致微生物死亡[4-5],不利于微生物对NH4+-N的降解。因此,在对高盐废水的脱氮处理中,通常使用膜分离[6]、蒸发结晶[7]、芬顿[8]和电渗析技术[9]等物化法进行脱盐预处理,这不但使运行成本高、工艺流程长,还会造成二次污染。虽然经物化脱盐处理后的高盐含氮废水可进一步通过生物法脱氮,但去除效果并不稳定[10-11],即使在低盐度环境(<2%),传统硝化、反硝化菌和常规异养菌等常见脱氮微生物的生长代谢及活性也会受到明显抑制[12-13]。具备异养硝化-好氧反硝化(heterotrophic nitrification-aerobic denitrification, HN-AD)功能的好氧脱氮菌在好氧条件下因具备同时硝化反硝化、且无中间产物亚硝态氮 (NO2−-N) 和硝态氮 (NO3−-N) 积累的特质得到广泛关注[14]。不仅如此,部分HN-AD菌属还兼具耐盐性,已被广泛应用于高盐废水处理过程,如不动杆菌属 (Acinetobacter) 、盐单胞菌属 (Halomonas) 、副球菌属 (Paracoccus) [15]等。然而,在工程应用中,许多工业废水的盐度波动大,这使得包括HN-AD菌在内的众多微生物难以快速适应不同的盐度环境,菌群无法实现高效富集,进而影响废水处理效果[16-17]。为了增强微生物对高盐胁迫的抵抗能力,已有研究[18]通过增加盐浓度驯化功能菌属耐盐性能的方式以期获得高去污效率、高富集丰度的耐盐型脱氮功能微生物。然而,在实际应用中却发现,即使经过长期驯化,功能微生物对高盐胁迫的抵抗能力仍较弱[19-20],原因在于功能微生物易流失、难截留导致富集丰度较低,最终影响废水处理效果的稳定性[19, 21-22]。因此,为解决这一问题,亟待研发一种即可提高微生物对高盐胁迫的抵抗能力,又可提高功能菌属生长富集能力的新技术。
微生物在逆境中可通过积累或从环境中吸收相容性溶质 (compatible solutes, CS) 来抵抗外部条件带来的胁迫作用,在不需要细胞内酶的任何特殊适应下即可保护细胞免受不可逆转的损害[23-24]。所以CS在细胞中发挥了重要作用,它不仅不会阻碍正常的细胞代谢,还可以平衡细胞质内的渗透压以增强微生物的活性[23, 25]。在VYRIDES等[26]的研究中,盐度为4%时,假单胞菌株 (Pseudomonas sp strain ADP) 产生的相容性溶质主要为海藻糖;ZHANG等[27]在使用颗粒污泥处理含盐养殖废水的过程中,添加1 000 μmol·L−1的海藻糖,可使产甲烷活性和磷酸酶活性分别提高22%和27%。而海藻糖作为一种价格低、易采购的典型相容性溶质,在高盐废水处理中已被成功应用[28-29]。其作为渗透调节剂易被微生物吸收利用,通过调节细胞渗透压帮助微生物快速适应高盐环境,提升去污能力[26]。目前,已有海藻糖用于高盐废水的厌氧处理系统的相关报道[29-30]。BAI等[30]研究了在序批式反应器中添加海藻糖考察了厌氧氨氧化细菌处理富氮含盐废水的长期脱氮性能,在添加浓度为300 μmol·L−1时,就可使NH4+-N、NO2−-N的去除率分别提高为32.4%和42.2%;杨振琳等[28]通过添加海藻糖强化厌氧化耦合反硝化工艺,在盐度为3.2%的模拟废水中加入250 μmol·L−1的海藻糖,NH4+-N和NO2−-N的去除速率分别提高了81.25%和75%。可见海藻糖对提高长期脱氮效果有显著性作用,但其在高盐废水好氧生物处理中的研究却鲜有报道。盐度显著影响微生物的物理和生化特性,长期作用甚至能够改变整个环境的微生物群落结构[31]。
本研究利用膜曝气生物膜反应器 (membrane aerobic biofilm reactor, MABR) 富集好氧脱氮菌,通过调节外加海藻糖的浓度,采用高通量测序等分析方法,从微生物脱氮性能、群落结构及脱氮功能基因丰度等层面,研究海藻糖浓度梯度对高盐废水中微生物的物种丰度、菌群多样性及脱氮功能基因的影响,旨在为推动好氧脱氮菌在高盐废水好氧生物脱氮处理的实际应用提供理论基础及新技术思路。
1. 材料与方法
1.1 MABR实验装置与运行条件
在实验过程中,建立了5个MABR,工作体积为0.85 L,反应装置见图1。反应器的膜组件由128根中空纤维膜组成,用于空气运输和生物膜附着,中空纤维是用复合聚合物材料制造,只允许气体分子渗透。纤维的外径为300 μm,内径为200 μm,膜孔径为0.1 μm,有效比表面积为1.76 cm2·cm−3。膜组件一端通过流量计和压力表连接到空气泵,另一端连接到底端曝气管形成氧循环,曝气压力设定为10 kPa,进出水均采用蠕动泵完成,水力停留时间为48 h[32]。反应器顶部留有取样口,用于采样和溶解氧 (DO) 监测等操作。
1.2 实验用水及菌液接种
合成的高盐高氮废水由无水CH3COONa (碳源) 、(NH4)2SO4 (氮源) 、NaCl和微量元素组成。进水COD为5 000 mg·L−1,NH4+-N为500 mg·L−1,盐度为2.5%,微量元素为50 mL·L−1。微量元素配方: MgSO4·7H2O 2.0 g·L−1,MnSO4·H2O 0.1 g·L−1,CaCl2 1.5 g·L−1,FeSO4·7H2O 0.1 g·L−1,K2HPO4 5.0 g·L−1。
该研究的接种菌液中主要为产碱杆菌(Alcaligenes)、不动杆菌(Acinetobacter sp.TAC-1)和假单胞菌 (Pseudomonas) 等具备HN-AD功能的好氧脱氮混合菌群。这些细菌主要分离于猪场沼液、垃圾渗滤液和化工废水,可耐受高浓度氨氮。为确保适当的菌液浓度和脱氮活性,首先进行菌液驯化,再分别接种于5个反应器中进行挂膜。挂膜完成后,分别加入不同浓度海藻糖 (0、40、120、360和1 080 μmol·L−1) 进行实验,对应反应器分别为C0、C40、C120、C360和C1 080。
1.3 水质分析方法及生物膜表观特征分析
反应器启动运行阶段的溶氧、盐度及pH值分别采用便携式溶氧仪、海水比重计及pH计进行直接测量。菌液浓度 (OD600 nm) 采用紫外分光光度法测定,进、出水NH4+-N、NO3−-N、NO2−-N、TN和COD的浓度均参照文献中的方法[33]进行检测。
利用扫描电镜 (scanning electron microscope, SEM) 技术表征反应器挂膜阶段的生物膜表观形态特征。将采集的生物膜样品经过固定、PBS清洗、乙醇梯度脱水 (30%、50%、70%、85%和95%质量分数的乙醇洗脱1次,100%乙醇洗脱2次(每次脱水时间为15~20 min)) 、冷冻干燥等步骤完成样品预处理,将制备完成的样品送至武汉铄思百检测技术有限公司并进行SEM观察。
1.4 DNA提取、高通量测序及脱氮功能基因表达
在各反应器稳定运行阶段,采集微生物样品(每个反应器重复采集3次样品,每个样品约0.5 g),将样品短期保存于−80 ℃冰箱中。采用通用检测试剂盒 (MOBIO实验室,美国) 提取样品的总基因组DNA,采用引物338F和806R扩增V3~V4区域的l6S rRNA基因,测序引物序列为338F(5'-ACTCCTACGGGAGGCAGCA-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')。采用Trimmomatic和Flash软件对测序序列进行拼接,通过Usearch 软件对具有97%相似性的序列进行OTU聚类,经Usearch_global 获得OTU序列丰度统计表,进行后续微生物群落多样性分析;基于京都基因和基因组百科全书(http://www.genome.jp·KEGG)数据库及PICRUSt1软件,对样品中微生物脱氮功能基因进行预测分析。
2. 结果与讨论
2.1 反应器启动及不同海藻糖浓度下的脱氮性能分析
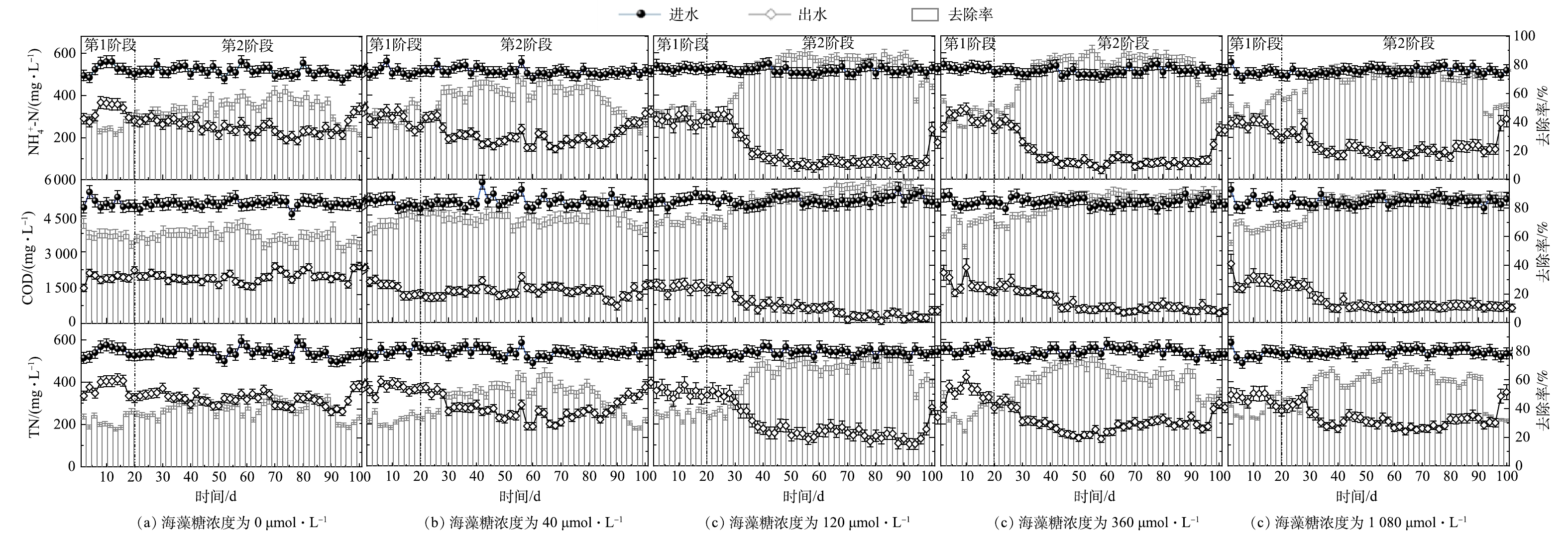
SEM表征结果显示,反应器启动运行20 d,膜丝上明显附着了大量的以杆菌和球菌为主的微生物 (图2) ,说明反应器于20 d内成功完成挂膜启动。该研究反应器菌液挂膜时间较文献报道相关结果[32-34]略有增加,这可能是因为盐度抑制了微生物的生长繁殖,从而导致挂膜周期延长。反应器启动运行阶段的污染物去除情况如图3(a)~图3(e)中第1阶段所示。5个平行反应器的NH4+-N、TN及COD去除率分别为32%~45%、32%~40%和60%~71%,无明显有害中间产物NO2−-N和NO3−-N的积累。启动阶段反应器脱氮性能较低,究其原因主要在于高盐环境对反应器富集的脱氮微生物的生长及活性存在影响。高盐度会使微生物细胞处于一个高渗环境,影响细胞正常生长代谢,进而降低污染物的去除率[35]。
在4个平行反应器中添加不同浓度海藻糖 (40、120、360和1 080 μmol·L−1) ,设定为实验组 (C40、C120、C360和C1 080) ,对照组 (C0) 不添加海藻糖,连续运行80 d结束。添加海藻糖后的反应器运行性能如图3(a)~图3(e)中第2阶段所示。相较于对照组,4个实验组中NH4+-N去除率分别提高了10.70%、32.72%、27.36%、19.45%,TN去除率分别提高了8.32%、28.36%、22.53%、17.63%,COD去除率分别提高了12.09%、31.14%、25.27%、25.06%。这说明添加海藻糖对高盐给微生物带来的高渗胁迫具有缓解作用,提高了系统脱氮性能。C120组的NH4+-N、TN及COD去除率最高,C360组的TN去除率及C1 080组的NH4+-N、TN去除率相较C120组降低,3组中COD去除率无明显变化。可以看出,外源海藻糖浓度与污染物去除率无线性相关性,最适海藻糖浓度为120 μmol·L−1。这主要是因为微生物对海藻糖的最大渗透调节剂有一定的吸收范围[28],当体系内海藻糖浓度超过微生物作为渗透调节剂的吸收浓度范围时,过剩的海藻糖可充当常规异养反硝化菌 (heterotrophic denitrified bacteria, HDB) 的有机碳源[28]。因此,在本研究中,高浓度海藻糖 (360、1 080 μmol·L−1) 条件可能对体系内HDB生长更有利,进而影响好氧脱氮菌群的富集与活性,降低了反应器脱氮性能。
2.2 外源性海藻糖作用下的微生物特性分析
1) 微生物α多样性分析。通过微生物群落分析研究不同海藻糖浓度对反应器中物种丰富度及多样性的影响,结果如表1所示。通过MiSeq Illumina测序分析获得269~303个OTU,覆盖指数均大于99%,说明测序深度包含测序样品中的全部细菌数。Ace指数和Chao指数均为物种丰富度的指标,实验组较对照组有所增加,表明添加海藻糖提升了高盐环境下系统内的物种丰富度。Shannon指数反映微生物多样性特征,其数值同样在实验组中有所增长,说明添加海藻糖丰富了高盐环境下系统内的菌群多样性。C120组的Chao指数、Ace指数以及Shannon指数均最高,说明120 μmol·L−1的海藻糖浓度对增强高盐胁迫下微生物群落的抵抗力稳定性最有利。
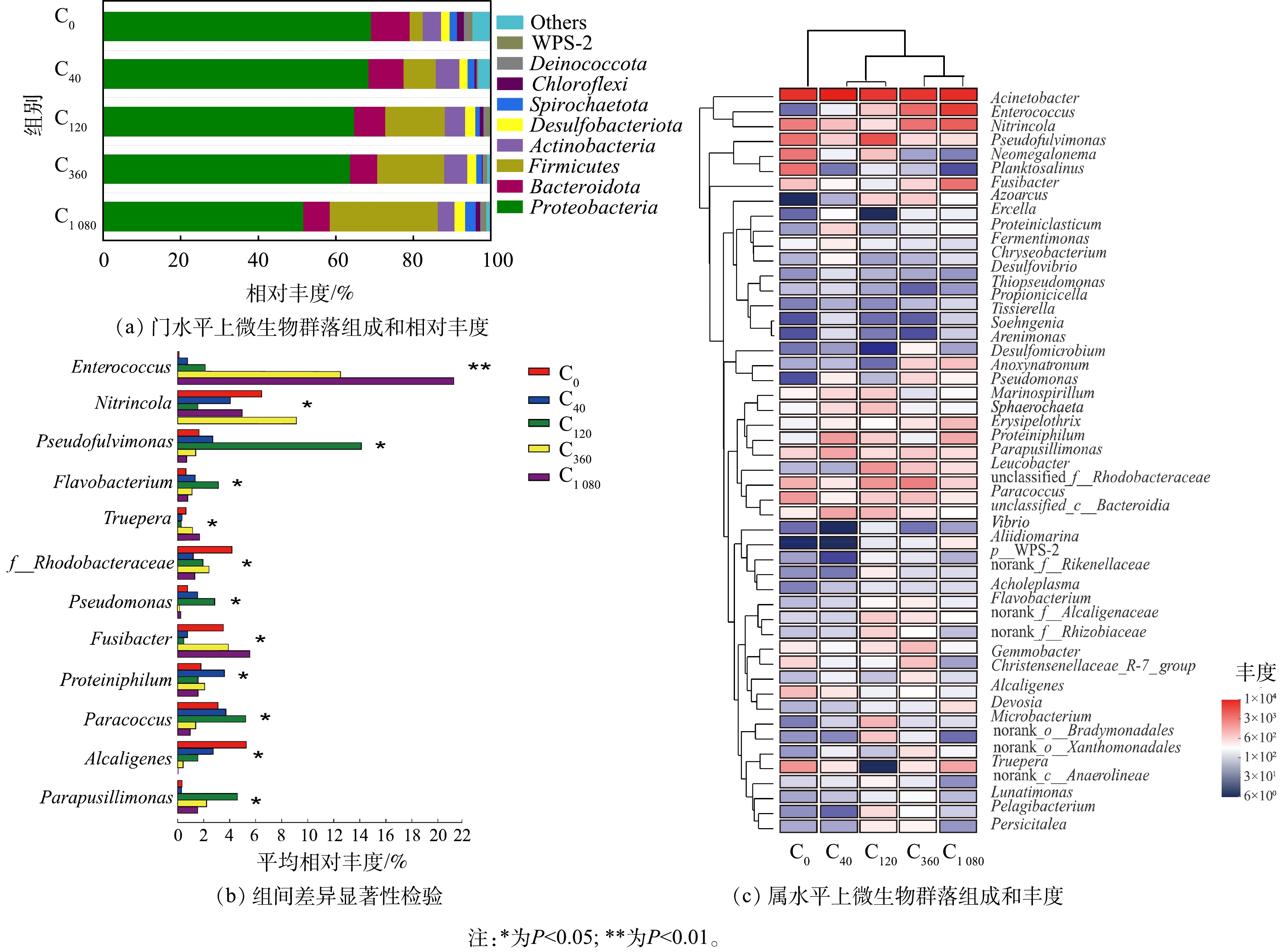
表 1 不同海藻糖浓度下微生物Alpha多样性指数Table 1. Alpha diversity indices at different trehalose concentrations反应器 OTUs 覆盖率/% Chao指数 Ace指数 Shannon指数 C0 269 99.82 320.50 314.21 3.06 C40 274 99.82 331.34 320.83 3.24 C120 303 99.82 375.63 370.12 3.83 C360 297 99.78 352.38 367.88 3.66 C1 080 286 99.82 330.13 332.30 3.35 2) 微生物群落组成分析。不同海藻糖浓度下微生物群落组成相似但相对丰度略有差异(图4)。如图4(a)所示,门水平相对丰度排名前3的优势菌门分别为变形菌(Proteobacteria)、拟杆菌(Bacteroidota)和厚壁菌(Firmicutes)。三者的总相对丰度在对照组C0中为82.60%,在各实验组 (C40、C120、C360和C1 080) 中分别提高了3.29%、5.64%、5.49%和3.84%,说明在高盐条件下添加海藻糖对系统中门水平的群落结构具有一定影响。有报道[36-37]指出,Proteobacteria和Bacteroidota在高盐、高氨氮废水处理中常占据主导地位,其包含着多样性最丰富的硝化和反硝化细菌 (如HN-AD菌) ;也有报道[38]指出,可在极端环境进行异养硝化的脱氮微生物 (如肠球菌属Enterococcus) 归属于Firmicutes。该3类菌门中微生物总相对丰度的增加说明添加海藻糖有利于高盐胁迫下脱氮菌群的生长富集。
由属水平相对丰度排名前50的微生物进行层级聚类Heatmap分析结果 (图4(c)) 可知,在C0组中,不动杆菌属 (Acinetobacter) 相对丰度为34.58%,是系统内的优势菌属,Acinetobacter在高氨氮浓度下是硝化和反硝化过程中生长的主要菌群,表现出高效的HN-AD能力[39],且具有耐受高盐、高氨氮和脱氮速率快的优点[40]。而添加海藻糖的4个实验组中,高丰度优势菌属仍为Acinetobacter且相对丰度保持稳定(分别为35.69%、34.95%、34.93%和31.04%)。这说明在高盐环境下,海藻糖对Acinetobacter生长富集的影响较弱,但Acinetobacter保证了高盐系统内的高脱氮效率。在C120组中,假黄褐藻属 (Pseudofulvimonas) 相对丰度明显高于对照组和其他实验组,并且其相丰度变化存在显著性差异 (P <0.05) (图4(b)) 。Pseudofulvimonas相对丰度在低浓度海藻糖时 (40、120 μmol·L−1),随海藻糖浓度的增加而增长,但在高浓度海藻糖时 (360、1 080 μmol·L−1) ,却随海藻糖浓度的增加而减少。Pseudofulvimonas为耐盐型HN-AD菌,是高盐废水处理过程中常见的脱氮功能微生物[41-42];同时,黄杆菌属 (Flavobacterium) [43]、红杆菌属 (Rhodobacteraceae) [44]、假单胞菌属 (Pseudomonas) [16]、副球菌属 (Paracoccus) [45]和产碱菌科 (Parapusillimonas) [46]等耐盐型HN-AD菌在海藻糖浓度作用下的相对丰度变化规律与Pseudofulvimonas一致并同样存在显著性差异 (P<0.05) (见图4(b)) 。Pseudofulvimonas通常与各种氮物质降解过程有关[47];Flavobacterium与生物絮体聚集和颗粒稳定性有关,其丰度增加有利于功能微生物的富集进而保证污染物稳定有效的去除[42, 48];Rhodobacteraceae是海水形成初始生物膜的主要定殖者[44],其具有较强的耐盐性能,能将NH4+-N转化为NO3−-N和NO2−-N,且可在曝气的条件下实现对NO3−-N的高效去除[49-50];Pseudomonas、Paracoccus具有亚硝酸盐还原和有机物降解等多种功能,在有机物去除方面起着关键作用[51-52]。当海藻糖浓度为120 μmol·L−1时,这些HN-AD菌属相对丰度均达到最高。说明低浓度海藻糖促进高盐废水中耐盐型HN-AD菌生长富集,使系统内主要发生异养硝化和好氧反硝化过程,可强化微生物对氮、碳污染物的去除性能。
在C360和C1 080组中,Enterococcus相对丰度由C0中的0.12%分别增至13.88%和21.22% (P <0.05) (图4(b)) 。Enterococcus是一种兼性脱氮菌[53],具有较强的脱氮耐盐性能及高效的产絮凝效果,在生长代谢过程中产生多糖、蛋白质、脂和核酸等成分,可促进水体中菌体细胞凝聚进而减缓功能微生物的流失[54-55]。Enterococcus相对丰度在C360和C1 080组得到明显提升,说明高浓度海藻糖的作用倾向于通过增强高盐条件下微生物凝聚能力,提高功能菌群富集。此外,硝化细菌属 (Nitrincola) 、特吕珀菌属 (Truepera) 和梭菌属 (Fusibacter) 3种HDB的相对丰度在高浓度海藻糖时 (360、1 080 μmol·L−1) 也呈现增长趋势。Nitrincola是一类耐盐碱的厌氧反硝化细菌[15],能够在极端环境中对地球化学元素循环起促进作用[56];Truepera[32]与厌氧反硝化作用密切相关[57],且能够在碱性、中等盐度和高温等多种极端条件下生长,有利于NO向N2O的转换[58-59];Fusibacter是一类耐盐、厌氧的棒杆细菌,可将硫酸盐和元素硫还原成硫化物,还能够广泛利用碳水化合物 (如乙酸、葡萄糖等) 生成CO2和H2等产物[60],且具有脱氮除磷的功能[61]。上述3种菌属均在高浓度氨氮环境的反硝化过程中发挥重要作用,其相对丰度在高海藻糖浓度作用下提高,也证实高浓度海藻糖促进高盐废水中HDB生长富集,使系统内主要发生常规异养反硝化过程。这主要是因为高浓度海藻糖促进Enterococcus相对丰度大幅增加,虽有利于微生物凝聚,但同时也产生大量菌胶团聚集堵塞膜孔,致使生物膜层出现缺氧环境,不利于好氧脱氮微生物的生长,继而引起HDB增殖。虽然HDB相对丰度在高海藻糖浓度下的增长促使C360和C1 080组的NH4+-N和TN去除率相比C0组有所提高,但其相比C40和C120组却呈下降趋势,推测耐盐型HN-AD菌的相对丰度变化对系统脱氮性能的影响相比HDB更为显著和重要,而HDB的相对丰度变化主要影响了系统的脱氮菌群结构。
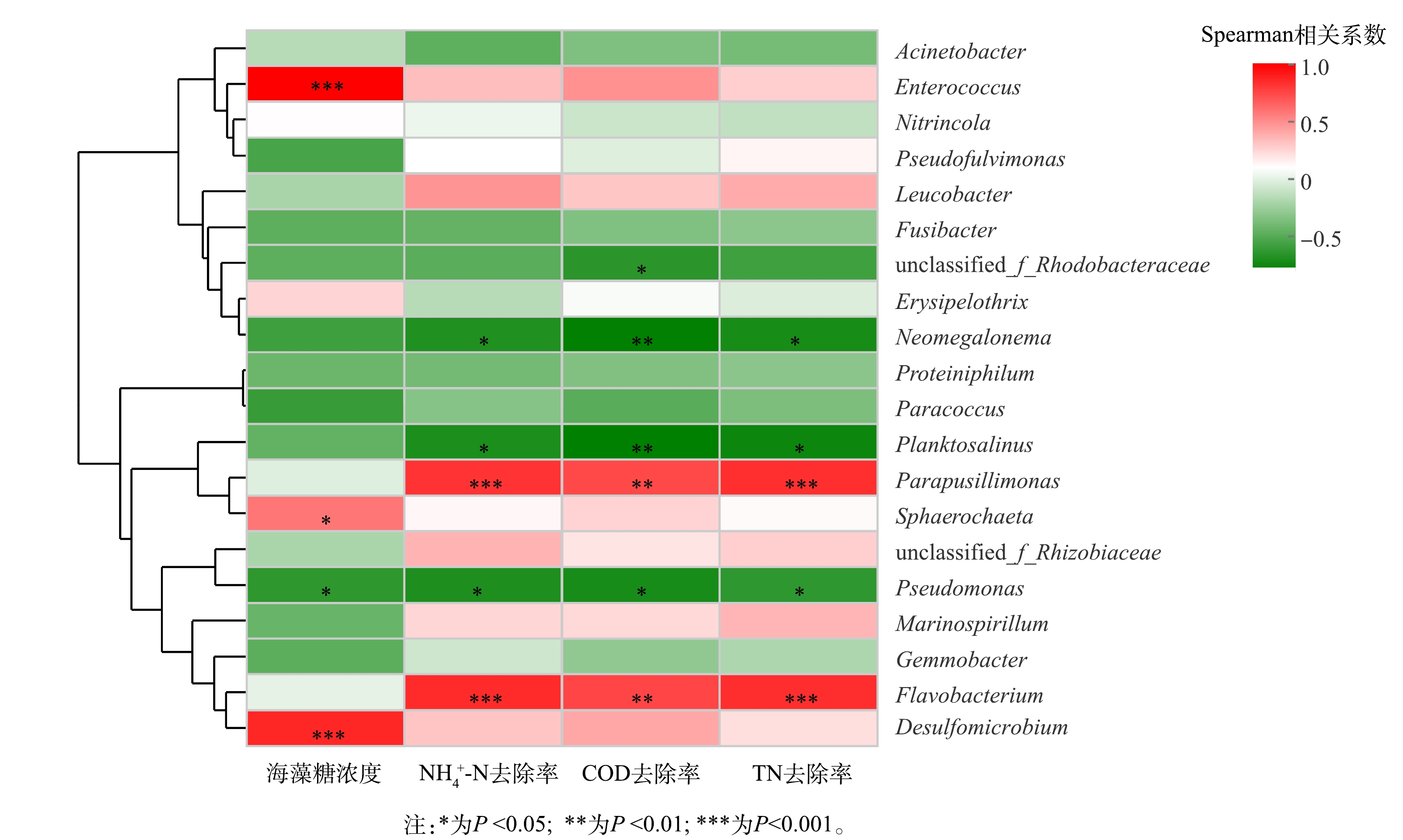
3) 环境因子相关性分析。通过相关性Heatmap图进一步分析环境因子对系统内属水平群落组成的影响,结果如图5所示。与NH4+-N、COD及TN去除率和海藻糖浓度4个因子均显著关联的只有Pseudomonas的相对丰度,且呈负相关;NH4+-N、COD及TN去除率与Flavobacterium、Parapusillimonas 2种耐盐型HN-AD菌属相对丰度呈正相关,与浮游盐属 (Planktosalinus) 、新巨藻属(Neomegalonema)相对丰度呈负相关。Planktosalinus归属黄杆菌科 (Flavobacteriaceae) ,而Flavobacteriaceae是废水系统发生污泥膨胀的指示微生物[62-63];Neomegalonema同样属于污泥膨胀菌群,其丰度变化用于表征氮磷失衡下废水中的微生物群落健康状况[64-65]。海藻糖浓度与Enterococcus、球毛菌属 (Sphaerochaeta) 和脱硫微杆菌属 (Desulfomicrobium) 相对丰度呈正相关。可以看出,不同菌属相对丰度受到海藻糖浓度、污染物去除率影响的情况存在差异,可证明耐盐型HN-AD菌确为系统内主要脱氮贡献者,显著影响反应器的脱氮性能;以Enterococcus为代表的传统脱氮菌和其他功能微生物的相对丰度变化规律则主要反映了海藻糖浓度梯度对高盐废水中脱氮菌群组成的差异影响。
2.3 脱氮功能基因预测分析
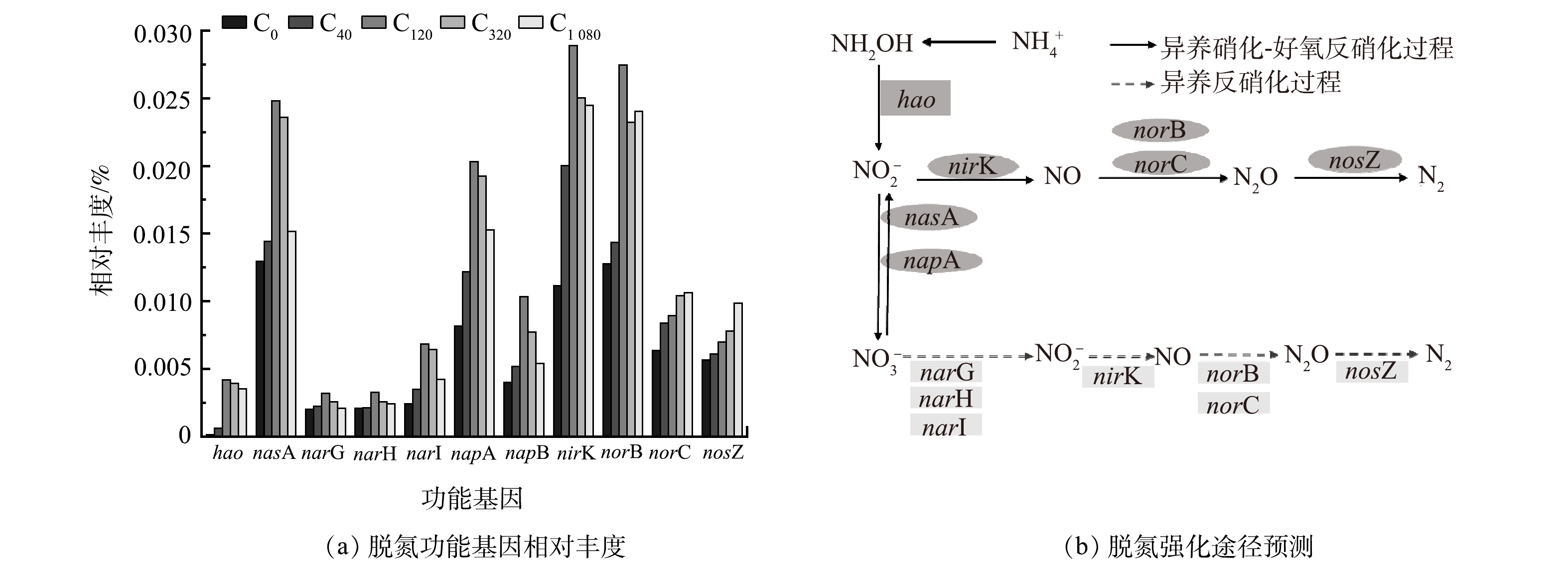
采用PICRUSt1对功能基因丰度进行分析,其相对丰度变化结果见图6(a)。该研究获得与硝化过程相关的羟胺氧化酶基因hao,是NH2OH氧化生成NO2−-N过程的关键酶基因[66],其在实验组 (C40、C120、C360和C1 080) 中相对丰度相较对照组 (C0) 分别提高了4.96倍、34.70倍、32.45倍和29.06倍,说明添加海藻糖明显加快系统内微生物的硝化进程。同时,还获得8个与反硝化过程相关的功能基因,包括硝酸盐还原酶(nasA、nasB、narG、narH、narI、napA、napB)、亚硝酸盐还原酶(nirK)、一氧化氮氧化酶(norB、norC)和一氧化二氮还原酶(nosZ)。4个实验组中反硝化功能基因总相对丰度较对照组分别提高了1.31倍、2.86倍、1.81倍和1.75倍,说明添加海藻糖同样促进了系统内微生物的反硝化进程。
硝酸还原酶催化细菌体内NO3−-N还原生成NO2−-N,是实现反硝化过程的关键酶之一。nasA是一种同化型硝酸盐还原酶基因,存在于细菌的细胞质中[67],也常见于HN-AD菌[68]。其在实验组中的相对丰度值相较对照组均有提高,低浓度海藻糖时 (40、120 μmol·L−1) ,nasA基因相对丰度随海藻糖浓度的增加而增长,于海藻糖浓度为120 μmol·L−1时达到最高值;但在高浓度海藻糖时 (360、1 080 μmol·L−1) ,其随海藻糖浓度增加出现降低。同样,异化型硝酸盐还原酶NAP的基因napA和napB相对丰度变化规律与nasA一致。NAP表达在好氧条件下占主导地位,常存于HN-AD菌中[69]。另一种异化型硝酸还原酶NAR的基因narG、narH和narI相对丰度却在海藻糖浓度为360 μmol·L−1和1 080 μmol·L−1时增加,而NAR表达在缺氧条件下占主导地位,常见于HDB[70]。以上结果说明,在高盐废水添加海藻糖可诱导增强以HN-AD菌和HDB为主的脱氮菌群的反硝化活性。低浓度海藻糖倾向于强化系统的异养硝化-好氧反硝化途径,而高浓度海藻糖则偏向于促进系统的异养反硝化途径 (图6(b)) 。
亚硝酸盐还原酶NIR是反硝化过程的另一类关键酶,驱动NO2−-N还原生成气体产物NO,存在于细胞膜外生物细胞质中,其基因有nirS和nirK 2种类型[71]。海藻糖的加入提高了nirK的相对丰度,且在海藻糖浓度为120 μmol·L−1时达到最高值,推进了系统的亚硝酸盐还原进程。NO还原酶基因 (norB和norC) 和nosZ分别是催化NO还原生成N2O、N2O进一步还原生成最终产物N2的关键酶基因。在污水处理中,反硝化细菌体内nosZ活性的降低或不具有nosZ是导致反硝化过程中温室气体N2O大量积累的主要因素[72]。该研究nosZ的相对丰度随着海藻糖浓度的增加而升高,说明添加海藻糖对控制好氧脱氮过程的N2O产生与积累具有一定作用。以上基因预测结果也进一步证明,海藻糖浓度为120 μmol·L−1时,反应器的NH4+-N、TN去除率最高 (图2) 。这主要是因为此海藻糖浓度条件激发HN-AD菌的硝化和反硝化进程达到最快,极大程度加速了NH4+-N氧化及NO3−-N和NO2−-N的还原,最终使反应器脱氮性能达到最优。
3. 结论
1) 添加海藻糖的实验组 (40、120、360和1 080 μmol·L−1) 中NH4+-N、TN和COD去除率相较对照组 (0 μmol·L−1) 显著提高,最适海藻糖浓度为120 μmol·L−1。外加海藻糖可优化高盐条件下的反应器脱氮性能。
2) 海藻糖浓度对脱氮菌群的相对丰度具有显著影响。低浓度海藻糖 (40、120 μmol·L−1) 有利于耐盐型HN-AD菌相对丰度的提高,而高浓度海藻糖 (360、1 080 μmol·L−1) 更倾向于促进HDB的富集;耐盐型HN-AD菌是系统的主要脱氮贡献者,其相对丰度变化与污染物去除率之间存在显著相关性,传统脱氮菌相对丰度变化则与高盐废水中脱氮菌群组成差异有关。耐盐型HN-AD菌对调控高盐条件下的反应器脱氮性能起着重要影响。
3) 海藻糖可有效提高以HN-AD菌和HDB为主的脱氮菌群的硝化和反硝化活性。在低浓度海藻糖 (40、120 μmol·L−1) 作用下,与HN-AD菌关联的硝化、反硝化基因(hao、nasA、napA和napB)丰度随海藻糖浓度的增加而增长,系统的异养硝化-好氧反硝化途径得到强化;在高浓度海藻糖 (360、1 080 μmol·L−1) 作用下,与HDB关联的反硝化基因 (narG、narH和narI) 相对丰度明显增加,系统的异养反硝化途径得到增强。
-
表 1 H2O2抑制条件下不同臭氧投加量的溴酸盐生成贡献率
Table 1. Contribution rate of Bromate formation at different ozone dosages with the addition of H2O2
臭氧/(mg·L−1) n(H2O2):n(O3) 不同反应时间下的f(·OH)/f(O3) 0.5 min 0.75 min 1 min 2 min 3 min 5 min 7 min 9 min 15 min 4.5 0 0.16/0.84 0.13/0.87 0.11/0.89 0.10/0.90 0.09/0.91 0.08/0.92 0.08/0.92 0.08/0.92 0.08/0.92 0.5 0.17/0.83 0.13/0.87 0.14/0.86 0.09/0.91 0.08/0.92 0.08/0.92 0.10/0.90 0.11/0.89 0.13/0.87 1 0.25/0.75 0.21/0.79 0.26/0.74 0.17/0.83 0.15/0.85 0.13/0.87 0.13/0.87 0.13/0.87 0.13/0.87 1.5 0.36/0.64 0.28/0.72 0.26/0.74 0.19/0.81 0.18/0.82 0.15/0.85 0.15/0.85 0.15/0.85 0.15/0.85 2 0.34/0.66 0.27/0.73 0.23/0.77 0.20/0.80 0.18/0.82 0.17/0.83 0.16/0.84 0.17/0.83 0.17/0.83 8.0 0 0.12/0.88 0.09/0.91 0.08/0.92 0.05/0.95 0.05/0.95 0.04/0.96 0.03/0.97 0.03/0.97 0.03/0.97 0.5 0.13/0.87 0.10/0.90 0.09/0.91 0.07/0.93 0.06/0.94 0.05/0.95 0.05/0.95 0.05/0.95 0.06/0.94 1 0.15/0.85 0.12/0.88 0.16/0.84 0.09/0.91 0.08/0.92 0.08/0.92 0.08/0.92 0.09/0.91 0.10/0.90 1.5 0.19/0.81 0.14/0.86 0.13/0.87 0.10/0.90 0.09/0.91 0.07/0.93 0.07/0.93 0.07/0.93 0.07/0.93 2 0.24/0.76 0.18/0.82 0.16/0.84 0.11/0.89 0.11/0.89 0.09/0.91 0.09/0.91 0.09/0.91 0.09/0.91 11.3 0 0.08/0.92 0.06/0.94 0.05/0.95 0.03/0.97 0.03/0.97 0.02/0.98 0.02/0.98 0.02/0.98 0.02/0.98 0.5 0.14/0.86 0.11/0.89 0.10/0.90 0.06/0.94 0.05/0.95 0.05/0.95 0.05/0.95 0.05/0.95 0.06/0.94 1 0.20/0.80 0.13/0.87 0.11/0.89 0.07/0.93 0.06/0.94 0.05/0.95 0.05/0.95 0.05/0.95 0.05/0.95 1.5 0.18/0.82 0.24/0.76 0.19/0.81 0.13/0.87 0.10/0.90 0.09/0.91 0.08/0.92 0.08/0.92 0.08/0.92 2 0.21/0.79 0.21/0.79 0.18/0.82 0.11/0.89 0.09/0.91 0.08/0.92 0.09/0.91 0.10/0.90 0.11/0.89 表 2 H2O2抑制条件下的Br-消耗的一级速率常数(kobs)
Table 2. kobs of Br- consumption with the addition of H2O2
n(H2O2):n(O3) 反应时间/min 拟合方程式 k/min-1 R2 0 0~10 y = −0.033 7x−0.019 70 0.033 7 0.985 10~25 y = −0.013 4x−0.234 00 0.013 4 0.976 0.5 0~6 y = −0.022 9x−0.018 86 0.022 9 0.950 6~25 y = −0.020 0x−0.038 59 0.020 0 0.990 1 0~8 y = −0.015 4x−0.011 67 0.015 4 0.955 8~25 y = −0.018 0x+0.011 12 0.018 0 0.990 1.5 0~10 y = −0.011 0x+0.005 83 0.011 0 0.971 10~25 y = −0.017 2x+0.076 27 0.017 2 0.983 2 0~15 y = −0.005 9x+0.003 51 0.005 9 0.991 15~25 y = -0.014 5x+0.135 60 0.014 5 0.983 -
[1] JIN X, JIN P, HOU R, et al. Enhanced WWTP effluent organic matter removal in hybrid ozonation-coagulation (HOC) process catalyzed by Al-based coagulant[J]. Journal of Hazardous Materials, 2017, 327: 216-224. doi: 10.1016/j.jhazmat.2016.12.043 [2] JIN X, SHI Y, HOU R, et al. Role of Al-based coagulants on a hybrid ozonation–coagulation (HOC) process for WWTP effluent organic matter and ibuprofen removal[J]. Environmental Science:Water Research & Technology, 2019, 5(3): 599-608. [3] JIN X, WANG Y, ZHANG W, et al. Mechanism of the hybrid ozonation-coagulation (HOC) process: Comparison of preformed Al13 polymer and in situ formed Al species[J]. Chemosphere, 2019, 229: 262-272. doi: 10.1016/j.chemosphere.2019.04.225 [4] 刘芳蕾, 张冬, 吕锡武. 臭氧生物活性炭工艺运行中产生溴酸盐的可能性分析[J]. 中国环境科学, 2014, 34(9): 2299-2305. [5] RUFFINO B, KORSHIN G V, ZANETTI M. Use of spectroscopic indicators for the monitoring of bromate generation in ozonated wastewater containing variable concentrations of bromide[J]. Water Research, 2020, 182: 116009. doi: 10.1016/j.watres.2020.116009 [6] JIN X, XIE X, LIU Y, et al. The role of synergistic effects between ozone and coagulants (SOC) in the electro-hybrid ozonation-coagulation process[J]. Water Research, 2020, 177: 115800. doi: 10.1016/j.watres.2020.115800 [7] 郝晓地, 甘微, 李季, 等. 臭氧降解污水厂二级出水有机物作用与效果分析[J]. 中国给水排水, 2021, 37(10): 1-7. [8] HOIGNé J. Chemistry of aqueous ozone and transformation of pollutants by ozonation and advanced oxidation processes[J]. Chemistry quality and treatment of drinking water, 1998, 5(2): 83-141. [9] QI Y. Ozonation of water and waste water: A practical guide to understanding ozone and its applications[J]. International Journal of Environmental Studies, 2010, 67(5): 795-796. doi: 10.1080/00207233.2010.517628 [10] 胡航恺, 徐浩丹, 卢晓辉, 等. 水中有机物对紫外光催化还原溴酸盐的影响[J]. 中国环境科学, 2022, 42(3): 1164-1172. [11] 吴纯德, 陈芳, 李商国, 等. NH4+和H2O2抑制臭氧氧化过程中溴酸盐形成的效能研究[J]. 环境工程学报, 2011, 5(10): 2233-2236. [12] 周娟, 陈欢, 李晓璐, 等. Pd/CeO2催化水中溴酸盐的加氢还原研究[J]. 中国环境科学, 2011, 31(8): 1274-1279. [13] VON GUNTEN U, OLIVERAS Y. Kinetics of the reaction between hydrogen peroxide and hypobromous acid: Implication on water treatment and natural systems[J]. Water Research, 1997, 31(4): 900-906. doi: 10.1016/S0043-1354(96)00368-5 [14] ULRICH P, URS V G. Bromate minimization during ozonation: Mechanistic considerations[J]. Environmental Science & Technology, 2001, 35(12): 2525-2531. [15] HOFMANN R, ANDREWS R C. Ammoniacal bromamines: a review of their influence on bromate formation during ozonation[J]. Water Research, 2001, 35(3): 599-604. doi: 10.1016/S0043-1354(00)00319-5 [16] VON GUNTEN U. Ozonation of drinking water: Part II. Disinfection and by-product formation in presence of bromide, iodide or chlorine[J]. Water Research, 2003, 37(7): 1469-1487. doi: 10.1016/S0043-1354(02)00458-X [17] 王永京, 杜旭, 金萌, 等. 氨氮及H2O2对溴酸盐和消毒副产物控制的影响[J]. 环境科学, 2017, 38(2): 616-621. [18] QI S, MAO Y, LV M, et al. Pathway fraction of bromate formation during O3 and O3/H2O2 processes in drinking water treatment[J]. Chemosphere, 2016, 144: 2436-2442. doi: 10.1016/j.chemosphere.2015.11.022 [19] BADER H, HOIGNé J. Determination of ozone in water by the indigo method[J]. Water Research, 1981, 15(4): 449-456. doi: 10.1016/0043-1354(81)90054-3 [20] GALAPATE R P, BAES A U, OKADA M. Transformation of dissolved organic matter during ozonation effects on trihalomethane formation potential[J]. Water Research, 2001, 35(9): 2201-2206. doi: 10.1016/S0043-1354(00)00489-9 [21] ZHANG T, CHEN W, MA J, et al. Minimizing bromate formation with cerium dioxide during ozonation of bromide-containing water[J]. Water Research, 2008, 42(14): 3651-3658. doi: 10.1016/j.watres.2008.05.021 [22] WEN G, PAN Z-H, MA J, et al. Reuse of sewage sludge as a catalyst in ozonation: Efficiency for the removal of oxalic acid and the control of bromate formation[J]. Journal of Hazardous Materials, 2012, 239-240: 381-388. doi: 10.1016/j.jhazmat.2012.09.016 [23] PSALTOU S, KARAPATIS A, MITRAKAS M, et al. The role of metal ions on p-CBA degradation by catalytic ozonation[J]. Journal of Environmental Chemical Engineering, 2019, 7(5): 103324. doi: 10.1016/j.jece.2019.103324 [24] ELOVITZ M S, URS V G. Hydroxyl radical/ozone ratios during ozonation processes. I. The Rct concept[J]. Ozone:Science & Engineering, 1999, 21(3): 239-260. [25] WANG Y, MAN T, ZHANG R, et al. Effects of organic matter, ammonia, bromide, and hydrogen peroxide on bromate formation during water ozonation[J]. Chemosphere, 2021, 285: 131352. doi: 10.1016/j.chemosphere.2021.131352 [26] YU J, WANG Y, WANG Q, et al. Implications of bromate depression from H2O2 addition during ozonation of different bromide-bearing source waters[J]. Chemosphere, 2020, 252: 126596. doi: 10.1016/j.chemosphere.2020.126596 [27] MIZUNO T, OHARA S, NISHIMURA F, et al. O3/H2O2 process for both removal of odorous algal-derived compounds and control of bromate ion formation[J]. Ozone:Science & Engineering, 2011, 33(2): 121-135. [28] ACERO J L, HADERLEIN S B, SCHMIDT T C, et al. MTBE oxidation by conventional ozonation and the combination ozone/hydrogen peroxide: Efficiency of the processes and bromate formation[J]. Environmental Science & Technology, 2001, 35(21): 4252-4259. [29] LEGUBE B, PARINET B, GELINET K, et al. Modeling of bromate formation by ozonation of surface waters in drinking water treatment[J]. Water Research, 2004, 38(8): 2185-2195. doi: 10.1016/j.watres.2004.01.028 [30] 强晨. 臭氧/过一硫酸盐组合工艺氧化含溴水过程溴酸盐的形成规律与控制方法[D]. 西安: 西安建筑科技大学, 2019. [31] DAVID YAO C C, HAAG W R. Rate constants for direct reactions of ozone with several drinking water contaminants[J]. Water Research, 1991, 25(7): 761-773. doi: 10.1016/0043-1354(91)90155-J [32] JEKEL M, ZUCKER I, HüBNER U. Options and limitations of hydrogen peroxide addition to enhance radical formation during ozonation of secondary effluents[J]. Journal of Water Reuse and Desalination, 2015, 5(1): 8-16. doi: 10.2166/wrd.2014.036 [33] 韩帮军, 马军, 张涛, 等. 臭氧催化氧化抑制溴酸盐生成效能的研究[J]. 环境科学, 2008, 29(3): 665-670. doi: 10.3321/j.issn:0250-3301.2008.03.021 [34] PINKERNELL U, LüKE, HANS J, et al. Selective photometric determination of peroxycarboxylic acids in the presence of hydrogen peroxide[J]. Analyst, 1997, 122(6): 567-571. doi: 10.1039/a700509a -




 下载:
下载: