-
在海水养殖过程中,饲料中的氮可以通过饵料残留、养殖生物代谢等途径进入水体,成为海水养殖废水中的主要污染物之一[1]。氨氮(NH3-N)是海水养殖废水中氮的主要存在形式[2]。在传统脱氮工艺中,通常先通过自养硝化将NH3-N转化为硝酸盐氮(NO3−-N),再通过异养反硝化将NO3−-N转化为气态氮,从而去除水体中总氮。由于自养硝化和异养反硝化所需的溶解氧(DO)、有机物等环境条件存在差异[3],通常将二者置于不同反应器中[4]或者好氧/缺氧环境在时间上交替出现的同一反应器中[5],这使得传统脱氮工艺往往存在系统体积大、反应时间长、操作和过程控制复杂、能耗物耗较高等不足。近些年的研究表明,硝化和反硝化过程可以在同一反应器中及相同操作条件下同时进行[6]。与传统脱氮工艺相比,同步硝化反硝化(SND)工艺可以减小反应器体积,缩短处理时间,简化过程控制,降低氧、有机碳源和碱度的消耗[7],有望成为一种新型的海水养殖废水脱氮工艺。
相较于市政污水,海水养殖废水的污染物负荷较低,因此,通常采用生物膜法对其进行处理。生物膜附着生长,具有一定厚度,传质阻力使得水体中DO、有机物等物质在生物膜内形成浓度梯度,从而为不同功能菌群生长提供适宜的微环境,促进SND发生[8]。生物膜SND的脱氮性能受DO[9]、温度[10]、pH[11]、碳氮比(C/N)[12]、水力停留时间(HRT)[13]等环境条件和运行参数的影响。其中,C/N是关键影响因素之一,需要保持在适当范围内,过高或过低都会破坏SND中硝化和反硝化的平衡[7,14-15]。海水养殖废水的C/N较低,通常需要补充有机碳源来满足异养反硝化的需求。甲醇、乙醇、乙酸钠等水溶性有机物经常被用作反硝化的外加碳源[16];然而,其投加量的精准调控比较困难,这不仅会导致系统运行复杂,还容易造成二次污染[17]。大量研究[18-19]表明,很多难溶于水但可生物降解的天然或人工合成聚合物在微生物胞外酶作用下能够释放可溶性小分子有机物。因此,这些难溶性的固态有机物可以用作异养反硝化的缓释碳源,降低外加碳源调控的难度。与天然聚合物(木屑、麦秆、稻草等)相比,人工合成聚合物(聚己内酯、聚羟基脂肪酸酯等)作为固态碳源具有脱氮效率高且较稳定、溶解性有机碳(DOC)和有害物质残留少、水体色度变化小等优点[20],故日益受到国内外研究者的关注。有研究表明,SND过程能够在以人工合成聚合物作为生物膜载体的反应器中进行,从而实现对低C/N污废水(市政污水、淡水养殖废水、渗沥液等)中NH3-N、NO3−-N和TN的同时去除[7, 21-22]。因此,基于人工合成聚合物的生物膜SND对海水养殖废水中氮的去除性能值得关注,但是,目前相关研究报道仍然较少。
本研究选取用途广泛的3-羟基丁酸/戊酸酯共聚物(PHBV)[23]作为人工合成聚合物固态碳源的代表,首先考察了其在非生物作用下的有机碳释放情况;然后构建了填充柱生物膜反应器,连续运行90 d,研究了基于PHBV的SND对海水养殖废水中NH3-N、NO3−-N和TN的去除性能,以期为海水养殖废水高效净化提供技术支持。
-
称取5.0 g 圆柱形PHBV颗粒(平均长度3.5 mm,平均截面直径3.0 mm,比表面积14.1 cm2·g−1),添加到250 mL锥形瓶中,然后加入250 mL实验用水;通入氮气2 min后,密封锥形瓶,并放入恒温培养箱中静置;分别在PHBV颗粒浸泡1、2、4、6、8、10、12、24、36、48、60、72 h后采集5 mL水样,测定其中DOC质量浓度;水样采集完毕后,立即向锥形瓶中通入氮气2 min,继续密封恒温培养。本研究共设置4个实验组,分别用于考察振荡速度、温度、盐度和初始pH对非生物作用下PHBV有机碳释放的影响,具体实验条件如表1所示。采用盐酸和NaOH调节初始pH;采用32‰盐度的人工海水和去离子水分别作为实验用水,将两者按体积比1∶1混合后得到盐度为16‰的实验用水。为了避免微生物对PHBV有机碳释放的影响,以上实验用水和实验装置均经灭菌处理。
-
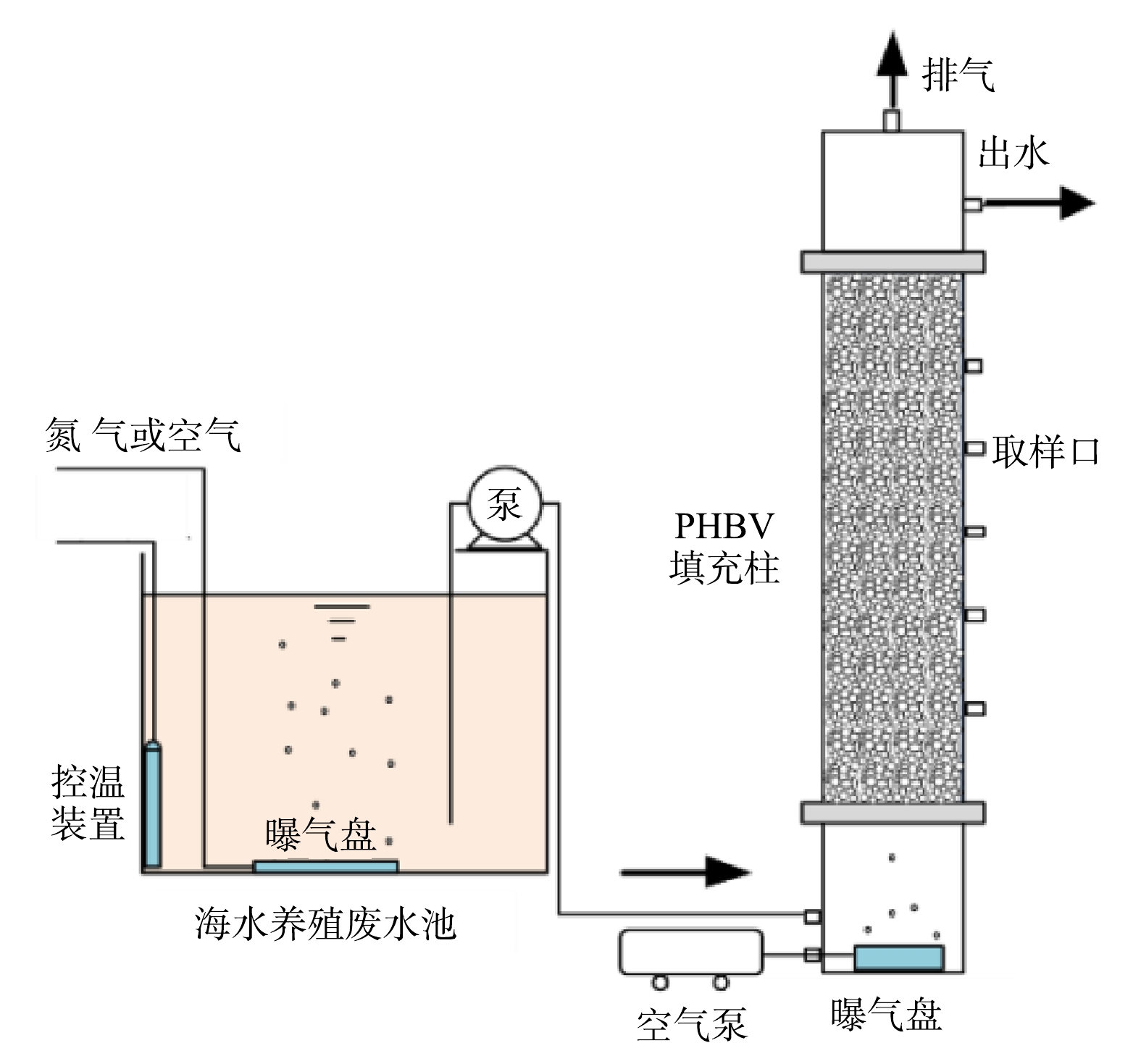
本研究采用上向流式填充柱生物膜反应器(图1)。填充柱为亚克力材料制成的密闭式圆柱体(内径10 cm,高度140 cm)。在距填充柱底端20 cm处设置承托板,板上均匀开孔。在承托板下部设置曝气装置;侧壁上设置进水口和进气口,分别与隔膜计量泵和空气泵连接。本研究采用前述圆柱形PHBV颗粒和陶粒(直径3~5 mm,比表面积3.9~4.5 m2·g−1,孔隙率47%~55%,表观密度1.4~1.6 g·cm−3)作为填料,将两者混合均匀(表观体积比为3∶1)后加入填料柱,填料层高度为100 cm;从填料层底部起,在填充柱侧壁上每隔20 cm设置1个取样口。填料层以上的柱体高度为20 cm,在侧壁和顶端分别设置出水口和排气口。
-
1)菌种驯化富集。为了提高反应器的挂膜启动效率,首先驯化富集可以协同发挥作用的硝化菌和反硝化菌。采用青岛近岸海域沉积物、海水养殖固体废弃物和城市污水处理厂回流污泥的混合物作为种泥。向天然海水中添加NH4Cl、KNO3、KH2PO4、NaHCO3、CH3COONa等分析纯化学药品配制培养液(50 mg·L−1 NH3-N、50 mg·L−1 NO3−-N、10 mg·L−1 PO43--P、150 mg·L−1 NaHCO3、C/N 1.0)。将种泥与培养液均匀混合后加入序批式反应器(SBR),初始污泥质量浓度约为3 g·L−1。SBR运行周期为24 h(进水0.5 h、完全混合21 h、沉淀2.0 h、排水0.5 h);完全混合期间进行间歇曝气,曝气时长1 h,DO质量浓度控制在1~2 mg·L−1,相邻2次曝气间隔1 h;每个周期结束时,排出SBR中80%的废水。SBR内的温度控制在30 oC左右。
2)反应器挂膜启动。将经过驯化富集的菌种均匀接种到填料层后,利用人工模拟海水养殖废水(25 mg·L−1 NH3-N、25 mg·L−1 NO3−-N、10 mg·L−1 PO43--P,32‰盐度)对反应器进行挂膜启动,依次经历序批式运行、体系内循环和连续运行3个阶段。在序批式运行阶段,向填充柱中注入海水养殖废水直至淹没填料层,进行连续曝气,DO质量浓度控制在1~2 mg·L−1,每天换水1次,共运行3 d。在体系内循环阶段,海水养殖废水以较小流速在填充柱和废水池之间循环(填料层HRT约为12 h),连续曝气(气水比为4~5),废水池每天换水1次,直至TN去除率超过60%。在连续运行阶段,填充柱保持连续进水,出水直接排放,连续曝气(气水比为4~5);当TN去除率超过60%后,逐步降低填料层HRT(12、8、6、4 h)。填料层HRT为4 h时,当TN去除率超过60%后,反应器挂膜启动完成。在挂膜启动期间,反应器内温度控制在23~25 oC。
3)反应器连续运行。利用人工模拟海水养殖废水作为进水(32‰盐度),生物膜反应器连续运行90 d,填料层HRT控制在2 h,温度为21~23 oC,气水比控制在4~5。每天监测进出水中NH3-N、NO3−-N、NO2−-N、TN、DOC、pH、DO等水质指标;反应器运行达到稳态后,从填充柱上各采样口采集水样,分析各水质指标沿填充柱高度的变化规律。
-
水样采集后,分别采用水银温度计、便携式溶解氧测定仪(WTW,德国)和实验室pH计(Mettler Toledo,瑞士)直接测定温度、DO质量浓度和pH。水样经0.45 μm醋酸纤维滤膜过滤后,分别采用营养盐自动分析仪(QuAAtro,SEAL,德国)和有机碳分析仪(Biotector,爱尔兰)测定其中的氮(NH3-N、NO2−-N、NO3−-N和TN)和DOC质量浓度。污泥质量浓度采用烘干称重法测定。填料层HRT (T,h)、氮去除率(R)、硝化速率(rn,g·(L·d)−1)和反硝化速率(rd,g·(L·d)−1)按照式(1)~式(4)进行计算。通过单因素方差分析判断实验数据之间是否存在显著性差异。
式中:V为填充柱中填料层的体积,L;n为填料层的空隙率;Q为填充柱进水流量,L·d−1;CN,in和CN,ef分别为进水和出水中氮的质量浓度,mg·L−1;CNH3,in和CNH3,ef分别为进水和出水中NH3-N的质量浓度,mg·L−1;CTN,in和CTN,ef分别为进水和出水中TN的质量浓度,mg·L−1。
-
在生物膜反应器中,固态碳源的有机碳释放过程由微生物作用和非生物作用共同决定。为了评估这两种作用的贡献,本研究首先考察了非生物作用下PHBV的有机碳释放规律。图2给出了不同振荡速度、温度、盐度和初始pH等条件下水相DOC质量浓度随PHBV浸泡时间的变化。随浸泡时间(0~72 h)的延长,水相DOC质量浓度未呈现出明显的上升趋势。这表明在非生物作用下PHBV难以向水体中释放有机碳,这是由PHBV对水和气的高阻隔性导致的。对图2(a)、图2(b)和图2(c)中的数据分别进行单因素方差分析,P值(0.31、0.76和0.57)均大于0.05,表明振荡速度(0~100 r·min−1)、温度(15~30 oC)和初始pH(5~8)对非生物作用下PHBV的有机碳释放未产生显著影响。不同盐度实验用水中DOC本底质量浓度的差异导致图2(d)中的数据存在显著差异;然而,盐度16‰水体的DOC质量浓度与另外2种水体DOC质量浓度的平均值无显著差异(P=0.08>0.05),表明盐度变化没有明显改变非生物作用下PHBV的有机碳释放。因此,在生物膜反应器中,PHBV的有机碳释放过程主要由生物膜内的微生物作用决定。在微生物分泌的胞外酶(脂肪酶)作用下,PHBV聚合链发生水解,形成水溶性小分子有机物(以乙酸和正丁酸为主,含有少量丙酸和异丁酸),进而用作微生物碳源和反硝化电子供体[18, 20]。
-
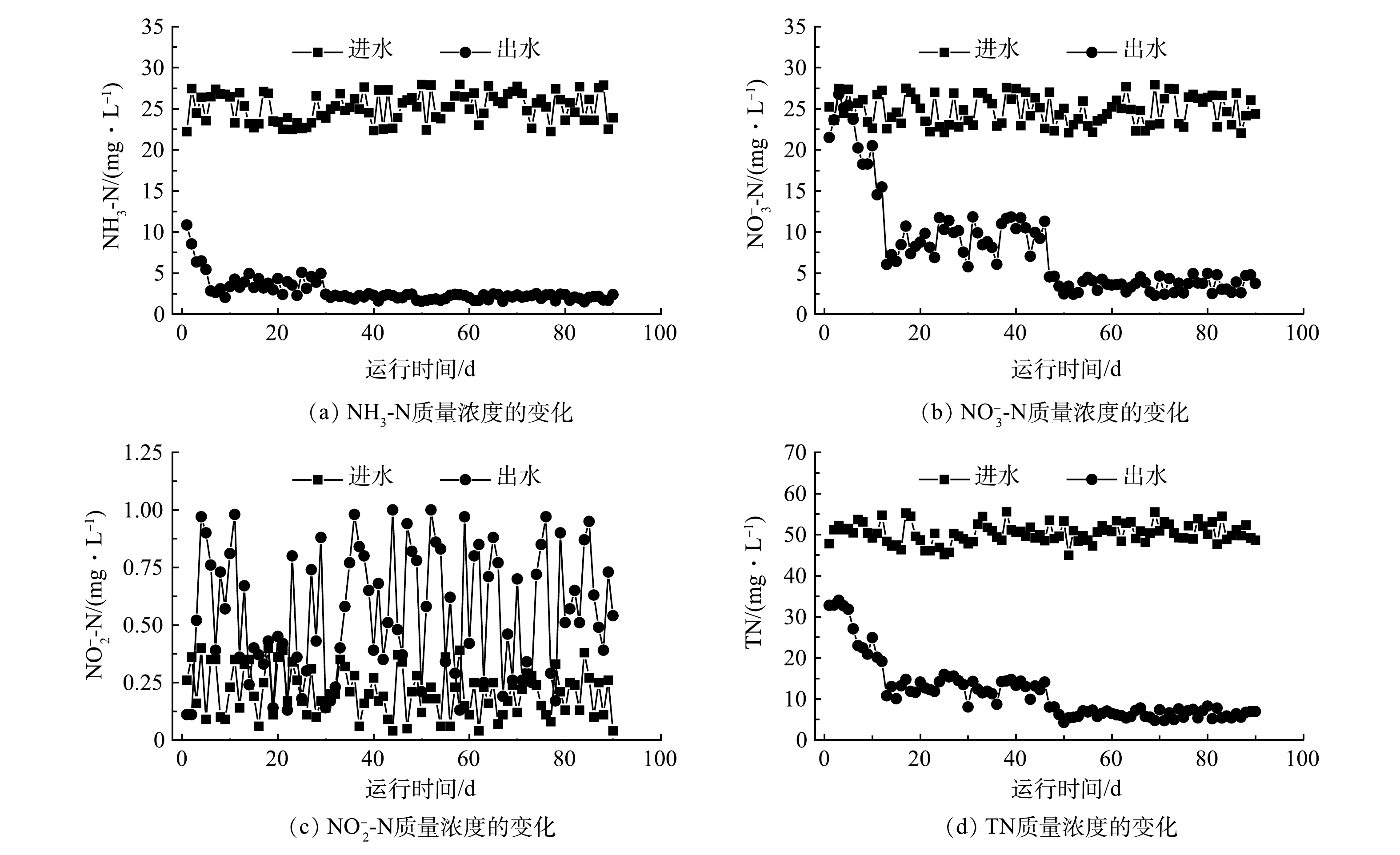
1)反应器出水氮质量浓度的变化。图3为生物膜反应器运行期间出水NH3-N、NO3−-N、NO2−-N和TN质量浓度随运行时间的变化。由图3(a)可见,1~5 d内,出水NH3-N质量浓度逐渐下降,去除率由51.1%逐渐上升到75.9%。这是因为反应器挂膜结束时的HRT为4 h,而连续运行实验阶段的HRT缩短至2 h,生物膜内的硝化菌需要逐渐适应由HRT缩短引起的反应器内部环境变化。6~30 d内,出水NH3-N质量浓度在2.05~5.08 mg·L−1内小幅波动,去除率为77.5%~92.3%。31~90 d内,反应器出水NH3-N质量浓度保持稳定,平均去除率为(91.8±1.3)%。反应器运行30 d后,硝化性能达到稳态,硝化速率为0.11 g·(L·d) -1。
如图3(b)和图3(d)所示,出水NO3−-N和TN质量浓度变化大致可以分为4个阶段。在1~6 d,进出水NO3−-N质量浓度差异不显著(P>0.05),但出水TN质量浓度明显低于进水且保持相对稳定。这表明该阶段内生物膜反应器具有一定的同步硝化反硝化能力,而且NO3−-N的生成与去除达到相对平衡。在7~12 d,出水NO3−-N和TN质量浓度快速降低。这表明随着运行时间的延长,生物膜反应器的反硝化性能逐渐增强,NO3−-N的去除量超过了生成量。在13~46 d,出水NO3−-N和TN质量浓度分别在5.77~11.83 mg·L−1和8.03~15.96 mg·L−1波动;在47~90 d,出水NO3−-N和TN质量浓度均保持稳定,平均去除率分别为(85.4±3.4)%和(87.5±2.2)%。生物膜反应器运行46 d后,反硝化性能达到稳态,反硝化速率为0.20 g·(L·d)−1。图3(c)表明,在整个生物膜反应器运行期内,出水NO2−-N质量浓度始终低于1.00 mg·L−1,平均值为(0.56±0.27) mg·L−1,略高于进水NO2−-N质量浓度((0.21±0.10) mg·L−1),表明反应器中发生了微弱的亚硝酸盐积累。短程硝化以及短程反硝化都可以生成亚硝酸盐。然而,以往研究表明在生物膜反应器中,短程硝化过程难以稳定存在,容易被全程硝化取代[24],而且NO2−-N是反硝化过程的高效电子受体[25]。由此推测,反应器内NO2−-N的微弱积累可能是由短程反硝化造成的。
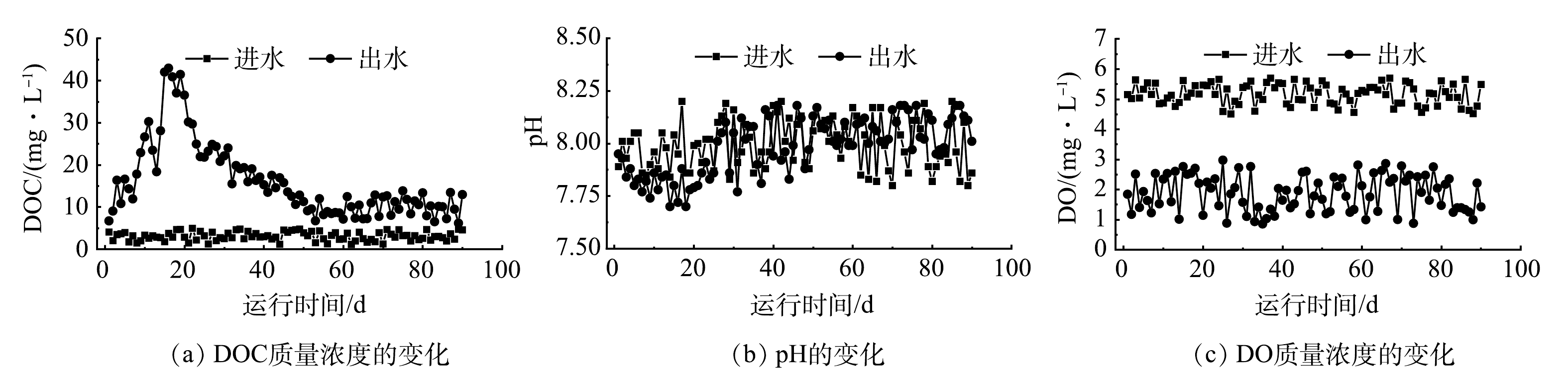
2)反应器出水DOC、DO质量浓度及pH的变化。由图4(a)可以看出,在反应器运行期内,出水DOC质量浓度始终高于进水。水体中DOC含量由填充柱内微生物作用下PHBV的有机碳释放过程以及异养反硝化等有机碳消耗过程共同决定。因此,整个运行期内有机碳释放速率高于消耗速率。1~16 d内,出水DOC质量浓度由6.70 mg·L−1快速升高至42.94 mg·L−1,表明该阶段有机碳消耗速率与释放速率的差距逐渐增大。这是因为运行初期生物膜尚未完全成熟,异养反硝化性能较弱(图3(b)),而且PHBV结构中较难分解的区域尚未暴露出来。17~46 d内,出水DOC质量浓度逐渐下降到13.59 mg·L−1,表明该阶段有机碳消耗速率与释放速率的差距逐渐缩小。其原因在于,该阶段生物膜逐渐成熟,异养反硝化性能逐渐增强(图3(b)),而且PHBV结构中较难分解的区域也逐渐暴露。47~90 d内,出水DOC质量浓度达到相对稳定状态((10.03±2.21) mg·L−1),表明有机碳消耗速率与释放速率的差距达到稳态。质量衡算结果表明,SND生物膜反应器达到稳态后,每去除1.00 g TN向出水中释放约0.15 g DOC。需要注意的是,可以对SND生物膜反应器中有机碳释放和消耗过程造成影响的运行参数(HRT、进水氮负荷、温度、曝气量等)均可以影响出水中有机物的残留量。因此,运行参数对SND生物膜反应器出水中有机物残留的影响规律值得进一步探究。
如图4(b)所示,在反应器运行期间,出水pH呈现逐渐上升趋势。出水pH由生物膜反应器中产酸和产碱过程决定。硝化反应消耗碱度,可以降低水体pH;微生物作用下PHBV释放出来的有机物中包含多种有机酸[26],可以增加水体酸度;异养反硝化反应产生碱度,可以提高水体pH。反应器运行初期出水pH低于进水pH,这是因为运行初期生物膜的异养反硝化性能较差,导致填充柱内碱度产量低于酸度产量。随着运行时间延长,生物膜异养反硝化性能逐渐提升,填充柱内碱度产量逐渐增加,使得出水pH与进水pH逐渐接近。在反应器运行后期,出水pH略高于进水pH,表明填充柱内碱度产量已经超过了酸度产量。如图4(c)所示,在反应器整个运行期间,出水口DO质量浓度(1.87±0.60) mg·L−1明显低于进水口DO质量浓度(5.17±0.34) mg·L−1。这是由填充柱内的硝化反应、好氧呼吸等耗氧过程造成的。结合图3(b)和图4(c)可以看出,尽管水体中始终存在较高质量浓度的DO,填充柱的反硝化性能并未受到明显抑制。其原因在于反硝化菌位于生物膜内层,外层的好氧菌和兼性菌消耗了进入生物膜的DO,为内层的反硝化菌创造了缺氧环境,保证了反硝化过程的顺利进行。
-
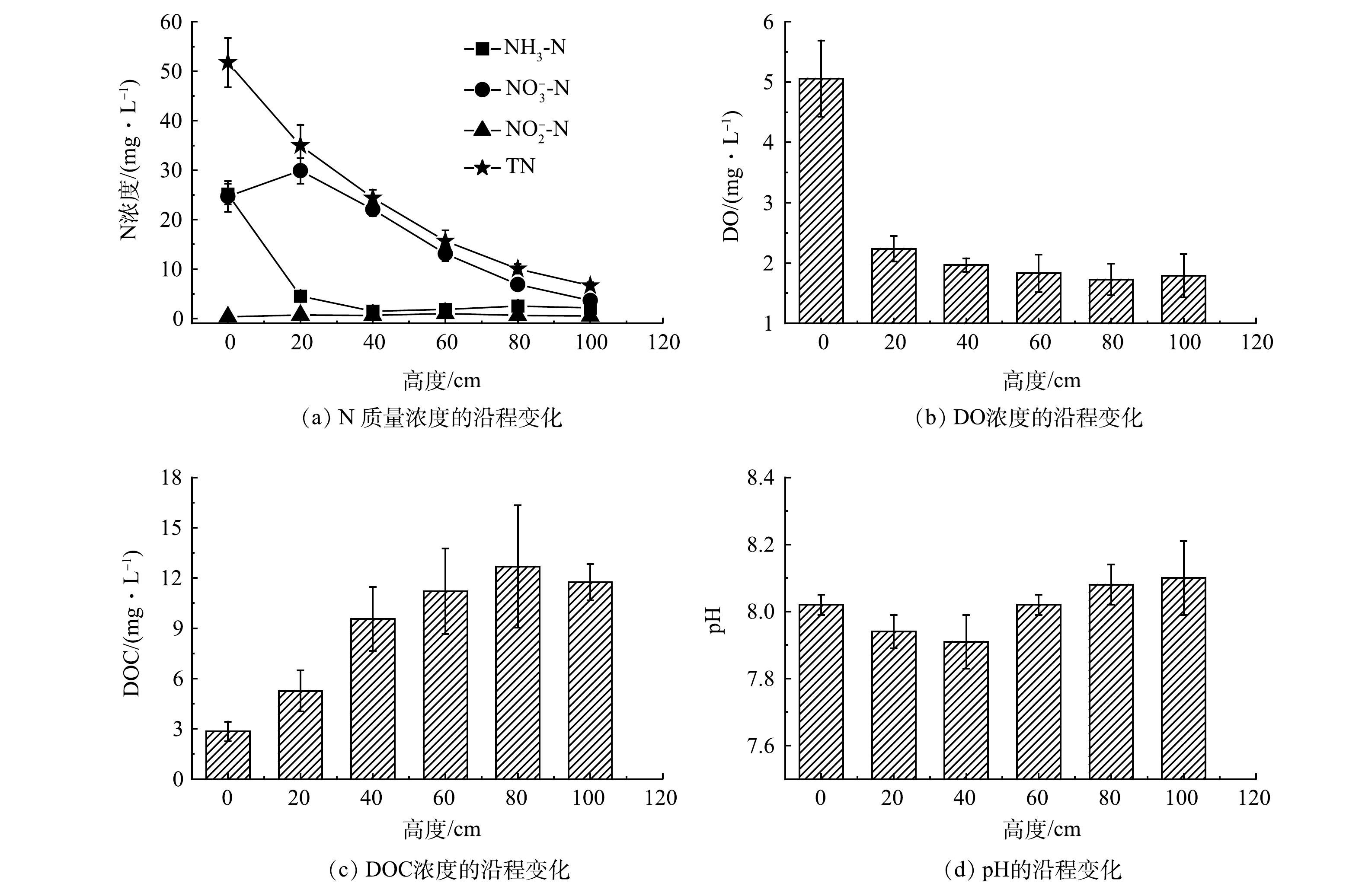
NH3-N、NO3−-N、NO2−-N、TN、DOC、DO质量浓度及pH随填充柱高度的变化规律如图5所示。由图5(a)可以看出,在0~20 cm内,NH3-N质量浓度快速降低,20 cm处的去除率已经达到82.1%。这表明硝化反应主要发生在该段柱体内,导致NO3−-N质量浓度由(24.70±3.11) mg·L−1上升到(29.87±2.59) mg·L−1。然而,在0~20 cm内TN质量浓度显著降低,20 cm处的去除率为32.5%,表明在该段柱体内也可以发生反硝化作用。在20~100 cm内,NH3-N质量浓度保持相对稳定,NO3−-N和TN质量浓度逐渐降低。这表明在该段柱体内进行的主要是反硝化反应,硝化反应可以忽略。由此可见,具有脱氮功能的生物膜在填充柱内的分布并不均匀,填充柱沿水流方向可以划分为不同的脱氮功能区;SND过程发生在柱体0~20 cm内,其硝化和反硝化速率分别为0.48 g·(L·d)−1和0.39 g·(L·d)−1;在20~100 cm内的反硝化速率为0.16 g·(L·d)−1。DO质量浓度随填充柱高度的变化(图5(b))也印证了这一点,在0~20 cm内快速降低,而后略有降低。水体中NO2−-N质量浓度呈现先上升而后下降的趋势(图5(a)),在60 cm处达到峰值(0.98 mg·L−1)。由于高质量浓度DO可以抑制硝化过程中NO2−-N的积累[24],而且超过20 cm柱体内的硝化反应可以忽略,因此,填充柱内的NO2−-N主要来自短程反硝化作用[27]。这也印证了前面对于NO2−-N微弱积累(图3(c))原因的推测。
如图5(c)所示,水体中DOC质量浓度在0~80 cm内逐渐升高,在80~100 cm内略有下降。这表明生物膜内的微生物难以完全消耗掉PHBV释放出来的有机物,残留的有机碳可以扩散进入水体中形成DOC。在0~40 cm内,水体pH逐渐降低(图5(d)),表明在该段柱体内硝化反应及PHBV有机碳释放过程产生的酸度超过了反硝化过程产生的碱度;在40~100 cm内,水体pH逐渐升高,这是因为该段柱体的硝化作用可以忽略,反硝化作用增强,导致酸度产量小于碱度产量。
-
以上所得研究结果表明,基于PHBV的生物膜SND可以有效去除海水养殖废水中的氮。SND脱氮效果由生物膜内的物质传递及微生物群落结构决定[7]。异养反硝化以硝酸盐作为电子受体,然而DO会与硝酸盐产生竞争,从而对反硝化产生抑制作用[28]。微环境理论认为,SND可以在好氧条件下进行是因为传质阻力和微生物消耗导致DO在生物膜内存在浓度梯度,使得生物膜外层和内层分别处于好氧和缺氧状态,可以为不同脱氮微生物提供适宜的生存环境[8]。好氧区和缺氧区的厚度不仅受供氧量的影响,还与有机碳源、pH、氮负荷、微生物组成等密切相关[7]。在以PHBV作为载体的生物膜内,有机碳源的传递过程与DO传递过程逆向。PHBV释放出来的有机物首先进入缺氧区,用作异养反硝化菌的电子供体;而后进入好氧区,被其中的好氧菌和兼性菌降解为CO2;未被利用的有机物则进入水相成为DOC。此外,填充柱不同区段内发生的脱氮过程不尽相同,可以推断生物膜内的微生物群落结构随填充柱高度改变。因此,下一步研究工作将重点监测生物膜厚度以及DO、pH和氮元素在生物膜内的空间分布,从微环境角度深入探究生物膜内物质传递对SND的影响;探究运行参数对出水中DOC残留量和有机物组成的影响规律,为出水风险评估提供依据;考察N2O的释放规律及其影响因素,阐明海水养殖废水SND脱氮工艺的气候效应;明确微生物群落结构的沿程变化,揭示海水养殖废水中PHBV驱动的生物膜SND脱氮的微生物机制。
-
1)非生物作用下PHBV难以向水体中释放有机碳,生物膜反应器中的有机碳释放主要依靠生物膜内的微生物作用。
2) SND可以在以PHBV和陶粒作为填料的填充柱生物膜反应器中实现。HRT为2 h时,生物膜反应器的运行状态逐渐稳定;达到稳态后,NH3-N和TN去除率为分别为(91.8±1.3)%和(87.5±2.2)%,硝化和反硝化速率分别为0.11 g·(L·d)−1和0.20 g·(L·d)−1;出水NO2−-N、DOC质量浓度及pH均高于进水,而出水口DO质量浓度低于进水口。
3)填充柱中氮、DOC、DO质量浓度及pH的沿程变化结果表明,填充柱沿水流方向可以划分为不同的脱氮功能区,SND过程发生在0~20 cm内,其硝化和反硝化速率分别为0.48 g·(L·d)−1和0.39 g·(L·d)−1;在20~100 cm内主要进行反硝化反应,其速率为0.16 g·(L·d)−1;反应器中微弱的亚硝酸盐积累可以归因于短程反硝化作用。
基于固态碳源的同步硝化反硝化反应器对海水养殖废水中氮的去除性能
Performance of simultaneous nitrification and denitrification reactor based on solid-phase carbon source on nitrogen removal from mariculture wastewater
-
摘要: 通过批次实验考察了非生物作用下3-羟基丁酸/戊酸酯共聚物(PHBV)的有机碳释放规律;以PHBV颗粒和陶粒作为填料建立了填充柱生物膜反应器,并通过长期(90 d)运行考察了其对海水养殖废水中氮的去除性能。结果表明,非生物作用下PHBV难以向水体中释放有机碳;以PHBV作为固态碳源的生物膜反应器可以实现同步硝化反硝化。反应器运行状态(HRT为2 h)稳定后,氨氮和总氮的去除率分别为(91.8±1.3)%和(87.5±2.2)%,硝化速率和反硝化速率分别为0.11 g·(L·d)−1和0.20 g·(L·d)−1。填充柱沿水流方向可以分为2个区段,0~20 cm柱体内主要进行同步硝化反硝化过程,20~100 cm柱体内主要进行反硝化过程;反应器中微弱的亚硝酸盐积累可以归因于短程反硝化。以上研究成果可以为海水养殖业绿色发展提供参考。
-
关键词:
- 固态碳源 /
- 3-羟基丁酸/戊酸酯共聚物(PHBV) /
- 同步硝化反硝化 /
- 生物膜反应器 /
- 海水养殖废水
Abstract: Batch experiments were conducted to investigate the organic carbon release of poly-3-hydroxybutyrate-co-hyroxyvelate (PHBV) under abiotic condition. A biofilm reactor packed with PHBV granules and ceramsite was established and operated for 90 d to determine its performance on nitrogen removal from mariculture wastewater. Batch experiment results indicate that the negligible release of organic carbon from PHBV to water occurred under abiotic condition. Simultaneous nitrification and denitrification could be achieved in the biofilm reactor utilizing PHBV as solid-phase carbon source. When the biofilm reactor reached steady-state operation status (HRT = 2 h), the removal efficiencies of ammonia and total nitrogen were (91.8±1.3)% and (87.5±2.2)%, respectively, together with the nitrification rate of 0.11 g·(L·d)−1and the denitrification rate of 0.20 g·(L·d)−1. The packed-bed reactor could be divided into two distinct sections, namely, the section of 0~20 cm for simultaneous nitrification and denitrification and the section of 20~100 cm for denitrification. Slight nitrite accumulation in the packed-bed reactor could be attributed to the short-cut denitrification. Therefore, the achievements of this study could provide a technical support for the green development of mariculture. -
大气环境颗粒物中的铬(Cr)主要以三价铬(Cr(Ⅲ))和六价铬(Cr(Ⅵ))2种价态存在。Cr(Ⅲ)是人体进行糖类和脂类等代谢活动必不可少的微量物质;Cr(Ⅵ)则是剧毒物质,具有致癌性。1990年,美国的《清洁空气法》将Cr(Ⅵ)化合物列入188种有害空气污染物,美国环境保护局也将其列入18种核心污染物[1]。我国的《环境空气质量标准》规定其年平均浓度限值为25 pg·m−3[2]。近年来,相关学者围绕Cr这种环境颗粒物中重要的有害过渡金属[3-5],展开了Cr的污染特征和来源解析、潜在生物危害和健康风险评估以及在环境中可能存在的化学作用等[6-9]方面的研究。
大气颗粒物产生化学过程往往只持续较短时间(大约几个小时)。切实模拟和研究其产生、传输、消耗的动态过程,需要在该时间精度内进行分析测定[10-11]。在高时空分辨率背景下,研究大气化学过程中过渡金属的污染特征,可为探索此类气溶胶的理化特性、并控制其潜在毒性提供重要见解。建立灵敏而可靠的测量方法需要解决3个问题:1)如何提高测量的灵敏度(达到更低的检测限);2)如何降低测量过程中的潜在干扰;3)如何在处理和测量过程中降低样品中待测物质的损失。目前,多数研究者倾向于使用原子吸收光谱技术测定样品中的总Cr,包括火焰原子吸收光谱法(FAAS)、石墨炉原子吸收光谱法、电热原子吸收光谱法(ET-AAS)等[12-13]。但是,此类方法的样品前处理较为繁琐,所需仪器设备造价昂贵。紫外/可见光分光光度法(UV/Vis)灵敏度很高,通过适当的显色试剂进行络合反应可在高吸收率条件下测量水溶性金属,常被用于溶液中金属浓度的高精度测量[14-15]。以此为基础,可通过配备长光液体波导毛细管来实现UV/Vis定量测定环境样品中的水溶性金属[16-17],结合测量系统的开发,还能有序测量环境颗粒物样品中的金属浓度[18-19]。
结合采样和前处理操作,设计并评估了一种基于分光光度法连续测量大气环境细颗粒物(PM2.5)中铬浓度的系统,以便于精确了解大气颗粒物中铬的污染水平及其来源,提供一种测量环境大气中水溶性痕量金属的思路,以期为开发实际监测技术奠定基础。
1. 材料与方法
1.1 试剂标准
实验所需化学药品纯度至少为光谱纯,配制的试剂和溶液使用由纯水机(Smart-DUV(F) SAIDE)生产(电阻率不低于18.2 MΩ)的超纯水和去离子水。用于试剂配制的实验器材和试剂保存的聚丙烯瓶在使用前均先用浓度为4 mol·L−1的HCl进行清洗,然后用超纯水反复冲洗干净后烘干置于干净环境中备用。
用于标定和校准的Cr(Ⅵ)标准溶液通过用重铬酸钾(K2Cr2O7,纯度为99.9%)和去离子水制备的100 μg·m−3母液稀释获得,在使用前取母液用去离子水稀释到需要的浓度梯度(0.5~8 ng·mL−1)。制备4 mol·L−1的HNO3和3 mol·L−1的NaOH用于酸化和调整溶液pH。用于前处理过程的0.1%的H2O2试剂通过用0.1 mol·L−1的NaOH溶液将0.044 mL 30%的H2O2水溶液定容稀释至1 L制备。将167 mg的二苯碳酰二肼(diphenylcarbazide,DPC)溶解于100 mL的丙酮(C3H6O,纯度为99.9%)中,再与1.67%的H2SO4溶液按照1∶1的体积比混合,制备用于光度法检测前络合反应的DPC试剂[16]。除Cr(Ⅵ)标准溶液,所有的试剂均不含铬。
1.2 样品采集与预处理
用中流量颗粒物采样器(XY-2200,青岛旭宇)通过石英膜(QMA-Whatman,20.3 cm
× 25.4 cm,Φ90 mm)采集环境大气细颗粒物(PM2.5),采样流速100 L·min−1。为降低膜上Cr的本底浓度并减少其在采样中的损失,在采样前将待采样的空白石英膜通过450 ℃高温烘烤6 h,再用2 g·L−1的NaHCO3溶液浸泡后置于清洁恒温箱内晾干密封。采样口距离地面150 cm,用除湿装置保证过程中采样器的环境干燥。样品膜用密封的聚丙烯袋封装并且在-10 ℃下低温保存。所有的样品在采样完成1 d内取回,在3 d内完成前处理和分析测定,以此减少采样过程中Cr的损失,减少测量误差。1.3 分光光度法检测系统及误差避免方法
分光光度检测系统由容量为112 μL、光程为50 cm的长光程流通池(liquid waveguide capillary cell,LWCC,LWCC-3050, World Precision Instruments, Inc., Sarasota, FL),钨灯光源(HL-2000-FHSA-LL,Ocean Optics, Inc., Dunedin, FL),光缆(QP450-1-XSR, Ocean Optics, Inc., Dunedin, FL)和光谱范围为200~900 nm的小型光谱仪(USB4000-UV-VIS,Ocean Optics, Inc., Dunedin, FL)组成。
分析过程中,Cr浓度由Cr(Ⅵ)与DPC反应产生的络合物在540 nm的吸光度进行测算。尽管DPC与大气环境中部分金属离子(Fe3+、Hg2+、Mo6+、Cu2+和V5+)会发生类似络合反应,但这些金属络合物的最大光吸收波长范围均不含540 nm,且相差较大[6]。因此,检测前加入DPC可保证结果基本不受其他金属离子干扰。设定光谱的积分时间为8 ms,每个样品平均次数为20次,光吸收谱图上800 nm处吸光度信号用于设定基线(即设定系统背景信号)。为去除检测仪器自身产生的背景吸光度,通过断开光源测得仪器的暗光谱,并在光谱分析软件中设定扣除暗光谱得到实测光谱数据,以便对系统进行自吸收校正。
1.4 系统运行流程
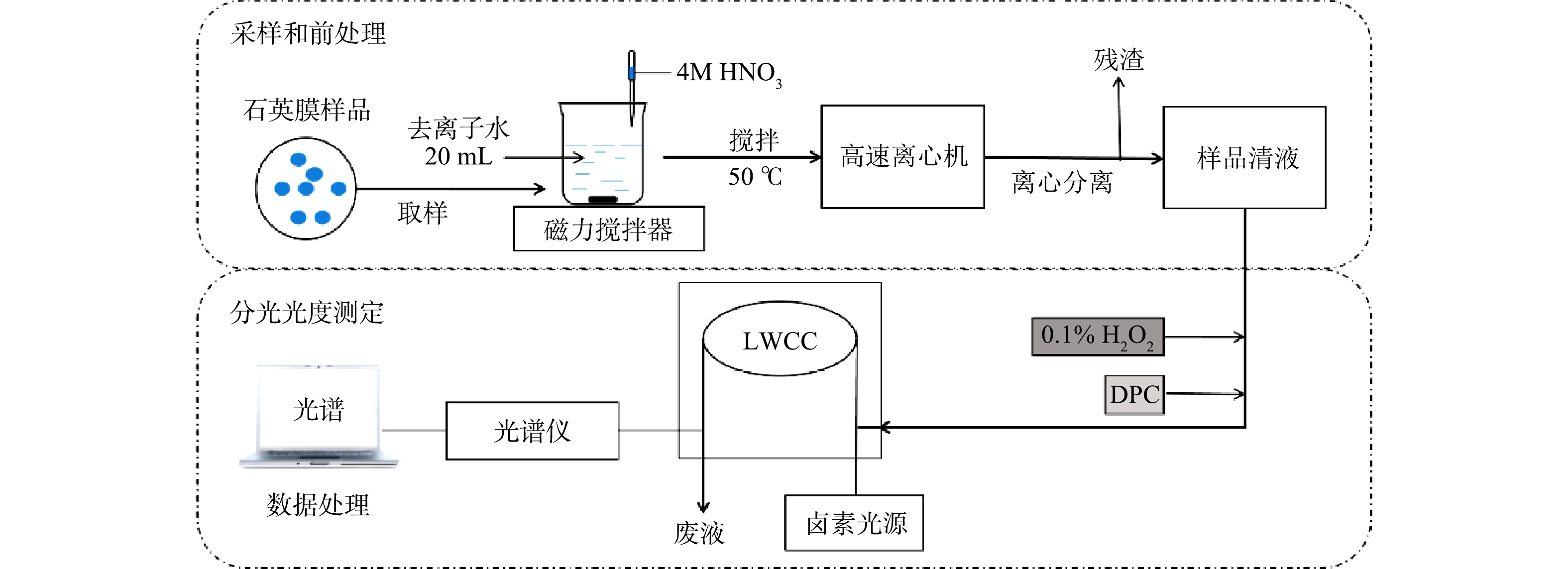
系统分为2个部分(见图1):石英膜采样和前处理操作的样品采集模块;以分光光度检测为基础的浓度分析模块。将采样后的石英膜用清洁陶瓷剪刀取样、剪碎,放入烧杯后加入20 mL的去离子水和1 mL浓度为4 mol·L−1的HNO3溶液。为尽可能溶解石英膜上采集的环境颗粒物,用磁力搅拌机将石英膜制成的酸化浆液加热(温度为50 ℃)搅拌40 min,分离出10 mL样品清液,装入棕色聚丙烯瓶中避光储存。每次测量后,用4 mol·L−1的HCl溶液清洗所有样品管路,再用超纯水洗净。
分光光度方法测定样品中的Cr浓度:1)络合反应。向样品溶液中加入0.1 mL 0.1%的H2O2试剂将样品溶液中的Cr(Ⅲ)转化为Cr(Ⅵ),同时加入0.1 mL的DPC试剂,静置10 min,待Cr络合物形成并稳定;2)样品注入。用带0.22 μm微孔滤膜(聚四氟乙烯,PTFE)的聚丙烯注射器将1 mL样品注入LWCC中;3)测定浓度。通入样品2~3 min后,待光谱稳定,得到光吸收谱图上540 nm处Cr络合物的最大吸收峰值,将该值扣减设定的800 nm基线值得出净峰高,并通过与标定结果的对比计算得出总Cr浓度。
1.5 采样点
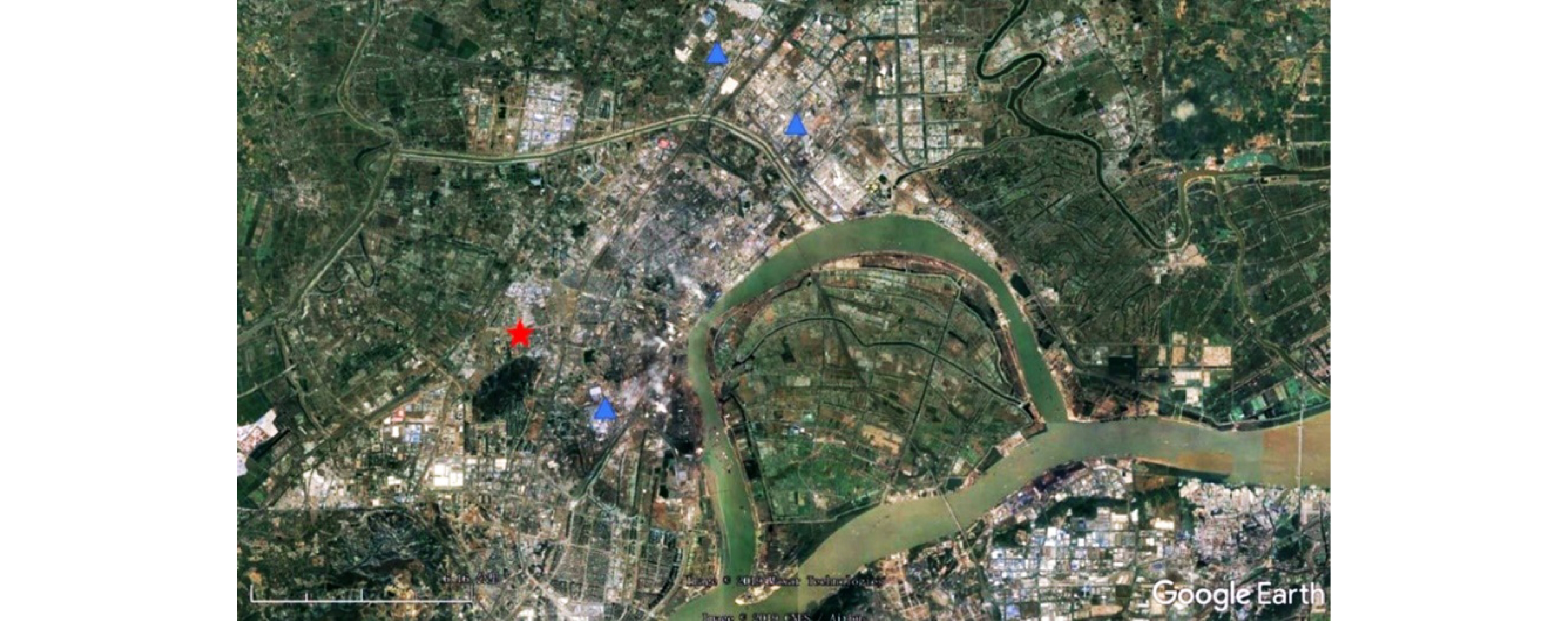
采样点设在南京信息工程大学气象观测场内,按12 h的时间间隔采集南京北郊大气颗粒物样品。设定样品采集的起始时间为每日6:30和18:30。采样点(红色星标)位于南京市中心以北大约15 km处,大型工业区(蓝色三角标)以西,靠近城区日常交通干道(见图2)。该地的PM2.5质量浓度数据由Met One Instruments公司的PM2.5在线监测仪进行实时在线监测,时间分辨率为1 h。
2. 结果与讨论
2.1 最佳样品测定条件的设定
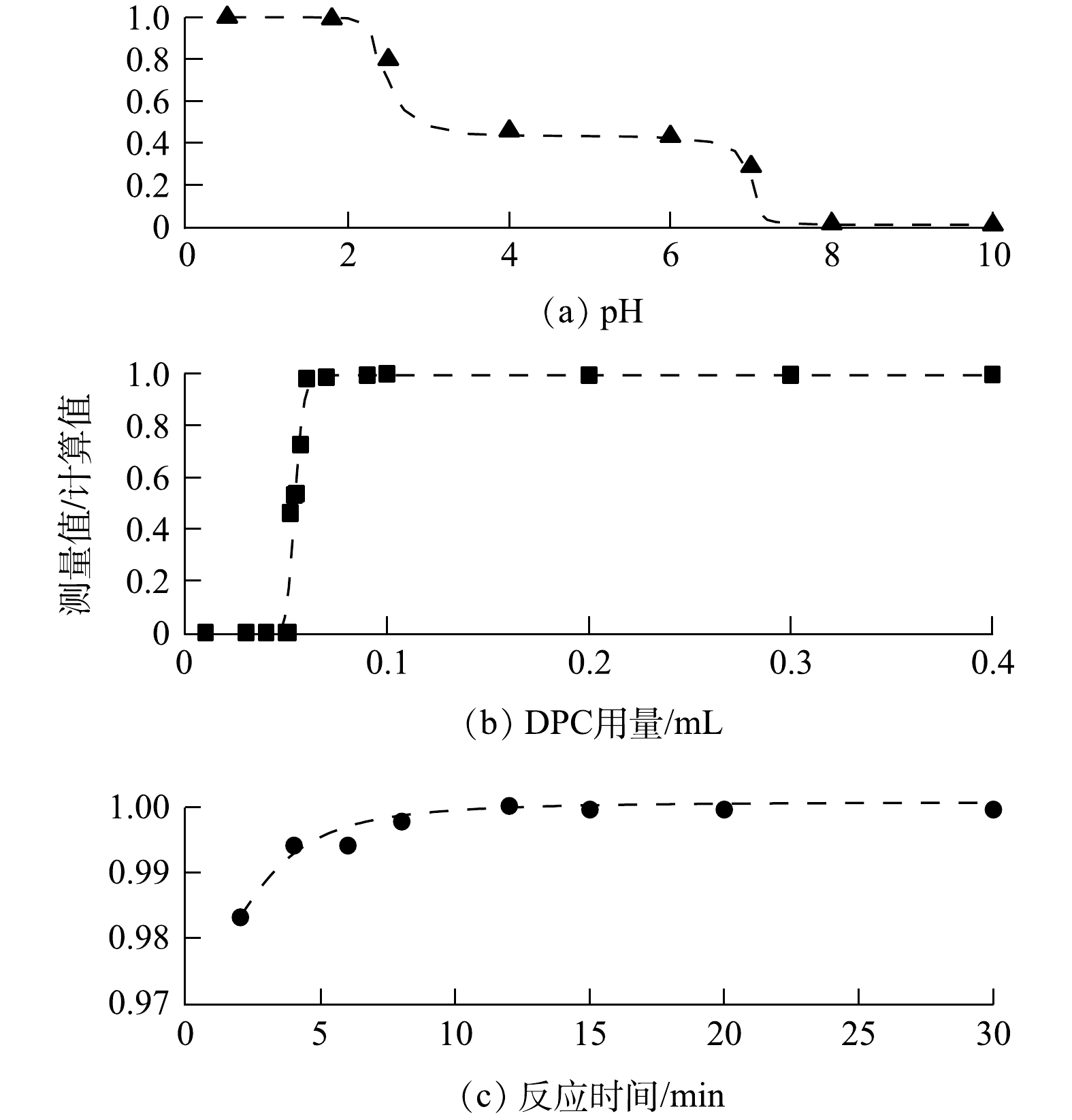
由于大气本底Cr浓度较低,每次取用10 mL浓度为5 ng·mL−1的Cr(Ⅵ)标准溶液进行条件实验。通过改变溶液的pH、DPC试剂的用量及预留的络合反应时间,根据条件实验结果来确定前述各项参数的最佳值或阈值。将仪器的测量值与标准样品浓度的计算值之比作为判别标准,比值越接近1,则结果对应的条件和参数更优。
在酸性环境下,Cr(Ⅵ)与DPC络合的效率随溶液pH的升高而降低,导致测定结果偏低;在碱性环境下,Cr(Ⅵ)无法发生络合反应。因此,需要对溶液体系进行酸化。按体积比加入去离子水和HNO3溶液,得到混合浆液的pH约为0.5。用3 mol·L−1 NaOH溶液调节混合浆液pH,结果如图3(a)所示。加入DPC的Cr络合物反应后溶液的最佳pH为0.5~1,故在前处理中无需调节溶液pH。溶液中过量的氧化剂H2O2将Cr(Ⅲ)氧化成Cr(Ⅵ)后,会优先和DPC发生反应,干扰Cr络合物的生成。DPC试剂的用量为0.1 mL时,可去除过量H2O2的干扰(见图3(b))。同时,所有试剂加入后静置10 min以保证溶液中的Cr络合物完全产生(见图3(c))。
2.2 标定曲线和检测限
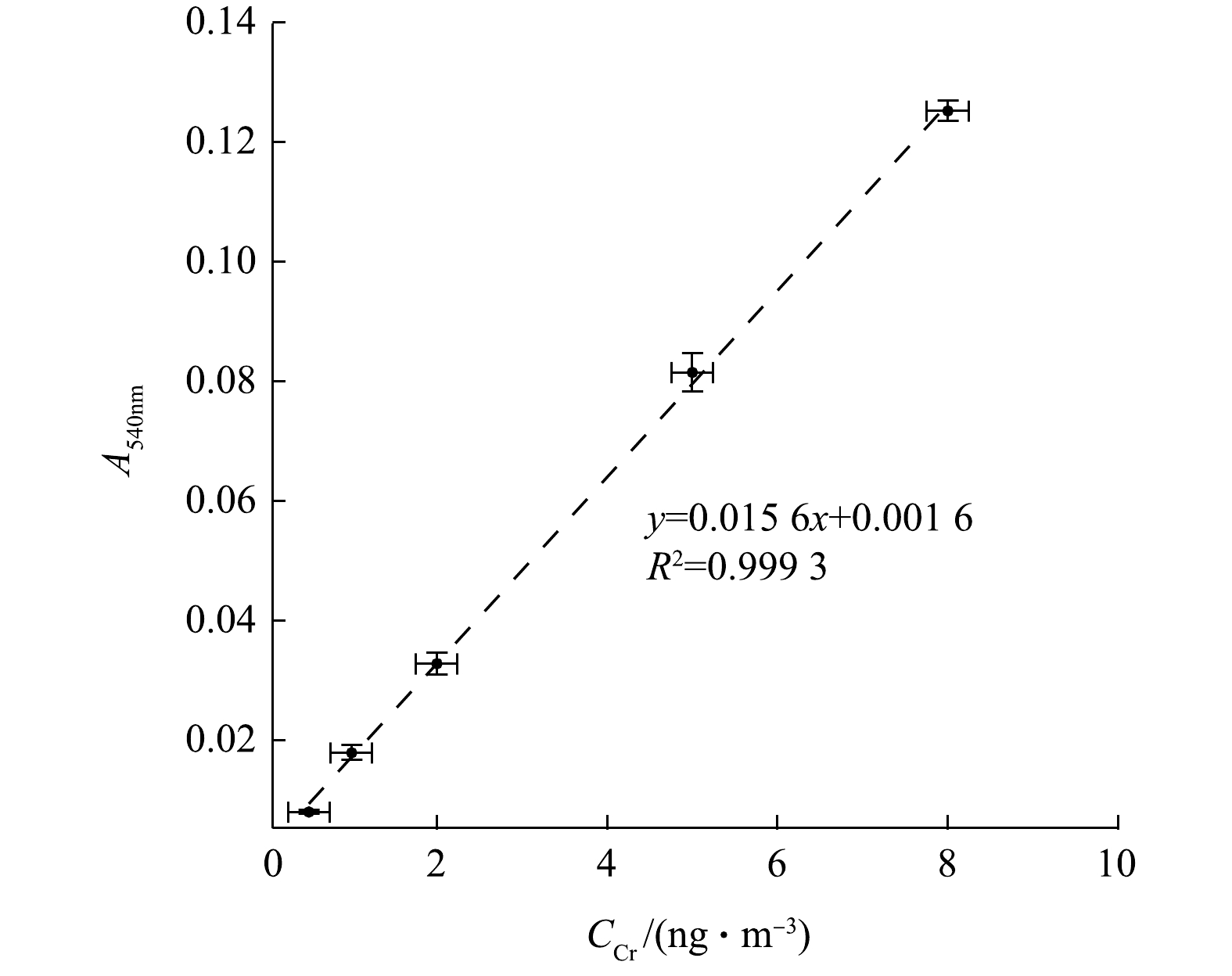
根据实际环境大气颗粒物中总Cr浓度,选择合适浓度梯度(0.5、1、2、5、8 ng·mL−1)的Cr(Ⅵ)标准溶液确定标准曲线。每次标定使用相同Cr(Ⅵ)母液,用去离子水稀释至所需浓度。图4为14 d内不同时间进行的5次标定结果的平均值,相同浓度的多次测定值范围以error bar形式在图中标出。几次标定得到的线性方程斜率在(0.015 6±0.000 2)mL·ng−1范围变化,并且所有标定曲线的R2均能达到0.99。系统分光光度测量的标定范围涵盖了一般环境大气颗粒物中Cr浓度范围。Cr浓度与其络合物的吸光度峰值呈稳定线性关系,多次标定反映出该结果重现性好。
根据空白样品吸光度峰值标准偏差的3倍来测算系统的检测限(limit of detection,LOD)。空白样品由空白石英膜按照样品的前处理过程制得。将加入DPC的空白样品通入LWCC测量吸光度峰值,LOD约为0.158 ng·mL−1,对应采样空气体积约为12 m−3。经过计算对应的环境颗粒物中Cr浓度为0.133 ng·m−3,大气颗粒物中Cr浓度至少比该LOD高一个数量级,故检测系统对Cr浓度的测定灵敏度较高,可满足大气监测需求。从上述空白样品的测定结果还表明,石英膜上Cr本底浓度极低,为(0.971±0.087)ng·g−1,不会干扰实际测量。
2.3 回收率实验
检测系统的回收率实验包括空白加标回收和样品加标回收两部分。空白样品的加标回收通过在空白石英膜上加入10 ng Cr(Ⅵ),再按照样品前处理步骤进行处理和分析测定,测定结果与理论值之比即空白加标回收率。用微升注射器(HAMILTON-7000)取用1 μL由相同Cr(Ⅵ)母液稀释所得浓度为10 μg·mL−1的Cr(Ⅵ)标液,直接加注在石英膜表面进行样品加标,以相同浓度的Cr(Ⅲ)标液(由纯度为99.99%的CrCI3·6H2O和去离子水制得)进行加标实验,通过加入0.1%的H2O2氧化Cr(Ⅲ)后,检测Cr(Ⅳ)浓度并与配置的Cr(Ⅲ)标液比较得到转化率。样品的加标回收则选用NIST商品化的城市颗粒物标准物质(NIST 1648 PM)作为样品。用清洁研钵将NIST样品磨碎,取2份(各5 mg)分别涂抹在空白石英膜上,其中1份加入10 ng Cr(Ⅵ)。将2份样品通过检测系统进行分析,2份样品测量的差值与加入标准Cr(Ⅵ)物质的理论值之比即加标回收率。上述实验均重复进行多次以减少偶然性误差。
由于使用高纯度的药品且系统测量受到干扰误差很小,Cr(Ⅵ) 空白加标回收率均值可达98%,标准偏差为2.4%(样品数为10);Cr(Ⅲ)的转化率为(95±2.6)%(样品数为10)。样品加标回收实验结果显示:在15个加标的标准环境样品中Cr(Ⅵ)回收率为(90.3±8.1)%;而对不加标的NIST标准样品中Cr浓度测定的误差范围为(9.6±3.3)%。ERG使用相同样品加标,通过碳酸盐缓冲液提取与离子色谱(IC)测得的回收率为((89.8±10)%, N=10)[20]。2组样品加标回收率经中位数检验并不存在统计上的显著差异,故该系统具有较好的采集和测量精度。
2.4 与ICP-MS方法的对比测试
ICP-MS是目前颗粒物中痕量金属的热门测定方法之一[21-22]。2014年,我国环境保护部将其确定为测量环境水样中多种痕量元素的标准方法(HJ 700-2014)。近年来,ICP-MS与各种分离技术联用已常见于Cr的相关研究中[23-25]。
将2016-12-17—2016-12-27在福州三中地区(PM2.5>80 μg·m−3)采集的高浓度大气颗粒物石英膜样品(膜规格:QMA-Whatman, 1851-050, Φ50 mm;采样时长3 h;采样流速16.7 L·min−1),分别通过本系统和ICP-MS测量总Cr浓度。
在进行ICP-MS测定前,将膜样品做密闭微波消解前处理。取用与本系统分析等量样品置于Teflon-TFM消解罐中,再加入10 mL HNO3和HCl的混合液(体积比为1:1),摇匀浸湿样品膜后放入微波消解仪(XT-9900A,上海新拓)中消解8 h。待消解罐冷却至室温,将其中的混合物用0.45 μm的醋酸纤维素滤膜进行过滤。将得到滤液用去离子水稀释至50 mL,用ICP-MS(X-Series2, US Thermo fisher)进行分析。
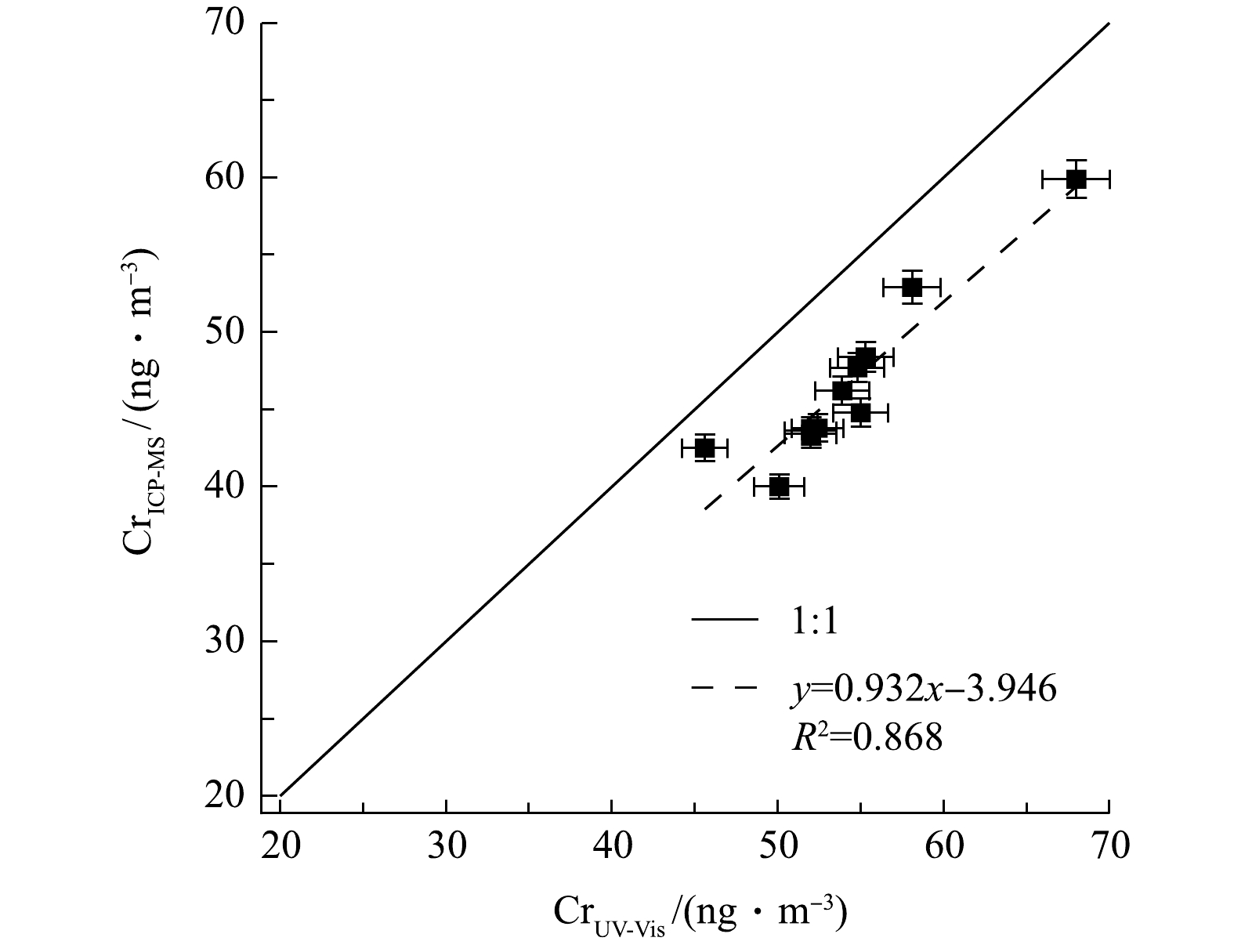
2种方法测量结果的相关性如图5所示,表明结果呈线性关系(斜率为0.932,R2为0.868)。该结果表明本系统对环境颗粒物中总Cr浓度测定的准确性与稳定性较好,也进一步证明本系统的前处理操作(包括酸化、加热搅拌等)能基本确保样品中所有含铬组分充分溶解,以得到可靠的测量结果。同时也表明若颗粒物样品含Cr组分中耐酸且难溶物质较多,会影响系统测量结果。
2.5 大气PM2.5中Cr浓度的外场实测
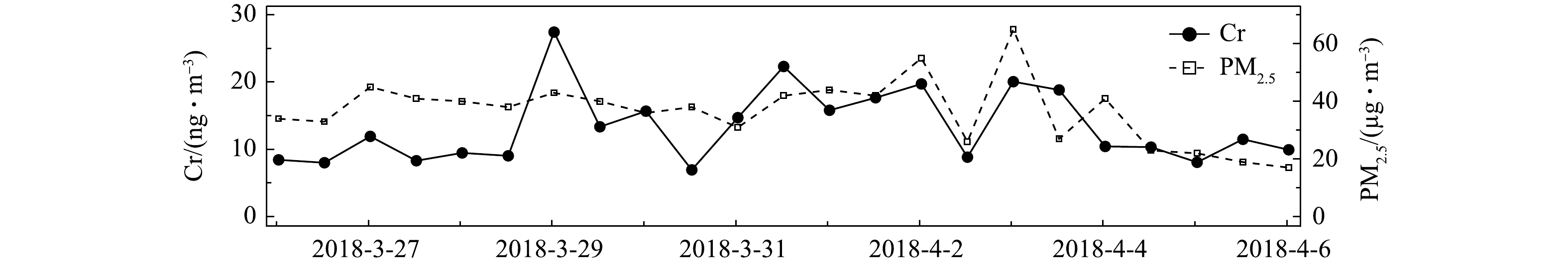
在2018-03-26—2018-04-06对环境大气PM2.5进行样品采集,每12 h采集1次,得到1周多的连续数据如图6所示。测得Cr浓度在采样期间出现了明显的变化,浓度为6.9~27.4 ng·m−3。该浓度水平与其他观测结果相似[27-28],Cr浓度的变化趋势与PM2.5的变化趋势基本一致。整个采样期间,Cr的日平均浓度为13.4 ng·m−3。而这段时间Cr浓度变化较大,这是由于春季空气污染过程频发,且受风向风速变化的影响较大。
分析Cr浓度的变化可发现,2018-03-28夜间到2018-03-29凌晨、2018-03-31白天、2018-04-01夜间到2018-04-02凌晨,以及2018-04-02夜间到2018-04-03凌晨这几个时段达到观测期间的峰值,平均值比日平均浓度高50%~67%;2018-03-30全天、2018-04-02白天Cr浓度降至观测期间日平均浓度的52%~60%;2018-04-04下午到2018-04-06凌晨,Cr浓度基本与采样期间的Cr日平均浓度持平。由于Cr被广泛用于工业生产,如冶金、铬镁耐火材料制造和电镀工艺等[29-31],交通工具的尾气排放和机械磨损[32]也会使环境大气颗粒物中含有这类过渡金属,Cr是地壳中的金属物质之一,故土壤粉尘和地面扬尘也为大气颗粒物中贡献了Cr[33-34]。结合采样点的地理位置分析可推断,大气颗粒物中的Cr主要来自早晚期间强烈的交通活动导致的直接排放和扬尘排放,以及偏东风带来的工业园区排放的污染气团。上述结果表明,本系统可对PM2.5中Cr浓度进行准确连续的测量。
3. 结语
1)设计并评估了一种基于分光光度法测量环境PM2.5中微量Cr的系统。系统通过膜采样经过前处理制成待测样品,再基于分光光度法测量样品中总Cr浓度。系统具有很好的灵敏度和重现性,采集效率较高,测量精度较好。用相同样品与ICP-MS测量结果的对比表明,系统可靠性和准确性均较好。外场采样观测的结果显示,系统具有足够的可靠性,在较少人工监管的情况下能够对环境细颗粒物中Cr进行较快速的连续测量。
2)设计中用到的通过替换金属络合试剂及对前处理步骤进行的优化方法,不仅能测定Cr的价态,还能帮助测定大气环境中部分金属浓度,为实现连续快捷地分析大气环境中水溶性金属离子的污染特征提供了参考。同时,根据大气颗粒物中Cr的来源可以判断,还应进一步研究不同季节大气中Cr的来源和日变化特征。
-
表 1 批次实验设计
Table 1. Design of batch experiments
实验组 振荡速度/(r·min-1) 温度/oC 盐度/‰ 初始pH I 0,100 22 32 8.0 II 0 15、22、30 32 8.0 III 0 22 0,16,32 8.0 IV 0 22 0 5.0、6.0、7.0、8.0 -
[1] DAUDA A B, AJADI A, TOLA-FABUNMI A S, et al. Waste production in aquaculture: Source, components and managements in different culture systems[J]. Aquaculture and Fisheries, 2019, 4(3): 81-88. doi: 10.1016/j.aaf.2018.10.002 [2] LUO G Z, XU J X, MENG H Y. Nitrate accumulation in biofloc aquaculture systems[J]. Aquaculture, 2020, 520: 734675. doi: 10.1016/j.aquaculture.2019.734675 [3] RAHIMI S, MODIN O, MIJAKOVIC I. Technologies for biological removal and recovery of nitrogen from wastewater[J]. Biotechnology Advances, 2020, 40: 107570. [4] 马秋莹, 李东, 封莉, 等. 前置反硝化生物滤池深度脱氮效能与影响因素[J]. 环境工程学报, 2017, 11(9): 4932-4936. [5] YUAN J Q, HUANG S B, YUAN H G, et al. Effects of chloramphenicol on the bacterial community structure and simultaneous nitrification and denitrification performance in a sequencing biofilm batch reactor[J]. Journal of Water Process Engineering, 2021, 42: 102095. doi: 10.1016/j.jwpe.2021.102095 [6] ZHAO J, FENG L J, YANG G F, et al. Development of simultaneous nitrification-denitrification (SND) in biofilm reactors with partially coupled a novel biodegradable carrier for nitrogen-rich water purification[J]. Bioresource Technology, 2017, 243: 800-809. doi: 10.1016/j.biortech.2017.06.127 [7] BHATTACHARYA R, MAZUMDER D. Simultaneous nitrification and denitrification in moving bed bioreactor and other biological systems[J]. Bioprocess and Biosystems Engineering, 2021, 44: 635-652. doi: 10.1007/s00449-020-02475-6 [8] 曹文娟, 徐祖信, 王晟. 生物膜中同步硝化反硝化的研究进展[J]. 水处理技术, 2012, 38(1): 1-5. doi: 10.3969/j.issn.1000-3770.2012.01.001 [9] 郑桂林, 张朝升, 曹勇锋, 等. DO在SBBR生物膜中传递及对同步硝化反硝化的影响[J]. 中国给水排水, 2016, 32(3): 22-26. [10] GUO J B, ZHANG L H, CHEN W, et al. The regulation and control strategies of a sequencing batch reactor for simultaneous nitrification and denitrification at different temperatures[J]. Bioresource Technology, 2013, 133: 59-67. doi: 10.1016/j.biortech.2013.01.026 [11] 黄胜娟, 荣宏伟, 林孟霞. pH对同步硝化反硝化生物膜内溶解氧分布的影响[J]. 环境工程学报, 2015, 9(9): 4233-4238. doi: 10.12030/j.cjee.20150923 [12] 郑丽纯, 汤兵, 郑义, 等. 不同C/N对半悬浮生物填料的同步硝化反硝化过程的影响[J]. 环境科学学报, 2018, 38(11): 4273-4282. [13] LANDES N, RAHMAN A, MORSE A, et al. Performance of a lab-scale membrane aerated biofilm reactor treating nitrogen dominant space-based wastewater through simultaneous nitrification-denitrification[J]. Journal of Environmental Chemical Engineering, 2021, 9(1): 104644. doi: 10.1016/j.jece.2020.104644 [14] 许育新, 孙鹂, 喻曼, 等. 同步硝化反硝化脱氮在水产养殖废水处理中的应用[J]. 浙江农业科学, 2015, 56(7): 1119-1121. [15] WANG J Y, RONG H W, CAO Y F, et al. Factors affecting simultaneous nitrification and denitrification (SND) in a moving bed sequencing batch reactor (MBSBR) system as revealed by microbial community structures[J]. Bioprocess and Biosystems Engineering, 2020, 43: 1833-1846. doi: 10.1007/s00449-020-02374-w [16] XU Z S, DAI X H, CHAI X L. Effect of different carbon sources on denitrification performance, microbial community structure and denitrification genes[J]. Science of the Total Environment, 2018, 634: 195-204. doi: 10.1016/j.scitotenv.2018.03.348 [17] LI P, ZUO J E, WANG Y J, et al. Tertiary nitrogen removal for municipal wastewater using a solidphase denitrifying biofilter with polycaprolactone as the carbon source and filtration medium[J]. Water Research, 2016, 93: 74-83. doi: 10.1016/j.watres.2016.02.009 [18] XU Z S, DAI X H, CHAI X L. Biological denitrification using PHBV polymer as solid carbon source and biofilm carrier[J]. Biochemical Engineering Journal, 2019, 146: 186-193. doi: 10.1016/j.bej.2019.03.019 [19] ZHAO J M, HE Q C, CHEN N, et al. Denitrification behavior in a woodchip-packed bioreactor with gradient filling for nitrate-contaminated water treatment[J]. Biochemical Engineering Journal, 2020, 154: 107454. doi: 10.1016/j.bej.2019.107454 [20] WANG J L, CHU L B. Biological nitrate removal from water and wastewater by solid-phasedenitrification process[J]. Biotechnology Advances, 2016, 34(6): 1103-1112. doi: 10.1016/j.biotechadv.2016.07.001 [21] 唐成婷, 罗国芝, 谭洪新, 等. 以PBS为载体和碳源的SND系统的脱氮效果研究[J]. 安全与环境学报, 2014, 14(5): 151-155. [22] SUN H M, YANG Z C, YANG F F, et al. Enhanced simultaneous nitrification and denitrification performance in a fixed-bed system packed with PHBV/PLA blends[J]. International Biodeterioration & Biodegradation, 2020, 146: 104810. [23] IBRAHIM M I, ALSAFADI D, ALAMRY K A, et al. Properties and applications of poly(3-hydroxybutyrate-co-3-hydroxyvalerate) biocomposites[J]. Journal of Polymers and the Environment, 2021, 29(4): 1010-1030. doi: 10.1007/s10924-020-01946-x [24] SOLIMAN M, ELDYASTI A. Ammonia-oxidizing bacteria (AOB): Opportunities and applications: A review[J]. Reviews in Environmental Science and Bio-technology, 2018, 17(2): 285-321. doi: 10.1007/s11157-018-9463-4 [25] DAIMS H, LUCKER S, WAGNER M. A new perspective on microbes formerly known as nitrite-oxidizing bacteria[J]. Trends in Microbiology, 2016, 24(9): 699-712. doi: 10.1016/j.tim.2016.05.004 [26] XU Z S, SONG L Y, DAI X H, et al. PHBV polymer supported denitrification system efficiently treated high nitrate concentration wastewater: Denitrification performance, microbial community structure evolution and key denitrifying bacteria[J]. Chemosphere, 2018, 197: 96-104. doi: 10.1016/j.chemosphere.2018.01.023 [27] DU R, PENG Y Z, JI J T, et al. Partial denitrification providing nitrite: Opportunities of extending application for anammox[J]. Environmental International, 2019, 131: 105001. doi: 10.1016/j.envint.2019.105001 [28] LU H J, CHANDRAN K, STENSEL D. Microbial ecology of denitrification in biological wastewater treatment[J]. Water Research, 2014, 64: 237-254. doi: 10.1016/j.watres.2014.06.042 -






 下载:
下载: