-
近年来,随着城市化规模的扩大和工业化的迅速发展,大气环境日益恶化,环境空气质量问题越来越被广大人民群众所关注[1-3]。2013年起国家实施环境空气质量新标准,完善了污染物项目和监测规范,提高了数据有效性要求,有利于进一步保护公众健康,环境空气质量管理由一次污染物控制向二次污染物为主的复合污染控制转变。同年,国家颁布并实施《大气污染防治行动计划》[4]明确提出重点省市需要建立重污染天气监测预警体系,提升空气质量监测预警能力,环境空气质量预报工作作为大气污染防控及重污染预警的基础工作,已成为环境监测部门核心业务之一,而预报方法的准确性决定了其可用性,对预报模式效果评估是实现预报预警的前提。
目前应用范围较广的环境空气质量预报方法有统计预报法[5]和数值预报法[6-7]。统计预报法[8-10]简单易行、成本低,适合短期预报,但缺少确定性污染机理,难以捕捉重污染过程且重污染预报准确率偏低;数值预报法对于区域性长期预报有一定优势,但在技术及硬件设施方面投入较大。其中,集合预报法同时运行多个空气质量预报模式,准确率较高。目前数值预报是包括沈阳市在内新疆[11]、江苏[12]和河南[13]省多城市预报工作选择的主要预报手段。沈阳市2018年建立环境空气质量多模式预报预警系统,现选取系统中国际主流预报模式中第三代空气质量预报和评估系统空气质量模式(congestion mitigation and air quality, CMAQ)及国内应用较多的嵌套网格空气质量模式系统(nested air quality prediction model system, NAQPMS)空气质量预报模式的预报数据,进行定量评估,对比2种预报模式在沈阳市2019年采暖季(1~3月、11月和12月)的预报效果,以期为东北地区城市大气污染变化和空气质量预报工作的发展提供经验借鉴。
-
研究监测数据来自沈阳市11个环境空气自动监测国控站,仪器监测、数据分析统计严格参照《环境空气质量标准:GB 3095—2012》[14]《环境空气质量指数(AQI)技术规定(试行):HJ 633—2012》[15]《环境空气质量技术评价规范(试行):HJ 663—2013》[16]等相关标准执行。
数值预报模式为嵌套网格空气质量预报系统NAQPMS模式及区域多尺度空气质量模型CMAQ模式。2种模式均为前一日20时发布未来3日预报,包括污染物浓度、AQI和首要污染物。本研究选取2种模式的24 h、48 h和72 h预报结果进行评估。
-
区域多尺度空气质量模型(CMAQ)是由美国环境保护局(Environmental Protection Agency, EPA)开发的第三代空气质量预报和评估系统,被广泛应用于区域环境质量评估、污染成因分析、决策研究和空气质量预报等方面。CMAQ模式突破了传统模式针对单一物种和单相物种的模拟,是一种适用于模拟城市或区域尺度臭氧、酸沉降、能见度和气溶胶等的多尺度综合空气质量模式,模式以WRF等中尺度气象模式作为气象驱动模型,以SMOKE等源排放处理模型作为源处理模型。主要由边界条件模块、初始条件模块、光分解速率模块、气象-化学预处理模块和化学传输模块构成[17]。化学转化模块是CMAQ模式的核心模块,其综合考虑了污染物在大气中的空气动力学过程、气象化学过程、气溶胶过程和云化学与动力过程。
嵌套网格空气质量预报模式系统(NAQPMS)由中国科学院大气物理研究所研制,是区域和城市尺度三维欧拉化学传输模式[18]。可模拟细颗粒物、臭氧、氮氧化物、二氧化硫和一氧化碳等大气痕量气体和大气气溶胶。被广泛应用于多尺度污染问题的研究,不但可以研究区域尺度的空气污染(沙尘、酸雨等污染物的跨区域传输),还可以研究城市尺度的空气质量的发生机理及变化规律,和不同尺度区域间空气质量变化的相互影响。
-
目前常用的空气质量评估指标很多,本研究选择平均偏差(MB)、均方根误差(RMSE)、平均分数偏差(MFB)、平均分数误差(MFE)和相关系数(r)等统计指标,具体公式见文献[19]。对2种数值预报模式污染物浓度预报值预报准确率进行检验,通过衡量预报值与实况值的偏离来评价预报结果的稳定性及可行度。其中,MB的大小主要表示样本总体预报值比实况值偏大或偏小的数值;RMSE 反应了预报值与实况值的差值,其值越接近0,表明预报效果越好;r表示预报值与实况值逐渐变化趋势的吻合程度,其值越接近1,表示预报效果越好;MFB、MFE是2个无量纲的统计量,合理预报范围为−60%≤MFB≤60%、MFE≤75%;理想水平范围−30%≤MFB≤30%、MFE≤50%。
-
依据《环境空气质量预报成效评估方法指南》[20]要求,常规业务预报评估可使用城市AQI范围准确率、AQI级别准确率及首要污染物准确率。
AQI范围准确率评估,当预报级别为优、良、轻度污染、中度污染时,预报范围以实况值±15为正确;当预报级别为重度污染、严重污染时,预报范围以实况值±30为正确,见式(1):
式(1)中,n表示AQI范围预报准确的天数,N表示评估预报总天数。
AQI级别准确率评估,当实况AQI级别在预报结果范围内,包含跨级别预报,则预报正确,否则错误,见式(2):
式(2)中,n表示AQI级别预报准确的天数,N表示评估预报总天数。
首要污染物准确率评估,当实况首要污染物为单一时,预报首要污染物为1个,且与实况相同,则预报正确;若预报首要污染物为2个,且其中1个与实况一致,则预报正确。当实况首要污染物为多个,若预报首要污染物与预报一致,则预报正确;若预报首要污染物为1个,与实况出现首要污染物中1个相同,也记为预报正确。当实况为优,无首要污染物,不做首要污染物预报评估,见式(3):
式(3)中,n表示首要污染物预报准确的天数,N表示评估时段内非优预报总天数。
-
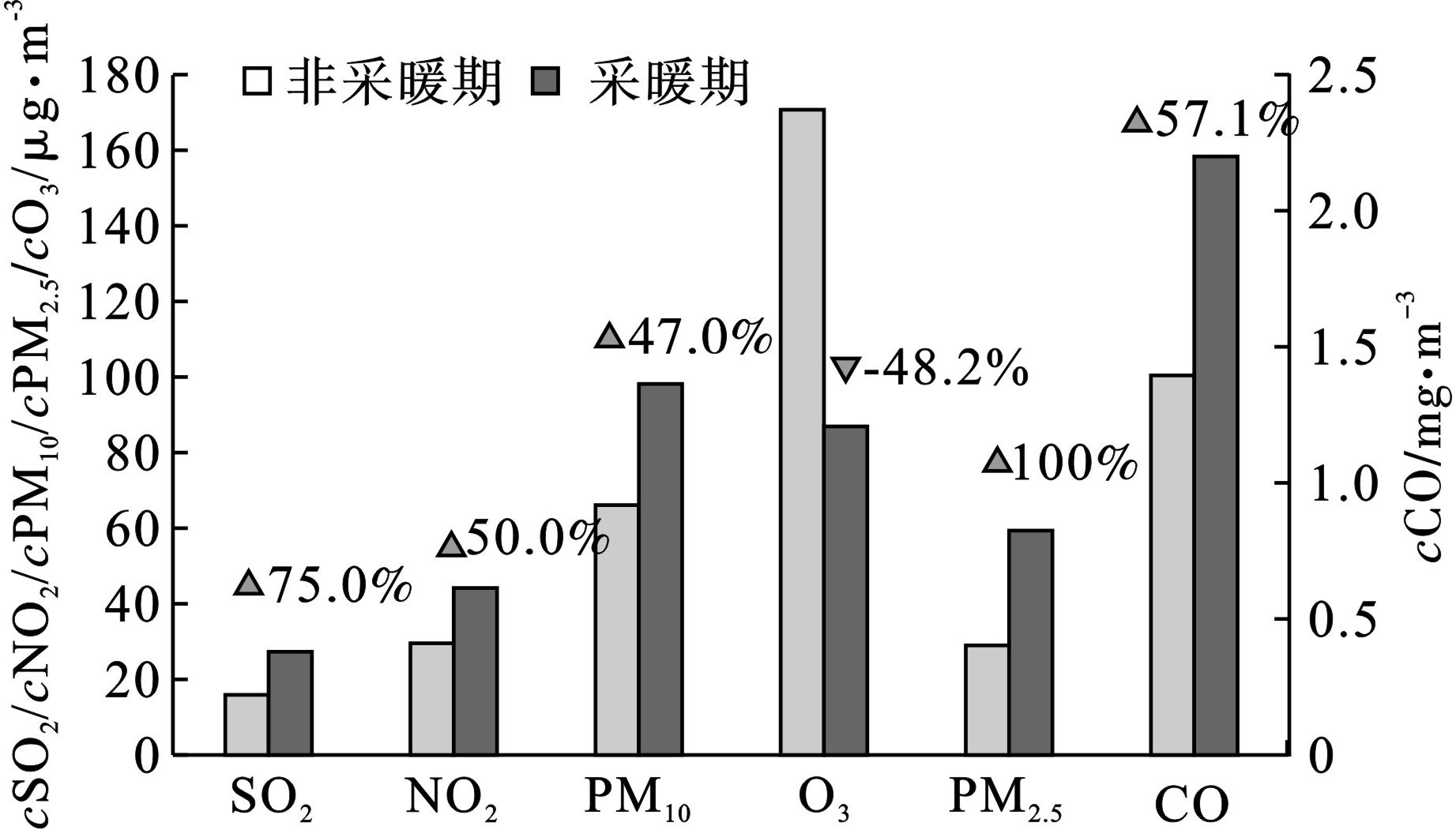
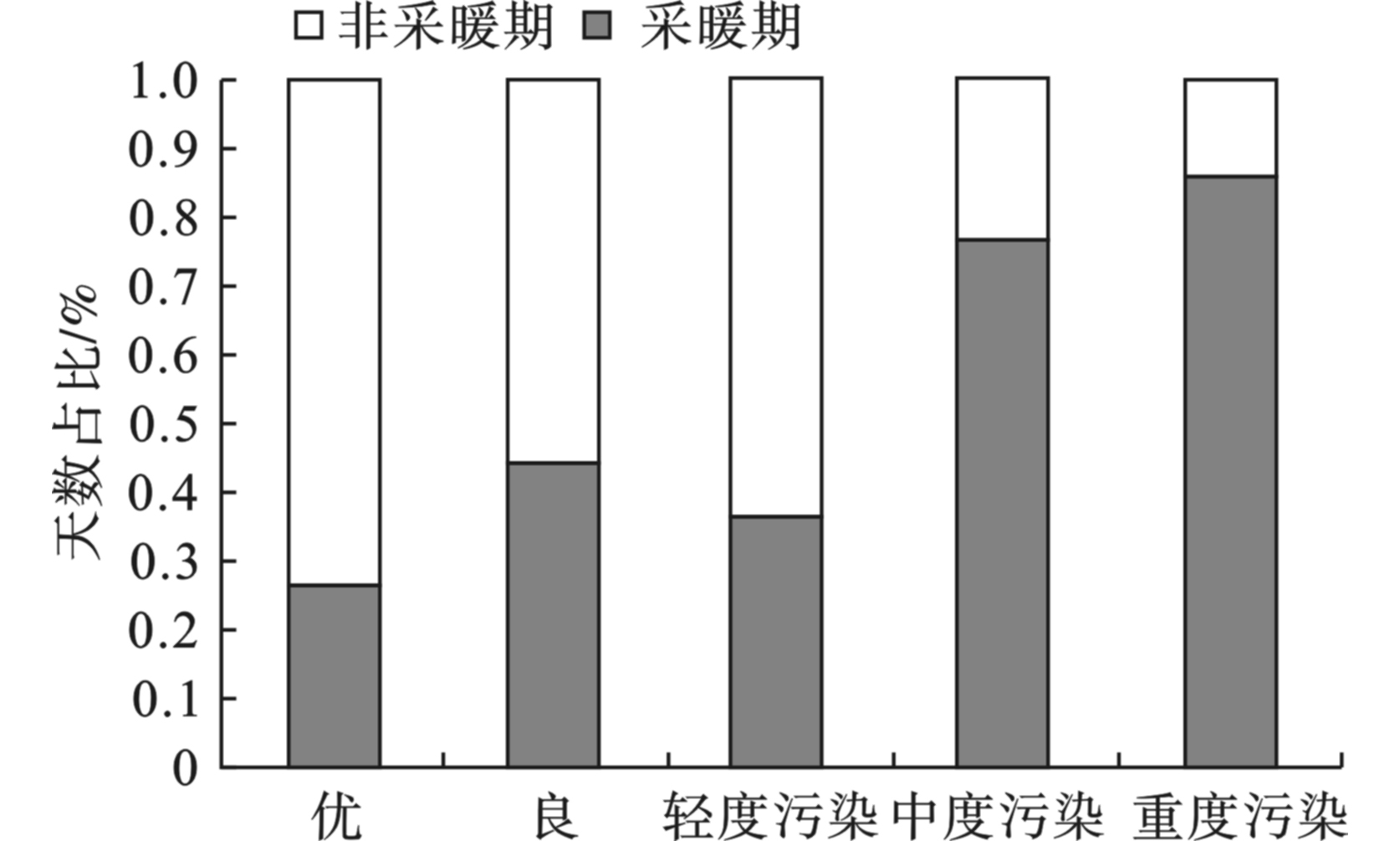
2019年1~3月、11月和12月为沈阳市采暖期,占全年总天数41.4%。对比6项主要污染物,采暖期仅臭氧浓度低于非采暖期,由于臭氧作为二次污染物,主要受温度、太阳辐射影响,由于冬季气温及太阳辐射较夏季均偏低,臭氧光化学反应减弱,臭氧浓度明显低于夏季,见图1。
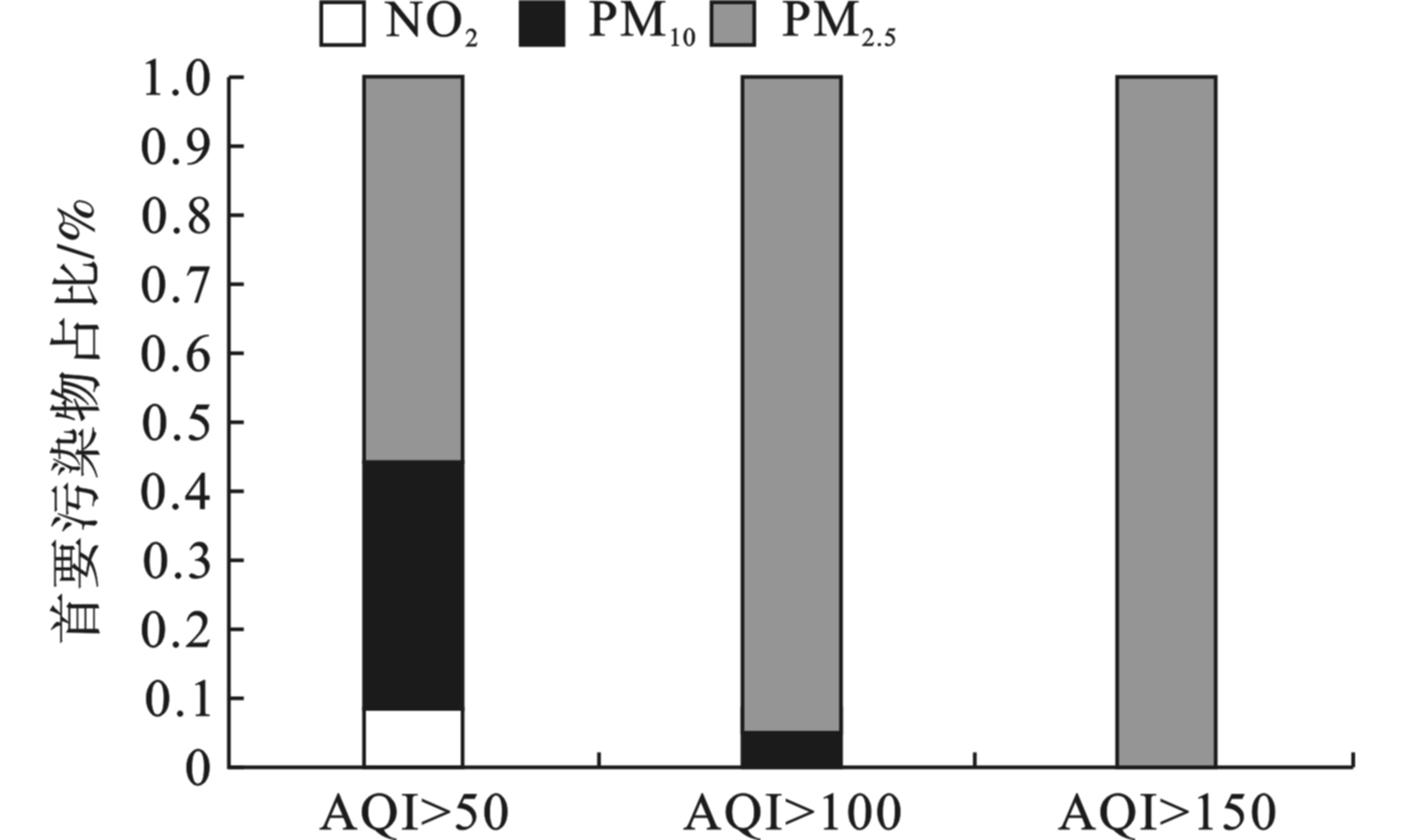
其他5项污染物浓度均高于非采暖季,其中,细颗粒物(PM2.5)浓度升高幅度最大,达到100%,二氧化硫(SO2)、二氧化氮(NO2)、一氧化碳(CO)和可吸入颗粒物(PM10)浓度上升幅度分别为75.0%、50.0%、57.1%和47.0%。2019年采暖期与非采暖期不同空气质量类别天数占比,采暖期优良天数占全年优良天数的39.8%,中度及以上污染天数占全年80%,见图2。进一步对比采暖期不同污染类别首要污染物变化,见图3。
当AQI ﹥50时(良,轻度及以上污染),出现3种首要污染物分别为NO2、PM10和PM2.5,PM2.5为首要污染物天数占总天数55.9%;AQI ﹥100(轻度及以上污染)出现2种首要污染物(PM10和PM2.5),PM2.5为首要污染物天数占总天数94.7%;AQI ﹥150(中度及以上污染)仅出现PM2.5一种首要污染,占总天数100%。
空气质量类别及污染物浓度对比结果均显示出采暖期空气质量差于非采暖季。当污染程度越重,首要污染物逐渐单一且集中表现为PM2.5,PM2.5成为采暖季的主要污染物。因此本文以PM2.5来分析采暖季的2种预报模式及其预报效果。
-
沈阳市采暖期中CAMQ、NAQPMS模式未来24、48和72 h的AQI范围预报、AQI级别预报及首要污染物预报准确率,见表1。
表1可知,2种模式的AQI范围预报、AQI级别预报均表现出预报准确率随预报时次延长准确率下降,即24 h准确率高于48、72 h。首要污染物预报准确率表现为各预报时次准确率相差不大。AQI范围预报、AQI级别预报准率最高的为CAMQ模式的24 h预报,准确率分别为43.7%、74.2%;首要污染物预报准确率最高的为NAQPMS模式48 h预报,准确率为60.9%。
2种预报模式中仅48 h首要污染物预报NAQPMS模式略高于CAMQ模式,其他各预报时次的AQI范围预报、AQI级别预报及首要污染物预报均表现为CAMQ模式准确率高于NAQPMS模式。综合3种评估分析,CAMQ模式预报准确率优于NAQPMS模式。
-
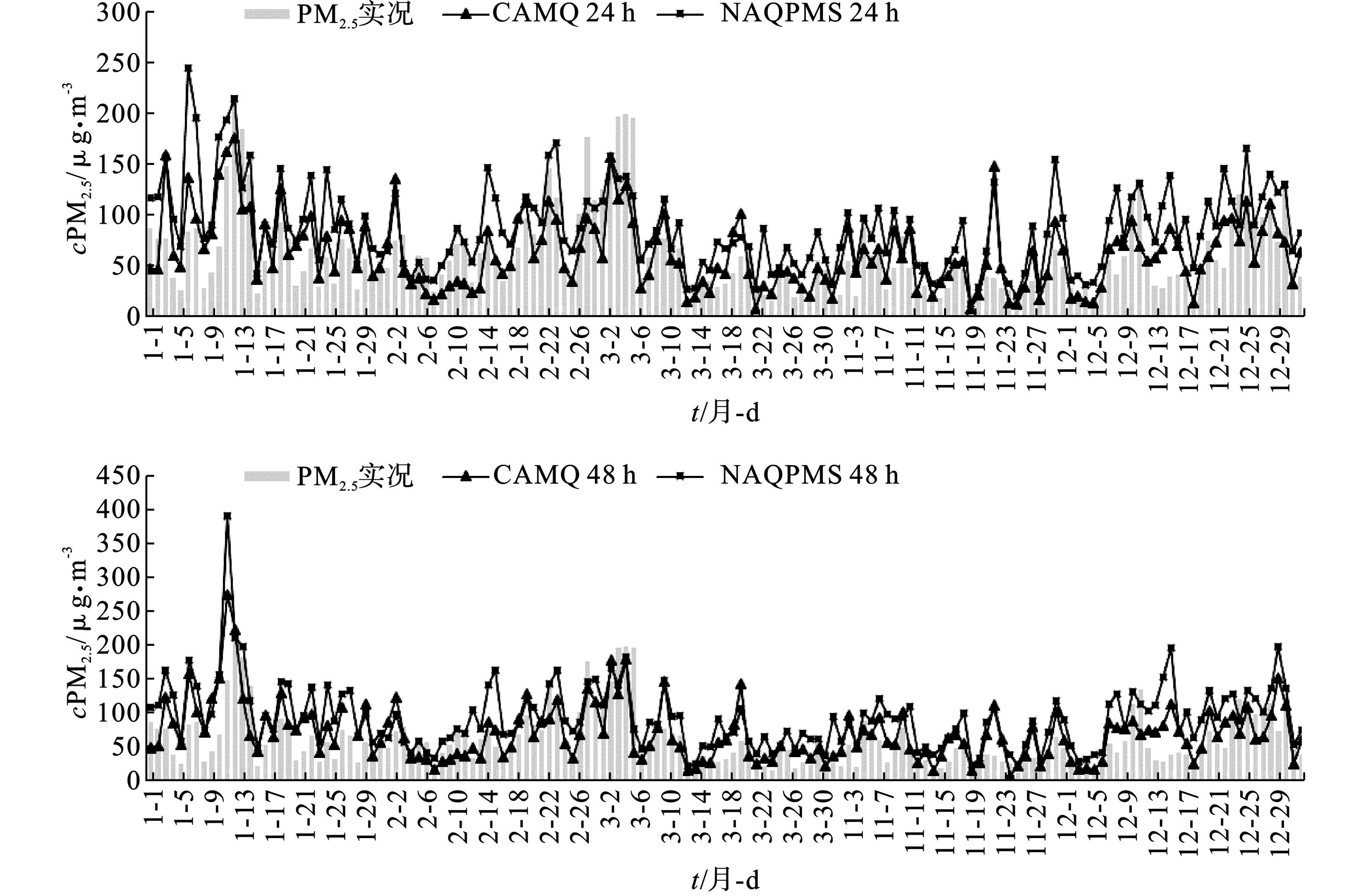
分别利用未来24、48 和72 h PM2.5预报浓度值与PM2.5实况浓度进行2019年采暖季PM2.5日均浓度对比分析。通过预报及实况浓度时间序列对比,来评估预报模式对污染物浓度累积及清除的预报能力。CAMQ、NAQPMS模式在3种预报时次中对PM2.5浓度预测值与实况值的变化趋势基本相似,说明2种模式对PM2.5浓度累积及清除过程具有一定的预报能力,但预报值与实况值仍存在一定偏差,预报模式均有优化空间,见图4。
2种预报模式在24、48和72 h预报中,在11月19~21日、12月7~8日、12月13~15日和12月20~21日均出现明显预报偏高情况,且预报趋势与实况相反。2种模式还存在对PM2.5浓度的峰值预判过度情况,1月10~12日、3月19~21日和11月19~20日出现预报浓度过高情况。
-
散点图用于对比成对的数值,对模型的模拟值与实况监测值间时空配对后,用来分析模式预报值与实况值的吻合程度,并可反映出预报值对实况值的高估或低估。设预报值处于实况值的0.5~2倍范围内认定为预报值可接受,采用FAC表示预报值在实况值0.5~2倍范围内的比例。
2019年采暖期CAMQ模式PM2.5浓度预报效果优于NAQPMS模式,CAMQ模式PM2.5浓度预报值基本集中在y=x附近,且呈收敛趋势;而NAQPMS模式PM2.5浓度预报值呈现明显偏高情况,多数集中在y=x于y=2x间,且随预报时间延长,预报高估情况愈加明显。2019年采暖期CAMQ模式的PM2.5浓度预报值FAC整体高于NAQPMS模式,随预报时长增加而降低。CAMQ模24 h预报FAC最高,达到88.7%,NAQPMS模式48 h、72 h 的FAC最低,为65.6%,见图5。
-
通过统计分析对CAMQ、NAQPMS模式PM2.5日均浓度预测能力进行定量评估。2种预报模式的预报效果,见表2。
对比多种统计指标,CAMQ、NAQPMS模式对PM2.5的预报能力均表现出预报时次越短,预报效果更优,24 h预报效果最优,48 h次之,72 h最差。从2种预报模式预报值与实况值的MB来看,CAMQ、NAQPMS模式预报值均高于实况值,偏离程度随预报时长增加而增大,CAMQ模式PM2.5浓度预报偏高在1.25~11.38 μg/m3之间,NAQPMS模式预报偏高在26.52~35.19 μg/m3之间。NAQPMS模式预报值的偏离程度大于CAMQ模式。2种预报模式对PM2.5浓度预报的NMB、NME和R2均符合−50%<NMB<80%,NME<150%,R2>0.3要求,CAMQ模式的NMB、NME均﹤50%,预报效果优于NAQPMS模式。2种预报模式对PM2.5浓度预报的RMSE表现为CAMQ模式每个预报时次的RMSE均小于NAQPMS模式,CAMQ模式预报值与实况值偏差小于NAQPMS模式。2种预报模式MFB及MFE评估结果显示,CAMQ模式3个预报时次的MFB及MFE均处于理想范围内,NAQPMS模式的MFB及MFE则落于合理范围。综合多种统计指标,CAMQ模式对PM2.5浓度预报效果优于NAQPMS模式。
-
本研究基于2019年采暖期(2019年1~3月、11月和12月)空气质量实况值,采用CAMQ、NAQPMS模式模拟了沈阳市PM2.5浓度,评估了2种模式对单一污染物的预报能力。以统计等级、范围和首要污染物准确率评估了预报模式对污染物综合预报能力。以上结果均表现出CAMQ模式优于NAQPMS 模式,可为人工订正预报提供参考。
(1)沈阳市采暖期环境空气质量污染程度重于非采暖期,采暖期除臭氧外其他5项污染物浓度均高于非采暖季,采暖期细颗粒物浓度较非采暖期上升幅度达到100%。采暖期中度及以上污染占全年80%,首要污染物以细颗粒物为主。
(2)CAMQ、NAQPMS模式等级、范围和首要污染物准确率均为24 h预报准确率最高,而CAMQ模式的24 h等级、范围和首要污染物准确率高于NAQPMS模式,CAMQ模式综合预报能力更优。
(3)时间序列对比结果显示2种预报模式预报值与实况值总体时间变化趋势一致,但仍存在偏差,均表现为预报值明显高估。散点图对比结果显示2种模式对细颗粒物浓度预报均存在不同程度高估,随预报时次增加,偏高程度增大。CAMQ模式24 h预报的可接受度最高,为88.7%。
(4)利用统计分析对比2种模式对细颗粒物预报效果进行定量评估,CAMQ、NAQPMS模式对PM2.5的预报能力均表现出预报时次越短,预报效果更优。CAMQ模式预报效果优于NAQPMS模式。CAMQ模式3个预报时次预报效果均达到理想水平。
沈阳市采暖期空气质量预报模式预报效果对比与评估
Evaluation and comparison of predication effects by several air quality prediction models in heating period
-
摘要: 利用2019年沈阳市采暖期环境空气质量监测数据,分析沈阳市采暖期空气质量状况及PM2.5污染特征,同时对CAMQ、NAQPMS模式等级、范围和首要污染物及PM2.5浓度24、48和72 h预报能力评估。结果表明,采暖期环境空气质量污染程度重于非采暖期,首要污染物以PM2.5为主。对比不同时效预报效果,24 h预报准确率高于48和72 h;CAMQ模式在不同预报时效中等级、范围和首要污染物准确率均高于NAQPMS模式。2种预报模式均能合理预测沈阳市PM2.5浓度的时空变化,但2种模式均存在预报结果偏高情况,NAQPMS模式预报偏高程度高于CAMQ模式。CAMQ模式预报效果可达到理想范围(−30%≤MFB≤30%、MFE≤50%),NAQPMS模式预报效果在合理范围(−60%≤MFB≤60%、MFE≤75%)。Abstract: Based on the ambient air quality monitoring data of the heating period in Shenyang in 2019, the air quality status and PM2.5 pollution characteristics were analyzed. In addition, the prediction abilities of CAMQ and NAQPMS in the level, range, primary pollutants and PM2.5 concentration with 24 hours, 48 hours and 72 hours were evaluated. The results showed that the pollution degree of air quality in the heating period was more serious than that in non-heating period, and the main pollutant was PM2.5. Comparing with the prediction effect of different aging time, the prediction accuracy of 24 hours was higher than that of 48 and 72 hours. The predicting accuracy of CAMQ model was higher than NAQPMS model in the grade, range and primary pollutants in different time periods. Two air quality models could reasonably predict temporal and spatial variations of PM2.5 concentrations in Shenyang. However, both of the two models had high prediction results, and the NAQPMS model was higher than the CAMQ model. The prediction effect of CAMQ model could reach an ideal level (−30%≤MFB≤30%, MFE≤50%), and the prediction effect of NAQPMS model was in the reasonable range (−60%≤MFB≤60%, MFE≤75%).
-
Key words:
- heating period /
- prediction model /
- assessment /
- ambient air
-
在植物浮床处理污水过程中,植物根系起到至关重要的作用。植物根系具有释氧、释放根系分泌物、拦截、吸附和吸收污染物的能力[1-5],并与微生物协同作用达到污染物去除的效果。挺水植物根系发达,茎秆粗壮、中空,有发达的通气组织,有利于氧在体内的传输并能传送到根区,形成氧化态的微环境促进根区的氧化还原反应和好氧微生物的活动。植物根系分泌物可以促进某些嗜磷、氮细菌的生长,从而间接提高净化率,有植物的湿地系统植物根部的细菌比介质处高1~2个数量级[6]。成水平等[7]研究发现香蒲和灯心草的存在有利于微生物在人工湿地纵深的扩展。植物浮床中挺水植物根系悬浮在水中,交织成良好的过滤网络,根须之间拦截颗粒物质,并且吸附和吸收溶解态污染物。
氮和磷作为植物营养元素,同时是污水处理中主要的污染物,植物根系类别的不同会影响植物强化脱氮除磷的效果。从植物营养学方面来说,植物的根系类型不同,它们吸收养分的效率就有一定差异。徐冰等[8]通过研究内蒙古锡林河流域草原植物发现双子叶植物根系中氮磷比例(0.379)显著高于单子叶植物(0.192)。WERAGODA et al[9]通过浮床实验认为根的粗细和密度影响植物根系参与污染物去除的作用。植物主要通过根系从介质中获得养分,因此介质和根系状况都影响养分的有效性。挺水植物大多为被子植物,被子植物分为单子叶和双子叶植物2类,他们不仅在子叶和叶脉上存在差异,根系结构也明显不同[10]。单子叶植物的主根不够发达,在与根连接的茎基和茎节等处长出许多不定根,并形成大量粗细差不多的各级侧根,是粗细比较均匀的须根系,根长与表面积也都比较大。双子叶植物的侧根和主根都可进行次生生长,形成粗细悬殊较大的不均匀的直根系结构。直根系在根长与总吸收表面积上都小于须根系。然而,以往的实验研究大多进行单个植物间脱氮除磷能力的比较[11-14],很少涉及植物根系类别的分析。
本研究通过模拟污水和实际污水分别培养美人蕉和水芹,探究污水中污染物去除效果,考察植物脱氮除磷贡献率和直根系、须根系对污染物的去除能力差异,以期为人工湿地或生物浮床的植物选择上提供新的支撑。
1. 材料与方法
1.1 供试植物
美人蕉和水芹都是多年生水生植物,在生态环境治理工程中常作为生物塘和表流湿地、人工浮床的配置植物应用。美人蕉株高1~2 m,叶片长披针形,蓝绿色,总状花序顶生,多花,花径约10 cm呈黄色、红色或粉红色;生长适宜温度15~28 ℃,低于10 ℃不利于生长,是单子叶草本植物。水芹茎秆直立有棱,叶片为羽状复叶,互生,叶缘具齿;复伞形花序,顶生,花白色;性喜温凉环境,不耐高温和干旱,每年有2个生长高峰季节,分别为12月~次年4月和9~11月,生长对养分需求量较大,是双子叶草本植物。
1.2 实验方法
实验用水箱为PP材质,长×宽×高=75 cm×25 cm×50 cm,下部一侧开孔装有阀门便于放水,水箱共12组,每组设置3个平行实验,配置厚5 cm泡沫板,放置于采光通风良好的玻璃房内。选择美人蕉和水芹2种,分别种植在污水和模拟污水中,同时设置不种植植物的污水空白组。根据实际污水特点,模拟污水中COD选用乙酸钠配制,采用尿素和氯化铵配制TN及NH4+-N,磷酸二氢钾配制TP和PO43−-P。模拟污水和实际污水中污染物初始浓度范围为COD(37~43 mg/L),TN(11.7~13.6 mg/L),NH4+-N(7.87~11.80 mg/L),TP(0.99~1.39 mg/L),PO43−-P(0.82~1.36 mg/L),pH 6.5~7.5。
将植株幼苗清洗干净,在自来水中培养1周后量取植株鲜重、茎长、根长、根数和根宽,选择2种植株各3棵进行植株干重及氮磷含量测定。每个植物处理组种植3棵相同植物植株,测量鲜重、根茎长度和根数。水箱用黑色塑料膜覆盖包裹四周,减少水中因光合作用生长的藻类对实验的影响。采水样2次/周,每次采集250 mL,采植物样1次/周,根据实验数据补充污水及模拟污水体积,持续进行5周。实验结束后选择每组生长良好的植株各3棵测量干重及氮磷含量。
1.3 数据处理
污染物去除率计算,见式(1):
stringUtils.convertMath(!{formula.content}) (1) 式中:C0为污染物如TN、NH4+-N、TP和PO43--P的初始浓度值,mg/L;Ce为实验结束时污染物的最终浓度值,mg/L;V1和V2为水箱中水的初始和最终体积,L。分子表示水中污染物总去除量,mg。
植物累积氮或磷总量(mg)计算,见式(2):
stringUtils.convertMath(!{formula.content}) (2) 式中:m1为初始植物干重,g;m2为最终植物干重,g;ρ1、ρ2为初始和最终氮或磷含量,mg/kg(干重)。
2. 分析与讨论
2.1 根系和分蘖数、微生物、生物量增长
经测定,实验中pH在6.5~8之间,适合挺水植物生长。实验前后植物生长平均值汇总,见表1。
表 1 实验前后植物生长平均值植物生长情况 M-水芹 M-美人蕉 W-水芹 W-美人蕉 茎长/cm 始 33 42 34 42 末 45 66 48 64 根长/cm 始 8 8 10 12 末 13 14 19 25 根数/个 始 47 14 55 17 末 60 36 87 48 分蘖数/个 始 0 0 0 0 末 7 7 7 8 鲜重/g 始 16.5 48.5 19.0 55 末 49.0 135.0 58.5 189 注:M表示模拟污水,W表示实际污水。 表1可知,实验结束时2种植物均有所生长,且茎基处分蘖出新枝和新根。水芹的生物量各项指标增加均比美人蕉增加较少,根数始终比美人蕉多但多为细小短须根。从植物根系角度分析,水芹是双子叶植物,根属于直根系,主要的主干根系都可以进行次生生长,粗细悬殊较大不均匀,根长和表面积都比较小;美人蕉是单子叶植物属须根系,主根不发达,有大量粗细差不多的各级侧根,根长和表面积都较大[15]。
2.2 氮去除情况分析
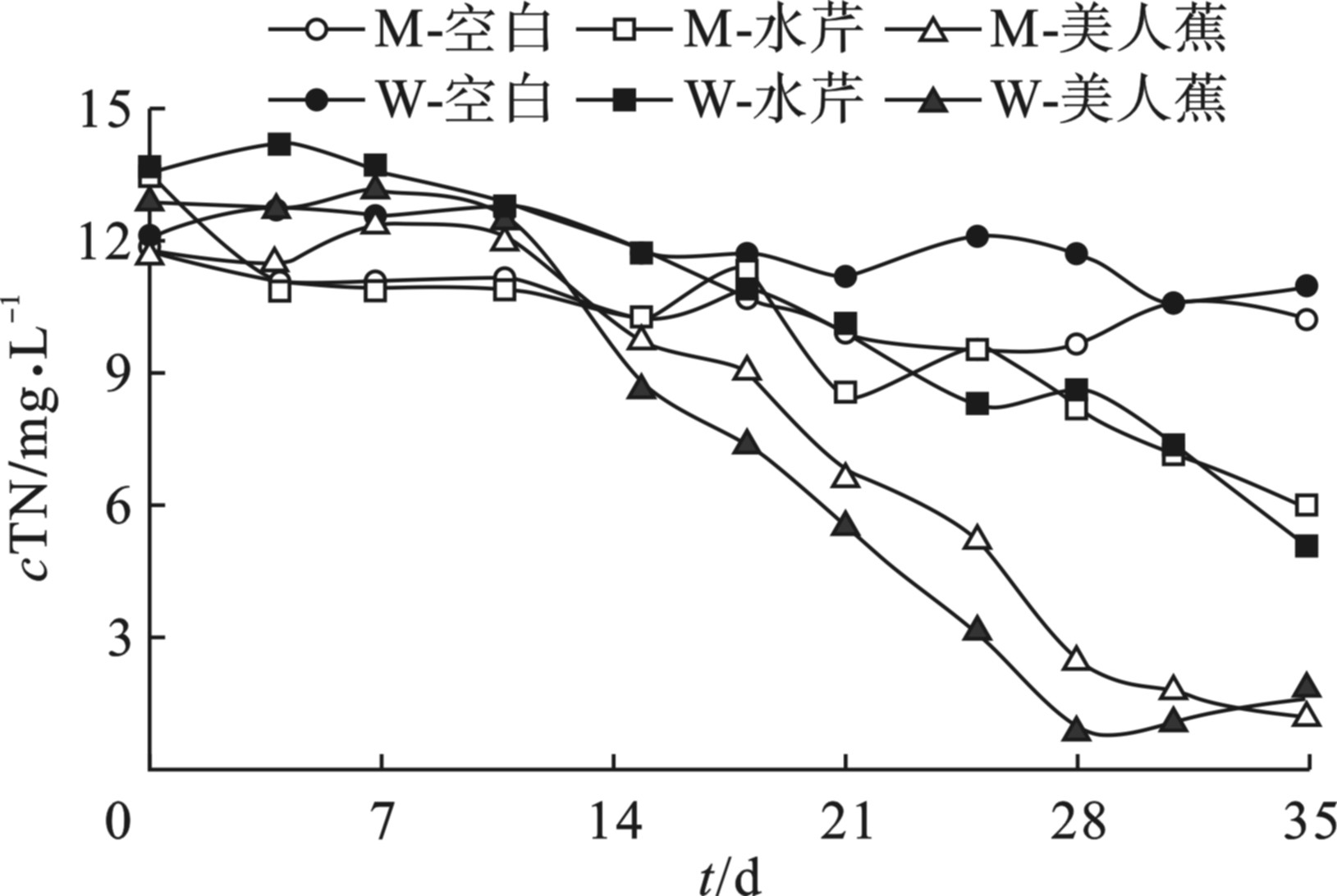
TN的去除效果随时间变化情况,见图1。
除空白对照组以外,TN浓度均有所减少,美人蕉组TN浓度降至最低。经过美人蕉处理后模拟污水TN浓度为1.14 mg/L,实际污水TN浓度为1.62 mg/L,水芹处理后模拟污水和实际污水TN浓度分别为5.85 和5.00 mg/L。从3方面分析原因:首先,种植植物后TN浓度较空白组明显下降,主要是挺水植物对氮的吸收增强了TN的去除效果,同时植物根系周围为微生物生存提供了好氧和缺氧环境,加强了硝化反硝化脱氮[16]。其次,实验中美人蕉较水芹TN去除量多,这与植物生长状况相对应,实验中美人蕉生长较水芹显著占优势,茎干挺拔,根系发达,而水芹生长缓慢。最后,同一植物处理组中模拟水和污水TN浓度相差较小,说明实验中植物吸收去除TN发挥主要作用,而不是污水中微生物反硝化脱氮。这可能是实验初始COD含量和植物根系分泌物较少[17],不能提供足够的碳源供反硝化细菌正常生长,导致实验中微生物反硝化脱氮效果微弱。
NH4+-N的去除效果,见图2。
模拟污水中NH4+-N在第1周浓度平均升高了约1.78 mg/L;2种污水中第2周NH4+-N浓度缓慢下降;第3周和4周植物组浓度下降迅速,空白组也呈下降趋势;第5周植物组浓度降至最低,空白组继续缓慢减少。最终,经过水芹和美人蕉处理后模拟污水NH4+-N浓度分别为0.09和0.07 mg/L,实际污水NH4+-N浓度分别为0.09和0.12 mg/L,空白组NH4+-N浓度分别为5.63和9.36 mg/L。对比可见,种植挺水植物有助于加快水中NH4+-N的去除。实验中NH4+-N浓度变化的几个原因如下:(1)污水中氮的形态主要是有机氮和NH4+-N,前期水中部分有机氮的氨化作用转化为NH4+-N使得浓度有所升高;(2)在植物处理组,植物根系吸收NH4+-N作为氮营养元素为生长养分,根据动力学原理[18]可知反应速率与底物浓度呈正相关,前期水中NH4+-N浓度迅速下降,后期由于水中NH4+-N浓度太低植物根系的吸收也相应减弱,浓度变化变缓;(3)污水中微生物同样参与了NH4+-N的转化去除,植物根系将光合作用产生的氧气传递到根际周围,为微生物创造有氧环境将NH4+-N硝化氧化为NO3−-N,而且由于植物根系的存在充当微生物附着载体,植物组微生物较空白组多,所以植物组NH4+-N去除效果较好。2种植物对NH4+-N去除效果无明显差异,进一步证实本实验中NH4+-N浓度对于美人蕉和水芹生长所需太低,达不到奢侈吸收的程度[19-20],最终植物生物量增长不明显。
2.3 磷去除情况分析
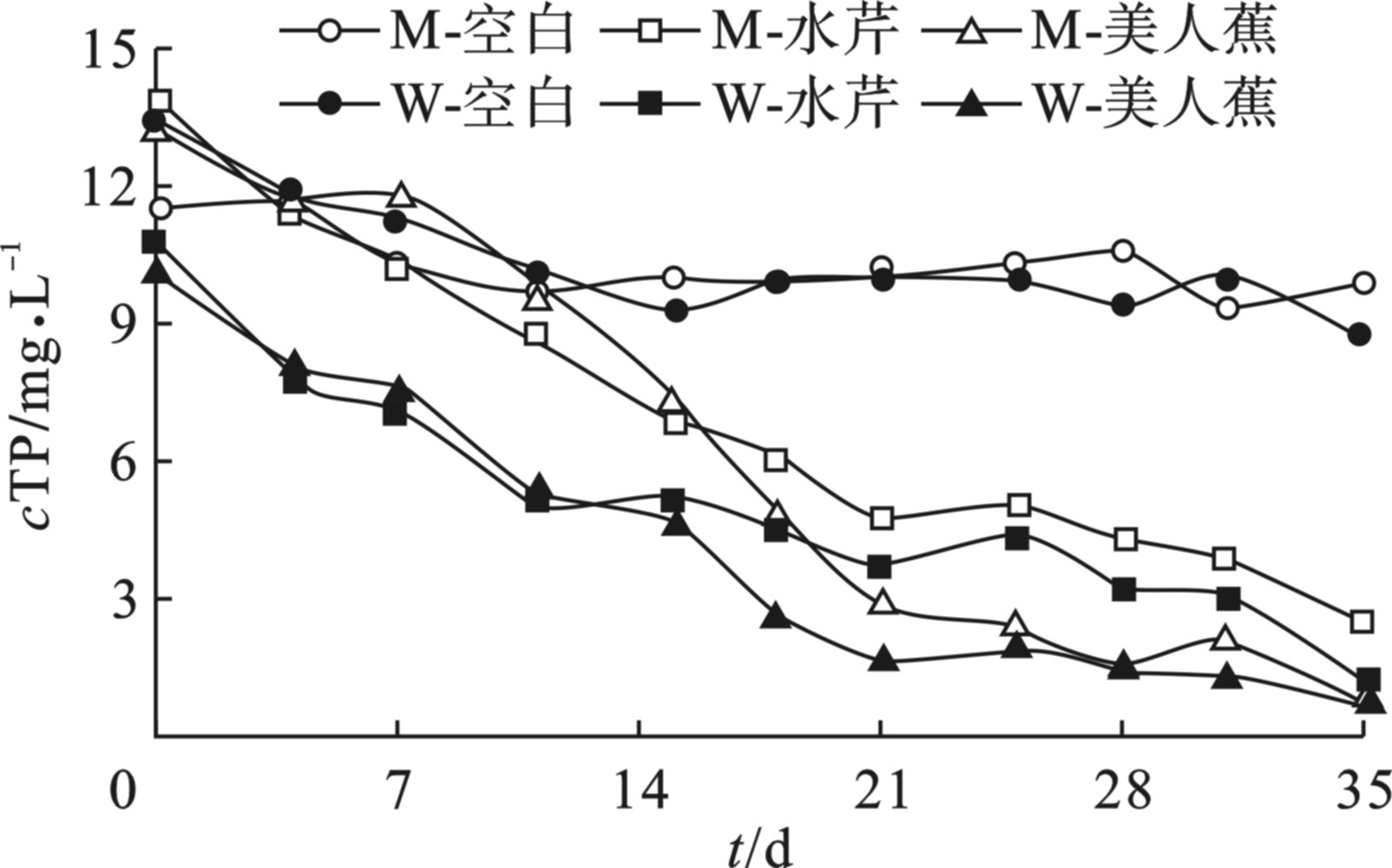
不同处理组中TP的去除效果,见图3。
TP浓度在不同处理组出现不同变化形式:种植美人蕉和水芹的实验中TP浓度下降明显,且美人蕉较水芹去除更多,空白对照中TP浓度几乎不变。TP初始浓度在1.02~1.39 mg/L范围内,最终美人蕉处理模拟污水和实际污水中浓度分别为0.07和0.08 mg/L。由此可见,种植水生植物对TP的去除有较大影响。
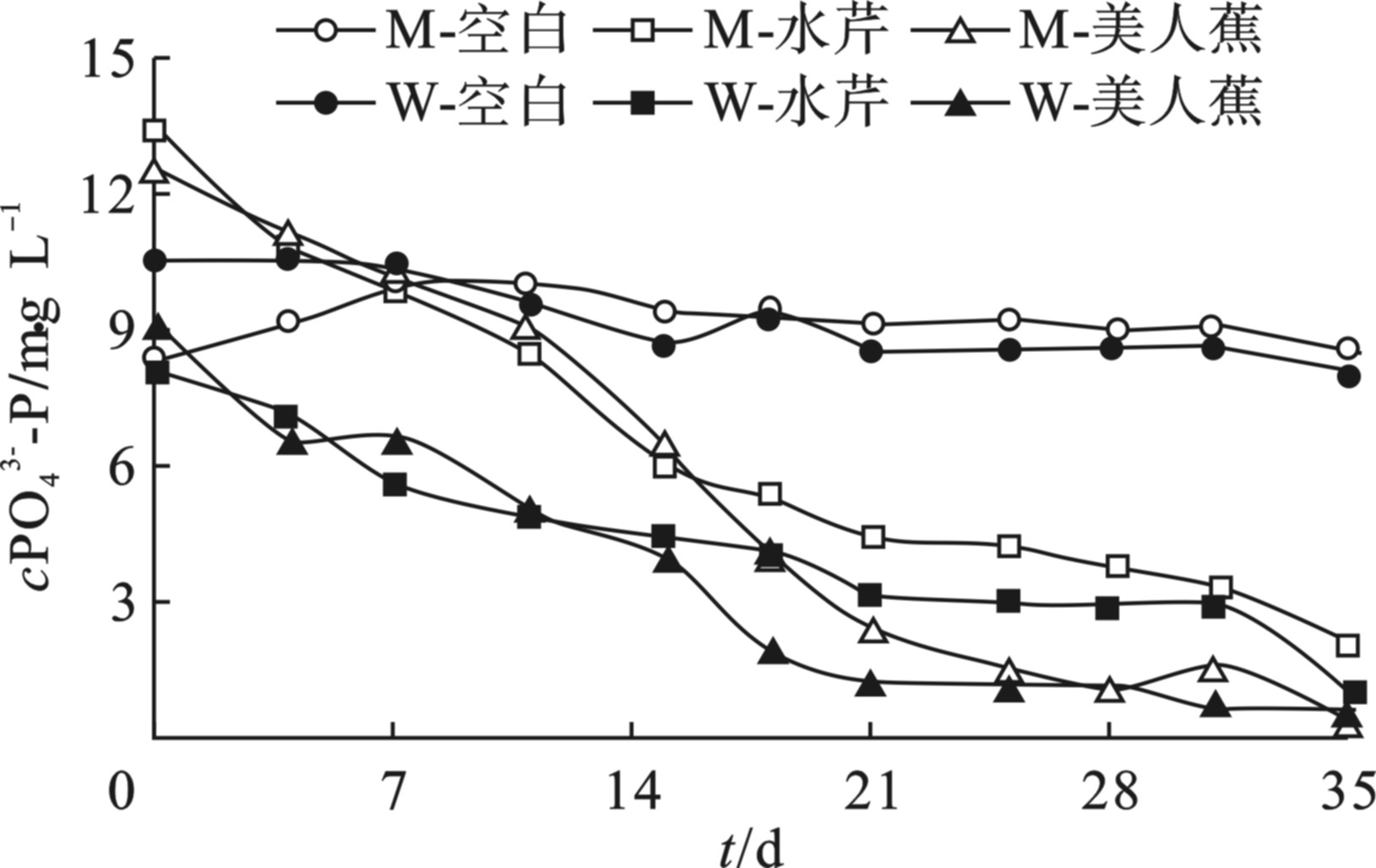
PO43--P浓度随时间变化的情况,见图4。
图4 中PO43--P与图3中TP相似的浓度变化曲线,说明TP以水溶态磷酸根形式存在并被去除,植物根系吸收PO43--P并通过导管运往地上部,参与体内代谢活动。另外,可能也存在PO43--P沉淀于水底而从水中去除的效果,与模拟污水相比,在污水空白组浓度也有所减少,减少了0.25 mg/L。实际污水取自污水处理厂过格栅进入沉砂池的污水,含有部分颗粒物质,在颗粒物下沉过程中会吸附、络合磷酸根,另外,污水中携带的铁和铝等金属离子会与水溶态磷酸根结合形成难溶磷酸盐化合物同颗粒物质一起下沉而去除部分PO43--P[21]。总的来说,TP的去除主要是通过植物吸收和沉淀作用,这与葛铜岗等[22]的串联式菖蒲浮床实验研究结果相似,该研究认为植物吸收对水体氮磷去除的贡献度在串联浮床系统中呈空间分布规律。
2.4 氮磷去除率及植物贡献率分析
植物处理后TN、TP的去除率和植物氮磷去除贡献率,见表2。
表 2 氮磷去除率及植物贡献率植物 氮 磷 去除率/% 去除量/mg 植物全氮量/mg 植物贡献率/% 去除率/% 去除量/mg 植物全磷量/mg 植物贡献率/% M-水芹 58.77 354.38 103.37 29.17 82.95 51.70 34.392 66.52 M-美人蕉 90.76 475.80 361.74 76.03 95.38 57.09 44.070 77.19 W-水芹 65.18 397.46 105.71 26.60 89.17 43.74 33.600 76.82 W-美人蕉 88.14 511.65 482.67 94.34 92.59 42.50 41.370 97.34 模拟污水空白中TN、TP减少率分别为20.06%和19.52%,实际污水空白组分别为14.73%和38.68%,证明美人蕉和水芹的种植都明显提高了污水中TN、TP的去除,并且不论是去除率还是植物贡献率的数值都表明美人蕉显然比水芹更适合浮床种植,TN去除率分别增加了31.99%和22.56%,TP去处理分别增加了12.43%和3.42%。同时,表2中显示水芹的TN去除贡献率显著低于美人蕉,仅26.60%~29.17%,可能是实验中反硝化脱氮效率低,水芹本身吸收积累的氮量少而导致TN去除率低。结合表1中植物生物量变化,植物生物量越大吸收的氮磷越多,植物脱氮除磷贡献率相应提高。如,实际污水种植的美人蕉生物量增长最大,其植物贡献率均超过90%,为所有实验中最大值。
美人蕉吸收贡献率占氮磷去除率均超过75%,是浮床实验的脱氮除磷主要途径;水芹吸收是磷去除的主要途径,氮去除率较低,对磷的贡献率分别为66.52%和76.82%,氮的贡献率分别为29.17%和26.60%。总的来说,实验中种植的美人蕉和水芹的氮磷去除效果,除了水芹对氮的处理,植物吸收均占主要作用,反硝化脱氮和微生物吸磷作用效果较差,而且须根系的美人蕉吸收作用更加明显。
2.5 讨论
根据叶创兴等[23]的《植物学》可知,水生植物的根系一般由主根、侧根和不定根等组成。主根是在种子萌发后首先生长出的向下垂直的根,随着主根长到一定长度后会在主根上产生分枝状的侧根,而不定根则是在茎的基部发出的根。单子叶植物对应的须根系植株,主根在植株幼苗期吸收水分并起支撑作用,但在不定根形成后就停止生长,进而形成以主根为端点、周围辐射以须状侧根和不定根的庞大类似球状的根系结构。须根系不定根的数量巨大,如,一株成熟的黑麦草的根有1 500万条,总长度能达到640 km,表面积相当于一个排球场面积,具有强大的吸附能力。双子叶植物的根是直根系,也称主根系,主根和侧根在粗度和长度方面差异很大。直根系主次分明,表现出发达的主根,在主根周围分布着匍匐状的侧根和不定根,表面积较须根系小。从根系特征分析,美人蕉属于须根系,水芹属于直根系。
从植物营养来看,氮是植物生长必需的常量营养元素,在植物细胞结构、新陈代谢和光合作用等生理活动中发挥重要作用,通过植物根系从周围介质中摄取而来[24]。然而,植物根系只能吸收铵根、硝酸根等无机态氮和部分小分子氨基酸,其他有机氮必须经过分解降解才能被植物吸收。根系不断从水中吸收氮素,植物生物量不断增加,水中TN浓度则逐渐较少。美人蕉的须根系根须在水中分布体积更大,表面形成的生物膜相互之间影响较小,能够更加有效地降解污染物;相对来说,水芹的根是直根系,根与根之间孔隙较小,容易形成厌氧空间,污染物降解可能受到影响。和氮素一样,磷素也是植物的必需常量元素,在植物生长发育、新陈代谢等生理活动中发挥着不可替代的重要作用,同时还参与植物细胞和组织、器官结构中的组成。植物根系对磷的吸收是主动吸收,可逆浓度吸收,需要消耗能量,其吸收速率受磷在介质中浓度高低影响,浓度越低吸收速率越低[25]。另外,须根系的美人蕉根系宽幅较直根系的水芹的根系宽幅大,细而长的根毛比表面积大能够吸收更大范围营养物,生长速率更快,生物量大,因此TP去除效果更加明显。
3. 结论
根系类型分别为须根系和直根系的美人蕉和水芹在污水中均能正常生长,在复合生态处理中具有强化脱氮除磷的能力,且美人蕉优于水芹。单子叶植物由于其须根系根部结构,根系表面积大于双子叶植物的直根系,且单子叶植物根系细且长,形成错综复杂的根系网络,能够吸收拦截较多营养元素,同时为微生物创造更大的栖息场所,较双子叶植物更有利于污染物的去除。所以,在污水复合生态治理工程中可以优先考虑单子叶植物种植。由于条件受限,本研究仅从水中污染物去除量方面分析认为单子叶植物的须根系较双子叶植物的直根系更适合污水复合生态治理,对植物根系结构和微生物生长状态如生物量和生物种类等缺少微观分析,后续将进一步从微观角度论证这一观点,为生态修复提供充分的理论支撑。
-
表 1 CAMQ、NAQPMS模式AQI预报效果评估对比
预报时次 范围准确率/% 级别准确率/% 首要污染物准确率/% CAMQ NAQPMS CAMQ NAQPMS CAMQ NAQPMS 24 h 43.7 27.8 74.2 66.2 60.3 58.9 48 h 31.8 21.9 74.2 61.6 59.6 60.9 72 h 34.4 20.5 67.5 55.6 60.3 57.0 表 2 2019年采暖期CAMQ、NAQPMS模式PM2.5浓度预报统计分析
统计指标 CAMQ NAQPMS 24 h 48 h 72 h 24 h 48 h 72 h MB 1.25 8.6 11.38 26.52 32.75 35.19 NMB/% 2.1 14.1 18.4 43.9 54.3 58.3 NME/% 37.7 45.1 48.7 54.4 62.6 66.6 r2 0.469 0.422 0.466 0.478 0.425 0.451 RMSE 30.92 36.83 38.33 42.11 49.94 50.98 MFB/% 3.7 13.5 15.9 42 48.3 50.9 MFE/% 37.2 44.2 48 47.5 52.7 54.9 注:平均偏差(MB)、标准化平均偏差(NMB)、标准化平均误差(NME)、和相关系数(r)、均方根误差(RMSE)、平均分数偏差(MFB)、平均分数误差(MFE)。 -
[1] 李令军, 王英, 李金香, 等. 2000~2010北京大气重污染研究[J]. 中国环境科学, 2012(1): 23-30. [2] 桂海林, 江琪, 康志明, 等. 2016年冬季北京地区一次重污染天气过程边界层特征[J]. 中国环境科学, 2019, 39(7): 53-61. [3] 李瑞, 李清, 徐健, 等. 秋冬季区域性大气污染过程对长三角北部典型城市的影响[J]. 环境科学, 2020, 41(4): 11-25. [4] 国务院. 大气污染防治行动计划(国发[2013]37号)[R]. 北京: 国务院, 2013. [5] 张朝能, 胡冰. 空气质量预报方法综述[J]. 云南环境科学, 2003, 22(2): 55 − 57. [6] 朱玉强. 几种空气质量预报方法的预报效果对比分析[J]. 气象, 2004(10): 30 − 33. doi: 10.3969/j.issn.1000-0526.2004.10.007 [7] 王扬锋, 马雁军, 权维俊, 等. 东北区域空气质量数值预报模式应用研究进展[J]. 气象与环境学报, 2020, 36(6): 130 − 136. doi: 10.3969/j.issn.1673-503X.2020.06.016 [8] 姜有山, 陈飞, 班欣, 等. 连云港市城市空气质量预报方法研究[J]. 气象科学, 2007(2): 220 − 225. doi: 10.3969/j.issn.1009-0827.2007.02.015 [9] 王庆梅, 张雪, 梅韩光. 兰州市大气污染特征与污染预报技术研究[J]. 中国环境监测, 2008(3): 56 − 62. doi: 10.3969/j.issn.1002-6002.2008.03.015 [10] 徐大海, 朱蓉. 大气平流扩散的箱格预报模型与污染潜势指数预报[J]. 应用气象学报, 2000, 11(1): 1 − 12. doi: 10.3969/j.issn.1001-7313.2000.01.001 [11] 李沫. 乌鲁木齐市空气质量多模式预报预警体系建设与应用[J]. 新疆环境保护, 2020, 42(2): 24 − 27. doi: 10.3969/j.issn.1008-2301.2020.02.005 [12] 江峰琴, 杨雪, 王晨波, 等. 江苏省区域空气质量多模式预报预警系统研究与设计[J]. 环境监控与预警, 2015, 7(2): 4-7. [13] 马琳, 魏巍, 张稳定. 2016年秋季新乡市空气质量模式预报效果评估[J]. 中国环境监测, 2017, 33(5): 89-94. [14] 环境保护部, 国家质量监督检验检疫局. 环境空气质量标准: GB3095—2012[S]. 北京: 中国环境科学出版社, 2012. [15] 环境保护部. 环境空气质量指数(AQI)技术规定(试行): HJ633—2012[S]. 北京: 中国环境科学出版社, 2012. [16] 环境保护部. 环境空气质量技术评价规范(试行) : HJ 663—2013[S]. 北京: 中国环境科学出版社, 2013. [17] 黄晓波, 殷晓鸿, 黄志炯, 等. 不同模式对珠三角地区细颗粒物污染模拟效果对比评估[J]. 环境科学学报, 2016, 36(10): 4 − 13. [18] 季冕, 尚晶晶, 张稳定. NAQPMS模型预报合肥、蚌埠和芜湖空气质量的效果评估[J]. 中国环境管理干部学院学报, 2018, 28(5): 62 − 66. [19] BOYLAN J W, RUSSELL A G. PM and light extinction model performance metrics, goals, and criteria for three-dimensional air quality models[J]. Atmospheric Environment, 2006, 40(26): 4946-4959. [20] 李建军. 环境空气质量预报成效评估方法技术指南[M]. 北京: 中国环境出版集团, 2018. -





 DownLoad:
DownLoad: