-
目前电子废弃物被公认为是世界上数量增长最快的生活垃圾。根据2020年发布的《The Global E-waste Monitor 202:Quantities, flows and the circular economy potential》显示[1],2019年全球产生了5360万吨电子废弃物,与2014年相比增长了21%;据预测到2030年全球电子废弃物产量将达到7400万吨。中国是世界上电子废弃物产量增长最快的国家,目前电子废弃物产量已超过美国跃居世界首位,据预测到2030年中国将产生2840万吨电子废弃物[2]。相较于庞大的产量,我国电子废弃物简易落后的拆解处理技术及装备,不合理、粗放式回收处理给环境和人类健康带来了严重的负面影响[3]。其中电子废弃物拆解区重金属污染问题早就受到研究者的关注。大量研究证实中国尤其是台州、贵屿和清远等传统电子废弃物拆解区环境中重金属污染严重,对生态环境和人体健康构成了潜在的巨大威胁[4-6]。
灰尘是一种重要的环境媒介,可以携带环境地表污染物的含量水平、分布、形态等信息。尤其是在电子产品使用过程和后续拆解、破碎过程,污染物不可避免的随着细小的碎屑释放出来,很容易与灰尘结合在一起,因此灰尘被认为是生态系统及人类健康风险的主要来源[7]。
本研究以上海市某正规电子废弃物手工拆解车间为主要研究对象,同时选取某高校研究生办公室和教室进行对照研究,采集室内灰尘样品。采样期间,电子废弃物手工拆解车间主要拆解回收废旧阴极射线管(CRT)电视机,拆解工人利用简单的工具对废旧CRT电视机进行手工拆解,分离出电视机外壳、CRT、电路板、电线以及扬声器等部件,日均拆解量为2000台左右。高校研究生办公室为电脑等电子产品密集使用场所,电脑的保有量为0.31台·m−2。高校教室中的电子产品较少,一般仅为教学多媒体。采集灰尘样品后,用ICP—OES法分析灰尘中Pb、Cu、Zn、As、Cd、Cr和Ni等7种重金属的含量;采用地累积指数法评价室内灰尘中重金属的污染程度;采用US EPA推荐的健康风险评模型,结合中国人群的暴露参数对人体室内灰尘暴露重金属的潜在健康风险进行评价。
-
2020年6—7月在上海市某正规电子废弃物手工拆解车间内采集废旧CRT电视机拆解工位处(CJGW)和拆解车间地面(CJDM)灰尘样品,在拆解车间外采集外部空地(CJWB)和公司周边道路(DL)灰尘样品,分别距拆解车间15 m和50 m左右,同时采集废旧CRT电视机外壳内灰尘样品;在对照点某高校研究生办公室(BGS)和教室(JS)地面采集灰尘样品。尽量对室内地面全面采集,以便反应实际情况。具体采样信息如表1所示。灰尘使用柔软的带柄毛刷采集,装入自封袋保存备用。同一类型采样点灰尘混合均匀后随机分为3份待测。
-
灰尘样品的消解参考本实验室先前研究[8]。灰尘样品过200目尼龙筛后,准确称取(0.2000±0.0002 )g置于聚四氟乙烯消解罐中,加入5 mL硝酸、3 mL氢氟酸和1 mL过氧化氢,微波辅助消解完成后,加入2 mL高氯酸赶酸,稀释定容至50 mL容量瓶中,过滤后待测。采用电感耦合等离子体发射光谱(ICP—OES)法测量灰尘中7种重金属(Pb、Cu、Zn、As、Cd、Cr、Ni)的含量,为保证实验准确性,每批样品均进行空白实验对照。结果表明空白样品中元素本底值低于仪器检出限,对样品检测结果无影响。各元素回收率范围在99%—118%之间,测试结果相对标准偏差均小于10%,符合重金属分析质量控制的要求。
-
地累积指数法(Geoaccumulation Index,Igeo)是由德国科学家Muller提出一种评价沉积物重金属污染程度的定量指标[9],现在也广泛应用于灰尘[10]和土壤[11]中重金属污染评价。本研究采用该方法对某正规电子废弃物手工拆解车间、某高校研究生办公室和教室灰尘中重金属含量进行污染评价。Igeo的计算公式为:
式中,ci表示灰尘中重金属i浓度,mg·kg−1;Bi表示重金属i的环境背景值,mg·kg−1,采用2016年上海市土壤重金属背景值[12],Pb、Cu、Zn、As、Cd、Cr 和 Ni的取值分别为26.3、31.6、106、7.66、0.20、84.2、44.3 mg·kg−1。评价标准为[13]:Igeo≤0表示无污染(unpolluted);0<Igeo≤1表示轻度中度污染(unpolluted to moderately polluted);1<Igeo≤2表示中度污染(moderately polluted);2<Igeo≤3表示中度—重度污染(moderately to strongly polluted);3<Igeo≤4表示重度污染(strongly polluted);4<Igeo≤5表示重度—极度污染(strongly to extremely polluted);5<Igeo≤10表示极度污染(extremely polluted)。
-
本文所关注的Pb、Cu、Zn、As、Cd、Cr和Ni对人体都具有慢性非致癌风险,同时As、Cd、Cr和Ni又具有致癌风险[14]。鉴于灰尘中重金属进入人体的途径主要包括呼吸吸入、经口摄入和皮肤接触等3种方式,采用美国环保署(US EPA)建立的人体暴露评估模型[15]和已有研究为基础,主要参考《中国人群暴露参数手册》[16]及已有研究[17-20]提供的暴露评估参数计算拆解车间、研究生办公室和教室人群经灰尘暴露重金属的暴露量,具体计算公式如下:
呼吸吸入途径:
经口摄入途径:
皮肤接触途径:
式中,ADDinhale、ADDingest和ADDdermal分别为呼吸吸入、经口摄入和皮肤接触的日均暴露量,mg·kg−1·d−1;Ci为灰尘中重金属i的浓度,mg·kg−1;CF为换算系数,取1×10−6 kg·mg−1。其他参数含义及取值见表2 。
-
非致癌风险的评估采用非致癌危害指数法;致癌风险的评估采用致癌风险指数法。根据以下公式计算非致癌风险商数(HQ),非致癌危险指数(HI)和致癌风险指数(CR):
式中,ADD非致癌为不同暴露途径下重金属日均暴露量,mg·kg−1·d−1;ADD致癌为不同暴露途径下重金属终生平均暴露量,mg·kg−1·d−1;RfD为参考剂量,mg·kg−1·d−1;SF为致癌斜率因子,(kg·d) ·mg−1。参考剂量和重金属致癌斜率因子见表3。评价标准[21]:HI<1,表示暴露人群非致癌健康风险低,HI>1,表示暴露人群存在潜在非致癌健风险。致癌风险评价标准:致癌风险可接受水平范围为10−6至10−4[17-19]。
-
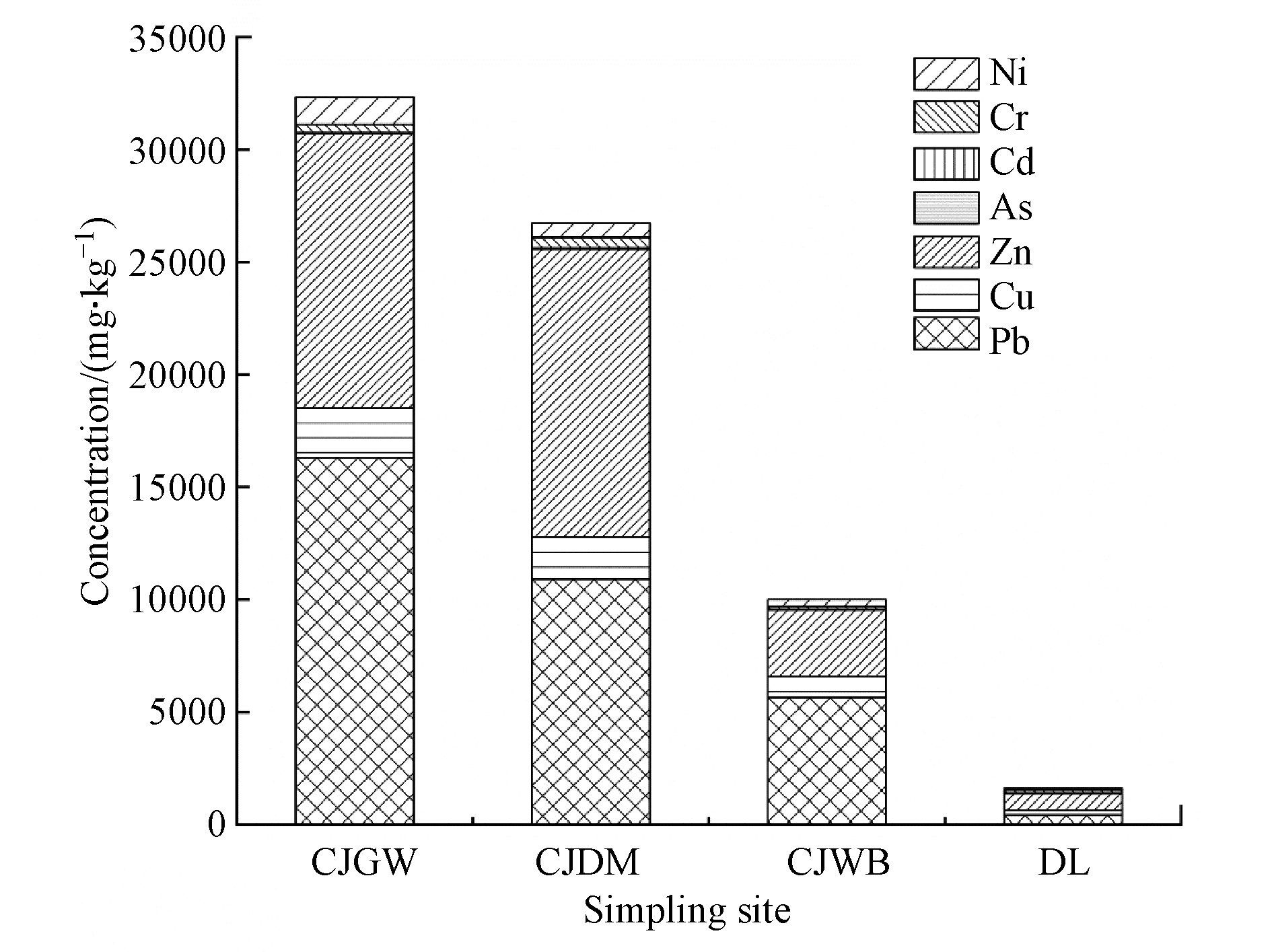
电子废弃物手工拆解车间室内外灰尘中重金属平均浓度见图1。拆解工位灰尘中Pb、Cu、Zn、As、Cd、Cr和Ni的浓度分别为16313、2204、12200、15.5、14.3、381、1199 mg·kg−1;拆解车间地面灰尘中Pb、Cu、Zn、As、Cd、Cr和Ni的浓度分别10910、1863、12806、34.7、7.01、475、631 mg·kg−1;车间外部空地灰尘中Pb、Cu、Zn、As、Cd、Cr和Ni的浓度分别为5652、920、2974、9.31、0.30、132、310 mg·kg−1;公司周边道路灰尘中Pb、Cu、Zn、As、Cd、Cr和Ni的浓度分别为409、226、749、8.54、1.03、137、80.2 mg·kg−1。可见,距拆解工位距离越远,灰尘中重金属含量越低。Leung等[22]发现贵屿家庭作坊式废旧线路板拆解车间地面灰尘中重金属浓度显著高于相邻道路(Pb:110000 mg·kg−1vs 22600 mg·kg−1;Cu:8360 mg·kg−1vs 6170 mg·kg−1;Zn:4420 mg·kg−1vs 2370 mg·kg−1;Ni:1500 mg·kg−1vs 304 mg·kg−1),其中道路灰尘中Pb和Cu的浓度分别是8 km外非电子废弃物拆解对照点的330倍和106倍,是30 km外的非电子废弃物拆解对照点的371倍和155倍。Wu等[23]也曾报道在浙江温岭随着距电子废弃物拆解工业园区距离的增加,室内外灰尘中Pb、Cr和Cd等重金属浓度逐渐降低。此外,本研究还发现,拆解工位灰尘中除As以外的其他6种重金属浓度,均显著高于电视机外壳内部(Pb:16313 mg·kg−1 vs 995 mg·kg−1;Cu:2204 mg·kg−1 vs 690 mg·kg−1;Zn:12200 mg·kg−1 vs 3553 mg·kg−1;Cd:14.3 mg·kg−1 vs 7.59 mg·kg−1;Cr:381 mg·kg−1 vs 189 mg·kg−1;Ni:1199 mg·kg−1 vs 243 mg·kg−1)。上述研究结果均表明重金属极易在电子废弃物拆解过程中释放到周围环境中,并且重金属从电子废弃物拆解点等点源的扩散是周边环境中重金属污染的主要来源。
在本研究中以拆解工位(CJGW)和车间地面(CJDM)灰尘中重金属的平均浓度作为该手工拆解车间(CJCJ)灰尘中的重金属浓度。由表4可得,电子废弃物手工拆解车间内灰尘中Pb、Cu、Zn、As、Cd、Cr和Ni的平均浓度分别为13611、2034、12503、25.1、10.7、428、915 mg·kg−1,分别是高校研究生办公室的76、6、10、2、3、6、2倍;分别是教室的268、40、33、6、27、19、49倍。本研究中电子废弃物手工拆解车间内灰尘中重金属的浓度与先前的研究结果水平基本相当。Fang等[17]调研了上海某废旧电视机手工拆解车间室内灰尘中重金属浓度,发现Pb、Cu、Cd、Cr和Ni的浓度分别为17830、2160、59.0、152、318 mg·kg−1。Deng等[24]调研了中国东部某规模化的废旧电视机手工拆解车间地面灰尘中重金属浓度,发现Pb、Cu、Cd、Cr、Ni的浓度为22900、856、31.1、208、667 mg·kg−1。本研究和先前的研究结果均证实[17,24],与Cu、Zn、As、Cd、Cr和Ni相比,Pb更容易通过电子废弃物手工拆解过程释放到环境中,是电子废弃物手工拆解车间中的首要污染物。这可能是因为老式彩色CRT电视机中含有大量的Pb,每台含量大约在2—3 kg[25]。但这些正规电子废弃物拆解车间室内灰尘中Pb的浓度均远远低于先前的粗放式拆解车间,如贵屿[22]家庭作坊式拆解车间Pb含量高达110000 mg·kg−1。上述研究结果表明在中国正规电子废弃物拆解取代非正规电子废弃物拆解确实能降低室内灰尘的重金属污染,但是即使是正规电子废弃物拆解车间室内灰尘的重金属含量依然相对较高,特别是Pb。鉴于Pb的神经毒性是全世界受关注的主要公共卫生问题[26],电子废弃物拆解技术及装备的升级势在必行。此外,贵阳办公室[27]室内灰尘中Pb、Zn和Cd的浓度分别为223、1535、2.20 mg·kg−1;北京办公室[28]室内灰尘中Cu、Cd和Cr的浓度分别为200、3.70、59.0 mg·kg−1,均与本研究结果相似。珠江高校教室[29]室内灰尘中7种重金属含量均高于本研究一个数量级。
-
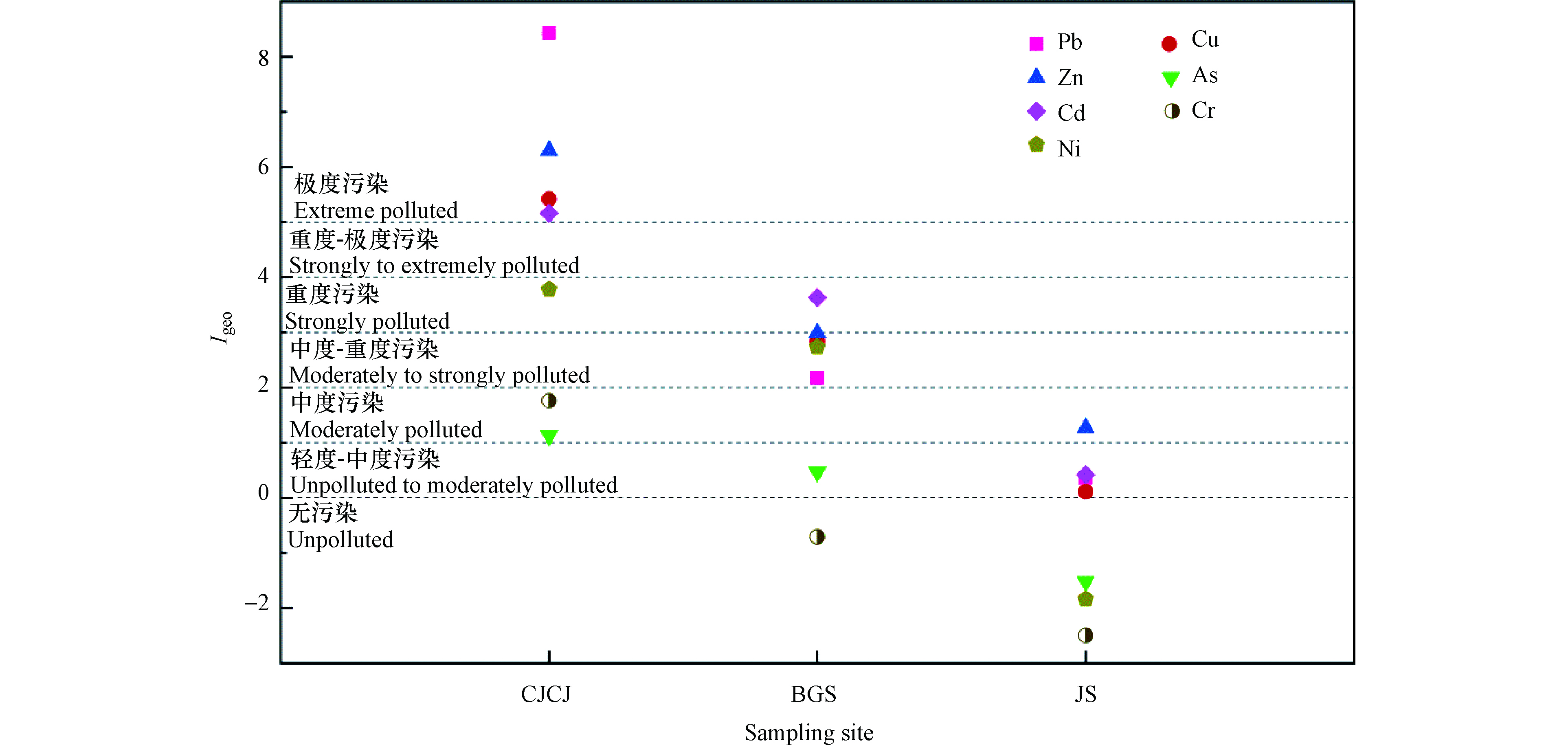
由图2可得,电子废弃物手工拆解车间室内灰尘中各重金属的地累积指数大小顺序为Pb(8.43)>Zn(6.30)>Cu(5.42)>Cd(5.16)>Ni(3.78)>Cr(1.76)>As(1.13),其中Pb、Zn、Cu和Cd处于极度污染水平,Ni处于重度污染水平,Cr和As处于中度污染水平;高校研究生办公室室内灰尘中各重金属的地累积指数大小顺序为Cd(3.62)>Zn(2.99)>Cu(2.84)>Ni(2.74)>Pb(2.18)> As(0.47)>Cr(-0.71),其中Cd处于重度污染水平,Zn、Cu、Ni和Pb处于中度—重度污染水平,As处于轻度—中度污染水平,Cr处于无污染水平;高校教室室内灰尘中各重金属的地累积指数大小顺序为Zn(1.27)>Cd(0.44)>Pb(0.36)>Cu(0.11)>Ni(-1.84)>As(-1.54)>Cr(-2.50),其中Zn处于中度污染水平,Cd、Pb和Cu处于轻度-中度污染水平,Ni、As和Cr处于无污染水平。可见,电子废弃物手工拆解车间室内灰尘重金属污染程度较为严重,远高于高校研究生办公室和教室,Pb、Zn、Cu、Cd和Ni均处于重度污染水平以上;另一方面,拆解车间室内重金属污染与电子废弃物拆解活动密切相关。
此外,先前的研究也证实即使是在拆解车间周边环境介质中重金属的污染程度也较为严重。例如,白建峰等[30]发现在新建电子废弃物拆解厂附近土壤中,As(2.47)和Cd(2.66)处于中度-重度污染水平;Tzoraki等[31]发现电子废弃物拆解厂附近土壤中,Pb和Zn处于重度-极度污染水平。此外,与本研究相比,南京市某高校学生办公室[32]灰尘中重金属污染程度更为严重,如Cd处于极度污染水平,Pb和Zn处于重度-极度污染水平,Cu处于重度污染水平,Ni处于中度污染水平。这可能是因为办公室内电子产品如电脑、打印机等数量较多,在使用过程中同样会释放重金属。
-
由表5可得,在电子废弃物手工拆解车间中3种暴露途径下Pb、Cu、Zn、As、Cd、Cr和Ni的总非致癌危险指数分别为2.26、3.03×10−2、2.51×10−2、6.26×10−2、7.68×10−3、1.25×10−1、2.57×10−2。非致癌危险指数小于1,则表明非致癌风险在安全范围内。在本研究中Pb的非致癌危险指数明显超过1,这表明Pb可能对拆解工人造成一定的非致癌风险。原因可能在于Pb在室内灰尘的浓度很高,并且在废旧CRT电视机拆解回收过程中可能更容易释放到灰尘中。此外,电子废弃物手工拆解车间内7种重金属所造成的总非致癌风险值为2.54,也大于1,超过了安全范围。总的来说,电子废弃物手工拆解车间内Pb是7种重金属中的主要污染物,可能会造成职业工人健康风险。Xu等[33]研究也发现Pb是电子废弃物拆解车间非致癌风险影响最大的重金属元素,在未来拆解过程中应首要加强对Pb的管控,降低Pb的扩散风险。
另一方面,在电子废弃物手工拆解车间内,就经口摄入途径而言,7种重金属HQingest的大小排序为Pb>Cr>As>Cu>Ni>Zn>Cd,总非致癌危险指数为2.46,其中Pb的贡献值最大(91%);就皮肤接触途径而言,7种重金属的总非致癌危险指数为7.36×10−2,小于1,其中Cr的贡献值占比55%,Pb占比20%,As占比19%;就呼吸吸入途径而言,7种重金属的总非致癌危险指数为2.55×10−3,远远小于1。总的来说,3种不同暴露途径的HQ排序为:经口摄入>皮肤接触>呼吸吸入,表明电子废弃物手工拆解车间室内灰尘中重金属暴露以经口摄入途径为主。
在对照点高校研究生办公室和教室,7种重金属的非致癌危险指数排序分别为As>Pb>Cr>Ni>Cu>Cd>Zn和As>Pb>Cr>Cd>Zn>Cu>Ni,且单个重金属的非致癌危险指数均小于1;此外,7种重金属所造成的的总非致癌风险值分别为5.12×10−2和1.35×10−2,也均小于1,表明人体健康风险可忽略。就经口摄入途径而言,对照点高校研究生办公室和教室7种重金属的非致癌危险指数分别为3.87×10−2和9.01×10−3;就皮肤接触途径而言,分别为1.24×10−2和4.44×10−3;就呼吸吸入途径而言,分别为1.55×10−4和4.44×10−5。可见,对照点3种不同暴露途径的HQ排序与电子废弃物手工拆解车间相一致,也与以往关于灰尘的研究结果[34]相一致。
从表6可见,在电子废弃物手工拆解车间、对照点高校研究生办公室和教室,4种致癌重金属所造成的的总致癌风险值分别为1.02×10−4、1.84×10−5和1.96×10−6。本研究中手工拆解车间内致癌风险与先前上海某废旧电视机手工拆解车间内PM2.5中Cr、Ni、Cd和Pb等4种致癌重金属所造成的致癌风险水平相当(1.46×10−4),但是超过了致癌风险可接受水平范围(10−6至10−4)。由此可见电子废弃物手工拆解活动可能对拆解工人存在一定致癌风险。但是Deng等[24]的研究却表明规模化废旧电视机手工拆解车间室内灰尘中Cd、Cr和Ni等3种致癌重金属的致癌风险值均未超过10−6。本研究中单个重金属的致癌风险最大的为Ni,其次为Cr;而在先前的研究中,单个重金属的致癌风险最大的均为Cr[17,24,35-36]。综合前文的结果Pb是非致癌风险中贡献值最大的重金属,电子废弃物拆解活动释放的重金属较易吸附到灰尘上,危害较大,因此拆解企业仍需加强对Pb、Ni和Cr排放的管理,降低职业工人的健康风险。此外,对照点高校研究生办公室和教室内致癌风险并未超过致癌风险可接受水平范围(10−6至10−4),表明对照点的致癌风险均相对较低,处于可接受水平。
-
(1)电子废弃物手工拆解车间室内灰尘中 Pb、Cu、Zn、As、Cd、Cr和Ni的含量均远远高于高校研究生办公室和教室,其中Pb为首要特征污染物;同时发现距拆解工位距离越远,灰尘中重金属含量越低,这也说明重金属从点源的扩散是周边环境中重金属污染的主要来源。
(2)地累积指数评价结果表明,电子废弃物手工拆解车间室内灰尘重金属污染程度远高于高校研究生办公室和教室,其中Pb、Zn、Cu和Cd处于极度污染水平,Ni处于重度污染水平,Cr和As处于中度污染水平,说明电子废弃物手工拆解车间室内灰尘重金属污染程度较为严重,且与电子废弃物拆解活动密切相关。
(3)健康风险评价结果表明,电子废弃物手工拆解车间室内灰尘重金属污染可能会造成一定的职业人群健康风险,其中Pb是造成非致癌风险的主要重金属,而Ni和Cr是造成致癌风险的主要重金属。这也说明在即使在正规电子废弃物回收处理过程中重金属污染的控制与削减技术仍需进一步加强。
电子废弃物拆解车间灰尘中重金属污染特征及职业人群健康风险评价
Pollution characteristics of heavy metals in the dust from e-waste dismantling workshop and health risk assessment of occupational population
-
摘要: 以上海市某正规电子废弃物手工拆解车间为研究对象,同时选取某高校研究生办公室和教室进行对照研究,采集室内灰尘样品,用电感耦合等离子体发射光谱(ICP—OES)法测定了灰尘中铅(Pb)、铜(Cu)、锌(Zn)、砷(As)、镉(Cd)、铬(Cr)和镍(Ni)的含量,采用地累积指数法(Igeo)评价了室内灰尘中重金属的污染程度,采用美国环保署(US EPA)推荐的健康风险评价模型,结合中国人群暴露参数,对人体室内灰尘暴露重金属的潜在健康风险进行评价。研究发现,电子废弃物手工拆解车间室内灰尘中Pb、Cu、Zn、As、Cd、Cr和Ni的平均浓度分别为13611、2034、12503、25.1、10.7、428、915 mg·kg−1,分别是高校研究生办公室的76、6、10、2、3、6、2倍;分别是教室的268、40、33、6、27、19、49倍,可见Pb是电子废弃物手工拆解车间室内灰尘的首要特征污染物;同时距拆解工位距离越远,灰尘中重金属含量越低,表明重金属从点源的扩散是周边环境中重金属污染的主要来源。地累积指数结果表明,电子废弃物手工拆解车间室内灰尘中重金属污染程度远远超过高校研究生办公室和教室,其中Pb(8.43)、Zn(6.30)、Cu(5.42)和Cd(5.16)处于极度污染水平,Ni(3.78)处于重度污染水平,Cr(1.76)和As(1.13)处于中度污染水平。健康风险评价结果表明,在电子废弃物手工拆解车间室内灰尘中Pb是造成非致癌风险的主要重金属,非致癌危险指数(HI)为2.26,大于1,表明Pb可能对拆解工人造成一定的非致癌风险;As、Cd、Cr和Ni的总致癌风险指数(CR)为1.02×10−4,超过了致癌风险可接受水平范围(10−6至10−4),表明电子废弃物拆解活动可能对拆解工人造成一定致癌风险,其中Ni和Cr是造成致癌风险的主要重金属。研究结果表明电子废弃物手工拆解车间室内灰尘中重金属的污染程度与拆解活动密切相关,且对拆解工人会造成一定程度的健康风险。Abstract: Taking a formal e-waste manual dismantling workshop in Shanghai as the research object and a postgraduate office and classrooms of a university as the control sites, indoor dust samples were collected. And the concentrations of lead (Pb), copper (Cu), zinc (Zn), arsenic (As), cadmium (Cd), chromium (Cr) and nickel (Ni) were detected by inductively coupled plasma emission spectrometer (ICP-OES). The pollution levels of heavy metals in the indoor dust were analyzed by the geo-accumulation index (Igeo) method. The potential health risk of human exposure to heavy metals from indoor dust was evaluated by the health risk assessment model recommended by the US EPA combined with the exposure parameters of the Chinese population. The results showed that the mean concentrations of Pb, Cu, Zn, As, Cd, Cr and Ni in the indoor dust of the e-waste manual dismantling workshop were 13611, 2034, 12503, 25.1, 10.7, 428, 915 mg·kg−1, which were 76, 6, 10, 2, 3, 6, 2 times higher than the postgraduate office, and 268, 40, 33, 6, 27, 19, 49 times higher than the classroom, respectively. Pb is the primary characteristic pollutant in the e-waste manual dismantling workshop. The concentrations of heavy metals showed a noticeable decreasing trend with the distance from the e-waste recycling site. It was obvious that the diffusion of heavy metals form the point pollution source made a dominant contribution to the heavy metal pollution in the surrounding areas. The results of the geoaccumulation index showed that in the indoor dust of the e-waste manual dismantling workshop, Pb (8.43), Zn (6.30), Cu (5.42) and Cd (5.16) were extremely polluted, Ni (3.78) was strongly polluted; Cr (1.76) and As (1.33) were moderately polluted. The results of the health risk assessment showed that in the indoor dust of e-waste manual dismantling workshop, Pb was the primary heavy metal causing non-carcinogenic risks. The non-carcinogenic hazard index (HI) of Pb was 2.26, greater than 1, indicating that Pb may pose a certain non-carcinogenic risk to the dismantling workers. The total carcinogenic risk (CR) of As, Cd, Cr and Ni was 1.02×10−4, higher than its threshold value (the range of threshold value was 10−6 to 10−4), indicating that e-waste dismantling activities may pose a certain carcinogenic risk to the dismantling workers, among which Ni and Cr were the main heavy metals causing carcinogenic risks. The results of this study suggested that in the indoor dust of the e-waste manual dismantling workshop, the pollution degree of heavy metals was closely related to the dismantling activities, and heavy metals might cause a certain degree of health risk to the dismantling workers.
-
Key words:
- e-waste dismantling /
- dust /
- heavy metals /
- pollution characteristics /
- health risk assessment
-
土壤是人类农业生产的物质基础,一旦遭受污染,会对粮食安全和人体健康造成危害。2014年发布的《全国土壤污染状况调查公报》[1]显示,我国土壤重金属污染问题不容乐观,污染土壤中约82.4%的土壤受到重金属及准金属污染,且土壤重金属污染具有隐蔽性、滞后性、治理难、周期长的特点[2]。重金属极易在土壤-植株体系内迁移和累积,会造成环境污染和生态破坏。因此,对土壤重金属的治理迫在眉睫。
目前,土壤重金属的处理方法包括物理法(土壤淋洗、蒸汽浸提、电动力学修复)、化学法(化学修复剂)和生物法(微生物催化降解、植物修复、动物修复)[3]。化学原位钝化技术因其成本低、见效快、处理效果显著而得到广泛的应用[4]。常用的钝化剂主要有石灰[5]、磷酸盐[6]、有机质[7-8]、金属氧化物[9-11]和黏土矿物[12]。其中,凹凸棒石是一种典型的含水富镁铝硅酸盐黏土矿物,具有独特的化学成分和物理结构,内表面积大、孔隙较多、离子交换能力强,在化工、环保和印染等领域得到了广泛的应用。谭科艳等[13]研究了凹凸棒石对铜锌镉重金属污染土壤的修复效果,结果表明,适量添加凹凸棒石黏土矿物可对Cu的平均修复率达到31.50%,对Zn元素的平均修复率达到26.15%,对Cd元素的平均修复率达到34.92%,能够有效减少蔬菜对Cu、Zn、Cd元素的吸收。马博[14]研究表明,凹凸棒石综合钝化能力更强,且在酸性较高的极端条件下效果优于膨润土和沸石,低配比凹凸棒石对衡阳尾矿中Cr、Zn、Cd、Pb、Cu的钝化效果显著。ZHANG等[15]发现,凹凸棒石的施加可显著降低Cu的生物可利用态质量分数,缓解重金属Cu对油菜植株的生理胁迫效应。
常用的凹凸棒石改性方法有无机改性、有机改性、生物质改性和微波改性[16]。LIANG等[17]通过制备巯基改性凹凸棒石钝化Cd污染土壤,可显著增强土壤颗粒对Cd的吸附,抑制农作物对重金属Cd的吸收。XU等[18]将纳米零价铁负载凹凸棒石施用进土壤中,可有效促进重金属Cd、Cr和Pb发生形态转变,并将其固定下来。甘肃省具有丰富的凹凸棒石矿藏,但常常因为品位较低未能得到大规模开发利用。为解决此问题,制备5种不同体积分数H2SO4、不同改性时间的酸改性凹凸棒石,探讨不同钝化材料的添加量对土壤重金属Cu和Zn的钝化效果,并结合环境风险指数和重金属修复效率评估酸改性凹凸棒石的最佳投加量,以期为农田重金属污染土壤的治理和甘肃省凹凸棒石的应用提供参考。
1. 材料与方法
1.1 实验原料
重金属复合污染土壤采自甘肃省白银市东大沟(36° 59′ 96′′ N,104° 22′ 76′′ E)。土壤的基本理化性质为pH 7.28、土壤电导率(EC)1457 µS·cm−1、重金属Cu质量分数为1029.11 mg·kg−1、重金属Ni质量分数为87.18 mg·kg−1、重金属Zn质量分数为707.51 mg·kg−1。其中,Cu和Zn均远超国家标准限值,分别为《土壤环境质量农用地土壤污染风险管控标准》(GB 15618-2018)[19]的5.15倍和2.83倍。
凹凸棒石质黏土复合矿物(简称为“凹凸棒石”)购自甘肃当地,原矿采自甘肃省临泽县板桥镇红色凹凸棒石矿,土状结构,粒度为2 mm左右,主要的矿物成分为凹凸棒石29.7%、石英21.8%、长石14.6%、白云石 6.3%、其他组分27.6%,是一种由凹凸棒石为主,石英和长石以及碳酸盐矿物等伴生的黏土质复合非金属矿物。其主要化学成分为:SiO2 48.38%、Al2O3 11.24%、Fe2O3 4.78%、MgO 7%、CaO 7.41%[20]。
1.2 实验方法
称取定量凹凸棒石,破碎、研磨,过200目筛(直径0.075 mm)。基于49种酸改性钝化材料的研究[21],制备5种优选酸改性凹凸棒石,具体配制条件见表1。将凹凸棒石粉末与不同体积分数的H2SO4溶液混合,固液比为1∶10(m∶v),500 r·min−1转速下搅拌一定时间后,烘干、研磨、过筛制得钝化材料。按2、4、8、16、24 g·kg−1的添加量,将酸改性凹凸棒石钝化材料加入到1.5 kg实际重金属复合污染土壤中,混合均匀,重量法添加去离子水,保持70%的田间持水量,钝化培育30 d后测定土壤的理化性质和重金属形态,每组处理设置不添加任何钝化材料的土壤样品作为对照,记为CK。
表 1 酸改性凹凸棒石的制备方法Table 1. The preparation method of acid modified attapulgite实验编号 H2SO4体积分数/% 反应时间/h A1 10.0 72 A2 12.5 48 A3 12.5 72 A4 12.5 96 A5 15.0 72 1.3 分析方法
采用X射线衍射仪(MiniFlex600,日本Rigaku公司)分析改性前后的凹凸棒石晶体物相组成,扫描速度为10°·min−1,角度为5°~80°,扫描过程采用Cu-Kα 辐照。采用扫描电子显微镜(GeminiSEM500,德国ZEISS公司)观察改性前后凹凸棒石的表面形貌,将样品过200目筛网,在15 kV电压下以相同倍率下放大观察分析。
采用pH计(pHS-3C,上海仪电科学仪器股份有限公司)测定土壤pH,固液比为1∶2.5(m∶v)。采用电导率仪(DDS-307A,上海仪电科学仪器股份有限公司)测定土壤EC,固液比为1∶5(m∶v)。采用BaCl2-H2SO4强迫交换法测定土壤阳离子交换量(CEC)。采用BCR连续提取法测定土壤重金属化学形态。土壤重金属总量经HCl-HNO3-HF-HClO4消解后,火焰原子吸收分光光度计(TAS-990,北京普析通用仪器有限责任公司)测定浓度。
本实验选用H2O和DTPA作为提取剂来评价土壤重金属的生物有效性。土壤重金属水溶态测定时,称取5 g土壤样品与50 mL蒸馏水均匀混合,25 ℃下充分振荡24 h,火焰原子吸收分光光度法测定上清液中重金属浓度。土壤重金属DTPA提取态测定时,称取2 g土壤样品与40 mL DTPA提取液均匀混合,25 ℃下振荡12 h,火焰原子分光光度法测定上清液中重金属浓度。
1.4 指数计算与数据处理方法
污染土壤的生态风险指数(Ecological risk index,ERI)指土壤中活性较高的生物有效态质量分数与重金属总量之比,用于表示土壤中重金属的生态环境风险,常用于底泥沉积物、土壤和污泥中重金属的风险评价,通常分为5个等级,即无风险(<1%)、低风险(1%~10%)、中风险(10%~30%)、高风险(30%~50%)、极高风险(>50%)。按式(1)计算[22-23]。
ERIm=CbsCs×100% (1) 式中:Cbs为土壤中有效态重金属的质量分数,mg·kg−1,Cs为土壤中重金属的质量分数,mg·kg−1。
此外,潜在风险指数(potential ecological risk index)可用于评价多种重金属复合污染的生态风险,可按式(2)、式(3)计算。
Eir=TirCidCib (2) RI=∑ni=1Eir (3) 式中:
Eir Cid Cib CCub CZnb Tir TCur TZnr 表 2 土壤中单一重金属(Er)的潜在生态风险指数Table 2. The potential ecological risk index of single heavy metal (Er) in SoilEr 风险程度 Er ≤ 40 低风险 40 ≤Er <80 中风险 80 ≤ Er < 160 较高风险 160 ≤ Er < 320 高风险 Er > 320 极高风险 表 3 土壤中复合重金属(RI)的潜在生态风险指数Table 3. The potential ecological risk index of total heavy metals (RI) in SoilRI 风险程度 RI ≤ 150 低风险 150 ≤ RI <300 中风险 300 ≤ RI <600 高风险 RI ≥ 600 极高风险 污染土壤中重金属的修复效率(Remediation ratio,RR)指BCR多级提取法中较稳定的重金属残渣态(S4)与土壤重金属4种形态总和的比值,可用于评估重金属的潜在活化风险,按式(4)计算[24]。
RR=S4S1+S2+S3+S4×100% (4) 式中: S1为重金属元素酸溶态质量分数,mg·kg−1;S2为重金属元素还原态质量分数,mg·kg−1;S3为重金属元素氧化态质量分数,mg·kg−1;S4为重金属元素残渣态质量分数,mg·kg−1。
2. 结果与讨论
2.1 土壤理化性质
土壤pH、电导率和阳离子交换量影响着重金属的化学形态,是评价重金属迁移转化和作物生长发育情况的重要指标[25]。施用不同酸改性凹凸棒石后的土壤pH见图1(a),与对照组相比,向土壤中施加5种酸改性凹凸棒石后,土壤pH均呈现显著降低的趋势。在同一投加量水平下,A3处理组pH显著低于其他处理组。这是因为,天然的凹凸棒石本身呈弱碱性,含有大量的羟基等官能团[26],而改性添加的H2SO4具有强酸性,能够和土壤及凹凸棒石中的碱性物质发生反应,从而降低土壤pH,调节土壤的酸碱度。本研究采用的实际污染土壤为北方地区常见的碱性土壤,酸改性凹凸石的施用有效改善了土壤的酸碱环境。不同酸改性凹凸棒石处理后的土壤EC见图1(b),在同一酸改性凹凸棒石处理组中,土壤EC随着添加量的增加而显著增加,且A5处理组EC值显著高于其他处理组。土壤CEC随着凹凸棒石添加量的增加而增加,但不同添加量间差异性不显著(图1(c))。除A4材料投加量为8 mg·kg−1时土壤CEC较高外,其他投加量水平下,A5处理组CEC也显著高于其他处理组。一方面,凹凸棒石的表面带有Na+、K+和Ca2+等阳离子,本身具有较高的阳离子交换容量,随着投加量的增加,土壤中带电的离子浓度升高,从而提高土壤电导率[27];另一方面,当改性时添加的H2SO4体积分数较大时,凹凸棒石表面会带有大量的H+,这些活泼的阳离子可能会和土壤中的Cu2+、Zn2+发生阳离子交换反应,提高土壤的EC和CEC [28]。
2.2 土壤重金属的生物有效态
土壤中重金属的水溶态可直观地反映重金属的生物可利用度,这部分形态的重金属质量分数很低,但是却可以直接被植物吸收利用,具有极强的迁移性和毒性,因此常常作为土壤重金属污染评价的重要指标[29]。不同改性凹凸棒石处理后的土壤生物有效态重金属质量分数见图2。从图2可以看出,添加酸改性凹凸棒石后,水溶态Cu和Zn的质量分数均较对照组显著降低。尽管随着投加量的增加,水溶态重金属质量分数出现了先降低后轻微升高的趋势,但差异并未达显著水平。实验结果表明,当投加量为16 g·kg−1时,酸改性凹凸棒石对Cu、Zn的钝化效果最好。其中,A5处理组中水溶态Cu的质量分数最低,较对照组降低了47.38%;A3处理组中水溶态Zn的质量分数最低,较对照组降低了64.44%。土壤中DTPA提取态重金属质量分数常常用来评估植物对重金属的吸收情况,DTPA络合剂能够与重金属离子结合,形成稳定的水溶性络合物,可直观地评价重金属的生物有效性[30]。添加酸改性凹凸棒石后,Cu和Zn的DTPA提取态质量分数均较对照组显著降低。当投加量为16 g·kg−1时,A5处理组中DTPA提取态Cu的质量分数最低,较对照组下降了24.25%,A3处理组中DTPA提取态Zn的质量分数最低,较CK下降了46.77%。DTPA提取态重金属的降低趋势与水溶态重金属基本保持一致。这与罗宁临等[31]的研究结果基本一致。造成以上结果的原因可能是:1)酸改性使得凹凸棒石表面和孔隙内的碳酸盐杂质得以去除,晶束团聚结构变得更加紧密,内表面积和缝隙增大,增强了其对重金属Cu、Zn的吸附能力[32];2)酸改性凹凸棒石的施用提高了土壤的阳离子交换容量,土壤中游离的Cu2+、Zn2+通过阳离子交换作用,与带有负电荷的凹凸棒石和土壤颗粒结合,显著降低了重金属的生物有效性[27,33];3)凹凸棒石表面带有大量的硅羟基等官能团,能与重金属发生络合反应,从而将其固定[14,34]。本研究结果说明,采用优质的钝化材料是降低土壤重金属毒性的关键,而控制合适的投加量对农田土壤的修复也至关重要。
2.3 土壤重金属形态分布
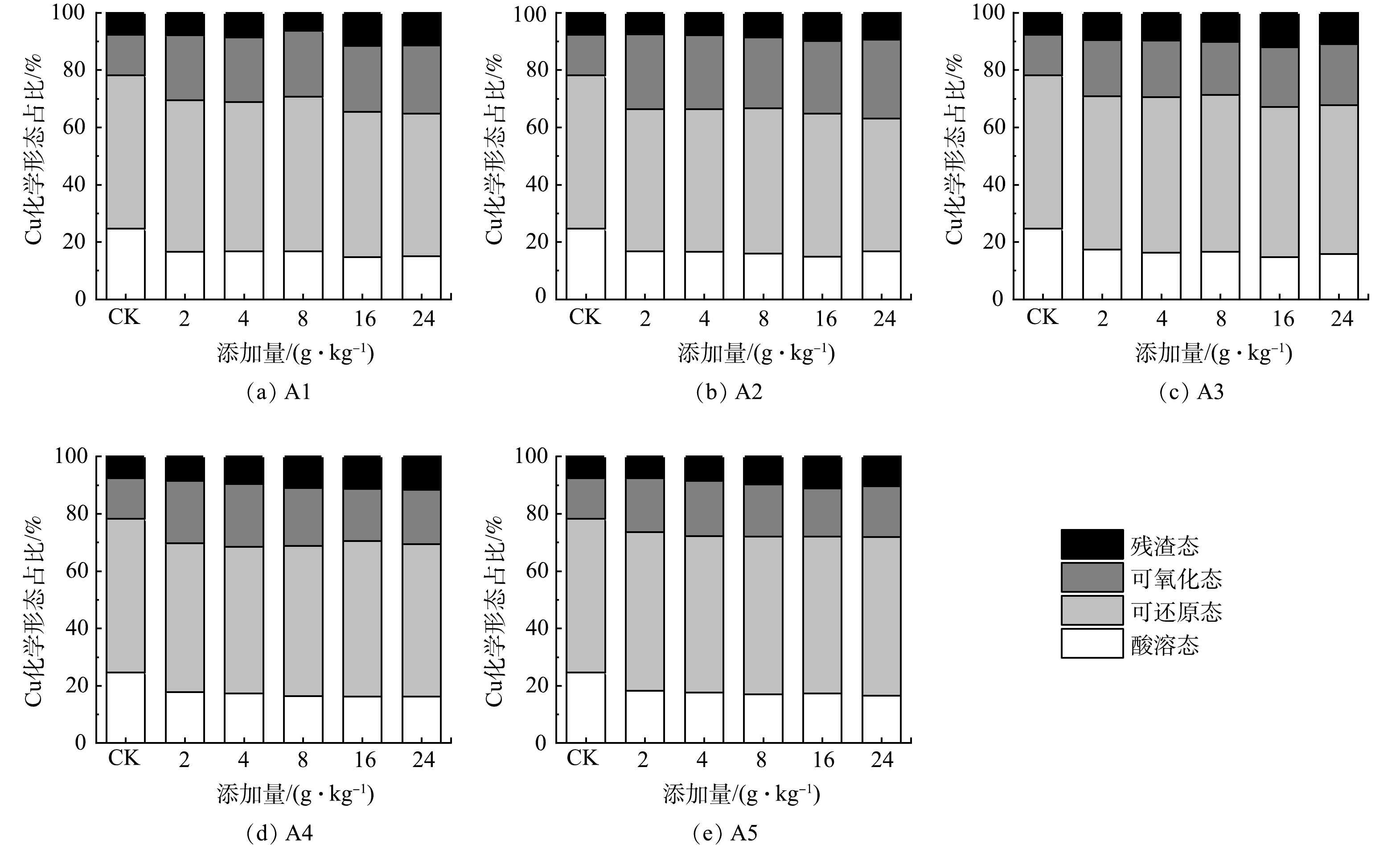
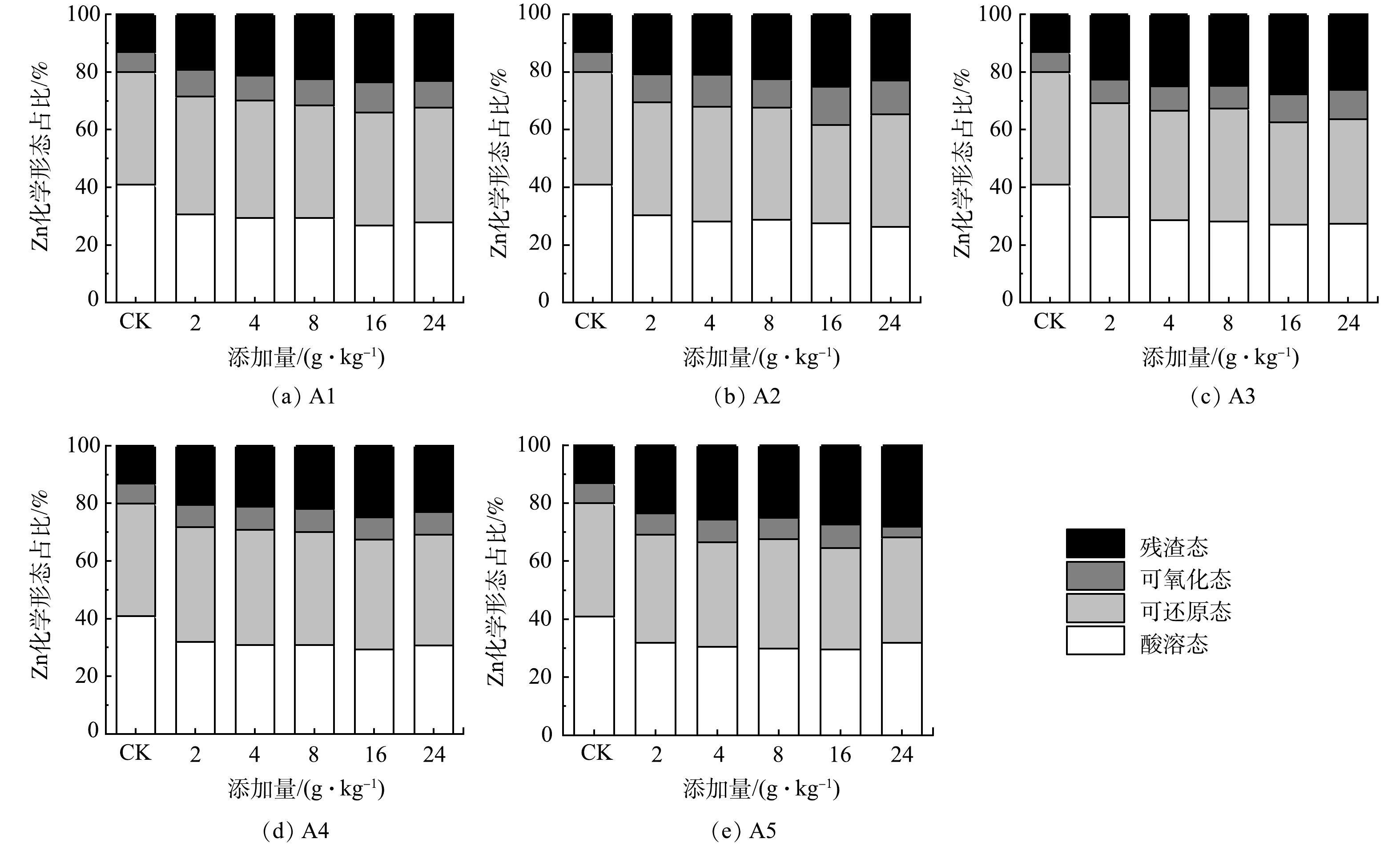
BCR多级提取法中,重金属各种形态的活性大小依次为酸溶态>可还原态>可氧化态>残渣态[35]。其中,酸溶态重金属的生物可利用度最高,可还原态和可氧化态重金属容易随着pH和氧化还原电位等环境条件的变化而变化,重新释放到环境介质中,残渣态重金属最稳定,不易在土壤中迁移转化,生态毒性最低[35-37]。酸改性凹凸棒石钝化后土壤中重金属形态分布见图3和图4。添加不同酸改性凹凸棒石后,酸溶态Cu和Zn的质量分数较对照组显著降低,而残渣态Cu和Zn的质量分数上升(图3,图4)。当投加量为16 g·kg−1时,A3处理组中酸溶态Cu和Zn的占比最低,残渣态Cu的比例较对照组上升了3.96%;残渣态Zn的比例较对照组上升了15.26%,这与武成辉等[38]和陶玲等[39]的研究结果一致。添加不同酸改性凹凸棒石可影响重金属在土壤中的形态,促进重金属从活性较高的酸溶态、可还原态向活性较低的可氧化态、残渣态转变,降低了Cu、Zn的生态毒性,实现了土壤的钝化修复。其原因可能是:1)凹凸棒石及其改性材料的添加可通过一系列吸附、离子交换、沉淀和络合作用降低酸溶态Cu、Zn质量分数[40];2)凹凸棒石经过酸处理后,起支撑作用的八面体和四面体溶解,导致凹凸棒石的孔道增大,比表面积增加,凹凸棒石的吸附性能提高[41];3)残渣态重金属 Cu、Zn一般存在于硅酸盐、原生和次生矿物等土壤的晶格中,当向污染土壤中施用酸改性凹凸棒石后,随着钝化时间的延长,低价的Cu2+、Zn2+可能会在凹凸棒石八面体或四面体结构中与Si4+发生晶格置换,能长期稳定在土壤中[42]。
2.4 酸改性凹凸棒石的表征分析
为验证上述作用机理,本实验对凹凸棒石改性前后的微观形貌和晶体结构进行表征,扫描电子显微镜图像如图5所示。供试凹凸棒石原矿(ATP)主要呈棒状晶束堆积结构,晶束较长,棒晶密实,孔道结构较少。经不同浓度H2SO4和不同活化时间处理后,凹凸棒石的棒晶发生解束,晶束变短,排列相对松散,可直接接触的点位增多,增强了凹凸棒石对重金属的吸附能力。这与陈雪芳[43]等的研究结果一致:酸改性能够溶解凹凸棒石中的八面体阳离子和四面体硅,使得八面体结构起主要的支撑作用,凹凸棒石孔道开放,孔径增大,比表面积增大,吸附性能提高。但是,当酸浓度较高时,会对层间的阳离子起较强的溶出作用,破坏晶体结构,进而降低凹凸棒石的吸附性能[44]。
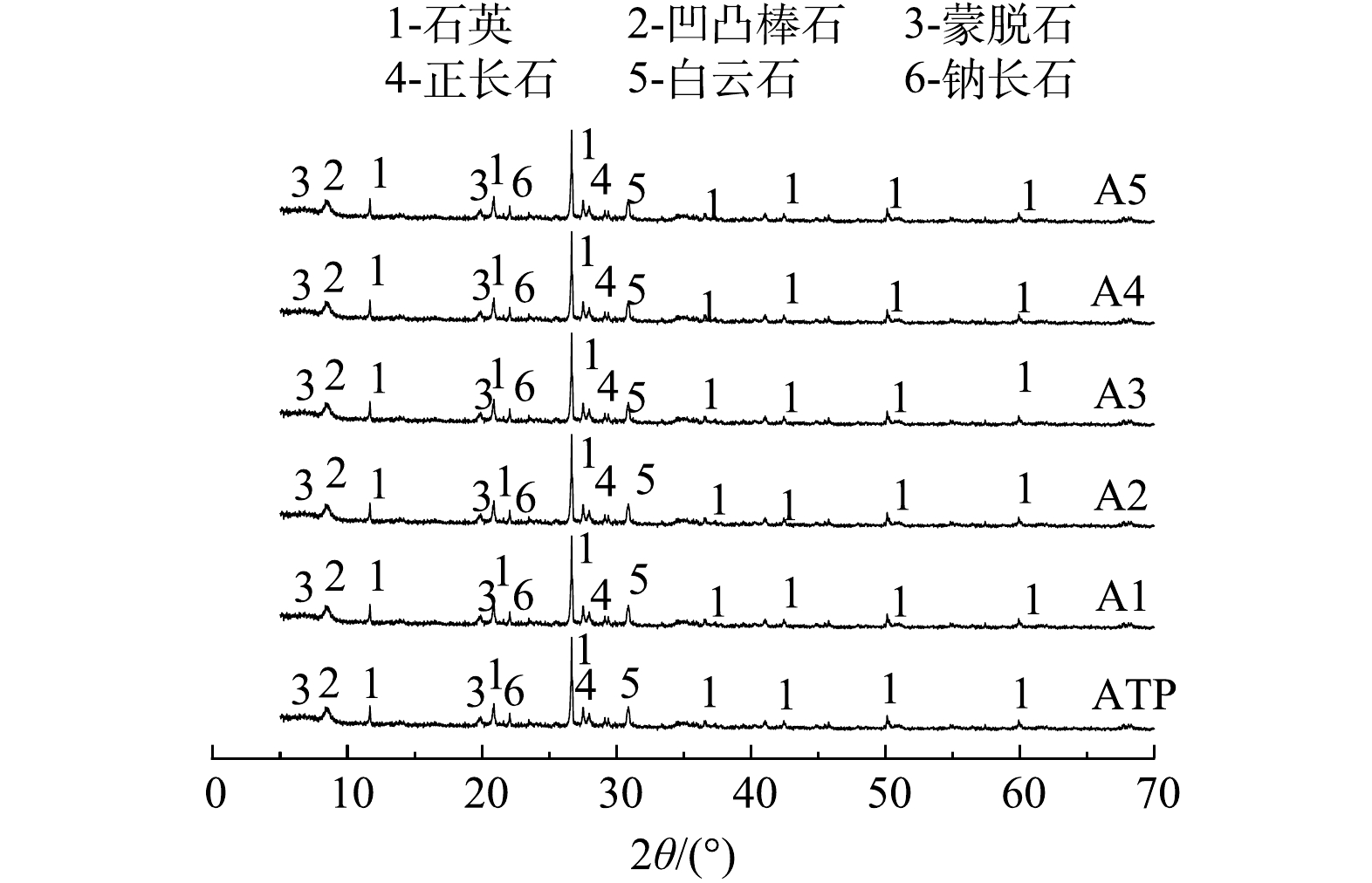
酸改性凹凸棒石的X射线衍射图谱结果见图6。凹凸棒石的特征峰位于8.40°处,与标准衍射图谱(JCPDFNo.020018)一致。石英特征衍射峰的存在证实了凹凸棒石中伴生有其他物相的杂质。从图中可以看出,经过酸改性后,凹凸棒石质黏土复合矿物物相组成及凹凸棒石、白云石物相的衍射峰峰强度没有明显改变,石英杂质的峰强度有轻微减弱。这表明,酸改性过程溶解了碳酸盐等杂质,但是并未破坏凹凸棒石的骨架结构。该结果与雷春生等[45]和张萍等[46]的研究结果一致。本研究结果表明,适宜的酸浓度和改性时间能够有效改善天然凹凸棒石原矿的表面形貌和孔隙结构,使得钝化材料孔隙结构增多,孔径变大,比表面积增大,促进了其对重金属的钝化修复。
2.5 土壤重金属的环境风险评价和钝化修复效率
与土壤中重金属的总量相比,水溶态Cu和Zn的质量分数占比不到0.01%。因此,本研究根据DTPA提取态重金属的质量分数来评价酸改性凹凸棒石钝化剂对土壤重金属的修复效率和生态风险。对照组污染土壤中Cu和Zn的环境风险指数分别对应为24.4%和11.51%。经不同的钝化材料处理后,土壤重金属的环境风险均较对照组显著降低(表4)。当施用A5钝化材料且投加量为16 g·kg−1时,酸改性凹凸棒石处理后Cu的环境风险指数降至最低。土壤Zn的环境风险由中风险降为低风险(表5),当施用A3材料且投加量为16 g·kg−1时,Zn的环境风险指数最低。
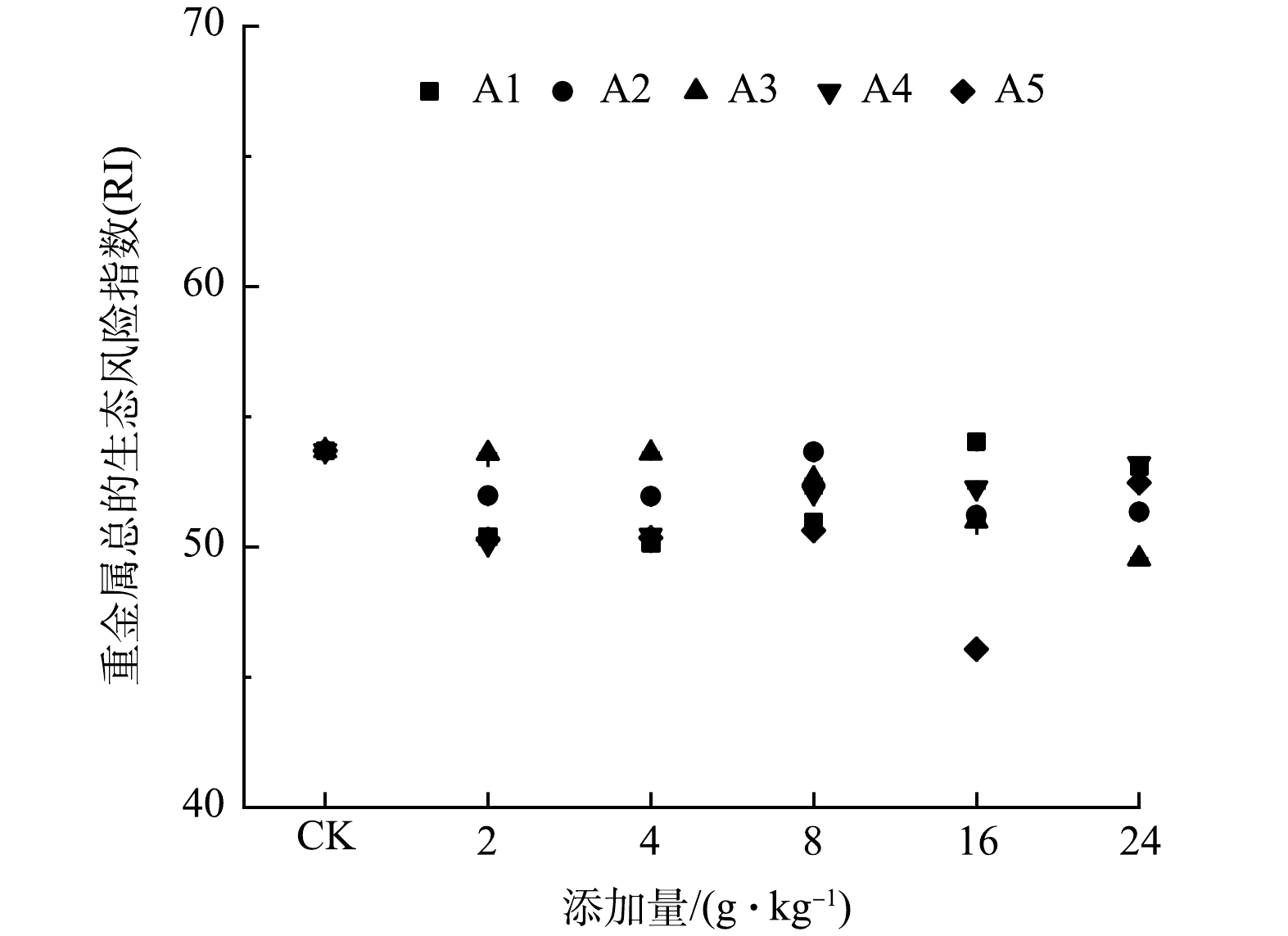
表 4 不同添加量酸改性凹凸棒石钝化土壤中Cu的环境风险指数Table 4. The environmental risk index of Cu in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) ERI/% A1 A2 A3 A4 A5 2 21.81±0.13Aa 20.80±0.02Ab 20.40±0.11Ac 20.35±0.07Ac 20.49±0.23Ac 4 21.72±0.06Aa 20.32±0.14Bb 19.88±0.26BCc 19.77±0.15BCc 20.28±0.13Ab 8 20.26±0.07Ba 19.97±0.14Cb 20.10±0.13ABab 19.42±0.18Dab 19.36±0.06Bc 16 19.80±0.15Ca 19.35±0.21Db 19.67±0.11Ca 19.87±0.07Ba 18.48±0.17Dc 24 19.43±0.18Dab 19.24±0.15Db 19.35±0.17Dab 19.56±0.10CDab 18.78±0.09Cc 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 表 5 不同添加量酸改性凹凸棒石钝化土壤中Zn的环境风险指数Table 5. The environmental risk index of Zn in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) ERI/% A1 A2 A3 A4 A5 2 9.47±0.03Aa 8.85±0.09Ab 8.55±0.11Ac 8.24±0.11Ad 8.31±0.04Ad 4 8.52±0.11BCab 8.59±0.11Ba 8.36±0.06Abc 8.00±0.08Bd 8.31±0.15Ac 8 8.83±0.10BCa 8.39±0.10Cb 8.48±0.19Ab 7.29±0.15Cc 8.21±0.20Ab 16 8.27±0.06Ca 8.13±0.09Da 6.13±0.10Bc 7.09±0.10Db 8.11±0.16Aa 24 8.88±0.66Ba 8.14±0.15Db 6.23±0.22Bd 7.00±0.09Dc 8.26±0.14Ab 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 在复合重金属污染土壤中,除了考虑单一重金属的环境风险外,受元素共存的联合作用影响,本研究评价了多种重金属的总环境风险指数RI。除添加量为16 g·kg−1的A1处理外,其他处理均显著降低了土壤RI。由图7可知,A3材料在较高添加量(≥8 g·kg−1)时,土壤RI指数随着添加量的增加显著降低。施用A5材料且添加量为16 g·kg−1时土壤中Cu、Zn的总生态风险指数达到最低。
钝化完成后,通常根据土壤中重金属的修复效率来评价钝化材料的实际应用价值。添加酸改性凹凸棒石后,Cu的修复效率随着投加量的增加呈先升高后轻微降低的趋势(表6),当钝化材料的投加量为16 g·kg−1时,重金属Cu的修复效率明显高于其他处理组。其中,A3处理组的钝化修复效率最高,达11.96%。重金属Zn修复效率的变化趋势与Cu基本一致(表7),当向土壤中施加16 g·kg−1的酸改性凹凸棒石后,Zn的修复效率明显高于其他处理组。其中,A3处理组Zn的钝化修复效率最高,为27.70%。
表 6 不同添加量酸改性凹凸棒石钝化土壤中Cu的修复效率Table 6. The remediation ratio of Cu in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) RR/% A1 A2 A3 A4 A5 2 7.90±0.22Dc 7.48±0.26Cc 9.52±0.12Ca 8.55±0.58Cb 7.64±0.17Dc 4 8.56±0.12Cb 7.82±0.31BCc 9.74±0.25Ca 9.62±0.23BCa 8.55±0.26Cb 8 9.11±0.12Bcd 8.53±0.24Bd 10.20±0.45BCb 11.01±0.62ABa 9.76±0.20Bbc 16 11.51±0.30Aa 9.87±0.28Ab 11.96±0.93Aa 11.24±0.15Aab 11.15±0.32Aab 24 11.30±0.31Aab 9.47±0.88Ac 11.00±0.38Bab 11.58±0.60Aa 10.35±0.74Bbc 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 表 7 不同添加量酸改性凹凸棒石钝化土壤中Zn的修复效率Table 7. The remediation ratio of Zn in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) RR/% A1 A2 A3 A4 A5 2 19.21±0.40Cc 20.83±0.38Cb 22.62±0.47Da 20.51±0.98Db 23.52±0.99Ca 4 21.20±0.48Bb 20.86±0.46Cb 24.86±1.00Ca 21.18±0.30CDb 25.63±0.30ABa 8 22.39±0.72ABb 22.50±0.60BCb 24.74±0.34Ca 21.97±0.52BCb 25.14±0.72BCa 16 23.55±0.12Ac 25.16±0.15Abc 27.70±0.11Aa 24.82±0.11Ac 27.40±0.14Aab 24 23.06±0.70Ab 22.91±0.15Bb 26.23±0.36Ba 23.06±0.39Bb 26.77±0.12ABa 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 3. 结论
1)当H2SO4的体积分数为12.5%和15%,改性时间为72 h时,制得的酸改性凹凸棒石对Cu、Zn的钝化效果最佳,其最优投加量为16 g·kg−1。
2)向土壤中施加酸改性凹凸棒石,可显著降低重金属Cu、Zn的生物有效态质量分数,当钝化材料的投加量为16 g·kg−1时,H2O提取态Cu、Zn分别降低了25.91%~47.87%和49.69%~65%,DTPA提取态Cu、Zn分别降低了8.63%~24.30%和28.26%~46.84%。这说明,16 g·kg−1凹凸棒石可以有效降低Cu、Zn的生物有效性。
3)酸改性凹凸棒石的添加促使重金属Cu、Zn由活性较高的酸溶态向活性较低的残渣态转变,提高土壤重金属修复效率,当H2SO4的体积分数为12.5%,改性时间为72 h时,向土壤中投加16 g·kg−1酸改性凹凸棒石,Cu、Zn的修复效率最高,可达11.96%和27.70%,此时Zn的环境风险最低,降至6.13%,处于低风险。
-
表 1 灰尘样品采样信息
Table 1. Dust sample sampling information
采样点Sampling points 采样位置Sampling locations 代号Name 样品数量Number 电子废弃物手工拆解车间内(1 间) 废旧CRT电视机拆解工位 CJGW 3 车间地面 CJDM 3 电子废弃物手工拆解车间外(2 个) 车间外部空地 CJWB 3 公司周边道路 DL 3 研究生办公室(2 间) 地面 BGS 3 教室(20 间) 地面 JS 3 废旧CRT电视机(15 个) 外壳内部 DSJK 3 表 2 不同人群的暴露参数取值
Table 2. Values of exposure parameters in different populations
参数Parameter 含义Implication 参考值Reference inhaleR /(m3·d−1) 呼吸摄入率 15.7[16] EF /(d·a−1) 人体暴露频率 250[17] ED /a 暴露持续时间 10[17]/4a PEF /(m3·kg−1) 颗粒排放因子 1.36×109[18] BW /kg 平均体重 61.9[16] AT非致癌 /d 平均接触时间 2500[17] / 1000b AT致癌 /d 平均终身接触时间 17500[19] ingestR /(mg·d−1) 灰尘摄入率 50[16] SA /cm2 皮肤接触污染物质面积 2253[17] / 4000c ABS 皮肤吸收因子 0.001 / 0.03[18] d AF /(mg·cm−2·d−1) 附着于皮肤的灰尘 0.22[20] 注:a,拆解车间人群持续暴露时间为10年,高校研究生办公室、教室人群暴露时间为4年;b,拆解车间人群平均接触时间为2500 d,高校研究生办公室、教室人群平均接触时间为1000天;c,办公室和教室接触人群取人体表面积的25%;d,As为0.03,其余元素为0.001。 a, the continuous exposure time of the population in the dismantling workshop is 10 years, and the exposure time of the population in the university graduate office and classroom is 4 years; b, the average contact time of the population in the dismantling workshop is 2500 days, and the average contact time of the population in the university graduate office and classroom is 1000 days; c, taking 25% of the human body surface area of the population in the university graduate office and classroom; d, As is 0.03, the other elements are 0.001. 表 3 重金属非致癌参考剂量(RfD)和致癌斜率因子(SF)[21]
Table 3. Non-carcinogenic reference dose (RfD) and carcinogenic slope factor (SF) of heavy metals
重金属Metal RfD /(mg·kg−1·d−1) SF /((kg·d)·mg−1) 呼吸吸入Inhale 经口摄入Ingest 皮肤接触Dermal 呼吸吸入Inhale 经口摄入Ingest 皮肤接触Dermal Cu 4.00×10−2 4.00×10−2 1.20×10−2 Pb 3.52×10−3 3.50×10−3 5.25×10−3 Zn 3.00×10−1 3.00×10−1 6.99×10−2 As 1.23×10−4 3.00×10−4 3.00×10−4 1.50 1.50 7.50 Cd 1.00×10−4 1.00×10−3 4.00×10−5 6.40 6.10 6.10 Cr 2.86×10−5 3.00×10−3 6.00×10−5 42.0 0.50 20.0 Ni 2.06×10−2 2.06×10−2 5.04×10−2 0.84 0.84a 0.84 注:a,无Ni的经口摄入致癌斜率因子参考值,此处参考呼吸吸入和皮肤接触。 a, Reference value of carcinogenic slope factor for oral intake without Ni, here refer to breathing inhalation and skin contact. 表 4 灰尘样品中重金属平均浓度(mg·kg−1)
Table 4. Mean heavy metal concentrations in indoor dust samples (mg·kg−1)
采样点Sampling point Pb Cu Zn As Cd Cr Ni CJCJ 13611 ± 3821 2034 ± 241 12503 ± 429 25.1 ± 13.6 10.7 ± 5.18 428 ± 66.6 915 ± 401 BGS 178 ± 12.0 340 ± 82.0 1268 ± 76.9 15.9 ± 1.75 3.66 ± 0.22 77.0 ± 3.35 442 ± 39.8 JS 50.8 ± 0.78 51.1 ± 13.4 383 ± 142 3.96 ± 1.40 0.40 ± 0.05 22.4 ± 4.96 18.6 ± 6.24 表 5 灰尘样品中重金属危险指数(HI)
Table 5. The hazard index of heavy metals in indoor dust samples
重金属 Metal CJCJ BGS JS HQinhale HQingest HQdermal HI HQinhale HQingest HQdermal HI HQinhale HQingest HQdermal HI Pb 5.15×10−4 2.24 1.48×10−2 2.26 2.70×10−6 1.18×10−2 1.38×10−4 1.19×10−2 7.69×10−7 3.35×10−3 3.93×10−5 3.39×10−3 Cu 6.77×10−6 2.93×10−2 9.69×10−4 3.03×10−2 4.53×10−7 1.96×10−3 1.15×10−4 2.08×10−3 6.81×10−8 2.95×10−4 1.73×10−5 3.12×10−4 Zn 5.55×10−6 2.40×10−2 1.02×10−3 2.51×10−2 2.25×10−7 9.75×10−4 7.37×10−5 1.05×10−3 6.80×10−8 2.95×10−4 2.23×10−5 3.17×10−4 As 2.72×10−5 4.82×10−2 1.43×10−2 6.26×10−2 6.90×10−6 1.23×10−2 6.47×10−3 1.87×10−2 1.72×10−6 3.05×10−3 1.61×10−3 4.66×10−3 Cd 1.42×10−6 6.16×10−3 1.53×10−3 7.68×10−3 1.95×10−7 8.45×10−4 3.72×10−4 1.22×10−3 2.15×10−8 9.33×10−5 1.23×10−3 1.33×10−3 Cr 1.99×10−3 8.23×10−2 4.08×10−2 1.25×10−1 1.43×10−4 5.92×10−3 5.21×10−3 1.13×10−2 4.17×10−5 1.72×10−3 1.51×10−3 3.28×10−3 Ni 5.92×10−6 2.56×10−2 1.04×10−4 2.57×10−2 1.15×10−6 4.96×10−3 3.57×10−5 5.00×10−3 4.82×10−8 2.09×10−4 1.50×10−6 2.10×10−4 ΣHI 2.55×10−3 2.46 7.36×10−2 2.54 1.55×10−4 3.87×10−2 1.24×10−2 5.12×10−2 4.44×10−5 9.01×10−3 4.44×10−3 1.35×10−2 表 6 灰尘样品中重金属致癌风险指数(CR)
Table 6. Carcinogenic risk of heavy metals in indoor dust samples
重金属 Metal CJCJ BGS JS CRinhale CRingest CRdermal CRT CRinhale CRingest CRdermal CRT CRinhale CRingest CRdermal CRT As 7.16×10−10 3.10×10−6 4.61×10−6 7.71×10−6 1.82×10−10 7.88×10−7 2.08×10−6 2.87×10−6 4.52×10−11 1.96×10−7 5.17×10−7 7.13×10−7 Cd 1.30×10−9 5.37×10−6 5.32×10−8 5.42×10−6 5.20×10−10 7.36×10−7 1.30×10−8 7.50×10−7 1.38×10−10 8.13×10−8 1.43×10−9 8.29×10−8 Cr 3.42×10−7 1.76×10−5 6.99×10−6 2.50×10−5 1.37×10−7 1.27×10−6 8.93×10−7 2.30×10−6 7.15×10−9 3.69×10−7 2.60×10−7 6.35×10−7 Ni 1.46×10−8 6.34×10−5 6.28×10−7 6.40×10−5 5.85×10−9 1.23×10−5 2.16×10−7 1.25×10−5 1.19×10−10 5.16×10−7 9.08×10−9 5.25×10−7 ΣCR 3.59×10−7 8.95×10−5 1.23×10−5 1.02×10−4 1.43×10−7 1.51×10−5 3.20×10−6 1.84×10−5 7.45×10−9 1.16×10−6 7.87×10−7 1.96×10−6 -
[1] FORTI V, BALDE C P, KUEHR R, et al. The Global E-waste Monitor 2020: Quantities, flows and the circular economy potential[M]. Bonn/Geneva/Rotterdam: United Nations University (UNU)/United Nations Institute for Training and Research (UNITAR)-co-hosted SCYCLE Programme, International Telecommunication Union (ITU) and International Soild Waste Association (ISWA), 2020. [2] ZENG X L, GONG R Y, CHEN W Q, et al. Uncovering the recycling potential of “New” WEEE in China [J]. Environmental Science & Technology, 2016, 50(3): 1347-1358. [3] OUABO R E, ODUNDIRAN M B, SANGODOYIN A Y, et al. Ecological risk and human health implications of heavy metals contamination of surface soil in e-waste recycling sites in douala, cameroun [J]. Jounal of Health and Pollution, 2019, 9(21): 190310. doi: 10.5696/2156-9614-9.21.190310 [4] SONG Q B, LI J H. Environmental effects of heavy metals derived from the e-waste recycling activities in China: A systematic review [J]. Waste Management (New York ), 2014, 34(12): 2587-2594. doi: 10.1016/j.wasman.2014.08.012 [5] SONG Q B, LI J H. A systematic review of the human body burden of e-waste exposure in China [J]. Environmental International, 2014, 68(7): 82-93. [6] SONG Q B, LI J H. A review on human health consequences of metals exposure to e-waste in China [J]. Environmental Pollution, 2015, 196(1): 450-461. [7] 杜曼曼, 丁庆玲, 王倩, 等. 宜兴市典型道路灰尘(<150 μm)组分中重金属污染特征及风险评价[J]. 环境化学, 2020, 39(6): 1689-1698. DU M M, DING Q L, WANG Q, et al. Characteristics and risk assessment of heavy metal pollution in typical road dust(<150 μm) components in Yixing City. Environmental Chemistry, 2020, 39(6): 1689-1698.
[8] 刘非凡, 白建峰, 顾卫华, 等. 烟曲霉f4对黑麦草修复电子废物拆解场地土壤重金属的影响 [J]. 环境工程学报, 2020, 14(7): 1886-1893. doi: 10.12030/j.cjee.201912062 LIU F F, BAI J F, GU W H, et al. Effects of aspergillus fumigatus F4 on heavy metals in soil of ryegrass remediation site of electronic waste dismantling site [J]. Journal of Environmental Engineering, 2020, 14(7): 1886-1893(in Chinese). doi: 10.12030/j.cjee.201912062
[9] MULLER G. Index of Geoaccumulation in Sediments of the Rhine River [J]. GeoJournal, 1969, 2(3): 109-118. [10] KHADEMI H, GABARRON M, ABBASPPUR A, et al. Environmental impact assessment of industrial activities on heavy metals distribution in street dust and soil [J]. Chemosphere, 2019, 217: 695-705. doi: 10.1016/j.chemosphere.2018.11.045 [11] MAURIZIO B. The importance of enrichment factor (EF) and geoaccumulation index (Igeo) to evaluate the soil Contamination [J]. Geology & Geophysics, 2016, 5(1): 1-4. [12] 赵一先. 环境影响评价中选取上海地区土壤重金属含量背景值的合理范围[J]. 科技创新与应用, 2016, 155(7): 158-158. ZHAO Y X. A reasonable range for selecting background value of heavy metal content in Soil in Shanghai area in environmental impact assessment [J]. Science Technology Innovation and Application, 2016, 155(7): 158-158(in hinese).
[13] WILSON M, SURENDRA P, SHANEEL C, et al. First assessment of metals contamination in road dust and roadside soil of Suva City, Fiji [J]. Archives of Environmental Contamination and Toxicology, 2019, 77(2): 249-262. doi: 10.1007/s00244-019-00635-8 [14] AYENUDDIN M, ABUSAYED M J, FERDOUSHI Z, et al. Carcinogenic and non-carcinogenic human health risk from exposure to heavy metals in surface water of Padma River [J]. Research Journal of Environmental Toxicology, 2018, 12(1): 18-23. doi: 10.3923/rjet.2018.18.23 [15] USEPA. Exposure Factors Handbook[R]. EPA/600/P-95/002Fa. Washington, DC: Environmental Protection Agency, Office of Research Development, 1997. [16] 赵秀阁, 段小丽. 中国人群暴露参数手册, 成人卷[M]. 北京: 中国环境出版社, 2013. ZHAO X G, DUAN X L. Manual of exposure parameters for Chinese population, Adults[M]. Beijing: China Environmental Science Press, 2013 (in Chinese).
[17] FANG W X, YANG Y C, XU Z M. PM10 and PM2.5 and health risk assessment for heavy metals in a typical factory for cathode ray tube television recycling [J]. Environmental Science & Technology, 2013, 47(21): 12469-12476. [18] LU X W, ZHANG X L, LI L Y, et al. Assessment of metals pollution and health risk in dust from nursery schools in Xi'an, China [J]. Environmental Reserach, 2014, 128(1): 27-34. [19] YEKEEN T A, XU X J, ZHANG Y L, et al. Assessment of health risk of trace metal pollution in surface soil and road dust from e-waste recycling area in China [J]. Environmental Science & Pollution Research, 2016, 23(17): 17511-17524. [20] TAN S Y, PRAVEENA S M, ABIDIN E Z, et al. A review of heavy metals in indoor dust and its human health-risk implications [J]. Reviews on Environmental Health, 2016, 31(4): 447-456. [21] 吴志远, 张丽娜, 夏天翔, 等. 基于土壤重金属及PAHs来源的人体健康风险定量评价∶以北京某工业污染场地为例 [J]. 环境科学, 2020, 41(9): 4180-4196. WU Z Y, ZHANG L N, XIA T X, et al. Quantitative assessment of human health risks based on soil heavy metals and PAHs sources: take a polluted industrial site of Beijing as an example [J]. Environmental Science, 2020, 41(9): 4180-4196(in Chinese).
[22] LEUNG A O W, DUZGOREN-AYDIN N S, CHEUNG K C, et al. Heavy metals concentrations of Surface dust from e-waste recycling and its human health implications in southeast China [J]. Environmental Science & Technology, 2008, 42(7): 2674-2680. [23] WU Y, LI Y, KANG D, et al. Tetrabromobisphenol A and heavy metal exposure via dust ingestion in an e-waste recycling region in Southeast China [J]. Science of the Total Environment, 2016, 541: 356-364. doi: 10.1016/j.scitotenv.2015.09.038 [24] DENG J J, GUO J, ZHOU X Y, et al. Hazardous substances in indoor dust emitted from waste TV recycling facility [J]. Environmental Science and Pollution Research, 2014, 21(12): 7656-7667. doi: 10.1007/s11356-014-2662-9 [25] OECD. Technical guidance for the environmentally sound management of specific waste streams: Used and scrap personal computers[R]. Paris: Organisation for Economic Cooperation and Development, 2003. [26] VERSTRAETEN S V, AIMO L, OTEIZA P I. Aluminium and lead: Molecular mechanisms of brain toxicity [J]. Archives of Toxicology, 2008, 82(11): 789-802. doi: 10.1007/s00204-008-0345-3 [27] 李晓燕, 汪浪, 张舒婷. 城市室内灰尘重金属水平、影响因素及健康风险: 以贵阳市为例[J]. 环境科学, 2016, 37(8): 2889-2896. LI X Y, WANG L, ZHANG S T. Heavy metal levels, influencing factors and health risks in urban indoor dust: A case study of Guiyang[J], Environmental Sciences, 2016, 37(8): 2889-2896.
[28] 曹治国, 余刚, 吕香英, 等. 北京市典型室内外灰尘中重金属的粒径和季节变异特征及人体暴露评估 [J]. 环境科学, 2016, 37(4): 1272-1278. CAO Z G, YU G, LU X Y, et al. The characteristics of particle size and seasonal variation of heavy metals in typical indoor and outdoor dust in Beijing and the evaluation of human exposure [J]. Environmental Sciences, 2016, 37(4): 1272-1278(in Chinese).
[29] 蔡云梅, 黄涵书, 任露陆, 等. 珠三角某高校室内灰尘重金属含量水平、来源及其健康风险评价 [J]. 环境科学, 2017, 38(9): 3620-3627. CAI Y M, HUANG H S, REN L L, et al. The level, source and health risk assessment of heavy metal content in indoor dust of a university in The Pearl River Delta [J]. Environmental Sciences, 2017, 38(9): 3620-3627(in Chinese).
[30] 白建峰, 李洋, 王鹏程, 等. 新建电子废弃物拆解厂附近土壤重金属污染评价及其来源分析 [J]. 安全与环境学报, 2016, 16(1): 333-336. BAI J F, LI Y, WANG P C, et al. Evaluation and source analysis of soil heavy metal pollution near the newly-built e-waste dismantling plant [J]. Journal of Safety and Environment, 2016, 16(1): 333-336(in Chinese).
[31] TZORAKI O, ZKERI E, LASITHIOTAKIS M, et al. Trace metals' contamination in water and soils in the vicinity of a small–medium waste electrical and electronic equipment recycling plant [J]. Environmental Progress & Sustainable Energy, 2020, 39(3): e13343. [32] 王芳, 王娟, 韩苗苗, 等. 大学校园室内PM2.5重金属污染特征及其健康风险评价 [J]. 东南大学学报(自然科学版), 2018, 48(5): 955-960. doi: 10.3969/j.issn.1001-0505.2018.05.026 WANG F, WANG J, HAN M M, et al. Characteristics of indoor PM2.5 heavy metal pollution and its health risk assessment in university campus [J]. Journal of Southeast University (Natural Science edition), 2018, 48(5): 955-960(in Chinese). doi: 10.3969/j.issn.1001-0505.2018.05.026
[33] XU F, LIU Y C, WANG J X, et al. Characterization of heavy metals and brominated flame retardants in the indoor and outdoor dust of e-waste workshops: Implication for on-site human exposure [J]. Environmental Science & Pollution Research International, 2015, 22(7): 5469-5680. [34] PRAGG C, MOHAMMED F K. Distribution and health risk assessment of heavy metals in road dust from an industrial estate in Trinidad, West Indies [J]. International Journal of Environmental Health Reserach, 2020, 30(3): 336-343. doi: 10.1080/09603123.2019.1609657 [35] XUE M Q, YANG Y C, RUAN J J, et al. Assessment of noise and heavy metals (Cr, Cu, Cd, Pb) in the ambience of the production line for recycling waste printed circuit boards [J]. Environmental Science & Technology, 2012, 46(1): 494-499. [36] 曹红梅, 赵留元, 穆熙, 等. 西北某电子垃圾拆解厂室内外重金属污染特征及暴露风险 [J]. 环境科学, 2019, 40(3): 1101-1110. CAO H M, ZHAO L Y, MU X, et al. Pollution characteristics and occupational exposure risk of heavy metals in indoor and outdoor ambient particles at a scaled electronic waste dismantling plant, Northwest China [J]. Environmental Science, 2019, 40(3): 1101-1110(in Chinese).
-




 DownLoad:
DownLoad: