-
生物质燃烧是我国华北区域秋冬季大气颗粒物污染的重要来源之一,燃烧过程中释放大量的CO、CO2、CH4、VOCs等气体和有机碳成分为主的气溶胶颗粒物,对局地和区域空气质量以及人体健康具有重要的影响[1-2]。据模式估算,由生物质燃烧排放的气溶胶约占全球一次有机碳的90%[3]。虽然2013年国务院颁布了“大气十条”治理空气污染,严格禁止秸杆露天焚烧,但是由于生物质锅炉、家用取暖等人为活动,导致生物质燃烧依然是我国大气颗粒物的重要来源[4-5],且近年来我国频发的重霾污染与生物质燃烧也密切相关[6]。
糖类化合物是大气颗粒物中广泛存在的有机物质[7],其中以左旋葡聚糖为代表的脱水糖(左旋葡聚糖、甘露聚糖、半乳聚糖)是含量最高的组分[8-9],左旋葡聚糖由于性质稳定且为纤维素在高温燃烧时产生,常被用作生物质燃烧的示踪物[10-11],生物质燃烧同时还释放少量的甘露聚糖和半乳聚糖[7]。大量的研究表明,在生物质燃烧较多的秋冬季,左旋葡聚糖的浓度显著高于其他两个季节[10]。其他糖类如葡萄糖主要通过植物的光合作用产生,多由植物的呼吸作用进入大气[12];阿拉伯糖醇和山梨醇和纤维醇主要来源于真菌和孢子的排放,常在源解析中用作真菌孢子排放的示踪物[13-14]。
石家庄市是京津冀地区重要工业城市,进入秋冬季节,灰霾污染频繁发生。姜建彪等[15]研究表明,石家庄市大气颗粒物中碳质组分浓度非常高,而糖类化合物在碳质组分中占有很大比例。因此,深入研究大气细粒子中糖类化合物的化学组成和来源,对控制石家庄市大气细粒子污染、减少灰霾污染的发生具有重要的意义。
-
采集点设在石家庄市中心广场(114°28′E、38°04′N),海拔15 m。采样仪器为天虹中流量颗粒物采样器(TH-100),流速为100L·min−1。采样滤膜选用石英滤膜(Whatman, d=90mm),采样前滤膜置于马弗炉中450 ℃焙烧4 h,样品称重前置于25 ℃,相对湿度为50%的恒温恒湿箱中平衡24 h,然后低温保存。将采样期分为秋、冬两个季节,每个季节选取一个月进行连续采样。其中秋季采样时间为2016年9月18日—10月17日;冬季采样时间为2016年12月15日—2017年1月13日。每日分昼夜采集,白天采集时间为8:00—19:30,夜晚采集时间为20:00—次日早上7:30,每次采集时间为11.5 h,釆样天气状况一般以晴,阴为主,避免雨雪过后的天气。采样期间温度和相对湿度变化见图1。由图1可见,采样期间平均气温秋季为(20.2±2.9)℃(白天)和(14.8±3.3)℃ (晚上),冬季分别为(4.2±1.5)℃(白天)和(0.49±2.6)℃(晚上);昼夜相对湿度秋季分别为66.0%±14.8%(白天)和87.0%±8.8% (晚上),,冬季分别为58.6%±14.1%(白天)和75.1%±13.9% (晚上),,夜间平均相对湿度均高于白天。
-
切取每张样品的1/4,剪成细条状置于10 mL提取瓶内,然后加入同位素标记的回收率指示物(13C-左旋葡聚糖),依次使用二氯甲烷和正己烷的混合试剂(V∶V=1∶1)、二氯甲烷和甲醇的混合试剂(V∶V=1∶1)各超声两遍,试剂加至采样膜被完全浸泡,盖好瓶盖,40 Hz超声15 min,将4次的提取液合并。利用旋转蒸发仪减压浓缩至0.5 mL左右(旋转蒸发时控制水浴温度为35 ℃),然后用二氯甲烷将样品转移到2 mL反应瓶中,用氮气吹干仪吹至近干,加入50 μL BSTFA+1% TMCs衍生化试剂和10 μL无水吡啶;70 ℃下恒温加热反应3 h,取出放至室温;加入浓度为2 mg·mL−1的六甲基苯20 μL作为内标,用正己烷定容至400 μL后进GC-MS分析。
-
本实验样品分析所采用的仪器为日本岛津气相色谱-质谱联用仪(2010plus/TQ8040, gas chromatograph-mass spectrometer, GC-MS),色谱柱为HP-5MS (30 m×0.25 mm×0.25 μm),载气为高纯氦气,流速为1.0 mL·min−1,进样量为1 μL,不分流模式。色谱柱温箱的升温程序为:初始温度50 ℃,保持2 min;以5 ℃·min−1的速率升至290 ℃,保持20 min。
本次实验对左旋葡聚糖(levoglucosan)、半乳聚糖(galactan)、甘露聚糖(mannosan)、果糖(fructose)、葡萄糖(glucose)、蔗糖(sucrose)、海藻糖(trehalose)、阿拉伯糖醇(arabitol)、山梨醇(sorbitol)、纤维醇(inositol)共10种糖醇进行了测定。本实验根据特性离子进行定性,内标法进行定量。各化合物的特征离子和定量离子信息见表1。
-
回收率指示物13C标记左旋葡聚糖的回收率范围为70%—110%,满足环境样品分析的要求。实验室空白和野外空白中都未检测到目标化合物,平行样的分析结果显示本方法具有良好的重现性,检测偏差小于15%。
-
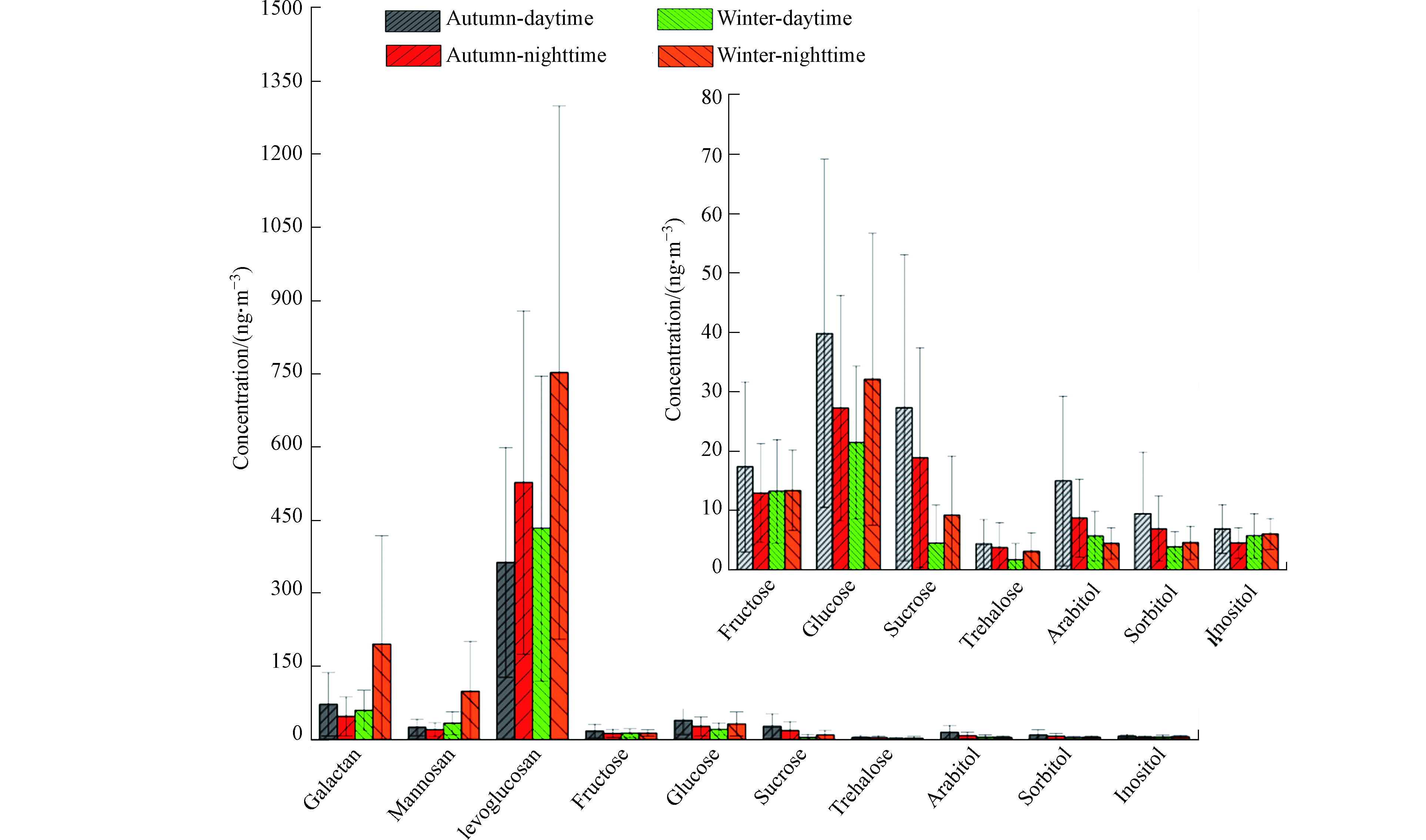
本研究共检测出10种糖醇化合物,分别为半乳聚糖、甘露聚糖、左旋葡聚糖、果糖、葡萄糖、海藻糖、蔗糖、山梨醇、阿拉伯醇和纤维醇,浓度结果见图2。从图2可以看出,石家庄市秋、冬季大气细粒子中糖醇总浓度分别为(629.57±446.05) ng·m−3和(950.45±821.63) ng·m−3,糖类物质总浓度变化范围是57.01—2411.5 ng·m−3,冬季平均总浓度要高于秋季。与国内外其它区域的相关研究对比发现,石家庄市秋冬季细粒子中糖类化合物的总浓度与中国香港大学校园[16]、美国德州Clarksville乡村[17]和中国上海郊区的浓度接近,低于北京[18]、广州城区[19],但要高于如美国、挪威等一些采样点[20-22]。
-
所采集的PM2.5样品中检测到的脱水糖主要包括左旋葡聚糖,半乳聚糖和甘露聚糖,是检测到的糖醇类化合物中的主要组成部分,分别占总浓度的87.4%(秋季)和91.9%(冬季)。其中左旋葡聚糖是最主要的糖类化合物质,约占检测糖醇总浓度的70%。左旋葡聚糖是纤维素燃烧的重要示踪物。纤维素分子是由7000—12000个右旋葡萄糖单体组成的长链线性聚合物[13],在高于300 ℃的高温下燃烧时经过高温裂变、歧化反应和不均反应产生独特的热解产物-左旋葡聚糖[12],以及少量的半乳聚糖和甘露聚糖。脱水糖的浓度均表现出夜晚高于白天的变化趋势,可能是因为秋天农民多在夜晚燃烧农作物秸秆,而冬天夜晚取暖造成的燃烧会产生比白天更多的脱水糖;同时夜晚大气混合层高度的降低也会使得糖类物质的浓度升高。不同脱水糖(左旋葡聚糖、甘露聚糖和半乳聚糖)之间浓度的比值可用来区分生物质燃烧的类型。Sang等[23]总结了软木、硬木、作物残渣的左旋葡聚糖/甘露聚糖(L/M)比值的均值依次为4.0±1.0、21.5±8.3、32.6±19.1;范围依次为2.5—8.8、13—35、12—56。在石家庄市秋冬季L/M的值分别为24.68±12.87(3.34—56.78)和20.87±9.10(7.46—55.54),表明石家庄市秋季作物残渣对大气中脱水糖类物质的贡献更多一些,而冬季硬木的贡献更多。
-
单糖和二糖在自然界中广泛存在,这主要是由于绿色植物的光合作用会产生大量的糖,比如葡萄糖、果糖、蔗糖等[10]。在石家庄市站点中所检测出的单糖和二糖类化合物主要是果糖、葡萄糖、蔗糖和海藻糖。蔗糖和海藻糖是大气颗粒物中主要的二糖,其中蔗糖是植物光合作用的主要产物,是植物储藏、积累和运输糖分的主要形式[15],Dahlman等[24]和Simoneit等[25]通过研究认为,蔗糖进入大气的主要途径是通过土壤的再悬浮作用,因此可将蔗糖作为一个土壤再悬浮的示踪物。海藻糖的性质十分稳定,是天然二糖中最稳定的非还原性糖[26],也常作为土壤再悬浮的重要示踪物用于大气颗粒物的源解析[27]。本研究中蔗糖和海藻糖在秋季白天的平均浓度分别为(27.28±25.74) ng·m−3和(4.31±4.14 )ng·m−3,夜间平均浓度分别为(18.83±18.54) ng·m−3和(3.72±4.18) ng·m−3,白天浓度高于夜间,而在冬季,这两种二糖的昼夜浓度表现为夜间浓度(蔗糖:(9.14±9.98 )ng·m−3,海藻糖:(3.05±3.16) ng·m−3)略高于白天的趋势(蔗糖:(4.44±6.43) ng·m−3,海藻糖:(1.65±2.72) ng·m−3),表明这两种糖类在秋季受植物活动排放的影响较大,而在冬季受气象条件的影响较大。
果糖和葡萄糖是植物中最常见的单糖,是多种花粉中含量最高的化合物,可将其作为花粉的示踪物质。秋天是农作物和水果成熟的季节,农作物收割、水果采摘和农田耕作都可向大气中排放果糖和葡萄糖。其次,生物质燃烧也对葡萄糖的浓度有一定贡献[26]。本研究中果糖和葡萄糖秋季的昼夜平均浓度表现为果糖白天((17.31±14.32) ng·m−3)高于夜间((12.90±8.33) ng·m−3)、葡萄糖白天((39.77±29.35) ng·m−3)高于夜间((27.2±18.99 )ng·m−3)的趋势;冬季的昼夜平均浓度表现为果糖白天((13.19±8.74) ng·m−3)和夜间((13.33±6.75) ng·m−3)基本持平、葡萄糖夜间((32.07±24.56 )ng·m−3)高于白天((21.39±12.87) ng·m−3)的趋势。这可能是由于秋季时白天植物光合作用和呼吸作用剧烈,而夜晚停止光合作用的原因导致。冬季温度低,植物的生命活动减弱,而夜晚取暖燃煤会排出少量的葡萄糖,所以导致冬季果糖基本持平,而葡萄糖夜晚明显高于白天。
-
在石家庄市大气细粒子中检测出的糖醇类化合物主要有阿拉伯糖醇、山梨醇和纤维醇,由图2可以看出,在石家庄市站点PM2.5样品中秋冬季节糖醇类物质的平均浓度分别为:(45.11±39.10) ng·m−3(白天)和(28.79±20.56) ng·m−3(夜间)、(24.57±16.82) ng·m−3(白天)和(30.91±20.51 )ng·m−3(夜间)。其中山梨醇和阿拉伯糖醇主要来源于真菌,多存在于绿色藻类、地衣真菌和低等植物中,高温高湿且阳光充足的环境有利于它们的活动,因此山梨醇和阿拉伯糖醇常被看作是真菌气溶胶的分子示踪物。秋季山梨醇和阿拉伯糖醇白天浓度明显高于夜间,主要原因是白天温度较高,藻类和真菌生命活动旺盛,代谢效率高。而冬季昼夜浓度差别不大,主要原因是冬季温度和湿度降低,使藻类和真菌代谢变弱。
-
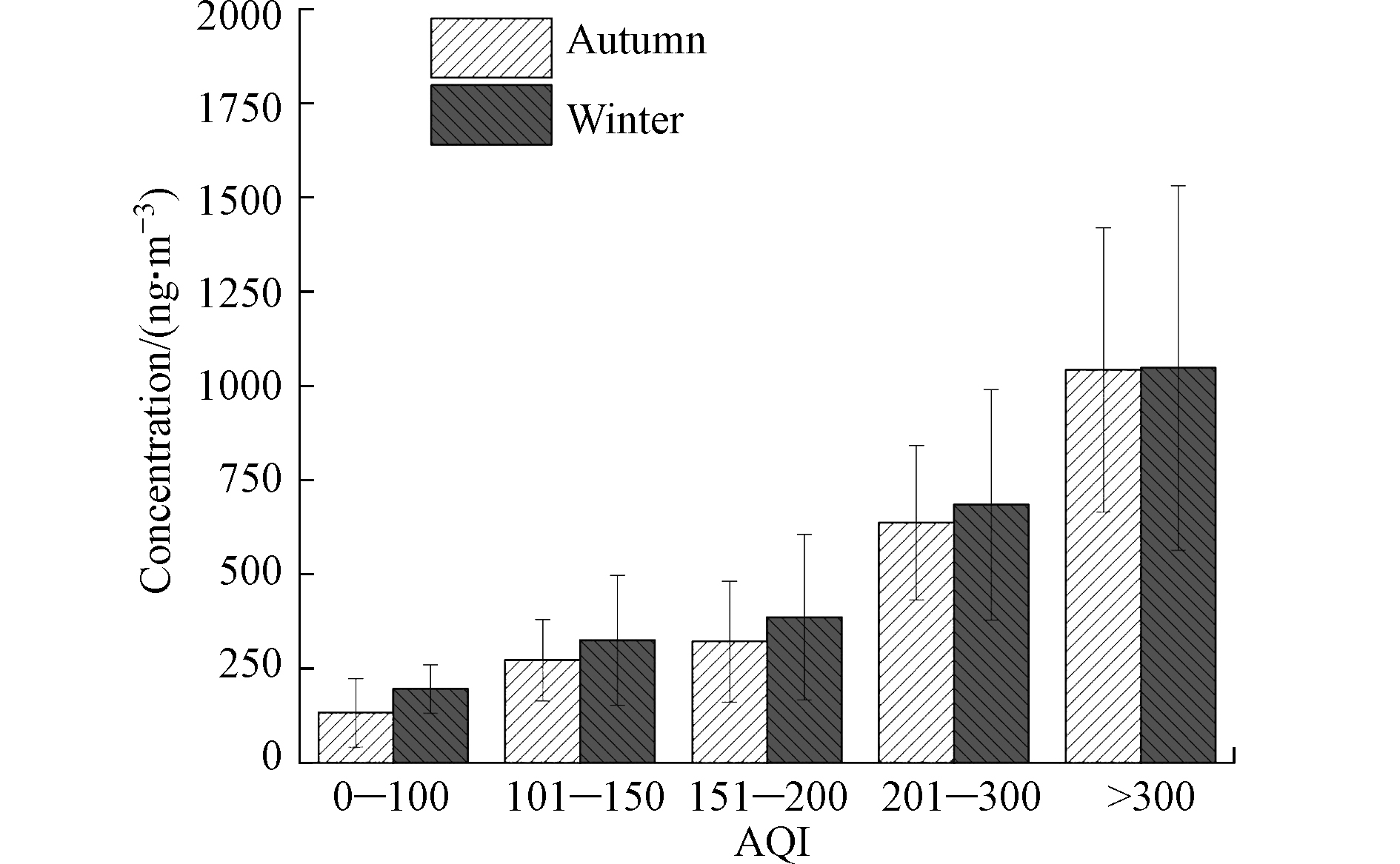
脱水糖是检测出来的最主要糖类,占糖类总浓度的80%以上,因此本研究重点分析了脱水糖在不同污染状况下的浓度特征,将空气质量指数AQI<100、101—150、151—200、201—300所对应的优良天、轻微污染、轻度污染、中度重污染和重度污染,将对应的脱水糖浓度进行分类统计,结果见图3。从图3可以看出,随着污染程度的加重,脱水糖的浓度也呈现上升的趋势,表明生物质燃烧对石家庄市大气污染的贡献不容忽视。
-
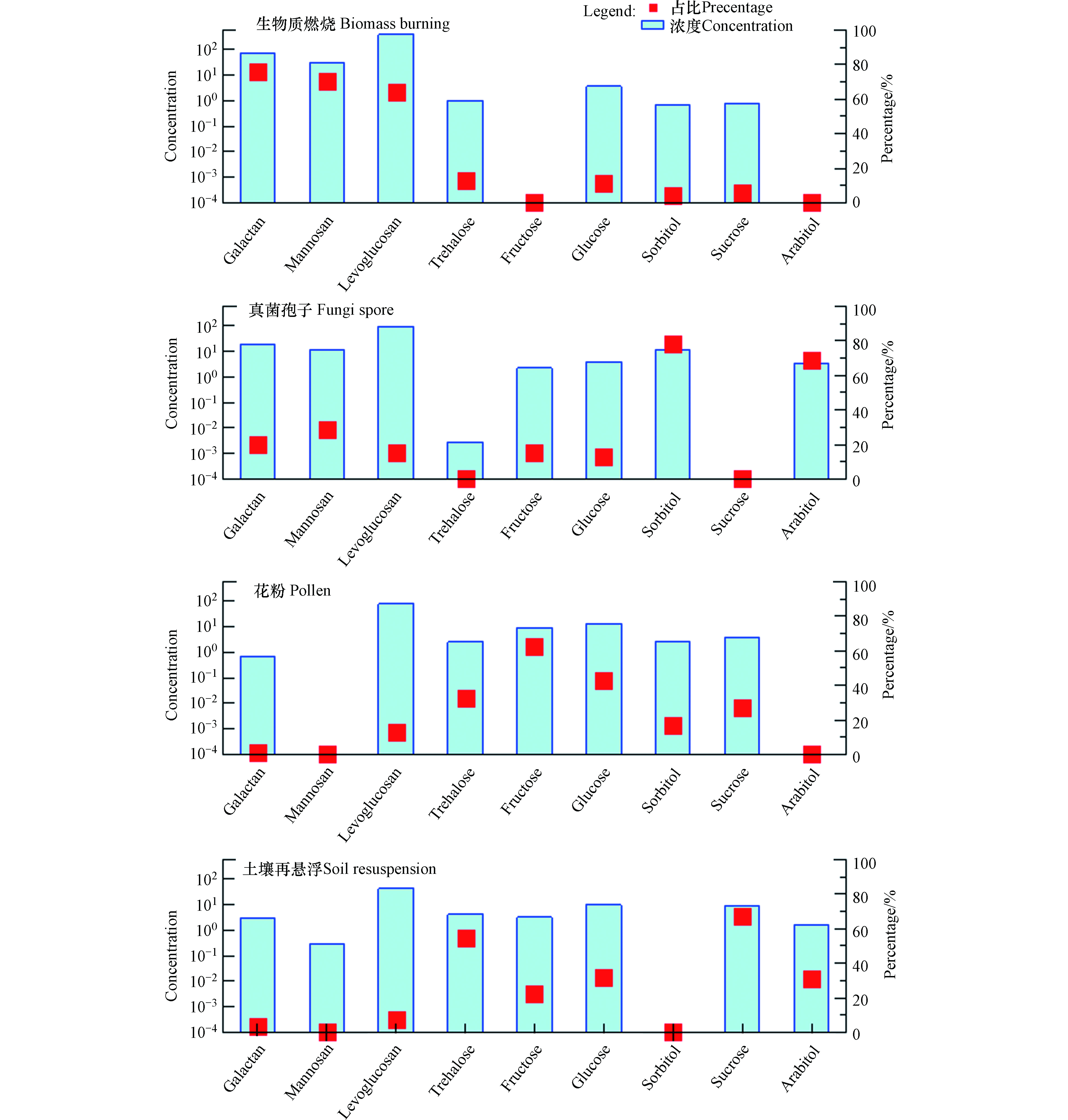
本研究应用PMF源解析模型对石家庄市采集的PM2.5中糖类化合物的来源进行分析,共120个样品。在PMF模型分析中,确定各种组分的不确定度,设定3—7个因子分别运行PMF,每种因子各计算50次。根据PMF模型分析结果的稳定性[28],得出4因子是石家庄市大气气溶胶中糖类化合物最优化的来源解析,结果如图4所示。
从图4中可以看出,因子1中的特征物是半乳聚糖、甘露聚糖和左旋葡聚糖,分别占其总量的81.6%、77.1%和70.7%,左旋葡聚糖等是生物质中纤维素在高温燃烧条件下生成的稳定性较高的特征产物,因此,因子1是指示生物质燃烧的贡献。因子2中阿拉伯糖醇和山梨醇为特征物质,分别占其总量的85.9%和84.3%,阿拉伯糖醇、山梨醇等糖醇类化合物多由真菌产生,因此,因子2是指示真菌孢子的贡献。因子3中果糖、葡萄糖为特征物质,分别占其总量的77.0%和62.5%,葡萄糖和果糖由植物自身产生,广泛分布在植物细胞中,是植物体内最常见的糖类化合物,且果糖通常被作为花粉的指示物,因此,因子3是指示农作物收割和花粉的贡献。因子4中蔗糖和海藻糖为特征物质,占其总量的72.6%和81.2%,海藻糖蔗糖可作为土壤再悬浮的指示物,因此,因子4是指示土壤再悬浮的贡献。同时因子4中还含有部分果糖和葡萄糖的贡献,暗示这两种糖类也可以通过土壤再悬浮的方式进入大气中。
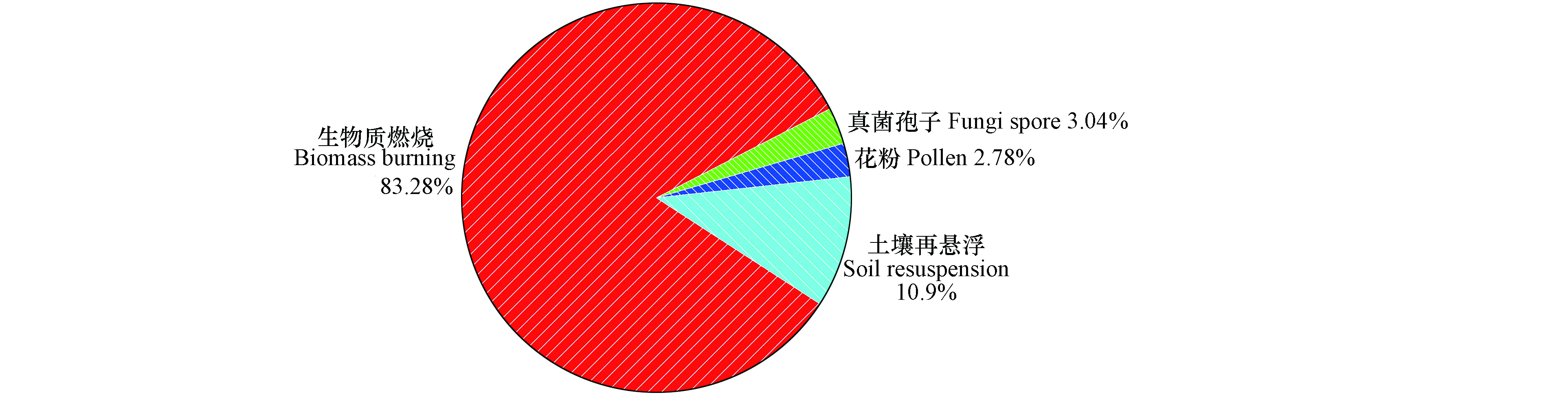
解析出来的4种来源对PM2.5中糖类的贡献率见图5。由图5可知,生物质燃烧排放对PM2.5中糖类的贡献最大,约占83%;其余3种排放源贡献较小,其中土壤再悬浮贡献约11%,真菌孢子源和花粉源各约占3%,表明石家庄市秋冬季受生物质燃烧的影响较大,土壤再悬浮也是一个不可忽视的因子。
-
(1)在2016—2017年秋冬季采样期间,石家庄市大气样品中均可监测出10种糖类物质,且脱水糖在所检测出的糖类化合物中是主要的糖类化合物。
(2)采集的石家庄市大气PM2.5样品中检测出的糖类化合物总浓度呈现出冬季>秋季的季节变化趋势,秋冬季糖类物质总浓度范围为57.01—2411.5 ng·m−3,平均浓度分别为(629.57±446.05) ng·m−3和(950.45±821.63) ng·m−3。
(3)石家庄市秋季以作物残渣为主要的生物质燃烧类型,冬季以硬木为主要的生物质燃烧类型。
(4)脱水糖类季节总浓度表现为冬季>秋季,且秋冬季均表现为夜间高于白天;单糖和二糖季节总浓度表现为秋季>冬季,其中,蔗糖秋季浓度明显高于冬季,其他糖类物质秋季浓度略高于冬季;糖醇类季节总浓度表现为秋季>冬季,阿拉伯糖醇浓度呈现为秋季明显高于冬季,其他糖醇的秋冬季浓度基本持平,且仅阿拉伯糖醇冬季平均浓度呈现为白天>夜间。
(5)应用PMF源解析模型对石家庄市秋冬季糖类化合物进行来源解析,得出石家庄市糖类化合物主要有生物质燃烧、真菌孢子、花粉、土壤再悬浮等来源,其中生物质燃烧是最主要的来源。
石家庄市秋冬季大气细粒子中糖类化合物的组成和来源
Studies on the composition and source of saccharides in autumn and winter PM2.5 in Shijiazhuang
-
摘要: 糖类化合物是大气颗粒物的重要组成部分,对局地甚至是全球气候变化有着重要的影响。本研究利用中流量颗粒物采样器分别于2016年9月18日—10月17日(秋季)和2016年12月15日—2017年1月13日(冬季)对石家庄市大气PM2.5样品进行了昼夜采集,并利用气相色谱质谱联用仪分析了样品中的10种糖类化合物,包括脱水糖、糖和糖醇。结果表明,石家庄市大气PM2.5中的糖类物质在秋冬季平均总浓度分别为(629.57±446.05 )ng·m−3和(950.45±821.63) ng·m−3,浓度变化范围是57.01—2411.5 ng·m−3。其中脱水糖类(包括左旋葡聚糖、半乳聚糖和甘露聚糖),冬季浓度要明显高于秋季,其主要来源于生物质燃烧,是秋冬季最主要的糖类物质,分别占糖类总浓度的87.4%(秋季)和91.9%(冬季);左旋葡聚糖/甘露聚糖(L/M)比值表明,石家庄市秋季以作物残渣为主要的生物质燃烧类型,而冬季以硬木为主要的生物质燃烧类型。单糖和二糖浓度变化趋势一致,均为秋季明显高于冬季,秋季白天高于夜间,冬季白天低于夜间。阿拉伯糖醇、山梨醇、纤维醇主要来源于真菌和孢子的排放,秋季浓度略高于冬季。PMF源解析结果表明,生物质燃烧(83%),真菌孢子排放(3%),花粉(3%)及土壤再悬浮(11%)是石家庄市大气细粒子中糖类物质的重要来源。Abstract: Saccharides are significant components of atmospheric particulate matter, and have an important impact on local and even global climate change. In this study, medium flow sampler was used to collect samples on diurnal/nocturnal basis in Shijiazhuang from September 18, 2016 to October 17, 2016 (autumn) and December 15, 2016 to January 13, 2017 (winter). 12 saccharides including dehydrated sugars, sugars, and sugar alcohols were detected using gas chromatography-mass spectrometry (GC-MS). The results showed that the average total concentrations of saccharides in the atmospheric PM2.5 in Shijiazhuang in autumn and winter were (629.57±446.05) ng·m−3 and (950.45±821.63) ng·m−3, ranging from 57.01 ng·m−3 to 2411.5 ng·m−3. Dehydrated saccharides (including levoglucosan, galactosan and mannosan) which mainly come from biomass combustion, were the most important saccharides, accounting for 87.4% (autumn) and 91.9% (winter) of the total detected saccharides. The ratio of Levoglucosan/mannosan (L/M) indicated that crop residues were the main burning type in autumn and hardwood was the main burning type in winter in shijiazhuang. Sucrose and trehalose were typical disaccharides which mainly derive from soil resuspension. The monosaccharide and disaccharide concentrations have the same change trend, both of which were significantly higher in autumn than in winter, autumn daytime was higher than nighttime, and winter daytime was lower than nighttime. Arabinol, sorbitol, and fibronol were common sugar alcohols, which mainly come from fungus and spore. The concentration of those sugar alcohols showed slightly higher level than that in winter. The results of PMF source analysis showed that biomass combustion (83%), fungal spore discharge (3%), pollen (3%) and soil re-suspension (11%) were important sources of detected saccharides in Shijiazhuang.
-
Key words:
- atmospheric fine particles /
- saccharides /
- Shijiazhuang /
- sources
-
近年来,电力行业已率先完成电站锅炉超低排放改造工作,氮氧化物 (NOx) 固定源排放控制任务的重心转移到焦化、钢铁等行业[1]。当前,烟气净化领域中应用较多的脱硝技术有选择性催化还原法 (selective catalytic reduction,SCR) 和选择性非催化还原法 (selective non-catalytic reduction,SNCR) 等。然而,由于投资运行成本高、系统复杂和氨易泄漏会造成二次污染等问题,这部分行业的超净排放任务实现难度较大[2-4]。湿法氧化脱硝技术具有操作管理简便、烟气条件适应性强和可实现多污染物同时脱除等优点,有望实现超净排放,故成为众多学者研究的热点[5]。当前研究较多的是采用向液相中投加氧化剂的形式氧化脱除烟气中的NOx,其效果虽好,但氧化剂为一次性消耗品,产生的废液需要处理。
采用电解NaCl溶液产生强氧化性的有效氯组分可用于烟气脱硝,并通过现场制备的方式可有效解决众多湿法脱硝氧化剂 (H2O2、KMnO4和NaClO2等) 储存运输过程的安全隐患及氧化成分分解消耗问题,同时脱硝液可循环电解使用,从而可有效减少氧化剂的投加成本[6]。
基于以上思路,本研究采用无隔膜法电解NaCl制备有效氯溶液,考察NaCl质量浓度、电解时间对有效氯组分生成的影响,并在自制的小型湿法鼓泡喷淋反应器中以NaCl电解液作为氧化吸收液进行模拟烟气脱硝实验,对电解氧化吸收液脱硝机理进行分析,同时考察氧化吸收体系因素 (有效氯初始质量浓度、反应体系初始pH和温度) 对烟气脱硝效果的影响,以期为低温湿法氧化脱硝技术工业化应用提供参考。
1. 材料与方法
1.1 材料与装置
实验采用NaCl、HCl、NaOH、C2H4O2、KI、NaS2O3·5H2O、Na2HPO4、KH2PO4等药品均为分析纯。本实验装置示意图如图1所示。装置可分为模拟烟气系统、有效氯溶液发生系统、氧化吸收系统及烟气分析系统。
在气体缓冲罐中,通入N2 (纯度为99.99%) 将NO (10%NO,N2为平衡气) 稀释至所需浓度,形成模拟烟气。本实验中,模拟烟气中的NO初始质量浓度设置为1 340 mg·m−3,烟气流量为2 L·min−1。有效氯溶液在电解发生器中产生,电解发生器槽电压电流可直接由直流恒压横流电源 (DQYY5-80,南通鼎麒电器有限公司) 进行调节。电解发生器阳极选用表面涂覆有钌铱等贵金属氧化物的纯钛板,阴级选用不锈钢板,电极板尺寸为80 mm×60mm×2 mm,并以3 mm的板间距并联均匀分布在发生装置内。氧化吸收过程是在实验室规模的底部带有砂芯布气器的鼓泡反应器 (
d h V 实验采用烟气分析仪 (Testo 350,德国德图公司) 分析进出口烟气中各组分的质量浓度,每次稳定采样时间为5 s。多余烟气通入5% HNO3和10% H2O2的混合液吸收瓶中,以吸收未被完全吸收的污染物。每次实验的循环保持15 min,所有实验重复3次。反应体系温度由恒温水浴锅 (HH-24,金坛市鑫鑫实验仪器有限公司) 控制;pH用pH计 (PHSJ-3F,上海雷磁科学仪器厂) 测定;有效氯质量浓度采用碘量法 (GB·T 5750.11-2006) [7]测定;电解液中各种氯氧化物的含量采用“五布碘量法”间接测定[8-9]。
1.2 数据处理
电流效率 (current efficiency,
CE CE=zFVCFAC6.00×104I′tMCl2×100% (1) 式中:z为析氯反应转移的电荷数,z = 2;F为法拉第常数,F = 96 486 C·mol−1;
CFAC V I' t MCl2 MCl2 NO转化率、NOx去除率的计算公式见式 (2) 。
η=C1−C2C1×100% (2) 式中:
η C1 C2 2. 结果与讨论
2.1 NaCl质量浓度对有效氯组分生成的影响
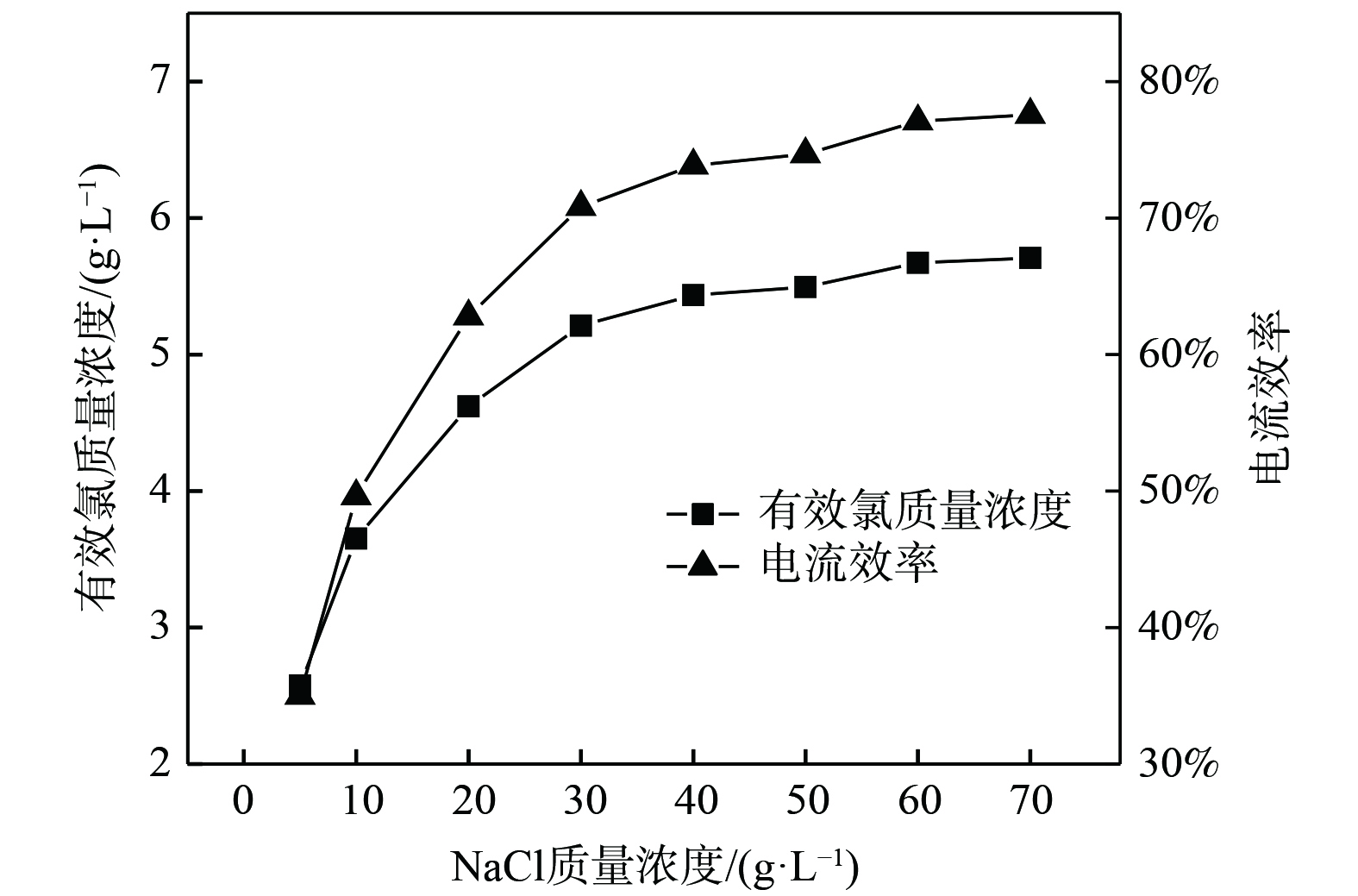
在电流密度为250 mA·cm−2、电解时间为5 min的条件下,研究了NaCl质量浓度对电解NaCl溶液制备有效氯质量浓度的影响,结果如图2所示。当电解时间一定时,电解液中有效氯质量浓度和电流效率随NaCl质量浓度增加而逐渐增加,而增幅不断减小。当NaCl质量浓度小于30 g·L−1时,电解液中Cl−质量浓度较低,有效氯生成速率主要受Cl−扩散速率的制约。同时,随着NaCl质量浓度增加,离子浓度也会增加,会使更多的离子参与电流传导,电导率随之增加,从而提高了电解过程的电流效率。当NaCl质量浓度大于30 g·L−1时,NaCl质量浓度继续增加对有效氯生成和电流效率影响较小。此时,电化学过程与电荷转移过程占主导作用。随着NaCl质量浓度继续增大,离子间距会缩小,离子间相互作用增强,离子运动阻力的增大会降低有效氯的生成速率[7]。综上所述,考虑到NaCl质量浓度超过30 g·L−1时,有效氯质量浓度增加量较少且会增大电解原料成本,将NaCl质量浓度定为30 g·L−1较合适。
2.2 电解时间对有效氯组分生成的影响
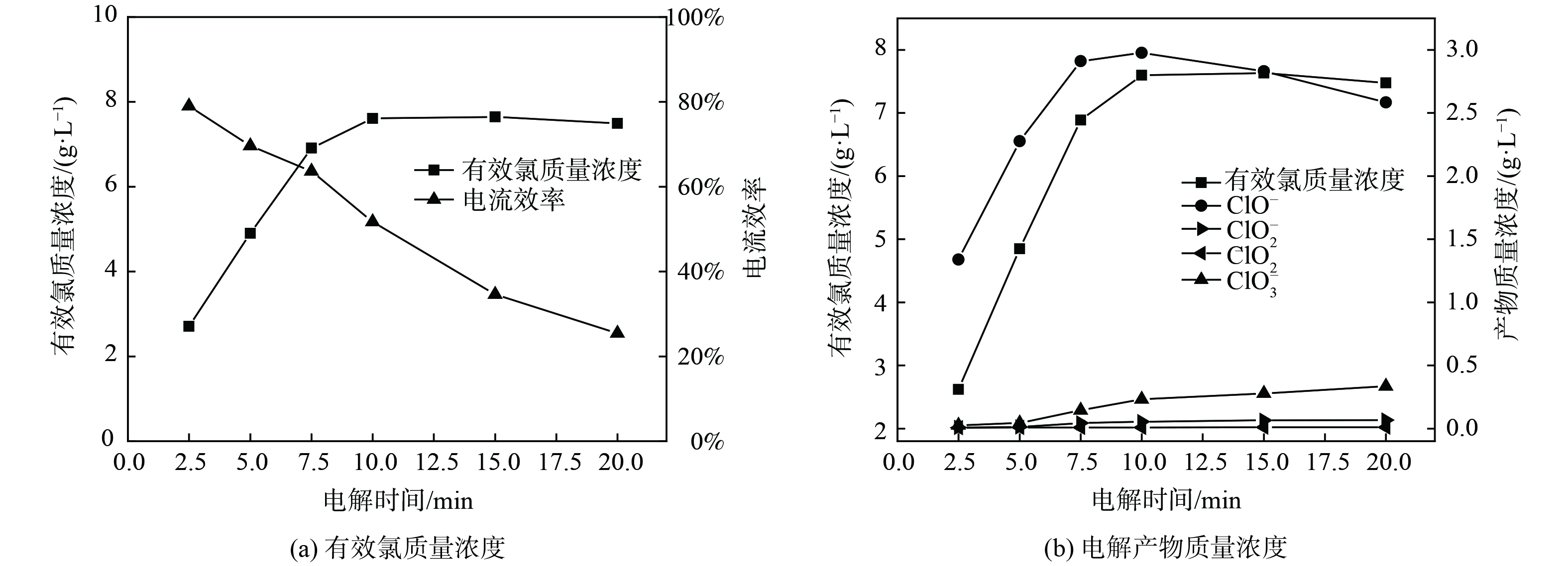
在NaCl质量浓度为30 g·L−1、电流密度为250 mA·cm−2的条件下,研究了有效氯的生成随电解时间变化的关系,结果如图3所示。图3 (a) 表明,随着电解时间延长,有效氯质量浓度逐渐增加而最终保持相对稳定,电流效率随电解时间的延长几乎呈线性下降。这是由于单位时间内参与阳极反应的Cl−因电解反应的发生不断消耗使得浓度降低;同时,在非恒温电解实验过程中,电流热效应会持续发生,温度升高会降低Cl2在电解液中的溶解度并促使有效氯组分扩散至阴级发生副反应,从而造成有效氯的分解[11]。图3 (b) 表明,当电解时间小于10 min时,ClO−质量浓度和副产物ClO3−质量浓度逐渐增高;当电解时间大于10 min后,ClO−质量浓度开始缓慢下降,而副产物ClO3−质量浓度持续增长。这是由于随着电解反应的发生,ClO−积累到一定浓度会加剧副反应的发生,ClO−进一步在阳极放电,产生ClO3−。电解过程ClO2−和ClO2的质量浓度始终不高,是由于电解反应主要以生成ClO−为主,生成ClO2−和ClO2的副反应不易发生。综上所述,为获得理想的电流效率 (效率大于60%) 和较高的有效氯质量浓度,电解时间可定为7.5 min。
2.3 NaCl电解氧化吸收液脱硝原理分析
烟气中95%以上的NOx是NO,而NO的溶解度极低[12]。湿法氧化脱硝技术是将烟气中的NO氧化为溶解度高、利于吸收的NO2,再进行下一步吸收反应。已知NO2/NO电对的标准电位为1.049 eV,故所采用的氧化剂电对的电势应大于该值[13]。表1为NaCl电解液中氧化成分、反应式及标准电位。NaCl电解液中氧化成分的电势高于1.049 eV的物质有Cl2、HClO、ClO2和NaClO3。
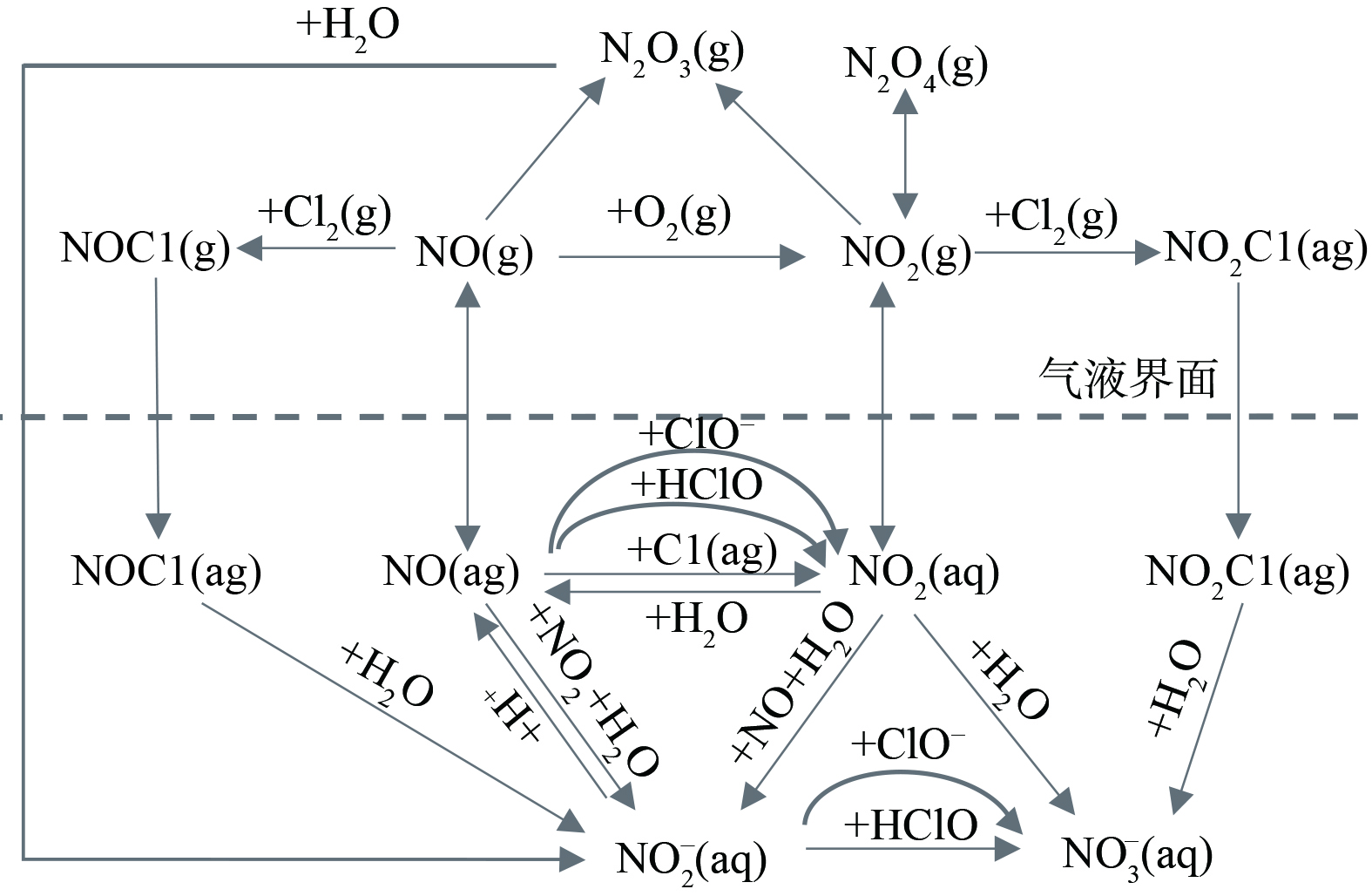
表 1 NaCl电解液中氧化成分、反应式以及标准电位Table 1. Oxidation components, reaction equations and standard potentials in NaCl electrolyte氧化成分 反应式 标准电位/eV Cl2 Cl2(aq)+2e = 2Cl− 1.358 HClO HClO+H++2e = Cl−+H2O 1.482 NaClO ClO−+H2O+2e= Cl−+2OH− 0.890 NaClO2 ClO2−+2H2O+4e = Cl−+4OH− 0.760 ClO2 ClO2+4H++5e = Cl−+2H2O 1.511 NaClO3 ClO3−+6H++6e = Cl−+3H2O 1.451 由2.2可知,电解反应主产物是ClO−,可推测有效氯溶液与烟气中的NOx发生氧化吸收的反应过程 (图4) [14-15]。NO的氧化吸收过程是从气相到液相的传质过程。由双膜理论可知,NO先由气膜进入液膜,在此过程中部分逸出Cl2可与NO反应结合,而在液膜中NO、NO2与有效氯组分反应,逐步被氧化为NO2−和NO3−,部分未被氧化的NO和NO2将以气态形式重新释放。
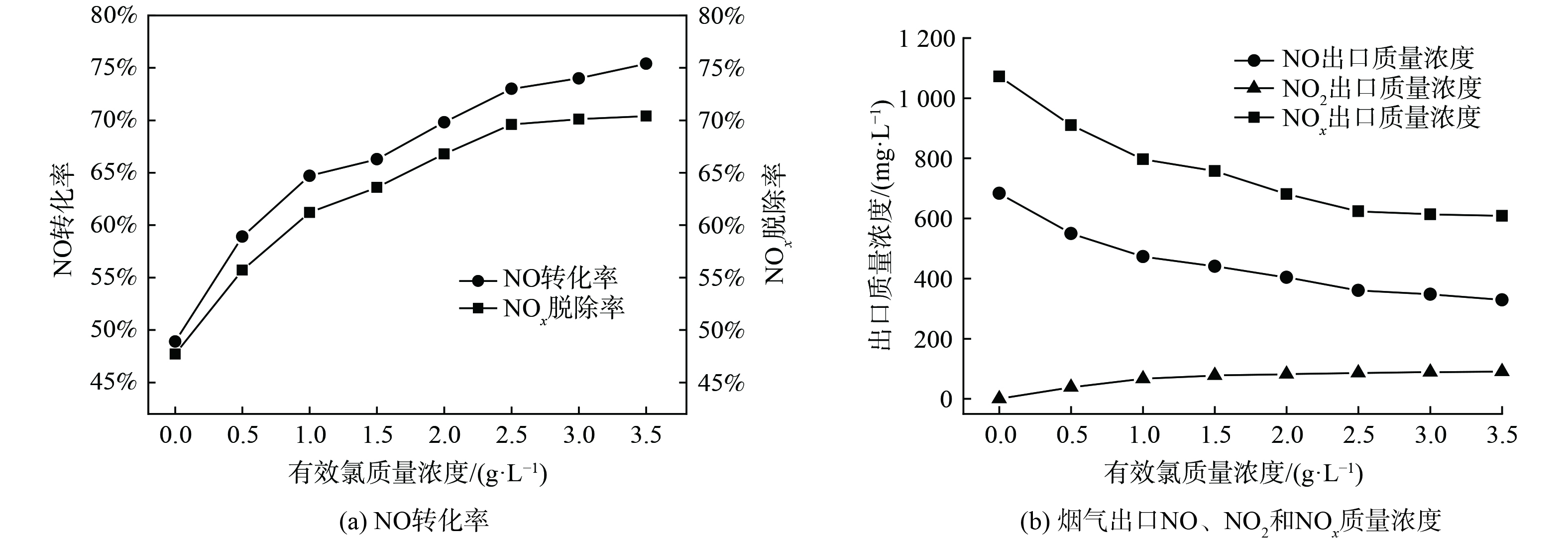
2.4 有效氯初始质量浓度对NOx脱除效果的影响
在反应体系温度为20 ℃、pH为9的实验条件下,研究了有效氯初始质量浓度对NOx脱除效果的影响,结果如图5所示。图5 (a) 是不同有效氯质量浓度对NOx脱除效果影响曲线图;图5 (b) 是不同有效氯质量浓度条件下的烟气出口NOx各组分质量浓度曲线图。随着有效氯初始质量浓度的增加,NO的转化率和NOx的去除率都逐渐增加后趋于平缓,烟气出口NOx各组分的质量浓度变化值减小。这是由于NO在液相中的溶解度较低,根据“双膜理论”,NO的氧化与吸收属于液膜控制,即由液相传质阻力控制。当溶液有效氯质量浓度从0增至2.5 g·L−1时,有效氯组分与NO间的传质增强,提高了NO的氧化率。当有效氯质量浓度达到2.5 g·L−1时,电解液氧化能力已满足氧化需求,继续提高质量浓度对NO氧化效果的提升较小[16]。综合考虑NO的转化率、NOx的去除率以及有效氯溶液的经济性,后续实验中有效氯质量浓度定为2.5 g·L−1。
2.5 氧化吸收液pH值对NOx脱除效果的影响
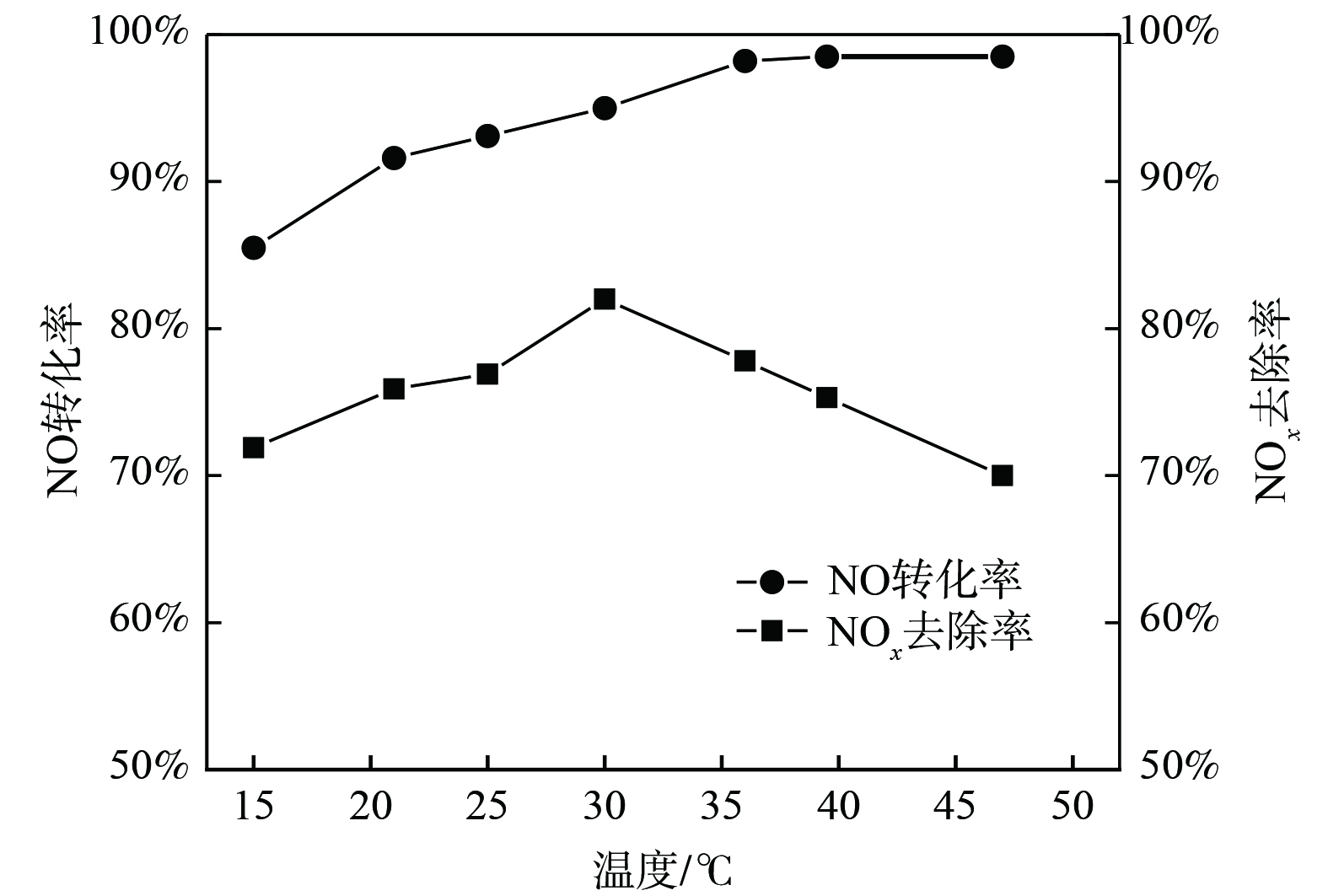
在有效氯初始质量浓度为2.5 g·L−1、反应体系温度为20 ℃的条件下,研究了pH对NOx脱除效果的影响,结果如图6所示。图6 (a) 是有效氯溶液中的主要成分随pH的变化图。因吸收液中有效组分随pH的不同发生改变,使其对应的氧化脱硝能力也发生改变,不同组分的氧化还原电位大小顺序为E(HClO/Cl−) > E(Cl2(aq)/Cl−) > E(ClO−/Cl−)[17-18]。因此,本实验探讨了NOx氧化脱除效果与反应体系pH的关系,结果如图6 (b) 所示。当pH < 4时,溶液的氧化还原电位较高,脱硝反应主要是HClO和Cl2的氧化吸收过程,有较高NO的转化率,但该酸性条件不利于氧化产物NO2的溶解吸收[19]。当4<pH<6时,吸收液中Cl2/HClO摩尔比降低,脱硝反应主要是HClO的氧化吸收过程,此时NO的转化率逐渐下降,氧化产物NO2的溶解度随pH的增加显著提高,总NOx去除率在pH为5时出现峰值。当pH > 7时,氧化吸收液中HClO/ClO−摩尔比逐渐降低,吸收液的氧化还原电位持续降低,NO转化率下降使得NOx的去除率随之下降。因此,综合NO的转化率和NOx的脱除率,并考虑酸性条件下设备腐蚀损耗,吸收液pH为5时脱硝效果最佳。
2.6 氧化吸收液温度对NOx脱除效果的影响
在有效氯初始质量浓度为2.5 g·L−1、反应体系pH为5的条件下,研究了吸收体系温度对NOx脱除效果的影响,结果如图7所示。随着吸收体系温度升高,NO转化率逐渐增加至稳定,而NOx去除率先增大后减少,并在30 ℃时取得峰值78.9%。NaCl电解氧化吸收液去除NO是气液传质反应,温度升高有助于增强液相组分的扩散传质并加快化学反应速率,从而促进NO的氧化[20-21];但温度升高增大了气液传质阻力,使得NO和氧化产物NO2溶解度降低。为获得较高NOx去除率,反应体系的温度控制在30 ℃为最佳。
2.7 最优条件下的平行实验
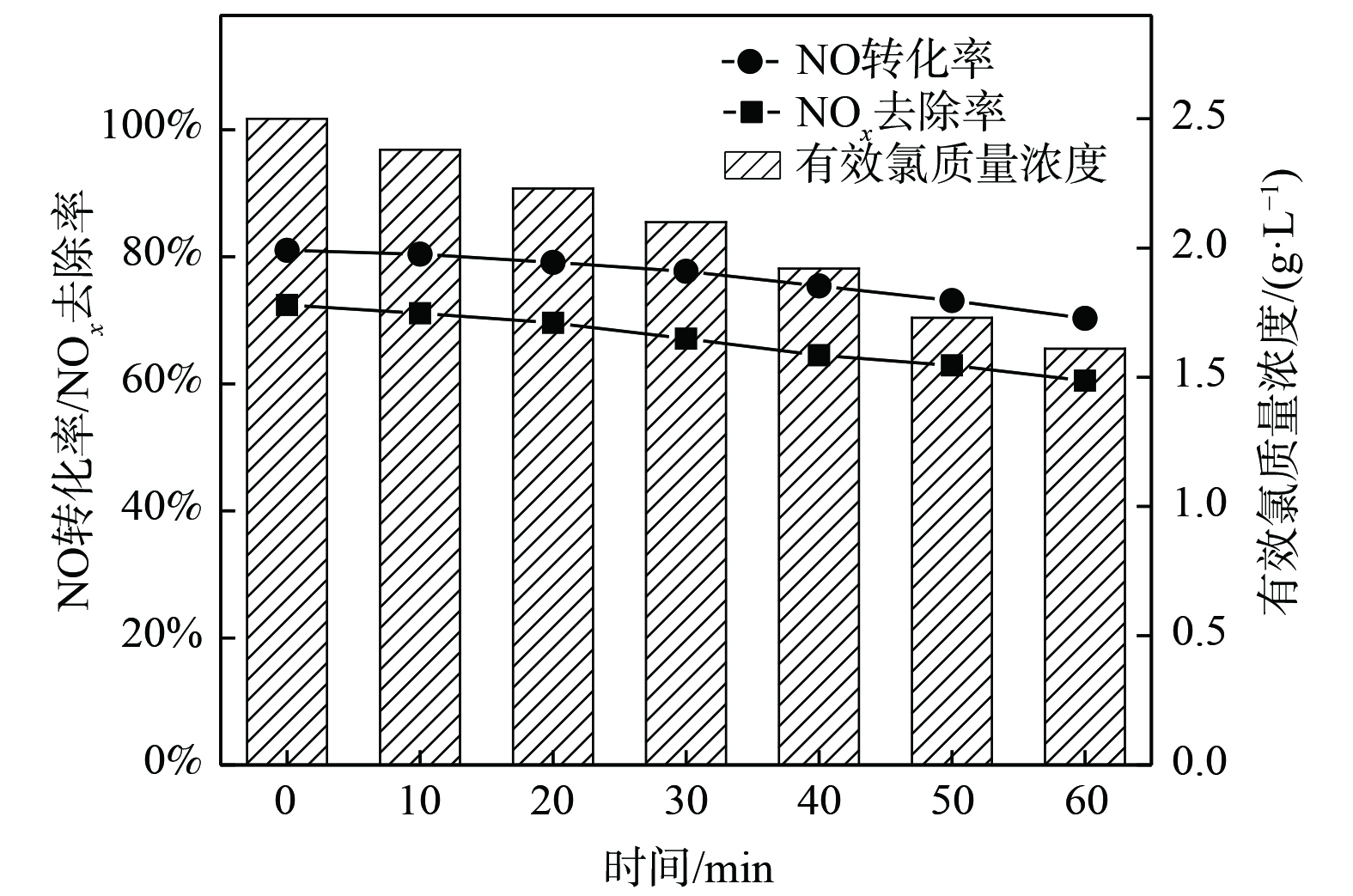
根据上述探讨的氧化吸收体系因素对烟气脱硝效果产生影响的所得结果,确定了最佳的反应条件:烟气流量为2 L·min−1,NO初始质量浓度为1 340 mg·m−3,吸收液有效氯初始质量浓度为2.5 g·L−1,反应体系pH为5,温度为30 ℃时,NO的转化率为91.1%,NOx去除率为78.9%。在最佳的反应条件下进行平行实验,结果如图8所示。在初始吸收液有效氯质量浓度一定的条件下,NO转化率、NOx去除率随时间的延长缓慢下降,在较长时间内保持较高的脱硝效果,NO的转化率从91.0%下降到80.3%,NOx的去除率从79%下降到60.5%。发生上述现象的原因有:一方面,随着氧化吸收液中有效成分与烟气中NO反应而被消耗,NO的氧化速率受到影响,同时溶液硝酸盐的累计也会影响NOx的吸收速率;另一方面,烟气中存在一定比例的酸性气体NO2,经吸收后会造成反应体系pH缓慢下降,有利于NO的氧化,但不利于氧化产物NO2的吸收,使得总NOx去除率降低加快。
3. 结论
1) 采用无隔膜法电解NaCl制备有效氯溶液,随着NaCl质量浓度和电解时间的增加,有效氯质量浓度逐渐增加,其增量逐渐减少,电解反应的主产物是ClO−,副产物主要是ClO3−。
2) 较高的有效氯NaCl质量浓度有利于NO氧化并促使NOx去除率升高;较低的pH有利于NO氧化,但不利于NOx去除,在弱酸条件下NOx去除效果最好;较高的温度有利于NO氧化,但不利于NOx去除。
3) 在最佳反应条件 (烟气流量为2 L·min−1,NO初始质量浓度为1 340 mg·m−3,吸收液有效氯初始NaCl质量浓度为2.5 g·L−1,反应体系pH为5,温度为30 ℃) 下,NO的转化率可达91.1%,NOx去除率可达78.9%,且能在较长时间内保持较高的烟气脱硝效果。
4) 基于研究结果,后期还应探讨更多的因素 (更加复杂的实际工业烟气、系统内氯气溢出逃逸、反应装置的氧化腐蚀等) 对NaCl电解氧化脱硝系统的影响,以期为其工业化应用提供更加全面的参考。
-
表 1 糖类硅烷化混合物的特征离子及定量离子
Table 1. Characteristic and quantitative ions of saccharides (derivatized by TMCs)
名称Name 分子式 Molecular formula 特征离子Qualitative ions 定量离子Quantitative ion Galactan C15H34O5Si3 73,147,204,217,333 217 Mannosan C15H34O5Si3 73,147,204,217,333 217 13C-Levoglucosan C15H34O5Si3 73,147,206,220,338 220 Levoglucosan C15H34O5Si3 73,147,204,217,333 217 Arabitol C20H52O5Si5 73,103,147,217,307 217 α-Fructose C21H52O6Si5 73,147,191,204,217 217 β-Fructose C21H52O6Si5 73,147,191,204,217 217 α-Glucose C21H52O6Si5 73,147,191,204,217 217 β-Glucose C21H52O6Si5 73,147,191,204,217 217 Sorbitol C24H62O6Si6 73,147,205,217,319 217 Inositol C24H62O6Si6 73,147,217,305,318 217 Sucrose C33H78O11Si7 73,147,191,217,361 217 Trehalose C33H78O11Si7 73,147,191,217,361 217 -
[1] SIMONEIT B R T. Biomass burning - A review of organic tracers for smoke from incomplete combustion [J]. Appl Geochem, 2002, 17(3): 129-162. doi: 10.1016/S0883-2927(01)00061-0 [2] ZHAO H M, ZHANG X L, ZHANG S C, et al. Effects of agricultural biomass burning on regional haze in China: A review [J]. Atmosphere-Basel, 2017, 8(5): 88-97. [3] ITO A, PENNER J E. Historical emissions of carbonaceous aerosols from biomass and fossil fuel burning for the period 1870-2000 [J]. Global Biogeochem Cycles, 2005, 19(2): 1-14. [4] CHENG Y, ENGLING G, HE K B, et al. The characteristics of Beijing aerosol during two distinct episodes: Impacts of biomass burning and fireworks [J]. Environ Pollut, 2014, 185: 149-157. doi: 10.1016/j.envpol.2013.10.037 [5] 高雅琴, 王红丽, 景盛翱, 等. 上海夏季PM2.5中有机物的组分特征、空间分布和来源 [J]. 环境科学, 2018, 39(5): 1978-1986. GAO Y Q, WANG H L, JING S A, et al. Chemical characterization, spatial distribution, and source identification of organic matter in PM2.5 in summertime Shanghai, China [J]. Environmental Science, 2018, 39(5): 1978-1986(in Chinese).
[6] CHEN J M, LI C L, RISTOVSKI Z, et al. A review of biomass burning: Emissions and impacts on air quality, health and climate in China [J]. Sci Total Environ, 2017, 579: 1000-1034. doi: 10.1016/j.scitotenv.2016.11.025 [7] SCARAMBONI C, URBAN R C, LIMA-SOUZA M, et al. Total sugars in atmospheric aerosols: An alternative tracer for biomass burning [J]. Atmospheric Environment, 2015, 100: 185-192. doi: 10.1016/j.atmosenv.2014.11.003 [8] ZHANG T, CLAEYS M, CACHIER H, et al. Identification and estimation of the biomass burning contribution to Beijing aerosol using levoglucosan as a molecular marker [J]. Atmospheric Environment, 2008, 42(29): 7013-7021. doi: 10.1016/j.atmosenv.2008.04.050 [9] SIMONEIT B R T, SCHAUER J J, NOLTE C G, et al. Levoglucosan, a tracer for cellulose in biomass burning and atmospheric particles [J]. Atmospheric Environment, 1999, 33(2): 173-182. doi: 10.1016/S1352-2310(98)00145-9 [10] LI X R, WEN T X, XIN J Y, et al. Spatial and seasonal variations of sugars (alcohol) in China: Emerging results from the CARE-China network [J]. Atmospheric Environment, 2019, 209: 136-143. doi: 10.1016/j.atmosenv.2019.04.029 [11] LI X R, LIU Y S, LI D, et al. Molecular composition of organic aerosol over an agricultural site in North China Plain: Contribution of biogenic sources to PM2.5 [J]. Atmospheric Environment, 2017, 164: 448-457. doi: 10.1016/j.atmosenv.2017.06.018 [12] KANAKIDOU M, SEINFELD J H, PANDIS S N, et al. Organic aerosol and global climate modelling: A review [J]. Atmospheric Chemistry and Physics, 2005, 5(4): 1053-1123. doi: 10.5194/acp-5-1053-2005 [13] ELBERT W, TAYLOR P E, ANDREAE M O, et al. Contribution of fungi to primary biogenic aerosols in the atmosphere: wet and dry discharged spores, carbohydrates, and inorganic ions [J]. Atmos Chem Phys, 2007, 7(17): 4569-4588. doi: 10.5194/acp-7-4569-2007 [14] 王鑫彤, 鞠法帅, 韩德文, 等. 大气颗粒物中生物质燃烧示踪化合物的研究进展 [J]. 环境化学, 2015, 34(10): 1885-1894. doi: 10.7524/j.issn.0254-6108.2015.10.2015040704 WANG X T, JU F S, HAN D W, et al. Research progress on the organic tracers of biomass burning in atmospheric aerosols [J]. Enviromental Chemistry, 2015, 34(10): 1885-1894(in Chinese). doi: 10.7524/j.issn.0254-6108.2015.10.2015040704
[15] 姜建彪, 常青, 冯媛, 等. 石家庄市大气颗粒物中有机碳和元素碳的季节变化特征 [J]. 环境监控与预警, 2017, 9(2): 41-45. doi: 10.3969/j.issn.1674-6732.2017.02.011 JIANG J B, CHANG Q, FENG Y, et al. Seasonal variation of organic carbon and elemental carbon in atmospheric particles in Shijiazhuang [J]. Environmental Monitoring and Forewarning, 2017, 9(2): 41-45(in Chinese). doi: 10.3969/j.issn.1674-6732.2017.02.011
[16] WAN E C H, YU J Z. Analysis of sugars and sugar polyols in atmospheric aerosols by chloride attachment in liquid chromatography / negative ion electrospray mass spectrometry [J]. Environmental Science& Technology, 2007, 41(7): 2459-2466. [17] JIA Y, CLEMENTS A L, FRASER M P. Saccharide composition in atmospheric particulate matter in the southwest US and estimates of source contributions [J]. Journal of Aerosol Science, 2010, 41(1): 62-73. doi: 10.1016/j.jaerosci.2009.08.005 [18] 梁林林, ENGLING G, 段凤魁, 等. 北京市大气气溶胶中糖类化合物的组成及来源 [J]. 环境科学, 2015, 36(11): 3935-3942. LIANG L L, ENGLING G, DUAN F K, et al. Composition and source apportionments of saccharides in atmospheric particulate matter in Beijing [J]. Environmental Sciences, 2015, 36(11): 3935-3942(in Chinese).
[19] 马社霞, 王真真, 毕新慧, 等. 广州大气气溶胶中糖类化合物的组成及主要来源 [J]. 科学通报, 2009, 5454(17): 2562-2567. MA S X, WANG Z Z, BI X H, et al. Composition and source of saccharides in aerosols in Guangzhou [J]. Chinese Sci Bull, 2009, 5454(17): 2562-2567(in Chinese).
[20] GRAHAM B, GUYON P, TAYLOR P E, et al. Organic compounds present in the natural Amazonian aerosol: Characterization by gas chromatography-mass spectrometry [J]. Journal of Geophysical Research: Atmospheres, 2003, 108(D24): 1-13. [21] NIEMALKAP J, DESHMUKH D K, DEB M K, et al. Mass loading and episodic variation of molecular markers in PM2.5 aerosols over a rural area in eastern central India [J]. Atmospheric Environment, 2015, 117: 41-50. doi: 10.1016/j.atmosenv.2015.07.003 [22] YTTRI K E, DYE C, KISS G. Ambient aerosol concentrations of sugars and sugar-alcohols at four different sites in Norway [J]. Atmos Chem Phys, 2007, 7(2): 5769-5803. [23] SANG X, ZHANG Z, CHAN C, et al. Source categories and contribution of biomass smoke to organic aerosol over the southeastern Tibetan Plateau [J]. Atmospheric Environment, 2013, 78: 113-123. doi: 10.1016/j.atmosenv.2012.12.012 [24] DAHLMAN L, PERSSON J, N SHOLM T, et al. Carbon and nitrogen distribution in the green algal lichens hypogymnia physodes and Platismatia glauca in relation to nutrient supply [J]. Planta, 2003, 217(1): 41-48. doi: 10.1007/s00425-003-0977-8 [25] SIMONEIT B R T, ELIASVO, KOBAYASHI M, et al. Sugars dominant water-soluble organic compounds in soils and characterization as tracers in atmospheric particulate matter [J]. Environmental Science& Technology, 2004, 38(22): 5939-5949. [26] MEDEIROS P M, CONTE M H, WEBER J C, et al. Sugars as source indicators of biogenic organic carbon in aerosols collected above the Howland Experimental Forest, Maine [J]. Atmospheric Environment, 2006, 40(9): 1694-1705. doi: 10.1016/j.atmosenv.2005.11.001 [27] 靳文斌, 李克文, 胥九兵, 等. 海藻糖的特性、功能及应用 [J]. 精细与专用化学品, 2015, 23(1): 30-33. doi: 10.3969/j.issn.1008-1100.2015.01.008 JIN W B, LI K W, XU J B, et al. The character and function of trehalose and its application [J]. Fine and Specialty Chemicals, 2015, 23(1): 30-33(in Chinese). doi: 10.3969/j.issn.1008-1100.2015.01.008
[28] BAUER H E, SCHUELLER G, WEINKE, et al. Significant contributions of fungalspores to the organic carbon and to the aerosol mass balance of the urban atmospheric aerosol [J]. Atmospheric Environment, 2008, 42(22): 5542-5549. doi: 10.1016/j.atmosenv.2008.03.019 -





 下载:
下载: