-
近年来,随着我国畜禽养殖业的集约化、规模化发展以及动物疾病复杂性的增加,抗生素多作为饲料添加剂用于预防、治疗动物疾病,促进动物生长。但被摄入体内的抗生素很难为动物机体完全吸收[1],有很大一部分(30%~90%)随着动物粪便以畜禽养殖废水的形式进入水体环境[2-3],导致畜禽养殖废水成为水体环境中抗生素污染的主要来源之一[4]。畜禽养殖废水中的抗生素进入环境中会发生非生物降解(光解、水解和氧化降解等)和生物降解(植物或微生物降解)反应。四环素类抗生素(tetracyclines,TCs)在中国及世界畜禽养殖业中的使用量均为最大[5]。猪场等养殖废水中的TCs残留量可达mg·L−1级别,在畜禽养殖排污口及周边水体则为几到几十μg·L−1级[6]。目前,废水中四环素类抗生素的去除手段主要分为以物化过程为主的常规处理工艺[7](如混凝、沉淀、消毒、过滤等)和深度处理工艺(如吸附、高级氧化、离子交换、生物处理和膜技术等)[8]。相比其他处理方法,微生物处理法成本低,易控制,条件简单,适用广,是去除废水中TCs的理想措施。TCs具有生物抑制作用,所以可生化性较差。零价铁(zero valence iron,ZVI)既是微生物的营养元素和高效催化剂,又是一种酶的激活剂[9],能提高有机物污染物的可生化性。A/O-MBR工艺易于延长污泥停留时间(sludge retention time,SRT),富集硝化细菌,提高污泥浓度,具有占地面积小、抗冲击负荷强[10]、对有毒污染物去除效率高等优点,因此,适用于畜禽养殖废水中TCs的去除。
本研究主要分析了盐酸四环素(tetracycline hydrochloride,TC-HCl)的降解特性,为废水中TC-HCl的归趋和环境行为的研究提供参考;同时利用零价铁与不锈钢网膜构成的原电池与传统A/O-MBR工艺相耦合,探究该工艺在畜禽养殖废水中TC-HCl净化处理中的适用性和优势,为畜禽养殖废水中TCs处理工艺的选择提供参考。
-
实验所用TC-HCl为阿拉丁试剂,纯度为96%,分子式为C22H25ClN2O8,相对分子质量为480.90,熔点为220~223 ℃,大鼠口服实验的半致死量为6 443 mg·kg−1。
-
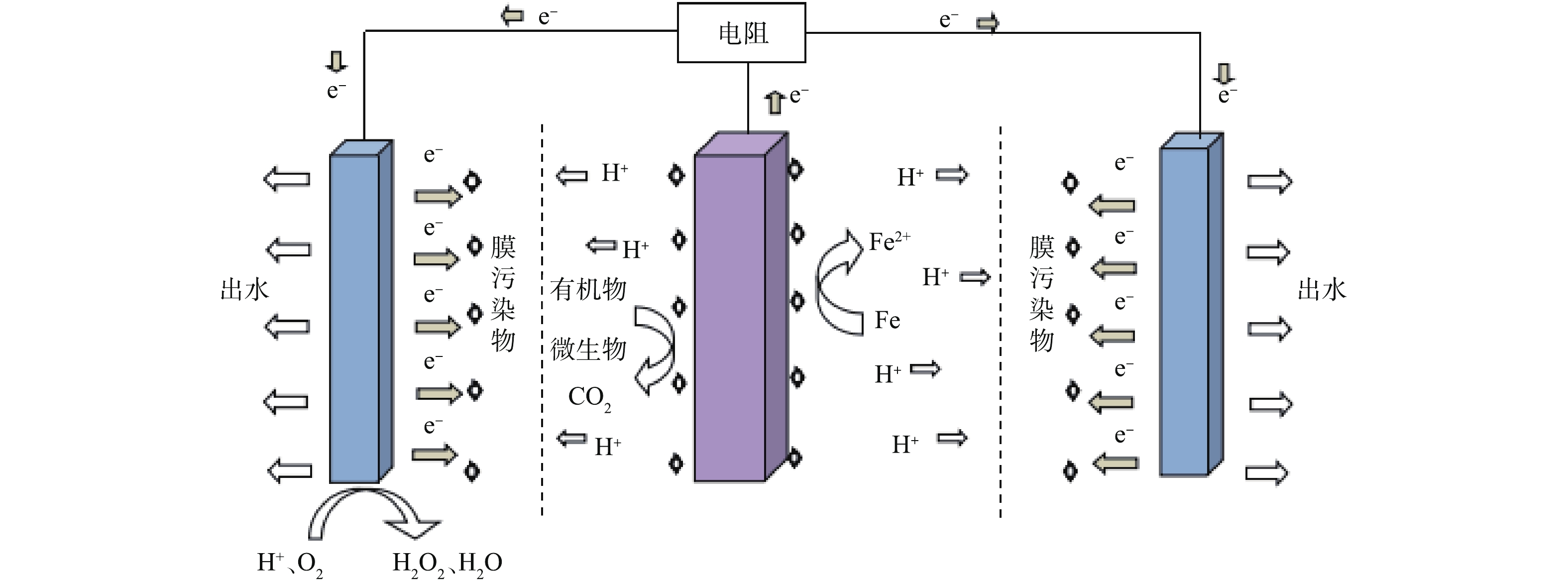
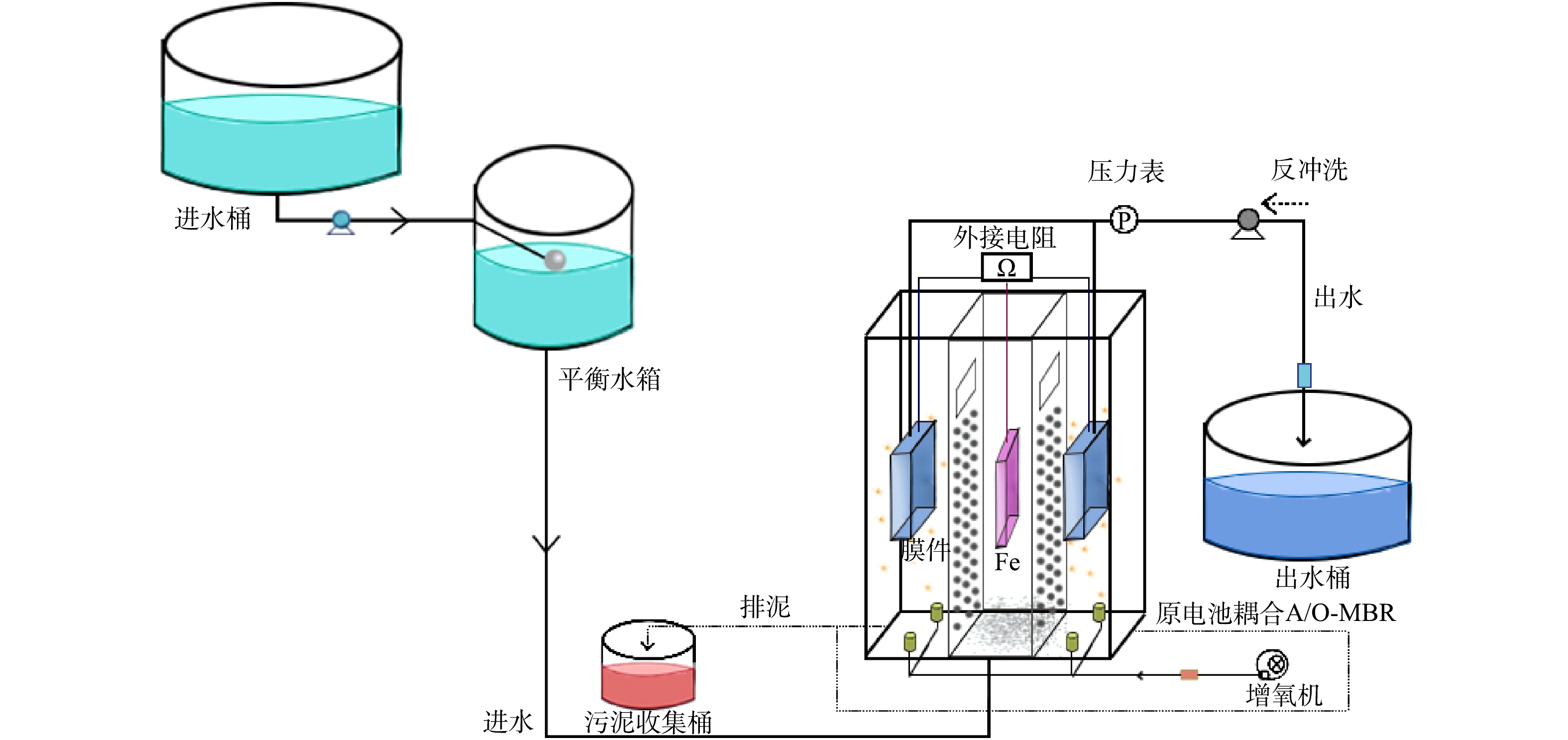
实验采用自主设计的原电池耦合A/O-MBR(见图1),反应器总体积为46 cm×28 cm×70 cm,好氧池与厌氧池的体积比为2∶1。厌氧池内置1块3 mm×200 mm×300 mm的铁片,底部填充有煤质柱状活性炭;好氧池内共置有4块有效膜面积为22.7 cm×17.5 cm的不锈钢网膜组件并填充以直径为15 mm的星型悬浮填料。铁片与不锈钢网膜间通过外接100 Ω电阻形成闭合回路。系统为底部进水,连续曝气,出水经不锈钢膜件过滤后抽出。实验通过投加蔗糖、氯化铵、磷酸二氢钾和盐酸四环素对畜禽养殖废水进行模拟,并维持进水COD、TN和TP分别为500、25和5 mg·L−1左右。实验混合液回流比为90%,水力停留时间(hydraulic retention time,HRT)为24 h,跨膜压差(transmembrane pressure,TMP)达到0.03 MPa时进行膜清洗。系统厌氧池(A池)与好氧池(O池)的电导率分别为826 μS·cm−1和658 μS·cm−1,开路电压为0.309 V,平均输出电压为0.164 V,功率密度为0.011 W·m−3。
构成原电池反应的实验原理如图2所示,厌氧阳极室在零价铁的氧化作用及微生物的产电作用下形成电子,好氧阴极室的氧气作为电子受体发生氧化还原反应。不锈钢膜件得电子后带负电,污染物(多带负电)不易吸附,与此同时,氧还原还可经二电子途径生成H2O2,原位去除附着在膜面上的污染物[11],有利于延缓膜污染,降低运行成本。
-
COD、NH3-N、TP、浊度的测定参考《水和废水监测分析方法》[12]。采用紫外可见分光光度法测定TC-HCl含量,检测方法准确性验证如下。
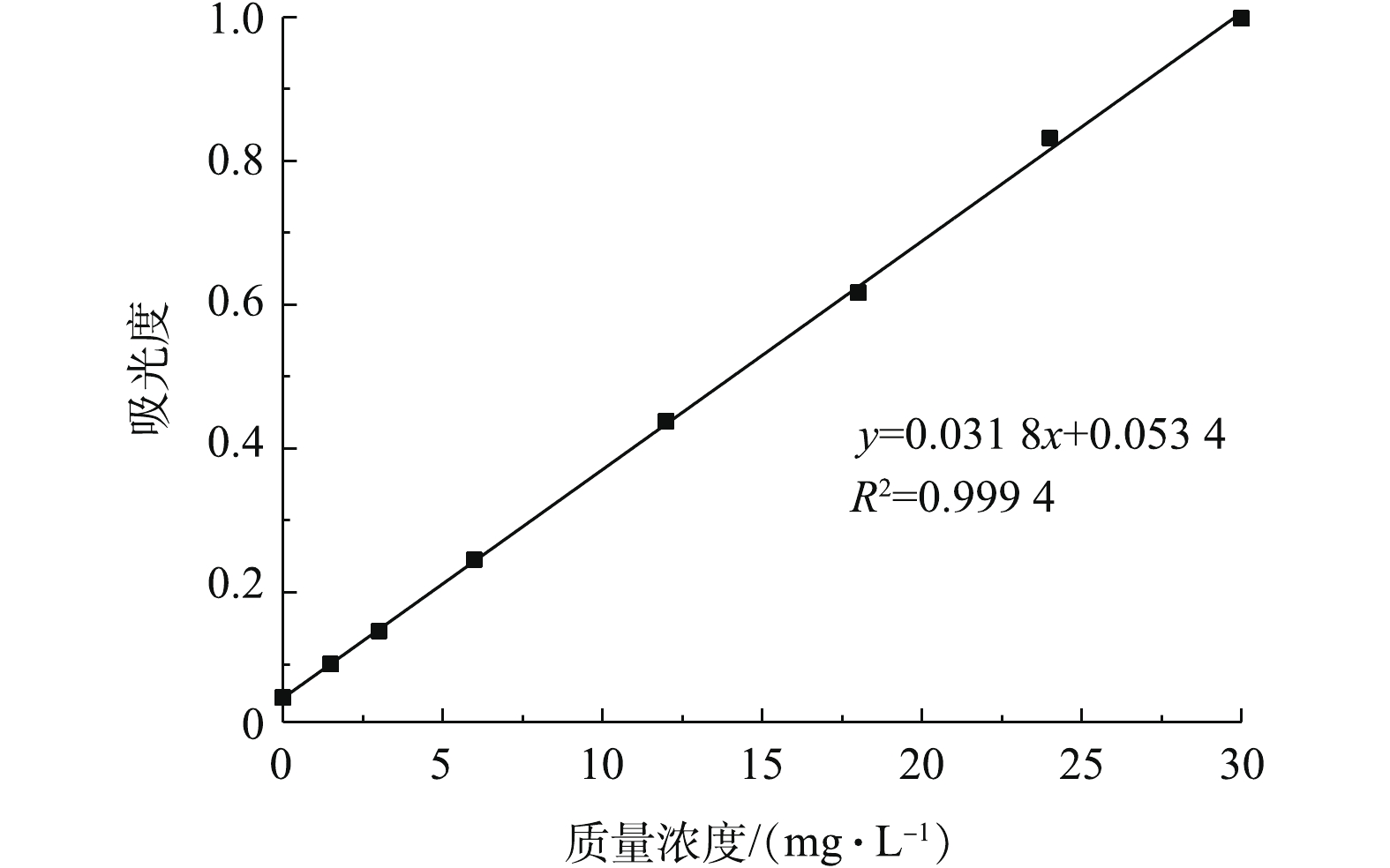
实验梯度配制不同质量浓度的TC-HCl标准溶液,测定356 nm下的吸光度,绘制标准工作曲线(见图3),对其进行线性拟合,R2为0.999 4,线性良好。
在不含抗生素的系统出水中,添加不同量的TC-HCl,进行回收率实验(见表1),实验结果显示,运用紫外分光光度法测定TC-HCl的平均回收率为97.45%~123.00%,相对标准偏差(n=6)为0.18%~4.15%。
以上结果表明,废水中可能含有的复杂物质成分对TC-HCl的检测无明显影响,可运用紫外分光光度法测定废水中的TC-HCl。
-
废水中的抗生素主要通过水解、光解以及微生物吸附降解等作用从水相中去除[13]。实验在250 mL的锥形瓶中进行,考察不同水质、温度、初始质量浓度和光照强度下TC-HCl的降解特性。以不含抗生素的模拟废水为溶剂,配置不同浓度的抗生素废水,密封置于恒温培养箱中,检测0、2、4、6、8、10、12、24、36、48、60 h时的TC-HCl含量。
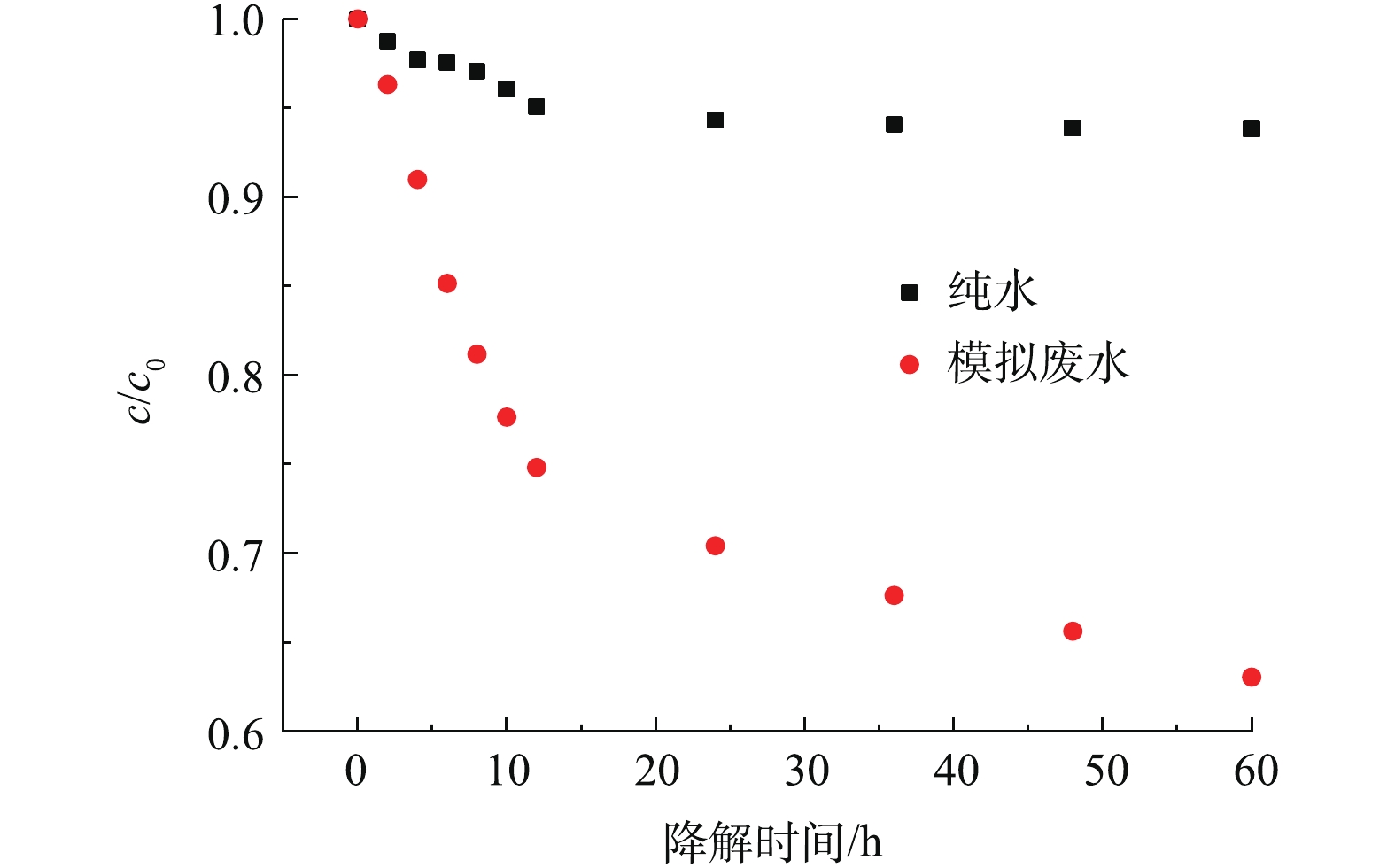
1)废水水质对TC-HCl降解效果的影响。当TC-HCl的初始质量浓度为30 mg·L−1时,在28 ℃下,恒温避光培养60 h后,考察废水水质对TC-HCl降解率的影响,结果如图4所示。不同水质下的TC-HCl降解速率差异显著(P<0.01),纯水中的降解度明显较低,最终降解率为6.20%。因纯水中不含微生物和营养元素,故TC-HCl主要发生水解反应;畜禽养殖废水中含有微生物和营养元素,TC-HCl可通过水解和微生物吸附分解作用从水相中去除,降解速率和降解率提高,最终降解率为36.95%。废水中的物质组成会影响TC-HCl的降解特性,微生物的吸附降解作用是水体中TC-HCl降解的重要途径。SELVAM等[14]研究发现,添加外源微生物,提高微生物活性可促进抗生素降解。许静等[15]研究土壤中5种磺胺类药物的降解情况发现,加入的外源微生物的吸附、降解作用是磺胺类药物在土壤中降解的主要途径。
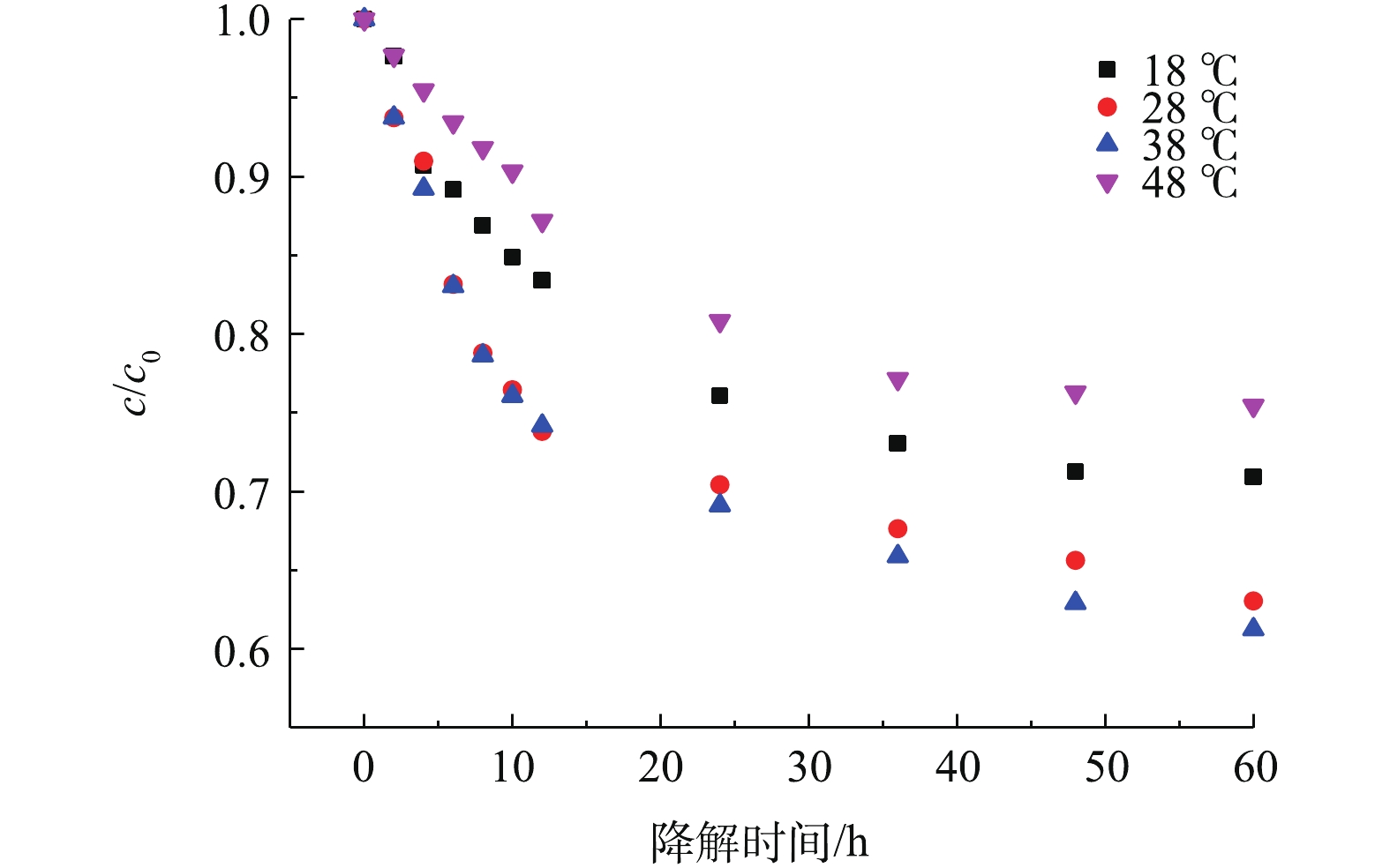
2)环境温度对TC-HCl降解效果的影响。抗生素废水中的优势菌群可通过水解、乙酰转化和氧化还原反应降解TCs[16],不同环境温度下微生物的活性不同。当畜禽养殖废水中的TC-HCl为30 mg·L−1时,分别于18、28、38、48 ℃下避光恒温培养60 h后,TC-HCl的降解情况如图5所示。18 ℃时,TC-HCl降解较为缓慢,降解率为29.07%。温度上升,微生物活性增强,对抗生素的吸附转化能力增强,TC-HCl的降解速率和降解率增大。温度是影响微生物生长发育的重要生态因子,根据SHELEFORD耐性定律[17]可知,任何一个生态因子对生物都存在最大和最小临界阈。在稳态条件下,当这种生态因子超过某种生物的耐受限度时,该生物就会受到损伤或无法生存[17]。继续升高温度至48 ℃,TC-HCl的降解速率和降解率下降,最终降解率为24.55%。由此可见,微生物对TC-HCl的吸附降解作用适于在较低温度下进行,TC-HCl优势菌群的最适生长温度应该为28~38 ℃。徐伊婷等[18]研究发现,经多次富集培养和筛选后得到的7株具四环素降解力的菌株,它们对四环素的降解率随着环境温度的增大,表现出缓慢上升(20~30 ℃)-稳定(30~35 ℃)-急速下降(35~40 ℃)的趋势。吴学玲等[19]在研究筛选出的1株四环素降解菌(拉乌尔菌属)降解性受温度的影响时发现,不同温度下,菌株的降解效能表现为25 ℃>30 ℃>35 ℃>20 ℃>40 ℃,当温度为25~35 ℃时,菌株降解性能较优。
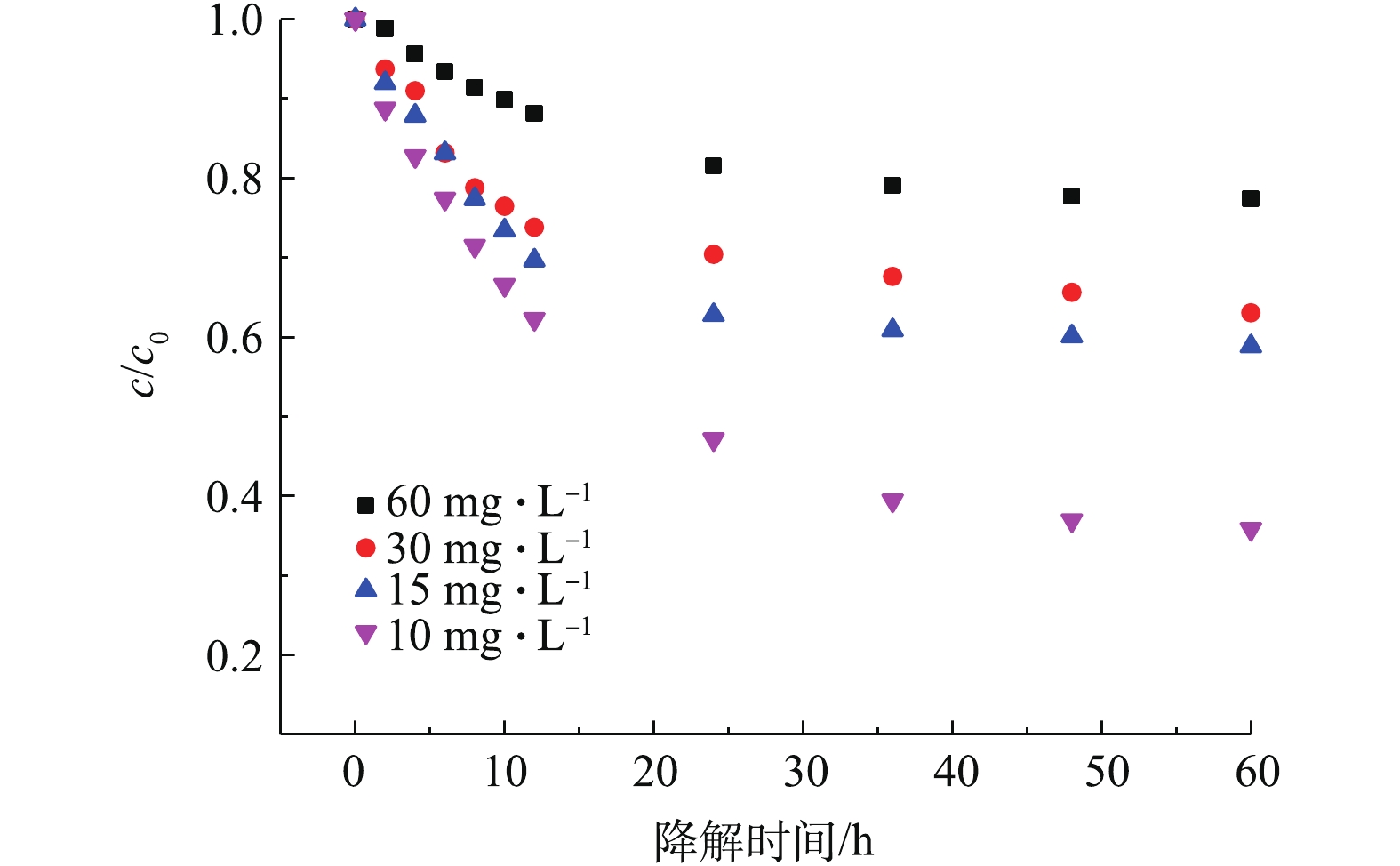
3)初始质量浓度对TC-HCl降解效果的影响。TC-HCl具有生物抑制性,不同初始质量浓度下的微生物活性不同。当畜禽养殖废水中TC-HCl的初始质量浓度分别为10、15、30、60 mg·L−1时,TC-HCl的降解情况如图6所示。在28 ℃避光恒温密封条件下,TC-HCl的降解率随着降解时间的延长而增大,前24 h降解最快,60 h后的降解率分别为64.15%、41.14%、36.95%和22.60%。当初始质量浓度为10 mg·L−1时,TC-HCl的降解率最大,浓度增大,TC-HCl的降解率和降解速率下降。生物降解和污泥吸附是TCs生物处理法的主要去除途径[20],TC-HCl会抑制厌氧微生物活性且浓度越高,抑制作用越强[21]。所以,运用微生物修复法处理废水中的TC-HCl时,应注意控制废水中TC-HCl的初始质量浓度。
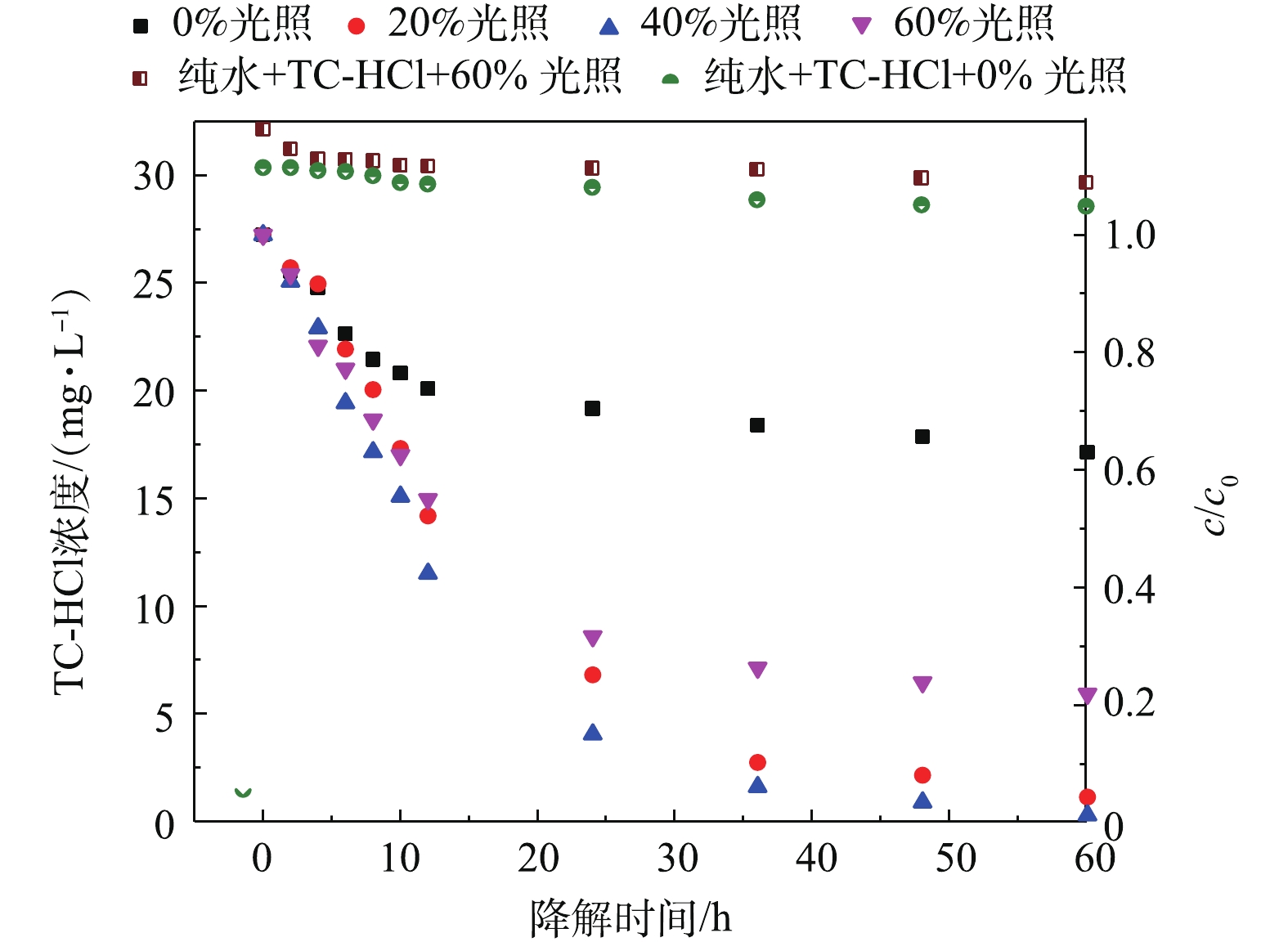
4)光照对TC-HCl降解效果的影响。光解是抗生素降解的途径之一。当光照强度分别为0%、20%、40%、60%时,模拟废水中TC-HCl的初始质量浓度为30 mg·L−1,在28 ℃下,恒温培养60 h,实验结果如图7所示。避光条件下,TC-HCl的降解率最低,为36.95%。当光照强度分别为20%、40%、60%时,TC-HCl降解率分别为95.66%、98.71%、78.09%。可见20%~40%的光照条件可以大幅促进废水中TC-HCl的降解,继续增大光照强度至60%,促进作用减弱。结合纯水中30 mg·L−1的TC-HCl在0%和60%光照下浓度的变化情况可知,在纯水中,光照并不影响TC-HCl的降解情况。这可能是因为,实验所用光照培养箱中的灯管为三基色直管荧光灯,培养对象所能吸收到的光波长多为≥400 nm的可见光,而纯水中的TC-HCl对大于400 nm的光几乎没有吸收,所以光照对纯水中TC-HCl的稳定性没有明显作用。在废水中,物质组成复杂,很多天然水体成分(如
NO−3 、Fe2+、Cl−、CO2−3 、SO2−4 、Ca2+、Me2+和可溶性有机质(DOM)等)对抗生素的直接与间接光解都有直接影响,如其中的DOM可通过滤光作用、吸附作用和DOM光致活性物种的产生影响抗生素降解;Ca2+和Me2+会与抗生素络合,从而影响其降解;Cl−可通过促进抗生素自敏化产生1O2,促进抗生素光解;水体中的不同物质成分对不同类别抗生素的光解影响具有很大的差异,这种差异与抗生素的结构、光解途径及产生的活性物种相关[22]。因此,模拟废水中TC-HCl的降解受光照影响较大。废水中抗生素的降解过程多符合一级反应动力学。计算方法[23-24]如式(1)所示。
式中:Ct为t时刻废水中的抗生素浓度,mg·L−1;C0为初始抗生素浓度,mg·L−1;K为反应速率常数,t为反应时间,h。
将TC-HCl的降解过程进行拟合,拟合效果较好(见表2)。避光条件下,TC-HCl的半衰期仅为6.4 h,可在最短的时间内达到降解平衡,但平衡时的浓度最高,降解率最小。在不同光照条件下,TC-HCl的半衰期随光照强度的增大,先增大后减小,平衡时的浓度先减小后增大。实验过程中发现,模拟废水中的TC-HCl在20%和40%光照下,培养一段时间后,溶液呈透亮的玫红色,60%光照下的溶液呈混浊的浅红色,0%光照下的溶液则为白色浊状。由此可见,在不同光照强度下,TC-HCl的降解机理有所不同;20%~40%光照下,DOM的滤光和吸附作用较弱,主要通过光致活性物种的产生影响TC-HCl的降解,
NO−3 、Fe2+、Cl−、CO2−3 等则可通过影响光解作用来影响TC-HCl的降解;60%光照下的溶液浊度随培养时间的延长而增大,DOM吸附作用增大的同时,滤光作用也增大,光照的促进作用下降甚至消失,平衡浓度较高。综上可知,畜禽养殖废水中的TC-HCl可通过微生物处理法去除。废水中TC-HCl降解的最适温度为28~38 ℃,最适光照强度为20%~40%。运用生物修复法处理TC-HCl时应注意控制TC-HCl的初始质量浓度。
-
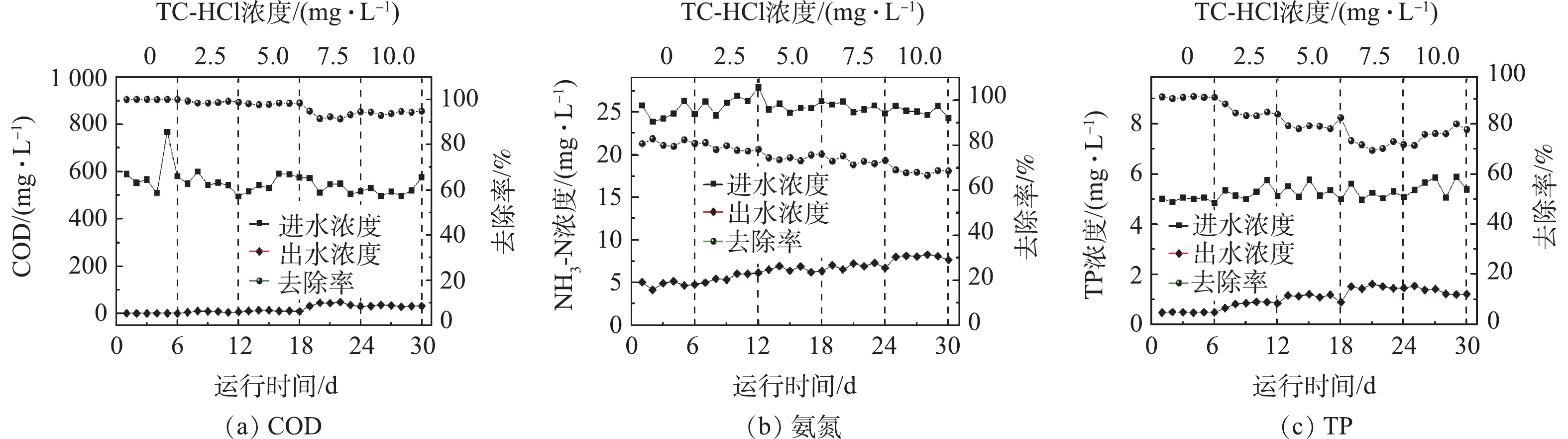
1) TC-HCl对原电池耦合A/O-MBR工艺运行稳定性的影响。实验利用原电池耦合A/O-MBR工艺去除含TC-HCl的畜禽养殖废水,考察TC-HCl初始质量浓度分别为0、2.50、5.00、7.50、10.00 mg·L−1时系统对COD、NH3-N和TP的24 h去除率,分析TC-HCl对系统运行稳定性的影响。实验结果如图8所示,当进水中不含TC-HCl时,系统的COD、NH3-N及TP去除率分别为99.87%(出水COD为0.776 mg·L−1)、80.85%(出水NH3-N浓度4.767 mg·L−1)和90.46%(出水TP浓度0.474 mg·L−1),去除效果良好,出水水质符合《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A的排放标准。在进水中添加TC-HCl后,系统NH3-N和TP的去除率与对照组间具有显著差异(P<0.01)。进水TC-HCl浓度增大,系统NH3-N去除率缓缓下降,当TC-HCl为10 mg·L−1时,系统NH3-N去除率最低(67.95%)。系统运行前期,TP去除率受TC-HCl的影响最大,TC-HCl为7.5 mg·L−1时,TP去除率达到最低(71.40%),TC-HCl浓度为10.0 mg·L−1时,TP去除率为76.04%,可见系统对废水中的TC-HCl具有一定的适应性。当TC-HCl浓度≤5.0 mg·L−1时,增大TC-HCl浓度,系统的COD去除率无显著性差异(P1=0.011,P2=0.117),进一步增大TC-HCl浓度,系统COD去除率明显下降,一段时间后又能维持新的稳定(TC-HCl浓度为7.5 mg·L−1和10.0 mg·L−1时,COD去除率无显著性差异(P=0.012>0.01)。
综上可知,原电池耦合A/O-MBR工艺具有良好的去污效能,添加TC-HCl对系统脱氮除磷作用具有显著抑制性,对COD去除率的影响较小。余忻[25]研究发现,抗生素废水的生物毒性与COD、NH3-N的Spearman相关性显著。李娟英等[26]研究TCs对硝化污泥的抑制作用发现,TCs会抑制硝化污泥表面保护膜的形成,使活性污泥细胞破裂、解体,从而导致硝化速率迅速降低。胡哲太等[27]研究表明,土霉素容易抑制好氧吸磷作用(类属TCs),对生物除磷具有显著的抑制作用。因为生物脱氮除磷过程繁复,涉及氨氧化细菌、硝化细菌、亚硝化细菌、反硝化细菌以及释磷菌和聚磷菌等一系列微生物[28],这些微生物对TC-HCl的耐受性都会影响系统脱氮除磷效率的受抑制程度。所以,系统脱氮除磷作用受TC-HCl的影响较大。
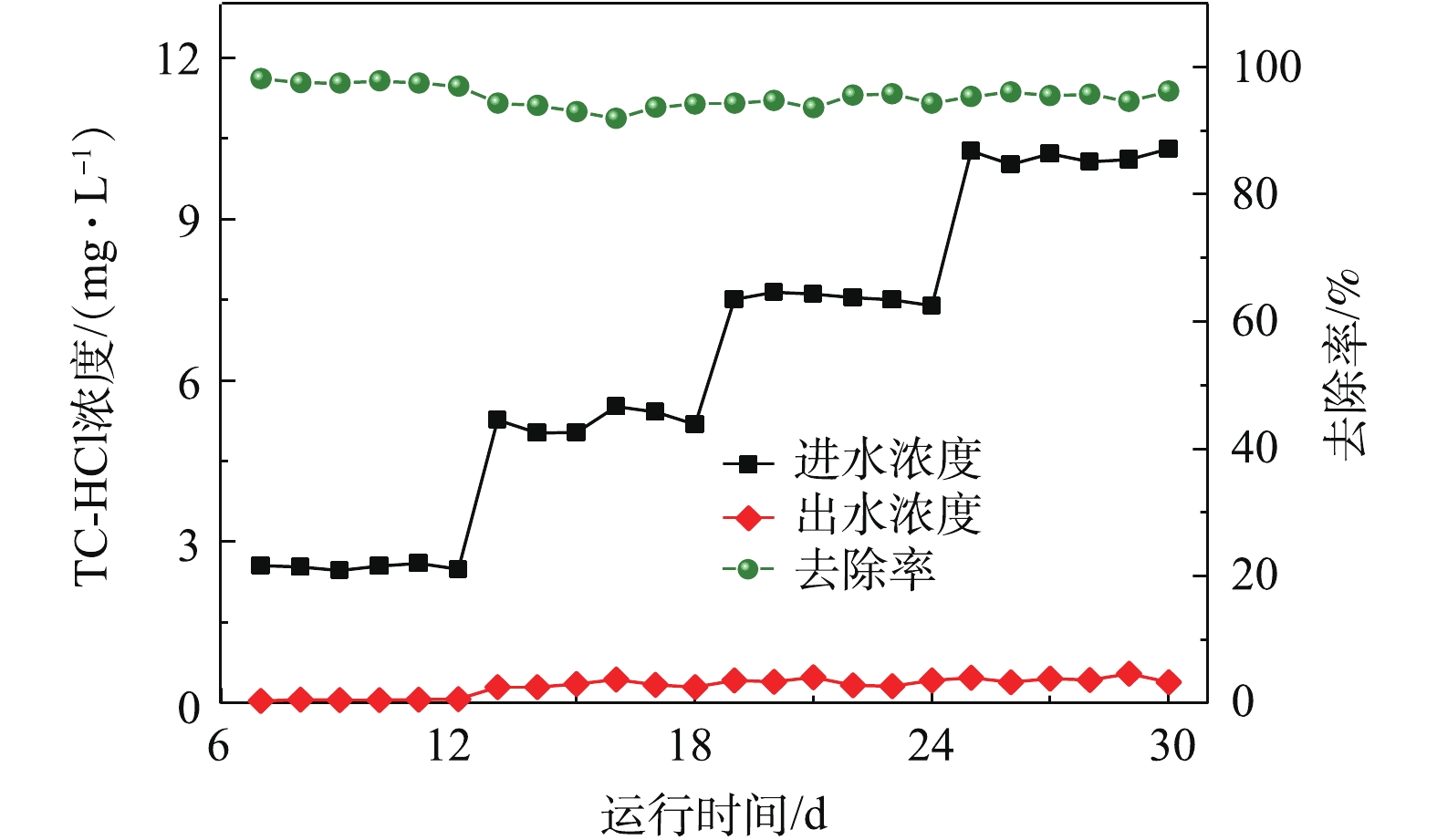
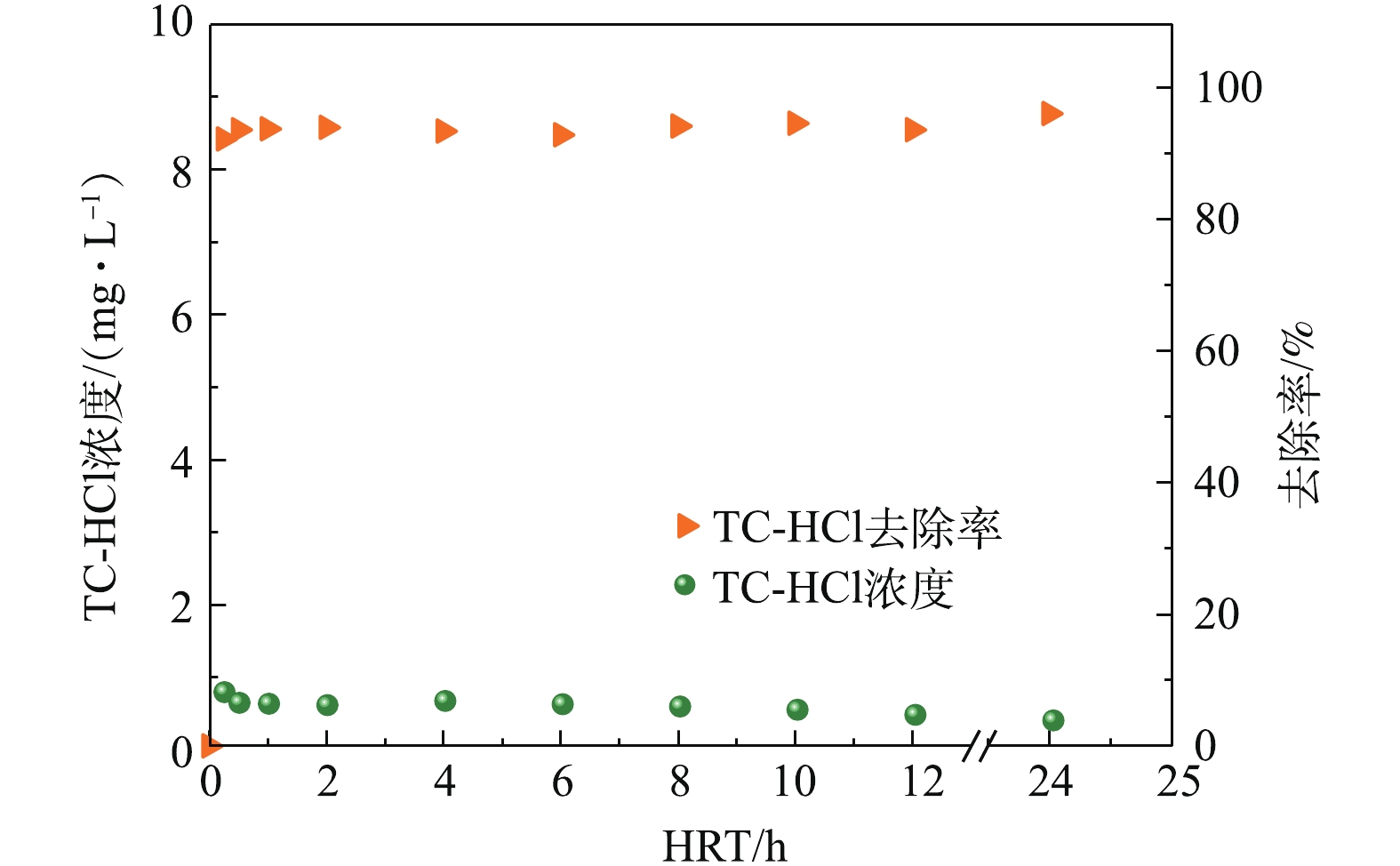
2)原电池耦合A/O-MBR对TC-HCl的去除效能。活性污泥对疏水性有机物TCs具有良好的吸附作用,是TCs在污泥中迁移转化和从污水中去除的主要方式,污泥吸附性能受初始质量浓度影响[29]。由图9可知,系统对初始质量浓度≤10.00 mg·L−1的TC-HCl的去除率均高于90%,去除效果良好。TC-HCl浓度由2.50 mg·L−1上升至5.00 mg·L−1时,TC-HCl去除率下降了3.42%,进一步增大浓度,TC-HCl去除率缓缓上升。TC-HCl浓度由7.50 mg·L−1上升至10.00 mg·L−1时,TC-HCl去除率无显著性差异(P=0.109>0.01)。在原电池耦合A/O-MBR工艺中,TC-HCl的去除主要通过活性污泥与活性炭的物理吸附作用和微生物的降解作用实现,在一定范围内,TC-HCl越大,活性污泥与活性炭的平衡吸附量越大。姜忠帅[30]发现,增大四环素浓度,可提高载铁活性炭对四环素的平衡吸附量,但增大到一定程度后,活性炭的平衡吸附量基本稳定。刘春燕等[31]的研究则表明,TCs初始浓度增大,活性污泥对TCs的吸附量增大,吸附速率降低,出水浓度增大。所以,增大TC-HCl浓度,一定程度上有利于活性炭和微生物的物理吸附,但四环素对活性污泥脱氢酶的产生具有明显的抑制作用,浓度越大,生物抑制作用越强[32],微生物降解作用减弱。可见,当TC-HCl浓度≥5.00 mg·L−1时,物理吸附在TC-HCl的去除中起主导作用。
实验考察了不同HRT下系统对TC-HCl的去除情况。由图10可知,当TC-HCl的初始质量浓度为10.00 mg·L−1时,系统对TC-HCl的15 min去除率可达92.02%,延长系统HRT,TC-HCl去除率在95%左右。TC-HCl在污水生物处理中的吸附作用显著,可通过表面络合、静电吸附和离子交换作用被活性污泥所吸附[33],从而从水相中去除。进水前期,活性炭和活性污泥中的吸附位点多,吸附速率快,随后吸附逐渐饱和,吸附速率趋近为零,吸附总量趋于平稳。
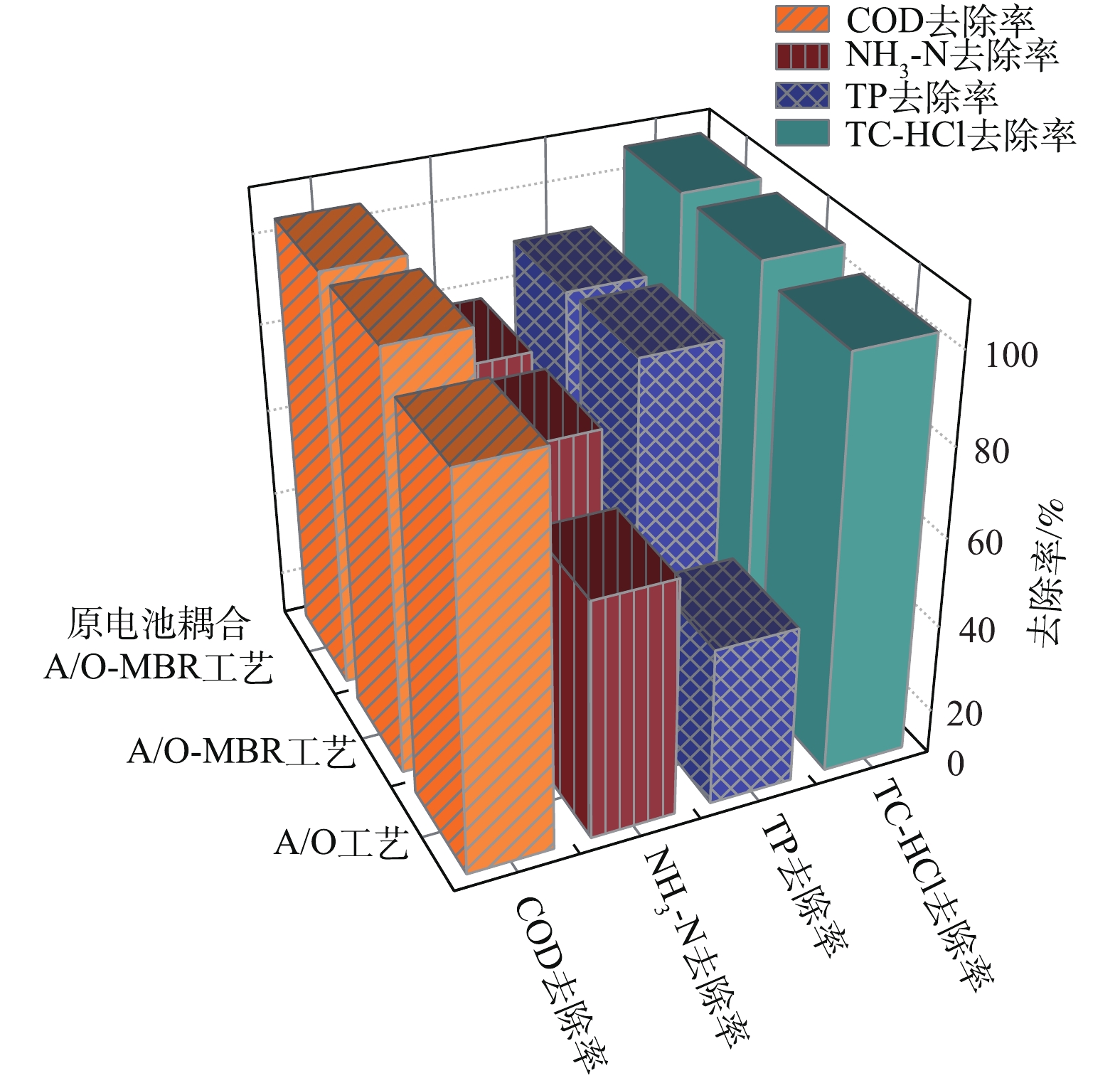
3)各工艺在系统运行过程中的效用。原电池耦合A/O-MBR工艺是糅合了A/O工艺、MBR工艺和电化学作用的新型集成工艺,为探究不同组合工艺的净化效能,实验维持TC-HCl的初始质量浓度为10 mg·L−1左右,连续运行6 d,测定开/闭路下A/O-MBR工艺和传统A/O工艺下系统进出水中主要污染物的含量,分析原电池耦合A/O-MBR工艺的运行优势。由图11可知,传统A/O工艺对COD和TC-HCl具有较好的去除效果,但氨氮和总磷去除率仅为53.82%和35.80%。耦合了MBR后的A/O工艺脱氮除磷效能分别提升至67.45%和80.93%。因为A/O工艺与MBR耦合之后,在膜的截留作用下,可实现SRT和HRT的分离,延长污泥泥龄,富集世代周期较长的硝化细菌和亚硝化细菌,增强硝化作用[34],提高氨氮去除率。而测定水中总磷时取的是包括悬浮物的混合水样[12],实验中A/O工艺的出水浊度为58.66 NTU,经A/O-MBR工艺膜滤作用后的出水浊度为32.90 NTU,有效去除了部分悬浮物,降低了出水TP浓度,提高了出水水质。开/闭路条件下的系统去污效能无显著性差异(P>0.01),但传统A/O-MBR工艺在运行过程中膜污染问题严重,运行成本较高,运用受限[35-36],将A/O-MBR工艺与原电池相耦合用于延缓膜污染具有一定的理论支撑。
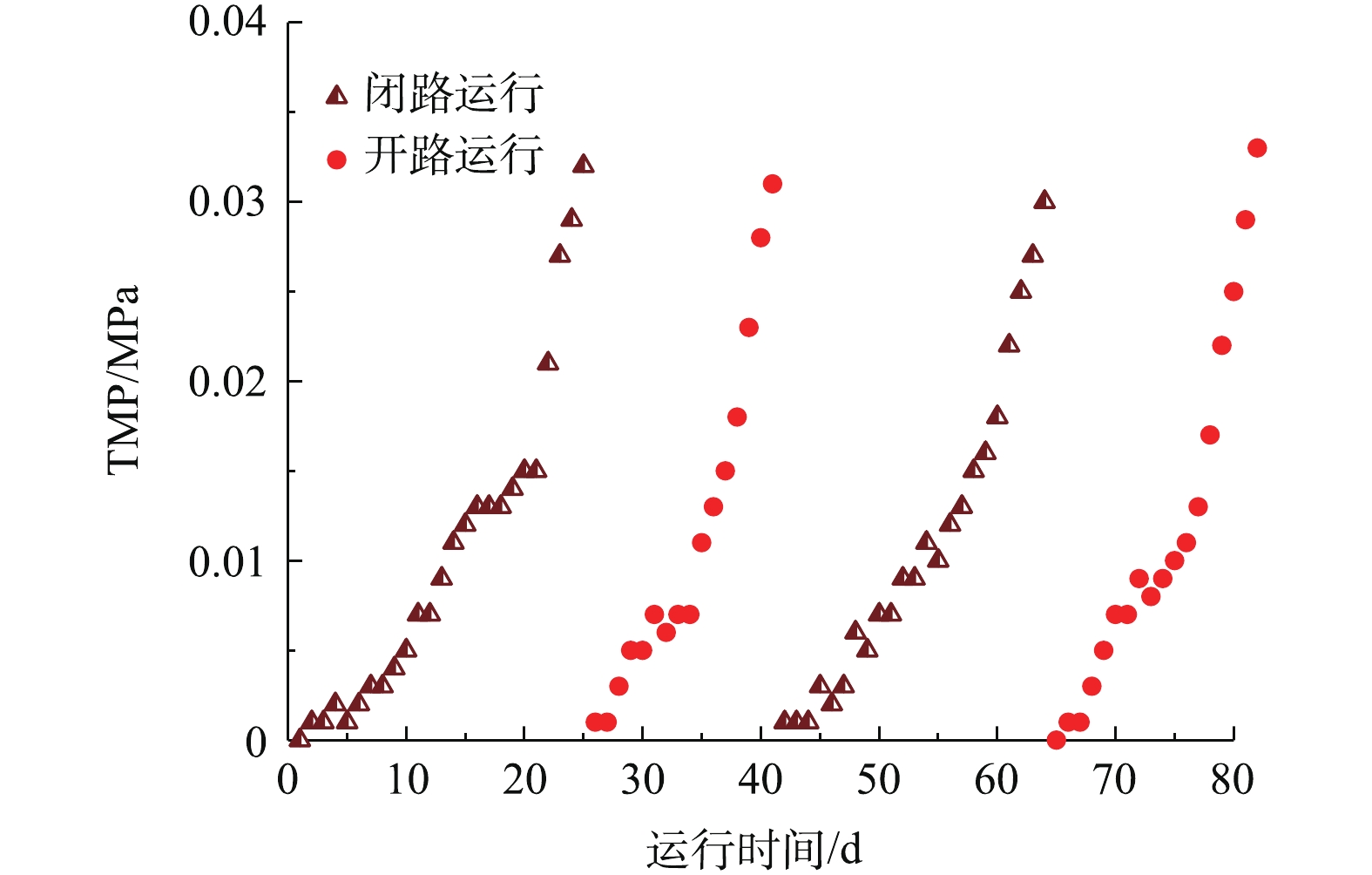
为探究耦合原电池对A/O-MBR工艺膜污染的影响,实验通过交替开/闭路的方式运行A/O-MBR工艺,由运行过程中跨膜压差(TMP)的变化,判断膜件的污染状况。由图12中TMP的变化趋势可知,系统在开路运行时,TMP的增长速度较快,在17 d左右,就可达到0.03 MPa。在闭路运行时,膜件的污染周期延长至24 d左右。根据膜污染的3阶段理论,膜污染过程分为初始污染、缓慢污染和快速污染3个阶段[37]。系统开/闭路下的TMP变化差异主要体现在前2个阶段。在闭路时,膜件因耦合原电池的作用表面带负电,与同样带负电荷的污染物间存在静电排斥作用,在前2个污染阶段,微生物不易附着在膜面上,有利于延缓膜污染[38]。随着系统的运行,微生物不断附着在膜面上,耦合原电池不再影响膜污染状况,TMP值迅速增大。
-
1)当环境温度为28~38 ℃、光照强度为20~40%时,废水中的TC-HCl可通过水解、光解及微生物吸附降解等作用从水相中去除;微生物的吸附分解作用是去除水体中TC-HCl的重要途径,可应用生物处理法去除畜禽养殖废水中的TC-HCl。
2)当原电池耦合A/O-MBR工艺的进水COD、TN和TP分别为500、25、5 mg·L−1时,系统出水水质可达《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A的标准;在进水中添加TC-HCl后,系统的脱氮除磷作用明显受抑制,但经短期驯化后可逐步适应;当TC-HCl的初始质量浓度为10.00 mg·L−1时,系统对TC-HCl的15 min去除率即可达92.02%,去除效果良好。
3) A/O-MBR工艺可明显强化传统A/O工艺的脱氮除磷效能;耦合原电池后,A/O-MBR工艺的膜件与污染物之间存在静电排斥力,有效延缓了膜污染,膜污染周期可提升至24 d左右。
原电池耦合A/O-MBR工艺去除畜禽养殖废水中的盐酸四环素
Removing tetracycline hydrochloride from livestock and poultry breeding wastewater by the coupling process of galvanic cell and A/O-MBR
-
摘要: 以畜禽养殖废水中的盐酸四环素(TC-HCl)为目标污染物,研究其在水环境中的降解特性,利用原电池与传统A/O-MBR工艺相耦合,去除水中的TC-HCl,并考察其效果。结果表明:废水中的物质组成、环境温度、TC-HCl初始质量浓度以及光照强度均会影响水体中TC-HCl的降解情况;TC-HCl的初始质量浓度为30 mg·L−1,在28 ℃、40%光照下恒温培养60 h后的降解率为98.70%,降解过程符合一级反应动力学(R2=0.991),半衰期为10.7 h。原电池耦合A/O-MBR工艺的进水COD、NH3-N和TP分别为500、25、5 mg·L−1时,系统出水水质可达《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准;对10.00 mg·L−1的TC-HCl,系统15 min去除率可达92.02%。A/O-MBR工艺可明显强化传统A/O工艺的脱氮除磷效能;耦合原电池可将膜污染周期提升至24 d左右,有效延缓膜污染。
-
关键词:
- 畜禽养殖废水 /
- 盐酸四环素 /
- 降解特性 /
- 原电池耦合A/O-MBR工艺
Abstract: Tetracycline hydrochloride (TC-HCl), one of the most detected antibiotics in livestock and poultry breeding wastewater, was taken as the target pollutant to study its degradation characteristics in the water environment. The coupling process of galvanic cell and the traditional A/O-MBR was used to remove TC-HCl from the simulated wastewater. The results showed that wastewater composition, ambient temperature, the initial mass concentration of TC-HCl and the light intensity affected on the degradation of TC-HCl in the wastewater. The degradation rate of TC-HCl with initial concentration of 30 mg·L−1 was 98.70% under 60 h thermostatic incubation conditions at 28 ℃ and 40% illumination. The degradation process followed the first-order reaction kinetics (R2=0.991), and the half-life was 10.7 h. When the influent concentration of COD, NH3-N and TP were 500, 25, 5 mg·L−1, respectively, the effluent water quality of the coupling process could meet the first level A criteria specified in Discharge Standard of Pollutants for Municipal Wastewater Treatment Plants (GB 18918-2002). After 15min treatment by the coupling process, the removal rate of TC-HCl with initial concentration of 10 mg·L−1 could reach 92.02%. The A/O-MBR process could significantly enhanced the nitrogen and phosphorus removal efficiency of the traditional A/O process. The coupled galvanic cell could extended the membrane pollution cycle to 24 d, which could effectively delay membrane fouling. -
表 1 系统出水检测方法的回收率(n=6)
Table 1. Recovery rate of detection method for system effluent (n=6)
序号 已知量/(mg·L−1) 添加量/(mg·L−1) 测得量/(mg·L−1) 回收率/% 相对标准偏差/% 1 0 0.9 1.107 123.00 4.15 2 0 1.5 1.775 118.33 1.77 3 0 3.0 3.409 113.63 0.53 4 0 6.0 6.331 105.52 1.31 5 0 12.0 11.986 99.88 0.79 6 0 15.0 14.814 98.76 0.37 7 0 18.0 18.050 100.28 0.92 8 0 24.0 23.611 98.38 0.54 9 0 27.0 26.815 99.31 0.18 10 0 30.0 29.234 97.45 0.29 表 2 光照下TC-HCl的一级动力学方程及参数
Table 2. First-order kinetic equation and parameters of TC-HCl under illumination conditions
光照/% 一级动力学方程 K t1/2/h R2 质量浓度/(mg·L−1) 0 Ct=11.28e−0.109 0t+20.94 0.109 0 6.4 0.977 30 20 Ct=32.04e−0.050 7t−1.09 0.050 7 13.7 0.986 30 40 Ct=31.92e−0.064 7t−1.16 0.064 7 10.7 0.991 30 60 Ct=25.70e−0.068 5t+6.09 0.068 5 10.1 0.994 30 -
[1] GUO T, LOU C L, ZHAI W W, et al. Increased occurrence of heavy metals, antibiotics and resistance genes in surface soil after long-term application of manure[J]. Science of the Total Environment, 2018, 635(19): 995-1003. [2] BERENDSEN B J A, LAHR J, NIBBELING C, et al. The persistence of a broad range of antibiotics during calve, pig and broiler manure storage[J]. Chemosphere, 2018, 204(15): 267-276. [3] 邱美珍, 谢菊兰, 任慧波, 等. 畜禽粪污中残留抗生素降解方法进展[J]. 激光生物学报, 2018, 27(4): 308-312. doi: 10.3969/j.issn.1007-7146.2018.04.003 [4] 李刚, 颜智勇, 谭秀益, 等. 畜禽养殖废水中抗生素检测技术研究进展[J]. 绿色科技, 2011(11): 97-99. doi: 10.3969/j.issn.1674-9944.2011.11.051 [5] 王瑞, 魏源送. 畜禽粪便中残留四环素类抗生素和重金属的污染特征及其控制[J]. 农业环境科学学报, 2013, 32(9): 1705-1719. doi: 10.11654/jaes.2013.09.002 [6] 张杏艳, 陈中华, 邓海明, 等. 水环境中四环素类抗生素降解及去除研究进展[J]. 生态毒理学报, 2016, 11(6): 44-52. [7] 陈凯杰. 试论饮用水中抗生素去除技术研究进展[J]. 科技经济导刊, 2018, 26(8): 103-105. [8] 朱学武, 成小翔, 甘振东, 等. 饮用水中抗生素去除技术研究进展[J]. 给水排水, 2017, 53(5): 135-141. doi: 10.3969/j.issn.1002-8471.2017.05.034 [9] 薛顺利, 刘振鸿, 李响, 等. 零价铁对餐厨垃圾与剩余污泥联合发酵产乳酸的影响[J]. 环境工程, 2017, 35(4): 106-110. [10] 程永伟, 武彦生, 高雄, 等. A/O+MBR组合工艺处理方便面厂生产废水[J]. 中国给水排水, 2018, 34(2): 103-106. [11] WANG Y K, LI W W, SHENG G P, et al. In-situ utilization of generated electricity in an electrochemical membrane bioreactor to mitigate membrane fouling[J]. Water Research, 2013, 47(15): 5794-5800. doi: 10.1016/j.watres.2013.06.058 [12] 国家环境保护总局. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002. [13] 陈小丽, 魏金华, 蔺中, 等. 抗生素的微生物降解研究进展[J]. 现代农业科技, 2018(16): 167-168. doi: 10.3969/j.issn.1007-5739.2018.16.104 [14] SELVAM A, ZHAO Z Y, LI Y C, et al. Degradation of tetracycline and sulfadiazine during continuous thermophilic composting of pig manure and sawdust[J]. Environmental Technology, 2013, 34(16): 2433-2441. doi: 10.1080/09593330.2013.772644 [15] 许静, 王娜, 孔德洋, 等. 有机肥源磺胺类抗生素在土壤中的降解规律及影响因素分析[J]. 环境科学学报, 2015, 35(2): 550-556. [16] 郑茂佳, 张恩栋, 孙静茹, 等. 四环素类抗生素生物降解研究进展[J]. 天津农业科学, 2018, 24(6): 72-76. doi: 10.3969/j.issn.1006-6500.2018.06.018 [17] 任南琪, 马放. 污染控制微生物学[M]. 哈尔滨: 哈尔滨工业大学出版社, 2002. [18] 徐伊婷, 李思雨, 祝溢靖, 等. 四环素降解菌的筛选及其降解特性[J]. 浙江树人大学学报(自然科学版), 2017, 17(3): 17-21. [19] 吴学玲, 吴晓燕, 李交昆, 等. 一株四环素高效降解菌的分离及降解特性[J]. 生物技术通报, 2018, 34(5): 172-178. [20] 张鹏飞, 刘晓文, 李杰, 等. 养殖废水中抗生素去除处理工艺的研究现状[J]. 净水技术, 2018, 37(4): 60-65. [21] 解永磊. UASB-A/O-Fenton组合工艺处理四环素类抗生素废水试验研究[D]. 天津: 天津理工大学, 2015 [22] 代志峰, 邰超, 张少栋, 等. 天然水体溶解性物质对5种抗生素光解的影响[J]. 中国环境科学, 2018, 38(6): 2273-2282. doi: 10.3969/j.issn.1000-6923.2018.06.030 [23] 王攀攀, 袁巧霞, 周文兵. 光催化降解沼液中四环素类抗生素效果及反应动力学研究[J]. 农业工程学报, 2018, 34(23): 193-198. doi: 10.11975/j.issn.1002-6819.2018.23.024 [24] 赵亚奇. A/O-MBR工艺对废水中抗生素的去除效能研究[D]. 哈尔滨: 哈尔滨工业大学, 2017. [25] 余忻. 抗生素废水的生物毒性与微生物耐药性及其控制技术研究[D]. 北京: 清华大学, 2014. [26] 李娟英, 胡谦, 陈美娜, 等. 抗生素类污染物对硝化污泥的生物抑制[J]. 环境工程学报, 2015, 9(7): 3325-3331. doi: 10.12030/j.cjee.20150741 [27] 胡哲太, 孙培德, 王如意, 等. 两类抗生素对EBPR系统的短期生物抑制作用实验研究[J]. 环境科学学报, 2017, 37(5): 1722-1731. [28] 马娟, 周猛, 俞小军, 等. 抗生素在污水生物脱氮除磷中的抑制效应[J]. 中国抗生素杂志, 2019, 44(2): 179-185. doi: 10.3969/j.issn.1001-8689.2019.02.005 [29] 宋现财. 四环素类抗生素在活性污泥上的吸附规律及其机理研究[D]. 天津: 南开大学, 2014. [30] 姜忠帅. 载铁活性炭同步去除水中四环素和铜的研究[D]. 南京: 东南大学, 2017. [31] 刘春燕, 解满俊, 许时良, 等. 活性污泥对四环素类抗生素的吸附特性研究[J]. 上海海洋大学学报, 2012, 21(4): 581-588. [32] 于洁. 四环素对好氧活性污泥的抑制及对活性污泥四环素抗性的影响研究[D]. 天津: 南开大学, 2014. [33] 张翔宇, 李茹莹, 季民. 污水生物处理中抗生素的去除机制及影响因素[J]. 环境科学, 2018, 39(11): 5276-5288. [34] 刘艳阳. 电凝聚强化A/O-MBR脱氮除磷实验研究[D]. 沈阳: 东北大学, 2014. [35] 黄丽坤, 王广智, 韩利明, 等. 悬浮载体复合MBR工艺处理电镀废水效能研究[J]. 中国环境科学, 2018, 38(7): 2490-2497. doi: 10.3969/j.issn.1000-6923.2018.07.013 [36] ISHIZAKI S, TERADA K, MIYAKE H, et al. Impact of anodic respiration on biopolymer production and consequent membrane fouling[J]. Environmental Science and Technology, 2016, 50(17): 9515-9523. doi: 10.1021/acs.est.6b00728 [37] 袁树森. 化学除磷-A/O-MBR组合工艺处理玉米深加工废水的效能研究[D]. 长春: 长春工程学院, 2018. [38] 印霞棐, 李秀芬, 华兆哲, 等. 不同电极间距下自生电场膜生物反应器中的膜污染行为分析[J]. 化工进展, 2018, 37(11): 4485-4492. -




 下载:
下载: