-
近年来,抗生素的滥用导致水体中抗生素含量逐渐增多,对人类健康及生态系统造成严重的威胁。然而,传统的物化法及生物处理法对污水中低浓度的抗生素处理效果普遍较差[1]。正渗透是新兴的膜分离技术,具有耗能低、操作条件要求低以及汲取液来源广等优势。有研究[2]发现,正渗透可以有效截留微量有机物,可有效去除污水中残留的抗生素、内分泌干扰物等。
混凝是常见的生活污水和工业废水的预处理方法,可去除废水中的悬浮物、胶体物质及部分有机物[3]。然而,混凝对抗生素的去除效果普遍较差。相关研究表明,正渗透对卡巴多及磺胺类抗生素[4]的去除率均小于5%,对四环素类抗生素[5]和甲磺酸曲伐沙星[6]去除也很有限。另外,作为常规污水处理的重要环节,混凝对后续膜处理的影响不能忽视。KIMURA等[7]关于混凝预处理对超滤和纳滤过程膜污染的研究表明,污染物在混凝环节去除越彻底,后续过程膜污染程度越轻。SUN等[8]研究混凝-超滤联合工艺中混凝预处理对膜污染的影响,指出在最佳混凝条件下膜污染程度最轻。混凝絮体在膜表面形成滤饼层,对水通量、污染物和盐通量均有不同的影响,而关于混凝对正渗透膜污染的研究较少。
本研究将混凝-正渗透工艺联用,探究了混凝剂的种类及其投加量对膜污染的影响,并且比较了不同污染情况下正渗透运行特性和抗生素的截留效果,此外,还分析了错流清洗条件对膜通量恢复率的影响。
-
实验试剂:头孢他啶(CAZ)、腐殖酸(HA)、聚合氯化铝(PAC)、氯化铁(FeCl3)、硫酸铝(Al2(SO4)3)、氯化钠(NaCl)、氢氧化钠(NaOH)均为分析纯;实验使用的正渗透膜为丹麦Aquaporin A/S公司生产的水通道蛋白膜。
实验仪器:电子天平(WN-Q20S,苏州奥豪斯电子科技有限公司);电导率仪(DDSJ-308F,上海雷磁精密科学仪器有限公司);COD消解仪(DRB200,哈希水质分析仪器有限公司);高效液相色谱仪(LC-20AT,岛津公司);pH计(SC200,哈希水质分析仪器有限公司);粒度电位仪(Zetasizer Nano,德芮克国际股份有限公司);Longer蠕动泵(YZ1515x-A,保定兰格恒流泵有限公司);水浴锅(HH-S6,江苏佳美仪器制造有限公司)。
-
称取1 g HA溶解到1 L 0.01 mol·L−1 NaOH溶液中,高速搅拌2 h后,制得HA标准储备液,在4 ℃下保存。模拟水样使用自来水配制,其中,HA含量为10 mg·L−1、CAZ为2 mg·L−1、NaCl为1.5 g·L−1。
将模拟水样pH调至7.0,分别投加PAC、FeCl3和Al2(SO4)3对水样进行预处理,混凝条件为200 r·min−1快速搅拌2 min,60 r·min−1慢速搅拌20 min,40 r·min−1慢搅10 min,静置沉淀30 min。取上清液作为后续FO实验的原料液。
-
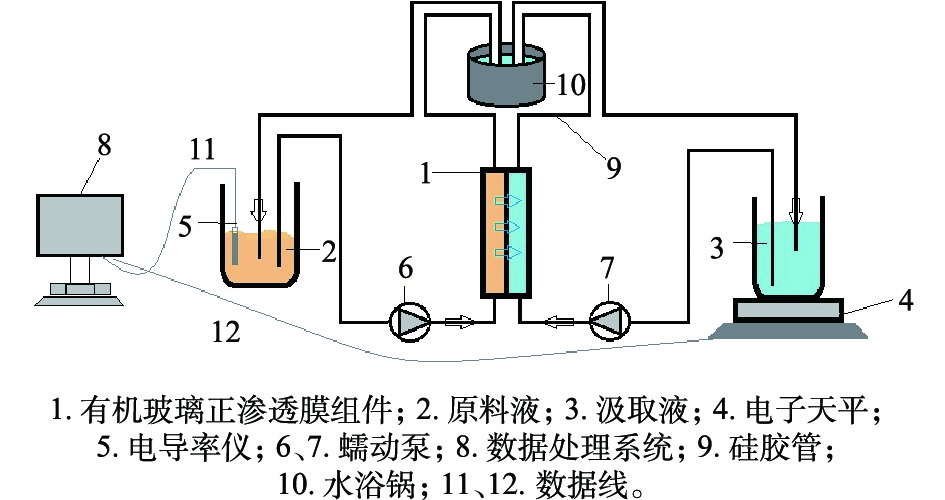
FO实验装置如图1所示。膜组件有2个对称膜池,膜池尺寸为:长110 mm,宽25 mm,高10 mm。实验选用FO模式。汲取液为30 g·L−1 NaCl溶液。膜表面流速为76 cm·min−1,温度为25 ℃。FO实验过程中须测定水通量(JW)、NaCl返混通量(JS)及CAZ截留率的变化。其中JW通过汲取液质量变化求得;JS由原料液电导率的变化得到;CAZ截留率则通过实验前后原料液中CAZ浓度变化来计算。
-
实验结束后,用去离子水进行错流膜冲洗,清洗速度分别为76 cm·min−1和38 cm·min−1,时间分别为30 min和60 min。清洗结束后,以去离子水作为原料液进行膜通量恢复率实验,其他条件同FO实验。经清洗后污垢膜的水通量与清洁膜水通量之比即为膜通量恢复率。
-
通过COD值间接表征HA的浓度。COD采用比色法测定;CAZ浓度采用高效液相色谱法(HPLC)测定;Zeta电位使用Zetasizer Nano系列粒度电位仪测定;膜表面显微形貌通过s-4700扫描电子显微镜观察;膜表面元素组成及含量通过ESCALAB 250型X射线光电子能谱仪分析。
-
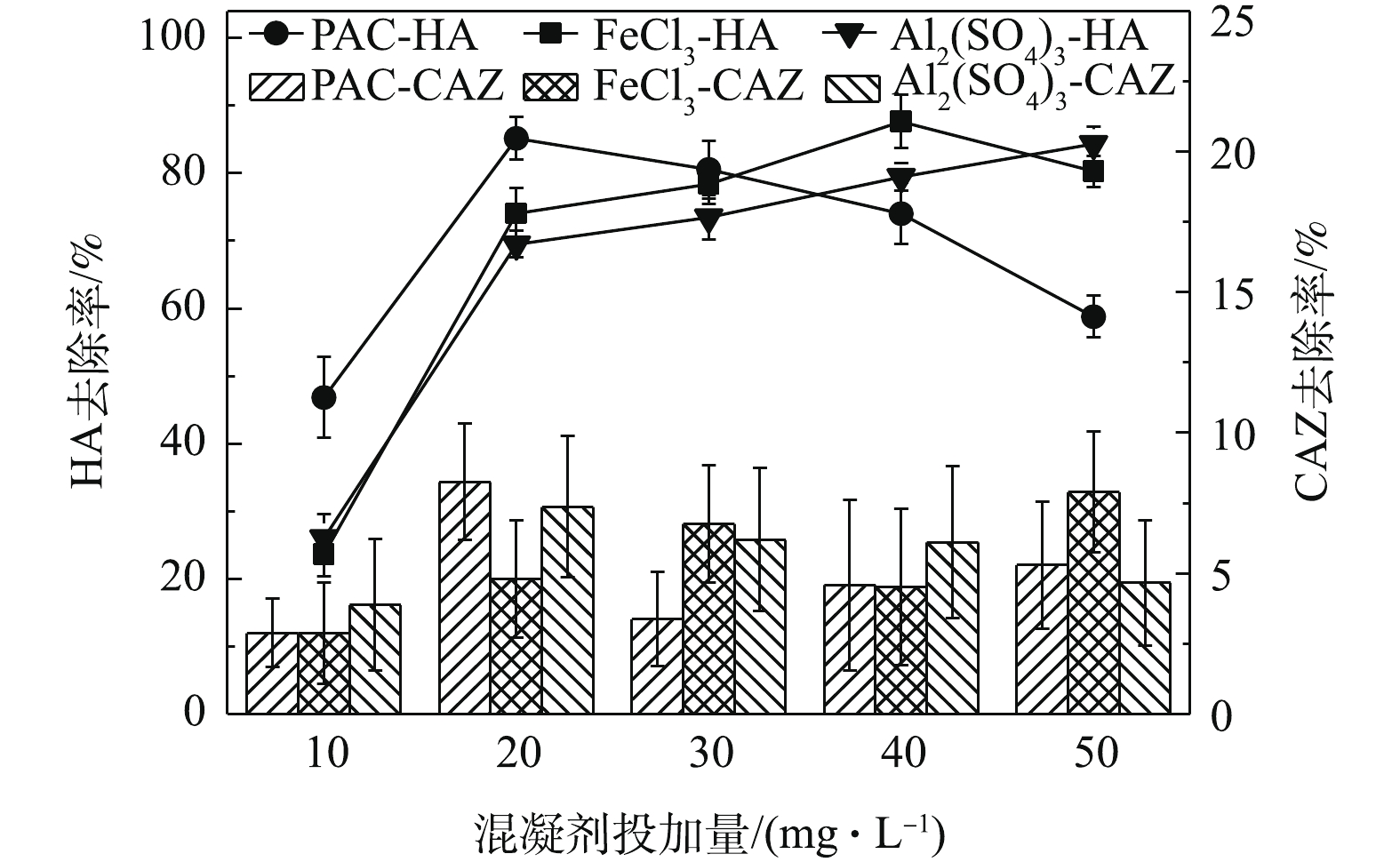
不同混凝剂预处理后,水样中HA及CAZ的去除效果如图2所示。由图2可以看出,混凝剂的种类及其投加量对原料液预处理效果的影响较大。随着PAC投加量的增加,HA去除率呈先升高再下降的趋势。投入PAC后,由于PAC与HA之间的化学吸附架桥作用,导致大颗粒的形成,因粒子发生电中和而失去带电性[9],胶体系统脱稳产生了沉淀现象。当PAC投加量较少(如10 mg·L−1)时,胶粒电中和未完全,粒子沉淀效果较差,HA去除率仅为46.8%;当PAC投加量为20 mg·L−1时,电中和较完全,胶粒之间斥力较小,沉淀效果较好,HA去除率增加到85.2%;但当PAC投加量继续增加到40 mg·L−1或50 mg·L−1时,体系发生了返混现象,HA去除率降低。对于FeCl3和Al2(SO4)3来说,投加量分别为40 mg·L−1和50 mg·L−1时,混凝沉淀效果达到最好。因此,从投加量上考虑,PAC作为混凝剂去除HA的方法最为经济。而混凝预处理对CAZ的去除效果不佳,去除率均小于10%。因此,须后续处理来提高水中CAZ的去除效果。
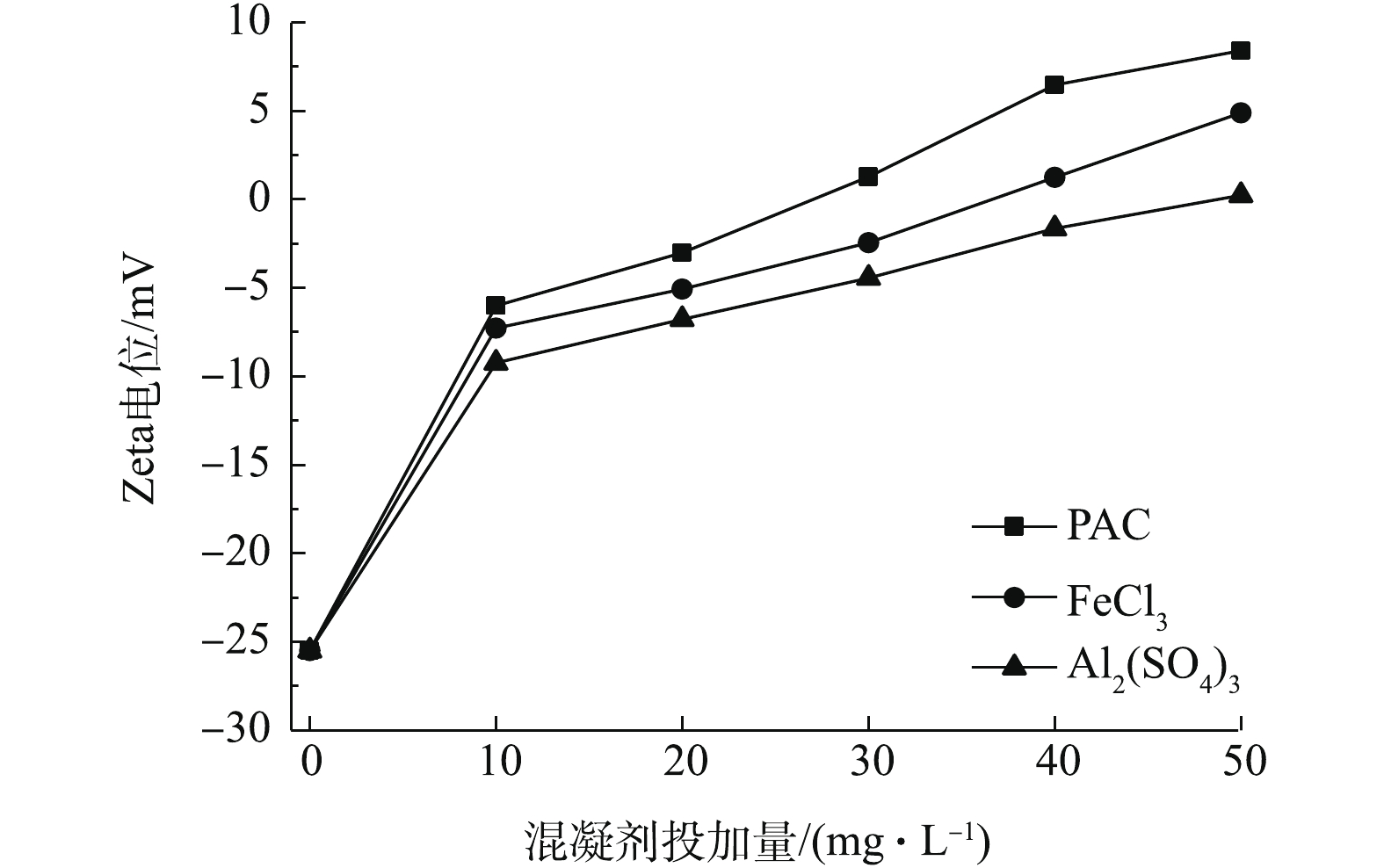
经混凝预处理,上清液Zeta电位的变化情况如图3所示。由图3可知,随着PAC投加量的增加,水样Zeta电位绝对值呈先减小后增大的趋势。PAC投加量从20 mg·L−1增至30 mg·L−1时,Zeta电位由负转正,其绝对值均较低;当PAC投加量继续增加,Zeta电位开始正向增大,这说明此时混凝剂投加过量;当PAC投加量达到50 mg·L−1时,Zeta电位为8.43 mV,此时,其绝对值最大。当FeCl3投加量为40 mg·L−1时,Zeta电位绝对值最小,与混凝效果在此条件下最优相对应;同样,Al2(SO4)3投加量为50 mg·L−1时,Zeta电位绝对值最小,此时混凝效果最佳。
Zeta电位绝对值越低,HA去除率越高,这与已有研究[10]的结果一致。随着混凝剂的投加,发生压缩双电层、电中和等作用,水样Zeta电位逐渐趋向于0,此时粒子趋于凝聚,混凝沉淀效果较好。但过量投加混凝剂会使胶体Zeta电位变为正值,发生再稳定现象,混凝效果变差。
-
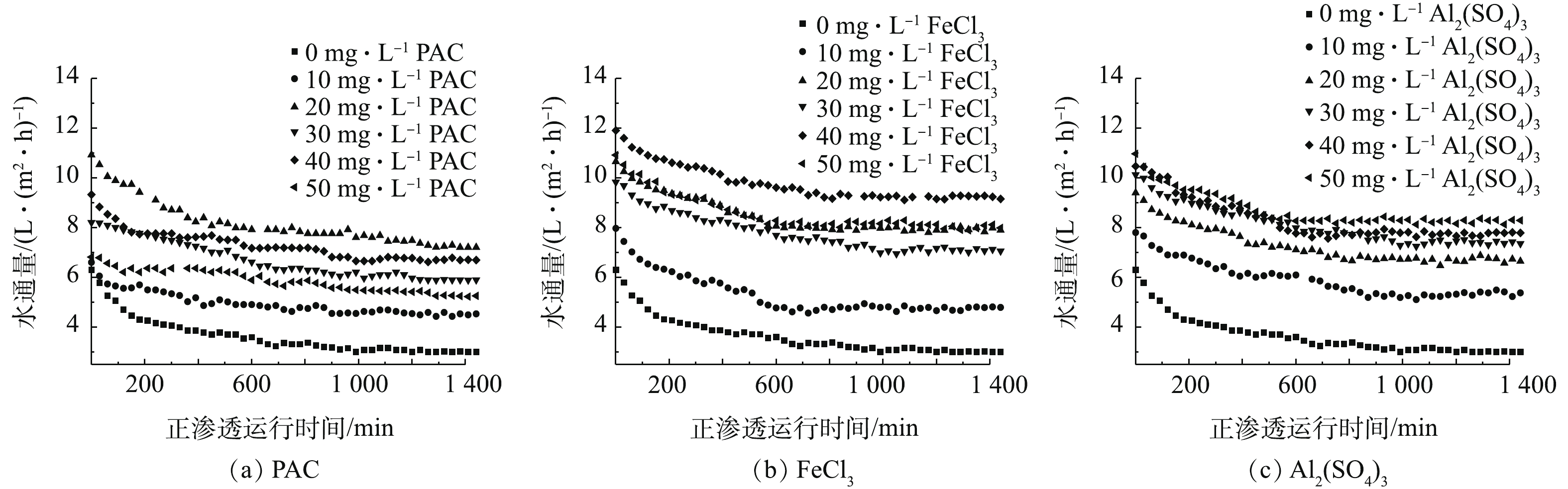
混凝预处理对水通量的影响如图4所示。如图4所示,当原料液不进行混凝预处理时,水通量最低,为3.0~6.3 L·(m2·h)−1。在PAC、FeCl3及Al2(SO4)3为最佳投加量的条件下,水通量均达到最高,分别为7.2~10.9 、9.1~11.9、8.1~10.9 L·(m2·h)−1。此外,混凝剂种类对水通量也有一定影响。经PAC预处理后,水通量较稳定,但水通量值较低。例如,当PAC投加量为30 mg·L−1时,预处理后的水通量为5.9~8.2 L·(m2·h)−1,而FeCl3和Al2(SO4)3预处理后,水通量分别达到了7.0~9.8 L·(m2·h)−1和7.3~10.1 L·(m2·h)−1。
水通量受膜表面污染层的影响较大,原料液中HA浓度越高,FO过程中形成的膜污染层越厚。随着FO实验的进行,污染层逐渐被压实,水分子所受的阻力增强,导致水通量降低。MI等[11]针对污染层对水通量的影响进行了研究,发现致密的污染层一旦形成,便可观察到水通量快速下降的现象。此外,污染层中积累的盐导致污染层的渗透压显著增加,降低了渗透驱动力,从而导致水通量降低。BELL等[12]通过一些方法去除污染层中的钠、氯等无机离子,发现水通量可有一定的提升。此外,水通量还与原料液的Zeta电位有关。Zeta电位绝对值越小,粒子越倾向于凝聚[13],在膜表面形成的污染层越密实,水分子跨膜运输时所受位阻作用越强,水通量越低。
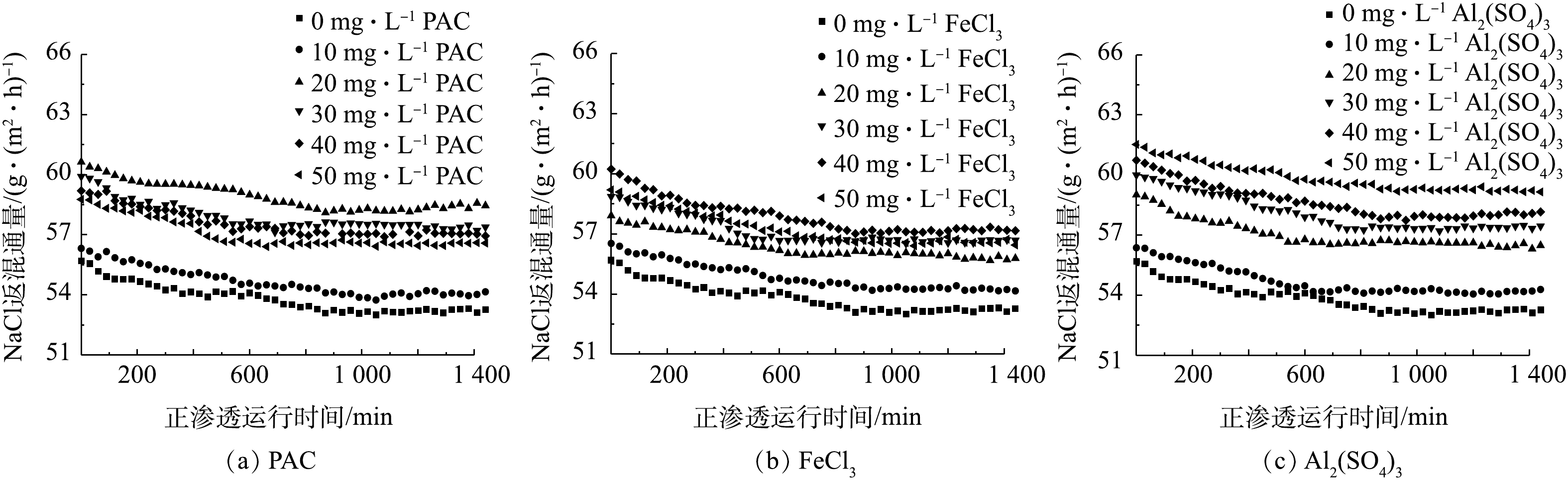
混凝预处理对NaCl返混通量的影响如图5所示。由图5可知,原料液未经预处理时,FO过程中NaCl返混通量最低,为53.1~55.7 g·(m2·h)−1。预处理后,NaCl返混通量均增加。整体来看,除3种混凝剂浓度均为20 mg·L−1外,其他浓度条件下,经Al2(SO4)3预处理后,盐返混通量较高。而较高的盐返混通量对于正渗透是不利的。因此,宜选用其他2种混凝剂来进行预处理。
此外,盐返混通量与HA去除率的变化规律一致。分析其原因为:预处理后原料液中残留的HA量越多,在膜表面形成的污染层越厚,污染层中累积的反向扩散过膜的NaCl就越多,进而导致浓差极化现象越明显。这种现象在一定程度上减缓了汲取液溶质向原料液的反向扩散,使NaCl返混通量降低。BOO等[14]研究了胶体污染对FO过程中盐返混的作用,发现盐从汲取液扩散到原料液并聚集在污染层中,导致盐的进一步反向扩散受到阻碍。XIE等[15]指出污染层厚度是影响溶质返混的主要因素,这与本研究的结论一致。
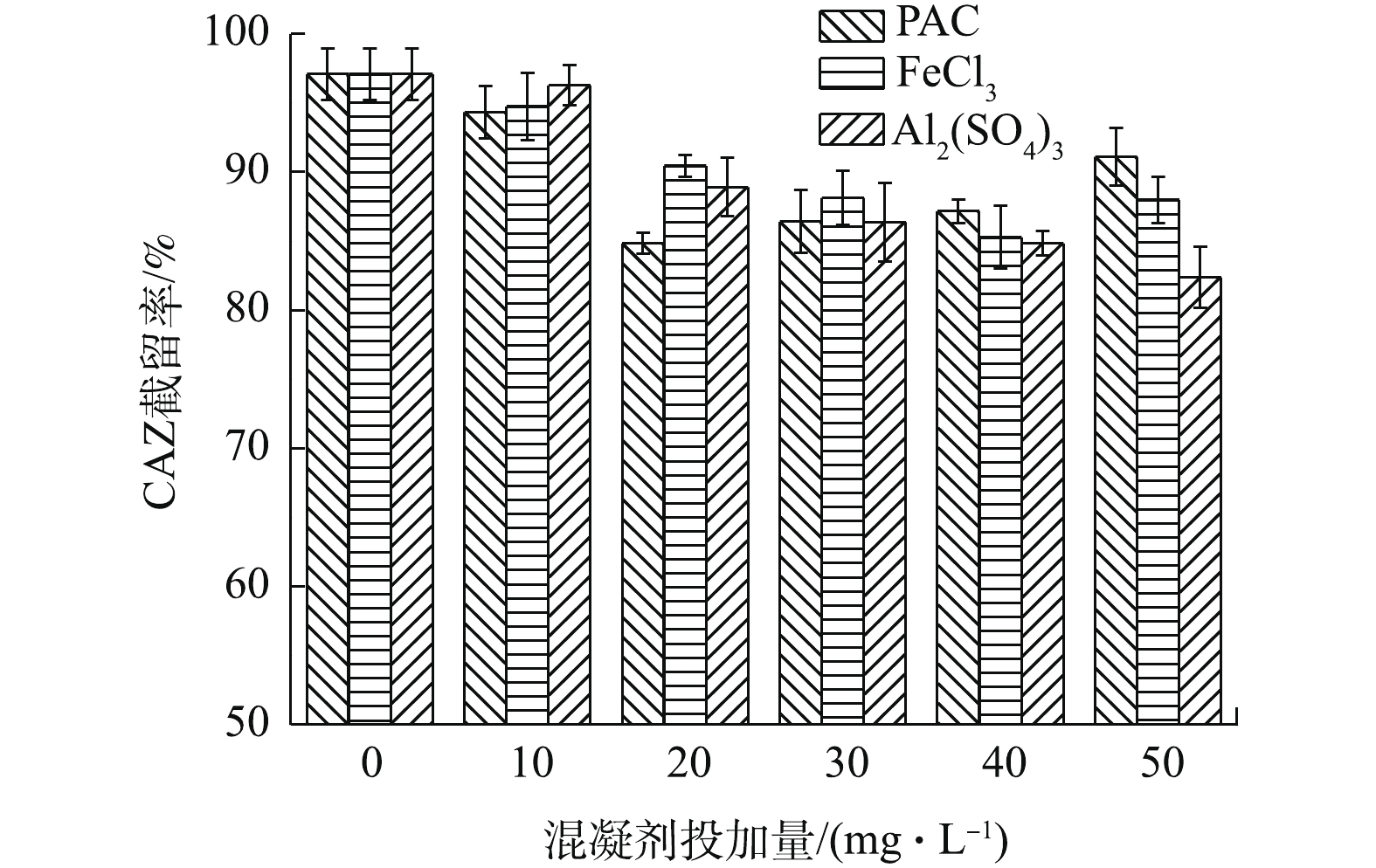
混凝预处理对FO过程中CAZ截留效果的影响如图6所示。由图6可知,FO过程对CAZ的截留效果较好,截留率均大于82%。原料液不进行预处理时,污染层最厚,对CAZ的截留效果最好,为97.1%。随着FeCl3投加量的增加,原料液中HA浓度变小,从而使FO过程形成的污染层变薄,对CAZ的截留作用有所减弱;当FeCl3投加量继续增加到50 mg·L−1时,混凝效果变差,原料液中HA浓度较大,污染层厚度增加,对CAZ的截留作用增强。
污染层的厚度显著影响了CAZ的截留效果。这主要归因于CAZ跨膜运输时所受的位阻作用。污染层越厚,CAZ所受位阻作用越强,截留率越高。虽然返混的盐会在污染层中积累从而增强浓差极化现象,使水通量和盐返混通量均降低的同时,减少了CAZ跨膜扩散时所受的阻力,理论上CAZ扩散更易,但由于污染层的存在,CAZ扩散时所受污染层阻碍作用占主导,使CAZ截留率升高。XIE等[16]研究了正渗透中HA污染层对卡马西平(CBZ)和磺胺甲恶唑(SMZ)在膜表面转移的影响规律,结果表明,随着HA浓度的增加,CBZ和SMZ的截留率均有所增加,这与本研究结果相一致。
-
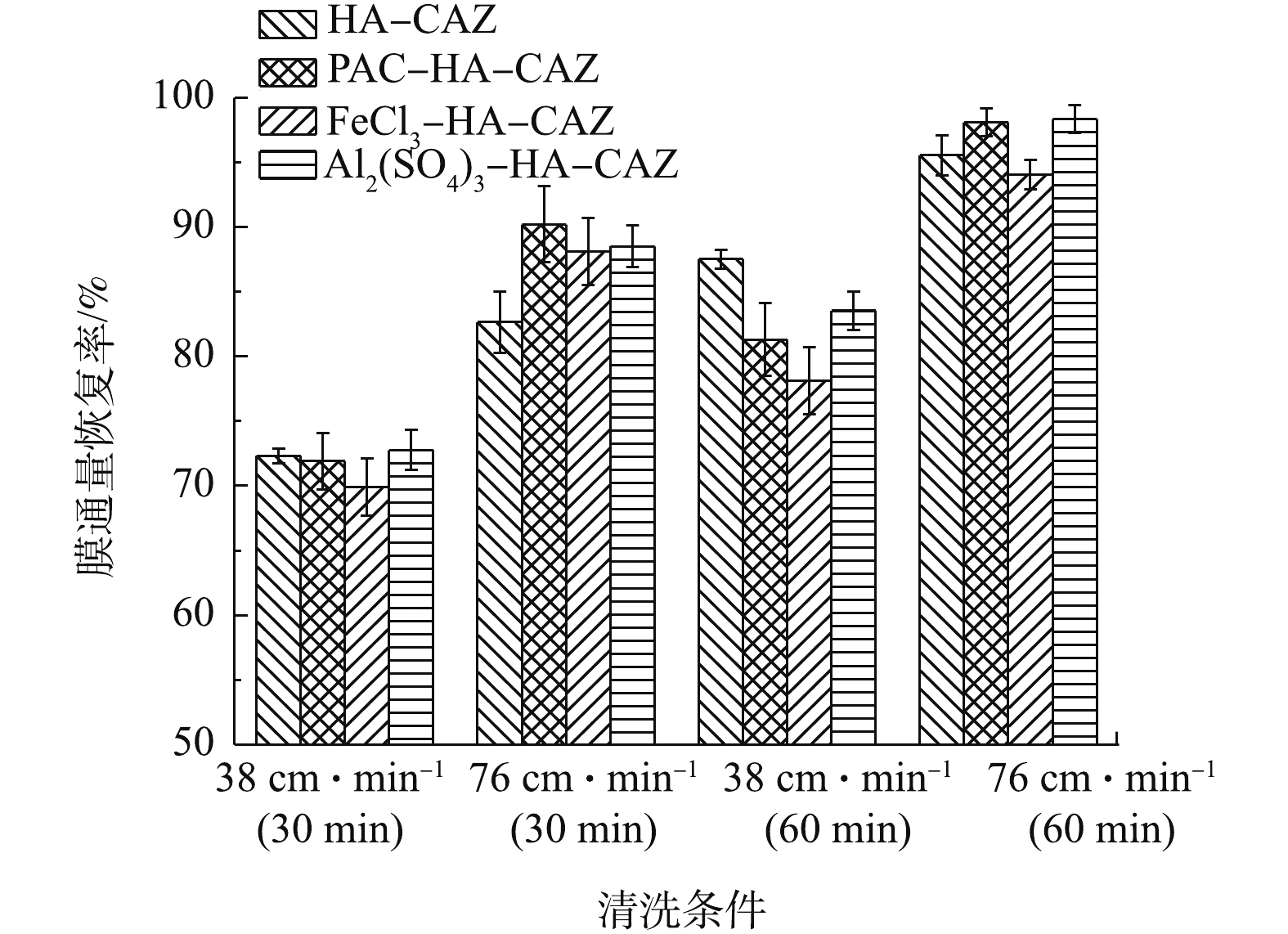
污染膜经清洗后,膜通量恢复率的变化如图7所示。由图7可知,通过物理清洗,膜通量恢复率均较高,这与已有研究[17]报道的结果一致。FO膜被HA模拟水样污染后,清洗时间对膜通量恢复率的影响较大;而经混凝预处理后污染的膜来说,清洗速度对膜通量恢复率的影响较大。对比污染膜表面元素组成及含量的变化,发现经FeCl3预处理后,膜表面铁元素质量分数为5.78%,而PAC和Al2(SO4)3预处理后膜表面铝元素质量分数分别为3.69%和2.42%,由此推测,这是FeCl3预处理后污染层更难清洗的原因之一。
图8为清洁膜及污垢膜清洗前后的SEM图像。对比污染膜清洗前后的膜表面形态,HA模拟水样污染形成的污垢层厚而松软,如图8(b)所示。水样经30 mg·L−1FeCl3预处理后,污染层变得薄而密实,如图8(d)所示。以76 cm·min−1速度清洗60 min后,此时,膜表面形态如图8(c)和图8(e)所示,污染层绝大多数被去除,膜表面形态大致可恢复到被污染前的状态。FO膜污染的可逆性使FO技术在污水治理方面的应用具有广阔的前景。
-
1)混凝预处理对正渗透过程中膜污染程度的影响是由原料液中HA残留量以及Zeta电位共同决定的。HA残留量越多,膜污染过程产生的滤饼层越厚;Zeta电位绝对值越小,FO过程产生的滤饼层越密实。滤饼层的厚度及密实度对正渗透过程中水通量、NaCl返混通量以及抗生素截留率均可造成一定的影响。
2)混凝预处理后,正渗透水通量有所增加,在混凝剂最佳投加量条件下,水通量达到最大值;混凝预处理后,盐返混通量随污染层厚度的减小而增加;此外,CAZ截留率随污染层厚度的减小而减小。
3)污垢膜经清洗后,膜通量恢复率较高。以76 cm·min−1错流速度清洗1 h后,膜通量恢复率均大于94%。污染层较厚,宜延长清洗时间;污染层较密实,宜提高清洗速度。
混凝对正渗透过程中抗生素去除特性及膜污染的影响
Effect of coagulation on antibiotic removal efficiency and membrane fouling during forward osmosis
-
摘要: 为探明混凝预处理对正渗透去除抗生素的影响以及混凝对后续膜处理的影响,选用PAC、FeCl3、Al2(SO4)3对正渗透原料液进行混凝预处理,考察了混凝预处理对正渗透水通量、NaCl返混通量、抗生素截留率及膜污染的影响。结果表明:混凝预处理对正渗透过程中膜污染程度的影响由原料液中HA残留量以及Zeta电位共同决定;经混凝预处理后,原料液中腐殖酸残留量越多,正渗透过程中所形成的滤饼层越厚,原料液Zeta电位绝对值越低,形成的滤饼层越密实。滤饼层的形态影响正渗透的浓差极化作用,进而影响正渗透的运行特性及抗生素的截留效果,同时决定了膜清洗的难易程度。Abstract: To determine the effects of coagulation pretreatment on the removal of antibiotics by forward osmosis the subsequent membrane treatment, PAC, FeCl3 and Al2(SO4)3 were used to conduct coagulation pretreatment. The effects of coagulation pretreatment on water flux, NaCl reverse flux, antibiotic rejection and membrane fouling during forward osmosis were investigated. The results showed that both HA residues in raw material liquor and zeta potential determined the effect of coagulation pretreatment on membrane fouling level. After coagulation pretreatment, the more residual HA led to the thicker filter cake layer, and the lower absolute value of Zeta potential resulted in the denser filter cake layer. The morphology of the filter cake layer affected the concentration polarization of the forward osmosis, and further affected operating characteristics of forward osmosis and antibiotic rejection, then determined the ease of membrane cleaning.
-
Key words:
- coagulation /
- forward osmosis /
- ceftazidime /
- membrane fouling
-
近年来,抗生素的滥用导致水体中抗生素含量逐渐增多,对人类健康及生态系统造成严重的威胁。然而,传统的物化法及生物处理法对污水中低浓度的抗生素处理效果普遍较差[1]。正渗透是新兴的膜分离技术,具有耗能低、操作条件要求低以及汲取液来源广等优势。有研究[2]发现,正渗透可以有效截留微量有机物,可有效去除污水中残留的抗生素、内分泌干扰物等。
混凝是常见的生活污水和工业废水的预处理方法,可去除废水中的悬浮物、胶体物质及部分有机物[3]。然而,混凝对抗生素的去除效果普遍较差。相关研究表明,正渗透对卡巴多及磺胺类抗生素[4]的去除率均小于5%,对四环素类抗生素[5]和甲磺酸曲伐沙星[6]去除也很有限。另外,作为常规污水处理的重要环节,混凝对后续膜处理的影响不能忽视。KIMURA等[7]关于混凝预处理对超滤和纳滤过程膜污染的研究表明,污染物在混凝环节去除越彻底,后续过程膜污染程度越轻。SUN等[8]研究混凝-超滤联合工艺中混凝预处理对膜污染的影响,指出在最佳混凝条件下膜污染程度最轻。混凝絮体在膜表面形成滤饼层,对水通量、污染物和盐通量均有不同的影响,而关于混凝对正渗透膜污染的研究较少。
本研究将混凝-正渗透工艺联用,探究了混凝剂的种类及其投加量对膜污染的影响,并且比较了不同污染情况下正渗透运行特性和抗生素的截留效果,此外,还分析了错流清洗条件对膜通量恢复率的影响。
1. 材料与方法
1.1 试剂与仪器
实验试剂:头孢他啶(CAZ)、腐殖酸(HA)、聚合氯化铝(PAC)、氯化铁(FeCl3)、硫酸铝(Al2(SO4)3)、氯化钠(NaCl)、氢氧化钠(NaOH)均为分析纯;实验使用的正渗透膜为丹麦Aquaporin A/S公司生产的水通道蛋白膜。
实验仪器:电子天平(WN-Q20S,苏州奥豪斯电子科技有限公司);电导率仪(DDSJ-308F,上海雷磁精密科学仪器有限公司);COD消解仪(DRB200,哈希水质分析仪器有限公司);高效液相色谱仪(LC-20AT,岛津公司);pH计(SC200,哈希水质分析仪器有限公司);粒度电位仪(Zetasizer Nano,德芮克国际股份有限公司);Longer蠕动泵(YZ1515x-A,保定兰格恒流泵有限公司);水浴锅(HH-S6,江苏佳美仪器制造有限公司)。
1.2 模拟水样的混凝预处理
称取1 g HA溶解到1 L 0.01 mol·L−1 NaOH溶液中,高速搅拌2 h后,制得HA标准储备液,在4 ℃下保存。模拟水样使用自来水配制,其中,HA含量为10 mg·L−1、CAZ为2 mg·L−1、NaCl为1.5 g·L−1。
将模拟水样pH调至7.0,分别投加PAC、FeCl3和Al2(SO4)3对水样进行预处理,混凝条件为200 r·min−1快速搅拌2 min,60 r·min−1慢速搅拌20 min,40 r·min−1慢搅10 min,静置沉淀30 min。取上清液作为后续FO实验的原料液。
1.3 FO实验
FO实验装置如图1所示。膜组件有2个对称膜池,膜池尺寸为:长110 mm,宽25 mm,高10 mm。实验选用FO模式。汲取液为30 g·L−1 NaCl溶液。膜表面流速为76 cm·min−1,温度为25 ℃。FO实验过程中须测定水通量(JW)、NaCl返混通量(JS)及CAZ截留率的变化。其中JW通过汲取液质量变化求得;JS由原料液电导率的变化得到;CAZ截留率则通过实验前后原料液中CAZ浓度变化来计算。
1.4 膜清洗实验
实验结束后,用去离子水进行错流膜冲洗,清洗速度分别为76 cm·min−1和38 cm·min−1,时间分别为30 min和60 min。清洗结束后,以去离子水作为原料液进行膜通量恢复率实验,其他条件同FO实验。经清洗后污垢膜的水通量与清洁膜水通量之比即为膜通量恢复率。
1.5 分析方法
通过COD值间接表征HA的浓度。COD采用比色法测定;CAZ浓度采用高效液相色谱法(HPLC)测定;Zeta电位使用Zetasizer Nano系列粒度电位仪测定;膜表面显微形貌通过s-4700扫描电子显微镜观察;膜表面元素组成及含量通过ESCALAB 250型X射线光电子能谱仪分析。
2. 结果与讨论
2.1 原料液混凝预处理效果
不同混凝剂预处理后,水样中HA及CAZ的去除效果如图2所示。由图2可以看出,混凝剂的种类及其投加量对原料液预处理效果的影响较大。随着PAC投加量的增加,HA去除率呈先升高再下降的趋势。投入PAC后,由于PAC与HA之间的化学吸附架桥作用,导致大颗粒的形成,因粒子发生电中和而失去带电性[9],胶体系统脱稳产生了沉淀现象。当PAC投加量较少(如10 mg·L−1)时,胶粒电中和未完全,粒子沉淀效果较差,HA去除率仅为46.8%;当PAC投加量为20 mg·L−1时,电中和较完全,胶粒之间斥力较小,沉淀效果较好,HA去除率增加到85.2%;但当PAC投加量继续增加到40 mg·L−1或50 mg·L−1时,体系发生了返混现象,HA去除率降低。对于FeCl3和Al2(SO4)3来说,投加量分别为40 mg·L−1和50 mg·L−1时,混凝沉淀效果达到最好。因此,从投加量上考虑,PAC作为混凝剂去除HA的方法最为经济。而混凝预处理对CAZ的去除效果不佳,去除率均小于10%。因此,须后续处理来提高水中CAZ的去除效果。
经混凝预处理,上清液Zeta电位的变化情况如图3所示。由图3可知,随着PAC投加量的增加,水样Zeta电位绝对值呈先减小后增大的趋势。PAC投加量从20 mg·L−1增至30 mg·L−1时,Zeta电位由负转正,其绝对值均较低;当PAC投加量继续增加,Zeta电位开始正向增大,这说明此时混凝剂投加过量;当PAC投加量达到50 mg·L−1时,Zeta电位为8.43 mV,此时,其绝对值最大。当FeCl3投加量为40 mg·L−1时,Zeta电位绝对值最小,与混凝效果在此条件下最优相对应;同样,Al2(SO4)3投加量为50 mg·L−1时,Zeta电位绝对值最小,此时混凝效果最佳。
Zeta电位绝对值越低,HA去除率越高,这与已有研究[10]的结果一致。随着混凝剂的投加,发生压缩双电层、电中和等作用,水样Zeta电位逐渐趋向于0,此时粒子趋于凝聚,混凝沉淀效果较好。但过量投加混凝剂会使胶体Zeta电位变为正值,发生再稳定现象,混凝效果变差。
2.2 混凝预处理对FO运行特性及其对CAZ去除的影响
混凝预处理对水通量的影响如图4所示。如图4所示,当原料液不进行混凝预处理时,水通量最低,为3.0~6.3 L·(m2·h)−1。在PAC、FeCl3及Al2(SO4)3为最佳投加量的条件下,水通量均达到最高,分别为7.2~10.9 、9.1~11.9、8.1~10.9 L·(m2·h)−1。此外,混凝剂种类对水通量也有一定影响。经PAC预处理后,水通量较稳定,但水通量值较低。例如,当PAC投加量为30 mg·L−1时,预处理后的水通量为5.9~8.2 L·(m2·h)−1,而FeCl3和Al2(SO4)3预处理后,水通量分别达到了7.0~9.8 L·(m2·h)−1和7.3~10.1 L·(m2·h)−1。
水通量受膜表面污染层的影响较大,原料液中HA浓度越高,FO过程中形成的膜污染层越厚。随着FO实验的进行,污染层逐渐被压实,水分子所受的阻力增强,导致水通量降低。MI等[11]针对污染层对水通量的影响进行了研究,发现致密的污染层一旦形成,便可观察到水通量快速下降的现象。此外,污染层中积累的盐导致污染层的渗透压显著增加,降低了渗透驱动力,从而导致水通量降低。BELL等[12]通过一些方法去除污染层中的钠、氯等无机离子,发现水通量可有一定的提升。此外,水通量还与原料液的Zeta电位有关。Zeta电位绝对值越小,粒子越倾向于凝聚[13],在膜表面形成的污染层越密实,水分子跨膜运输时所受位阻作用越强,水通量越低。
混凝预处理对NaCl返混通量的影响如图5所示。由图5可知,原料液未经预处理时,FO过程中NaCl返混通量最低,为53.1~55.7 g·(m2·h)−1。预处理后,NaCl返混通量均增加。整体来看,除3种混凝剂浓度均为20 mg·L−1外,其他浓度条件下,经Al2(SO4)3预处理后,盐返混通量较高。而较高的盐返混通量对于正渗透是不利的。因此,宜选用其他2种混凝剂来进行预处理。
此外,盐返混通量与HA去除率的变化规律一致。分析其原因为:预处理后原料液中残留的HA量越多,在膜表面形成的污染层越厚,污染层中累积的反向扩散过膜的NaCl就越多,进而导致浓差极化现象越明显。这种现象在一定程度上减缓了汲取液溶质向原料液的反向扩散,使NaCl返混通量降低。BOO等[14]研究了胶体污染对FO过程中盐返混的作用,发现盐从汲取液扩散到原料液并聚集在污染层中,导致盐的进一步反向扩散受到阻碍。XIE等[15]指出污染层厚度是影响溶质返混的主要因素,这与本研究的结论一致。
混凝预处理对FO过程中CAZ截留效果的影响如图6所示。由图6可知,FO过程对CAZ的截留效果较好,截留率均大于82%。原料液不进行预处理时,污染层最厚,对CAZ的截留效果最好,为97.1%。随着FeCl3投加量的增加,原料液中HA浓度变小,从而使FO过程形成的污染层变薄,对CAZ的截留作用有所减弱;当FeCl3投加量继续增加到50 mg·L−1时,混凝效果变差,原料液中HA浓度较大,污染层厚度增加,对CAZ的截留作用增强。
污染层的厚度显著影响了CAZ的截留效果。这主要归因于CAZ跨膜运输时所受的位阻作用。污染层越厚,CAZ所受位阻作用越强,截留率越高。虽然返混的盐会在污染层中积累从而增强浓差极化现象,使水通量和盐返混通量均降低的同时,减少了CAZ跨膜扩散时所受的阻力,理论上CAZ扩散更易,但由于污染层的存在,CAZ扩散时所受污染层阻碍作用占主导,使CAZ截留率升高。XIE等[16]研究了正渗透中HA污染层对卡马西平(CBZ)和磺胺甲恶唑(SMZ)在膜表面转移的影响规律,结果表明,随着HA浓度的增加,CBZ和SMZ的截留率均有所增加,这与本研究结果相一致。
2.3 膜污染及水通量的恢复研究
污染膜经清洗后,膜通量恢复率的变化如图7所示。由图7可知,通过物理清洗,膜通量恢复率均较高,这与已有研究[17]报道的结果一致。FO膜被HA模拟水样污染后,清洗时间对膜通量恢复率的影响较大;而经混凝预处理后污染的膜来说,清洗速度对膜通量恢复率的影响较大。对比污染膜表面元素组成及含量的变化,发现经FeCl3预处理后,膜表面铁元素质量分数为5.78%,而PAC和Al2(SO4)3预处理后膜表面铝元素质量分数分别为3.69%和2.42%,由此推测,这是FeCl3预处理后污染层更难清洗的原因之一。
图8为清洁膜及污垢膜清洗前后的SEM图像。对比污染膜清洗前后的膜表面形态,HA模拟水样污染形成的污垢层厚而松软,如图8(b)所示。水样经30 mg·L−1FeCl3预处理后,污染层变得薄而密实,如图8(d)所示。以76 cm·min−1速度清洗60 min后,此时,膜表面形态如图8(c)和图8(e)所示,污染层绝大多数被去除,膜表面形态大致可恢复到被污染前的状态。FO膜污染的可逆性使FO技术在污水治理方面的应用具有广阔的前景。
3. 结论
1)混凝预处理对正渗透过程中膜污染程度的影响是由原料液中HA残留量以及Zeta电位共同决定的。HA残留量越多,膜污染过程产生的滤饼层越厚;Zeta电位绝对值越小,FO过程产生的滤饼层越密实。滤饼层的厚度及密实度对正渗透过程中水通量、NaCl返混通量以及抗生素截留率均可造成一定的影响。
2)混凝预处理后,正渗透水通量有所增加,在混凝剂最佳投加量条件下,水通量达到最大值;混凝预处理后,盐返混通量随污染层厚度的减小而增加;此外,CAZ截留率随污染层厚度的减小而减小。
3)污垢膜经清洗后,膜通量恢复率较高。以76 cm·min−1错流速度清洗1 h后,膜通量恢复率均大于94%。污染层较厚,宜延长清洗时间;污染层较密实,宜提高清洗速度。
-
-
[1] REUNGOAT J, MACOVA M, ESCHER B I, et al. Removal of micropollutants and reduction of biological activity in a full scale reclamation plant using ozonation and activated carbon filtration[J]. Water Research, 2010, 44(2): 625-637. doi: 10.1016/j.watres.2009.09.048 [2] ALTURKI A A, MCDONALD J A, KHAN S J, et al. Removal of trace organic contaminants by the forward osmosis process[J]. Separation and Purification Technology, 2013, 103: 258-266. doi: 10.1016/j.seppur.2012.10.036 [3] MATILAINEN A, VEPSÄLÄINEN M, SILLANPÄÄ M. Natural organic matter removal by coagulation during drinking water treatment: A review[J]. Advances in Colloid and Interface Science, 2010, 159(2): 189-197. doi: 10.1016/j.cis.2010.06.007 [4] ADAMS C, WANG Y, LOFTIN K, et al. Removal of antibiotics from surface and distilled water in conventional water treatment processes[J]. Journal of Environmental Engineering, 2002, 128(3): 253-260. doi: 10.1061/(ASCE)0733-9372(2002)128:3(253) [5] CHOI K J, KIM S G, KIM S H. Removal of antibiotics by coagulation and granular activated carbon filtration[J]. Journal of Hazardous Materials, 2008, 151(1): 38-43. doi: 10.1016/j.jhazmat.2007.05.059 [6] BUNDY M M, DOUCETTE W J, MCNEILL L, et al. Removal of pharmaceuticals and related compounds by a bench-scale drinking water treatment system[J]. Journal of Water Supply: Research and Technology-AQUA, 2007, 56(2): 105-115. doi: 10.2166/aqua.2007.091 [7] KIMURA K, ANDO N. Maximizing biopolymer removal by coagulation for mitigation of fouling in the following membrane process[J]. Separation and Purification Technology, 2016, 163: 8-14. doi: 10.1016/j.seppur.2016.02.013 [8] SUN S, YANG Z, HUANG X, et al. Coagulation performance and membrane fouling of polyferric chloride/epichlorohydrin-dimethylamine in coagulation/ultrafiltration combined process[J]. Desalination, 2015, 357: 163-170. doi: 10.1016/j.desal.2014.11.031 [9] DEMPSEY B A, GANHO R M, O'MELIA C R. The coagulation of humic substances by means of aluminum salts[J]. Journal of American Water Works Association, 1984, 76(4): 141-150. doi: 10.1002/j.1551-8833.1984.tb05315.x [10] XU Y, CHEN T, CUI F, et al. Effect of reused alum-humic-flocs on coagulation performance and floc characteristics formed by aluminum salt coagulants in humic-acid water[J]. Chemical Engineering Journal, 2016, 287: 225-232. doi: 10.1016/j.cej.2015.11.017 [11] MI B, ELIMELECH M. Chemical and physical aspects of organic fouling of forward osmosis membranes[J]. Journal of Membrane Science, 2008, 320(1/2): 292-302. [12] BELL E A, POYNOR T E, NEWHART K B, et al. Produced water treatment using forward osmosis membranes: Evaluation of extended-time performance and fouling[J]. Journal of Membrane Science, 2017, 525: 77-88. doi: 10.1016/j.memsci.2016.10.032 [13] ELIMELECH M, CHEN W H, WAYPA J J. Measuring the zeta (electrokinetic) potential of reverse osmosis membranes by a streaming potential analyzer[J]. Desalination, 1994, 95(3): 269-286. doi: 10.1016/0011-9164(94)00064-6 [14] BOO C, LEE S, ELIMELECH M, et al. Colloidal fouling in forward osmosis: Role of reverse salt diffusion[J]. Journal of Membrane Science, 2012, 390: 277-284. [15] XIE M, NGHIEM L D, PRICE W E, et al. Impact of organic and colloidal fouling on trace organic contaminant rejection by forward osmosis: Role of initial permeate flux[J]. Desalination, 2014, 336: 146-152. doi: 10.1016/j.desal.2013.12.037 [16] XIE M, NGHIEM L D, PRICE W E, et al. Impact of humic acid fouling on membrane performance and transport of pharmaceutically active compounds in forward osmosis[J]. Water Research, 2013, 47(13): 4567-4575. doi: 10.1016/j.watres.2013.05.013 [17] CHOI B G, KIM D I, HONG S. Fouling evaluation and mechanisms in a FO-RO hybrid process for direct potable reuse[J]. Journal of Membrane Science, 2016, 520: 89-98. doi: 10.1016/j.memsci.2016.07.035 -




 下载:
下载: