-
近年来,工业化的迅速发展造成了许多环境污染问题。染料废水作为一种典型的工业废水因其水量大、色度高、组成成分复杂而导致其处理难度非常高[1]。若未经处理而排放到自然水体,将会污染水源,威胁生态环境,并且其生物毒性通过食物链而最终在人体积累,严重危害人体健康[2]。目前,染料废水的去除方法主要有物理法、化学法及生物法[3-4]。物理法是目前研究染料废水处理最为广泛的一种处理方法,其中吸附法作为一种绿色高效的去除技术被广泛地应用于染料废水的去除。吸附剂的选择对于使用吸附法去除染料废水至关重要。目前,常用的吸附材料有活性炭、焦炭、沸石、壳聚糖以及天然黏土矿物等[5]。但是这些吸附剂的吸附容量不高,或者选择吸附性差。因此,开发一种高效和大吸附量的吸附剂用于染料废水的去除非常必要。
金属有机骨架是通过共价键或者离子共价键自组装金属中心离子和有机配体形成的具有周期性网络结构的配位聚合物[6]。因其高的比表面积和可调的孔径[7]、丰富的结构和组成成分、配位不饱和位点能够结合特定官能团[8]等特点而被广泛应用于储能、气液相分离、催化、光学和磁学等领域[9-11]。沸石咪唑基骨架(ZIFs)作为MOFs材料的一种,具有优异的化学稳定性和吸附性能。张琪颖[12]研究了ZIF-8对硝基苯酚(PNP)的吸附效果,研究表明,ZIF-8在反应最佳条件下能够高效选择性地吸附PNP。同时,磁性纳米复合材料作为吸附剂应用于水处理中也受到广泛关注。孙杨等[13]利用自制Fe3O4磁性材料与MOF-5合成磁性Fe3O4@MOF-5复合材料,被证明Fe3O4@MOF-5复合材料对于刚果红是良好的吸附剂。基于上述研究,本研究采用聚苯乙烯磺酸钠(PSS)处理Fe3O4表面诱导生长ZIF-8壳层,在常温搅拌下,成功合成磁性核壳金属有机骨架Fe3O4@ZIF-8,通过SEM、TEM、XRD、FT-IR及VSM对其进行形貌分析,考察了刚果红初始浓度及接触时间、Fe3O4@ZIF-8用量、pH等因素对Fe3O4@ZIF-8吸附偶氮染料刚果红废水的影响;确定了其吸附动力学和吸附等温线;探讨了Fe3O4@ZIF-8的选择吸附性能以及循环再生性能,研究可为复合金属有机骨架材料在染料吸附去除方面的应用提供参考。
-
仪器:电子天平(AL104,梅特勒-多利多仪器上海有限公司);超纯水机(Ther-mo Scientific Barnstead EasypureⅡ);精密增力电动搅拌器(金坛市新航仪器厂);真空干燥箱(DZF-6020型,上海浦东荣丰科学仪器有限公司);恒温干燥箱(101-1型,上海东星建材实验设备有限公司);pH计(PHB-4型,上海仪电科学仪器股份有限公司);双功能水浴恒温振荡器(SHA-B,金坛市科析仪器有限公司);扫描电镜(Quanta FEG型,美国FEI公司);分光光度计(PhotoLab-7600型,赛莱默中国分析仪器有限公司)。
材料与试剂:六水合硝酸锌(Zn(NO3)2·6H2O)(分析纯,国药化学试剂有限公司);2-甲基咪唑(C4H6N2)(分析纯,阿拉丁试剂有限公司);聚苯乙烯磺酸钠(PSS)(30%,阿拉丁试剂有限公司);甲醇(CH3OH)(分析纯,阿拉丁试剂有限公司);Fe3O4纳米颗粒(99%,成都麦卡希有限公司);氢氧化钠(NaOH)(分析纯,重庆川东化工有限公司);盐酸(HCl)(分析纯,重庆川东化工有限公司);氯化钠(优级纯,阿拉丁试剂有限公司);刚果红(分析纯,阿拉丁试剂有限公司);去离子水,实验室自制。
-
Fe3O4@ZIF-8的合成参照文献中的方法[14]。将1.5 g的聚苯乙烯磺酸钠(PSS)溶解在150 mL去离子水中并超声处理30 min,配制成PSS溶液,将0.25 g的Fe3O4纳米颗粒加入到PSS溶液中并在室温下超声30 min,然后,通过外部磁体将Fe3O4纳米粒子与溶液分离并用水洗涤3次;处理后的Fe3O4纳米微粒投加到ZIF-8的合成液中(1.19 g硝酸锌,2.63 g二甲基咪唑和80 mL甲醇),在50 ℃水浴条件下,机械搅拌8 h,然后通过磁铁把合成的Fe3O4@ZIF-8磁性核壳颗粒与反应体系分离。用甲醇溶液洗涤磁性粒子3次,并在真空干燥箱中60 ℃烘干12 h,最后获取Fe3O4@ZIF-8。
-
采用扫描电子显微镜(SEM,Quanta FEG,FEI公司,美国)和透射电子显微镜(TEM,Tecnai F30,FEI公司,美国)对磁性金属有机骨架Fe3O4@ZIF-8的微观形貌进行分析。采用X射线衍射(XRD,X/Pert PRO MPD,帕纳科分析仪器有限公司,荷兰)对Fe3O4@ZIF-8的晶体结构进行表征。Fe3O4@ZIF-8表面官能团信息采用傅里叶变换红外分光光度计(FT-IR,Nicolet iS50,Nicolet公司,美国)测定。Fe3O4@ZIF-8的磁学性能采用振动样品磁强计(7400型,Lake shore公司,美国)进行测试。
-
本实验选择阴离子偶氮染料刚果红为模拟染料废水,研究磁性金属有机骨架Fe3O4@ZIF-8材料对其去除效果,在一系列规格为50 mL的锥形瓶内,倒进20 mL刚果红染料溶液,准确投加一定质量的Fe3O4@ZIF-8吸附剂,把锥形瓶放入振荡器中,25 ℃下恒温振荡,吸附一段时间后,用磁铁将吸附剂Fe3O4@ZIF-8从溶液中分离出来,取上层溶液用分光光度计测定光度值,然后分别计算Fe3O4@ZIF-8的吸附容量和刚果红去除率。
去除率和单位吸附量的计算方法见式(1)和式(2)。
式中:
η 为去除率;C0为刚果红的初始浓度,mg·L−1;C为刚果红浓度,mg·L−1;q为吸附剂的吸附量,mg·g−1;V为溶液体积,L;m为Fe3O4@ZIF-8质量,g。1)吸附动力学实验。取不同初始浓度的20 mL刚果红溶液,并投加Fe3O4@ZIF-8吸附剂10 mg。在25 ℃下进行恒温振荡,分别吸附5、10、20、30、60、90、120、180和240 min后,离心混合溶液并测定上清液的吸光度。吸附数据由一级动力学方程[15]和二级动力学方程[16]来进行拟合。一级动力学方程见式(3),二级动力学方程见式(4)。
式中:qe为吸附剂的平衡吸附量,mg·g−1;q为吸附剂在t时刻的吸附量,mg·g−1;t为吸附时间,min;K1为一级动力学速率常数,min−1;K2为二级动力学速率常数,g·(mg·min)−1。
2)吸附等温线测定。配置20 mL初始浓度为50~300 mg·L−1的刚果红溶液,加入10 mg的Fe3O4@ZIF-8吸附剂。将混合溶液的pH调节至6,并在25、30、35 ℃下进行振荡,直至吸附达到平衡。吸附数据由Langmuir吸附等温方程[17](见式(5))和Freundlich吸附等温方程[18](见式(6))进行拟合。
式中:qe为吸附剂的平衡吸附量,mg·g−1;Ce为平衡质量浓度,mg·L−1;q为Fe3O4@ZIF-8的最大吸附量,mg·g−1;b为吸附能有关常数;Kf为Freundlich系数;n为Freundlich常数。
3)选择吸附实验。在实验中,使用Fe3O4@ZIF-8作为吸附剂以吸附刚果红、直接蓝86、甲基橙、亚甲基蓝染料,以此来考察Fe3O4@ZIF-8的选择吸附性能。取30 mg·L−1的不同染料20 mL,加入10 mg的Fe3O4@ZIF-8,在恒定温度下吸附12 h,测定吸附后的浓度。
4)循环性能实验。Fe3O4@ZIF-8吸附50 mg·L−1的刚果红溶液后,使用蒸馏水反复冲洗吸附剂,随后采用0.1 mol·L−1的NaOH溶液进行解吸,然后烘干用于下一个周期中。重复5次,考察Fe3O4@ZIF-8的吸附解吸能力。
-
1) SEM和TEM分析。图1(a)~(c)是在不同放大倍数下的SEM图,可以看出,Fe3O4@ZIF-8纳米粒子呈现不规则的立方体结构,并且表面分布了很多ZIF-8晶体。图1(d)~(f)为Fe3O4@ZIF-8在不同放大倍数下的TEM图,可以看出,该复合材料呈现明显的核壳形态,ZIF-8已成功地生长在Fe3O4纳米颗粒表面。这种磁性复合材料的平均粒径在200 nm左右。SEM和TEM表征很好地证明了合成的材料即为核壳结构的Fe3O4@ZIF-8。
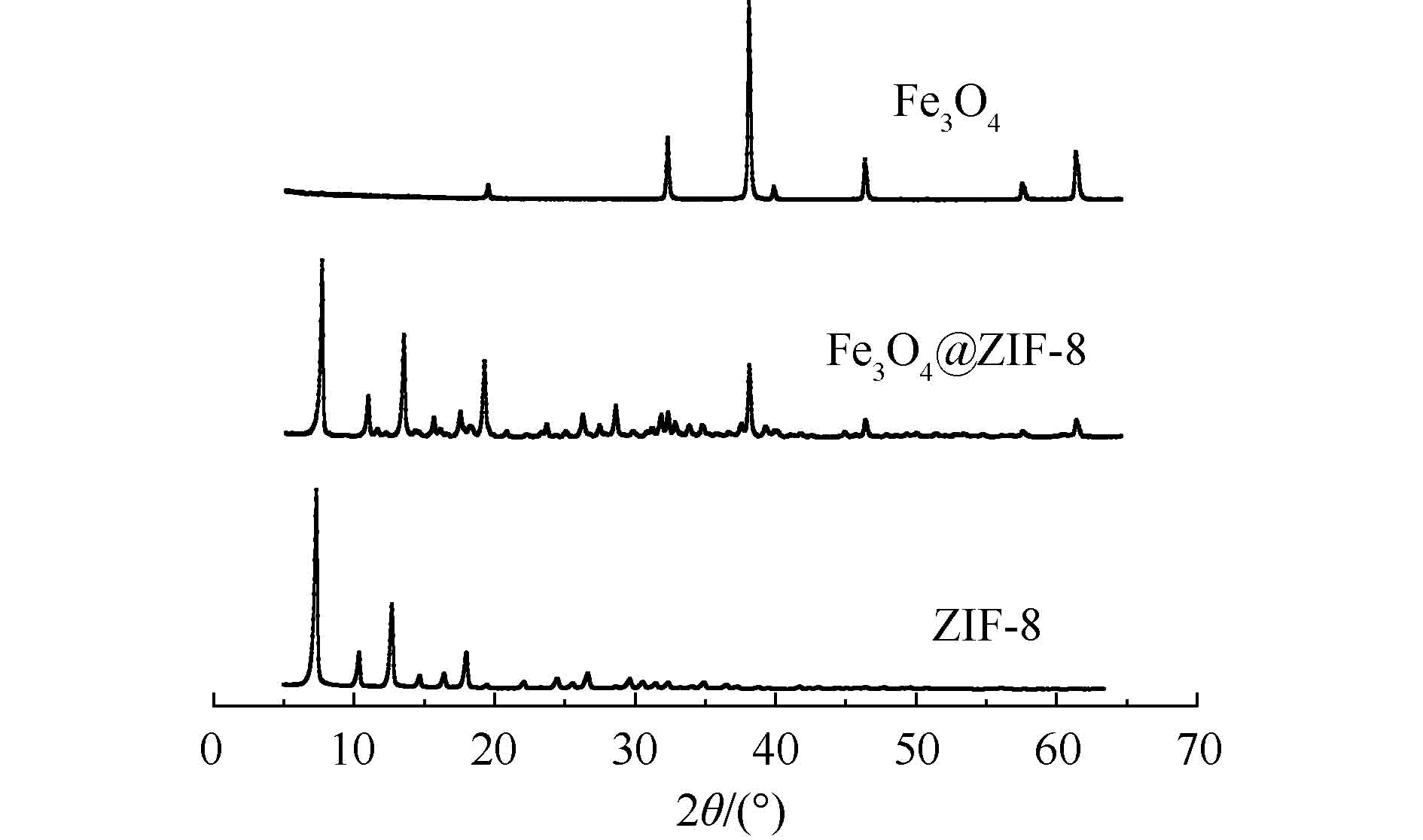
2) XRD分析。由图2可知,Fe3O4@ZIF-8材料在2θ为30.16°、35.52°、43.18°、53.52°、57.06°处均出现了特征峰,与实验中Fe3O4的表征图谱比较,特征峰的位置相同,分别对应的是Fe3O4的(220)、(311)、(400)、(422)和(511)衍射晶面。同时,在(011)、(002)、(112)、(022)、(013)、(222)处均出现了与实验表征的ZIF-8 图谱对应一致的衍射峰。所以,可断定Fe3O4@ZIF-8已成功合成,且Fe3O4@ZIF-8中Fe3O4的晶型结构没有遭到破坏。这说明Fe3O4@ZIF-8不仅具备ZIF-8的高效吸附性能,同时还具有Fe3O4的磁性分离性能。
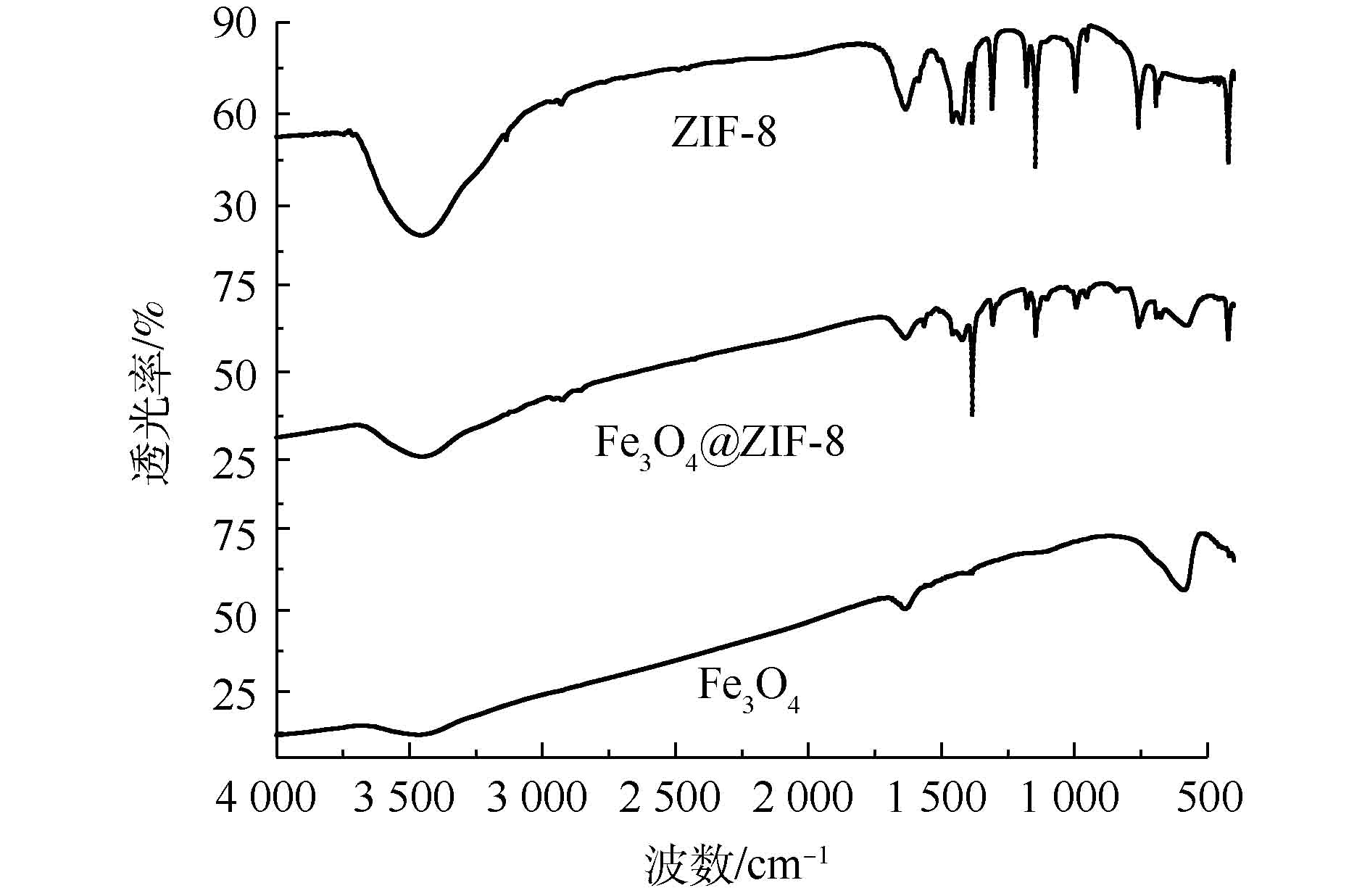
3) FT-IR分析。从图3中的Fe3O4@ZIF-8红外图谱可知,在3 454 cm−1处出现了对应于水分子中的O—H键的特征吸收峰。3 135 cm−1和2 926 cm−1分别归属于ZIF-8结构中咪唑分子芳香族与脂肪族的C—H键的特征峰。咪唑环中C=N键的伸缩振动峰出现在1 565 cm−1处,C—N键的振动吸收峰出现在1 146和993 cm−1处。在420 cm−1处出现了Zn—N官能团振动峰,最重要的是在580 cm−1处出现了属于Fe3O4的Fe—O振动吸收峰[19]。综合上述分析,可以进一步确定成功合成的核壳结构物质就是Fe3O4@ZIF-8。
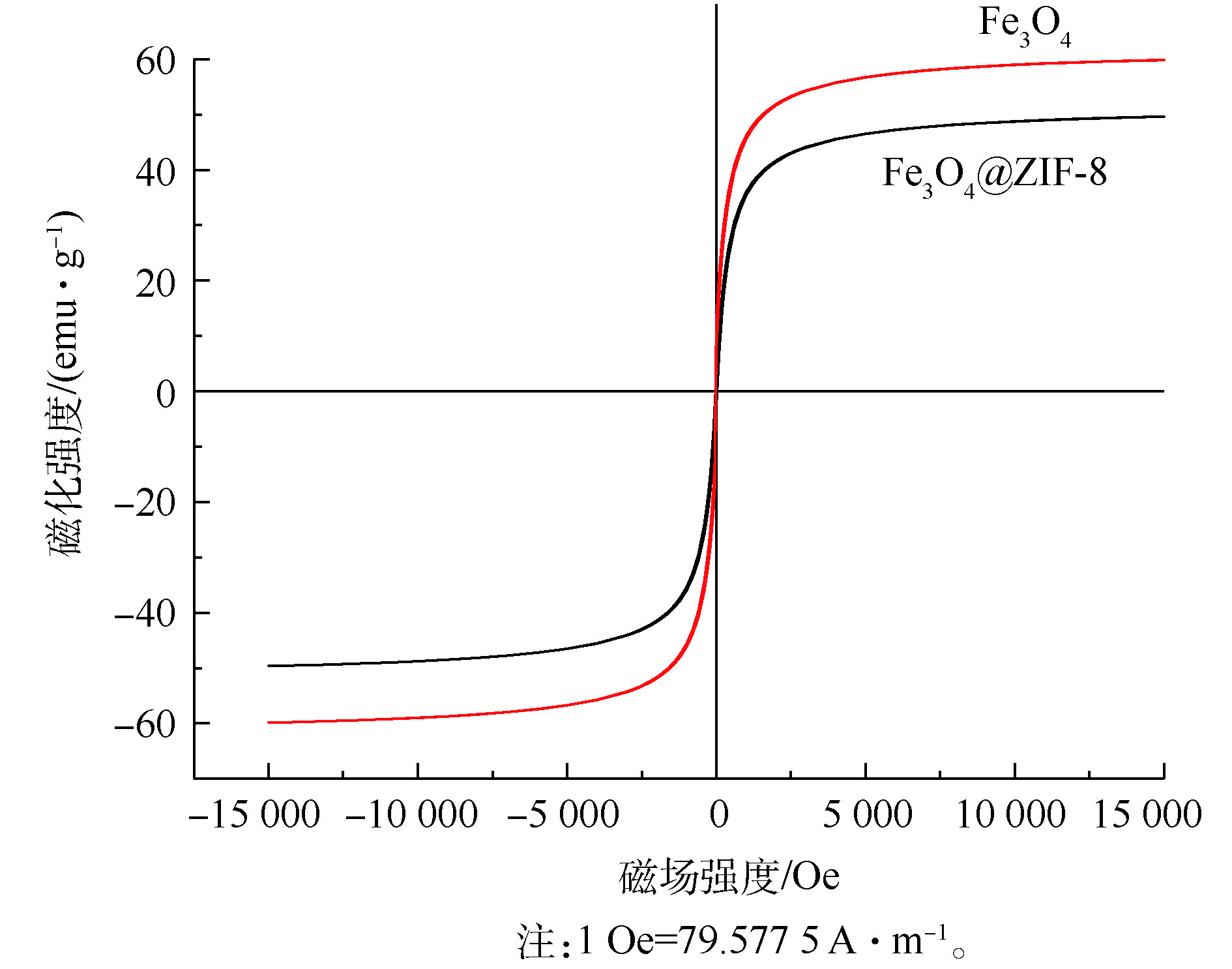
4) VSM分析。如图4所示,Fe3O4@ZIF-8的磁滞回线为过原点的S型曲线,表明Fe3O4@ZIF-8材料是典型的超顺磁性。Fe3O4@ZIF-8的饱和磁化强度为49.68 emu·g−1,由于ZIF-8在壳层的覆盖,Fe3O4@ZIF-8的磁饱和度相对于Fe3O4有所降低,但是Fe3O4@ZIF-8仍然具有优异的磁学性能。
-
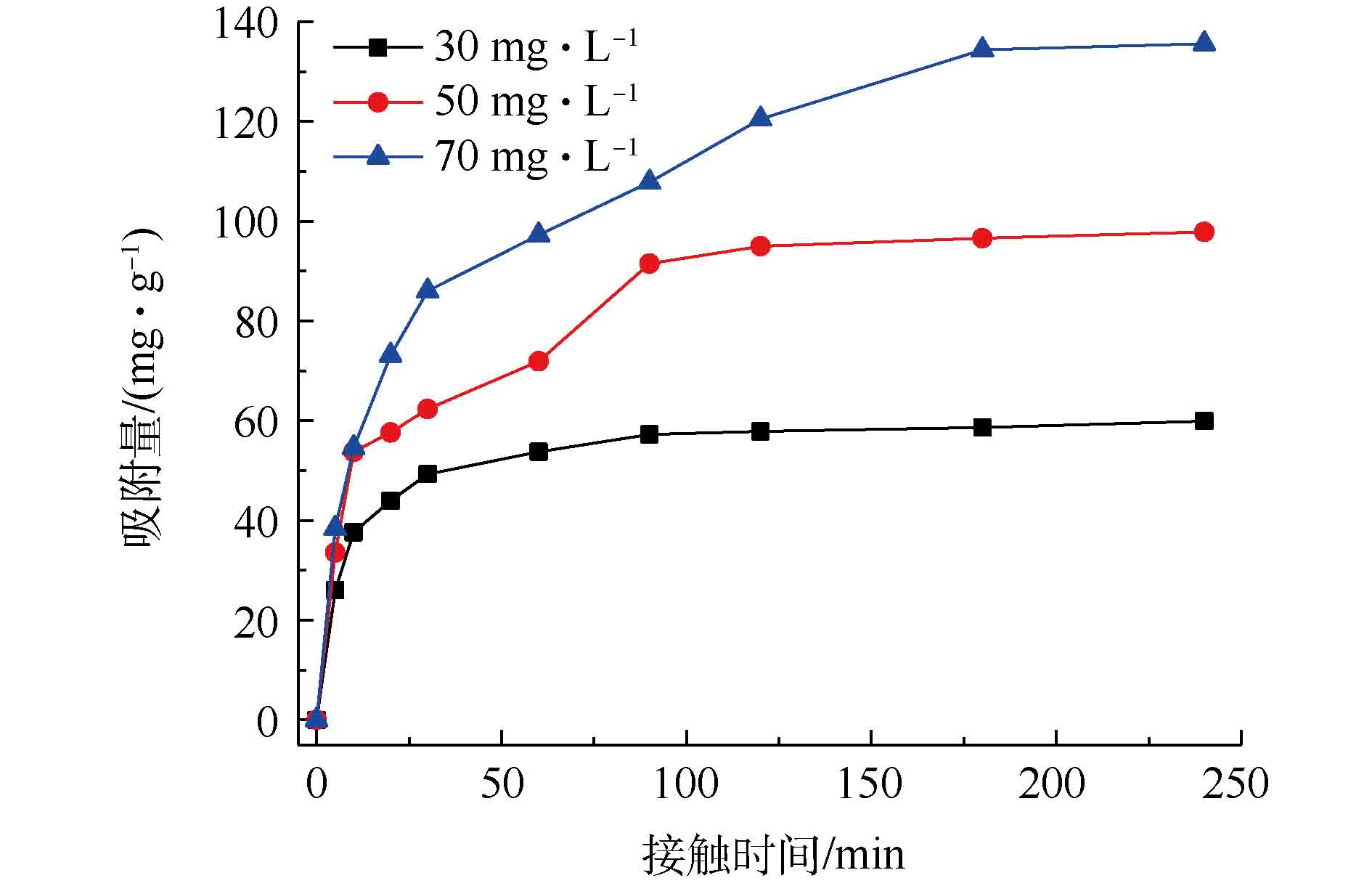
从图5可以看出,在同一浓度下,Fe3O4@ZIF-8的单位吸附容量随着反应时间的增加而增加,在反应的前10 min左右,单位吸附容量已达平衡吸附量的50%。这表明反应最初是快速吸附阶段。当反应时间为180 min时,Fe3O4@ZIF-8的单位吸附量逐渐达到平衡。并且在不同的刚果红初始浓度下,随着初始浓度的升高,Fe3O4@ZIF-8的单位吸附量也逐渐升高。当初始浓度由30 mg·L−1升高到70 mg·L−1时,Fe3O4@ZIF-8的单位吸附量由60 mg·g−1升高到136 mg·g−1。
-
图6为Fe3O4@ZIF-8投加量对吸附效果的影响,当Fe3O4@ZIF-8投加量为5 mg时,吸附除去率达到68.7%,从5 mg变化到10 mg时,Fe3O4@ZIF-8对刚果红染料的去除率升高到95.2%。当Fe3O4@ZIF-8投加量大于10 mg,其去除率约为98%,刚果红的吸附去除率升高幅度不大,并且随着Fe3O4@ZIF-8吸附剂投加量的不断增长,其单位吸附容量是一直减少的,这是因为当染料初始浓度和体积恒定时,单位质量的吸附剂吸附染料的量随着吸附剂投加量的增多而减少。并且过多的吸附剂量将导致吸附剂位点的聚集和重叠,增加了扩散的难度。同时,从经济角度来看,过多的吸附剂投加会造成成本的增加。因此,选择Fe3O4@ZIF-8吸附剂的用量为500 mg·L−1。
-
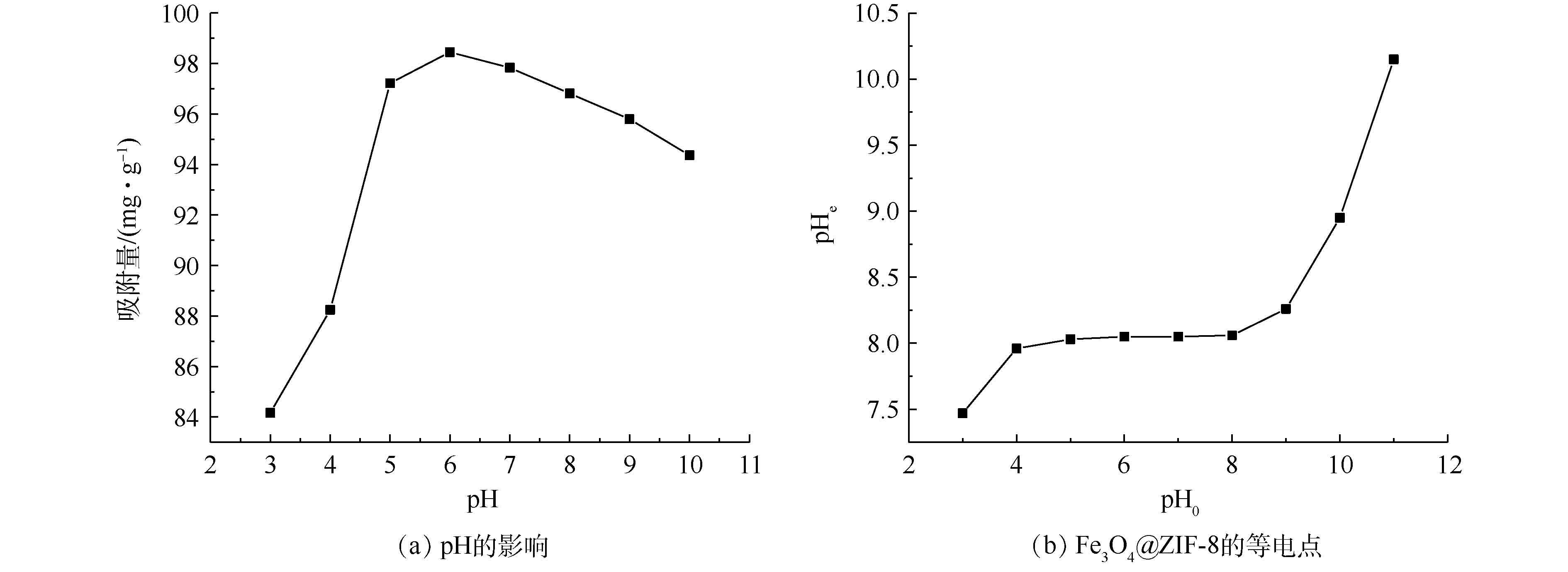
移取20 mL的 50 mg·L−1的刚果红溶液,通过0.05 mol·L−1的NaOH溶液和0.05 mol·L−1的HCl溶液调节pH从3变化到10,Fe3O4@ZIF-8吸附剂的投加量为10 mg,在 25 ℃条件下以180 r·min−1的速度恒温振荡6 h,利用磁铁将吸附剂与溶液分离,然后通过分光光度计测定溶液的分光度,考察初始的pH对Fe3O4@ZIF-8吸附效果的影响,实验结果如图7所示。如图7(a)所示,当pH<6.0时,Fe3O4@ZIF-8的单位吸附容量随着pH的升高而升高,而且升高幅度很大;在pH=6.0时,单位吸附量达到最大值,这是由于Fe3O4@ZIF-8表面带的正电荷数量增加,与刚果红分子产生静电引力导致吸附量升高;当pH>6.0时,单位吸附量随着pH的升高而减小。这可由图7(b)来解释。实验测得Fe3O4@ZIF-8的等电点为8.37。当pH<8.37时,Fe3O4@ZIF-8表面是带有正电荷的,而刚果红分子带有负电荷,Fe3O4@ZIF-8因为强烈的静电引力而吸附刚果红染料,随后pH的升高,溶液中的OH−逐渐增多并且和阴离子刚果红染料竞争Fe3O4@ZIF-8的吸附位点,从而导致吸附量下降。当pH>8.37时,Fe3O4@ZIF-8表面由原来的正电荷转为负电荷,它与带负电的刚果红分子相互排斥导致其单位吸附容量减少有关。因此,在低pH时,静电引力使刚果红吸附量增加,随着pH的升高,刚果红与Fe3O4@ZIF-8之间产生静电斥力,吸附量逐渐降低。
-
由图8可知,吸附数据的拟合结果是二级动力学模型明显优于一级动力学模型,其线性相关性更高。具体的拟合数据如表1所示,一级动力学模型和二级动力学模型拟合的效果都很好,其中二级动力学模型拟合的可决系数R2均大于0.99,并且在不同初始浓度的刚果红溶液下,通过二级动力学模型计算的Fe3O4@ZIF-8单位吸附容量与通过实验获得的实际单位吸附容量相接近。这与之前报道的ZIF-8吸附刚果红染料的研究[20]一致。因此,偶氮染料刚果红在Fe3O4@ZIF-8上的吸附过程满足二级动力学模型。这表明Fe3O4@ZIF-8吸附刚果红的过程属于化学吸附过程。
-
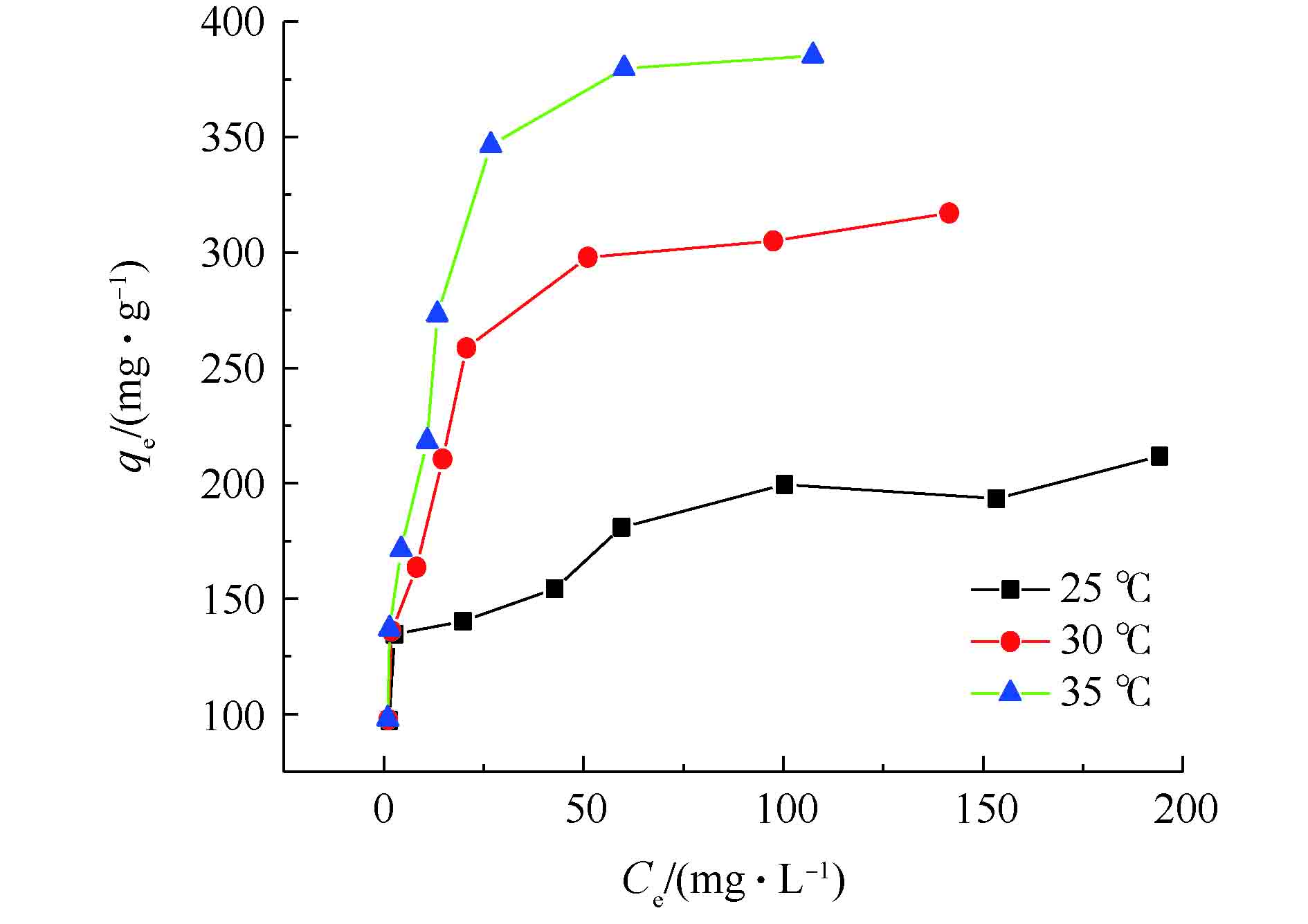
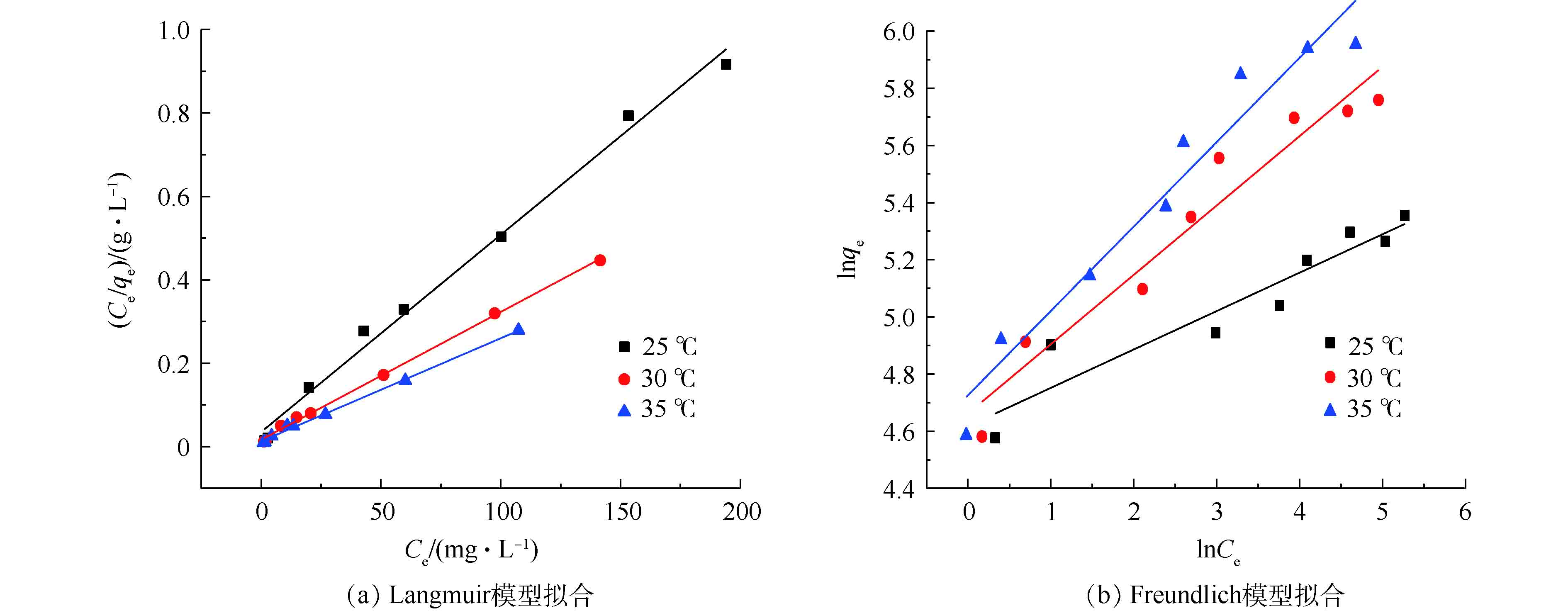
由图9可知,当反应温度升高时,Fe3O4@ZIF-8对偶氮染料刚果红的单位吸附容量不断增加。温度由25 ℃升到35 ℃时,平衡吸附量由211 mg·g−1升高到385 mg·g−1,说明吸附反应为吸热反应。并且随着刚果红初始浓度C0的增加,吸附达到饱和时的平衡浓度Ce增加,平衡吸附量的变化趋势是先快速增加后逐渐变缓。利用Langmuir吸附等温方程和Freundlich吸附等温方程分别线性拟合吸附等温线中的数据,得到等温方程的模拟结果(如图10所示)。吸附等温方程相关参数见表2。由图10可知,Langmuir等温吸附模型具有更高的线性相关性。由表2可知,Langmuir模型计算得到的可决系数更高(R2>0.99),故Fe3O4@ZIF-8的吸附等温线符合Langmuir模型。这表明Fe3O4@ZIF-8对刚果红染料的吸附行为是单层吸附。同时,RL值均在0~1之间,表明吸附容易进行。因此,Langmuir吸附等温线模型适用于Fe3O4@ZIF-8对刚果红的去除。通过Langmuir吸附等温模型计算得到的Fe3O4@ZIF-8最大单位吸附容量为405 mg·g−1。
-
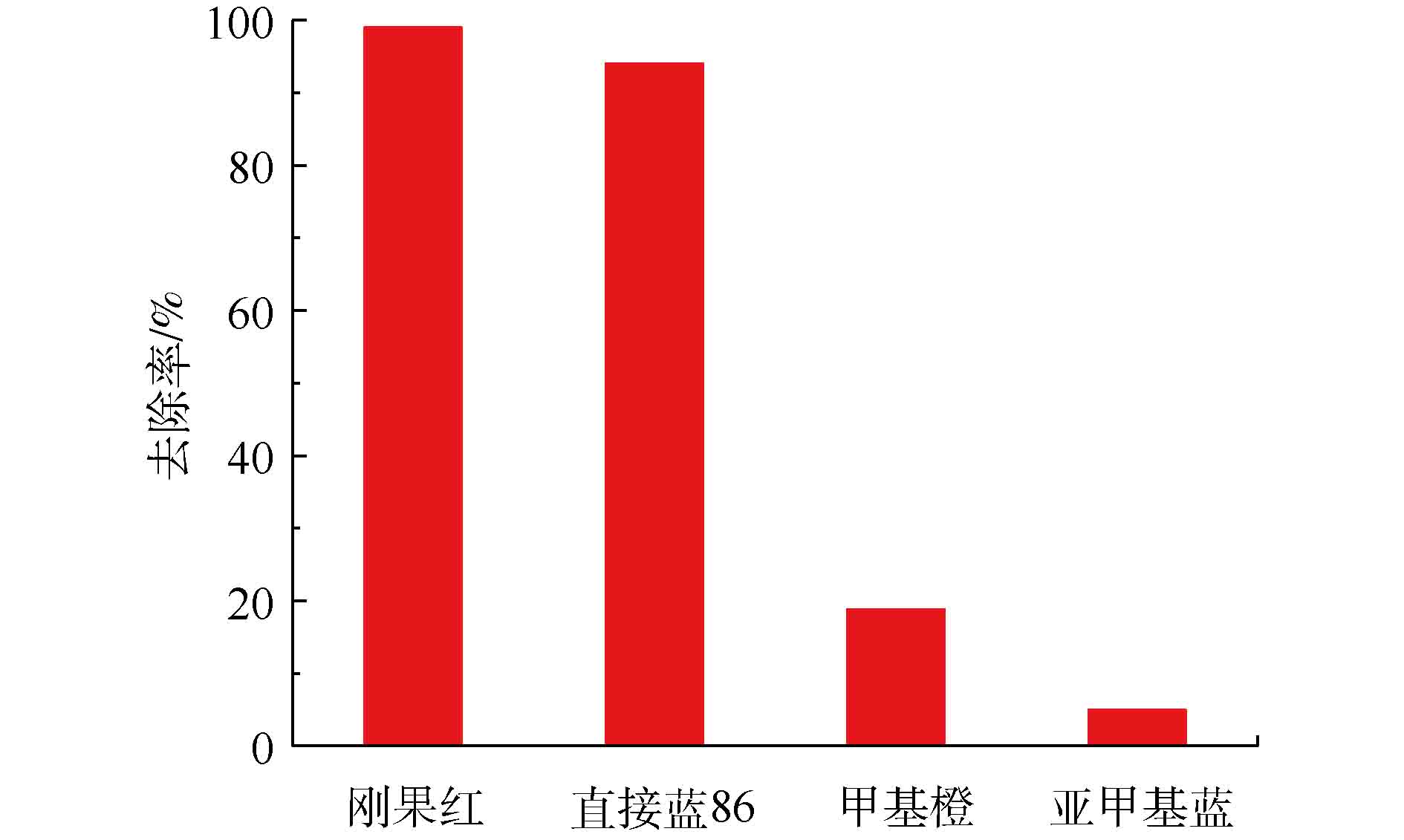
本实验考察了Fe3O4@ZIF-8对染料的选择吸附性能,结果如图11所示。Fe3O4@ZIF-8对于染料的去除率为刚果红>直接蓝86 >甲基橙>亚甲基蓝。这说明Fe3O4@ZIF-8对染料分子的结合能力有差别,并且可能和染料分子的结构和组成有关系。亚甲基蓝是表面带有正电荷的阳离子类型的偶氮染料,在实验条件下,表面带有正电荷的Fe3O4@ZIF-8和亚甲基蓝染料发生静电互斥,造成亚甲基蓝的吸附容量非常低。而其他3种染料都是表面带负电荷的阴离子型偶氮染料,Fe3O4@ZIF-8对刚果红的去除率接近100%,对直接蓝86的去除率也非常高,甲基橙的去除率就非常低。这可能是因为刚果红和直接蓝86染料分子带有2个—SO3基团,而甲基橙带有1个—SO3基团,造成Fe3O4@ZIF-8对染料分子的静电引力的强弱存在差别[21]。同时,直接蓝86染料的分子质量和分子体积大于刚果红染料,造成直接蓝86的去除率低于刚果红染料。因此,Fe3O4@ZIF-8适用于去除阴离子类型的偶氮染料刚果红。
-
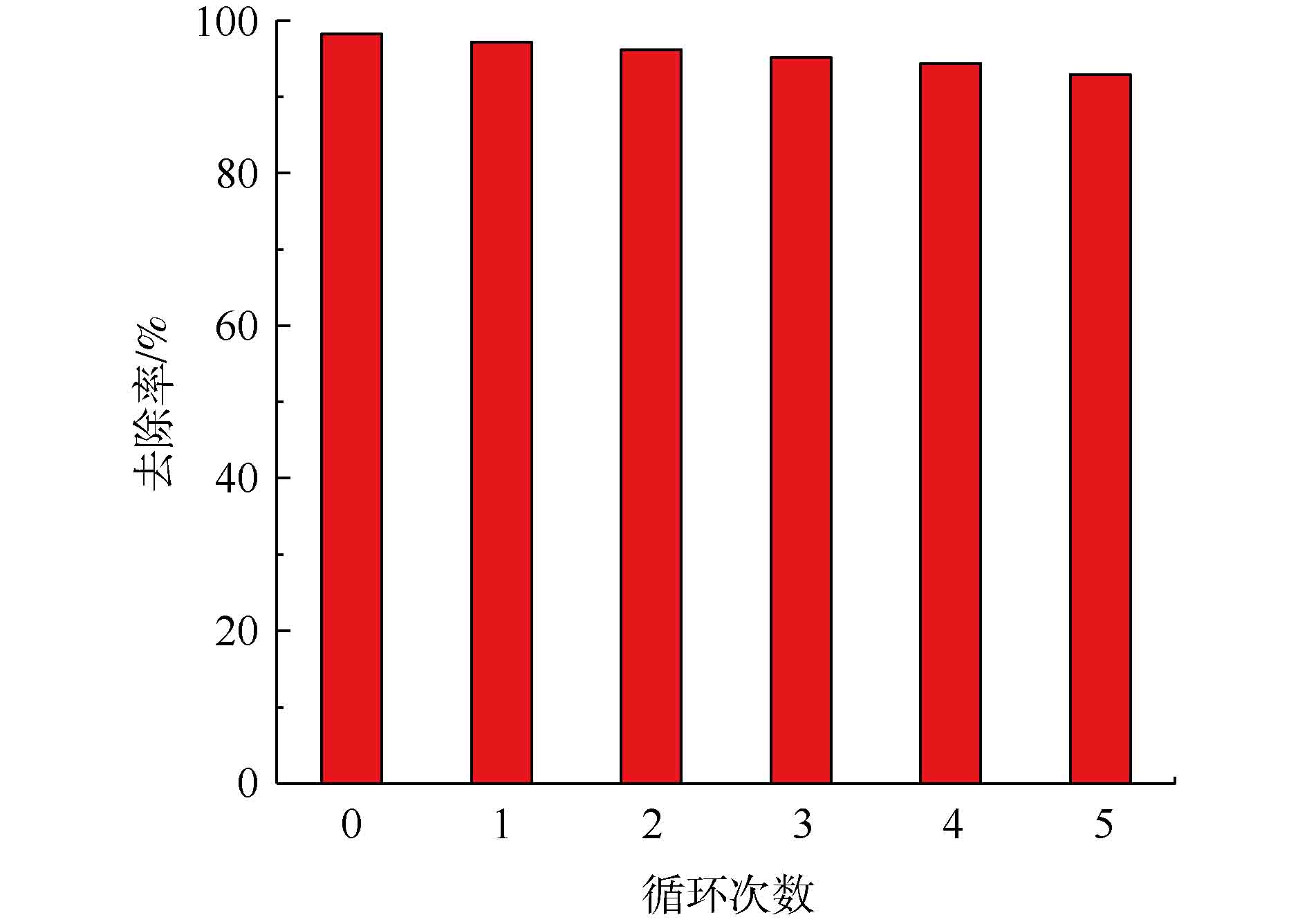
在实验中,对吸附剂Fe3O4@ZIF-8的重复利用效果进行了实验验证。由图12可知,当循环次数增加时,Fe3O4@ZIF-8对刚果红染料的去除率是不断下降的,但是下降的幅度非常小。经过5次循环后,去除率从最开始的98%下降到93%,只下降了5%。显然,Fe3O4@ZIF-8具备非常优异的循环吸附特性,该材料可以重复用于阴离子偶氮染料刚果红废水的去除。
-
1)采用常温机械搅拌法成功将Fe3O4纳米颗粒和金属有机骨架ZIF-8复合,制备出磁性核壳金属有机骨架Fe3O4@ZIF-8。
2) 将Fe3O4@ZIF-8作为新型吸附材料,系统考察了其对刚果红染料的吸附效果。当刚果红初始浓度为70 mg·L−1时,Fe3O4@ZIF-8对刚果红的去除率达到98%。实验表明,Fe3O4@ZIF-8的吸附量随着刚果红初始浓度的增加而增加,同时pH对吸附效果有很大的影响,低pH时,Fe3O4@ZIF-8和刚果红之间产生静电吸引;随着pH的不断升高,刚果红与Fe3O4@ZIF-8之间产生静电斥力,吸附量逐渐降低。
3) Fe3O4@ZIF-8吸附刚果红的动力学符合二级动力学模型,等温线符合Langmuir模型,Fe3O4@ZIF-8对刚果红的吸附是物理吸附与化学吸附并存,静电引力是其主要的吸附机理。
4) Fe3O4@ZIF-8吸附材料展示出优异的循环吸附性能以及对刚果红染料的高效选择性。因此,磁性核壳金属有机骨架Fe3O4@ZIF-8作为新型吸附材料在去除刚果红染料方面有着巨大的潜力。
磁性金属有机骨架Fe3O4@ZIF-8的制备及对偶氮染料刚果红的高效吸附
Preparation of magnetic metal organic framework Fe3O4@ZIF-8 and its high efficient adsorption towards azo dye congo red
-
摘要: 采用常温搅拌法,在聚苯乙烯磺酸钠(PSS)处理过的Fe3O4表面诱导生长ZIF-8壳层,成功合成了磁性核壳金属有机骨架Fe3O4@ZIF-8,并对其吸附去除偶氮染料刚果红的性能进行了探究,考察了刚果红初始浓度和接触时间、Fe3O4@ZIF-8投加量以及pH对刚果红去除的影响。SEM、TEM、XRD、FT-IR及VSM表征结果证明,ZIF-8纳米颗粒已成功负载于Fe3O4表面,形成了典型的核壳结构,并且具有优异的磁学性能。吸附实验结果表明,反应最佳pH为6,吸附剂投加量为500 mg·L−1;当反应时间达到180 min 时,吸附达到平衡。吸附反应的吸附动力学和吸附等温线分析表明,刚果红染料在Fe3O4@ZIF-8上的吸附动力学符合二级动力学方程,吸附等温线符合Langmuir模型。Fe3O4@ZIF-8吸附剂对刚果红具有高效的选择吸附性能并且在循环吸附中展现出良好的循环吸附性能。因此,磁性核壳金属有机骨架Fe3O4@ZIF-8作为吸附剂在去除刚果红染料方面有着广阔的应用前景。
-
关键词:
- 磁性金属有机骨架 /
- Fe3O4@ZIF-8 /
- 刚果红 /
- 吸附动力学
Abstract: The magnetic core-shell metal organic framework Fe3O4@ZIF-8 was successfully synthesized by treating the surface of Fe3O4 with sodium polystyrene sulfonate (PSS) and inducing ZIF-8 shell growth on it under continuous stirring at room temperature. The performance of adsorption and removal of azo dye congo red by Fe3O4@ZIF-8 was investigated. The effects of initial concentration and contact time, Fe3O4@ZIF-8 dosage and pH on congo red removal were investigated. The characterization of SEM, TEM, XRD, FT-IR and VSM showed that ZIF-8 nanoparticles have been successfully loaded on the surface of Fe3O4 to form a typical core-shell structure with excellent magnetic properties. The experimental results showed that the optimum pH was 6, the dosage of adsorbent was 500 mg·L−1, and the adsorption equilibrium was achieved at the reaction time of 180 min. The adsorption kinetics of congo red on Fe3O4@ZIF-8 was in accordance with the second-order kinetic equation, and the adsorption isotherm followed Langmuir model. Fe3O4@ZIF-8 adsorbent had high selective adsorption performance for congo red and presented good reusability in cyclic adsorption. Therefore, magnetic core-shell metal-organic framework Fe3O4@ZIF-8 had broad application prospects in the removal of congo red dyes as adsorbent.-
Key words:
- magnetic metal organic framework /
- Fe3O4@ZIF-8 /
- congo red /
- adsorption kinetics
-
近年来,工业化的迅速发展造成了许多环境污染问题。染料废水作为一种典型的工业废水因其水量大、色度高、组成成分复杂而导致其处理难度非常高[1]。若未经处理而排放到自然水体,将会污染水源,威胁生态环境,并且其生物毒性通过食物链而最终在人体积累,严重危害人体健康[2]。目前,染料废水的去除方法主要有物理法、化学法及生物法[3-4]。物理法是目前研究染料废水处理最为广泛的一种处理方法,其中吸附法作为一种绿色高效的去除技术被广泛地应用于染料废水的去除。吸附剂的选择对于使用吸附法去除染料废水至关重要。目前,常用的吸附材料有活性炭、焦炭、沸石、壳聚糖以及天然黏土矿物等[5]。但是这些吸附剂的吸附容量不高,或者选择吸附性差。因此,开发一种高效和大吸附量的吸附剂用于染料废水的去除非常必要。
金属有机骨架是通过共价键或者离子共价键自组装金属中心离子和有机配体形成的具有周期性网络结构的配位聚合物[6]。因其高的比表面积和可调的孔径[7]、丰富的结构和组成成分、配位不饱和位点能够结合特定官能团[8]等特点而被广泛应用于储能、气液相分离、催化、光学和磁学等领域[9-11]。沸石咪唑基骨架(ZIFs)作为MOFs材料的一种,具有优异的化学稳定性和吸附性能。张琪颖[12]研究了ZIF-8对硝基苯酚(PNP)的吸附效果,研究表明,ZIF-8在反应最佳条件下能够高效选择性地吸附PNP。同时,磁性纳米复合材料作为吸附剂应用于水处理中也受到广泛关注。孙杨等[13]利用自制Fe3O4磁性材料与MOF-5合成磁性Fe3O4@MOF-5复合材料,被证明Fe3O4@MOF-5复合材料对于刚果红是良好的吸附剂。基于上述研究,本研究采用聚苯乙烯磺酸钠(PSS)处理Fe3O4表面诱导生长ZIF-8壳层,在常温搅拌下,成功合成磁性核壳金属有机骨架Fe3O4@ZIF-8,通过SEM、TEM、XRD、FT-IR及VSM对其进行形貌分析,考察了刚果红初始浓度及接触时间、Fe3O4@ZIF-8用量、pH等因素对Fe3O4@ZIF-8吸附偶氮染料刚果红废水的影响;确定了其吸附动力学和吸附等温线;探讨了Fe3O4@ZIF-8的选择吸附性能以及循环再生性能,研究可为复合金属有机骨架材料在染料吸附去除方面的应用提供参考。
1. 实验部分
1.1 实验仪器与试剂
仪器:电子天平(AL104,梅特勒-多利多仪器上海有限公司);超纯水机(Ther-mo Scientific Barnstead EasypureⅡ);精密增力电动搅拌器(金坛市新航仪器厂);真空干燥箱(DZF-6020型,上海浦东荣丰科学仪器有限公司);恒温干燥箱(101-1型,上海东星建材实验设备有限公司);pH计(PHB-4型,上海仪电科学仪器股份有限公司);双功能水浴恒温振荡器(SHA-B,金坛市科析仪器有限公司);扫描电镜(Quanta FEG型,美国FEI公司);分光光度计(PhotoLab-7600型,赛莱默中国分析仪器有限公司)。
材料与试剂:六水合硝酸锌(Zn(NO3)2·6H2O)(分析纯,国药化学试剂有限公司);2-甲基咪唑(C4H6N2)(分析纯,阿拉丁试剂有限公司);聚苯乙烯磺酸钠(PSS)(30%,阿拉丁试剂有限公司);甲醇(CH3OH)(分析纯,阿拉丁试剂有限公司);Fe3O4纳米颗粒(99%,成都麦卡希有限公司);氢氧化钠(NaOH)(分析纯,重庆川东化工有限公司);盐酸(HCl)(分析纯,重庆川东化工有限公司);氯化钠(优级纯,阿拉丁试剂有限公司);刚果红(分析纯,阿拉丁试剂有限公司);去离子水,实验室自制。
1.2 磁性金属有机骨架Fe3O4@ZIF-8的制备
Fe3O4@ZIF-8的合成参照文献中的方法[14]。将1.5 g的聚苯乙烯磺酸钠(PSS)溶解在150 mL去离子水中并超声处理30 min,配制成PSS溶液,将0.25 g的Fe3O4纳米颗粒加入到PSS溶液中并在室温下超声30 min,然后,通过外部磁体将Fe3O4纳米粒子与溶液分离并用水洗涤3次;处理后的Fe3O4纳米微粒投加到ZIF-8的合成液中(1.19 g硝酸锌,2.63 g二甲基咪唑和80 mL甲醇),在50 ℃水浴条件下,机械搅拌8 h,然后通过磁铁把合成的Fe3O4@ZIF-8磁性核壳颗粒与反应体系分离。用甲醇溶液洗涤磁性粒子3次,并在真空干燥箱中60 ℃烘干12 h,最后获取Fe3O4@ZIF-8。
1.3 材料表征
采用扫描电子显微镜(SEM,Quanta FEG,FEI公司,美国)和透射电子显微镜(TEM,Tecnai F30,FEI公司,美国)对磁性金属有机骨架Fe3O4@ZIF-8的微观形貌进行分析。采用X射线衍射(XRD,X/Pert PRO MPD,帕纳科分析仪器有限公司,荷兰)对Fe3O4@ZIF-8的晶体结构进行表征。Fe3O4@ZIF-8表面官能团信息采用傅里叶变换红外分光光度计(FT-IR,Nicolet iS50,Nicolet公司,美国)测定。Fe3O4@ZIF-8的磁学性能采用振动样品磁强计(7400型,Lake shore公司,美国)进行测试。
1.4 吸附实验
本实验选择阴离子偶氮染料刚果红为模拟染料废水,研究磁性金属有机骨架Fe3O4@ZIF-8材料对其去除效果,在一系列规格为50 mL的锥形瓶内,倒进20 mL刚果红染料溶液,准确投加一定质量的Fe3O4@ZIF-8吸附剂,把锥形瓶放入振荡器中,25 ℃下恒温振荡,吸附一段时间后,用磁铁将吸附剂Fe3O4@ZIF-8从溶液中分离出来,取上层溶液用分光光度计测定光度值,然后分别计算Fe3O4@ZIF-8的吸附容量和刚果红去除率。
去除率和单位吸附量的计算方法见式(1)和式(2)。
η=C0−CC0×100% (1) q=(C0−C)Vm (2) 式中:
η 为去除率;C0为刚果红的初始浓度,mg·L−1;C为刚果红浓度,mg·L−1;q为吸附剂的吸附量,mg·g−1;V为溶液体积,L;m为Fe3O4@ZIF-8质量,g。1)吸附动力学实验。取不同初始浓度的20 mL刚果红溶液,并投加Fe3O4@ZIF-8吸附剂10 mg。在25 ℃下进行恒温振荡,分别吸附5、10、20、30、60、90、120、180和240 min后,离心混合溶液并测定上清液的吸光度。吸附数据由一级动力学方程[15]和二级动力学方程[16]来进行拟合。一级动力学方程见式(3),二级动力学方程见式(4)。
ln(qe−q)=lnqe−K1t (3) tq=1K2q2e+tqe (4) 式中:qe为吸附剂的平衡吸附量,mg·g−1;q为吸附剂在t时刻的吸附量,mg·g−1;t为吸附时间,min;K1为一级动力学速率常数,min−1;K2为二级动力学速率常数,g·(mg·min)−1。
2)吸附等温线测定。配置20 mL初始浓度为50~300 mg·L−1的刚果红溶液,加入10 mg的Fe3O4@ZIF-8吸附剂。将混合溶液的pH调节至6,并在25、30、35 ℃下进行振荡,直至吸附达到平衡。吸附数据由Langmuir吸附等温方程[17](见式(5))和Freundlich吸附等温方程[18](见式(6))进行拟合。
Ceqe=1qb+Ceq (5) lnqe=lnKf+1nlnCe (6) 式中:qe为吸附剂的平衡吸附量,mg·g−1;Ce为平衡质量浓度,mg·L−1;q为Fe3O4@ZIF-8的最大吸附量,mg·g−1;b为吸附能有关常数;Kf为Freundlich系数;n为Freundlich常数。
3)选择吸附实验。在实验中,使用Fe3O4@ZIF-8作为吸附剂以吸附刚果红、直接蓝86、甲基橙、亚甲基蓝染料,以此来考察Fe3O4@ZIF-8的选择吸附性能。取30 mg·L−1的不同染料20 mL,加入10 mg的Fe3O4@ZIF-8,在恒定温度下吸附12 h,测定吸附后的浓度。
4)循环性能实验。Fe3O4@ZIF-8吸附50 mg·L−1的刚果红溶液后,使用蒸馏水反复冲洗吸附剂,随后采用0.1 mol·L−1的NaOH溶液进行解吸,然后烘干用于下一个周期中。重复5次,考察Fe3O4@ZIF-8的吸附解吸能力。
2. 结果与讨论
2.1 Fe3O4@ZIF-8表征
1) SEM和TEM分析。图1(a)~(c)是在不同放大倍数下的SEM图,可以看出,Fe3O4@ZIF-8纳米粒子呈现不规则的立方体结构,并且表面分布了很多ZIF-8晶体。图1(d)~(f)为Fe3O4@ZIF-8在不同放大倍数下的TEM图,可以看出,该复合材料呈现明显的核壳形态,ZIF-8已成功地生长在Fe3O4纳米颗粒表面。这种磁性复合材料的平均粒径在200 nm左右。SEM和TEM表征很好地证明了合成的材料即为核壳结构的Fe3O4@ZIF-8。
2) XRD分析。由图2可知,Fe3O4@ZIF-8材料在2θ为30.16°、35.52°、43.18°、53.52°、57.06°处均出现了特征峰,与实验中Fe3O4的表征图谱比较,特征峰的位置相同,分别对应的是Fe3O4的(220)、(311)、(400)、(422)和(511)衍射晶面。同时,在(011)、(002)、(112)、(022)、(013)、(222)处均出现了与实验表征的ZIF-8 图谱对应一致的衍射峰。所以,可断定Fe3O4@ZIF-8已成功合成,且Fe3O4@ZIF-8中Fe3O4的晶型结构没有遭到破坏。这说明Fe3O4@ZIF-8不仅具备ZIF-8的高效吸附性能,同时还具有Fe3O4的磁性分离性能。
3) FTIR分析。从图3中的Fe3O4@ZIF-8红外图谱可知,在3 454 cm−1处出现了对应于水分子中的O—H键的特征吸收峰。3 135 cm−1和2 926 cm−1分别归属于ZIF-8结构中咪唑分子芳香族与脂肪族的C—H键的特征峰。咪唑环中C=N键的伸缩振动峰出现在1 565 cm−1处,C—N键的振动吸收峰出现在1 146和993 cm−1处。在420 cm−1处出现了Zn—N官能团振动峰,最重要的是在580 cm−1处出现了属于Fe3O4的Fe—O振动吸收峰[19]。综合上述分析,可以进一步确定成功合成的核壳结构物质就是Fe3O4@ZIF-8。
4) VSM分析。如图4所示,Fe3O4@ZIF-8的磁滞回线为过原点的S型曲线,表明Fe3O4@ZIF-8材料是典型的超顺磁性。Fe3O4@ZIF-8的饱和磁化强度为49.68 emu·g−1,由于ZIF-8在壳层的覆盖,Fe3O4@ZIF-8的磁饱和度相对于Fe3O4有所降低,但是Fe3O4@ZIF-8仍然具有优异的磁学性能。
2.2 刚果红初始浓度及接触时间的影响
从图5可以看出,在同一浓度下,Fe3O4@ZIF-8的单位吸附容量随着反应时间的增加而增加,在反应的前10 min左右,单位吸附容量已达平衡吸附量的50%。这表明反应最初是快速吸附阶段。当反应时间为180 min时,Fe3O4@ZIF-8的单位吸附量逐渐达到平衡。并且在不同的刚果红初始浓度下,随着初始浓度的升高,Fe3O4@ZIF-8的单位吸附量也逐渐升高。当初始浓度由30 mg·L−1升高到70 mg·L−1时,Fe3O4@ZIF-8的单位吸附量由60 mg·g−1升高到136 mg·g−1。
2.3 Fe3O4@ZIF-8投加量的影响
图6为Fe3O4@ZIF-8投加量对吸附效果的影响,当Fe3O4@ZIF-8投加量为5 mg时,吸附除去率达到68.7%,从5 mg变化到10 mg时,Fe3O4@ZIF-8对刚果红染料的去除率升高到95.2%。当Fe3O4@ZIF-8投加量大于10 mg,其去除率约为98%,刚果红的吸附去除率升高幅度不大,并且随着Fe3O4@ZIF-8吸附剂投加量的不断增长,其单位吸附容量是一直减少的,这是因为当染料初始浓度和体积恒定时,单位质量的吸附剂吸附染料的量随着吸附剂投加量的增多而减少。并且过多的吸附剂量将导致吸附剂位点的聚集和重叠,增加了扩散的难度。同时,从经济角度来看,过多的吸附剂投加会造成成本的增加。因此,选择Fe3O4@ZIF-8吸附剂的用量为500 mg·L−1。
2.4 pH的影响
移取20 mL的 50 mg·L−1的刚果红溶液,通过0.05 mol·L−1的NaOH溶液和0.05 mol·L−1的HCl溶液调节pH从3变化到10,Fe3O4@ZIF-8吸附剂的投加量为10 mg,在 25 ℃条件下以180 r·min−1的速度恒温振荡6 h,利用磁铁将吸附剂与溶液分离,然后通过分光光度计测定溶液的分光度,考察初始的pH对Fe3O4@ZIF-8吸附效果的影响,实验结果如图7所示。如图7(a)所示,当pH<6.0时,Fe3O4@ZIF-8的单位吸附容量随着pH的升高而升高,而且升高幅度很大;在pH=6.0时,单位吸附量达到最大值,这是由于Fe3O4@ZIF-8表面带的正电荷数量增加,与刚果红分子产生静电引力导致吸附量升高;当pH>6.0时,单位吸附量随着pH的升高而减小。这可由图7(b)来解释。实验测得Fe3O4@ZIF-8的等电点为8.37。当pH<8.37时,Fe3O4@ZIF-8表面是带有正电荷的,而刚果红分子带有负电荷,Fe3O4@ZIF-8因为强烈的静电引力而吸附刚果红染料,随后pH的升高,溶液中的OH−逐渐增多并且和阴离子刚果红染料竞争Fe3O4@ZIF-8的吸附位点,从而导致吸附量下降。当pH>8.37时,Fe3O4@ZIF-8表面由原来的正电荷转为负电荷,它与带负电的刚果红分子相互排斥导致其单位吸附容量减少有关。因此,在低pH时,静电引力使刚果红吸附量增加,随着pH的升高,刚果红与Fe3O4@ZIF-8之间产生静电斥力,吸附量逐渐降低。
2.5 吸附动力学
由图8可知,吸附数据的拟合结果是二级动力学模型明显优于一级动力学模型,其线性相关性更高。具体的拟合数据如表1所示,一级动力学模型和二级动力学模型拟合的效果都很好,其中二级动力学模型拟合的可决系数R2均大于0.99,并且在不同初始浓度的刚果红溶液下,通过二级动力学模型计算的Fe3O4@ZIF-8单位吸附容量与通过实验获得的实际单位吸附容量相接近。这与之前报道的ZIF-8吸附刚果红染料的研究[20]一致。因此,偶氮染料刚果红在Fe3O4@ZIF-8上的吸附过程满足二级动力学模型。这表明Fe3O4@ZIF-8吸附刚果红的过程属于化学吸附过程。
表 1 Fe3O4@ZIF-8对刚果红染料的动力学拟合参数Table 1. Parameters of kinetic models for CR onto Fe3O4@ZIF-8初始浓度/(mg·L−1) qe, exp/(mg·g−1) 一级动力学模型 二级动力学模型 qe, cal/(mg·g−1) K1 R2 qe, cal/(mg·g−1) K2 R2 30 60 26 0.021 0.947 61 0.002 25 0.999 50 98 71 0.024 0.978 104 0.000 63 0.995 70 136 124 0.023 0.963 145 0.000 32 0.993 注:qe,exp和qe,cal为平衡吸附量实验值和拟合值。 2.6 吸附等温线
由图9可知,当反应温度升高时,Fe3O4@ZIF-8对偶氮染料刚果红的单位吸附容量不断增加。温度由25 ℃升到35 ℃时,平衡吸附量由211 mg·g−1升高到385 mg·g−1,说明吸附反应为吸热反应。并且随着刚果红初始浓度C0的增加,吸附达到饱和时的平衡浓度Ce增加,平衡吸附量的变化趋势是先快速增加后逐渐变缓。利用Langmuir吸附等温方程和Freundlich吸附等温方程分别线性拟合吸附等温线中的数据,得到等温方程的模拟结果(如图10所示)。吸附等温方程相关参数见表2。由图10可知,Langmuir等温吸附模型具有更高的线性相关性。由表2可知,Langmuir模型计算得到的可决系数更高(R2>0.99),故Fe3O4@ZIF-8的吸附等温线符合Langmuir模型。这表明Fe3O4@ZIF-8对刚果红染料的吸附行为是单层吸附。同时,RL值均在0~1之间,表明吸附容易进行。因此,Langmuir吸附等温线模型适用于Fe3O4@ZIF-8对刚果红的去除。通过Langmuir吸附等温模型计算得到的Fe3O4@ZIF-8最大单位吸附容量为405 mg·g−1。
表 2 Langmuir和Freundlich常数及可决系数Table 2. Langmuir and Freundlich adsorption constants and correlation coefficients温度/℃ Langmuir模型 Freundlich模型 qmax /(mg·g−1) b/(L·mg−1) RL R2 Kf /(L·g−1) n R2 25 211 0.135 0.024 0.992 101.21 7.44 0.881 30 327 0.184 0.018 0.998 105.81 4.12 0.934 35 405 0.192 0.017 0.996 112.78 3.39 0.944 2.7 Fe3O4@ZIF-8的选择吸附性能
本实验考察了Fe3O4@ZIF-8对染料的选择吸附性能,结果如图11所示。Fe3O4@ZIF-8对于染料的去除率为刚果红>直接蓝86 >甲基橙>亚甲基蓝。这说明Fe3O4@ZIF-8对染料分子的结合能力有差别,并且可能和染料分子的结构和组成有关系。亚甲基蓝是表面带有正电荷的阳离子类型的偶氮染料,在实验条件下,表面带有正电荷的Fe3O4@ZIF-8和亚甲基蓝染料发生静电互斥,造成亚甲基蓝的吸附容量非常低。而其他3种染料都是表面带负电荷的阴离子型偶氮染料,Fe3O4@ZIF-8对刚果红的去除率接近100%,对直接蓝86的去除率也非常高,甲基橙的去除率就非常低。这可能是因为刚果红和直接蓝86染料分子带有2个—SO3基团,而甲基橙带有1个—SO3基团,造成Fe3O4@ZIF-8对染料分子的静电引力的强弱存在差别[21]。同时,直接蓝86染料的分子质量和分子体积大于刚果红染料,造成直接蓝86的去除率低于刚果红染料。因此,Fe3O4@ZIF-8适用于去除阴离子类型的偶氮染料刚果红。
2.8 Fe3O4@ZIF-8的循环再生性
在实验中,对吸附剂Fe3O4@ZIF-8的重复利用效果进行了实验验证。由图12可知,当循环次数增加时,Fe3O4@ZIF-8对刚果红染料的去除率是不断下降的,但是下降的幅度非常小。经过5次循环后,去除率从最开始的98%下降到93%,只下降了5%。显然,Fe3O4@ZIF-8具备非常优异的循环吸附特性,该材料可以重复用于阴离子偶氮染料刚果红废水的去除。
3. 结论
1)采用常温机械搅拌法成功将Fe3O4纳米颗粒和金属有机骨架ZIF-8复合,制备出磁性核壳金属有机骨架Fe3O4@ZIF-8。
2) 将Fe3O4@ZIF-8作为新型吸附材料,系统考察了其对刚果红染料的吸附效果。当刚果红初始浓度为70 mg·L−1时,Fe3O4@ZIF-8对刚果红的去除率达到98%。实验表明,Fe3O4@ZIF-8的吸附量随着刚果红初始浓度的增加而增加,同时pH对吸附效果有很大的影响,低pH时,Fe3O4@ZIF-8和刚果红之间产生静电吸引;随着pH的不断升高,刚果红与Fe3O4@ZIF-8之间产生静电斥力,吸附量逐渐降低。
3)Fe3O4@ZIF-8吸附刚果红的动力学符合二级动力学模型,等温线符合Langmuir模型,Fe3O4@ZIF-8对刚果红的吸附是物理吸附与化学吸附并存,静电引力是其主要的吸附机理。
4)Fe3O4@ZIF-8吸附材料展示出优异的循环吸附性能以及对刚果红染料的高效选择性。因此,磁性核壳金属有机骨架Fe3O4@ZIF-8作为新型吸附材料在去除刚果红染料方面有着巨大的潜力。
-
表 1 Fe3O4@ZIF-8对刚果红染料的动力学拟合参数
Table 1. Parameters of kinetic models for CR onto Fe3O4@ZIF-8
初始浓度/(mg·L−1) qe, exp/(mg·g−1) 一级动力学模型 二级动力学模型 qe, cal/(mg·g−1) K1 R2 qe, cal/(mg·g−1) K2 R2 30 60 26 0.021 0.947 61 0.002 25 0.999 50 98 71 0.024 0.978 104 0.000 63 0.995 70 136 124 0.023 0.963 145 0.000 32 0.993 注:qe,exp和qe,cal为平衡吸附量实验值和拟合值。 表 2 Langmuir和Freundlich常数及可决系数
Table 2. Langmuir and Freundlich adsorption constants and correlation coefficients
温度/℃ Langmuir模型 Freundlich模型 qmax /(mg·g−1) b/(L·mg−1) RL R2 Kf /(L·g−1) n R2 25 211 0.135 0.024 0.992 101.21 7.44 0.881 30 327 0.184 0.018 0.998 105.81 4.12 0.934 35 405 0.192 0.017 0.996 112.78 3.39 0.944 -
[1] 龚正君, 周文波, 陈钰. 花生壳活性炭对水中荧光素钠的吸附及动力学[J]. 环境工程学报, 2013, 7(1): 221-225. [2] 叶琳. 改性豆渣对污水中染料物质的吸附研究[D]. 重庆: 西南大学, 2014. [3] GREENWALD M J, REDDING A M, CANNON F S. A rapid kinetic dye test to predict the adsorption of 2-methylisoborneol onto granular activated carbons and to identify the influence of pore volume distributions[J]. Water Research, 2015, 68: 784-792. doi: 10.1016/j.watres.2014.10.022 [4] LIU F, GUO Z, LING H, et al. Effect of pore structure on the adsorption of aqueous dyes to ordered mesoporous carbons[J]. Microporous & Mesoporous Materials, 2016, 227: 104-111. [5] YANG R, LI H J, HUANG M, et al. A review on chitosan-based flocculants and their applications in water treatment[J]. Water Research, 2016, 95: 59-89. doi: 10.1016/j.watres.2016.02.068 [6] CHAMPNESS N R, SCHRODER M. Extended networks formed by coordination polymers in the solid state[J]. Current Opinion in Solid State & Materials Science, 1998, 3(4): 419-424. [7] LU W G, WEI Z W, GU Z Y, et al. Tuning the structure and function of metal-organic frameworks via linker design[J]. Chemical Society Reviews, 2014, 43(16): 5561-5593. doi: 10.1039/C4CS00003J [8] EVANS J D, SUMBY C J, DOONAN C J. Post-synthetic metalation of metal-organic frameworks[J]. Chemical Society Reviews, 2014, 43(16): 5933-5951. doi: 10.1039/C4CS00076E [9] LEE J Y, FARHA O K, ROBERTS J, et al. Metal-organic framework materials as catalysts[J]. Chemical Society Reviews, 2009, 38(5): 1450-1459. doi: 10.1039/b807080f [10] KRENO L E, KIRSTY L, FARHA O K, et al. Metal-organic framework materials as chemical sensors[J]. Chemical Reviews, 2011, 112(2): 1105-1125. [11] LI J R, JULIAN S, ZHOU H C. Metal-organic frameworks for separations[J]. Chemical Reviews, 2012, 112(2): 869-932. doi: 10.1021/cr200190s [12] 张琪颖. 基于金属有机骨架材料的高效吸附剂研发[D]. 济南: 济南大学, 2016. [13] 孙杨, 陆广明, 唐祝兴. 磁性纳米材料Fe3O4@MOF-5的制备及其对刚果红吸附性能的研究[J]. 辽宁化工, 2017, 46(11): 12-14. [14] 张通. ZIF-8包覆的核-壳结构材料的合成及其应用[D]. 大连: 大连理工大学, 2015. [15] ZHOU L C, MENG X G, FU J W, et al. Highly efficient adsorption of chlorophenols onto chemically modified chitosan[J]. Applied Surface Science, 2014, 292(1): 735-741. [16] MOGHADDAM H K, PAKIZEH M. Experimental study on mercury ions removal from aqueous solution by MnO2 /CNTs nanocomposite adsorbent[J]. Journal of Industrial & Engineering Chemistry, 2015, 21: 221-229. [17] LORENC-GRABOWSKA E, RUTKOWSKI P. High basicity adsorbents from solid residue of cellulose and synthetic polymer co-pyrolysis for phenol removal: Kinetics and mechanism[J]. Applied Surface Science, 2014, 316(1): 435-442. [18] YANG G, CHEN H L, QIN H D, et al. Amination of activated carbon for enhancing phenol adsorption: Effect of nitrogen-containing functional groups[J]. Applied Surface Science, 2014, 293(3): 299-305. [19] LI B J, CAO H Q, SHAO J, et al. Superparamagnetic Fe3O4 nanocrystals@graphene composites for energy storage devices[J]. Journal of Materials Chemistry, 2011, 21(13): 5069-5075. doi: 10.1039/c0jm03717f [20] 顾兵. 沸石咪唑酯骨架结构材料(ZIF-8)对染料废水中刚果红的吸附效果和特征分析研究[D]. 南京: 南京农业大学, 2015. [21] 张湛杭, 张景丽, 刘建明. 金属有机骨架ZIF-67对刚果红的吸附性研究[J]. 天津城建大学学报, 2017, 23(4): 267-272. -





 下载:
下载: