酸化破乳-萃取-蒸氨预处理用于催化湿式过氧化氢氧化处理煤气化废水
Acidification demulsion-extraction-steamed ammonia pretreatment for catalytic wet peroxide oxidation of coal gasification wastewater treatment
-
摘要: 调酸-萃取-蒸氨工序预处理煤气化废水温度达87~95℃,联合高温催化湿式过氧化氢氧化(catalitic wet peroxide oxidation,CWPO)处理煤气化废水,可显著提高废水可生化性。比较了3% Fe/椰壳炭、3% Fe/Al2O3在CWPO过程中的催化性能。实验结果表明,在反应条件为80℃、pH0为4、H2O2加入量为7.8~10.5 mg·L-1、空速(LHSV)为0.5 h-1时,3% Fe/椰壳炭对预处理煤气化出水COD去除率高达60%,对总酚的去除率高达90%以上,H2O2利用率大于99%,色度由初始1 000倍降至2倍,此外,出水B/C为0.51,达到进入生化处理系统的水质要求。
-
关键词:
- 煤气化废水 /
- 催化湿式过氧化氢氧化 /
- 催化剂
Abstract: A method of high temperature CWPO with a combination pretreatment process of acidification demulsion, extraction and steamed ammonia whose effluent presented its temperature as high as 87 to 95℃ was investigated to improve the biodegradability of coal gasification wastewater. Compared 3%Fe/Al2O3 and 3%Fe/SAC, over 60% of COD and 90% of the total phenol could be removed under the optimized condition(temperature of 80℃, pH0 of 4,H2O2 of 7.8 to 10.5 mg·L-1, LHSV of 0.5 h-1) with 3%Fe/SAC for the pretreatment of coal gasification effluent. COD removal rate as high as 60%, the total phenol removal rate as high as 90% above, the H2O2 utilization rate was more than 99% and chromaticity by initial 1 000 times down to 2 times, in addition, the effluent could reach the requirements of water quality standard for biochemical treatment system due to its high biodegradability as B/C=0.51.-
Key words:
- coal gasification wastewater /
- catalytic wet peroxide oxidation /
- catalyst
-
随着我国肉鸡、蛋鸡集约化养殖的发展,鸡粪产量不断增加。据不完全统计,2015年,鸡粪(包括尿液)排放量高达3.93×109 t[1]。大量未经处理的鸡粪直接排放,对水体、土壤、大气等环境造成严重污染[2]。鸡粪富含有机质,具有较高的能源转化潜力[3],仅2015年,鸡粪产沼潜力高达2.75×1011 m3,折算为标准状况下的天然气体积,可达1.72×1011 m3[4]。因此,厌氧消化是降低鸡粪污染、实现其资源化利用的有效处理方法[5],特别是高固体(总固体浓度(TS)>6%[6])鸡粪厌氧消化因较高的产能效率以及较少的二次污染物产生量而具有广泛的工程应用前景。
在典型畜禽粪便中,鸡粪的蛋白质组分最高,为牛粪、猪粪的2倍[7],在厌氧消化的水解阶段,易被转化为氨氮(包括
NH+4 和游离氨NH3)[8]。氨氮浓度超过临界值后,对厌氧菌的正常生理代谢产生不利影响,导致消化效率低下,出现氨抑制现象[9]。而高固体鸡粪厌氧消化面临着更大的氨抑制风险,使得消化过程中进料浓度的提升存在一定困难。据报道,鸡粪厌氧消化的进料TS负荷阈值为5%~6%[10-11],提高负荷不仅伴随着氨氮浓度的上升,还会限制系统传质能力而加剧氨抑制[12],影响发酵性能和体系稳定性。DALKILIC等[13]采用两相完全混合式厌氧反应器(continuous stirred tank reactor, CSTR)进行鸡粪半连续发酵实验,结果表明,当进料TS由3.7%增至8.25%,氨氮和挥发性脂肪酸(volatile fatty acids,VFAs)分别累积至3.5 g·L−1和6.0 g·L−1时,挥发性固体(volatile solid,VS)产气率逐步减少。NIU等[14]利用CSTR研究TS为10%的鸡粪高温厌氧消化,发现反应器连续运行45 d后,其稳定性随氨氮的上升而明显降低。乔玮等[15]采用批次实验,对不同进料TS条件下鸡粪连续中温消化的污泥进行活性测试,发现当鸡粪TS为10%时,氨氮的大量累积导致微生物利用乙酸的产甲烷能力下降了59%。目前,研究[16-18]普遍认为,采用逐步提升消化体系氨氮水平的方式驯化微生物,是强化厌氧菌耐氨能力,维持反应器稳定运行的有效途径。但以逐级提高进料浓度为基础而实现的高固体鸡粪连续厌氧消化性能仍须深入探讨。为此,本研究通过逐级提高进料TS的方法,利用CSTR研究不同进料浓度下鸡粪中温厌氧消化的长期运行效果,探究不同氨氮浓度对消化产气性能和有机物降解性能的影响,揭示高固体鸡粪消化过程中氨抑制的形成规律,为大力发展以高固体鸡粪为原料的沼气工程提供参考。
1. 材料与方法
1.1 接种泥和基质
接种泥取自西安市第五污水处理厂连续稳定运行的中温厌氧消化器。新鲜鸡粪取自陕西省杨凌示范区某养鸡场,挑拣出鸡粪中的鸡毛、石子等杂物,测得TS为(33.2±1.4)%,保存于−18 ℃冰箱冷冻室中。使用时采用多功能高速粉碎机(常州国华,878A)对其进行少量多次粉碎,粉碎时间为3 min,捣碎速度为10 000 r·min−1,直至粉碎成匀浆状为止,加水稀释至一定TS,充分搅拌,确保基质的均质性。接种泥及实验各阶段基质特性如表1所示。
表 1 接种泥和各阶段基质特性Table 1. Characteristics of seed sludge and substrate of each phase接种泥及阶段 运行时间/d TS/% VS/% pH TCOD/(g·L−1) SCOD/(g·L−1) TAN/(g·L−1) OLR/(g·(L·d)−1) 接种泥 0 1.18±0.05 0.74±0.05 7.15±1.20 3.25±0.14 1.00±0.16 0.24±0.04 — 阶段1 1~34 5.20±0.56 4.00±0.24 7.30±0.46 45.7±0.46 1.48±0.40 1.26±0.04 1.32±0.11 阶段2 35~55 7.24±0.36 5.51±0.56 7.54±0.26 68.2±0.37 1.27±0.07 1.24±0.03 1.81±0.07 阶段3 56~75 9.30±0.26 7.26±0.31 7.61±0.43 90.8±0.26 1.29±0.07 1.58±0.04 2.45±0.05 阶段4 76~100 6.22±0.26 4.78±0.32 7.40±0.13 54.1±0.26 1.40±0.04 1.20±0.07 1.57±0.03 注:TCOD为总化学需氧量;SCOD为溶解性化学需氧量;TAN为总氨氮浓度;OLR为有机负荷(以VS计)。 1.2 实验装置和操作条件
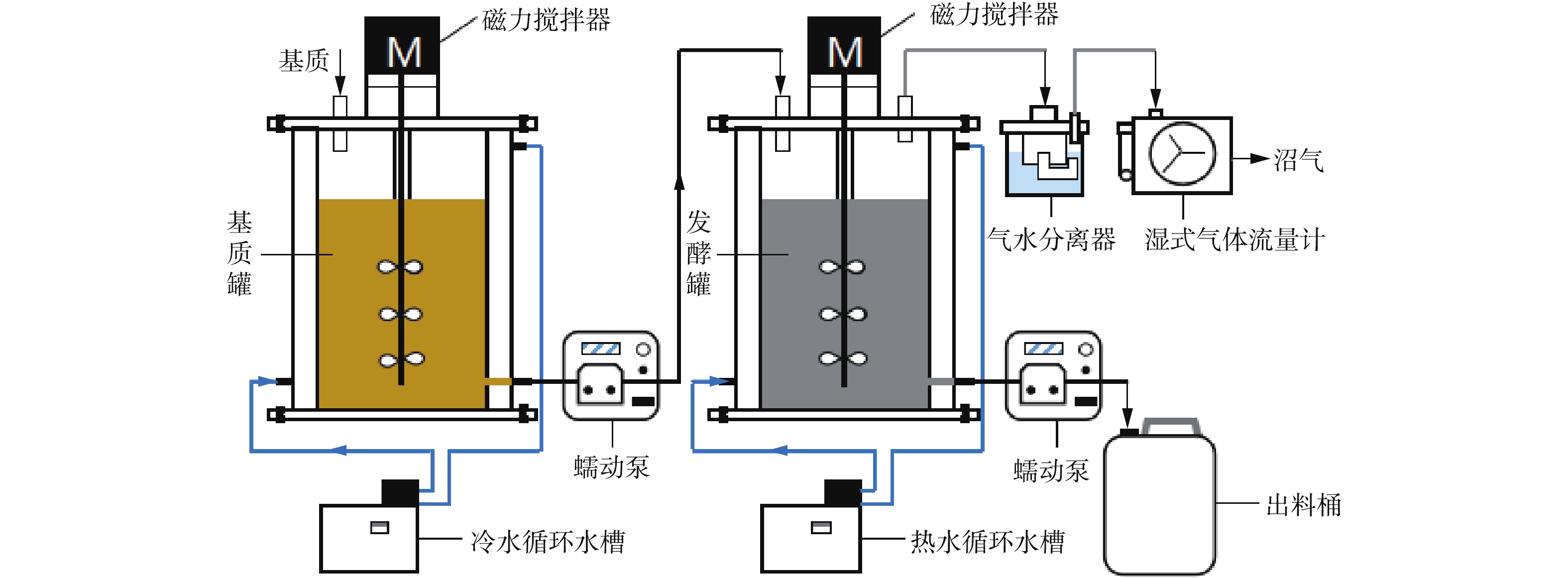
实验装置CSTR如图1所示。反应器有效体积为6 L。基质罐与发酵罐均具有水浴夹层,通过恒温循环水槽将罐体温度分别控制在(4±0.5) ℃和(35±0.5) ℃。采用磁力搅拌装置进行连续搅拌,速度为60 r·min−1,实现物料的完全混合。鸡粪厌氧消化连续实验的水力停留时间(hydraulic retention time,HRT)为30 d,通过配有时间控制器的蠕动泵精准进料与出料,每日分为8次,每次进出料体积为25 mL。本实验共分为4个阶段,阶段1~阶段4的进料TS分别为(5.20±0.56)%、(7.24±0.36)%、(9.30±0.26)%和(6.22±0.26)%,产气率与甲烷含量稳定7 d以上,调节进料TS进入下一阶段[19]。每天测定沼气产量,每周测定2次基质与消化液pH、碱度、VFAs、TCOD、SCOD、TAN、TS、VS、SS、VSS以及沼气成分。
1.3 指标测定方法
TS、VS、SS和VSS采用重量法测定。pH采用pH计(赛多利斯,PB-10)测定。COD、TAN、碱度采用APHA(1995)标准方法测定。基质与消化液在15 000g、4 ℃高速冷冻离心机中离心20 min,取上清液,过0.45 μm玻璃纤维滤膜后,测定TAN、SCOD、VFAs、碱度。VFAs和沼气成分采用气相色谱(岛津GC-2014,stablilwax-DA色谱柱,30 m×0.32 mm×0.50 μm,FID检测器;P-Q填充柱,2 m×2 mm,TCD检测器)测定。气体生成量由湿式气体流量计(日本品川,WK-0.5A)测定,并将其换算为标准状况下的沼气体积。
1.4 数据分析方法
1)游离氨浓度(free ammonia,FA)[20]按式(1)计算。
CFA=1714CTAN×10pHexp(6334273+t)+10pH (1) 式中:CFA为游离氨浓度,g·L−1;CTAN为总氨氮浓度,g·L−1;t为厌氧消化温度,℃;pH为消化液中的pH。
2)为进一步探讨逐级提高进料浓度引起的氨氮变化对鸡粪中温厌氧消化性能的影响,利用Boltzmann模型中的计算方法[21](见式(2)),分别对VS产甲烷率和VS去除率进行动力学拟合。各参数因模拟对象不同而存在差异,以TAN对产甲烷的影响为例进行分析。
Y=A2+(A1−A2)1+exp(X−x0dX) (2) 式中:Y为VS产甲烷率,L·g−1;A1为VS产甲烷率的初始值(左水平渐近线),L·g−1;A2为VS产甲烷率的终值(右水平渐近线),L·g−1;X为TAN浓度,g·L−1;x0为拐点,g·L−1;dX为X的导数。
在模型中,通过参数A1、A2、x0和dX描述抑制的影响,其中dX表示变化的抑制程度。采用Origin 8.0非线性拟合获得上述动力学参数。
3)各指标在阶段1~阶段4之间的差异显著性通过SPSS18.0软件进行单因素方差分析(P<0.05);采用Origin 8.0软件作图。
2. 结果与讨论
2.1 不同进料TS条件下鸡粪厌氧消化效果
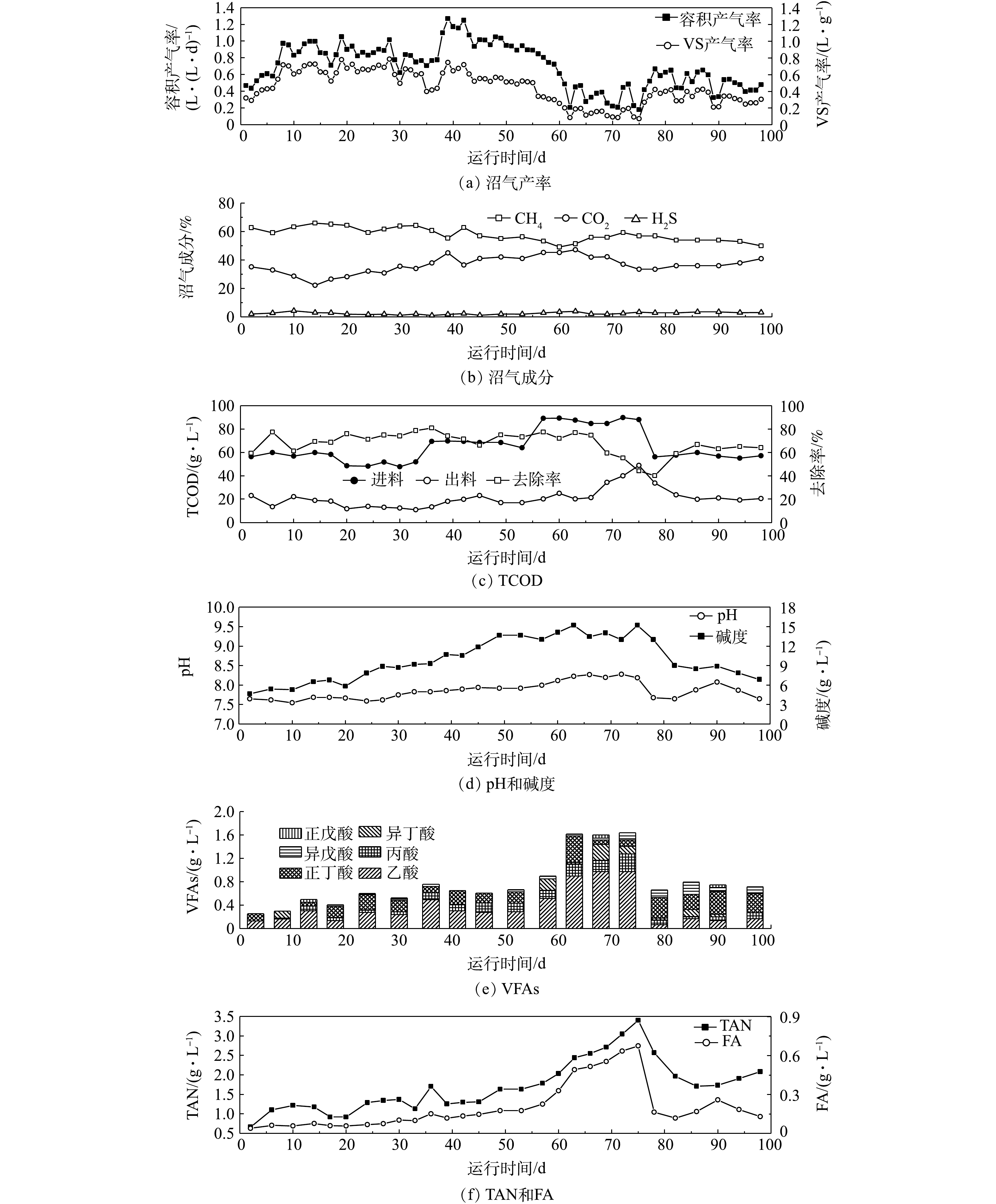
不同进料TS条件下鸡粪厌氧消化效果如图2、表2和表3所示。在连续实验中,CSTR共运行100 d,主要分为4个阶段,各阶段的进料TS分别为(5.20±0.56)%、(7.24±0.36)%、(9.30±0.26)%和(6.22±0.26)%。在运行1~34 d(阶段1),基质TS为(5.20±0.56)%,进料OLR(以VS计)为(1.32±0.11) g·(L·d)−1,鸡粪厌氧消化VS产气率稳定在(0.61±0.14) L·g−1,此时甲烷含量为(62.4±2.6)%,pH维持在7.5以上,没有发生VFAs的积累,VFAs与碱度比值稳定在0.06±0.01,未超过研究报道的抑制阈值0.5[22],表明厌氧消化反应器运行良好。实验运行的35~55 d(阶段2),提高基质TS为(7.24±0.36)%,在运行前8 d,单位容积产气量快速增加,最高值达到1.27 L·(L·d)−1,随后有所降低,最终稳定在(0.96±0.21) L·(L·d)−1。相比第1阶段,VS产气率略有下降,但与其他研究相比,仍处于较高水平[13]。TCOD去除率保持在(71.0±2.4)%,pH逐渐升高至8.0左右,同时TAN和FA增加至(1.51±0.03) g·L−1和(0.15±0.02) g·L−1,而甲烷含量始终维持在55%以上,未出现VFAs累积,VFAs/碱度比值稳定在0.06±0.02,说明反应器运行稳定。
表 2 不同进料TS条件下厌氧消化效果参数的变化Table 2. Variation of performance parameters of anaerobic digestion at different feeding concentrations阶段 容积产气率/(L·(L·d)−1) VS产气率/(L·g−1) CH4/% CO2/% TS/% TS去除率/% VS去除率/% TCOD去除率/% 1 0.75±0.18b 0.64±0.05a 62.4±2.6a 33.0±2.2b 2.11±0.24c 59.4±2.1a 66.7±4.1a 73.2±3.6a 2 0.96±0.21a 0.54±0.03b 58.9±1.4b 39.6±3.4a 2.91±0.24b 60.9±1.7a 63.1±4.5ab 71.0±2.4a 3 1.03~0.18 0.34~0.07 58.2~47.1 35.1~45.7 3.85~7.04 58.1~23.4 64.3~39.2 69.2~42.3 4 0.51±0.10c 0.33±0.07c 53.0±1.7c 37.4±2.2a 3.23±0.21a 48.4±2.8b 60.1±2.5b 63.5±2.9b 注:数据后不同小写字母表示不同阶段之间差异显著(P<0.05)。 表 3 不同进料TS条件下厌氧消化稳定性参数的变化Table 3. Variation of stability parameters of anaerobic digestion at different feeding concentrations阶段 pH 碱度(以CaCO3计)/(g·L−1) VFAs/(g·L−1) VFAs/碱度 TAN/(g·L−1) FA/(g·L−1) 1 7.67±0.19c 6.68±0.06b 0.53±0.02c 0.06±0.01a 1.06±0.11c 0.07±0.02b 2 7.89±0.41b 11.9±0.32a 0.65±0.04b 0.06±0.02a 1.51±0.03b 0.15±0.02a 3 8.17±0.04a 13.0~15.2 1.62±0.02a 0.07~0.13 1.63~3.40 0.23~0.68 4 7.80±0.17b 8.05±0.89b 0.75±0.04b 0.08±0.02a 1.88±0.16a 0.17±0.05a 注:数据后不同小写字母表示不同阶段之间差异显著(P<0.05)。 实验运行的56~75 d(阶段3),继续提高基质TS为(9.30±0.26)%,OLR(以VS计)上升为(2.45±0.05) g·(L·d)−1,产气速率迅速下降,经过为期12 d的波动后,容积产气率最终下跌至0.18 L·(L·d)−1,VS产气率仅为0.07 L·g−1,甲烷含量一度减少至50%以下,TCOD、TS和VS去除率明显降低,表明反应器产气性能和有机污染物降解能力大幅度下降,消化效果发生恶化。相应的VFAs出现累积,显著升高至(1.62±0.02) g·L−1(P<0.05),但pH未见下降,继续提升至8.2左右,这可能是体系中的碱度和氨氮起到了缓冲作用所致,此时碱度(以CaCO3计)达到最高,为15.2 g·L−1,TAN和FA分别由1.63 g·L−1和0.23 g·L−1逐步增加为3.40 g·L−1和0.68 g·L−1,上述现象表明反应器已受到严重抑制。尽管有研究[23]指出,采用逐级提高进料浓度的方法可引导细菌适应基质环境,进而加强消化效率,但本实验中过高的基质TS导致VFAs和氨氮双重累积,其中TAN与FA均已超出此前报道的中温消化抑制阈值(3.0 g·L−1[24]和0.20 g·L−1[25])。由于仅当氨抑制引起的VFAs累积致使消化液pH低于7时,才有可能发生酸抑制[26],由此推断,此时厌氧消化过程受到了由TAN升高所引发的FA逐步累积而造成的氨抑制,并非氨氮与VFAs联合抑制。
为了防止氨氮持续上升以及由此带来的氨抑制进一步恶化,实验运行的76~100 d(阶段4),进料TS下调为(6.22±0.26)%,容积产气率和VS产气率均迅速回升,分别稳定在(0.51±0.10) L·(L·d)−1和(0.33±0.07) L·g−1,甲烷含量恢复至(53.0±1.7)%,累积的VFAs下降为(0.75±0.04) g·L−1,此时总氨氮浓度也降至(1.88±0.16) g·L−1,有机物去除率较第3阶段明显提高,说明反应器氨抑制现象得到了有效缓解,也表明进料TS浓度为(9.30±0.26)%条件下出现的氨抑制是可逆性抑制[26]。尽管降低进料TS减轻了消化体系的氨负荷,甲烷发酵恢复了正常,但通过比较发现,此条件下VS产气率较第1阶段和第2阶段下降了38.9%~48.4%,而VFAs和氨氮浓度水平仍然较高,因此,推断该阶段反应器处于“抑制稳定状态”,即工艺运行稳定而甲烷产率低。此状态是由FA、pH和VFAs三者之间的交互作用引起的[27],阶段3末期,FA累积影响了产甲烷菌活性[28],导致VFAs累积,随即引发阶段4初期pH的下降,而pH降低则会减少FA,对氨抑制起到一定的缓解作用,微生物活性逐渐恢复;抑制缓解后产甲烷菌消耗掉积累的VFAs,同时引起pH上升,继而导致FA增加,如此循环往复。若反应器长期处于抑制稳定状态,FA、pH和VFAs的持续波动可能会干扰微生物的恢复过程,导致系统更加脆弱,易失稳,NIELSEN等[29]的研究结果证实了上述推测。因此,正确把控进料TS浓度是维持有机物料与微生物之间平衡关系、从源头避免氨抑制发生的关键。
2.2 鸡粪中温厌氧消化各运行阶段COD物料平衡
COD物料衡算可以表征底物在厌氧消化过程中的变化[30],进而评估反应器运行期间整个工艺的合理性和设计的可行性。不同运行阶段COD物料平衡情况如图3所示。由于连续实验中进料、出料以及化学测定等过程存在一定误差,因此,各阶段不同形态COD所占进料TCOD的比例在81.1%~106.8%的范围内波动。
由图3可知,在阶段1,有79.4%的进料COD转换成了甲烷,21.8%的COD转为VSS,1.18%的COD转为VFAs。提高鸡粪TS至(7.24±0.36)%时,转换成甲烷和VFAs的COD含量略有降低,分别为71.8%和1.11%,但下降量并不显著(P>0.05),转换成VSS的COD升高至33.1%。
在阶段3,继续提高鸡粪TS至(9.30± 0.26)%,转换成甲烷的COD仅占19.4%,VSS和VFAs的COD所占比例显著上升为69.8%和2.12%(P<0.05),达到第1阶段和第2阶段的2倍左右,与图2中VFAs累积、TCOD降解率下降结果一致。一方面,在氨抑制发生阶段,甲烷转化率及有机物降解率降低,大部分COD以VSS的形式残留在消化液中,有悖于厌氧消化工艺实现资源化和减量化的绿色理念;另一方面,受高浓度氨氮影响的产甲烷菌降低了VFAs的利用速率,从而打破耗酸与产酸之间的动态平衡,导致VFAs上升,若长时间连续进料TS为9.30%,持续增加的氨氮会严重抑制产甲烷菌活性,加剧VFAs累积,造成酸和氨的联合抑制,最终消化体系崩溃[26]。因此,从反应器运行效果考虑,不建议厌氧消化反应器进料浓度高达9.30%。
在阶段4,降低鸡粪TS为(6.22±0.26)%,转换为甲烷的COD增加,达到39.9%,发酵液中以VSS和VFAs形式存在的COD减少为39.8%和1.03%,与图3中产气量增加、VFAs累积消除的实验结果相一致。
2.3 氨氮对厌氧消化VS产甲烷率和VS去除率的影响
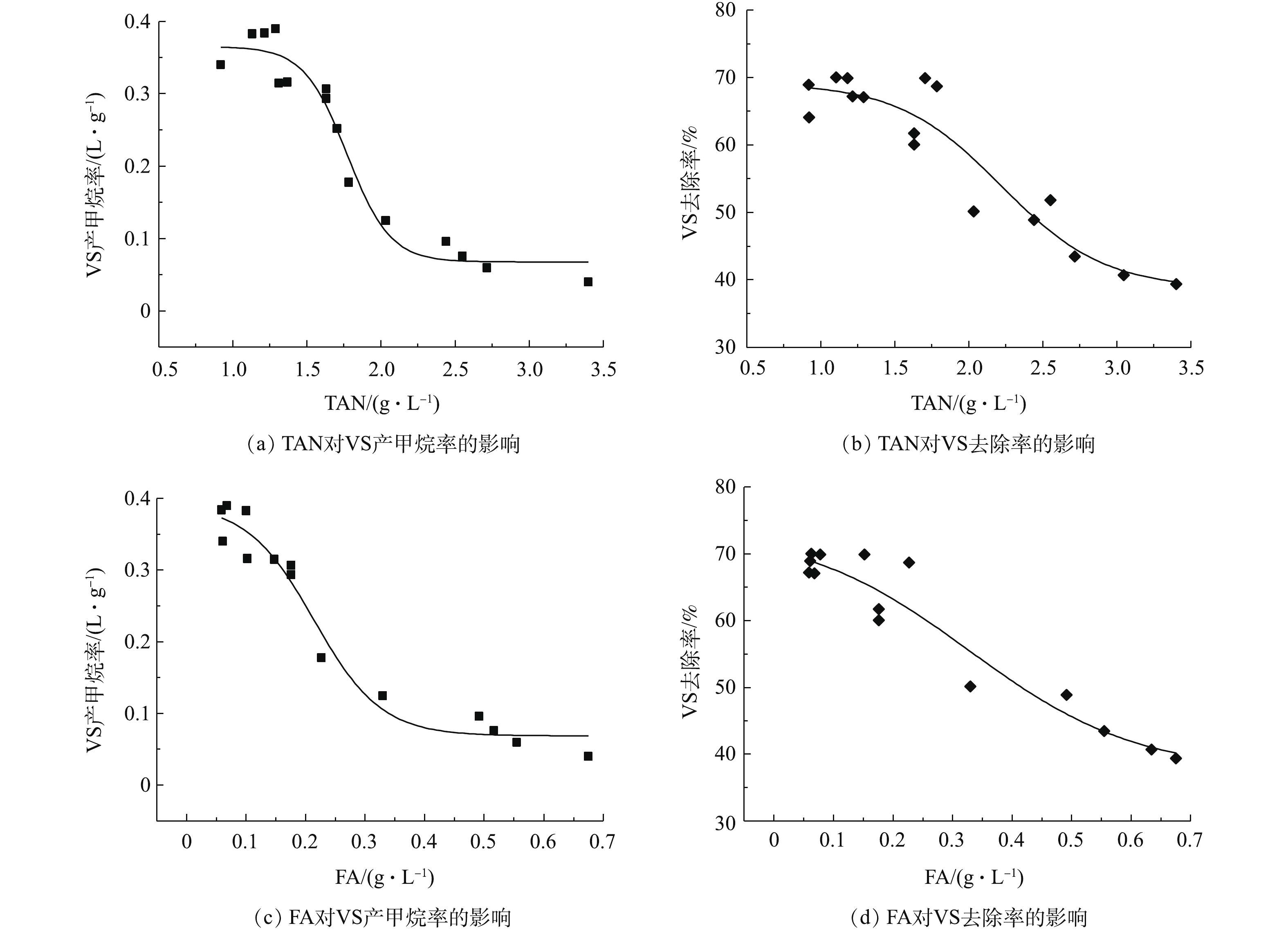
VS产甲烷率和VS去除率是评价厌氧消化性能的重要参数。其中,VS产甲烷率是反映消化产气效果的直观指标,VS去除率通常可表征有机物的降解效率。因此,以VS产甲烷率和VS去除率作为氨抑制响应参数,通过Boltzmann模型对连续实验结果(阶段1~阶段3)进行模拟,以进一步探讨高固体鸡粪厌氧消化氨抑制的形成过程,结果如图4所示,拟合动力学参数如表4所示,并分别计算得出VS产甲烷率和VS去除率减少10%、50%、80%所对应的氨氮浓度,即IC10、IC50、IC80。
表 4 模型拟合动力学参数和抑制阈值Table 4. Kinetic parameters of model fitting and inhibition thresholds抑制因子 指标 动力学参数 抑制阈值 A1 A2 x0 dX IC10/(g·L−1) IC50/(g·L−1) IC80/(g·L−1) TAN VS产甲烷率 0.37±0.02 0.07±0.01 1.70±0.04 0.15±0.05 1.48 1.84 2.35 VS去除率 69.2±3.11 38.7±5.06 2.22±0.19 0.35±0.16 2.04 2.60 3.87 FA VS产甲烷率 0.39±0.03 0.07±0.01 0.21±0.02 0.06±0.02 0.10 0.24 0.41 VS去除率 73.8±9.50 37.3±8.67 0.33±0.08 0.14±0.11 0.28 0.49 0.76 由图2和图4可知,进料TS的逐级增加伴随着氨氮浓度的上升,当氨氮增至某临界值后,VS产甲烷率和VS去除率不断下降,表明反应器产气及有机物降解性能出现恶化,消化系统受到氨抑制。氨氮对消化过程的抑制主要包括2类:1)离子化的NH4+影响甲烷生产酶的合成;2)疏水的氨分子直接进入菌体细胞内导致质子失衡,改变胞内pH[31-32]。一般认为,FA是氨抑制的直接抑制因子,其毒性引起发酵菌生命代谢活动异常,从而造成底物利用率下降、产气量减少等一系列问题[18],因此,在本研究中,TAN升高所引发的FA持续累积,导致高固体鸡粪厌氧消化氨抑制逐步形成。目前,已有大量研究[9, 28, 33]表明,过高的氨氮浓度通过影响嗜乙酸产甲烷菌活性而制约甲烷的产生,戴晓虎等[34]还证实了水解菌中蛋白降解菌种同样会受到FA的毒性抑制,造成VS降解率下降。明确氨氮抑制阈值对维持功能菌活性,调控反应器平稳运行具有重要意义。
由表4可知,TAN对VS产甲烷率的IC10、IC50、IC80分别为1.48、1.84、2.35 g·L−1。这与SUNG等[35]的研究结果一致,在高pH厌氧体系中,TAN为1.5~3.0 g·L−1时微生物受到氨负荷的冲击。在阶段3,TAN最大值高达3.40 g·L−1,表明反应器产气效果的急剧下降是受到总氨氮的严重抑制所致。TAN对VS降解率的IC10、IC50、IC80分别为2.04、2.60、3.87 g·L−1。与甲烷产率相比,VS降解率受TAN抑制的阈值相对较高,表明其对TAN的抑制响应具有一定滞后性,这可能由于消化体系稀释了进料浓度,造成VS降解率短暂性偏高[36]。
FA对VS产甲烷率的IC10、IC50、IC80分别为0.10、0.24、0.41 g·L−1。而ELHADJ等[37]利用批次实验研究了合成城市生活垃圾中温厌氧消化,发现进料TS为6.53%的条件下,FA的IC50为0.21 g·L−1,低于本实验中的半抑制浓度,这可能是逐级提高进料浓度使微生物得到适应性驯化,从而提高了对FA的承受能力所致。FA对VS去除率的IC10、IC50、IC80分别为0.28、0.49、0.76 g·L−1。甲烷产率和VS去除率受FA抑制的浓度变化规律与TAN类似,后者对FA的抑制响应同样具有滞后性。因此,选取VS产甲烷率作为氨抑制预警参数更具有时效性。由抑制阈值可知,产气性能良好的连续厌氧消化系统中微生物所能承受的FA为0.10 g·L−1(IC10),对照图2、表2和表3得到对应的进料TS浓度,结果为(7.24±0.36)%,此阶段消化效果明显,反应器运行稳定。因此,为保证反应器长期高效平稳运行,建议鸡粪连续中温厌氧消化的进料浓度不超过7.24%。
3. 结论
1)进料TS为(5.20±0.56)%(阶段1)和(7.24±0.36)%(阶段2),鸡粪中温厌氧消化VS产气率稳定在0.54~0.64 L·g−1,VFAs稳定在0.53~0.65 g·L−1,反应器运行良好。进料TS提高为(9.30±0.26)%(阶段3),VS产气率迅速下降至0.07 L·g−1,有机物(以COD计)的甲烷转化率降低为19.4%,VFAs和氨氮出现双重累积,分别高达(1.62±0.02) g·L−1和3.40 g·L−1,消化过程受到氨抑制。
2)逐级提高进料浓度造成消化系统TAN上升,继而引发FA的持续累积,VS产甲烷率和VS去除率不断下降,导致高固体鸡粪厌氧消化氨抑制逐步形成。与甲烷产率相比,VS去除率对TAN和FA的抑制响应具有滞后性。
3)进料TS浓度降低为(6.22±0.26)%(阶段4),氨抑制得到有效缓解,但反应器处于“抑制稳定状态”。
4)为保证反应器长期高效平稳运行,建议鸡粪连续中温厌氧消化的进料浓度不超过7.24%。
-
[1] ZHANG W Q, MA J, YANG S D, et al. Pretreatment of coal gasification wastewater by acidification demulsion[J]. Chinese Journal of Chemical Engineering, 2006, 14(3):398-401 [2] GAI H J, JIANG Y B, QIAN Y, et al. Conceptual design and retrofitting of the coal-gasification wastewater treatment process[J]. Chemical Engineering Journal, 2008, 138(1/2/3):84-94 [3] ZHANG W H, WEI C H, CHAI X S, et al. The behaviors and fate of polycyclic aromatic hydrocarbons (PAHs) in a coking wastewater treatment plant[J]. Chemosphere, 2012, 88(2):174-182 [4] 何锋. 煤化工废水的来源与特点及其相应的处理技术探究[J]. 科技视界, 2012(23):320-321 [5] CAUDO S, CENTI G, GENOVESE C, et al. Copper-and iron-pillared clay catalysts for the WHPCO of model and real wastewater streams fromolive oil milling production[J]. Applied Catalysis B:Environmental, 2007, 70(1/2/3/4):437-446 [6] KENNEDYA L J,VIJAYAB J J, SEKARANA G, et al. Equilibrium, kinetic and thermodynamic studies on the adsorption of m-cresol onto micro-and mesoporous carbon[J]. Journal of Hazardous Materials, 2007, 149(1):134-143 [7] CEZAR C, CARMEN T, MATEI M, et al. Catalytic wet peroxide oxidation of phenol over Fe-exchanged pillared beidellite[J]. Water Resource, 2003, 37(5):1154-1160 [8] SERGIO N, MERCEDES A, HERMENEGILDO G. Heterogeneous Fenton catalysts based on clays, silicas and zeolites[J]. Applied Catalysis B:Environmental, 2010, 99(1):1-26 [9] ZAZO J A,BEDIA J,FIERRO C M, et al. Highly stable Fe on activated carbon catalysts for CWPO upon FeCl3 activation of lignin from black liquors[J]. Catalysis Today, 2012, 187(1):115-121 [10] ANISSA D, NAFAÂ A. Heterogeneous catalytic wet peroxide oxidation of paraquat in the presence of modified activated carbon[J]. Applied Catalysis B:Environmental, 2010, 97(1/2):227-235 [11] MACARENA M, ZAHARA M P, JOSE A C, et al. Improved wet peroxide oxidation strategies for the treatment of chlorophenols[J]. Chemical Engineering Journal, 2013, 228(14):646-654 [12] MACARENA M, ZAHARA M P, NIEVES M, et al. A ferromagnetic gamma-alumina-supported iron catalyst for CWPO. Application to chlorophenols[J]. Applied Catalysis B:Environmental, 2013, 136:218-224 [13] CARLA D L, FERNANDO I, PAOLA M, et al. Alumina supported Fenton-like systems for the catalytic wet peroxide oxidation of phenol solutions[J]. Industrial & Engineering Chemistry Research, 2012, 51(26):8979-8984 [14] 国家环境保护总局. 水和废水监测分析方法[M]. 4版. 北京:中国环境科学出版社,2002 [15] 姜成春, 庞素艳, 马军,等. 钛盐光度法测定Fenton氧化中的过氧化氢[J]. 中国给水排水, 2006, 22(4):88-91 [16] LI Y M, GU G W, ZHAO J F, et al. Anoxic degradation of nitrogenous heterocyclic compoundsby acclimated activated sludge[J]. Process Biochemistry, 2001, 37(1):81-86 [17] BOSSMANN S H, OLIVEROS E, GOEB S, et al. New evidence against hydroxyl radicals as reactive intermediates in the thermal and photochemically enhanced Fenton reactions[J]. Journal of Physical Chemistry A, 1998, 102(28):5542-5550 [18] FEMANDO M, ISABEL P, CHRISTINA B, et al. Chemical surface modified-activated carbon cloth for catalytic wet peroxide oxidation of phenol[J]. Journal of Chemical Technology and Biotechnology, 2014, 89(8):1182-1188 [19] BAUTISTA P, MOHEDANO A F, CASAS J A, et al. An overview of the application of Fenton oxidation to industrial wastewaters treatment[J]. Journal of Chemical Technology and Biotechnology, 2008, 83(10):1323-1338 [20] CRISTINA F, PERE-LLUÍS C, FRANCESC C, et al. Solar photoelectro-Fenton degradation of cresols using a flow reactor with a boron-doped diamond anode[J]. Applied Catalysis B:Environmental, 2007, 75(1/2):17-28 [21] CHU Y Y,ZHANG D M,LIU L, et al. Electrochemical degradation of m-cresol using porous carbon-nanotube-containing cathode and Ti/SnO2-Sb2O5-IrO2 anode:Kinetics, byproducts and biodegradability[J]. Journal of Hazardous Materials, 2013, 252-253:306-312 [22] LIU P J, HE S B, WEI H Z, et al. Characterization of α-Fe2O3/γ-Al2O3 catalysts for catalytic wet peroxide oxidation of m-cresol[J]. Industrial & Engineering Chemistry Research, 2015, 54(1):130-136 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 1593
- HTML全文浏览数: 1236
- PDF下载数: 477
- 施引文献: 0



 DownLoad:
DownLoad: