-
社会经济的快速发展和城市化进程加速推动了污泥体量的增加,2022年我国干污泥产量已达到1300万吨以上[1 − 2]. 同时,污泥富含丰富的磷、矿物质和有机质,具有较高的资源化前景[3 − 4]. 污泥热解是指在缺氧或者无氧条件下,将污泥加热至一定温度使得污泥发生有机质裂解、水分挥发、小分子聚合等热化学反应,最终转化为气态、液态和固态(生物炭)[5 − 7]. 在热解过程中,随着有机物的裂解和小分子物质的挥发,污泥中的磷(P)、钾(K)等营养元素得到有效的富集,并且重金属可以生成硅铝结合态化合物,从而实现重金属的惰性转变[8 − 12].
污泥单独热解生成的生物炭具有比表面积较小、孔隙结构不完善、对土壤的改良效益不明显的问题,通过添加共热解物质、调整污泥热解参数等方法可以优化污泥基生物炭的土壤改良特性[13 − 15]. 污泥共热解的添加物包括生物质、碱土金属、塑料等,调节热解参数例如温度、时间和气氛[16 − 18]. 以秸秆为代表的生物质添加物可以提高混合物有机质含量、增强生成的污泥基生物炭的芳香结构,并且污泥中重金属可通过与生物质中的矿物成分结合、惰性转变等方式降低其生物活性[19]. 以氧化钙为代表的碱土金属与污泥共热解,可促使污泥中的磷转化为羟基磷酸钙的形式从而提高其有效磷的转化效率[20]. 以聚氯乙烯(PVC)为代表的塑料添加物,会促使污泥中重金属转变为金属氯化物的形态,使其在热解过程更容易挥发[21 − 22]. 以上污泥共热解方法以不同的机制有效提高了污泥基生物炭的物化特性使得其具备一定的土壤改良特性[23].
我国土壤污染严重,酸性土壤主要分布于中国南方、约占陆域面积的30%以上[24],有机污染土壤和重金属污染土壤主要与制药厂、工厂和农用地相关,总体呈现南方污染高于北方、东部发达地区高于中部地区,且二者呈现出明显的复合污染特征[25]. 污泥基生物炭可以从多方面对污染土壤起到改良作用,一方面污泥的碱性可有效中和土壤中的酸性、稳定土壤中的活性金属/重金属[26];另一方面,污泥基生物炭的多孔性质可改善污染土壤的结构和持水能力并为微生物的生长提供寄居场所. 最重要的,P是一种不可再生资源,污泥基生物炭中富含以P为代表的植物和微生物生长必须的矿物营养成分,不仅可提高土壤肥力、改善土壤品质也可以实现不可再生资源的回收利用[27]. 因此,污泥基生物炭应用于土壤改良具有良好的发展前景.
现有的对生物炭土壤改良的综述文章大多是技术成熟且已经投入市场应用的生物质类等生物炭,而对污泥基生物炭作为改良剂的相关机理探究还不够充足,缺乏对污泥定向热解和污泥基生物炭对土壤修复作用机制的分析和研究. 具体来说,一方面,污泥与不同物质在共热解过程中的相互作用机制,共热解条件因素对污泥重金属以及P的迁移转化影响还不够清晰;另一方面,污泥基生物炭的物化性质对土壤肥力、pH、微生物以及碳平衡等的作用效应还需要进行系统的分析评估. 因此,本综述拟基于国内外污泥的热解方法、污泥基生物炭物化性质演变及其土壤回用效果的最新研究进行深入的探讨与分析. 通过分析污泥基生物炭的热解制备及土壤回用效应的研究现状,明确不同热解工艺对重金属、P迁移转化的影响机制以及土壤回用过程中的增益作用,指导和丰富污泥基生物炭的定向热解和土壤改良机制的研究,为我国污泥资源化处置提供基础研究数据.
-
为了提高污泥基生物炭对污染土壤的改良特性,有必要在热解过程控制热解条件以实现污泥基生物炭有效磷的强化和重金属固化并降低以多环芳烃为首的有机污染物,一般来说,可采用添加共热解添加剂、控制热解温度以及酸碱、浸渍、蒸汽等的改性强化方法[28 − 29]. 目前污泥共热解物质主要有生物质、碱土金属、磷酸盐类、塑料等,可在污泥热解过程产生协同/拮抗作用,不仅影响污泥基生物炭中P和重金属的存在形态,还对产率有一定的影响.
如表1所示,生物质类添加剂主要包括食物残渣、木屑、秸秆等,生物质添加剂可通过芳香结构螯合污泥重金属、活性基团络合重金属、增加重金属挥发比例等方式降低污泥基生物炭的活性重金属. Wang等[30]将食物残渣与污泥共热解,促进了高岭石(Al2Si2O5(OH)4)和金属磷酸盐结晶化合物的形成,重金属结合在该复杂晶体化合物中大大降低了其重金属的风险指数. Yang等[31]将稻壳与污泥共热解明显降低了Pb和Cd的含量,并且其形态分别转变为更加稳定的PbAl2O4和CdAl2O4,污泥基生物炭生态风险降低了1—2级. Wang等[32]将污泥和棉花秸秆共热解,棉花秸秆在热解过程产生的以羧基、羟基、酚羟基等为首的丰富有机官能团与重金属发生络合反应从而起到稳定重金属的效应.
碱金属也是一种常用的污泥共热解添加剂,Tang等[33]将CaO添加于污泥,在700 ℃共热解发现污泥中的重金属得到有效固定,且P以羟基磷灰石的形态富集. Han等[34]将CaO/Fe2O3与污泥共热解,发现CaO能与污泥中的As2O3、As2S3和NaAsO2反应生成Ca(AsO2)2稳定形态物质. 田[35]还在污泥中添加K3PO4,发现相比不添加共热解物质时产物中出现了磷酸金属盐等结合态,分析发现PO43-的添加可以促进污泥中金属氧化物与之作用形成结合态. 此外,一些塑料添加物也证实可有效固化污泥的重金属[36]. Li等[37]将污泥与载金属聚氯乙烯共热解可有效固定除Pb外的重金属,且随着载金属聚氯乙烯热解占比越大,重金属稳定态分数增加,对Pb的消极效果是载金属聚氯乙烯中PbSO4的释放导致. 李志远等[21]同样的采用污泥与聚氯乙烯进行共热解,发现加入PVC使得重金属转化为容易挥发的金属氯化物形态,降低了生物炭中As、Zn等的残留量.
综上分析,污泥与生物质共热解更容易生成孔隙结构丰富的污泥基生物炭,且Pb等重金属常与铝化合物结合形成稳定化合物;污泥与碱土金属共热解,可以对As等重金属起到较好的固定作用;而当污泥与塑料共热解降低重金属残留量的同时塑料中原本还有的金属化合物还会对某些金属固定带来负面作用.
-
热解气氛,尤其是氧气的存在比例会影响污泥在热解中的氧化还原反应,从而决定污泥基生物炭的性质. 氮气是热解常用的惰性保护气,Tang等[33]的研究采用N2作为保护气研究CaO与污泥共热解,还有研究采用CO2作为热解气体[38]. 相比N2,CO2气氛可以在热解过程为污泥中的还原物质(如C原子)提供氧原子,进而影响污泥基生物炭的O/C. 另外,研究还发现相比 N2气氛,CO2气氛条件下会抑制甲烷的生成,这是因为在高温条件下会促使CH4与H2O(g)作用生成CO反应的进行,而CO在排出过程中遇到氧气又会被还原成为CO2[39]. Huang等[40]将污泥与水葫芦在CO2/O2气体条件下共热解,当二者比值为7/3时热解产物在1000 ℃减重最少,结构最稳定,且此气体比例下热解过程活化能最低反应易于进行. 分析发现,在有氧气存在的热解气氛条件下,Ca的赋存形态会发生变化,N2气氛下主要以CaCO3形态存在,低氧条件下CaO为主要存在形态,这也是低氧条件下生物炭pH较高的原因. 氧气的存在还会导致产生大量飞灰颗粒,不易挥发的金属以氧化物形态留存在飞灰中从而被带走,降低生物炭中重金属的留存率[41]. CO2气氛还能降低热解污泥的活化能并减少酸类化合物的生成[42],当有生物质参与热解时,氧气的存在会影响CO2和CO的产生量,进而影响生物炭孔径结构[43]. CO2气氛在热解反应的最初有增大热解混合物比表面积和孔体积的效用,但在更高的温度条件下(>500 ℃),CO2会导致大孔数量增多、比表面积减小.
惰性气氛有助于调控污泥混合物的定向发展,而CO2气氛不仅能促进污泥基生物炭孔隙结构的完善,形成丰富的芳香烃结构,促进金属形成稳定形态,还能通过控制氧气比例调控混合物活化能,调控生物炭pH以及重金属的留存率.
-
热解温度是决定产物生物炭结构的主要因素. 表2可以看出,污泥单独热解时随着热解温度的增大,污泥基生物炭的比表面积也逐渐增大[44].
但是,共热解物质添加后,尤其是柳木与污泥共热解相比污泥单独热解时比表面积明显增大,此时温度对污泥基生物炭孔隙结构的影响变得不明显[45]. 在相同热解温度条件下,停留时间的长短也影响着生物炭的比表面积,这是因为污泥与共热解物质泥中含有的半纤维素、纤维素、木质素在不同温度阶段分解状态不同. 例如,在400 ℃时停留时间的增大促进有机质的继续分解;当温度升高有机质分解完全(500 ℃),此时停留时间的增大会使生物炭基体呈熔融态,部分灰分可能会堵住孔隙结构;温度继续升高(700 ℃),生物炭中的碳酸盐分解出CO2等气体迫使生物炭重新形成孔径结构.
热解升温速率对生物炭的性质也有一定影响,Zhu等[46]改变升温速率分别为10、20、30 ℃·min−1,发现升温速率越低污泥随温度升高减重更快,这是因为介质扩散和传热需要一定的时间,升温速率过高会延迟热解反应,增大整个热解过程的时长. 升温速率越高生物炭产率越低,气体产量越高. Wang等[47]改变升温速率分别为10、20、30 ℃·min−1,发现随着升温速率的改变,热解产物的总失重相同,表明升温速率不影响有机物的分解效率,只是达到热解终温的快慢不同. Huang等[40]改变升温速率分别为10、20、40 ℃·min−1,发现随着热解升温速率的提升,污泥随温度热解减重速率减小,这是因为增大加热速率不利于热解物质的燃尽,增大了热解时长,但有利于挥发分的分离和燃烧.
-
污泥中含有4%—9%的P[49 − 50],其主要存在形态包括有机磷(OP)和无机磷(IP),有机磷一般以核酸、磷脂、含磷蛋白等形式存在,而无机磷包括磷灰石无机磷(AP)和非磷灰石无机磷(NAIP).
热解温度、添加剂是影响污泥P转化的关键因素,而热解气氛对P的迁移转化影响很小[51]. OP沸点较低,在热解过程中会随着温度的升高而逐渐分解转化为其他含磷化合物,即OP在热解过程中发生脱水、脱羧、聚合等反应,一个或多个与磷酸基团相连的有机官能团丢失并释放正磷酸盐及焦磷酸盐[49, 52 − 53],原来被这些有机官能团占据的位置会被金属阳离子(Ca2+、Fe3+和Al3+)重新占据,即OP释放的正磷酸盐与金属离子一起形成矿物或立即吸附到其他固相表面. 因此,提高温度或低灰分、高挥发性的污泥有利于OP向IP的转化,促进IP的富集. 污泥单独热解时P主要与铁、铝等结合生成难以分解的磷酸铁盐、磷酸铝盐等. 以CaO为首的碱金属添加剂,已经被证实可促进NAIP向AP转化,且P与其他金属离子的反应顺序为: Ca2+> Mg2+> Al3+> Fe3+[54 − 57]. 当添加CaO等共热解物质后污泥中的非磷灰石IP逐渐转化为钙磷酸盐等磷灰石IP,但是羟基磷灰石的形成取决于Ca/P. 通常Ca/P比值控制在1.50—1.67,热解温度控制在600—900 ℃更有利于羟基磷灰石的形成[58]. Tang等[33]采用添加CaO、控制热解温度定向调控污泥热解过程促使P转化为羟基磷酸钙物相(P targeted transformation to hydroxyapatite),简称“P2THAP”,并且通过玉米盆栽实验证实该污泥基生物炭再生P肥养分供给效果媲美甚至超越传统化学P肥. 另外有研究指出,随着热解温度的提高,制出的生物炭对P具有更高吸附能力且解吸量也在逐渐降低,从而在生物炭上形成较稳定的磷酸盐化合物并能实现对P的缓慢释放[59].
-
污泥在热解富集P资源的同时,污泥中携带的重金属也同时被富集,不利于污泥基生物炭的土壤回用. 重金属在污泥基生物炭中的存在与热解过程的挥发度和物质流分配密切相关,Hg、Se等高挥发性重金属在低温热解阶段易挥发存在于气态产物中,Ba、Cr、Co、Cu、Ni等低挥发性重金属主要留存在污泥基生物炭中,Pb、Cd、Zn、As、Sn、Ti等中等挥发性重金属通过挥发冷凝富集于生物油中[60]. 因此,降低污泥基生物炭中的重金属生态风险可以通过提高热解温度将易挥发重金属减量、中挥发性和低挥发性重金属形成稳定态重金属固定来实现. 但是,过高热解温度会破坏生物炭的孔隙结构,促使芳香族化合物分解形成C=C稳定结构.
刘菲菲等[61]采用微波热解发现,随着热解温度的提升,生物炭中的稳定态重金属占比逐渐增大,对几种重金属的固定效果由好到差依次为Cr>Pb>Ni>Cu>Zn,这可能与重金属氧化物的可挥发性和稳定性相关. Xu等[62]分别添加CaO和MgO与污泥共热解,相比原污泥热解污泥基生物炭中残渣态重金属比例最高可以达到99%,并且通过浸出毒性研究发现MgO与污泥共热解制备生物炭对重金属的固定效果更优. 添加CaO对重金属固定效果由好到次依次为Pb>Cu>Cr>Cd,添加改为MgO时重金属固定效果依次为Pb>Cu>Cd>Cr. 分析发现,吸附差异主要取决于共热解添加物所能提供的吸附位点以及各吸附位点与重金属之间的吸附次序. 共热解添加物可以促进重金属的固定,张进等[63]将稻壳与污泥等比例共热解,相比原污泥中Mn、Ni、Cr、Zn、Pb、Cu的有效态含量下降百分比分别为85.94%、79.83%、76.83%、63.41%、31.74%、30.76%,这是由于稻壳含有丰富的Si元素并且在热解过程中含Si化合物与重金属结合固定降低了重金属的生物有效性. 汪刚等[64]研究了添加不同塑料对污泥定向热解产物的影响,发现塑料在热解过程中产生的自由氯易与重金属发生结合生成高挥发性的重金属氯化物. 以上研究中污泥与各物质共热解制备的污泥基生物炭中重金属存在形态如图1所示,发现重金属在迁移转化过程中有一部分与P发生耦合作用,可以在固定重金属的同时实现P富集. 但是,二者之间的耦合机制还有待进一步探究,且结合态的稳定性以及分解后的存在形态也是制约污泥基生物炭应用的一大问题.
-
污泥通过定向热解生成含有官能团和芳香结构的生物炭,可以很好的削减有机污染物,例如降低多环芳烃(polycyclic aromatic hydrocarbons, PAHs)、全氟及多氟化合物(per-and polyfluoroalkyl substances,PFAS)、多氯联苯(polychlorinated biphenyls,PCBs)等的浓度. 当采用柳木和污泥按照4:6的比例混合,在温度为700 ℃、气氛为CO2条件下定向热解制得生物炭[45],能够有效降低3—6环的PAHs,使其占比低至9.0%. PFAS通常在热解温度450 ℃以下就可以被分解挥发,且在500 ℃以上全氟辛烷磺酰基化合物(PFOS)和全氟辛酸(PFOA)的去除率就可以达到90.0%以上[65]. MOŠKO等[66]对污泥热解发现700 ℃及以上且保留足够停留时间(>30 min)PAHs、PCBs等大多数可以挥发到气相,去除效率可达99.8%以上,污泥中含有的抗生素等药物大多也挥发或者分解. ALIPOUR等 [67]发现了同样的规律,并且Brown等 [68]对木炭热解也发现随着温度升高产物毒性和PAHs浓度显著降低. Buss[69]对污泥热解有机污染物的综述也表明,当温度高于500 ℃对药物等有机物的削减率达到99.0%以上. 因此,挥发性和热降解是去除PAHs、PCBs、药物等有机污染物的最重要手段,但是需要对其热解保持中高温条件并维持一定时间.
综合以上分析,污泥热解想同时达到P固定与缓释、重金属低生物有效性、有毒物质含量降低可以通过调节热解气氛、热解温度以及共热解添加物来实现. 从污泥基生物炭的孔隙结构以及生物产气的角度考虑,CO2可以作为较优的热解气氛选择,在降低活化能促进反应进行的同时完善污泥基生物炭的孔隙结构. 在中高温度条件下控制热解速率可以实现对有机物的大部分降解,还能实现重金属的固定. 但是,高温会影响热解气氛对孔径结构的调控,而共热解添加物的引入会让热解气氛对孔径结构的影响减弱,同时共热解添加物可以为重金属的固定提供不同的吸附位点. 高温(700 ℃)条件下的污泥基生物炭对P有较强的吸附能力且解吸率低. 因此,保持较高的热解终温并且调控CO2/O2热解配比能有效富集P、固定重金属以及去除有机污染物,而对特定重金属的固定则取决于共热解添加物所能提供的吸附位点.
-
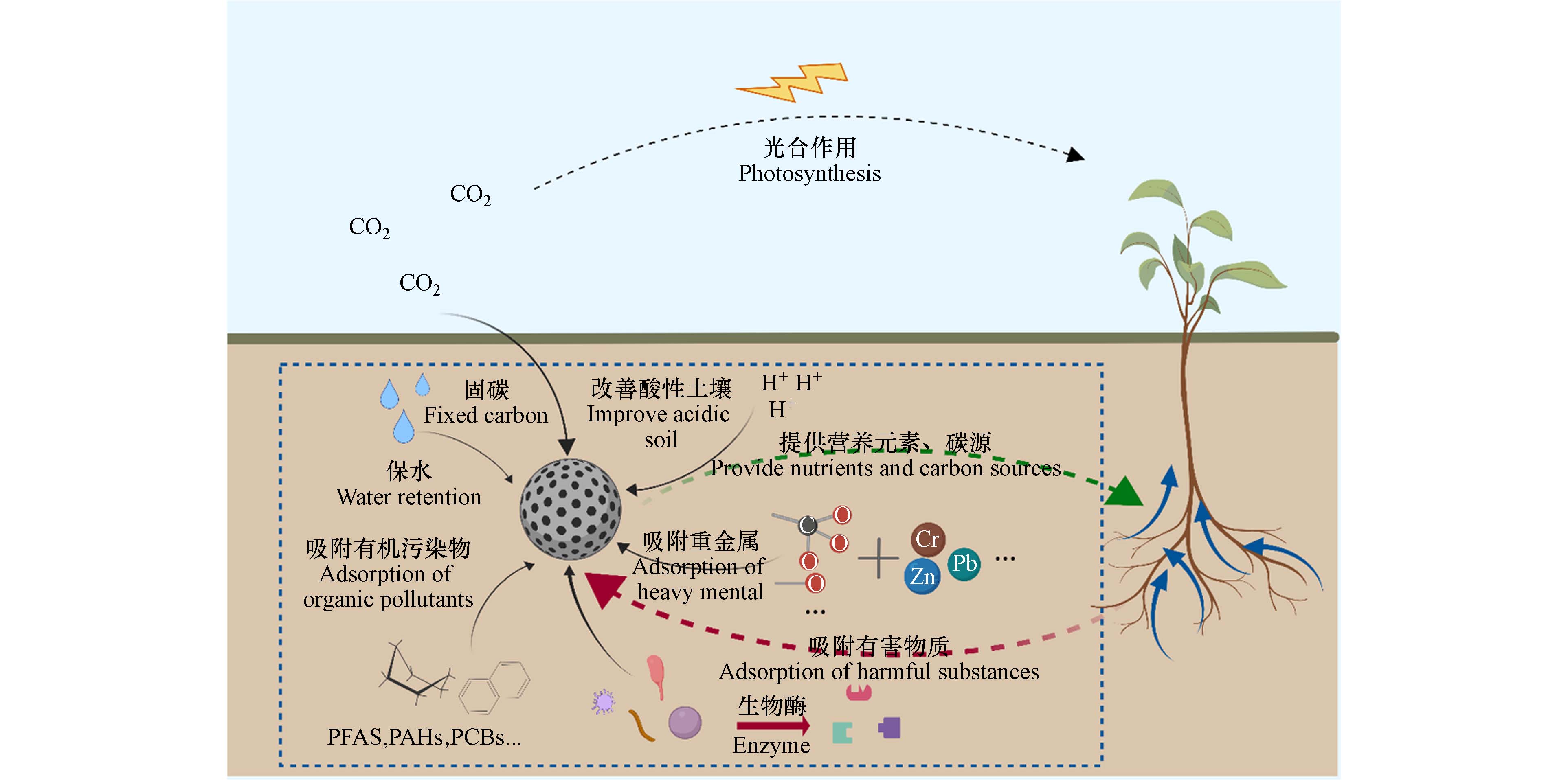
我国鼓励将处理后的污泥作为土壤改良剂用于土壤改良,而污泥基生物炭已经被大量的科学研究证明具有良好的土壤改良效果,对土壤的各种改良效果如图2所示.
污泥基生物炭修复酸性土壤是一种比较温和的方法,可以促进土壤生物活性、改善土壤理化性质并降低污染物的毒性[70 − 72]. 污泥基生物炭改善酸性土壤主要通过与酸性土壤中的H+发生中和反应以及生物炭中的阳离子释放与土壤H+交换,降低土壤H+含量,提高土壤的pH值,但是硝化作用释放质子会让土壤酸度逐渐恢复原来状态[73]. 因此,污泥基生物炭改善土壤pH与污泥中无机氮的存在形态有关,当以NH4+-N形态存在时,回用至土壤会降低土壤的pH,而当以游离氨的形态存在时则能提高土壤pH[74]. 卢再亮等[73]发现在500 ℃定向热解制备的污泥基生物炭相比低温热解生物炭对酸性土壤的改良效果更好,这是由于污泥基生物炭中的盐基阳离子与土壤中的交换性Al3+和H+发生离子交换. 王秋利等[75]将污泥与木屑按照2:1的比例在500 ℃热解2 h制备生物炭,回用至酸性土壤中经过培养发现,土壤的pH由4.37增长至6.69. 另外,酸性土壤相比其他土壤Cd含量较高,将污泥与木屑定向热解的生物炭添加土壤后能很好地固定并降低酸性土壤Cd含量,Cd含量降低约46%,对Hg和Pb也有同样的作用.
污泥基生物炭可以通过吸附土壤中的重金属和有机污染物达到修复受污染的土壤的目的,其稳定的碳质结构还能进一步促进土壤恢复. 污泥基生物炭的高表面积和孔隙结构使其具有较强的吸附能力,而其内部富含阳离子和氧化物的羟基可以以氢键和离子键结合有害物质. 周佳丽等[76]研究发现KOH改性后的污泥基生物炭对Pb2+有明显的吸附作用,吸附后的污泥基生物炭Pb2+含量由4.28%增加到19.05%,而镁离子和钙离子的含量下降,可能是Pb2+与其发生了离子交换. 另外,红外光谱发现Pb以—CO3自由基及Pb—O的形式负载在生物炭表面,即吸附Pb2+的方式主要是通过矿物沉淀、离子交换、含氧官能团络合及ᴨ键结合. 污泥基生物炭对有机污染物的吸附效果也较好,ZIELIŃSKA等[44]将700 ℃下热解污泥得到的生物炭加5%至富含PAHs的土壤中,使得改良后的土壤对菲的吸收率从8.3%提高到20.3%,芘从14.5%提高到31.7%,但是土壤中含有的溶解有机碳(DOC)和黏土矿物会影响生物炭的吸附效果. KRAHN等[77]的研究发现污泥基生物炭可以作为PFAS的有效吸附剂,这是因为污泥基生物炭拥有较低的C/N,因此生物炭碳结构外围有更多带正电的官能团,有助于与PFAS的带负电荷的羧酸头基进行阴离子交换从而实现对PFAS吸附[78 − 80]. 污泥基生物炭还可以有效吸附土壤中的抗生素等,污泥基生物炭C—O—Fe结构中的Fe是活化过二硫酸盐降解四环素的反应位点[81 − 82]. 因此,污泥生物炭界面结构可以有效活化过二硫酸盐有效吸附降解四环素[83 − 84].
污泥与生物质定向热解的产物生物炭还可以被用来改善盐碱土壤,例如韩剑宏等[85]将污泥和玉米秸秆按照5:2的比例混合在500 ℃定向热解制备生物炭并将其回用至盐碱土壤中,有机碳和可交换阳离子量相比原土壤增长了约9倍,大大提高了土壤的肥力和缓冲能力,而水溶性盐的含量降低约45%,消除了高盐含量对土壤肥力的不利影响.
-
生物炭的高比表面积和负电荷表面可以改善土壤结构,并增加土壤团聚体的稳定性. 生物炭的大量孔隙不仅可以作为微生物依附的结构,还可以增加土壤的保水性和通透性,提高土壤的水分和养分供应能力,更有利于土壤微生物的生长. 污泥基生物炭中含有的水溶性有机物主要由氨基酸和小分子碳水化物等组成,也可以被土壤中的微生物分解利用[75]. Tang等[86]的研究表明生物炭大孔(>50 nm)可以为微生物提供栖息的空间,而中孔(2—50 nm)和介孔(<2 nm)可以为微生物储存所需营养物质. 污泥热解制得的生物炭回用土壤对生物多样性也有影响,例如王秋利等[75]在500 ℃将木屑与污泥按照1:2的比例混合热解2 h,将制得的生物炭回用至土壤中. 经过培养,回用生物炭土壤对比原土壤Shannon指数变大,即生物群落多样性增大;Chao指数也增大,即物种总数增多. 在同样的条件下,将热解温度升至800 ℃,发现两种指数反而下降,即对土壤微生物群落的多样性和物种数有相反的作用. 另外,有研究发现PAHs苯环数决定其对土壤微生物的正/负影响[87],低环PAHs(苯环数≤4)可以被土壤微生物分解利用,高环PAHs(苯环数>4)则能与细胞表面的膜磷脂结合破坏细胞膜的功能. 因此,可以通过定向热解调控污泥基生物炭中活性成分,在土壤回用时起到促进土壤微生物的生长繁殖的作用[88 − 89].
生物炭添加至土壤中对土壤中酶活性的影响有两种不同的观点:一是认为,生物炭表面的羧基、羟基等会与土壤酶的氨基发生脱水缩合,改变土壤酶的活性位点及官能团结构从而降低土壤酶的活性. 土壤中脲酶和脱氢酶的活性是表征土壤氮素供应强度的重要指标,而污泥基生物炭的添加能明显增大这两种酶的活性[29]. 有机质可以通过离子键、氢键、共价键以及离子交换等方式固定土壤中酶分子,以此降低酶活性. 污泥基生物炭释放出的溶解性有机质还会抑制土壤中酸性磷酸酶的活性,降低土壤中有效磷的浓度[90];二是认为,生物炭对酶吸附的同时也会吸附底物,从而增大酶与底物的接触概率,促进酶促反应的进行[91]. 有研究总结发现,污泥在热解过程中可能会产生环境持久性自由基(environmentally persistent free radicals,EFPRs)[92],而EFPRs会氧化酶活性位点,对酶结构造成损害,从而抑制生物酶活性[93].
-
污泥基生物炭一方面在热解过程相较于燃烧可减少碳的释放量,另一方面将其应用于土壤可增大土壤的碳固存量. PARIYAR等[94]的研究表明,由于脱水和脱羧反应,较高热解温度能获得O/C、H/C较低的生物炭,550 ℃和600 ℃热解得到的生物炭更适于土壤碳固存,当生物炭中O/C<0.6时,半衰期最少可达100年[95]. Gusiatin等[96]将污水污泥、木屑、秸秆等物质共热解制备生物炭发现随着热解温度上升,生物炭的固定碳含量升至20%以上,将生物炭添加至土壤中发现土壤中溶解性碳含量随时间推移在不断下降,例如Hu等[97]将生物炭加入土壤中减少了50%的二氧化碳排放. 另外,有研究者从猪粪、污水污泥和小麦秸秆中提取的生物炭研究生物炭对二氧化碳的吸附行为,发现提高吸附温度和含水量可促进二氧化碳的吸收从物理过程转变为化学过程. 生物炭中的Mg、Ca、Fe、K 等矿物成分通过矿物反应可以诱导CO2的化学吸附,占总吸附量的17.7%—50.9%. 污泥基生物炭中的FeOOH被吸附的CO2转化为Fe(OH)2CO3[98],而猪粪生物炭中吸附的CO2则沉淀为K2Ca(CO3)2和CaMg(CO3)2,这导致两种生物炭中的不溶性无机碳显著增加,可以在土壤应用中形成稳定碳库. 对于小麦秸秆生物炭,吸附的二氧化碳诱导CaCO3转化为可溶性Ca(HCO3)2,从而导致可溶性无机碳的增加[99].
另外,污泥基生物炭的添加会通过影响土壤微生物群落进而影响土壤碳封存. Schwander等[100]报道了一种非天然的酶催化固碳途径,而这些固碳作用酶大多来自异养微生物等,而污泥基生物炭不仅可以为异养微生物提供寄居场所,还能为其提供营养物质,形成高效固碳循环[101]. 污泥基生物炭不仅可以抑制土壤中CO2的释放,对CH4也有吸收作用从而实现碳固定. 例如土壤中含有产CH4菌和 CH4氧化菌,添加生物炭可以改善土壤的通透性和保水性. 土壤孔隙度增大促使氧气含量增大抑制产CH4菌的活性,较高的含水率能增强CH4氧化菌的活性,从而减少CH4释放实现碳封存[102]. 综合以上分析,污泥基生物炭影响土壤碳封存主要包括以下几种途径. 污泥基生物炭施加到土壤中会影响土壤中有机碳库的矿化,进而导致CO2排放增加;污泥基生物炭可以吸附土壤中释放的CO2;污泥基生物炭可以显著影响参与二氧化碳代谢的土壤微生物活性和多样性,从而在很大程度上影响土壤碳释放[103 − 104].
目前,污泥基生物炭应用于实际土壤改良还相对较少,一方面原因是受其本身重金属毒性限制,另一方面经济成本也是需要考虑的一大问题. 其中,热解温度、停留时间和升温速率是影响热解过程能耗的关键因素,这些因素决定了污泥基生物炭的成本. 有研究将热解成本与市面商品做了对比,Wang等[47]将棉花秸秆与污泥共热解,制备1 t生物炭的成本约为350元,而市场上腐殖酸和生石灰每吨的成本分别为700元、1100元,制备生物炭的成本远低于市场具有相同肥效的商品肥. 因此,明确所需土壤改良剂的性质之后对污泥进行定向热解不仅可以实现污泥的无害化处理,还能降低原本处理成本节约资源.
-
本文综述了污泥热解条件变化对污泥基生物炭物化性质和土壤改良效益的影响. 碱土金属、生物质与污泥共热解能使磷转化为土壤有效磷,还能通过与正磷酸盐、羟基化合物、金属氧化物等结合的方式固定污泥本身含有的重金属,并且污泥中含有的多环芳烃、全氟化合物等物质经过热解去除率可以达到90%及以上. 热解的温度会影响污泥基生物炭的pH、孔径大小和比表面积,而通过调控共热解添加物不仅可以定向调配污泥基生物炭中磷和重金属的存在形态还能增大其比表面积,优化孔隙结构. 热解一般采用氮气为主的惰性气氛以实现污泥的定向热解,而采用CO2热解气氛相比氮气能形成更丰富和优化的孔隙结构且降低反应的活化能. 因此,通过调控热解条件可调控污泥基生物炭的特性以应用不同场景,例如污泥与生物质的共热解能用来改良盐碱地;提高热解温度,可以增大污泥基生物炭的pH用来改善土壤酸化;而碱土金属共热解制备的污泥基生物炭具有缓释磷肥的功效同时还能吸附重金属及有机污染物,降低土壤生态风险修复受污染土壤.
污泥定向热解富集磷的机理目前已经研究较多,且对污泥基生物炭重金属最终形态也有所了解,但是在污泥热解过程中重金属的迁移转化机制还有待进一步明确,关于磷和重金属在热解过程中存在的关联机制也尚不清楚,还需要进一步研究. 另外,将污泥热解产物转化为增值产品仍然存在实际运行困难. 基于此,本综述提出以下展望:明确重金属在污泥热解过程中的动力学过程,以及P与重金属之间的关联转化机制对其安全土壤回用尤为重要;热解产物生物气、生物油也应该实现同步回收,它们也应该被进一步加工利用,可以代替普通肥料、气体燃料及交通燃料. 因此,需要对热解工艺进一步研究和创新,明确重点元素迁移转化机制指导实现生物炭的定向制备,降低污泥处理成本并将其转化为可增值产品,使污泥在资源回收利用中由小规模向大规模发展.
污泥共热解制备污泥基生物炭及其在土壤回用中的改良效益
Directional pyrolysis of sludge to prepare sludge-based biochar with soil improvement function
-
摘要: 随着全球污泥产量的快速增长,对其的资源化处置是亟待解决的现实问题. 相较于传统的填埋以及新型的焚烧工艺,污泥热解可实现污泥的无害化、减量化并生成具有土壤改良潜力的污泥基生物炭,是污泥处理的一种较优选择. 本文以市政污泥为研究对象,全面综述了污泥不同热解方法对生成污泥基生物炭的物化性质和其对土壤改良效应的影响,重点介绍了污泥中磷和重金属在不同热解工艺中的迁移转化机制,污泥基生物炭对土壤物化性质的影响机理、对污染土壤的修复机制、对土壤中微生物和微生物酶等的作用机制. 通过以上分析,能够以此为理论支撑指导制备具有定向改良土壤功能的污泥基生物炭. 本综述将有助于污泥定向热解制备污泥基生物炭的进一步发展,为污泥基生物炭土壤改良提供理论参考和支持.Abstract: With the rapid growth of global sludge production, how to recycle it into resource is an urgent realistic problem. Compared with traditional direct landfill disposal and incineration, pyrolysis of sewage sludge is a superior disposal method not only because it can realize the harmlessness and reduction of sludge, but also can generate sludge biochar, which has potential value for soil improvement. In this paper, the effects of different pyrolysis methods on sludge properties and soil improvement effects were comprehensively reviewed. The migration and transformation mechanisms of phosphorus and heavy metals in pyrolysis of sewage sludge, the effects of sewage sludge biochar on soil characteristics, the remediation mechanisms of sewage sludge biochar on heavy metal and organic contaminated soil, and the effects of sewage sludge biochar on soil microorganisms and microbial enzymes were mainly introduced. Through the above analysis, this can be used as a theoretical support to guide the preparation of sludge-based biochar with the function of directional soil improvement. This review will contribute to the further studies of tailored pyrolysis of sewage sludge, and provide theoretical reference and support for using sewage sludge biochar in soil improvement.
-
邻苯二甲酸酯(phthalate esters, PAEs)又称酞酸酯,是一类重要的合成有机物,被广泛应用于塑料制造[1],常用作涂料、润滑剂、粘合剂、杀虫剂、包装和化妆品的添加剂[2]。有文献报道了国内23个城市的90个自来水厂141个水源水样中均检出了邻苯二甲酸单酯(MPAEs)[3],邻苯二甲酸二丁酯(DBP)是PAEs中的一种,在增塑剂中应用最为广泛,极易从塑料中释放到环境中[4-5],是一种环境激素类物质,具有致癌、致畸与致突变作用[6-8],因此,开展PAEs此类污染物在不同环境中的降解研究对于生态环境安全保障尤为重要。
目前,对DBP污染的生物降解研究主要集中在高效降解菌的筛选、驯化及降解机理等方面[9-10],游离态菌株在实际应用中存在降解周期长、菌体易流失、环境耐受性差等问题,因此,国内外学者利用固定化微生物技术解决生物降解的缺陷,已应用在处理生活废水[11]、池塘模拟废水[12]、难降解有机废水[13-14]等水污染治理方面。为了得到具有高固定化强度和高微生物活性的固定化系统,可选择两种及以上的固定化材料结合起来的复合固定化法,例如:采用聚乙烯醇和海藻酸钠为包埋材料、活性炭为吸附材料、CaCl2的饱和硼酸溶液为交联剂,同时,负载较强生物活性的高效降解混合菌势必会提高生物解吸的效率,最终获得对底物优异的降解性能[15],具有较强的实际应用性。
本研究以DBP为目标污染物,开展了DBP降解混合菌(以下简称DP3)的包埋-吸附-交联固定化条件优化及降解特性研究,以聚乙烯醇(PVA)和海藻酸钠(SA)为包埋材料、活性炭为吸附材料,CaCl2的饱和硼酸溶液为交联剂,采用正交试验确定最佳固定化制备条件,并以游离态混合菌为对照,研究了pH值、盐度、DBP浓度对固定化混合菌降解性能的影响,研究结果可为DBP降解菌在环境修复中的应用提供理论依据和技术支持。
1. 实验部分(Experimental section)
1.1 供试菌剂及菌悬液制备
本研究供试混合菌DP3由本实验室保存的DBP高效降解菌鲍曼不动杆菌、唐氏不动杆菌、弗氏柠檬酸杆菌菌悬液复配而成。各菌株的菌悬液制备方法为:将菌液接种到LB培养基,于30 ℃,150 r·min−1摇床活化培养,将活化好的培养液5000 r·min−1离心5 min,收集的菌体用pH=7.2磷酸盐缓冲液清洗2遍,生理食盐水清洗3遍,重新离心,弃去上清液。取适量湿菌体用无菌水配制成菌悬液,调节OD600至1.0。混合菌DP3由各菌悬液按3∶3∶2比例配制生成。
1.2 仪器、药品和培养基
气相色谱-质谱联用仪(7890B-7000C,美国Agilent公司);超声清洗器(KQ5200DB,昆山市超声仪器有限公司); 旋转蒸发器(RE5299,海亚荣生化仪器厂);紫外分光光度计(UV-5100B,上海分析仪器有限公司)。
本研究所用药品除特别注释均为分析纯,其中邻苯二甲酸二丁酯标样购自美国Accustandard公司,色谱纯正己烷购自上海赛默飞世尔科技有限公司。
牛肉膏蛋白胨培养基(LB):牛肉膏5 g,蛋白胨10 g,NaCl 5 g,蒸馏水1 L,pH值为7.2—7.4。
无机盐培养基(MSM):K2HPO45.1 g,KH2PO4 2.5 g,(NH4)2SO4 2.0 g,MgCl2 0.16 g,微量元素溶液1.0 mL;微量元素溶液:CaCl2 20 mg,Na2MoO4·2H2O 2.4 mg,FeSO4·7H2O 1.8 mg,MnCl2·4H2O 1.5 mg。
模拟人工污水:葡萄糖0.1700 g;可溶性淀粉0.1600 g;CH3COONa 0.2330 g;NH4Cl 0.45 g;KNO3 0.1 g;(NH4)2SO4 0.0284 g;KH2PO4 0.0700 g;Na2CO3 0.0600 g;pH=7.2,去离子水1.0 L。121 ℃灭菌30 min后使用。
1.3 测试分析方法
1.3.1 DBP提取及检测方法
取待测的DBP无机培养基溶液50 mL于150 mL锥形瓶中,加入等体积正己烷,常温下超声提取30 min静置。利用分液漏斗取出上层有机相,加入4 g无水硫酸钠干燥并浓缩至0.5 mL,最后用正己烷定容至1 mL,转入棕色2 mL样品瓶,待测。
GC-MS色谱条件:Agilent HP-5MS UI色谱柱(30 m×0.25 mm×0.25 μm);进样口温度为280 ℃;程序升温:初始柱温80 ℃,保持1 min,以20 ℃·min−1上升至280 ℃,保持4 min,载气:氦气,流速1 mL·min−1; 进样方式:不分流进样;进样量:1 μL。
GC-MS质谱条件:电子轰击离子源模式(EI),离子源温度300 ℃,四极杆温度150 ℃,MSD传输线温度300 ℃,电子能量70 eV;扫描范围为50—550 m/z[16]。
1.3.2 扫描电镜样品的制备
取外形规则的固定化凝胶球用0.1 mol·L−1的PBS 缓冲溶液清洗3次,每次10—15 min,在4 ℃下,2.5%戊二醛固定12 h,0.1 mol·L−1的PBS缓冲溶液清洗3次,每次10—15 min,依次在50%、70%、80%、90%和100%质量浓度的乙醇溶液中脱水1次,每次30 min,然后用1∶1的乙醇和乙酸异戊酯置换乙醇1次,乙酸异戊酯置换乙醇2次,每次30 min,于CO2临界点干燥,切片,将样品固定在样品托上,喷金,待测。
1.4 DBP混合菌固定化及正交试验
选择PVA和SA包埋材料,活性炭粉末(过1 mm筛)作为吸附剂,氯化钙和硼酸作为交联剂。首先,称取一定量的活性炭,将制备好的5 mL菌悬液与活性炭混合,摇床振荡吸附0.5 h。然后,将PVA和SA按一定比例混合后加入30 mL蒸馏水浸泡12 h,灭菌后冷却至30 ℃后,加入吸附有菌体的活性炭,接着,用无菌水定容至50 mL,搅拌均匀后用注射器从20 cm高处将其缓慢匀速滴加至一定质量分数的氯化钙-饱和硼酸溶液中(用Na2CO3调pH 6.7左右),磁力搅拌,凝胶颗粒交联24 h。最后,用无菌水和生理盐水分别冲洗2次,保存于4 ℃冰箱中,备用。
为确定混合菌最佳固定化制备条件,选定海藻酸钠(SA)、聚乙烯醇(PVA)、活性炭(AC)和CaCl2质量分数为试验因素,各因素分别设置3个水平,按L9(34)正交表设计正交试验(表 1)。
表 1 正交试验设计Table 1. Orthogonal design of immobilization水平Level 因素Factor A:PVA/% B:SA/% C:AC/% D:CaCl2 /% 1 8 1 1 1 2 10 2 2 2 3 12 3 3 3 1.5 固定化混合菌DP3和固定化空白凝胶球对DBP降解率的测定
取灭菌的无机盐培养基50 mL,保持DBP的最终浓度分别为10、20、50、100、200、500、1000 mg·L−1。根据最佳固定化制备条件结果(A2B2C3D1),将制备好的固定化凝胶球和不接菌空白凝胶球按照相同的接种量接种到锥形瓶中,于150 r·min−1、30 ℃恒温培养。每个处理设3个重复,测试24 h的降解率。
DBP降解率=DBP初始浓度−DBP残留浓度DBP初始浓度×100% 1.6 不同环境因素对固定化和游离态微生物降解性能的比较
在灭菌的三角瓶中加入1000 mg·L−1的DBP的正己烷溶液0.5 mL,挥发尽正己烷,然后加入灭菌的无机盐培养基50 mL,保持DBP的最终浓度为10 mg·L−1,分别加入制备好的固定化微生物凝胶球和菌悬液,使接菌量保持一致。研究不同环境因素(pH、NaCl浓度和DBP浓度)对固定化微生物的降解性能:pH(4、5、6、7、8、9、10);NaCl浓度(5、10、20、50、100 g·L−1);DBP浓度(10、20、50、100、200 mg·L−1)。每个处理设3个重复。30 ℃、转速150 r·min−1下培养,测定3 d固定化和游离态混合菌的降解率。
1.7 固定化DBP混合菌的长期稳定性及模拟人工污水DBP降解试验
取灭菌的无机盐培养基50 mL,加入制备好的固定化微生物凝胶球,保持DBP的最终浓度为10 mg·L−1,于150 r·min−1、30 ℃ 恒温培养 3 d。每个处理设3个重复,重复20次,研究固定化DBP混合菌的长期降解稳定性。
取灭菌的模拟人工污水50 mL,实验方法同长期稳定性试验,测定6 d固定化微生物凝胶球和游离态混合菌在模拟人工污水中的降解率。
1.8 降解动力学模型
采用一阶动力学模型对降解数据进行拟合,模型方程如下:
Ct=C0e−Kt t1/2=ln2K 式中,Ct是t(d)时体系中DBP的总浓度(mg·L−1);C0是初始时DBP总浓度(mg·L−1);K是微生物降解一阶动力学参数(d−1);t1/2是半衰期(d)。
2. 结果与讨论 (Results and discussion)
2.1 DBP降解混合菌固定化条件优化
为考察聚乙烯醇(PVA)、海藻酸钠(SA)、活性炭(AC)、CaCl2浓度等4种因素对包埋小球降解DBP能力的综合影响,确定固定化载体最佳制备条件,以DBP去除率为目标值设计正交试验,结果如表2所示。对比各因素所对应的R值可知,各因素对固定化混合菌降解DBP能力的影响由大到小依次为C:AC含量>A:PVA含量>B:SA含量>D:CaCl2含量,根据各因素所对应的Ⅰj、Ⅱj、Ⅲj可知各因素之间最优组合为A2B2C3D1。
表 2 固定化条件优化正交试验结果Table 2. Orthogonal experimental results序号Number 因素Factor DBP去除率/%DBP Removal rate PVA SA AC CaCl2 1 1 1 1 1 88.57 2 1 2 2 2 93.88 3 1 3 3 3 95.62 4 2 1 2 3 95.73 5 2 2 3 1 99.86 6 2 3 1 2 91.58 7 3 1 3 2 95.77 8 3 2 1 3 90.15 9 3 3 2 1 94.33 Ⅰj 92.69 93.36 90.10 94.25 Ⅱj 95.72 94.63 94.65 93.74 Ⅲj 93.42 93.84 97.08 93.83 Rj 3.03 1.27 6.98 0.51 2.2 DBP降解混合菌固定化凝胶球微观结构分析
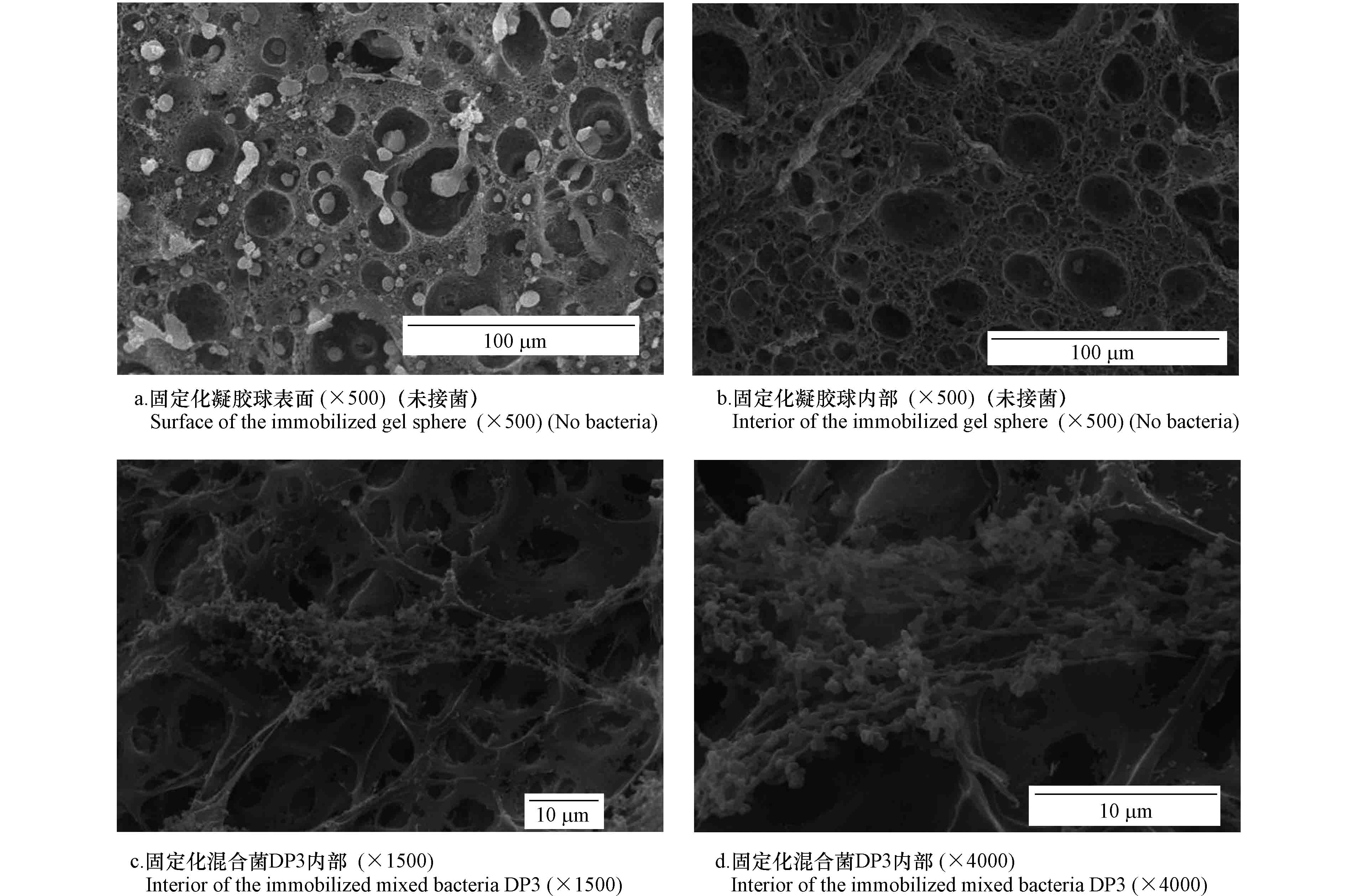
固定化空白和微生物凝胶球进行扫描电镜前处理制备,喷金后观察其表面和内部结构,结果如图1所示。由图1(a)可以发现,固定化空白凝胶球的表面不光滑,存在密集的孔穴;从图1(b)可知,在固定化空白凝胶球内部,PVA-SA-AC复合材料构筑由孔道相互连通的大量空腔,呈孔网结构。图1(c)、(d)发现,混合菌DP3以网状菌落交织被复合材料包埋吸附在凝胶球的内部,由于菌体明显小于内部孔径,有利于微生物在内部的自由运动、增殖和快速摄取营养物质和溶解氧[17]。邻苯二甲酸二丁酯分子自由进入凝胶球内部与微生物产生作用被降解,外密内疏结构对维持固定化微生物良好的内部环境起到了重要的作用,是保证固定化混合菌较高DBP降解率的重要因素。
2.3 固定化混合菌DP3和空白凝胶球对DBP的降解性能
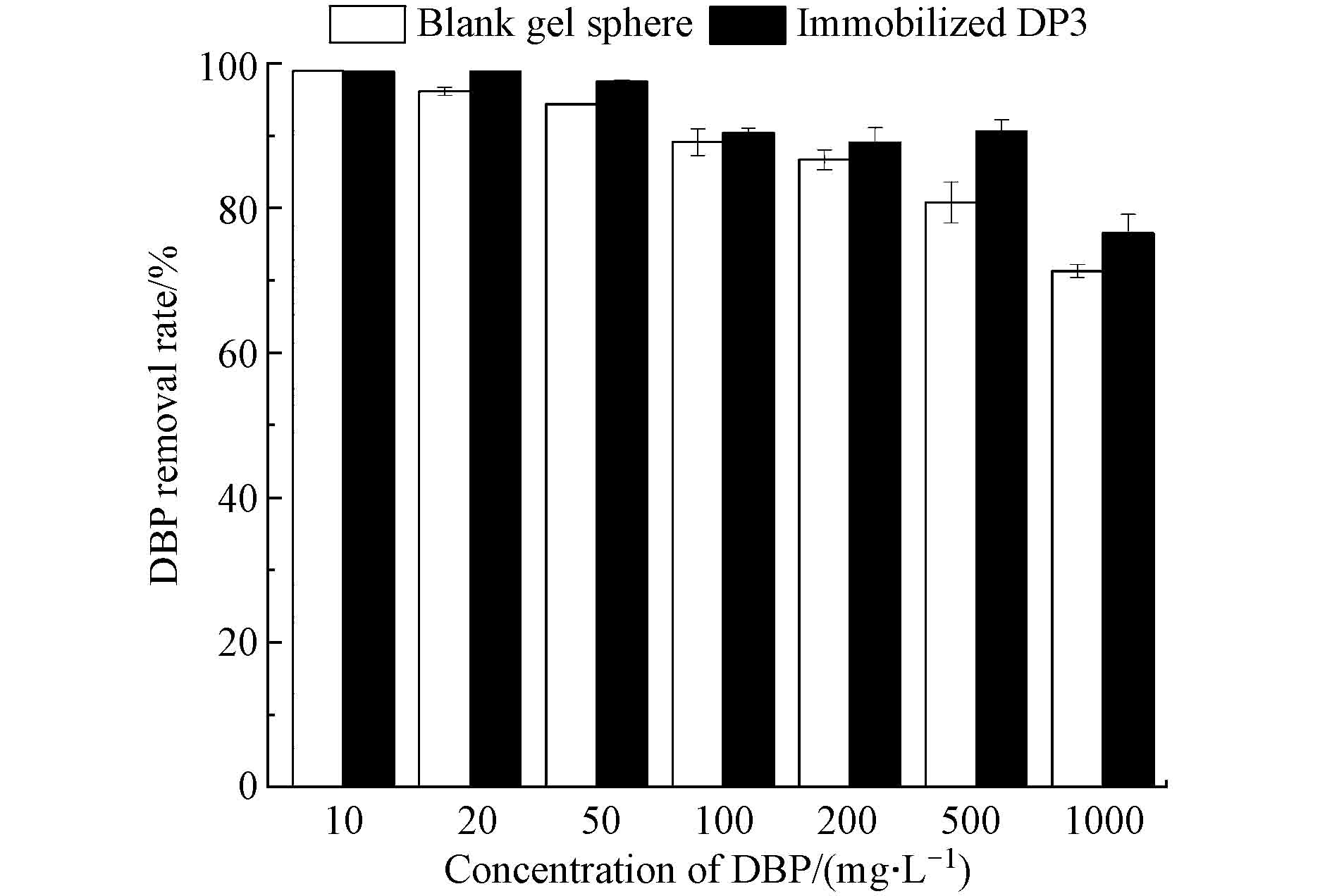
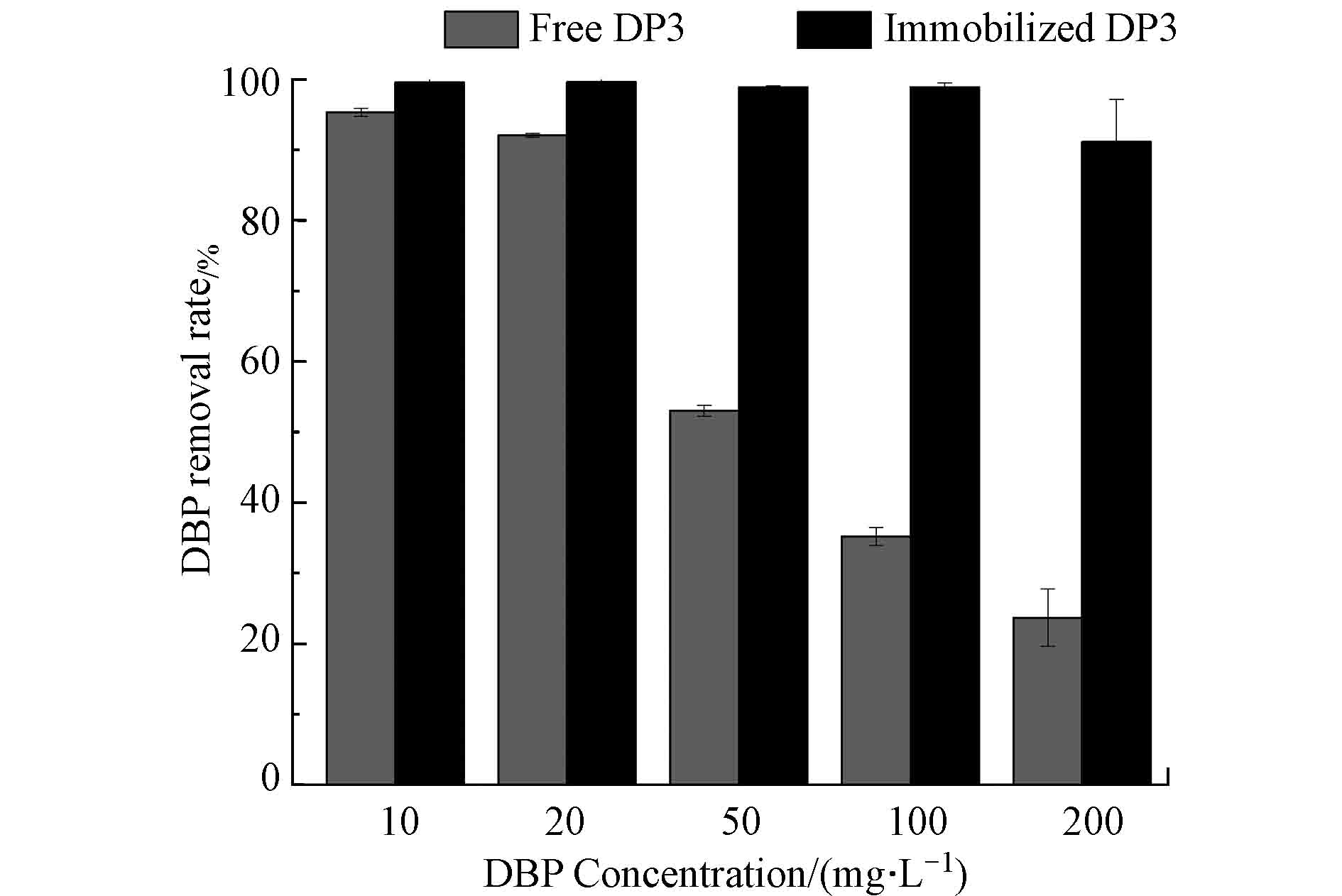
为了解固定化混合菌DP3去除DBP的机理,对比了固定化DP3和空白凝胶球对DBP的去除效果,结果如图2所示,DBP的浓度为10 mg·L−1时,固定化DP3和空白凝胶球对DBP的去除率均能达到99%以上;DBP的浓度在20—200 mg·L−1时,空白凝胶球对DBP的去除率呈现缓慢下降趋势,DBP的浓度为500 mg·L−1时,吸附平衡达到相对饱和,同时,DBP浓度的升高,为负载在小球中混合菌DP3提供可利用碳源,进而提高了微生物的活性[18],所以,DBP浓度在500—1000 mg·L−1时,固定化DP3对DBP去除效率显著优于空白凝胶球,随着DBP浓度的降低,平衡向吸附作用方向移动,残余的DBP被吸附至小球内被微生物降解,由此可见,经过包埋-吸附联合固定化后的混合菌DP3能够保持较高生物活性。
2.4 不同环境因素对固定化混合菌DP3降解能力的影响
2.4.1 pH
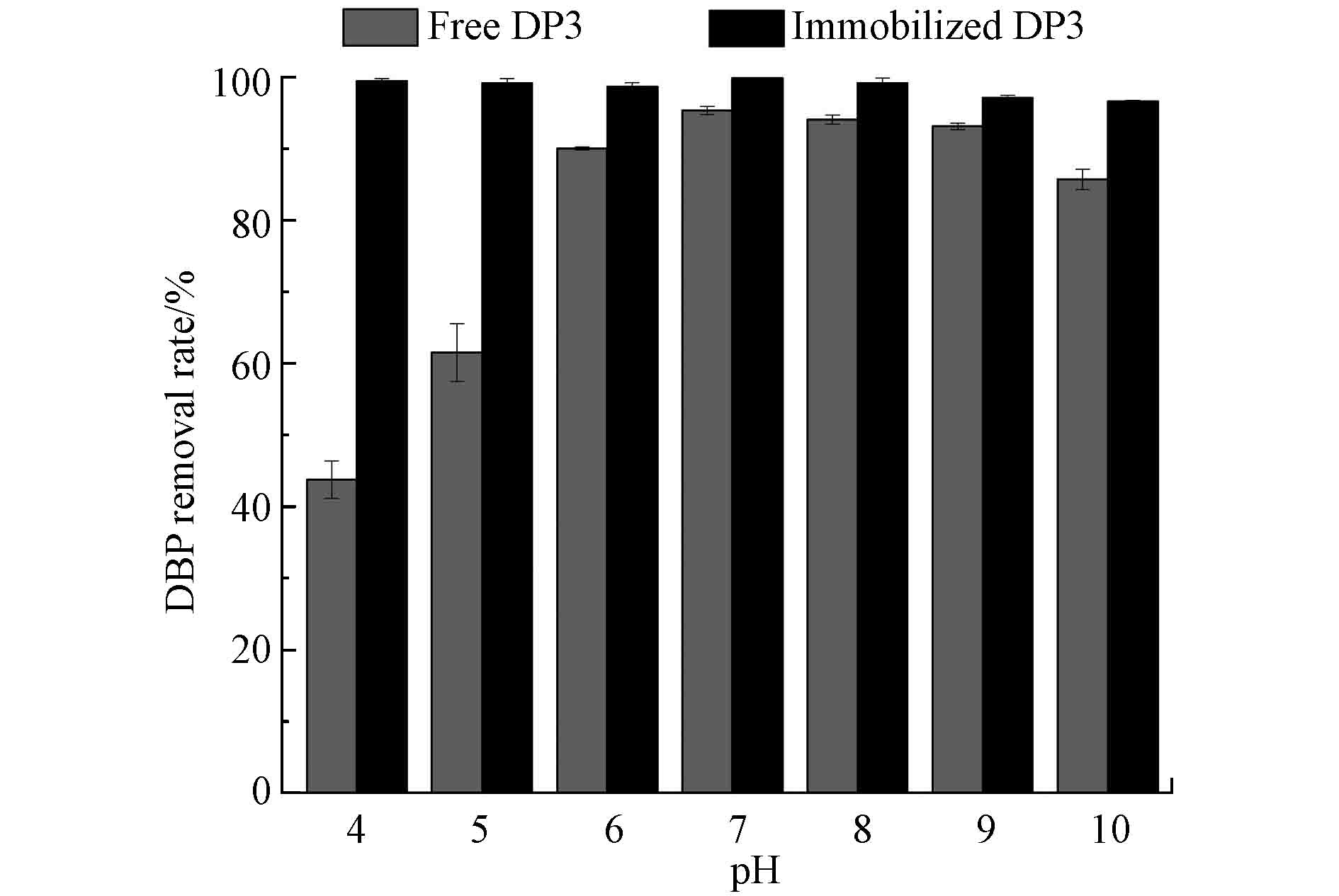
以游离态混合菌DP3为对照,开展了pH值对固定化DP3降解DBP的影响研究,如图3所示,pH值在6—9时,固定化和游离态混合菌DP3对DBP的降解能力相对较为稳定,pH值为7时,3 d内对DBP降解率均可达到最大值,而处于较强的酸碱条件时,游离态混合菌DP3的降解能力显著下降,在pH4—6之间时最为明显。而固定化混合菌DP3的pH值变化对DBP降解能力的影响极小,在pH9—10之间有极微小的变化,明显高于游离态混合菌DP3的降解能力。这是由于固定化凝胶球具有外层紧密,向内逐渐松散的结构特征,能够对包埋的混合菌起到一定的保护作用,而且固定化载体上负载的—NH2、—COOH等基团能够对酸碱环境进行缓冲[19]。对于游离态混合菌DP3来说,较强的酸碱条件改变了细胞膜的通透性,并且导致DBP降解酶失活[20-21],从而影响游离态混合菌对DBP的降解能力。所以,固定化混合菌DP3对pH的耐受范围明显高于游离态混合菌DP3,可以保持稳定的生物活性,显示出固定化技术的优势。
2.4.2 NaCl浓度
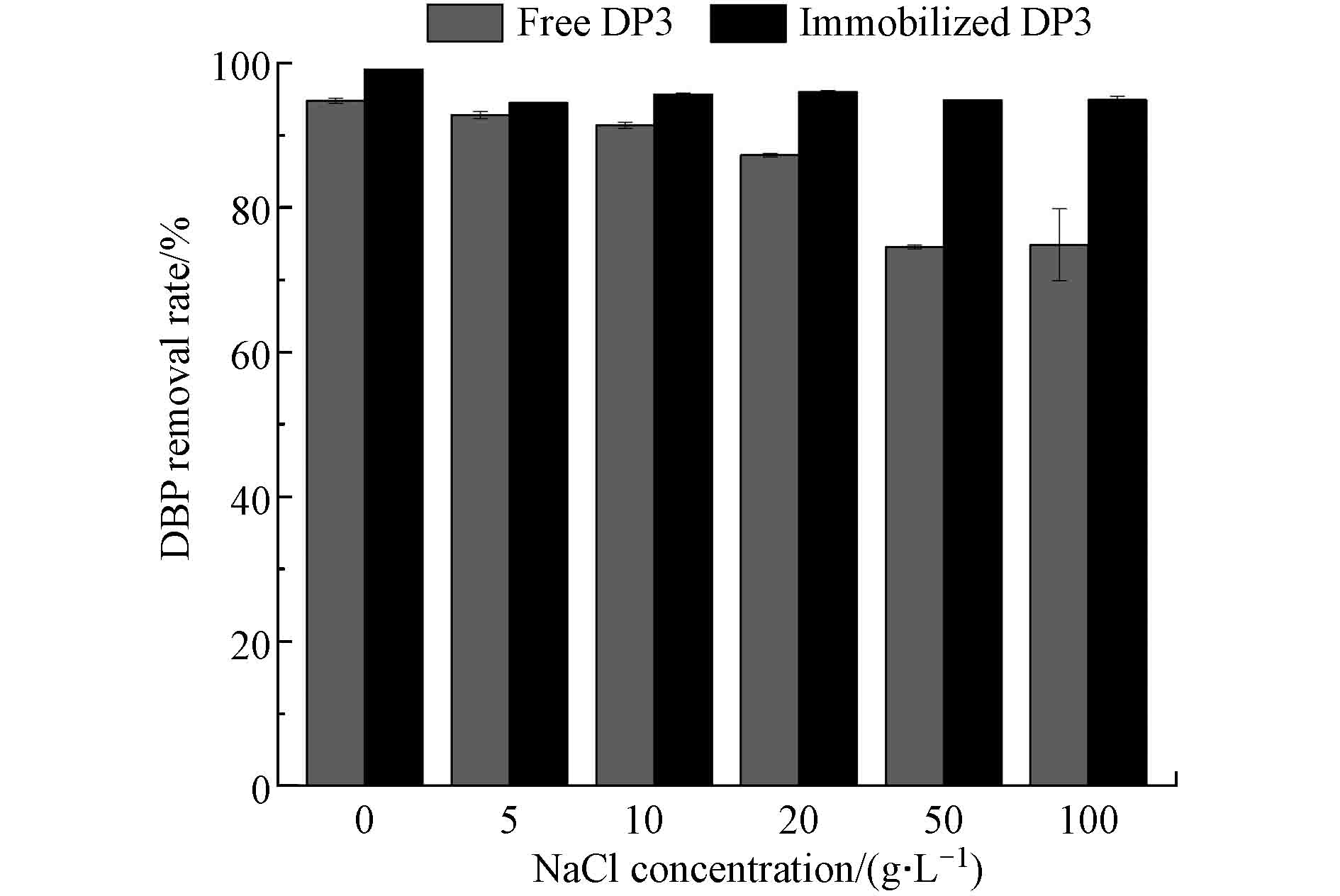
NaCl浓度对固定化和游离态混合菌DP3降解DBP的影响如图4所示,NaCl浓度为0 g·L−1时,固定化和游离态混合菌DP3对DBP在3 d时的降解率均可达到最大值,分别为99.13%和94.77%。NaCl浓度在5—10 g·L−1之间时,游离态混合菌对DBP降解效果较为稳定,NaCl浓度在20—100 g·L−1之间时,随着NaCl浓度增大,游离态混合菌对DBP的降解效果逐渐下降,而固定化后的混合菌对DBP的降解效果较为稳定,且显著高于游离态混合菌的降解效果。这是由于随着盐度提高,细胞内与外界的渗透压逐渐失去平衡,使得细胞内的水分慢慢向外界流失,致细胞脱水,菌株生长受到抑制,进而影响菌株对DBP的降解,而固定化后,固定化材料对混合菌起到良好的保护作用并为其提供一个适宜的生长环境,随着NaCl浓度增大,固定化复合菌对DBP的降解效果也有所降低,这可能是由于小球外表面附着的混合菌受到NaCl浓度影响,而失去活性,从而影响其对DBP的降解效果。
2.4.3 DBP浓度
DBP浓度对固定化和游离态混合菌DP3降解DBP的影响如图5所示,当DBP浓度处于10—20 mg·L−1时,固定化和游离态混合菌DP3对DBP有着显著的降解作用,而且DBP浓度为10 mg·L−1,时,1 d内固定化混合菌DP3对DBP降解效果可达到98.84%,与游离态混合菌相比,其降解率显著提高35.11%,当DBP浓度大于20 mg·L−1时,随着DBP浓度的增加,游离态混合菌DP3对DBP的降解能力明显下降;而固定化混合菌DP3对DBP的降解能力随着DBP浓度的增加较为稳定,且显著高于游离态混合菌DP3。在DBP浓度为200 mg·L−1时,固定化混合菌DP3对DBP在3 d时的降解效果仍可达到91.15%。这是由于DBP具有细胞毒性[22],高浓度的DBP会抑制菌株的生长,进而影响游离态混合菌对DBP的降解效率,而固定化材料具有外紧内松的结构特征,DBP向内部扩散时浓度递减,对混合菌起到良好的缓冲作用[23]。可知,固定化的混合菌微生物密度较高,包埋、吸附材料对于DBP的吸附作用也可使微生物与污染物更好的接触,从而使得固定化混合菌对高浓度DBP降解能力明显高于游离态混合菌。
2.4.4 固定化混合菌DP3和游离态混合菌DP3的降解动力学
固定化和游离态混合菌DP3降解不同浓度的DBP(10、20、50、100、200 mg·L−1),从拟合方程(表3)可知,固定化和游离态混合菌DP3对底物降解符合一阶动力学方程,随着底物浓度的逐渐增大,固定化DP3对其降解性能降低,说明固定化DP3对底物DBP的浓度具有一定的耐受范围。相对游离态,降解同等浓度的底物,固定化DP3的半衰期缩短,降解速度明显增加,对底物DBP的耐受性增强,据推测是因为包埋载体的底物传质阻力降低了高浓度有毒底物的冲击,同时负载的微生物密度较高,少量菌体失活不会对整个体系微生物的降解活性产生影响[24]。
表 3 固定化DP3的DBP降解动力学方程Table 3. Equation of DBP degradation kinetics by immobilized DP3名称Name 初始浓度/(mg·L−1)Initial concentration 动力学方程Degradation kinetics 动力学参数/h−1Kinetic parameter t1/2/h R2 10 lnC=−0.1859t+2.3026 0.1859 3.7284 0.8022 20 lnC=−0.1869t+2.9957 0.1869 3.7089 0.8008 固定化DP3 50 lnC=−0.1540t+3.9120 0.1540 4.5014 0.8487 100 lnC=−0.0977t+4.6052 0.0977 7.0951 0.9283 200 lnC=−0.0922t+5.2983 0.0922 7.5175 0.9353 10 lnC=−0.0426t+2.3026 0.0426 16.2671 0.8869 20 lnC=−0.0352t+2.9957 0.0352 19.7153 0.9181 游离态DP3 50 lnC=−0.0105t+3.9120 0.0105 65.9889 0.9916 100 lnC=−0.0060t+4.6052 0.0060 114.8983 0.9972 200 lnC=−0.0037t+5.2983 0.0037 184.4257 0.9989 2.5 固定化混合菌DP3的长期稳定性
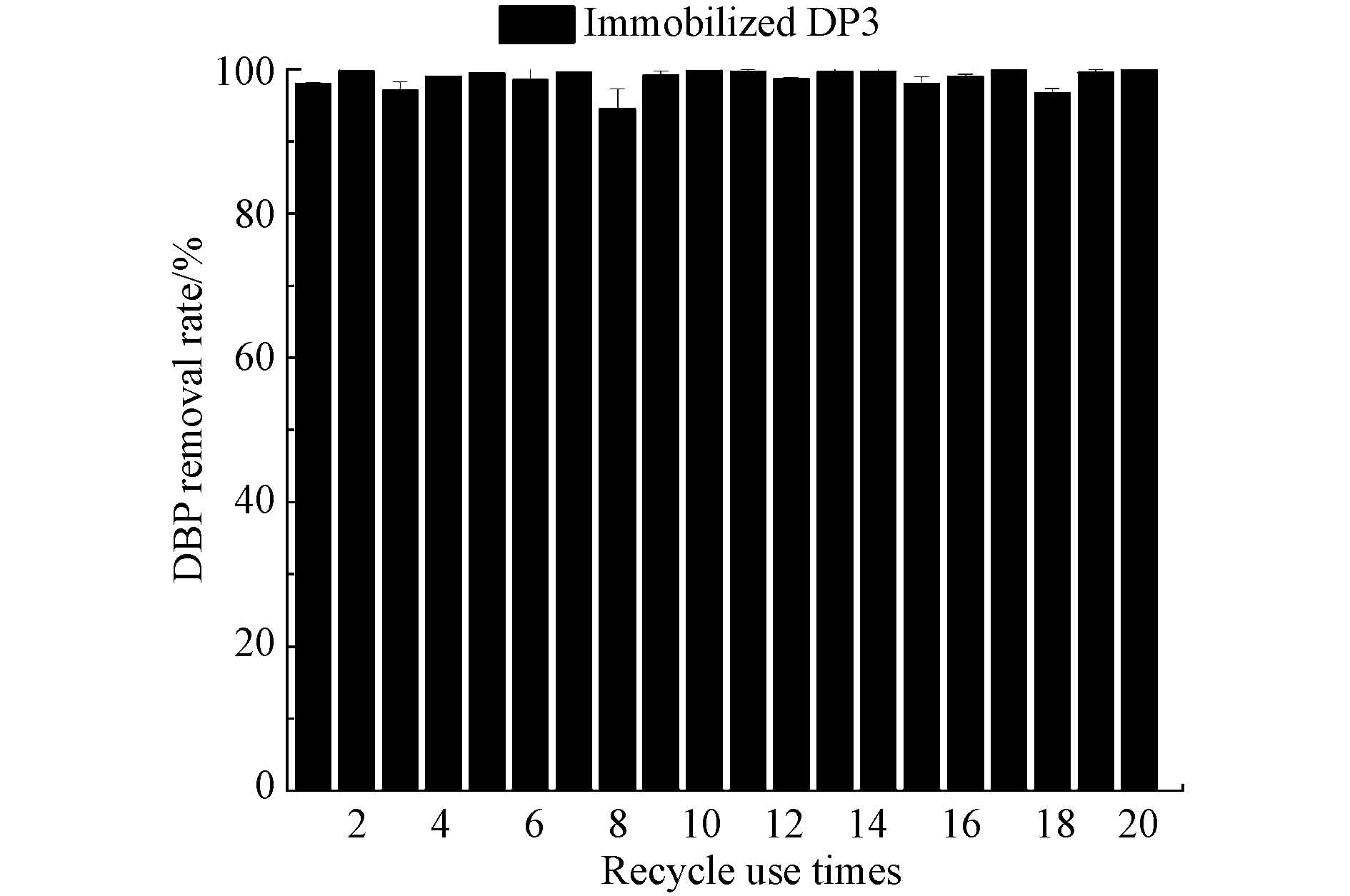
为考察固定化混合菌DP3重复使用的稳定性,在固定化DP3最佳制备和环境条件下,对10 mg·L−1 DBP进行降解实验,固定化混合菌DP3凝胶球重复循环使用20次,结果如图6所示,凝胶球始终保持良好的降解活性,且稳定,1 d内,重复20次固定化混合菌DP3对DBP的降解效果仍能达到99.95%,说明固定化混合菌在前期使用中受到DBP的驯化,催化其生物活性,重复过程中优化了降解性能,反映出固定化混合菌DP3降解DBP具有优异的长期稳定性,这就为实际应用中奠定了理论基础,达到节约成本的目的[25]。
2.6 固定化混合菌降解模拟人工污水的DBP
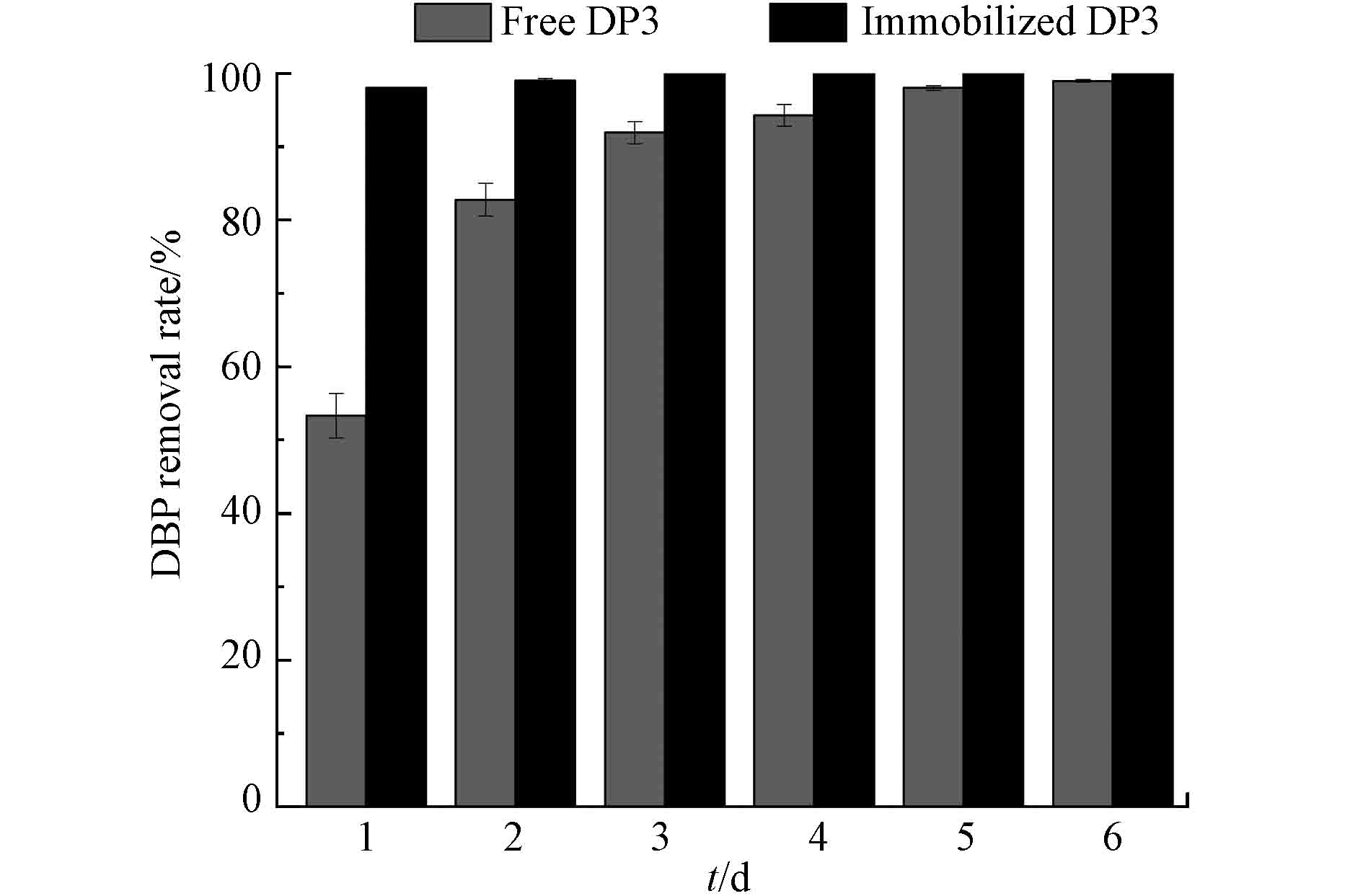
为验证固定化混合菌在实际生产中的降解能力,将固定化混合菌DP3加入10 mg·L−1 DBP的模拟人工污水中,以游离态混合菌DP3作为对照,由图7结果显示,在1 d时,游离态DP3对DBP的降解率为53.33%,固定化DP3为98.03%,降解效率显著提升,2 d后,固定化DP3达到99.98%,模拟人工污水中的DBP几乎可以完全降解,结果表明,固定化混合菌DP3表现出良好的降解能力,具有显著的应用价值。
3. 结论(Conclusion)
(1)采用正交试验确定固定化混合菌DP3的最佳制备条件为:聚乙烯醇(PVA)质量分数10%,海藻酸钠(SA)质量分数2%,活性炭(AC)质量分数3%,CaCl2质量分数1%。与游离态混合菌的降解效果相比,该条件下所制备的固定化混合菌DP3,1 d时对DBP的降解效果可达到98.84%,降解率提升35.11%。
(2)考察了不同环境条件(pH值、NaCl浓度、底物浓度)对固定化与游离态混合菌DP3降解DBP的影响,在pH4—10、NaCl浓度在5—100 g·L−1、底物浓度在10-200 mg·L−1时,对DBP的降解率均在90%以上,固定化混合菌DP3的降解率显著优于游离态混合菌。此外,固定化混合菌DP3在模拟人工污水中1 d时对DBP的降解率可达98.03%,
(3)固定化混合菌DP3对底物降解符合一阶动力学方程,相比游离态而言,降解同等浓度的底物,固定化DP3的半衰期缩短,降解速度明显增加,对底物DBP的耐受性增强。同时,固定化混合菌DP3重复对DBP进行降解20次,降解效果仍可达到99.95%,且无破碎现象。SEM扫描结果表明固定化混合菌DP3以网状菌落交织被复合材料包埋吸附在凝胶球的内部。进一步证实并解释了固定化混合菌具有较高DBP降解效率的原因。
-
表 1 不同添加物对磷、重金属形态以及产率的影响
Table 1. Effects of different additives on phosphorus and heavy metal speciation and yield
共热解添加物Co-pyrolysis additives 污泥/生物质Sludge/biomass 热解温度/℃Pyrolysis temperature 升温速率/(℃·min−1)Heating rate 热解时长/hSoaking time H/C O/C pH 产率/%Yield 磷、重金属存在形态Forms of phosphorus and heavy metals 比表面积/(m2·g−1)Specific surface area 参考文献Reference 生物质 食物残渣 3:1 550 10 1 0.06 0.41 8.70 65.70 — 18.95 [30] 2:2 0.05 0.56 8.60 69.50 18.74 1:3 0.08 1.00 8.70 73.10 21.99 木屑 9:1 500 — 2 0.21 0.30 9.30 60.10 PbAl2O4、CdAl2O4 — [31] 7:3 0.09 0.09 9.20 50.70 — 5:5 0.08 0.03 9.10 44.10 — 棉花秸秆 9:1 650 — 2 0.86 — 9.40 57.50 — 23.75 [32] 7:3 0.69 — 9.30 51.00 25.50 5:5 0.60 — 9.20 45.00 31.25 3:7 0.55 — 9.10 38.00 31.75 1:9 0.48 — 9.00 32.50 33.75 碱土金属 CaO Ca/P=1.41 700 10 2 — — — — Ca5(PO4)3OH — [33] Ca/P=1.67 Ca/P=1.91 CaO/Fe2O3 Fe2O3/CaO=4:1 450 — — — — — — Ca(AsO2)2 — [34] 650 — 850 8.97 磷酸盐 K3PO4 1:5 500 10 3 0.11 — 11.10 49.70 KMgPO4、K4P2O7、KCaPO4 — [36] 塑料 聚氯乙烯 19:1 400 10 2 0.88 0.53 4.00 70.70 金属氯化物 — [37] 3:1 0.73 0.37 2.90 62.00 1:3 0.99 0.22 2.90 36.40 载金属聚氯乙烯 19:1 0.90 0.61 7.00 72.40 — 3:1 1.84 0.84 7.20 73.30 1:3 2.76 0.91 10.90 73.80 表 2 热解温度对污泥基生物炭孔隙结构的影响
Table 2. Effect of pyrolysis temperature on the pore structure of sludge-based biochar
热解物质Pyrolysis material 热解温度/℃Pyrolysis temperature 升温速率/(℃·min−1)Heating rate 热解时长/hSoaking time pH 孔隙结构Pore structure 参考文献Reference 污泥 700 25 5 — 平均孔径 6.61 nm比表面积 54.05 m2·g−1 [44] 污泥 500 25 5 — 平均孔径 9.28 nm比表面积 31.81 m2·g−1 污泥/柳木=8:2 700 10 3 12.5 比表面积 99.0 m2·g−1 [45] 污泥/柳木=6:4 700 10 3 12.5 比表面积 104.1 m2·g−1 污泥/棉花秸秆=1:9 650 — 2 9 平均孔径为3—4 nm比表面 ~33 m2·g−1总孔体积 ~0.071 m3·g−1 [48] 污泥/棉花秸秆=3:7 650 — 2 9 平均孔径为3—4 nm比表面 ~33 m2·g−1总孔体积 ~0.065 m3·g−1 -
[1] 丁洪, 余居华, 郑祥洲, 等. 中国城市污泥应用对作物产量、品质和土壤质量的影响[J]. 生态环境学报, 2021, 30(9): 1933-1942. DING H, YU J H, ZHENG X Z, et al. Review on effect of municipal sewage sludge application on yield and quality of crops and soil quality in China[J]. Ecology and Environmental Sciences, 2021, 30(9): 1933-1942 (in Chinese).
[2] 中华人民共和国住房和城乡建设部. 2022年城乡建设统计年鉴[EB/OL]. [2023-11-16]. [3] FANG L, WANG Q M, LI J S, et al. Feasibility of wet-extraction of phosphorus from incinerated sewage sludge ash (ISSA) for phosphate fertilizer production: A critical review[J]. Critical Reviews in Environmental Science and Technology, 2021, 51(9): 939-971. doi: 10.1080/10643389.2020.1740545 [4] CHU X, NI Y, WANG X, et al. A win-win situation for environment and economy: Analysis of maximizing benefits in municipal sludge treatment plants[J]. Journal of Cleaner Production, 2023, 419: 138271. doi: 10.1016/j.jclepro.2023.138271 [5] 肖懿, 王理明, 李东阳, 等. 市政污泥热解特性及含碳官能团演化过程分析[J]. 环境工程学报, 2023, 17(5): 1589-1598. doi: 10.12030/j.cjee.202211170 XIAO Y, WANG L M, LI D Y, et al. Pyrolysis characteristics of municipal sludge and transformation of carbon-containing functional groups during pyrolysis process[J]. Chinese Journal of Environmental Engineering, 2023, 17(5): 1589-1598 (in Chinese). doi: 10.12030/j.cjee.202211170
[6] HU A B, ZHENG Y L, WANG Z, et al. Tracking the transformation pathway of dissolved organic matters (DOMs) in biochars under sludge pyrolysis via reactomics and molecular network analysis[J]. Chemosphere, 2023, 342: 140149. doi: 10.1016/j.chemosphere.2023.140149 [7] 张吉琛, 刘婷然, 董志强, 等. 污泥生物炭的催化机理及应用研究进展[J]. 环境化学, 2023, 42(6): 2018-2031. doi: 10.7524/j.issn.0254-6108.2022120203 ZHANG J C, LIU T R, DONG Z Q, et al. Mechanism and application for removal of contaminants by sludge-derived biochar catalyst: A review[J]. Environmental Chemistry, 2023, 42(6): 2018-2031 (in Chinese). doi: 10.7524/j.issn.0254-6108.2022120203
[8] FANG L, YAN F, CHEN J J, et al. Novel recovered compound phosphate fertilizer produced from sewage sludge and its incinerated ash[J]. ACS Sustainable Chemistry & Engineering, 2020, 8(17): 6611-6621. [9] ZHANG W Q, HE Y H, XING X X, et al. In-depth insight into the effects of intrinsic calcium compounds on the pyrolysis of hazardous petrochemical sludge[J]. Journal of Hazardous Materials, 2023, 455: 131593. doi: 10.1016/j.jhazmat.2023.131593 [10] LI J, PAN L J, LI Z W, et al. Unveiling the migration of Cr and Cd to biochar from pyrolysis of manure and sludge using machine learning[J]. Science of the Total Environment, 2023, 885: 163895. doi: 10.1016/j.scitotenv.2023.163895 [11] FANG L, LI J S, DONATELLO S, et al. Recovery of phosphorus from incinerated sewage sludge ash by combined two-step extraction and selective precipitation[J]. Chemical Engineering Journal, 2018, 348: 74-83. [12] 张洁, 张少逸, 梁学峰, 等. 污泥热解生物炭中重金属化学形态分布的影响因素研究进展[J]. 环境化学, 2022, 41(10): 3254-3266. doi: 10.7524/j.issn.0254-6108.2021070402 ZHANG J, ZHANG S Y, LIANG X F, et al. Research progress on influence factors on heavy metals chemical speciation distribution in sludge pyrolysis biochar[J]. Environmental Chemistry, 2022, 41(10): 3254-3266 (in Chinese). doi: 10.7524/j.issn.0254-6108.2021070402
[13] FANG L, LI J S, DONATELLO S, et al. Use of Mg/Ca modified biochars to take up phosphorus from acid-extract of incinerated sewage sludge ash (ISSA) for fertilizer application[J]. Journal of Cleaner Production, 2020, 244: 118853. doi: 10.1016/j.jclepro.2019.118853 [14] MA C W, ZHANG F X, HU J H, et al. Co-pyrolysis of sewage sludge and waste tobacco stem: Gas products analysis, pyrolysis kinetics, artificial neural network modeling, and synergistic effects[J]. Bioresource Technology, 2023, 389: 129816. doi: 10.1016/j.biortech.2023.129816 [15] 卢欢亮, 叶向东, 汪永红, 等. 热解温度对污泥生物炭的表面特性及重金属安全性的影响[J]. 环境工程学报, 2015, 9(3): 1433-1439. doi: 10.12030/j.cjee.20150373 LU H L, YE X D, WANG Y H, et al. Effects of pyrolysis temperature on surface properties and heavy metal safety of sludge-derived biochar[J]. Chinese Journal of Environmental Engineering, 2015, 9(3): 1433-1439 (in Chinese). doi: 10.12030/j.cjee.20150373
[16] 赵佳琪, 黄亚继, 李志远, 等. 污泥和聚氯乙烯共热解三相产物特性[J]. 化工进展, 2023, 42(4): 2122-2129. ZHAO J Q, HUANG Y J, LI Z Y, et al. Characteristics of three-phase products from co-pyrolysis of sewage sludge and PVC[J]. Chemical Industry and Engineering Progress, 2023, 42(4): 2122-2129 (in Chinese).
[17] 王玉, 余广炜, 汪刚, 等. 污泥与不同添加剂共热解对重金属的影响[J]. 环境科学与技术, 2022, 45(3): 163-170. WANG Y, YU G W, WANG G, et al. Effects of co-pyrolysis of sludge and different additives on heavy metals in biochar[J]. Environmental Science & Technology, 2022, 45(3): 163-170 (in Chinese).
[18] 郭江山, 顾卫华, 白建峰, 等. 污泥与磷酸二氢钙共热解对残渣特性及Cr稳定性的影响[J]. 环境工程, 2022, 40(3): 45-50,88. GUO J S, GU W H, BAI J F, et al. Effect of co-pyrolysis of sewage sludge and ca(h2po4)2 on residue characteristic and chromium stability[J]. Environmental Engineering, 2022, 40(3): 45-50,88 (in Chinese).
[19] HUANG C, MOHAMED B A, LI L Y. Comparative life-cycle energy and environmental analysis of sewage sludge and biomass co-pyrolysis for biofuel and biochar production[J]. Chemical Engineering Journal , 2023, 457: 141284. [20] MENG J T, WANG J, YANG F L, et al. Study on the multiple roles of CaO on nitrogen evolution mechanism of protein inside sewage sludge pyrolysis[J]. Chemical Engineering Journal, 2023, 458: 141039. doi: 10.1016/j.cej.2022.141039 [21] 李志远, 黄亚继, 赵佳琪, 等. 污泥与聚氯乙烯共热解重金属特性[J]. 化工进展, 2023, 42(9): 4947-4956. LI Z Y, HUANG Y J, ZHAO J Q, et al. Characterization of heavy metals during co-pyrolysis of sludge with PVC[J]. Chemical Industry and Engineering Progress, 2023, 42(9): 4947-4956 (in Chinese).
[22] LING C C Y, LI S F Y. Synergistic interactions between sewage sludge, polypropylene, and high-density polyethylene during co-pyrolysis: An investigation based on iso-conversional model-free methods and master plot analysis[J]. Journal of Hazardous Materials, 2023, 455: 131600. doi: 10.1016/j.jhazmat.2023.131600 [23] 李娜, 张惠民, 孟记朋, 等. 污泥与不同生物质共热解制备生物炭及生物炭的土地应用[J]. 可再生能源, 2018, 36(10): 1423-1430. doi: 10.3969/j.issn.1671-5292.2018.10.001 LI N, ZHANG H M, MENG J P, et al. Preparation of biochar from sewage sludge with different biomass by co-pyrolysis and its land application[J]. Renewable Energy Resources, 2018, 36(10): 1423-1430 (in Chinese). doi: 10.3969/j.issn.1671-5292.2018.10.001
[24] 赵学强, 潘贤章, 马海艺, 等. 中国酸性土壤利用的科学问题与策略[J]. 土壤学报, 2023, 60(5): 1248-1263. ZHAO X Q, PAN X Z, MA H Y, et al. Scientific issues and strategies of acid soil use in China[J]. Acta Pedologica Sinica, 2023, 60(5): 1248-1263 (in Chinese).
[25] 葛锋, 张转霞, 扶恒, 等. 我国有机污染场地现状分析及展望[J]. 土壤, 2021, 53(6): 1132-1141. GE F, ZHANG Z X, FU H, et al. Distribution of organic contaminated sites in China: Statu quo and prospect[J]. Soils, 2021, 53(6): 1132-1141 (in Chinese).
[26] 苏加强, 汪淼, 曲自超, 等. 污泥/凹凸棒石共热解生物炭对土壤重金属的钝化效果研究[J]. 环境科学与管理, 2023, 48(9): 88-93. SU J Q, WANG M, QU Z C, et al. Stabilization efficiency of biochar prepared by co-pyrosis with sludge and attapulgite on heavy metals in soils[J]. Environmental Science and Management, 2023, 48(9): 88-93 (in Chinese).
[27] FANG L, LI J S, GUO M Z, et al. Phosphorus recovery and leaching of trace elements from incinerated sewage sludge ash (ISSA)[J]. Chemosphere, 2018, 193: 278-287. doi: 10.1016/j.chemosphere.2017.11.023 [28] 王旭东, 任雪冰, 汤舒, 等. 污泥生物炭在土壤改良中的应用研究[J]. 中国农业科技导报, 2023, 25(6): 165-173. WANG X D, REN X B, TANG S, et al. Application of sludge biochar in soil improvement[J]. Journal of Agricultural Science and Technology, 2023, 25(6): 165-173 (in Chinese).
[29] 曹秀芹, 刘丰, 柴莲莲, 等. 污泥生物炭制备与其对土壤环境影响的研究进展[J]. 环境工程, 2022, 40(3): 203-211. CAO X Q, LIU F, CHAI L L, et al. Research progress on preparation of sludge based biochar and its effect on soil environment[J]. Environmental Engineering, 2022, 40(3): 203-211 (in Chinese).
[30] WANG X D, CHANG V W C, LI Z W, et al. Co-pyrolysis of sewage sludge and food waste digestate to synergistically improve biochar characteristics and heavy metals immobilization[J]. Waste Management, 2022, 141: 231-239. doi: 10.1016/j.wasman.2022.02.001 [31] YANG Y Q, CUI M H, REN Y G, et al. Towards understanding the mechanism of heavy metals immobilization in biochar derived from co-pyrolysis of sawdust and sewage sludge[J]. Bulletin of Environmental Contamination and Toxicology, 2020, 104(4): 489-496. doi: 10.1007/s00128-020-02801-4 [32] WANG Z P, SHU X Q, ZHU H N, et al. Characteristics of biochars prepared by co-pyrolysis of sewage sludge and cotton stalk intended for use as soil amendments[J]. Environmental Technology, 2020, 41(11): 1347-1357. doi: 10.1080/09593330.2018.1534891 [33] TANG S Q, LIANG J M, XU X M, et al. Targeting phosphorus transformation to hydroxyapatite through sewage sludge pyrolysis boosted by quicklime toward phosphorus fertilizer alternative with toxic metals compromised[J]. Renewable and Sustainable Energy Reviews, 2023, 183: 113474. doi: 10.1016/j.rser.2023.113474 [34] HAN H D, HU S, LU C F, et al. Inhibitory effects of CaO/Fe2O3 on arsenic emission during sewage sludge pyrolysis[J]. Bioresource Technology, 2016, 218: 134-139. doi: 10.1016/j.biortech.2016.06.075 [35] 田天. 磷酸盐共热解污泥基生物炭的理化性质研究[D]. 北京: 中国地质大学(北京), 2021. TIAN T. Study on the Physicochemical Properties of Phosphate Copyrolyzed Sewage Sludge-based Biochar[D]. Beijing: China University of Geosciences, 2021 (in Chinese).
[36] HUANG H J, YANG T, LAI F Y, et al. Co-pyrolysis of sewage sludge and sawdust/rice straw for the production of biochar[J]. Journal of Analytical and Applied Pyrolysis, 2017, 125: 61-68. doi: 10.1016/j.jaap.2017.04.018 [37] LI W J, MENG J, ZHANG Y L, et al. Co-pyrolysis of sewage sludge and metal-free/metal-loaded polyvinyl chloride (PVC) microplastics improved biochar properties and reduced environmental risk of heavy metals[J]. Environmental Pollution, 2022, 302: 119092. doi: 10.1016/j.envpol.2022.119092 [38] JINDAROM C, MEEYOO V, RIRKSOMBOON T, et al. Thermochemical decomposition of sewage sludge in CO2 and N2 atmosphere[J]. Chemosphere, 2007, 67(8): 1477-1484. doi: 10.1016/j.chemosphere.2006.12.066 [39] 蔡旭, 黄群星, 王飞, 等. 污泥在CO2气氛下热解CO与CH4的生成特性[J]. 环境工程学报, 2016, 10(7): 3779-3786. CAI X, HUANG Q X, WANG F, et al. CO and CH4 emission characteristics during sewage sludge pyrolysis in CO2 atmosphere[J]. Chinese Journal of Environmental Engineering, 2016, 10(7): 3779-3786 (in Chinese).
[40] HUANG L M, LIU J Y, HE Y, et al. Thermodynamics and kinetics parameters of co-combustion between sewage sludge and water hyacinth in CO2/O2 atmosphere as biomass to solid biofuel[J]. Bioresource Technology, 2016, 218: 631-642. doi: 10.1016/j.biortech.2016.06.133 [41] 徐智, 郭朝晖, 徐锐, 等. 控氧热解过程中污染稻草生物炭的组分特性及其重金属累积特征[J]. 环境科学, 2023, 44(2): 1051-1062. XU Z, GUO Z H, XU R, et al. Component properties and heavy metal accumulation characteristics of contaminated rice straw biochar during oxygen-controlled pyrolysis[J]. Environmental Science, 2023, 44(2): 1051-1062 (in Chinese).
[42] CHEN J C, ZHANG J H, LIU J Y, et al. Co-pyrolytic mechanisms, kinetics, emissions and products of biomass and sewage sludge in N2, CO2 and mixed atmospheres[J]. Chemical Engineering Journal, 2020, 397: 125372. doi: 10.1016/j.cej.2020.125372 [43] 张琳, 姚锡文, 刘清华, 等. 热解温度和气氛对松木屑热解气化特性的影响研究[J]. 能源与节能, 2022(5): 24-26,49. ZHANG L, YAO X W, LIU Q H, et al. Effects of pyrolysis temperature and atmosphere on pyrolysis and gasification characteristics of pine sawdust[J]. Energy and Energy Conservation, 2022(5): 24-26,49 (in Chinese).
[44] ZIELIŃSKA A, OLESZCZUK P. Attenuation of phenanthrene and pyrene adsorption by sewage sludge-derived biochar in biochar-amended soils[J]. Environmental Science and Pollution Research International, 2016, 23(21): 21822-21832. doi: 10.1007/s11356-016-7382-x [45] KOŃCZAK M, GAO Y Z, OLESZCZUK P. Carbon dioxide as a carrier gas and biomass addition decrease the total and bioavailable polycyclic aromatic hydrocarbons in biochar produced from sewage sludge[J]. Chemosphere, 2019, 228: 26-34. doi: 10.1016/j.chemosphere.2019.04.029 [46] ZHU X F, ZHAO L, FU F Y, et al. Pyrolysis of pre-dried dewatered sewage sludge under different heating rates: Characteristics and kinetics study[J]. Fuel, 2019, 255: 115591. doi: 10.1016/j.fuel.2019.05.174 [47] WANG X H, JIA J C. Effect of heating rate on the municipal sewage sludge pyrolysis character[J]. Energy Procedia, 2012, 14: 1648-1652. doi: 10.1016/j.egypro.2011.12.1146 [48] WANG Z P, XIE L K, LIU K, et al. Co-pyrolysis of sewage sludge and cotton stalks[J]. Waste Management, 2019, 89: 430-438. doi: 10.1016/j.wasman.2019.04.033 [49] QIAN T T, JIANG H. Migration of phosphorus in sewage sludge during different thermal treatment processes[J]. ACS Sustainable Chemistry & Engineering, 2014, 2(6): 1411-1419. [50] WESTERHOFF P, LEE S, YANG Y, et al. Characterization, recovery opportunities, and valuation of metals in municipal sludges from U. S. wastewater treatment plants nationwide[J]. Environmental Science & Technology, 2015, 49(16): 9479-9488. [51] 钱婷婷. 磷在固体废物热处理过程中的迁移转化及再利用[D]. 合肥: 中国科学技术大学, 2014. QIAN T T. Transformation Behavior of Phosphorus during the Thermal Treatment of Solid Wastes and Its Utilization[D]. Hefei: University of Science and Technology of China, 2014 (in Chinese).
[52] SUN D Q, HALE L, KAR G, et al. Phosphorus recovery and reuse by pyrolysis: Applications for agriculture and environment[J]. Chemosphere, 2018, 194: 682-691. doi: 10.1016/j.chemosphere.2017.12.035 [53] HUANG R X, TANG Y Z. Speciation dynamics of phosphorus during (hydro)thermal treatments of sewage sludge[J]. Environmental Science & Technology, 2015, 49(24): 14466-14474. [54] CHEN J J, TANG S Q, YAN F, et al. Efficient recovery of phosphorus in sewage sludge through hydroxylapatite enhancement formation aided by calcium-based additives[J]. Water Research, 2020, 171: 115450. doi: 10.1016/j.watres.2019.115450 [55] CHEN J J, AIHEMAITI A, XIA Y, et al. The effect of soil amendment derived from P-enhanced sludge pyrochar on ryegrass growth and soil microbial diversity[J]. Science of the Total Environment, 2022, 813: 152526. doi: 10.1016/j.scitotenv.2021.152526 [56] LI J S, LI Y L, LIU F F, et al. Pyrolysis of sewage sludge to biochar: Transformation mechanism of phosphorus[J]. Journal of Analytical and Applied Pyrolysis, 2023, 173: 106065. doi: 10.1016/j.jaap.2023.106065 [57] FANG Z Q, ZHUANG X Z, ZHANG X H, et al. Influence of paraments on the transformation behaviors and directional adjustment strategies of phosphorus forms during different thermochemical treatments of sludge[J]. Fuel, 2023, 333: 126544. doi: 10.1016/j.fuel.2022.126544 [58] 孟详东, 黄群星, 严建华, 等. 磷在污泥热解过程中的迁移转化[J]. 化工学报, 2018, 69(7): 3208-3215. MENG X D, HUANG Q X, YAN J H, et al. Migration and transformation of phosphorus during pyrolysis process of sewage sludge[J]. CIESC Journal, 2018, 69(7): 3208-3215 (in Chinese).
[59] 施川, 张盼月, 郭建斌, 等. 污泥生物炭的磷吸附特性[J]. 环境工程学报, 2016, 10(12): 7202-7208. SHI C, ZHANG P Y, GUO J B, et al. Phosphorus adsorption performance onto sewage sludge biochar[J]. Chinese Journal of Environmental Engineering, 2016, 10(12): 7202-7208 (in Chinese).
[60] LI D N, SHAN R, JIANG L X, et al. A review on the migration and transformation of heavy metals in the process of sludge pyrolysis[J]. Resources, Conservation and Recycling, 2022, 185: 106452. doi: 10.1016/j.resconrec.2022.106452 [61] 刘菲菲, 李京书, 李彦龙, 等. 污泥微波热解过程中磷和重金属共富集特性研究[C]//中国环境科学学会2022年科学技术年会--环境工程技术创新与应用分会场论文集(四). 沈阳航空航天大学, 2022: 6. LIU F F, LI J S, LI Y L, et al. Study on the co-enrichment characteristics of phosphorus and heavy metals in the process of sludge microwave pyrolysis [C]//2022 Annual Meeting of Science and Technology of Chinese Society of Environmental Sciences-Environmental Engineering Technology Innovation and Application Branch (4). Shenyang Aerospace University, 2022: 6(in Chinese).
[62] XU G R, ZOU J L, LI G B. Stabilization/solidification of heavy metals in sludge ceramsite and leachability affected by oxide substances[J]. Environmental Science & Technology, 2009, 43(15): 5902-5907. [63] 张进, 刁韩杰, 王敏艳, 等. 稻壳与污泥共热解对污泥炭特性及其重金属生态风险的影响[J]. 环境科学学报, 2019, 39(4): 1250-1256. ZHANG J, DIAO H J, WANG M Y, et al. Effects of rice husk and sewage sludge co-pyrolysis on characteristics of the sludge biochar and its ecological risk of heavy metals[J]. Acta Scientiae Circumstantiae, 2019, 39(4): 1250-1256 (in Chinese).
[64] 汪刚, 余广炜, 谢胜禹, 等. 添加不同塑料与污泥混合热解对生物炭中重金属的影响[J]. 燃料化学学报, 2019, 47(5): 611-620. WANG G, YU G W, XIE S Y, et al. Effect of co-pyrolysis of different plastics with sewage sludge on heavy metals in the biochar[J]. Journal of Fuel Chemistry and Technology, 2019, 47(5): 611-620 (in Chinese).
[65] LONGENDYKE G K, KATEL S, WANG Y X. PFAS fate and destruction mechanisms during thermal treatment: A comprehensive review[J]. Environmental Science. Processes & Impacts, 2022, 24(2): 196-208. [66] MOŠKO J, POHOŘELÝ M, CAJTHAML T, et al. Effect of pyrolysis temperature on removal of organic pollutants present in anaerobically stabilized sewage sludge[J]. Chemosphere, 2021, 265: 129082. doi: 10.1016/j.chemosphere.2020.129082 [67] ALIPOUR M, ASADI H, CHEN C R, et al. Fate of organic pollutants in sewage sludge during thermal treatments: Elimination of PCBs, PAHs, and PPCPs[J]. Fuel, 2022, 319: 123864. doi: 10.1016/j.fuel.2022.123864 [68] BROWN R A, KERCHER A K, NGUYEN T H, et al. Production and characterization of synthetic wood chars for use as surrogates for natural sorbents[J]. Organic Geochemistry, 2005, 37(3): 321-333. [69] BUSS W. Pyrolysis solves the issue of organic contaminants in sewage sludge while retaining carbon—Making the case for sewage sludge treatment via pyrolysis[J]. ACS Sustainable Chemistry & Engineering, 2021, 9(30): 10048-10053. [70] JONES S, BARDOS R P, KIDD P S, et al. Biochar and compost amendments enhance copper immobilisation and support plant growth in contaminated soils[J]. Journal of Environmental Management, 2016, 171: 101-112. [71] SHEIKH L, YOUNIS U, SHAHZAD A S, et al. Evaluating the effects of cadmium under saline conditions on leafy vegetables by using acidified biochar[J]. Pakistan Journal of Botany, 2023, 55: 33-39. [72] DENG Y, HUANG Q, GU W H, et al. Application of sludge-based biochar generated by pyrolysis: A mini review[J]. Energy Sources, Part A: Recovery, Utilization, and Environmental Effects, 2020: 1-10. [73] 卢再亮, 李九玉, 姜军, 等. 生活污水污泥制备的生物质炭对红壤酸度的改良效果及其环境风险[J]. 环境科学, 2012, 33(10): 3585-3591. LU Z L, LI J Y, JIANG J, et al. Amelioration effects of wastewater sludge biochars on red soil acidity and their environmental risk[J]. Environmental Science, 2012, 33(10): 3585-3591 (in Chinese).
[74] 张丛光, 尚高原, 邱凌, 等. 污泥—生物炭耦合还田技术研究进展[J]. 西北林学院学报, 2017, 32(3): 84-90. ZHANG C G, SHANG G Y, QIU L, et al. Research progress of the application technology of sludge and biochar[J]. Journal of Northwest Forestry University, 2017, 32(3): 84-90 (in Chinese).
[75] 王秋利, 韩勇. 污泥基生物炭在矿区土壤重金属污染治理中的应用[J]. 能源与环保, 2023, 45(5): 43-48. WANG Q L, HAN Y. Application of sludge-based biochar on treatment of heavy metal pollution in mining area soil[J]. China Energy and Environmental Protection, 2023, 45(5): 43-48 (in Chinese).
[76] 周佳丽, 林伟雄, 关智杰, 等. 响应曲面法优化KOH改性污泥生物炭的制备及其强化去除Pb(Ⅱ)的研究[J]. 环境科学学报, 2022, 42(8): 194-207. ZHOU J L, LIN W X, GUAN Z J, et al. Optimization of preparation of KOH-modified sludge biochar by response surface method and its enhanced Pb(Ⅱ)removal[J]. Acta Scientiae Circumstantiae, 2022, 42(8): 194-207 (in Chinese).
[77] KRAHN K M, CORNELISSEN G, CASTRO G, et al. Sewage sludge biochars as effective PFAS-sorbents[J]. Journal of Hazardous Materials, 2023, 445: 130449. doi: 10.1016/j.jhazmat.2022.130449 [78] FABREGAT-PALAU J, VIDAL M, RIGOL A. Modelling the sorption behaviour of perfluoroalkyl carboxylates and perfluoroalkane sulfonates in soils[J]. Science of the Total Environment, 2021, 801: 149343. doi: 10.1016/j.scitotenv.2021.149343 [79] GAGLIANO E, SGROI M, FALCIGLIA P P, et al. Removal of poly- and perfluoroalkyl substances (PFAS) from water by adsorption: Role of PFAS chain length, effect of organic matter and challenges in adsorbent regeneration[J]. Water Research, 2020, 171: 115381. doi: 10.1016/j.watres.2019.115381 [80] DENG S B, YU Q, HUANG J, et al. Removal of perfluorooctane sulfonate from wastewater by anion exchange resins: Effects of resin properties and solution chemistry[J]. Water Research, 2010, 44(18): 5188-5195. doi: 10.1016/j.watres.2010.06.038 [81] WANG H Z, GUO W Q, LIU B H, et al. Sludge-derived biochar as efficient persulfate activators: Sulfurization-induced electronic structure modulation and disparate nonradical mechanisms[J]. Applied Catalysis B:Environmental, 2020, 279: 119361. doi: 10.1016/j.apcatb.2020.119361 [82] 李韬略, 袁雪红, 陈传胜, 等. Fe2+耦合热活化过硫酸盐降解土壤中四溴双酚A[J]. 环境化学, 2023, 42(8): 2730-2739. doi: 10.7524/j.issn.0254-6108.2022031501 LI T L, YUAN X H, CHEN C S, et al. Degradation of tetrabromobisphenol A by ferrous coupling thermally activated persulfate in soil[J]. Environmental Chemistry, 2023, 42(8): 2730-2739 (in Chinese). doi: 10.7524/j.issn.0254-6108.2022031501
[83] PREMARATHNA K S D, RAJAPAKSHA A U, SARKAR B, et al. Biochar-based engineered composites for sorptive decontamination of water: A review[J]. Chemical Engineering Journal, 2019, 372: 536-550. doi: 10.1016/j.cej.2019.04.097 [84] KANG X D, ZHANG Q Y, LIU X F, et al. The interface mechanism of sludge biochar activating persulfate to remove tetracycline: The role of the C-O-Fe bridge at the carbon surface[J]. Journal of Cleaner Production, 2023, 384: 135514. doi: 10.1016/j.jclepro.2022.135514 [85] 韩剑宏, 李艳伟, 姚卫华, 等. 玉米秸秆和污泥共热解制备的生物质炭及其对盐碱土壤理化性质的影响[J]. 水土保持通报, 2017, 37(4): 92-98,105. HAN J H, LI Y W, YAO W H, et al. Co-pyrolysis preparing biochar with corn straw and sewage sludge and its effects on saline soil improvement[J]. Bulletin of Soil and Water Conservation, 2017, 37(4): 92-98,105 (in Chinese).
[86] TANG J Y, ZHANG L H, ZHANG J C, et al. Physicochemical features, metal availability and enzyme activity in heavy metal-polluted soil remediated by biochar and compost[J]. Science of the Total Environment, 2020, 701: 134751. doi: 10.1016/j.scitotenv.2019.134751 [87] FERNÁNDEZ-LUQUEÑO F, VALENZUELA-ENCINAS C, MARSCH R, et al. Microbial communities to mitigate contamination of PAHs in soil: Possibilities and challenges: A review[J]. Environmental Science and Pollution Research International, 2011, 18(1): 12-30. doi: 10.1007/s11356-010-0371-6 [88] BARAN S, BIELIŃSKA J E, OLESZCZUK P. Enzymatic activity in an airfield soil polluted with polycyclic aromatic hydrocarbons[J]. Geoderma, 2004, 118(3/4): 221-232. [89] 张晶, 张惠文, 丛峰, 等. 长期灌溉含多环芳烃污水对稻田土壤酶活性与微生物种群数量的影响[J]. 生态学杂志, 2007, 26(8): 1193-1198. ZHANG J, ZHANG H W, CONG F, et al. Effects of long-term PAHs-containing wastewater irrigation on lowland rice soil enzyme activities and microbial populations[J]. Chinese Journal of Ecology, 2007, 26(8): 1193-1198 (in Chinese).
[90] ALLISON S D. Soil minerals and humic acids alter enzyme stability: Implications for ecosystem processes[J]. Biogeochemistry, 2006, 81(3): 361-373. doi: 10.1007/s10533-006-9046-2 [91] TAVOLARO P, TAVOLARO A, MARTINO G. Influence of zeolite PZC and pH on the immobilization of cytochrome c: A preliminary study regarding the preparation of new biomaterials[J]. Colloids and Surfaces. B, Biointerfaces, 2009, 70(1): 98-107. doi: 10.1016/j.colsurfb.2008.12.019 [92] YUAN Z H, HUANG Q J, WANG Z Q, et al. Medium-low temperature conditions induce the formation of environmentally persistent free radicals in microplastics with conjugated aromatic-ring structures during sewage sludge pyrolysis[J]. Environmental Science & Technology, 2022, 56(22): 16209-16220. [93] LIU Y, DAI Q Y, JIN X Q, et al. Negative impacts of biochars on urease activity: High pH, heavy metals, polycyclic aromatic hydrocarbons, or free radicals?[J]. Environmental Science & Technology, 2018, 52(21): 12740-12747. [94] PARIYAR P, KUMARI K, JAIN M K, et al. Evaluation of change in biochar properties derived from different feedstock and pyrolysis temperature for environmental and agricultural application[J]. Science of the Total Environment, 2020, 713: 136433. doi: 10.1016/j.scitotenv.2019.136433 [95] CHEN J F, DING L S, WANG P Y, et al. The estimation of the higher heating value of biochar by data-driven modeling[J]. Journal of Renewable Materials, 2022, 10(6): 1555-1574. doi: 10.32604/jrm.2022.018625 [96] GUSIATIN Z M, KURKOWSKI R, BRYM S, et al. Properties of biochars from conventional and alternative feedstocks and their suitability for metal immobilization in industrial soil[J]. Environmental Science and Pollution Research International, 2016, 23(21): 21249-21261. doi: 10.1007/s11356-016-7335-4 [97] HU Y H, THOMSEN T P, FENTON O, et al. Effects of dairy processing sludge and derived biochar on greenhouse gas emissions from Danish and Irish soils[J]. Environmental Research, 2023, 216(Pt 2): 114543. [98] XU X Y, KAN Y, ZHAO L, et al. Chemical transformation of CO2 during its capture by waste biomass derived biochars[J]. Environmental Pollution, 2016, 213: 533-540. doi: 10.1016/j.envpol.2016.03.013 [99] ZHAO L, SUN Z F, PAN X W, et al. Sewage sludge derived biochar for environmental improvement: Advances, challenges, and solutions[J]. Water Research X, 2023, 18: 100167. doi: 10.1016/j.wroa.2023.100167 [100] SCHWANDER T, SCHADA von BORZYSKOWSKI L, BURGENER S, et al. A synthetic pathway for the fixation of carbon dioxide in vitro[J]. Science, 2016, 354(6314): 900-904. doi: 10.1126/science.aah5237 [101] GONG F Y, LI Y. Fixing carbon, unnaturally[J]. Science, 2016, 354(6314): 830-831. doi: 10.1126/science.aal1559 [102] 程功, 刘廷玺, 李东方, 等. 生物炭和秸秆还田对干旱区玉米农田土壤温室气体通量的影响[J]. 中国生态农业学报(中英文), 2019, 27(7): 1004-1014. CHENG G, LIU T X, LI D F, et al. Effects of biochar and straw on greenhouse gas fluxes of corn fields in arid regions[J]. Chinese Journal of Eco-Agriculture, 2019, 27(7): 1004-1014 (in Chinese).
[103] KAZEMI SHARIAT PANAHI H, DEHHAGHI M, OK Y S, et al. A comprehensive review of engineered biochar: Production, characteristics, and environmental applications[J]. Journal of Cleaner Production, 2020, 270: 122462. doi: 10.1016/j.jclepro.2020.122462 [104] KUZYAKOV Y, BOGOMOLOVA I, GLASER B. Biochar stability in soil: Decomposition during eight years and transformation as assessed by compound-specific 14C analysis[J]. Soil Biology and Biochemistry, 2014, 70: 229-236. doi: 10.1016/j.soilbio.2013.12.021 -




 DownLoad:
DownLoad: