-
地下水占全球淡水资源的22.6%,其质量会给人们的生产和生活带来极大影响[1 − 2]. 但是以石油烃、苯系物、多环芳烃等为代表的疏水性有机污染物在地下水中富集[3 − 8],不仅威胁动植物生存,更使人类的健康与发展受到影响. 因此,亟需构建绿色高效的疏水性有机污染物去除方法来修复受污染的地下水.
亲脂疏水性是制约疏水性有机污染物修复的关键因素之一. 表面活性剂可通过提高水中疏水性污染物的溶解度来增强污染含水层的修复效率[9]. 表面活性剂可分为化学、生物和类表面活性剂. 表面活性剂的浓度超过一定值时形成大量称为“胶束”的聚集体,该浓度称为临界胶束浓度(CMC). 当表面活性剂的浓度高于CMC时,分子形成胶团包裹住污染物从而实现增溶. Butler等[10]研究了表面活性剂溶液中非水相液体混合物的增溶行为,发现表面活性剂对疏水性化合物溶解度的强化作用远大于亲水性化合物. Kommalapati等[11]研究了源自Sapindusmukorossi的天然表面活性剂皂素的性能,与商用表面活性剂性能相当.
虽然表面活性剂对疏水性污染物具有一定的增溶效果,但化学表面活性剂相对生物表面活性剂对环境造成的二次污染更大. 且因生产方式不同,大多数生物和类表面活性剂产量低且成本高,无法规模化使用[12 − 13]. 例如,鼠李糖脂在生产过程中的最大产量只能达到10 g·L−1左右[14]. 因此,采用表面活性剂增溶疏水性有机污染物时,除考虑增溶效果以外,需将毒性和成本纳入评价体系,以优化最佳表面活性剂筛选方法. 此外,无机盐和助剂常通过改变表面活性剂的聚集行为和分散性能,影响表面活性剂的表面电荷和分子构象来强化表面活性剂的增溶效果. 因此,在筛选最佳表面活性剂时,考虑无机盐和助剂添加浓度对提高疏水性有机污染物的去除效率也至关重要.
本研究选取菲、氯苯、正十六烷作为多环芳烃、苯系物和石油烃等典型疏水性有机污染物的代表,以10种常见的表面活性剂为研究对象,从成本、毒性、增溶效果等方面对各表面活性剂的性能进行综合评价,并筛选适用于目标污染物的3种表面活性剂. 通过添加不同浓度的助剂和无机盐,探究其对3类表面活性剂强化各污染物增溶性能的影响. 筛选确定最优表面活性剂,为地下水中疏水性有机污染物绿色高效去除方法的构建提供思路与依据.
-
试剂:菲(95%,成都华夏化学试剂有限公司)、氯苯(AR,99%,上海阿拉丁生化科技股份有限公司)、正十六烷(AR,98%,上海易恩化学技术有限公司)、鼠李糖脂(纯度为95%,西安瑞捷生物科技有限公司)、十二烷基硫酸钠(AR,成都市科隆化学品有限公司)、十二烷基苯磺酸钠(AR,90%,成都市科隆化学品有限公司)、烷基糖苷0814(50%,山东优索化工科技有限公司)、吐温80(AR,99%,成都西亚化工股份有限公司)、曲拉通X-100(AR,99%,成都西亚化工股份有限公司)、槐糖脂(山东优索化工科技有限公司)、腐植酸(95%,北京沃凯生物科技有限公司)、皂素(98%,成都华夏化学试剂有限公司)、茶皂素 (60%,山东优索化工科技有限公司);氯化钠(AR,99.5%,成都市科隆化学品有限公司)、1,2-丙二醇(AR,99%,成都市科隆化学品有限公司)、正己烷(HPLC,98%,成都市科隆化学品有限公司)、二氯甲烷(HPLC,99.9%,成都市科隆化学品有限公司)等溶剂均为分析纯.
仪器:冷冻水浴恒温振荡器(JBXL-70,晶玻,常州普天仪器制造有限公司);台式高速离心机(L550,湘仪,湖南湘仪实验室仪器开发有限公司);电子天平(FB124,舜宇,上海舜宇恒平科学仪器有限公司);表面张力仪(BZY-1,上海衡平仪器仪表厂);气相色谱仪(GC-2010 Pro,岛津,日本);马尔文激光粒度仪(Zen3600,Malvern,英国).
-
通过使用表面张力仪对10种表面活性剂进行测定,得到各种表面活性剂的临界胶束浓度(CMC)和其它理化性质见(表1). 相对于传统的化学表面活性剂,生物表面活性剂的CMC大多远远小于化学表面活性剂,由于生物表面活性剂的价格较为昂贵,较低的CMC也有利于节约其用量,从而降低因价格昂贵带来的影响. 类表面活性剂腐植酸虽然和表面活性剂的作用机理和效果相似,但是CMC相较于其他9种常见的表面活性剂较大,增溶效果有待探究.
-
分别配制浓度为1 CMC的表面活性剂溶液,移取10 mL表面活性剂溶液于20 mL胶塞的玻璃瓶中,再在不同瓶子中分别加入稍过量的菲固体、氯苯液体和正十六烷液体,于30 ℃下以160 r·min−1转速分别振荡1、3、5、8、12、24、48 h. 平衡后,将样品取出以
4000 r·min−1离心10 min,分离未溶解的菲、氯苯、正十六烷,移取适量上清液,加入分液漏斗中,分别利用等量正己烷对菲和正十六烷进行萃取吸取上清液,用等量二氯甲烷对氯苯进行萃取,取下层液体,之后重复进行2次萃取以减小其对污染物测定的误差. 每个梯次样品设置3个平行样[15].用气相色谱仪测定溶液中的菲和氯苯以及正十六烷的浓度,气相条件分别为:
菲:进样口温度为300 ℃,载气为氦气,流速为1.2 mL·min−1,进样量1 μL,采用不分流进样模式,程序升温过程条件为:起始温度50 ℃下保持1 min,以30 ℃·min−1升至180 ℃,接着以3.5 ℃·min−1升至225 ℃,再以30 ℃·min−1升至300 ℃保持5 min,标准混合溶液的分离时间为18 min[16].
氯苯:进样口温度220 ℃;分流进样,分流比10:1;色谱柱升温程序:初始温度50 ℃保持1 min,以20 ℃·min−1升至130 ℃,再以10 ℃·min−1升至230 ℃,保持5 min[17].
正十六烷:载气为99.99%氮气,进样口温度250 ℃,分流比30:1,检测器温度300 ℃,氢气流量30 mL·min−1,空气流量300 mL·min−1,进样量1 μL. 初始160 ℃,保留1 min,以20 ℃·min−1升温至260 ℃,保留6 min[18].
-
通过对比在常态下利用表面活性剂强化对污染物的最大增溶效果与表面活性剂的价格之比,选取比值排在前3的表面活性剂进行稳定性测试. 评价系数的计算见式(1). 评价系数EC越大,则表示效果越好.
式中:EC为评价系数;S表面活性剂对污染物的增溶倍数;P为表面活性剂成本,元.
-
依据以上实验结果,分别选取评价系数最大的3种表面活性剂,在1.2节确定各自污染物对应选取的表面活性剂所达到最大增溶浓度的时间(t0)后,设置表面活性剂浓度都为1 CMC. 在这3种表面活性剂溶液中加入NaCl,使NaCl浓度分别达到0、1、10、20 mg·L−1. 到达t0时间后,将样品取出以
4000 r·min−1离心10 min,去除未溶解的污染物,移取适量上清液加入分液漏斗,按照1.3节所述方法进行萃取和测定,每组样品设置3个平行样.表面张力测定:离心结束后取部分样品,倒入玻璃培养皿中5 mm后,直接将挂片淹没在溶液中进行测试,待稳定后进行读数. 每组试验进行3次,取平均值作为最终试验结果.
-
通过在1.4部分中选取的表面活性剂,设置其浓度为1 CMC,在溶液中加入助剂1,2-丙二醇,使1,2-丙二醇分别达到0、0.1、0.5、1 mol·L−1,振荡时间t0. 按1.5节所述方法测定样品中污染物浓度和样品的表面张力.
-
10种表面活性剂对不同污染物的增溶效果见图1,显示在48 h的时间内,增溶效果随着时间的增加,不同表面活性剂对不同的污染物增溶作用呈现出显著差别.
不同时间段内对于菲的增溶效果显示(图1(a—c)),在第48 h后对菲的增溶效果最佳的3种表面活性剂分别为:茶皂素、皂素、吐温80. 吐温80在短时间内显示对菲的增溶效果出现较大增长,之后又快速趋于平稳,得到的增溶效果比茶皂素差,相比在空白状态下增溶效果提升了7.59倍. 随着时间的不断延长,茶皂素对菲的增溶效果不断增强,且更为稳定.
对氯苯具有最佳增溶效果的表面活性剂分别为:吐温80、十二烷基苯磺酸钠、十二烷基硫酸钠(图1e,f,g). 所有表面活性剂对氯苯的增溶性能在12 h内快速增大后又逐渐开始降低,主要在于氯苯具有强挥发性,被增溶的氯苯产生了挥发[19]. 吐温80相对于空白状态下最大增溶效果提升了2.73倍.
对正十六烷具有最佳增溶效果的表面活性剂分别为:鼠李糖脂、腐植酸、皂素(图1i,j,k). 5 h之内腐植酸对正十六烷的增溶效果最佳,但是随着时间的推移,增溶效果开始减弱,可能是由于腐植酸作为一种环境友好型吸附剂,氧化程度较高,极性强,芳构度小,脂肪键多,分子中具有较高含量的羧基、酚羟基和酮型羧基等活性基团,可能通过吸附的方式将水中增溶的正十六烷进行吸附,从而使得水中的正十六烷基浓度逐渐降低[20 − 21]. 鼠李糖脂对正十六烷的增溶效果最佳,相对于空白状态下增溶效果提升了13.41倍,并且到达最大增溶浓度后正十六烷浓度趋于稳定.
类表面活性剂腐植酸存在增溶性能的可能原因是其和表面活性剂有相似的能力,使得疏水性污染物可以大大提升其在水溶液中的溶解度,从而达到增溶的目的. 通过对氯苯和正十六烷的增溶结果可以看出,随时间变化两种疏水性污染物的增溶量先增大后开始减小,其主要原因是因为腐植酸中的脂肪结构促进了腐植酸对疏水性物质的吸附,通过物理吸附、分配、氢键、共价键等途径与污染物进行结合,从而固定、沉淀疏水性有机污染物,使得被增溶的氯苯和正十六烷在水中的含量减小[22 − 29]. 之所以菲浓度没有降低,可能是固体菲的粒径过大导致无法通过物理性的吸附去除.
-
本研究10种表面活性剂的毒性按照由高到低排列为:十二烷基苯磺酸钠>十二烷基硫酸钠>曲拉通X-100>吐温80>腐植酸>皂素>茶皂素>槐糖脂>鼠李糖脂[30 − 40]( 烷基糖苷0814未查到). 表面活性剂的毒性基本遵循着化学表面活性剂>生物表面活性剂,由于类表面活性剂涉及的物质范围较广,没有相对确切的毒性大小,所以以腐植酸作为类表面活性剂代表进行评价. 评价系数及相关指标见表2.
在毒性排序的基础上,通过对比表2中这10种表面活性剂的评价系数,分别筛选出对应每种污染物的3种表面活性剂,如表3所示.
-
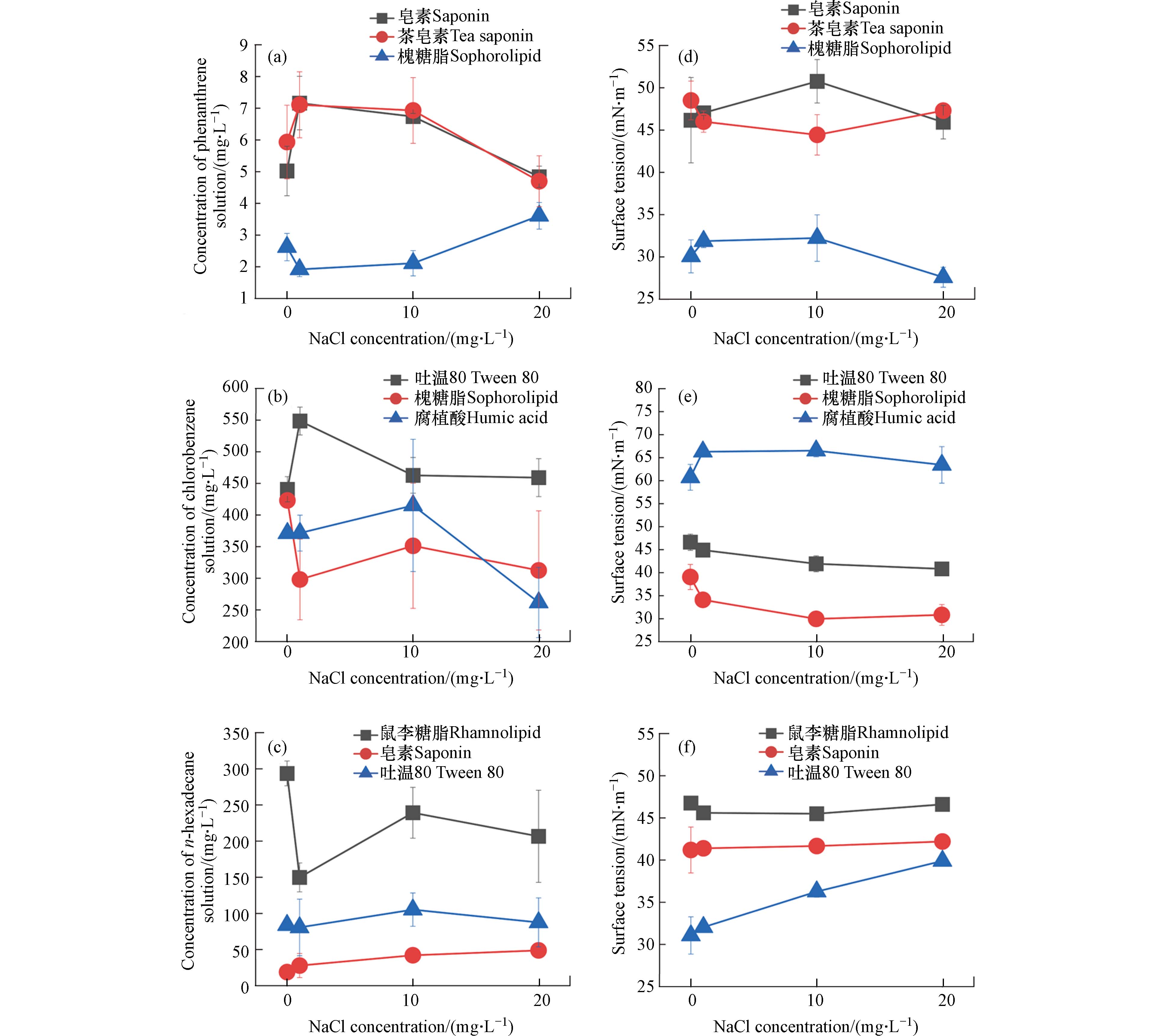
通过向表面活性剂溶液中添加不同量的NaCl,测定溶解在表面活性剂中污染物含量以及表面张力的变化. NaCl浓度对表面活性剂增溶菲的影响效果见图2(a)和图2(d),随着NaCl浓度增大,皂素和茶皂素对菲的增溶效果开始增强,而槐糖脂则产生了抑制作用. 当NaCl浓度超过1 mg·L−1时,皂素和茶皂素对菲的增溶效果出现抑制的状况. 与之相反,槐糖脂呈现促进作用. 对于溶液的表面张力,随着NaCl浓度的增大,皂素和茶皂素溶液的表面张力都远远大于槐糖脂,但对于这3种表面活性剂而言,表面张力变化趋势都较稳定.
NaCl浓度对表面活性剂增溶氯苯的影响效果见图2(b)和图2(e),显示随着NaCl浓度增大,吐温80在NaCl达到1 mg·L−1时达到最大,然后随着NaCl浓度的增大,增溶效果降低. 腐植酸先呈现促进作用,在NaCl达到10 mg·L−1之后增溶效果逐渐呈现抑制效果. 图2(e)显示溶液的表面张力并没有出现太明显变化,表示NaCl浓度对溶液稳定性影响较小.
NaCl浓度对表面活性剂增溶正十六烷的影响效果见图2(c)和图2(f),显示随着NaCl浓度的增大,鼠李糖脂对正十六烷的增溶效果呈现抑制作用,当NaCl浓度增大到1 mg·L−1时,逐渐开始出现增溶增强的效果,但整体呈现抑制作用,而皂素以及吐温80对正十六烷的增溶效果并没有随着NaCl的浓度而出现明显变化. 溶液的表面张力在添加鼠李糖脂和皂素的溶液中未出现明显变化,显示溶液较为稳定,而添加吐温80溶液的表面张力随着NaCl浓度的增大而增大.
以上结果表明无机盐的添加会造成溶液中被增溶的污染物含量变化及表面张力变动,尤其是对于离子型表面活性剂影响更为明显[41 − 42]. 无机盐离子会影响离子型表面活性剂的聚集和吸附,离子型表面活性剂的界面活性受溶液内电解质含量的影响很大,使得双电层受到压缩,从而带有相同电荷的亲水基之间的排斥作用也随之减弱,结果导致表面活性剂的吸附量出现变化. 离子型表面活性剂中加入无机盐后,带相同电荷的极性基之间的排斥作用减弱,导致CMC值发生变化[43 − 46]. 同时也会降低溶液的表面张力,使改变胶束聚集体的微观结构并增强胶束生长,引起表面活性剂的可逆相变,使得表面活性剂可能析出产生沉淀.
无机盐的加入可能会对非离子表面活性的结构产生影响,其主要通过改变溶剂的极性,影响表面活性剂的溶解性和胶束的形成,增加溶剂的离子强度. 这可能会使非离子表面活性剂的胶束更加紧密,从而增强其增溶作用. 并且无机盐的加入改变了溶液的离子环境,影响表面活性剂分子在溶液表面的排列和密度,减少表面活性剂分子在溶液表面的吸附,进而影响表面张力[47 − 48].
生物表面活性剂通常具有更复杂的结构,无机盐可能通过影响其立体构型来改变其增溶性能,并对体系本身离子强度变化产生影响,从而改变表面活性剂的分子结构和官能团的活性,进而影响其增溶能力和表面张力[49].
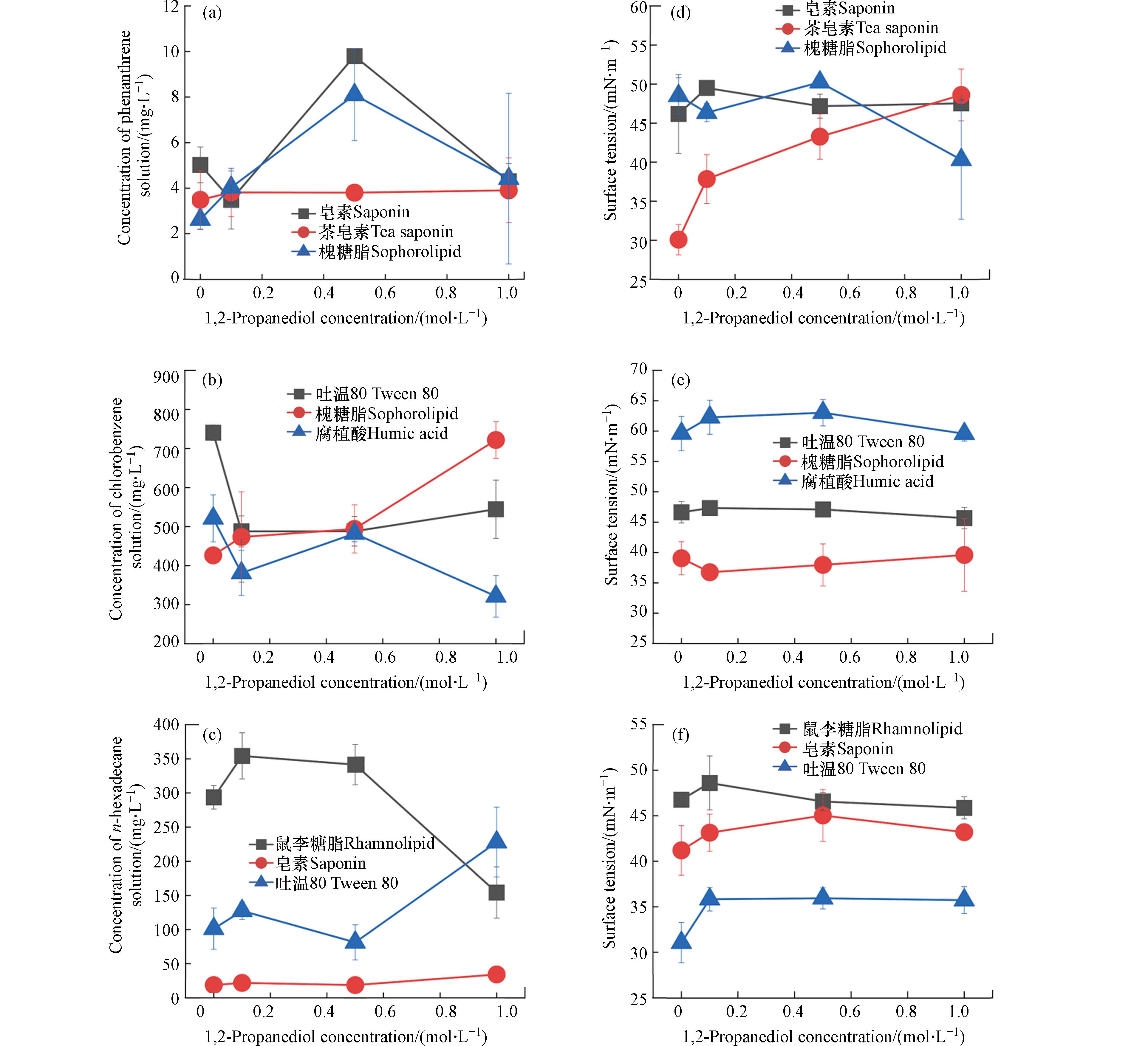
通过向表面活性剂溶液中添加不同量的1,2-丙二醇,测定溶解在表面活性剂中污染物含量以及表面张力的变化. 1,2-丙二醇浓度对表面活性剂增溶菲的影响效果见图3(a)和图3(d). 随着1,2-丙二醇浓度增大,茶皂素对菲的增溶效果并没有出现明显的变化;槐糖脂随着1,2-丙二醇浓度增大对菲的增溶效果逐渐增大,直到1,2-丙二醇浓度超过0.5 mol·L−1后开始呈现抑制作用;皂素在1,2-丙二醇浓度达到0.1 mol·L−1前呈现逐渐抑制的作用,当1,2-丙二醇浓度大于0.1 mol·L−1时,对菲的增溶效果呈现促进效果,直到1,2-丙二醇浓度超过0.5 mol·L−1后呈现抑制作用;对于溶液表面张力,随着1,2-丙二醇浓度的增大,皂素溶液的表面张力并没有出现明显的变化;槐糖脂的表面张力开始呈现较为稳定,当1,2-丙二醇浓度超过0.5 mol·L−1时,表面张力开始降低;而茶皂素溶液的表面张力随着1,2-丙二醇浓度的增大而增大.
1,2-丙二醇浓度对表面活性剂增溶氯苯的影响效果见图3(b)和图3(e). 随着1,2-丙二醇浓度的增大,对槐糖脂和吐温80呈现出促进增溶的效果,对于腐植酸则相反,呈现出抑制作用. 1,2-丙二醇浓度的变化并未明显改变表面张力.
1,2-丙二醇浓度对表面活性剂增溶正十六烷的影响效果见图3(c)和图3(f). 随着1,2-丙二醇浓度的增大,皂素对正十六烷的增溶效果并未出现明显变化;而鼠李糖脂对其的增溶效果随着1,2-丙二醇浓度增大先逐渐增大,直到1,2-丙二醇浓度超过0.5 mol·L−1后开始出现抑制;而吐温80的增溶效果随着1,2-丙二醇浓度的增大而增大. 对于溶液表面张力,鼠李糖脂和皂素溶液的表面张力并未出现明显变化,但随着1,2-丙二醇浓度的增大吐温80溶液的表面张力快速增大后保持稳定.
-
粒径分析结果表明(表4),对于菲的体系,随着1,2-丙二醇添加量的增加,粒径逐渐减小至100 nm以下,形成了微乳体系. 在氯苯体系中,添加吐温80和腐植酸也使体系趋向微乳化. 但使用槐糖脂时,粒径先减小后增大,表明低浓度的1,2-丙二醇更倾向于形成微乳体系,这主要是由于复配效应增加了污染物的溶解度. 对于正十六烷体系,鼠李糖脂和吐温80在增溶污染物时,复配作用的影响大于微乳体系的影响. 低浓度的1,2-丙二醇会形成微乳体系,从而增强增溶效果,但高浓度的助剂添加可能抑制粒径减小,更倾向于复配作用.
由于1,2-丙二醇属于醇类助剂,醇具有一定程度的亲油性质,微乳液体系可能发生相变化,增溶能力提高,使得污染物的增溶量加大,而且醇的加入在一定程度上可能会让溶液形成微乳体系,单相微乳液区域有所扩大使得体系变稳定. 但在高浓度助剂情况下可能会和表面活性剂对污染物的增溶产生拮抗作用,从而减弱增溶效果[50 − 56].
-
(1) 从增溶效果上来看,对菲增溶效果的最佳的表面活性剂为茶皂素,对氯苯增溶效果最佳为吐温80,对正十六烷增溶效果最佳为鼠李糖脂,对于空白条件下增溶效果的倍数分别提升了7.59倍、2.73倍、13.41倍.
(2) 在考虑毒性、价格等因素并计算评价系数后,对菲最适的表面活性剂为皂素,对氯苯最适合的表面活性剂为吐温80,对正十六烷最适的表面活性剂为鼠李糖脂.
(3) 利用皂素在对菲进行增溶的过程中,NaCl浓度为1 mg·L−1,1,2-丙二醇浓度为0.5 mol·L−1时为最佳,增溶效果大约提升12.82倍;利用吐温80对氯苯的增溶过程中,只添加1 mg·L−1NaCl浓度时效果最佳(+333%);利用鼠李糖脂增溶正十六烷时,只添加浓度为0.1 mol·L−1的1,2-丙二醇时效果最好,增溶效果提升15.65倍. 相对于非离子表面活性剂,盐浓度和助剂浓度的变化对离子型表面活性剂对影响更加明显.
本研究的相关成果可为表面活性剂强化地下水中疏水性有机污染物绿色高效去除方法的构建提供新思路与依据.
表面活性剂增溶典型疏水性有机污染物性能评价
Evaluation of typical hydrophobic organic pollutant solubility enhancement by surfactants
-
摘要: 水溶性低是限制疏水性有机污染物修复的主要因素之一. 表面活性剂常用于增强其水溶性,但表面活性剂筛选与综合评价仍不完善. 本文选取10种表面活性剂,综合评价了其对菲、氯苯、正十六烷的增溶性能及无机盐、助剂的影响. 结果表明,皂素对菲的增溶效果最佳,添加1 mg·L−1 NaCl或0.5 mol·L−1 1,2-丙二醇的强化效果最显著(+
1282 %). 吐温80对氯苯的增溶效果最佳,1 mg·L−1 NaCl强化吐温80对氯苯的增溶效果最强,达到了3.33倍,而1,2-丙二醇却起到了抑制作用,表明二者形成的微乳体系产生了拮抗作用. 鼠李糖脂对正十六烷具有最佳增溶性能,且0.1 mol·L−1 1,2-丙二醇强化鼠李糖脂增溶正十六烷的效果最明显,约为15.65倍,而NaCl却产生抑制作用. 通过综合评价,确定了增溶典型疏水性有机污染物的最优表面活性剂,为其绿色高效疏水性有机污染物去除方法的构建提供了理论和技术支撑.Abstract: Low water solubility is one of the main limiting factors for the remediation of hydrophobic organic pollutants. Surfactants are widely used to enhance their water solubility, yet the screening and comprehensive evaluation of proper surfactants still require further investigation. In the present study, 10 surfactants were selected, and their solubilization performance on phenanthrene, chlorobenzene, and n-hexadecane, as well as the influence of inorganic salts and additives, was comprehensively evaluated. Results showed that Saponin had the best solubilization effect on phenanthrene, and the addition of 1 mg·L−1 NaCl or 0.5 mol·L−1 1,2-propanediol had the most significant enhancing efficiency (+1282 %). Tween 80 had the optimal solubilization effect on chlorobenzene. 1 mg·L−1 NaCl increased the solubilizing efficiency of Tween 80 by approximately 3.33 times, while 1,2-propanediol had an inhibitory effect, indicating an antagonistic effect. Rhamnolipids had the best solubilization performance on n-hexadecane, and the enhancing effect of 0.1 mol·L-1 1,2-propanediol on solubilization of n-hexadecane was the greatest, increasing it by 15.65 times, while NaCl had an inhibitory effect. In conclusion, the optimal surfactants for solubilizing typical hydrophobic organic pollutants were determined, The findings provide theoretical and technical support for the development of green and efficient methods for the removal of hydrophobic organic pollutants.-
Key words:
- surfactants /
- solubilization effect /
- phenanthrene /
- chlorobenzene /
- n-hexadecane
-
地下水占全球淡水资源的22.6%,其质量会给人们的生产和生活带来极大影响[1 − 2]. 但是以石油烃、苯系物、多环芳烃等为代表的疏水性有机污染物在地下水中富集[3 − 8],不仅威胁动植物生存,更使人类的健康与发展受到影响. 因此,亟需构建绿色高效的疏水性有机污染物去除方法来修复受污染的地下水.
亲脂疏水性是制约疏水性有机污染物修复的关键因素之一. 表面活性剂可通过提高水中疏水性污染物的溶解度来增强污染含水层的修复效率[9]. 表面活性剂可分为化学、生物和类表面活性剂. 表面活性剂的浓度超过一定值时形成大量称为“胶束”的聚集体,该浓度称为临界胶束浓度(CMC). 当表面活性剂的浓度高于CMC时,分子形成胶团包裹住污染物从而实现增溶. Butler等[10]研究了表面活性剂溶液中非水相液体混合物的增溶行为,发现表面活性剂对疏水性化合物溶解度的强化作用远大于亲水性化合物. Kommalapati等[11]研究了源自Sapindusmukorossi的天然表面活性剂皂素的性能,与商用表面活性剂性能相当.
虽然表面活性剂对疏水性污染物具有一定的增溶效果,但化学表面活性剂相对生物表面活性剂对环境造成的二次污染更大. 且因生产方式不同,大多数生物和类表面活性剂产量低且成本高,无法规模化使用[12 − 13]. 例如,鼠李糖脂在生产过程中的最大产量只能达到10 g·L−1左右[14]. 因此,采用表面活性剂增溶疏水性有机污染物时,除考虑增溶效果以外,需将毒性和成本纳入评价体系,以优化最佳表面活性剂筛选方法. 此外,无机盐和助剂常通过改变表面活性剂的聚集行为和分散性能,影响表面活性剂的表面电荷和分子构象来强化表面活性剂的增溶效果. 因此,在筛选最佳表面活性剂时,考虑无机盐和助剂添加浓度对提高疏水性有机污染物的去除效率也至关重要.
本研究选取菲、氯苯、正十六烷作为多环芳烃、苯系物和石油烃等典型疏水性有机污染物的代表,以10种常见的表面活性剂为研究对象,从成本、毒性、增溶效果等方面对各表面活性剂的性能进行综合评价,并筛选适用于目标污染物的3种表面活性剂. 通过添加不同浓度的助剂和无机盐,探究其对3类表面活性剂强化各污染物增溶性能的影响. 筛选确定最优表面活性剂,为地下水中疏水性有机污染物绿色高效去除方法的构建提供思路与依据.
1. 材料与方法(Materials and methods)
1.1 试剂与仪器
试剂:菲(95%,成都华夏化学试剂有限公司)、氯苯(AR,99%,上海阿拉丁生化科技股份有限公司)、正十六烷(AR,98%,上海易恩化学技术有限公司)、鼠李糖脂(纯度为95%,西安瑞捷生物科技有限公司)、十二烷基硫酸钠(AR,成都市科隆化学品有限公司)、十二烷基苯磺酸钠(AR,90%,成都市科隆化学品有限公司)、烷基糖苷0814(50%,山东优索化工科技有限公司)、吐温80(AR,99%,成都西亚化工股份有限公司)、曲拉通X-100(AR,99%,成都西亚化工股份有限公司)、槐糖脂(山东优索化工科技有限公司)、腐植酸(95%,北京沃凯生物科技有限公司)、皂素(98%,成都华夏化学试剂有限公司)、茶皂素 (60%,山东优索化工科技有限公司);氯化钠(AR,99.5%,成都市科隆化学品有限公司)、1,2-丙二醇(AR,99%,成都市科隆化学品有限公司)、正己烷(HPLC,98%,成都市科隆化学品有限公司)、二氯甲烷(HPLC,99.9%,成都市科隆化学品有限公司)等溶剂均为分析纯.
仪器:冷冻水浴恒温振荡器(JBXL-70,晶玻,常州普天仪器制造有限公司);台式高速离心机(L550,湘仪,湖南湘仪实验室仪器开发有限公司);电子天平(FB124,舜宇,上海舜宇恒平科学仪器有限公司);表面张力仪(BZY-1,上海衡平仪器仪表厂);气相色谱仪(GC-2010 Pro,岛津,日本);马尔文激光粒度仪(Zen3600,Malvern,英国).
1.2 表面活性剂CMC测定
通过使用表面张力仪对10种表面活性剂进行测定,得到各种表面活性剂的临界胶束浓度(CMC)和其它理化性质见(表1). 相对于传统的化学表面活性剂,生物表面活性剂的CMC大多远远小于化学表面活性剂,由于生物表面活性剂的价格较为昂贵,较低的CMC也有利于节约其用量,从而降低因价格昂贵带来的影响. 类表面活性剂腐植酸虽然和表面活性剂的作用机理和效果相似,但是CMC相较于其他9种常见的表面活性剂较大,增溶效果有待探究.
表 1 表面活性剂的理化参数及测定的CMC值Table 1. Physicochemical parameters and measured CMC values of the surfactants表面活性剂Surfactant 分子式Molecular formula 相对分子量Relative molecular mass 临界胶束浓度/(mg·L−1)CMC 吐温80 C64H124O261 1310 152.44 十二烷基苯磺酸钠 C12H25C6H4SO3Na 348 1037.16 十二烷基硫酸钠 C12H25OSO3Na 288 1173.96 鼠李糖脂 Rha-C10 — 32.56 曲拉通X-100 C34H62O11 646.85 197.38 烷基糖苷0814 C6H11O5 320.42 131.25 槐糖脂 C34H56O14 688.80 125.24 腐植酸 — — 2972.92 皂素 C27H42O3 1645.29 1566.85 茶皂素 C13H8Cl2N2O4 1645.30 733.236 1.3 增溶平衡实验
分别配制浓度为1 CMC的表面活性剂溶液,移取10 mL表面活性剂溶液于20 mL胶塞的玻璃瓶中,再在不同瓶子中分别加入稍过量的菲固体、氯苯液体和正十六烷液体,于30 ℃下以160 r·min−1转速分别振荡1、3、5、8、12、24、48 h. 平衡后,将样品取出以
4000 r·min−1离心10 min,分离未溶解的菲、氯苯、正十六烷,移取适量上清液,加入分液漏斗中,分别利用等量正己烷对菲和正十六烷进行萃取吸取上清液,用等量二氯甲烷对氯苯进行萃取,取下层液体,之后重复进行2次萃取以减小其对污染物测定的误差. 每个梯次样品设置3个平行样[15].用气相色谱仪测定溶液中的菲和氯苯以及正十六烷的浓度,气相条件分别为:
菲:进样口温度为300 ℃,载气为氦气,流速为1.2 mL·min−1,进样量1 μL,采用不分流进样模式,程序升温过程条件为:起始温度50 ℃下保持1 min,以30 ℃·min−1升至180 ℃,接着以3.5 ℃·min−1升至225 ℃,再以30 ℃·min−1升至300 ℃保持5 min,标准混合溶液的分离时间为18 min[16].
氯苯:进样口温度220 ℃;分流进样,分流比10:1;色谱柱升温程序:初始温度50 ℃保持1 min,以20 ℃·min−1升至130 ℃,再以10 ℃·min−1升至230 ℃,保持5 min[17].
正十六烷:载气为99.99%氮气,进样口温度250 ℃,分流比30:1,检测器温度300 ℃,氢气流量30 mL·min−1,空气流量300 mL·min−1,进样量1 μL. 初始160 ℃,保留1 min,以20 ℃·min−1升温至260 ℃,保留6 min[18].
1.4 对表面活性剂增溶效果的评价
通过对比在常态下利用表面活性剂强化对污染物的最大增溶效果与表面活性剂的价格之比,选取比值排在前3的表面活性剂进行稳定性测试. 评价系数的计算见式(1). 评价系数EC越大,则表示效果越好.
stringUtils.convertMath(!{formula.content}) (1) 式中:EC为评价系数;S表面活性剂对污染物的增溶倍数;P为表面活性剂成本,元.
1.5 无机盐的影响
依据以上实验结果,分别选取评价系数最大的3种表面活性剂,在1.2节确定各自污染物对应选取的表面活性剂所达到最大增溶浓度的时间(t0)后,设置表面活性剂浓度都为1 CMC. 在这3种表面活性剂溶液中加入NaCl,使NaCl浓度分别达到0、1、10、20 mg·L−1. 到达t0时间后,将样品取出以
4000 r·min−1离心10 min,去除未溶解的污染物,移取适量上清液加入分液漏斗,按照1.3节所述方法进行萃取和测定,每组样品设置3个平行样.表面张力测定:离心结束后取部分样品,倒入玻璃培养皿中5 mm后,直接将挂片淹没在溶液中进行测试,待稳定后进行读数. 每组试验进行3次,取平均值作为最终试验结果.
1.6 助剂的影响
通过在1.4部分中选取的表面活性剂,设置其浓度为1 CMC,在溶液中加入助剂1,2-丙二醇,使1,2-丙二醇分别达到0、0.1、0.5、1 mol·L−1,振荡时间t0. 按1.5节所述方法测定样品中污染物浓度和样品的表面张力.
2. 结果与讨论(Results and discussion)
2.1 10种表面活性剂对菲、氯苯、正十六烷的增溶效果
10种表面活性剂对不同污染物的增溶效果见图1,显示在48 h的时间内,增溶效果随着时间的增加,不同表面活性剂对不同的污染物增溶作用呈现出显著差别.
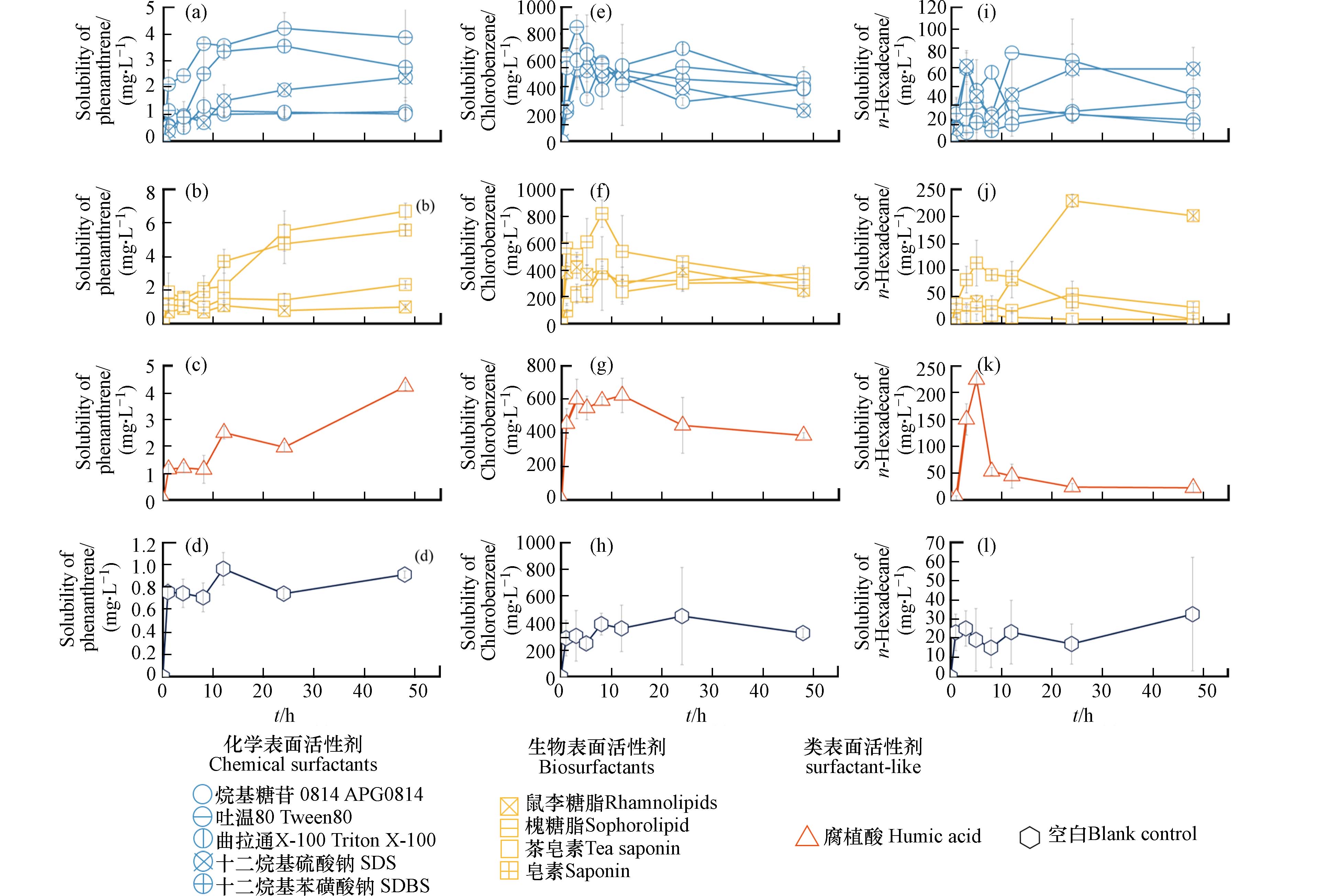 图 1 10种表面活性剂在不同时间梯度下对菲、氯苯和正十六烷的增溶效果Figure 1. Ten surfactants' solubilization effects on phenanthrene, chlorobenzene, and n-hexadecane at various time gradients图中的(a)、(b)、(c)和(d)分别体现了化学表面活性剂、生物表面活性剂、表面活性剂类似物以及在对照(空白)条件下对菲的增溶作用. 类似地,(e)、(f)、(g)和(h)展示了对氯苯的效果,(i)、(j)、(k)和(l)则展示了对正十六烷溶解性的影响Figures (a), (b), (c), and (d) depict the solubilizing action on phenanthrene by chemical surfactants, biosurfactants, surfactant analogs, and under control (blank) conditions, respectively. Similarly, (e), (f), (g), and (h) demonstrate the effects on chlorobenzene, and (i), (j), (k), and (l) show the corresponding effects on n-hexadecane
图 1 10种表面活性剂在不同时间梯度下对菲、氯苯和正十六烷的增溶效果Figure 1. Ten surfactants' solubilization effects on phenanthrene, chlorobenzene, and n-hexadecane at various time gradients图中的(a)、(b)、(c)和(d)分别体现了化学表面活性剂、生物表面活性剂、表面活性剂类似物以及在对照(空白)条件下对菲的增溶作用. 类似地,(e)、(f)、(g)和(h)展示了对氯苯的效果,(i)、(j)、(k)和(l)则展示了对正十六烷溶解性的影响Figures (a), (b), (c), and (d) depict the solubilizing action on phenanthrene by chemical surfactants, biosurfactants, surfactant analogs, and under control (blank) conditions, respectively. Similarly, (e), (f), (g), and (h) demonstrate the effects on chlorobenzene, and (i), (j), (k), and (l) show the corresponding effects on n-hexadecane不同时间段内对于菲的增溶效果显示(图1(a—c)),在第48 h后对菲的增溶效果最佳的3种表面活性剂分别为:茶皂素、皂素、吐温80. 吐温80在短时间内显示对菲的增溶效果出现较大增长,之后又快速趋于平稳,得到的增溶效果比茶皂素差,相比在空白状态下增溶效果提升了7.59倍. 随着时间的不断延长,茶皂素对菲的增溶效果不断增强,且更为稳定.
对氯苯具有最佳增溶效果的表面活性剂分别为:吐温80、十二烷基苯磺酸钠、十二烷基硫酸钠(图1e,f,g). 所有表面活性剂对氯苯的增溶性能在12 h内快速增大后又逐渐开始降低,主要在于氯苯具有强挥发性,被增溶的氯苯产生了挥发[19]. 吐温80相对于空白状态下最大增溶效果提升了2.73倍.
对正十六烷具有最佳增溶效果的表面活性剂分别为:鼠李糖脂、腐植酸、皂素(图1i,j,k). 5 h之内腐植酸对正十六烷的增溶效果最佳,但是随着时间的推移,增溶效果开始减弱,可能是由于腐植酸作为一种环境友好型吸附剂,氧化程度较高,极性强,芳构度小,脂肪键多,分子中具有较高含量的羧基、酚羟基和酮型羧基等活性基团,可能通过吸附的方式将水中增溶的正十六烷进行吸附,从而使得水中的正十六烷基浓度逐渐降低[20 − 21]. 鼠李糖脂对正十六烷的增溶效果最佳,相对于空白状态下增溶效果提升了13.41倍,并且到达最大增溶浓度后正十六烷浓度趋于稳定.
类表面活性剂腐植酸存在增溶性能的可能原因是其和表面活性剂有相似的能力,使得疏水性污染物可以大大提升其在水溶液中的溶解度,从而达到增溶的目的. 通过对氯苯和正十六烷的增溶结果可以看出,随时间变化两种疏水性污染物的增溶量先增大后开始减小,其主要原因是因为腐植酸中的脂肪结构促进了腐植酸对疏水性物质的吸附,通过物理吸附、分配、氢键、共价键等途径与污染物进行结合,从而固定、沉淀疏水性有机污染物,使得被增溶的氯苯和正十六烷在水中的含量减小[22 − 29]. 之所以菲浓度没有降低,可能是固体菲的粒径过大导致无法通过物理性的吸附去除.
2.2 表面活性剂性能评价
本研究10种表面活性剂的毒性按照由高到低排列为:十二烷基苯磺酸钠>十二烷基硫酸钠>曲拉通X-100>吐温80>腐植酸>皂素>茶皂素>槐糖脂>鼠李糖脂[30 − 40]( 烷基糖苷0814未查到). 表面活性剂的毒性基本遵循着化学表面活性剂>生物表面活性剂,由于类表面活性剂涉及的物质范围较广,没有相对确切的毒性大小,所以以腐植酸作为类表面活性剂代表进行评价. 评价系数及相关指标见表2.
表 2 对菲、氯苯、正十六烷增溶的表面活性剂评价系数及相关参数Table 2. Surfactant evaluation coefficients and related parameters for the phenanthrene, chlorobenzene and n-hexadecane solubilization表面活性剂Surfactant 类型Type 毒性排名(从低到高)Toxicity ranking (from low to high) 价格/元Price 菲的增溶倍数Solubilization ratio of phenanthrene 评价系数Evaluation coefficient 增溶氯苯倍数Solubilization times of chlorobenzene 评价系数Evaluation coefficient 增溶正十六烷倍数Solubilization ratio of n-hexadecane 评价系数Evaluation coefficient 烷基糖苷0814 非离子型表面活性剂 — 9—25 2.87 0.32—0.11 1.56 0.06—0.17 1.31 0.05—0.15 吐温80 非离子型表面活性剂 6 10—16 5.66 0.57—0.35 2.80 0.17—0.28 3.39 0.21—0.34 曲拉通X-100 非离子型表面活性剂 7 14—20 1.35 0.09—0.07 1.55 0.08—0.11 2.68 0.13—0.19 鼠李糖脂 生物表面活性剂 1 300 1.05 0.003 1.03 0.00342 13.41 0.0447 槐糖脂 生物表面活性剂 2 260 1.91 0.007 2.15 0.0083 3.21 0.0124 腐植酸 类表面活性剂 5 430 2.65 0.006 1.73 0.0040 11.80 0.0274 茶皂素 生物表面活性剂 3 360 7.45 0.021 1.14 0.0032 1.60 0.0044 皂素 生物表面活性剂 4 90—300 6.41 0.07—0.02 0.95 0.003— 0.0105 5.89 0.02-0.07 十二烷基硫酸钠 阴离子型表面活性剂 8 10—25 2.57 0.26—0.10 1.91 0.077—0.191 2.68 0.11—0.28 十二烷基苯磺酸钠 阴离子型表面活性剂 9 12—50 4.77 0.40—0.10 2.73 0.055—0.224 1.14 0.02—0.10 在毒性排序的基础上,通过对比表2中这10种表面活性剂的评价系数,分别筛选出对应每种污染物的3种表面活性剂,如表3所示.
表 3 根据评价系数针对不同污染物选用的3种表面活性剂Table 3. Three surfactants selected for different pollutants based on evaluation factors有机污染物Organic pollutants 1号表面活性剂Surfactant No.1 2号表面活性剂Surfactant No.2 3号表面活性剂Surfactant No.3 菲 皂素 茶皂素 槐糖脂 氯苯 吐温80 槐糖脂 腐植酸 正十六烷 鼠李糖脂 皂素 吐温80 2.3 不同浓度无机盐及助剂对表面活性剂增溶性能的影响
通过向表面活性剂溶液中添加不同量的NaCl,测定溶解在表面活性剂中污染物含量以及表面张力的变化. NaCl浓度对表面活性剂增溶菲的影响效果见图2(a)和图2(d),随着NaCl浓度增大,皂素和茶皂素对菲的增溶效果开始增强,而槐糖脂则产生了抑制作用. 当NaCl浓度超过1 mg·L−1时,皂素和茶皂素对菲的增溶效果出现抑制的状况. 与之相反,槐糖脂呈现促进作用. 对于溶液的表面张力,随着NaCl浓度的增大,皂素和茶皂素溶液的表面张力都远远大于槐糖脂,但对于这3种表面活性剂而言,表面张力变化趋势都较稳定.
NaCl浓度对表面活性剂增溶氯苯的影响效果见图2(b)和图2(e),显示随着NaCl浓度增大,吐温80在NaCl达到1 mg·L−1时达到最大,然后随着NaCl浓度的增大,增溶效果降低. 腐植酸先呈现促进作用,在NaCl达到10 mg·L−1之后增溶效果逐渐呈现抑制效果. 图2(e)显示溶液的表面张力并没有出现太明显变化,表示NaCl浓度对溶液稳定性影响较小.
NaCl浓度对表面活性剂增溶正十六烷的影响效果见图2(c)和图2(f),显示随着NaCl浓度的增大,鼠李糖脂对正十六烷的增溶效果呈现抑制作用,当NaCl浓度增大到1 mg·L−1时,逐渐开始出现增溶增强的效果,但整体呈现抑制作用,而皂素以及吐温80对正十六烷的增溶效果并没有随着NaCl的浓度而出现明显变化. 溶液的表面张力在添加鼠李糖脂和皂素的溶液中未出现明显变化,显示溶液较为稳定,而添加吐温80溶液的表面张力随着NaCl浓度的增大而增大.
以上结果表明无机盐的添加会造成溶液中被增溶的污染物含量变化及表面张力变动,尤其是对于离子型表面活性剂影响更为明显[41 − 42]. 无机盐离子会影响离子型表面活性剂的聚集和吸附,离子型表面活性剂的界面活性受溶液内电解质含量的影响很大,使得双电层受到压缩,从而带有相同电荷的亲水基之间的排斥作用也随之减弱,结果导致表面活性剂的吸附量出现变化. 离子型表面活性剂中加入无机盐后,带相同电荷的极性基之间的排斥作用减弱,导致CMC值发生变化[43 − 46]. 同时也会降低溶液的表面张力,使改变胶束聚集体的微观结构并增强胶束生长,引起表面活性剂的可逆相变,使得表面活性剂可能析出产生沉淀.
无机盐的加入可能会对非离子表面活性的结构产生影响,其主要通过改变溶剂的极性,影响表面活性剂的溶解性和胶束的形成,增加溶剂的离子强度. 这可能会使非离子表面活性剂的胶束更加紧密,从而增强其增溶作用. 并且无机盐的加入改变了溶液的离子环境,影响表面活性剂分子在溶液表面的排列和密度,减少表面活性剂分子在溶液表面的吸附,进而影响表面张力[47 − 48].
生物表面活性剂通常具有更复杂的结构,无机盐可能通过影响其立体构型来改变其增溶性能,并对体系本身离子强度变化产生影响,从而改变表面活性剂的分子结构和官能团的活性,进而影响其增溶能力和表面张力[49].
通过向表面活性剂溶液中添加不同量的1,2-丙二醇,测定溶解在表面活性剂中污染物含量以及表面张力的变化. 1,2-丙二醇浓度对表面活性剂增溶菲的影响效果见图3(a)和图3(d). 随着1,2-丙二醇浓度增大,茶皂素对菲的增溶效果并没有出现明显的变化;槐糖脂随着1,2-丙二醇浓度增大对菲的增溶效果逐渐增大,直到1,2-丙二醇浓度超过0.5 mol·L−1后开始呈现抑制作用;皂素在1,2-丙二醇浓度达到0.1 mol·L−1前呈现逐渐抑制的作用,当1,2-丙二醇浓度大于0.1 mol·L−1时,对菲的增溶效果呈现促进效果,直到1,2-丙二醇浓度超过0.5 mol·L−1后呈现抑制作用;对于溶液表面张力,随着1,2-丙二醇浓度的增大,皂素溶液的表面张力并没有出现明显的变化;槐糖脂的表面张力开始呈现较为稳定,当1,2-丙二醇浓度超过0.5 mol·L−1时,表面张力开始降低;而茶皂素溶液的表面张力随着1,2-丙二醇浓度的增大而增大.
1,2-丙二醇浓度对表面活性剂增溶氯苯的影响效果见图3(b)和图3(e). 随着1,2-丙二醇浓度的增大,对槐糖脂和吐温80呈现出促进增溶的效果,对于腐植酸则相反,呈现出抑制作用. 1,2-丙二醇浓度的变化并未明显改变表面张力.
1,2-丙二醇浓度对表面活性剂增溶正十六烷的影响效果见图3(c)和图3(f). 随着1,2-丙二醇浓度的增大,皂素对正十六烷的增溶效果并未出现明显变化;而鼠李糖脂对其的增溶效果随着1,2-丙二醇浓度增大先逐渐增大,直到1,2-丙二醇浓度超过0.5 mol·L−1后开始出现抑制;而吐温80的增溶效果随着1,2-丙二醇浓度的增大而增大. 对于溶液表面张力,鼠李糖脂和皂素溶液的表面张力并未出现明显变化,但随着1,2-丙二醇浓度的增大吐温80溶液的表面张力快速增大后保持稳定.
2.4 不同浓度助剂对表面活性剂增溶体系中粒径的影响
粒径分析结果表明(表4),对于菲的体系,随着1,2-丙二醇添加量的增加,粒径逐渐减小至100 nm以下,形成了微乳体系. 在氯苯体系中,添加吐温80和腐植酸也使体系趋向微乳化. 但使用槐糖脂时,粒径先减小后增大,表明低浓度的1,2-丙二醇更倾向于形成微乳体系,这主要是由于复配效应增加了污染物的溶解度. 对于正十六烷体系,鼠李糖脂和吐温80在增溶污染物时,复配作用的影响大于微乳体系的影响. 低浓度的1,2-丙二醇会形成微乳体系,从而增强增溶效果,但高浓度的助剂添加可能抑制粒径减小,更倾向于复配作用.
表 4 不同1,2-丙二醇添加量下不同体系中粒径的变化Table 4. Changes in particle size in different systems with different amounts of 1,2-propanediol added体系名称System name 0 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 0 mol·L−1 0.1 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 0.1 mol·L−1 0.5 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 0.5 mol·L−1 1 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 1 mol·L−1 皂素+菲 93.97 87.49 28.72 23.21 茶皂素+菲 126.50 26.56 25.23 23.01 槐糖脂+菲 165.4 58.57 55.49 52.27 吐温80+氯苯 112.53 7.07 18.40 32.40 槐糖脂+氯苯 7189 1188 1398 4394 腐植酸+氯苯 115.3 96.02 71.03 43.1 鼠李糖脂+正十六烷 645.5 2091 1393 1274 皂素+正十六烷 >10 μm 116.9 70.21 142.2 吐温80+正十六烷 >10 μm 4956 2876 340.3 由于1,2-丙二醇属于醇类助剂,醇具有一定程度的亲油性质,微乳液体系可能发生相变化,增溶能力提高,使得污染物的增溶量加大,而且醇的加入在一定程度上可能会让溶液形成微乳体系,单相微乳液区域有所扩大使得体系变稳定. 但在高浓度助剂情况下可能会和表面活性剂对污染物的增溶产生拮抗作用,从而减弱增溶效果[50 − 56].
3. 结论(Conclusions)
(1) 从增溶效果上来看,对菲增溶效果的最佳的表面活性剂为茶皂素,对氯苯增溶效果最佳为吐温80,对正十六烷增溶效果最佳为鼠李糖脂,对于空白条件下增溶效果的倍数分别提升了7.59倍、2.73倍、13.41倍.
(2) 在考虑毒性、价格等因素并计算评价系数后,对菲最适的表面活性剂为皂素,对氯苯最适合的表面活性剂为吐温80,对正十六烷最适的表面活性剂为鼠李糖脂.
(3) 利用皂素在对菲进行增溶的过程中,NaCl浓度为1 mg·L−1,1,2-丙二醇浓度为0.5 mol·L−1时为最佳,增溶效果大约提升12.82倍;利用吐温80对氯苯的增溶过程中,只添加1 mg·L−1NaCl浓度时效果最佳(+333%);利用鼠李糖脂增溶正十六烷时,只添加浓度为0.1 mol·L−1的1,2-丙二醇时效果最好,增溶效果提升15.65倍. 相对于非离子表面活性剂,盐浓度和助剂浓度的变化对离子型表面活性剂对影响更加明显.
本研究的相关成果可为表面活性剂强化地下水中疏水性有机污染物绿色高效去除方法的构建提供新思路与依据.
-
表 1 表面活性剂的理化参数及测定的CMC值
Table 1. Physicochemical parameters and measured CMC values of the surfactants
表面活性剂Surfactant 分子式Molecular formula 相对分子量Relative molecular mass 临界胶束浓度/(mg·L−1)CMC 吐温80 C64H124O261 1310 152.44 十二烷基苯磺酸钠 C12H25C6H4SO3Na 348 1037.16 十二烷基硫酸钠 C12H25OSO3Na 288 1173.96 鼠李糖脂 Rha-C10 — 32.56 曲拉通X-100 C34H62O11 646.85 197.38 烷基糖苷0814 C6H11O5 320.42 131.25 槐糖脂 C34H56O14 688.80 125.24 腐植酸 — — 2972.92 皂素 C27H42O3 1645.29 1566.85 茶皂素 C13H8Cl2N2O4 1645.30 733.236 表 2 对菲、氯苯、正十六烷增溶的表面活性剂评价系数及相关参数
Table 2. Surfactant evaluation coefficients and related parameters for the phenanthrene, chlorobenzene and n-hexadecane solubilization
表面活性剂Surfactant 类型Type 毒性排名(从低到高)Toxicity ranking (from low to high) 价格/元Price 菲的增溶倍数Solubilization ratio of phenanthrene 评价系数Evaluation coefficient 增溶氯苯倍数Solubilization times of chlorobenzene 评价系数Evaluation coefficient 增溶正十六烷倍数Solubilization ratio of n-hexadecane 评价系数Evaluation coefficient 烷基糖苷0814 非离子型表面活性剂 — 9—25 2.87 0.32—0.11 1.56 0.06—0.17 1.31 0.05—0.15 吐温80 非离子型表面活性剂 6 10—16 5.66 0.57—0.35 2.80 0.17—0.28 3.39 0.21—0.34 曲拉通X-100 非离子型表面活性剂 7 14—20 1.35 0.09—0.07 1.55 0.08—0.11 2.68 0.13—0.19 鼠李糖脂 生物表面活性剂 1 300 1.05 0.003 1.03 0.00342 13.41 0.0447 槐糖脂 生物表面活性剂 2 260 1.91 0.007 2.15 0.0083 3.21 0.0124 腐植酸 类表面活性剂 5 430 2.65 0.006 1.73 0.0040 11.80 0.0274 茶皂素 生物表面活性剂 3 360 7.45 0.021 1.14 0.0032 1.60 0.0044 皂素 生物表面活性剂 4 90—300 6.41 0.07—0.02 0.95 0.003— 0.0105 5.89 0.02-0.07 十二烷基硫酸钠 阴离子型表面活性剂 8 10—25 2.57 0.26—0.10 1.91 0.077—0.191 2.68 0.11—0.28 十二烷基苯磺酸钠 阴离子型表面活性剂 9 12—50 4.77 0.40—0.10 2.73 0.055—0.224 1.14 0.02—0.10 表 3 根据评价系数针对不同污染物选用的3种表面活性剂
Table 3. Three surfactants selected for different pollutants based on evaluation factors
有机污染物Organic pollutants 1号表面活性剂Surfactant No.1 2号表面活性剂Surfactant No.2 3号表面活性剂Surfactant No.3 菲 皂素 茶皂素 槐糖脂 氯苯 吐温80 槐糖脂 腐植酸 正十六烷 鼠李糖脂 皂素 吐温80 表 4 不同1,2-丙二醇添加量下不同体系中粒径的变化
Table 4. Changes in particle size in different systems with different amounts of 1,2-propanediol added
体系名称System name 0 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 0 mol·L−1 0.1 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 0.1 mol·L−1 0.5 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 0.5 mol·L−1 1 mol·L−11,2-丙二醇时的粒径/nmParticle size of 1,2-propanediol at 1 mol·L−1 皂素+菲 93.97 87.49 28.72 23.21 茶皂素+菲 126.50 26.56 25.23 23.01 槐糖脂+菲 165.4 58.57 55.49 52.27 吐温80+氯苯 112.53 7.07 18.40 32.40 槐糖脂+氯苯 7189 1188 1398 4394 腐植酸+氯苯 115.3 96.02 71.03 43.1 鼠李糖脂+正十六烷 645.5 2091 1393 1274 皂素+正十六烷 >10 μm 116.9 70.21 142.2 吐温80+正十六烷 >10 μm 4956 2876 340.3 -
[1] 蒋鹏. 地下水有机污染修复技术探究[J]. 资源节约与环保, 2018(8): 83. JIANG P. Study on the remediation techniques of organic pollution in groundwater[J]. Resources Economization & Environmental Protection, 2018(8): 83 (in Chinese).
[2] DAS C R, DAS S, PANDA S. MLR index-based principal component analysis to investigate and monitor probable sources of groundwater pollution and quality in coastal areas: A case study in East India[J]. Environmental Monitoring and Assessment, 2023, 195(10): 1158. doi: 10.1007/s10661-023-11804-7 [3] LIU F J, LIU H W, ZHU H, et al. Remediation of petroleum hydrocarbon-contaminated groundwater by biochar-based immobilized bacteria[J]. Biochemical Engineering Journal, 2023, 197: 108987. doi: 10.1016/j.bej.2023.108987 [4] WANG J C, ZHAO Y S, SUN J C, et al. The distribution and sources of polycyclic aromatic hydrocarbons in shallow groundwater from an alluvial-diluvial fan of the Hutuo River in North China[J]. Frontiers of Earth Science, 2019, 13(1): 33-42. doi: 10.1007/s11707-018-0701-4 [5] 王姣. 染料厂地下水质分析及含氯苯废水处理工艺探讨[J]. 天津化工, 2022, 36(3): 83-86. WANG J. Analysis of groundwater quality in dyeing factory and discussion on treatment process of chlorobenzene wastewater[J]. Tianjin Chemical Industry, 2022, 36(3): 83-86 (in Chinese).
[6] 王先稳. 华北平原土壤地下水中多环芳烃污染特征及迁移模拟研究[D]. 北京: 北京林业大学, 2020. WANG X W. Pollution characteristics and transport simulation research of polycyclic aromatic hydrocarbons in soil and groundwater in North China Plain[D]. Beijing: Beijing Forestry University, 2020 (in Chinese).
[7] 徐蓉桢. 不同地区地下水中半挥发性有机污染物的分布特征与现状评价[D]. 北京: 中国地质大学(北京), 2018. XU R Z. The distribution characteristics and assessment of semivolatile organic compounds in groundwater in different areas[D]. Beijing: China University of Geosciences, 2018 (in Chinese).
[8] 刘洋. 鼠李糖脂协调石油烃类污染物生物降解的机制研究[D]. 长沙: 湖南大学, 2018. LIU Y. The mechanism study for rhamnolipid-mediated biodegradation of petroleum hydrocarbons contaminants[D]. Changsha: Hunan University, 2018 (in Chinese).
[9] MUSHTAQ S, ASLAM Z, ALI R, et al. Surfactant modified waste ash for the removal of chloro and nitro group substituted benzene from wastewater[J]. Water Science and Technology, 2022, 86(8): 1969-1980. doi: 10.2166/wst.2022.324 [10] BUTLER E C, HAYES K F. Micellar solubilization of nonaqueous phase liquid contaminants by nonionic surfactant mixtures: Effects of sorption, partitioning and mixing[J]. Water Research, 1998, 32(5): 1345-1354. doi: 10.1016/S0043-1354(97)00360-6 [11] KOMMALAPATI R R, VALSARAJ K T, CONSTANT W D, et al. Aqueous solubility enhancement and desorption of hexachlorobenzene from soil using a plant-based surfactant[J]. Water Research, 1997, 31(9): 2161-2170. doi: 10.1016/S0043-1354(97)00052-3 [12] CASAS J, GARCÍA-OCHOA F. Sophorolipid production by Candida bombicola: Medium composition and culture methods[J]. Journal of Bioscience and Bioengineering, 1999, 88(5): 488-494. doi: 10.1016/S1389-1723(00)87664-1 [13] GUILMANOV V, BALLISTRERI A, IMPALLOMENI G, et al. Oxygen transfer rate and sophorose lipid production by Candida bombicola[J]. Biotechnology and Bioengineering, 2002, 77(5): 489-494. doi: 10.1002/bit.10177 [14] LANG S, WULLBRANDT D. Rhamnoselipids–biosynthesis, microbial production and application potential[J]. Applied Microbiology and Biotechnology, 1999, 51(1): 22-32. doi: 10.1007/s002530051358 [15] 郭利果, 苏荣国, 梁生康, 等. 鼠李糖脂生物表面活性剂对多环芳烃的增溶作用[J]. 环境化学, 2009, 28(4): 510-514. GUO L G, SU R G, LIANG S K, et al. Solubilization of polycyclic aromatic hydrocarbons by rhamnolipid biosurfactant[J]. Environmental Chemistry, 2009, 28(4): 510-514 (in Chinese).
[16] 郝星杰, 郑劼, 吴宇, 等. 利用气相色谱串联质谱技术测定泥页岩中菲、萘及其甲基化产物的方法研究[J]. 四川化工, 2021, 24(1): 35-38. HAO X J, ZHENG J, WU Y, et al. Study on the determination of phenanthrene, naphthalene and their methylation products in shale by gas chromatography tandem mass spectrometry[J]. Sichuan Chemical Industry, 2021, 24(1): 35-38 (in Chinese).
[17] 顾兴为. 顶空-气相色谱质谱法同时测定地表水中氯苯和二氯苯[J]. 化学工程师, 2023, 37(2): 28-30. GU X W. Simultaneous determination of chlorobenzene and dichlorobenzene in surface water by headspace gas chromatography-mass spectrometry[J]. Chemical Engineer, 2023, 37(2): 28-30 (in Chinese).
[18] 李迎鹤, 刘东, 于杰, 等. 正十六烷降解菌的分离、鉴定及降解特性研究[J]. 哈尔滨商业大学学报(自然科学版), 2022, 38(2): 131-136. LI Y H, LIU D, YU J, et al. Isolation, identification and degradation characteristics of n-hexadecane degrading bacteria[J]. Journal of Harbin University of Commerce (Natural Sciences Edition), 2022, 38(2): 131-136 (in Chinese).
[19] 王湘徽, 祝欣, 龙涛, 等. 氯苯类易挥发有机污染土壤异位低温热脱附实例研究[J]. 生态与农村环境学报, 2016, 32(4): 670-674. WANG X H, ZHU X, LONG T, et al. Case study on ex-situ remediation of chlorobenzene-like volatile organic compounds(VOCs) contaminated soil with technique of low-temperature thermal desorption[J]. Journal of Ecology and Rural Environment, 2016, 32(4): 670-674 (in Chinese).
[20] 郝全龙, 谯华, 周从直, 等. 腐殖质吸附土壤有机污染物研究进展[J]. 当代化工, 2014, 43(10): 2068-2071. HAO Q L, QIAO H, ZHOU C Z, et al. Research progress in soil organic pollutants adsorption by humus[J]. Contemporary Chemical Industry, 2014, 43(10): 2068-2071 (in Chinese).
[21] 张立超, 包先明, 余福波, 等. 富里酸和胡敏酸在蒙脱石上的吸附特性[J]. 环境科学研究, 2013, 26(12): 1333-1339. ZHANG L C, BAO X M, YU F B, et al. Studies on the adsorption mechanisms of fulvic acid and humic acid on smectite[J]. Research of Environmental Sciences, 2013, 26(12): 1333-1339 (in Chinese).
[22] MERYEMOGLU B, OZSEL B K. Humic acids derived from lignocellulosic biomass: Characterization and utilizing for environmental applications[J]. Water, Air, & Soil Pollution, 2022, 233(10): 402. [23] 霍夫里特 M, 斯泰因比歇尔 A(著). 郭圣荣(译). 生物高分子(第1卷)[M]. 北京: 化学工业出版社, 2004. HOFRICHTER M. , STEINBÜCHEL A. (Eds. ). GUO S R. (Translator). Biopolymers, Volume 1[M]. Beijing: Chemical Industry Press, 2004(in Chinese).
[24] LIU X C, GE W, ZHANG X M, et al. Biodegradation of aged polycyclic aromatic hydrocarbons in agricultural soil by Paracoccus sp. LXC combined with humic acid and spent mushroom substrate[J]. Journal of Hazardous Materials, 2019, 379: 120820. doi: 10.1016/j.jhazmat.2019.120820 [25] 郭梦卓, 徐佰青, 乔显亮, 等. 表面活性剂强化过硫酸钠氧化修复石油烃污染土壤[J]. 土壤, 2023, 55(1): 171-177. GUO M Z, XU B Q, QIAO X L, et al. Surfactant enhancement in remediation of petroleum hydrocarbon contaminated soil by sodium persulfate[J]. Soils, 2023, 55(1): 171-177 (in Chinese).
[26] ZHUANG Z, HAZELTON P. An investigation of the efficiency of fulvic acid and straw water amendments for arsenic uptake from groundwater by Vetiveria zizanioides[J]. Advanced Materials Research, 2013, 864-867: 1233-1239. doi: 10.4028/www.scientific.net/AMR.864-867.1233 [27] PERMINOVA I V, GRECHISHCHEVA N Y, KOVALEVSKII D V, et al. Quantification and prediction of the detoxifying properties of humic substances related to their chemical binding to polycyclic aromatic hydrocarbons[J]. Environmental Science & Technology, 2001, 35(19): 3841-3848. [28] 李岳. 建设用地污染土壤与地下水修复技术研究[J]. 皮革制作与环保科技, 2023, 4(10): 181-183. LI Y. Research of remediation technology of contaminated soil and groundwater in construction land[J]. Leather Manufacture and Environmental Technology, 2023, 4(10): 181-183 (in Chinese).
[29] 陈静, 黄占斌. 腐植酸在土壤修复中的作用[J]. 腐植酸, 2014(4): 30-34,65. CHEN J, HUANG Z B. Effect of humic acid on soil restoration[J]. Humic Acid, 2014(4): 30-34,65 (in Chinese).
[30] 陈清香, 吕军仪. 表面活性剂十二烷基苯磺酸钠(SDBS)和十二烷基磺酸钠(SDS)对安氏伪镖水蚤的急性毒性研究[J]. 生态毒理学报, 2010, 5(1): 76-82. CHEN Q X, LV J Y. Acute toxicity of sodium dodecyl benzene sulfonate (SDBS) and sodium dodecyl sulfate (SDS) to the copepod, Pseudodiaptomus annandalei[J]. Asian Journal of Ecotoxicology, 2010, 5(1): 76-82 (in Chinese).
[31] 申琼, 王冰, 杨宝灵, 等. 表面活性剂对斜生栅藻的生态毒性研究[J]. 安全与环境学报, 2011, 11(1): 1-3. SHEN Q, WANG B, YANG B L, et al. Acute toxicity of several surfactants to Scenedesmus obliquus[J]. Journal of Safety and Environment, 2011, 11(1): 1-3 (in Chinese).
[32] 文莉, 芦苇, 蒋倩, 等. 茶皂素毒性刺激性试验及抑菌作用研究[J]. 中国油脂, 2011, 36(6): 58-60. WEN L, LU W, JIANG Q, et al. Toxicity, irritation and bacteriostasis of tea saponin[J]. China Oils and Fats, 2011, 36(6): 58-60 (in Chinese).
[33] 何晓玲, 高进勇, 邵敬伟. 茶皂素对蚯蚓、小菜蛾及枯萎病原真菌的急性毒性研究[J]. 福州大学学报(自然科学版), 2007, 35(5): 785-788. HE X L, GAO J Y, SHAO J W. Acute toxicity effect on earthworm, plutella xylostella and fusarium oxysporum by tea saponin[J]. Journal of Fuzhou University (Natural Science Edition), 2007, 35(5): 785-788 (in Chinese).
[34] NIKONOVA A A, MIZANDRONTSEV I B, BAZHENOV B N, et al. Toxic effect of anionic surfactants on freshwater sponge Lubomirskia baikalensis and its endosymbiotic microalgae Chlorella sp[J]. Diversity, 2023, 15(1): 77. doi: 10.3390/d15010077 [35] INVALLY K, JU L K. Biolytic effect of rhamnolipid biosurfactant and dodecyl sulfate against phagotrophic Alga Ochromonas danica[J]. Journal of Surfactants and Detergents, 2017, 20(5): 1161-1171. doi: 10.1007/s11743-017-2005-1 [36] LI G X, LAN G H, LIU Y Q, et al. Evaluation of biodegradability and biotoxicity of surfactants in soil[J]. RSC Advances, 2017, 7(49): 31018-31026. doi: 10.1039/C7RA02105D [37] JOHANN S, SEILER T B, TISO T, et al. Mechanism-specific and whole-organism ecotoxicity of mono-rhamnolipids[J]. Science of the Total Environment, 2016, 548-549: 155-163. doi: 10.1016/j.scitotenv.2016.01.066 [38] YUAN Z Y, LI Y, HU Y L, et al. Chitosan nanoparticles and their Tween 80 modified counterparts disrupt the developmental profile of zebrafish embryos[J]. International Journal of Pharmaceutics, 2016, 515(1-2): 644-656. doi: 10.1016/j.ijpharm.2016.10.071 [39] RAMIREZ D, SHAW L J, COLLINS C D. Ecotoxicity of oil sludges and residuals from their washing with surfactants: Soil dehydrogenase and ryegrass germination tests[J]. Environmental Science and Pollution Research, 2021, 28(11): 13312-13322. doi: 10.1007/s11356-020-11300-2 [40] HWANG D, SHIN H, JEONG H, et al. Shampoo characteristics of botanical extract containing green tea, Saururus chinensis and Prunus padus[J]. Korean Chemical Engineering Research, 2015, 53(6): 663-666. doi: 10.9713/kcer.2015.53.6.663 [41] ZHAO T T, XU G Y, YUAN S L, et al. Molecular dynamics study of alkyl benzene sulfonate at air/water interface: Effect of inorganic salts[J]. The Journal of Physical Chemistry. B, 2010, 114(15): 5025-5033. doi: 10.1021/jp907438x [42] SANGWAI A V, SURESHKUMAR R. Binary interactions and salt-induced coalescence of spherical micelles of cationic surfactants from molecular dynamics simulations[J]. Langmuir:the ACS Journal of Surfaces and Colloids, 2012, 28(2): 1127-1135. doi: 10.1021/la203745d [43] 王鹤霏. 表面活性剂增效分离去除水中芳香有机污染物特征的研究[D]. 大连: 大连理工大学, 2019. WANG H F. Study of characteristics of surfactant enhanced separation and removal of aromatic organic contaminants from aqueous solutions[D]. Dalian: Dalian University of Technology, 2019 (in Chinese).
[44] KOIDE Y, GOTO S. Effect of scission on alignment of nonionic surfactant micelles under shear flow[J]. Soft Matter, 2023, 19(23): 4323-4332. doi: 10.1039/D3SM00167A [45] TURNER A, XU J. Influence of ionic surfactants on the flocculation and sorption of palladium and mercury in the aquatic environment[J]. Water Research, 2008, 42(1-2): 318-326. doi: 10.1016/j.watres.2007.07.018 [46] PEREIRA R F P, VALENTE A J M, BURROWS H D, et al. Structural characterization of solid trivalent metal dodecyl sulfates: From aqueous solution to lamellar superstructures[J]. RSC Advances, 2013, 3(5): 1420-1433. doi: 10.1039/C2RA21906A [47] 李文斌. 两性—阴(阳)离子复配修饰黏土的修饰机制及其对菲、Cr(Ⅵ)的吸附[D]. 杨凌: 西北农林科技大学, 2016. LI W B. Modification mechanism of amphoteric-cationic and amphoteric-anionic modified clays and its adsorption to phenanthrene and Cr(Ⅵ)[D]. Yangling: Northwest A & F University, 2016 (in Chinese).
[48] 朱清清. 表面活性对土壤中重金属污染的去除研究[D]. 上海: 东华大学, 2011. ZHU Q Q. Study on the removal of heavy metals from soils by surfactants[D]. Shanghai: Donghua University, 2011 (in Chinese).
[49] 王美娜, 王瑞娟, 王毅琳. 表面活性剂体系在水溶液中的聚集行为与液液相分离[C]//中国化学会. 第十七届全国化学热力学和热分析学术会议论文集. 中国科学院化学研究所, 2014: 2. WANG M N, WANG R J, WANG Y L. Aggregation Behavior of Surfactant Systems in Aqueous Solutions and Liquid-Liquid Phase Separation [C] // Chinese Academy of Sciences The 17th National Conference on Thermodynamics and Thermal Analysis of the Chinese Chemical Society Proceedings. Institute of Chemistry, 2014: 2.
[50] YAMAGUCHI S, KUNIEDA H. Determination of a three-phase Tie triangle (the hydrophile–lipophile balance plane) in a composition tetrahedron: evaluation of the composition of adsorbed mixed-surfactant and the monomeric solubilities of short-chain surfactant[J]. Langmuir, 1997, 13(26): 6995-7002. doi: 10.1021/la970413m [51] SHALVIRI A, SHARMA A C, PATEL D, et al. Low-surfactant microemulsions for enhanced topical delivery of poorly soluble drugs[J]. Journal of Pharmacy & Pharmaceutical Sciences, 2011, 14(3): 315-324. [52] ZHANG H X, ZHU Z X, WU Z X, et al. Investigation on the formation and stability of microemulsions with Gemini surfactants: DPD simulation[J]. Journal of Dispersion Science and Technology, 2023, 44(4): 698-707. doi: 10.1080/01932691.2021.1961588 [53] LIU L, LIU X L, HAN Y, et al. Emulsion polymerization of styrene with amphiphilic random copolymer as surfactant: Predominant droplet nucleation[J]. Journal of Applied Polymer Science, 2009, 113(6): 4023-4031. doi: 10.1002/app.30483 [54] WU J, MEI P, LAI L. Microemulsion and interfacial properties of anionic/nonionic surfactant mixtures based on sulfonate surfactants: The influence of alcohol[J]. Journal of Molecular Liquids, 2023, 371: 120814. doi: 10.1016/j.molliq.2022.120814 [55] 李旬强. 正丁酸作为助表面活性剂形成的微乳液及其增溶性能研究[D]. 济南: 山东师范大学, 2011. LI X Q. Study on microemulsions formed by normal butyric acid as co-surfactant and its solubilization performance[D]. Jinan: Shandong Normal University, 2011 (in Chinese).
[56] CALLENDER S P, WETTIG S. Phase behavior of non-ionic surfactant-medium chain triglyceride-water microemulsion systems[J]. Journal of Surfactants and Detergents, 2021, 24(4): 603-629. doi: 10.1002/jsde.12510 -






 DownLoad:
DownLoad: