-
离子型稀土矿浸出液中含有Pb2+、Cd2+、Mn2+、Zn2+、Cu2+、Fe2+、Ni2+等多种重金属离子[1]. 原地浸矿工艺中,浸矿剂在雨水的冲刷下将携带稀土和重金属离子进入下游水体[2]. 这些含有重金属的废水如果处理不当将进一步导致地下水的污染,从而影响生态系统的稳定以及人类的健康[3].
常见的处理重金属废水方法包括化学沉淀法,膜分离法和吸附法[4]. 其中吸附法因其简单、低成本、有效和环保性等优点而被广泛应用[5 − 6]. 生物炭来源广泛、制备简单、具有多孔结构、较大比表面积和丰富的表面官能团,是良好的吸附材料[7 − 8],被广泛用于有毒元素污染水体的修复与治理. 水葫芦,学名凤眼莲(Eichhornia crassipes),生长繁殖速度极快,易大面积覆盖水面,从而限制水体流动,消耗水中溶解氧,破坏河道生态环境并影响水质,是我国最具侵略性的物种之一. 但其富含纤维素和木质素,热解而成的生物炭具有更多的表面官能团,具有价格低廉、原料易获取、吸附效果好、环境友好等多重优点,是较为理想的生物炭原料,合理利用水葫芦能够在一定程度缓解水生态环境的治理压力.
原始的水葫芦生物炭(WHBC)对重金属的吸附能力有限,所以需要寻求有效的改性手段增加其吸附能力. 研究表明,使用化学活化剂可有效改善生物炭的表面官能团以及增加活性位点[9]. 目前应用比较广泛的化学活化剂有氢氧化钠[10]、氢氧化钾[11]、磷酸[9]和氯化锌[12]等,但是上述活化剂在使用过程中可能会产生酸碱损坏设备和重金属析出等弊端. 因此,亟需选用更合适的化学活化剂并改善制备条件来提升生物炭对Pb2+和Ni2+的吸附效果. 碳酸钠是一种环保性能较好的原料物质,用其作为生物炭改性的化学活化剂,具有安全、简便且低成本的优点. 响应曲面法是一种统计工具,可以高效地评估各种因素的交互效应. Box-Behnken(BBD)设计,中心复合设计和三水平因子设计是最常用的用于设计响应曲面法的方法[13]. 其中,BBD实验设计可以简化实验方案,且结果准确度较高[14],已广泛应用于多种生物炭的制备[15 − 16].
本研究以水葫芦为对象,碳酸钠为化学活化剂制备,采用响应曲面法中的BBD设计优化水葫芦生物炭的制备条件,得到性能最优的改性水葫芦生物炭(SWHBC),用于吸附溶液中的Pb2+和Ni2+,并对其进行表征. 通过吸附实验验证了所制备材料对Pb2+和 Ni2+的吸附能力与吸附机理. 并将SWHBC应用于离子型稀土矿山小流域受污染地表水中重金属离子去除,评估其实际应用效果.
-
水葫芦取自江西省赣州市某池塘,将取回的水葫芦清洗干净并去掉根部,烘干粉碎后备用. 实验试剂包括碳酸钠(Na2CO3)、六水合氯化镍(NiCl2·6H2O)、硝酸铅(Pb(NO3)2)、氢氧化钠(NaOH)、硝酸(HNO3),均为分析纯. 离子型稀土矿山周边受污染的自然水体取自江西省赣州市龙南某矿区.
实验仪器包括扫描电子显微镜(SEM,JSM-IT800,Japan);物理吸附仪(BET,Micromeritics ASAP
2460 ,USA);有机元素分析仪(EA,Elementar UNICUBE,Germany);傅立叶红外光谱仪(FT-IR,Nicolet iS5,USA);X 射线粉末衍射仪(XRD,D8 Advance,Germany);电感耦合等离子体发射光谱仪(ICP-OES,PQ9000,Germany). -
采用碳酸钠浸渍法改性水葫芦生物炭. 为确定最优制备条件,本研究利用响应面法(RSM)优化实验条件. 本文选取浸渍质量比(Na2CO3/WH,g·g−1,0.5—1.5)、加热温度(300—600 ℃)和加热时间(2—3 h)的3个变量[15 − 17]并通过单因素实验指导后续关于响应面浸渍质量比,加热温度以及加热时间的实验参数设计. 将10 g干燥并粉碎的水葫芦与一定质量的碳酸钠充分混合后加入100 mL超纯水,搅拌均匀后浸渍24 h. 之后在烘箱中以105 ℃的温度烘干备用. 将预处理的水葫芦在管式炉中进行高温热解制备生物炭,以5 ℃·min−1的加热速率加热到指定温度并保持一定的时间,期间持续通入氩气. 在生物炭冷却至室温后用石英研钵研磨充分并洗涤过滤,直至滤液pH恒定,放入烘箱烘干备用.
分别通过加热时间、加热温度及浸渍质量比3组单因素实验,确定单因素下各个制备条件的最佳参数,之后使用Box-Behnken(BBD)设计实验并分析上述3个因素影响改性生物炭材料吸附Pb2+和 Ni2+的主效应和交互作用.
-
通过分批实验,对所有制备的水葫芦生物炭的吸附性能进行研究. 所有吸附实验材料的投加量均为1 g·L−1. 在批量实验中,将0.02 g生物炭和20 mL的
1000 mg·L−1Pb2+溶液和200 mg·L−1的Ni2+溶液加入到50 mL的离心管中. 溶液在室温下以200 r·min−1的速度振荡12 h. 用0.1 mol·L−1的硝酸和氢氧化钠溶液调整溶液的pH值. 吸附实验结束后的溶液经0.45 μm滤膜后,使用ICP-OES测定溶液中剩余重金属离子的浓度.溶液初始pH的影响. 调整初始溶液至pH3—7进行吸附实验,之后测量剩余重金属离子的浓度.
吸附动力学. 采用拟一级(1) 和拟二级(2)动力学方程[18]对吸附动力学数据进行分析:
式中,
qe 和qt (mg·g−1)分别为平衡时和t (h) 时材料对重金属的吸附量,k1(min−1)和k2[g·(mg·min) -1]分别为对应拟一级模型和拟二级模型的速率常数.等温吸附. 采用Langmuir模型(3)和 Freundlich模型(4)[19]对等温吸附数据进行拟合,公式如下:
式中,
Ka 为Langmuir常数,KF 为Freundlich常数,n 为吸附过程中强度变化指数和吸附偏差指数.Qm 表示Langmuir最大吸附容量(mg·g−1).竞争吸附. 分别在Ni2+浓度固定为100 mg·L−1的不同浓度Pb2+溶液,以及Pb2+浓度固定为500 mg·L−1的不同Ni2+浓度溶液中进行等温吸附实验,使用Langmuir模型和Freundlich模型进行拟合.
-
实际离子型稀土矿山地表水对SWHBC材料的吸附性能进行评价:分别将0.01 g、0.02 g、0.04 g和0.1 g的 SWHBC 和20 mL实际离子型稀土矿山地表水置于50 mL离心管中进行吸附实验.
-
通过一系列表征研究了碳酸钠对水葫芦生物炭性状的影响. 利用扫描电子显微镜(SEM)对材料的表观形貌特征进行了分析; 使用物理吸附仪(BET)分析材料的比表面积和孔径; 利用有机元素分析仪(EA)分析材料的元素组成;通过傅立叶红外光谱仪(FT-IR)来分析材料表面官能团以及吸附重金属前后表面官能团的变化;材料表面的晶体结构采用X 射线粉末衍射仪(XRD)进行分析.
-
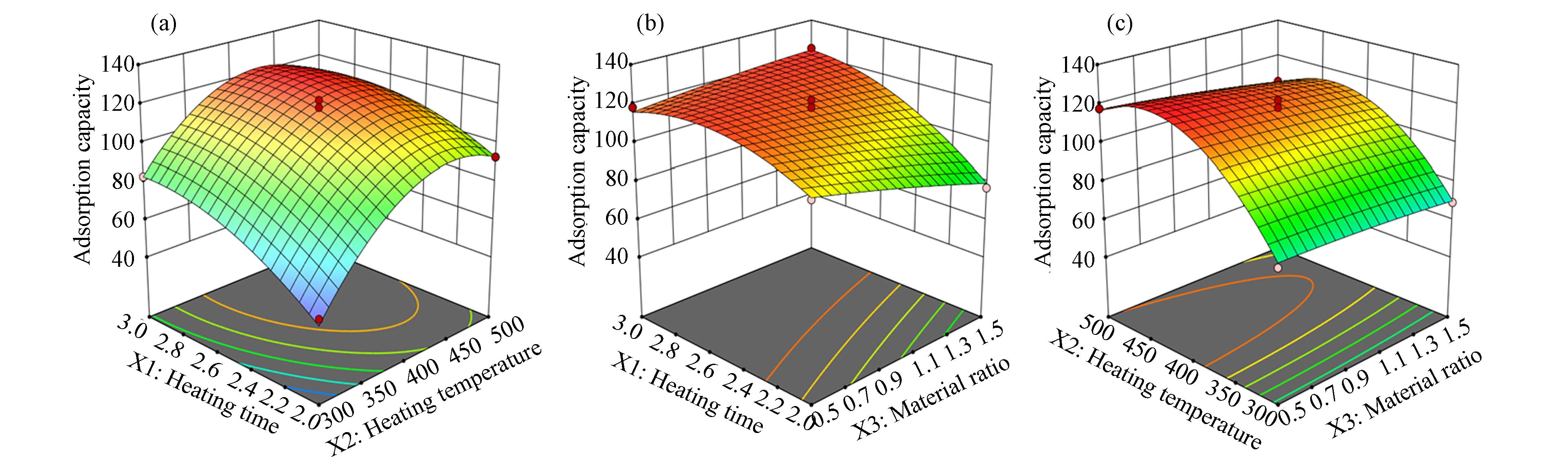
加热时间(X1)对SWHBC吸附性能的影响. 为探究加热时间对SWHBC性能的影响,在加热温度为500 ℃、浸渍质量比为1的条件下,在1—3 h的加热时间范围内进行了试验. 结果如图1(a)所示,在其他条件不变的情况下,随着加热时间的增加,材料对 Pb2+和 Ni2+的吸附效果先增加后减小,在2.5 h时达到最大值. 所以选择加热时间2.5 h作为优化实验的中心值.
加热温度(X2)对SWHBC吸附性能的影响. 加热温度在 300—600 ℃范围内,浸渍质量比为1,加热时间为2.5 h. 结果如图1(b)所示, 在加热温度为400 ℃时,材料对Pb2+和 Ni2+的吸附量均达到最大值,所以选择 400 ℃ 作为优化实验的中心值.
浸渍质量比对(X3)对SWHBC吸附性能的影响. 浸渍质量比在0.5—2之间,保持加热温度为400 ℃,加热时间为2 h. 结果如图1(c)所示,在浸渍质量比(Na2CO3/WH,g·g−1)为1时,吸附量达到最大值,因此选择1作为浸渍质量比的中心值进行优化设计实验.
-
根据单因素实验结果,通过Design-Expert 13软件使用Box-Behnken Design设计并制备了17组水葫芦生物炭样品并测试了其对 Pb2+和 Ni2+的吸附性能. 之后使用响应曲面法预测制备的最优条件和制备条件之间的相互作用,采用了等式中所示的二阶回归方程(5):
式中,Y为预测响应值;
β0 为常数;其中,βi 、βii 、βij 分别为线性效应系数、二次效应系数和交互效应系数;ε 为随机误差;Xi 和Xj 为独立因子的无量纲编码预测因子.实验结果见表1,表中的编码值−1、0和1分别代表每个因素的低、中、高水平. 根据实验结果,得到对响应值为Pb2+吸附能力的
Yq1 的二阶回归方程(6)和响应值为Ni2+吸附能力的Yq2 的二阶回归方程(7).采用二次回归模型分析实验结果的方差,P值<0.05,F值越高,则说明模型的适用性好[20]. 表2为响应值为Pb2+吸附量的方差分析. 从表2中可以看出,P值<
0.0001 ,F值=36.87,说明该模型非常适合本实验. 模型拟合的相关系数R2 =0.9793 、R2adj =0.9528 和R2pre = 0.8076.R2adj 和R2pre 的差值小于0.2,则表明实验数值和预测数值较吻合[21]. 模型的信噪比为22.7587 ,均远高于4,表明二次回归模型与实验结果吻合较好[22]. 变异系数CV为5.62%<10%,该模型拟合较好,实验可信度和精度较高[23].各影响因子的P值可以检验该因素对实验的显著性. P值<0.0001 表现为非常显著,P值>0.05 则表现为不显著[24]. 由表2可知,加热温度和加热时间对材料Pb2+的吸附量影响一般显著和非常显著,浸渍质量比的影响不显著. 加热时间1和加热温度2以及加热时间1和浸渍质量比3的交互影响为一般显著,加热温度2和浸渍质量比3的交互影响为不显著. 根据P值大小分析,碳酸钠改性水葫芦生物炭对吸附Pb2+性能的影响因素有:X2>X1>X3,相互作用项的影响为:X1X2>X1X3>X2X3.响应值为Ni2+吸附量的方差分析结果如表3所示. 模型的P值<
0.0001 ,F值为67.33,且R2=0.9886 、R2adj =0.9739 和R2pre =0.8951 均表明该模型的适用性. 并且该模型的信噪比为28.0627 ,变异系数CV为3.58%,均符合要求. 加热时间和加热温度对材料吸附Ni2+的能力表现为非常显著,浸渍质量比表现为一般显著. 加热时间和加热温度以及加热时间和浸渍质量比的交互影响为一般显著,加热温度和浸渍质量比的交互影响为不显著. 碳酸钠改性水葫芦生物炭对吸附Ni2+性能的影响因素有:X2>X1>X3,相互作用项的影响为:X1X3>X1X2>X2X3. -
通过二次回归模型,图2为 Pb2+吸附能力为响应值,加热时间(X1)、加热温度(X2)以及浸渍质量比(X3)3种制备条件相互作用的三维响应面图. 从图2(a)可以看出,随着加热时间和加热温度的增加,吸附能力先增加,然后下降. 加热温度、加热时间以及二者的交互作用都是显著的. 图2(b)可以看出,浸渍质量比的影响比较小,与方差分析的结果一致. 图2(c)可以看出,加热温度的影响是显著的.
图3为Ni2+吸附能力为响应值,加热时间、加热温度以及浸渍质量比3种制备条件相互作用的三维响应面图. 图3(a)和(c)可以看出加热温度、加热时间以及二者的交互作用的影响是显著的,曲面坡度越陡反映其影响越显著. 图3(b)可以看出加热时间和浸渍质量比之间的交互作用是显著的.
根据不同的最优条件,对Pb2+吸附量和Ni2+吸附量两种单独响应进行了优化. 最佳的Pb2+吸附和Ni2+吸附条件可能是相互影响的. 因此,需要在两个响应的最佳条件之间做出选择. 由于Pb2+污染在离子型矿山开采中污染较大,并且由响应面分析3种制备因素对2种响应值的影响较为相似,因此本研究主要考虑优化Pb2+吸附量. 根据Design-Expert 13软件预测在加热时间为2.90 h,加热温度为 421.79 ℃,浸渍质量比为1.41时,对Pb2+的吸附量为763.86 mg·g−1,在此条件下对Ni2+的吸附量预测值为124.12 mg·g−1. 在此实验条件下进行了3次平行实验,得到对Pb2+的平均吸附量为758.42 mg·g−1,对Ni2+的平均吸附量为118.19 mg·g−1. 误差分别为0.71%和4.77%,与预测值接近.
-
图4 显示的WHBC和SWHBC的SEM图. SEM图像显示WHBC表面光滑,没有孔隙的迹象. 相比之下,SWHBC的表面明显被腐蚀,在表面发现了大量的蚀刻坑,有利于重金属离子进入生物炭的孔隙.
WHBC和SWHBC的元素组成如表4所示. 改性后生物炭的碳和氧元素含量均增加. 生物炭的原子比H/C由原来的0.062减小到0.033,O/C和(O+N)/C比值由0.459和0.498增加到0.587和0.621,表明生物炭的芳香性、亲水性和极性大小均有所增加[6]. 生物炭的含氧官能团和极性的增加都能促进生物炭对重金属污染物的去除[25].
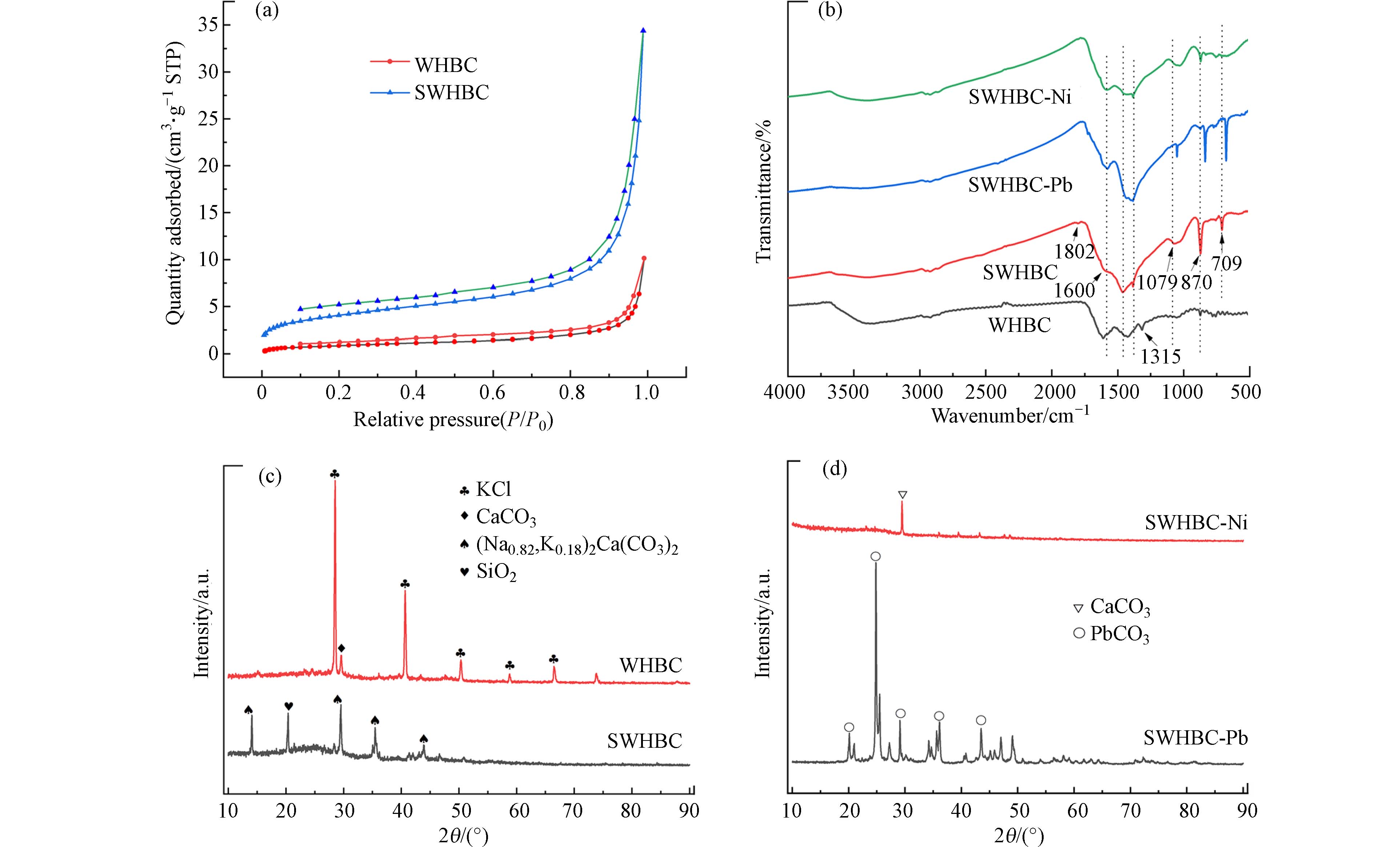
图5(a)显示的WHBC和SWHBC的吸附-解吸等温线. 4种生物炭的吸附-解吸等温线符合典型的Ⅳ吸附等温线H3型滞后曲线,这表明这些孔是介孔的. 根据孔径分布,这些生物炭的平均孔径在2—50 nm范围内,这进一步证实了它们的介孔特性. 由表5可知,改性之后,生物炭的比表面积、总孔体积和微孔体积均有所增加,生物炭的平均孔径减小,这主要是由于热解过程中 Na2CO3与焦油和挥发性物质的结合,从而通过化学活化在通道壁内形成微孔[26 − 27].
吸附剂材料中的表面官能团是影响重金属吸附的主要因素之一[28]. 采用傅里叶变换红外光谱(FTIR)对WHBC 、 SWHBC进行了分析,所得光谱如图5(b)所示.
2860 —2940 cm−1和3410 —3420 cm−1对应于C—H峰和—OH峰的拉伸[29]. 改性后,材料在1315 cm−1和1616 cm−1处—CH3和羰基中C=O的振动峰[30]消失,在1079 cm−1出现的新峰为酯基和羧基等有机化合物的C—O伸缩[31]. 在约1600 cm−1处是羧基的C=O振动峰[32]. 生物炭中的羧酸和酯等含氧官能团表现出对重金属的吸附能力[6]. 在700—900 cm−1处出现了—OH的弯曲峰[33].1381 cm−1和1463 cm−1处出现芳香C=C的峰[34]代表着生物炭芳香性的增加.C—N键出现在1385 cm−1处[35]. 含氮官能团和羧基等官能团均为极性官能团,红外光谱的结果与元素分析一致. 吸附后,—OH、C=C、C—O等结构的红外峰均出现了偏移或减弱,表明这些表面官能团均参与了吸附过程.WHBC和SWHBC的XRD光谱图如图5(c)所示. 改性前,28.315°、40.474°、50.129°、58.573°、66.311°处的峰与KCl相匹配(PDF 97-024-0503). 29.623°处的峰线对应于CaCO3的衍射峰(PDF 97-000-0150). 改性后,13.888°、29.274°、35.341°、42.531°处的峰与Nyerereite矿石[(Na0.82K0.18)2Ca(CO3)2,PDF 97-010-0085]的特征峰相匹配. Nyerereite是一种首次在火山矿石中发现的碳酸盐矿物,其在温度为300—500 ℃条件下生成[36 − 37]. 图5(d)中,吸附结束后该矿物成分消失,生成了PbCO3和CaCO3,表明吸附过程通过碳酸盐与重金属离子发生了离子交换和共沉淀作用.
-
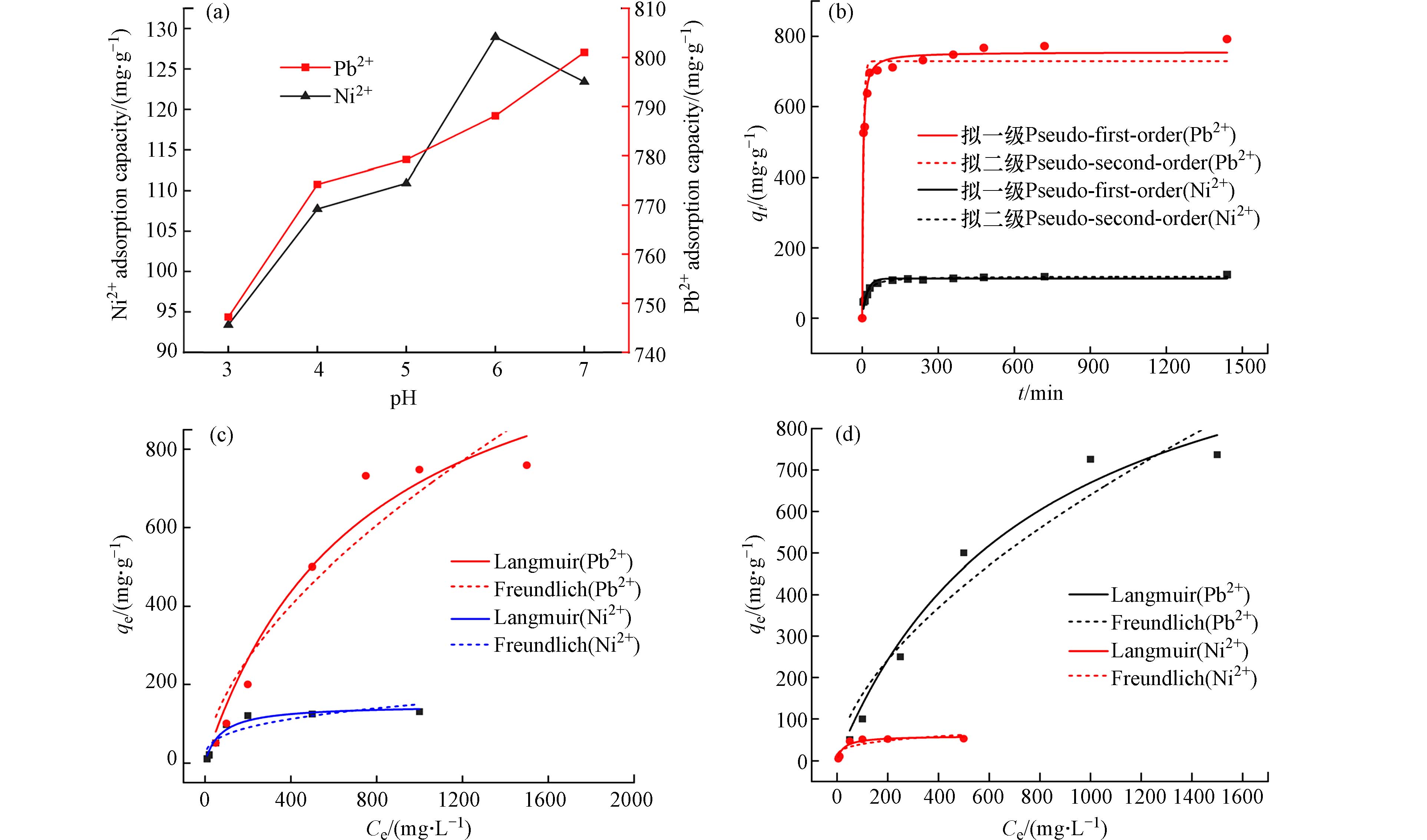
图6(a)为不同初pH下SWHBC 对重金属离子的吸附效果. 随着pH从3增加到7,生物炭对Pb2+的吸附效果逐渐增加,对Ni2+的吸附效果先增加后减小并在pH为6时达到最大值. 这是由于在酸性条件下H3O+与重金属离子在水溶液中产生了竞争[30]. 表现为酸性环境下SWHBC对Pb2+和Ni2+的吸附能力较差. 随着pH值的增加,脱质子作用的增强降低了竞争吸附. 随着pH继续增加,溶液中的OH−的增加影响了材料对Ni2+的吸附. 考虑到pH为7时,Pb2+会沉淀,因此SWHBC对Pb2+和Ni2+的最佳吸附pH为6.
SWHBC对Pb2+和Ni2+的吸附动力学如图6(b)所示. 在前2 h,由于生物炭表面有大量的吸附位点,生物炭对Pb2+和Ni2+的吸附量急剧增加,之后随着吸附位点的减少吸附速率下降直至达到吸附平衡. 生物炭对Pb2+和 Ni2+吸附动力学的拟合参数如表6所示,拟二级动力学模型对SWHBC吸附Pb2+和Ni2+的过程拟合更好,说明生物炭吸附 Pb2+和 Ni2+的过程以化学吸附为主[38]. 同样,拟二级模型对Pb2+和Ni2+的平衡吸附能力计算值分别为754.95 mg·g−1和118.999 mg·g−1,这些结果与吸附实验(758.42 mg·g−1和 118.19 mg·g−1)基本一致.
采用非线性Langmuir 模型和非线性Freundlich 模型拟合了SWHBC 对Pb2+和Ni2+的吸附等温线,模型的拟合曲线和相关如图6(c)和表7所示. 如图6所示,随着Pb2+和Ni2+的浓度增加,材料的吸附量急剧增加,之后趋于稳定. 等温吸附模型得出SWHBC对Pb2+和 Ni2+的最大吸附量分别为
1247.085 mg·g−1和147.091 mg·g−1. 分析材料吸附Pb2+的Langmuir和Freundlich模型相关系数,可知两个模型对SWHBC 吸附Pb2+的吸附平衡特性均能很好的描述. 表明生物炭对Pb2+的吸附是单层吸附和多层吸附共同作用的[39]. 而Langmuir模型和SWHBC吸附 Ni2+的特性更加拟合,表明SWHBC对于Ni2+的吸附更趋向于单层吸附.多金属的吸附等温线拟合和相关系数如图6(d)和表7所示,离子之间的竞争影响了所有重金属的吸附. 与单金属吸附相比,多金属吸附等温线的初始线性部分更短. 在多金属体系中,SWHBC对Pb2+和Ni2+的最大吸附量分别减小为
1195.75 mg·g−1和59.101 mg·g−1. 相比于单金属体系,多金属体系下对Pb2+的最大吸附量略微减小,对Ni2+的最大吸附量大幅降低,表明吸附选择顺序是Pb2+>Ni2+,具有一定的吸附选择性.由各种原材料制备并改性的生物炭及其对Pb2+和Ni2+的最大吸附量见表8. 通过比较可以看出,相比已经报道的文献,利用碳酸钠改性水葫芦制备的生物炭对水中Pb2+和Ni2+的吸附容量分别为
1247.085 mg·g−1和147.091 mg·g−1,具有明显的优势. SWHBC对Pb2+和Ni2+的吸附容量比未改性的水葫芦生物炭以及其他改性的生物炭都要大. 由此可见,就吸附容量而言,SWHBC是具有一定优势的. 因此,SWHBC是一种去除水中Pb2+和Ni2+污染的有效潜在吸附剂. -
离子型稀土开采时,通常使用硫酸镁和硫酸铵作为浸矿剂[47]. 实际离子型矿山周边水体中含有NH4+N、Pb、Ni、Mg、Mn、Fe、Zn、Cu等离子. 采集的实际水体中氨氮的浓度为159.76 mg·L−1,pH为3.64. 这些金属阳离子和较低的pH阻碍了吸附剂对目标重金属的吸附. 所以需要增加投加量来控制目标污染物的浓度. 表9为不同投加量的SWHBC对实际离子型稀土矿山地表水的处理效果. 材料投加量为5 g·L−1时,Pb2+、 Ni2+、Cu2+、Fe2+和Zn2+的去除率达到了99.98%、88.77%、96.38%、99.20%和96.55%. 吸附后Pb2+和Zn2+的浓度达到了《地表水环境质量标准》(GB3838—2002 )Ⅰ类水标准. Cu2+的浓度达到了《地表水环境质量标准》(GB3838—2002 )Ⅱ类水标准. Fe2+的浓度达到了集中式生活饮用水地表水源地补充项目标准限值. Ni2+的浓度虽然未达标集中式生活饮用水地表水源地特定项目标准限值,但是其浓度较低,对地下水污染较小. 对 Mn2+的去除率为65.93% ,但溶液中剩余Mn2+较多,需要使用额外的处理方法. 以上结果表明,本研究中的SWHBC材料可有效地去除实际离子型稀土矿山地表水中的多种金属离子.
-
从SEM和BET分析结果来看,SWHBC具有更加大的比表面积和更加丰富的孔结构,有利于重金属离子在孔隙中的扩散,但是SWHBC的比表面积增大不明显并且SWHBC的吸附主要是化学吸附,所以孔隙扩散不是主要吸附机理.
由元素分析和红外光谱分析可知,改性后的生物碳的极性和含氧官能团数量均有所增加. 根据相似相溶的原理,极性强的生物炭更容易吸附水中的污染物[25]. 对比图5(b)中SWHBC吸附重金属前后的FTIR光谱图,SWHBC在709 cm−1和870 cm−1处代表的—OH,
1079 cm−1和1600 cm−1处代表C—O和C=O以及在1385 cm−1处的C—N在吸附重金属后发生了偏移和减弱. 官能团的变化涉及表面络合机制,这是由于重金属离子与生物炭所形成的络合物会改变官能团周围的化学环境,从而导致红外光谱官能团的位移和峰强度的变化[6],这表明SWHBC表面存在的羧基和酯基等含氧官能团和极性官能团与重金属产生了络合作用. SWHBC吸附Pb2+和Ni2+后的XRD光谱图如图5(d)所示,材料表面的Nyerereite矿物[(Na0.82K0.18)2Ca(CO3)2]分别转变成PbCO3和CaCO3,说明Pb2+和Ni2+与该矿物发生了离子交换和共沉淀作用.综上所述,碳酸钠在热解过程中促进了生物炭比表面积、孔结构、极性和表面含氧官能团的增加,并且在高温下和材料生成了碳酸盐矿物,通过孔隙扩散,离子交换,共沉淀和表面络合作用吸附重金属离子.
-
(1)采用响应面法-BBD设计优化了碳酸钠改性水葫芦生物炭(SWHBC)的制备条件. 针对Pb2+吸附的SWHBC最佳制备条件为:加热时间为2.90 h,加热温度为421.79 ℃,浸渍质量比为1.41. 其中加热温度对生物炭吸附效果的影响最大,浸渍质量比的影响最小. 采用SWHBC吸附Pb2+和Ni2+,实际吸附量为758.42 mg·g−1和118.19 mg·g−1,与预测值(763.86 mg·g−1和124.12 mg·g−1)的误差为 0.71%和4.77%.
(2)通过吸附实验分析,SWHBC吸附Pb2+和 Ni2+的最佳pH为 6,吸附过程以化学吸附为主,是单层吸附和多层吸附共同作用的. 等温吸附模型得出SWHBC对Pb2+和 Ni2+的最大吸附量分别为
1247.085 mg·g−1和147.091 mg·g−1,并且生物炭对Pb2+表现有明显的吸附选择性. 各种表征表明 SWHBC 吸附Pb2+和Ni2+的机理主要涉及离子交换、共沉淀、表面络合作用和孔隙扩散.(3)SWHBC对实际离子型稀土矿山废水中的多种金属离子具有良好的去除效果,其中对Pb2+和Ni2+的去除率为99.98% 和88.77%,处理后Pb2+的浓度达到了《地表水环境质量标准》(GB3838—2002)Ⅰ类水标准. 因此,碳酸钠改性水葫芦生物炭可作为处理含Pb2+和Ni2+离子型稀土矿山废水的有效吸附剂.
碳酸钠改性水葫芦生物炭及其对离子型稀土矿地表水中Pb2+和Ni2+的吸附
Modification of water hyacinth biochar with sodium carbonate and removal of Pb2+ and Ni2+ from surface water of ionic rare earth mines
-
摘要: 水葫芦制备的生物炭(WHBC)因其多孔结构、丰富的化学表面基团和矿物组成而被认为具有较大的环境修复潜力. 为更大程度提升WHBC对重金属离子的吸附能力,本研究以水葫芦为原料,碳酸钠为化学活化剂,采用浸渍法并在高温下热解得到碳酸钠改性水葫芦生物炭(SWHBC),并以Pb2+和 Ni2+的吸附性能为考察对象,在单因素实验的基础上,采用响应曲面法-Box-Behnken Design(BBD)设计对改性生物炭材料的加热时间、加热温度和浸渍质量比(Na2CO3/WH,g·g−1)等3种基本制备条件进行优化. 结果表明,最佳制备条件是浸渍质量比为1.41、温度为421.79 ℃ 和加热时间为2.90 h. 最优条件下所制备的SWHBC对Pb2+和Ni2+的实际吸附量分别为758.42 mg·g−1和118.19 mg·g−1. 用拟二级动力学模型和Langmuir模型能更好地拟合吸附过程,获得的SWHBC对Pb2+和Ni2+最大理论吸附能力分别为
1247.085 mg·g−1和147.091 mg·g−1. 采用SEM、BET、EA、XRD以及FTIR对WHBC和SWHBC的形貌、比表面积、元素组成、矿物类型和官能团进行表征. 结果表明,碳酸钠在热解过程中产生化学活化促进生物炭比表面积、极性和含氧官能团的增加,通过极性官能团和含氧官能团与重金属的络合作用以及孔隙扩散吸附重金属. 并且碳酸钠和水葫芦中的KCl和CaCO3反应生成的Nyerereite矿物在吸附过程中参与了离子交换和共沉淀作用. 因此SWHBC吸附重金属离子的主要机理包括离子交换、共沉淀、表面络合作用和孔隙扩散. SWHBC对离子型稀土矿山受污染地表水中多种金属离子具有显著去除效果,其中对Pb2+和Ni2+的去除率达到了99.98%和88.77%,处理后 Pb2+的浓度达到了《地表水环境质量标准》(GB3838—2002)Ⅰ类水标准,表明本研究所制备材料是一种去除受污染水体中Pb2+和 Ni2+的有效吸附剂.Abstract: Biochar prepared from water hyacinth (WHBC) is considered to have significant environmental remediation potential due to its porous structure, abundant chemical surface groups and mineral composition. In order to further enhance the adsorption capacity of WHBC on heavy metal ions, water hyacinth was used as the raw material and sodium carbonate as a chemical activator in this study. The sodium carbonate-modified water hyacinth biochar (SWHBC) was obtained through impregnation and pyrolysis under high temperatures. The adsorption performance of SWHBC on Pb2+ and Ni2+ were further investigated and optimized by response surface methodology- Box-Behnken Design (BBD), based on one-way experiment under three basic preparation conditions including heating time, heating temperature and impregnation mass ratio (Na2CO3/WH, g·g−1). The results showed that the optimal preparation conditions were an impregnation mass ratio of 1.41 and heating at 421.79 ℃ for 2.90 hours. The actual adsorption capacities of Pb2+ and Ni2+ by SWHBC prepared under the optimal conditions were 758.42 mg·g−1 and 118.19 mg·g−1, respectively. The adsorption process was better fitted by pseudo-second-order kinetic and Langmuir models, and the maximum theoretical adsorption capacities of SWHBC for Pb2+ and Ni2+ were1247.085 mg·g−1 and 147.091 mg·g−1, respectively. In addition, the morphology, specific surface area, elemental composition, mineral type and functional groups of WHBC and SWHBC were characterized by SEM, BET, EA, XRD and FTIR. The results showed that the chemical activation of sodium carbonate during the pyrolysis process promoted the increase of specific surface area, polarity and oxygenated functional groups of the biochar, which led to the adsorption of heavy metals through complexation with heavy metals and pore diffusion of the polar and oxygenated functional groups. In addition, Nyerereite minerals generated by the reaction between sodium carbonate and KCl and CaCO3 in the water hyacinth were involved in ion exchange and co-precipitation during the adsorption process. Therefore, the main mechanisms of heavy metal adsorption by SWHBC include ion exchange, coprecipitation, surface complexation and pore diffusion. Furthermore, SWHBC has significant removal effects on various metal ions in the polluted surface water of ionic rare earth mine, in which the removal rates of Pb2+ and Ni2+ reached 99.98% and 88.77%, respectively. The treated concentrations of Pb2+ met the standards of Class Ⅰ water quality according to the “Environmental Quality Standards for Surface Water”, which indicated that the SWHBC material is an effective adsorbent for removing Pb2+ and Ni2+ contamination from the wastewater.-
Key words:
- water hyacinth /
- sodium carbonate /
- biochar /
- heavy metal /
- adsorption mechanism /
- response surface methodology.
-
重金属具有毒性强、来源广、易富集且难降解等特征,对环境和人体健康有着间接和直接的危害,其在自然生态系统的分布、迁移转化和毒性效应一直是环境学科研究的前沿热点问题之一[1-5]. 重金属在自然生态系统的分布特征对于深入认知和评估其环境行为和生态效应具有重要的指示意义. 研究表明,沉积物作为水生态系统中重金属主要的汇,可以作为水生态系统中重金属污染程度的“指示剂”[6-8]. 沉积物中的重金属可通过多途径如水动力扰动、化学和生物方式释放至天然水环境中,对水生生物和人类健康造成潜在和直接的影响甚至是毒性效应 [9-10]. As、Pb、Hg、Cd、Cr、Cu 是《土壤环境监测技术规范》(HJ/T166-2004)中监测的重金属,研究表明,这6种金属所造成污染及潜在生态风险更为严重[11-12]. 沉积物中有机物和营养盐是沉积物中重要组成部分,其中有机质对沉积物中重金属及有毒化合物的毒性、环境迁移力及营养盐交换有重要的作用[13-14]. 氮和磷不仅可为水体中浮游生物提供养分,亦可在水体和沉积物中迁移转化,研究表明,沉积物是水体中氮和磷的重要内源[15]. 因此,探究和明确沉积物中重金属、有机质和营养盐的含量特征和潜在风险,将为湖泊水环境污染防控策略提供科学依据.
湖泊对于维护地区生态健康,调节气候并为人类社会提供多种服务,特别是生境脆弱的西北地区,具有重要的作用[16]. 半咸水湖泊,又称为微咸水湖,是指湖水矿化度在1—35 g·L−1的湖泊,半咸水湖泊中鱼类生物量相对淡水湖泊较低,浮游动物与浮游植物占比低于淡水湖泊[17]. 西北地区湖泊多以半咸水湖泊为主,水动力环境较为封闭,地下水排泄能力较弱,易受人类活动和气候变化的影响[18-19]. 宁夏沙湖地处西北内陆干旱荒漠区域,是宁夏最大的天然半咸水湖泊,对于宁夏的生态调控起着不可或缺的作用[20]. 沙湖水生态环境脆弱,具备半咸水湖泊鲜明的特点. 由于补水短缺、水产养殖与旅游开发不合理性等因素,导致过量营养盐进入宁夏沙湖,影响多种元素在沉积物-水界面的分布特性及生物有效性. 重金属吸附在沉积物表面,在特定条件下,会向水体中再度释放,成为潜在污染源,同时对底栖动物产生毒性,对湖泊生态系统产生影响. 当前,针对沙湖的相关研究主要集中于水环境和浮游动植物多样性方面[21-22],这对于评估重金属在典型湖泊湿地的分布特性及风险是不利的. 2014年王春霞等[23]对沉积物重金属分布特征分析,但研究时间较早且未对宁夏沙湖沉积物中重金属污染特征、潜在风险进行分析.
本研究通过监测沙湖表层沉积物的理化指标和重金属含量,分析理化指标和重金属的空间分布特征,运用单因子污染指数法、地积累指数法和潜在生态风险指数法等多种手段对沉积物重金属污染特征进行评价和分析,并通过相关性分析和主成分分析对沉积物中重金属与营养盐相关性及来源解析. 本研究对揭示宁夏沙湖沉积物重金属分布情况,强化污染防治具有重要指导意义.
1. 材料与方法 (Materials and methods)
1.1 研究区域
宁夏沙湖自然保护区(E 106°19′6″—106°24′10″,N 38°45′17″—38°49′42″)位于银川平原中北部,贺兰山东麓的蝶型静水湖泊,堤岸分隔的6个小型湖沼. 水域总面积3498.39 hm2,海拔1093—1102 m. 气候属典型的大陆性半湿润半干旱气候,年平均气温为 9.75 ℃,年降水量为 174.7 mm,多集中在6—9月,年蒸发量为1400.0—1600.0 mm,平均水深2.2 m,最深处为4.0—6.0 m [20]. 宁夏沙湖自然保护区位于银川断陷盆地的中心地带,堆积了大量河湖物质,下伏地层为细沙、黏土和湖相地层. 地势低洼,地面高程1088—1110 m,坡度平缓,沟渠纵横,土壤沼泽化、潜育化和盐渍化现象普遍. 沙湖是具有构造湖和牛轭湖双重特征的湖泊,兼具生物多样性保护、水源涵养、治污纳污、调节绿洲生态和调蓄防洪等多种功能.
1.2 样点的布设和样品采集
根据宁夏沙湖水域特点设置9个采样点:采样点1(S1,1号曝气机),采样点2(S2,2号曝气机),采样点3(S3,3号曝气机),采样点4(S4,新澄清池入水口),采样点5(S5,湖心),采样点6(S6,鸟岛),采样点7(S7,2号桥),采样点8(S8,假日酒店东侧),采样点9(S9,1号拦水坝北侧),如图1所示.
 图 1 宁夏沙湖采样点分布[20]Figure 1. Locations of sampling sites in Sand Lake of Ningxia
图 1 宁夏沙湖采样点分布[20]Figure 1. Locations of sampling sites in Sand Lake of Ningxia于2018年4月18日(春)、7月22日(夏)、10月25日(秋)、2019年1月23日(冬)使用彼得森采泥器(PSC-1,采泥面积1/40 m2)采集表层沉积物(深度约为25 cm),用GPS导航定位采样点,确保采样地点相同. 样品采集时间为早上8:00—11:00. 每个采样点采集3个平行样品,去除动植物残体及石块,混合后装入自封袋带回实验室,−20 ℃保存. 采集的沉积物置于阴凉通风的地方阴干、混匀,研磨后过100目筛后备用.
1.3 检测方法
根据《土壤农化分析方法》[24] 中的方法,测定沉积物的 pH、有机质(OM)、总氮(TN)、总磷(TP)、硝态氮(NO3−-N)和总盐的含量. 重金属含量 (As、Pb、Hg、Cd、Cr、和 Cu)按照相关国家标准(GB15618-1995、GB/T17141-1997、HJ491-2019)测定.
1.4 评价方法
1.4.1 单因子污染指数
基于单因子污染指数法评价不同采样点营养盐和重金属污染物超标情况. 公式为:
PIi=Ci/Si PIi是沉积物重金属i的污染指数;Ci是沉积物中重金属i的实测含量;Si 是重金属 i的评价标准含量,本研究采用宁夏沙湖沉积物元素平均值作为标准值[23](表1).
Table 1. Soil background value and toxicity coefficient of heavy metal elements项目Items As Pb Hg Cd Cr Cu 背景值/(mg·kg−1)Background value 11.40 27.10 0.04 0.35 58.10 22.70 毒性系数Toxic coefficient 10 5 40 30 2 5 1.4.2 地积指数评价
运用Muller[26]提出的地理累积指数(Geo - accumulate Index, Igeo)确定宁夏沉积物重金属污染的定量程度,如公式(1):
Igeo=log2[Ci/k×Cn] (1) Ci是重金属含量的实测值;Cn是计算所需的背景值,本研究采用宁夏沙湖沉积物元素平均值作为背景值从而更加真实地反映其污染现状[23],k为1.5;按Igeo可将沉积物污染指数分为以下7类:Igeo<0,清洁;0 ≤ Igeo<1,轻度污染;1 ≤ Igeo<2中度污染;2 ≤ Igeo<3,偏重度污染;3 ≤ Igeo <4 ,重度污染;4 ≤ Igeo<5,严重污染;≥ 5极严重污染.
1.4.3 潜在生态风险评价方法
采用Hakanson[27]方法对沉积物重金属污染情况进行潜在生态风险评价,公式如(2)、(3):
Er=Tir×Ci/CiB (2) RI=n∑i=1Eir (3) 其中,Eir是第i种元素潜在生态风险系数;RI是潜在生态风险指数;Tir 是第i种重金属的毒性系数;Ci为沉积物中第i种重金属的实测值;CBi为第i种重金属的背景值. 本研究所采用的重金属背景值和毒性系数见表1. 重金属潜在生态风险程度评价标准见表2.
表 2 沉积物重金属潜在生态风险程度评价标准Table 2. Potential ecological risk assessment indicators and classification in sediment风险指数 Risk index 轻微 Slight 中等 Medium 强 Strong 很强 Very strong 极强 Pole-strength 危害系数(Er) Er﹤40 40 ≤ Er﹤80 80 ≤ Er ﹤160 160 ≤ Er﹤320 Er ≥ 320 生态风险指数(RI) RI﹤150 150 ≤ RI﹤300 300 ≤ RI﹤600 600 ≤ RI﹤1200 RI ≥1200 1.5 数据分析
数据统计和计算使用Excel 2020,显著性分析、相关性分析和主成分分析采用JMP Pro V13.2.0分析,采用Orgin 2021绘图.
2. 结果与讨论 (Results and discussion)
2.1 沉积物理化特征
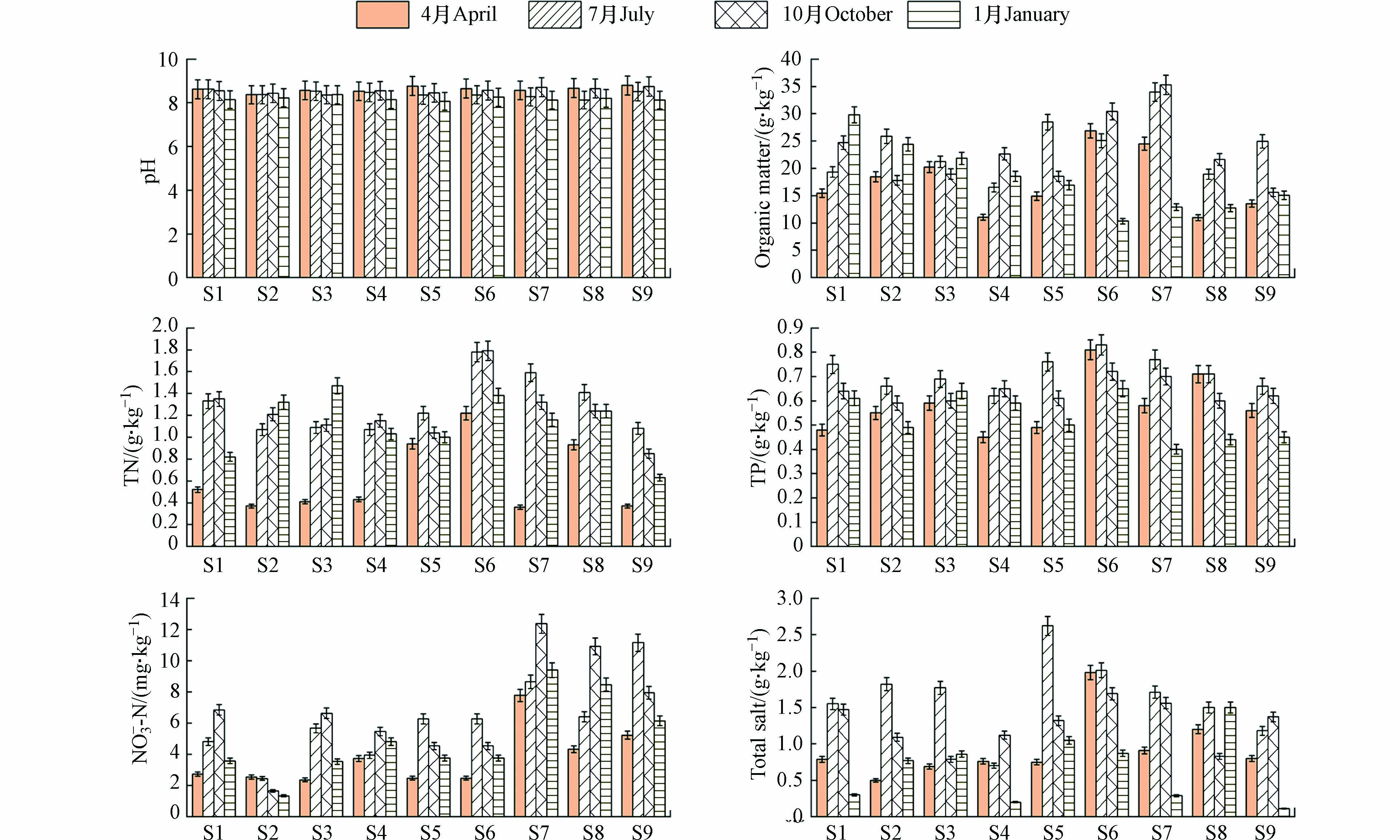
对宁夏沙湖各采样点沉积物理化性质进行分析(图2),结果表明,宁夏沙湖各采样点pH值范围为8.13—8.79,平均值为8.41,呈半碱性,各样点间pH无显著空间分布趋势,在不同季节间无明显差异,说明pH受外界影响较小,主要受湖泊自然运动与沉积作用影响.
OM是营养物质的载体,对氮、磷等营养元素在沉积物中的迁移、矿化起到重要作用[28]. 采样点沉积物中OM含量范围为10.34—35.27 g·kg−1,平均值为20.50 g·kg−1. S7各季节平均值最高,含量为26.66 g·kg−1,S8各季节平均含量最低,含量为16.06 g·kg−1。S7采样点分布大量水生植物,有利于OM富集. 夏季(7月)OM含量最高,含量为23.80 g·kg−1,春季(4月)含量最低,含量为17.34 g·kg−1,表明宁夏沙湖夏季沉积物营养物质丰富,肥力较高. TN变化范围在0.37—1.79 g·kg−1,TN全年平均值分别为1.06 g·kg−1,其中S6各季节平均含量最高,含量为1.54 g·kg−1,S9各季节平均值最低,含量为0.73 g·kg−1 .夏季(7月)TN含量最高为1.29 g·kg−1,春季(1月)含量最低为0.62 g·kg−1. TP范围在0.40—0.83 g·kg−1 之间,平均值为0.62 g·kg−1,其中S6各季节平均含量最高,含量为0.75 g·kg−1 ,S9各季节平均值最低,含量为0.57 g·kg−1. 夏季(7月)TP含量最高,含量为0.72 g·kg−1,春季(4月)含量最低,含量为0.53 g·kg−1. 沉积物中有机氮和有机磷主要来自水体中生物排泄物以及生物残体[28],S6位于鸟岛,生物排泄物较多,并且位于旅游区受人类活动影响较大,S6采样点各季节TN和TN平均值含量较高. 沉积物中OM、TN和 TP含量均在春季最低,夏季最高。因为夏季水温较高,水温是影响沉积物氮和磷释放的关键因素之一,随着夏季水温升高,底栖生物活动加强,增加对底泥扰动,通过发生硝化和反硝化等作用促进沉积物中生物残体向盐类物质转化[29]。在夏季宁夏沙湖有大量外源性氮磷营养盐会随着补水水源进入宁夏沙湖湖区内,而春季补水量减少,入湖外源性氮磷营养盐降低.
沉积物
NO−3 NO−3 NO−3 NO−3 NO−3 根据卞培旺等的研究结果,全盐量越高,腐蚀速率越大[30]. 宁夏沙湖沉积物全盐含量变化范围为0.11—2.62 g·kg−1,平均值为1.12 g·kg−1,S5和S6采样点全盐含量高于其他采样点,分别为1.64 g·kg−1、1.44 g·kg−1,表明该区域底质环境具有一定的腐蚀性. 夏季(7月)全盐含量最高,含量为1.65 g·kg−1,冬季(1月)含量最低,含量为0.66 g·kg−1.
Ji等的研究结果表明,同一湖泊中沉积物理化性质差异主要是受人类活动影响[31]. 本研究中人类活动较为密集的区域(S5、S6和S7)沉积物中OM、TN、TP和
NO−3 NO−3 NO−3 2.2 重金属分布特征及污染评价
2.2.1 沉积物重金属的含量分析
宁夏沙湖沉积物重金属含量特征如表3所示. 所有采样点中,仅S3和S4采样点As含量超过宁夏省潮土土壤重金属背景值,分别是宁夏省潮土土壤重金属背景值的1.01倍和1.08倍. S3、S4、S5和S6采样点As含量超过宁夏沙湖沉积物重金属平均值. 所有采样点中Pb和Cd含量都较高,均超过中国土壤元素背景值和宁夏省潮土土壤重金属背景值[32-33],但所有采样点中Pb低于宁夏沙湖沉积物重金属平均值,S2、S4、S5、S6和S8采样点中Cd含量超过宁夏沙湖沉积物重金属平均值. S1、S7和S8采样点中Hg含量超过中国土壤元素背景值,分别是中国土壤Hg含量背景值的1.23、1.08和1.08倍. S1、S5、S7、S8和S9采样点中Hg含量超过超过宁夏省潮土土壤重金属背景值和宁夏沙湖沉积物重金属平均值. 在所有采样点的沉积物中,Cr均未超过中国土壤元素背景值,仅S1、S3、S6和S8采样点超过宁夏省潮土土壤重金属背景值,S1、S2、S3、S5、S6、S7和S8超过宁夏沙湖沉积物重金属平均值. 所有采样点中只有S3采样点Cu含量超过中国土壤元素背景值,S1、S2、S3和S8采样点Cu含量超过宁夏省潮土土壤重金属背景值,分别是宁夏省潮土土壤重金属背景值的1.19、1.09、1.3、1.24倍. 各个采样点沉积物中6种重金属含量均未超过土壤环境质量农用地土壤污染风险管控标准(GB15618-2018,pH >7.5,田地性质为其他),说明宁夏沙湖沉积物重金属污染程度较轻. S1沉积物中的Hg显著高于其他采样点,S3沉积物中的Cr和Cu显著高于其他采样点,S6沉积物中的Cd显著高于其他采样点(P < 0.05). 整体上看,受人类活动干扰较多的区域S1、S6重金属含量相对较高,王春霞对宁夏沙湖2014年沉积物重金属分布研究结果也支持了本文研究结论[23] .
表 3 宁夏沙湖沉积物重金属含量特征Table 3. Characteristics of the amount of heavymetals in Ningxia Sand Lake采样点Site 指标Index As Pb Hg Cd Cr Cu S1 平均值 /(mg·kg−1) 8.83 18.32 0.08a 0.02 63.74ab 22.21abc 标准差 /(mg·kg−1) 4.07 4.14 0.01 0.01 1.34 3.11 变异系数/% 46.15 22.59 16.01 35.73 2.10 14.00 S2 平均值 /(mg·kg−1) 10.38 20.46 0.03ab 0.41 60.39ab 20.42abc 标准差 /(mg·kg−1) 2.52 3.15 0.02 0.36 2.72 2.42 变异系数 /% 24.29 15.40 66.67 86.15 4.50 11.85 S3 平均值 /(mg·kg−1) 12.65 21.71 0.02b 0.27 66.54a 24.42a 标准差 /(mg·kg−1) 1.52 1.91 0.01 0.16 3.09 4.97 变异系数 /% 11.98 8.82 38.78 55.03 4.64 20.36 S4 平均值 /(mg·kg−1) 13.55 16.61 0.02b 0.45 54.92cd 17.66abc 标准差 /(mg·kg−1) 1.38 2.38 0.01 0.33 4.73 2.99 变异系数 /% 10.17 14.30 59.98 72.83 8.61 16.93 S5 平均值 /(mg·kg−1) 9.81 17.17 0.06ab 0.42 59.06bc 14.67c 标准差 /(mg·kg−1) 3.15 2.87 0.03 0.16 3.30 1.98 变异系数/% 32.07 16.74 47.76 37.76 5.58 13.47 S6 平均值 /(mg·kg−1) 12.20 17.57 0.02ab 0.46a 64.22ab 15.13c 标准差 /(mg·kg−1) 2.91 6.07 0.01 0.18 3.68 1.21 变异系数 /% 23.84 34.52 47.94 17.67 5.73 8.00 S7 平均值 /(mg·kg−1) 11.52 16.92 0.07b 0.19 60.70ab 17.44abc 标准差 /(mg·kg−1) 2.03 6.73 0.04 0.16 2.86 1.79 变异系数/% 17.65 39.77 54.82 85.22 4.72 10.25 S8 平均值 /(mg·kg−1) 10.14 20.88 0.07ab 0.45 63.09ab 23.10ab 标准差 /(mg·kg−1) 2.61 3.28 0.04 0.30 5.40 3.32 变异系数 /% 25.78 15.72 54.82 66.18 8.56 14.38 S9 平均值 /(mg·kg−1) 10.61 19.55 0.04ab 0.11 51.16d 16.70bc 标准差 /(mg·kg−1) 3.74 4.71 0.03 0.078 1.77 4.48 变异系数 /% 35.19 24.08 81.86 68.47 3.46 26.84 中国土壤元素背景值[32] 9.7 7.9 0.065 0.103 66.6 24.1 宁夏省潮土土壤重金属背景值[33] 12.5 11.4 0.032 0.105 61.2 18.7 GB15618-2018 1 20 240 1.0 0.8 350 100 宁夏沙湖沉积物重金属平均值[23] 11.4 27.1 0.04 0.35 58.1 22.7 注:同列平均数后的小写字母不同表示同一种重金属元素在采样点之间存在显著差异(P < 0.05).Different lowercase letters after the mean in the same column indicate significant differences between sampling sites for the same heavy metal element (P < 0.05). 1表示《土壤环境质量标准 农用地土壤污染风险管控标准》(GB15618-2018),pH >7.5,田地性质为其他.Indicates Soil Environmental Quality Standard Soil Contamination Risk Control Standard for Agricultural Land (GB15618-2018), pH > 7.5, and the field nature is other. 湖泊自身环境的差异,加上人类活动干扰等因素影响,不同区域重金属存在一定差异性[34-35] . 结果表明,S1采样点中As的差异性最大,变异系数为46.15%;S2、S3、S4、S7和S8采样点中Cd的差异性最大,变异系数分别为86.15%、55.03%、72.83%、85.22%和66.18%;S2、S4和S9采样点中Hg的差异性最大,变异系数分别为66.67%、59 .98%和81.86%. As、Hg和Cd变异系数较高,说明在空间上分布不均匀[36-37].
宁夏沙湖沉积物中6 种重金属含量均值由高到低顺序为 Cr > Cu > Pb > As > Cd > Hg( 表4) . 沉积物中重金属含量受沉积物理化性质(如:OM、TN、TP、粒径等因素)以及温度等多种因素影响[38]. 结果表明:夏季(7月)和秋季(10月)沉积物中Pb、Hg、Cd、Cr和Cu的平均浓度高于春季(4月)和冬季(1月). 夏季和秋季温度较高,温度较高时加速了沉积物中重金属释放速度. 研究表明OM和TP含量与重金属含量呈正相关[39],但TN含量高时,沉积物吸附重金属量降低. 图2表明沉积物中OM、TN和TP在夏季和秋季含量较高,但TN含量较高时,并没有使得沉积物中重金属吸附能力降低,这可能时因为湖泊之间因所处地理环境存在一定差异. 因此,宁夏沙湖重金属含量呈现不同季节差异与水温、OM、TN和TP有关. 从变异系数来看,春季和夏季变异系数最高的是Cd,其次是Hg,最小的是Cr,表明Cd和Hg含量在春季和夏季沉积物中差异较大. 秋季和冬季变异系数最高的是Cd,其次是Hg,最小的是Cr,表明Hg和Cd含量在秋季和冬季沉积物中差异较大.
表 4 宁夏沙湖沉积物重金属含量季节变化特征Table 4. Seasonal variation characteristics of heavy metal content in sediment of Sand Lake in Ningxia季节 Season 指标 Index As Pb Hg Cd Cr Cu 春季 Spring 最大值 14.60 24.48 0.07 0.64 63.20 20.40 最小值 7.66 11.30 0.01 0.02 49.00 11.90 平均值 /(mg·kg−1) 12.10 18.0 0.03 0.30 57.80 16.00 标准差 /(mg·kg−1) 2.60 3.80 0.0 0.20 5.50 3.10 变异系数 /% 20% 20% 60% 80% 10% 20% 夏季 Summer 最大值 14.01 24.48 0.08 0.94 68.29 29.1 最小值 4.14 14.69 0.01 0.03 50.30 15.80 平均值 /(mg·kg−1) 10.78 20.29 0.05 0.50 62.68 21.43 标准差 /(mg·kg−1) 3.20 3.60 0.0 0.30 5.50 4.80 变异系数 /% 30% 20% 60% 60% 10% 20% 秋季 Autumn 最大值 13.61 25.39 0.09 0.77 70.10 28.4 最小值 7.19 13.96 0.01 0.02 62.07 15.20 平均值 /(mg·kg−1) 10.90 20.10 0.04 0.30 62.60 21.50 标准差 /(mg·kg−1) 2.90 2.90 3.80 0.0 0.20 4.70 变异系数 /% 30% 20% 70% 70% 10% 20% 冬季 Winter 最大值 13.73 22.88 0.09 0.34 65.9 20.8 最小值 5.80 11.23 0.01 0.01 51.96 14.6 平均值 /(mg·kg−1) 10.58 16.82 0.04 0.15 58.60 17.39 标准差 /(mg·kg−1) 3.00 3.00 4.90 0.0 0.10 4.40 变异系数 /% 30% 30% 80% 90% 10% 20% 2.2.2 沉积物重金属单因子污染指数法评价
运用单因子污染指数法,对宁夏沙湖沉积物重金属评价,结果显示(见表5),各采样点6种重金属元素单因子污染指数均小于1,表明沙湖沉积物质量状况良好. 各采样点6种重金属单因子污染指数排序为 Cr > As > Pb > Cd > Cu > Hg,其中Cr的单因子污染指数最大,平均值达到0.89,其次为As和Pb,平均值分别为0.71和0.70,其余重金属单因子污染指数均小于0.7. Cr、Pb和As的单因子污染指数较高,应引起足够重视,加强此类沉积物重金属元素监测.
表 5 宁夏沙湖重金属单因子污染指数Table 5. Single-factor standard index for heavy metals in Ningxia Sand Lake采样点Site As Pb Hg Cd Cr Cu S1 0.57 0.68 0.32 0.04 0.96 0.74 S2 0.67 0.82 0.11 0.83 0.91 0.68 S3 0.82 0.80 0.27 0.57 0.98 0.83 S4 0.87 0.61 0.29 0.98 0.81 0.60 S5 0.63 0.63 0.75 0.85 0.87 0.50 S6 0.79 0.65 0.42 0.92 0.94 0.51 S7 0.74 0.62 0.25 0.38 0.89 0.59 S8 0.65 0.77 0.86 0.91 0.93 0.79 S9 0.93 0.72 0.81 0.32 0.88 0.74 平均值 0.71 0.70 0.42 0.65 0.89 0.64 2.2.3 沉积物重金属地积指数法评价
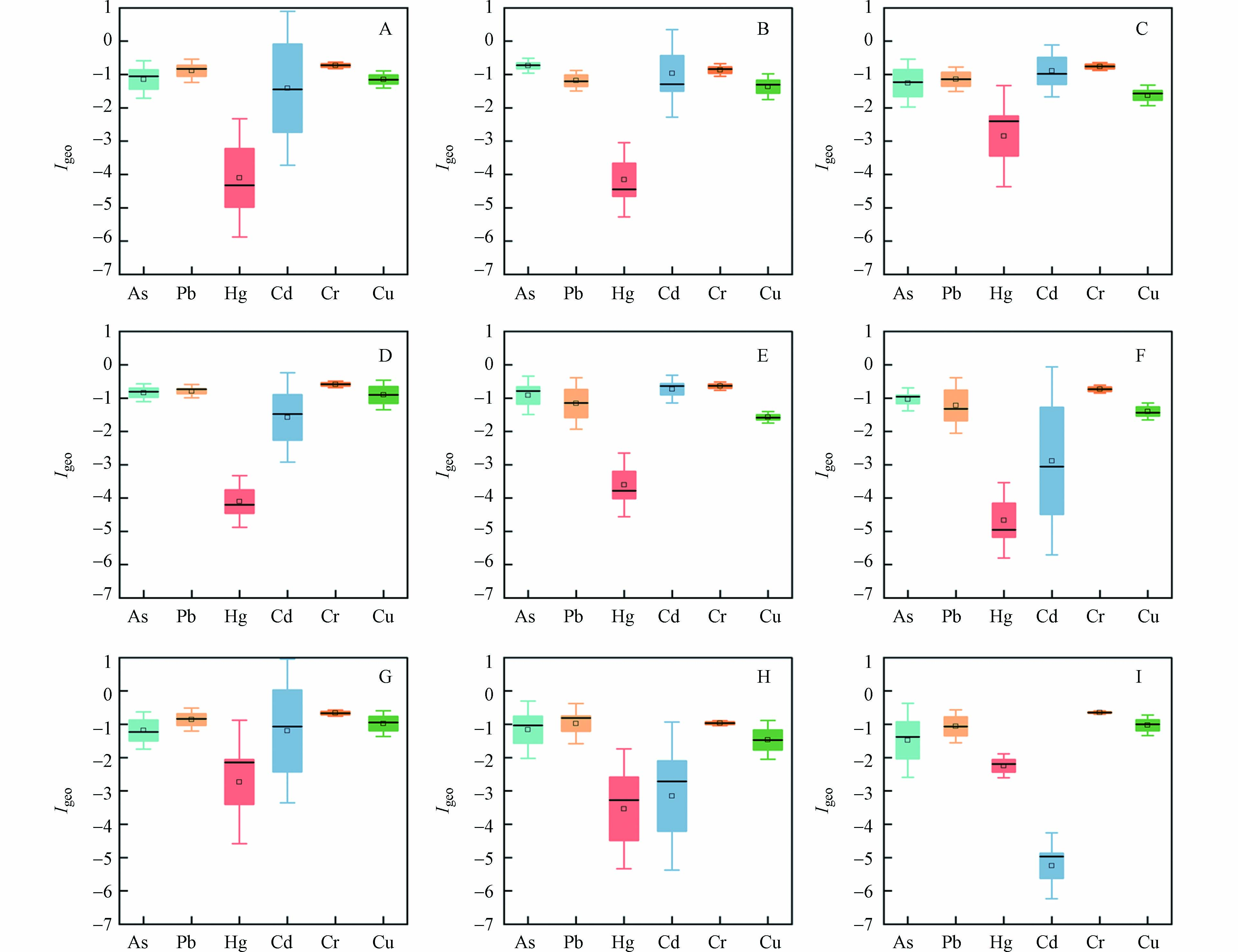
地积累指数对宁夏沙湖沉积物重金属的污染程度进行了评价(图3). S1采样点重金属地积指数排序依次为:Hg > Cr > Cu > Pb > As > Cd;S2采样点重金属地积指数排序依次为:Cr > Cd > Pb > Cu >As > Hg;S3采样点重金属地积指数排序依次为:Cr > Pb > As > Cu > Cd > Hg;S4采样点重金属地积指数排序依次为:Cd > As > Cr > Pb > Cu > Hg;S5和S6采样点重金属地积指数排序依次为:Cr > Cd > Hg > Pb >As > Cu,Cr > Cd > As > Pb >Hg > Cu;S7采样点重金属地积指数排序依次为:Cr > As >Pb > Cu > Cd > Hg;S8采样点重金属地积指数排序依次为:Cr > Cd > Hg > Cu > Pb >As;S9采样点重金属地积指数排序依次为:Cr > Pb > As > Cu > Hg > Cd. 所有地积指数均小于0,污染等级为清洁. 重金属年均值从大到小为 Cr > As > Pb > Cu > Cd > Hg,其中,Cr 地累积指数(-0.76)最大,在宁夏沙湖环境监测工作中需重点关注此金属元素.
空间分布结果为S8(−0.89) > S5(−1.11) > S9(−1.14) > S2(−1.16)> S4(−1.18) > S7(−1.49) > S1(−1.66) > S3(−2.09). S2、S3、S5、S7、和S8沉积物各采样点地积指数差异较小,可以推断,S2、S3、S5、S7、和S8采样点沉积物中的重金属来源相似,其余采样点沉积物中重金属地积指数差别较大,表明重金属来源有所不同.
2.2.4 沉积物重金属潜在生态风险指数法评价
潜在生态风险系数(Er)分析结果(表6),可以看出宁夏沙湖沉积物中Cd和Hg的风险等级最高,Cd处于中等生态风险(40 ≤ Er﹤80),Hg处于强生态风险(80 ≤ Er﹤160),Cd和Hg潜在生态风险系数分别在5.07—108.93和45.83—159.38之间,均值达到了74.98和83.76,其中Cd波动较大. S1和S9采样点中金属Cd潜在生态风险系数指数低于40,处于轻微生态风险(Er < 40),S3和S7处于中等生态风险(40 ≤ Er < 80),S2、S4、S5、S6和S8处于强生态风险. S7采样点中金属Hg潜在生态风险系数指数低于40,处于轻微生态风险,S2、S3、S4和S6处于中等生态风险,S1、S5、S8和S9处于强生态风险. 金属AS、Pb、Cr和Cu处于轻微生态风险(Er﹤40).
表 6 宁夏沙湖沉积物重金属潜在生态风险指数值及污染等级Table 6. Potential ecological risk index values and pollution levels of heavy metals in sediment of Ningxia Sand Lake采样点Site Er RI 危害程度Hazard level As Pb Hg Cd Cr Cu S1 22.77 13.52 159.38 5.07 7.48 15.11 223.32 中等 S2 26.78 15.10 56.93 99.16 7.08 27.78 232.84 中等 S3 32.64 16.03 45.83 68.66 7.81 16.61 187.58 中等 S4 34.96 12.26 46.92 108.12 6.44 12.01 220.72 中等 S5 25.32 12.67 120.36 101.98 6.93 9.98 277.24 中等 S6 31.49 12.97 66.77 109.87 7.53 10.30 238.93 中等 S7 29.74 12.49 39.24 45.71 7.12 11.863 146.17 轻微 S8 26.17 15.41 137.83 108.93 7.40 15.71 311.45 强 S9 27.39 14.43 80.56 27.29 6.00 11.36 167.04 中等 平均值 28.58 13.88 83.76 74.98 7.09 14.52 222.81 中等 贡献率/% 12.83 6.23 37.59 33.65 3.18 6.52 潜在生态风险指数(RI)结果可以得出(表6),宁夏沙湖沉积物中重金属RI值范围为167.04—311.45,均值为 222.81,所有采样点RI值均未超过600,采样点S7处于轻微生态风险(RI < 150),采样点S8处于强生态风险(300 ≤ RI < 600),其余采样点处于中等生态风险(150 ≤ RI < 300).
此外,表层沉积物中重金属Hg和Cd是重金属潜在生态风险的主要来源,贡献率分别达到了37.59%和33.65%. As贡献率达到了12.83%,Pb和Cu贡献了分别为6.23%和6.58%,Cr总贡献率低于4.00%. 在其他湖泊、水库和湿地也发现了类似结果[40-42]. 因此,未来应对宁夏沙湖沉积物重金属污染提高重视,特别是重金属Hg和Cd.
有研究表明采用多种评价方法评价沉积物重金属,能够更好说明沉积物中重金属复合污染特征[43],本研究采用单因子污染指数、地积指数和潜在风险指数综合地积累指数,评价宁夏沙湖沉积物重金属污染级别,整体来看,宁夏沙湖沉积物状态良好,其中Cr、As和Pb单因子污染指数和地积指数相对较高,而潜在风险指数结果与单因子污染指数和地积指数评价略有不同,Cd、Hg和As潜在风险指数较高,已往研究结果也呈现出潜在风险指数评价与单因子污染指数和地积指数评价结果略有不同[11,40,44]. 从空间上来看,三种评价方法均显示S8和S5采样点沉积物中重金属污染指数相对较高.
2.3 重金属、营养盐沉积物来源分析
2.3.1 沉积物重金属、营养盐相关分析
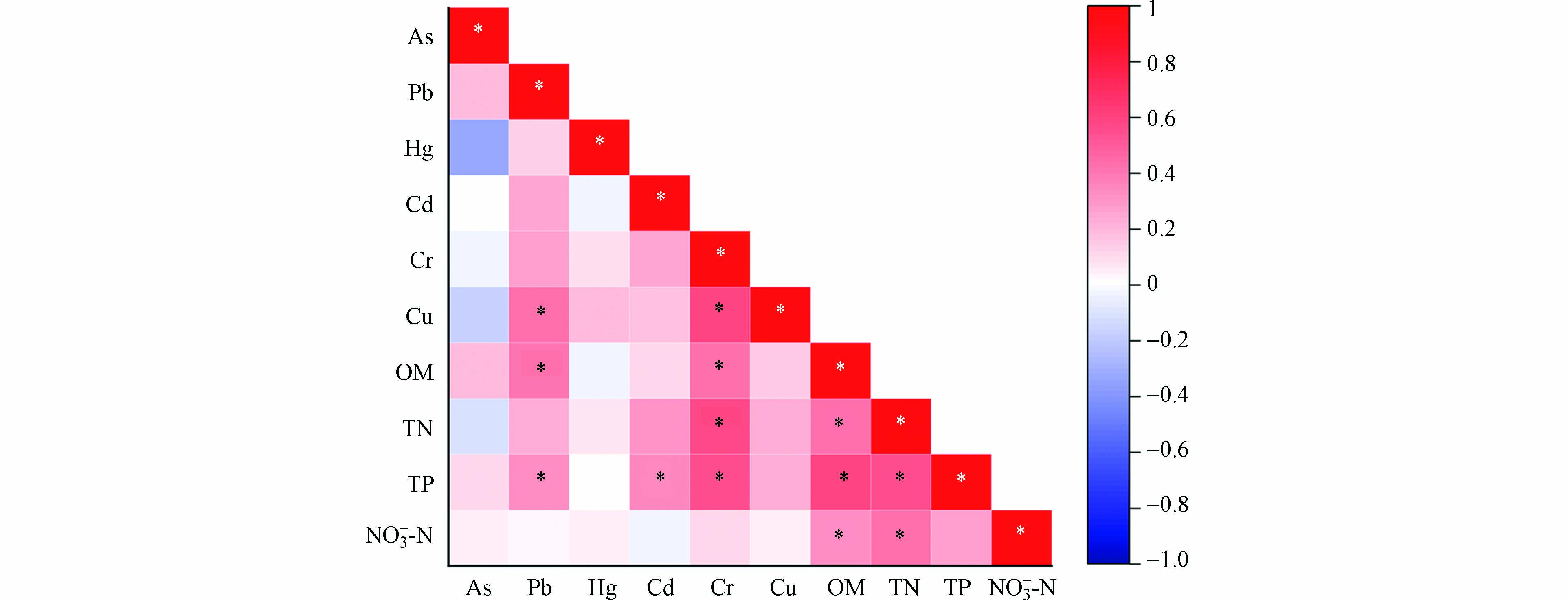
Pearson相关性分析结果如图4所示,结果表明 Cr 与 Cu、OM、TN、TP呈显著正相关(P < 0.05),Cr 与 Cu、OM、TN、TP具有相似的污染来源或产生了复合污染. OM与TN、TP和NO3−-N呈显著正相关(P < 0.05),说明沉积物OM的降解和释放对宁夏沙湖TN、TP和NO3−-N具有重要影响. TP与TN呈显著正相关(P < 0.05),说明TN和TP来源相同. As和Hg与其他元素的相关性都不高. 这表明 Pb、Cd、Cr、Cu、OM、TN、TP 具有相似的污染来源,而As和Hg的污染来源特征可能与自身的物理化学性质以及沉积物中含沙量有关[45].
2.3.2 沉积物重金属、营养盐主成分分析
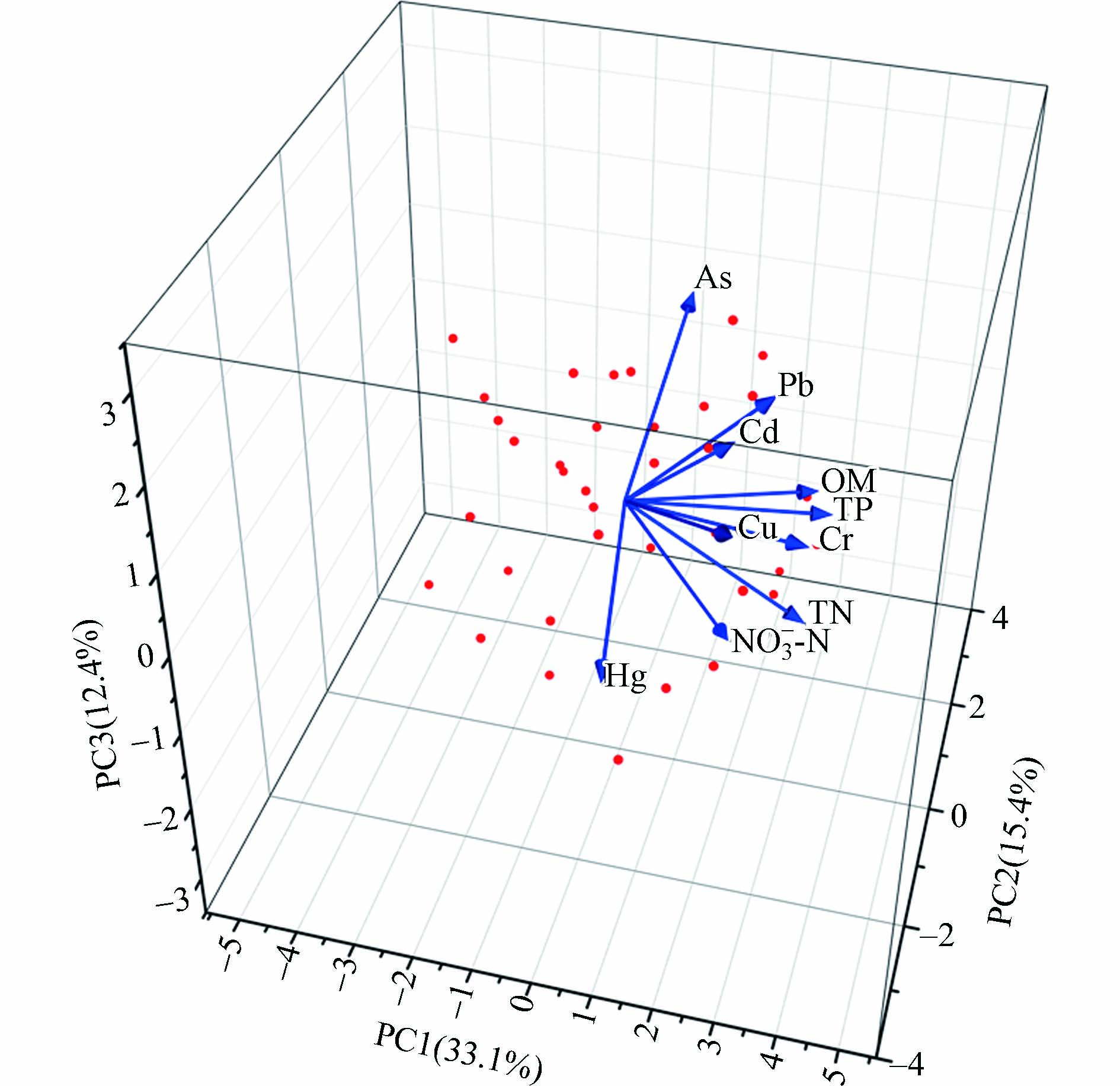
宁夏沙湖沉积物重金属主成分分析结果见表7和图5,前3个成分的方差累积贡献率达60.86%. 主成分1的贡献率是33.09 %,Cr与OM、TP和TN具有高正荷载(载荷 > 0.7),可推测Cr与OM、TP和TN具有强相关,这与Pearson相关性分析结果一致. Pb和Cu具有较高正载荷(载荷 > 0.5)推测这2种重金属具有相同的来源. 有研究表明重金属Pb和Cu含量主要来源于交通运输[46]和人类活动有关[47-48],沙湖大部分区域处于旅游区,交通和人类活动频繁,可能会造成沉积物中重金属Pb和Cu含量累积. 因此,重金属Pb和Cu主要来源于交通运输和人类活动. 宁夏沙湖中所有采样点Cr含量均低于中国土壤元素背景值,变异系数较低,且地累积指数处于清洁水平,推测宁夏沙湖沉积物中Cr可能与自身理化性质有关,属于自然来源. 因此在本研究中主成分1代表该轴的重金属主要来源于人类活动和自然来源. 主成分2的贡献率是15.40%,其中As具有高载荷(> 0.7),地累积指数评价结果显示宁夏沙湖沉积物的重金属As处于清洁水平,推测As属于重金属的自然来源,成分2重金属也来源于自然来源. 主成分3的贡献率12.37%,所有元素载荷均小于0.5.
表 7 宁夏沙湖沉积物重金属主成分载荷分布Table 7. Principal component load distribution of heavy metals of Ningxia Sand Lake元素Elements 因子载荷Factor loadings 因子1 Factor 1 因子2 Factor 2 因子3 Factor 3 As 0.0468 0.7579 0.3455 Pb 0.5755 0.0071 0.4928 Hg 0.1248 −0.6738 −0.1809 Cd 0.4328 −0.0163 0.3106 Cr 0.7798 −0.2011 0.0990 Cu 0.5531 −0.5078 0.3273 OM 0.7060 0.3543 −0.0946 TN 0.7545 −0.0064 −0.3676 TP 0.7959 0.1970 −0.0640 NO3−−N 0.3967 0.2198 −0.6927 特征值 3.3088 1.5396 1.2371 贡献率/% 33.0881 15.3964 12.3712 累计贡献率/% 33.0881 48.4844 60.85559 3. 结论 (Conclusion)
(1)宁夏沙湖的OM、TN、TP、NO3−-N和全盐年平均值分别为20.50 g·kg−1、1.06 g·kg−1、0.62 g·kg−1、5.8 mg·kg−1和1.12 g·kg−1. 在人类活动密集区(S5、S6和S7)沉积物中有机质和营养盐高于其他区域,人类活动影响宁夏沙湖沉积物有机质和营养盐的空间分布. 全盐含量在夏季最高,冬季最低,夏季OM、TN和TP含量最高,春季含量最低,NO3−-N含量在秋季含量最高,春季最低. 水温和外源营养盐输入对宁夏沙湖沉积物有机质和营养盐含量具有重要的调节作用.
(2)单因子污染指数评价结果表明沙湖沉积物质量状况良好,单因子污染指数排序为 Cr > As > Pb > Cd > Cu > Hg,其中Cr单因子污染指数最高,应引起重视并加强日常监测.
(3)沉积物中6种重金属元素年地累积指数值均小于0,污染等级为清洁. 单个重金属年均值从大到小为 Cr > As > Pb > Cd > Cu > Hg,其中Cr 地累积指数最大.
(4)宁夏沙湖沉积物中Cd和Hg的风险等级最高,其中Cd和Cu是造成宁夏沙湖沉积物重金属生态风险的主要重金属. 宁夏沙湖积物中重金属RI值均值为222.81,采样点S7处于轻微生态风险,采样点S8处于强生态风险,其余采样点处于中等生态风险.
(5)相关分析结果表明:Pb、Cd、Cr、Cu、OM、TN、TP 具有相似的污染来源,主要来源是人为来源和自然来源.
(6)生态风险较高的区域主要位于人类活动较密集区域,应加强该区域监测,关注Cr、Pb、Hg和As监测.
-
表 1 Box-Behnken Design实验设计和结果
Table 1. Experimental design and results for Box-Behnken Design
序号Nnmber 编码值Coded levels 制备条件Preparation conditions Pb2+吸附能力/(mg·g−1)Pb2+AdsorptionCapacity Ni2+吸附能力/(mg·g−1)Ni2+AdsorptionCapacity 加热时间/h Heating time (X1) 加热温度/℃Heating temperature (X2) 浸渍质量比/(g·g−1)Material ratio (X3) 1 −1 −1 0 2 300 1 173.70 49.20 2 0 0 0 2.5 400 1 632.90 116.90 3 1 −1 0 3 300 1 479.40 82.90 4 −1 0 −1 2 400 0.5 609.30 105.50 5 0 1 1 2.5 500 1.5 678.00 105.56 6 0 0 0 2.5 400 1 710.20 113.78 7 0 −1 1 2.5 300 1.5 353.30 69.40 8 1 0 1 3 400 1.5 751.80 124.25 9 0 0 0 2.5 400 1 665.60 114.92 10 1 1 0 3 500 1 650.50 106.16 11 −1 0 1 2 400 1.5 546.70 77.07 12 0 1 −1 2.5 500 0.5 647.70 117.76 13 −1 1 0 2 500 1 555.30 93.00 14 0 0 0 2.5 400 1 689.90 118.38 15 0 0 0 2.5 400 1 688.00 122.14 16 1 0 −1 3 400 0.5 641.60 118.44 17 0 −1 −1 2.5 300 0.5 408.40 73.80 表 2 SWHBC 对Pb2+吸附能力的方差分析
Table 2. ANOVA for BBD for adsorption capacity of Pb2+ by SWHBC
方差来源Source of variance 平方和Sum of squares 自由度Degrees of freedom 均方Mean square F值F-value P值P-value 模型 3.544×105 9 39377.58 36.87 < 0.0001 X1-加热时间 50928.36 1 50928.36 47.68 0.0002 X2-加热温度 1.559×105 1 1.559×105 145.94 < 0.0001 X3-浸渍质量比 64.98 1 64.98 0.06 0.8123 X1X2 11077.56 1 11077.56 10.37 0.0146 X1X3 7464.96 1 7464.96 6.99 0.0332 X2X3 1823.29 1 1823.29 1.71 0.2327 X12 9923.62 1 9923.62 9.29 0.0186 X22 1.133×105 1 1.133×105 106.09 < 0.0001 X32 309.78 1 309.78 0.29 0.6069 残差 7476.62 7 1068.09 失拟项 4012.71 3 1337.57 1.54 0.3336 误差 3463.91 4 865.98 总和 3.619×105 16 表 3 SWHBC 对 Ni2+吸附能力的方差分析
Table 3. ANOVA for BBD for adsorption capacity of Ni2+ by SWHBC
方差来源Source of variance 平方和Sum of squares 自由度Degrees of freedom 均方Mean square F值F-value P值P-value 模型 Model 7843.82 9 871.54 67.33 < 0.0001 X1-加热时间 1430.59 1 1430.59 110.52 < 0.0001 X2-加热温度 2707.74 1 2707.74 209.19 < 0.0001 X3-浸渍质量比 192.28 1 192.28 14.85 0.0063 X1X2 105.47 1 105.47 8.15 0.0245 X1X3 293.09 1 293.09 22.64 0.0021 X2X3 15.21 1 15.21 1.18 0.3143 X12 409.51 1 409.51 31.64 0.0008 X22 2537.07 1 2537.07 196.01 < 0.0001 X32 4.62 1 4.62 0.36 0.5692 残差 90.61 7 12.94 失拟项 47.83 3 15.94 1.49 0.3449 误差 42.78 4 10.69 总和 7934.43 16 表 4 WHBC 和SWHBC 的元素组成
Table 4. The element composition of WHBC 和 SWHBC
元素/%Element WHBC SWHBC C 45.27 46.61 H 2.82 2.42 O 20.80 27.39 N 1.73 1.54 S 0.81 0.35 表 5 生物炭的比表面积和孔径参数
Table 5. Specific surface area and pore diameter parameters of biochar
生物炭Biochar 比表面积/( m2 总体积/( cm3 微孔体积/( cm3 平均孔径/nmPore size WHBC 3.2017 0.015705 0.000305 19.6209 SWHBC 13.5641 0.053298 0.002129 15.7175 表 6 生物炭对Pb2+和Ni2+吸附动力学的拟合参数
Table 6. Fitting parameters of adsorption kinetic of Pb2+和 Ni2+onto SWHBC
模型Model 参数Parameters Pb2+ Ni2+ 拟一级模型Pseudo-first-order model Kt(min−1) 0.18913 0.05291 qe 729.055 112.814 R2 0.95891 0.92786 拟二级模型Pseudo-second-order model K2 4.58672 ×10−46.83439 ×10−4qe 754.95 118.999 R2 0.98468 0.9688 表 7 生物炭对Pb2+和 Ni2+的单金属和多金属吸附等温线的拟合参数
Table 7. Fitting Parameters of Monometal and Polymetal Adsorption Isotherms for Pb2+and Ni2+ on Biochar
模型Model 参数Parameters Pb2+ Ni2+ Monometal-Langmuir qe 1247.085 147.091 Ka 0.00135 0.0134 R2 0.94744 0.98468 Monometal-Freundlich KF 11.36 16.517 n 0.5948 0.3185 R2 0.92786 0.85116 Polymetal-Langmuir qe 1195.75 59.101 Ka 0.00127 0.03815 KF 0.97878 0.94157 Polymetal-Freundlich KF 9.9227 10.986 n 0.60315 0.27737 R2 0.94109 0.72494 表 8 Pb2+和 Ni2+最大吸附能力与其他报道的吸附剂的比较
Table 8. Comparison of maximum adsorption capacity of Pb2+ and Ni2+ with other reported adsorbents
原料Raw material 吸附容量/(mg·g−1)Adsorption capacity 改性方法Method of modification 参考文献References Pb2+ Ni2+ 水葫芦 251.39 — 无 [22] 棕榈仁壳 171.7 — H3PO4 [40] 玉米秸秆 243.90 64.94 H3PO4 [41] 192.31 60.24 NaOH 蓖麻 76 — K2CO3 [42] 污水污泥 57.48 — KOH [43] 椰壳 — 23.29 KMnO4 [44] 活性污泥 274 — ZnCl2 [45] 枣籽 188.76 40.61 HCl [46] 水葫芦 1247.085 147.091 Na2CO3 本研究 注:“—”为无明确数据. Notes: “—” refers to no clear data. 表 9 不同投加量 SWHBC 对离子型稀土矿山地表水金属离子的吸附效果
Table 9. Adsorption effects of different dosages of SWHBC on metal ions in ionic rare earth mine wastewater
金属离子(mg·L−1)Metal ion Pb2+ Mn2+ Mg2+ Fe2+ Zn2+ Cu2+ Ni2+ 投加量(g·L−1)Dosage 0 1.770±0.11 65.080±2.28 544.70±23.30 0.376±0.06 1.045±0.05 0.829±0.077 0.893±0.01 0.5 0.960±0.09 61.635±0.84 515.50±14.70 0.158±0.10 1.090±0.04 0.138±0.023 0.866±0.02 1 0.438±0.09 60.260±0.95 508.80±5.40 0.083±0.01 1.056±0.03 0.133±0.003 0.891±0.02 2 0.0022 ±0.00351.570±8.60 521.10±5.93 0.0197 ±0.010.537±0.03 0.091±0.003 0.752±0.03 5 0.0003 ±0.0004 22.176±3.26 521.10±16.00 0.003±0.005 0.036±0.05 0.03±0.04 0.100±0.01 -
[1] 张培善, 陶克捷. 中国稀土矿主要矿物学特征[J]. 中国稀土学报, 1985, 3(3): 1-6. doi: 10.3321/j.issn:1000-4343.1985.03.001 ZHANG P S, TAO K J. Mineralogical charaterist1cs of rare earth minerals in China[J]. Journal of the Chinese Rare Earth Society, 1985, 3(3): 1-6 (in Chinese). doi: 10.3321/j.issn:1000-4343.1985.03.001
[2] 王炯辉, 张喜, 陈道贵, 等. 南方离子型稀土矿开采对地下水的影响及其监控[J]. 科技导报, 2015, 33(18): 23-27. WANG J H, ZHANG X, CHEN D G, et al. Influence of during south ion-absorbed-type rare earth deposit mining on groundwater and it’s monitoring[J]. Science & Technology Review, 2015, 33(18): 23-27 (in Chinese).
[3] GUDDETI S S, KURAKALVA R M. Potential toxic element contamination and non-carcinogenic risk assessment of groundwater from rapidly growing urban areas in Telangana, India[J]. Environmental Science and Pollution Research International, 2023, doi. org/10.1007/s11356-023-28378-z.GUDDETI S S,KURAKALVA R M.Potential toxic element contamination and non-carcinogenic risk assessment of groundwater from rapidly growing urban areas in Telangana,India[J].Environmental Science and Pollution Research International,2023, doi.org/10.1007/s11356-023-28378-z. [4] AN Q, JIANG Y Q, NAN H Y, et al. Unraveling sorption of nickel from aqueous solution by KMnO4 and KOH-modified peanut shell biochar: Implicit mechanism[J]. Chemosphere, 2019, 214: 846-854. doi: 10.1016/j.chemosphere.2018.10.007 [5] BEN SALEM D, OUAKOUAK A, TOUAHRA F, et al. Easy separable, floatable, and recyclable magnetic-biochar/alginate bead as super-adsorbent for adsorbing copper ions in water media[J]. Bioresource Technology, 2023, 383: 129225. doi: 10.1016/j.biortech.2023.129225 [6] 梅杨璐, 徐晋, 张寅, 等. 氮改性对生物炭理化性质的影响及其对废水中铜离子的吸附特性[J]. 环境化学, 2022, 41(5): 1796-1808. doi: 10.7524/j.issn.0254-6108.2021012302 MEI Y L, XU J, ZHANG Y, et al. Effect of nitrogen modification on the properties of biochars and their adsorption behavior on Cu2+ removal from wastewater[J]. Environmental Chemistry, 2022, 41(5): 1796-1808 (in Chinese). doi: 10.7524/j.issn.0254-6108.2021012302
[7] WIJEYAWARDANA P, NANAYAKKARA N, LAW D, et al. Performance of biochar mixed cement paste for removal of Cu, Pb and Zn from stormwater[J]. Environmental Research, 2023, 232: 116331. doi: 10.1016/j.envres.2023.116331 [8] SUN C, CHEN T, HUANG Q X, et al. Enhanced adsorption for Pb(II) and Cd(II) of magnetic rice husk biochar by KMnO4 modification[J]. Environmental Science and Pollution Research, 2019, 26(9): 8902-8913. doi: 10.1007/s11356-019-04321-z [9] HOSLETT J, GHAZAL H, KATSOU E, et al. The removal of tetracycline from water using biochar produced from agricultural discarded material[J]. Science of the Total Environment, 2021, 751: 141755. doi: 10.1016/j.scitotenv.2020.141755 [10] YANG H F, LI X M, WANG Y T, et al. Effective removal of ammonium from aqueous solution by ball-milled biochar modified with NaOH[J]. Processes, 2023, 11(6): 1671. doi: 10.3390/pr11061671 [11] JEDYNAK K, CHARMAS B. Adsorption properties of biochars obtained by KOH activation[J]. Adsorption, 2023: 1-17. [12] 匡开月, 刘畅, 俞志敏, 等. 加拿大一枝黄花衍生炭对Cr(Ⅵ)吸附性能研究[J]. 生物学杂志, 2022, 39(4): 55-60,71. doi: 10.3969/j.issn.2095-1736.2022.04.055 KUANG K Y, LIU C, YU Z M, et al. Adsorption performance of Cr(Ⅵ)by activated biochar derived from Solidago canadensis L[J]. Journal of Biology, 2022, 39(4): 55-60,71 (in Chinese) doi: 10.3969/j.issn.2095-1736.2022.04.055
[13] HARIF S, ABOULHASSAN M A, BAMMOU L, et al. Improving the removal of anionic surfactant in cardboard industry wastewater by coagulation/flocculation: Process optimization with response surface methodology[J]. Water, Air, & Soil Pollution, 2023, 234(7): 477. [14] ARNI L A, HAPIZ A, ABDULHAMEED A S, et al. Design of separable magnetic chitosan grafted-benzaldehyde for azo dye removal via a response surface methodology: Characterization and adsorption mechanism[J]. International Journal of Biological Macromolecules, 2023, 242: 125086. doi: 10.1016/j.ijbiomac.2023.125086 [15] ZHAO Z Q, SHEN X L, GAO L J, et al. Adsorption and co-adsorption of 2, 4-difluoroaniline and copper (II) using nickel-manganese ferrite magnetic biochar derived from orange peel[J]. Water, Air, & Soil Pollution, 2023, 234(7): 1-19. [16] GUO R S, YAN L L, RAO P H, et al. Nitrogen and sulfur co-doped biochar derived from peanut shell with enhanced adsorption capacity for diethyl phthalate[J]. Environmental Pollution, 2020, 258: 113674. doi: 10.1016/j.envpol.2019.113674 [17] ZHANG Z L, LI Y, DING L, et al. Novel sodium bicarbonate activation of cassava ethanol sludge derived biochar for removing tetracycline from aqueous solution: Performance assessment and mechanism insight[J]. Bioresource Technology, 2021, 330: 124949. doi: 10.1016/j.biortech.2021.124949 [18] CHEN T W, LUO L, DENG S H, et al. Sorption of tetracycline on H3PO4 modified biochar derived from rice straw and swine manure[J]. Bioresource Technology, 2018, 267: 431-437. doi: 10.1016/j.biortech.2018.07.074 [19] ZHOU R J, WANG Y B, ZHANG M, et al. Adsorptive removal of phosphate from aqueous solutions by thermally modified copper tailings[J]. Environmental Monitoring and Assessment, 2019, 191(4): 198. doi: 10.1007/s10661-019-7336-0 [20] DIXIT S, YADAV V L. Optimization of polyethylene/polypropylene/alkali modified wheat straw composites for packaging application using RSM[J]. Journal of Cleaner Production, 2019, 240: 118228. doi: 10.1016/j.jclepro.2019.118228 [21] 杜晓燕, 韩伟胜, 孟子涵, 等. 基于响应曲面法制备钢渣-花生壳基生态活性炭及其吸附性能研究[J]. 工程科学学报, 2023, 45(6): 979-986. DU X Y, HAN W S, MENG Z H, et al. Preparation of steel slag-peanut shell-based ecological activated carbon based on response surface method and its adsorption performance[J]. Chinese Journal of Engineering, 2023, 45(6): 979-986 (in Chinese).
[22] ZHOU R J, ZHANG M, LI J Y, et al. Optimization of preparation conditions for biochar derived from water hyacinth by using response surface methodology (RSM) and its application in Pb2+ removal[J]. Journal of Environmental Chemical Engineering, 2020, 8(5): 104198. doi: 10.1016/j.jece.2020.104198 [23] 郝海艳, 王刚, 徐敏, 等. 响应面法优化制备螯合絮凝剂巯基乙酰化聚丙烯酰胺[J]. 环境化学, 2016, 35(6): 1269-1279. doi: 10.7524/j.issn.0254-6108.2016.06.2015091104 HAO H Y, WANG G, XU M, et al. Optimization of preparation conditions of chelating flocculant with mercaptoacetyl polyacrylamide by response surface methodology[J]. Environmental Chemistry, 2016, 35(6): 1269-1279 (in Chinese). doi: 10.7524/j.issn.0254-6108.2016.06.2015091104
[24] GHANI Z A, YUSOFF M S, ZAMAN N Q, et al. Optimization of preparation conditions for activated carbon from banana pseudo-stem using response surface methodology on removal of color and COD from landfill leachate[J]. Waste Management, 2017, 62: 177-187. doi: 10.1016/j.wasman.2017.02.026 [25] LIU Y C, JI X G, GAO Z L, et al. Adsorption characteristics and removal mechanism of malathion in water by high and low temperature calcium-modified water hyacinth-based biochar[J]. Journal of Cleaner Production, 2023, 411: 137258. doi: 10.1016/j.jclepro.2023.137258 [26] OUYANG T, ZHANG T Y, WANG H Z, et al. High-throughput fabrication of porous carbon by chemical foaming strategy for high performance supercapacitor[J]. Chemical Engineering Journal, 2018, 352: 459-468. doi: 10.1016/j.cej.2018.06.184 [27] BISPO M D, SCHNEIDER J K, Da SILVA OLIVEIRA D, et al. Production of activated biochar from coconut fiber for the removal of organic compounds from phenolic[J]. Journal of Environmental Chemical Engineering, 2018, 6(2): 2743-2750. doi: 10.1016/j.jece.2018.04.029 [28] YANG X D, WAN Y S, ZHENG Y L, et al. Surface functional groups of carbon-based adsorbents and their roles in the removal of heavy metals from aqueous solutions: A critical review[J]. Chemical Engineering Journal, 2019, 366: 608-621. doi: 10.1016/j.cej.2019.02.119 [29] AHMAD GANIE Z, KHANDELWAL N, CHOUDHARY A, et al. Clean water production from plastic and heavy metal contaminated waters using redox-sensitive iron nanoparticle-loaded biochar[J]. Environmental Research, 2023, 235: 116605. doi: 10.1016/j.envres.2023.116605 [30] 吴权佳, 王铎, 叶涛, 等. 剩余污泥裂解灰陶粒吸附酸性矿山废水中Zn2+、Cu2+、Pb2+性能及机理[J]. 有色金属(冶炼部分), 2023(8): 149-158. WU Q J, WANG D, YE T, et al. Performance and mechanism of Zn2+, Cu2+ and Pb2+ adsorption by surplus sludge lysed ash ceramsite in acid mine drainage[J]. Nonferrous Metals (Extractive Metallurgy), 2023(8): 149-158 (in Chinese).
[31] NOUIOUA A, BEN SALEM D, OUAKOUAK A, et al. Production of biochar from Melia azedarach seeds for the crystal violet dye removal from water: Combining of hydrothermal carbonization and pyrolysis[J]. Bioengineered, 2023, 14(1): 290-306. doi: 10.1080/21655979.2023.2236843 [32] SUN D Z, LI F Y, JIN J W, et al. Qualitative and quantitative investigation on adsorption mechanisms of Cd(II) on modified biochar derived from co-pyrolysis of straw and sodium phytate[J]. Science of the Total Environment, 2022, 829: 154599. doi: 10.1016/j.scitotenv.2022.154599 [33] UDAWATTA M M, de SILVA R C L, de SILVA D S M. Facile, green approach for aqueous methylene blue dye adsorption: Coconut vinegar treated Trema orientalis wood biochar[J]. Environmental Engineering Research, 2023, 28(5): 220617. [34] HAMID Y, LIU L, USMAN M, et al. Functionalized biochars: Synthesis, characterization, and applications for removing trace elements from water[J]. Journal of Hazardous Materials, 2022, 437: 129337. doi: 10.1016/j.jhazmat.2022.129337 [35] 贺庆丽, 姚合宝, 冯忠耀, 等. 碳氮膜的红外光谱特性分析[J]. 光子学报, 2002, 31(9): 1106-1108. HE Q L, YAO H B, FENG Z Y, et al. The character analysis of C-N film infraed absorption spectrum[J]. Acta Photonica Sinica, 2002, 31(9): 1106-1108 (in Chinese).
[36] GOLOVIN A V, KORSAKOV A V, ZAITSEV A N. in situ ambient and high-temperature Raman spectroscopic studies of nyerereite (Na, K)2Ca(CO3)2: Can hexagonal zemkorite be stable at earth-surface conditions?[J]. Journal of Raman Spectroscopy, 2015, 46(10): 904-912. doi: 10.1002/jrs.4756 [37] GOLOVIN A V, SHARYGIN I S, KAMENETSKY V S, et al. Alkali-carbonate melts from the base of cratonic lithospheric mantle: Links to kimberlites[J]. Chemical Geology, 2018, 483: 261-274. doi: 10.1016/j.chemgeo.2018.02.016 [38] XIE X, HE J T, HUANG J H, et al. Hyperbranched dithiocarbamate-modified biochar: A promising adsorbent for selective removal of Pb(II) from wastewater[J]. Sustainability, 2023, 15(2): 1245. doi: 10.3390/su15021245 [39] 吴有龙, 徐嘉龙, 马中青, 等. KOH活化法制备气化稻壳活性炭及其吸附性能[J]. 生物质化学工程, 2021, 55(1): 31-38. WU Y L, XU J L, MA Z Q, et al. Preparation of activated carbon from gasified rice husk char activated by KOH and its adsorption properties[J]. Biomass Chemical Engineering, 2021, 55(1): 31-38 (in Chinese).
[40] DECHAPANYA W, KHAMWICHIT A. Biosorption of aqueous Pb(II) by H3PO4-activated biochar prepared from palm kernel shells (PKS)[J]. Heliyon, 2023, 9(7): e17250. doi: 10.1016/j.heliyon.2023.e17250 [41] LIU C C, LIN J X, CHEN H J, et al. Comparative study of biochar modified with different functional groups for efficient removal of Pb(II) and Ni(II)[J]. International Journal of Environmental Research and Public Health, 2022, 19(18): 11163. doi: 10.3390/ijerph191811163 [42] BAKAL P P, DAS G. Biochar derived from the stem of Ricinus communis L. and Colocasia esculanta: Efficient adsorbent for the removal of Cd(II) and Pb(II) ions from an aqueous environment[J]. Journal of Water Chemistry and Technology, 2023, 45(3): 200-210. doi: 10.3103/S1063455X23030025 [43] ZHANG J J, SHAO J G, JIN Q Z, et al. Sludge-based biochar activation to enhance Pb(Ⅱ) adsorption[J]. Fuel, 2019, 252: 101-108. doi: 10.1016/j.fuel.2019.04.096 [44] 张凤智, 王敦球, 曹星沣, 等. 高锰酸钾改性椰壳生物炭对水中Cd(Ⅱ)和Ni(Ⅱ)的去除性能及机制[J]. 环境科学, 2023, 44(6): 3278-3287. ZHANG F Z, WANG D Q, CAO X F, et al. Removal performance and mechanism of potassium permanganate modified coconut shell biochar for Cd(Ⅱ) and Ni(Ⅱ) in aquatic environment[J]. Environmental Science, 2023, 44(6): 3278-3287 (in Chinese).
[45] van VEENHUYZEN B, TICHAPONDWA S, HÖRSTMANN C, et al. High capacity Pb(II) adsorption characteristics onto raw- and chemically activated waste activated sludge[J]. Journal of Hazardous Materials, 2021, 416: 125943. doi: 10.1016/j.jhazmat.2021.125943 [46] MAHDI Z, EL HANANDEH A, YU Q J. Preparation, characterization and application of surface modified biochar from date seed for improved lead, copper, and nickel removal from aqueous solutions[J]. Journal of Environmental Chemical Engineering, 2019, 7(5): 103379. doi: 10.1016/j.jece.2019.103379 [47] 邓振乡, 秦磊, 王观石, 等. 离子型稀土矿山氨氮污染及其治理研究进展[J]. 稀土, 2019, 40(2): 120-129. DENG Z X, QIN L, WANG G S, et al. Ammonia nitrogen pollution and progress in its treatment of ionic rare earth mines[J]. Chinese Rare Earths, 2019, 40(2): 120-129 (in Chinese).
-




 下载:
下载: