-
砷是地球上分布最广的剧毒类金属,具有生物累积性和不可降解性,可通过水、大气和食物等途径进入人体并对人体健康造成危害[1-4],目前已被国际癌症研究中心等列为一类致癌物. 砷的来源主要包括岩石的自然风化和人类生产和生活产生的含砷废弃物[5],环境砷污染问题随着人类社会的发展和工业化进程的加速而呈加剧趋势[6],特别是在人口密集、人类活动强烈的沿海地区. 含砷物质通过径流输送、直接排放、大气沉降等多种方式源源不断进入河口区域,其中的砷及砷化物可在水生生物体内积累,干扰其新陈代谢,甚至对生物群落结构产生影响,导致生态系统失衡[3,7],并可能经由食物链对人类健康产生潜在威胁. 进入水体中的砷等化学物质大部分会通过各种物理、化学和生物途径迅速由水相转入固相并最终进入沉积物中累积,使得河口和近岸区域沉积物成为污染物的主要存储库[8]. 另一方面,当水体环境发生变化时,沉积物结合的砷还可通过化学和生物循环再次回到水中,导致水体二次砷污染[9-10]. 因此,沉积物既是水体污染物的汇,又是水体污染物的源,其质量状况直接关系到水质的优劣.
珠江口位于粤港澳大湾区的核心部位,也是我国环境污染最严重的入海河口之一,其中也包括重金属污染. 砷虽不是金属,但因其毒性与重金属相近,因而在环境重金属污染研究中,也常把砷计入其中. 但通过查阅近40年来的调查数据发现,关于珠江口海域砷的监测数据相对其他重金属依然少得多,且由于不同时期的调查工作覆盖范围有差异,布设样点的位置、疏密程度、采用的测试分析方法等不同,使得关于珠江口表层沉积物砷含量的统计结果差异颇大[11-17],可比性差,不利于区域环境演化趋势分析.
伶仃洋是珠江口各种污染物含量最高的海区[11]. 本项工作即选取珠江口伶仃洋为研究区域,分析其表层沉积物和水体中砷含量的时空变化特征,以期为区域环境保护和综合治理提供基础依据.
-
珠江口由虎门等八大口门构成,是珠江水系穿越珠江三角洲平原后汇入南海的入海口(图1). 珠江水系由西江、北江、东江等组成,流经滇、黔、桂、粤、湘、赣等多个省份,水系携带流域的碎屑物质至下游冲积平原区发生沉积. 珠江上游来沙的80%沉积在珠江口,而其中的60%以上又沉积在由东四口门(虎门、蕉门、洪奇门、横门)水道构成的伶仃洋[18]. 珠江水系主干河流在珠江三角洲平原内逐级分叉,相互沟通,形成密集河网,入海河口则是整个河网的汇,因此,来自三角洲城市群人为排放的污染物质也在河口区域发生汇聚. 而海陆交互作用的水文条件,又使河口区产生着比海洋更为剧烈的物理、化学和生物作用,由此所出现的吸附、絮凝和沉淀作用又特别有利于化学物质在该区域大量富集[8]. 因此,伶仃洋海区接纳了珠江上游来砂中的大部分,构成该河口湾的四大口门又连接广州、佛山、中山、东莞等工业密集城市,直接受纳的污染物量巨大,因而环境问题相对更为严峻.
-
以珠江口伶仃洋海域为研究区,分别于2010年12月和2020年12月在该区域开展了野外调查取样工作,其中,2010年布设了28个站点,2020年布设了26个站点,两次布设站点的位置基本相同(仅个别有调整)(图1). 调查中均使用抓斗式重力采泥器采集了表层沉积物样品,现场装入聚乙烯袋中密封,室内冷冻保存. 每个沉积物样品取100 g左右,经过冷冻干燥、去除砂砾和贝屑、用玛瑙研钵研磨至200目等前处理后,称取其中的0.50 g左右置于聚四氟乙烯坩埚中,经盐酸+硝酸+氢氟酸+高氯酸消解,使用电感耦合等离子体质谱法(ICP-MS)测试了其中砷等化学元素的含量. 2010年采集的样品于2013年12月在中国科学院海洋研究所完成分析测试工作,使用仪器为美国PE公司ELAN 9000型质谱仪;2020年的样品于当年12月下旬在中国广州分析测试中心完成分析测试工作,使用仪器为德国耶拿Plasma Quant MS型质谱仪,测试过程中均使用了标样、平行样及空白样进行质量监控.
另外,2020年新增了水样采集工作,取水深度为0—0.5 m,每个站点取水5 L,分装于无菌水样袋保存. 现场使用多参数水质仪(美国,HACH-HQ40D)测定了水样的酸碱度(pH)和盐度(Practical salinity units,PSU);使用抽滤器配合0.45 μm 微孔滤膜(Whatman公司)过滤分离水体与悬浮颗粒物,收集滤液并取其中200 mL装聚乙烯瓶用于砷等元素含量分析. 水样砷含量测试参考行业标准《HJ 694—2014水质汞砷硒铋和锑的测定-原子荧光法》的方法,于2020年12月下旬在中国广州分析测试中心完成,测试仪器为AFS-9780型双道原子荧光光度计,砷检出限为0.30 μg·L−1,过程中均使用标样、平行样及空白样进行质量监控.
-
采用Zoller等提出的富集系数(Enrichment factor,EF)法[21]判断砷富集程度,评价人为活动对表层沉积物中砷累积的影响程度,公式如下:
式中,EFi为元素富集系数,Ci为实测元素含量,Cn为参比元素含量. 本研究采用图1所示钻孔中第四纪沉积物砷平均含量(8.17 mg·kg−1)作为砷背景值[20];选取保守元素Al做为参比元素,其在珠江三角洲第四纪沉积物中的背景含量为69617.65 mg·kg−1 [22].
-
采用瑞典科学家Hakanson[23]提出的潜在生态危害指数法对伶仃洋表层沉积物砷污染的潜在生态危害进行评估,公式如下:
式中,
Eir 为潜在生态危害系数,Ci 和C0 分别为元素含量实测值和参比值(采用珠江三角洲第四纪沉积物砷含量均值8.17 mg·kg−1 [20]);Ti 为毒性响应系数,本文参考Hakanson[23]和徐争启等[24]的计算结果,砷的毒性系数取值10. -
2020年12月的伶仃洋水体盐度和酸碱度测试结果显示,其时该水域表层水的盐度和pH值分别为0.32—28.90‰(平均13.84‰)和 7.60—8.03(平均7.87),二者在空间上均呈现了从口门向外海方向递增的特点.
-
据中华人民共和国国家环境保护标准HJ 694—2014,水中溶解态砷,指未经酸化的样品经0.45 μm孔径滤膜过滤后所测定的砷的含量;总砷指未经过滤的样品经消解后所测得的砷的含量. 测得2020年12月时伶仃洋水体溶解态砷含量为1.60—2.50 μg·L−1(平均2.10 μg·L−1),变异系数为0.10,空间差异性小,且与水体的盐度及酸碱度无明显相关性. 这与贾钧博等[25]测得的2019年12月时伶仃洋四大口门表层水溶解态砷含量(1.80—2.40 μg·L−1,平均2.00 μg·L−1)非常接近. 此外,杜韶娴[26]测得2011年珠江口八大口门水体样品的总砷含量为1.0—4.0 μg·L−1;张亚南等[27]测得2006—2007年珠江口及其附近海域水体总砷含量为0.90—4.40 μg·L−1,平均约2.00 μg·L−1;张银英等[28]测得1992年11月时珠江口近岸水体总砷平均含量为2.30 μg·L−1;20世纪70年代开展的珠江口大面积基线污染调查结果显示,1976—1978年珠江口水体的总砷含量为0.40—4.50 μg·L−1,从河口、沿岸往外海,水体砷浓度无明显梯度变化[29]. 通常,水体的总砷含量高于溶解态砷含量,因此,通过以上对比可见,珠江口水体砷平均含量在过去的40多年间并未发生明显变化,甚至接近于世界未污染海水中总砷的平均含量(一般介于1.00—2.00 μg·L−1)[30],这可能与珠江水系径流量大,河口海域开阔,潮流显著,水体交换频繁,对陆源污染物有较强的稀释和自净能力有关[29]. 关于珠江口咸淡水交汇区水体中砷的自净规律试验结果也证实,砷污染物进入水体后,基本可以在1 d内完成大部分自净作用,特别是在最开始的6 h自净作用速度最快,且动态条件比静态条件更有利于水中砷的自净[28]. 因此,进入水体中的砷大部分通过各种物理、化学和生物途径迅速由水相转入固相(悬浮颗粒物和沉积物)并最终进入到沉积物中累积.
-
分析结果显示,2020年12月采集的伶仃洋表层沉积物样品中砷含量范围为19.20—89.90 mg·kg−1,平均含量为52.98 mg·kg−1,较2010年时(7.00—47.30 mg·kg−1,平均25.40 mg·kg−1)增加了1倍. 依据中国海洋沉积物质量标准 GB 18668—2002,沉积物砷的质量标准为:一类≤20 mg·kg−1,二类≤65 mg·kg−1,三类≤93 mg·kg−1. 按砷质量标准划分,伶仃洋水域表层沉积物在2010年时,82.1%为二类,17.9%为一类;2020年时,30.8%为三类,61.5%为二类,7.7%为一类.
变异系数可以较好地反映数据的空间分布情况. 计算得到2010年时砷含量的变异系数为0.35,2020年时为0.38,均表现为中等变异,即,以上两个时段的伶仃洋表层沉积物砷含量空间差异性都较为显著. 但在分布规律上又有明显不同(图2),2010年时沉积物砷含量大致呈现从口门、近岸区域向河口下游和远岸方向递减的特征,2020年时则表现为与10年前基本相反的趋势,沉积物砷含量由近岸区域向远岸方向递增,与其上部水体的盐度及酸碱度的空间变化趋势相似.
虽然关于珠江口沉积物污染的调查研究工作自20世纪70年代以来已陆续开展了很多,但如上文所述,不同时期开展的调查研究工作在覆盖范围、取样情况、分析测试手段等方面差异显著. 例如,温伟英与何悦强1981年开展的调查工作中,表层沉积物取样深度为0—30 cm,采用Ag-DDC比色法测得珠江口(涵盖八大口门)45个沉积物样的砷含量范围为3.00—27.34 mg·kg−1,平均16.67 mg·kg−1 [11];1997年刘芳文等开展的伶仃洋沉积物调查中,首先使用重力采样器获取柱状样品,再取沉积物柱样顶部的0—5 cm作为表层样,采用原子吸收法和比色法测得21个表层样的砷含量范围为1.00—9.00 mg·kg−1,平均5.24 mg·kg−1[12];甘华阳等于2003—2005年在珠江口采集一批沉积物柱样,并取其顶部0—20 cm的沉积物作为表层样,采用ICP-OES法测得76个样品的砷含量范围为5.54—104.00 mg·kg−1,平均26.36 mg·kg−1[14];Bi等于2005—2008年使用与甘华阳等[14]同样的采样方法,获得291个珠江口表层沉积物样,并采用原子荧光法测得样品的砷含量范围为1.93—39.49 mg·kg−1,平均21.90 mg·kg−1[16];等等,导致统计数据的可比性较差,因此,这里暂时不做更长时间尺度的详细对比分析.
-
珠江三角洲及河口区的沉积物主要为西江、北江等珠江流域的碎屑物质经风化、剥蚀、搬运而来 [18],流域内的岩石类型对下游沉积物中的砷含量影响显著[31]. 唐志敏等[20]曾在珠江三角洲平原选择了从西、北江交汇区向现代河口方向纵列分布的4个站点采集沉积物岩芯(位置见图1)并做化学分析,结果显示,该地区的第四纪沉积物砷含量普遍小于10.00 mg·kg−1,平均为8.17 mg·kg−1,可将其视为该研究区域沉积物砷的背景值,即,自然来源的砷总量. 地壳中砷的含量一般为1.50—2.00 mg·kg−1 [32-33],与之相比,研究区域的沉积物砷背景值本身已显著高于地壳平均水平,这与西、北江上游发育有众多富砷多金属矿床直接相关[22,34].
除去自然背景,则沉积物中剩余的砷源自人为排放. 富集系数法是分析表生环境中污染物富集程度和受人为影响程度的有效手段[35],据Sutherland[36]和Blaser等[37]的分级方案,统计了伶仃洋表层沉积物中砷的富集系数(EF)(表1). 结果显示,2010年时砷的EF值介于0.94—4.99间,平均为2.61,反映沉积物中砷的富集程度及受人为影响程度以中度级为主(71.43%),其次为轻微级(25%). 2020年时砷的EF值介于2.17—12.73间,平均为6.47. 砷的EF值均大于2,指示2020年时所有调查站点的表层沉积物都受到了中度以上人为污染影响,其中中度级的占比约30%,显著级的占比约70%,人为排放量的增加应是伶仃洋表层沉积物中的砷较10年前进一步富集的主因.
西江和北江流域盆地内有色金属矿床的开采活动被认为是珠江流域所有河流沉积物中砷的最重要来源[34,38-40]. 以西江的刁江流域为例,前人研究指出,该流域沉积物中锌、铅、镉和砷含量的90%以上来源于硫化物矿床开采活动[34]. 尽管近年来环保措施逐步出台,但据2015年采集的珠江流域样本分析结果,其时西江和北江表层沉积物中砷的平均含量依然在30.00 mg·kg−1左右,最高含量超过100.00 mg·kg−1[38-39](表2). 北江输沙量虽然相对西江要少很多[18],但北江沉积物重金属含量也非常高[39-40],因而其贡献也不可忽视.
除来自珠江流域的砷外,环珠江口城市群排放的废弃物也是导致河口沉积物砷污染的重要因素. 珠江口作为三角洲河网的汇,自改革开放以来,伴随三角洲地区工业的快速发展和人口的急剧增加,受纳的近源的(相对于珠江流域盆地)生产和生活废物量也激增. 例如,环伶仃洋的广州、东莞、佛山、中山等一度都是化工、电镀、印染等重金属污染行业的聚集地带,工业生产排放的含重金属和砷的污染物主要经虎门、蕉门、洪奇门和横门等各口门水道进入河口区. 农业生产中含砷化肥和农药的大量使用致使土壤砷污染不断加剧[41-42],据统计,改革开放后的40年间,珠三角地区表层土壤的砷平均含量从9.20 mg·kg−1上升到了17.18 mg·kg−1[43],而土壤中的砷又可通过地表径流或渗流等形式进入河口. 因此,农业生产中含砷化肥和农药的使用也是造成水系砷污染的另外一个来源[44] .
以上来自陆域的污染物主要经由各口门进入珠江口. 据《广东海洋环境质量公报》公布的数据显示,2002至2017年间经珠江口八大口门排放入海的砷总量以2005—2008年最高,2009年起大幅回落,之后开始小幅度逐年减少,但截至2017年,年通量依然高于2002年(图3). 据此数据判断,近10年间经八大口门进入珠江口的陆域来源的砷量虽然依然较大,但应不足以导致伶仃洋表层沉积物砷的含量增加1倍. 因此推测,来自海域上的某些因素应该也起到了一定的作用,例如人类海上活动的加剧等.
珠江口伶仃洋是我国乃至世界沿海地区航线最密集、船舶密度最大的水域之一. 伶仃洋沿岸主要分布有广州、东莞、佛山、中山、珠海等港口,据2022年的《广东统计年鉴》,2000—2020年间,这些港口的年货物吞吐量呈直线上升趋势,其中2020年(107463万吨)比2010年(64447万吨)增加了近1倍. 此外,水上工程项目的施工活动增加,如位于伶仃洋上的大型建设项目港珠澳大桥、深中通道等,主要施工期均在2010—2020年间. 船舶活动以及海上建设工程都可直接向水中排污,其中可能含有砷;同时也会加剧对伶仃洋海域底泥的扰动作用,使吸附有砷的较早期沉积的颗粒物重新进入水体,经过再悬浮—再沉降作用,成为表层沉积物中的一部分.
另外,据《中国海洋生态环境状况公报》(2001—2021年),珠江口水体的富营养化逐年加剧,其结果会导致:一方面可使更多的砷等化学物质在河口区被有机质吸附截留;另一方面还可促进还原条件的增强,这有利于沉积物中的铁、锰、铝水合氧化物和氢氧化物还原,使受之吸附的砷被释放并重新进入上覆水体,这部分砷在向上迁移的过程中随着氧化环境的增强再次被吸附并沉淀到沉积物的表面[9-10].
人类海域活动排污量的增加,以及因受扰动或者水环境变化从底泥中重新进入上覆水中的砷在再次沉降之前可随水流向远岸方向又运移一段距离,这些可能都是导致2020年伶仃洋表层沉积物砷含量空间分布特征较10年前发生变化的重要原因.
-
本文使用Hakanson潜在生态危害指数法评估伶仃洋表层沉积物砷污染的潜在生态危害,其结果显示,2010年时伶仃洋表层沉积物砷的潜在生态危害系数
Eir 值为8.74—59.12(平均31.76),以轻微生态危害为主;2020年时的Eir 值为24.00—112.38(平均66.22),以中等—强生态危害为主(表3),砷污染潜在生态危害程度较10年前加剧.此外还应引起关注的是,在有氧条件中砷主要以五价态存在,在缺氧环境中则更易以三价态的形式存在,而三价砷的毒性更大[45]. 因此,珠江河口区富营养化的加剧可促进沉积物中的五价砷向三价砷转变,从而进一步增加砷的潜在生态风险[46].
-
(1)珠江口水体砷含量在最近的40余年间变化甚微,平均含量均在2.00 μg·L−1左右,且空间上无明显梯度变化. 这应与河口区水体对污染物有较强的稀释和自净能力有关.
(2)珠江口伶仃洋表层沉积物中的砷含量较其上覆水中的含量要高的多,且呈现了逐渐累积的特征,2020年的表层沉积物砷含量较2010年时增加了1倍. 初步分析认为,导致近10年来伶仃洋海域表层沉积物砷进一步富集的原因主要有:①来自陆域的砷输入总量依然较大;②加剧的水上人为活动向水域中输入了更多的含砷污染物;③人类活动的强烈扰动以及水环境变化导致了底泥中的砷释放并转移到了表层.
(3)伶仃洋表层沉积物砷含量的空间分布特征在最近的10年间也发生了明显变化,总体上由2010年的“由近岸向远岸方向递减”发展为了2020年的“由近岸向外海方向递增”的特点. 导致这一变化的主要原因包括:①人类水上活动的排污量增加,而其排放活动主要发生在离岸较远的区域;②从底泥中释放并重新进入上覆水中的砷,在再次沉降之前随水流向远岸方向运移了一段距离.
(4)2020年时伶仃洋表层沉积物砷污染的潜在生态危害较10年前进一步加剧,应予以持续关注.
珠江口伶仃洋水体及表层沉积物砷污染时空变化
Temporal and spatial change of Arsenic pollution in water and surface sediments of Lingding Bay, Pearl River Estuary
-
摘要: 为了解珠江口伶仃洋砷污染状况,分别于2010年12月和2020年12月在该海域布点取样,样点布设位置和数量基本一致. 2010年仅采集了表层沉积物样品,2020年采集了表层沉积物和水体样品,分别使用原子荧光法和ICP-MS法测试了水体和沉积物砷含量. 结果显示,2020年时伶仃洋水体中溶解态的砷含量在2 μg·L−1左右,空间差异性小,与1976年以来的其他调查结果相近,指示该海域的水体砷含量在近40余年间未发生明显变化. 2020年时表层沉积物砷平均含量为52. 98 mg·kg−1,较2010年时(平均25.40 mg·kg−1)增加了1倍;空间分布上,由2010年时总体上从口门水道向外海方向递减的特征变为了2020年时的由近岸向远岸方向递增的特点. 综合分析认为,近10年间,除来自陆域的砷输入总量依然较大之外,持续加剧的海上人类活动可能向水中排放了更多的含砷污染物,加上人类活动的强烈扰动及水环境变化(如持续富营养化)导致的底泥中的砷释放和再沉淀作用等,共同导致了砷在沉积物表层的进一步富集和在空间上的重新分配. 总之,珠江口伶仃洋区域砷污染的潜在风险依然较为严峻,后期仍需加强监测和修复等相关工作.Abstract: In December 2010 and December 2020, samples were taken in the Lingding Bay of the Pearl River Estuary to investigate its arsenic pollution change. These samplings were of nearly the same locations and quantities. Only surface sediment samples were collected in 2010, while surface sediment and water samples were collected in 2020. The arsenic contents of the water samples and all sediment samples were measured by using atomic fluorescence spectrometry (AFS) and ICP-MS, respectively. The results showed that the dissolved arsenic content in the water of Lingding Bay was about 2 μg·L−1 with no significant deference in geographical distribution, which was similar to previous results since 1976, indicating that the arsenic content in the water of this sea area has not changed significantly during the past 40 years. The mean arsenic content of surface sediment was 52.98 mg·kg−1 in 2020, which is twice as that in 2010 (25.40 mg·kg−1 on average). In 2010, the arsenic content of surface sediment decreased gradually from the watercourses to the open sea, while the spatial distribution characteristics of sediments arsenic content in 2020 was almost opposite to that in 2010. After a comprehensive analysis, it was believed that the main reasons for these changes in arsenic content of surface sediment during the past 10 years were as follows: 1) The total amount of arsenic input from land areas was still large, 2) increased human activities on the water input more arsenic containing pollutants into the water, 3) The intense disturbance of human activities and changes of water environment had led to the release and transfer of arsenic in the sediment to the surface. In general, the potential risk of arsenic pollution in the Lingding Bay of the Pearl River Estuary was still severe. Further monitoring and remediation work should be enhanced in the later stage.
-
Key words:
- Lingding Bay /
- water /
- surface sediment /
- arsenic pollution /
- spatio-temporal change.
-
随着国家对环境保护的不断重视以及人民群众对碧水蓝天、美好环境热切需求的不断增长,以流域治理、湿地建设、“碧水绕城” “美丽乡村”等为代表的水环境治理项目越来越多[1]。城市化水平较高的地区,人们的生产生活活动对城市湖泊水体的影响更为突出,尤其是作为河流蓄泄的枢纽湖泊(如嘉兴南湖),其水环境治理一直是生态环境领域的难点。
国内外比较成熟的湖泊生态修复理论主要包括多稳态理论、营养盐浓度限制理论和生物操纵理论[2]。多稳态理论指在相同的外部环境条件下,浅水型湖泊可能处在“草型清水态”和“藻型浊水态”2种完全不同的状态[3],2种状态之间存在着临界阈值[4-5];营养盐浓度限制理论强调营养盐对生物群落的限制与驱动,是湖泊多稳态保持和转化的动力[2];生物操纵理论通过生物调控治理藻类水华[6]而应用在富营养化湖泊的治理中[7]。柯杰等[8]认为湖泊湿地修复技术主要包括物理技术、生物技术和化学技术。物理技术中的环保疏浚是采取人工、机械的措施适当去除水体中的污染底泥,以降低底泥中污染物的释放通量和生态风险,并对疏浚后的污染底泥进行安全处理处置的技术,是河流、湖泊(水库) 水污染治理的重要技术之一[9]。南京玄武湖采用的围堰分区干式法[10-11],西安兴庆湖采用的高压水枪水力冲挖方式[12],杭州西湖采用的环保绞吸式挖泥船疏浚方式[13]等均属于比较常见的环保疏浚技术。但环保疏浚缺乏与生态修复技术之间的衔接,如疏浚底泥的二次利用、无害化处置通常缺乏考虑[14]。其他物理技术包括通过机械、设备对城市湖泊湿地进行换水、补水,实现水量稀释,可以快速降低营养盐浓度[8],比如常用的混凝-沉淀、磁混凝技术、超磁分离一体化工艺等。其中超磁分离一体化工艺已在巢湖塘西河[15]生态补水、吴江同里古镇[16]景观补水、北京总装航天城人工湖[17]活水循环等水环境项目中进行广泛应用。在生物技术方面,以沉水植物为主或结合其他修复技术的原位生态修复已十分普遍,在太湖[18-19]、上海临港滴水湖[20]、杭州西湖[21]、昆明滇池草海[22]等均有广泛应用。化学技术主要是指利用药剂、化学工艺对湖泊进行治理,在城市湖泊水体生态修复方面应用较少。
与传统城市湖泊相比,浙江嘉兴南湖作为嘉兴主要河流的交汇处,其水体库容小、水力停留时间短,形式上更接近“河流型湖泊”。南湖作为5A级景区,往来游客众多,游船航次频繁,关注度极高,生态修复对水体的扰动相对更为受限。本研究以嘉兴南湖生态环境修复工程(一期)项目为例,基于南湖水环境调查的已有成果[23-26],对南湖水质问题和水体浑浊原因进行分析,提出嘉兴南湖生态系统构建的整理思路和关键技术,并对工程实施后的效果进行评价,以期为平原河网水系、开放性水域、高浊度水体的城市湖泊治理提供借鉴和参考。
1. 南湖水体概况与生态修复难点
1.1 南湖水体概况
南湖位于浙江省嘉兴市区,湖体南北长、东西狭,常年水面面积为0.52 km2,是嘉兴市各主要河流蓄泄的枢纽,是海盐塘、平湖塘、嘉善塘等多条河流的起点、终点交汇处[27]。南湖水体悬浮物(SS)含量较高,透明度较低(基本维持在25 cm左右),总磷(TP)远远高于水环境功能区考核的Ⅲ类标准(湖泊标准)[28-29]。而南湖水体由于透明度低,光线条件差,湖区水底基本上无沉水植物覆盖。换水周期是湖泊水环境的一个重要参数,影响着水体中污染物与营养物的质量浓度与停留时间,同时也影响着水体中发生的生物与化学反应过程时间的长短[30]。南湖换水周期仅为1.59 d[31],水力停留时间短,每天的水体交换量大,导致上游来水所带来的悬浮性颗粒物很难沉降。
南湖水体中TP质量浓度为0.121~0.388 mg·L−1,平均为0.246 mg·L−1,超过地表水Ⅴ类水质标准(湖泊标准)[29]。空间分布显示,水体中TP的空间分布差异性显著,质量浓度较高的区域主要集中在西南部及东南部的南湖入湖河道,而低值区主要分布在南部堤岸及周围区域[23]。南湖水体中TN质量浓度为3.81~4.99 mg·L−1,平均为4.32 mg·L−1,超过地表水Ⅴ类水质标准(湖泊标准)[29]。空间分布显示,TN质量浓度从南湖西南角和东南角向北部出口逐渐递减,而在湖心岛的南部堤岸周围的TN质量浓度明显低于其他区域[24]。NH3-N的质量浓度相对较低(0.67~1.67 mg·L−1),在地表水Ⅲ~Ⅴ类水质标准(湖泊标准)[29]之间波动,均值为1.22 mg·L−1,NH3-N的空间分布与TN较为相似[24]。近年来,南湖水质持续好转,NH3-N指标年均可达到Ⅲ类水标准(湖泊标准)[29],但TN和TP含量依然很高,大部分月份的TP仍在0.20 mg·L−1以上,颗粒形态磷占比达到60%以上。总体来看,水质仍处于地表水劣Ⅴ类水平(湖泊标准)[29]。
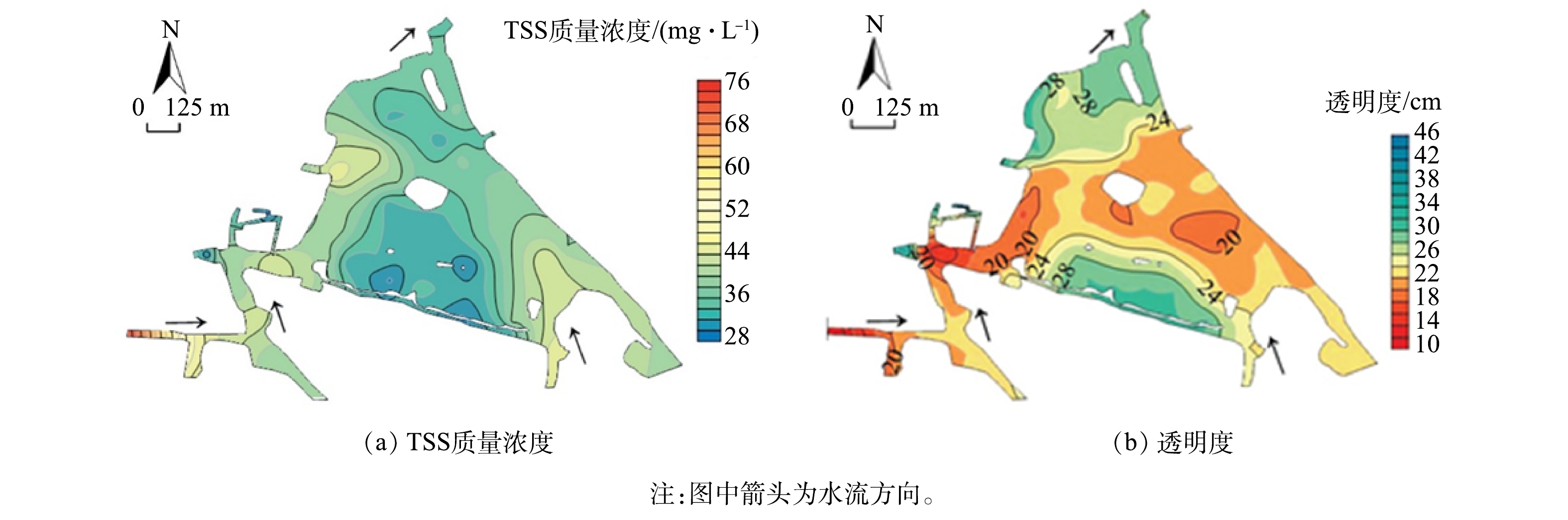
南湖水体悬浮物质量浓度为29.2~75.2 mg·L−1,均值为39.0 mg·L−1。与国内其他主要湖泊相比,南湖水体悬浮物质量浓度均值略低于巢湖,高于其他湖泊[25](表1)。入河道悬浮物中粒径为10~50 μm的颗粒占比较大,而湖区水体中悬浮物粒径以4~10 μm为主,湖区底泥最上层颗粒粒径多以10~50 μm 为主。这说明河道携带的悬浮物粒径为10~50 μm的颗粒可沉降下来,但粒径为10 μm 以下的悬浮物很难通过重力沉降下来。南湖水体悬浮物质量浓度大小主要受上游来水及湖区船舶活动的影响,航道区域悬浮物质量浓度明显高于周边水体[25]。南湖水系中的水体悬浮物分布[25]如图1所示。
表 1 南湖与国内其他湖泊水体中的TSS质量浓度及其均值Table 1. TSS mass concentration and its mean value in Nanhu Lake and other domestic lakes湖泊名称 质量浓度/( mg·L−1) 均值/( mg·L−1) 东湖 13. 80~23. 76 18. 72 蠡湖 1. 00~78. 00 17. 35 鄱阳湖 5. 00~72. 00 23. 87 梁子湖 2. 83~26. 85 12. 41 洪湖 2. 24~25. 66 10. 98 太湖 11. 08~85. 40 34. 31 巢湖 17. 80~67. 53 42. 76 南湖 29. 20~75. 20 38. 95 南湖水体透明度为10~46 cm,均值为25 cm,南湖湖区水体透明度的空间分布差异性较为显著,水体透明度较低的地方主要集中在西南水域以及湖体航道[26]。河流、湖泊中船舶的航行对于水体底部的沉积物具有很大的扰动作用[32],特别是船舶尾部的螺旋桨对于浅水河流及湖泊底泥扰动的作用更为巨大。南湖游船、巡逻艇、执法船、保洁船等船舶扰动引起底泥再悬浮是航道区域透明度低的主要原因。南湖水系中的水体透明度分布情况[26]如图1所示。
1.2 南湖水体生态修复的难点
南湖周边多为景观块石护岸和直立式岸坡,上游河道多为浆砌块石或钢筋混凝土直立式岸坡。该类型岸坡生态型差,近岸侧几乎无挺水植物。受水体浑浊、透明度低、氮磷超标等影响,南湖湖区水下几乎无沉水植物。南湖生态环境恢复的困难主要有以下几点。
1)水体透明度低,水深条件差。光线是沉水植物生存的最基本条件,这是因为沉水植物需要通过光合作用进行代谢活动,因此水下光照条件是影响沉水植物生长存活的最主要因素。影响水下光照条件的主要指标包括水深、透明度、悬浮物浓度、藻类等。在常水位为1.16 m时,南湖平均水深为2.8 m,而南湖水体透明度均值只有25 cm。沉水植物生长所需的光补偿深度一般应为水体透明度的1.5倍[33],按照南湖目前的水深条件,其水体透明度远远不能满足沉水植物生长的基本条件,这也是南湖生态系统构建面临的最大困难。
2)景区内施工,沉水植物种植方式受限。沉水植物的常见种植方式主要包括扦插法、抛投法等。扦插法根据种植水深的不同又分为浅水扦插(水深一般小于0.5 m)和船上扦插(水深为0.5~2.0 m)。浅水扦插的前提是需对拟种植区域进行抽水,形成干地作业环境,再根据植物的生长习性逐渐蓄水,直至达到设计常水位。沉水植物“扦插”种植具有生产效率高、苗木成活率高、定位造型易控制等优点。抛投法则分为配重抛投和带土抛投。抛投法虽然施工效率快、无需降水,但是水草成型不规则、容易飘草,且成活率低。嘉兴南湖为5A级景区,且处于城市核心区,邻近红船保护区域,严禁抽水作业,故只能采用水上抛投的施工方法。
3)湖区船舶多,船行波扰动大。在沉水植物生长初期,由于幼苗尚未扎根,船舶引起的船行波作用会影响沉水植物幼苗的正常扎根,直接威胁沉水植物的成活。南湖湖心岛与会景园之间有固定的红船游览航线,嘉兴水上巴士也从小瀛洲入南湖。此外,南湖管理单位众多,海事、港航、水上派出所、名胜公司、旅发公司等均有执法或巡逻船舶,湖区船舶密度大、航线分散,影响沉水植物的成活率。
2. 南湖水体生态修复系统的构建
2.1 生态系统构建的整体思路
水体透明度的主要影响因子包括光学衰减系数、悬浮物及叶绿素a等[34]。南湖透明度低的关键原因是悬浮物质量浓度高。沉水植物生长的基本条件是光照强度,此外,水深条件、污染物浓度、波浪条件等也能影响沉水植物的正常生长。综合来看,嘉兴南湖生态修复的核心就是要提升水体透明度和恢复湖区水下生态系统。
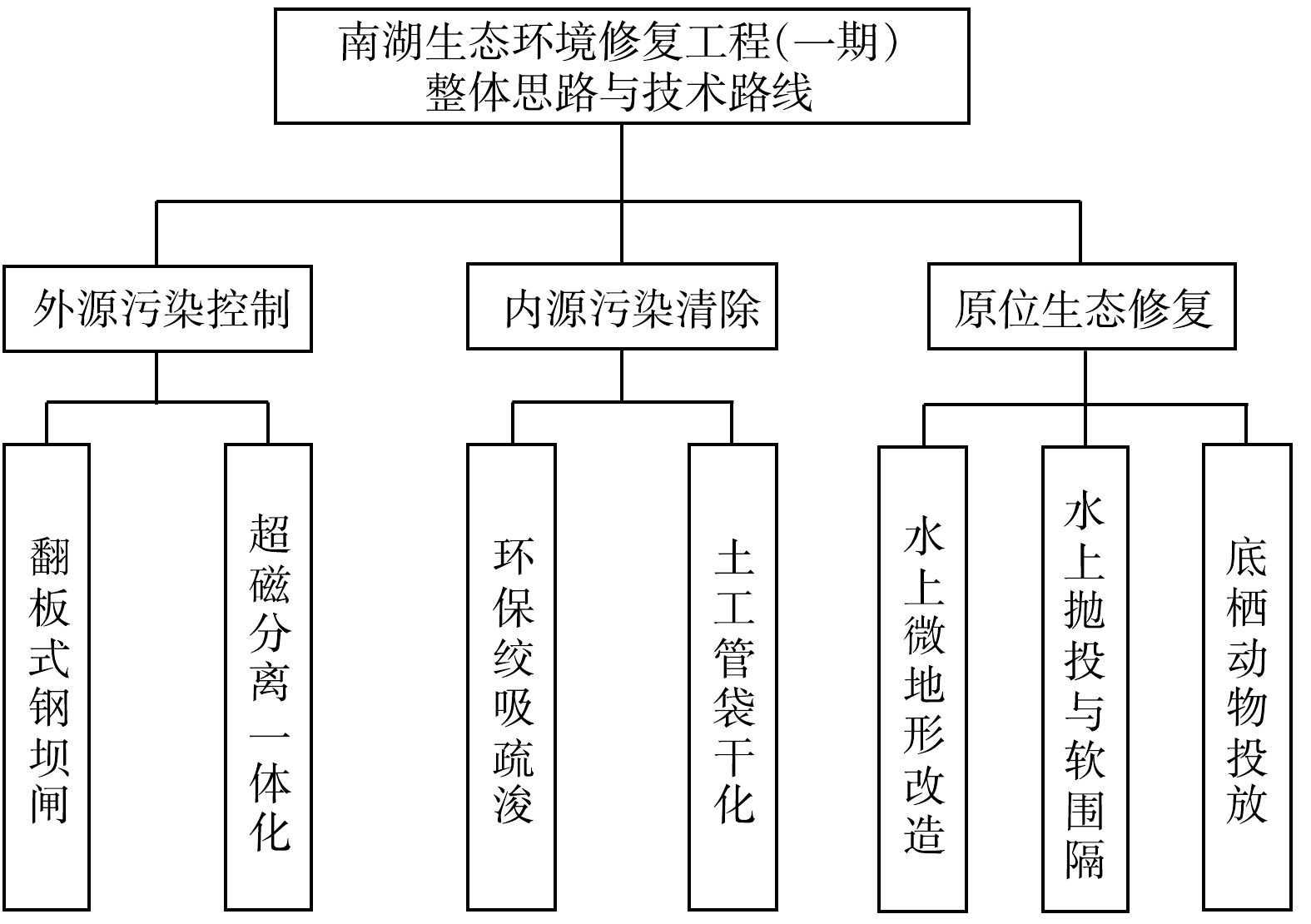
嘉兴南湖生态环境修复工程(一期)项目实施的主要目的是改善南湖水体质量,恢复湖区生态系统,实现南湖水质、生态及景观的全面提升。本项目的质量目标是使湖区水体透明度达到80 cm,沉水植物覆盖率达到25%。以沉水植物为主导,与水生动物相结合构建的水下生态系统作为一种新兴的河湖水体治理技术,已被许多工程采用,以实现湖泊氮磷污染、维持清水态湖泊的目标[35]。为实现工程治理目标,项目团队创新性地采用了前期“水养草”、后期“草养水”的治理理念。前期通过一系列工程措施提升水体透明度等指标,以便为沉水植物创造生长条件。后期待沉水植物恢复良好、“水下森林”生态系统构建成功后,再通过沉水植物生态系统的自净能力提升水体透明度等指标。南湖生态系统构建的整体思路如图2所示。
2.2 外源污染控制
1)翻板式钢坝闸——水量调控。上游来水悬浮物质量浓度高[25]、TP污染物高[23],为防止上游浊水持续进入南湖,在南湖上游河道(青龙港、采菱桥港、宝莲桥港、长盐塘、张家门港)修建水量调控的闸坝措施。拦河闸坝的结构形式通常有直升式钢闸门、上翻式液压门、倒卧式液压门、钢坝、橡胶坝等。直升式闸门上部结构较大,整体景观效果差;上翻式液压门闸门开启时,影响通航且景观效果差;倒卧式液压门闸门开启以后河道易产生淤积。本工程的水量调控措施主要采用了5座带船舶自动识别的自动化控制翻板式钢坝闸,既能满足设计对外源污染的拦截及水体交换的控制,又不影响正常通航秩序,同时钢坝启闭机室为地下结构,建成后美观大方,最大程度地保证了节能、环保、人居和谐。上游长盐塘钢坝建设实施和建成后现场照片如图3所示。
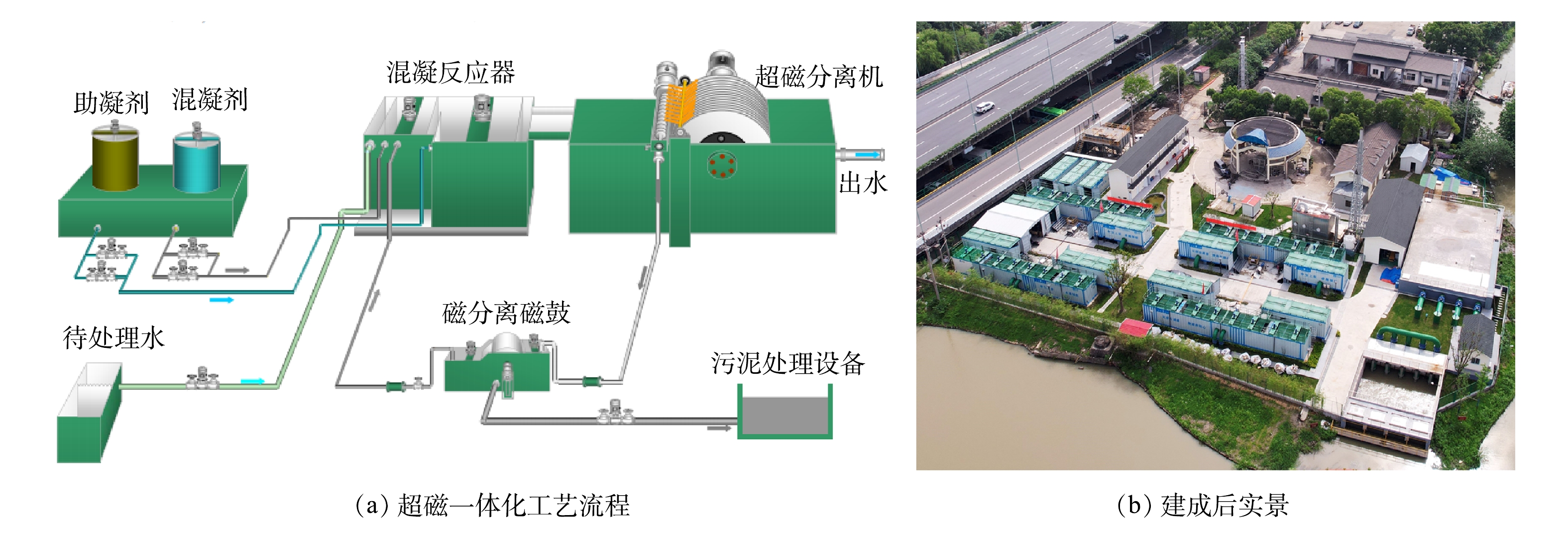
2)超磁分离一体化工艺——净水降浊。悬浮物的去除通常可采用混凝-沉淀、磁粉-混凝工艺等措施。混凝-沉淀工艺在我国大中型水厂中应用较为普遍,但是工艺所需占地面积较大,而南湖位于嘉兴核心城区,无法满足工艺所需的占地需求。超磁分离一体化工艺作为磁粉-混凝工艺的典型代表,通过磁盘吸附进行固液分离,实现水体快速净化,具有占地面积小、处理速度快、自动化程度高、模块化快速安装的优点[17],特别适合嘉兴南湖等城市核心区用地面积紧张的水环境治理项目。超磁设备部分主要由16个标准集装箱组成,土建部分由取水池、调蓄池、加药间、磁粉仓库等组成,全部的设备和土建集中在嘉兴大桥南侧大约3 000 m2场地内,整个超磁设备的补水规模达到20×104 t·d−1。超磁分离一体化工艺流程[17]和建成后实景如图4所示。
2.3 内源污染清除
环保绞吸疏浚与土工管袋干化技术——去除底泥污染物。环保疏浚的目的主要是为了清除污染底泥,一般以清淤厚度作为控制标准,而非传统疏浚的增加通航水深。内河或湖泊、湿地的环保清淤常用船机包括抓斗式挖泥船、反铲式挖泥船、链斗式挖泥船、绞吸式挖泥船等。前3种挖泥船的挖泥工艺均为“挖-运-抛”,泥驳靠泊、抛泥均需要作业时间,导致工艺不能连续作业,影响施工效率;而绞吸式挖泥船的最大优点就是可以连续作业,施工效率较高。嘉兴南湖湖区的清淤采用了加装整流罩的环保绞吸挖泥船,减小了因绞刀切削疏浚土导致的污染物再悬浮,疏浚土通过排泥管线输送至处理场地,利用土工管袋干化的方式,实现了疏浚土减量化、无害化的处理。同时,干化后的疏浚土可以作为绿化种植土回收利用,干化尾水再次通过超磁分离一体化设备处理,实现达标排放,疏浚工艺全程环保化处理[36]。
2.4 原位生态修复
1)水上微地形改造技术——重塑水下地形。微地形改造的目的是改变近岸侧沉水植物种植区域的水深条件,重塑水下地形,为沉水植物种植建立良好的下部基础。南湖南岸成功堤一侧为景观块石护岸,其他位置多为直立式护岸结构,基本无自然岸坡,近岸侧水深接近湖区平均水深,无梯级过渡。南湖的近岸侧微地形改造采用松木桩护脚,松木桩内侧为土工袋装土,防止内侧土方冲刷渗漏,微地形改造区域主体采用种植土散装回填。松木桩施打、袋装土填筑和散装土回填均采用平板驳船配合反铲挖机施工。微地形改造后,近岸侧沉水植物种植区域水深由2.5 m左右恢复至1.5 m左右,为沉水植物种植创造了良好的水深、地形和土质条件。
2)水上抛投与软围隔技术——带水栽植沉水植物。嘉兴南湖由于不具备抽水干地作业施工的条件,故沉水植物不能采用常规的扦插种植方式。本次沉水植物种植采用了水上小型作业辅助船舶、沉水植物带土或配重抛投的带水栽植方式。带土抛投是直接将植物基地的苦草连土带苗铲起,装入周转箱中并运输至项目现场。抛投时将土块分成小丛,直接投放至湖底,这种方式仅限于种植根系发达的苦草。配重抛投是将沉水植物包裹在切割好的网片上,并放入石子后用橡皮筋扎牢,做成球状,将加工好的单个个体放入泡沫箱或周转箱中并运输至项目现场,按照密度直接投放至水底。虽然水上抛投施工效率和幼苗成活率低,但受限于南湖苛刻的施工条件,也取得了良好的施工效果。另一方面,为了减少南湖湖区频繁的船舶航行所带来的船行波影响,在沉水植物种植区域外围布置软围隔,用以削减船行波、风成浪等对沉水植物幼苗扎根的不良影响。此外,在沉水植物种植前期,通过拉网赶鱼、软围隔隔断等措施,防止食草性鱼类在沉水植物生长初期啃食幼苗,确保沉水植物的成活率。沉水植物水上抛投和软围隔如图5所示。
3) 底栖动物投放——构建完整的生态系统。完整的“水下森林”生态系统是以沉水植物为主体,并辅以螺类、蚌类等底栖动物,以及水中的草食性、肉食性鱼类等生物群落共同组成。嘉兴南湖除恢复了湖区25%面积、约14.8×104 m2的沉水植物外,还配套投放了约5.6 t的螺类、蚌类和虾类,如铜锈环齿螺、背角无齿蚌、三角帆蚌、日本沼虾,重新构建了南湖的“水下森林”生态系统。
3. 工程实施效果评价
3.1 整体效果
通过南湖生态环境修复工程(一期)项目的实施,南湖水体感官明显好转,水体污染物指标显著改善,水体透明度基本达到设计要求,沉水植物恢复良好。翻板式钢坝闸、超磁分离一体化工艺、环保绞吸疏浚与土工管袋干化、水上抛投与软围隔等关键技术在南湖水体生态修复过程中发挥了重要作用。
1)翻板式钢坝闸兼具美观、通航、挡水、船舶自动识别的作用,克服了传统挡水建筑物影响通航或者占用水域面积影响景观效果的缺点,尤其适用于城市核心区域、通航河道挡水或拦河建筑物的建设。
2)超磁分离一体化工艺设备具有占地面积小、噪音低、自动化程度高、安装速度快等优点,特别适合嘉兴南湖此类治理工期紧张、用地限制、环保要求高的项目。
3)湖区环保疏浚采用环保绞吸疏浚和土工管袋干化结合的技术,土工管袋干化后的尾水创新性地采用超磁分离一体化设备进行二次处理。南湖所采用的环保疏浚技术减小了疏浚过程中的底泥再悬浮,实现了疏浚土的减量化、无害化处置。
4)沉水植物水上抛投与软围隔技术解决了南湖不能抽水作业的难题,配合水生动物的投放,南湖水下森林生态系统恢复良好,为南湖水体生态修复奠定了基础。
3.2 南湖水质监测效果
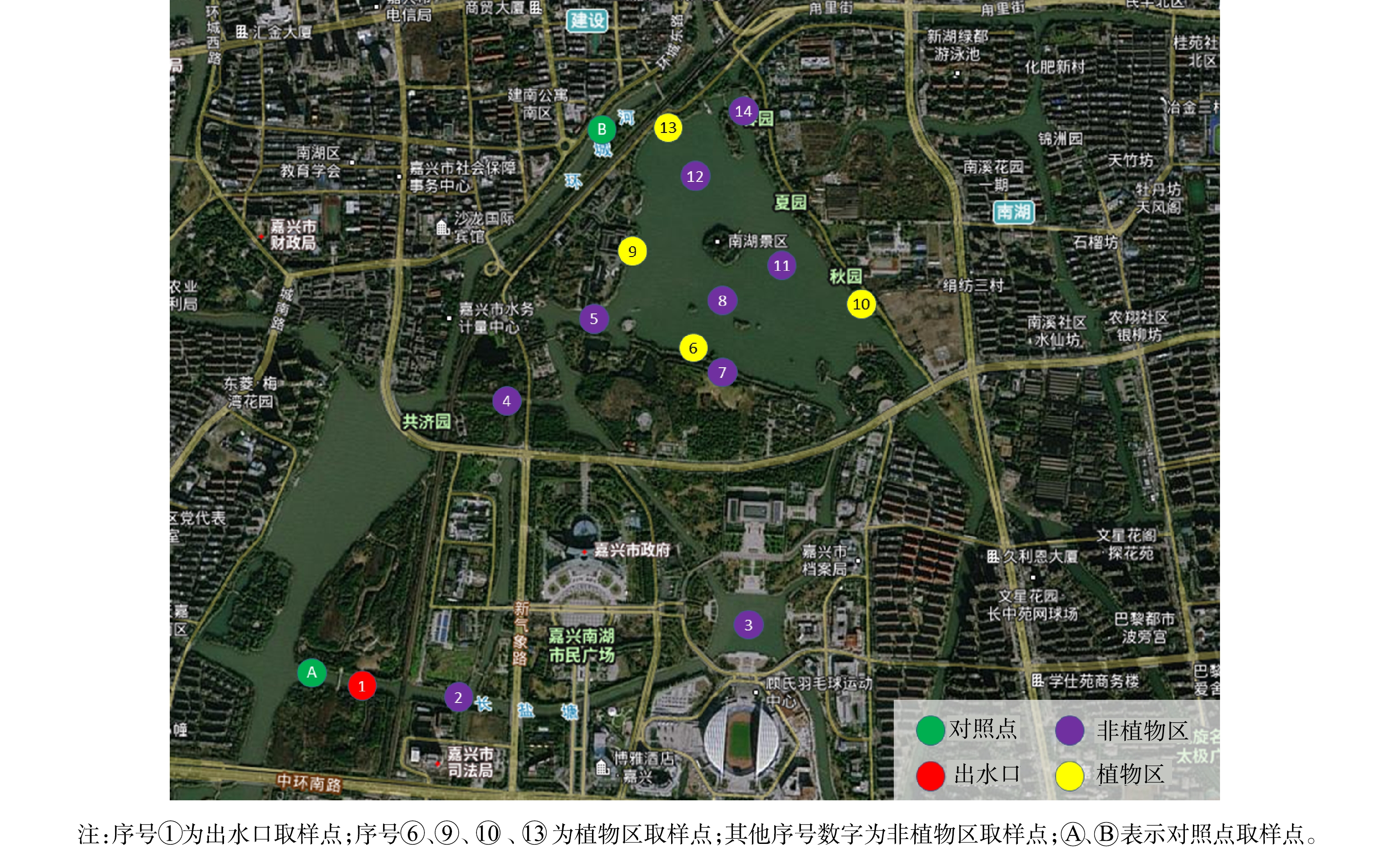
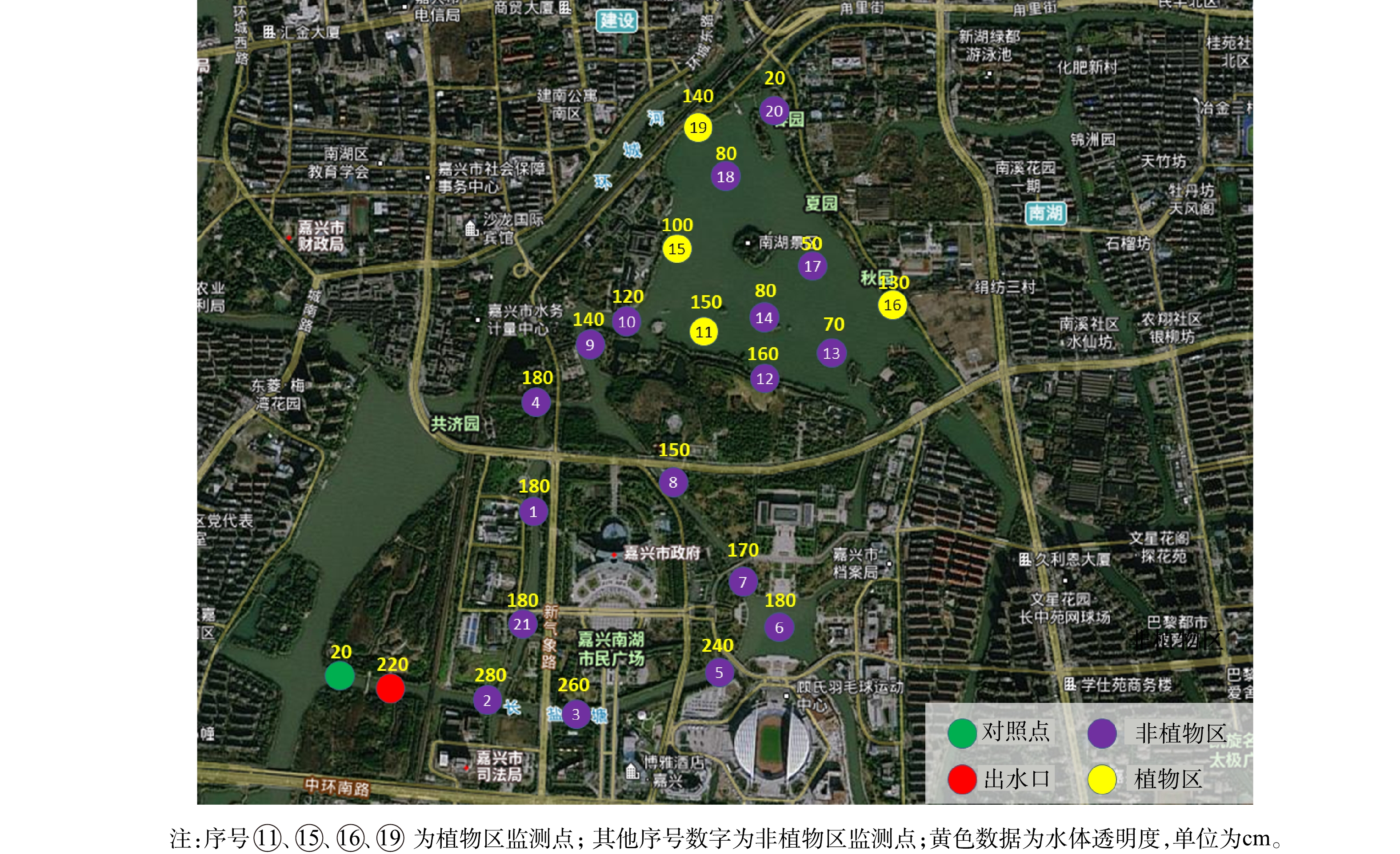
该工程完工后,项目组开展了多次水质监测,NH3-N稳定达到地表Ⅱ类水标准(湖泊标准)[29],COD稳定达到地表Ⅲ类水标准(湖泊标准)[29],南湖(除下游海盐塘出口外)大部分区域TP指标基本达到了地表Ⅱ类水标准(湖泊标准)[29]。为进一步验证工程实施效果,选取工程完工后2021年6月1日至2021年6月24日的6次水质监测数据,汇总后取平均值,进行分析讨论。各监测点、对照点位置分布及具体水质监测数据如图6、表2所示。为了验证超磁分离一体化设备对土工管袋干化后的尾水处理效果,对尾水水质进行了监测,监测数据如表3所示。
表 2 南湖水质监测数据平均值Table 2. Average value of water quality monitoring data of Nanhu lake取样点位 浊度/NTU COD/(mg·L−1) NH3-N/(mg·L−1) TP/(mg·L−1) 叶绿素a/(μg·L−1) SS/(mg·L−1) TN/(mg·L−1) 1号点 3 14 0.301 0.011 8 13 2.69 2号点 3 13 0.337 0.012 8 13 2.74 3号点 3 16 0.318 0.011 12 12 2.55 4号点 3 17 0.271 0.018 9 16 2.71 5号点 4 18 0.197 0.016 11 13 2.47 6号点 4 13 0.082 0.017 16 14 1.84 7号点 4 14 0.056 0.017 11 14 1.75 8号点 7 18 0.126 0.022 18 24 2.43 9号点 3 15 0.060 0.016 16 14 2.12 10号点 3 13 0.097 0.014 15 14 2.20 11号点 10 16 0.110 0.038 20 26 2.54 12号点 11 16 0.110 0.039 21 29 2.54 13号点 8 13 0.111 0.026 32 19 2.44 14号点 14 18 0.141 0.060 13 32 2.59 对照点A 16 14 0.485 0.149 17 28 2.48 对照点B 22 17 0.292 0.161 10 42 2.98 表 3 疏浚土干化尾水水质监测数据Table 3. Monitoring indicators of tail water quality from dredged soil drying日期 COD/(mg·L−1) NH3-N /(mg·L−1) SS/(mg·L−1) pH 磷酸盐/(mg·L−1) 2021-01-01 21 1.93 <4 7.56 0.02 2021-01-07 17 1.84 <4 7.47 0.04 2021-01-14 14 1.92 <4 7.39 0.05 2021-01-21 20 1.84 <4 7.44 0.04 由表2可以看出,河道1号点为超磁分离一体化设备出水口(最终入水系位置),对照点A靠近超磁分离一体化设备取水口,对照点A和河道1号点分别位于长盐塘钢坝的上/下游,通过水量调控措施(长盐塘钢坝)分隔开。2处位置的水质数据分析结果表明:1)超磁分离一体化设备出水浊度可以维持在3 NTU左右,与项目组对超磁设备直接出水的浊度每日监测数据基本一致;2)超磁分离一体化设备可以显著去除水体中的TP(去除率为92.61%),对NH3-N(去除率为37.94%)也有一定的去除作用,但是对TN、COD等的去除不明显。
通过对沉水植物种植区域悬浮物质量浓度进行对比分析可以看出,湖区沉水植物种植区(6、9、10、13号点)的悬浮物平均质量浓度15.25 mg·L−1明显低于湖区其他区域(8、11、12号点)的平均质量浓度26.33 mg·L−1,沉水植物种植区域悬浮物下降比值为42.09%。这表明沉水植物对水体中悬浮物具有明显的吸附作用。项目组利用水下摄像机对沉水植物进行观察也发现,植物叶片上附着了大量的悬浮性颗粒物。因此,通过沉水植物吸附、收割打捞、生长、吸附这一循环过程,能够实现水中悬浮物的转移去除。
由表2可以看出,南湖下游平湖塘出口位置(14号点)TP指标明显优于平湖塘位置(对照点B)。这表明现有工程治理措施及沉水植物系统已发挥一定的作用,但是悬浮物质量浓度和浊度改善效果不明显。因此,项目团队在南湖下游小瀛洲出口位置布置了流量计,对出入湖流量进行了监测。监测数据表明每天仍有大量的浊水通过下游出口进入南湖。这可能是由于嘉兴南湖水系仍受到不规则半日潮每天2次涨潮所带来的水流顶托的影响,对南湖正常的清水补给、置换产生了一定的削弱。
由表3可以看出,土工管袋干化后的尾水经4次检测,悬浮物SS均不超过4 mg·L−1,优于《污水综合排放标准》(GB 8978-1996)一级A标准10 mg·L−1的要求,实现了疏浚土尾水的达标排放。
3.3 南湖水体感官效果
南湖生态环境修复工程(一期)项目完工后,湖区大部分水体透明度已达到80 cm以上(图7),湖区水体颜色由黄色变为浅绿色,重现了嘉兴南湖“秀水泱泱”的美丽画卷(图8和图9)。由南湖水体透明度的监测数据和湖区感官效果改善情况可以看出: 1)南湖水系水体透明度沿两条清水入湖路线“长盐塘→蒋水港→壕股塔→平湖塘出口”和“长盐塘→七一广场→金谷桥港→壕股塔→平湖塘出口”呈下降趋势,表明在项目治理前期(水养草阶段),超磁分离一体化设备的清水补给是南湖水系透明度提升的关键; 2)南湖平湖塘出口区域的透明度仅有20 cm,表明每天涨潮流潮汐顶托进入南湖的浊水对靠近出口区域的水体透明度影响很大。
3.4 建议
1)在现有工程措施的基础之上,如果能在南湖出口位置修建水量调控措施(如翻板式钢坝闸或橡胶坝),将南湖水系完全封闭,并通过水量和水位的精细化调控,可能会进一步提升南湖水体透明度,且可以减少超磁分离一体化设备处理量并大幅缩减设备的运维成本。
2)超磁一体化设备购置费用和运维成本偏高,仍需针对不同水环境项目选择性价比更优的处理设备。
3)南湖由于不能降水作业,沉水植物种植方式受限,故只能采用水上抛投方式,这导致沉水植物成活率偏低。在沉水植物种植条件允许的情况下,利用抽水作业进行浅水扦插种植仍是施工综合效率高、成活率高、造型美观的最佳种植方式。
4)通过无人机航拍视频发现,游船航经区域呈现明显的“浑浊带”,表明船行波对底泥扰动造成的底泥再悬浮作用非常明显。如果能对南湖游船进行“电动化改造”、减小吃水深度,或者通过管理手段控制航行频次和航行速度,可能会更加有利于湖区水体透明度的改善。
4. 结论
1)嘉兴南湖生态环境修复工程(一期)项目完工后,水质监测结果表明,南湖主要水质指标(COD、NH3-N、TP)基本达到地表水Ⅲ类(湖泊标准),湖区大部分区域水体透明度达到80 cm以上,水体颜色由黄色变为浅绿色。由此可以看出,南湖生态环境修复的整理思路和技术路线是可行的。
2)超磁分离一体化设备适合在城市核心区处理高浊度水体,可以显著去除水体中的TP(去除率为92.61%),对NH3-N(去除率为37.94%)也有一定的去除作用,但是对TN、COD等的去除不明显。
3)以“沉水植物”为主体的水下森林生态系统对悬浮型颗粒物具有明显的去除作用,沉水植物种植区域悬浮物下降了42.09%。同时,在沉水植物养护阶段,应及时进行补种、收割、打捞,并通过沉水植物品种的搭配保证四季常绿,以确保沉水植物的长效净化作用。
4)湖区疏浚采用环保绞吸疏浚与土工管袋干化相结合的技术,减少了疏浚过程中的底泥再悬浮,土工管袋干化后的尾水采用超磁分离一体化设备二次处理,悬浮物SS指标均不超过4 mg·L−1,实现了疏浚土尾水的达标排放。
-
表 1 伶仃洋表层沉积物中砷富集系数统计表
Table 1. Statistics of enrichment factor of arsenic in surface sediments of Lingding Bay
富集系数Enrichment factor 富集(人为影响)程度Enrichment (human impact) degree 占比/% Percentage 2020年 2010年 ≤1 无 0.00 3.57 1—2 轻微 0.00 25.00 2—5 中度 34.62 71.43 5—20 显著 65.38 0.00 表 2 沉积物砷含量统计表(mg·kg−1)
Table 2. The statistical characteristics of arsenic in the Pearl River Estuary and Delta(mg·kg−1)
样本类型Sample type 采样时间Sampling time 含量范围Range 平均值Average 样本数Number of samples 文献Reference 分析方法Method 伶仃洋表层沉积物 2010 7.00—47.30 25.40 28 本研究 ICP-MS 2020 19.20—89.90 52.98 26 本研究 ICP-MS 珠江三角洲第四纪沉积物 — 1.00—45.71 8.17 171 [20] ICP-OES 西江沉积物(河池以下) 2015 11.12—107.18 34.23 68 [38] ICP-MS 西江沉积物(梧州以下) 2015 12.88—68.10 29.74 22 [39] ICP-OES 北江沉积物(韶关以下) 2015 1.44—95.80 28.39 16 [39] ICP-OES 东江沉积物(惠州以下) 2015 3.44—22.54 9.59 10 [39] ICP-OES 表 3 伶仃洋表层沉积物砷污染潜在生态危害系数
Eir Table 3. Potential ecological risk factor of arsenic pollution in surface sediments of Lingding Bay
Eir 风险程度 Risk degree 占比/%Percentage 2020年 2010年 Eir 轻微 15.38 82.14 40≤ Eir 中等 53.85 17.86 80≤ Eir 强 30.77 0.00 160≤ Eir 很强 0.00 0.00 Eir 极强 0.00 0.00 -
[1] 董飞, 卢瑛, 张建国, 等. 珠江三角洲稻田土壤砷及其向水稻籽粒迁移特征 [J]. 生态环境学报, 2009, 18(6): 2137-2140. doi: 10.3969/j.issn.1674-5906.2009.06.025 DONG F, LU Y, ZHANG J G, et al. Soil arsenic concentration in paddy fields and its transfer to rice (Oryza sativa L. ) grain in Pearl River Delta [J]. Ecology and Environmental Sciences, 2009, 18(6): 2137-2140(in Chinese). doi: 10.3969/j.issn.1674-5906.2009.06.025
[2] 陈保卫, LE X C. 中国关于砷的研究进展 [J]. 环境化学, 2011, 30(11): 1936-1943. CHEN B W, LE X C. Recent progress in arsenic research in China [J]. Environmental Chemistry, 2011, 30(11): 1936-1943(in Chinese).
[3] FLORA S J S (Edited). Handbook of Arsenic Toxicology[M]. Academic Press, Oxford: Academic Press, 2015. [4] WANG J W, WAN Y J, CHENG L, et al. Arsenic in outdoor air particulate matter in China: Tiered study and implications for human exposure potential [J]. Atmospheric Pollution Research, 2020, 11(4): 785-792. doi: 10.1016/j.apr.2020.01.006 [5] MATSCHULLAT J. Arsenic in the geosphere-a review [J]. Science of the Total Environment, 2000, 249(1/2/3): 297-312. [6] 王奎克, 朱晟, 郑同, 等. 砷的历史在中国 [J]. 自然科学史研究, 1982, 1(2): 115-126. WANG K K, ZHU S, ZHENG T, et al. The history of arsenic in China [J]. Studies in the History of Natural Sciences, 1982, 1(2): 115-126(in Chinese).
[7] 胡文渊, 赵帅营, 张涛, 等. 砷污染下阳宗海浮游动物群落特征及其影响因素 [J]. 生态学杂志, 2021, 40(10): 3195-3204. HU W Y, ZHAO S Y, ZHANG T, et al. Characteristics and driving factors of zooplankton community in arsenic-polluted Yangzong Lake [J]. Chinese Journal of Ecology, 2021, 40(10): 3195-3204(in Chinese).
[8] 蓝先洪. 珠江口表层沉积物的地球化学特征 [J]. 海洋湖沼通报, 1989(4): 53-61. LAN X H. Geochemical characteristics of surface sediment in the Pearl River Estuary [J]. Transactions of Oceanology and Limnology, 1989(4): 53-61(in Chinese).
[9] SMEDLEY P L, KINNIBURGH D G. A review of the source, behaviour and distribution of arsenic in natural waters [J]. Applied Geochemistry, 2002, 17(5): 517-568. doi: 10.1016/S0883-2927(02)00018-5 [10] GORNY J, BILLON G, LESVEN L, et al. Arsenic behavior in river sediments under redox gradient: A review [J]. Science of the Total Environment, 2015, 505: 423-434. doi: 10.1016/j.scitotenv.2014.10.011 [11] 温伟英, 何悦强. 珠江口海岸带底质污染现状分析[C]//珠江口海岸带和海涂资源综合调查研究文集(二). 广州: 广东科技出版社, 1985. WEN W Y, HE Y Q. Analysis on the current situation of sediment pollution in the coastal zone of the Pearl River Estuary[C]//Collected papers on the comprehensive investigation of the coastal zone and sea beach resources in the Pearl River Estuary (Ⅱ). Guangzhou: Guangdong Science and Technology Press, 1985(in Chinese).
[12] 刘芳文, 颜文, 黄小平, 等. 珠江口沉积物中重金属及其相态分布特征 [J]. 热带海洋学报, 2003, 22(5): 16-24. LIU F W, YAN W, HUANG X P, et al. Distributional characteristics of heavy metal and its available phases in sediments from Zhujiang River mouth [J]. Journal of Tropical Oceanography, 2003, 22(5): 16-24(in Chinese).
[13] 石要红, 梁开, 夏真. 珠江口伶仃洋海底表层沉积物重金属污染及潜在生态危害评价 [J]. 南海地质研究, 2006(1): 52-59. SHI Y H, LIANG K, XIA Z. Pollution of heavy metals in the Lingdingyang of Pearl River Estuary and its assessment of potential ecological risk [J]. Geological Research of South China Sea, 2006(1): 52-59(in Chinese).
[14] 甘华阳, 梁开, 郑志昌. 珠江口表层沉积物中微量元素地球化学 [J]. 海洋地质与第四纪地质, 2010, 30(4): 131-139. GAN H Y, LIANG K, ZHENG Z C. Trace elements geochemical characteristics of the surface sediments of pear river estuary [J]. Marine Geology & Quaternary Geology, 2010, 30(4): 131-139(in Chinese).
[15] 倪志鑫, 张霞, 蔡伟叙, 等. 珠江口沉积物中重金属分布、形态特征及风险分析 [J]. 海洋环境科学, 2016, 35(3): 321-328. NI Z X, ZHANG X, CAI W X, et al. Distribution, speciation and risk assessment of trace metals in surface sediment of the Zhujiang Estuary [J]. Marine Environmental Science, 2016, 35(3): 321-328(in Chinese).
[16] BI S P, YANG Y, XU C F, et al. Distribution of heavy metals and environmental assessment of surface sediment of typical estuaries in Eastern China [J]. Marine Pollution Bulletin, 2017, 121(1/2): 357-366. [17] 吴鹏, 刘永, 李纯厚, 等. 珠江口沉积物中重金属和石油污染对微生物群落结构的影响 [J]. 海洋湖沼通报, 2022, 44(1): 106-114. WU P, LIU Y, LI C H, et al. Effects of heavy metals and oil in sediments of Pearl River Estuary on microbial community [J]. Transactions of Oceanology and Limnology, 2022, 44(1): 106-114(in Chinese).
[18] 黄镇国, 李平日, 张仲英. 珠江三角洲形成发育演变[M]. 广州: 科学普及出版社广州分社, 1982. HUANG Z G, LI P R, ZHANG Z Y, et al. Formation, development and evolution of Pearl River Delta[M]. Guangzhou: Guangzhou Branch of Science Popularization Press, 1982(in Chinese).
[19] XIONG H X, ZONG Y Q, HUANG G Q, et al. Human drivers accelerated the advance of Pearl River Deltaic shoreline in the past 7500 years [J]. Quaternary Science Reviews, 2020, 246: 106545. doi: 10.1016/j.quascirev.2020.106545 [20] 唐志敏, 侯青叶, 游远航, 等. 珠三角平原区第四系剖面重金属分布特征及其影响因素 [J]. 地球科学进展, 2017, 32(8): 885-898. TANG Z M, HOU Q Y, YOU Y H, et al. Distribution characteristics and influencing factors of heavy metals in Pearl River Delta quaternary boreholes [J]. Advances in Earth Science, 2017, 32(8): 885-898(in Chinese).
[21] ZOLLER W H, GLADNEY E S, DUCE R A. Atmospheric concentrations and sources of trace metals at the South pole [J]. Science, 1974, 183(4121): 198-200. doi: 10.1126/science.183.4121.198 [22] 李文胜, 窦磊, 刘子宁. 珠江三角洲平原区第四纪沉积物地球化学特征及其控制因素 [J]. 华南地质与矿产, 2016, 32(1): 68-77. LI W S, DOU L, LIU Z N. Element geochemical characteristics and controlling factors of the Quaternary Sediments in the Pearl River Delta plain [J]. Geology and Mineral Resources of South China, 2016, 32(1): 68-77(in Chinese).
[23] HAKANSON L. An ecological risk index for aquatic pollution control. a sedimentological approach [J]. Water Research, 1980, 14(8): 975-1001. doi: 10.1016/0043-1354(80)90143-8 [24] 徐争启, 倪师军, 庹先国, 等. 潜在生态危害指数法评价中重金属毒性系数计算 [J]. 环境科学与技术, 2008, 31(2): 112-115. XU Z Q, NI S J, TUO X G, et al. Calculation of heavy metals' toxicity coefficient in the evaluation of potential ecological risk index [J]. Environmental Science & Technology, 2008, 31(2): 112-115(in Chinese).
[25] 贾钧博, 张嘉成, 张浩楠, 等. 珠江口水体中重金属含量及其生态风险评价 [J]. 东莞理工学院学报, 2021, 28(1): 54-60. JIA J B, ZHANG J C, ZHANG H N, et al. Content and ecological risk assessment of heavy metal in Pearl River Estuary [J]. Journal of Dongguan University of Technology, 2021, 28(1): 54-60(in Chinese).
[26] 杜韶娴. 珠江出海口门水环境中砷、汞、铅、镉的测定及评价[D]. 广州: 华南理工大学, 2012. DU S X. Determination and evaluation of arsenic, mercury, lead and cadmium in the water environment of the Pearl River Estuary[D]. Guangzhou: South China University of Technology, 2012 (in Chinese).
[27] 张亚南, 贺青, 陈金民, 等. 珠江口及其邻近海域重金属的河口过程和沉积物污染风险评价 [J]. 海洋学报, 2013, 35(2): 178-186. ZHANG Y N, HE Q, CHEN J M, et al. Heavy metals' process in water and pollution risk assessment in surface sediments of the Zhujiang River Estuary [J]. Acta Oceanologica Sinica, 2013, 35(2): 178-186(in Chinese).
[28] 张银英, 郑庆华, 何悦强, 等. 珠江口咸淡水交汇区水中CODMn、油类、砷自净规律的试验研究 [J]. 热带海洋, 1995, 14(3): 67-74. ZHANG Y Y, ZHENG Q H, HE Y Q, et al. An experimental study on the self-purification of CODMn, oil and As in the mixing area of saltwater and freshwater in Zhujiang River Estuary [J]. Tropic Oceanology, 1995, 14(3): 67-74(in Chinese).
[29] 柯东胜. 珠江口海水中砷的含量和分布 [J]. 海洋环境科学, 1985, 4(2): 24-27. KE D S. Content and distribution of arsenic in seawater of the Pearl River Estuary [J]. Marine Environmental Science, 1985, 4(2): 24-27(in Chinese).
[30] KALIA K, KHAMBHOLJA D B. Arsenic contents and its biotransformation in the marine environment//Hand-book of arsenic toxicology[M]. Oxford: Academic Press, 2015: 675-700. [31] 柳青青, 杨忠芳, 周国华, 等. 中国东部主要入海河流As元素分布、来源及影响因素分析 [J]. 现代地质, 2012, 26(1): 114-124. LIU Q Q, YANG Z F, ZHOU G H, et al. Distribution, sources and impact factors of arsenic in the major rivers of Eastern China [J]. Geoscience, 2012, 26(1): 114-124(in Chinese).
[32] TAYLOR S R, McLENNAN S M. The geochemical evolution of the continental crust [J]. Reviews of Geophysics, 1995, 33(2): 241-265. doi: 10.1029/95RG00262 [33] HANS WEDEPOHL K. The composition of the continental crust [J]. Geochimica et Cosmochimica Acta, 1995, 59(7): 1217-1232. doi: 10.1016/0016-7037(95)00038-2 [34] WU W H, QU S Y, NEL W, et al. Tracing and quantifying the sources of heavy metals in the upper and middle reaches of the Pearl River Basin: New insights from Sr-Nd-Pb multi-isotopic systems [J]. Chemosphere, 2022, 288: 132630. doi: 10.1016/j.chemosphere.2021.132630 [35] 张秀芝, 鲍征宇, 唐俊红. 富集因子在环境地球化学重金属污染评价中的应用 [J]. 地质科技情报, 2006, 25(1): 65-72. ZHANG X Z, BAO Z Y, TANG J H. Application of the enrichment factor in evaluating of heavy metals contamination in the environmental geochemistry [J]. Geological Science and Technology Information, 2006, 25(1): 65-72(in Chinese).
[36] SUTHERLAND R A. Bed sediment-associated trace metals in an urban stream, Oahu, Hawaii [J]. Environmental Geology, 2000, 39(6): 611-627. doi: 10.1007/s002540050473 [37] BLASER P, ZIMMERMANN S, LUSTER J, et al. Critical examination of trace element enrichments and depletions in soils: As, Cr, Cu, Ni, Pb, and Zn in Swiss forest soils [J]. Science of the Total Environment, 2000, 249(1/2/3): 257-280. [38] 汝旋. 人类活动对河流表层沉积物中重金属分布区域差异性的影响评估: 以西江为例[D]. 广州: 华南理工大学, 2018. RU X. Impact assessment of human activities on regional difference of heavy metals distribution in river surface sediments-Taking Xijiang River as an example[D]. Guangzhou: South China University of Technology, 2018 (in Chinese).
[39] 唐志敏. 珠江水系对冲积平原区土壤环境质量的影响[D]. 北京: 中国地质大学(北京), 2017. TANG Z M. Influence of Pearl River system on soil environmental quality in alluvial plain area[D]. Beijing: China University of Geosciences, 2017 (in Chinese).
[40] 赵艺, 刘子宁, 陈恩. 珠江水系沉积物重金属元素含量特征及评价 [J]. 地球, 2013, 7: 273-273,120. ZHAO Y, LIU Z N, CHEN E. Content characteristics and evaluation of heavy metals in sediments of Pearl River system [J]. The Earth, 2013, 7: 273-273,120(in Chinese).
[41] LI C, SANCHEZ G M, WU Z F, et al. Spatiotemporal patterns and drivers of soil contamination with heavy metals during an intensive urbanization period (1989–2018) in Southern China [J]. Environmental Pollution, 2020, 260: 114075. doi: 10.1016/j.envpol.2020.114075 [42] 安礼航, 刘敏超, 张建强, 等. 土壤中砷的来源及迁移释放影响因素研究进展 [J]. 土壤, 2020, 52(2): 234-246. AN L H, LIU M C, ZHANG J Q, et al. Sources of arsenic in soil and affecting factors of migration and release: A review [J]. Soils, 2020, 52(2): 234-246(in Chinese).
[43] 黄光庆, 杨龙, 蒋冲, 等. 粤港澳大湾区城市群生态系统变化研究[M]. 广州: 广东省科技出版社, 2022. HUANG G Q, YANG L, JIANG C, et al. Study on the ecosystem change of urban agglomeration in the Greater Bay Area of Guangdong, Hong Kong and Macao [M]. Guangzhou: Guangdong Science and Technology Press, 2022(in Chinese).
[44] 吴万富, 徐艳, 史德强, 等. 我国河流湖泊砷污染现状及除砷技术研究进展[J]. 环境科学与技术, 2015, 38(增刊1): 190-197. WU W F, XU Y, SHI D Q, et al. The arsenic pollution status of the rivers and lakes in China and the research progress on arsenic removal techniques[J]. Environmental Science & Technology, 2015, 38(Sup 1): 190-197 (in Chinese).
[45] DANG D H, TESSIER E, LENOBLE V, et al. Key parameters controlling arsenic dynamics in coastal sediments: An analytical and modeling approach [J]. Marine Chemistry, 2014, 161: 34-46. doi: 10.1016/j.marchem.2014.02.005 [46] LI L, REN J L, CAO X H, et al. Process study of biogeochemical cycling of dissolved inorganic arsenic during spring phytoplankton bloom, southern Yellow Sea [J]. Science of the Total Environment, 2017, 593/594: 430-438. doi: 10.1016/j.scitotenv.2017.03.113 -






 DownLoad:
DownLoad: