-
自2019年底以来,由严重急性呼吸综合征冠状病毒-2(Severe Acute Respiratory Syndrome Coronavirus 2,SARS-CoV-2)引发的新型冠状病毒肺炎疫情(Coronavirus disease 2019,COVID-19)仍在全球范围内蔓延. 截止2022年10月5日,已有615,777,700例确诊,6,527,192个死亡病例[1]更新为最新数据. 新冠病毒疫情已成为全世界二战以来最严重的突发公共卫生事件,严重危害人类健康并阻碍了社会经济发展. SARS-CoV-2是一种具有囊膜、基因组为线性单股正链的RNA病毒,具有非常强的传染性,主要通过飞沫、密切接触和气溶胶等途径传播[2]. 消毒是传染病疫情防控的有效手段,是确保“大灾之后无大疫”的有力保障,对保证人民的生命健康具有重要作用.
新冠疫情后,气载病原体及其引起的健康危害受到越来越多的关注. 但是,过量使用消毒剂可导致显著的人体健康危害[3-4]. 大规模环境消杀后,残留消毒剂和消毒副产物会成为新的污染源,危及环境和生态安全[5]. 本文总结了气载病原体、国内外相关标准、常用空气消毒方式及其灭活效果以及残留消毒剂和消毒副产物的生态及健康危害,并展望了未来的发展趋势.
-
气载病原体包括致病细菌、致病真菌及病毒等,它们可附着在细微颗粒物上,或以气溶胶的形式在空气中扩散并传播,可引起呼吸系统疾病[6-7]. 常见的病原微生物及其相关疾病如表1所示.
-
在室内外大气环境中检测到许多病原菌,如假单胞菌(Pseudomonas)、乳球菌(Lactococcus)、不动杆菌(Acinetobacter)、棒状杆菌(Corynebacterium)、葡萄球菌(Staphylococcus)和芽孢杆菌(Bacillus)等[28-30]. 相比于普通细菌,病原菌对极端环境的耐受能力更强[31]. 例如,芽孢杆菌可以形成卵圆形的内生孢子从而具有更强的耐受能力,有研究表明其相对丰度随着空气质量恶化而增加[32]. 芽孢杆菌是一种常见的病原菌,不仅存在于室外大气中,而且广泛存在于一些特殊的空气环境中,如垃圾焚烧厂[9]、医院[10]和污水处理厂[11]等. 蜡状芽孢杆菌可引起人类食物中毒、严重感染和菌血症[12].
多重耐药细菌在医院环境很常见,如耐头孢他啶铜绿假单胞菌和耐亚胺培南鲍曼不动杆菌[33-34]. 金黄色葡萄球菌是一种共生菌,也是一种条件致病菌[35],可导致皮肤感染、血流感染、感染性心内膜炎、骨髓炎和肺部感染. 金黄色葡萄球菌易获得耐药基因,尤其容易耐甲氧西林,并在医院废水中被检出[15-17]. 病原微生物的耐药性给疾病治疗带来困难,对人体健康产生极大威胁.
-
气载病毒主要包括鼻病毒(Rhinovirus)、流感病毒(Influenza virus)、水痘-带状疱疹病毒(Varicella-zoster virus)、麻疹病毒(Measles virus)、腮腺炎病毒(Mumps virus)、汉坦病毒(Hantavirus)以及冠状病毒(Coronavirus)等[21-27]. 这些病毒可能会引发流感、水痘、麻疹、腮腺炎以及呼吸道疾病等. 呼吸道病毒可通过飞沫、密切接触和气溶胶传播. 流感病毒、鼻病毒和新冠病毒等均可通过生物气溶胶传播[2].
-
空气中的优势真菌主要包括青霉菌(Penicillium)、链格孢菌(Alternaria)、枝孢菌(Cladosporium)和曲霉菌(Aspergillus)等[36]. 真菌是潜在的过敏原,接触其孢子可能会引起易感个体的免疫反应,可能导致过敏性鼻炎、支气管哮喘或外源过敏性肺泡炎等疾病发生[37]. 在家禽养殖场和谷磨厂等空气中,青霉菌、曲霉菌和毛霉菌(Mucor)为优势菌[38]. 在医院环境中常见真菌包括曲霉菌、青霉菌、镰刀菌(Fusarium)、枝孢菌等,均具有潜在的致病性[19-20]. 新生隐球菌(Cryptococcus neoformans)是一种病原真菌,其可通过呼吸道进入人体引发致命的隐球菌脑膜炎[39].
-
我国最新《室内空气质量标准》(GB/T18883—2022)只对空气中细菌总数进行了限定,采用撞击式微生物采样器采样,其标准限值为1500 CFU·m−3,对真菌和病毒没有限值[40]. 国内研究一般使用由中国科学院生态中心推荐使用的大气微生物评价建议标准对大气空气微生物污染状况进行评价,该标准评价内容如表2所示[41]. 我国各公共场所空气质量标准如表3所示[42]. 不同国家或组织提供的生物气溶胶细菌和真菌的标准差距较大,各国细菌限值标准在500—10000 CFU·m−3之间[43-44],真菌限值标准则在50—2500 CFU·m−3之间[44-45],但是由于各国采样标准与环境不同,仅对数值进行对比参考意义较小[46]. 其中美国食品药物管理局(U. S. Food and Drug Administration)不提供具体限制数值;欧盟则根据病原微生物浓度进行污染程度分类[42].
-
常用消毒方法按照作用原理可分为物理消毒和化学消毒两大类,各消毒方式主要作用机理及优缺点如表4所示.
-
紫外线消毒是一种公认的高效杀菌方法,其因使用方便且无化学残留在医院及许多公共场所广泛应用[52]. 紫外光的波长范围为10—400 nm,低于240 nm的紫外线易产生臭氧[53]. 紫外线辐照会破坏或改变微生物的遗传物质(DNA和RNA),形成胸腺嘧啶二聚体(遗传物质的光产物),干扰核酸的复制和转录,从而导致微生物死亡[54]. 紫外线空气消毒的效率取决于空气微生物对紫外线的敏感性、紫外线辐照度强度和紫外线辐照剂量[55]. 紫外线对病毒、细菌、原生动物和真菌都有良好的消杀效果[56]. Kim等[57]研究表明,254 nm低压汞紫外灯(强度为1.5—4.6 mJ·cm−2)对鼠伤寒沙门氏杆菌、单核细胞增生李斯特菌、大肠杆菌、黄曲霉菌和金黄色葡萄球菌气溶胶的去除率可达到99.68%—99.99%. Yang等[58]研究表明,在通风管道中,紫外线对空气中粘质沙雷氏菌、产碱假单胞菌、大肠杆菌、肠沙门氏菌和表皮葡萄球菌的消杀效果较好,在高入口速度(6 m·s−1)的条件下,对被试菌中耐光性最强的表皮葡萄球菌的灭活率为76.1%. Walker等[59]研究发现,噬菌体MS2和腺病毒气溶胶都对紫外线消毒有很强的抵抗力,而冠状病毒气溶胶的敏感性则是MS2和腺病毒气溶胶的7倍至10倍,更容易被消灭. 与细菌气溶胶不同,对于紫外线消毒,高相对湿度对病毒气溶胶没有显著保护作用. 杨晶雪等[60]研究表明,在医院环境中经紫外线直接照射法消毒10 min时,根据室内空气菌落数计算,空气灭菌率为31.45%;消毒20 min时,空气灭菌率为63.24%;消毒30 min时,空气灭菌率可达到89.44%,空气中含菌量合格.
紫外线消毒虽然具有诸多优点,但杀菌波长的紫外线直接照射到人体皮肤上会造成损伤,特别是眼睛对紫外线格外敏感. 除此之外,紫外线消毒后的细菌仍存在光复活的风险,这可能会降低紫外消毒的效率[61].
-
2020年,国家卫生健康委员会颁布了《消毒剂使用指南》[62]以规范化学消毒剂的使用方法. 当前,国内外常用的消毒剂主要有8类,包括醇类消毒剂、含氯消毒剂、过氧化物类消毒剂、季铵盐类消毒剂、醛类消毒剂、酚类消毒剂、含碘消毒剂和过硫酸氢钾类[63]. 常用于空气消毒的消毒剂有含氯消毒剂和过氧化物类消毒剂.
-
含氯消毒剂是高效的广谱消毒剂,包括次氯酸盐、次氯酸(HOCl)、二氧化氯(ClO2)和三氯异氰尿酸(C3O3N3Cl3)等[62]. HOCl可以穿透细菌细胞壁,通过破坏细胞膜上的结合酶阻断细胞呼吸,破坏细胞膜的脂质和蛋白质改变细胞膜通透性,造成胞内离子、DNA和蛋白质泄露,从而导致细胞内稳态的恶化,最终使细胞死亡[64-65]. 对于病毒,HOCl破坏其蛋白质外壳并损伤其核酸,抑制遗传功能从而达到消灭效果[66]. 次氯酸水主要成分为HOCl,还含有多种氧化剂和自由基,除游离氯外还具有其他抗菌活性.
有研究表明,HOCl对10种细菌和2种真菌(白色念珠菌和黑曲霉菌)均有显著杀灭效果[67]. Hakimullah等[68]研究表明,使用含有100 mg·L−1活性氯的次氯酸水对农场含有新城疫病毒的气溶胶进行消毒可以使病毒完全灭活. Boecker等[69]验证了HOCl可对人口稠密的室内场所进行空气消毒,该研究认为,使用200 mg·L−1活性氯浓度的HOCl进行空气消毒预计不会刺激人体组织.
次氯酸钠(NaClO)是常用的含氯消毒剂之一,具有价格低廉和消毒效果好等优点[70],经常用于物体表面消毒和空气消毒. NaClO在水中水解成的HOCl是其消毒的有效成分,因此其消毒机制与HOCl大致相同. Ishikawa等[71]研究表明,83 mg·L−1的雾化NaClO在饱和湿度下能够杀灭枯草芽孢杆菌孢的活性.
ClO2是一种高效广谱消毒剂,它对细菌(铜绿假单胞菌、大肠杆菌[72]、金黄色葡萄球菌和鲍曼不动杆菌[73]等)、病毒(脊髓灰质炎病毒[74]、人流感病毒[75]和麻疹病毒 [76]等)、真菌(木霉属、青霉属[77]等)及原生生物[78]都具有较强的灭活能力. ClO2可快速穿透细胞壁,其可以氧化细胞内的氨基酸如半胱氨酸、酪氨酸和色氨酸以及细胞内含巯基的酶,从而阻止蛋白质的合成和细菌代谢,导致细菌死亡[79]. ClO2能改变病毒蛋白质成分,使病毒外壳蛋白失活从而抑制病毒攻击宿主细胞的能力[80]. 也有研究表明,ClO2对基因组破坏效果较小,不抑制基因组的复制功能[81]. Lu等[82]研究表明,0.3 mg·m−3的ClO2雾化消毒可以有效降低宠物店室内生物气溶胶浓度,并且较快的气流速度有利于雾化ClO2消毒剂在室内空间的扩散,从而提高消毒性能. 在学校食堂[83]和图书馆中[84],ClO2消毒也可以有效降低气溶胶中细菌和真菌数量. Boonrattanakij等[85]研究表明,使用0.3 mg·m−3的ClO2对健身房的空气进行15 min消毒后,空气中细菌和真菌浓度符合官方空气质量标准,且气流速度对细菌和真菌的去除没有显著影响,这可能是因为在该研究中使用的气流速度(0.3 m·min−1)已足以将消毒剂快速扩散到房间空间中.
在用于处理物体表面微生物时,与HClO和ClO2相比,NaClO活性较低. Thorn等[86]研究表明,在100 mg·L−1游离氯的浓度下,对金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌和临床耐甲氧西林金黄色葡萄球菌菌株的生物气溶胶消毒效果顺序为次氯酸水>ClO2>NaClO. 还有研究表明,ClO2的抗病毒性能比NaClO约高出10倍[9]. Erosy等[65]通过次氯酸水、NaClO和ClO2对粪肠球菌的消毒作用也发现其灭菌活性顺序为次氯酸水>ClO2>NaClO. 3种消毒剂都通过破坏细胞膜完整性、使离子浓度失衡和破坏细胞成分(如DNA、蛋白质和脂质分子)等途径来灭活细菌. 尽管NaClO消毒剂效果逊于次氯酸水和ClO2,但由于次氯酸水和ClO2化学性质不稳定,用于消毒时常常需要现场生成,与之相比,NaClO更容易储存. HOCl使用简便、安全,对人体无刺激性损伤,更适于临床推广[87].
-
过氧化物消毒剂主要有过氧化氢(H2O2)、过氧乙酸(CH3COOOH)、过氧戊二酸(C10H14O8)和臭氧(O3),有效成分主要是活性氧物种(reactive oxygen species,ROS),其主要是通过氧化破坏细胞膜、损坏细胞内蛋白质和核酸以及抑制能量生产,从而抑制微生物生长与繁殖[88-90]. 过氧化物类消毒剂对于细菌、孢子、真菌和病毒(如轮状病毒、腺病毒、甲型流感病毒和脊髓灰质炎病毒)等微生物具有广谱高效的杀灭作用[91-93].
H2O2是常用的过氧化物消毒剂. Masotti等[94]研究表明,H2O2雾化消毒和O3消毒均可有效灭活乳品厂室内空气中枝孢菌属、青霉菌属、隐球菌属、德巴利菌属、棒状菌属和孢子菌属等微生物. Choi等[95]验证了H2O2雾化消毒是医院环境进行消毒的有效方法,医院病房和急诊室经消毒后表面取样,革兰氏阳性菌CFUs数量下降超过90%. Popov等[96]也证实了H2O2气雾剂可以显著减少医院空气和物体表面微生物污染. Tuladhar等[93]研究表明,176 μg·L−1的H2O2蒸汽是一种有效的杀病毒剂,可有效杀灭室内空气中肠道和呼吸道病毒,包括脊髓灰质炎病毒、人类诺如病毒、鼠诺如病毒、轮状病毒、腺病毒和甲型流感(H1N1)病毒. Horn等[97]]研究发现,H2O2蒸汽消毒与病房中艰难梭菌(从1.38例到0.90例/1000个患者日)、耐万古霉素肠球菌(从0.21例到0.01例/1000个患者日)和产超广谱β-内酰胺酶的革兰氏阴性菌(从0.16例到0.01例/1000个患者日)的感染显著减少相关.
O3在空气中快速分解生成活性氧原子(O)或与水分子反应生成羟基自由基(OH·),它们可以通过氧化微生物中的不饱和键使得蛋白质以及核酸等物质变性,从而杀灭微生物,其在室内空气清洁[98]、食品保鲜[99]和医院消毒[100]等方面都有广泛应用. Girgin等[101]研究发现当O3接触细菌的细胞壁时,其氧化作用会在细胞中产生孔洞,随着孔洞扩大细菌就会失去形状,发生破裂. O3可能与真菌孢子外壳、核酸物质以及细胞内的酶发生反应并导致真菌死亡[102]. O3灭活病毒的主要机制是对遗传物质的直接破坏,O3还可能对病毒的外部蛋白质衣壳层造成损害[103]. Manning等[104]研究表明,O3可有效杀灭N95口罩中的铜绿假单胞菌. Ding等[105]研究表明O3消毒对耐氯孢子有效,因为它会破坏细胞结构和基因片段. O3生成简单,成本低廉,使用安全,可快速分解回氧气,不会产生消毒副产物,半衰期约为20 min,由于气体可以渗透到房间的所有区域,它比液体喷雾消毒剂更具穿透性[106]. O3的氧化活性是HOCl的25倍,是次氯酸盐的2500 到3000倍[107].
张淼等[108]研究表明,低剂量C10H14O8对公共场所空气消毒效果显著,消毒后公共场所的空气质量达到国家标准,消毒作用持续时间可达100 min以上. 谭金煜等[109]在医院采取CH3COOOH气溶胶喷雾法与气体熏蒸消毒法对病房进行消毒. 结果表明两种消毒方式全部合格,但气溶胶喷雾法由于操作简单优于气体熏蒸消毒法. Tso等[110]研究表明,相对于H2O2和CH3COOOH,ClO2更适合用于消灭副溶血性弧菌. Chhetri等[111]研究表明ClO2、CH3COOOH和H2O2的对藻类的毒性依次降低.
对于一些微生物来说,H2O2的消毒效果显著优于NaClO. Montagna等[112]研究发现1.5% H2O2对铜绿假单胞菌、肺炎克雷伯菌、粪肠球菌和金黄色葡萄球菌菌株的消毒效果明显高于5% NaClO(P<0.0001). Barbut等[113]研究表明,在有艰难梭菌感染患者的房间使用50 mL·m−3的H2O2干雾消毒系统对艰难梭菌孢子的空气消毒效果明显优于0.5% NaClO溶液,为艰难梭菌感染患者的室内消毒提供了一种新的选择. 但也有研究表明,对于某些微生物而言,NaClO消毒剂的消毒效果更优. Kingsley等[114]研究表明,诺如病毒对几种常用过氧化物消毒剂如ClO2、CH3COOOH和H2O2具有明显的抗性,而氯(NaClO)消毒剂则可以作为诺如病毒的有效消毒剂. Lineback等[115]研究发现,对于金黄色葡萄球菌和铜绿假单胞菌,NaClO和H2O2消毒剂的杀菌效果明显高于季铵氯化物消毒剂.
-
等离子体是气体在高压作用下发生电离后产生的电中性气态物质,被称为物质存在的第4种形态,等离子体中包括大量高活性物质,如活性氧(原子氧、单线态氧、超氧阴离子、O3和羟基自由基)和活性氮(原子氮、激发态氮和一氧化氮)等[116]. 等离子体消毒快速高效,可用于物体表面消毒和空气消毒. 等离子体消毒的主要机制是活性氧、羟基自由基、O3和其他活性粒子共同作用于微生物,导致微生物灭活,这些基于氧和氮的活性物质对脂质、蛋白质和DNA等生物分子具有强烈的氧化作用[117]. 研究发现,等离子体消毒对白色葡萄球菌有良好消灭效果,并且在一定范围内,对空气消毒效果随温度和湿度的升高而增强,与作用时间成正比[118]. Zhang等[119]研究发现,等离子体消毒在冷链环境空气中灭活新冠病毒具有良好效果,等离子体产生的活性物质灭活病毒的能力优于传统O3消毒. 闫妍等[120]研究发现,高压放电激发产生的等离子体与电极板上的纳米二氧化钛光触媒系统协同作用,对空气中白色葡萄球菌和H1N1甲型流感病毒都有良好消杀效果. 非热大气等离子体处理和脉冲氙紫外线(PX-UV)处理广泛用于医院环境的消毒,对金黄色葡萄球菌、表皮葡萄球菌和酵母菌都有良好消灭效果[121]. 然而等离子体消毒过程中会有O3和氮氧化物等副产物的产生,并且等离子体消毒价格昂贵且操作具有一定的危险性.
-
半导体材料在光激发下会产生光生电子空穴对,其具有很强的氧化/还原能力,与氧气或水反应可以生成活性氧物种(ROS),如·OH、·O2−和H2O2等. 常用的光催化消毒材料还包括ZnO、Bi2WO6、NiMoO4和Pd-BiFeO3等[122]. 光催化消毒具有高效、低成本、安全等优点,其杀伤机制为氧化导致细胞壁和细胞质膜的降解,进而引起细胞内容物泄漏、细胞溶解、核酸受到破坏,最终导致生物体的完全矿化[123]. 光催化对大肠杆菌、乳酸杆菌、耐甲氧西林金黄色葡萄球菌、铜绿假单胞菌等细菌,黑曲霉菌青霉菌酵母菌等真菌,脊髓灰质炎病毒、人流感病毒和SARS冠状病毒以及原生动物和藻类都有良好消杀效果[124]. 二氧化钛(TiO2)光催化剂能够杀死多种革兰氏阴性和革兰氏阳性细菌、丝状和单细胞真菌、藻类、原生动物、哺乳动物病毒和噬菌体[125]. 磁性g-C3N4/NiFe2O4复合材料也是一种具有高消毒活性的光催化材料,可以有效杀灭黄曲霉[126].
-
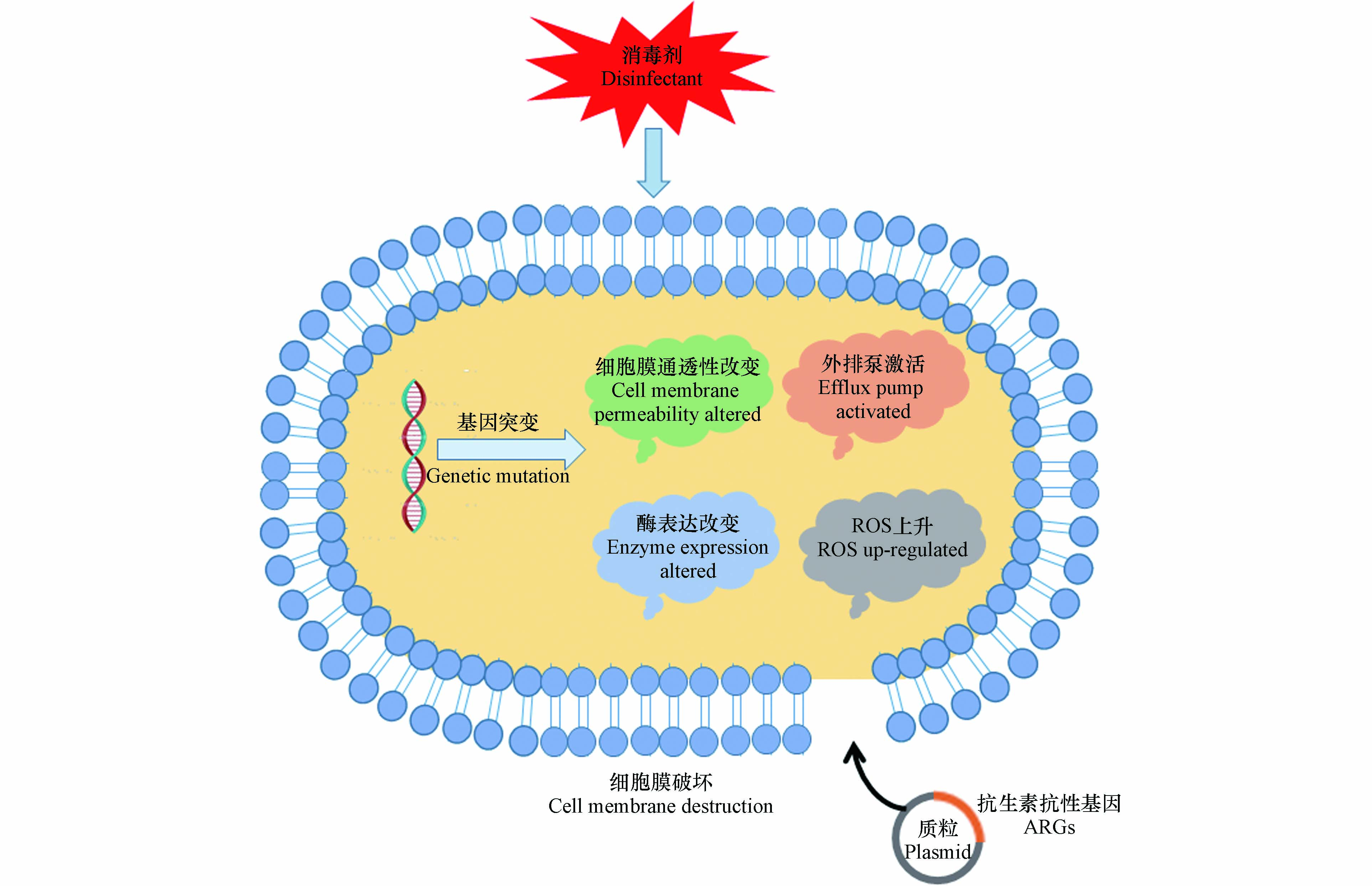
消毒剂大量使用会增加消毒剂抗性和抗生素耐药性,从而导致了全球严重的生态安全问题. 越来越多的研究报道了氯消毒剂在促进消毒剂抗性和抗生素耐药性方面的作用. Khan等[127]研究表明,细菌对氯消毒剂的抗性与抗生素耐药性之间显著相关. Lu等[4]指出,新冠病毒疫情期间消毒抗菌剂的过度使用可加速耐药菌的产生及传播,从而增加耐药菌大流行到来的风险,并威胁未来的公共健康. 常用空气消毒方式诱导病原菌产生耐药性的机理如图1所示.
-
各种消毒剂的强氧化性会引起微生物的氧化应激反应. 消毒剂诱导细菌形成抗生素抗性细菌(antibiotic resistance bacteria, ARB)是通过氧化应激诱导的基因表达或突变等方式. 多种消毒剂可以诱导基因突变,通过细胞膜通透性的改变、抗生素靶位点的修饰、降解抗生素或外排泵的激活[128]来增强微生物的抗生素抗性.
Tong等[129]研究表明,100 mg·L−1 NaClO可增加假单胞菌属的消毒剂抗性和抗生素耐药性. 由氧化应激引发的SOS反应(对DNA损伤的保护反应)使细菌对氯消毒剂产生抗性. 抗生素耐药性的增加可归因于膜通透性降低,MuxABC-OpmB外排泵、β-内酰胺酶和抗氧化酶的表达增加. 研究结果揭示了氯消毒剂对促进微生物的消毒剂抗性和抗生素耐药性的影响. Hou等[130]研究表明,铜绿假单胞菌在暴露于4 mg·L−1 NaClO后对头孢他啶、氯霉素和氨苄青霉素的耐药性提高了1.4—5.6倍. 并且发现GPx和SOD水平显著提高,这两种抗氧化酶保护细菌免受ROS损失. 由氧化应激反应引起的MexEF-OprN 外排泵的表达提高是抗生素耐药性增加的主要原因. Lv等[131]研究4种典型的消毒副产物二溴乙酸、二氯乙腈、溴酸钾和3-氯-4-(二氯甲基)-5-羟基-2(5H)-呋喃酮(MX)对细菌耐药性的影响,铜绿假单胞菌暴露于消毒副产物后,对10种单独抗生素和多种抗生素的耐药性均出现不同程度的提高,得出结论所选择的消毒副产物可以诱导抗生素耐药性,甚至是多药耐药性产生. 林辉等[132]发现,在医院环境中,由于消毒剂的频繁使用,导致了菌株对消毒剂产生抗性. 比如物体表面消毒时,消毒剂氯含量达到1000 mg·L−1才能消灭微生物. 在医院污染监控中采集的7株产β-内酰胺酶的铜绿假单胞菌的含氯消毒剂杀灭率与标准菌株的含氯消毒剂杀灭率相比呈不同程度降低.
-
消毒剂可以促进基因水平转移使得细菌获得外源性可移动遗传元件,如携带抗生素抗性基因(antibiotic resistance genes, ARGs)的质粒和整合子等,从而使ARGs在属间交换或产生新型ARB,并且可移动遗传元件较难被消毒剂降解[133-134]. Zhang等[135]研究发现,3种广泛使用的消毒剂(游离氯、氯胺和H2O2)在亚抑制浓度下可以促进ARGs在大肠杆菌菌株内以及从大肠杆菌到鼠伤寒沙门氏菌的跨属转移. 然而,暴露于高于亚抑制浓度的消毒剂则会显著抑制ARGs转移.
目前尚未发现紫外线消毒诱导病原菌产生耐药性的证据. Choi等[136]将耐甲氧西林金黄色葡萄球菌(MRSA)、产碳青霉烯酶(KPC)的肺炎克雷伯菌和产金属β-内酰胺酶(MBL)的肺炎克雷伯菌连续暴露于紫外线辐照25个生长周期循环,结果表明多重耐药细菌暴露于紫外线后,不会产生紫外线抗性. 紫外线/氯处理可以潜在地提高再生水的微生物安全性,减少ARGs和移动遗传元件(MGEs)的数量[137].
-
据报道,疫情暴发以来,武汉市消毒剂的累积使用量超过了5000 吨,其中以含氯消毒剂为主[5]. 含氯消毒剂可以与环境中污染物产生化学反应,生成多种消毒副产物(DBPs)[138]. 这些残留的化学消毒剂及DBPs会通过自然沉降、雨水冲刷等方式进入水环境和土壤环境,造成二次污染. 消毒剂残留及消毒副产物可直接作用于水生生物和微生物,从而影响到水生态系统[138].
新冠疫情期间(2020年2—3月),武汉市部分湖泊水体上覆水中余氯最高检出值达0.4 mg·L−1. 随着疫情的持续,武汉市河湖水环境中消毒剂的残留现象仍然持续[5]. 同年9月,张坤锋等[139]对武汉市饮用水水源进行采样,结果表明,采样的26个点位中仍有16个检出游离氯或总余氯,部分点位游离氯超过了国家地表水标准,其中最大浓度为0.04 mg·L−1. 同时在10个点位中检出24种DBPs,总DBPs浓度范围为0.11—104.73 μg·L−1,平均值7.26 μg·L−1. 生态风险评估结果表明,三氯甲烷对水生生物有较高的生态风险. 有研究表明,DBPs可能会改变浮游植物群落的结构,可能会促进水生生态系统中蓝藻水华的爆发[140].
-
美国环境保护署(U.S. Environmental Protection Agency, US EPA)设置的空气氯暴露浓度限值为0.5 mL·m−3,短期暴露于空气中的氯时,1—3 mL·m−3会轻微刺激鼻子,5 mL·m−3造成眼睛刺激,5—15 mL·m−3引发喉咙刺激,30 mL·m−3造成即刻胸痛、呕吐、呼吸频率变化和咳嗽,40—60 mL·m−3引起肺损伤(中毒性肺炎)和肺水肿(肺部液体),接触430 mL·m−3 30 min后死亡,在接触1000 mL·m−3后几分钟死亡[3]. 这些影响还取决于暴露的时间. 一般来说,患有呼吸道疾病的人,如过敏或花粉热,或重度吸烟者,往往比健康的人或非吸烟者受到更严重的影响[3].
HOCl是人体天然存在的抗菌剂. 在活化的中性粒细胞中,氯离子通过过氧化反应生成HOCl,其有助于抵抗感染[141]. HOCl消毒剂的pH值接近中性,氯浓度较低,对人体健康无害[142].
NaClO的高氧化性则对人体具有一定的毒害作用. Slaughter等[143]总结了NaClO中毒的临床病例,发现NaClO引起的毒性与其氧化能力和溶液的pH值有关,其与黏膜和皮肤接触时具有腐蚀性. NaClO少量意外摄入不太可能引起临床显著毒性,但大量摄入可能会导致腐蚀性胃肠道损伤和全身损伤,包括代谢性酸中毒、高钠血症和高氯血症. 长期或广泛皮肤接触NaClO可能导致皮肤刺激或皮肤损伤,高浓度接触则会导致严重的化学皮肤灼伤. 仅吸入少量NaClO可能会对上呼吸道造成轻微刺激. 眼部暴露于NaClO引起的角膜损伤通常是轻微的,伴有灼热不适和角膜上皮的表面紊乱,并在1 d或2 d内恢复. 较高浓度的NaClO可能会引起严重的眼睛刺激. 采用NaClO消毒也会产生较多的消毒副产物,如三氯乙酸、二氨乙酸和氯仿等,对人体具有毒害作用. 但是有研究表明少量NaClO的短时间暴露不会引起急性毒性作用. Murashevych等[144]研究证明,含有(1.7±0.13)mg·m−3活性氯的NaClO气溶胶吸入不会引起大鼠急性毒性作用.
根据美国国家职业安全与健康研究所(NIOSH))的标准,ClO2工作8 h平均允许暴露水平为0.1 mL·m−3,短期(15 min)暴露水平限值为0.3 mL·m−3[145]. 高浓度ClO2的强氧化性也会引起人体毒性作用. Lardieri等[146]统计了一些已发表的病例报告中描述的高浓度ClO2的毒性作用,包括引发高铁血红蛋白血症、中毒性刺激性皮炎、菊池藤本病和溶血性贫血. 在作者统计的55个病例中,有45例属于急性毒性,6例属于慢性毒性. 但是有研究验证了低浓度ClO2及其中间产物ClO2−和ClO3−没有慢性毒性,只有高剂量才会引发毒性作用.
Akamatsu等[147]研究了长期低浓度ClO2空气暴露对大鼠的毒性效应. 对大鼠进行长达6个月的0.1 mL·m−3的持续空气暴露,结果表明在体重、食物和水消耗以及相对器官重量方面没有观察到显着差异. 在血液学检查和组织病理学中,没有观察到与ClO2相关的显著变化. 因此该研究认为ClO2气体达0.3 mg·m−3,超过了对微生物有效的水平,连续暴露于大鼠全身6个月,没有毒性作用.
Xia等[148]通过90 d的喂食实验,研究了ClO2、ClO2−和ClO3−在水中的混合物对大鼠的亚慢性毒性. 对增重、食物食用效率、血清指标、肝/体重、肾/体重比、肝肾组织病理学检查进行分析. 结果表明,浓度为553 mg·L−1的ClO2及其副产物ClO2−和ClO3−溶液无毒. Couri等[149]总结研究ClO2、ClO2−和ClO3−在水中对的大鼠、小鼠和鸡的毒性实验,得出只有在较高剂量(高达1000 mg·L−1)时动物的血液学参数才会发生显著变化. 在慢性研究中,大鼠在其饮用水中给予高达1000 mg·L−1剂量的ClO2和高达100 mg·L−1的NaClO2或NaClO3一年. 实验组在红细胞形态和渗透性方面表现出变化,在较高剂量氯化合物下大鼠发生溶血性贫血,且血液中谷胱甘肽的含量减少. Stratilo等[150]评估ClO2消毒剂和NaClO消毒剂在人类皮肤角质形成细胞原代培养物的相对毒性. 结果表明ClO2消毒剂的毒性比NaClO低2个数量级.
-
对于过氧化物而言,许多研究表明,过氧化物低浓度长期暴露存在毒害作用,高浓度短期暴露则有刺激性和强氧化性等危害,而低浓度短期暴露则显示出对人体或实验动物无毒害作用. 并且过氧化物大多数快速降解为水和氧气,其降解产物无毒害作用.
根据NIOSH的标准,H2O2工作8 h平均允许暴露水平为1 mL·m−3[145]. H2O2低浓度长期暴露对人体存在毒害作用,如造成人体呼吸道损伤等. Hartwig等[151]研究证明,工人暴露于1.2—2.4 mL·m−3的H2O2,会导致眼睛和喉咙发炎、鼻塞、咳嗽和哮喘症状,显示严重的吸入毒性. Suenaka等[152]报道,工人长期暴露于浓度低于1.5 mg·m−3的H2O2,会出现手部皮肤粗糙,头发脱色等现象. 在一项为期28 d的研究中发现[153],大鼠暴露于浓度为0、2、10、25 mL·m−3的H2O2蒸汽中,每天6 h,每周5 d,结果显示出浓度依赖性肺中毒. 研究表明H2O2是对黏膜和气道的刺激物.
研究表明低浓度H2O2短时间暴露对大鼠无毒害作用. 浓度为0.5%的H2O2是一种低浓度稳定型的消毒灭菌剂. Mohanan等[154]用新西兰白兔验证0.5%H2O2气溶胶的皮肤毒性,并用大鼠验证其吸入毒性,结果表明新西兰白兔没有出现皮肤过敏症状. 实验组大鼠与对照组相比,均未显示死亡、临床毒性迹象和体重减轻的现象.
O3是一种刺激性气体,长期接触已被证明可能导致肺功能下降和哮喘等呼吸系统疾病[3],其毒性可以根据浓度和暴露时间来决定[155]. 根据NIOSH的标准,O3工作8 h平均允许暴露水平为0.1 mL·m−3[145]. 然而用于消毒的有效O3水平很容易超过规定的O3浓度[156]. 在0.1—1.0 mL·m−3的短期O3暴露率下,人体会产生头痛、流鼻血、眼睛刺激、喉咙干燥和呼吸窘迫等症状[157]. 在较高的暴露水平1—100 mL·m−3下,症状变得更加严重,包括哮喘、疲倦和食欲下降等[158]. Niu等[159]研究表明个人短期接触0.02 mL·m−3左右浓度的O3可能导致急性呼吸道炎症.
CH3COOOH消毒过程无有毒物质残留,但CH3COOOH刺激性气味强,对眼睛与皮肤黏膜有刺激性,且对金属物品和纺织品会产生破坏. Viola等[160]发现,将 L929 成纤维细胞暴露于1%CH3COOOH和 2.5% NaClO,结果表明CH3COOOH组细胞活力低于NaClO组,坏死细胞百分比高于NaClO组(P < 0.05). 两种消毒剂都减少了细胞代谢,导致细胞骨架的破坏,造成外部形态的变化,导致蛋白质在粗面内质网中积累,并主要通过坏死诱导细胞死亡. 尽管它们具有相同的细胞毒性机制,但1% CH3COOOH比2.5% NaClO具有更大的细胞毒性. Chhetri等[161]研究表明,ClO2、CH3COOOH和H2O2的慢性毒性依次降低但稳定性随着毒性降低而增加. Small等[162]研究发现,NaClO暴露比CH3COOOH或H2O2暴露导致铜绿假单胞菌更多的基因组变化,证明其遗传毒性更强.
-
目前物理消毒方法存在操作不便及消杀效果较差的问题. 化学消毒虽然使用简便且消杀效果好,但是其不规范的使用会引起人体健康危害以及生态危害,因此需要确定其安全使用方式,避免过度消毒.
关于消毒剂的生态风险评价目前大多数局限于水体,在其他介质如物体表面和空气中,其生态风险尚不明确. 目前仍缺乏化学消毒剂在空气介质中诱导气载微生物产生抗性的机理研究,许多消毒剂的生态安全性有待考察. 未来研究应聚焦于化学消毒剂诱导气载微生物产生消毒剂抗性和耐药性的研究,尤其是微生物消毒剂抗性和耐药性产生机制的研究以及消毒过程中可移动遗传元件在抗性水平转移中发挥作用的研究. 为科学有效地使用消毒剂、减少消毒剂抗性风险提供理论支持.
新冠病毒肺炎疫情中常用空气消毒对气载病原体的消杀作用及其生态健康危害研究进展
Research progress on disinfection effects, ecological and health hazards of common air disinfection methods on airborne pathogens during COVID-19 pandemic
-
摘要: 新型冠状病毒肺炎(Coronavirus disease 2019,COVID-19)疫情中,物理法消毒和化学法消毒是较为常用的消毒方式. 常用化学消毒剂包括过氧化物类消毒剂和含氯消毒剂,因其消杀效率高、操作简便等优点而被广泛使用. 然而,过量使用消毒剂会导致消毒剂残留,并产生消毒副产物,进而引发生态与健康危害. 因此,需要规范使用空气消毒方式,并需深入研究其在多种环境介质中引发的健康与生态安全风险. 本文总结了空气传播病原微生物、国内外空气微生物相关标准、常用空气消毒方式及其灭活效果、残留消毒剂和消毒副产物的生态及健康危害,并展望了未来的发展趋势.Abstract: During the epidemic of Coronavirus Disease 2019 (COVID-19), physical and chemical disinfections are commonly used. The chemical disinfectants include chlorine-contained and peroxide-based disinfectants, which are widely used because of their high efficiency and easy operation. However, excessive application of disinfectants can lead to disinfectant residues and disinfection by-products (DBPs), which would induce ecological and health hazards. Therefore, it is necessary to standardize the air disinfection, and to further study the health and ecological safety risks of disinfectants in a variety of environmental matrices. This paper summarizes the airborne microorganisms, relevant standards of airborne microorganisms, common air disinfection methods and their inactivation effects, the ecological and health hazards of residual disinfectants and DBPs, and also prospects the future development trends of air disinfection.
-
自2019年底以来,由严重急性呼吸综合征冠状病毒-2(Severe Acute Respiratory Syndrome Coronavirus 2,SARS-CoV-2)引发的新型冠状病毒肺炎疫情(Coronavirus disease 2019,COVID-19)仍在全球范围内蔓延. 截止2022年10月5日,已有615,777,700例确诊,6,527,192个死亡病例[1]更新为最新数据. 新冠病毒疫情已成为全世界二战以来最严重的突发公共卫生事件,严重危害人类健康并阻碍了社会经济发展. SARS-CoV-2是一种具有囊膜、基因组为线性单股正链的RNA病毒,具有非常强的传染性,主要通过飞沫、密切接触和气溶胶等途径传播[2]. 消毒是传染病疫情防控的有效手段,是确保“大灾之后无大疫”的有力保障,对保证人民的生命健康具有重要作用.
新冠疫情后,气载病原体及其引起的健康危害受到越来越多的关注. 但是,过量使用消毒剂可导致显著的人体健康危害[3-4]. 大规模环境消杀后,残留消毒剂和消毒副产物会成为新的污染源,危及环境和生态安全[5]. 本文总结了气载病原体、国内外相关标准、常用空气消毒方式及其灭活效果以及残留消毒剂和消毒副产物的生态及健康危害,并展望了未来的发展趋势.
1. 气载病原体(Airborne pathogen)
气载病原体包括致病细菌、致病真菌及病毒等,它们可附着在细微颗粒物上,或以气溶胶的形式在空气中扩散并传播,可引起呼吸系统疾病[6-7]. 常见的病原微生物及其相关疾病如表1所示.
属Genus 种Species 革兰染色/核酸Gram staining/Nucleic acid 来源Source 相关疾病Relevant diseases 参考文献References 假单胞菌属(Pseudomonas) 荧光假单胞菌、类鼻疽假单胞菌和铜绿假单胞菌等 阳性 室外大气、污水处理厂、医院、垃圾焚烧厂 人类食物中毒、呼吸系统感染和菌血症 [8] 芽孢杆菌属(Bacillus) 蜡状芽孢杆菌和炭疽芽孢杆菌等 阳性 自然界广泛存在 炭疽病、食物中毒 [9-12] 不动杆菌属(Acinetobacter) 醋酸钙不动杆菌、洛菲不动杆菌和鲍曼不动杆菌等 阴性 医院 呼吸道感染、皮肤伤口感染,泌尿生殖道感染,肺炎,肺脓肿,还可引起败血症,心内膜炎,脑膜炎,脑脓肿 [13] 棒状杆菌属(Corynebacterium) 白喉棒状杆菌 阳性 白喉病 [14] 葡萄球菌属(Staphylococcus) 金黄色葡萄球菌 阳性 自然环境 软组织、皮肤和伤口的机会性感染,也可引起血液感染、肺炎等炎症和败血症 [15-17] 链球菌属(Streptococcus) 肺炎链球菌 阳性 肺炎、继发性胸膜炎、中耳炎、乳突炎、心内膜炎及化脓性脑膜炎等 [18] 曲霉属(Aspergillus flavus) 真菌性呼吸道感染、角膜炎和眼内炎 [19-20] 鼻病毒(Rhinovirus) RNA 普通感冒 [21] 流感病毒(Influenza virus) RNA 急性高热、全身疼痛、显著乏力和呼吸道症状 [22] 水痘-带状疱疹病毒(Varicella-zoster virus) DNA 水痘、带状胞疹 [23] 麻疹病毒(Measles virus) RNA 麻疹 [24] 腮腺炎病毒(Mumps virus) RNA 腮腺炎 [25] 汉坦病毒(Hantavirus) RNA 汉坦病毒肺综合征、汉坦病毒肾综合征出血热(HFRS) [26] 冠状病毒(Coronavirus) RNA 呼吸道综合征 [27] 1.1 空气传播细菌
在室内外大气环境中检测到许多病原菌,如假单胞菌(Pseudomonas)、乳球菌(Lactococcus)、不动杆菌(Acinetobacter)、棒状杆菌(Corynebacterium)、葡萄球菌(Staphylococcus)和芽孢杆菌(Bacillus)等[28-30]. 相比于普通细菌,病原菌对极端环境的耐受能力更强[31]. 例如,芽孢杆菌可以形成卵圆形的内生孢子从而具有更强的耐受能力,有研究表明其相对丰度随着空气质量恶化而增加[32]. 芽孢杆菌是一种常见的病原菌,不仅存在于室外大气中,而且广泛存在于一些特殊的空气环境中,如垃圾焚烧厂[9]、医院[10]和污水处理厂[11]等. 蜡状芽孢杆菌可引起人类食物中毒、严重感染和菌血症[12].
多重耐药细菌在医院环境很常见,如耐头孢他啶铜绿假单胞菌和耐亚胺培南鲍曼不动杆菌[33-34]. 金黄色葡萄球菌是一种共生菌,也是一种条件致病菌[35],可导致皮肤感染、血流感染、感染性心内膜炎、骨髓炎和肺部感染. 金黄色葡萄球菌易获得耐药基因,尤其容易耐甲氧西林,并在医院废水中被检出[15-17]. 病原微生物的耐药性给疾病治疗带来困难,对人体健康产生极大威胁.
1.2 空气传播病毒
气载病毒主要包括鼻病毒(Rhinovirus)、流感病毒(Influenza virus)、水痘-带状疱疹病毒(Varicella-zoster virus)、麻疹病毒(Measles virus)、腮腺炎病毒(Mumps virus)、汉坦病毒(Hantavirus)以及冠状病毒(Coronavirus)等[21-27]. 这些病毒可能会引发流感、水痘、麻疹、腮腺炎以及呼吸道疾病等. 呼吸道病毒可通过飞沫、密切接触和气溶胶传播. 流感病毒、鼻病毒和新冠病毒等均可通过生物气溶胶传播[2].
1.3 空气传播真菌
空气中的优势真菌主要包括青霉菌(Penicillium)、链格孢菌(Alternaria)、枝孢菌(Cladosporium)和曲霉菌(Aspergillus)等[36]. 真菌是潜在的过敏原,接触其孢子可能会引起易感个体的免疫反应,可能导致过敏性鼻炎、支气管哮喘或外源过敏性肺泡炎等疾病发生[37]. 在家禽养殖场和谷磨厂等空气中,青霉菌、曲霉菌和毛霉菌(Mucor)为优势菌[38]. 在医院环境中常见真菌包括曲霉菌、青霉菌、镰刀菌(Fusarium)、枝孢菌等,均具有潜在的致病性[19-20]. 新生隐球菌(Cryptococcus neoformans)是一种病原真菌,其可通过呼吸道进入人体引发致命的隐球菌脑膜炎[39].
2. 国内外空气质量标准中的微生物指标(Microbial indices in domestic and foreign air quality standards)
我国最新《室内空气质量标准》(GB/T18883—2022)只对空气中细菌总数进行了限定,采用撞击式微生物采样器采样,其标准限值为1500 CFU·m−3,对真菌和病毒没有限值[40]. 国内研究一般使用由中国科学院生态中心推荐使用的大气微生物评价建议标准对大气空气微生物污染状况进行评价,该标准评价内容如表2所示[41]. 我国各公共场所空气质量标准如表3所示[42]. 不同国家或组织提供的生物气溶胶细菌和真菌的标准差距较大,各国细菌限值标准在500—10000 CFU·m−3之间[43-44],真菌限值标准则在50—2500 CFU·m−3之间[44-45],但是由于各国采样标准与环境不同,仅对数值进行对比参考意义较小[46]. 其中美国食品药物管理局(U. S. Food and Drug Administration)不提供具体限制数值;欧盟则根据病原微生物浓度进行污染程度分类[42].
表 2 中国科学院生态环境研究中心推荐的微生物气溶胶评价标准[41]Table 2. Evaluation standards for microbial aerosol recommended by the Eco-Environmental Research Center of the Chinese Academy of Sciences[41]污染程度Pollution level 细菌/(CFU·m−3)Bacteria 真菌/(CFU·m−3)Fungi 微生物总浓度/(CFU·m−3)Total microbial concentration 极重度污染 >45000 >15000 >60000 重度污染 20000 — 45000 6000 — 15000 30000 — 60000 中度污染 10000 — 20000 2500 — 6000 15000 — 30000 轻度污染 5000 — 10000 1000 — 2500 10000 — 15000 微污染 2500 — 5000 750 — 1000 5000 — 10000 较清洁 1000 — 2500 500 — 750 3000 — 5000 清洁 <1000 <500 <3000 场所Place 细菌数量Bacteria population 标准Standard 撞击法/(CFU·m−3)Impacting method 沉降法/(个·皿−1)Sedimentation 旅店客房 普通旅店、招待所 2500 30 旅店业卫生标准(GB9663—1996) 1—2星级饭店、宾馆和非星级带空调的饭店、宾馆 l500 10 3—5星级饭店、宾馆 l000 10 文化娱乐场所 影剧院、音乐厅录像厅(室) 4000 40 文化娱乐场所卫生标准(GB9664—1996) 游艺厅、舞厅 4000 40 酒吧、茶座、咖啡厅 2500 30 理发店、美容店 4000 40 理发店、美容店卫生标准(GB9666—1996) 游泳馆 4000 40 游泳场所卫生标准(GB9667—1996) 体育馆 4000 40 体育馆卫生标准(GB9668—1996) 图书馆、博物馆、美术馆 2500 30 图书馆、博物馆、美术馆、展览馆卫生标准(GB9669—1996) 商场(店)书店 7000 75 商场 (店)、书店卫生标准(GB9670—1996) 医院 医院候诊室 4000 40 医院候诊室卫生标准(GB9671—1996) 采用空气洁净技术的诊疗 场所,洁净手 术部和其他洁净场所 150 4 医院消毒卫生标准(GB15982—2012) 公共交通等候室 候车室和候船室 7000 75 公共交通等候室卫生标准(GB9672—1996) 候机室 4000 40 公共交通工具 旅客列车车厢 4000 40 公共交通工具卫生标准(GB9673—1996) 轮船客舱 4000 40 飞机客舱 2500 30 饭馆(餐厅) 4000 40 饭馆(餐厅)卫生标准(GB16153—1996) 公共场所集中空调通风系统送风 500(细菌)500(真菌)不得检出β-溶血性链球菌和嗜肺军团菌 公共场所集中空调通风系统卫生规范(ws394—2012) 3. 常用空气消毒方法及其消杀毒效果(Commonly-used air disinfection methods and their disinfection effects)
常用消毒方法按照作用原理可分为物理消毒和化学消毒两大类,各消毒方式主要作用机理及优缺点如表4所示.
表 4 常用空气消毒方式、作用机制及其优缺点Table 4. Mechanisms, advantages and disadvantages of the commonly-used air disinfection methods消毒方式Disinfection method 作用机制Mechanism 优点Advantages 缺点Disadvantages 物理消毒 空气过滤、静电吸附技术[47-51] 过滤、静电吸附 清洁、低成本、操作简便 只能捕集微生物,无法杀灭微生物,有二次感染风险. 物理消毒 紫外辐射 破坏细菌病毒中的DNA或RNA的分子结构,达到杀菌消毒的效果. 清洁、低成本 穿透能力差,消毒有死角;杀菌持久效果短;紫外线照射对人体有害;紫外消毒后有光复活的风险. 化学消毒 次氯酸 次氯酸可以穿透细菌细胞壁,通过破坏细胞膜上的结合酶、脂质和蛋白质来阻断细胞呼吸作用并且改变细胞膜通透性,造成胞内离子、DNA、蛋白质泄露,从而导致细胞内稳态的恶化,最终使细胞死亡 高效、广谱、无残留 不稳定 化学消毒 次氯酸钠 次氯酸钠在水中水解成次氯酸作为其消毒的有效成分,因此其消毒机制与次氯酸大致相同 高效、广谱 不稳定;对人体有毒害作用;腐蚀性;降解产生副产物 化学消毒 二氧化氯 二氧化氯较易吸附并穿过细胞壁,其可以氧化细胞内的氨基酸如半胱氨酸、酪氨酸和色氨酸以及细胞内含巯基的酶,从而阻止蛋白质的合成和细菌代谢,导致细菌死亡 高效、广谱、清洁、持久、无致癌副产物产生 易发生低浓度爆炸;有轻微异味;不稳定;高浓度危害人体健康 化学消毒 过氧化氢 过氧化物消毒剂的有效成分主要是活性氧. 其杀菌机制主要是通过氧化破坏细胞膜,损坏细胞内的蛋白质和核酸以及抑制能量生产,从而影响微生物结构和功能 高效、广谱、无残留 高浓度危害人体健康 化学消毒 过氧乙酸 过氧乙酸氧化能力很强,通过氧化微生物内的酶杀死微生物. 并且过氧乙酸亦具有酸的特性,对杀菌起到一定作用. 高效、广谱 对人体有刺激性;对金属有腐蚀性;不稳定 化学消毒 光催化 当近紫外线UVA照射到光催化材料上时,入射光子会激发活性氧的产生,从而达到杀菌效果 高效、广谱、清洁、 效果不稳定;费用高;对光源有较高要求. 化学消毒 臭氧 臭氧可产生活性氧原子及羟基自由基氧化微生物,也可以直接氧化微生物,使得氨基酸、蛋白质、核酸等物质变性,从而致使微生物失活 高效、广谱、清洁、效果持久、杀菌彻底 臭氧危害人体健康;腐蚀建筑材料;消毒后需要时间排放 化学消毒 低温等离子体 等离子体消毒主要通过产生活性氧、羟基自由基、O3和其他活性粒子对微生物的脂质、蛋白质和DNA等生物分子强烈氧化从而灭活微生物. 高速粒子的击穿以及紫外线的作用也对微生物灭活起到一定贡献 清洁、高效、广谱 价格昂贵;穿透性差;设备使用要求条件高 3.1 物理消毒方法
3.1.1 紫外线消毒
紫外线消毒是一种公认的高效杀菌方法,其因使用方便且无化学残留在医院及许多公共场所广泛应用[52]. 紫外光的波长范围为10—400 nm,低于240 nm的紫外线易产生臭氧[53]. 紫外线辐照会破坏或改变微生物的遗传物质(DNA和RNA),形成胸腺嘧啶二聚体(遗传物质的光产物),干扰核酸的复制和转录,从而导致微生物死亡[54]. 紫外线空气消毒的效率取决于空气微生物对紫外线的敏感性、紫外线辐照度强度和紫外线辐照剂量[55]. 紫外线对病毒、细菌、原生动物和真菌都有良好的消杀效果[56]. Kim等[57]研究表明,254 nm低压汞紫外灯(强度为1.5—4.6 mJ·cm−2)对鼠伤寒沙门氏杆菌、单核细胞增生李斯特菌、大肠杆菌、黄曲霉菌和金黄色葡萄球菌气溶胶的去除率可达到99.68%—99.99%. Yang等[58]研究表明,在通风管道中,紫外线对空气中粘质沙雷氏菌、产碱假单胞菌、大肠杆菌、肠沙门氏菌和表皮葡萄球菌的消杀效果较好,在高入口速度(6 m·s−1)的条件下,对被试菌中耐光性最强的表皮葡萄球菌的灭活率为76.1%. Walker等[59]研究发现,噬菌体MS2和腺病毒气溶胶都对紫外线消毒有很强的抵抗力,而冠状病毒气溶胶的敏感性则是MS2和腺病毒气溶胶的7倍至10倍,更容易被消灭. 与细菌气溶胶不同,对于紫外线消毒,高相对湿度对病毒气溶胶没有显著保护作用. 杨晶雪等[60]研究表明,在医院环境中经紫外线直接照射法消毒10 min时,根据室内空气菌落数计算,空气灭菌率为31.45%;消毒20 min时,空气灭菌率为63.24%;消毒30 min时,空气灭菌率可达到89.44%,空气中含菌量合格.
紫外线消毒虽然具有诸多优点,但杀菌波长的紫外线直接照射到人体皮肤上会造成损伤,特别是眼睛对紫外线格外敏感. 除此之外,紫外线消毒后的细菌仍存在光复活的风险,这可能会降低紫外消毒的效率[61].
3.2 化学消毒方法
2020年,国家卫生健康委员会颁布了《消毒剂使用指南》[62]以规范化学消毒剂的使用方法. 当前,国内外常用的消毒剂主要有8类,包括醇类消毒剂、含氯消毒剂、过氧化物类消毒剂、季铵盐类消毒剂、醛类消毒剂、酚类消毒剂、含碘消毒剂和过硫酸氢钾类[63]. 常用于空气消毒的消毒剂有含氯消毒剂和过氧化物类消毒剂.
3.2.1 含氯消毒剂
含氯消毒剂是高效的广谱消毒剂,包括次氯酸盐、次氯酸(HOCl)、二氧化氯(ClO2)和三氯异氰尿酸(C3O3N3Cl3)等[62]. HOCl可以穿透细菌细胞壁,通过破坏细胞膜上的结合酶阻断细胞呼吸,破坏细胞膜的脂质和蛋白质改变细胞膜通透性,造成胞内离子、DNA和蛋白质泄露,从而导致细胞内稳态的恶化,最终使细胞死亡[64-65]. 对于病毒,HOCl破坏其蛋白质外壳并损伤其核酸,抑制遗传功能从而达到消灭效果[66]. 次氯酸水主要成分为HOCl,还含有多种氧化剂和自由基,除游离氯外还具有其他抗菌活性.
有研究表明,HOCl对10种细菌和2种真菌(白色念珠菌和黑曲霉菌)均有显著杀灭效果[67]. Hakimullah等[68]研究表明,使用含有100 mg·L−1活性氯的次氯酸水对农场含有新城疫病毒的气溶胶进行消毒可以使病毒完全灭活. Boecker等[69]验证了HOCl可对人口稠密的室内场所进行空气消毒,该研究认为,使用200 mg·L−1活性氯浓度的HOCl进行空气消毒预计不会刺激人体组织.
次氯酸钠(NaClO)是常用的含氯消毒剂之一,具有价格低廉和消毒效果好等优点[70],经常用于物体表面消毒和空气消毒. NaClO在水中水解成的HOCl是其消毒的有效成分,因此其消毒机制与HOCl大致相同. Ishikawa等[71]研究表明,83 mg·L−1的雾化NaClO在饱和湿度下能够杀灭枯草芽孢杆菌孢的活性.
ClO2是一种高效广谱消毒剂,它对细菌(铜绿假单胞菌、大肠杆菌[72]、金黄色葡萄球菌和鲍曼不动杆菌[73]等)、病毒(脊髓灰质炎病毒[74]、人流感病毒[75]和麻疹病毒 [76]等)、真菌(木霉属、青霉属[77]等)及原生生物[78]都具有较强的灭活能力. ClO2可快速穿透细胞壁,其可以氧化细胞内的氨基酸如半胱氨酸、酪氨酸和色氨酸以及细胞内含巯基的酶,从而阻止蛋白质的合成和细菌代谢,导致细菌死亡[79]. ClO2能改变病毒蛋白质成分,使病毒外壳蛋白失活从而抑制病毒攻击宿主细胞的能力[80]. 也有研究表明,ClO2对基因组破坏效果较小,不抑制基因组的复制功能[81]. Lu等[82]研究表明,0.3 mg·m−3的ClO2雾化消毒可以有效降低宠物店室内生物气溶胶浓度,并且较快的气流速度有利于雾化ClO2消毒剂在室内空间的扩散,从而提高消毒性能. 在学校食堂[83]和图书馆中[84],ClO2消毒也可以有效降低气溶胶中细菌和真菌数量. Boonrattanakij等[85]研究表明,使用0.3 mg·m−3的ClO2对健身房的空气进行15 min消毒后,空气中细菌和真菌浓度符合官方空气质量标准,且气流速度对细菌和真菌的去除没有显著影响,这可能是因为在该研究中使用的气流速度(0.3 m·min−1)已足以将消毒剂快速扩散到房间空间中.
在用于处理物体表面微生物时,与HClO和ClO2相比,NaClO活性较低. Thorn等[86]研究表明,在100 mg·L−1游离氯的浓度下,对金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌和临床耐甲氧西林金黄色葡萄球菌菌株的生物气溶胶消毒效果顺序为次氯酸水>ClO2>NaClO. 还有研究表明,ClO2的抗病毒性能比NaClO约高出10倍[9]. Erosy等[65]通过次氯酸水、NaClO和ClO2对粪肠球菌的消毒作用也发现其灭菌活性顺序为次氯酸水>ClO2>NaClO. 3种消毒剂都通过破坏细胞膜完整性、使离子浓度失衡和破坏细胞成分(如DNA、蛋白质和脂质分子)等途径来灭活细菌. 尽管NaClO消毒剂效果逊于次氯酸水和ClO2,但由于次氯酸水和ClO2化学性质不稳定,用于消毒时常常需要现场生成,与之相比,NaClO更容易储存. HOCl使用简便、安全,对人体无刺激性损伤,更适于临床推广[87].
3.2.2 过氧化物消毒剂
过氧化物消毒剂主要有过氧化氢(H2O2)、过氧乙酸(CH3COOOH)、过氧戊二酸(C10H14O8)和臭氧(O3),有效成分主要是活性氧物种(reactive oxygen species,ROS),其主要是通过氧化破坏细胞膜、损坏细胞内蛋白质和核酸以及抑制能量生产,从而抑制微生物生长与繁殖[88-90]. 过氧化物类消毒剂对于细菌、孢子、真菌和病毒(如轮状病毒、腺病毒、甲型流感病毒和脊髓灰质炎病毒)等微生物具有广谱高效的杀灭作用[91-93].
H2O2是常用的过氧化物消毒剂. Masotti等[94]研究表明,H2O2雾化消毒和O3消毒均可有效灭活乳品厂室内空气中枝孢菌属、青霉菌属、隐球菌属、德巴利菌属、棒状菌属和孢子菌属等微生物. Choi等[95]验证了H2O2雾化消毒是医院环境进行消毒的有效方法,医院病房和急诊室经消毒后表面取样,革兰氏阳性菌CFUs数量下降超过90%. Popov等[96]也证实了H2O2气雾剂可以显著减少医院空气和物体表面微生物污染. Tuladhar等[93]研究表明,176 μg·L−1的H2O2蒸汽是一种有效的杀病毒剂,可有效杀灭室内空气中肠道和呼吸道病毒,包括脊髓灰质炎病毒、人类诺如病毒、鼠诺如病毒、轮状病毒、腺病毒和甲型流感(H1N1)病毒. Horn等[97]]研究发现,H2O2蒸汽消毒与病房中艰难梭菌(从1.38例到0.90例/1000个患者日)、耐万古霉素肠球菌(从0.21例到0.01例/1000个患者日)和产超广谱β-内酰胺酶的革兰氏阴性菌(从0.16例到0.01例/1000个患者日)的感染显著减少相关.
O3在空气中快速分解生成活性氧原子(O)或与水分子反应生成羟基自由基(OH·),它们可以通过氧化微生物中的不饱和键使得蛋白质以及核酸等物质变性,从而杀灭微生物,其在室内空气清洁[98]、食品保鲜[99]和医院消毒[100]等方面都有广泛应用. Girgin等[101]研究发现当O3接触细菌的细胞壁时,其氧化作用会在细胞中产生孔洞,随着孔洞扩大细菌就会失去形状,发生破裂. O3可能与真菌孢子外壳、核酸物质以及细胞内的酶发生反应并导致真菌死亡[102]. O3灭活病毒的主要机制是对遗传物质的直接破坏,O3还可能对病毒的外部蛋白质衣壳层造成损害[103]. Manning等[104]研究表明,O3可有效杀灭N95口罩中的铜绿假单胞菌. Ding等[105]研究表明O3消毒对耐氯孢子有效,因为它会破坏细胞结构和基因片段. O3生成简单,成本低廉,使用安全,可快速分解回氧气,不会产生消毒副产物,半衰期约为20 min,由于气体可以渗透到房间的所有区域,它比液体喷雾消毒剂更具穿透性[106]. O3的氧化活性是HOCl的25倍,是次氯酸盐的2500 到3000倍[107].
张淼等[108]研究表明,低剂量C10H14O8对公共场所空气消毒效果显著,消毒后公共场所的空气质量达到国家标准,消毒作用持续时间可达100 min以上. 谭金煜等[109]在医院采取CH3COOOH气溶胶喷雾法与气体熏蒸消毒法对病房进行消毒. 结果表明两种消毒方式全部合格,但气溶胶喷雾法由于操作简单优于气体熏蒸消毒法. Tso等[110]研究表明,相对于H2O2和CH3COOOH,ClO2更适合用于消灭副溶血性弧菌. Chhetri等[111]研究表明ClO2、CH3COOOH和H2O2的对藻类的毒性依次降低.
对于一些微生物来说,H2O2的消毒效果显著优于NaClO. Montagna等[112]研究发现1.5% H2O2对铜绿假单胞菌、肺炎克雷伯菌、粪肠球菌和金黄色葡萄球菌菌株的消毒效果明显高于5% NaClO(P<0.0001). Barbut等[113]研究表明,在有艰难梭菌感染患者的房间使用50 mL·m−3的H2O2干雾消毒系统对艰难梭菌孢子的空气消毒效果明显优于0.5% NaClO溶液,为艰难梭菌感染患者的室内消毒提供了一种新的选择. 但也有研究表明,对于某些微生物而言,NaClO消毒剂的消毒效果更优. Kingsley等[114]研究表明,诺如病毒对几种常用过氧化物消毒剂如ClO2、CH3COOOH和H2O2具有明显的抗性,而氯(NaClO)消毒剂则可以作为诺如病毒的有效消毒剂. Lineback等[115]研究发现,对于金黄色葡萄球菌和铜绿假单胞菌,NaClO和H2O2消毒剂的杀菌效果明显高于季铵氯化物消毒剂.
3.2.3 等离子体消毒
等离子体是气体在高压作用下发生电离后产生的电中性气态物质,被称为物质存在的第4种形态,等离子体中包括大量高活性物质,如活性氧(原子氧、单线态氧、超氧阴离子、O3和羟基自由基)和活性氮(原子氮、激发态氮和一氧化氮)等[116]. 等离子体消毒快速高效,可用于物体表面消毒和空气消毒. 等离子体消毒的主要机制是活性氧、羟基自由基、O3和其他活性粒子共同作用于微生物,导致微生物灭活,这些基于氧和氮的活性物质对脂质、蛋白质和DNA等生物分子具有强烈的氧化作用[117]. 研究发现,等离子体消毒对白色葡萄球菌有良好消灭效果,并且在一定范围内,对空气消毒效果随温度和湿度的升高而增强,与作用时间成正比[118]. Zhang等[119]研究发现,等离子体消毒在冷链环境空气中灭活新冠病毒具有良好效果,等离子体产生的活性物质灭活病毒的能力优于传统O3消毒. 闫妍等[120]研究发现,高压放电激发产生的等离子体与电极板上的纳米二氧化钛光触媒系统协同作用,对空气中白色葡萄球菌和H1N1甲型流感病毒都有良好消杀效果. 非热大气等离子体处理和脉冲氙紫外线(PX-UV)处理广泛用于医院环境的消毒,对金黄色葡萄球菌、表皮葡萄球菌和酵母菌都有良好消灭效果[121]. 然而等离子体消毒过程中会有O3和氮氧化物等副产物的产生,并且等离子体消毒价格昂贵且操作具有一定的危险性.
3.2.4 光催化消毒
半导体材料在光激发下会产生光生电子空穴对,其具有很强的氧化/还原能力,与氧气或水反应可以生成活性氧物种(ROS),如·OH、·O2−和H2O2等. 常用的光催化消毒材料还包括ZnO、Bi2WO6、NiMoO4和Pd-BiFeO3等[122]. 光催化消毒具有高效、低成本、安全等优点,其杀伤机制为氧化导致细胞壁和细胞质膜的降解,进而引起细胞内容物泄漏、细胞溶解、核酸受到破坏,最终导致生物体的完全矿化[123]. 光催化对大肠杆菌、乳酸杆菌、耐甲氧西林金黄色葡萄球菌、铜绿假单胞菌等细菌,黑曲霉菌青霉菌酵母菌等真菌,脊髓灰质炎病毒、人流感病毒和SARS冠状病毒以及原生动物和藻类都有良好消杀效果[124]. 二氧化钛(TiO2)光催化剂能够杀死多种革兰氏阴性和革兰氏阳性细菌、丝状和单细胞真菌、藻类、原生动物、哺乳动物病毒和噬菌体[125]. 磁性g-C3N4/NiFe2O4复合材料也是一种具有高消毒活性的光催化材料,可以有效杀灭黄曲霉[126].
4. 常用空气消毒方法诱导病原菌形成耐药菌(Commonly-used air disinfection methods induce pathogenic bacteria to form drug-resistant bacteria)
消毒剂大量使用会增加消毒剂抗性和抗生素耐药性,从而导致了全球严重的生态安全问题. 越来越多的研究报道了氯消毒剂在促进消毒剂抗性和抗生素耐药性方面的作用. Khan等[127]研究表明,细菌对氯消毒剂的抗性与抗生素耐药性之间显著相关. Lu等[4]指出,新冠病毒疫情期间消毒抗菌剂的过度使用可加速耐药菌的产生及传播,从而增加耐药菌大流行到来的风险,并威胁未来的公共健康. 常用空气消毒方式诱导病原菌产生耐药性的机理如图1所示.
4.1 消毒剂促进细菌突变形成耐药菌
各种消毒剂的强氧化性会引起微生物的氧化应激反应. 消毒剂诱导细菌形成抗生素抗性细菌(antibiotic resistance bacteria, ARB)是通过氧化应激诱导的基因表达或突变等方式. 多种消毒剂可以诱导基因突变,通过细胞膜通透性的改变、抗生素靶位点的修饰、降解抗生素或外排泵的激活[128]来增强微生物的抗生素抗性.
Tong等[129]研究表明,100 mg·L−1 NaClO可增加假单胞菌属的消毒剂抗性和抗生素耐药性. 由氧化应激引发的SOS反应(对DNA损伤的保护反应)使细菌对氯消毒剂产生抗性. 抗生素耐药性的增加可归因于膜通透性降低,MuxABC-OpmB外排泵、β-内酰胺酶和抗氧化酶的表达增加. 研究结果揭示了氯消毒剂对促进微生物的消毒剂抗性和抗生素耐药性的影响. Hou等[130]研究表明,铜绿假单胞菌在暴露于4 mg·L−1 NaClO后对头孢他啶、氯霉素和氨苄青霉素的耐药性提高了1.4—5.6倍. 并且发现GPx和SOD水平显著提高,这两种抗氧化酶保护细菌免受ROS损失. 由氧化应激反应引起的MexEF-OprN 外排泵的表达提高是抗生素耐药性增加的主要原因. Lv等[131]研究4种典型的消毒副产物二溴乙酸、二氯乙腈、溴酸钾和3-氯-4-(二氯甲基)-5-羟基-2(5H)-呋喃酮(MX)对细菌耐药性的影响,铜绿假单胞菌暴露于消毒副产物后,对10种单独抗生素和多种抗生素的耐药性均出现不同程度的提高,得出结论所选择的消毒副产物可以诱导抗生素耐药性,甚至是多药耐药性产生. 林辉等[132]发现,在医院环境中,由于消毒剂的频繁使用,导致了菌株对消毒剂产生抗性. 比如物体表面消毒时,消毒剂氯含量达到1000 mg·L−1才能消灭微生物. 在医院污染监控中采集的7株产β-内酰胺酶的铜绿假单胞菌的含氯消毒剂杀灭率与标准菌株的含氯消毒剂杀灭率相比呈不同程度降低.
4.2 消毒剂促进耐药基因水平转移
消毒剂可以促进基因水平转移使得细菌获得外源性可移动遗传元件,如携带抗生素抗性基因(antibiotic resistance genes, ARGs)的质粒和整合子等,从而使ARGs在属间交换或产生新型ARB,并且可移动遗传元件较难被消毒剂降解[133-134]. Zhang等[135]研究发现,3种广泛使用的消毒剂(游离氯、氯胺和H2O2)在亚抑制浓度下可以促进ARGs在大肠杆菌菌株内以及从大肠杆菌到鼠伤寒沙门氏菌的跨属转移. 然而,暴露于高于亚抑制浓度的消毒剂则会显著抑制ARGs转移.
目前尚未发现紫外线消毒诱导病原菌产生耐药性的证据. Choi等[136]将耐甲氧西林金黄色葡萄球菌(MRSA)、产碳青霉烯酶(KPC)的肺炎克雷伯菌和产金属β-内酰胺酶(MBL)的肺炎克雷伯菌连续暴露于紫外线辐照25个生长周期循环,结果表明多重耐药细菌暴露于紫外线后,不会产生紫外线抗性. 紫外线/氯处理可以潜在地提高再生水的微生物安全性,减少ARGs和移动遗传元件(MGEs)的数量[137].
5. 常用空气消毒方式残留消毒剂和消毒副产物的生态及健康危害(Ecological and health hazards of residual disinfectants and disinfection by-products in commonly-used air disinfection methods)
5.1 生态危害
据报道,疫情暴发以来,武汉市消毒剂的累积使用量超过了5000 吨,其中以含氯消毒剂为主[5]. 含氯消毒剂可以与环境中污染物产生化学反应,生成多种消毒副产物(DBPs)[138]. 这些残留的化学消毒剂及DBPs会通过自然沉降、雨水冲刷等方式进入水环境和土壤环境,造成二次污染. 消毒剂残留及消毒副产物可直接作用于水生生物和微生物,从而影响到水生态系统[138].
新冠疫情期间(2020年2—3月),武汉市部分湖泊水体上覆水中余氯最高检出值达0.4 mg·L−1. 随着疫情的持续,武汉市河湖水环境中消毒剂的残留现象仍然持续[5]. 同年9月,张坤锋等[139]对武汉市饮用水水源进行采样,结果表明,采样的26个点位中仍有16个检出游离氯或总余氯,部分点位游离氯超过了国家地表水标准,其中最大浓度为0.04 mg·L−1. 同时在10个点位中检出24种DBPs,总DBPs浓度范围为0.11—104.73 μg·L−1,平均值7.26 μg·L−1. 生态风险评估结果表明,三氯甲烷对水生生物有较高的生态风险. 有研究表明,DBPs可能会改变浮游植物群落的结构,可能会促进水生生态系统中蓝藻水华的爆发[140].
5.2 对人体健康危害
5.2.1 含氯消毒剂及其消毒副产物
美国环境保护署(U.S. Environmental Protection Agency, US EPA)设置的空气氯暴露浓度限值为0.5 mL·m−3,短期暴露于空气中的氯时,1—3 mL·m−3会轻微刺激鼻子,5 mL·m−3造成眼睛刺激,5—15 mL·m−3引发喉咙刺激,30 mL·m−3造成即刻胸痛、呕吐、呼吸频率变化和咳嗽,40—60 mL·m−3引起肺损伤(中毒性肺炎)和肺水肿(肺部液体),接触430 mL·m−3 30 min后死亡,在接触1000 mL·m−3后几分钟死亡[3]. 这些影响还取决于暴露的时间. 一般来说,患有呼吸道疾病的人,如过敏或花粉热,或重度吸烟者,往往比健康的人或非吸烟者受到更严重的影响[3].
HOCl是人体天然存在的抗菌剂. 在活化的中性粒细胞中,氯离子通过过氧化反应生成HOCl,其有助于抵抗感染[141]. HOCl消毒剂的pH值接近中性,氯浓度较低,对人体健康无害[142].
NaClO的高氧化性则对人体具有一定的毒害作用. Slaughter等[143]总结了NaClO中毒的临床病例,发现NaClO引起的毒性与其氧化能力和溶液的pH值有关,其与黏膜和皮肤接触时具有腐蚀性. NaClO少量意外摄入不太可能引起临床显著毒性,但大量摄入可能会导致腐蚀性胃肠道损伤和全身损伤,包括代谢性酸中毒、高钠血症和高氯血症. 长期或广泛皮肤接触NaClO可能导致皮肤刺激或皮肤损伤,高浓度接触则会导致严重的化学皮肤灼伤. 仅吸入少量NaClO可能会对上呼吸道造成轻微刺激. 眼部暴露于NaClO引起的角膜损伤通常是轻微的,伴有灼热不适和角膜上皮的表面紊乱,并在1 d或2 d内恢复. 较高浓度的NaClO可能会引起严重的眼睛刺激. 采用NaClO消毒也会产生较多的消毒副产物,如三氯乙酸、二氨乙酸和氯仿等,对人体具有毒害作用. 但是有研究表明少量NaClO的短时间暴露不会引起急性毒性作用. Murashevych等[144]研究证明,含有(1.7±0.13)mg·m−3活性氯的NaClO气溶胶吸入不会引起大鼠急性毒性作用.
根据美国国家职业安全与健康研究所(NIOSH))的标准,ClO2工作8 h平均允许暴露水平为0.1 mL·m−3,短期(15 min)暴露水平限值为0.3 mL·m−3[145]. 高浓度ClO2的强氧化性也会引起人体毒性作用. Lardieri等[146]统计了一些已发表的病例报告中描述的高浓度ClO2的毒性作用,包括引发高铁血红蛋白血症、中毒性刺激性皮炎、菊池藤本病和溶血性贫血. 在作者统计的55个病例中,有45例属于急性毒性,6例属于慢性毒性. 但是有研究验证了低浓度ClO2及其中间产物ClO2−和ClO3−没有慢性毒性,只有高剂量才会引发毒性作用.
Akamatsu等[147]研究了长期低浓度ClO2空气暴露对大鼠的毒性效应. 对大鼠进行长达6个月的0.1 mL·m−3的持续空气暴露,结果表明在体重、食物和水消耗以及相对器官重量方面没有观察到显着差异. 在血液学检查和组织病理学中,没有观察到与ClO2相关的显著变化. 因此该研究认为ClO2气体达0.3 mg·m−3,超过了对微生物有效的水平,连续暴露于大鼠全身6个月,没有毒性作用.
Xia等[148]通过90 d的喂食实验,研究了ClO2、ClO2−和ClO3−在水中的混合物对大鼠的亚慢性毒性. 对增重、食物食用效率、血清指标、肝/体重、肾/体重比、肝肾组织病理学检查进行分析. 结果表明,浓度为553 mg·L−1的ClO2及其副产物ClO2−和ClO3−溶液无毒. Couri等[149]总结研究ClO2、ClO2−和ClO3−在水中对的大鼠、小鼠和鸡的毒性实验,得出只有在较高剂量(高达1000 mg·L−1)时动物的血液学参数才会发生显著变化. 在慢性研究中,大鼠在其饮用水中给予高达1000 mg·L−1剂量的ClO2和高达100 mg·L−1的NaClO2或NaClO3一年. 实验组在红细胞形态和渗透性方面表现出变化,在较高剂量氯化合物下大鼠发生溶血性贫血,且血液中谷胱甘肽的含量减少. Stratilo等[150]评估ClO2消毒剂和NaClO消毒剂在人类皮肤角质形成细胞原代培养物的相对毒性. 结果表明ClO2消毒剂的毒性比NaClO低2个数量级.
5.2.2 过氧化物消毒剂
对于过氧化物而言,许多研究表明,过氧化物低浓度长期暴露存在毒害作用,高浓度短期暴露则有刺激性和强氧化性等危害,而低浓度短期暴露则显示出对人体或实验动物无毒害作用. 并且过氧化物大多数快速降解为水和氧气,其降解产物无毒害作用.
根据NIOSH的标准,H2O2工作8 h平均允许暴露水平为1 mL·m−3[145]. H2O2低浓度长期暴露对人体存在毒害作用,如造成人体呼吸道损伤等. Hartwig等[151]研究证明,工人暴露于1.2—2.4 mL·m−3的H2O2,会导致眼睛和喉咙发炎、鼻塞、咳嗽和哮喘症状,显示严重的吸入毒性. Suenaka等[152]报道,工人长期暴露于浓度低于1.5 mg·m−3的H2O2,会出现手部皮肤粗糙,头发脱色等现象. 在一项为期28 d的研究中发现[153],大鼠暴露于浓度为0、2、10、25 mL·m−3的H2O2蒸汽中,每天6 h,每周5 d,结果显示出浓度依赖性肺中毒. 研究表明H2O2是对黏膜和气道的刺激物.
研究表明低浓度H2O2短时间暴露对大鼠无毒害作用. 浓度为0.5%的H2O2是一种低浓度稳定型的消毒灭菌剂. Mohanan等[154]用新西兰白兔验证0.5%H2O2气溶胶的皮肤毒性,并用大鼠验证其吸入毒性,结果表明新西兰白兔没有出现皮肤过敏症状. 实验组大鼠与对照组相比,均未显示死亡、临床毒性迹象和体重减轻的现象.
O3是一种刺激性气体,长期接触已被证明可能导致肺功能下降和哮喘等呼吸系统疾病[3],其毒性可以根据浓度和暴露时间来决定[155]. 根据NIOSH的标准,O3工作8 h平均允许暴露水平为0.1 mL·m−3[145]. 然而用于消毒的有效O3水平很容易超过规定的O3浓度[156]. 在0.1—1.0 mL·m−3的短期O3暴露率下,人体会产生头痛、流鼻血、眼睛刺激、喉咙干燥和呼吸窘迫等症状[157]. 在较高的暴露水平1—100 mL·m−3下,症状变得更加严重,包括哮喘、疲倦和食欲下降等[158]. Niu等[159]研究表明个人短期接触0.02 mL·m−3左右浓度的O3可能导致急性呼吸道炎症.
CH3COOOH消毒过程无有毒物质残留,但CH3COOOH刺激性气味强,对眼睛与皮肤黏膜有刺激性,且对金属物品和纺织品会产生破坏. Viola等[160]发现,将 L929 成纤维细胞暴露于1%CH3COOOH和 2.5% NaClO,结果表明CH3COOOH组细胞活力低于NaClO组,坏死细胞百分比高于NaClO组(P < 0.05). 两种消毒剂都减少了细胞代谢,导致细胞骨架的破坏,造成外部形态的变化,导致蛋白质在粗面内质网中积累,并主要通过坏死诱导细胞死亡. 尽管它们具有相同的细胞毒性机制,但1% CH3COOOH比2.5% NaClO具有更大的细胞毒性. Chhetri等[161]研究表明,ClO2、CH3COOOH和H2O2的慢性毒性依次降低但稳定性随着毒性降低而增加. Small等[162]研究发现,NaClO暴露比CH3COOOH或H2O2暴露导致铜绿假单胞菌更多的基因组变化,证明其遗传毒性更强.
6. 存在问题及展望(Existing problems and prospects)
目前物理消毒方法存在操作不便及消杀效果较差的问题. 化学消毒虽然使用简便且消杀效果好,但是其不规范的使用会引起人体健康危害以及生态危害,因此需要确定其安全使用方式,避免过度消毒.
关于消毒剂的生态风险评价目前大多数局限于水体,在其他介质如物体表面和空气中,其生态风险尚不明确. 目前仍缺乏化学消毒剂在空气介质中诱导气载微生物产生抗性的机理研究,许多消毒剂的生态安全性有待考察. 未来研究应聚焦于化学消毒剂诱导气载微生物产生消毒剂抗性和耐药性的研究,尤其是微生物消毒剂抗性和耐药性产生机制的研究以及消毒过程中可移动遗传元件在抗性水平转移中发挥作用的研究. 为科学有效地使用消毒剂、减少消毒剂抗性风险提供理论支持.
-
属Genus 种Species 革兰染色/核酸Gram staining/Nucleic acid 来源Source 相关疾病Relevant diseases 参考文献References 假单胞菌属(Pseudomonas) 荧光假单胞菌、类鼻疽假单胞菌和铜绿假单胞菌等 阳性 室外大气、污水处理厂、医院、垃圾焚烧厂 人类食物中毒、呼吸系统感染和菌血症 [8] 芽孢杆菌属(Bacillus) 蜡状芽孢杆菌和炭疽芽孢杆菌等 阳性 自然界广泛存在 炭疽病、食物中毒 [9-12] 不动杆菌属(Acinetobacter) 醋酸钙不动杆菌、洛菲不动杆菌和鲍曼不动杆菌等 阴性 医院 呼吸道感染、皮肤伤口感染,泌尿生殖道感染,肺炎,肺脓肿,还可引起败血症,心内膜炎,脑膜炎,脑脓肿 [13] 棒状杆菌属(Corynebacterium) 白喉棒状杆菌 阳性 白喉病 [14] 葡萄球菌属(Staphylococcus) 金黄色葡萄球菌 阳性 自然环境 软组织、皮肤和伤口的机会性感染,也可引起血液感染、肺炎等炎症和败血症 [15-17] 链球菌属(Streptococcus) 肺炎链球菌 阳性 肺炎、继发性胸膜炎、中耳炎、乳突炎、心内膜炎及化脓性脑膜炎等 [18] 曲霉属(Aspergillus flavus) 真菌性呼吸道感染、角膜炎和眼内炎 [19-20] 鼻病毒(Rhinovirus) RNA 普通感冒 [21] 流感病毒(Influenza virus) RNA 急性高热、全身疼痛、显著乏力和呼吸道症状 [22] 水痘-带状疱疹病毒(Varicella-zoster virus) DNA 水痘、带状胞疹 [23] 麻疹病毒(Measles virus) RNA 麻疹 [24] 腮腺炎病毒(Mumps virus) RNA 腮腺炎 [25] 汉坦病毒(Hantavirus) RNA 汉坦病毒肺综合征、汉坦病毒肾综合征出血热(HFRS) [26] 冠状病毒(Coronavirus) RNA 呼吸道综合征 [27] 表 2 中国科学院生态环境研究中心推荐的微生物气溶胶评价标准[41]
Table 2. Evaluation standards for microbial aerosol recommended by the Eco-Environmental Research Center of the Chinese Academy of Sciences[41]
污染程度Pollution level 细菌/(CFU·m−3)Bacteria 真菌/(CFU·m−3)Fungi 微生物总浓度/(CFU·m−3)Total microbial concentration 极重度污染 >45000 >15000 >60000 重度污染 20000 — 45000 6000 — 15000 30000 — 60000 中度污染 10000 — 20000 2500 — 6000 15000 — 30000 轻度污染 5000 — 10000 1000 — 2500 10000 — 15000 微污染 2500 — 5000 750 — 1000 5000 — 10000 较清洁 1000 — 2500 500 — 750 3000 — 5000 清洁 <1000 <500 <3000 场所Place 细菌数量Bacteria population 标准Standard 撞击法/(CFU·m−3)Impacting method 沉降法/(个·皿−1)Sedimentation 旅店客房 普通旅店、招待所 2500 30 旅店业卫生标准(GB9663—1996) 1—2星级饭店、宾馆和非星级带空调的饭店、宾馆 l500 10 3—5星级饭店、宾馆 l000 10 文化娱乐场所 影剧院、音乐厅录像厅(室) 4000 40 文化娱乐场所卫生标准(GB9664—1996) 游艺厅、舞厅 4000 40 酒吧、茶座、咖啡厅 2500 30 理发店、美容店 4000 40 理发店、美容店卫生标准(GB9666—1996) 游泳馆 4000 40 游泳场所卫生标准(GB9667—1996) 体育馆 4000 40 体育馆卫生标准(GB9668—1996) 图书馆、博物馆、美术馆 2500 30 图书馆、博物馆、美术馆、展览馆卫生标准(GB9669—1996) 商场(店)书店 7000 75 商场 (店)、书店卫生标准(GB9670—1996) 医院 医院候诊室 4000 40 医院候诊室卫生标准(GB9671—1996) 采用空气洁净技术的诊疗 场所,洁净手 术部和其他洁净场所 150 4 医院消毒卫生标准(GB15982—2012) 公共交通等候室 候车室和候船室 7000 75 公共交通等候室卫生标准(GB9672—1996) 候机室 4000 40 公共交通工具 旅客列车车厢 4000 40 公共交通工具卫生标准(GB9673—1996) 轮船客舱 4000 40 飞机客舱 2500 30 饭馆(餐厅) 4000 40 饭馆(餐厅)卫生标准(GB16153—1996) 公共场所集中空调通风系统送风 500(细菌)500(真菌)不得检出β-溶血性链球菌和嗜肺军团菌 公共场所集中空调通风系统卫生规范(ws394—2012) 表 4 常用空气消毒方式、作用机制及其优缺点
Table 4. Mechanisms, advantages and disadvantages of the commonly-used air disinfection methods
消毒方式Disinfection method 作用机制Mechanism 优点Advantages 缺点Disadvantages 物理消毒 空气过滤、静电吸附技术[47-51] 过滤、静电吸附 清洁、低成本、操作简便 只能捕集微生物,无法杀灭微生物,有二次感染风险. 物理消毒 紫外辐射 破坏细菌病毒中的DNA或RNA的分子结构,达到杀菌消毒的效果. 清洁、低成本 穿透能力差,消毒有死角;杀菌持久效果短;紫外线照射对人体有害;紫外消毒后有光复活的风险. 化学消毒 次氯酸 次氯酸可以穿透细菌细胞壁,通过破坏细胞膜上的结合酶、脂质和蛋白质来阻断细胞呼吸作用并且改变细胞膜通透性,造成胞内离子、DNA、蛋白质泄露,从而导致细胞内稳态的恶化,最终使细胞死亡 高效、广谱、无残留 不稳定 化学消毒 次氯酸钠 次氯酸钠在水中水解成次氯酸作为其消毒的有效成分,因此其消毒机制与次氯酸大致相同 高效、广谱 不稳定;对人体有毒害作用;腐蚀性;降解产生副产物 化学消毒 二氧化氯 二氧化氯较易吸附并穿过细胞壁,其可以氧化细胞内的氨基酸如半胱氨酸、酪氨酸和色氨酸以及细胞内含巯基的酶,从而阻止蛋白质的合成和细菌代谢,导致细菌死亡 高效、广谱、清洁、持久、无致癌副产物产生 易发生低浓度爆炸;有轻微异味;不稳定;高浓度危害人体健康 化学消毒 过氧化氢 过氧化物消毒剂的有效成分主要是活性氧. 其杀菌机制主要是通过氧化破坏细胞膜,损坏细胞内的蛋白质和核酸以及抑制能量生产,从而影响微生物结构和功能 高效、广谱、无残留 高浓度危害人体健康 化学消毒 过氧乙酸 过氧乙酸氧化能力很强,通过氧化微生物内的酶杀死微生物. 并且过氧乙酸亦具有酸的特性,对杀菌起到一定作用. 高效、广谱 对人体有刺激性;对金属有腐蚀性;不稳定 化学消毒 光催化 当近紫外线UVA照射到光催化材料上时,入射光子会激发活性氧的产生,从而达到杀菌效果 高效、广谱、清洁、 效果不稳定;费用高;对光源有较高要求. 化学消毒 臭氧 臭氧可产生活性氧原子及羟基自由基氧化微生物,也可以直接氧化微生物,使得氨基酸、蛋白质、核酸等物质变性,从而致使微生物失活 高效、广谱、清洁、效果持久、杀菌彻底 臭氧危害人体健康;腐蚀建筑材料;消毒后需要时间排放 化学消毒 低温等离子体 等离子体消毒主要通过产生活性氧、羟基自由基、O3和其他活性粒子对微生物的脂质、蛋白质和DNA等生物分子强烈氧化从而灭活微生物. 高速粒子的击穿以及紫外线的作用也对微生物灭活起到一定贡献 清洁、高效、广谱 价格昂贵;穿透性差;设备使用要求条件高 -
[1] World Health Organization. WHO coronavirus disease(COVID-19) dashboard[EB/OL]. [2022-10-5]. [2] WANG C C, PRATHER K A, SZNITMAN J, et al. Airborne transmission of respiratory viruses [J]. Science, 2021, 373(6558): eabd9149. doi: 10.1126/science.abd9149 [3] Agency for Toxic Substances and Disease Registry (ATSDR). Toxicological profile for chlorine [S]. Atlanta, GA: U. S. Department of Health and Human Services, Public Health Service, 2010. [4] LU J, GUO J H. Disinfection spreads antimicrobial resistance [J]. Science, 2021, 371(6528): 474. [5] 尹炜, 王超, 张洪, 等. 新冠肺炎疫情期消毒剂的使用对水环境的影响: 以武汉市为例 [J]. 人民长江, 2020, 51(5): 29-33,88. YIN W, WANG C, ZHANG H, et al. Effects of disinfectants on aquatic environment in Wuhan City during COVID-19 pandemic [J]. Yangtze River, 2020, 51(5): 29-33,88(in Chinese).
[6] GÓRNY R L. Filamentous microorganisms and their fragments in indoor air: A review [J]. Annals of Agricultural and Environmental Medicine, 2004, 11(2): 185-197. [7] 雷长红. 空气微生物污染及其控制的研究进展 [J]. 职业与健康, 2013, 29(24): 3348-3350. LEI C H. The research progress of air microbial contamination and its control [J]. Occupation and Health, 2013, 29(24): 3348-3350(in Chinese).
[8] AZAM M W, KHAN A U. Updates on the pathogenicity status of Pseudomonas aeruginosa [J]. Drug Discovery Today, 2019, 24(1): 350-359. doi: 10.1016/j.drudis.2018.07.003 [9] LI L Y, WANG Q, BI W J, et al. Municipal solid waste treatment system increases ambient airborne bacteria and antibiotic resistance genes [J]. Environmental Science & Technology, 2020, 54(7): 3900-3908. [10] TSAY M D, TSENG C C, WU N X, et al. Size distribution and antibiotic-resistant characteristics of bacterial bioaerosol in intensive care unit before and during visits to patients [J]. Environment International, 2020, 144: 106024. doi: 10.1016/j.envint.2020.106024 [11] YANG K X, LI L, WANG Y J, et al. Airborne bacteria in a wastewater treatment plant: Emission characterization, source analysis and health risk assessment [J]. Water Research, 2019, 149: 596-606. doi: 10.1016/j.watres.2018.11.027 [12] SPENCER R C. Bacillus anthracis [J]. Journal of Clinical Pathology, 2003, 56(3): 182-187. doi: 10.1136/jcp.56.3.182 [13] CASTILHO S R A, GODOY C S M, GUILARDE A O, et al. Acinetobacter baumannii strains isolated from patients in intensive care units in Goiânia, Brazil: Molecular and drug susceptibility profiles [J]. PLoS One, 2017, 12(5): e0176790. doi: 10.1371/journal.pone.0176790 [14] TROST E, BLOM J, de CASTRO SOARES S, et al. Pangenomic study of Corynebacterium diphtheriae that provides insights into the genomic diversity of pathogenic isolates from cases of classical diphtheria, endocarditis, and pneumonia [J]. Journal of Bacteriology, 2012, 194(12): 3199-3215. doi: 10.1128/JB.00183-12 [15] CHEN L F. The changing epidemiology of methicillin-resistant Staphylococcus aureus: 50 years of a superbug [J]. American Journal of Infection Control, 2013, 41(5): 448-451. doi: 10.1016/j.ajic.2012.06.013 [16] BECKER K, BALLHAUSEN B, KÖCK R, et al. Methicillin resistance in Staphylococcus isolates: The “mec alphabet” with specific consideration of mecC, a mec homolog associated with zoonotic S. aureus lineages [J]. International Journal of Medical Microbiology, 2014, 304(7): 794-804. doi: 10.1016/j.ijmm.2014.06.007 [17] THOMPSON J M, GÜNDOĞDU A, STRATTON H M, et al. Antibiotic resistant Staphylococcus aureus in hospital wastewaters and sewage treatment plants with special reference to methicillin-resistant Staphylococcus aureus (MRSA) [J]. Journal of Applied Microbiology, 2013, 114(1): 44-54. doi: 10.1111/jam.12037 [18] KIM M, HEO S T, OH H, et al. Human zoonotic infectious disease caused by Streptococcus equi subsp. zooepidemicus [J]. Zoonoses and Public Health, 2022, 69(2): 136-142. doi: 10.1111/zph.12895 [19] MARTINS-DINIZ J N, Da SILVA R A M, MIRANDA E T, et al. Monitoramento de fungos anemófilos e de leveduras em unidade hospitalar [J]. Revista De Saúde Pública, 2005, 39(3): 398-405. [20] GONÇALVES C L, MOTA F V, FERREIRA G F, et al. Airborne fungi in an intensive care unit [J]. Revista Brasleira De Biologia, 2018, 78(2): 265-270. [21] LU Q B, WO Y, WANG L Y, et al. Molecular epidemiology of human Rhinovirus in children with acute respiratory diseases in Chongqing, China [J]. Scientific Reports, 2014, 4: 6686. doi: 10.1038/srep06686 [22] BELSER J A, LASH R R, GARG S, et al. The eyes have it: Influenza virus infection beyond the respiratory tract [J]. The Lancet Infectious Diseases, 2018, 18(7): e220-e227. doi: 10.1016/S1473-3099(18)30102-6 [23] SCHMIDT-CHANASIT J, SAUERBREI A. Evolution and world-wide distribution of varicella-zoster virus clades [J]. Infection, Genetics and Evolution, 2011, 11(1): 1-10. doi: 10.1016/j.meegid.2010.08.014 [24] REUTER D, SCHNEIDER-SCHAULIES J. Measles virus infection of the CNS: Human disease, animal models, and approaches to therapy [J]. Medical Microbiology and Immunology, 2010, 199(3): 261-271. doi: 10.1007/s00430-010-0153-2 [25] HVIID A, RUBIN S, MÜHLEMANN K. Mumps [J]. Lancet, 2008, 371(9616): 932-944. doi: 10.1016/S0140-6736(08)60419-5 [26] FIGUEIREDO L T M, de SOUZA W M, FERRÉS M, et al. Hantaviruses and cardiopulmonary syndrome in south America [J]. Virus Research, 2014, 187: 43-54. doi: 10.1016/j.virusres.2014.01.015 [27] ASHRAF O, VIRANI A, CHEEMA T. Covid-19 [J]. Critical Care Nursing Quarterly, 2021, 44(1): 128-137. doi: 10.1097/CNQ.0000000000000346 [28] FAN C L, LI Y P, LIU P X, et al. Characteristics of airborne opportunistic pathogenic bacteria during autumn and winter in Xi'an, China [J]. Science of the Total Environment, 2019, 672: 834-845. doi: 10.1016/j.scitotenv.2019.03.412 [29] HU Z C, LIU H, ZHANG H, et al. Temporal discrepancy of airborne total bacteria and pathogenic bacteria between day and night [J]. Environmental Research, 2020, 186: 109540. doi: 10.1016/j.envres.2020.109540 [30] LIANG Z S, YU Y, YE Z K, et al. Pollution profiles of antibiotic resistance genes associated with airborne opportunistic pathogens from typical area, Pearl River Estuary and their exposure risk to human [J]. Environment International, 2020, 143: 105934. doi: 10.1016/j.envint.2020.105934 [31] LIU H, ZHANG X, ZHANG H, et al. Effect of air pollution on the total bacteria and pathogenic bacteria in different sizes of particulate matter [J]. Environmental Pollution, 2018, 233: 483-493. doi: 10.1016/j.envpol.2017.10.070 [32] WEI M, LIU H F, CHEN J M, et al. Effects of aerosol pollution on PM2.5-associated bacteria in typical inland and coastal cities of Northern China during the winter heating season [J]. Environmental Pollution, 2020, 262: 114188. doi: 10.1016/j.envpol.2020.114188 [33] ASGHAR A H, FAIDAH H S. Frequency and antimicrobial susceptibility of gram-negative bacteria isolated from 2 hospitals in Makkah, Saudi Arabia [J]. Saudi Medical Journal, 2009, 30(8): 1017-1023. [34] SOLOMON F B, WADILO F, TUFA E G, et al. Extended spectrum and metalo beta-lactamase producing airborne Pseudomonas aeruginosa and Acinetobacter baumanii in restricted settings of a referral hospital: A neglected condition [J]. Antimicrobial Resistance and Infection Control, 2017, 6: 106. doi: 10.1186/s13756-017-0266-0 [35] FRANK D N, FEAZEL L M, BESSESEN M T, et al. The human nasal microbiota and Staphylococcus aureus carriage [J]. PLoS One, 2010, 5(5): e10598. doi: 10.1371/journal.pone.0010598 [36] KALYONCU F. Relationship between airborne fungal allergens and meteorological factors in Manisa City, Turkey [J]. Environmental Monitoring and Assessment, 2010, 165(1): 553-558. [37] LUGAUSKAS A, KRIKSTAPONIS A, SVEISTYTE L. Airborne fungi in industrial environments: Potential agents of respiratory diseases [J]. Annals of Agricultural and Environmental Medicine:AAEM, 2004, 11(1): 19-25. [38] ROY S, BHATTACHARYA S G. Airborne fungal spore concentration in an industrial township: Distribution and relation with meteorological parameters [J]. Aerobiologia, 2020, 36(4): 575-587. doi: 10.1007/s10453-020-09653-9 [39] 丁浩, 何光军, 王琳淇. 人类环境病原真菌: 新生隐球菌的社会行为 [J]. 生物工程学报, 2017, 33(9): 1555-1566. DING H, HE G J, WANG L Q. Party for killing: The social behaviors in Cryptococcus neoformans [J]. Chinese Journal of Biotechnology, 2017, 33(9): 1555-1566(in Chinese).
[40] 国家质量监督检验检疫总局;卫生部. 室内空气质量标准: GB/T 18883—2002[S]. 北京: 中国标准出版社, 2003. Ministry of Health of the People’s Republic of China. Indoor air quality STANDARD: GB/T 18883—2002[S]. Beijing: Standards Press of China, 2003(in Chinese).
[41] 李沅津, 杨庆, 赵茹涵, 等. A~2O工艺污水处理厂微生物气溶胶逸散特征及暴露风险评价 [J]. 环境科学学报, 2021, 41(9): 3457-3463. LI Y J, YANG Q, ZHAO R H, et al. Emission characteristics and exposure risk assessment of microbial aerosols from WWTP with A2O treatment process [J]. Acta Scientiae Circumstantiae, 2021, 41(9): 3457-3463(in Chinese).
[42] 张铭健, 曹国庆. 国内外室内空气微生物限值标准简介及对比分析 [J]. 暖通空调, 2019, 49(5): 40-45,33. ZHANG M J, CAO G Q. Introduction and comparative analysis of indoor air microbial threshold in domestic and foreign standards [J]. Heating Ventilating & Air Conditioning, 2019, 49(5): 40-45,33(in Chinese).
[43] World Health Organization (WHO). Guidelines for concentration and exposure-response measurements of fine and ultra-fine particulate matter for use in epidemiological studies [S]. 2002. [44] Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung (IFA). Verfahren zur Bestimmung der Schimmelpilzkonzentration in der Luft am Arbeitsplatz (#9430) [S]. 2004. [45] OPPLIGER A, RUSCA S, CHARRIÈRE N, et al. Assessment of bioaerosols and inhalable dust exposure in Swiss sawmills [J]. The Annals of Occupational Hygiene, 2005, 49(5): 385-391. [46] BRANDL H. Bioaerosols in indoor environment - A review with special reference to residential and occupational locations [J]. The Open Environmental & Biological Monitoring Journal, 2011, 4(1): 83-96. [47] 国家市场监督管理总局, 国家标准化管理委员会. 高效空气过滤器: GB/T 13554—2020[S]. 北京: 中国标准出版社, 2020. Standardization Administration of the People’s Republic of China. High efficiency particulate air filter: GB/T 13554—2020[S]. Beijing: Standards Press of China, 2020(in Chinese).
[48] 张辉, 贾颖, 石彤, 等. 新型空气净化器净化性能研究 [J]. 天津大学学报(自然科学与工程技术版), 2020, 53(3): 301-308. ZHANG H, JIA Y, SHI T, et al. Purification performance of a novel air purifier [J]. Journal of Tianjin University (Science and Technology), 2020, 53(3): 301-308(in Chinese).
[49] 陈杨, 钱幺, 李君喜. 静电在空气净化器中的应用 [J]. 纺织科技进展, 2020(6): 38-41. doi: 10.3969/j.issn.1673-0356.2020.06.011 CHEN Y, QIAN Y, LI J X. Application of static electricity in air purifiers [J]. Progress in Textile Science & Technology, 2020(6): 38-41(in Chinese). doi: 10.3969/j.issn.1673-0356.2020.06.011
[50] 伍诚麟, 田金, 许锋. 不同原理空气消毒净化器效果与分析 [J]. 医院管理论坛, 2022, 39(1): 83-87. doi: 10.3969/j.issn.1671-9069.2022.01.024 WU C L, TIAN J, XU F. Effect analysis of air disinfection purifier with different principles [J]. Hospital Management Forum, 2022, 39(1): 83-87(in Chinese). doi: 10.3969/j.issn.1671-9069.2022.01.024
[51] 刘勇. 吸附—静电场综合式空气净化机研制在医院应用实验研究[D]. 长沙: 中南大学, 2011. LIU Y. Evaluation research on the adsorbing and electrostatic field synthetic action mode of air dynamic purification system application in hospital[D]. Changsha: Central South University, 2011.
[52] DAVIDSON B L. Bare-bulb upper-room germicidal ultraviolet-C (GUV) indoor air disinfection for COVID-19 [J]. Photochemistry and Photobiology, 2021, 97(3): 524-526. doi: 10.1111/php.13380 [53] BERGMAN R S. Germicidal UV sources and systems [J]. Photochemistry and Photobiology, 2021, 97(3): 466-470. doi: 10.1111/php.13387 [54] FRANZ C M A P, SPECHT I, CHO G S, et al. UV-C-inactivation of microorganisms in naturally cloudy apple juice using novel inactivation equipment based on Dean vortex technology [J]. Food Control, 2009, 20(12): 1103-1107. doi: 10.1016/j.foodcont.2009.02.010 [55] NARDELL E A. Tuberculosis in New York City: Focal transmission of an often fatal disease [J]. the Journal of the American Medical Association, 1996, 276(15): 1259-1260. doi: 10.1001/jama.1996.03540150061032 [56] YAUN B R, SUMNER S S, EIFERT J D, et al. Inhibition of pathogens on fresh produce by ultraviolet energy [J]. International Journal of Food Microbiology, 2004, 90(1): 1-8. doi: 10.1016/S0168-1605(03)00158-2 [57] KIM D K, KANG D H. UVC LED irradiation effectively inactivates aerosolized viruses, bacteria, and fungi in a chamber-type air disinfection system [J]. Applied and Environmental Microbiology, 2018, 84(17): e00944-18. [58] YANG Y, ZHANG H H, NUNAYON S S, et al. Disinfection efficacy of ultraviolet germicidal irradiation on airborne bacteria in ventilation ducts [J]. Indoor Air, 2018, 28(6): 806-817. doi: 10.1111/ina.12504 [59] WALKER C M, KO G. Effect of ultraviolet germicidal irradiation on viral aerosols [J]. Environmental Science & Technology, 2007, 41(15): 5460-5465. [60] 杨晶雪, 孙雷, 杜丽, 等. 紫外线照射消毒法对空气消毒净化的效果评价 [J]. 中国卫生标准管理, 2016, 7(22): 188-189. YANG J X, SUN L, DU L, et al. The effect of ultraviolet radiation disinfection on air disinfection and purification [J]. China Health Standard Management, 2016, 7(22): 188-189(in Chinese).
[61] 陆海, 李雪琪, 冯伟豪. 复活光强对大肠杆菌光复活影响的研究进展 [J]. 长春工程学院学报(自然科学版), 2021, 22(3): 99-103. LU H, LI X Q FENG W H. The research progress on the influence of light resurrection by photoractivation light intensity to Escherichia coli [J]. Journal of Changchun Institute of Technology (Natural Sciences Edition), 2021, 22(3): 99-103(in Chinese).
[62] 国家卫生健康委办公厅. 消毒剂使用指南 [J]. 中国感染控制杂志, 2020, 19(2): 196-198. doi: 10.12138/j.issn.1671-9638.20206153 National Health Commission of the People’s Republic of China. Guidelines on disinfectant use [J]. Chinese Journal of Infection Control, 2020, 19(2): 196-198(in Chinese). doi: 10.12138/j.issn.1671-9638.20206153
[63] 贾栗, 何俊, 金虹, 等. 新冠肺炎疫情常用化学消毒剂的健康危害及其防护 [J]. 中国消毒学杂志, 2020, 37(10): 781-785. JIA L, HE J, JIN H, et al. Health hazards and protection of commonly used chemical disinfectants in COVID-19 [J]. Chinese Journal of Disinfection, 2020, 37(10): 781-785(in Chinese).
[64] CHUANG C Y, YANG S, CHANG M Y, et al. Inactivation efficiency to Bacillus subtilis and Escherichia coli bacterial aerosols of spraying neutral electrolyzed water [J]. Journal of the Air & Waste Management Association, 2013, 63(12): 1447-1456. [65] ERSOY Z G, DINC O, CINAR B, et al. Comparative evaluation of disinfection mechanism of sodium hypochlorite, chlorine dioxide and electroactivated water on Enterococcus faecalis [J]. LWT-Food Science & Technology, 2019, 102: 205-213. [66] WIGGINTON K R, PECSON B M, SIGSTAM T, et al. Virus inactivation mechanisms: Impact of disinfectants on virus function and structural integrity [J]. Environmental Science & Technology, 2012, 46(21): 12069-12078. [67] ONO T, YAMASHITA K, MURAYAMA T, et al. Microbicidal effect of weak acid hypochlorous solution on various microorganisms [J]. Biocontrol Science, 2012, 17(3): 129-133. doi: 10.4265/bio.17.129 [68] HAKIM H, THAMMAKARN C, SUGURO A, et al. Aerosol disinfection capacity of slightly acidic hypochlorous acid water towards Newcastle disease virus in the air: An in vivo experiment [J]. Avian Diseases, 2015, 59(4): 486-491. doi: 10.1637/11107-042115-Reg.1 [69] BOECKER D, BREVES R, ZHANG Z T, et al. Antimicrobial activity in the gasphase with hypochloric acid [J]. Current Directions in Biomedical Engineering, 2021, 7(2): 511-514. doi: 10.1515/cdbme-2021-2130 [70] 陈丽珠. 次氯酸钠消毒控制微生物的效果评价 [J]. 工业用水与废水, 2015, 46(5): 18-20,61. doi: 10.3969/j.issn.1009-2455.2015.05.004 CHEN L Z. Effect of microbial controlling by sodium hypochlorite disinfection [J]. Industrial Water & Wastewater, 2015, 46(5): 18-20,61(in Chinese). doi: 10.3969/j.issn.1009-2455.2015.05.004
[71] ISHIKAWA S, UENO S, MITSUI M, et al. Construction of its evaluation system in originally designed test-chamber system and sporicidal activity of aerosolized hypochlorite solution to Bacillus subtilis spores [J]. Biocontrol Science, 2019, 24(1): 57-65. doi: 10.4265/bio.24.57 [72] OFORI I, MADDILA S, LIN J, et al. Chlorine dioxide oxidation of Escherichia coli in water - A study of the disinfection kinetics and mechanism [J]. Journal of Environmental Science and Health, Part A, 2017, 52(7): 598-606. doi: 10.1080/10934529.2017.1293993 [73] HINENOYA A, AWASTHI S P, YASUDA N, et al. Chlorine dioxide is a better disinfectant than sodium hypochlorite against multi-drug resistant Staphylococcus aureus, Pseudomonas aeruginosa, and Acinetobacter baumannii [J]. Japanese Journal of Infectious Diseases, 2015, 68(4): 276-279. doi: 10.7883/yoken.JJID.2014.294 [74] ALVAREZ M E, O'BRIEN R T. Mechanisms of inactivation of poliovirus by chlorine dioxide and iodine [J]. Applied and Environmental Microbiology, 1982, 44(5): 1064-1071. doi: 10.1128/aem.44.5.1064-1071.1982 [75] TOTARO M, BADALUCCO F, COSTA A L, et al. Effectiveness of disinfection with chlorine dioxide on respiratory transmitted, enteric, and bloodborne viruses: A narrative synthesis [J]. Pathogens , 2021, 10(8): 1017. [76] SANEKATA T, FUKUDA T, MIURA T, et al. Evaluation of the antiviral activity of chlorine dioxide and sodium hypochlorite against feline calicivirus, human influenza virus, measles virus, canine distemper virus, human herpesvirus, human adenovirus, canine adenovirus and canine parvovirus [J]. Biocontrol Science, 2010, 15(2): 45-49. doi: 10.4265/bio.15.45 [77] WEN G, XU X Q, HUANG T L, et al. Inactivation of three Genera of dominant fungal spores in groundwater using chlorine dioxide: Effectiveness, influencing factors, and mechanisms [J]. Water Research, 2017, 125: 132-140. doi: 10.1016/j.watres.2017.08.038 [78] LORET J F, ROBERT S, THOMAS V, et al. Comparison of disinfectants for biofilm, protozoa and Legionella control [J]. Journal of Water and Health, 2005, 3(4): 423-433. doi: 10.2166/wh.2005.047 [79] OGATA N. Denaturation of protein by chlorine dioxide: Oxidative modification of tryptophan and tyrosine residues [J]. Biochemistry, 2007, 46(16): 4898-4911. doi: 10.1021/bi061827u [80] NOSS C I, HAUCHMAN F S, OLIVIERI V P. Chlorine dioxide reactivity with proteins [J]. Water Research, 1986, 20(3): 351-356. doi: 10.1016/0043-1354(86)90083-7 [81] JIN M, SHAN J Y, CHEN Z L, et al. Chlorine dioxide inactivation of enterovirus 71 in water and its impact on genomic targets [J]. Environmental Science & Technology, 2013, 47(9): 4590-4597. [82] LU M C, HUANG D J, HSU C S, et al. Improvement of indoor air quality in pet shop using gaseous chlorine dioxide [J]. Environmental Monitoring and Assessment, 2018, 190(7): 371. doi: 10.1007/s10661-018-6723-2 [83] HSU C S, LU M C, HUANG D J. Effect of gaseous chlorine dioxide on student Cafeteria bioaerosols [J]. Clean - Soil, Air, Water, 2014, 42(1): 12-19. doi: 10.1002/clen.201100293 [84] HSU C S, LU M C, HUANG D J. Disinfection of indoor air microorganisms in stack room of university library using gaseous chlorine dioxide [J]. Environmental Monitoring and Assessment, 2015, 187(2): 17. doi: 10.1007/s10661-014-4235-2 [85] BOONRATTANAKIJ N, YOMCHINDA S, LIN F J, et al. Investigation and disinfection of bacteria and fungi in sports fitness center [J]. Environmental Science and Pollution Research, 2021, 28(37): 52576-52586. doi: 10.1007/s11356-021-14323-5 [86] THORN R M S, ROBINSON G M, REYNOLDS D M. Comparative antimicrobial activities of aerosolized sodium hypochlorite, chlorine dioxide, and electrochemically activated solutions evaluated using a novel standardized assay [J]. Antimicrobial Agents and Chemotherapy, 2013, 57(5): 2216-2225. doi: 10.1128/AAC.02589-12 [87] 李志强. 高压氧舱紫外线和次氯酸两种方法空气消毒效果对比分析 [J]. 中国医学工程, 2015, 23(10): 170-171. LI Z Q. Comparative analysis of air disinfection effect of ultraviolet and hypochlorous acid in hyperbaric oxygen chamber [J]. China Medical Engineering, 2015, 23(10): 170-171(in Chinese).
[88] LINLEY E, DENYER S P, McDONNELL G, et al. Use of hydrogen peroxide as a biocide: New consideration of its mechanisms of biocidal action [J]. Journal of Antimicrobial Chemotherapy, 2012, 67(7): 1589-1596. doi: 10.1093/jac/dks129 [89] WANG D, YAMAKI S, KAWAI Y J, et al. Sanitizing efficacy and antimicrobial mechanism of peracetic acid against histamine-producing bacterium, Morganella psychrotolerans [J]. LWT-Food Science & Technology, 2020, 126: 109263. [90] FINNEGAN M, LINLEY E, DENYER S P, et al. Mode of action of hydrogen peroxide and other oxidizing agents: Differences between liquid and gas forms [J]. Journal of Antimicrobial Chemotherapy, 2010, 65(10): 2108-2115. doi: 10.1093/jac/dkq308 [91] LEGGETT M J, SCHWARZ J S, BURKE P A, et al. Mechanism of sporicidal activity for the synergistic combination of peracetic acid and hydrogen peroxide [J]. Applied and Environmental Microbiology, 2015, 82(4): 1035-1039. [92] LEROUGE S, SIMMONS A, SIMMONS A, et al. Sterilisation of Biomaterials and Medical Devices[M]. Woodhead Publishing, 2012 [93] TULADHAR E, TERPSTRA P, KOOPMANS M, et al. Virucidal efficacy of hydrogen peroxide vapour disinfection [J]. Journal of Hospital Infection, 2012, 80(2): 110-115. doi: 10.1016/j.jhin.2011.10.012 [94] MASOTTI F, VALLONE L, RANZINI S, et al. Effectiveness of air disinfection by ozonation or hydrogen peroxide aerosolization in dairy environments [J]. Food Control, 2019, 97: 32-38. doi: 10.1016/j.foodcont.2018.10.022 [95] CHOI J, LEE M, LEE Y, et al. Effectiveness of plasma-treated hydrogen peroxide mist disinfection in various hospital environments [J]. International Journal of Environmental Research and Public Health, 2021, 18(18): 9841. doi: 10.3390/ijerph18189841 [96] POPOV D A, ANUCHINA N M. Microbiological efficacy of hospital environment decontamination by hydrogen peroxide aerosol [J]. Biomedical Engineering, 2016, 50(2): 92-95. doi: 10.1007/s10527-016-9595-1 [97] HORN K, OTTER J A. Hydrogen peroxide vapor room disinfection and hand hygiene improvements reduce Clostridium difficile infection, methicillin-resistant Staphylococcus aureus, vancomycin-resistant enterococci, and extended-spectrum β-lactamase [J]. American Journal of Infection Control, 2015, 43(12): 1354-1356. doi: 10.1016/j.ajic.2015.06.029 [98] TUNG T C W, NIU J L, BURNETT J, et al. Determination of ozone emission from a domestic air cleaner and decay parameters using environmental chamber tests [J]. Indoor and Built Environment, 2005, 14(1): 29-37. doi: 10.1177/1420326X05049648 [99] BERMÚDEZ-AGUIRRE D, BARBOSA-CÁNOVAS G V. Disinfection of selected vegetables under nonthermal treatments: Chlorine, acid citric, ultraviolet light and ozone [J]. Food Control, 2013, 29(1): 82-90. doi: 10.1016/j.foodcont.2012.05.073 [100] LARA FERNÁNDEZ G E, ARIOSA ACUÑA C M, BORROTO RODRÍGUEZ V, et al. Ozono Como método de desinfección del ambiente hospitalario [J]. Acta Médica Costarricense, 2020, 62(2): 72-78. [101] GIRGIN ERSOY Z, BARISCI S, DINC O. Mechanisms of the Escherichia coli and Enterococcus faecalis inactivation by ozone [J]. LWT- Food Science & Technology, 2019, 100: 306-313. [102] KHADRE M A, YOUSEF A E, KIM J G. Microbiological aspects of ozone applications in food: A review [J]. Journal of Food Science, 2001, 66(9): 1242-1252. doi: 10.1111/j.1365-2621.2001.tb15196.x [103] WU G H, SELDEN D, FOOKS A R, et al. Inactivation of rabies virus [J]. Journal of Virological Methods, 2017, 243: 109-112. doi: 10.1016/j.jviromet.2017.02.002 [104] MANNING E P, STEPHENS M D, DUFRESNE S, et al. Disinfection of Pseudomonas aeruginosa from N95 respirators with ozone: A pilot study [J]. BMJ Open Respiratory Research, 2021, 8(1): e000781. doi: 10.1136/bmjresp-2020-000781 [105] DING W Q, JIN W B, CAO S, et al. Ozone disinfection of chlorine-resistant bacteria in drinking water [J]. Water Research, 2019, 160: 339-349. doi: 10.1016/j.watres.2019.05.014 [106] HUDSON J B, SHARMA M, VIMALANATHAN S. Development of a practical method for using ozone gas as a virus decontaminating agent [J]. Ozone:Science & Engineering, 2009, 31(3): 216-223. [107] ARJMAND M M, NADERI M, GHOLAMI S. Investigation of the survival of bacteria under the influence of supporting electrolytes KCl, CuI and NaBr in the electrochemical method [J]. Pizhūhish Dar Bihdāsht-i Muḥīṭ., 2018, 4(2): 104-111. [108] 张淼, 李鹏飞, 孙文娟, 等. 过氧戊二酸对公共场所空气消毒效果分析 [J]. 沈阳医学院学报, 2006, 8(2): 147-149. doi: 10.3969/j.issn.1008-2344.2006.02.039 ZHANG M, LI P F, SUN W J, et al. Study on disinfecting public rooms with perglutaric acid [J]. Journal of Shenyang Medical College, 2006, 8(2): 147-149(in Chinese). doi: 10.3969/j.issn.1008-2344.2006.02.039
[109] 谭金煜, 尹世辉, 张馨心, 等. 过氧乙酸在医院内空气消毒中的效果分析 [J]. 中国卫生标准管理, 2017, 8(18): 129-130. doi: 10.3969/j.issn.1674-9316.2017.18.068 TAN J Y, YIN S H, ZHANG X X, et al. Effect of peracetic acid on disinfection of air in hospital [J]. China Health Standard Management, 2017, 8(18): 129-130(in Chinese). doi: 10.3969/j.issn.1674-9316.2017.18.068
[110] TSO K M, NI B, WONG H C. Oxidative disinfectants activate different responses in Vibrio parahaemolyticus [J]. Journal of Food Protection, 2019, 82(11): 1890-1895. doi: 10.4315/0362-028X.JFP-19-191 [111] CHHETRI R K, BAUN A, ANDERSEN H R. Algal toxicity of the alternative disinfectants performic acid (PFA), peracetic acid (PAA), chlorine dioxide (ClO2) and their by-products hydrogen peroxide (H2O2) and chlorite (ClO2−) [J]. International Journal of Hygiene and Environmental Health, 2017, 220(3): 570-574. doi: 10.1016/j.ijheh.2016.11.011 [112] MONTAGNA M T, TRIGGIANO F, BARBUTI G, et al. Study on the in vitro activity of five disinfectants against nosocomial bacteria [J]. International Journal of Environmental Research and Public Health, 2019, 16(11): 1895. doi: 10.3390/ijerph16111895 [113] BARBUT F, MENUET D, VERACHTEN M, et al. Comparison of the efficacy of a hydrogen peroxide dry-mist disinfection system and sodium hypochlorite solution for eradication of Clostridium difficile spores [J]. Infection Control and Hospital Epidemiology, 2009, 30(6): 507-514. doi: 10.1086/597232 [114] KINGSLEY D H, VINCENT E M, MEADE G K, et al. Inactivation of human norovirus using chemical sanitizers [J]. International Journal of Food Microbiology, 2014, 171: 94-99. doi: 10.1016/j.ijfoodmicro.2013.11.018 [115] LINEBACK C B, NKEMNGONG C A, WU S T, et al. Hydrogen peroxide and sodium hypochlorite disinfectants are more effective against Staphylococcus aureus and Pseudomonas aeruginosa biofilms than quaternary ammonium compounds [J]. Antimicrobial Resistance & Infection Control, 2018, 7(1): 154. [116] SCHOLTZ V, PAZLAROVA J, SOUSKOVA H, et al. Nonthermal plasma—a tool for decontamination and disinfection [J]. Biotechnology Advances, 2015, 33(6): 1108-1119. doi: 10.1016/j.biotechadv.2015.01.002 [117] LAROUSSI M. Low temperature plasma-based sterilization: Overview and state-of-the-art [J]. Plasma Processes and Polymers, 2005, 2(5): 391-400. doi: 10.1002/ppap.200400078 [118] 王妍彦, 张伟, 班海群, 等. 等离子体对空气消毒效果影响因素的研究 [J]. 中国卫生检验杂志, 2014, 24(10): 1463-1464. WANG Y Y, ZHANG W, BAN H Q, et al. Study on the influencing factors of plasma in air disinfection effect [J]. Chinese Journal of Health Laboratory Technology, 2014, 24(10): 1463-1464(in Chinese).
[119] ZHANG H, CHEN M, HUANG L L, et al. Using cold atmospheric plasma treated-air for COVID-19 disinfection in cold-chain environment [J]. Journal of Physics D:Applied Physics, 2021, 54(40): 40LT01. doi: 10.1088/1361-6463/ac13f7 [120] 闫妍, 高亚楠, 李其玮, 等. 等离子体与纳米二氧化钛光触媒协同对室内空气消毒效果研究 [J]. 中国消毒学杂志, 2022, 39(2): 83-86. YAN Y, GAO Y N, LI Q W, et al. Purification and disinfection effect of indoor air by plasma coupling Ag/TiO2 nanophotocatalysis system [J]. Chinese Journal of Disinfection, 2022, 39(2): 83-86(in Chinese).
[121] WANG S N, LI J J, LIU Y X, et al. Pulsed xenon ultraviolet and non-thermal atmospheric plasma treatments are effective for the disinfection of air in hospital blood sampling rooms [J]. Photodiagnosis and Photodynamic Therapy, 2019, 27: 137-140. doi: 10.1016/j.pdpdt.2019.05.034 [122] ELGOHARY E A, MOHAMED Y M A, EL NAZER H A, et al. A review of the use of semiconductors as catalysts in the photocatalytic inactivation of microorganisms [J]. Catalysts, 2021, 11(12): 1498. doi: 10.3390/catal11121498 [123] 王洪波, 崔娅琴, 李莹莹, 等. 水和废水纳米TiO2光催化消毒国外研究进展 [J]. 山东建筑大学学报, 2012, 27(1): 105-110. WANG H B, CUI Y Q, LI Y Y, et al. Foreign research progress of TiO2 photocatalytic disinfection for water and wastewater [J]. Journal of Shandong Jianzhu University, 2012, 27(1): 105-110(in Chinese).
[124] FOSTER H A, DITTA I B, VARGHESE S, et al. Photocatalytic disinfection using titanium dioxide: Spectrum and mechanism of antimicrobial activity [J]. Applied Microbiology and Biotechnology, 2011, 90(6): 1847-1868. doi: 10.1007/s00253-011-3213-7 [125] 于小迪, 王洪波, 刘麒, 等. 二氧化钛光催化消毒技术在水处理中的研究 [J]. 环境科学与管理, 2013, 38(1): 81-86. doi: 10.3969/j.issn.1673-1212.2013.01.021 YU X D, WANG H B, LIU Q, et al. Application of titanium dioxide photocatalytic disinfection in water treatment [J]. Environmental Science and Management, 2013, 38(1): 81-86(in Chinese). doi: 10.3969/j.issn.1673-1212.2013.01.021
[126] SUN D, MAO J, CHENG L, et al. Magnetic g-C3N4/NiFe2O4 composite with enhanced activity on photocatalytic disinfection of Aspergillus flavus [J]. Chemical Engineering Journal, 2021, 418: 129417. doi: 10.1016/j.cej.2021.129417 [127] KHAN S, BEATTIE T K, KNAPP C W. Relationship between antibiotic- and disinfectant-resistance profiles in bacteria harvested from tap water [J]. Chemosphere, 2016, 152: 132-141. doi: 10.1016/j.chemosphere.2016.02.086 [128] WALSH C. Molecular mechanisms that confer antibacterial drug resistance [J]. Nature, 2000, 406(6797): 775-781. doi: 10.1038/35021219 [129] TONG C Y, HU H, CHEN G, et al. Chlorine disinfectants promote microbial resistance in Pseudomonas sp [J]. Environmental Research, 2021, 199: 111296. doi: 10.1016/j.envres.2021.111296 [130] HOU A M, YANG D, MIAO J, et al. Chlorine injury enhances antibiotic resistance in Pseudomonas aeruginosa through over expression of drug efflux pumps [J]. Water Research, 2019, 156: 366-371. doi: 10.1016/j.watres.2019.03.035 [131] LV L, JIANG T, ZHANG S H, et al. Exposure to mutagenic disinfection byproducts leads to increase of antibiotic resistance in Pseudomonas aeruginosa [J]. Environmental Science & Technology, 2014, 48(14): 8188-8195. [132] 林辉, 郑剑, 宋启发, 等. 含氯消毒剂对产β内酰胺酶铜绿假单胞菌杀菌效果的研究 [J]. 中国消毒学杂志, 2008, 25(2): 145-147. LIN H, ZHENG J, SONG Q F, et al. Study on efficacy of chlorine-containing disinfectant in killing pseudomonas aeruginosa producing β- lactamase [J]. Chinese Journal of Disinfection, 2008, 25(2): 145-147(in Chinese).
[133] ZHANG Q Q, TIAN G M, JIN R C. The occurrence, maintenance, and proliferation of antibiotic resistance genes (ARGs) in the environment: Influencing factors, mechanisms, and elimination strategies [J]. Applied Microbiology and Biotechnology, 2018, 102(19): 8261-8274. doi: 10.1007/s00253-018-9235-7 [134] JIN M, LIU L, WANG D N, et al. Chlorine disinfection promotes the exchange of antibiotic resistance genes across bacterial Genera by natural transformation [J]. The ISME Journal, 2020, 14(7): 1847-1856. doi: 10.1038/s41396-020-0656-9 [135] ZHANG Y, GU A Z, HE M, et al. Subinhibitory concentrations of disinfectants promote the horizontal transfer of multidrug resistance genes within and across Genera [J]. Environmental Science & Technology, 2017, 51(1): 570-580. [136] CHOI H, CHATTERJEE P, HWANG M, et al. Can multidrug-resistant organisms become resistant to ultraviolet (UV) light following serial exposures?Characterization of post-UV genomic changes using whole-genome sequencing [J]. Infection Control and Hospital Epidemiology, 2022, 43(1): 72-78. doi: 10.1017/ice.2021.51 [137] YE C S, CHEN Y M, FENG L, et al. Effect of the ultraviolet/chlorine process on microbial community structure, typical pathogens, and antibiotic resistance genes in reclaimed water [J]. Frontiers of Environmental Science & Engineering, 2022, 16(8): 100. [138] KARR J R. Defining and assessing ecological integrity: Beyond water quality [J]. Environmental Toxicology and Chemistry, 1993, 12(9): 1521-1531. doi: 10.1002/etc.5620120902 [139] 张坤锋, 昌盛, 涂响, 等. 新冠疫情下武汉典型饮用水水源中DBPs污染特征与风险评估 [J]. 环境科学, 2022, 43(2): 878-886. doi: 10.13227/j.hjkx.202106099 ZHANG K F, CHANG S, TU X, et al. Pollution characteristics and risk assessment of DBPs in typical drinking water sources in Wuhan under the COVID-19 pandemic [J]. Environmental Science, 2022, 43(2): 878-886(in Chinese). doi: 10.13227/j.hjkx.202106099
[140] CUI H J, ZHU X S, ZHU Y J, et al. Ecotoxicological effects of DBPs on freshwater phytoplankton communities in co-culture systems [J]. Journal of Hazardous Materials, 2022, 421: 126679. doi: 10.1016/j.jhazmat.2021.126679 [141] ALBRICH J M, McCARTHY C A, HURST J K. Biological reactivity of hypochlorous acid: Implications for microbicidal mechanisms of leukocyte myeloperoxidase [J]. Proceedings of the National Academy of Sciences of the United States of America, 1981, 78(1): 210-214. doi: 10.1073/pnas.78.1.210 [142] ISSA-ZACHARIA A, KAMITANI Y, MORITA K, et al. Sanitization potency of slightly acidic electrolyzed water against pure cultures of Escherichia coli and Staphylococcus aureus, in comparison with that of other food sanitizers [J]. Food Control, 2010, 21(5): 740-745. doi: 10.1016/j.foodcont.2009.11.002 [143] SLAUGHTER R J, WATTS M, VALE J A, et al. The clinical toxicology of sodium hypochlorite [J]. Clinical Toxicology, 2019, 57(5): 303-311. doi: 10.1080/15563650.2018.1543889 [144] MURASHEVYCH B, GIRENKO D, MASLAK H, et al. Acute inhalation toxicity of aerosolized electrochemically generated solution of sodium hypochlorite [J]. Inhalation Toxicology, 2022, 34(1/2): 1-13. [145] National Institute for Occupational Safety and Health. NIOSH pocket guide to chemical hazards: No. 2005-149 [S]. 2005. [146] LARDIERI A, CHENG C, JONES S C, et al. Harmful effects of chlorine dioxide exposure [J]. Clinical Toxicology, 2021, 59(5): 448-449. doi: 10.1080/15563650.2020.1818767 [147] AKAMATSU A, LEE C, MORINO H, et al. Six-month low level chlorine dioxide gas inhalation toxicity study with two-week recovery period in rats [J]. Journal of Occupational Medicine and Toxicology, 2012, 7: 2. doi: 10.1186/1745-6673-7-2 [148] XIA Q D, ZHANG G M, WANG L. Study on subchronic toxicity of chlorine dioxide and by-products in water [J]. Journal of Environmental Science and Health, Part A, 2006, 41(7): 1347-1353. doi: 10.1080/10934520600657016 [149] COURI D, ABDEL-RAHMAN M S, BULL R J. Toxicological effects of chlorine dioxide, chlorite and chlorate [J]. Environmental Health Perspectives, 1982, 46: 13-17. doi: 10.1289/ehp.824613 [150] STRATILO C W, CRICHTON M K F, SAWYER T W. Decontamination efficacy and skin toxicity of two decontaminants against Bacillus anthracis [J]. PLoS One, 2015, 10(9): e0138491. doi: 10.1371/journal.pone.0138491 [151] HARTWIG A, COMMISSION M. Hydrogen peroxide//The MAK Collection for Occupational Health and Safety[M]. 2019: 2108–2113. [152] SUENAKA T, ALASKA S, HIRATA M. A survey of occupational exposure to hydrogen peroxide-H2O2exposure level and its effects on lipid peroxide and its related enzyme activities//Proceedings of Osaka Prefecture Institute of Public Health, Edition of Industrial Health[C]. 1984. [153] European Chemical Industry Council (CEFIC). Hydrogen peroxide: 28-day inhalation study: 2002–0082-DKT [S]. 2002. [154] MOHANAN P V, SANGEETHA V, SABAREESWARAN A, et al. Safety of 0.5% hydrogen peroxide mist used in the disinfection gateway for COVID-19 [J]. Environmental Science and Pollution Research International, 2021, 28(47): 66602-66612. doi: 10.1007/s11356-021-15164-y [155] PASCUAL A, LLORCA I, CANUT A. Use of ozone in food industries for reducing the environmental impact of cleaning and disinfection activities [J]. Trends in Food Science & Technology, 2007, 18: S29-S35. [156] POPPENDIECK D, HUBBARD H, WARD M, et al. Ozone reactions with indoor materials during building disinfection [J]. Atmospheric Environment, 2007, 41(15): 3166-3176. doi: 10.1016/j.atmosenv.2006.06.060 [157] VITHU P, DEB B R, RANJIT S, et al. Ozone technology in food processing: A review [J]. Trends in Biosciences, 2016, 8(16): 4031-4047. [158] GULAFSHA M, MDS A P. Miracle of ozone in dentistry: An overview [J]. World Journal of Pharmaceutical Research, 2019, 8(3): 665-677. [159] NIU Y, CHEN R J, XIA Y J, et al. Personal ozone exposure and respiratory inflammatory response: The role of DNA methylation in the arginase-nitric oxide synthase pathway [J]. Environmental Science & Technology, 2018, 52(15): 8785-8791. [160] VIOLA K S, RODRIGUES E M, TANOMARU-FILHO M, et al. Cytotoxicity of peracetic acid: Evaluation of effects on metabolism, structure and cell death [J]. International Endodontic Journal, 2017, 51: e264-e277. [161] CHHETRI R K, BAUN A, ANDERSEN H R. Acute toxicity and risk evaluation of the CSO disinfectants performic acid, peracetic acid, chlorine dioxide and their by-products hydrogen peroxide and chlorite [J]. Science of the Total Environment, 2019, 677: 1-8. doi: 10.1016/j.scitotenv.2019.04.350 [162] SMALL D A, CHANG W, TOGHROL F, et al. Comparative global transcription analysis of sodium hypochlorite, peracetic acid, and hydrogen peroxide on Pseudomonas aeruginosa [J]. Applied Microbiology and Biotechnology, 2007, 76(5): 1093-1105. doi: 10.1007/s00253-007-1072-z -




 DownLoad:
DownLoad: