-
全氟化合物(polyfluoroalkyl substances,PFASs)具有良好的疏水疏油性、高活性和热稳定性,被广泛应用于工业生产和民用成品制备[1]. 随着含氟产品的生产、使用和处理,PFASs被释放到周围的环境中. 同时,该物质具有环境持久性、远距离迁移性和生物蓄积性,使得其最终进入到整个生态系统中,作为一类持久性有机污染物对周围的生态环境和生物物种造成潜在风险[2-6]. 尽管国内外已经对传统的PFASs做出管控[7-8],但鉴于该类物质在生产过程中不可或缺,使得近些年氟化工生产商研制出更多的含氟替代品,用结构类似的以及短链的PFASs[9]代替传统PFASs来满足市场需求. 目前,已有研究表明,这类替代品同样具有环境持久性以及生物毒性,且在环境中已被大量检出[10].
工业生产排放是PFASs最主要的来源,目前,关于PFASs进入环境有两种猜想:一种是半挥发性、挥发性PFASs随大气运动远距离传输[11],另一种是水体环流带动离子态PFASs迁移[12]. 河流承载了来自工业生产过程中产生的PFASs,最终进入海洋中[13]. 所以,了解水环境中PFASs在水体与沉积物的分配机制对理解PFASs在环境中的迁移转化规律具有重要意义.
太浦河是连接东太湖和黄浦江的重要河段,是上海市重要的饮用水水源地之一,为上海市西南5区提供原水. 目前,太浦河的水质调查多围绕抗生素[14]、重金属[15]等展开,而对于PFASs在太浦河中的时空分布特征以及在沉积物和水中分配规律的了解非常有限. 大量研究表明,PFASs的碳链长度会影响沉积物的吸附量[16-17],沉积物本身的理化性质,如总有机碳(total organic carbon,TOC)[18-20]也会影响到水环境中PFASs的分配规律. 因此,研究PFASs链长以及太浦河中沉积物的TOC含量对PFASs在水环境中分布特征的影响,可以揭示PFASs在河流中的迁移转化规律.
本研究以传统、替代和短链的24种PFASs为研究对象,针对太浦河流域的水体和沉积物,于冬、夏两季采样并分析该河段重要点位的水体和沉积物样品中目标PFASs的污染水平和分布规律,研究该流域目标PFASs季节性变化规律,解析PFASs在太浦河不同介质中的归趋、分布特征和来源,不仅为饮用水安全风险评估提供数据,还可为控制PFASs的排放提供科学依据.
-
主要仪器包括:高效液相色谱-串联质谱(Waters公司,美国),全自动氮吹仪(睿科仪器股份有限公司,厦门),超声波清洗器(安谱实验科技股份有限公司,上海),全自动固相萃取仪(睿科仪器股份有限公司,厦门),低温真空冷冻干燥机(昊博低温真空设备有限公司,上海),总有机碳分析仪(耶拿分析仪器股份公司,德国),电子分析天平(岛津实验器材有限公司,上海).
实验过程中使用的甲醇、乙腈(色谱纯)购于德国Merck公司,乙酸铵(色谱纯)购于美国ANPEL公司,氨水(>25%)购于上海易恩化学技术有限公司. 标准品(>98%)均购于加拿大惠灵顿公司,具体信息如表1所示.
-
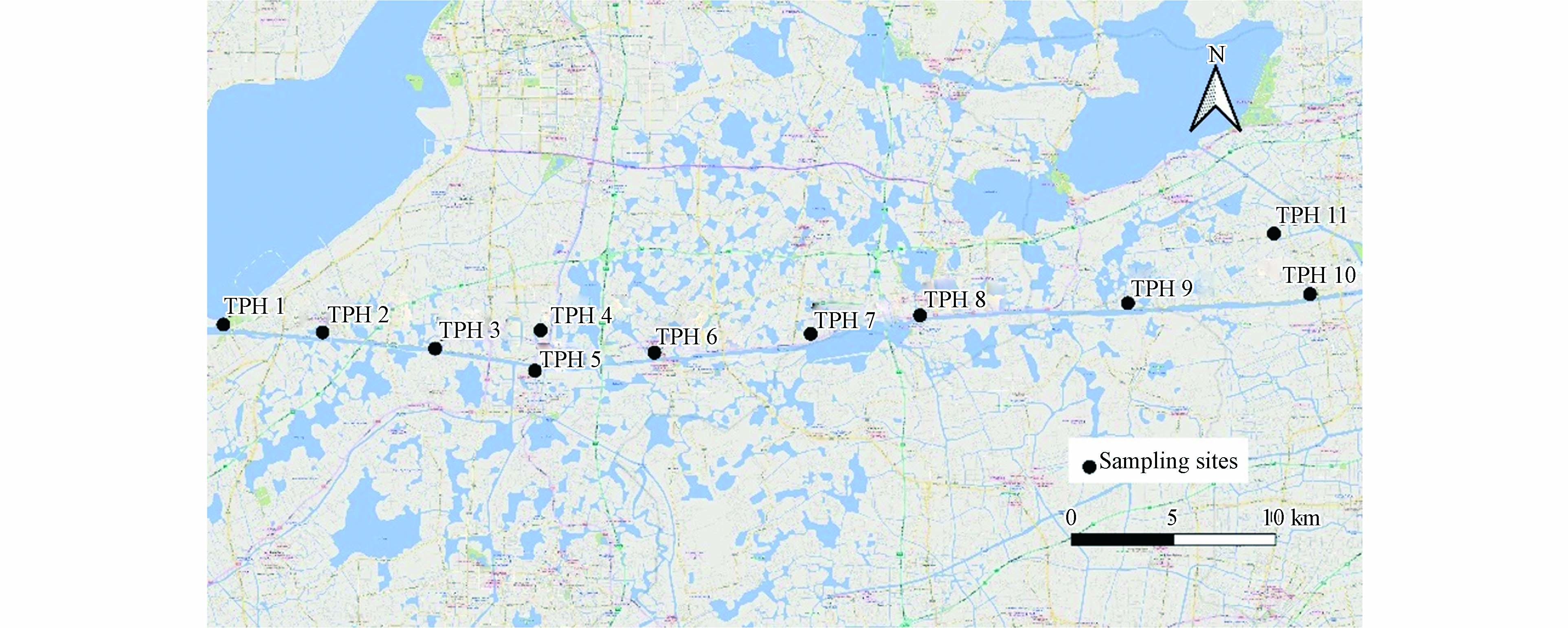
本研究于2022年1、7月期间采集了太浦河流域的19份水样与6份沉积物样品,具体采样点和采集情况如图1和表2所示. 使用不锈钢采水器采集水面以下0.5—1 m处的水样,装入1 L高密度聚乙烯容器中. 使用不锈钢抓斗式采泥器采集采水处附近1 m2范围内的沉积物样品,并装入不锈钢容器中. 对于入河口、航运发达和工业繁华的点位(TPH1、TPH3、TPH4、TPH11),收集两个平行样,混合均匀后进行前处理,以减少采样过程中的随机性. 水样采集后在24 h内完成预处理,沉积物样品冻干并过100目筛(0.15 mm)后,装入聚丙烯袋中于−20 ℃保存,待进一步处理.
-
水样前处理在刘晓雷等[21]方法上进行了优化,具体过程为:取250 mL水样,过0.7 μm的GF/F玻璃纤维滤膜(Whatman公司,英国),加入5 ng内标后混匀待用. 依次用5 mL 0.1%的氨水/甲醇(V:V)溶液以及5 mL超纯水(Milli-Q)活化Oasis-WAX固相萃取柱(500 mg,6 mL),将水样以3 mL·min−1的流速通过预活化的WAX小柱富集目标PFASs. 用5 mL 25 mmol的乙酸铵水溶液和5 mL 80%甲醇/水溶液淋洗小柱,气推除去残余水分. 最后,用10 mL 0.1%的氨水/甲醇溶液和5 mL 0.1%的氨水/乙腈溶液洗脱,气推并收集洗脱液. 洗脱液在水浴加热45 ℃条件下氮吹至近干,用500 μL的2 mmol·L−1乙酸铵水溶液:甲醇(30:70,V:V)的溶剂复溶,通过0.22 μm PTFE针式滤器转移至聚丙烯进样小瓶中.
沉积物前处理在Shi等[22]的方法上进行改进:称取1 g冻干后的沉积物样品,加入5 ng内标和5 mL的甲醇溶剂. 涡旋混匀2 min,在30 ℃下超声20 min,最后3000 r·min-1离心10 min后,抽取上清液过0.45 μm的玻璃纤维针式滤器至另一个50 mL离心管中. 重复上述提取步骤两次,将提取的上清液合并后氮吹至近干,复溶后将溶液转移至进样小瓶.
-
24种PFASs的分析仪器为Waters Acquity HPLC@I Class液相色谱仪串联Waters Xevo TQ-XS micro质谱仪,色谱柱为ACQUITY UPLC®BEH C18(ϕ2.1 mm
× 100 mm,1.7 μm,美国Waters公司). 流动相A为5 mmol的乙酸铵水溶液,流动相B为乙腈,采用梯度洗脱的方式:0—3.5 min,10%—50% B;3.5—6.0 min,50%—95% B;6—8 min,95% B;8—8.5 min,95%—10% B;8.5—10 min,10% B. 进样量为1 μL,流速为0.3 mL·min−1,色谱柱柱温为40 ℃.质谱条件为:采用多重反应离子监测模式(MRM),电喷雾负离子扫描模式(ESI-),离子源温度150 ℃,脱溶剂气温度500 ℃,脱溶剂气流速1000 L·h−1,毛细管电压3 kV,氮气作为脱溶剂气和锥孔气,氩气作为碰撞气.
-
本研究实验过程中使用的器皿均为聚丙烯材料,使用前用纯水和甲醇润洗并晾干,全自动固相萃取仪使用结束后,用纯水和甲醇对管路进行二次冲洗,每次实验均设置空白对照以及溶剂空白,每个点位的样品设置3个平行,尽可能减少环境因素对实验结果的影响. 对24种PFASs在0.14—50 ng·mL−1的浓度区间内配制7个浓度梯度的标曲,加入10 ng·mL−1的内标. 24种PFASs在此浓度区间内具有良好的线性关系(R2>0.995). 分别向7个空白样中加入一定量的标准品(250 mL水样中加0.25 ng和1 ng标准品,1 g沉积物样品中加0.5 ng和1 ng标准品),根据7次平行的标准偏差计算方法检出限(MDL),计算公式为:MDL=t(n-1,α=0.01)×S, t分布;n为样品自由度;S为加标样品减去空白样品的标准偏差. 向3个空白样品中分别加入高、中、低浓度(水样:4、20、50 ng·L−1;沉积物:1、5、10 ng·g−1)的混标,得到水和沉积物的加标回收率. 水体中PFASs的回收率在71.67%—105.33%,相对标准偏差均小于20%;沉积物中PFASs的回收率在60.17%—149.43%,相对标准偏差均小于20%,PFASs在水体和沉积物介质中的MDL分别在0.104—1.006 ng·L−1和0.050—0.131 ng·g−1,均满足痕量分析的要求.
-
数据处理使用Excel 2016和Origin 2016软件. 统计时,若PFASs含量<MDL,数值以0计算. 选取同一点位的水样和沉积物中PFASs的含量来计算分配系数,计算公式[23]为:
式中,
Kd —PFASs的水-沉积物的分配系数,L·kg−1;Cs —沉积物中PFASs的含量,μg·kg−1;Cw —水体中PFASs的含量,μg·L−1;Koc —PFASs经有机碳校正后的水-沉积物的分配系数,L·kg−1;foc —沉积物中TOC的质量分数. -
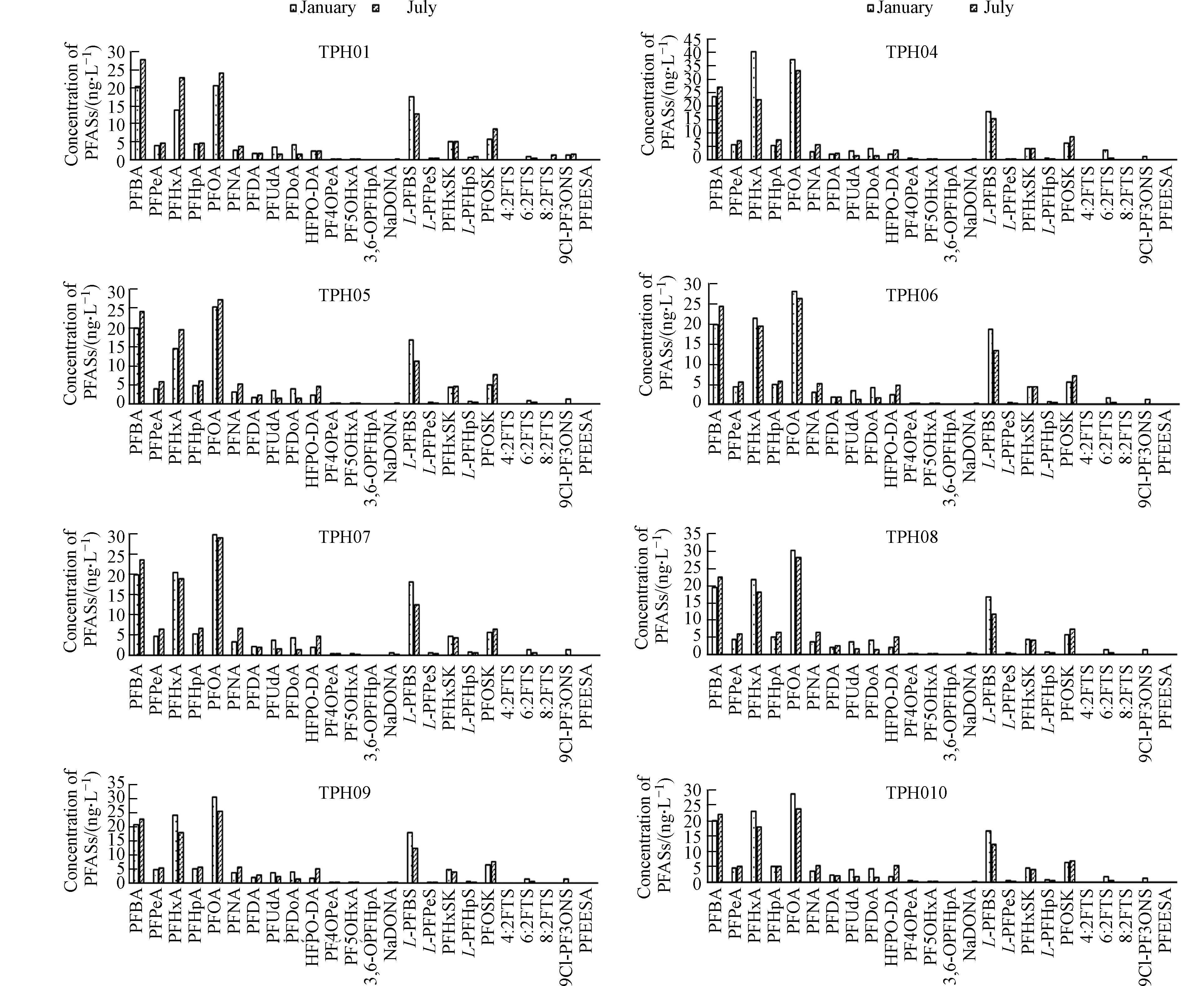
本研究分别在2022年1月份与7月份采集太浦河表层河水并检测,冬、夏季水体中24种目标PFASs的浓度水平对比和各点位的PFASs含量见图2和图3. 结果表明,冬季太浦河水体中共检出了20种PFASs,除3,6-OPFHpA、4:2FTS、8:2FTS和PFEESA未检出外,其他目标PFASs检出率在37.5%—100%,说明目标PFASs在太浦河水体中普遍存在.
Σ PFASs浓度范围在108.67—162.59 ng·L−1,其中PFHxA和PFOA的检出浓度较大,平均浓度为22.44 ng·L−1和28.86 ng·L−1,略大于金磊[24]在太浦河流域的调查结果(PFHxA和PFOA的平均浓度为18.25 ng·L−1和24.81 ng·L−1),中位数浓度为21.56 ng·L−1和29.26 ng·L−1. 24种目标PFASs中,PFCAs和PFSAs的检出率为100%,其他种类的目标PFASs检出率较小且浓度水平低.夏季太浦河水体中共检出了21种PFASs,除3,6-OPFHpA、4:2FTS和PFEESA未检出外,其他目标PFASs检出率在18.18%—100%.
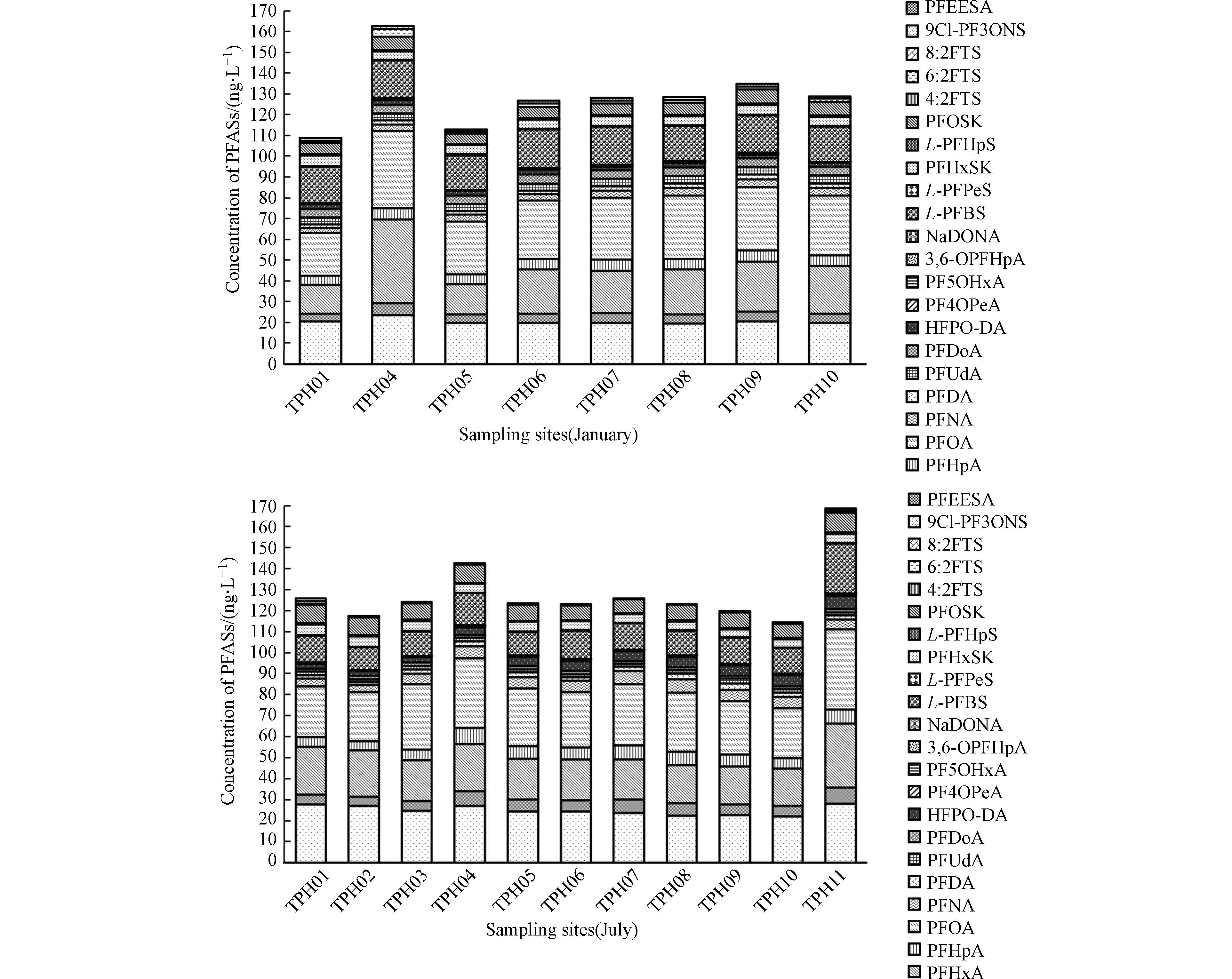
Σ PFASs浓度范围在114.24—168.62 ng·L−1,其中PFBA和PFOA的检出浓度较大,平均浓度为24.92 ng·L−1和28.18 ng·L−1,中位数浓度为24.36 ng·L−1和27.30 ng·L−1. 由图2可以看出,冬、夏两季各点位水体中PFASs浓度与种类差异较小,没有表现出明显的季节性变化. 研究表明,湿沉降是影响河流中PFASs浓度的一个重要因素[25-27],工业生产未能处理的PFASs随着降水和地表径流进入周围的水体,会出现湿季(夏季)水体中PFASs含量、种类高于干季(冬季)的现象. 通过查询中国气象局资料发现,太浦河流域2022年1月份的月累积降水量为50—100 mm,与2022年7月份的数据相同,没有表现出季节性变化特征. 此外,太浦河附近污染源排放较为稳定. 故此次监测结果没有体现出明显差异.由图3可以看出,太浦河各点位水体中
Σ PFASs波动不大,冬季在128 ng·L−1左右,夏季在125 ng·L−1左右,总体低于东太湖水体中Σ PFASs的含量(176 ng·L−1左右)[28]. 这与太湖流域汇集了来自江苏境内氟化工厂和纺织工业产生的PFASs,而太浦河附近大型的氟化工厂少有关. 在京杭大运河附近的TPH4和南横港附近的TPH11,水体中PFASs的总浓度明显高于其他地点的水样. 这两个点位所在河段都是重要的航道,航运活动频繁,船只与码头的防水油脂和保护油漆中的含氟物质会使附近水体中PFASs突增[29]. -
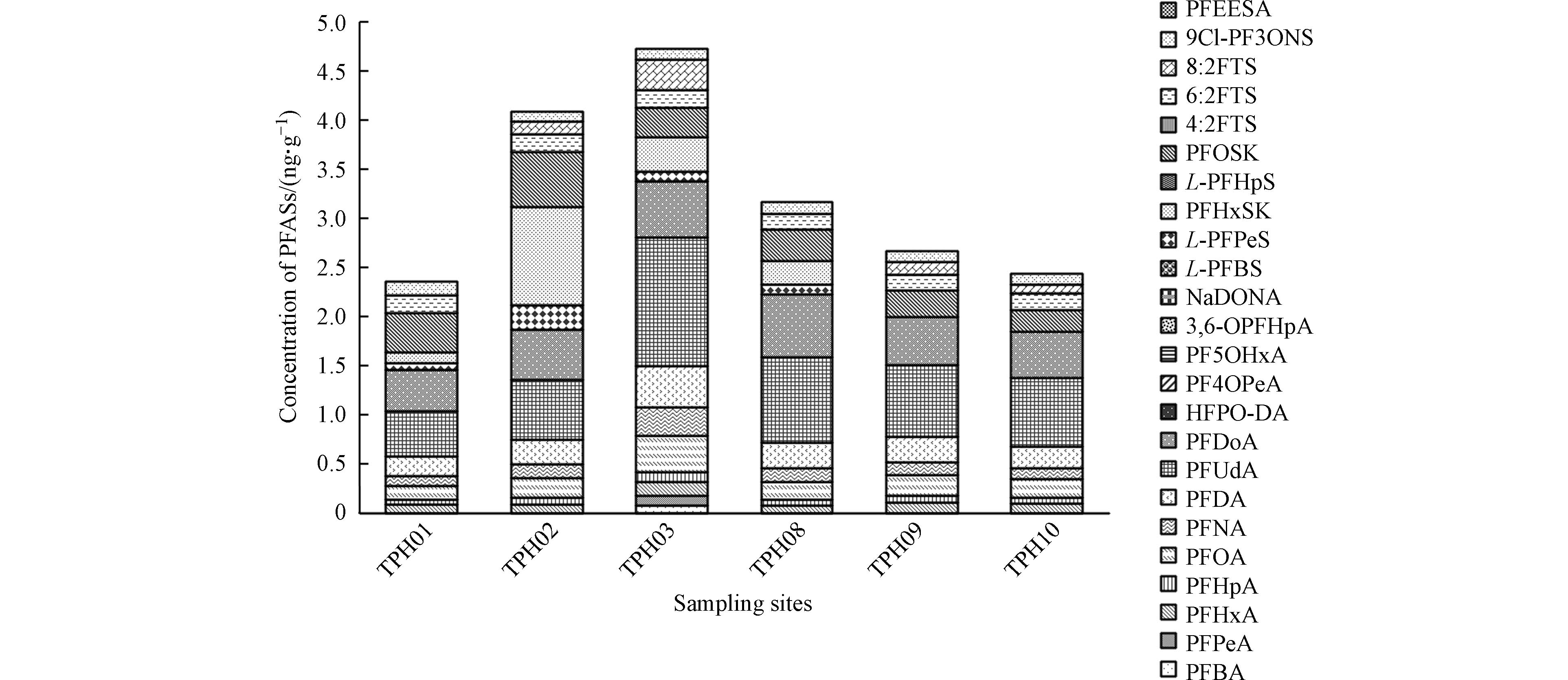
沉积物是持久性有机污染物的一个重要归趋[30],本研究沿太浦河采集了6个点位的沉积物并检测其PFASs的含量. 除HFPO-DA、PF4OPeA、PF5OHxA、3,6-OPFHpA、NaDONA、L-PFBS、L-PFHpS、4:2FTS和PFEESA外,15种目标PFASs在太浦河沉积物中都有不同程度的检出,检出率在16.67%—100%,
Σ PFASs在2.36—4.73 ng·g−1(dw),小于太湖流域沉积物中Σ PFASs的含量(5.8—35 ng·g−1(dw))[28]. PFUdA和PFDoA检出浓度最大,平均浓度为0.78 ng·g−1(dw)和0.52 ng·g−1(dw),中位数浓度为0.72 ng·L−1(dw)和0.50 ng·L−1(dw).从各点位沉积物中目标PFASs的含量变化(图4)可以看出,TPH2和TPH3沉积物中PFASs的含量较高,其它点位沉积物中PFASs含量则较少. 调查发现,TPH2和TPH3点位沿岸的纺织业和造纸业发达,而PFASs在纺织、造纸等领域有着广泛的应用[31-32],随着其生产、使用和处置过程,将会有大量的PFASs进入周围的水环境中,并使得该点位附近沉积物中PFASs含量增大.
-
太浦河上游与东太湖相连接,其中PFOA是太湖中最主要的PFASs[28],本次研究结果也表明太浦河水体中PFOA浓度最高. 从图5可以看出,除PFOA外,太浦河表层水体中碳链长度<7的PFASs含量和检出率明显高于长链PFASs,短链的PFHxA、PFBA和L-PFBS是水中主要的PFASs,占比为46.45%,这可能是短链的PFASs相较于长链PFASs具有更大的溶解度[33]和更高的迁移率. 水体中检测到浓度最高的PFSAs是PFBS,PFOS对PFASs的贡献率显著下降,说明《斯德哥尔摩公约》的限制[34]对控制PFOS的生产排放取得了较好的效果. 而现有的法规也加强了对长链PFASs的监管,新型的短链PFASs(PFHxA、PFBA和L-PFBS)逐渐代替了传统的长链PFASs(PFOA和PFOS),并在水环境中被大量检测到[35].
长链PFASs在沉积物中浓度最大,沉积物中长链(依据经济合作与发展组织的准确定义:
≥ 6个碳原子的PFSAs,以及≥ 7个碳原子的其它PFASs)的PFASs对Σ PFASs的贡献率是短链PFASs的7.76倍,与之前报道的长链PFASs较短链PFASs更易吸附在沉积物上一致[36]. 这可能与长链PFASs化学性质更稳定[37],且水溶性弱有关[38]. 在相同碳链长度情况下,不同官能团的PFASs在沉积物和水体中分配情况也不相同:沉积物中同碳链长度的PFSAs浓度普遍大于PFCAs,与水体中的情况相反,这与Lau等[38]研究结果一致,说明PFSAs比PFCAs更易附着在沉积物上.影响PFASs在水环境中分配的因素除了碳链长度外[16],还包括了沉积物中
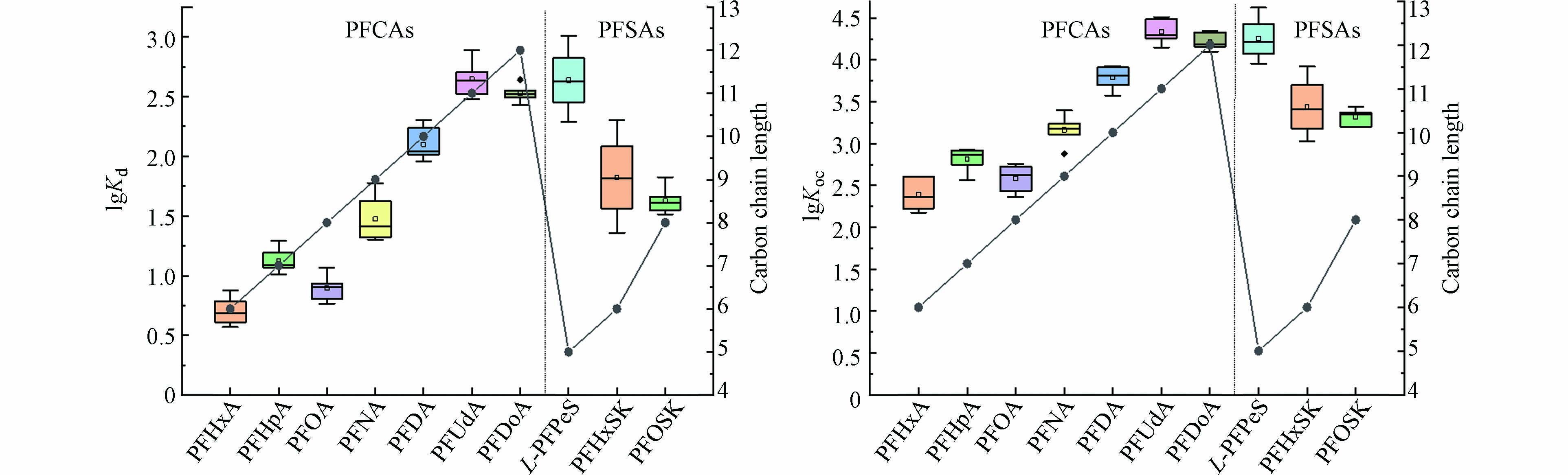
foc [39]、水的硬度和pH值[16]. 其中分配作用中起主导作用的是沉积物的有机质与脂肪,它们可作为有机溶剂将水相中溶解度较小的PFASs萃取到沉积物中,并随着时间推移达到平衡[40]. 本研究选取不同碳链长度的PFCAs和PFSAs,研究它们在沉积物和水体间的分配系数lgKd和lgKoc. 从图6可以看出,PFHxA、PFHpA和PFOA的lgKd在0.57—1.29,变化趋势较小,但从PFOA开始到PFUdA,lgKd随着碳链长度的增加而呈明显的增长趋势,这与杨洪法等[41]和Wang等[42]研究结果一致. 与杨洪法等[41]研究得到的PFSAs的lgKd随碳链长度增加而增加不同,3种PFSAs的lgKd随碳链长度变化趋势不明显,这可能是与沉积物中短链PFSAs的检出率(67%)低于长链PFSAs的检出率(100%)有关. 经foc 校正后, 不同PFASs的lgKoc变化趋势见图6. 其变化趋势与lgKd完全一致,除沉积物中存在点位未检出的L-PFPeS和PFHxSK外,各PFCAs和PFSAs的lgKoc均比lgKd高1.69个对数单位. 这表明,在水环境体系中,foc 是影响PFASs在水体和沉积物中分配情况的重要因素[23]. 除去未检出的情况,相同碳链长度PFCAs的lgKoc值均低于PFSAs:PFHxA比PFHxSK的lgKoc值低1个单位左右,PFOA比 PFOSK的lgKoc值低0.8个单位左右,说明PFSAs较PFCAs更易吸附在沉积物上. -
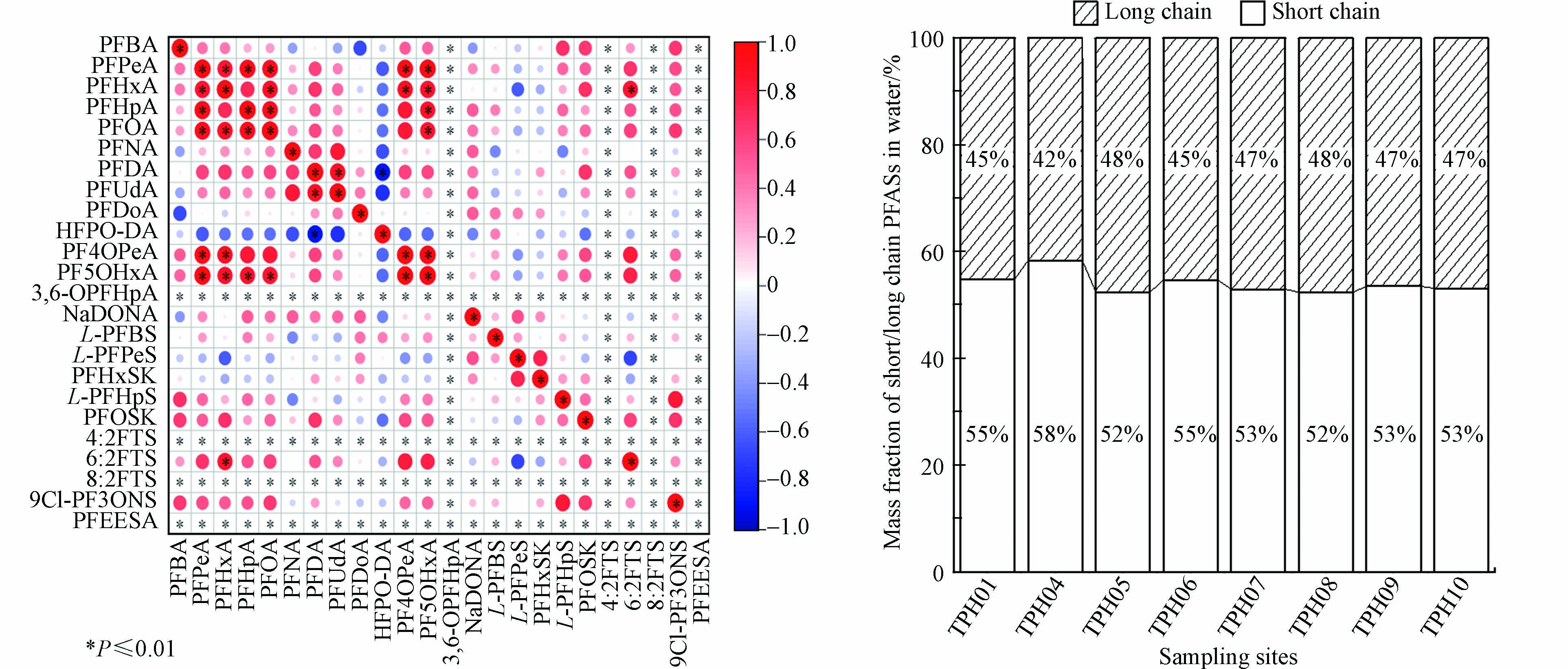
太浦河周围水系发达,航运和渔业在发展过程中产生的PFASs将会直接排入周围的水体,除此之外,半挥发态、挥发态的前体物随大气运动以及离子态的PFASs随水流进行远距离输送[11-12],都可能是太浦河水环境中PFASs的重要来源. 目前推断水环境中PFASs潜在来源常用的方法是各PFASs间的相关性分析[43],本研究选用1月份水样监测数据进行分析,水体中各PFASs间Spearman相关分析和短/长链的质量分数见图7(a)和图7(b). PFOS与PFHxA呈显著性相关(P<0.01),这与肖少可等研究结论一致[44]. 由图7(a)可知,PFPeA与PFOA、PFHpA、PFHxA、PF4OPeA和PF5OHxA呈显著性正相关(P<0.01),PFHxA与PFOA、6:2FTS、PF4OPeA和PF5OHxA呈显著性正相关(P<0.01),PFHpA与PF5OHxA和PFOA呈显著性正相关(P<0.01),PFOA与PF5OHxA呈显著性正相关(P<0.01),PFUdA与PFDA呈显著性正相关(P<0.01),PF4OPeA与PF5OHxA呈显著性正相关(P<0.01),说明它们可能具有相同的来源. 还可根据河流方向,不同点位间短/长链的比值,来判断外源输入(短链多)和点源排放(长链多)对水体中PFASs的贡献率[45]. 根据图7(b)可以看出,太浦河水体中短链PFASs与长链PFASs占比相近,且各点变化趋势不大,说明该地区水体中PFASs的来源包括了外源输入和点源排放,且两个来源的贡献值相当.
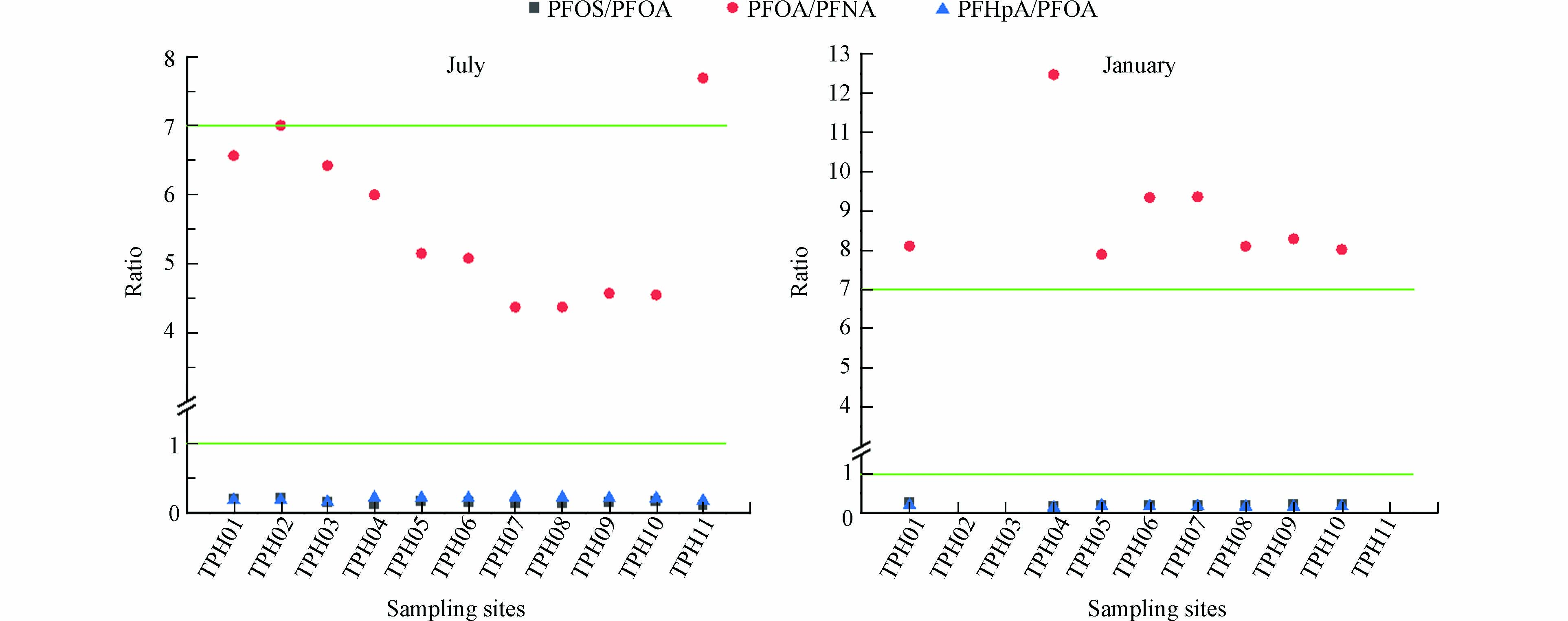
比值法是研究PFASs来源的另一个重要方法,通过分析水样的PFOS/PFOA、PFOA/PFNA和PFHpA/PFOA值来追溯源头. PFOS/PFOA值常用于探讨PFASs的潜在来源,PFOS/PFOA>1说明是PFOS的点源污染,PFOS/PFOA<1则表明是降雨输入[46]. 由图8可知,冬、夏两季各点位PFOS/PFOA值均<1,这与太湖和珠江三角洲地区的研究情况是一致的[47-48],说明降雨对太浦河流域PFASs浓度变化的影响较大[46]. 可以根据PFOA/PFNA值来判断PFASs是否来自于大气运输(PFOA/PFNA<7),工厂直排(7<PFOA/PFNA<15)还是前体物降解(PFOA/PFNA>15)[49]. 本研究中PFOA/PFNA值随着季节变化存在很大差异,夏季河体内PFASs主要受到大气远距离传输影响,冬季则与河道周围的工业活动有关. 各点位在不同季节的PFHpA/PFOA值均<1,同样说明了太浦河水体中的PFASs与周围工业活动和降雨输入有关[49]. 建议对太浦河中PFASs的污染进行控制,通过加强生产过程和产业排污规范化管理,以减少点源污染.
-
(1)太浦河流域11个点位水体中目标PFASs普遍检出,
Σ PFASs在114.24—168.62 ng·L−1. 其中PFBA和PFOA的检出浓度较大,平均浓度为24.92 ng·L−1和28.18 ng·L−1. 太浦河各点位水体中Σ PFASs的波动不大,仅在水运发达的点位出现PFASs突增的情况,且该流域PFASs季节性规律并不明显.(2)太浦河流域沉积物中目标PFASs检出的种类较少,检出率和检出浓度较低. 有15种PFASs被检出,
Σ PFASs在2.36—4.73 ng·g−1(dw). PFUdA和PFDoA检出浓度最大,平均浓度为0.78 ng·g−1(dw)和0.52 ng·g−1(dw). 沉积物中PFASs的含量与周围工业发展有关.(3)碳链长度、PFASs官能团结构和
foc 是影响PFASs在水-沉积物分配的重要因素. 长链PFASs较短链PFASs更易吸附在沉积物中,PFCAs的lgKd和lgKoc随着碳链长度的增加而呈明显的增长趋势,在相同碳链长度情况下,PFSAs较PFCAs在沉积物中分配系数更大.(4)对水体中各PFASs间Spearman相关分析得出,多种PFASs间呈显著性正相关,它们可能具有相同的来源. 不同点位间短/长链PFASs的比值相近,说明该地区水体的PFASs的来源包括了外源输入和点源排放,且两个来源的贡献值相当. 通过PFOS/PFOA、PFOA/PFNA和PFHpA/PFOA值分析发现,降雨与工业活动是造成太浦河流域PFASs污染的主要因素,夏季河体内PFASs主要受到大气远距离传输的影响,冬季则与河道周围的工业活动有关.
太浦河水体和沉积物中24种全氟化合物分布特征
Distribution characteristics of 24 perfluorocarbons in Taipu River and sediments
-
摘要: 本研究以24种全氟化合物(polyfluoroalkyl substances,PFASs)为研究对象,于冬、夏两季采集了太浦河流域重要点位的水样以及沉积物,并采用固相萃取、液液萃取联合高效液相色谱-串联质谱(HPLC/MS-MS)的方法,探讨PFASs在太浦河流域水环境中的时空分布特征以及分配行为. 结果显示,水体中PFASs的总质量浓度范围在114.24—168.62 ng·L−1,主要的污染物为全氟丁酸(PFBA)和全氟辛酸(PFOA),平均浓度为24.92 ng·L−1和28.18 ng·L−1;沉积物中
Σ PFASs在2.36—4.73 ng·g−1(dw,干重),主要的污染物为全氟十一酸(PFUdA)和全氟十二酸(PFDoA),平均浓度为0.78 ng·g−1(dw)和0.52 ng·g−1(dw). 水样的监测结果显示,各点位PFASs总浓度波动不大,仅在个别点位出现PFASs突增的情况. PFASs在太浦河流段没有明显的季节性差异,这与今年夏季降雨量少的情况有关. PFASs在沉积物-水的分配行为表明,PFASs在沉积物-水的分配系数与总有机碳(total organic carbon,TOC)的含量、PFASs碳链长度以及PFASs官能团结构有关. 短链PFASs主要存在于水体中,长链PFASs则主要分布在沉积物中;全氟磺酸类(PFSAs)较全氟羧酸类(PFCAs)更易吸附在沉积物中. 对PFASs来源解析发现:水体中PFASs的来源包括了外源输入和点源排放,夏季河体内PFASs主要受到大气远距离传输影响,冬季则与河道周围的工业活动有关.Abstract: In this study, the spatial and temporal distribution characteristics and distribution behavior of 24 kinds of perfluoroalkyl substances (PFASs) in the water environment of the Taipu River Basin were explored. Water samples and sediments from important points in the Taipu River Basin were collected in winter and summer. Solid-phase extraction, liquid-liquid extraction and high-performance liquid chromatography tandem mass spectrometry (HPLC/MS-MS) were employed to analyzed the target compounds. The results showed that the total mass concentration of PFASs in water ranged from 114.24 ng·L−1 to 168.62 ng·L−1. The dominant pollutants were perfluorobutyric acid (PFBA) and perfluorooctanoic acid (PFOA), with average concentrations of 24.92 ng·L−1 and 28.18 ng·L−1 ; In the sediment, PFASs ranged from 2.36 ng·g−1 (dw) to 4.73 ng·g−1 (dw). The dominant pollutants were perfluorodecanoic acid (PFUdA) and perfluoro dodecanoic acid (PFDoA), with average concentrations of 0.78 ng·g−1 (dw) and 0.52 ng·g−1 (dw). The results of water samples showed that the total concentration of PFASs does not fluctuate much among most points, only a sudden increase occurred at individual points. There was no obvious seasonal difference in PFASs in the Taipu River section, which is related to the low rainfall in this summer. The distribution behavior of PFASs in sediment water showed that the distribution coefficient of PFASs in sediment water is related to the content of total organic carbon (TOC) of the sediment, the carbon chain length of PFASs and the functional group structure of PFASs. Short chain PFASs mainly exists in water, while long chain PFASs mainly in sediments; Compared to perfluorocarboxylic acids (PFCAs), perfluorosulfonic acids (PFSAs) are more easily adsorbed to sediments. The analysis of the source of PFASs shows that the source of PFASs in the water body includes external input and point source discharge. In summer, PFASs in the river is mainly affected by long-distance atmospheric transmission, and in winter, it is related to industrial activities around the river. -
酸雨作为工业过程伴生的环境问题,关乎全球环境. 作为酸雨污染大国,我国近40%面积受酸雨污染,对农业生产危害不容忽视[1-2]. 酸雨作用于叶面,诱发H+与叶片中阳离子竞争结合位点与离子替换,致细胞酸化坏死,酸雨中SO2经气孔对植株产生伤害[3-5]. 细胞内酸性物质累积使线粒体和叶绿体超微结构改变,导致叶绿素功能异常,呼吸及光合作用减弱[6];酸雨胁迫还引发活性氧累积,引起细胞膜脂质过氧化损伤[7],抑制抗氧化酶基因表达及活性[8]. 种子萌发和苗期生理生化指标受酸雨影响巨大[7]. 酸雨导致土壤酸化,使土壤中铝、镉等有害元素析出,抑制根系活性[9-10]、养分吸收、代谢及生长. 土壤酸化进一步造成微生物多样性[10]及活性降低[8],阻滞植物生长发育. 大量研究表明,玉米[11-12]、水稻[13]、小麦[14]其生长发育过程中物质转运吸收效率在pH低于5的条件下会明显受阻,当pH进一步降低到3以下时,多种作物的生理生态过程将出现停滞的现象[12]. 随着全球人口激增,酸雨威胁粮食生产安全. 人们通过农药及化肥增强作物抗性以期产量增加的努力,对环境和人体健康存在隐患. 因此,在当下无法控制酸雨污染、培育抗逆(酸雨)植株的现实条件下,寻找一种低污染、见效快、易推广的化控减灾技术与产品,迫在眉睫.
农业上稀土元素(rare earth elements, REE)镧使用广泛[15-17]. 稀土施用水稻[13]、油菜[12]和黄瓜幼苗[18],其处理组氮、磷、钾等含量远高于对照组,生长更优. 油菜叶绿素含量、硝酸还原酶活性及根系活力、产量增效明显[12]. REE提高糯玉米幼苗PSⅡ最大量子产额和电子传递率,增强光合作用与抗氧化酶活性(减少丙二醛累积)及幼苗抗逆性[19]. 众多实践证明,La3+能提高玉米、苏丹草、紫花苜蓿[20-22]抗盐碱能力,降低玉米和小麦[14, 20]叶片蒸腾速率,增强植株抗逆性. 作为植物成分的氨基酸,既是植物生存的养分,也可凭其络合能力对植物的生理生态形成调节作用[23]. 如氨基酸浸种能缩短水稻与高粱种子萌发时间,提高淀粉酶活性与种子活力[24]. 甘氨酸缩短小油菜生育周期[24],提高烟草叶面积[25]、叶绿素含量及光合作用[25]. 色氨酸增加草莓叶厚(密)度,促进生长发育[26]. 脯氨酸能提高水稻细胞抗氧化酶活性及叶绿素和类胡萝卜素含量,减少丙二醛累积,增加植株抗逆性及生物量[27];氨基丁酸能提高烟草抗氧化酶活性,缓解盐碱对生长发育胁迫[25]. 谷氨酸提高严寒中小白菜叶含水量、鲜重、光合效率及对低温耐受性,甘氨酸增加棉花过氧化物酶等活,控制细胞活性氧水平,增强植株抗逆性[28].
稀土-氨基酸络合物具优良性能、稳定结构、原料获取便捷、合成过程精炼,较单独施用更有优势,其以较高的性价比已成为提高植物抗逆性、用途广泛的产品之一. Zhong等[29]发现,镧螯合氨基酸能缓解铜离子对水稻胁迫;周芸[30]在研究氨基酸稀土微肥时也看到,它能有效提高花生果实干物质累积、果实密度及出仁率,促进增产. 遗憾的是,有关特定稀土螯合氨基酸用于作物化控减灾的研究尚少.
本文采用模拟酸雨(pH3.0)处理玉米(Zea mays L.)、水稻(Oryza sativa L.)、小麦(Triticum aestivum L.)等3种作物的实验设计,运用生理生化等技术手段,初步研究新型氨基酸螯合镧(La(Ⅲ)-AA)对酸雨胁迫下植物质膜透性(MP)、抗氧化系统(过氧化物酶POD、过氧化氢酶CAT、超氧阴离子自由基ROS产生速率、丙二醛MDA含量)、光合作用能力(叶绿素含量)、脯氨酸(PRO)含量及氮代谢(硝酸还原酶NR)等生理指标影响,为酸雨胁迫下作物化控减灾,以及调控产品的选择提供依据.
1. 材料及方法(Materials and methods)
1.1 氨基酸螯合镧(La(Ⅲ)-AA)及其供试溶液的配制
参照ZHONG等人[29]的研究成果,在60 ℃及pH8的条件下以10%碱性蛋白酶水解大豆分离蛋白(SPI) 2 h,随后经100 ℃高温灭活10 min,取上清液在4 ℃、10000 r·min−1下离心10 min. 50 ℃条件将上述制备液与La (NO3)3·6H2O以1.5∶1的体积比反应5 h制得螯合液. 将螯合液置于4 ℃、10000 r·min−1下离心10 min,上清液用丙酮沉淀干燥,最终得到氨基酸螯合镧(La(Ⅲ)-AA)供试品.
经过前人研究可知,植物体生长发育过程中其表面叶绿素含量与逆境情况呈现负相关[31],且在酸雨胁迫过程中植物体内叶绿素含量会出现明显的降低,因此本次研究综合参照Zhong等[29]有关La(Ⅲ)-AA对Cu2+胁迫研究以及前期预实验针对La(Ⅲ)-AA对3种作物的喷施后叶绿素表现结果综合研判,确定20 mg·L−1的施用浓度作为本轮研究的施用浓度.
1.2 模拟酸雨溶液的配制
模拟酸雨配制参考江南地区酸雨降水条件,并参照陈俊彤等[4]有关茼蒿的研究和实验用书方案[32]进行配制,其比例为
SO2−4 NO−3 1.3 供试材料预处理及实验设计
玉米(Zea mays L.)、水稻(Oryza sativa L.)、小麦(Triticum aestivum L.)由相城区种苗繁育基地提供,选取苗种茁壮,高度约为60 cm,5—6叶玉米(Zea mays L.)幼苗、高度约为45 cm,4—5叶水稻(Oryza sativa L.)幼苗和高度约为35 cm,2—3节小麦(Triticum aestivum L.)幼苗的种苗移栽,随后在实验室预栽培5—10 d以适应新的生长实验条件,选取繁育室温度控制在(25±2) ℃[32],以T5型全光谱组培灯作为辐射光源(OPPLE、T5-1058-18 W),光子通量密度设置为2000 μmol·m−2·s−1,光照距离为15 cm,并随幼苗生长而随时调整辐射光源高度[4, 19, 32]. 实验过程中,光暗比为9 h/15 h[32],每3 d进行一次换水,每日早晚各通气1次,实验过程均采用Hoagland培养液水基培养以满足植株幼苗的生长需求[30]. 实验过程中不同组别的设置方式如表1中所示.
表 1 实验组叶片喷施方式Table 1. Spraying method of leaves before experiment时间 Period 对照组 BK Group 酸雨组 AR Group 叶喷组 BS Group 第一天 蒸馏水 蒸馏水 20 mg·L−1 La(Ⅲ)-AA 第二天 蒸馏水 酸雨(pH 3.0) 酸雨(pH 3.0) 为增加喷施溶液在植物叶片表面的沾附能力,在蒸馏水中添加3—5滴聚山梨酯-80,La(Ⅲ)-AA 20 mg·L−1溶液及酸雨处理液中添加1—2滴为宜[4,33],实验周期内植株幼苗均栽种于15穴育苗盘(高度×边长为98 mm×75 mm)中,每穴1株幼苗以便处理.
供试植株经表1方式处理后培养24 h开始计算实验时间,随后在实验时间第1、5、10、15 天对3种供试植株幼苗的组织进行生理指标测定,为减少人为测定误差,每个时间节点每个品种均随机选取3株进行测定,单一样本进行5次测定取平均值作为实验数据.
1.4 生理指标测定种类及方法
质膜透性测定(MP),采用电导率法[34];过氧化物酶(POD)、超氧阴离子自由基产生速率(ROS)以及硝酸还原酶(NR)活性,其测定方法参照植物生理学实验指导(第五版)执行[32];丙二醛(MDA)含量,采用硫代巴比妥酸法测定[3];叶绿素含量,通过SPAD502手持式叶绿素仪直接测定法来表示[35];脯氨酸含量(PRO),采用磺基水杨酸-茚三酮法[35].
1.5 数据采集与分析
研究中数据分析统计均采用SPSS 22.0软件进行,平均值、标准差和相对值,单因素方差分析差异性,采用最小显著性差数法(LSD),即以P<0.05作为差异显著的判断标准,图表采用Origin Pro 2017进行绘制.
2. 结果与讨论(Results and analysis)
2.1 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗质膜透性(MP)的影响
细胞质膜是分隔细胞内外环境屏障,用以维持细胞微环境稳态. 图1显示,随酸雨胁迫时间延长,玉米、水稻、小麦幼苗质膜透性较对照组(BK)增加(小麦15 d除外);预喷施La(Ⅲ)-AA组(BS)的3种作物,质膜透性增幅弱于酸雨组(玉米1 d除外),甚至低于BK组(玉米10 d、15 d,水稻10 d、15 d,小麦组5 d、10 d、15 d);BS组相对于AR组则是呈现降低态势(玉米1 d除外),其差异极值分别出现在10 d(玉米)、10 d(水稻)、10 d(小麦),BS组相对电导率仅为AR组的51.42%、54.22%和45.95%. 其质膜透性结果与姚梦婕等[34]对稀土铈对酸雨胁迫过程中水稻幼苗的防护具有相似的情况,表明质膜是非生物胁迫过程中逆境作用靶位,大量自由基攻击膜脂不饱和脂肪酸双键,细胞质膜氧化分解受损[4],失去离子筛选功能,进而导致大量有害离子和游离基团涌入胞内形成强大破坏力,最终造成加剧细胞膜脂过氧化,对质膜形成更严重破坏,植株生理功能不断恶化[5]. 酸雨胁迫下,质膜透性与相对电导率增加,植物受害加重,抗逆性减弱[36]. 而随着La(Ⅲ)-AA的施加其在植物叶片表面形成保护膜,氨基酸成分在提供营养物质的同时对酸性环境起到了良好的缓冲作用,进而对质膜起到良好保护 [4, 7],从而减少外界H+、SO2等有害物质输入诱发的植株体自由基成分的代谢失衡. La(Ⅲ)-AA所表现出的缓冲作用与冯宗炜[2]早期所提出的提高土壤缓冲能力进而防治酸雨的对策具有异曲同工之妙. 上述结果可知,酸雨胁迫使作物膜损伤、质膜透性增加. La(Ⅲ)-AA可明显增强植株细胞质膜稳定性,降低质膜透性,从而减轻酸雨胁迫对植株造成伤害.
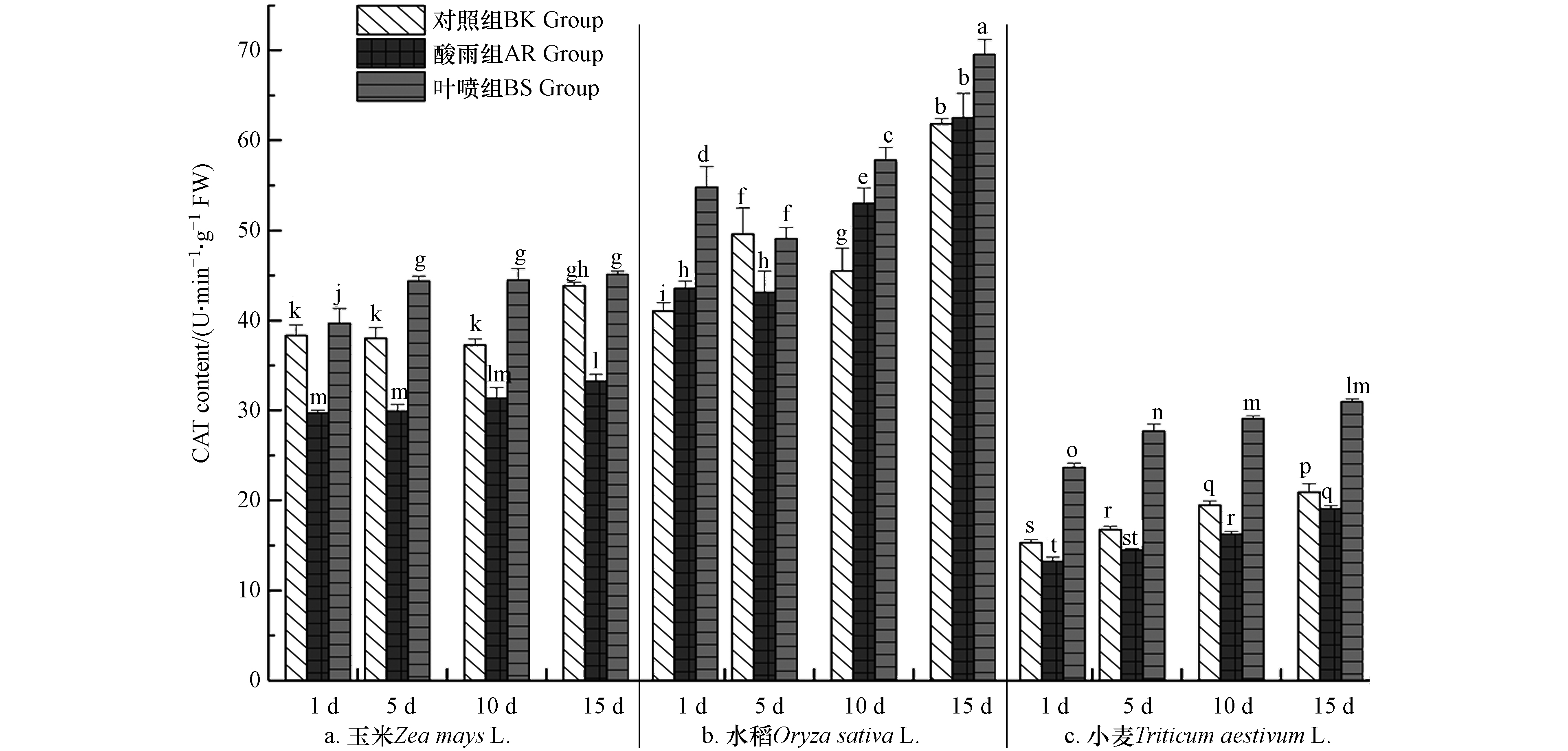
2.2 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗过氧化氢酶(CAT)活性的影响
CAT酶能清除植物体内过氧化氢,防止质膜过氧化损伤,延缓植物衰老. 图2中数据直观的表明,小麦CAT活性相较于玉米和水稻,总体偏低,其酶活最高点也仅为玉米种BK组最低酶活的80.51%;植株体内CAT活性AR组低于BK组(水稻1 d、10 d、15 d除外),表明酸雨对于作物CAT酶活性有着抑制,且随着时间延长,系统的CAT酶活均出现了增长(水稻10 d除外);BS组其CAT活性相较于BK组有较为显著的提升,说明La(Ⅲ)-AA对作物体内CAT酶活有促进作用;而BS组酶活均高于AR组,且在3种作物中的差异极值分别出现在5 d(玉米)、1 d(水稻)、10 d(小麦),La(Ⅲ)-AA使得BS组相较于AR组种CAT活性显著提高了48.68%、29.43%、78.61%,结果表明酸雨使得作物体CAT酶活性受抑. 而La(Ⅲ)-AA 能够很好的消除酸雨对CAT酶的抑制作用,且使得CAT酶活大幅度提高,有效地对植株体内产生的过氧化氢起到应答作用,将植物体内过氧化氢含量维持在较为稳定的水平,更好地为作物生长发育提供保障.
2.3 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗过氧化物酶(POD)活性的影响
POD酶活性及同工酶表达形式与植物生长发育过程相关,其酶活随植株老化不断升高[4]. 图3数据可知,POD酶活在不同作物中呈现出较大差异,其在玉米植株中活性表现最低而在小麦中活性最高;单一植株组内数据比对不难发现,POD活性随着时间的延长总体呈现出下降的趋势,且酸雨胁迫下植株体内POD酶活性显著升高(除小麦1 d);La(Ⅲ)-AA则有效降低了酸雨胁迫下POD酶活,且在1 d(玉米)、10 d(水稻)、15 d(小麦)时使得其与AR组相差最大,分别为AR组的48.3%、57.92%、50.44%,以至于玉米1 d、10 d、15 d,水稻5 d、10 d,小麦5 d、10 d、15 d时,其POD活性低于BK组. 上述结果表明,酸雨胁迫下植株内过氧化物及游离自由基含量逐步增多,加速植株体的老化. 而La(Ⅲ)-AA有效地为植株提供了防护作用,减少其机体内过氧化物产生量,进而表现为POD含量大幅度降低,由此可见其某种程度上不仅能够有效地缓解酸雨胁迫对作物机体的破坏,而且对植物生理发育具有促进作用.
植物体中两大标志性抗氧化酶系统(CAT和POD)的结果变化表明,植物在系统演化过程中,构建出修复逆境伤害的机制[13]. 酸雨胁迫下,作物自身应答机制发挥作用,体内抗氧化物酶协同作用,维持细胞稳态. 此轮研究结果中AR组CAT活性在出现显著低于BK组的现象,其与唐加红等[14]对小麦抗旱的研究有所出入,小麦在干旱胁迫下其体内的三大抗氧化酶系均呈现出明显的增长. 推测造成此次变化的主要原因是由于POD作用于不同底物,在氧化底物同时将氧还原成H2O2,后者被CAT再次分解(CAT活性增长存在一定延迟性),因此本轮研究中CAT酶活随时间延续呈渐增趋势(图2),而POD酶活增幅则明显趋前(图3). 而此种CAT略微延迟的现象在任鹏辉[22]对紫花苜蓿的抗盐胁迫过程中得以呈现. 植株通过CAT及POD酶活变化,不断调节自身机能,从而更好适应酸雨胁迫,为植株生长发育提供保障. 而通过上述BS组与AR组的数据分析结果可以了解到,La(Ⅲ)-AA能够有效缓解酸雨胁迫对抗氧化酶所产生的影响,因此La(Ⅲ)-AA对植物体抗氧化酶系起到了积极的促进作用.
2.4 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗超氧阴离子自由基(ROS)产生速率的影响
逆境条件下,植物产生较多ROS给机体造成不可逆转伤害,抑制植物长发育[22]. 玉米、水稻、小麦作物体内ROS含量如图4所示,由于物种差异ROS产生速率在玉米中远高于水稻和小麦;酸雨胁迫下AR组ROS产生速率相较BK组均有显著的增长;BS组在La(Ⅲ)-AA 作用下ROS速率得以降低,且均低于AR组和BK组(小麦10 d除外),BS组相较于AR组,在10 d(玉米)、1 d(水稻)、15 d(小麦)ROS降低最为明显,分别降低了28.44%、39.47%、42.31%. 以上数据得以证明酸雨对植株体的生长发育产生了较为严重的胁迫作用,其植株体的质膜受损从而加大其体内ROS的不断升高和累积,如不加以控制最终会造成不可逆的伤害,其与金琎等[11]对玉米的酸雨抗性研究具有相同的结果趋势. 而随着La(Ⅲ)-AA的施用其ROS速率得到了较为有效的抑制,其不仅能够缓解酸雨胁迫给植物体所带来的危害,而且能够对植株体生长发育环境形成优良的缓冲,减少植物所受到的环境胁迫影响.
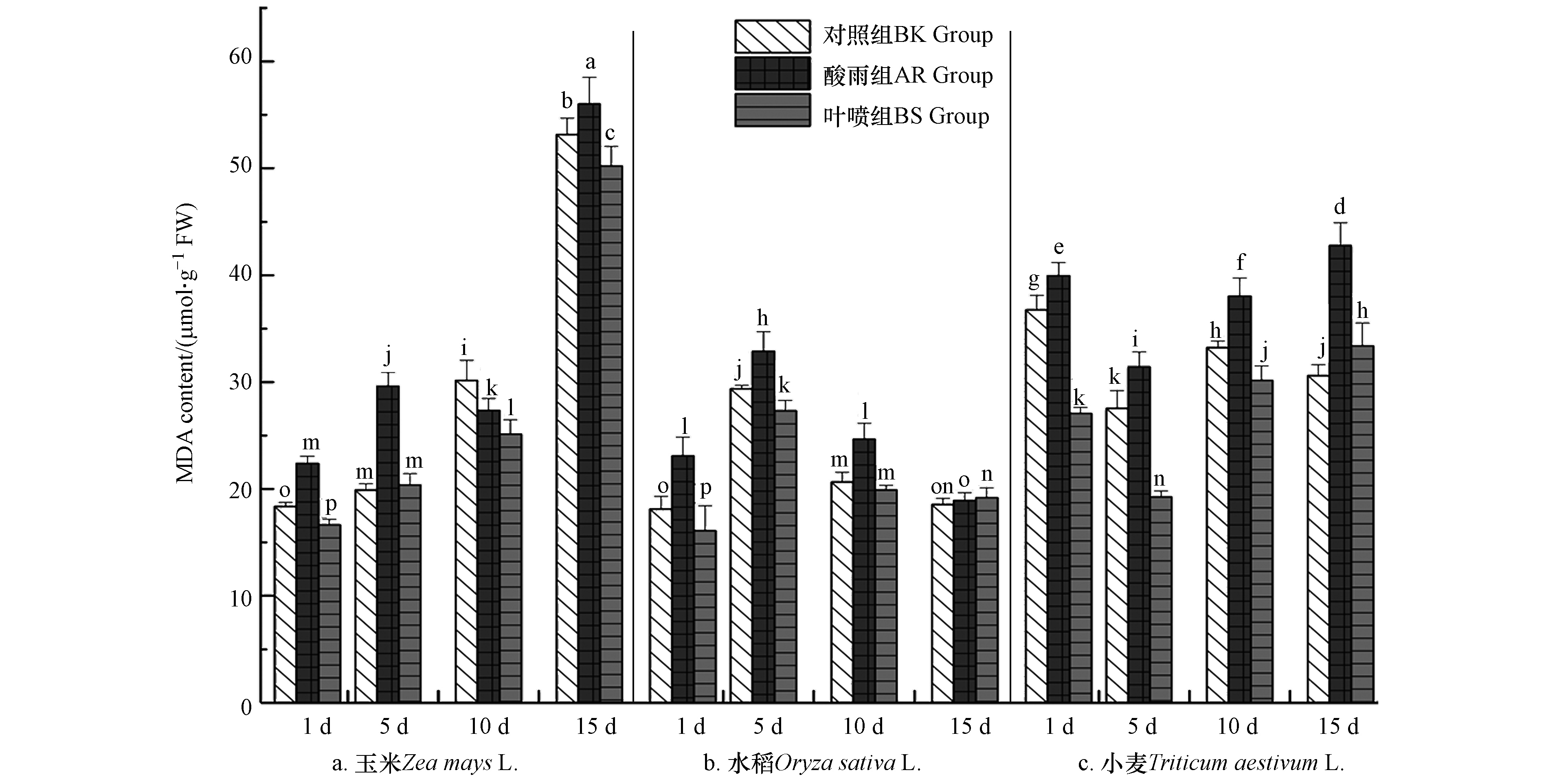
2.5 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗中丙二醛(MDA)含量的影响
植株体过氧化最直接的产物便是MDA,其能够有效地反映植株体当前的健康水平[4]. 图5中数据可以清晰的观察到,玉米和小麦作物中MDA的水平随着培育时间的延长总体呈现上升的趋势,而水稻种的MDA则在5 d达到最高,随后逐步回落;随着酸雨对作物胁迫时间的逐步延长,玉米和小麦中的MDA均出现持续的累积,这两种作物MDA的最高值均出现在15 d的AR组,而水稻作物中的MDA在5 d后呈现稳步回落,直至15 d其组内3种处理方式作物中MDA含量接近,AR组及BS组回归到正常水平;除水稻15 d外,BS组中MDA的含量相较于AR组均有着显著的降低,其降低的峰值在5 d(玉米)、1 d(水稻)和5 d(小麦),分别降低了31.03%、34.78%、38.71%. 其结果与巩东辉等[16]对螺旋藻的生理生态指标研究具有一定的相似性. 在外界环境胁迫下细胞质膜失去了其原本的防护作用, ROS的大量增加加剧其胞内物质的过氧化,其过氧化产物MDA便呈现出增长趋势,进而其反作用于细胞质膜,亦是对其形成更严重破坏,植株生理功能不断恶化[5]. 由此可见,酸雨会加速MDA在植株体内的累积进而对植株体产生破坏作用. 而La(Ⅲ)-AA对酸雨胁迫下植物中MDA的产生具有缓解作用,能够较为有效的减少植物机体损伤.
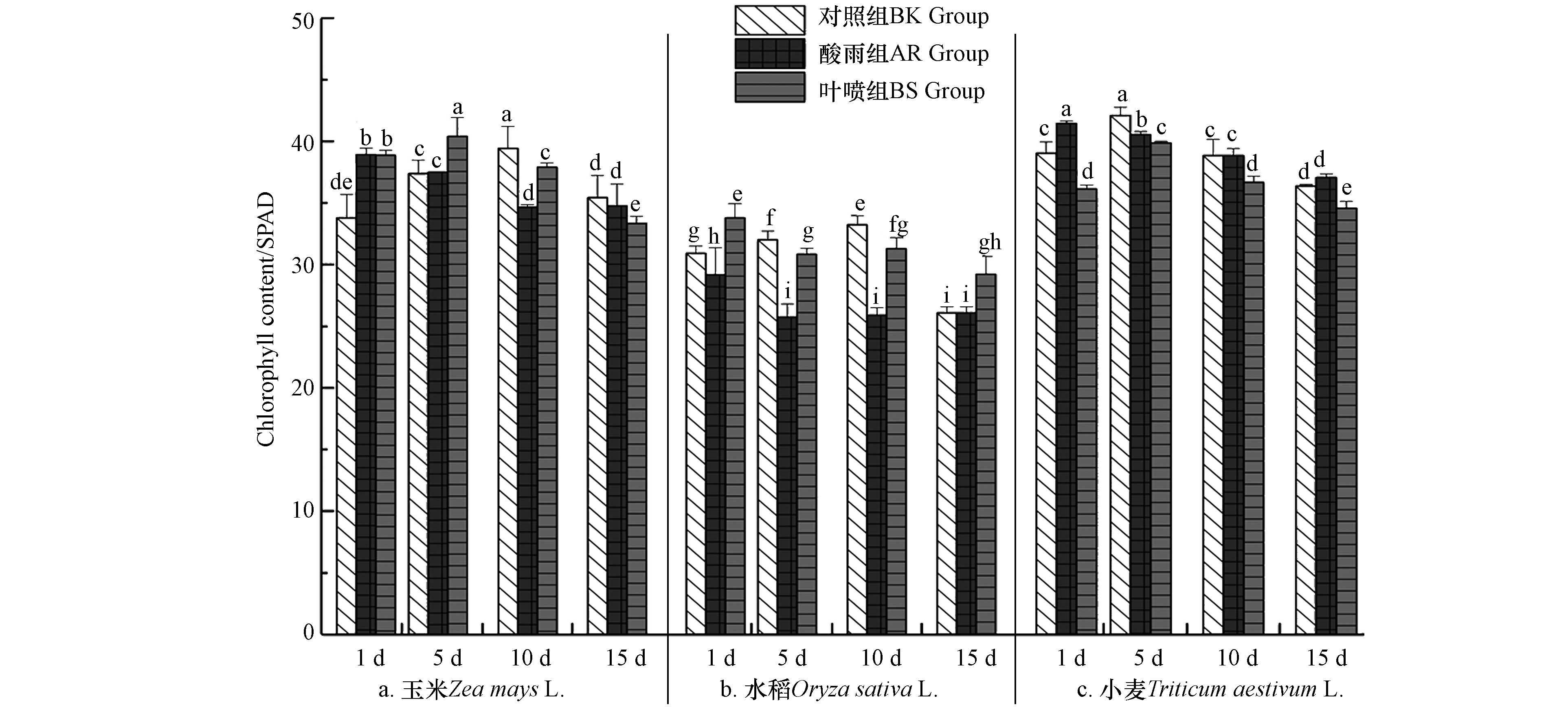
2.6 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗中叶绿素含量的影响
叶绿素是植物体光合作用及碳代谢的关键节点,其存在对植物体生长发育起到决定性作用. 图6可以了解到,叶绿素在3种作物叶片中的含量随着培育时间的延长总体呈现先扬后抑的趋势,BK组叶绿素最高点分别出现在10 d(玉米)、10 d(水稻)、5 d(小麦);酸雨的环境胁迫情况总体在水稻种体现的更为明显,其AR组的叶绿素含量均显著低于BK组,而在玉米和小麦体内则出现了分化,玉米组1 d时AR组叶绿素含量高于BK组14.71%,与此同时小麦组1 d和15 d中亦是出现AR组高于BK组的情况;而BS组中水稻和玉米作物的叶绿素含量相较AR组均有一定幅度的增长,水稻中为18.76%(10 d),玉米中为4.21%(10 d),而小麦作物中La(Ⅲ)-AA对其叶绿素含量反而会有降低的影响. 造成小麦作物中La(Ⅲ)-AA表现不佳的因素与李月福等[12]研究中油菜幼苗的应激过程具有一定的相似性,La(Ⅲ)的对植株叶绿素的改观效果与植株本体所受到的胁迫程度具有一定的相关性,其在不同胁迫状况下La(Ⅲ)的左右效果往往具有一定差异,此时适当调整降低La(Ⅲ)浓度便可获得较优的效果. 而酸雨胁迫过程中叶片细胞叶绿体结构受害,色素合成途径受阻,叶绿素合成量减少并伴随叶绿素降解[22],随胁迫时间延长,叶绿素含量渐降(图6)并因此影响植株体生理活性. 而La(Ⅲ)-AA能够在叶表面进入叶细胞后,供植物生长所需微量元素和必需氨基酸,从而缓解酸雨污染对细胞微环境扰动. 或将叶绿素中心的Mg取代,进而形成夹心螯合物,在提高叶绿素稳定性同时,也使其捕获波长较短能量较高光子的能力大幅提高,有助于光合效率提升[33],增强其对CO2催化能力,提高机体内糖类物质累积. 综合数据表明,不同植株体对酸雨和La(Ⅲ)-AA的作用不尽相同,但总体来说La(Ⅲ)-AA能够有效缓解酸雨所带来的影响.
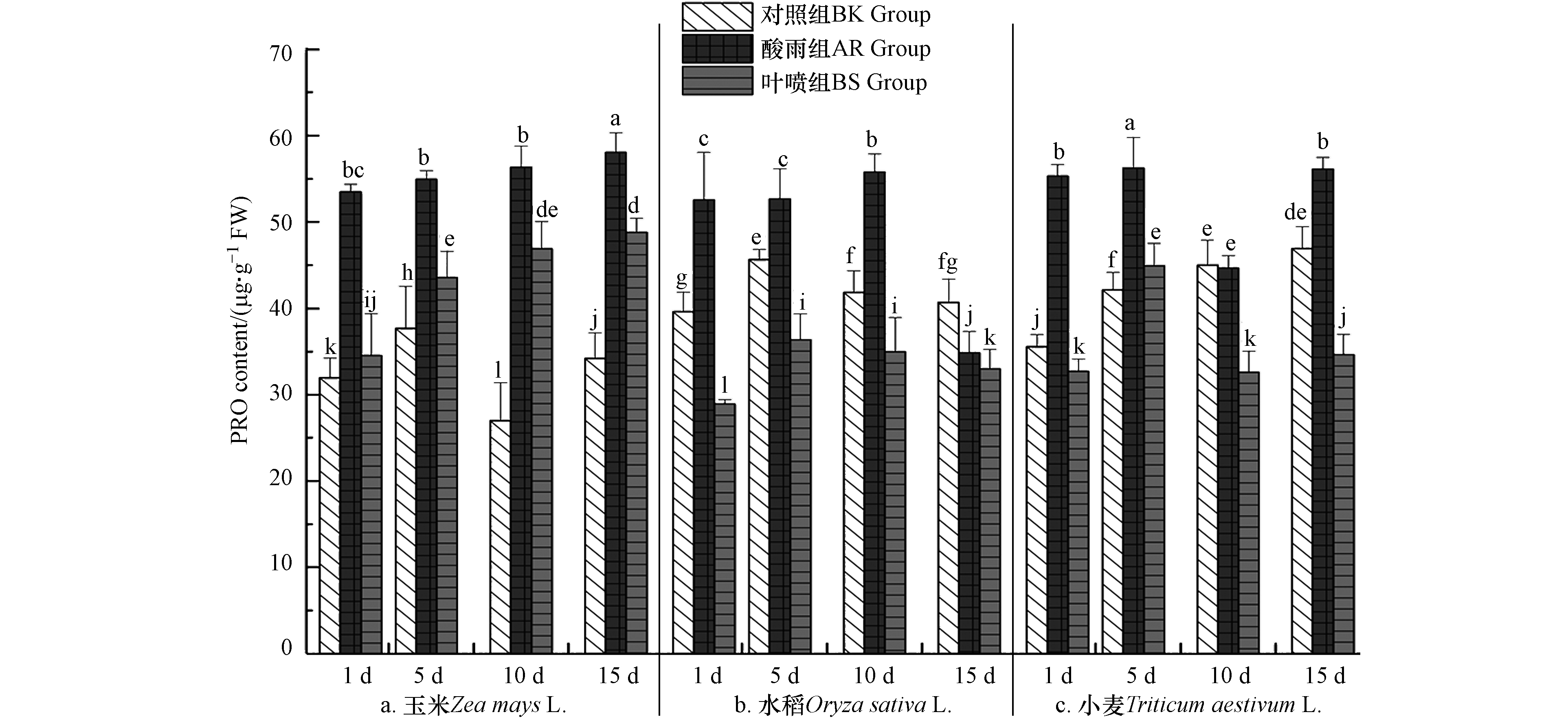
2.7 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗中脯氨酸(PRO)含量的影响
游离态PRO在构成植物蛋白的同时在维持渗透压、稳定分子结构、调节细胞氧化过程方面亦是具有重要作用[4]. PRO的改变情况如图7中所示,PRO在不同植物体中的含量总体趋于平稳,3组作物中BK组中PRO均在40 μg·g−1FW上下浮动;酸雨胁迫使得植物体做出对应的应答反应,3种作物中AR组的PRO含量均出现了显著的提高;而BS组中PRO含量相较于AR组均大幅度降低,3种作物中均在1 d出现最大的减少幅度,分别为36.23%(玉米)、47.17%(水稻)、41.82%(小麦),且在玉米和水稻中多次出现BS组低于BK组的现象. PRO并不是独立存在的个体,其在植株体受到外界环境胁迫的过程中会进行大量的累积[5],体内PRO与抗氧化物酶协同作用,维持细胞稳态. 即当亲水性强的PRO含量升高、游离态PRO广泛存在时,为稳定细胞内大分子蛋白,降低功能蛋白酸解及渗透压调节和平衡等代谢过程[7]提供保障[12]. 上述结果表明,酸雨对植株体生理生化产生了严重的干扰和破坏,PRO在植物体内大量的积累以稳定植物体细胞所带来的渗透压从而为植株更好的生长提供必要条件. 而La(Ⅲ)-AA为作物在酸雨胁迫下提供了优良的缓冲作用,使得酸雨危害大大的减少,为植物体抗逆性提供坚实的保障.
2.8 La(Ⅲ)-AA 对酸雨胁迫下植株幼苗氮代谢的影响
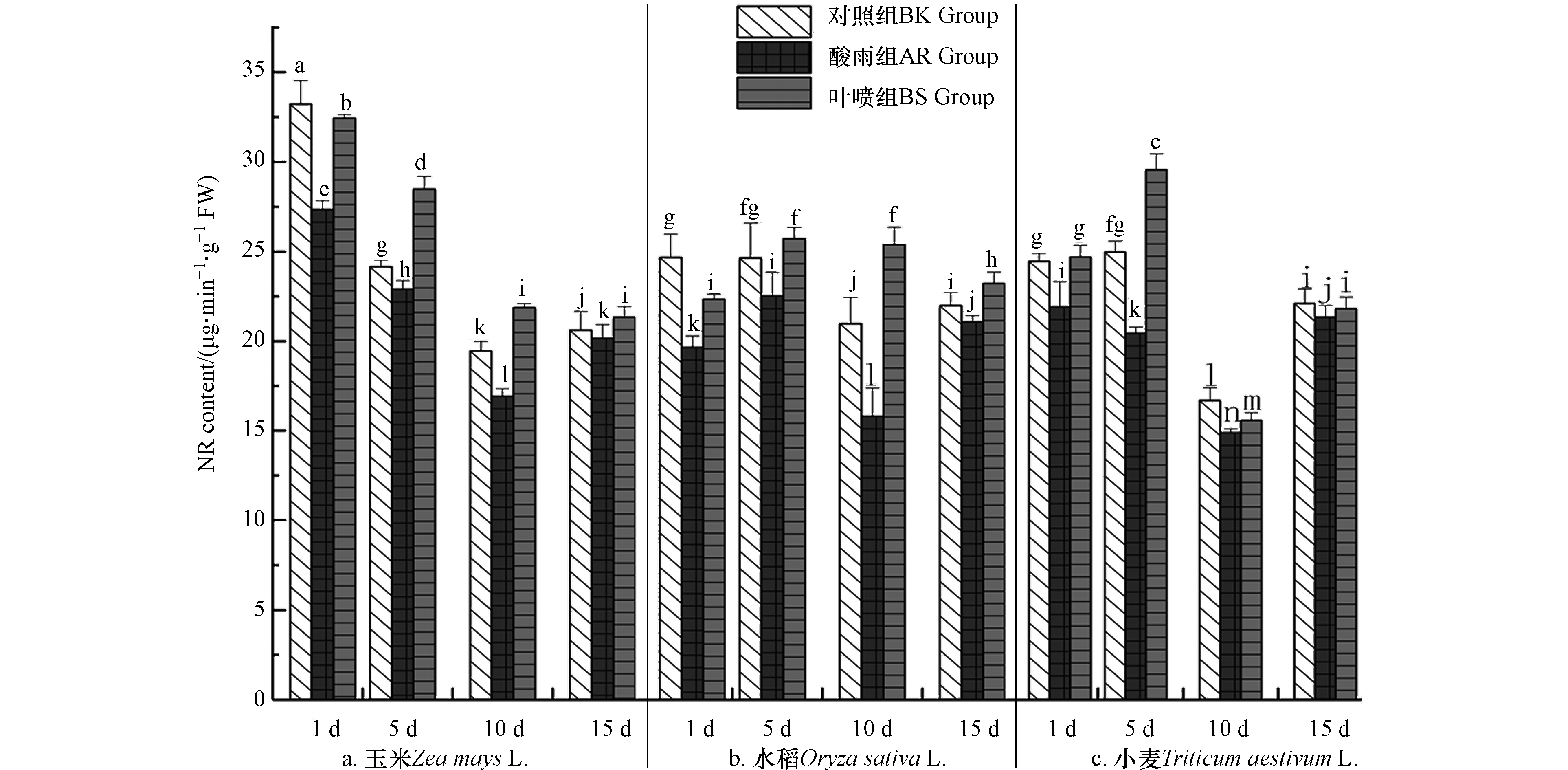
硝酸还原酶(NR)是N元素有效利用的关键酶,其能够较直观地反映出植物体N代谢的强度[32]. NR活性如图7中所示,总体看来3种作物中NR活性呈现出先抑后扬的趋势,BK组均在10 d出现最低值,随后升高;AR组中NR活性均出现了不同程度降低;BS组NR活性具有大幅度提高,玉米(5 d、10 d、15 d)、水稻(5 d、10 d、15 d)、小麦(1 d、5 d)多次高于BK组,相较于AR组,在5 d(玉米)、10 d(水稻)、5 d(小麦)NR增幅最为显著,分别增长了21.37%、60.63%、46.50%,与AR组形成鲜明的对比. 酸雨胁迫下对叶绿素的影响逐渐传递并表现为到氮代谢过程的干扰,叶绿素含量渐降(图6)并因此影响NR酶活. 这是因为,NR酶是以细胞色素作为电子供体[35],色素合成受阻引起NR酶催化反应减弱(图8),细胞内NO3-还原成NO2-速率降低,降低植物氮代谢水平. 且亚硝酸盐转化NO是多种代谢途径的信号物质,如根系生长、营养物质吸收及有机酸代谢[18]. 植物氮代谢水平降低,影响其生长发育,降低抗逆性,最终表现为酸雨对3种作物伤害.
而La(Ⅲ)-AA 施用后可以使得ROS进一步减少,与此同时保持了细胞微环境稳态,其最直接的结果便是,细胞叶绿体微结构、叶绿素含量与细胞色素电子传递链功能趋于正常,以满足NR酶促反应对光电子需求[30],确保NR酶活与细胞内NO3-还原成NO2-速率,维持植物氮代谢水平,以及信号物质NO参与的多种代谢途径调控[33]. 植物氮代谢正常对其生长发育、抗逆性不无裨益,并最终促进植物更好生长发育,产量提高.
上述数据不难看出,酸雨对于植物体氮代谢具有较大的抑制作用,不利于植物生长. 而La(Ⅲ)-AA能够显著提升NR活性,增强植株体对酸雨胁迫的抗性,且其在一定程度上能够促进作物本身的氮代谢强度,提高物质积累,进而对作物生长发育过程形成增益.
实验中还观察到,3种作物各项生理生化指标对酸雨胁迫强度、时长存在差异反应(图1—8),根据已有报道推测,或与3种作物对酸雨胁迫的敏感性有关. 如在耐酸性的生态适应上,水稻耐酸性强于小麦、玉米[37-38]. 当然,更准确的答案也许要在酸雨胁迫下,植物逆境基因确认与响应上寻求.
3. 结论(Conclusion)
(1)酸雨胁迫对3中经济作物造成显著损伤,作物体内MP、ROS产生速率、MDA含量、PRO含量、POD活性均显著升高. 与此同时,叶绿素含量、CAT活性、NR活性则显著降低;
(2)预施La(Ⅲ)-AA溶液,可有效缓解酸雨对作物产生的胁迫伤害,MP、ROS产生速率、MDA含量、PRO含量降低,CAT和NR活性提高,POD活性趋于稳定;
(3)预施La(Ⅲ)-AA产生防护效果,为化控酸雨损害作物的研究提供新的可行性.
-
表 1 实验所用标准品
Table 1. Standards used in the experiment
分类Classification 化合物Compounds 缩写Abbreviation 内部标准品Internal standards 碳链长度Carbon chain length 全 氟 羧 酸 类(PFCAs) 全氟丁酸 PFBA MPFBA 4 全氟戊酸 PFPeA M5PFPeA 5 全氟己酸 PFHxA M5PFHxA 6 全氟庚酸 PFHpA M4PFHpA 7 全氟辛酸 PFOA M8PFOA 8 全氟壬酸 PFNA M9PFNA 9 全氟癸酸 PFDA M6PFDA 10 全氟十一酸 PFUdA M7PFUdA 11 全氟十二酸 PFDoA MPFDoA 12 全氟及多氟聚醚羧酸类(PFECAs) 六氟环氧丙烷二聚酸 HFPO-DA M5PFHxA 5 全氟-4-恶戊二酸 PF4OPeA M8PFOA 4 全氟-5-氧代己酸 PF5OHxA M5PFHxA 5 全氟-3,6-二噁庚酸 3,6-OPFHpA M5PFHxA 5 4,8-二氧-3H-全氟辛酸钠 NaDONA M8PFOA 7 全氟磺酸类(PFSAs) 全氟丁烷磺酸盐 L-PFBS M3PFBS 4 全氟-1-戊烷磺酸钠 L-PFPeS M8PFOS 5 全氟己烷磺酸钾 PFHxSK M3PFHxS 6 全氟-1-庚烷磺酸钾 L-PFHpS M8PFOA 7 全氟辛烷磺酸钾 PFOSK M8PFOS 8 氟调聚醇类(PFOH) 氟调聚物磺酸盐 4:2 4:2FTS M8PFOS 6 氟调聚物磺酸盐 6:2 6:2FTS M8PFOS 8 氟调聚物磺酸盐 8:2 8:2FTS M8PFOS 10 全氟及多氟聚醚磺酸类(PFESAs) 9-氯十六氟-3-氧杂环己酮-1-磺酸钾 9Cl-PF3ONS M9PFNA 8 全氟烷基醚磺酸盐 PFEESA M6PFDA 4 表 2 太浦河1、7月份采样情况
Table 2. Sampling of Taipu River in January and July
采样时间Sampling time 水样Water sample 沉积物Sediment 1月January TPH1、TPH4—TPH10 — 7月July TPH1—TPH11 TPH1—TPH3、TPH8—TPH10 -
[1] GIESY J P, KANNAN K. Global distribution of perfluorooctane sulfonate in wildlife [J]. Environmental Science & Technology, 2001, 35(7): 1339-1342. [2] 张美, 楼巧婷, 邵倩文, 等. 全氟化合物污染现状及风险评估的研究进展 [J]. 生态毒理学报, 2019, 14(3): 30-53. ZHANG M, LOU Q T, SHAO Q W, et al. Research progress of perfluorinated compounds pollution status and risk assessment [J]. Asian Journal of Ecotoxicology, 2019, 14(3): 30-53(in Chinese).
[3] AHRENS L. Polyfluoroalkyl compounds in the aquatic environment: A review of their occurrence and fate [J]. Journal of Environmental Monitoring, 2011, 13(1): 20-31. doi: 10.1039/C0EM00373E [4] DREYER A, WEINBERG I, TEMME C, et al. Polyfluorinated compounds in the atmosphere of the Atlantic and Southern Oceans: Evidence for a global distribution [J]. Environmental Science & Technology, 2009, 43(17): 6507-6514. [5] KIM E J, PARK Y M, PARK J E, et al. Distributions of new stockholm convention POPs in soils across South Korea [J]. Science of the Total Environment, 2014, 476/477: 327-335. doi: 10.1016/j.scitotenv.2014.01.034 [6] LI F S. Perfluorinated compounds in Haihe River and Dagu drainage canal in Tianjin, China [J]. Chemosphere, 2011, 84(2): 265-271. doi: 10.1016/j.chemosphere.2011.03.060 [7] 赵永辉, 王以燕, 李富根. 欧盟高度关注物质名单 [J]. 世界农药, 2014, 36(5): 37-42. doi: 10.3969/j.issn.1009-6485.2014.05.009 ZHAO Y H, WANG Y Y, LI F G. Candidate list of substances of very high concern for authorization in EU [J]. World Pesticides, 2014, 36(5): 37-42(in Chinese). doi: 10.3969/j.issn.1009-6485.2014.05.009
[8] WANG T, WANG Y W, LIAO C Y, et al. Perspectives on the inclusion of perfluorooctane sulfonate into the Stockholm convention on persistent organic pollutants [J]. Environmental Science & Technology, 2009, 43(14): 5171-5175. [9] RITTER S K. Fluorochemicals go short [J]. Chemical & Engineering News Archive, 2010, 88(5): 12-17. [10] SUN M, AREVALO E, STRYNAR M, et al. Legacy and emerging perfluoroalkyl substances are important drinking water contaminants in the Cape Fear River watershed of North Carolina [J]. Environmental Science & Technology Letters, 2016, 3(12): 415-419. [11] ELLIS D A, MARTIN J W, SILVA A O, et al. Degradation of fluorotelomer alcohols: A likely atmospheric source of perfluorinated carboxylic acids [J]. Environmental Science & Technology, 2004, 38(12): 3316-3321. [12] ARMITAGE J, COUSINS I T, BUCK R C, et al. Modeling global-scale fate and transport of perfluorooctanoate emitted from direct sources [J]. Environmental Science & Technology, 2006, 40(22): 6969-6975. [13] PREVEDOUROS K, COUSINS I T, BUCK R C, et al. Sources, fate and transport of perfluorocarboxylates [J]. Environmental Science & Technology, 2006, 40: 32-44. [14] 程铭, 张波, 何义亮, 等. 太浦河金泽水源地抗生素抗性基因赋存特征 [J]. 环境化学, 2019, 38(11): 2405-2414. doi: 10.1002/etc.4546 CHENG M, ZHANG B, HE Y L, et al. Occurrence and distribution of antibiotic resistance genes in Jinze Reservoir and surrounding area of Taipu River [J]. Environmental Chemistry, 2019, 38(11): 2405-2414(in Chinese). doi: 10.1002/etc.4546
[15] 孙晓宇, 杨雾晨, 唐晓迪, 等. 太浦河流域锑污染环境风险评估 [J]. 环境保护科学, 2017, 43(3): 120-124. doi: 10.16803/j.cnki.issn.1004-6216.2017.03.022 SUN X Y, YANG W C, TANG X D, et al. Environmental risk assessment of antimony pollution in Taipu River Basin [J]. Environmental Protection Science, 2017, 43(3): 120-124(in Chinese). doi: 10.16803/j.cnki.issn.1004-6216.2017.03.022
[16] HIGGINS C P, LUTHY R G. Sorption of perfluorinated surfactants on sediments [J]. Environmental Science & Technology, 2006, 40(23): 7251-7256. [17] 赵振国. 吸附作用应用原理 [J]. 热能动力工程, 2005, 20(6): 631. ZHAO Z G. Application principle of adsorption [J]. Journal of Engineering for Thermal Energy and Power, 2005, 20(6): 631(in Chinese).
[18] ZHAO L X, ZHU L Y, YANG L P, et al. Distribution and desorption of perfluorinated compounds in fractionated sediments [J]. Chemosphere, 2012, 88(11): 1390-1397. doi: 10.1016/j.chemosphere.2012.05.062 [19] YOU C, JIA C X, PAN G. Effect of salinity and sediment characteristics on the sorption and desorption of perfluorooctane sulfonate at sediment-water interface [J]. Environmental Pollution, 2010, 158(5): 1343-1347. doi: 10.1016/j.envpol.2010.01.009 [20] ZHANG Y, MENG W, GUO C S, et al. Determination and partitioning behavior of perfluoroalkyl carboxylic acids and perfluorooctanesulfonate in water and sediment from Dianchi Lake, China [J]. Chemosphere, 2012, 88(11): 1292-1299. doi: 10.1016/j.chemosphere.2012.03.103 [21] 刘晓雷, 刘婕, 郭睿, 等. 超高效液相色谱-串联质谱法测定表层水中全氟及多氟化合物 [J]. 分析化学, 2018, 46(9): 1400-1407. doi: 10.11895/j.issn.0253-3820.171373 LIU X L, LIU J, GUO R, et al. Ultra performance liquid chromatography-tandem mass spectrometry for determination of per-and polyfluorinated compounds in surface water [J]. Chinese Journal of Analytical Chemistry, 2018, 46(9): 1400-1407(in Chinese). doi: 10.11895/j.issn.0253-3820.171373
[22] SHI Y L, PAN Y Y, WANG J M, et al. Distribution of perfluorinated compounds in water, sediment, biota and floating plants in Baiyangdian Lake, China [J]. Journal of Environmental Monitoring:JEM, 2012, 14(2): 636-642. doi: 10.1039/C1EM10772K [23] AHRENS L, TANIYASU S, YEUNG L W Y, et al. Distribution of polyfluoroalkyl compounds in water, suspended particulate matter and sediment from Tokyo Bay, Japan [J]. Chemosphere, 2010, 79(3): 266-272. doi: 10.1016/j.chemosphere.2010.01.045 [24] 金磊. 黄浦江上游太浦河水源水体中全氟化合物赋存特征及风险评价 [J]. 净水技术, 2021, 40(1): 54-59. doi: 10.15890/j.cnki.jsjs.2021.01.010 JIN L. Risk assessment and occurrence characteristics of PFCs in water body of Taipu water source in upstream of Huangpu River [J]. Water Purification Technology, 2021, 40(1): 54-59(in Chinese). doi: 10.15890/j.cnki.jsjs.2021.01.010
[25] ZHAO L J, ZHOU M, ZHANG T, et al. Polyfluorinated and perfluorinated chemicals in precipitation and runoff from cities across eastern and central China [J]. Archives of Environmental Contamination and Toxicology, 2013, 64(2): 198-207. doi: 10.1007/s00244-012-9832-x [26] LIU W, JIN Y H, QUAN X, et al. Perfluorosulfonates and perfluorocarboxylates in snow and rain in Dalian, China [J]. Environment International, 2009, 35(4): 737-742. doi: 10.1016/j.envint.2009.01.016 [27] TANIYASU S, YAMASHITA N, MOON H B, et al. Does wet precipitation represent local and regional atmospheric transportation by perfluorinated alkyl substances? [J]. Environment International, 2013, 55: 25-32. doi: 10.1016/j.envint.2013.02.005 [28] PAN G, ZHOU Q, LUAN X, et al. Distribution of perfluorinated compounds in Lake Taihu (China): Impact to human health and water standards [J]. Science of the Total Environment, 2014, 487: 778-784. doi: 10.1016/j.scitotenv.2013.11.100 [29] PAUL A G, JONES K C, SWEETMAN A J. A first global production, emission, and environmental inventory for perfluorooctane sulfonate [J]. Environmental Science & Technology, 2009, 43(2): 386-392. [30] CHAPMAN P M, POWER E A, DEXTER R N, et al. Evaluation of effects associated with an oil platform, using the sediment quality triad [J]. Environmental Toxicology and Chemistry, 1991, 10(3): 407-424. doi: 10.1002/etc.5620100313 [31] KISSA E. Fluorinated surfactants: Synthesis, properties, applications[M]. M. Dekker, 1994. [32] 张兴桃, 王海潮, 徐礼生, 等. 全氟己烷磺酸暴露影响小鼠肠道菌群组成的初步研究 [J]. 宿州学院学报, 2019, 34(12): 77-80. ZHANG X T, WANG H C, XU L S, et al. A primary study on the changes of intestinal flora in mice exposed to perfluorohexane sulfonic acid [J]. Journal of Suzhou University, 2019, 34(12): 77-80(in Chinese).
[33] PAN C G, YU K F, WANG Y H, et al. Perfluoroalkyl substances in the riverine and coastal water of the Beibu Gulf, South China: Spatiotemporal distribution and source identification [J]. Science of the Total Environment, 2019, 660: 297-305. doi: 10.1016/j.scitotenv.2019.01.019 [34] UNEP. Listing of perfluorooctane sulfonic acid (PFOS), its salts and perfluorooctane sulfonyl fluoride (PFOSF) in Annex B of the Stockholm Convention on Persistent Organic Pollutants[S]. Unep/Pops/Cop. 4/17: 15-18. [35] WANG S Q, MA L Y, CHEN C, et al. Occurrence and partitioning behavior of per- and polyfluoroalkyl substances (PFASs) in water and sediment from the Jiulong Estuary-Xiamen Bay, China [J]. Chemosphere, 2020, 238: 124578. doi: 10.1016/j.chemosphere.2019.124578 [36] LEE Y M, LEE J Y, KIM M K, et al. Concentration and distribution of per- and polyfluoroalkyl substances (PFAS) in the Asan Lake area of South Korea [J]. Journal of Hazardous Materials, 2020, 381: 120909. doi: 10.1016/j.jhazmat.2019.120909 [37] OLSEN G W, CHURCH T R, MILLER J P, et al. Perfluorooctanesulfonate and other fluorochemicals in the serum of American Red Cross adult blood donors [J]. Environmental Health Perspectives, 2003, 111(16): 1892-1901. doi: 10.1289/ehp.6316 [38] LAU C, ANITOLE K, HODES C, et al. Perfluoroalkyl acids: A review of monitoring and toxicological findings [J]. Toxicological Sciences, 2007, 99(2): 366-394. doi: 10.1093/toxsci/kfm128 [39] AHRENS L, YEUNG L W Y, TANIYASU S, et al. Partitioning of perfluorooctanoate (PFOA), perfluorooctane sulfonate (PFOS) and perfluorooctane sulfonamide (PFOSA) between water and sediment [J]. Chemosphere, 2011, 85(5): 731-737. doi: 10.1016/j.chemosphere.2011.06.046 [40] 戴树桂. 环境化学[M]. 2版. 北京: 高等教育出版社, 2006. DAI S G. Environmental Chemistry[M]. 2nd ed. Beijing: Higher Education Press, 2006(in Chinese).
[41] 杨洪法, 史斌, 周云桥, 等. 中、韩滨海城市化区域水体全氟化合物的空间特征及生态风险 [J]. 环境科学, 2020, 41(4): 1607-1618. doi: 10.13227/j.hjkx.201910153 YANG H F, SHI B, ZHOU Y Q, et al. Spatial characteristics and ecological risks of perfluoroalkyl substances in coastal urbanized areas of China and South Korea [J]. Environmental Science, 2020, 41(4): 1607-1618(in Chinese). doi: 10.13227/j.hjkx.201910153
[42] WANG P, LU Y L, WANG T Y, et al. Transport of short-chain perfluoroalkyl acids from concentrated fluoropolymer facilities to the Daling River estuary, China [J]. Environmental Science and Pollution Research, 2015, 22(13): 9626-9636. doi: 10.1007/s11356-015-4090-x [43] GAO Y, FU J J, ZENG L X, et al, Occurrence and fate of perfluoroalkyl substances in marine sediments from the Chinese Bohai Sea, Yellow Sea, and East China Sea[J]. Environmental Pollution, 2014, 194: 60-68. [44] 肖少可. 传统和替代全氟化合物在北部湾的空间分布、生物富集及营养级迁移[D]. 南宁: 广西大学, 2021. XIAO S K. Spatial distribution, bioaccumulation and trophic transfer of legacy and alternative per-and polyfluoroalkyl substances in the Beibu Gulf[D]. Nanning: Guangxi University, 2021(in Chinese).
[45] 孟晶, 王铁宇, 王佩, 等. 淮河流域土壤中全氟化合物的空间分布及组成特征 [J]. 环境科学, 2013, 34(8): 3188-3194. doi: 10.13227/j.hjkx.2013.08.027 MENG J, WANG T Y, WANG P, et al. Spatial distribution and composition of perfluorinated compounds in soils around the Huaihe River [J]. Environmental Science, 2013, 34(8): 3188-3194(in Chinese). doi: 10.13227/j.hjkx.2013.08.027
[46] YANG Q Q, WANG S L, LIU W J, et al. Spatial distribution of perfluoroalkyl acids (PFAAs) and their precursors and conversion of precursors in seawater deeply affected by a city in China [J]. Ecotoxicology and Environmental Safety, 2020, 194: 110404. doi: 10.1016/j.ecoenv.2020.110404 [47] GUO C S, ZHANG Y, ZHAO X, et al. Distribution, source characterization and inventory of perfluoroalkyl substances in Taihu Lake, China [J]. Chemosphere, 2015, 127: 201-207. doi: 10.1016/j.chemosphere.2015.01.053 [48] PAN C G, YING G G, LIU Y S, et al. Contamination profiles of perfluoroalkyl substances in five typical rivers of the Pearl River Delta region, South China [J]. Chemosphere, 2014, 114: 16-25. doi: 10.1016/j.chemosphere.2014.04.005 [49] 王之芬, 梁新秀, 占笔成, 等. 快速城市化流域全氟化合物的污染特征及生态风险 [J]. 北京大学学报(自然科学版), 2019, 55(3): 543-552. doi: 10.13209/j.0479-8023.2019.029 WANG Z F, LIANG X X, ZHAN B C, et al. Pollution characteristics and ecological risk of perfluorinated compounds in a rapidly urbanizing catchment [J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2019, 55(3): 543-552(in Chinese). doi: 10.13209/j.0479-8023.2019.029
-









 DownLoad:
DownLoad: