-
多环芳烃(polycyclic aromatic hydrocarbons,PAHs)具有来源广、排放量大,且存在潜在致癌风险等特征,因此成为国内外广泛关注的有机污染物. 中国卫生统计数据表明,30年来,大气中PAHs污染增长迅速,同期中国肺癌的发生率也呈倍数增长[1]. 研究表明,中国室外PAHs污染造成的肺癌风险增量为1.6%,在极端高风险地区肺癌风险增量高达44%[2].
流行病学研究表明,呼吸暴露PAHs导致的人群肺癌风险与大气PAHs浓度水平密切相关[3]. 通常而言,大气环境中PAHs浓度水平显著低于职业暴露环境下的浓度水平,以往研究中基于高浓度建立的剂量-效应关系不适用于大气环境暴露的健康风险评估,因此应建立大气PAHs致癌风险与暴露量的定量关系. 当前研究中评估PAHs长期呼吸暴露的肺癌风险的常见方法为基于超额终生致癌风险(Incremental Lifetime Cancer Risk, ILCR)的概率风险模型. 然而风险评估结果存在较大不确定性,尽管相关参数取值的选择是基于大量调查分析,并选取致癌因子的95%置信区间上限来取值. 有研究进一步引入了人群归因模型(population Attributable Fraction, PAF)来对风险评估结果进行对比,以降低模型的不确定性. 如Hong等[4]采用该方法评估了亚洲典型国家(中国、日本、韩国等)的癌症风险水平,同时对比了采用ILCR和PAF两种模型估算的健康风险水平,并表明两者的评估结果呈现良好的线性关系. 此外,大气PAHs的致癌风险与排放源密切相关[5]. 主要排放源在区域的空间异质性分布极大的影响了PAHs的致癌风险分布,给区域尺度下人群的健康管理带来不确定性,尤其是快速城市化区域多污染排放源和人口分布的高度异质性导致城市尺度致癌风险分布空间差异加大. 目前已有研究探讨了大尺度PAHs的风险分布差异[2, 6-8]. 然而对于城市不同区域风险分布差异[9-10]的归因还需要进一步探讨,尤其是不同人群间的风险差异.
本研究以安徽省省会合肥市为案例开展大气PAHs浓度监测与呼吸暴露肺癌风险评价. 安徽近年来经历了快速的城市化过程,省会合肥市的人口和经济的快速增长导致典型的复合源排放特征[11]. 因此,针对该城市区域PAHs暴露肺癌风险分布差异,获取不同模型应用于城市尺度肺癌风险评估的不确定性,为城市尺度下健康风险综合管控提供科学依据.
-
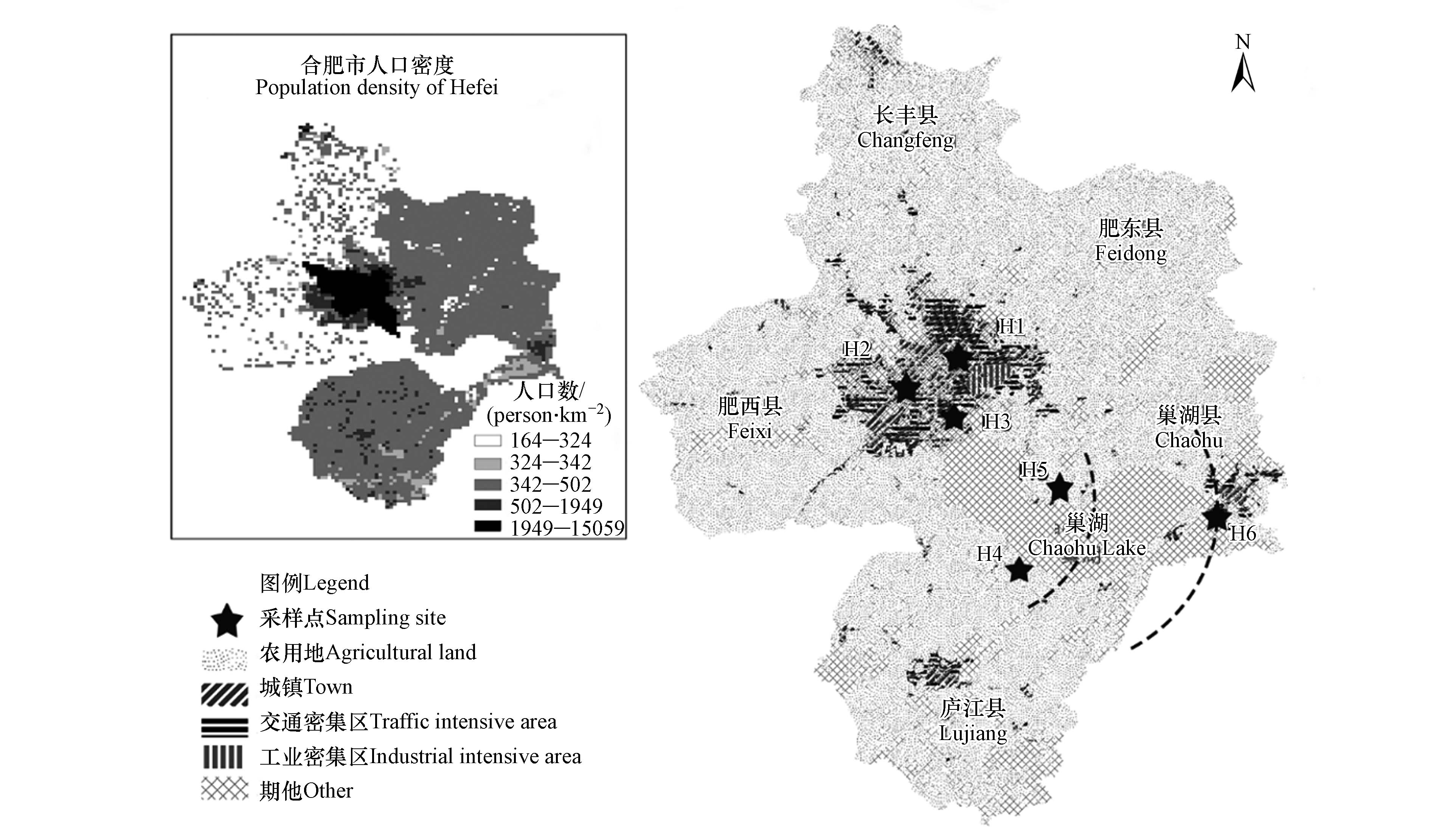
研究采用小流量大气采样器对安徽省典型区域的6个采样点进行了全年份不同季节的持续采样工作(2019年,春:3—5月;夏:6—8月;秋:9—11月;冬:11—12月),样点分布于安徽省省会城市——合肥市,考虑城市和和郊区不同排放特征,以及城市发展特征进行采样点布设,包括市中心采样点3个(分别为H1,H2,H3),以及郊区采样点3个(分别为H4,H5,H6). 区域采样点的布设按照距离城市中心的距离进行布点,其中H1位于市中心,H2和H3围绕市中心在城镇区域布局,H4和H5位于城市近郊,H6位于城市远郊. 在不同距离上采样点的布设主要考虑距离交通干线、工业区较近的区位,而郊区的3个采样点则考虑农业活动和人口密集程度差异布设,其中H6是郊区样点中人口密度相对较高区域,而H4和H5是农业活动强度相对较高区域,结合郊区监测位点的便利性和可达性基础上,在郊区布设了采样点(图1). 研究采用玻璃纤维膜(GFF)采集颗粒态样品,用聚氨基甲酸乙酯泡沫(PUF)吸附气态样品,其流量恒定为(5 ± 0.1) L·min–1,连续采样72 h. 采样前分别用甲醇和二氯甲烷超声去除GFF和PUF残留的有机物,同时采样前采样器的接头和不锈钢管均用去污剂清洗干净, 烘干后用丙酮擦净.
-
将回收率指示物加入PUF和滤膜,用体积比为1:1的正己烷/二氯甲烷混合溶剂索氏抽提48 h;抽提液经旋转蒸发,在内径为1 cm的硅胶层析柱净化(12 cm硅胶和6 cm氧化铝);用15 mL正己烷和二氯甲烷(体积比为7:3)混合溶剂淋洗,淋洗液再旋转蒸发至1 mL后转移至2 mL细胞瓶中氮吹至0.5 mL;加入内标(2-fluoro-1,1-biphenyl, p-terbenyl-d14, and DahA-d14). 回收率指示物为:萘-d8,指示萘和苊;二氢苊-d10,指示二氢苊和芴;菲-d10,指示菲、蒽、荧蒽、芘和苯并[a]蒽;䓛-d12,指示䓛、苯并[b]荧蒽和苯并[k]荧蒽;苝-d12,指示苯并[a]芘、茚并[1,2,3-cd]芘、二苯并[a,h]蒽和苯并[g,h,i]芘[12].
利用气相色谱-质谱联用仪(GC-MS, Agilent 7890A-5975C)定量分析16种PAHs,色谱分离使用HP-5MS毛细管色谱柱(30 m×0.25 mm×0.25 μm). 升温程序如下:初始温度为60 °C维持1 min, 以20 °C·min−1升温至150 °C, 再以4 °C·min–1升至300 °C保留6 min. 载气为高纯He(99.99%),流速为1 mL·min–1; 进样口温度为280 °C;传输线温度为310 °C; 四极杆和离子源温度分别为150 °C和230 °C.
-
使用内标法定量PAHs, 9个不同浓度梯度的PAHs标准溶液(10、20、50、100、200、500、1000、2000、5000 ng·mL–1)绘制标准曲线(R2 > 0.99),回收率分别为萘-d8(54%±12%)、二氢苊-d10 (80%±11%)、菲-d10(71%±13%)、䓛-d12(73%±14%)、苝-d12(68%±10%).
-
研究采用PAF模型和ICLR模型共同评估PAHs的健康风险. PAF可以在特定时期内,消除某些危险因素后,评估特定人群类型可减少某种疾病发病数的比例,即人群中癌症发病病例可归因于PAHs呼吸暴露导致的发病病例占发病总数的比例,根据Zhang等[2]采用的方法,PAHs浓度监测点所在区位的大气呼吸暴露导致的肺癌人群归因百分数计算如下:
其中,CBaPeq为毒性当量因子(TEF)转化后的BaP毒性当量浓度,具体参数见表1[13];rr(CBaPeq)是与CBaPeq浓度相关的B[a]Peq风险水平,污染物的浓度可以采用剂量-反应模型进行估算[14]. URR是B[a]P浓度为100 μg·m–3时年均暴露的基准单位相对风险,中国人群该值建议为4.49[15];终身暴露期是70a,基础背景值暴露量为100.
而ILCR可以表征一定规模人群中肺癌风险发病人数,本研究根据Wang等[16]的方法,采用ILCR评估大气苯并[a]芘终身暴露(70a)所引发的额外肺癌发病人数(10−6). 各监测点的大气呼吸暴露的终身致癌风险计算如下:
其中,IR是呼吸速率(m3·h−1),ET是日室外暴露时间(h·d–1),EF是室外暴露频率(d·a–1),ED是持续暴露时间(a),BW是体重(kg),AT是终身暴露时间(假设为70a,25550 d);CSF是呼吸暴露BaP的致癌斜率因子 (mg·kg–1·d–1). 研究将人群按照年龄划分为3组,分别为儿童(1—11岁)、青少年(11—17岁)和成人(>18岁),并基于表1中不同人群的风险参数分别计算室外呼吸暴露风险,并分析人群风险差异.
-
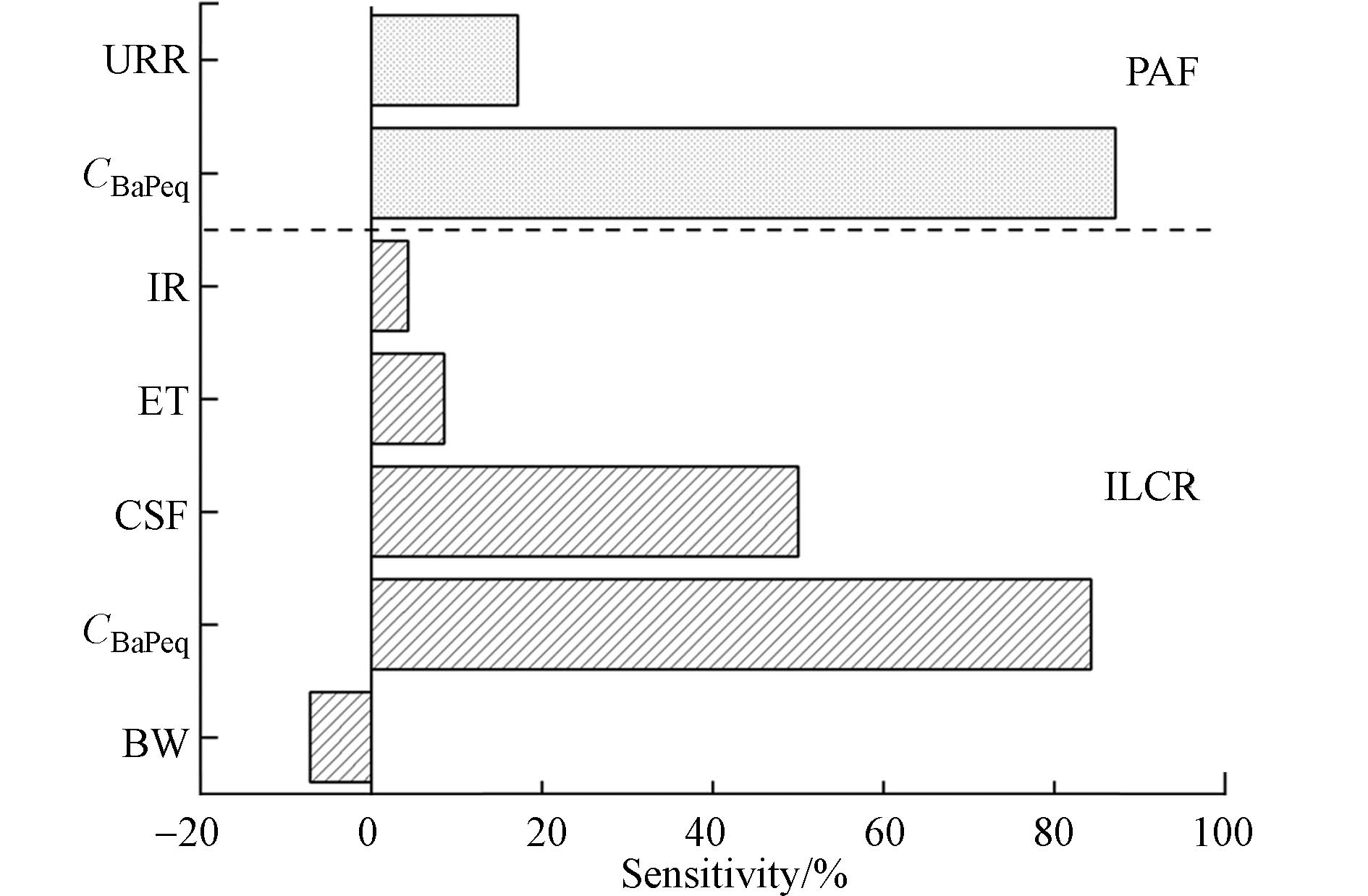
为了确定各因子对预测结果的影响,本研究采用蒙特卡罗模型模拟CBaPeq和URR对PAF的影响,模拟CBaPeq、呼吸速率(IR)、暴露时间(ET)、体重(BW)和CSF对ILCR的影响,所有这些参数均假设为对数正态分布[16] ,蒙特卡罗模拟在Crystal Ball 7.2中运行10000次.
-
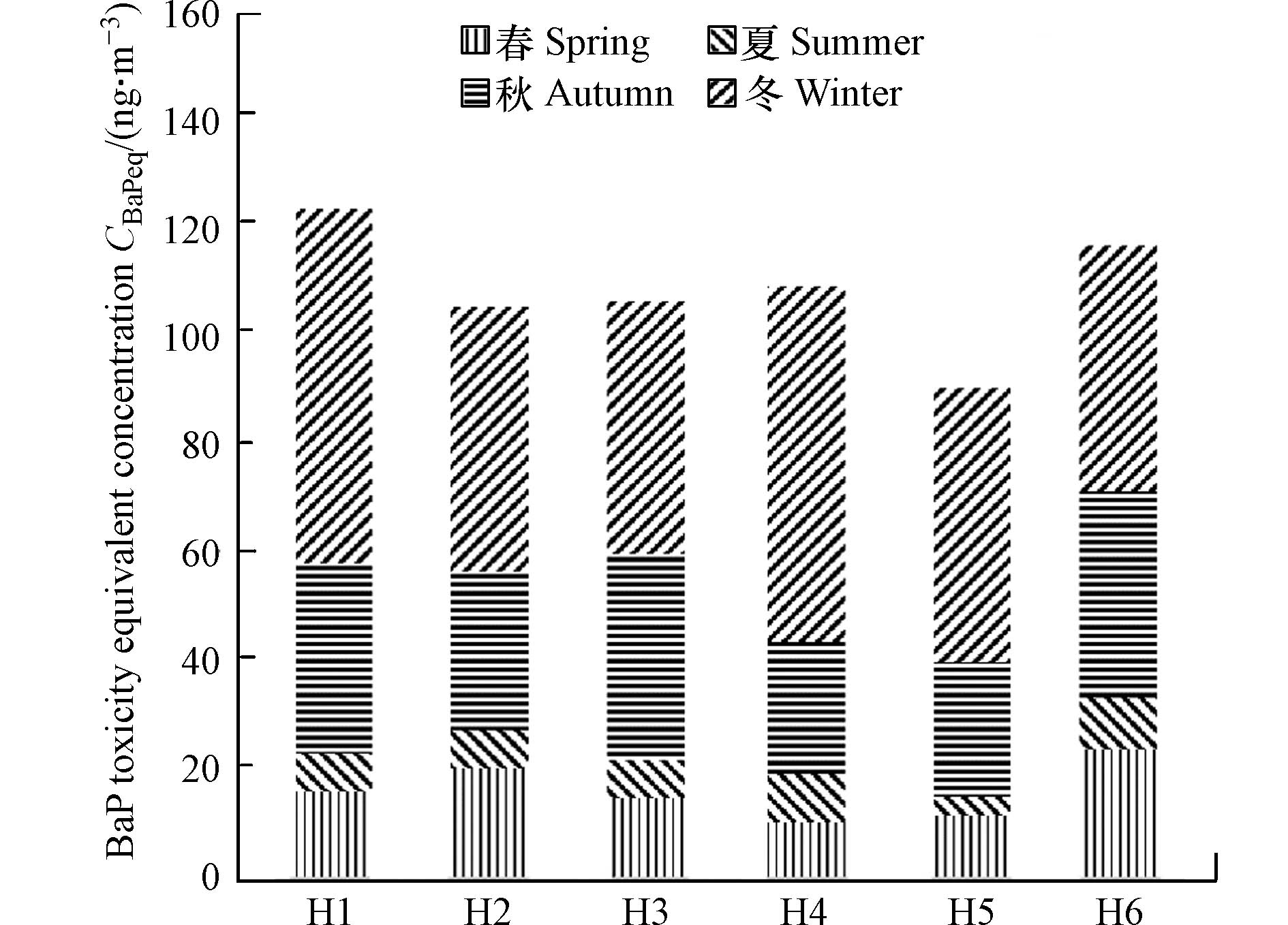
合肥城市CBaPeq浓度为0.121—2.24 ng·m–3,算术平均值为(0.743±0.586)ng·m3,所有数据经对数转化后符合正态分布(P=0.2). 其中H1和H6的年均CBaPeq浓度高于其他点位,主要由于H1位于城市中心,四周环绕交通道路、工业等复合污染源影响, H6虽然位于郊区,但所处位点具有明显的建成区,包括城镇住宅、交通工业等,同样为复合源影响. H2、H3和H4的污染物浓度没有明显差异,但由图1可知,三者污染来源不完全相同,其中H2和H3主要受到交通源影响,而H4则主要受到农业源影响. 稻谷、小麦和玉米是中国农业活动秸秆燃烧产生PAHs的主要作物类型,由《安徽省统计年鉴》可知,H4所处的庐江县,3种作物生产最大区域,约为巢湖市的2—3倍,因此H4的污染物浓度远高于H5.
城市区域大气中CBaPeq浓度呈现显著的季节性差异(图2),并呈现典型的秋冬季节高浓度排放特征. 冬季大气中CBaPeq浓度最大为(1.12±0.805)ng·m–3,显著高于春夏秋3个季节(P值均小于0.05). 秋季CBaPeq浓度虽然高于春夏,但仅与排放浓度最低的春季(0.269±0.121)ng·m–3,存在显著性差异. 冬季大气中CBaPeq浓度显著偏高原因一方面在于冬季采暖导致化石燃料和生物质燃料排放增加,另一方面也在于气温较低,大气边界层稳定,污染物不易扩散[17-18].
-
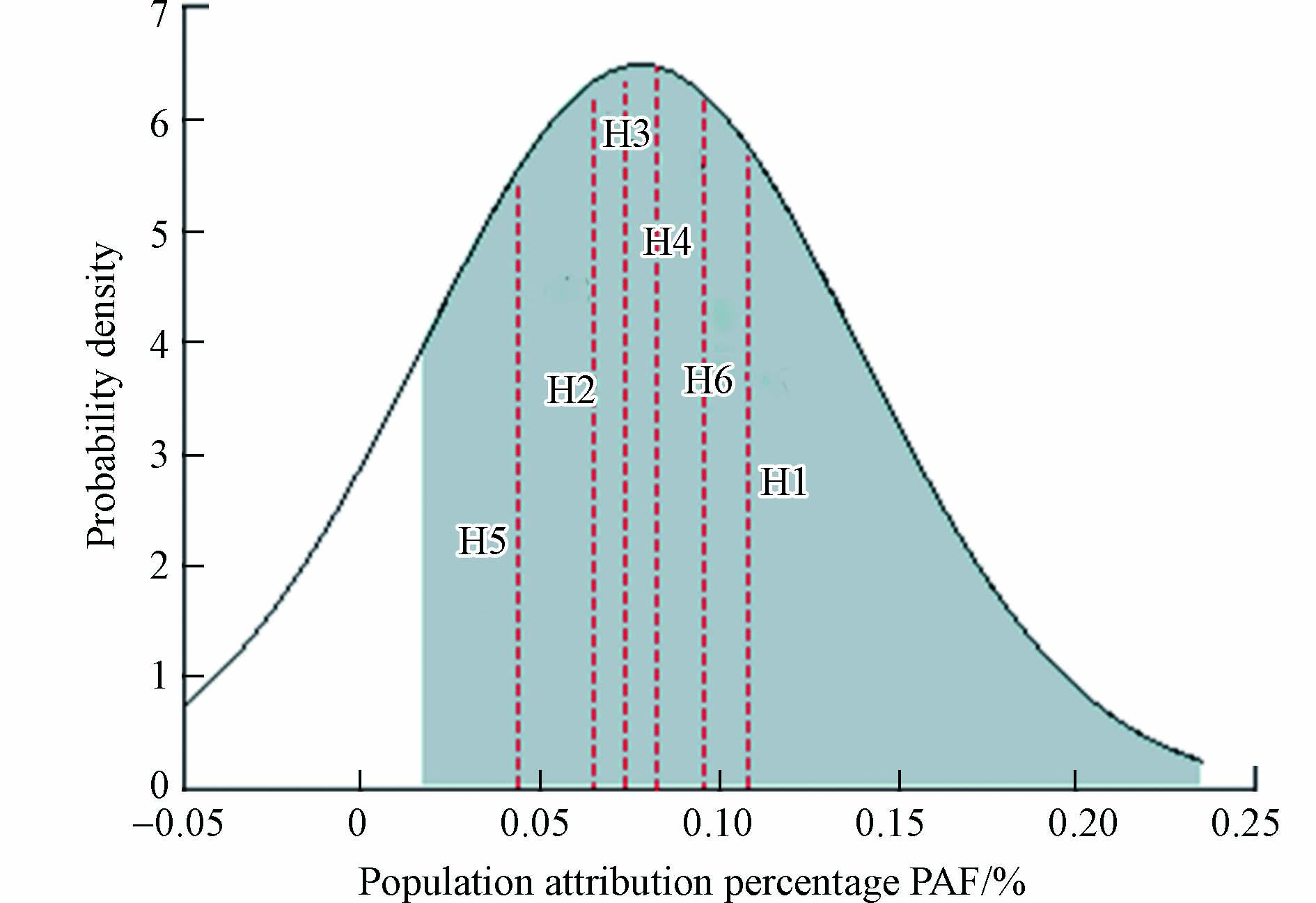
PAHs暴露浓度水平参数rr(CBaPeq)的算数均值约为1.0008,其5%,25%,75%和95%百分位数的计算值分别为1.0002、1.0003、1.0011和1.0023,基于此可获得PAHs的肺癌风险概率分布(图3). 研究结果显示,城市尺度PAHs肺癌风险水平符合正态分布,PAF风险值平均为(0.78‰±0.62‰). 各采样点H1所在区位PAF值最大,为(1.1‰±1.0‰),归因于人口密度最大,污染浓度最高,其次为H6,该点位于郊区县中心,人口密度较高,因此PAF值相对较高. 其他采样点PAF值为H6 > H4> H3 > H2 > H5,H5污染浓度和人口密度都相对较低,该处PAF值仅为(0.49‰±0.26‰).
表2列举了基于PAF模型计算的不同国家和城市尺度下PAHs暴露肺癌风险. 本研究结果低于文献报道的水平值[2,19-21]. 例如,Zhang等[2]估算2003年中国居民PAHs暴露肺癌风险PAF平均值为16‰. 洪文俊等[19]估算中国PAHs暴露肺癌风险PAF平均值为8.8‰,而同期韩国和日本的PAF平均值为0.38‰—0.85‰. 我国山西晋中和北京的平均PAF值分别为77‰和71‰[20],该异常高值的原因,一方面是这些研究除分析了16种母体PAHs外,还分析了其他母体PAHs和硝基PAHs,另一方面,与这两个地区PAHs排放强度较大有关,其中山西是炼焦大省,北京是交通高度密集区,这都是PAHs排放的主要来源[22]. 此外,本研究与国内研究PAF值差异较大主要是由于数据来源的差异,国家尺度核算多基于经验数据估算,重点反映区域整体的风险水平,而对于更为精细化的城市不同点位的风险评估则存在较大不确定性.
-
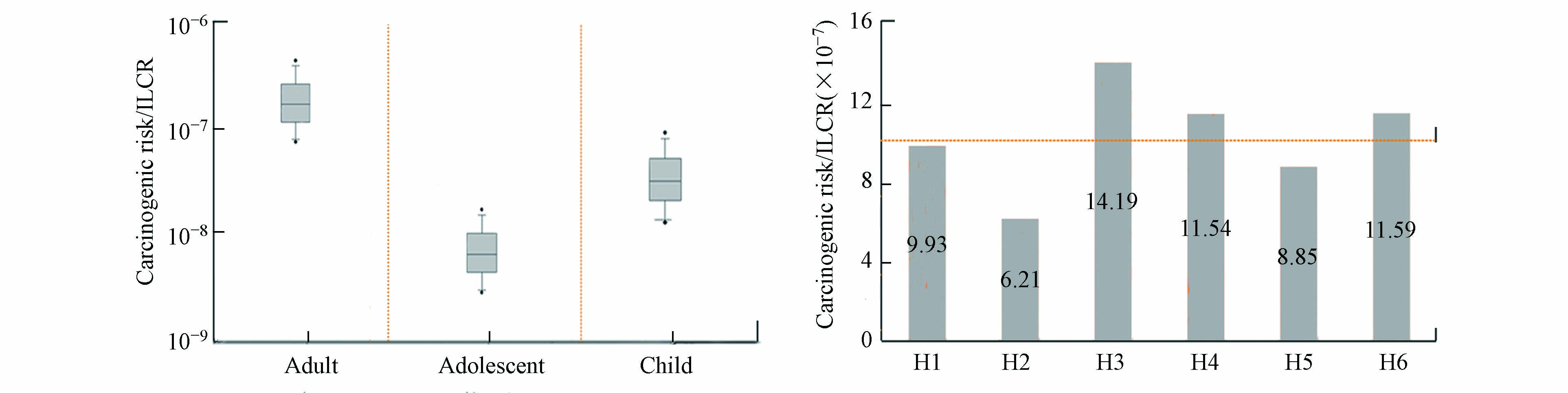
基于ICLR模型和蒙特卡洛方法,可知儿童、青少年和成人三组人群室外呼吸暴露大气中PAHs导致的ILCR分别为(6.59±5.20)×10−8、(1.23±0.97)×10−8和(1.99±1.57)×10−7(图4),终身致癌风险ILCR均低于美国EPA推荐的可接受致癌风险水平(1×10−6). 近年来,合肥市采取了一系列大气污染管控措施,包括服务业调整,降低交通污染源排放,包括农业秸秆燃烧控制以及郊区、农村地区电气化,减少生物质燃烧源排放[23],较大程度地降低了大气PAHs污染水平. 在各监测点位中,H3、H6和H4的ILCR值相对较高,这与PAF模拟结果相近. 此外,相对于PAF,ILCR体现了不同年龄段人群的致癌风险,儿童的致癌风险高于青少年,主要源于儿童的风险易感性较高.
由表3可知,不同地区成人和儿童的ILCR值的差异较大. 例如北京、太原等北方城市儿童的ILCR值显著低于成人,这主要是由于北方城市秋冬季节温度偏低,污染物浓度高而儿童室外活动频率低所致[21, 24]. 环渤海区域和广州市儿童的ILCR值略高于成人,主要是因为这些研究除了考虑儿童易感性,还考虑了市内污染来源和室外活动时间[25-26]. 以上研究中儿童和成人的健康风险差异往往在2—5倍,与本研究结果一致. 而巴基斯坦和印度(坎普尔)儿童和成人的风险值差异相对较小(1—2倍) [27-28]. 前人研究表明,不同人群之间的基因、饮食对于PAHs暴露肺癌风险均会产生影响[2, 6],比如越南、印度较低致癌风险受到饮食习惯和人种的易感性差异影响[4]. 因此,针对不同人群的健康风险差异的研究应引起重视.
-
PAHs呼吸暴露产生的健康风险不确定性主要取决于大气中PAHs的浓度(CBaPeq)、呼吸速率(IR)、居民室外活动(暴露时间)(ET)、呼吸大气PAHs的致癌斜率因子(CSF). 通过蒙特卡罗模拟发现,CBaPeq的ILCR的预测结果影响最大,相对贡献率高于80%(图5),同时CSF也是影响ILCR预测结果的重要因子(51%),而体重(BW)、IR和ET对ILCR的预测结果影响较小,相对贡献率分别为-7%、4%和8%. 大气中CBaPeq也是影响PAF预测结果的最重要因子,相对贡献率为89%,其次为URR(B[a]P浓度为100 μg·m−3时每年暴露的基准单位相对风险),其相对贡献率为40%. 由此可见,大气中CBaPeq的浓度是影响健康风险评价的关键因子,因此获取能代表区域污染的数据最为关键,增加采样点位和采样频次可以获得更多数据以此确定区域浓度. 本研究通过检验CBaPeq的分布特征后,通过蒙特卡罗10000次模拟获得城市区域大气中CBaPeq的分布,并进行PAF和ILCR计算. 此外,考虑到人口密度对大气PAHs浓度的影响,很多研究建议采用人口加权浓度进行健康风险评价. 本研究未进行人口加权浓度计算,所以对预测结果造成一定不确定性影响.
-
本文基于合肥市大气中PAHs浓度,通过苯并[a]芘等效毒性系数得到总的BaPeq,结合适用的人群呼吸暴露参数和模型定量计算不同位点的呼吸暴露量及肺癌风险,结果如下:
(1)大气中PAHs的年平均浓度为(10.76±10.93 )ng·m–3,高浓度区域主要分布于城市中心交通要道附近,低浓度区域主要分布于远郊,浓度分布由城市中心向外围逐渐降低.
(2)室外PAHs呼吸暴露所导致的额外肺癌发病率为4.33×10−6,PAF值主要受浓度分布和人群密度影响.
(3)基于ILCR模型可知,本研究中平均每百万人群暴露于大气PAHs所产生的额外肺癌发病人数为9.47,与PAF模型计算结果具有较好的一致性.
基于PAF和ICLR模型的大气多环芳烃人体暴露肺癌风险评价:以合肥市为例
Lung cancer risk assessment of the exposure to atmospheric polycyclic aromatic hydrocarbons based on population attributable fraction and incremental lifetime cancer risk models: A case study in Hefei
-
摘要: 城市有机污染物排放引起的致癌风险是当前人群健康研究关注热点. 本研究以安徽省会合肥市为案例,以多环芳烃(PAHs)为研究对象,结合实地采样分析以及超额终生致癌风险模型(ILCR)和人群归因模型(PAF)对城市不同区域、季节、人群的致癌风险进行评估,并采用蒙特卡洛模型解析不同模型的致癌风险评估差异. 研究表明,合肥市大气PAHs暴露所引起的额外肺癌每百万人为9.47,ILCR与PAF模型模拟结果具有较好的一致性,而PAF模型的参数敏感性较高. 合肥城市PAHs的致癌风险的空间分布、季节变化以及人群分布都存在显著的空间异质性:城市中心道路交通高排放区和郊区农业活动强度大区域的致癌风险较高;秋冬PAHs的浓度水平较高导致较高致癌风险;室外活动频繁的成年人致癌风险高,儿童的风险易感性高. 因此,城市人群健康风险综合管控需要系统考虑不同污染排放源的分布差异.
-
关键词:
- 多环芳烃(PAHs) /
- 人群归因模型 /
- 超额终生致癌风险 /
- 暴露肺癌风险
Abstract: The cancer risk caused by exposure to atmospheric organic pollutants in cities has raised increasing global concern. However, the spatial characteristics of the cancer risk in cities remain largely unknown because there are large differences in the distribution of pollution source and population density. In this study, we analyzed the 16 U.S. EPA priority polycyclic aromatic hydrocarbons (PAHs) in the atmosphere in Hefei, the capital city of Anhui province, over one year period. We also estimated the lung cancer risk caused by exposure to atmospheric PAHs based on the population attributable fraction (PAF) and incremental lifetime cancer risk (ILCR) models. Results indicated that the average excess inhalation risk were 9.47 cancer cases per million people. The overall PAF value was 0.78‰, coinciding well with the ILCR value. The cancer risk at urban sites were noticeably higher than those at tourist area site and rural site. The cancer risk was higher in winter and autumn than those in summer and spring. Adults had higher risk of lung cancer than children and adolescents. -
近年来,越来越多的沿海地区采用海水淡化或海水直接利用技术作为缓解淡水紧缺危机的方法[1],而海水冲厕技术即为海水直接利用技术之一。使用海水冲厕可有效缓解我国沿海城市生活用淡水资源的供需矛盾[2],但采用此技术会产生大量的高含盐生活污水,给污水处理带来了巨大挑战[3]。有研究[4]表明,膜生物反应器(membrane bioreactor, MBR)对于处理高盐废水有较为显著的效果,MBR中的活性微生物经培养驯化后,能适应不同盐度的废水。ZHANG等[5]运用MBR工艺处理海水养殖废水时,当盐度由0 g·L−1增加到30 g·L−1时,MBR对COD和NH4+-N的去除率均保持在90%以上。然而MBR运行过程中产生的膜污染仍是影响MBR工艺稳定运行及阻碍其进一步商业化应用的主要因素[6]。
电化学MBR是近年来发展起来的新型污水处理技术[7],有研究表明,电场是缓解膜污染、提高出水水质的有效清洁的途径之一[8],其属于使用物化法控制膜污染的范畴,具有清洗效果好、过程稳定、无需外加化学药剂、没有二次污染、成本低等特点,可为拓展MBR的工程化应用提供技术支撑[9]。DUDCHENKO等[10]采用改性导电膜,建立了膜阴极MBR,发现在-3 V和-5 V下运行100 min时,TMP分别降低了33%和51%,外加电场可有效缓解膜污染。但外加电场的MBR系统应用于处理高盐废水的研究较少。本研究采用电强化的陶瓷膜MBR(E-MBR)处理模拟的海水冲厕水,通过与传统MBR(C-MBR)进行对比,考察了在不同电流密度下外加电场MBR系统运行性能、体系内活性污泥特性以及系统运行过程中膜污染行为的变化规律,以期为外加电场MBR处理含盐污水的实际应用提供参考。
1. 材料与方法
1.1 实验装置和进水水质
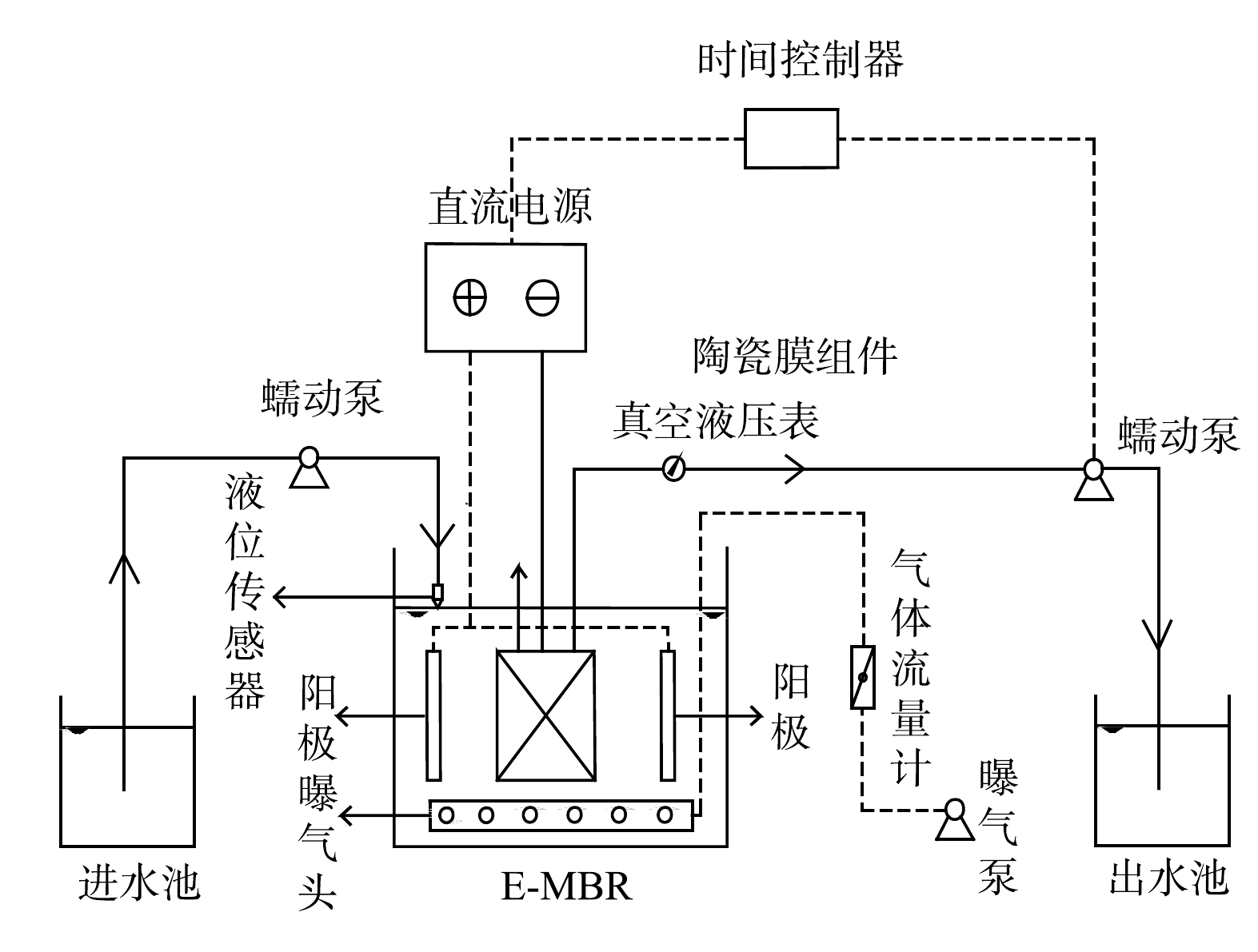
E-MBR装置如图1所示。反应器采用有机玻璃材料,有效容积为12 L(20 cm×15 cm×40 cm)。膜孔径为0.1 μm的平板陶瓷膜置于反应器中央,采用双侧过滤,有效过滤面积为0.05 m2。钛丝插入膜组件中与直流电源的负极相连,作为E-MBR的阴极。2片石墨板阳极置于膜组件两侧距膜表面3.5 cm处,2块阳极板的有效面积均为0.025 m2。电极夹为铁质电极夹。进水由液位传感器控制,反应器液面低于设定的界面时自动进水。蠕动泵控制出水,保持恒定通量为20 L·(m2·h)−1,工作10 min,停止2 min,电场在出水停止时施加。另一个相同大小但是不施加电场的C-MBR与E-MBR平行运行,作为对照组。
本实验中1、2、3阶段设置的电流密度分别为2、2.6、3.2 A·m−2,对应的电流分别为0.1、0.13和0.16 A,每个阶段运行过程中保持电流恒定。反应器内接种污泥为驯化后适应10‰盐度污水的活性污泥,反应器内初始MLSS约为3 g·L−1,第2和第3阶段开始前会对E-MBR和C-MBR进行排泥,使得施加新的电流密度前2个反应器内的MLSS保持在3 g·L−1左右。进水为模拟海水冲厕水,组分为500 mg·L−1无水乙酸钠,400 mg·L−1 NH4Cl,30 mg·L−1 KH2PO4,pH为7.5~8(投加NaHCO3),10 000 mg·L−1海水晶,盐度和微量元素均由海水晶提供。模拟废水通过蠕动泵进入MBR中,经过膜组件过滤出水,出水采用蠕动泵抽吸方式,在恒定通量条件下运行。利用数字压力表记录TMP的变化,当TMP上升到40 kPa,取出膜组件,用海绵球擦洗并用去离子水冲洗膜表面滤饼层,如膜通量仍不稳定,用0.3%(体积分数)的NaClO溶液浸泡2 h,再用去离子水冲洗浸泡2 h并反冲洗5 min。
1.2 测试方法
COD、NH4+-N、TP和MLSS均采用国家规定的标准方法测定,比氨氧化速率(SAOR)的测定方法参考文献[11]。采用激光粒度分析仪测定污泥粒径分布(particle size distribution,PSD),污泥混合液的Zeta电位采用Zeta电位分析仪(Zetasizer Nano Z,Malvern Instruments,UK)测定。SMP(soluble microbial product)和EPS(extracellular polymeric substance)是影响膜污染的重要因素。采用离心过滤法提取SMP,采用热提取法提取EPS[12]。上述提取物均经0.45 μm滤膜过滤,采用蒽酮比色法测定多糖含量,采用Folin-酚分光光度法测定蛋白质。通过膜污染过程中阻力分布分析,可以得出造成膜污染增加的主要因素。根据达西(Darcy’s law)定律公式可以得到膜总阻力RT,膜固有阻力Rm,膜浓差极化阻力Rcp,膜面滤饼层阻力Rc以及膜孔阻力Rb。
2. 实验结果与讨论
2.1 电流密度对污染物去除的影响
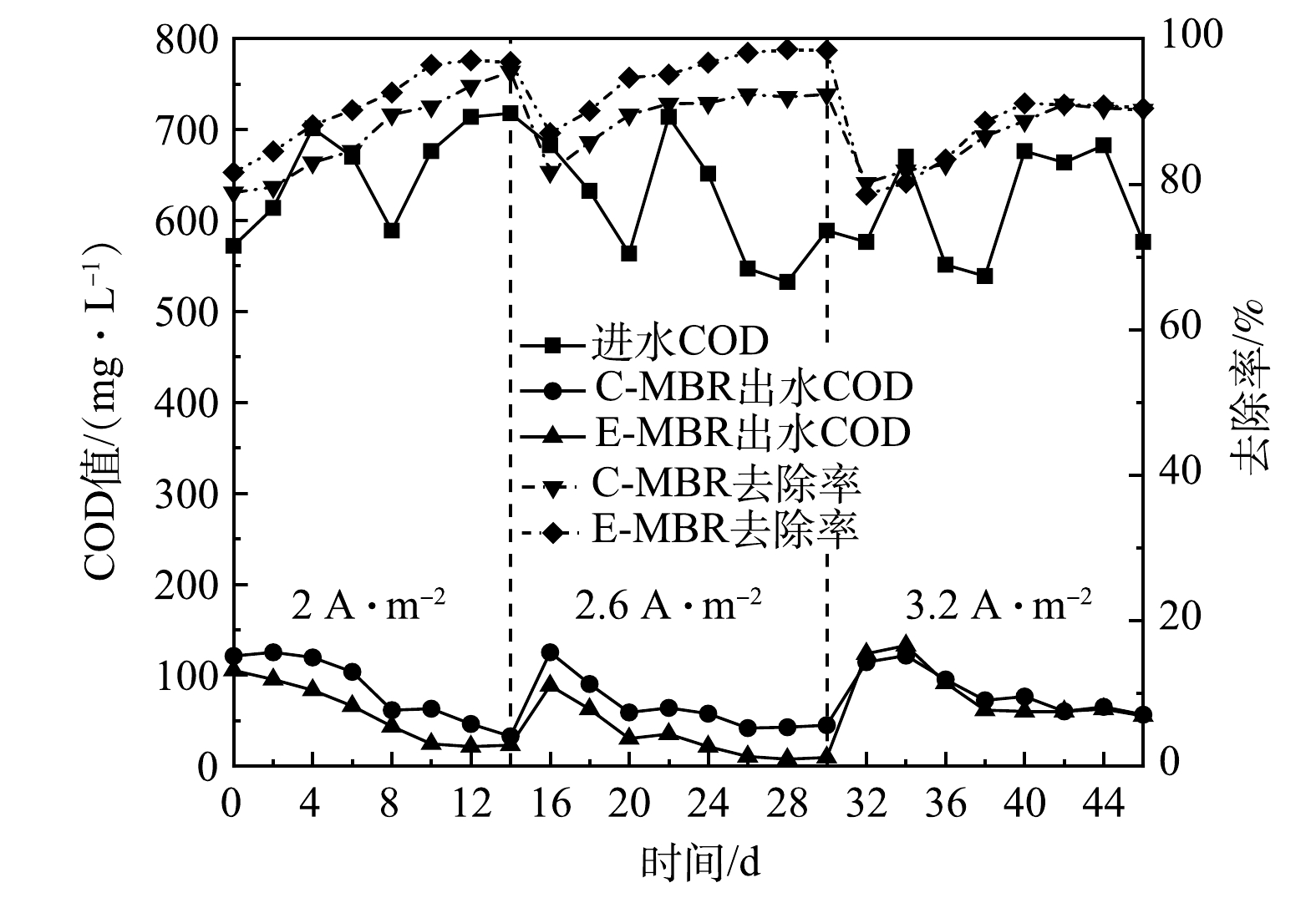
1)对COD去除效果的影响。如图2所示,当电流密度为2 A·m−2时,E-MBR系统运行初期COD的去除率为81.6%,略高于C-MBR的COD去除率(78.83%),经过一定的适应时间,E-MBR和C-MBR系统中COD去除率均可达到95%以上。但由图2可以看出,此运行期间,E-MBR系统COD的去除率均高于C-MBR。电流密度为2.6 A·m−2时E-MBR和C-MBR的运行效果与电流密度为2 A·m−2时的效果类似,E-MBR对COD的去除效果优于C-MBR,但在此阶段E-MBR中COD去除率达到90%需要的时间(2 d)短于电流密度为2 A·m−2阶段需要的时间(6 d)。由图2可知,在同样适应时间内,电流密度为2.6 A·m−2阶段的COD去除率要明显高于电流密度为2 A·m−2的阶段。第2阶段系统运行末期,E-MBR中COD去除率稳定在98%以上,略高于第1阶段末96%的去除率。其原因可能归为以下2点:适宜的弱电场对细胞代谢产生电刺激,提高微生物活性,促进了有机物的降解[13];随着电流密度的增大,体系中产生的具有氧化活性的物质浓度提高,进一步将有机物污染物降解为小分子有机物甚至矿化为二氧化碳和水[14]。继续提高电流密度至3.2 A·m−2,此阶段运行末期系统达到稳定状态,E-MBR系统COD的去除率稳定在90%左右,相较于前2个阶段有所降低。不同于前2个阶段中E-MBR对COD去除效果均优于C-MBR,此阶段E-MBR中COD去除率没有显著提高,与C-MBR对COD的去除效果相近。这是因为系统中污泥的活性在过大的电场作用下被抑制,从而导致系统中COD的去除率下降[15]。
2)对NH4+-N去除效果的影响。如图3(a)所示,在电流密度为2 A·m−2时,经过一段时间的适应,E-MBR和C-MBR中NH4+-N的去除率均可达到98%以上;当电流密度为2.6 A·m−2时,E-MBR系统在此阶段运行末期对NH4+-N的去除率达到了99%,高于此阶段下C-MBR系统95%的NH4+-N去除率。前2个阶段末期,E-MBR出水中NH4+-N的质量浓度均保持在1.5 mg·L−1左右,符合我国《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准[16],出水水质良好。第3阶段(电流密度为3.2 A·m−2),C-MBR对NH4+-N的去除率依旧良好,可达95%,但E-MBR对NH4+-N的去除率明显降低,平均去除率仅为88.33%,显著低于上一阶段96.37%的平均去除率。这是因为MBR中污泥的活性在过高的电流密度下被抑制,NH4+-N的去除率也随之降低[17]。
图3(b)为电流密度对微生物SAOR的影响结果。可见,随着电流密度的增大,E-MBR系统中SAOR呈先升高后降低趋势,当电流密度由2 A·m−2增加至2.6 A·m−2时,SAOR由(3.86±0.18) mg·(h·g)−1(以MLSS计)增加至(4.88±0.12) mg·(h·g)−1,升高了26.42%。电流密度升至3.2 A·m−2时,SAOR降低为(3.06±0.15) mg·(h·g)−1,相比于第2阶段降低了37.30%。上述结果表明,在适宜的电场强度范围内,增大电流密度可以显著提高系统中氨氧化菌活性,电流密度过大则会对氨氧化菌活性产生抑制作用。此结果与电流密度为2 A·m−2和2.6 A·m−2下NH4+-N去除效果显著高于3.2 A·m−2条件下NH4+-N去除效果的结果一致。
体系中氨氮的去除依赖于生物作用下的氧化作用和外加电场后产生的电氧化作用。膜的高效截留作用使世代周期较长的硝化菌和亚硝化菌在反应器内呈现出优先生长繁殖的趋势,并且避免了硝化菌的流失,硝化过程更完全,从而使膜出水的氨氮浓度逐渐降低[18];另一方面,在适宜范围内,随着电流密度的增大,电氧化作用相应增强,体系中产生的H2O2可以将NH4+-N氧化为氮气和水,促使污染物浓度降低[19]。
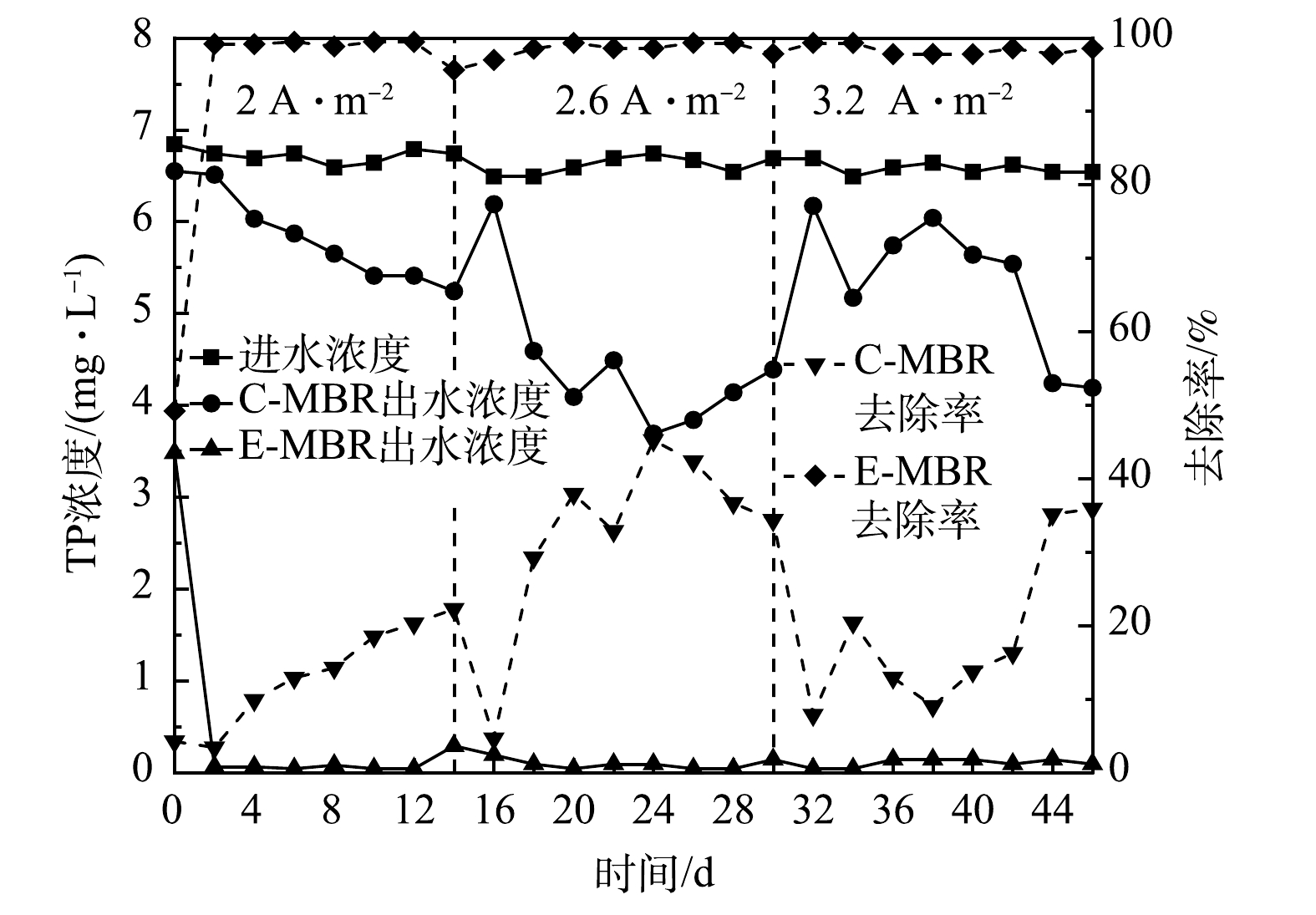
3)对总磷去除效果的影响。如图4所示,运行第1天时,E-MBR系统TP的去除率为49.22%,显著高于C-MBR对TP的去除率(4.22%)。第2天,E-MBR系统TP的去除率升至99.17%,此后TP的去除率一直稳定在99%以上。第2阶段和第3阶段E-MBR的TP去除率也一直维持在98%左右,远远高于C-MBR系统中TP的去除率。在第1、2、3阶段,随着反应器的运行,每一阶段末期C-MBR的TP去除率均稳定在35%左右。导致2个体系TP去除率差异如此大的原因可能归为以下2点:一是电场对聚磷菌生长的影响,电场作用下聚磷菌的活性增强——体系中产生的H2O2进入细胞体内分解产生大量O2,促进细胞的呼吸及氧化还原作用,减缓了对水分的吸收速率,与能量代谢有关的酶活性迅速提高,从而提高对TP的去除[20];二是电场作用下,阳极铁电极夹释放出的亚铁离子与混合液中的磷发生反应生成了不溶沉淀[21]。由图4可见,E-MBR系统电流密度增大至3.2 A·m−2时,TP的去除率并没有与上述COD和NH4+-N去除率在此阶段呈下降趋势相一致。这可能是由于菌种对电场的耐受差异决定的:去除磷的微生物与去除COD和NH4+-N的微生物对电场的响应情况、耐受程度不同,即在较高的电场强度下,去除COD和NH4+-N的微生物活性首先受到抑制,而去除磷的微生物活性依旧保持。
2.2 电流密度对污泥特性的影响
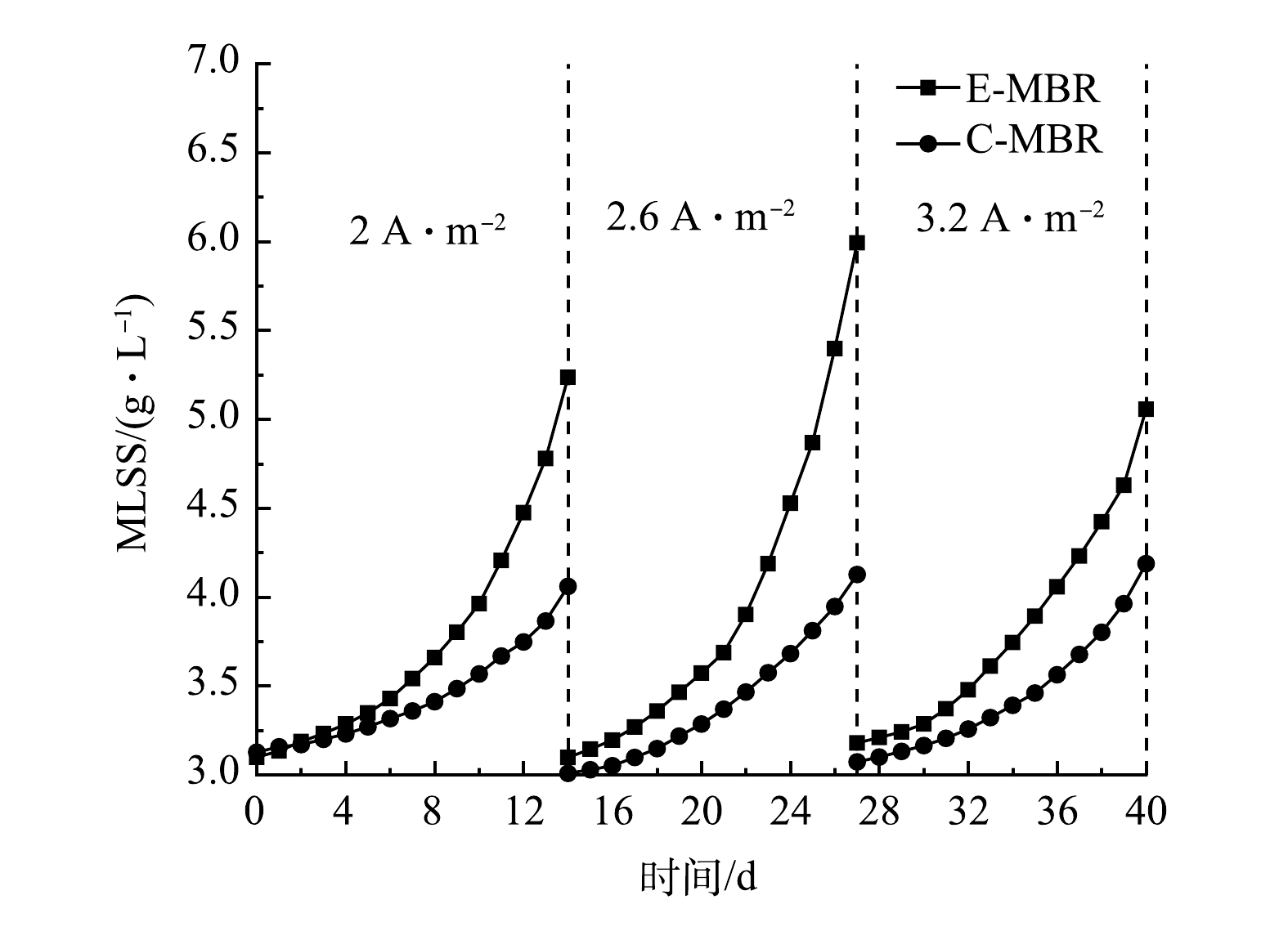
1)电流密度对污泥浓度的影响。考察了不同电流密度下2个系统MLSS的变化,结果如图5所示。电流密度为2 A·m−2时,C-MBR中MLSS由最初的3.13 g·L−1升至最终的4.06 g·L−1,增长了30%,此阶段E-MBR中MLSS阶段末比阶段初增长了69%。电流密度为2.6 A·m−2时,C-MBR阶段末比阶段初增长了37%,E-MBR阶段末比阶段初增长了93%。电流密度为3.2 A·m−2时,C-MBR阶段末比阶段初增长了36%,E-MBR阶段末比阶段初增长了59%。以上结果表明,施加适当的电场可促进MLSS的升高,电流密度为2.6 A·m−2时MLSS增长最快,电流密度为3.2 A·m−2时MLSS增长最缓慢。电场对污泥浓度的影响主要体现在电场对微生物活性的影响,适宜的电场强度作用下,体系中某些酶(脱氢酶、氨单加氧酶、亚硝酸盐还原酶、硝酸盐还原酶等)的活性增强甚至被激活,从而促进酶的生物活性反应[22]。适宜的微电场也可调节微生物代谢,使微生物细胞膜的通透性得以增强,营养基质离子的定向迁移在电场作用下被强化[23]。
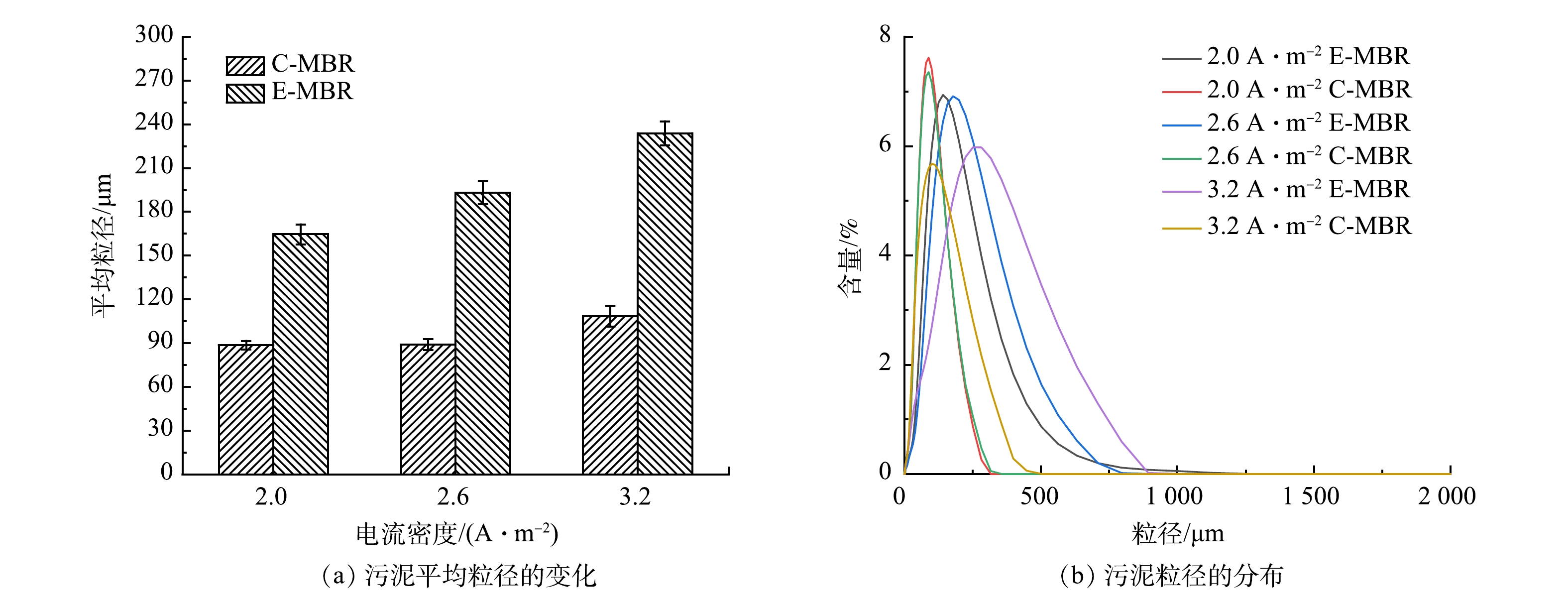
2)电流密度对污泥粒径的影响。电场作用下污泥粒径的变化见图6。由图6(a)可以看出,各阶段E-MBR系统中污泥的平均粒径均显著大于C-MBR系统中的污泥粒径。施加的电场产生的电絮凝作用对污泥颗粒的最大影响之一就是促进污泥颗粒团聚[24]。在第1阶段,外加电场后污泥的平均粒径由对照反应器的89 μm增加至165 μm;第2阶段由89 μm增加至193 μm;第3阶段由108 μm增加至234 μm。进一步考察了各阶段2个系统中污泥粒径分布情况。由图6(b)可知,E-MBR中污泥粒径的分布更加集中,污泥粒径的分布可能更加均匀。均匀性可以通过污泥分散性指数(DSI)表征,DSI值越小,污泥分布越均匀。进一步计算两系统各阶段DSI值可得:电流密度为2 A·m−2时,C-MBR系统的DSI为0.931,E-MBR系统的DSI为0.815;电流密度为2.6 A·m−2时,C-MBR系统的DSI为0.908,比E-MBR系统大了0.062;电流密度为3.2 A·m−2时,C-MBR系统的DSI为1.08,E-MBR系统的DSI为1.072。这说明,外加电场后,DSI值降低,体系中污泥粒径的均匀性得到了有效提高。滤饼层阻力的大小是膜污染总阻力大小的决定性因素之一,滤饼层的形成与系统DSI的大小有一定关系,DSI降低,表明附着在膜表面的滤饼层阻力越小,形成的滤饼层越松散[25]。由此可知,外加电场后,较大粒径的活性污泥可以减少膜孔的堵塞,减缓膜污染的程度[26],同时污泥絮体均匀性的提高同样减缓了膜污染速度。
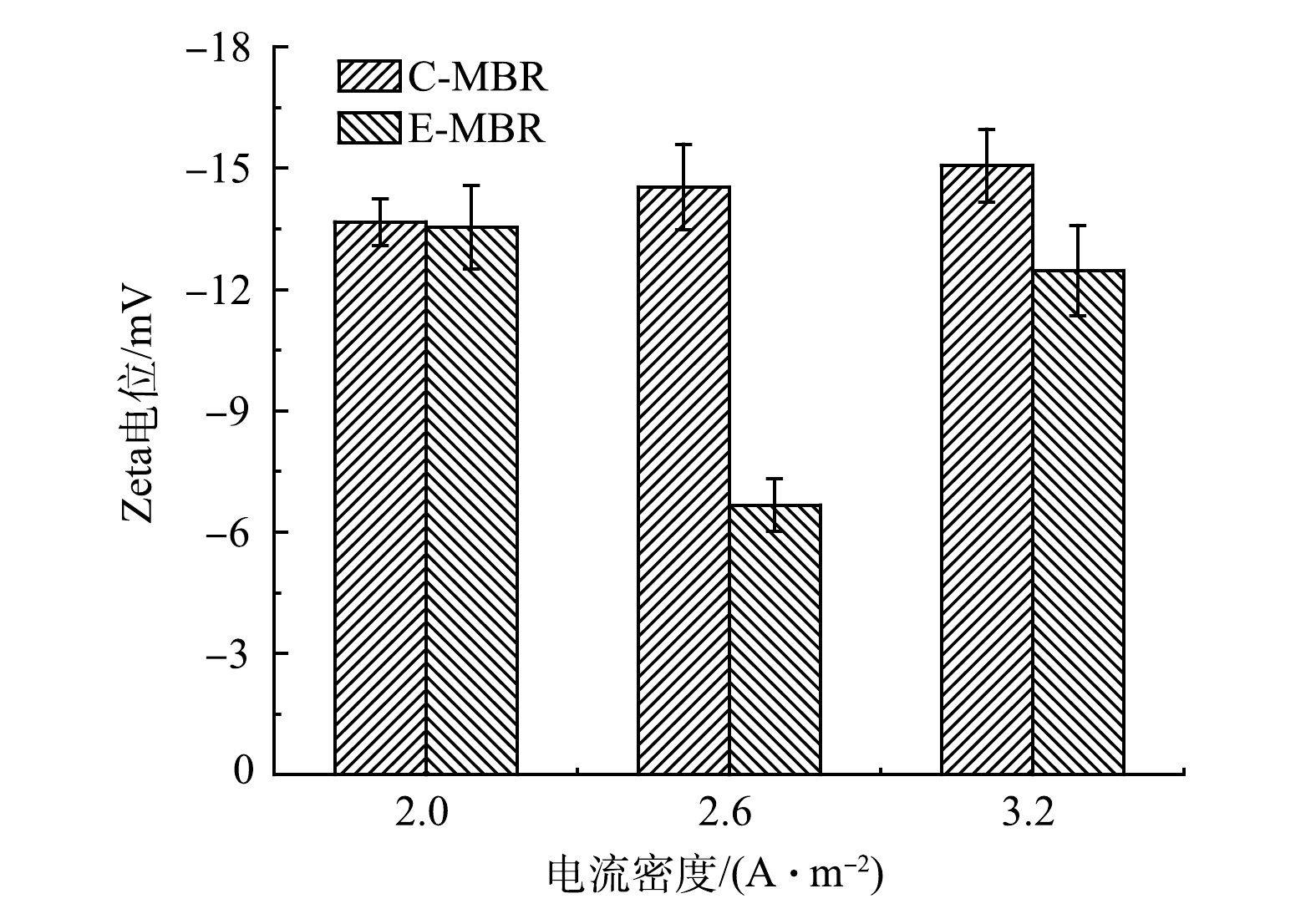
3)电流密度对污泥Zeta电位的影响。如图7所示,电流密度为2 A·m−2时,E-MBR系统的Zeta电位(绝对值13.53 mV)略小于C-MBR系统(13.67 mV)。电流密度增大至2.6 A·m−2时,2个系统Zeta电位的差值显著变大,C-MBR系统的Zeta电位为14.53 mV,E-MBR的Zeta电位为6.67 mV,下降了7.86 mV。电流密度为3.2 A·m−2时,C-MBR的Zeta电位为15.07 mV,E-MBR的Zeta电位为12.47 mV,下降了2.6 mV。电场降低污泥的Zeta电位表明电场的施加降低了污泥颗粒之间的排斥力,使得污泥颗粒更易团聚,较大的污泥颗粒更不易引起膜污染[27],这与前述电流密度对污泥粒径影响的结果是一致的。
2.3 不同电流密度下膜污染分析
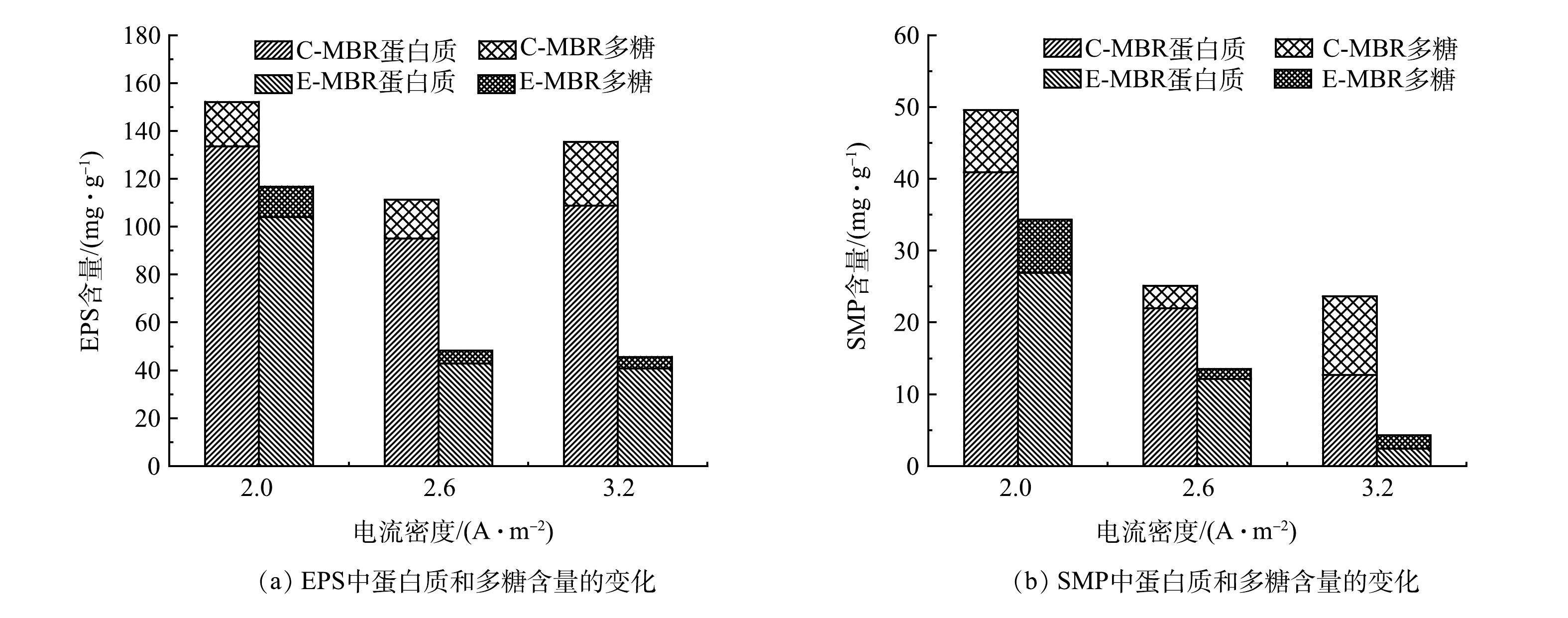
1)电流密度对膜污染物质的影响。SMP和EPS是影响膜污染的重要因素。图8反映了不同电流密度下EPS、SMP中蛋白质和多糖含量变化的情况。两系统混合液EPS中蛋白质和多糖含量如图8(a)所示。电流密度为2 A·m−2时,C-MBR中蛋白质含量为133.62 mg·g−1(以MLSS计),多糖含量为18.48 mg·g−1;相较于C-MBR,E-MBR中蛋白质含量降低了22.16%(104.01 mg·g−1),多糖含量降低了31.01%(12.75 mg·g−1)。第2阶段,C-MBR中蛋白质含量为95.08 mg·g−1,多糖含量为16.08 mg·g−1;相较于C-MBR,E-MBR中蛋白质含量降低了54.94%(42.84 mg·g−1),多糖含量降低了66.54%(5.38 mg·g−1)。第3阶段,C-MBR中蛋白质含量为108.8 mg·g−1,多糖含量为26.61 mg·g−1;相较于C-MBR,E-MBR中蛋白质含量降低了62.63%(40.66 mg·g−1),多糖含量降低了81.47%(4.93 mg·g−1)。从各阶段2个体系EPS中蛋白质和多糖含量的对比结果来看,随着电场强度的增大,EPS中蛋白质和多糖含量显著减少,从而在一定程度上缓解膜污染。产生此现象的原因可能有以下2点:一是电场作用可以刺激微生物活性,增强微生物的代谢能力,使得微生物不需要再分泌更多的EPS来改变生存环境,因此抑制了EPS的生成[28]; 二是电场作用下体系中产生的具有高氧化作用的H2O2和·OH可以致使EPS的含量降低[29]。
系统中另一主要膜污染物质SMP中蛋白质和多糖含量的变化与EPS一致,E-MBR系统SMP中蛋白质和多糖含量随着电流密度的增大而降低。这可能是由于系统中施加了适当的电场,具有较高的有机污染物处理效率,减少了系统中活性污泥的有机负荷,从而降低了SMP中蛋白质和多糖的含量。
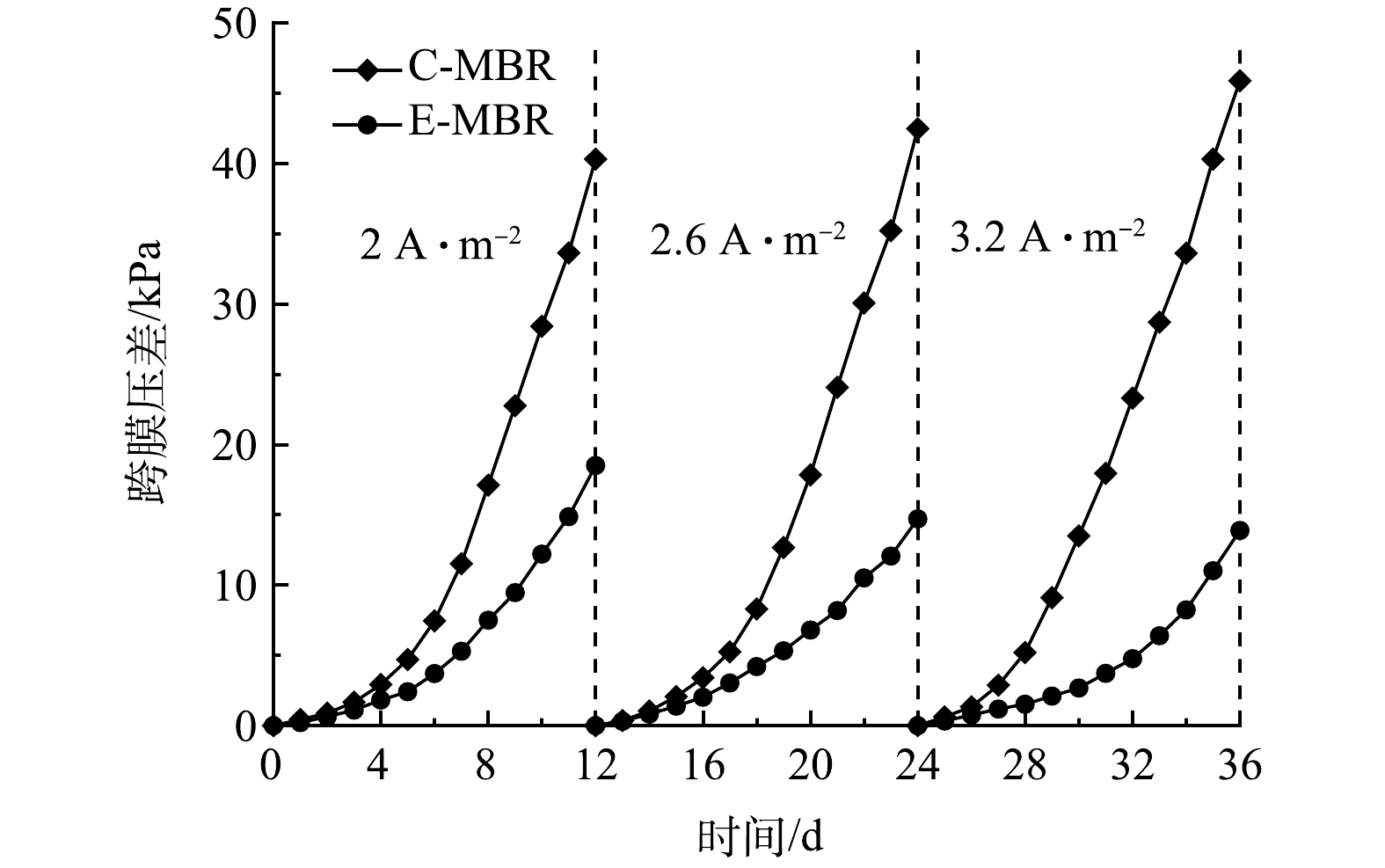
2)电流密度对系统TMP的影响。跨膜压差是反应膜污染程度的重要指标之一,跨膜压差越高膜污染越严重[30]。理论上,本研究E-MBR系统存在的电场作用会缓解膜污染情况,保持膜出水通量恒定。每个阶段TMP随时间的变化情况如图9所示。可见,每个阶段2个反应器TMP的变化均是由最初的平稳增长变为快速增长。在C-MBR中,TMP在运行前期略有增加,从第4天开始TMP迅速增加直至40 kPa。E-MBR中,从第6~8天开始,TMP的增长速率开始加快。每个阶段末期,C-MBR的TMP值分别为40.3、42.5、45.9 kPa,相对应时间下E-MBR的TMP值为18.5、14.7、13.9 kPa,分别比C-MBR降低了54.09%、65.37%和69.74%。对比3个阶段E-MBR系统TMP的增长,可以看出,电流密度越大,TMP增长越缓慢,膜污染缓解程度越明显。以上结果可以归因于以下3点:一是电场作用下,膜组件表面带负电,混合液中带负电的污泥絮体、大分子有机物或胶体在电场排斥力的作用下,向远离膜面的方向移动[31];二是附着在膜表面的污染物质会被混合液中电场作用下产生的H2O2和·OH等强氧化剂原位降解,膜污染从而得到缓解[32];三是电场作用下污泥性质发生改变,例如污泥Zeta电位变小,污泥粒径增大,这些均可以缓解膜污染。
3)电流密度对膜污染阻力分布的影响。根据Darcy公式算出不同电流密度下E-MBR和C-MBR体系中RT,Rm,Rcp,Rc以及Rb,表1为两系统中的膜污染阻力分布值。
表 1 3个阶段E-MBR和C-MBR中膜阻力分布表Table 1. Distribution of membrane resistance in E-MBR and C-MBR at three stages 1011 m−1阶段 实验组 RT Rm Rcp Rc Rb 第1阶段 E-MBR 3.24 0.091 1.54 0.673 0.929 第1阶段 C-MBR 4.36 0.090 1.28 1.88 1.11 第2阶段 E-MBR 2.51 0.089 1.04 0.46 0.92 第2阶段 C-MBR 3.62 0.094 0.596 1.57 1.23 第3阶段 E-MBR 2.77 0.094 1.16 0.496 1.02 第3阶段 C-MBR 5.75 0.09 1.92 2.4 1.29 由表1可知,在第1、2、3阶段中,C-MBR的膜总阻力分别为E-MBR的1.35、1.44和2.07倍。这表明外加电场可有效减少膜阻力,缓解膜污染,延长膜的使用期限。对于膜的特定阻力(Rm、Rcp、Rc、Rb),Rc为每个阶段下2个系统中数值差异较大的指标,第1阶段,相较于C-MBR的Rc值,E-MBR减少64.2%,第2阶段降低了70.7%,第3阶段减少了79.33%。以上结果表明E-MBR中膜污染得到有效控制的决定性因素为微电场作用,并且外加电场是通过有效控制膜表面的滤饼层阻力来缓解膜污染。
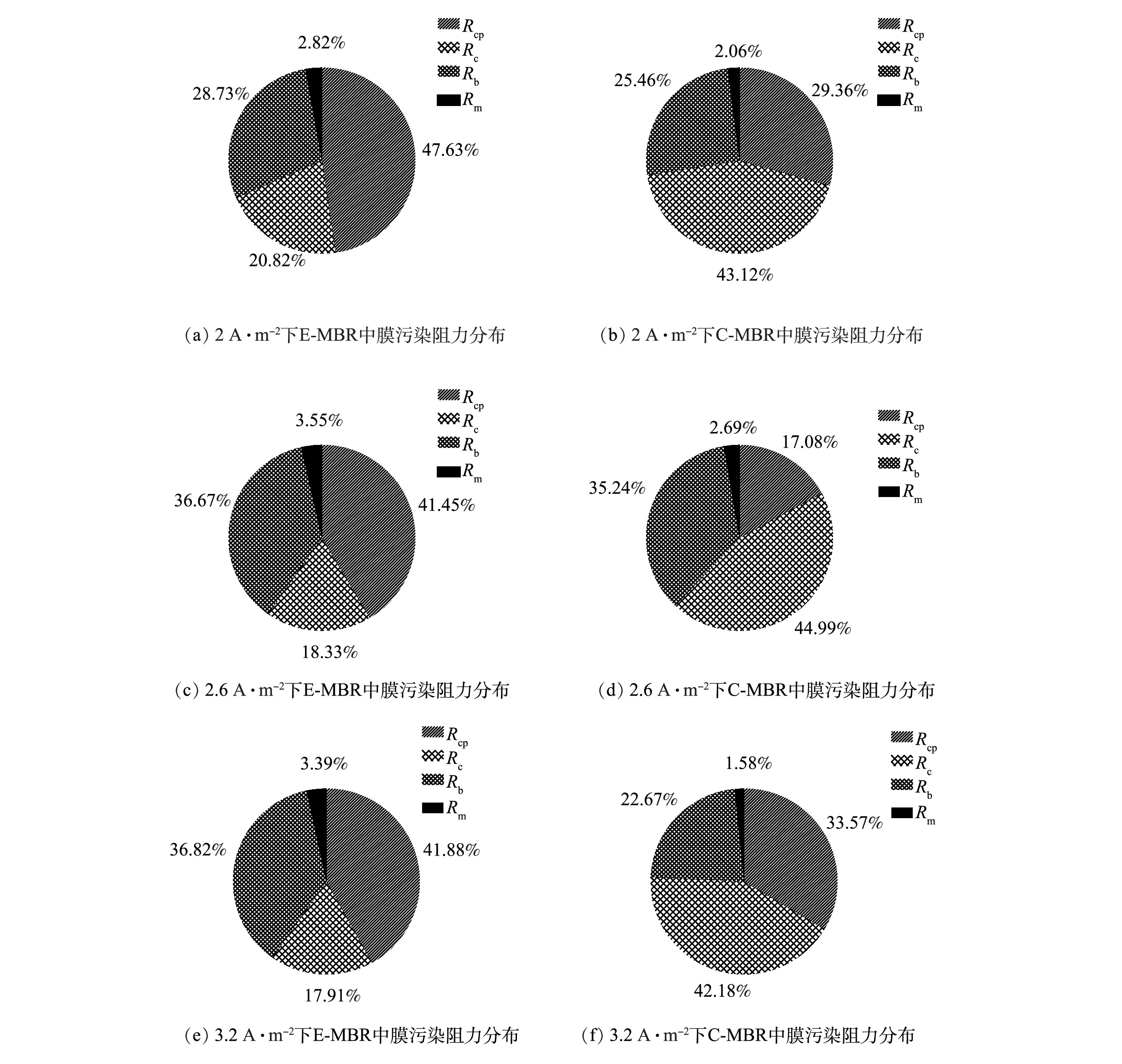
根据Rm,Rcp,Rc以及Rb所占的百分比绘制饼状图,结果如图10所示。电流密度为2 A·m−2时,E-MBR膜面滤饼层阻力占总阻力的20.82%,相比之下C-MBR中Rc占比显著增高,增加至43.12%。电流密度为2.6 A·m−2和3.2 A·m−2时,E-MBR中Rc占比均显著低于C-MBR。这主要是因为:在电场力的作用下,带负电的污泥颗粒和污染物会远离膜面,从而粘附在膜组件表面的污染物质所形成的滤饼层便会少于对照组[33]。同时,对于已经粘附在膜面的污染物质,外加电场会对其产生排斥力,在与C-MBR同等的曝气条件下,E-MBR膜组件表面的污染物质更容易在曝气产生的剪切力作用下脱离膜面。
通过对比3个阶段E-MBR中Rc所占百分比可以看出,随着电流密度的增加,Rc在系统总阻力中所占比例逐渐减少。这与2.3中的2)得到的“电流密度越大,TMP增长越缓慢,膜污染缓解程度越明显”结论一致。
由图10可见,每个电流密度阶段下C-MBR和E-MBR中Rm和Rb占比相当,Rm均保持在2%左右,Rb均保持在30%左右,但是每个阶段下Rcp在2个反应器中的占比相差较大,且均为E-MBR中的Rcp占比大于C-MBR的Rcp占比。有研究表明[34],造成此差异的原因可能为,外加电场可能会引起反应器内混合液中有机物质的增加,从而导致浓差极化阻力在膜污染中所占比例增大。
3. 结论
1)构建了外加电场E-MBR体系,在适宜范围内,当电流密度增大时,依赖于生物降解作用和电氧化作用,COD和NH4+-N的去除效果提升。电流密度进一步增大至3.2 A·m−2时,COD和NH4+-N的去除率降低,这是因为电流密度过大会对MBR中活性污泥的活性产生抑制作用;系统对于TP的去除由于菌种对电场的耐受差异,电流密度增大至3.2 A·m−2时去除磷的微生物活性依旧保持,所以不会降低TP的去除率。
2)对比C-MBR系统,外加电场促进MLSS的升高,且在电流密度为2.6 A·m−2时MLSS增长最快;E-MBR中,污泥粒径更大,且污泥絮体的均匀性提高;E-MBR中污泥的Zeta电位绝对值降低,有利于缓解膜污染。
3)随着电流密度的增大,EPS和SMP中蛋白质和多糖含量显著减少,且始终低于C-MBR系统中的含量。以TMP为判据,电流密度越大,TMP增长越缓慢,膜污染缓解程度越明显。具体分析膜污染阻力的分布可以看出,膜面滤饼层阻力的占比随着电流密度的增大逐渐减少,且E-MBR中Rc占比始终显著低于C-MBR。E-MBR与C-MBR相比能有效缓解膜污染。
-
表 1 终身致癌风险暴露模型参数
Table 1. Parameters for estimating the ICLR values
参数Parameters 少儿Child 青少年Adolescent 成人Adult 呼吸速率IR/(m3·h–1) 1.1±0.07 1.4±0.04 1.5±0.05 暴露时间ET/(h·d–1) 2.5±0.1 1.67±0.1 3.68±0.2 暴露频率EF/(d·a–1) 365 365 365 持续暴露时间ED/a 11 6 53 终身暴露时间AT/d 25550 25550 25550 体重(BW)/kg 19.0±6.28 47.3±7.30 60.8±3.97 CSF/(kg·d–1·mg–1) 3.9±1.8 3.9±1.8 3.9±1.8 表 2 不同国家和地区PAHs肺癌风险的PAF值对比(‰)
Table 2. Comparation of the PAF values in literatures among different countries and regions
国家/地区Country/region 采样点Site 样本数Sample number 采样时间Sampling duration PAHs种类数PAH number PAF均值Averaged PAF value 参考文献Reference 中国 城镇和郊区 — 2003 16 16‰ [2] 中国 城镇和郊区 176 2012-2013 47 8.8‰ [19] 韩国 城镇和郊区 176 2012-2013 47 0.85‰ [19] 日本 城镇和郊区 176 2012-2013 47 0.38‰ [19] 北京 城镇和郊区 10 2013-2014 39 71‰ [20] 晋中 城镇和郊区 10 2013-2014 39 77‰ [20] 合肥 城镇和郊区 6 2019 16 0.78‰ 本研究 中国 郊区 114 2013 16 3.38‰ [21] 表 3 不同国家和地区PAHs肺癌风险的ILCR值对比
Table 3. Comparation of the ICLR values among different countries and regions
国家/地区Country/region 样本数Sample number 采样时间Sampling duration PAHs种类数PAH number ILCR 参考文献Reference 儿童Child 青少年Adolescent 成人Adult 北京 10 2013—2014 39 1.78×10−4 2.01×10−4 3.40×10−4 [21] 太原 16 2009—2010 15 1.74×10−6 — 7.95×10−6 [24] 环渤海 7258 2010—2019 7 2.70×10−5 2.40×10−5 1.88×10−5 [25] 广州 96 2010 16 3.03×10−6 — 2.92×10−6 [26] 合肥 6 2021 16 6.59×10−8 1.23×10−8 1.99×10−7 本研究 巴基斯坦 21 2021 16 1.40×10−5 4.76×10−6 2.58×10−5 [27] 坎普尔 24 2013—2014 16 2.08×10−5 — 3.57×10−5 [28] -
[1] 阿米拉, 耿柠波, 曹蓉, 等. 大气颗粒物中典型有机物的分析方法和污染特征研究进展 [J]. 环境化学, 2021, 40(12): 3774-3786. doi: 10.7524/j.issn.0254-6108.2020081204 A M L, GENG N B, CAO R, et al. Research progress of analytical methods and pollution characteristics of typical organic pollutant in atmospheric particulate matter [J]. Environmental Chemistry, 2021, 40(12): 3774-3786(in Chinese). doi: 10.7524/j.issn.0254-6108.2020081204
[2] ZHANG Y X, TAO S, SHEN H Z, et al. Inhalation exposure to ambient polycyclic aromatic hydrocarbons and lung cancer risk of Chinese population [J]. Proceedings of the National Academy of Sciences of the United States of America, 2009, 106(50): 21063-21067. doi: 10.1073/pnas.0905756106 [3] PETIT P, MAÎTRE A, PERSOONS R, et al. Lung cancer risk assessment for workers exposed to polycyclic aromatic hydrocarbons in various industries [J]. Environment International, 2019, 124: 109-120. doi: 10.1016/j.envint.2018.12.058 [4] HONG W J, JIA H L, MA W L, et al. Distribution, fate, inhalation exposure and lung cancer risk of atmospheric polycyclic aromatic hydrocarbons in some Asian countries [J]. Environmental Science & Technology, 2016, 50(13): 7163-7174. [5] 陈琳钰, 陈仙仙, 何欢, 等. 室内灰尘中多环芳烃及其衍生物的赋存与人体暴露研究进展 [J]. 环境化学, 2021, 40(2): 404-415. doi: 10.7524/j.issn.0254-6108.2020062304 CHEN L Y, CHEN X X, HE H, et al. Occurrence and human exposure of polycyclic aromatic hydrocarbons and their derivatives in indoor dust: A review of recent studies [J]. Environmental Chemistry, 2021, 40(2): 404-415(in Chinese). doi: 10.7524/j.issn.0254-6108.2020062304
[6] SHEN H Z, TAO S, LIU J F, et al. Global lung cancer risk from PAH exposure highly depends on emission sources and individual susceptibility [J]. Scientific Reports, 2014, 4: 6561. doi: 10.1038/srep06561 [7] SHRIVASTAVA M, LOU S J, ZELENYUK A, et al. Global long-range transport and lung cancer risk from polycyclic aromatic hydrocarbons shielded by coatings of organic aerosol [J]. Proceedings of the National Academy of Sciences of the United States of America, 2017, 114(6): 1246-1251. doi: 10.1073/pnas.1618475114 [8] MORADI M, HUNG H, LI J, et al. Assessment of alkylated and unsubstituted polycyclic aromatic hydrocarbons in air in urban and semi-urban areas in Toronto, Canada [J]. Environmental Science & Technology, 2022, 56(5): 2959-2967. [9] 夏冰心, 吉正元, 韩新宇, 等. 玉溪市大气颗粒物中PAHs污染特征与健康风险评估 [J]. 环境化学, 2020, 39(8): 2093-2104. doi: 10.7524/j.issn.0254-6108.2019061002 XIA B X, JI Z Y, HAN X Y, et al. Pollution characteristics and health risk assessment of PAHs in atmospheric particulates in Yuxi City [J]. Environmental Chemistry, 2020, 39(8): 2093-2104(in Chinese). doi: 10.7524/j.issn.0254-6108.2019061002
[10] 董小艳, 王琼, 杨一兵, 等. 2017年春节期间北京市城区和郊区大气PM2.5及其中多环芳烃的污染特征 [J]. 环境化学, 2018, 37(10): 2191-2198. doi: 10.7524/j.issn.0254-6108.2017122503 DONG X Y, WANG Q, YANG Y B, et al. Characterization of ambient PM2.5 and PAHs during 2017 Spring Festival in urban and suburb areas of Beijing [J]. Environmental Chemistry, 2018, 37(10): 2191-2198(in Chinese). doi: 10.7524/j.issn.0254-6108.2017122503
[11] 夏琳琳, 魏建峰, 杨琦玲, 等. 安徽燃煤电厂多环芳烃的历史排放量及影响因素分析 [J]. 环境化学, 2022, 41(8): 2606-2613. doi: 10.7524/j.issn.0254-6108.2021041702 XIA L L, WEI J F, YANG Q L, et al. The historical emissions of polycyclic aromatic hydrocarbons(PAHs)from coal-fired power plants in Anhui and influencing factors [J]. Environmental Chemistry, 2022, 41(8): 2606-2613(in Chinese). doi: 10.7524/j.issn.0254-6108.2021041702
[12] CAI F X, WANG R W, CAI J W, et al. Investigation of the maturation effects on biomarker distributions in bituminous coals [J]. Organic Geochemistry, 2022, 173: 104496. doi: 10.1016/j.orggeochem.2022.104496 [13] WU C C, BAO L J, GUO Y, et al. Barbecue fumes: An overlooked source of health hazards in outdoor settings? [J]. Environmental Science & Technology, 2015, 49(17): 10607-10615. [14] ARMSTRONG B, HUTCHINSON E, UNWIN J, et al. Lung cancer risk after exposure to polycyclic aromatic hydrocarbons: A review and meta-analysis [J]. Environmental Health Perspectives, 2004, 112(9): 970-978. doi: 10.1289/ehp.6895 [15] GIBBS G W. Estimating residential polycyclic aromatic hydrocarbon (PAH) related lung cancer risks using occupational data [J]. The Annals of Occupational Hygiene, 1997, 41: 49-53. [16] WANG S B, JI Y Q, ZHAO J B, et al. Source apportionment and toxicity assessment of PM2.5-bound PAHs in a typical iron-steel industry city in northeast China by PMF-ILCR [J]. Science of the Total Environment, 2020, 713: 136428. doi: 10.1016/j.scitotenv.2019.136428 [17] HONG W J, JIA H L, YANG M, et al. Distribution, seasonal trends, and lung cancer risk of atmospheric polycyclic aromatic hydrocarbons in North China: A three-year case study in Dalian City [J]. Ecotoxicology and Environmental Safety, 2020, 196: 110526. doi: 10.1016/j.ecoenv.2020.110526 [18] WANG G Y, WANG Y, YIN W J, et al. Seasonal exposure to PM2.5-bound polycyclic aromatic hydrocarbons and estimated lifetime risk of cancer: A pilot study [J]. Science of the Total Environment, 2020, 702: 135056. doi: 10.1016/j.scitotenv.2019.135056 [19] 洪文俊. 亚洲五国大气土壤中PAHs分布特征及健康风险评价[D]. 大连: 大连海事大学, 2016. HONG W J. Air and soil distribution, transport and ecological risk of polycyclic aromatic hydrocarbons in five Asian countries[D]. Dalian: Dalian Maritime University, 2016 (in Chinese).
[20] 王蕊. 我国部分地区大气可吸入颗粒物中多环芳烃的初步研究[D]. 乌鲁木齐: 新疆大学, 2015. WANG R. The preliminary study of PM10-bound polycyclic aromatic hydrocarbons during winter and summer in some region, China[D]. Urumqi: Xinjiang University, 2015 (in Chinese).
[21] NIU L L, XU C, ZHOU Y T, et al. Tree bark as a biomonitor for assessing the atmospheric pollution and associated human inhalation exposure risks of polycyclic aromatic hydrocarbons in rural China [J]. Environmental Pollution, 2019, 246: 398-407. doi: 10.1016/j.envpol.2018.12.019 [22] SHEN H Z, HUANG Y, WANG R, et al. Global atmospheric emissions of polycyclic aromatic hydrocarbons from 1960 to 2008 and future predictions [J]. Environmental Science & Technology, 2013, 47(12): 6415-6424. [23] 赵旭辉, 史天哲, 马啸, 等. 江淮地区城市O3污染过程的非典型特征及其前体物来源分析 [J]. 环境化学, 2022, 41(3): 834-849. doi: 10.7524/j.issn.0254-6108.2021062401 ZHAO X H, SHI T Z, MA X, et al. Atypical characteristics of urban O3 pollution process and the source analysis of precursor pollutants in Yangtze-Huaihe Region [J]. Environmental Chemistry, 2022, 41(3): 834-849(in Chinese). doi: 10.7524/j.issn.0254-6108.2021062401
[24] XIA Z H, DUAN X L, TAO S, et al. Pollution level, inhalation exposure and lung cancer risk of ambient atmospheric polycyclic aromatic hydrocarbons (PAHs) in Taiyuan, China [J]. Environmental Pollution, 2013, 173: 150-156. doi: 10.1016/j.envpol.2012.10.009 [25] ZHANG X, WANG X L, ZHAO X L, et al. Using deterministic and probabilistic approaches to assess the human health risk assessment of 7 polycyclic aromatic hydrocarbons [J]. Journal of Cleaner Production, 2022, 331: 129811. [26] WANG W, HUANG M J, KANG Y, et al. Polycyclic aromatic hydrocarbons (PAHs) in urban surface dust of Guangzhou, China: Status, sources and human health risk assessment [J]. Science of the Total Environment, 2011, 409(21): 4519-4527. [27] AAMIR M, YIN S S, LIU Y X, et al. Dietary exposure and cancer risk assessment of the Pakistani population exposed to polycyclic aromatic hydrocarbons [J]. Science of the Total Environment, 2021, 757: 143828. doi: 10.1016/j.scitotenv.2020.143828 [28] SINGH D K, GUPTA T. Effect through inhalation on human health of PM1 bound polycyclic aromatic hydrocarbons collected from foggy days in northern part of India [J]. Journal of Hazardous Materials, 2016, 306: 257-268. doi: 10.1016/j.jhazmat.2015.11.049 -




 下载:
下载: