-
四环素(TC)常被用作饲料添加剂应用于畜牧业及水产养殖业[1-2],因在动物体内吸收率较低,常以原药和代谢产物的形式随粪尿排出体外,造成水体及土壤环境污染[3]. 目前,常规的处理工艺无法有效去除废水中抗生素,因此导致TC能够在不同的水源甚至饮用水中被检测到[4-5]. TC在地表水中的浓度可达μg∙L−1级别[6],尽管浓度较低,但同样能增强细菌耐药性,从而对生态环境和人类健康造成潜在威胁[7-8].
地表水中的可溶性有机物可通过光化学反应产生H2O2[9],而水体中H2O2与有机污染物的氧化还原反应有密切关系,能够影响化学物质的降解转化和生态效应[10]. 水中的Cu2+、Fe2+等过渡金属离子可催化H2O2分解为∙OH(E0=2.80 V)[11],而自然水体的沉淀物中广泛存在过渡金属氧化物,能够缓慢的释放出金属离子催化H2O2产生活性物质形成类Fenton反应降解水中有机物[12]. 水合氧化铁(HFO)广泛分布于沉积物和土壤中[13],具有很强的亲水性、较高的表面羟基密度和电子传输[14] 等特性. 现有关于HFO对水中污染物的去除研究多集中于吸附作用方面[15-16],鲜有关于水合氧化铁在水环境中催化H2O2降解抗生素污染物方面的报道.
本研究以HFO为材料,模拟其催化H2O2降解TC反应过程,优化反应条件并探索HFO/H2O2体系的潜在氧化机制,同时采用超高效液相色谱串联质谱(LC-TOF-MS/MS)的分析结果,鉴定TC代谢转化产物并提出了TC可能的降解途径. 研究结果可为探讨自然水体中HFO催化降解TC提供理论参考,也可为含TC废水处理提供技术支撑.
-
盐酸四环素纯度>98%,购自于上海源叶生物科技有限公司;六水合氯化铁(FeCl3∙6H2O),分析纯,购自于天津市科密欧化学试剂有限公司;过氧化氢(H2O2),质量分数30%,购自于上海沃凯生物技术有限公司;乙腈和甲醇,色谱级,购自于美国Merck公司;氢氧化钠、盐酸、苯醌、硫代硫酸钠、叔丁醇等均为分析纯,购自于西陇化工股份有限公司;实验用水均为超纯水.
-
水合氧化铁(HFO)的制备方法参考文献 [17] 并做修改,在磁力搅拌下,将10.0 g的FeCl3∙6H2O溶解在100 mL超纯水中,然后用1 mol∙L−1的NaOH溶液将FeCl3∙6H2O溶液的pH值调至7.0. 形成的悬浮液连续搅拌1 h,并在室温下陈化24 h,然后通过离心(4500 r·min−1,5 min)法收集沉淀的水合氧化铁颗粒,然后用超纯水洗涤3次,去除残留离子. 最后,将水合氧化铁冷冻干燥,在玛瑙研钵中研磨,并通过200目筛,收集并存储在棕色玻璃瓶中备用.
-
ESCALAB 250Xi 型X-射线衍射仪测试样品的X射线衍射(XRD)谱图; Tristar II 3020M全自动比表面积和孔隙分析仪测定样品的比表面积和孔径; JES-FA200电子顺磁共振波谱仪(EPR)测试反应体系中产生的自由基种类; Nicolette iS50傅立叶红外-拉曼光谱仪测试样品红外光谱(FTIR); Cary Eclipse荧光分光光度计测试样品的三维荧光光谱(3D EMM).
-
配制50 mL初始pH6.5的四环素溶液(40 mg∙L−1),分别加入HFO、H2O2和HFO/H2O2(其中HFO为20 mg,H2O2为5 mmol∙L−1),在25 ℃的水浴温度下以150 r∙min−1速率震荡,反应一定时间后取样,样品用0.2 mol∙L−1的硫代硫酸钠溶液(甲醇:水 体积比为 1:1)稀释1倍,终止反应,样品经10000 r∙min−1离心10 min后取上清液过0.22 μm水相滤膜过滤后用UPLC测定.
探讨H2O2浓度的影响,将实验中H2O2浓度分别设置为0、0.5、1、2、5、10 mmol∙L−1;探讨初始pH影响时用0.1 mol∙L−1的NaOH或HCl调节溶液pH值分别为2、3、5、6.5、9、10;比较共存离子的影响时在HFO/H2O2反应体系中分别添加25 mmol∙L−1和50 mmol∙L−1的不同离子(Na+、Ca2+、Mg2+、
NO−3 、HCO−3 、SO2−4 ). -
为研究催化反应体系中的活性氧种类,分别使用叔丁醇(TBA)和苯醌(BQ)作为羟基自由基(∙OH)和超氧自由基(∙O2-)的抑制剂,采用电子自旋共振谱(EPR)验证体系中∙OH和∙O2-,∙OH和∙O2-自由基的捕获剂是100 mmol∙L−1 DMPO.
-
使用Waters UPLC-VWD型超高效液相色谱检测溶液中TC. 色谱柱为ACQUITY UPLC BEH C18反相柱(100 mm × 2.1 mm i.d.,1.7 μm),检测波长为254 nm,进样量为10 μL,柱温40 ℃,流动相A为1‰甲酸,流动相B为乙腈. 梯度设置:95.0% A(0 min)、5.0% A(2.5 min)、95.0% A(3.51 min)、95.0% A(5 min),流速为0.30 mL∙min−1.
-
式中,C0和Ct分别代表四环素的起始质量浓度和t时刻的质量浓度,单位mg∙L−1.
所有数据均以3次重复的平均值±标准偏差表示,并使用Origin 8.5绘制数据. 使用SPSS 21.0软件对数据进行统计分析.
-
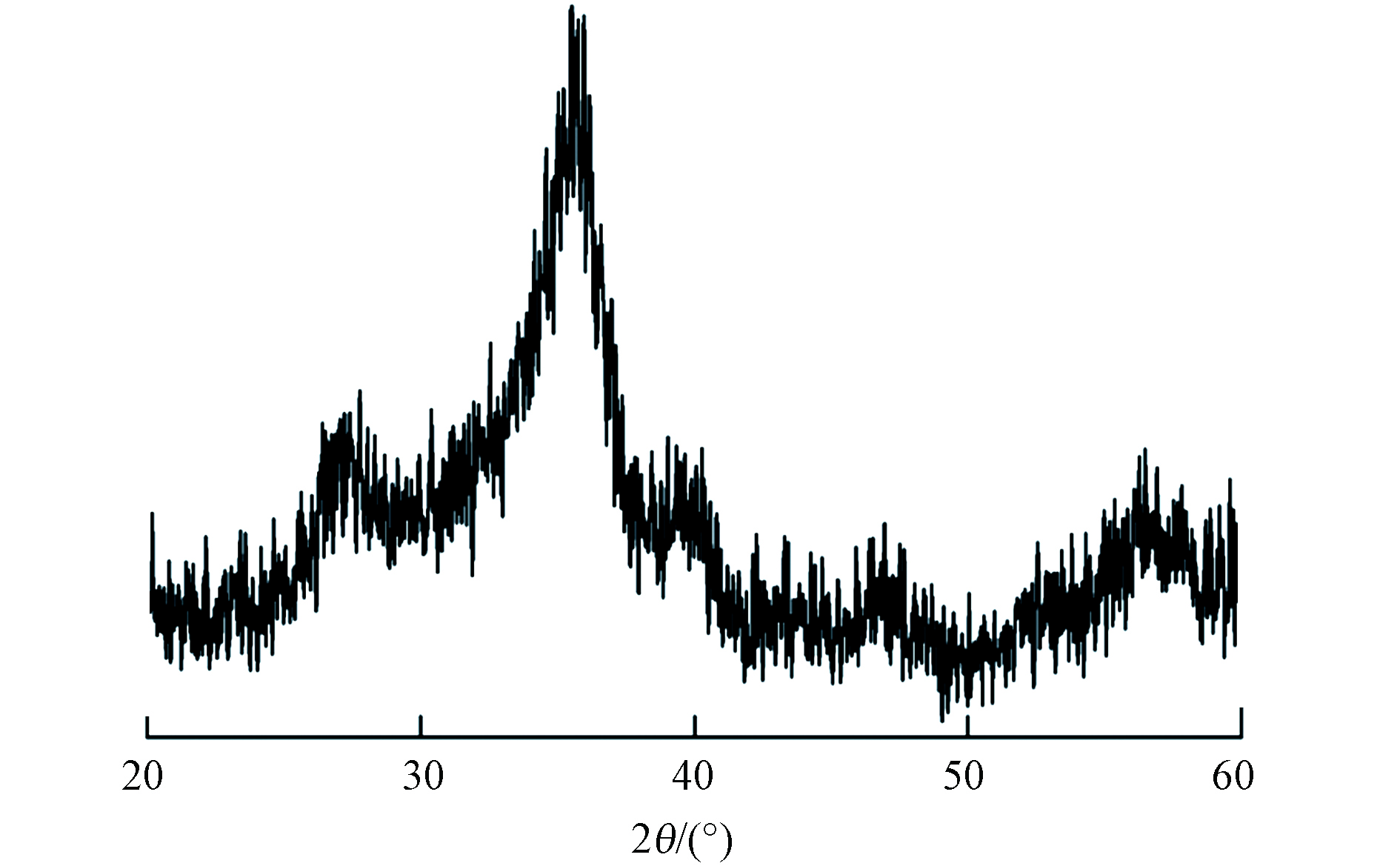
HFO的XRD图谱如图1所示. 图1中未出现较强的衍射特征峰,这表明水合氧化铁不具有晶体结构. 水合氧化铁在36.4º处出现1个宽峰,出峰位置与水铁矿相似 (JCPDS No. 29-0712)[18] ,表明合成的水合氧化铁为无定形铁氧化物.
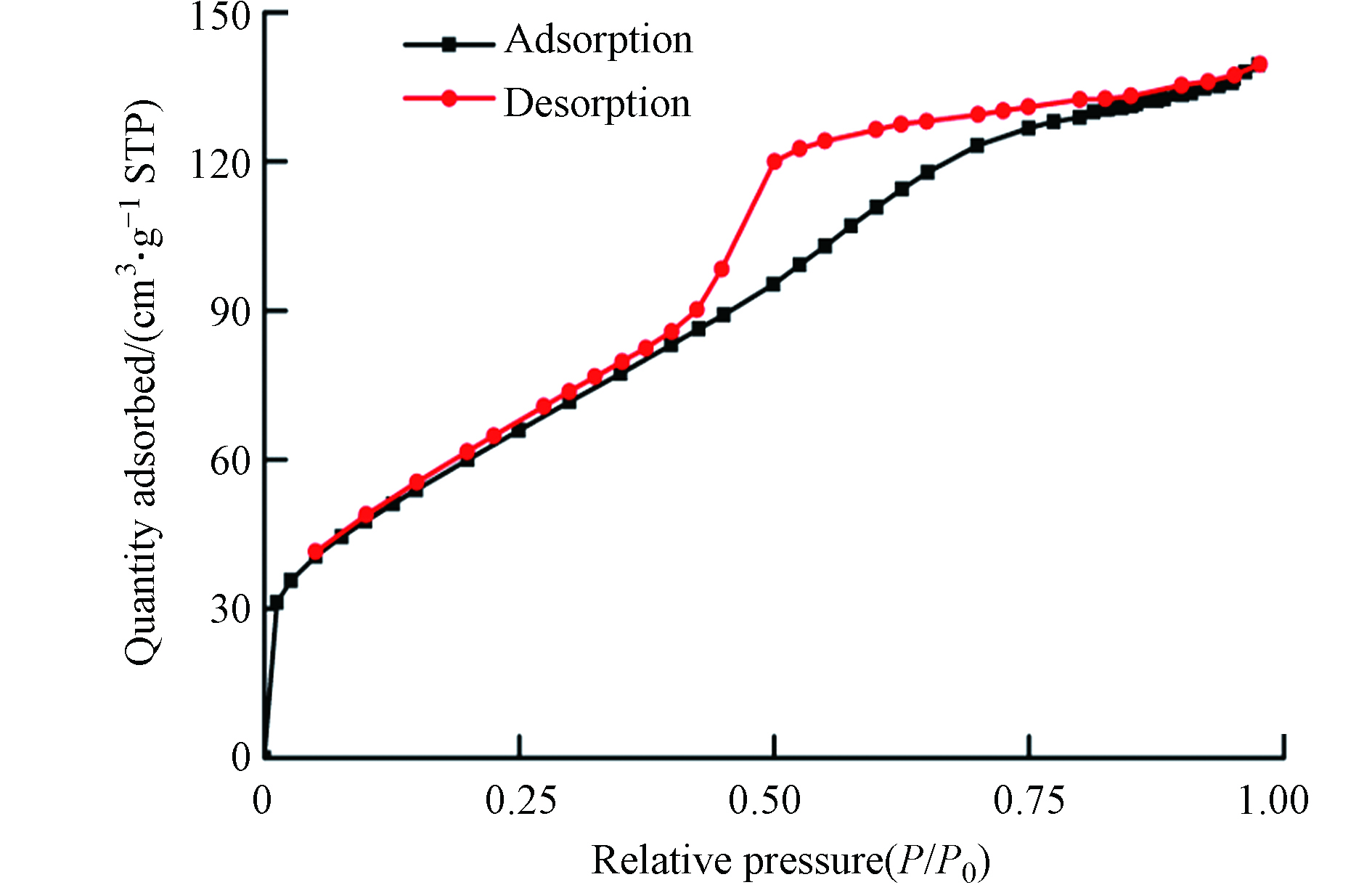
HFO的氮气吸附解吸曲线如图2所示. HFO的N2吸附-脱附曲线属于V型等温线并具有H4型滞后回环,表明合成的样品中主要存在的是介孔结构[19]. 水合氧化铁的比表面积,孔体积和孔径分别为226.796 m2∙g−1、0.167 cm3∙g−1和3.495 nm. 由上述数据可知,水合氧化铁的孔隙结构较为发达,拥有较高的比表面积,可提供更多的Fe活性位点,有利于催化H2O2降解污染物.
-
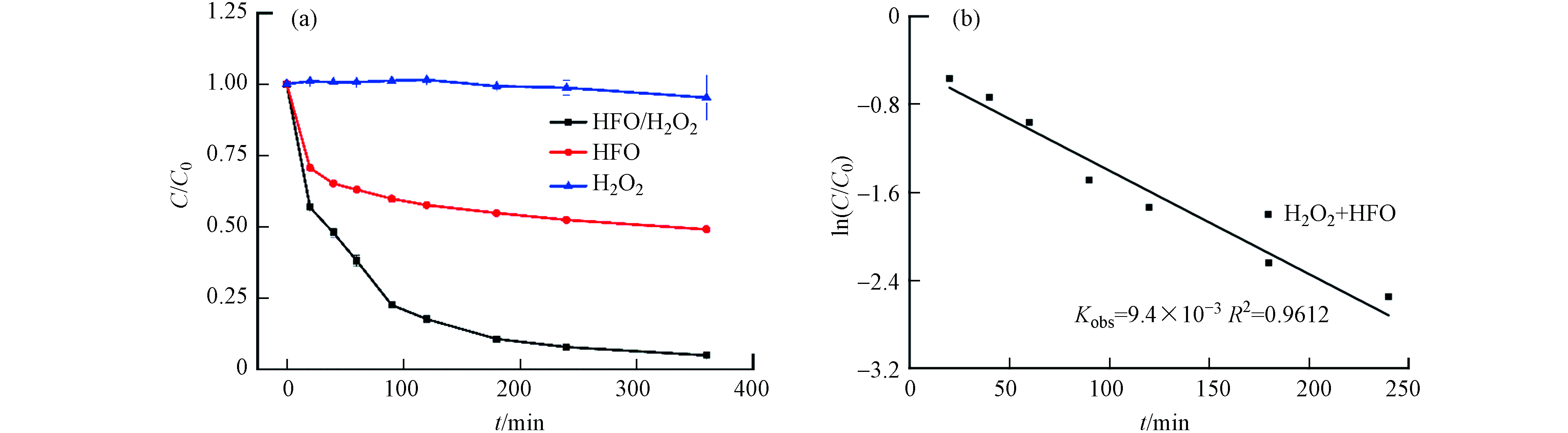
不同反应体系(H2O2、HFO和H2O2/HFO)下TC的降解动态如图3(a)所示. 当H2O2单独存在时,0—6 h内TC浓度几乎不变,这表明仅仅使用H2O2难以直接降解TC. 单独加入HFO时,四环素去除率为54%. 这可能是因为催化剂和TC发生了吸附反应. 在H2O2/HFO体系下,TC的去除率可达97%,这表明HFO可有效地催化H2O2氧化降解TC. 在实验中采用拟一级动力学拟合HFO/H2O2体系的降解数据,如图3(b)所示,与该模型相对吻合(R2>0.9),相对应的表观速率常数为9.4×10−3 min−1,这表明HFO可以有效催化激活H2O2生成自由基,促进TC的降解.
-
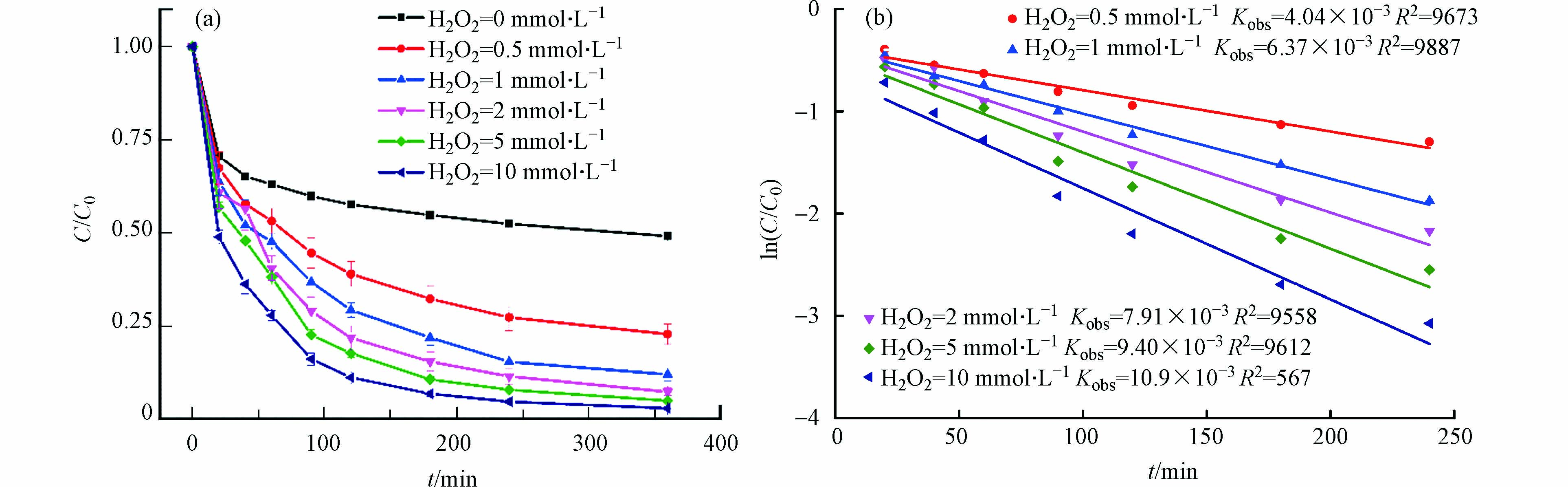
H2O2浓度会直接影响自由基的生成,进而影响TC的降解效率[20]. 不同H2O2浓度对TC降解的影响见图4.
H2O2的浓度从0 mmol∙L−1增加到10 mmol∙L−1时,TC的去除率从54%增加到98%. 采用拟一级动力学模型拟合HFO催化不同浓度H2O2降解四环素的过程,结果见图4(b). 当H2O2的浓度从0.5 mmol∙L−1增加到10 mmol∙L−1时,其相对应的表观速率常数从4.04×10−3 min−1增加到10.9×10−3 min−1,这表明随着H2O2浓度增加促进了TC的降解速率. 这主要是由于随着H2O2浓度的增加,HFO能够催化H2O2产生更多的自由基降解TC.
-
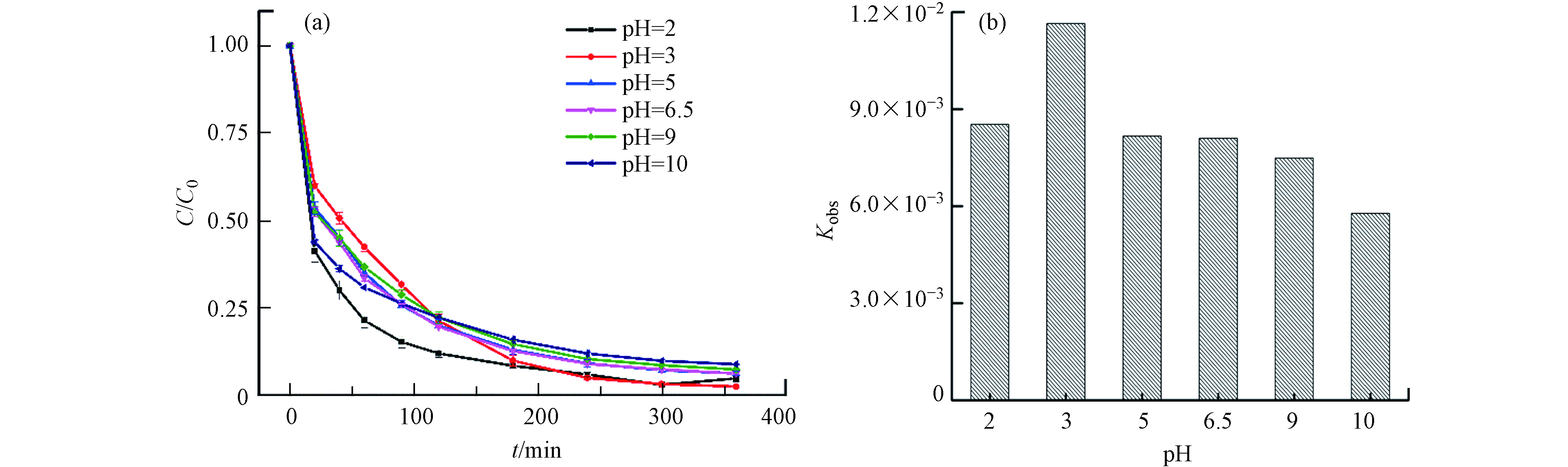
溶液初始pH值对TC降解速率的影响如图5所示,在酸性条件下,TC具有更高的降解速率和去除率. 这可以归因于,在酸性条件下,HFO催化剂表面更容易溶解出Fe(Ⅱ)和Fe(Ⅲ)催化H2O2生成自由基降解TC. 由图5(a)可知,初始pH值在2—10之间时催化剂对TC都具有良好的降解效果,降解效率都在90%之上. 可见HFO催化H2O2对TC的降解有着较好的pH适应性.
-
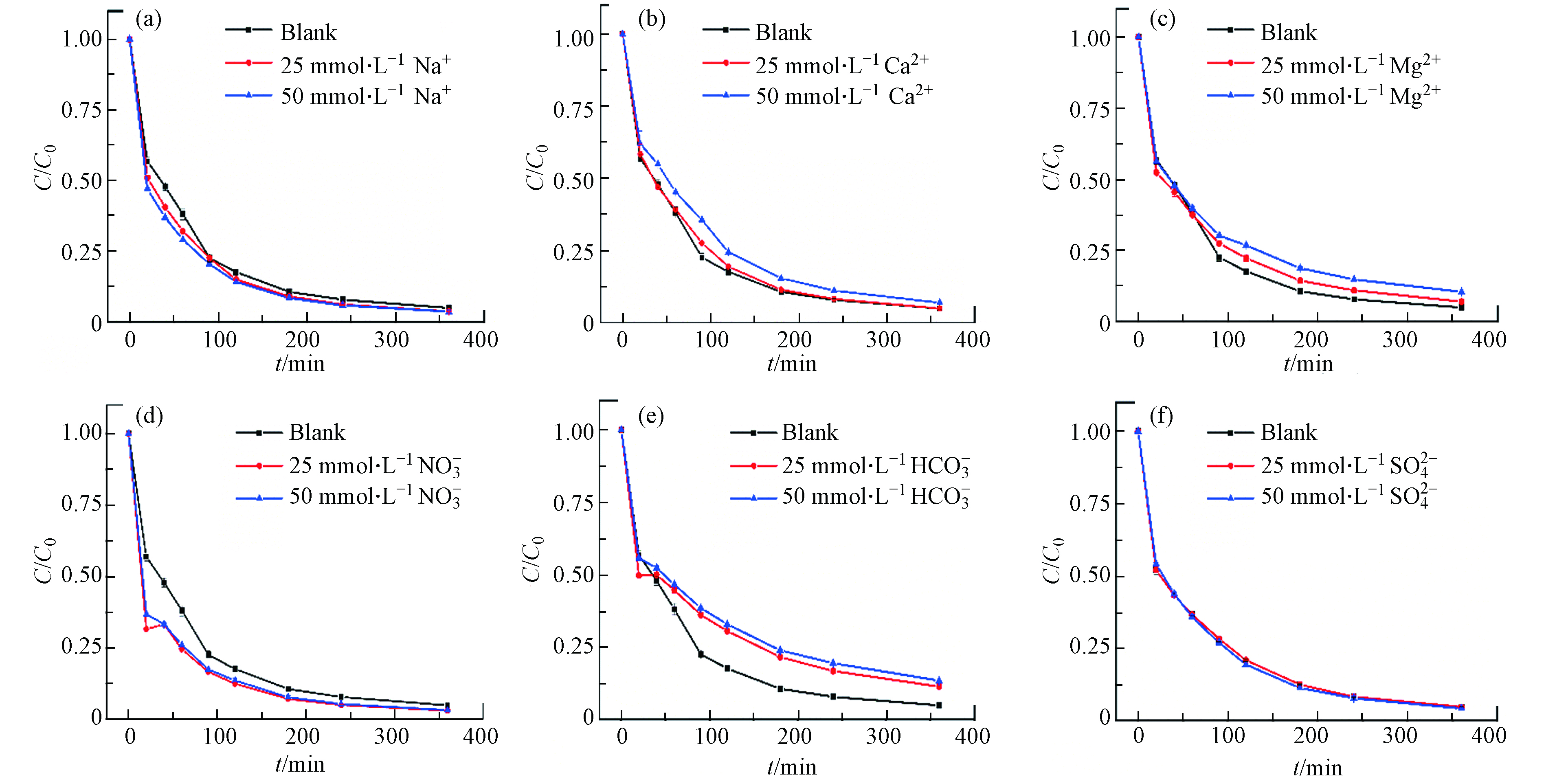
由于在实际水体中含有大量的阴离子和阳离子,因此在实验中研究了共存Na+、Ca2+、Mg2+、
NO−3 、HCO−3 、SO2−4 等离子对HFO催化H2O2降解TC的影响. 各共存离子对HFO催化H2O2降解四环素的影响结果如图6所示.Na+、Ca2+、
NO−3 和SO2−4 浓度在25 mmol∙L−1和50 mmol∙L−1时,对HFO催化H2O2降解TC基本没有影响. 由图6(c)和(e)可以观察到,Mg2+和HCO−3 会降低HFO催化H2O2降解TC的降解率,这可能是由于Mg2+与TC竞争吸附位点从而影响TC的去除[21],而HCO−3 与HFO/H2O2体系中的自由基发生反应以生产氧化还原电位较低的HCO−3 ∙和CO−3 ∙,从而抑制TC的降解. -
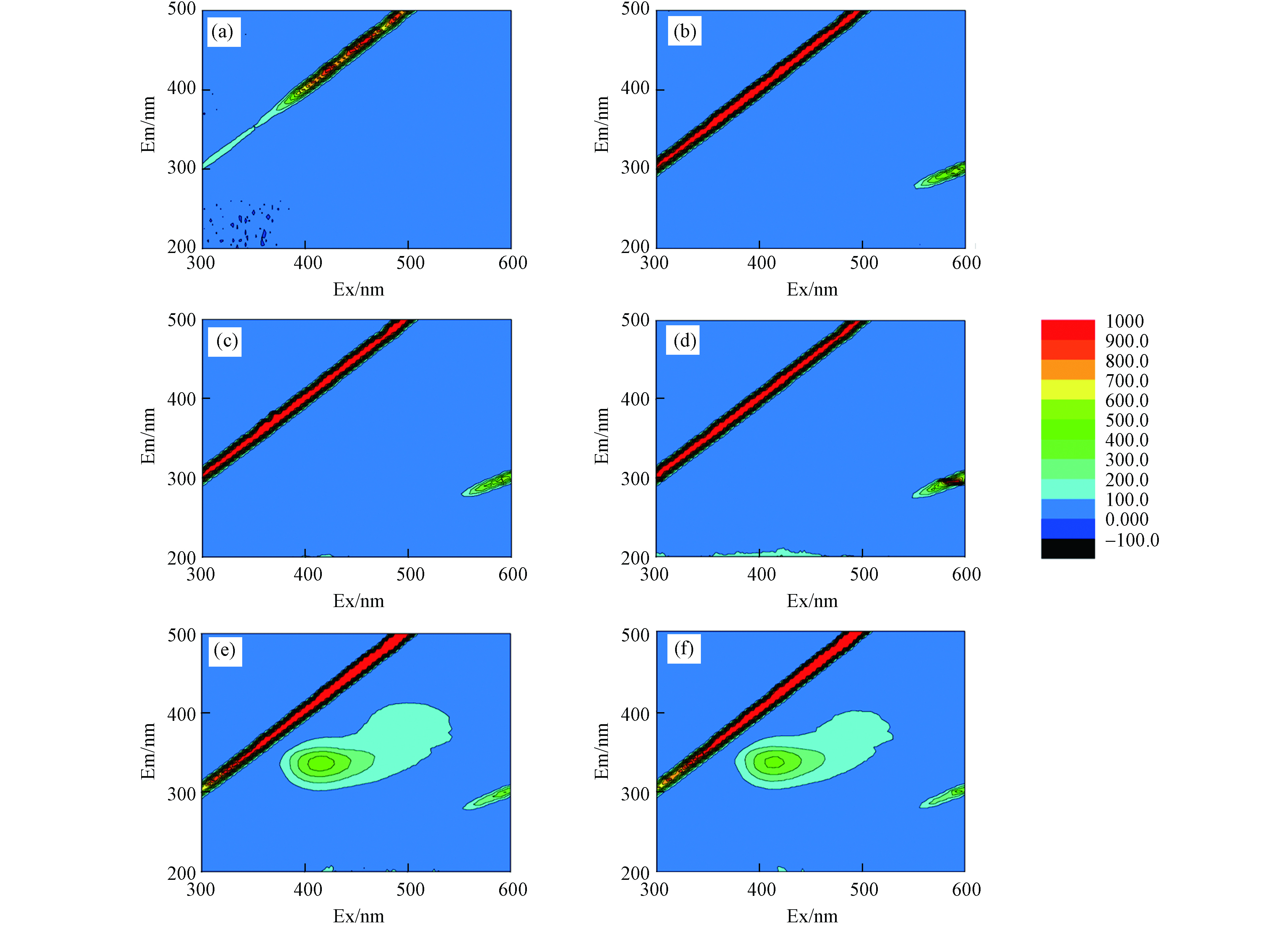
采用荧光光谱技术检测分析了四环素在不同体系(TC、H2O2/TC、HFO/TC和H2O2/HFO/TC)反应后的三维荧光特征及其指纹特征. 在实验中收集了6个样品(M1-M6),M1:初始TC溶液的三维荧光光谱、M2:HFO/TC体系在黑暗中振荡6 h后,离心取上清液测定的三维荧光光谱、M3:H2O2/TC体系在黑暗中震荡4 h后,离心取上清液测定的三维荧光光谱、M4:H2O2/TC体系在黑暗中振荡6 h后,离心取上清液测定的三维荧光光谱、M5:HFO/H2O2/TC体系在黑暗中震荡4 h后,离心取上清液测定的三维荧光光谱、M6:HFO/H2O2/TC体系在黑暗中振荡6 h后,离心取上清液测定的三维荧光光谱. M1-M6的三维荧光如图7所示.
Shi等 [22] 研究表明在三维荧光中,TC的存在会起到荧光淬灭作用. 如图7(a)、(b)、(c)和(d)所示,在TC、HFO/TC和H2O2/TC体系中均未检测到荧光信号,这表明在TC、HFO/TC和H2O2/TC体系中TC分子均没有被完全去除. 由图7(e)和(f)可知,在HFO/H2O2体系中,出现了一个对应于类腐殖酸区域的荧光峰(λEX/λEM=(305—330 nm)/(430—450 nm) )[23],且峰强度随着反应的进行而减弱,表明TC及其降解产物在HFO/H2O2体系中不断被降解.
-
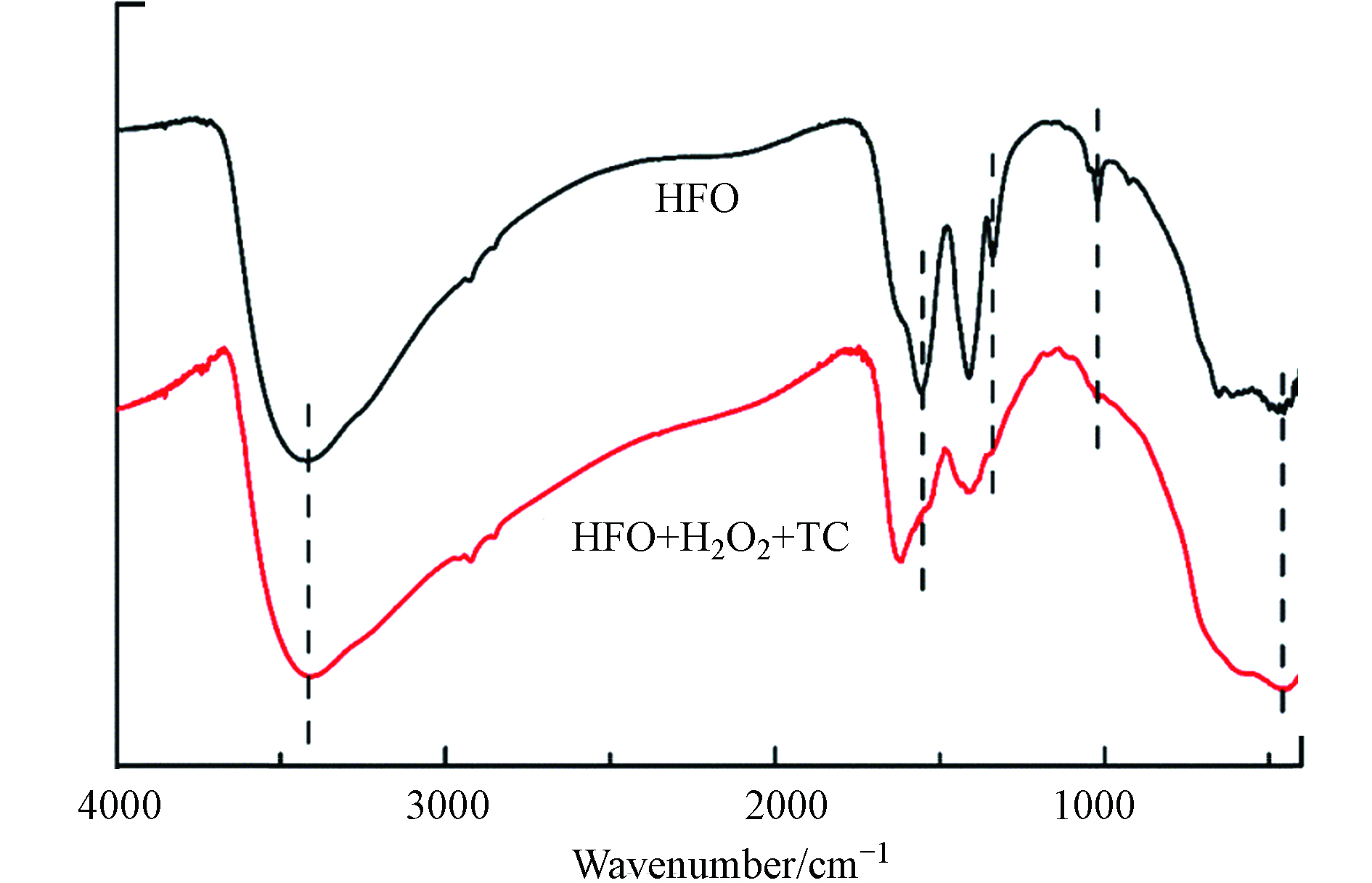
图8为HFO在催化反应前后的FTIR图谱. 由图8可知,HFO的红外光谱中出现了—OH(3405 cm−1、1629 cm−1)这表明了羟基的存在. 444 cm−1处为Fe—O键伸缩振动峰,1023 cm−1处为Fe—OH键伸缩振动峰[24]. HFO在催化过程中,Fe—O的出峰位置从444 cm−1迁移到463 cm−1,Fe—OH的吸收峰消失,这表明Fe—O和Fe—OH官能团参与了催化作用. 在3405 cm−1处的羟基伸缩振动峰移至3416 cm−1,这表明在催化反应过程中羟基参与了反应.
-
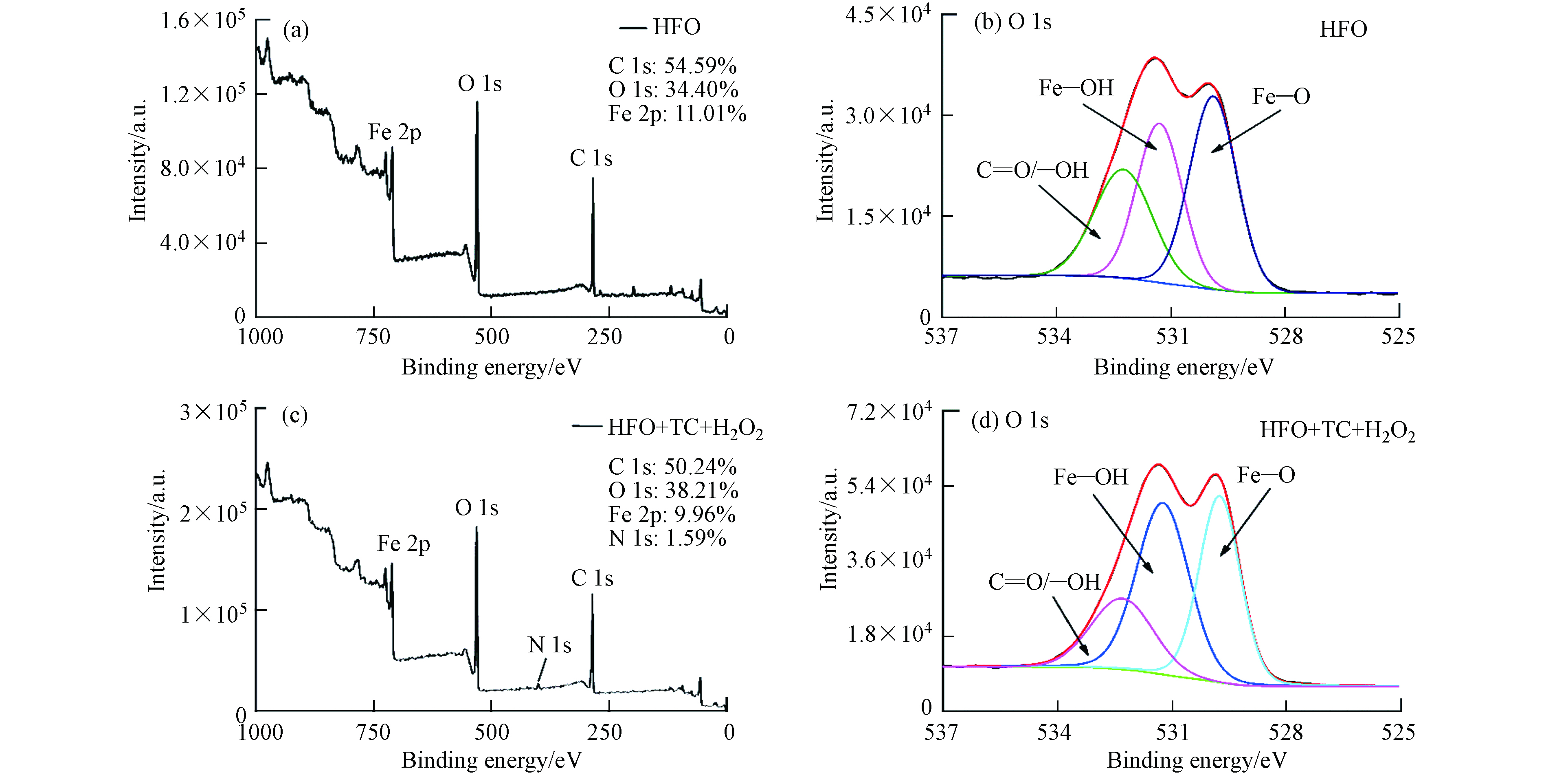
图9为HFO催化反应前后的XPS分析结果. 由图9(a)和(c)可知,HFO的全扫描能谱中出现了C 1s、O 1s和Fe 2p的3个能区,而HFO催化后的全扫描能谱中出现了C 1s、O 1s、Fe 2p和N1s的4个能区,这表明HFO在催化过程中吸附了一定量的TC及其降解产物. 图9(b)和(d)为HFO催化前后O 1s的高分辨扫描能谱,其中530 eV、531 eV和532 eV处的3个主峰分别对应Fe—O、Fe—OH和C=O/OH的结合能[25]. 其中催化后Fe—OH峰面积从32%增加值43%,Fe—O的峰面积从40%降低到37%,这表明HFO在催化过程中部分Fe—O官能团转变成Fe—OH官能团,铁主要分布在HFO的表面.
-
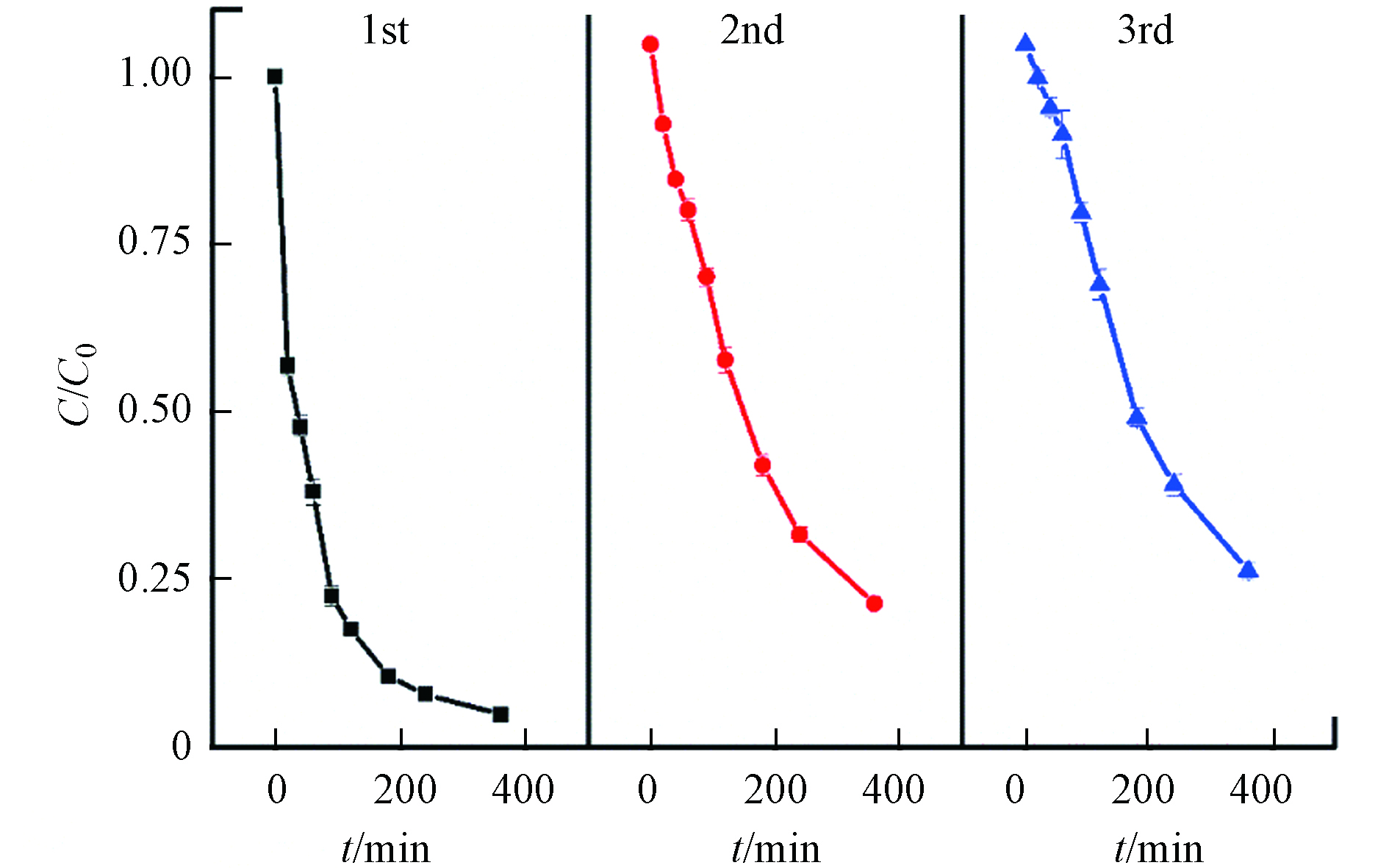
催化剂的稳定性和可重复利用性对其在实际应用中至关重要. 通过连续反应3次循环实验评估HFO在黑暗处催化H2O2降解TC的效率,以验证HFO的可重复利用性,结果如图10所示. 经过3次循环实验后,在360 min内对TC的降解速率逐渐降低,表明HFO上的某些催化活性位点可能会随Fe的浸出而损失[26]. HFO经历3次循环后,TC在360 min内的去除率分别为95%、80%和75%. 因此,在HFO/H2O2具有可重复应用的潜力.
-
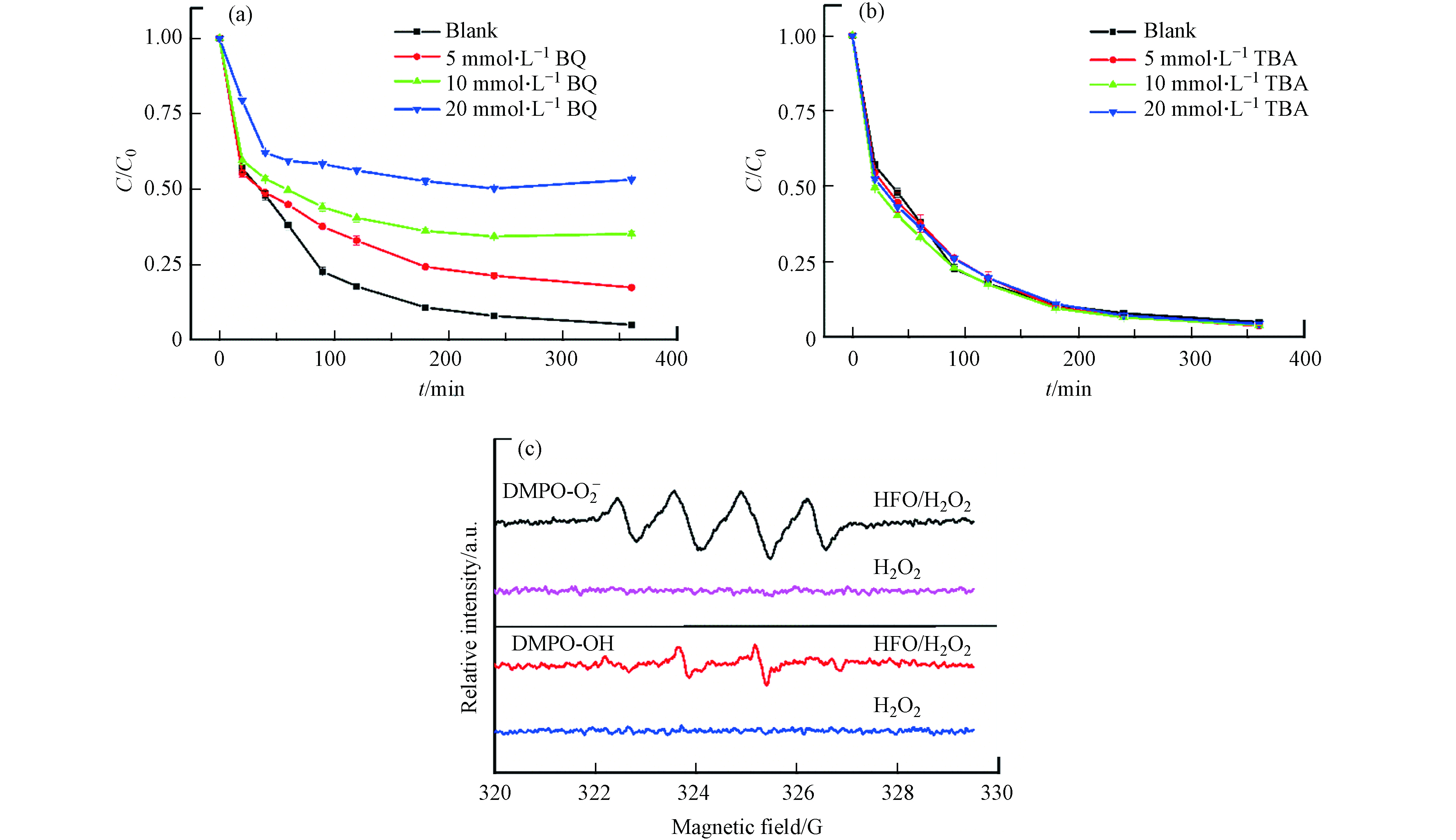
通过自由基淬灭实验和电子自旋共振波谱仪测定反应体系中的主要自由基. 在淬灭实验中分别使用苯醌(BQ)和叔丁醇(TBA)对类Fenton反应过程中产生的∙O2-和∙OH进行淬灭[27]. 如图11(a)所示,当反应溶液中分别添加5、10、20 mmol∙L−1的苯醌时,在360 min内,TC的降解率从95%分别下降到82%、64%和46%. 但是当添加5、10、20 mmol∙L−1的叔丁醇时,在360 min内,TC的降解率几乎没有下降,说明HFO/H2O2反应体系中产生的主要活性物质是∙O2-[28].
为了进一步确认反应机理,通过EPR检测反应体系中的活性物质,采用DMPO作为∙OH和∙
O−2 的捕获剂[29]. 由图11(c)可知,单独的H2O2并未产生DMPO-∙O−2 信号峰和DMPO-∙OH信号峰. 而在HFO/H2O2反应体系中,发现明显的DMPO-∙O−2 信号峰. 以上结果表明,HFO/H2O2体系降解四环素的主要活性物种是∙O−2 . -
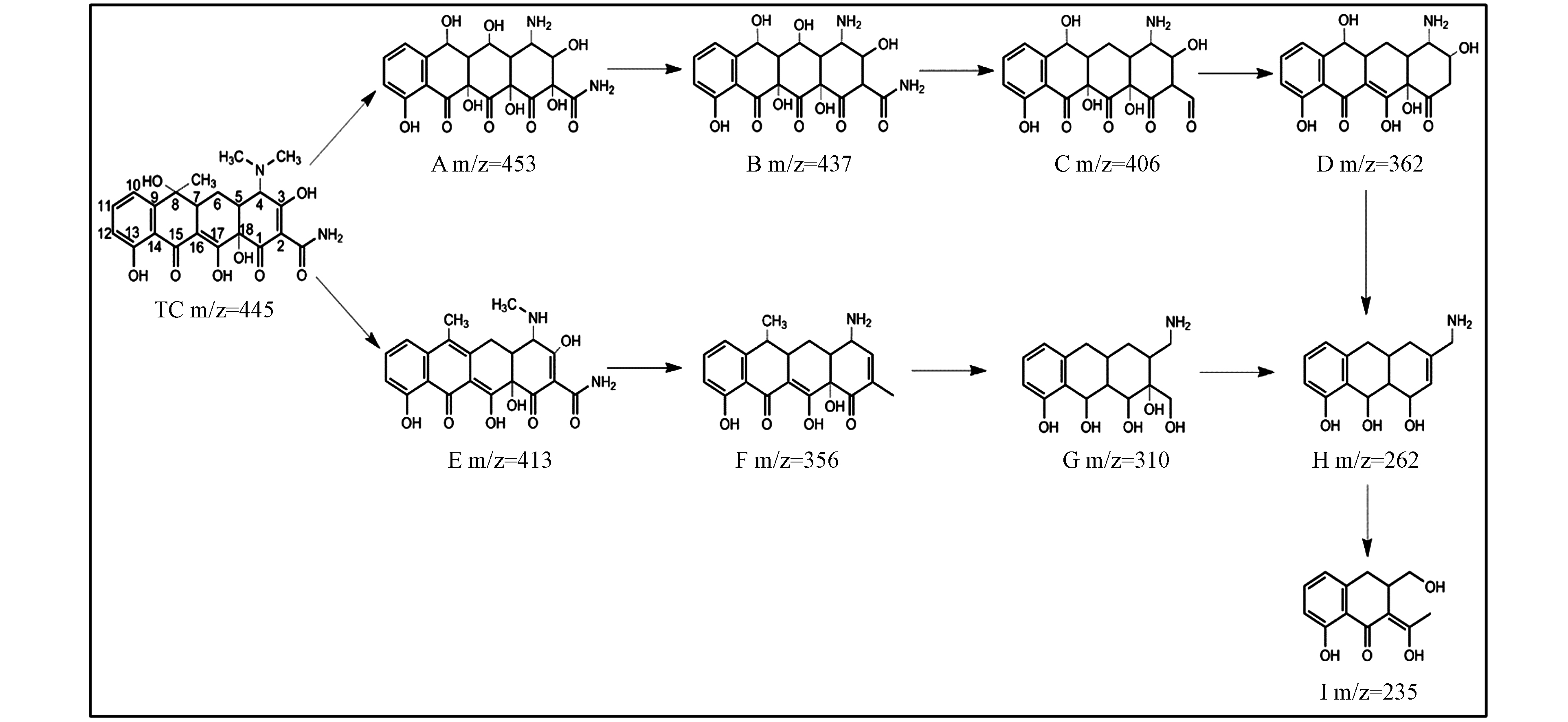
利用LC-TOF-MS共检测到9种TC的中间降解产物,质荷比(m/z)分别为:A(m/z=453)、B(m/z=437)、C(m/z=406)、D(m/z=362)、E(m/z=413)、F(m/z=356)、G(m/z=310)、H(m/z=262)和I(m/z=235). 根据分子量、理论分子量和文献报道,推测HFO/H2O2降解TC中间产物的结构和反应路径如图12所示.
TC降解途径Ⅰ,TC上碳碳双键羟基化,生成产物A(m/z=453)[30],通过A脱羟基形成产物B(m/z=437),通过C—N键断裂和脱羟基形成产物C(m/z=406),通过去甲基化作用将产物 C 进一步转化为产物 D(m/z =362)[31],通过开环、去甲基化和去羟基将产物D转化为产物H(m/z=262),然后产物H通过开环和加羟基化为产物I(m/z=235)[32],最后产物I被转化为小分子物质并进一步氧化为H2O和CO2. 降解途径Ⅱ,TC去甲基和羟基生成产物E(m/z=413)[33],通过E去甲基、脱羟基和NH2形成产物F(m/z =356),F通过开环和C=C双键的氢加成变成产物G(m/z=310),G通过脱C18上的羧基(—C—OH)和羟基生产H(m/z=262),最后再进一步通过开环和加羟基化为产物I(m/z=235)[32],最后产物I被转化为小分子物质并进一步氧化为H2O和CO2.
-
HFO/H2O2体系在H2O2的浓度为5 mmol∙L−1,催化剂为0.4 mg∙L−1,pH=3,温度25 ℃的反应条件下可在180 min内去除水中90%的TC. 在pH为2—10的范围内和共存离子存在时,HFO都可有效的催化H2O2降解水体中的TC,HFO/H2O2体系降解TC的主要活性物质是∙O2-. TC降解过程中出现了9种中间产物,说明TC主要是通过羟基化、去甲基、去酰胺基和开环等途径被降解成小分子化合物. 本研究揭示了HFO对TC催化降解作用,说明自然界存在的HFO在TC降解和代谢过程中起到重要作用.
水合氧化铁催化类Fenton反应降解水中四环素
Degradation of tetracycline in aqueous solution via a Fenton-like reaction catalyzed by hydrous ferric oxide
-
摘要: 环境中抗生素污染及其降解过程是当前研究的热点问题,为探讨自然过程中铁氧化物(水合氧化铁,HFO)在氧化剂(过氧化氢,H2O2)存在条件下对四环素(TC)的降解作用及TC代谢途径,采用湿沉淀法合成HFO,研究了其催化H2O2高效降解水中TC的效果,同时通过X射线衍射(XRD)、N2吸附-脱附、光电子能谱仪(XPS)、傅立叶红外-拉曼光谱仪(FTIR)等手段对样品进行了表征,阐明了HFO催化H2O2降解TC的机理. 结果表明,HFO具有介孔结构,HFO/H2O2体系可在180 min内去除水中90%的TC,3次连续循环后去除率保持75%,表现出良好的催化活性和稳定性;HFO在催化过程中部分Fe—O官能团转变成Fe—OH官能团,∙
O−2 为主要活性物质;TC降解过程中出现9种中间产物,说明TC主要是通过羟基化、去甲基、去酰胺基和开环等途径被降解成小分子化合物.-
关键词:
- 水合氧化铁 /
- 非均相Fenton反应 /
- 四环素 /
- 降解途径
Abstract: Antibiotic pollution in the aquatic environment and the degradation pathways of antibiotic has become a hot topic. Hydrous ferric oxide (HFO) was synthesized by wet precipitation method to simulate the catalytic degradation of tetracycline (TC) with H2O2. The physicochemical properties of the HFO were characterized by XRD, N2 adsorption-desorption isotherm, XPS, and FTIR to explore the degradation mechanism. The results showed that HFO exhibited a mesoporous structure. The removal rate of TC in HFO/H2O2 system within 180 min reached 90%, and the degradation rates of TC remained 75% after 3 cycles. The main active species of HFO/H2O2 system was ·O−2 , which was confirmed by electron spin resonance (ESR) analysis and radical trapping experiments. Nine intermediate products were identified via the liquid chromatography tandem mass spectrometry (LC-TOF-MS) analysis during TC degradation process which indicated that hydroxylation, demethylation, deamidate and break of benzene ring were the main pathways for the degradation of TC. -
造成环境空气污染的主要挥发性有机化合物中,以苯、甲苯、乙苯、二甲苯等为首的苯系物因其熔沸点较低,极易挥发,且具有对人体健康的致癌和非致癌危害而备受关注[1]. 环境空气苯系物主要源于工业生产、装修材料、燃料排放、垃圾和废弃物等[2-4],在人体内累积易导致呼吸系统、血液系统、生殖系统和神经系统疾病,长期接触致癌物苯、乙苯甚至会导致严重疾病,如淋巴瘤、白血病等[5-6]. 再生塑料颗粒以废弃的塑料制品为原料加工而成,因其在经济、技术和环境友好性上的可替代性[7-8],使人们逐步将再生塑料颗粒作为主要的加工原料. 其生产过程中的苯系物污染,主要源于各类增塑剂、阻燃剂等有机溶剂[9-11]. 针对苯系物对人体的危害,已有学者评估了高剂量的苯系物在室内环境、家具制造、大气污染、职业暴露等方面的健康风险[12-15],对塑料制品中添加剂对人体的健康影响也有一定研究[16-18]. 低剂量的苯系物在非职业暴露下可能存在健康风险[19,20],因而低剂量苯系物对作业人员的健康风险逐渐成为关注热点[21-23]. 有学者针对消费品和工业产品进行了基于暴露场景假设的特定暴露源苯系物健康风险评估研究[24-26],由于生产需求,从事再生塑料颗粒加工的作业人员对塑料颗粒这一特定暴露源的直接接触不可避免,并且是一个长期、稳定,并伴随作业人员整个职业周期的过程,因此,需要关注从再生塑料颗粒中挥发的苯系物对作业人员的健康风险.
本文采集市面上25种以聚丙烯 (polypropylene, PP)、高密度聚乙烯 (high density polyethylene, HDPE)、丙烯腈-丁二烯-苯乙烯共聚物 (acrylonitrile butadiene styrene, ABS)、高抗冲击聚苯乙烯(high impact polystyrene, HIPS)、聚酰胺 (polyamide, PA)为主要成分的再生塑料颗粒,检测并分析8种苯系物(苯、甲苯、乙苯、对二甲苯、间二甲苯、邻二甲苯、苯乙烯、异丙苯)的挥发浓度. 根据美国环境保护署 (United States Environmental Protection Agency, USEPA)推荐的暴露模型,构建“两步法”风险评估模型:暴露量计算模型和风险表征模型,并基于暴露场景假设法构建了再生塑料颗粒加工车间暴露环境,评估可挥发性苯系物对作业人员的健康影响风险水平.
1. 材料与方法(Materials and methods)
1.1 样品采集
针对PP、HDPE、ABS、HIPS、PA等5种常见再生塑料颗粒,采集25种不同用途的再生塑料颗粒用于检测苯系物挥发浓度,其基本属性如表1所示. 本文所研究的再生塑料颗粒样品均为加工成品塑料颗粒,每包重量为25 kg,再生塑料颗粒单个样品的尺寸均小于1 cm×1 cm×1 cm.
表 1 实验样品基本属性表Table 1. Basic properties of experimental samples样品编号Sample number 材质Material 颜色Colour 其他特性Other features 用途Application 1 PP 黑色 NE. 家电配件、玩具、日用品 2 PP 油黑 NE. 塑料外壳、塑料配件、板材、改性等注塑压板产品 3 HDPE 白色 NE. 家电部件,电动工具配件 4 HDPE 绿色 NE. 购物袋、化肥内衬薄膜 5 HDPE 浅蓝色 NE. 日用品、瓶盖 6 HDPE 深蓝色 NE. 塑料托盘 7 HDPE 黑色 高密度中空 保温管、螺纹管等 8 HDPE 黑色 NE. 用于盛放清洁剂、化学品、化妆品等的容器 9 HDPE 棕色-1 NE. 遮阳网,植被网,渔网等 10 HDPE 棕色-2 NE. 电器外壳 11 HDPE 棕色-3 NE. 木塑 12 HDPE 棕色-4 NE. 电缆护套、穿线管、工具箱 13 ABS 黑色-1 NE. 网络机顶盒 14 ABS 黑色-2 NE. 超声波3D眼镜 15 ABS 黑色-3 环保防火 家电外壳、小音响、电话机 16 ABS 黑色-4 环保不防火 电脑主机面板 17 ABS 黑色-5 防火不环保 电源外壳产品、小家电、移动电源外壳 18 ABS 黑色-6 不环保不防火 电器外壳、咖啡机外壳、手机外壳 19 ABS 灰白色-1 NE. 机顶盒外壳 20 ABS 灰白色-2 NE. 家具脚、椅子脚 21 ABS 白色-3 环保防火 行李箱 22 ABS 白色-4 环保不放火 调色喷油、调色音响 23 HIPS 灰白色 NE. 手机指环 24 HIPS 黑色 NE. 衣架 25 PA 白色 NE. 电子电器外壳 NE.,不存在其他特性. NE.,no other features 1.2 苯系物挥发浓度测定
称取苯、甲苯、乙苯、对二甲苯、间二甲苯、邻二甲苯、苯乙烯、异丙苯标准样品(纯度≥99%,国家标准物质信息网)各0.2000 g加入到有少量丙酮溶液(纯度≥99 %,国药集团化学试剂有限公司)的100 mL容量瓶中,摇匀混合后加入丙酮溶液定容,得到浓度为2 g·L−1的标准贮备液. 再用丙酮溶液稀释成0.1、0.05、0.02、0.01 g·L−1的系列标准使用液,放入冰箱中保存备用. 实验中设置空白基质,除不加样品外还采用与样品检测相同的程序,并且要求其检测结果小于定量限. 由于再生塑料颗粒样品的尺寸均小于1 cm×1 cm×1 cm,因此不用预处理,直接将样品低温冷冻后迅速放入研磨机中,研磨后备用.
对苯系物等挥发性组分进行分析,采用顶空进样法对组分进行气相色谱-质谱(Gas Chromatography-Mass Spectrometry, GC-MS)分析时的效果良好[27]. 电子天平称量待测样品0.1000 g置于20 mL顶空瓶内,放入顶空自动进样装置. 顶空进样器条件:加热箱140 ℃,定量环150 ℃,传输线160 ℃,GC循环时间60 min,样品瓶平衡时间45 min. 色谱质谱条件见表2. 在设定条件下,分别向5个含有0.1000 g空白基质的顶空瓶内加入含0.1、0.2 、0.5、1.0、2.0 μg的混合标准溶液,进行检测分析并绘制标准曲线. 取待测样品0.1000 g置于顶空瓶内,迅速盖上瓶盖,放入顶空自动进样装置,在140℃ 平衡温度下平衡45 min,然后注入GC-MS(Agilent 7697A,20 mL 顶空进样瓶,安捷伦公司,美国)对可挥发性苯系物含量进行检测分析.
表 2 色谱质谱条件Table 2. GC-MS conditionsGC-MS参数GC-MS parameter 设定条件Conditions 色谱柱 DB-5MS柱(30 m×0.25 mm×0.25 μm) 进样口 温度230 ℃ 柱箱 初始温度35 ℃,平衡时间5 min,终止温度250 ℃,升温速率20 ℃·min−1,保温时间10 min,柱流量1 mL·min−1 色谱质谱接口 温度280 ℃ 离子源 电子离子源(EI源)温度230 ℃ 四极杆 温度150 ℃ 离子化能量 70 eV 载气 He气,纯度≥99.999% 质量扫描范围 SCAN(29—400 m/z) 进样方式 分流进样,分流比10:1 溶剂延迟时间 4.5 min 所有实验数据均基于以上设计过程,重复 3 次,实验中按照标准溶液建立的苯系物工作曲线其相 关性 r 2 为 0.992—0.995.
1.3 “两步法”健康风险评估模型
根据USEPA的暴露评估公式[28-30],构建“两步法”健康风险评估模型:第一步为暴露量计算模型,在工业生产中,吸入是接触可挥发性苯系物的主要暴露途径[31]. 因此,第一步用于计算在再生塑料颗粒加工过程中,可挥发性苯系物对作业人员的呼吸暴露量;第二步是风险表征模型,用于评估苯系物对作业人员经呼吸暴露的健康风险水平.
1.3.1 暴露量计算模型
根据再生塑料颗粒加工过程苯系物对不同暴露群体的影响不同,参考一般工业厂房设计规范,设计再生塑料颗粒加工暴露场景为:单层厂房面积为500 m2,高度为6 m,厂区内通风状态一般,作业人员实行三班倒制,每天工作8 h. 并根据劳动强度,将作业人员划分为中度体力劳动男性(女性)和重度体力劳动男性(女性)共四类.
暴露量计算分为作业人员呼吸所接触到的可挥发性苯系物浓度Cinh (mg·m−3)、吸入量Iinh (mg)及经呼吸暴露量Exinh [mg·kg−1·d−1]三部分,其计算公式参照(1)、(2)、(3). 模型中各参数设定见表3,当参数无具体参考时,从暴露评估最严苛角度,选取导致最危险状态的参数取值.
表 3 暴露评估模型参数取值Table 3. Parameter values of exposure assessment model参数Parameter 物理意义Physical meaning 单位Unit 描述Description 重度体力劳动男性Men with heavy physical labor 重度体力劳动女性Women with heavy physical labor 中度体力劳动男性Men with moderately physical labor 中度体力劳动女性Women with moderately physical labor 参考文献Reference C 可挥发性苯系物浓度 mg·kg−1 人体经呼吸接触到的再生塑料中苯系物浓度 浓度关键值 浓度关键值 浓度关键值 浓度关键值 本文研究 M 再生塑料颗粒重量 kg 人体一天内接触到再生塑料的重量 2400 2400 2400 2400 本研究 Vroom 作业空间大小 m3 暴露场景中作业场所周围空间大小 3000 3000 3000 3000 本研究 Fv 挥发系数 无量纲 苯系物挥发到空气中的量与再生塑料本身所含苯系物总量之比 1 1 1 1 本研究 D 稀释因子 无量纲 再生塑料中苯系物释放到空气中时由于外界环境影响而被稀释的程度 0.1 0.1 0.1 0.1 本研究 AIR 呼吸速率 m3·h−1 人体对空气的吸入率 2.85 2.13 1.90 1.42 [32] ET 暴露时间 h·d−1 人体每天接触再生塑料的时间 8 8 8 8 本研究 ED 暴露持续时间 d 特定时间段内人体与再生塑料接触时间 350×25 350×25 350×25 350×25 [33] BW 平均体重 kg 人体体重 64.07 64.07 55.86 55.86 [34] AT 平均暴露时间(非致癌) a 人体在某一时期暴露于苯系物的总时间量(致癌风险计算时取终身暴露时间) 25 25 25 25 [33] 平均暴露时间(致癌) a 70 70 70 70 [30] Cinh=C×MVroom×Fv×D (1) Iinh=Cinh×AIR×ET×ED (2) Exinh=Iinh×1BW×AT (3) 1.3.2 风险表征模型
评估作业人员健康风险时,可挥发性苯系物按照其可能导致的不同健康危害效应分为致癌和非致癌风险两类[35],从而将风险表征模型分为非致癌风险表征模型和致癌风险表征模型. 式(4)为非致癌风险Rnc计算公式,式(5)为致癌风险Rc计算公式,综合风险R采用累加的方式,见式(6),其中i指第i种物质,j指第j种暴露途径. 此外,致癌污染物的斜率因子SF和非致癌物的参考剂量RfD均采用USEPA综合风险信息系统[36]提供的资料,见表4. 式中
1×10−6 表 4 再生塑料颗粒中苯系物经呼吸暴露的RfD和SFTable 4. RfD and SF of benzene homologues in regenerated plastic particles through respiratory exposure苯系物Benzene homologues RfD/(mg·kg−1·d−1) SF/(kg·d·mg−1) 苯 4.00×10−3 5.50×10−2 甲苯 8.00×10−2 — 乙苯 1.00×10−1 1.10×10−2 对二甲苯 2.00×10−1 — 间二甲苯 2.00×10−1 — 邻二甲苯 2.00×10−1 — 苯乙烯 2.00×10−1 — 异丙苯 1.00×10−1 — —不涉及该项. not involved. Rnc=ExRfD×10−6 (4) Rc=1−exp(−SF×Ex) (5) R=∑i∑jRnij (6) 2. 结果与讨论 (Results and discussion)
2.1 再生塑料颗粒加工厂房内可挥发性苯系物浓度水平
将再生塑料颗粒中8种可挥发性有机苯系物的检测数据作简单统计,见表5. 可挥发性苯系物在25种再生塑料颗粒样本中均有检出,甲苯和异丙苯的检出率最高(92%). 可挥发性苯系物的总体检测浓度范围在9.26×10−8 —8.68×10−1 mg·kg−1,总体挥发浓度较低. 其中,苯乙烯的挥发量最多,平均浓度达到0.198 mg·kg−1,间二甲苯次之,苯的挥发量最小.
表 5 再生塑料颗粒中苯系物检测及分析结果Table 5. Detection and analysis results of benzene homologues in recycled plastic particles苯系物Benzene homologues 检测浓度范围/(mg·kg−1)Concentration range 平均值/(mg·kg−1)Average 检出率/%Detection ratio P2.5—P97.5/(mg·kg−1) P50/(mg·kg−1) 标准差Standard deviation 标准稳健度Standard robustness 苯 3.78×10−4—8.43×10−3 2.26×10−3 64 3.78×10−4—8.43×10−3 1.61×10−3 2.11×10−3 1.41×10−3 甲苯 7.42×10−6—1.07×10−1 2.27×10−2 92 5.04×10−5—1.07×10−1 7.08×10−3 3.34×10−2 1.05×10−2 乙苯 3.85×10−4—1.05×10−1 2.86×10−2 88 3.91×10−4—1.05×10−1 4.62×10−3 3.77×10−2 6.20×10−3 对二甲苯 7.98×10−4—3.02×10−2 5.59×10−3 88 8.01×10−4—2.93×10−2 3.33×10−3 6.74×10−3 3.53×10−3 间二甲苯 9.26×10−8—7.83×10−3 3.10×10−3 24 0—7.83×10−3 2.66×10−3 3.08×10−3 3.92×10−3 邻二甲苯 3.17×10−4—5.32×10−1 7.62×10−2 84 3.17×10−4—5.30×10−1 2.12×10−3 1.63×10−1 2.67×10−3 苯乙烯 7.13×10−4—8.68×10−1 1.98×10−1 88 7.30×10−4—8.62×10−1 4.34×10−3 2.83×10−1 5.01×10−3 异丙苯 2.20×10−5—4.02×10−2 7.88×10−3 92 4.28×10−5—3.88×10−2 9.42×10−4 1.05×10−2 4.77×10−4 进一步结合四分位稳健法 (inter quartile range, IQR) 分析检测数据,除间二甲苯外,其余7种苯系物检测数据标准差远大于标准稳健度,说明IQR在异常值检出的灵敏度上明显高于传统分析方法[38],间二甲苯由于检出率低,采用传统分析方法效果更好. 因此,间二甲苯选用样本平均值作为再生塑料中可挥发性苯系物的检测浓度关键值,检测浓度范围作为作业人员可能接触的可挥发性苯系物浓度范围. 对其余7种苯系物,取P50作为检测浓度关键值,P2.5—P97.5作为浓度范围.
结合式(1)计算厂房内可挥发性苯系物浓度Cinh,见表6. 在设定的暴露场景下,厂房内8种苯系物浓度水平排序为:甲苯>乙苯>苯乙烯>对二甲苯>间二甲苯>邻二甲苯>苯>异丙苯,浓度均值为2.71×10−4 mg·m−3,虽然各苯系物浓度水平结果同El-Hashemy等[39]监测印刷厂、Singh等[40]监测购物中心内苯系物浓度水平结果略有差异,但一致得到了甲苯浓度是苯系物中浓度最高的这一结论,说明构建的暴露场景具有适用性,从而保证了后续评价结果的可靠性. 将厂房内苯系物浓度水平同《工作场所有害因素职业接触限值》标准进行比对,结果表明8种苯系物浓度范围上限平均低于标准限值4—5个数量级,属于低污染水平.
表 6 厂房内可挥发性苯系物浓度水平Table 6. Concentration levels of volatile benzene homologues in the plant苯 甲苯 乙苯 对二甲苯 间二甲苯 邻二甲苯 苯乙烯 异丙苯 Cinh /(mg·m−3) 1.29×10−4 5.66×10−4 3.70×10−4 2.66×10−4 2.48×10−4 1.70×10−4 3.47×10−4 7.54×10−5 浓度范围/(mg·m−3) 3.02×10−5—6.74×10−4 4.04×10−6—8.54×10−3 3.13×10−5—8.38×10−3 6.41×10−5—2.34×10−3 7.41×10−9—6.26×10−4 2.54×10−5—4.24×10−2 5.84×10−5—6.90×10−2 3.42×10−6—3.11×10−3 TWA/(mg·m−3) 6 50 100 50 50 50 50 268 TWA:8 h时间加权平均容许浓度;职业接触限值参考[41],其中异丙苯限值参考[42]. TWA:8 h time-weighted average allowable concentration;Occupational exposure and the cumene limit value references[41-42]. 2.2 暴露量分析
再生塑料颗粒中具有非致癌影响的苯系物包括甲苯、对二甲苯、间二甲苯、邻二甲苯、苯乙烯、异丙苯,具有致癌影响的物质包括苯、乙苯. 由于致癌物质危险性较高,其非致癌影响也应当考虑. 综上,结合式(1)—(3)计算可挥发性苯系物对四类暴露群体的暴露量,结果见表7所示.
表 7 不同暴露人群暴露量Table 7. Exposure of different exposure groups类型Type 苯系物Benzene homologues 暴露量/(mg·(kg·d)−1)Exposure 重体力劳动男性Men with heavy physical labor 重体力劳动女性Women with heavy physical labor 中度体力劳动男性Men with moderately physical labor 中度体力劳动女性Women with moderately physical labor 非致癌影响 苯 4.3951×10−5 3.7676×10−5 2.9301×10−5 2.5117×10−5 甲苯 1.9328×10−4 1.6568×10−4 1.2885×10−4 1.1045×10−4 乙苯 1.2612×10−4 1.0811×10−4 8.4081×10−5 7.2075×10−5 对二甲苯 9.0769×10−5 7.7808×10−5 6.0513×10−5 5.1872×10−5 间二甲苯 8.4627×10−5 7.2543×10−5 5.6418×10−5 4.8362×10−5 邻二甲苯 5.7874×10−5 4.9610×10−5 3.8582×10−5 3.3073×10−5 苯乙烯 1.1848×10−4 1.0156×10−4 7.8985×10−5 6.7707×10−5 异丙苯 2.5716×10−5 2.2044×10−5 1.7144×10−5 1.4696×10−5 总和 7.2880×10−4 6.2474×10−4 4.8587×10−4 4.1649×10−4 致癌影响 苯 1.5697×10−5 1.3456×10−5 1.0465×10−5 8.9704×10−6 乙苯 4.5043×10−5 3.8612×10−5 3.0029×10−5 2.5741×10−5 总和 6.0740×10−5 5.2067×10−5 4.0493×10−5 3.4711×10−5 8种可挥发性苯系物的非致癌暴露影响排序为:甲苯>乙苯>苯乙烯>对二甲苯>间二甲苯>邻二甲苯>苯>异丙苯,其中甲苯的暴露量最高,Exinh(重度体力劳动男性)=1.9328×10−4 mg·kg−1·d−1,占非致癌影响总暴露量的39.78 %,乙苯次之,占25.96 %. 2种具有致癌影响的物质中乙苯的暴露量高于苯,占致癌影响总暴露量的74.16 %.
综合分析发现,在从事重体力活动时,男性作业人员呼吸速率要远远大于女性,因而暴露量排序为Exinh(重体力劳动男性)>Exinh(重体力劳动女性)>Exinh(中度体力劳动男性)>Exinh(中度体力劳动女性). 此外,由于8种苯系物均具有非致癌暴露影响,因此可挥发性苯系物对不同群体暴露量的主要来源是非致癌影响暴露量.
2.3 作业人员健康风险评估
2.3.1 致癌风险水平
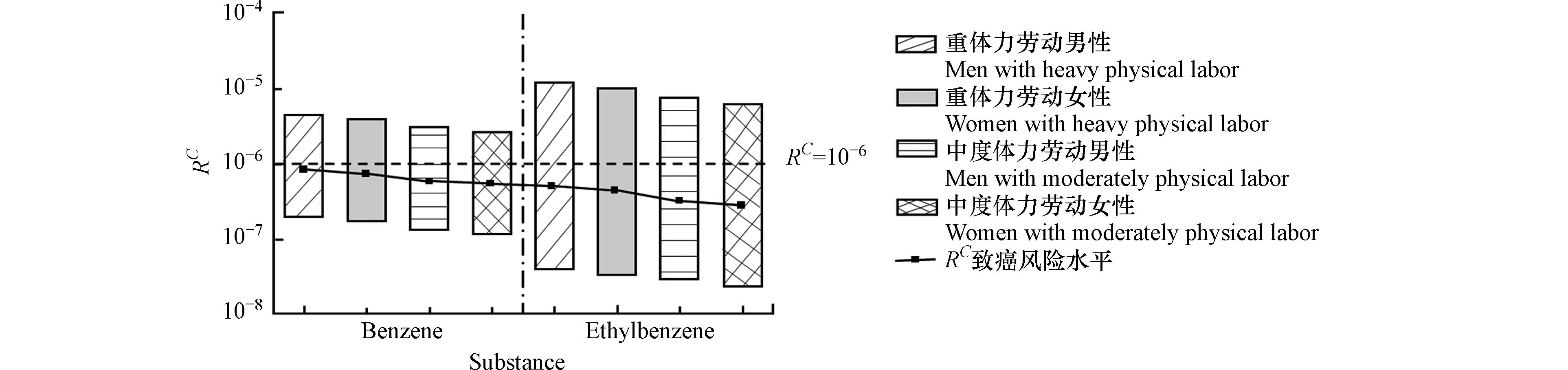
苯及乙苯对四类暴露群体的致癌风险水平排序为:Rc(重度体力劳动男性)>Rc(重度体力劳动女性)>Rc(中度体力劳动男性)>Rc(中度体力劳动女性),见图1. 致癌风险水平差异与暴露量差异相关,劳动强度越高单位体重的暴露量越高,导致相应的致癌风险水平越高.
苯对四类暴露群体的致癌风险水平均小于USEPA提出的可忽略风险水平10−6,但其致癌风险水平范围上限Rc依次为4.5204×10−6、3.8749×10−6、3.0136×10−6、2.5833×10−6,介于潜在风险水平范围10−4—10−6,说明对人体具有潜在风险.
乙苯对四类暴露群体的致癌风险水平均低于10−6,但其致癌风险水平范围的上限均为10−5数量级,高于风险可忽略水平10−6,这可能是由于再生塑料颗粒的品控不足,导致塑料颗粒成品中乙苯浓度分布范围较广,导致致癌风险水平范围最小值与最大值相差3个数量级,因此,企业应严格把控再生塑料颗粒质量,将乙苯浓度降低至10−3数量级,可使致癌风险水平低于10−6.
2.3.2 非致癌风险水平
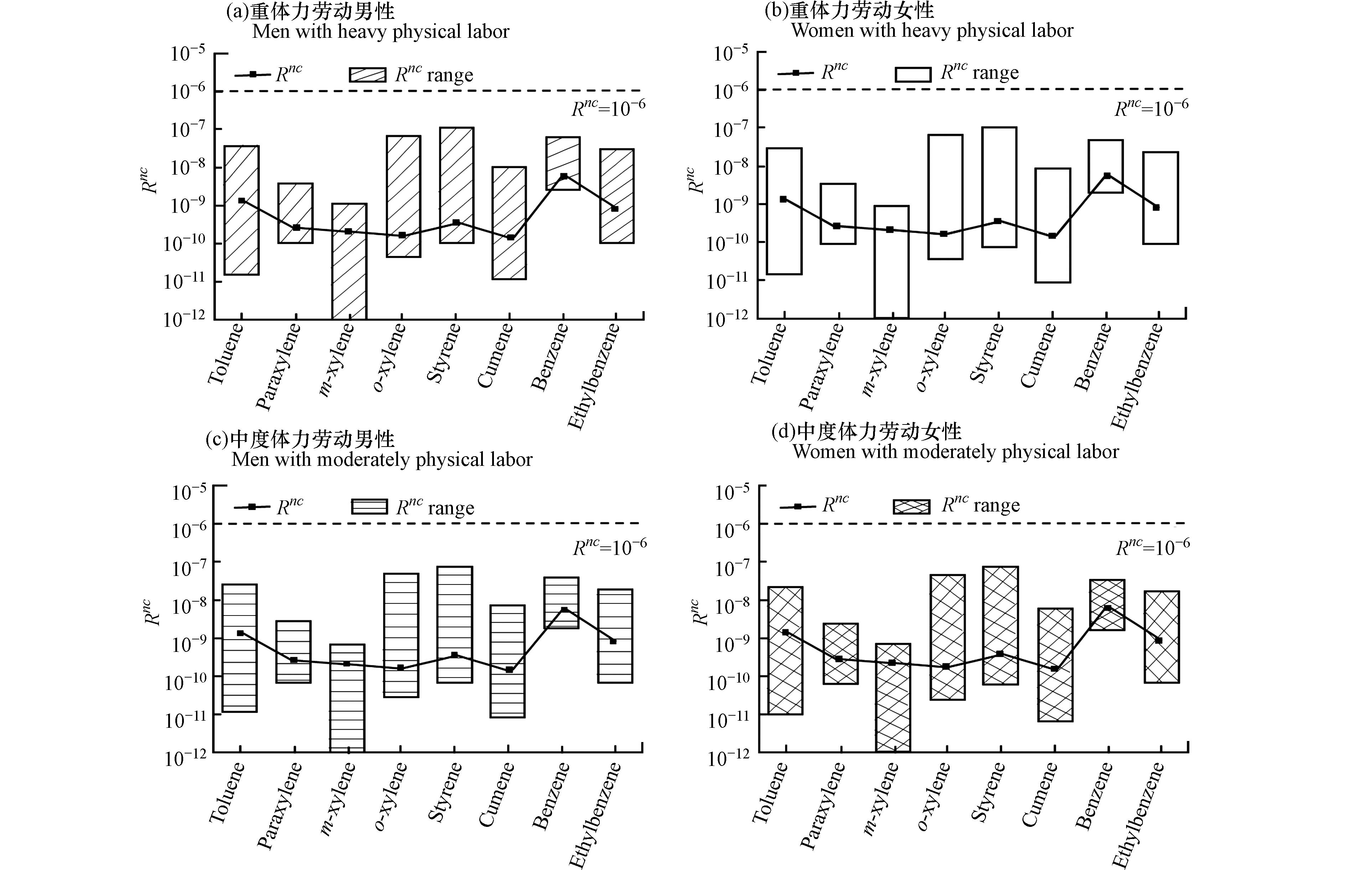
由图2所示,8种可挥发性苯系物的非致癌风险水平排序为:苯>甲苯>乙苯>苯乙烯>对二甲苯>间二甲苯>邻二甲苯>异丙苯,乙苯作为具有致癌影响物质,其非致癌风险水平低于甲苯,是由于乙苯对工人的暴露量低于甲苯,因而其非致癌风险水平较低. 此外,8种苯系物非致癌风险水平及风险水平范围上限均小于USEPA提出的可忽略水平10−6,可以认为8种苯系物对作业人员不存在明显的非致癌健康风险.
2.3.3 综合风险水平
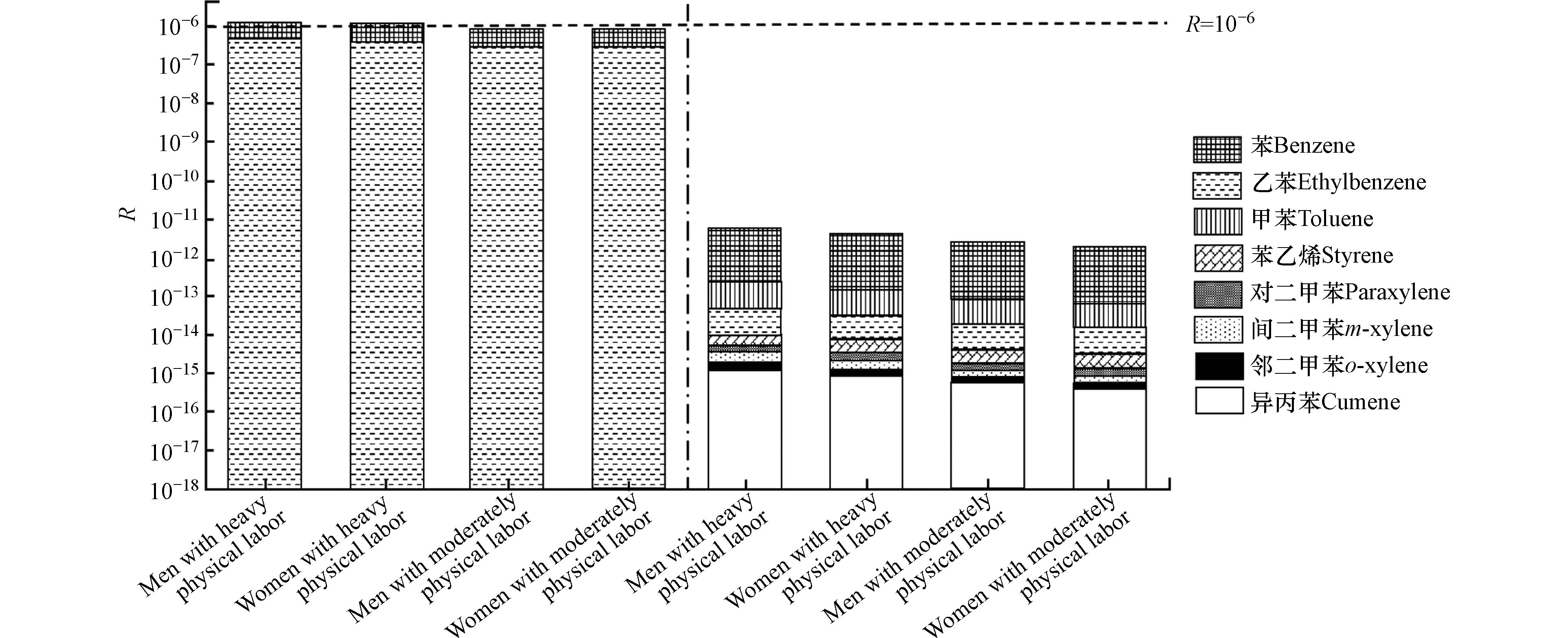
根据图3所示,苯系物对作业人员的健康风险主要来自苯和乙苯的致癌风险,其中苯是再生塑料颗粒致癌风险和非致癌风险的主要来源.
苯及乙苯对四类暴露群体的致癌风险水平均低于可忽略水平10−6,当作业人员同时受到苯和乙苯暴露时,重度体力劳动男性和女性的综合致癌风险水平依次为1.3588×10−6、1.1648×10−6,均高于可忽略水平10−6,表明当受单一致癌物质暴露时,即使致癌风险水平处于可忽略水平,但存在多种致癌物质暴露时,其风险累积会超过可忽略水平. 中度体力劳动男性和女性的综合致癌风险水平虽略低于10−6,但当苯取P97.5为浓度关键值时,R(中度体力劳动男性)=3.3439×10−6、R(中度体力劳动女性)=2.4991×10−6,或当乙苯取P97.5为浓度关键值时,R(中度体力劳动男性)=8.0634×10−6、R(中度体力劳动女性)=6.0264×10−6,其致癌风险水平均高于10−6,表明中度体力劳动男性和女性的仍存在潜在的综合致癌风险,再生塑料颗粒企业应当警惕致癌物质累积作用下对作业人员的健康风险影响. 而8种苯系物的综合非致癌风险水平低于10−6,风险可忽略,说明对作业人员没有明显的非致癌健康风险.
3. 结论(Conclusion)
(1)对25种再生塑料颗粒样本检测结果表明,8种可挥发性苯系物均有检出,总体检测浓度范围在9.26×10−8 mg·kg−1 —8.68×10−1 mg·kg−1,其中苯乙烯的挥发量最多,平均浓度达到0.098 mg·kg−1.
(2)场景模拟显示,再生塑料颗粒加工过程中,作业环境中8种苯系物浓度范围上限平均低于《工作场所有害因素职业接触限值》限制4—5个数量级,处于较低水平.
(3)暴露量计算模型结果表明,非致癌暴露影响的主要来源是甲苯,占非致癌影响总暴露量的39.78 %;致癌暴露影响的主要来源是乙苯,占致癌影响总暴露量的74.16 %. 且苯系物的非致癌影响总暴露量高于致癌影响总暴露量,对男性作业人员的暴露量大于女性作业人员,对从事重度体力劳动的作业人员暴露量大于从事中度体力劳动的.
(4)风险表征模型结果表明,可挥发性苯系物对作业人员的健康风险主要为苯和乙苯的综合致癌风险,对重度体力劳动男性和女性的综合致癌风险水平均高于可忽略水平10−6. 此外,8种苯系物对四类暴露群体不存在明显的非致癌风险.
-
-
[1] 孙晓雯, 李振炫, 黄利东, 等. 邻苯二甲酸及丙二酸对方解石吸附四环素的影响 [J]. 环境化学, 2019, 38(12): 2746-2756. doi: 10.7524/j.issn.0254-6108.2019011506 SUN X W, LI Z X, HUANG L D, et al. Effect of organic dicarboxylic acid on the adsorption of tetracycline by calcite [J]. Environmental Chemistry, 2019, 38(12): 2746-2756(in Chinese). doi: 10.7524/j.issn.0254-6108.2019011506
[2] 詹杰, 魏树和. 四环素在土壤和水环境中的分布及其生态毒性与降解 [J]. 生态学报, 2015, 35(9): 2819-2825. ZHAN J, WEI S H. The distribution and eco-toxicology of tetracycfine in soil and water environment and its degradation: A review [J]. Acta Ecologica Sinica, 2015, 35(9): 2819-2825(in Chinese).
[3] CHEE-SANFORD J C, MACKIE R I, KOIKE S, et al. Fate and transport of antibiotic residues and antibiotic resistance genes following land application of manure waste [J]. Journal of Environmental Quality, 2009, 38(3): 1086-1108. doi: 10.2134/jeq2008.0128 [4] 丁剑楠, 刘舒娇, 邹杰明, 等. 太湖表层水体典型抗生素时空分布和生态风险评价 [J]. 环境科学, 2021, 42(4): 1811-1819. DING J N, LIU S J, ZOU J M, et al. Spatiotemporal distributions and ecological risk assessments of typical antibiotics in surface water of Taihu Lake [J]. Environmental Science, 2021, 42(4): 1811-1819(in Chinese).
[5] WANG L F, LI H, DANG J H, et al. Occurrence, distribution, and partitioning of antibiotics in surface water and sediment in a typical tributary of Yellow River, China [J]. Environmental Science and Pollution Research, 2021, 28(22): 28207-28221. doi: 10.1007/s11356-021-12634-1 [6] CHEN Y Y, MA Y L, YANG J, et al. Aqueous tetracycline degradation by H2O2 alone: Removal and transformation pathway [J]. Chemical Engineering Journal, 2017, 307: 15-23. doi: 10.1016/j.cej.2016.08.046 [7] WANG M J, SONG Y M, ZHANG H J, et al. Insights into the mutual promotion effect of graphene oxide nanoparticles and tetracycline on their transport in saturated porous media [J]. Environmental Pollution, 2021, 268: 115730. doi: 10.1016/j.envpol.2020.115730 [8] JI L L, WAN Y Q, ZHENG S R, et al. Adsorption of tetracycline and sulfamethoxazole on crop residue-derived ashes: Implication for the relative importance of black carbon to soil sorption [J]. Environmental Science & Technology, 2011, 45(13): 5580-5586. [9] COOPER W J, ZIKA R G, PETASNE R G, et al. Photochemical formation of hydrogen peroxide in natural waters exposed to sunlight [J]. Environmental Science & Technology, 1988, 22(10): 1156-1160. [10] 魏西会, 刘素美, 张经, 等. 天然水体中微量过氧化氢的测定方法 [J]. 海洋科学, 2008, 32(10): 96-100. WEI X H, LIU S M, ZHANG J, et al. Measurement methods of hydrogen peroxide determination in natural waters [J]. Marine Sciences, 2008, 32(10): 96-100(in Chinese).
[11] 彭建彪, 张耀宗, 张亚, 等. 一种席夫碱铜配合物催化过氧化氢氧化降解三氯生 [J]. 环境化学, 2019, 38(5): 977-984. PENG J B, ZHANG Y Z, ZHANG Y, et al. Oxidative removal of triclosan with hydrogen peroxide catalyzed by a Schiff base Cu(Ⅱ)-complex [J]. Environmental Chemistry, 2019, 38(5): 977-984(in Chinese).
[12] 王徐越, 孙振亚, 谢裕兴, 等. “光催化铁循环”作用对自组装TiO2-FeOOH复合膜活性的影响 [J]. 环境化学, 2018, 37(11): 2555-2564. doi: 10.7524/j.issn.0254-6108.2018010204 WANG X Y, SUN Z Y, XIE Y X, et al. “Photocatalysis Iron Cycling” effect on the photocatalytic activity of self-assembled TiO2-FeOOH nano-films [J]. Environmental Chemistry, 2018, 37(11): 2555-2564(in Chinese). doi: 10.7524/j.issn.0254-6108.2018010204
[13] ZHANG H L, ELSKENS M, CHEN G X, et al. Phosphate adsorption on hydrous ferric oxide (HFO) at different salinities and pHs [J]. Chemosphere, 2019, 225: 352-359. doi: 10.1016/j.chemosphere.2019.03.068 [14] WANG N N, ZHENG T, ZHANG G S, et al. A review on Fenton-like processes for organic wastewater treatment [J]. Journal of Environmental Chemical Engineering, 2016, 4(1): 762-787. doi: 10.1016/j.jece.2015.12.016 [15] WENG Y T, VEKEMAN J, ZHANG H L, et al. Unravelling phosphate adsorption on hydrous ferric oxide surfaces at the molecular level [J]. Chemosphere, 2020, 261: 127776. doi: 10.1016/j.chemosphere.2020.127776 [16] HAN M F, WANG Y W, ZHAN Y H, et al. Efficiency and mechanism for the control of phosphorus release from sediment by the combined use of hydrous ferric oxide, calcite and zeolite as a geo-engineering tool [J]. Chemical Engineering Journal, 2022, 428: 131360. doi: 10.1016/j.cej.2021.131360 [17] GU C, KARTHIKEYAN K G. Interaction of tetracycline with aluminum and iron hydrous oxides [J]. Environmental Science & Technology, 2005, 39(8): 2660-2667. [18] HOFMANN A, PELLETIER M, MICHOT L, et al. Characterization of the pores in hydrous ferric oxide aggregates formed by freezing and thawing [J]. Journal of Colloid and Interface Science, 2004, 271(1): 163-173. doi: 10.1016/j.jcis.2003.11.053 [19] 马黎, 赵丽, 王世敏, 等. 分级微纳结构TiO2空心球的制备及其在DSSC中的应用 [J]. 中国科学:化学, 2012, 42(7): 1022-1028. doi: 10.1360/032011-584 MA L, ZHAO L, WANG S M, et al. Preparation of TiO2 hollow spheres with hierarchical micro/nano architectures and its application in dye sensitized solar cells [J]. Scientia Sinica Chimica), 2012, 42(7): 1022-1028(in Chinese). doi: 10.1360/032011-584
[20] 蒋琦, 姜哲昊, 陈荣, 等. Fe(Ⅲ)-Salen功能化纳米Fe3O4复合材料的合成及其对三氯苯的催化降解性能 [J]. 环境化学, 2017, 36(8): 1744-1751. doi: 10.7524/j.issn.0254-6108.2017010901 JIANG Q, JIANG Z H, CHEN R, et al. Preparation of Fe(Ⅲ)-Salen-functionalized nano-Fe3O4 magnetic composite and its catalytic degradation of 2, 4, 6-trichlorophenol [J]. Environmental Chemistry, 2017, 36(8): 1744-1751(in Chinese). doi: 10.7524/j.issn.0254-6108.2017010901
[21] ZANG J, WU T T, SONG H H, et al. Removal of tetracycline by Hydrous ferric oxide: Adsorption kinetics, isotherms, and mechanism [J]. International Journal of Environmental Research and Public Health, 2019, 16(22): 4580. doi: 10.3390/ijerph16224580 [22] SHI Y J, XING S F, WANG X H, et al. Changes of the reactor performance and the properties of granular sludge under tetracycline (TC) stress [J]. Bioresource Technology, 2013, 139: 170-175. doi: 10.1016/j.biortech.2013.03.037 [23] GUAN R P, YUAN X Z, WU Z B, et al. Efficient degradation of tetracycline by heterogeneous cobalt oxide/cerium oxide composites mediated with persulfate [J]. Separation and Purification Technology, 2019, 212: 223-232. doi: 10.1016/j.seppur.2018.11.019 [24] 孙健, 徐兆郢, 赵平歌, 等. 水合氧化铁负载量对丙烯酸树脂基复合吸附剂的结构及除磷影响 [J]. 复合材料学报, 2021, 38(8): 2595-2604. doi: 10.13801/j.cnki.fhclxb.20201019.002 SUN J, XU Z Y, ZHAO P G, et al. Effect of hydrated ferric oxide loadings on structure and phosphate adsorption of acrylic polymer-supported composite adsorbents [J]. Acta Materiae Compositae Sinica, 2021, 38(8): 2595-2604(in Chinese). doi: 10.13801/j.cnki.fhclxb.20201019.002
[25] ZHU W X, WANG J D, WANG Y L, et al. Study on sulfadimethoxine removal from aqueous solutions by hydrous ferric oxides [J]. Water Science and Technology, 2016, 74(5): 1136-1142. doi: 10.2166/wst.2016.246 [26] GONG C, CHEN F, YANG Q, et al. Heterogeneous activation of peroxymonosulfate by Fe-Co layered doubled hydroxide for efficient catalytic degradation of Rhoadmine B [J]. Chemical Engineering Journal, 2017, 321: 222-232. doi: 10.1016/j.cej.2017.03.117 [27] CAI C, KANG S P, XIE X J, et al. Efficient degradation of bisphenol A in water by heterogeneous activation of peroxymonosulfate using highly active cobalt ferrite nanoparticles [J]. Journal of Hazardous Materials, 2020, 399: 122979. doi: 10.1016/j.jhazmat.2020.122979 [28] WANG W, ZHU Q, QIN F, et al. Fe doped CeO2 nanosheets as Fenton-like heterogeneous catalysts for degradation of salicylic acid [J]. Chemical Engineering Journal, 2018, 333: 226-239. doi: 10.1016/j.cej.2017.08.065 [29] PU M J, NIU J F, BRUSSEAU M L, et al. Ferrous metal-organic frameworks with strong electron-donating properties for persulfate activation to effectively degrade aqueous sulfamethoxazole [J]. Chemical Engineering Journal, 2020, 394: 125044. doi: 10.1016/j.cej.2020.125044 [30] PENG X M, WU J Q, ZHAO Z L, et al. Activation of peroxymonosulfate by single-atom Fe-g-C3N4 catalysts for high efficiency degradation of tetracycline via nonradical pathways: Role of high-valent iron-oxo species and Fe-Nx sites [J]. Chemical Engineering Journal, 2022, 427: 130803. doi: 10.1016/j.cej.2021.130803 [31] LI J, ZHU J L, FANG L Z, et al. Enhanced peroxymonosulfate activation by supported microporous carbon for degradation of tetracycline via non-radical mechanism [J]. Separation and Purification Technology, 2020, 240: 116617. doi: 10.1016/j.seppur.2020.116617 [32] XIN S S, MA B R, LIU G C, et al. Enhanced heterogeneous photo-Fenton-like degradation of tetracycline over CuFeO2/biochar catalyst through accelerating electron transfer under visible light [J]. Journal of Environmental Management, 2021, 285: 112093. doi: 10.1016/j.jenvman.2021.112093 [33] DU C Y, ZHANG Z, TAN S Y, et al. Construction of Z-scheme g-C3N4/MnO2/GO ternary photocatalyst with enhanced photodegradation ability of tetracycline hydrochloride under visible light radiation [J]. Environmental Research, 2021, 200: 111427. doi: 10.1016/j.envres.2021.111427 -







 DownLoad:
DownLoad: