-
非法药物的滥用影响着人类健康、社会安定与国家经济,如今有170多个国家和地区存在着非法药物滥用的问题,全球非法药物的制造、贩卖和滥用问题日趋严重[1]. 因此,预防非法药物的使用,及时掌握区域非法药物的种类及消费量,精准追踪溯源,压缩违法犯罪活动空间,已经成为各国需要面临的共同问题. 最初关于非法药物的滥用情况是通过问卷调查、犯罪统计等传统社会调查方法获得的,但是这些调查方法具有一定的主观性与滞后性,可能导致非法药物消费情况的不正确评估. 2001年Daughton[2]提出一种污水流行病学的概念来评估非法药物的消费情况,即通过收集污水管道、泵站或者污水处理厂(WWTPs)进水处废水样品,测定污水中药物残留及其代谢物的浓度,结合WWTPs日处理量、服务区人口及药物排泄率等参数推算出WWTPs服务区域内非法药物的消费量. 与传统社会调查方法相比,污水流行病学能够在一定程度上克服主观因素影响,实时、客观地量化不同时间和地区的药物消费情况和人群使用趋势.
2005年Zuccato等[3]首次将这种概念应用于实际,通过收集意大利河流和WWTPs的水样以测定可卡因的含量. 结果发现, 1000名年轻人平均每天使用至少(27±5)剂的可卡因,远超官方报道的数字,随后基于污水流行病学的污水分析法作为一种客观、准确、有效的监测方法,在各国得到了广泛的运用[3-7]. 非法药物进入人体后以母体原型或者代谢产物的形式排泄,这些非法药物具有难降解特性,可以通过排水管网汇入WWTPs,但是污水中成分复杂,会对非法药物及其代谢物的测定产生干扰,且污水中大部分目标药物残留物(drug target residues,DTRs)的浓度极低,因此,污水样品的前处理显得尤为重要. 绝大部分报道都采用固相萃取(solid-phase-extraction,SPE)作为污水的前处理方式[8-9],如果SPE条件不同,对非法药物的萃取回收率也会不同,所以选定合适的SPE条件对污水中非法药物的测定至关重要.
国外的一些研究发现,重大节日如音乐节等期间污水中非法药物的负荷量较正常周呈现出增加的趋势[9-10]. Jiang等[11]发现,中国台湾垦丁地区青年节期间非法药物的浓度明显高于旅游淡季,而关于内地典型旅游城市重大节假日期间非法药物的滥用量鲜有报道. 本研究采用污水分析法对中国典型旅游城市桂林市某污水处理厂的重大节假日与日常生活期间进水废水中常见非法药物甲基苯丙胺和氯胺酮及其代谢物的浓度进行检测,并通过反推模型推算不同时期的甲基苯丙胺与氯胺酮的滥用量. 同时运用SPE技术比较前处理条件(Oasis HLB 和Oasis MCX 两种SPE柱)对模拟样品中甲基苯丙胺和氯胺酮及其代谢物的萃取回收率,选定最适合桂林市污水中甲基苯丙胺(METH)和氯胺酮(KET)及其代谢物苯丙胺(AMP)和去甲氯胺酮(NK)前处理的方法. 从而为桂林市该区域非法药物的滥用与测定信息提供初步数据,以期为毒品滥用监测及禁毒工作提供科学依据.
-
甲基苯丙胺(METH)、苯丙胺(AMP)、氯胺酮(KET)、去甲氯胺酮(NK)标准溶液及其相应的氘代内标替代物溶液METH-D5、AMP-D5、KET-D4、NK-D4购自美国Cerilliant公司,甲醇(HPLC级),甲酸(HPLC级)均购自上海麦克林生化科技有限公司. 氨水(AR)、盐酸(AR)购自杭州龙山精细化工有限公司,实验室用水均为超纯水.
主要仪器及耗材:固相萃取柱(Waters Oasis MCX,60 mg,3 mL;Waters Oasis HLB 60 mg,3 mL)购自美国Waters公司,高效液相色谱-串联质谱联用仪:Agilent 1260-6460,氮吹仪(上海精其仪器有限公司),12位固相萃取装置(上海析友分析仪器有限公司)等.
-
分别吸取METH、AMP、KET、NK的标准溶液(1 mg·mL−1)用甲醇配制成质量浓度为100 μg·mL−1的混合标准一级储备液,取同位素内标溶液(100 μg·mL−1)用甲醇配制成质量浓度为10 μg·mL−1的混合同位素内标一级储备液. 使用时将混合标准一级储备液用甲醇配制成质量浓度为0.5—250 μg·L−1不同浓度梯度的标准曲线混合溶液,再分别用50 mL纯水制备成浓度梯度为1—500 ng·L−1的模拟样品. 上述每个浓度梯度的模拟样品等量加入100 μL混合同位素(50 μg·L−1)内标溶液,以补偿样品制备过程中的基质效应和损失.
-
2021年10月2日—7日、10月17日—23日、12月21日—26日采集桂林市某污水处理厂的进水处废水样品,该污水处理厂主要服务桂林市中南区,只接收生活污水. 污水处理厂设计处理约38万居民人口的生活废水,3次采样期间平均日处理量分别为94826、92341、60074 m3·d−1,与全国其它地区的污水处理厂相比,该污水处理厂的处理水量属于中等偏下水平[7]. 使用便携式自动采样器(启恒环保HX-A型)每半个小时等量采集废水,等比例混合24 h的污水样品,混合样品收集完后立即用浓盐酸酸化至pH=2并在-20 ℃条件下储存,直至分析.
-
将采集后的混合样品解冻后使用玻璃纤维滤膜(0.45 μm)过滤,取50 mL过滤后的废水样品加入50 μg·L−1的混合同位素内标溶液100 μL,充分混合后使用下述最优的SPE条件进行前处理,每个样品制备3个平行样,空白样品与样品同时同步骤测定. Oasis-HLB和Oasis-MCX这两种SPE柱对碱性化合物具有高选择性和灵敏度,本研究事先使用超纯水制备成模拟样品考察这两种SPE柱对甲基苯丙胺和氯胺酮的萃取回收率.
参照Nd等[12]的方法使用Oasis-HLB(Waters Oasis HLB 60 mg,3 mL)固相萃取柱对非法药物进行富集. 依次使用6 mL甲醇和6 mL超纯水活化SPE柱,随后在HLB固相萃取柱上加入有混合同位素内标的50 mL污水样品,样品在SPE柱上以约1 mL·min−1的速率萃取,使用3 mL超纯水清洗SPE柱,柱子在真空下干燥20 min,最后用6 mL甲醇洗脱,洗脱液40 ℃氮吹至近干,再用500 μL甲醇溶液复溶,复溶液过0.22 μm有机滤膜后上机测定. 使用Oasis-MCX(Waters Oasis MCX 60 mg,3 mL)固相萃取柱富集非法药物时参照Jin等[13]的方法. SPE柱依次用4 mL甲醇和4 mL pH=2的超纯水活化,以1 mL·min−1的速率上样,上样结束后将SPE柱真空干燥20 min,使用4 mL的甲醇淋洗萃取柱,最后将4 mL的5%氨水-甲醇以1 mL·min−1的速率洗脱并收集洗脱液,萃取完成后将洗脱液40 ℃氮吹至近干,用300 μL的0.1%甲酸水溶液复溶,复溶液过0.22 μm有机滤膜后上机测定.
-
色谱条件:液相色谱柱:Shim-pack GIST C18(100 mm×2.1 mm,2 μm,日本岛津),柱温:30 ℃,进样量3 μL,流动相为0.1%甲酸水溶液(A相)—乙腈(B相)体系,流速为0.3 mL·min−1,洗脱梯度为:0—1.5 min:20% B;1.5—2.25 min:80% B;2.25—3.1 min:95% B;3.1—5.0 min:20% B,保留时间为8 min.
质谱条件:以电喷雾电离(ESI),采用正离子模式,多反应监测(MRM)模式检测,毛细管电压:3000 V,负离子:3000 V,干燥气温度:325 ℃,干燥气流量:12 L·min−1,脱溶剂和雾化气体是氮气,雾化器压力:40 psi,经优化后,METH、METH-D5、AMP、AMP-D5、KET、KET-D4、NK、NK-D4质谱参数如表1所示.
-
对分析方法的检测限(LOD)、定量限(LOQ)、萃取回收率、基质效应进行验证保证分析过程中的质量控制,每10个样品中包含使用加标内标的超纯水程序空白,以检查潜在干扰和污染.
在50 mL pH=2的超纯水中定量加入目标分析物的混合标准溶液(METH、AMP、KET和NK)和等量的混合内标溶液,混合标准溶液梯度共设置3个低(10 ng·L−1)、中(50 ng·L−1)、高浓度(400 ng·L−1),每个浓度梯度设置7个平行,同时设置一组流程空白,流程空白仅加入等量的混合内标溶液不加目标分析物,分别使用”1.3”中所述的两种SPE方法对模拟样品进行前处理并进行测定. 根据空白和加标样品的测定数据计算提取回收率,以S/N>3为检出限,S/N>10为定量限,并且分别对样品连续多次测定(n=3)和多天重复测定(n=3)来衡量仪器的日内精密度与日间精密度.
-
目标分析物测定完浓度后,通过反推模型公式即可得到该区域的非法药物的消费量. 非法药物的反算公式如下:
千人日均消费量是每千人每日的药物消费量,单位是mg·d−1;目标物浓度是污水厂每个采样周期内DTRs的平均浓度,单位是ng·L−1;进水流量是污水厂采样周期内的进水流量平均值,单位是L·d−1;
f代谢物 是METH和KET代谢产物的校正因子分别为3.67和21.2[14-17]. -
利用SPSS 22.0(IBM, USA)对数据进行分析,非法药物及其代谢物的浓度单位为 ng·L−1,千人日均消费量的单位为 mg·d−1. 采用皮尔森相关分析检验非法药物与其代谢物之间的相关性,采用单因素方差分析检验不同时期非法药物浓度和滥用量的差异,采用t检验分析节假日与日常生活期间非法药物浓度和滥用量的差异,所有的结果均以P<0.05判定是否存在显著性.
-
本研究以3倍、10倍信噪比计算出检出限和定量限. 标准工作曲线范围为1—500 ng·L−1,目标分析物与相应氘代内标的定量离子对峰面积比y为纵坐标、标准曲线中目标物的含量x为横坐标进行线性回归,得到线性方程. 结果见表2,结果显示,两种固相萃取条件下,四种毒品及其代谢物质量浓度在曲线范围内呈现较良好的线性关系,其相关系数R2为0.9911—0.9977,LODs为0.65—1.43 ng·L−1,LOQs为1.91—4.32 ng·L−1.
分别制备低、中、高的3个浓度(10、50、400 ng·L−1)的混合储备溶液,在3种处理条件下进行测试:在纯水样本处理前添加混合储备溶液,纯水样本SPE处理后添加储备溶液,纯水样品不做处理直接添加储备溶液,每组处理条件设置7组平行样,测定完后计算萃取回收率、基质效应及精密度. 计算结果如表3所示,计算得到使用Oasis MCX固相萃取柱处理纯水样品时平均回收率为81.44%—105.92%,基质效应范围为72.36%—124.61%. 而使用HLB固相萃取柱进行前处理时,平均回收率为64.45%—109.52%,基质效应范围为61.38%—130.54%,两种前处理方法得到的RSDs均小于10%.
通过比较两种SPE柱及固相萃取条件的萃取回收率和基质效应,发现混合型阳离子交换固相萃取小柱Oasis MCX对这4种毒品及其代谢物的分离效果良好,较亲水亲脂反相吸附萃取小柱Oasis HLB的回收率更高,能够更好地满足本研究中非法药物定量准确度的要求. 根据研究表明,Oasis MCX的吸附剂是含亲水基团的聚苯乙烯/二乙烯基苯共聚物上键合磺酸基团,能更有效的提取碱性化合物[18-19]. 甲基苯丙胺和氯胺酮及其代谢产物具有含氮的碱性基团,因此Oasis MCX柱能够更有效满足富集要求,所以本研究在现实污水样品前处理及后续实验中均考虑1.3使用Oasis-MCX固相萃取柱萃取富集目标分析物的方法.
-
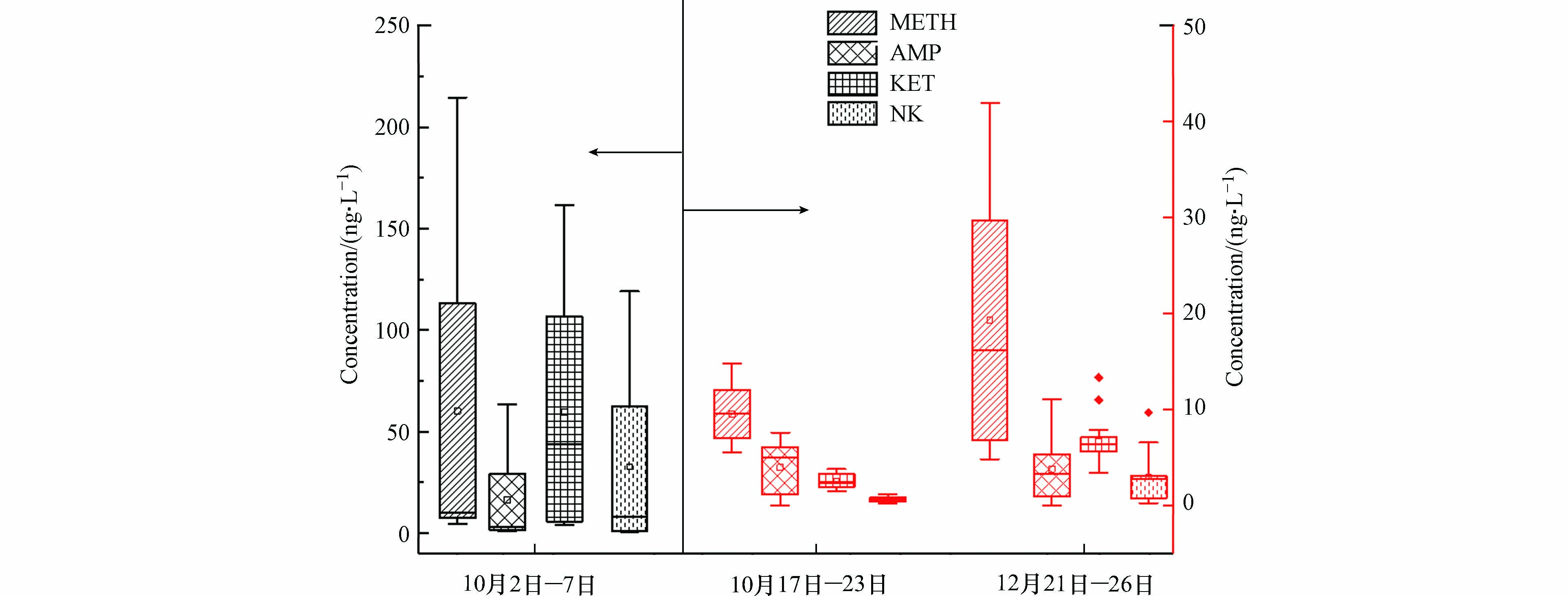
本研究采样期间,WWTP相应的非法药物及其代谢物的浓度水平如图1所示. 这4种毒品及其代谢物在全部污水样品中都有检出,其中METH检出率为100%,AMP的检出率为76%. 重大节假日期间(国庆假期)采集的样品中METH的浓度范围为(6.49±2.44)—(214.46±0.25)ng·L−1,平均浓度为(60.17±0.75)ng·L−1. 后续两次非节假日期间测定样品中METH浓度范围分别为(6.78±0.35)—(13.87±1.07)ng·L−1和(5.57±0.72)—(30.85±10.93)ng·L−1,平均浓度分别为(9.40±1.03)ng·L−1和(19.30±8.20)ng·L−1. AMP在重大节假日期间的浓度范围为(1.62±0.63)—(58.62±6.85)ng·L−1,非节假日期间AMP浓度范围分别为ND(未检出)—(6.48±0.74)ng·L−1和ND—(9.62±2.05)ng·L−1. KET和NK并没有在所有样品中检出,检出率分别为76.47%和57.45%. 重大节假日期间样品中KET的浓度范围为(4.59±0.48)—(144.77±23.61) ng·L−1,非节假日期间样品中KET的最高浓度为(9.00±3.76)ng·L−1. NK在重大节假日期间的浓度范围为(1.02±0.39)—(114.57±6.67)ng·L−1,非节假日期间NK的最高浓度为(3.42±0.54)ng·L−1. 由上述结果得出,重大节假日期间非法药物及其代谢物的浓度显著高于非节假日期间(P<0.05),苯丙胺类兴奋剂和氯胺酮是各种娱乐场所和聚会中常用的违禁药物,重大节假日期间大量的娱乐活动使桂林市非法药物的使用可能具有节假日效应. 而日常生活期间12月份WWTP进水废水中毒品及其代谢物浓度较10月份浓度普遍提升(P<0.05),这可能是气温降低,人们生活用水减少,没有过多的稀释生活污水目标分析物的含量.
根据METH的药代动力学研究表明,大约42%±17%的METH未经过人体代谢通过尿液排出体外,摄入后的30%的AMP和40%的METH在尿液中以原型排出,而高达7%的METH在代谢后以AMP的形式排出[20],如果污水中的AMP与METH浓度比值范围在0.08—0.15则被认为是由METH代谢产生的[21-22]. 本研究中METH和AMP浓度之间有着显著性正相关(P<0.01,r=0.995),但绝大多数AMP和METH的浓度比大于0.15,表明该区域可能存在外在AMP的来源. 研究表明,服用部分合法药物例如治疗帕金森病的辅助药物可以经过人体代谢产生METH,但其对污水中浓度基本没有贡献,且在中国,尚无含有可直接代谢为AMP成分的处方药[22]. 因此,桂林市该WWTP所服务区域存在着METH和AMP滥用共存的现象,可能有非法制毒泄漏或倾倒苯丙胺兴奋剂等行为[23]. 将本研究与其他地区污水中苯丙胺兴奋剂浓度比较时发现该区域的平均浓度低于其他城市的平均浓度,中国广州市WWTPs的进水废水中METH的平均浓度为(145.6±100.3)ng·L-1[15],Xu等[24]报道的青岛WWTPs废水中METH的最高浓度高达1016.0 ng·L−1. 桂林市该区域的日常生活期间AMP的平均浓度为(4.01±1.48)ng·L−1,低于北京(15.2 ng·L−1)、上海(22.7 ng·L−1)、深圳(26.4 ng·L−1)的浓度水平[7, 25]. NK和KET浓度之间也呈现出显著性正相关(P<0.01,r=0.992). 人体摄入KET后30%的代谢产物为其原型,还有1.6%和6%代谢为脱氢去甲氯胺酮(DNKET)和去甲氯胺酮(NK)[24],KET经人体代谢后污水中残留的KET与NK原理比值为0.27—2.10[26]. 而本研究KET的浓度与NK的浓度的比值为0.19—6.84,表明可能存在向污水管网直接倾倒氯胺酮的情况,致使污水中KET的浓度总体上高于NK. 本区域非法药物的实际浓度比值都超过理论比值可能与桂林市持续开展一系列的禁毒活动有关,根据后续研究报道[27],从2021年第一季度开始桂林市公安局进行城市生活污水毒情检测,精准追踪溯源,对污水检测毒品含量高的区域,采取多种措施压缩毒品违法犯罪活动空间,从而可能存在向污水管网恶意倾倒或排放非法药物的现象.
-
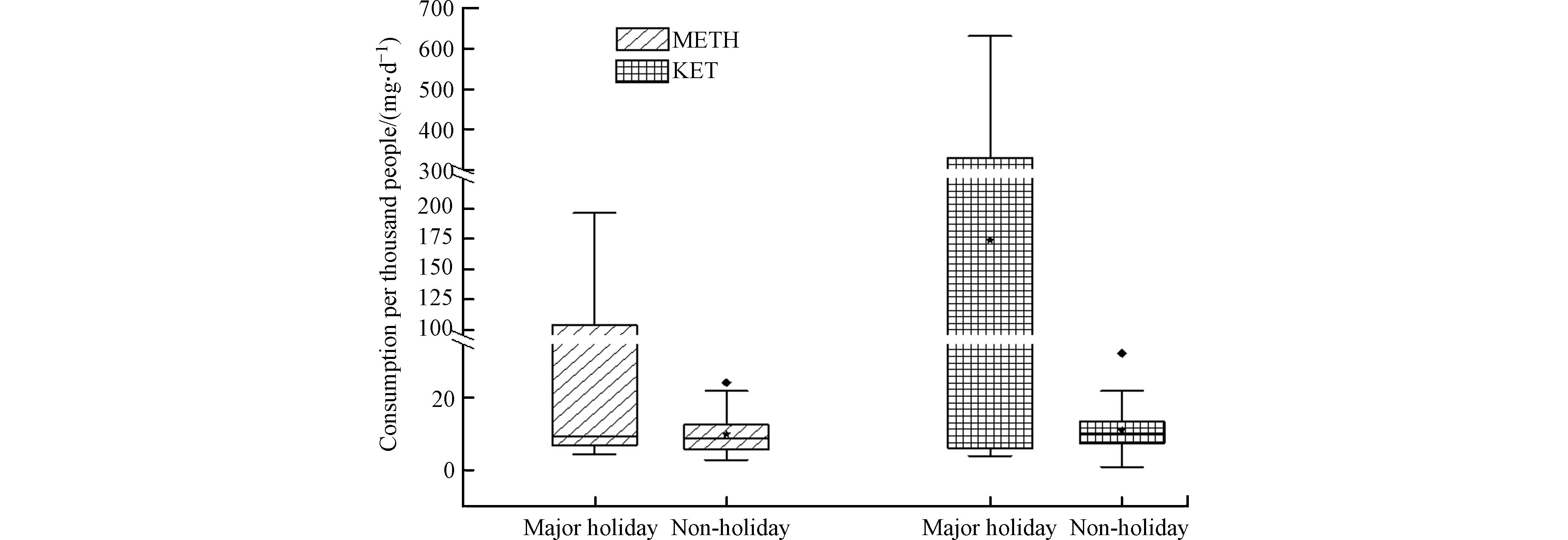
通过反推模型对广西桂林市该WWTP服务区的METH和KET的消费量进行了回测,结果如图2所示. 该污水厂服务区域重大节假日期间METH的千人日均消费量范围为(5.94±2.44)—(196.4±0.25)mg·d−1,平均值为(55.11±94.22)mg·d−1,非节假日期间METH的千人日均消费量范围为(3.23±0.72)—(17.90±10.93)mg·d−1,平均值为(9.79±4.25)mg·d−1·. 以NK作为DTR进行对KET的消费量进行反演,结果得出桂林市该区域重大节假日期间KET的千人日均消费量范围为(5.37±0.39)—(606.12±6.67)mg·d−1,平均值为(173.82±1.83)mg·d−1,而非节假日的KET的千人日均消费量范围为(1.93±0.15)—(15.21±0.83)mg·d−1,平均值为(10.50±1.05)mg·d−1.
日常生活期间桂林市METH与KET的消费量没有明显的差异(P>0.05),但是重大节假日期间非法药物的滥用量存在着暴增的现象(P<0.05),说明桂林市非法药物的消费具有明显的节假日效应. 重大节假日期间桂林市该区域METH和KET的千人日均消费量与东北和广州节假日期间的浓度相当[15, 28],日常生活期间METH的千人日均消费量低于全国千人日均消费水平,根据以往研究报道我国主要城市的污水厂进水废水中的METH千人日均消费量为97.70 mg·d−1[7, 29]. 相比于中国主要城市的METH消费量,KET在中国城市的总体消费量要低得多,但是KET消费量的空间变化高于METH. 与北京(每千人2.2 mg·d−1)、上海(每千人9.1 mg·d−1)相比,本研究的KET消费量更高,这与华南地区KET的消费量大于华北地区的事实相符[7]. 本研究通过对桂林市重大节假日与日常生活期间非法药物的滥用量调查发现,重大节假日期间非法药物消费量显著高于日常生活期间的消费量,表明重大节假日期间非法药物滥用的管控不容忽视,仍需要对桂林市的非法药物滥用情况进行长期监测,深入开展“清源断流”行动,全力遏制非法药物滥用危害.
-
(1)比较了Oasis MCX固相萃取柱与Oasis HLB固相萃取柱对甲基苯丙胺与氯胺酮及其代谢产物的萃取回收率. 研究发现Oasis MCX固相萃取柱对模拟样品中这4种毒品及其代谢物的分离效果更好. Oasis MCX固相萃取柱处理模拟样品时平均回收率为81.44%—105.92%,基质效应范围为72.36%—124.61%.
(2)桂林市该污水处理厂进水样品中METH与KET的检出率分别为100%和76.47%. AMP/METH与KET/NK的浓度比值超过理论代谢范围,说明桂林市开展一系列禁毒活动后,可能存在向污水管网恶意倾倒或排放非法药物的现象.
(3)桂林市该污水厂服务地区的日常生活期间METH的千人日均消费量最高为(17.90±10.93)mg·d−1,国庆节期间千人日均消费量最高为(196.4±0.25)mg·d−1. 日常生活期间KET的千人日均消费量最高为(15.21±0.83)mg·d−1,而国庆节期间千人日均消费量最高为(606.12±6.67)mg·d−1. 节假日期间非法药物的滥用量存在着暴增的现象,桂林市该区域非法药物的消费具有显著的节假日效应,表明桂林市节假日期间非法药物滥用的管控不容忽视.
基于污水流行病学评估旅游城市非法药物的滥用情况
Assessment of illicit drug abuse in tourist cities based on wastewater-based epidemiology
-
摘要: 基于污水流行病学法已经在各国广泛应用于评估非法药物的消费情况. 本研究利用SPE-HPLC-MS技术,比较了前处理条件(Oasis MCX和Oasis HLB固相萃取柱)对模拟样品中甲基苯丙胺(METH)与氯胺酮(KET)及其主要代谢产物苯丙胺(AMP)和去甲氯胺酮(NK)的萃取回收率,结果发现Oasis MCX固相萃取柱更适合METH与KET及其代谢产物的萃取. 萃取方法优化后,利用污水流行病学法对桂林市重大节假日(国庆假期)和日常生活中METH和KET滥用情况进行了研究,通过分析METH和KET及其代谢物在某污水处理厂进水浓度,反算了其在该处理厂服务区域的消费量. 研究结果表明,METH的代谢产物苯丙胺(AMP)与METH的浓度比值、KET与其代谢产物去甲氯胺酮(NK)的浓度比值都超过理论代谢范围,可能存在METH和KET直接向污水管网恶意倾倒或排放的现象. 重大节假日期间METH和KET的千人日均消费量分别为(55.11±94.22)mg·d−1和(173.82±1.83)mg·d−1,而日常生活期间的千人日均消费量分别为(9.79±4.25)mg·d−1和(10.50±1.05)mg·d−1. 重大节假日期间测定的非法药物消费量都显著高于非节假日期间,说明桂林市该区域的非法药物使用着存在节假日效应.Abstract: Wastewater-based epidemiology has been widely used in various countries to assess the consumption of illicit drugs. In this study, SPE-HPLC-MS technology was used to compare the extraction recoveries of methamphetamine (METH), ketamine (KET) and their main metabolites amphetamine (AMP) and norketamine (NK) in simulated samples under different pretreatment conditions (Oasis MCX and Oasis HLB solid phase extraction columns). The results showed that Oasis MCX solid phase extraction column was more suitable for the extraction of METH, KET and their main metabolites. After optimization of extraction method, the abuse of METH and KET in major holiday(National Day) and daily life in Guilin city was investigated. The consumption of METH and KET in the service area of the plant was calculated by measuring the concentration of METH, KET and their metabolites in the influent of that plant. The results showed that the concentration ratio of the metabolite METH, amphetamine (AMP) to METH and the concentration ratio of KET to its metabolite, norketamine (NK), exceeded the theoretical metabolic range. There may be malicious dumping or discharge of METH and KET directly into the sewer network in the investigated area. The average daily consumption of METH and KET per thousand people during major holidays was (55.11±94.22) mg·d−1 and (173.82±1.83) mg·d−1, respectively. However, the average daily consumption per thousand people during daily life was (9.79±4.25) mg·d−1 and (10.50±1.05) mg·d−1. The concentrations and consumption of illegal drugs measured during major holidays were significantly higher than those during non-holidays, indicating that there was holiday effect on the use of illegal drugs in the region of Guilin.
-
Key words:
- illegal drugs /
- sewage analysis /
- solid phase extraction /
- consumption
-
非法药物的滥用影响着人类健康、社会安定与国家经济,如今有170多个国家和地区存在着非法药物滥用的问题,全球非法药物的制造、贩卖和滥用问题日趋严重[1]. 因此,预防非法药物的使用,及时掌握区域非法药物的种类及消费量,精准追踪溯源,压缩违法犯罪活动空间,已经成为各国需要面临的共同问题. 最初关于非法药物的滥用情况是通过问卷调查、犯罪统计等传统社会调查方法获得的,但是这些调查方法具有一定的主观性与滞后性,可能导致非法药物消费情况的不正确评估. 2001年Daughton[2]提出一种污水流行病学的概念来评估非法药物的消费情况,即通过收集污水管道、泵站或者污水处理厂(WWTPs)进水处废水样品,测定污水中药物残留及其代谢物的浓度,结合WWTPs日处理量、服务区人口及药物排泄率等参数推算出WWTPs服务区域内非法药物的消费量. 与传统社会调查方法相比,污水流行病学能够在一定程度上克服主观因素影响,实时、客观地量化不同时间和地区的药物消费情况和人群使用趋势.
2005年Zuccato等[3]首次将这种概念应用于实际,通过收集意大利河流和WWTPs的水样以测定可卡因的含量. 结果发现, 1000名年轻人平均每天使用至少(27±5)剂的可卡因,远超官方报道的数字,随后基于污水流行病学的污水分析法作为一种客观、准确、有效的监测方法,在各国得到了广泛的运用[3-7]. 非法药物进入人体后以母体原型或者代谢产物的形式排泄,这些非法药物具有难降解特性,可以通过排水管网汇入WWTPs,但是污水中成分复杂,会对非法药物及其代谢物的测定产生干扰,且污水中大部分目标药物残留物(drug target residues,DTRs)的浓度极低,因此,污水样品的前处理显得尤为重要. 绝大部分报道都采用固相萃取(solid-phase-extraction,SPE)作为污水的前处理方式[8-9],如果SPE条件不同,对非法药物的萃取回收率也会不同,所以选定合适的SPE条件对污水中非法药物的测定至关重要.
国外的一些研究发现,重大节日如音乐节等期间污水中非法药物的负荷量较正常周呈现出增加的趋势[9-10]. Jiang等[11]发现,中国台湾垦丁地区青年节期间非法药物的浓度明显高于旅游淡季,而关于内地典型旅游城市重大节假日期间非法药物的滥用量鲜有报道. 本研究采用污水分析法对中国典型旅游城市桂林市某污水处理厂的重大节假日与日常生活期间进水废水中常见非法药物甲基苯丙胺和氯胺酮及其代谢物的浓度进行检测,并通过反推模型推算不同时期的甲基苯丙胺与氯胺酮的滥用量. 同时运用SPE技术比较前处理条件(Oasis HLB 和Oasis MCX 两种SPE柱)对模拟样品中甲基苯丙胺和氯胺酮及其代谢物的萃取回收率,选定最适合桂林市污水中甲基苯丙胺(METH)和氯胺酮(KET)及其代谢物苯丙胺(AMP)和去甲氯胺酮(NK)前处理的方法. 从而为桂林市该区域非法药物的滥用与测定信息提供初步数据,以期为毒品滥用监测及禁毒工作提供科学依据.
1. 材料与方法(Materials and methods)
1.1 实验试剂及仪器
甲基苯丙胺(METH)、苯丙胺(AMP)、氯胺酮(KET)、去甲氯胺酮(NK)标准溶液及其相应的氘代内标替代物溶液METH-D5、AMP-D5、KET-D4、NK-D4购自美国Cerilliant公司,甲醇(HPLC级),甲酸(HPLC级)均购自上海麦克林生化科技有限公司. 氨水(AR)、盐酸(AR)购自杭州龙山精细化工有限公司,实验室用水均为超纯水.
主要仪器及耗材:固相萃取柱(Waters Oasis MCX,60 mg,3 mL;Waters Oasis HLB 60 mg,3 mL)购自美国Waters公司,高效液相色谱-串联质谱联用仪:Agilent 1260-6460,氮吹仪(上海精其仪器有限公司),12位固相萃取装置(上海析友分析仪器有限公司)等.
1.2 标准溶液的配制
分别吸取METH、AMP、KET、NK的标准溶液(1 mg·mL−1)用甲醇配制成质量浓度为100 μg·mL−1的混合标准一级储备液,取同位素内标溶液(100 μg·mL−1)用甲醇配制成质量浓度为10 μg·mL−1的混合同位素内标一级储备液. 使用时将混合标准一级储备液用甲醇配制成质量浓度为0.5—250 μg·L−1不同浓度梯度的标准曲线混合溶液,再分别用50 mL纯水制备成浓度梯度为1—500 ng·L−1的模拟样品. 上述每个浓度梯度的模拟样品等量加入100 μL混合同位素(50 μg·L−1)内标溶液,以补偿样品制备过程中的基质效应和损失.
1.3 样品采集
2021年10月2日—7日、10月17日—23日、12月21日—26日采集桂林市某污水处理厂的进水处废水样品,该污水处理厂主要服务桂林市中南区,只接收生活污水. 污水处理厂设计处理约38万居民人口的生活废水,3次采样期间平均日处理量分别为94826、92341、60074 m3·d−1,与全国其它地区的污水处理厂相比,该污水处理厂的处理水量属于中等偏下水平[7]. 使用便携式自动采样器(启恒环保HX-A型)每半个小时等量采集废水,等比例混合24 h的污水样品,混合样品收集完后立即用浓盐酸酸化至pH=2并在-20 ℃条件下储存,直至分析.
1.4 样品前处理
将采集后的混合样品解冻后使用玻璃纤维滤膜(0.45 μm)过滤,取50 mL过滤后的废水样品加入50 μg·L−1的混合同位素内标溶液100 μL,充分混合后使用下述最优的SPE条件进行前处理,每个样品制备3个平行样,空白样品与样品同时同步骤测定. Oasis-HLB和Oasis-MCX这两种SPE柱对碱性化合物具有高选择性和灵敏度,本研究事先使用超纯水制备成模拟样品考察这两种SPE柱对甲基苯丙胺和氯胺酮的萃取回收率.
参照Nd等[12]的方法使用Oasis-HLB(Waters Oasis HLB 60 mg,3 mL)固相萃取柱对非法药物进行富集. 依次使用6 mL甲醇和6 mL超纯水活化SPE柱,随后在HLB固相萃取柱上加入有混合同位素内标的50 mL污水样品,样品在SPE柱上以约1 mL·min−1的速率萃取,使用3 mL超纯水清洗SPE柱,柱子在真空下干燥20 min,最后用6 mL甲醇洗脱,洗脱液40 ℃氮吹至近干,再用500 μL甲醇溶液复溶,复溶液过0.22 μm有机滤膜后上机测定. 使用Oasis-MCX(Waters Oasis MCX 60 mg,3 mL)固相萃取柱富集非法药物时参照Jin等[13]的方法. SPE柱依次用4 mL甲醇和4 mL pH=2的超纯水活化,以1 mL·min−1的速率上样,上样结束后将SPE柱真空干燥20 min,使用4 mL的甲醇淋洗萃取柱,最后将4 mL的5%氨水-甲醇以1 mL·min−1的速率洗脱并收集洗脱液,萃取完成后将洗脱液40 ℃氮吹至近干,用300 μL的0.1%甲酸水溶液复溶,复溶液过0.22 μm有机滤膜后上机测定.
1.5 仪器条件
色谱条件:液相色谱柱:Shim-pack GIST C18(100 mm×2.1 mm,2 μm,日本岛津),柱温:30 ℃,进样量3 μL,流动相为0.1%甲酸水溶液(A相)—乙腈(B相)体系,流速为0.3 mL·min−1,洗脱梯度为:0—1.5 min:20% B;1.5—2.25 min:80% B;2.25—3.1 min:95% B;3.1—5.0 min:20% B,保留时间为8 min.
质谱条件:以电喷雾电离(ESI),采用正离子模式,多反应监测(MRM)模式检测,毛细管电压:3000 V,负离子:3000 V,干燥气温度:325 ℃,干燥气流量:12 L·min−1,脱溶剂和雾化气体是氮气,雾化器压力:40 psi,经优化后,METH、METH-D5、AMP、AMP-D5、KET、KET-D4、NK、NK-D4质谱参数如表1所示.
表 1 优化后的毒品及其代谢物的质谱参数Table 1. Optimized MS parameters of drugs and their metabolites化合物Compound name 母离子Precursor ion 子离子Product ion 碎裂电压/VFragmentor 碰撞能量/eVCollision energy METH 150.1 91.1 85 17 65.1 45 METH-D5 155.2 92 17 7 91 7 AMP 136.1 119.1 58 5 91.1 13 AMP-D5 141.1 124.2 58 5 93.1 13 KET 238.1 125 98 25 89.1 65 KET-D4 242.1 129.1 98 25 92.1 69 NK 224.1 207.1 88 10 125 22 NK-D4 228.1 211.1 83 10 129.1 22 1.6 方法验证与质量控制
对分析方法的检测限(LOD)、定量限(LOQ)、萃取回收率、基质效应进行验证保证分析过程中的质量控制,每10个样品中包含使用加标内标的超纯水程序空白,以检查潜在干扰和污染.
在50 mL pH=2的超纯水中定量加入目标分析物的混合标准溶液(METH、AMP、KET和NK)和等量的混合内标溶液,混合标准溶液梯度共设置3个低(10 ng·L−1)、中(50 ng·L−1)、高浓度(400 ng·L−1),每个浓度梯度设置7个平行,同时设置一组流程空白,流程空白仅加入等量的混合内标溶液不加目标分析物,分别使用”1.3”中所述的两种SPE方法对模拟样品进行前处理并进行测定. 根据空白和加标样品的测定数据计算提取回收率,以S/N>3为检出限,S/N>10为定量限,并且分别对样品连续多次测定(n=3)和多天重复测定(n=3)来衡量仪器的日内精密度与日间精密度.
1.7 非法药物消费量计算
目标分析物测定完浓度后,通过反推模型公式即可得到该区域的非法药物的消费量. 非法药物的反算公式如下:
千人日均消费量(mg⋅d−1)=目标物分析物浓度(ng⋅L−1)×进水流量(L⋅d−1)×f代谢物服务区人口 千人日均消费量是每千人每日的药物消费量,单位是mg·d−1;目标物浓度是污水厂每个采样周期内DTRs的平均浓度,单位是ng·L−1;进水流量是污水厂采样周期内的进水流量平均值,单位是L·d−1;
f代谢物 1.8 数据分析
利用SPSS 22.0(IBM, USA)对数据进行分析,非法药物及其代谢物的浓度单位为 ng·L−1,千人日均消费量的单位为 mg·d−1. 采用皮尔森相关分析检验非法药物与其代谢物之间的相关性,采用单因素方差分析检验不同时期非法药物浓度和滥用量的差异,采用t检验分析节假日与日常生活期间非法药物浓度和滥用量的差异,所有的结果均以P<0.05判定是否存在显著性.
2. 结果与讨论(Results and discussion)
2.1 方法学验证
本研究以3倍、10倍信噪比计算出检出限和定量限. 标准工作曲线范围为1—500 ng·L−1,目标分析物与相应氘代内标的定量离子对峰面积比y为纵坐标、标准曲线中目标物的含量x为横坐标进行线性回归,得到线性方程. 结果见表2,结果显示,两种固相萃取条件下,四种毒品及其代谢物质量浓度在曲线范围内呈现较良好的线性关系,其相关系数R2为0.9911—0.9977,LODs为0.65—1.43 ng·L−1,LOQs为1.91—4.32 ng·L−1.
表 2 不同SPE柱条件下目标物的线性范围、回归方程、相关系数、检出限和定量限Table 2. Linear ranges, regression equation, correlation coefficients, limits of detection(LOD), and limits of quantitation(LOQ) of DTRs under different SPE column conditions分析物Analyte 线性范围/(ng·L−1)Linear range 回归方程Regression equation R2 检出限/(ng·L−1)LOD 定量限/(ng·L−1)LOQ MCX METH 1—500 y = 0.0565x + 0.8173 0.9963 0.72 2.36 AMP 1—500 y = 0.0505x + 0.6301 0.9977 0.94 2.74 KET 1—500 y = 0.0344x + 0.404 0.9970 0.65 1.91 NK 1—500 y = 0.0291x + 0.4297 0.9944 1.22 3.60 HLB METH 1—500 y = 0.0377x + 0.98 0.9916 1.35 4.17 AMP 1—500 y = 0.031x + 1.0509 0.9859 1.43 4.32 KET 1—500 y = 0.0218x + 0.3735 0.9950 0.76 2.18 NK 1—500 y = 0.0196x + 0.3346 0.9911 0.94 2.89 分别制备低、中、高的3个浓度(10、50、400 ng·L−1)的混合储备溶液,在3种处理条件下进行测试:在纯水样本处理前添加混合储备溶液,纯水样本SPE处理后添加储备溶液,纯水样品不做处理直接添加储备溶液,每组处理条件设置7组平行样,测定完后计算萃取回收率、基质效应及精密度. 计算结果如表3所示,计算得到使用Oasis MCX固相萃取柱处理纯水样品时平均回收率为81.44%—105.92%,基质效应范围为72.36%—124.61%. 而使用HLB固相萃取柱进行前处理时,平均回收率为64.45%—109.52%,基质效应范围为61.38%—130.54%,两种前处理方法得到的RSDs均小于10%.
表 3 不同SPE柱条件下目标物的回收率、基质效应和精密度Table 3. Recovery, matrix effect and precision of the DTRs under different SPE column conditions回收率/%Recovery(n=7) 基质效应/%Matrix effects 精密度/%RSD 分析物Analyte 日内Intraday 日间Interday 10 ng·L−1 50 ng·L−1 400 ng·L−1 10 ng·L−1 50 ng·L−1 400 ng·L−1 10 ng·L−1 50 ng·L−1 400 ng·L−1 10 ng·L−1 50 ng·L−1 400 ng·L−1 MCX METH 105.41 105.92 103.51 75.24 98.43 102.43 3.54 2.91 3.16 6.42 5.33 5.58 AMP 97.16 103.04 98.27 87.52 104.92 89.59 4.16 2.36 4.04 6.24 5.04 5.25 KET 104.63 96.12 105.31 72.36 106.36 110.54 2.48 4.87 3.55 8.68 4.82 7.03 NK 81.44 92.33 103.64 122.43 124.61 101.92 2.13 3.32 2.73 9.75 8.13 8.62 HLB METH 95.72 109.52 93.18 61.38 125.41 112.43 5.82 4.90 5.36 5.53 6.49 6.24 AMP 95.15 99.84 102.42 130.54 101.47 95.60 4.03 6.93 6.35 6.14 7.33 7.90 KET 64.45 81.32 72.03 64.46 105.53 88.74 5.00 4.24 6.84 8.18 8.62 9.04 NK 68.86 73.54 80.01 103.60 115.51 105.27 5.09 4.16 6.08 9.06 9.70 8.43 通过比较两种SPE柱及固相萃取条件的萃取回收率和基质效应,发现混合型阳离子交换固相萃取小柱Oasis MCX对这4种毒品及其代谢物的分离效果良好,较亲水亲脂反相吸附萃取小柱Oasis HLB的回收率更高,能够更好地满足本研究中非法药物定量准确度的要求. 根据研究表明,Oasis MCX的吸附剂是含亲水基团的聚苯乙烯/二乙烯基苯共聚物上键合磺酸基团,能更有效的提取碱性化合物[18-19]. 甲基苯丙胺和氯胺酮及其代谢产物具有含氮的碱性基团,因此Oasis MCX柱能够更有效满足富集要求,所以本研究在现实污水样品前处理及后续实验中均考虑1.3使用Oasis-MCX固相萃取柱萃取富集目标分析物的方法.
2.2 非法药物的赋存特征
本研究采样期间,WWTP相应的非法药物及其代谢物的浓度水平如图1所示. 这4种毒品及其代谢物在全部污水样品中都有检出,其中METH检出率为100%,AMP的检出率为76%. 重大节假日期间(国庆假期)采集的样品中METH的浓度范围为(6.49±2.44)—(214.46±0.25)ng·L−1,平均浓度为(60.17±0.75)ng·L−1. 后续两次非节假日期间测定样品中METH浓度范围分别为(6.78±0.35)—(13.87±1.07)ng·L−1和(5.57±0.72)—(30.85±10.93)ng·L−1,平均浓度分别为(9.40±1.03)ng·L−1和(19.30±8.20)ng·L−1. AMP在重大节假日期间的浓度范围为(1.62±0.63)—(58.62±6.85)ng·L−1,非节假日期间AMP浓度范围分别为ND(未检出)—(6.48±0.74)ng·L−1和ND—(9.62±2.05)ng·L−1. KET和NK并没有在所有样品中检出,检出率分别为76.47%和57.45%. 重大节假日期间样品中KET的浓度范围为(4.59±0.48)—(144.77±23.61) ng·L−1,非节假日期间样品中KET的最高浓度为(9.00±3.76)ng·L−1. NK在重大节假日期间的浓度范围为(1.02±0.39)—(114.57±6.67)ng·L−1,非节假日期间NK的最高浓度为(3.42±0.54)ng·L−1. 由上述结果得出,重大节假日期间非法药物及其代谢物的浓度显著高于非节假日期间(P<0.05),苯丙胺类兴奋剂和氯胺酮是各种娱乐场所和聚会中常用的违禁药物,重大节假日期间大量的娱乐活动使桂林市非法药物的使用可能具有节假日效应. 而日常生活期间12月份WWTP进水废水中毒品及其代谢物浓度较10月份浓度普遍提升(P<0.05),这可能是气温降低,人们生活用水减少,没有过多的稀释生活污水目标分析物的含量.
根据METH的药代动力学研究表明,大约42%±17%的METH未经过人体代谢通过尿液排出体外,摄入后的30%的AMP和40%的METH在尿液中以原型排出,而高达7%的METH在代谢后以AMP的形式排出[20],如果污水中的AMP与METH浓度比值范围在0.08—0.15则被认为是由METH代谢产生的[21-22]. 本研究中METH和AMP浓度之间有着显著性正相关(P<0.01,r=0.995),但绝大多数AMP和METH的浓度比大于0.15,表明该区域可能存在外在AMP的来源. 研究表明,服用部分合法药物例如治疗帕金森病的辅助药物可以经过人体代谢产生METH,但其对污水中浓度基本没有贡献,且在中国,尚无含有可直接代谢为AMP成分的处方药[22]. 因此,桂林市该WWTP所服务区域存在着METH和AMP滥用共存的现象,可能有非法制毒泄漏或倾倒苯丙胺兴奋剂等行为[23]. 将本研究与其他地区污水中苯丙胺兴奋剂浓度比较时发现该区域的平均浓度低于其他城市的平均浓度,中国广州市WWTPs的进水废水中METH的平均浓度为(145.6±100.3)ng·L-1[15],Xu等[24]报道的青岛WWTPs废水中METH的最高浓度高达1016.0 ng·L−1. 桂林市该区域的日常生活期间AMP的平均浓度为(4.01±1.48)ng·L−1,低于北京(15.2 ng·L−1)、上海(22.7 ng·L−1)、深圳(26.4 ng·L−1)的浓度水平[7, 25]. NK和KET浓度之间也呈现出显著性正相关(P<0.01,r=0.992). 人体摄入KET后30%的代谢产物为其原型,还有1.6%和6%代谢为脱氢去甲氯胺酮(DNKET)和去甲氯胺酮(NK)[24],KET经人体代谢后污水中残留的KET与NK原理比值为0.27—2.10[26]. 而本研究KET的浓度与NK的浓度的比值为0.19—6.84,表明可能存在向污水管网直接倾倒氯胺酮的情况,致使污水中KET的浓度总体上高于NK. 本区域非法药物的实际浓度比值都超过理论比值可能与桂林市持续开展一系列的禁毒活动有关,根据后续研究报道[27],从2021年第一季度开始桂林市公安局进行城市生活污水毒情检测,精准追踪溯源,对污水检测毒品含量高的区域,采取多种措施压缩毒品违法犯罪活动空间,从而可能存在向污水管网恶意倾倒或排放非法药物的现象.
2.3 消费量计算
通过反推模型对广西桂林市该WWTP服务区的METH和KET的消费量进行了回测,结果如图2所示. 该污水厂服务区域重大节假日期间METH的千人日均消费量范围为(5.94±2.44)—(196.4±0.25)mg·d−1,平均值为(55.11±94.22)mg·d−1,非节假日期间METH的千人日均消费量范围为(3.23±0.72)—(17.90±10.93)mg·d−1,平均值为(9.79±4.25)mg·d−1·. 以NK作为DTR进行对KET的消费量进行反演,结果得出桂林市该区域重大节假日期间KET的千人日均消费量范围为(5.37±0.39)—(606.12±6.67)mg·d−1,平均值为(173.82±1.83)mg·d−1,而非节假日的KET的千人日均消费量范围为(1.93±0.15)—(15.21±0.83)mg·d−1,平均值为(10.50±1.05)mg·d−1.
日常生活期间桂林市METH与KET的消费量没有明显的差异(P>0.05),但是重大节假日期间非法药物的滥用量存在着暴增的现象(P<0.05),说明桂林市非法药物的消费具有明显的节假日效应. 重大节假日期间桂林市该区域METH和KET的千人日均消费量与东北和广州节假日期间的浓度相当[15, 28],日常生活期间METH的千人日均消费量低于全国千人日均消费水平,根据以往研究报道我国主要城市的污水厂进水废水中的METH千人日均消费量为97.70 mg·d−1[7, 29]. 相比于中国主要城市的METH消费量,KET在中国城市的总体消费量要低得多,但是KET消费量的空间变化高于METH. 与北京(每千人2.2 mg·d−1)、上海(每千人9.1 mg·d−1)相比,本研究的KET消费量更高,这与华南地区KET的消费量大于华北地区的事实相符[7]. 本研究通过对桂林市重大节假日与日常生活期间非法药物的滥用量调查发现,重大节假日期间非法药物消费量显著高于日常生活期间的消费量,表明重大节假日期间非法药物滥用的管控不容忽视,仍需要对桂林市的非法药物滥用情况进行长期监测,深入开展“清源断流”行动,全力遏制非法药物滥用危害.
3. 结论(Conclusion)
(1)比较了Oasis MCX固相萃取柱与Oasis HLB固相萃取柱对甲基苯丙胺与氯胺酮及其代谢产物的萃取回收率. 研究发现Oasis MCX固相萃取柱对模拟样品中这4种毒品及其代谢物的分离效果更好. Oasis MCX固相萃取柱处理模拟样品时平均回收率为81.44%—105.92%,基质效应范围为72.36%—124.61%.
(2)桂林市该污水处理厂进水样品中METH与KET的检出率分别为100%和76.47%. AMP/METH与KET/NK的浓度比值超过理论代谢范围,说明桂林市开展一系列禁毒活动后,可能存在向污水管网恶意倾倒或排放非法药物的现象.
(3)桂林市该污水厂服务地区的日常生活期间METH的千人日均消费量最高为(17.90±10.93)mg·d−1,国庆节期间千人日均消费量最高为(196.4±0.25)mg·d−1. 日常生活期间KET的千人日均消费量最高为(15.21±0.83)mg·d−1,而国庆节期间千人日均消费量最高为(606.12±6.67)mg·d−1. 节假日期间非法药物的滥用量存在着暴增的现象,桂林市该区域非法药物的消费具有显著的节假日效应,表明桂林市节假日期间非法药物滥用的管控不容忽视.
-
表 1 优化后的毒品及其代谢物的质谱参数
Table 1. Optimized MS parameters of drugs and their metabolites
化合物Compound name 母离子Precursor ion 子离子Product ion 碎裂电压/VFragmentor 碰撞能量/eVCollision energy METH 150.1 91.1 85 17 65.1 45 METH-D5 155.2 92 17 7 91 7 AMP 136.1 119.1 58 5 91.1 13 AMP-D5 141.1 124.2 58 5 93.1 13 KET 238.1 125 98 25 89.1 65 KET-D4 242.1 129.1 98 25 92.1 69 NK 224.1 207.1 88 10 125 22 NK-D4 228.1 211.1 83 10 129.1 22 表 2 不同SPE柱条件下目标物的线性范围、回归方程、相关系数、检出限和定量限
Table 2. Linear ranges, regression equation, correlation coefficients, limits of detection(LOD), and limits of quantitation(LOQ) of DTRs under different SPE column conditions
分析物Analyte 线性范围/(ng·L−1)Linear range 回归方程Regression equation R2 检出限/(ng·L−1)LOD 定量限/(ng·L−1)LOQ MCX METH 1—500 y = 0.0565x + 0.8173 0.9963 0.72 2.36 AMP 1—500 y = 0.0505x + 0.6301 0.9977 0.94 2.74 KET 1—500 y = 0.0344x + 0.404 0.9970 0.65 1.91 NK 1—500 y = 0.0291x + 0.4297 0.9944 1.22 3.60 HLB METH 1—500 y = 0.0377x + 0.98 0.9916 1.35 4.17 AMP 1—500 y = 0.031x + 1.0509 0.9859 1.43 4.32 KET 1—500 y = 0.0218x + 0.3735 0.9950 0.76 2.18 NK 1—500 y = 0.0196x + 0.3346 0.9911 0.94 2.89 表 3 不同SPE柱条件下目标物的回收率、基质效应和精密度
Table 3. Recovery, matrix effect and precision of the DTRs under different SPE column conditions
回收率/%Recovery(n=7) 基质效应/%Matrix effects 精密度/%RSD 分析物Analyte 日内Intraday 日间Interday 10 ng·L−1 50 ng·L−1 400 ng·L−1 10 ng·L−1 50 ng·L−1 400 ng·L−1 10 ng·L−1 50 ng·L−1 400 ng·L−1 10 ng·L−1 50 ng·L−1 400 ng·L−1 MCX METH 105.41 105.92 103.51 75.24 98.43 102.43 3.54 2.91 3.16 6.42 5.33 5.58 AMP 97.16 103.04 98.27 87.52 104.92 89.59 4.16 2.36 4.04 6.24 5.04 5.25 KET 104.63 96.12 105.31 72.36 106.36 110.54 2.48 4.87 3.55 8.68 4.82 7.03 NK 81.44 92.33 103.64 122.43 124.61 101.92 2.13 3.32 2.73 9.75 8.13 8.62 HLB METH 95.72 109.52 93.18 61.38 125.41 112.43 5.82 4.90 5.36 5.53 6.49 6.24 AMP 95.15 99.84 102.42 130.54 101.47 95.60 4.03 6.93 6.35 6.14 7.33 7.90 KET 64.45 81.32 72.03 64.46 105.53 88.74 5.00 4.24 6.84 8.18 8.62 9.04 NK 68.86 73.54 80.01 103.60 115.51 105.27 5.09 4.16 6.08 9.06 9.70 8.43 -
[1] LIU Y, LIN D Y, WU B L, et al. Ketamine abuse potential and use disorder [J]. Brain Research Bulletin, 2016, 126: 68-73. doi: 10.1016/j.brainresbull.2016.05.016 [2] DAUGHTON C G, TERNES T A. Pharmaceuticals and personal care products in the environment: Agents of subtle change? [J]. Environmental Health Perspectives, 1999, 107(Suppl 6): 907-938. doi: 10.1289/ehp.99107s6907 [3] ZUCCATO E, CHIABRANDO C, CASTIGLIONI S, et al. Cocaine in surface waters: A new evidence-based tool to monitor community drug abuse [J]. Environmental Health:a Global Access Science Source, 2005, 4: 14. [4] CHIAIA A C, BANTA-GREEN C, FIELD J. Eliminating solid phase extraction with large-volume injection LC/MS/MS: Analysis of illicit and legal drugs and human urine indicators in US wastewaters [J]. Environmental Science & Technology, 2008, 42(23): 8841-8848. [5] METCALFE C, TINDALE K, LI H X, et al. Illicit drugs in Canadian municipal wastewater and estimates of community drug use [J]. Environmental Pollution, 2010, 158(10): 3179-3185. doi: 10.1016/j.envpol.2010.07.002 [6] LAI F Y, BRUNO R, LEUNG H W, et al. Estimating daily and diurnal variations of illicit drug use in Hong Kong: A pilot study of using wastewater analysis in an Asian metropolitan city [J]. Forensic Science International, 2013, 233(1/2/3): 126-132. [7] DU P, LI K Y, LI J, et al. Methamphetamine and ketamine use in major Chinese cities, a nationwide reconnaissance through sewage-based epidemiology [J]. Water Research, 2015, 84: 76-84. doi: 10.1016/j.watres.2015.07.025 [8] KRIZMAN-MATASIC I, KOSTANJEVECKI P, AHEL M, et al. Simultaneous analysis of opioid analgesics and their metabolites in municipal wastewaters and river water by liquid chromatography-tandem mass spectrometry [J]. Journal of Chromatography A, 2018, 1533: 102-111. doi: 10.1016/j.chroma.2017.12.025 [9] BIJLSMA L, CELMA A, CASTIGLIONI S, et al. Monitoring psychoactive substance use at six European festivals through wastewater and pooled urine analysis [J]. Science of the Total Environment, 2020, 725: 138376. doi: 10.1016/j.scitotenv.2020.138376 [10] BENAGLIA L, UDRISARD R, BANNWARTH A, et al. Testing wastewater from a music festival in Switzerland to assess illicit drug use [J]. Forensic Science International, 2020, 309: 110148. doi: 10.1016/j.forsciint.2020.110148 [11] JIANG J J, LEE C L, FANG M D, et al. Impacts of emerging contaminants on surrounding aquatic environment from a youth festival [J]. Environmental Science & Technology, 2015, 49(2): 792-799. [12] DAGLIOGLU N, GUZEL E Y, KILERCIOGLU S. Assessment of illicit drugs in wastewater and estimation of drugs of abuse in Adana Province, Turkey [J]. Forensic Science International, 2019, 294: 132-139. doi: 10.1016/j.forsciint.2018.11.012 [13] JIN H B, YANG D, HAO Y B, et al. Estimation of the psychoactive substances consumption within 12 wastewater treatment plants service areas in a certain city of Guangxi, China applying wastewater-based epidemiology [J]. Science of the Total Environment, 2021, 778: 146370. doi: 10.1016/j.scitotenv.2021.146370 [14] LIU S Y, YU W J, WANG Y R, et al. Tracing consumption patterns of stimulants, opioids, and ketamine in China by wastewater-based epidemiology [J]. Environmental Science and Pollution Research International, 2021, 28(13): 16754-16766. doi: 10.1007/s11356-020-12035-w [15] ZHANG X H, HUANG R H, LI P, et al. Temporal profile of illicit drug consumption in Guangzhou, China monitored by wastewater-based epidemiology [J]. Environmental Science and Pollution Research International, 2019, 26(23): 23593-23602. doi: 10.1007/s11356-019-05575-3 [16] 刘春叶, 王喆, 冯佳铭, 等. 污水流行病学调查辽宁和吉林两省甲基苯丙胺滥用量和流行率 [J]. 环境化学, 2018, 37(8): 1763-1769. doi: 10.7524/j.issn.0254-6108.2017121802 LIU C Y, WANG Z, FENG J M, et al. Methamphetamine consumption and prevalence in Liaoning and Jilin Provinces investigated by sewage epidemiology [J]. Environmental Chemistry, 2018, 37(8): 1763-1769(in Chinese). doi: 10.7524/j.issn.0254-6108.2017121802
[17] ZHENG Q D, REN Y, WANG Z, et al. Assessing patterns of illicit drug use in a Chinese City by analyzing daily wastewater samples over a one-year period [J]. Journal of Hazardous Materials, 2021, 417: 125999. doi: 10.1016/j.jhazmat.2021.125999 [18] 陈培培, 杜鹏, 周子雷, 等. 污水中新精神活性物质的分析方法优化及验证 [J]. 环境科学, 2018, 39(8): 3736-3743. doi: 10.13227/j.hjkx.201712251 CHEN P P, DU P, ZHOU Z L, et al. Optimization and validation of the analytical method to detect new psychoactive substances in wastewater [J]. Environmental Science, 2018, 39(8): 3736-3743(in Chinese). doi: 10.13227/j.hjkx.201712251
[19] BIJLSMA L, SANCHO J V, PITARCH E, et al. Simultaneous ultra-high-pressure liquid chromatography-tandem mass spectrometry determination of amphetamine and amphetamine-like stimulants, cocaine and its metabolites, and a Cannabis metabolite in surface water and urban wastewater [J]. Journal of Chromatography A, 2009, 1216(15): 3078-3089. doi: 10.1016/j.chroma.2009.01.067 [20] PACHECO FERREIRA A, . Estimaciones del consumo de drogas ilícitas derivadas del análisis de Aguas residuales: Una revisión crítica[J]. Revista De La Universidad Industrial De Santander Salud, 2019: 69-80. [21] ZUCCATO E, CHIABRANDO C, CASTIGLIONI S, et al. Estimating community drug abuse by wastewater analysis [J]. Environmental Health Perspectives, 2008, 116(8): 1027-1032. doi: 10.1289/ehp.11022 [22] KHAN U, NICELL J A. Sewer epidemiology mass balances for assessing the illicit use of methamphetamine, amphetamine and tetrahydrocannabinol [J]. Science of the Total Environment, 2012, 421/422: 144-162. doi: 10.1016/j.scitotenv.2012.01.020 [23] 王喆. 基于市政污水分析监测城市甲基苯丙胺滥用长期趋势[D]. 大连: 大连海事大学, 2019. WANG Z. Long-term monitoring of urban methamphetamine abuse based on municipal wastewater analysis[D]. Dalian: Dalian Maritime University, 2019(in Chinese).
[24] BAKER D R, BARRON L, KASPRZYK-HORDERN B. Illicit and pharmaceutical drug consumption estimated via wastewater analysis. Part A: Chemical analysis and drug use estimates [J]. The Science of the Total Environment, 2014, 487: 629-641. doi: 10.1016/j.scitotenv.2013.11.107 [25] XU Z Q, DU P, LI K Y, et al. Tracing methamphetamine and amphetamine sources in wastewater and receiving waters via concentration and enantiomeric profiling [J]. Science of the Total Environment, 2017, 601/602: 159-166. doi: 10.1016/j.scitotenv.2017.05.045 [26] MOORE K A, SKLEROV J, LEVINE B, et al. Urine concentrations of ketamine and norketamine following illegal consumption [J]. Journal of Analytical Toxicology, 2001, 25(7): 583-588. doi: 10.1093/jat/25.7.583 [27] 巫美桥红, 莫世鹏. 临桂区: 推进智慧禁毒 实现精确防控[N]. 广西日报, 2021-05-17(9). [28] 姚远. 东北典型城市甲基苯丙胺节假日滥用规律研究[D]. 大连: 大连海事大学, 2019. YAO Y. Methamphetamine use pattern in holidays at A typical city of northeast China[D]. Dalian: Dalian Maritime University, 2019(in Chinese).
[29] DU P, ZHENG Q D, THOMAS K V, et al. A revised excretion factor for estimating ketamine consumption by wastewater-based epidemiology - Utilising wastewater and seizure data [J]. Environment International, 2020, 138: 105645. doi: 10.1016/j.envint.2020.105645 -






 DownLoad:
DownLoad: