-
自工业革命以来,化石燃料燃烧、化肥施用以及畜牧业发展等使得向大气中排放的活性氮激增,而大约60%的活性氮以干湿沉降的形式返回陆地和水生生态系统,导致全球氮沉降量增加了2.5倍[1]. 过量的氮沉降可引发土壤营养元素淋失[2]、水体富营养化[3]、生物多样性丧失[4]和氮饱和[5]等负面效应,进而影响了陆地和水生生态系统的健康和服务功能[6].
氨(NH3) 是大气中含量最丰富的碱性气体,可与酸性气体(HNO3和H2SO4)快速反应形成铵盐气溶胶,对空气质量和人体健康产生危害[7]. 存在于大气中的NH3和铵盐以干湿沉降的形式重新进入陆地或水生生态系统,是大气氮沉降的重要活性氮组分[8]. 已有研究表明,美国的氮沉降已经由NOy沉降转变为以NHx沉降为主,而NHx在中国的氮沉降中也起着关键作用,如作为全球NH3浓度较高的热点区之一的华北平原,NHx沉降占总氮沉降量的71%—88%[9-10]. 尽管欧盟已针对畜禽养殖和化肥施用实施NH3减排,但全球大部分地区仍未对NH3排放进行有效管控,在2002—2013年间,卫星观测到美国、欧盟和中国的农业区每年大气NH3的浓度分别以2.61%、1.83%和2.27%的速率显著上升[11-12]. 因此,确定和量化NH3的主要来源,从而制定有针对性的减排措施,对于氮污染防控具有重要的科学意义和迫切的现实需求.
NH3的来源复杂多变,已有研究认为,氮肥挥发、牲畜排放、化石燃料燃烧和交通运输排放是大气中NH3的主要来源[13-14]. 卫星和地面观测资料显示,我国NH3的高值区华北平原,除了农业区外,城市大气NH3浓度也相对较高,因而大气中的NH3尤其是城市大气环境中的NH3主要来源是农牧业等农业源还是工业和机动车排放等非农业源存在争议[15-16]. 稳定氮同位素技术为解析痕量气体和颗粒物来源提供了有效工具,不同NH3源排放的NH3具有不同的氮同位素特征[17]. Feng等基于氮稳定同位素方法比较了华北平原典型农业县农村和城市中冬季大气NH3的主要来源,发现农村地区大气NH3的排放源以施肥和畜牧业等农业源为主(56%±3%),而城市地区则主要来自化石燃料、废弃物和生物质燃烧等非农业源(56%±2%)[18]. Pan等通过对大气气溶胶中氨氮的δ15N值研究发现,北京冬季雾霾污染期间气溶胶中NH3有90%来自于化石燃料燃烧排放[16]. Wu等利用MixSIAR同位素混合模型解析了夏季北京城区3个不同高度边界层气溶胶中NH4+的来源,认为农业源对城市气溶胶中NH4+的贡献随着距离地面高度的升高而增加,距离地面8 m处农业源的贡献率为47%,而高海拔区域(距离地面120 m和260 m)农业源的贡献率达到51%—56%[19]. 由于NH3形成气溶胶态NH4+过程中,NH3↔ NH4+之间的平衡反应导致15N在气溶胶中的NH4+中优先富集,而14N在NH3中优先富集,从而使得气溶胶中NH4+的δ15N-NH4+值普遍高于前体气NH3的δ15N-NH3值[20-21]. 因此,为确保NH3溯源准确,在分析过程中应充分考虑NH3从源到汇的氮同位素分馏[22]. 目前,关于大气氮沉降化合物来源的研究主要集中在森林[6]、草地[4]、农田[7, 20]和城市[21, 23],关于水库氮沉降化合物来源的研究相对较少,少量基于稳定同位素溯源的研究主要集中在湿沉降[24-25],针对水源地干沉降中氨氮来源的研究鲜见报道.
丹江口水库是我国重大跨流域调水工程南水北调中线工程的水源地,取水口位于淅川县的陶岔. 根据近3个年度《河南省环境质量年报》提供的数据,丹江口水库取水口水质总体良好,水质符合Ⅱ类标准,但是总氮参与评价则其水质符合Ⅳ类标准,潜在威胁不容忽视[26]. 已有研究表明,大气氮沉降是丹江口水库外源氮输入的重要途径之一,其中氨氮在大气途径的外源氮输入中占主导地位[27]. 本文以南水北调中线工程水源地淅川库区为研究对象,分析了库区大气干沉降中氨氮浓度及同位素的季节和空间变化特征,在此基础上,运用稳定同位素模型(SIAR)解析干沉降中氨氮的主要污染来源,为探索库区水体氮污染控制途径提供理论基础和数据支撑.
-
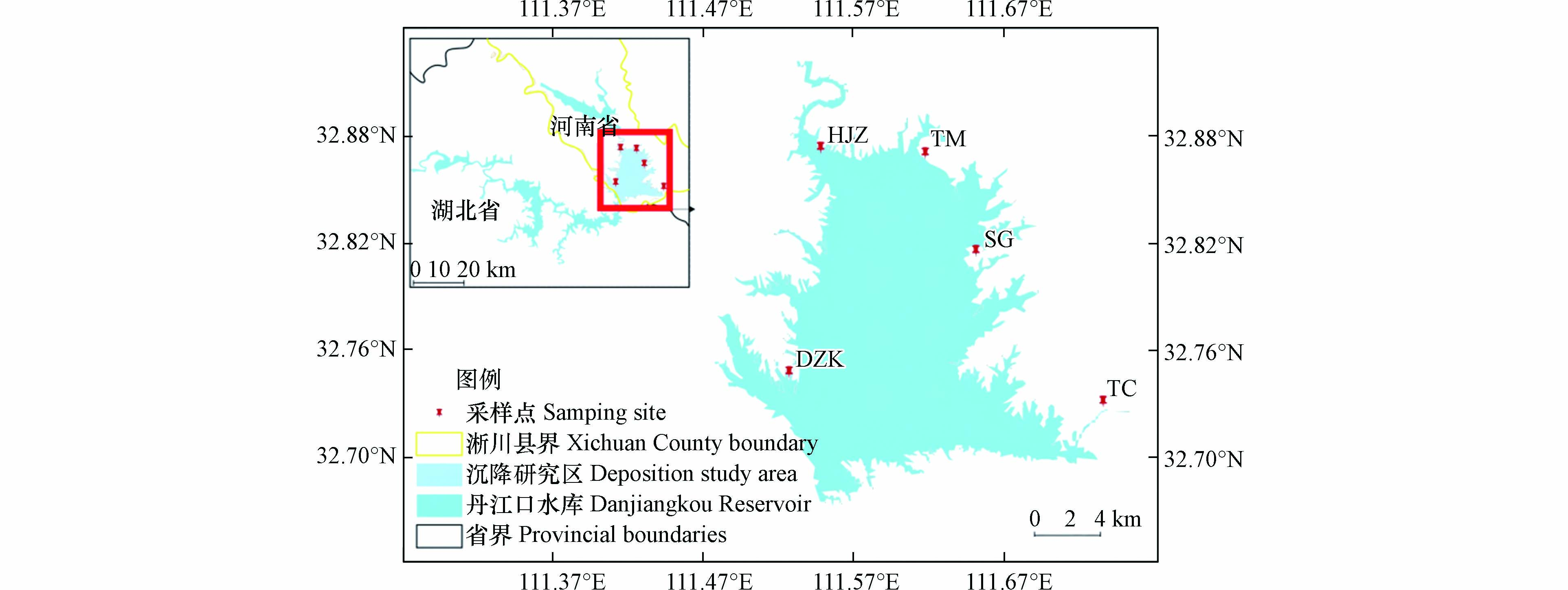
丹江口水库(32°36'—33°48' N,110°59'—111°49'E) 地处汉江干流与丹江交汇处下游0.8 km处,水域横跨鄂、豫两省,是南水北调中线工程水源地,取水口位于河南省淅川县. 丹江口水库淅川库区属北亚热带季风型大陆性气候,年均气温15.7 ℃,平均风速为2.5 m·s−1,年平均降水量为817.3 mm,自然降水分布不均,主要集中在6—8月. 库区位于暖温带落叶阔叶林向北亚热带常绿落叶阔叶混交林的过渡区,自然条件优越,森林保存完好,以常绿落叶阔叶林、针阔混交林、马尾松林、杉木林等为主,植物种类达1000多种. 区域内经济以农业为主,牲畜养殖为家庭散养. 库区周边土地利用类型主要为耕地和林地,以种植小麦、玉米和果树为主,主要施用尿素、复合肥和有机肥,年施肥量约为600 kg·hm−2[28]. 库区周边工业活动极少,存在一定的交通污染.
-
在丹江口水库淅川库区周边设置了5个监测点,监测点布设与库区现有的河南省水库水质自动监测站一致,分别是渠首所在地陶岔(TC)、支流老鹳河和丹江交汇处的黑鸡嘴(HJZ)、渔船和游船停靠的宋岗港口(SG)、紧邻耕地的土门(TM)以及紧邻园地和耕地的党子口(DZK),采样点位置及情况介绍如图1和表1所示.
于2019年9月—2020年8月,采用降水降尘自动采样器(SYC-2,中国青岛崂山电子仪器总厂)采集大气干沉降样品,采用湿法收集于干沉降采样缸(聚乙烯树脂材料,高度约50 cm,半径 7.5 cm)进行样品采集. 每月月初干沉降缸处于敞开状态,降水发生的瞬间安装在采样器侧面的感应装置自动将干沉降缸用盖密封,降水结束后盖子自动打开. 干沉降样品每周采集1次,测试时将每月采集的4个样品合并为1个样品. 夏季预先在干沉降缸内装入5 cm 高度蒸馏水和2 mol·L−1 的硫酸铜溶液1 mL,防止细菌和藻类生长,干沉降缸随时添加蒸馏水,确保液面高度;冬季在沉降缸中添加10 mL乙二醇,以防止溶液结冰. 采集样品置于棕聚乙烯瓶中,冰箱-20 ℃保存,1周内完成分析工作.
采用纳氏试剂法测定干沉降样品中氨氮(NH4+-N,检出限为0.025—2.00 mg·L−1)浓度,具体测试方法参考《水和废水监测分析方法》(第四版)[29]. 为保证数据的有效性和精密度,NH4+-N浓度测定采用平行双样,取2组测试结果的平均值作为检测值,相对偏差小于5%;每测定10个样品加入1个标准样品分析,加标回收率为95%—105%. 采用稳定同位素比质谱仪MAT-253测定氨氮同位素(δ15N-NH4+),分析方法参考文献[20, 30−31]. 首先加入BrO−将样品中NH4+氧化为NO2−,然后在强酸性条件下加入盐酸羟胺将NO2−还原成N2O,最后将所产生的N2O气体通入到同位素比质谱仪中进行稳定氮同位素比值测定. 样品中NH4+-N浓度低于12 μmol·L−1,不能检出δ15N-NH4+. 采用IAEA N1(δ15N=+0.4‰)、USGS25(δ15N=-30.4‰)和USGS26(δ15N=+53.7‰)的3种国际标准样的同位素测定结果,对样品中δ15N-NH4+结果进行校准. 3次平行测试的δ15N标准偏差小于0.3‰. δ15N-NH4+测试在中国科学院沈阳应用生态研究所完成.
-
干沉降通量采用推算法计算[27],即:
式中,Fd为大气NH4+-N月干沉降通量(kg·hm−2);Cr为观测月干沉降样品NH4+-N浓度(mg·L−1);Vd为干沉降样品体积( mL );S为干沉降缸的底面积(m2);10−2为单位换算系数.
-
NH3在大气中存在动力学和平衡分馏. 动力学反应为单向反应且发生时间短,生成的NH4+的δ15N值接近NH3的δ15N值,一般假设动力学反应的氮同位素分馏为0‰[20]. 平衡反应生成的NH4+随着在空气中转化或滞留时间而增加,所测δ15N-NH4+值不能完全表征初始NH3源的同位素信息[20-21]. 因此使用同位素质量平衡模型计算了初始NH3源的δ15N值,计算公式如下所示[21]:
式中,δ15N-NH3表示干沉降中NH4+-N初始源的同位素值;δ15N-NH4+(p)表示样品中测试的NH4+同位素值;f值为初始NH3转化为NH4+的比例(f= NH3/(NH3+NH4+),具体数值见前期研究[28];
εNH+4-NH3 为NH3和NH4+之间的平衡同位素分馏系数,已有研究发现,εNH+4-NH3 与温度之间存在线性拟合关系[32],计算公式如下所示[21]:式中,T表示温度(℃). 实验结果表明,
εNH+4-NH3 在25 ℃下的值为+33‰[33]. -
综合采样点地理位置以及NH3的可能来源,本研究期间大气NH3主要来源于化肥释放、畜禽排放、交通排放和燃料燃烧[28]. 化肥释放源、畜禽排放源、交通排放源和燃料燃烧源源谱的δ15N-NH3特征值采用文献报道的结果,分别为-28.3‰±5.8‰、-11.7‰±2.4‰、+4.2‰±1.8‰和-8.2‰±5.5‰[17]. 采用基于贝叶斯方程的稳定同位素模型(SIAR)分析不同来源对干沉降中NH4+-N的贡献程度,在RStudio软件中运行SIAR程序包.
-
采用描述性统计分析干沉降NH4+-N浓度及沉降通量的均值、标准差和变异系数等统计特征值;采用单因素方差分析分别比较干沉降中NH4+-N浓度及沉降通量在季节和空间上的差异显著性. 统计分析采用SPSS22.0软件包,绘图使用Origin10.0.
-
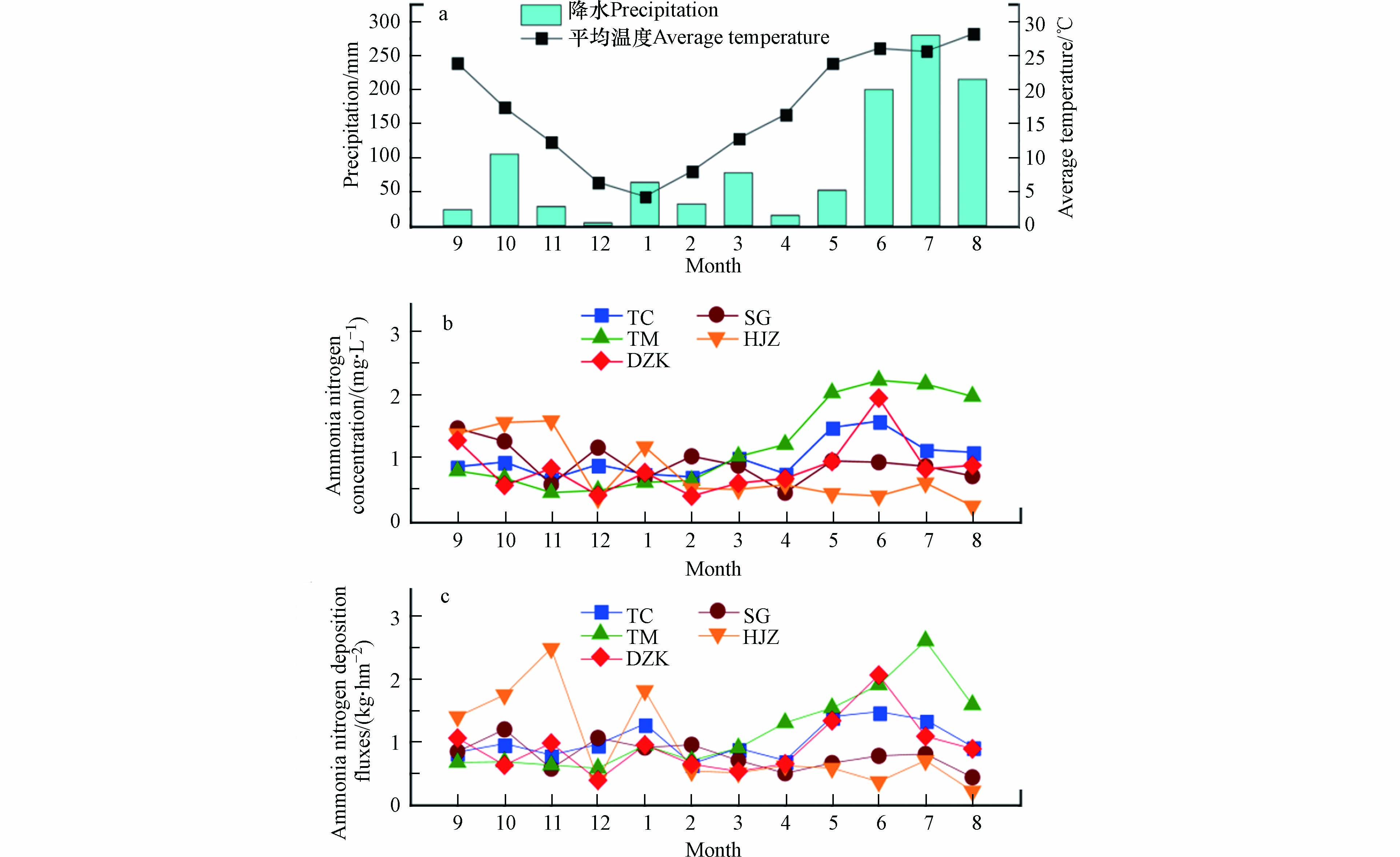
对丹江口水库淅川库区周边布设的5个监测点进行了为期1年的NH4+-N干沉降监测,库区月均气温、月均降水量以及不同监测点干沉降中NH4+-N浓度和沉降通量变化如图2和图3所示.
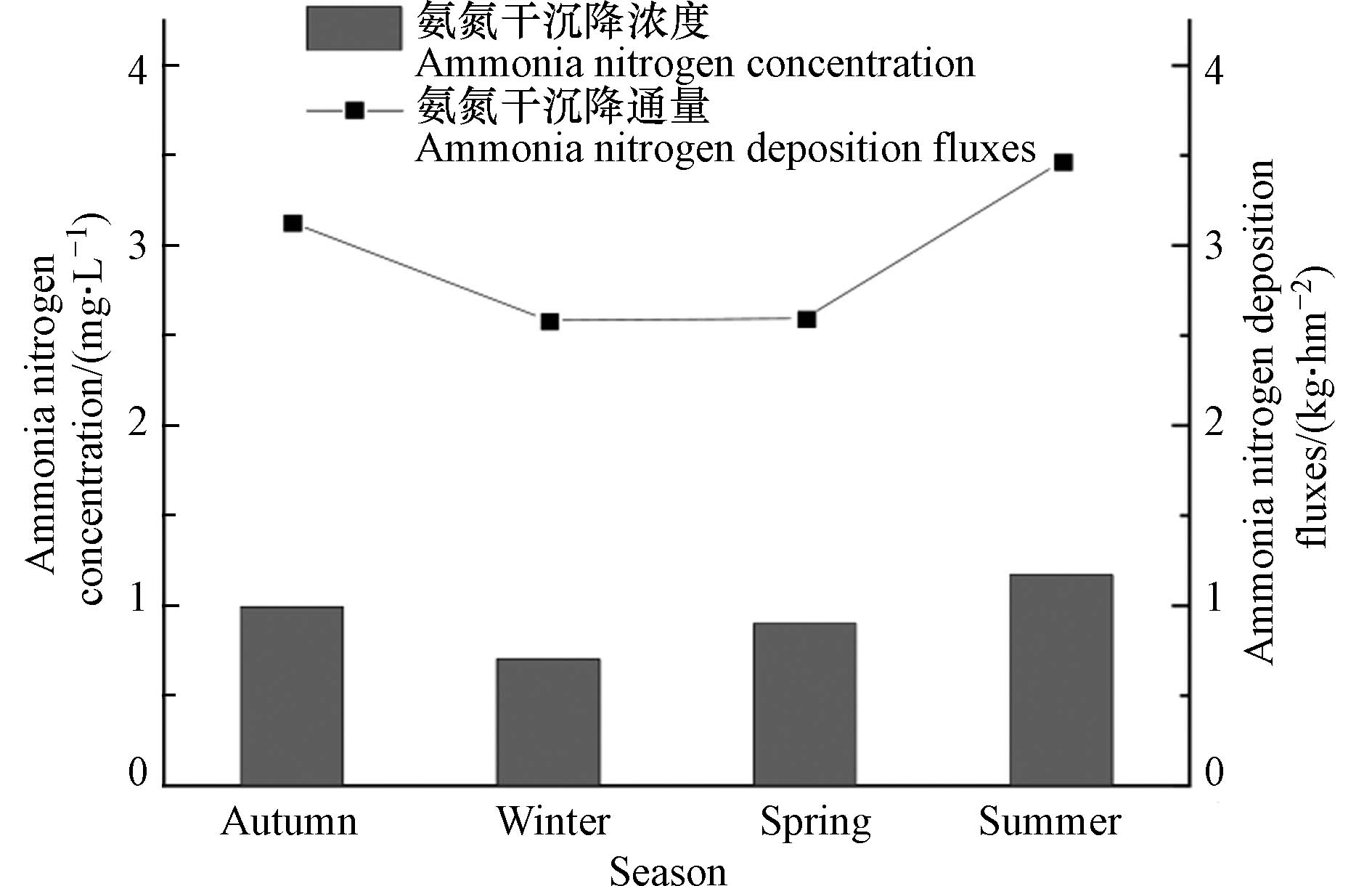
由图2(a)可知,全年库区温度变化明显,夏季(6—8月)炎热,气温相对稳定,月平均温度变化范围为25.6—28.2 ℃;冬季(12—次年2月)温度较低,温度变化范围为4.3—8.0 ℃;春季(3—5月)温度变化较大,整体上温度由低向高变化,温度变化范围介于12.8—23.8 ℃之间;秋季(9—11月)则相反,温度缓慢降低,温度变化范围介于12.3—23.9 ℃之间. 全年库区降水量主要集中在夏季,累计降水量694.6 mm,占总降水量的63.4%. 由图2(b)可知,丹江口水库淅川库区全年大气干沉降中NH4+-N月均浓度变化范围为0.24—2.23 mg·L−1,均值为0.96 mg·L−1,变异系数为26%. 从空间来看,干沉降中NH4+-N的月均浓度从大到小依次为:土门(TM)(1.19 mg·L−1),陶岔 (TC)(0.99 mg·L−1),宋岗(SG)(0.86 mg·L−1),党子口(DZK)(0.84 mg·L−1),黑鸡嘴(HJZ)(0.78 mg·L−1)(图2(b)). 从季节来看,干沉降中NH4+-N的月均浓度从大到小依次为:夏季(1.26 mg·L−1),秋季(0.99 mg·L−1),春季(0.90 mg·L−1),冬季(0.70 mg·L−1)(图3). 其中,NH4+-N月均浓度最大值出现在土门(TM)的6月份,最小值出现在黑鸡嘴(HJZ)点的8月份. 由图2(c)可知,丹江口水库淅川库区全年大气干沉降中NH4+-N沉降通量为11.77 kg·hm−2. 从空间来看,全年干沉降中NH4+-N沉降通量从大到小依次为:土门(TM)(14.16 kg·hm−2),陶岔 (TC)(12.36 kg·hm−2),黑鸡嘴(HJZ)(11.48 kg·hm−2),党子口(DZK)(11.32 kg·hm−2),宋岗(SG)(9.55 kg·hm−2)(图2(c)). 从季节来看,干沉降中NH4+-N沉降通量从大到小依次为:夏季(3.47 kg·hm−2),秋季(3.13 kg·hm−2),春季(2.59 kg·hm−2),冬季(2.58 kg·hm−2)(图3).
与我国其他水库大气干沉降中NH4+-N浓度对比(表2),受季风气候影响,丹江口水库淅川库区高于其他地区. 课题组前期研究发现,库区干沉降中NH4+-N沉降通量占氮素总沉降通量的20.4%[27]. 根据美国政府针对山地湖泊污染状况评估制定的氮沉降临界负荷为1.5 kg·hm−2·a−1[34]以及我国水域生态系统氮沉降临界负荷为10.0—20.0 kg·hm−2·a−1[35]来看,NH4+-N干沉降对丹江口水库水体氮污染存在一定的潜在生态风险.
单因素方差分析结果表明,干沉降中NH4+-N浓度在季节上表现出极显著差异性(F=5.152, P<0.01),在空间上表现出显著差异性(F=3.671, P<0.05). NH4+-N干沉降通量在季节上表现出显著差异性(F=2.949, P<0.05),在空间上则差异性不显著(F=0.900, P>0.05)(表3).
作为南水北调中线工程水源地,淅川县为了确保一库清水永续北送,库区周边以农业开发为主. 夏季是农作物生长的季节,施肥比较集中,氮肥施用后,在水解的过程中,土壤pH上升,导致土壤中NH4+-N含量快速增加,从而产生大量的NH3挥发,高温天气也使得NH3的挥发量增加[40]. 此外,高温也促进了畜禽粪便等NH3的排放[36],促使大气中NH3的浓度达到了年内最高峰,大量的NH3排放进入大气,随后在短距离内又沉降到地面,进而使得夏季干沉降中NH4+-N浓度较高. 秋季是农作物收获和播种的季节,施肥量高于春季和冬季,氮肥挥发使得秋季干沉降中的NH4+-N浓度也相对较高. NH3自排放源排放后一部分在附近源区数公里范围内沉降,剩余部分极易与水和酸性气体发生化学反应生成NH4+. 研究区大气NH3与NH4+的气粒转化比f值在春、夏、秋的3个季节均大于0.5,而在冬季小于0.5[28],表明春、夏、秋季节季淅川库区大气NHx以大气NH3存在为主,而冬季则气溶胶态NH4+是主导了NHx含量. 相较于春冬季节,夏季的温湿条件更有助于NH3↔NH4+之间的气固转化速度加快,从而使得大气NH3与酸性物质反应生成更多的(NH4)2SO4和NH4NO3等铵盐[41-42]. 在空间上,以农业活动区为主的TM观测点NH4+-N干沉降通量最高,而渔船和游船停靠码头的SG观测点则NH4+-N干沉降通量最低,也进一步说明氮肥施用是库区干沉降中NH4+-N的重要来源. 因此,农业区大气NH4+-N污染较为严重,存在较高的NH4+-N大气沉降输入.
-
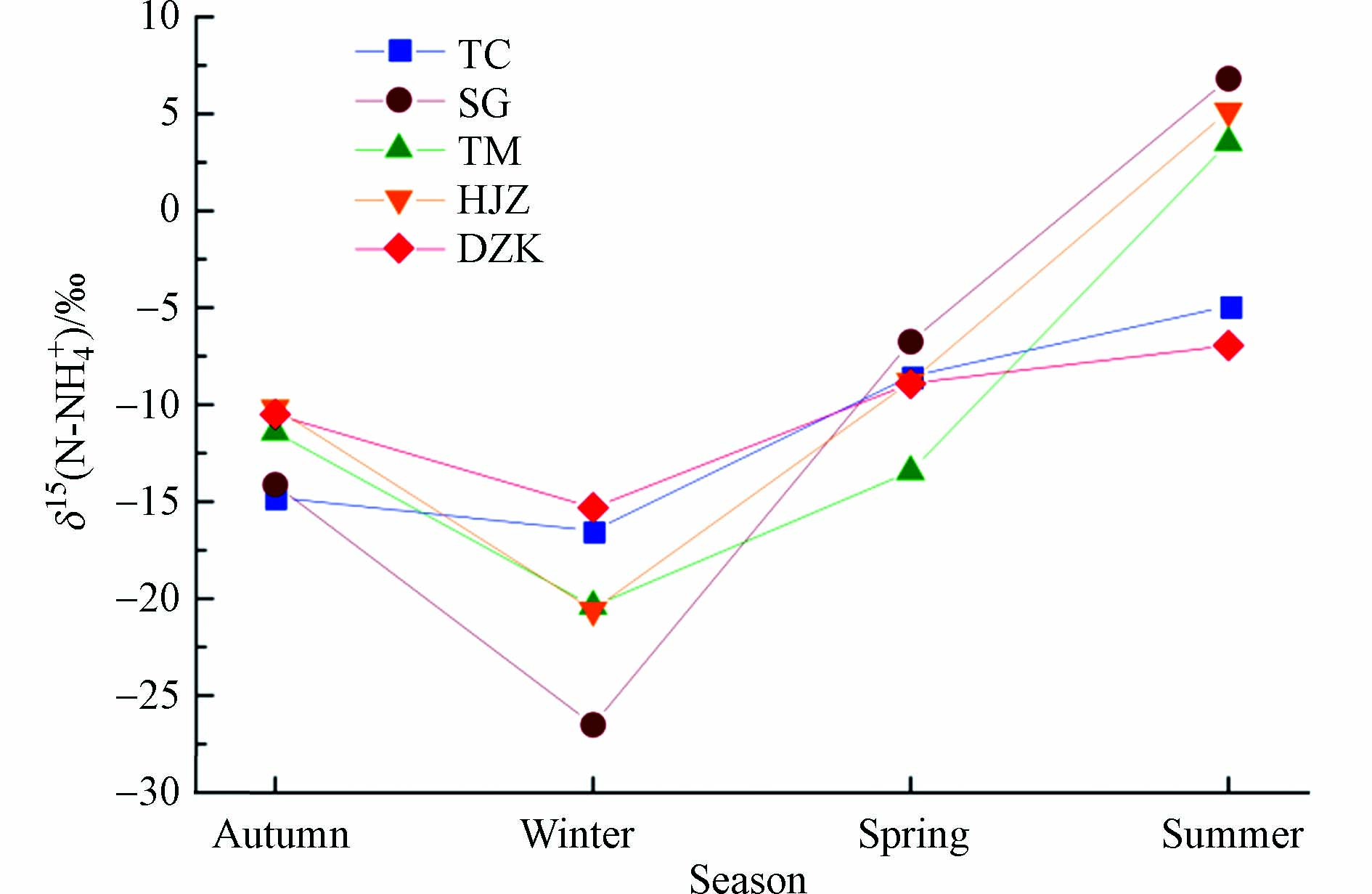
丹江口水库淅川库区干沉降中δ15N-NH4+分布如图4所示. 由图4可知,干沉降中δ15N-NH4+值范围为-26.50‰—+6.81‰,存在较大波动,平均值为-9.20‰. 从空间上来看,黑鸡嘴(HJZ)、宋岗(SG)、党子口(DZK)、土门(TM)、陶岔(TC) 5个监测点干沉降中δ15N-NH4+值分别为−20.60‰—+5.14‰、−26.50‰—+6.81‰、−15.32‰—−6.95‰、−20.39‰—+3.51‰、−14.78‰—−4.91‰,平均值分别为−8.61‰、−10.14‰、−10.42‰、−10.43‰、−11.18‰. 从季节来看,干沉降中δ15N-NH4+的平均值在夏季(0.72‰)最高,春季(−9.29‰)和秋季(−12.20‰)次之,冬季(−19.86‰)最低.
干沉降中δ15N-NH4+值在季节和空间上的差异性与NH4+-N沉降通量相似,在季节上表现出极显著差异性(F=4.546, P<0.01),在空间上差异性不显著(F=1.334, P>0.05)(表3). 有研究表明,δ15N-NH4+值的季节性波动与δ15N-NH3的变化有关[43-45]. Kawashima和Kurahashi研究结果表明,受农业源的影响,颗粒物中δ15N-NH4+值表现出夏季高冬季低的趋势[46];Kundu和Park等认为气团携带了较高δ15N-NH4+值的生物质燃烧源导致韩国济州岛和白翎岛夏季和秋季δ15N-NH4+值较高[43-44]. 一般认为,在同位素动力学分馏的影响下,NH4+↔NH3相互转化达到平衡的过程中,重同位素15N在气溶胶NH4+中优先富集,而轻同位素14N优先释放,因此,较高的NH3浓度使得δ15N-NH3值较低[20-21]. 而本研究的监测结果显示,夏季较高NH3浓度情况下,δ15N-NH4+值也较高,说明干沉降中较高的δ15N-NH4+值可能受排放源和同位素平衡分馏效应的影响. 课题组研究表明,研究区夏季气粒转化比f值 (f= NH3/(NH3+NH4+)约为0.8,冬季约为0.4[28]. 夏季大气NH3处于富余状态,使得大气NH3向颗粒态NH4+转化过程加快,富余的NH4+与大气中的SO42−反应生成(NH4)2SO4,剩余的NH4+与NO3−或 Cl−反应生成NH4NO3或NH4Cl[23]. 同时夏季高温降低了大气颗粒物中挥发性铵盐(NH4NO3或NH4Cl)的稳定性[47],使反应逆向进行,从而增加了大气 NH3的浓度. 因此,夏季NH3↔NH4+之间频繁的转化过程使得同位素平衡分馏效应增强,从而得到干沉降中较高的δ15N-NH4+值. 此外,研究区夏季存在含有较高δ15N值的氮肥和畜禽粪便等挥发性NH3排放源,在高温下使得δ15N-NH4+达到了最大值.
-
不同污染源排放的NH3具有不同的氮同位素组成,因此利用δ15N-NH3可以表征和量化NH3污染来源[48]. 根据丹江口水库淅川库区NH4+-N的f值及平衡同位素分馏系数
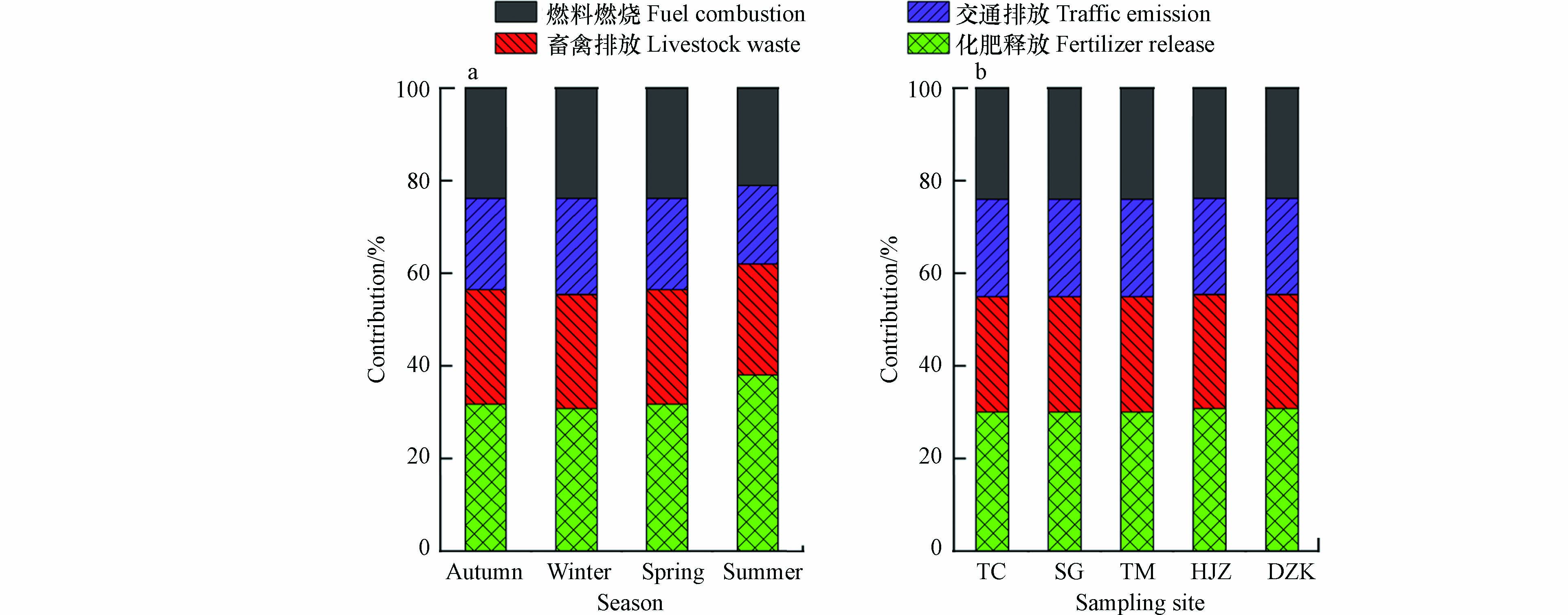
εNH+4-NH3 ,计算得出干沉降中NH4+-N初始源的δ15N-NH3值范围是−54.23‰—−24.98‰. 将计算所得的干沉降中NH4+-N初始源的δ15N-NH3值和文献报道的4种δ15N-NH3特征值用于SIAR模型进行源解析分析,计算得到丹江口水库淅川库区不同NH3排放源对干沉降中NH4+-N的贡献. 不同NH3污染源排放对库区干沉降中NH4+-N 的季节贡献率和空间贡献率如图5所示.由图5可知,化肥释放、畜禽排放、交通排放和燃料燃烧对干沉降中NH4+-N的贡献率分别为33%—40%、23%—25%、16%—19%、21%—23%,平均值分别为36%、24%、18%、22%. 由此可知,库区干沉降中NH4+-N的主要来源于农业源(化肥释放和畜禽排放),其贡献率为57%—63%,平均贡献率为60%. 其中,夏季农业源贡献率最高(63%),春季(59%)和冬季(58%)次之,秋季最低(57%)(图5(a)). 夏季农业源中64%来源于化肥释放,也进一步证实了夏季高温以及氮肥的大量施用是影响库区干沉降中NH4+-N的主要因素. 在党子口(DZK)、黑鸡嘴(HJZ)、陶岔(TC)、土门(TM)、宋岗(SG) 5个监测点的农业源贡献率分别为58%、57%、56%、56%、55%,其中党子口(DZK)农业源对干沉降中NH4+-N的贡献率最高、宋岗(SG)最低(图5(b)). 有研究表明,NH3通量在覆盖有植被的土地上具有双向性,一般采用大气与植物叶片界面的NH3补偿点来确定NH3通量是排放还是沉降[49]. 当大气中NH4+-N浓度高于补偿浓度时,NH3由大气向地表沉降;反之,则NH3由地表向大气排放[50]. 党子口(DZK)为典型的果园种植区,施肥使得果木冠层具有相对较高的NH3补偿点,氮肥的大量损失尤其是NH3挥发显著增加了大气中NH4+-N的沉降量,因而党子口(DZK) 农业源的贡献率相对较高. 宋岗(SG)位于码头,来往船只和车流量相对较大,交通排放源的贡献率增加,从而农业源的贡献率最低.
-
本研究解析了不同NH3排放源对干沉降中NH4+-N的贡献率,但是分析过程中仍然存在不确定性. 研究表明,NH4+-N来源解析与本地化NH3排放源的氮同位素源谱(δ15N-NH3)、气粒转化比f值以及温度密切相关[20-21]. 本文缺少本地化NH3排放源的δ15N-NH3值,而是引用文献报道的源谱,没有考虑不同NH3排放源的氮同位素特征值的区域差异. 同时,没有实测本地废弃物排放源的δ15N-NH3值,在运用SIAR进行源解析的过程中没有考虑废弃物源对干沉降中NH4+-N的贡献,也使得NH4+-N来源解析得到的贡献率存在差异. 大气气粒相互转化的复杂化学过程造成大气NH3源的δ15N值计算值与初始NH3源的δ15N值存在差异,也导致了溯源结果的不确定性. 此外,氮同位素平衡分馏系数
εNH+4-NH3 随着温度变化发生了改变. 根据公式(3),εNH+4-NH3 与温度呈线性拟合关系,温度降低1 ℃,则εNH+4-NH3 下降0.15‰[20]. 基于贝叶斯方程的稳定同位素模型虽然考虑了氮同位素平衡分馏对NH3污染源解析的影响,但本研究采用月平均温度计算εNH+4-NH3 ,也使得NH4+-N的来源解析存在一定的不确定性. 因此,在今后的工作中要重点考虑上述因素,以降低对溯源结果不确定性的影响. -
(1)丹江口水库淅川库区全年大气干沉降中NH4+-N月均浓度变化范围为0.24—2.23 mg·L−1,均值为0.96 mg·L−1;全年大气干沉降中NH4+-N沉降通量为11.77 kg·hm−2.
(2)库区干沉降中NH4+-N浓度和沉降通量在季节上分别表现出极显著差异性(P<0.01)和显著差异性(P<0.05),NH4+-N浓度在空间上也表现出显著差异性(P<0.05),沉降通量在空间上差异性不显著(P>0.05). 夏季NH4+-N浓度和沉降通量均最高,冬季最低,主要与夏季高温和大量氮肥施用有关.
(3)库区干沉降中δ15N-NH4+值范围为-26.50‰—+6.81‰,平均值为-9.20‰. δ15N-NH4+值在季节上表现出极显著差异性(P<0.01),在空间上差异性不显著(P>0.05). δ15N-NH4+值在夏季最高,春季和秋季次之,冬季最低,呈现夏季偏正,秋冬春季偏负的特征.
(4)库区干沉降中NH4+-N的主要来源于化肥释放和畜禽排放等农业源,其贡献率为58%—64%,平均贡献率为60%,其中化肥释放源和畜禽排放源贡献率分别为36%和24%. 夏季农业源贡献率最高(64%),其中42%来源于化肥释放,进一步证实了夏季高温以及氮肥的大量施用是影响库区干沉降中NH4+-N的主要因素.
丹江口水库淅川库区大气氨氮干沉降特征及源解析
Analysis of characteristics and sources of dry atmospheric ammonia nitrogen deposition in the Xichuan area of Danjiangkou reservoir
-
摘要: 为了解丹江口水库淅川库区大气干沉降中氨氮的沉降特征和主要来源,于2019年9月—2020年8月对库区周边设置的5个大气监测点进行干沉降样品采集,测定并分析了样品中氨氮浓度及其氮同位素,基于贝叶斯混合模型量化了氨氮的主要来源. 结果表明,库区大气干沉降中氨氮月均浓度为0.96 mg·L-1,全年大气干沉降中氨氮沉降通量为11.77 kg·hm-2,δ15N-NH4+值月均值为-9.20‰. 干沉降中氨氮沉降通量、浓度和δ15N-NH4+值的季节差异显著,均表现出夏季最高、春季和秋季次之、冬季最低的变化规律,主要与夏季高温和氮肥施用有关. 运用稳定同位素模型(SIAR)分析发现,库区干沉降中氨氮的主要污染源为农业源,贡献率为60%,其中化肥释放源和畜禽排放源贡献率分别为36%和24%. 夏季农业源贡献率最高,其中64%来源于化肥释放,进一步证实了夏季高温以及氮肥的大量施用是影响库区干沉降中氨氮的主要因素. 研究结果为探索库区水体氮污染控制途径提供理论基础和数据支撑.Abstract: In order to know the characteristics and sources of dry atmospheric ammonia nitrogen deposition in the Xichuan area of Danjiangkou reservoir, the dry deposition samples were collected at the five atmospheric deposition monitoring sites around the reservoir from September 2019 to August 2020.The concentrations and δ15N values of ammonia nitrogen were determined, and the fractional contributions of potential ammonia nitrogen sources were quantitatively calculated using a Bayesian mixing model. The results showed that the monthly averaged concentration of ammonia nitrogen was 0.96 mg·L-1, the annual flux of ammonia nitrogen dry deposition was 11.77 kg·hm-2, and the monthly averaged value of δ15N-NH4+ was -9.20‰ in the dry deposition samples. Significant seasonal differences in the fluxes of ammonia nitrogen dry deposition, concentrations and δ15N values of ammonia nitrogen were found, showing the following order: summer > spring > autumn > winter, which was mainly due to the application of chemical nitrogen fertilizers and high temperature in summer. The fractional contributions of chemical nitrogen fertilizer and livestock wastes were 36% and 24%, respectively, indicating that agricultural release contributed most. In summer, the fractional contribution of agricultural release was the largest, accounting for 64%, which further confirmed that ammonia nitrogen in dry atmospheric deposition primarily was controlled by high temperatures in summer and massive application of chemical nitrogen fertilizers. The results of this study may provide the theoretical and data support in controlling nitrogen pollution into the reservoir.
-
Key words:
- ammonia nitrogen /
- dry deposition /
- nitrogen isotopes /
- source analysis /
- Danjiangkou reservoir.
-
偶氮染料是纺织业中使用最多的一类染料 [1],具有难降解的特性。常见的处理方法包括物化法、化学法和生物法。物化法不能彻底降解污染物,化学法成本过高,生物法降解缓慢[2],因此限制了这些方法的应用。
次氯酸钠氧化法广泛用于降解废水中的污染物,并以污染物去除效率高、设备简单、经济性等优点而受到人们的重视。NaClO溶液的稳定性较差,大大降低了其氧化性的利用率。此外,采用NaClO直接氧化废水,会产生具有强致癌性的氯代有机物。增强NaClO的氧化性和消除氯代有机物对拓宽其在水处理中的应用极为重要。镍基催化剂能促进NaClO溶液的分解增强其氧化性,且以催化效果好、便宜等优点而备受关注[3]。NaClO在氧化镍的作用下生成具有极强活性的原子氧,迅速氧化废水中的污染物,从而达到去除COD和脱色的目的[4-5]。本课题组研发的NaClO催化氧化法能有效降解活性艳红K-2BP、酸性大红3R等偶氮染料,活性艳红K-2BP的脱色率在120 min达到94%以上[6],而酸性大红3R的脱色率在35 min达到90%以上。原子氧在脱色降解过程起了主导作用,因此未在染料降解产物中发现氯代有机物。
研究染料的分子结构与脱色性能之间的关系对废水的处理至关重要。染料种类繁多,结构各异,可以采用QSPR (quantitative molecular structure-properties relationships)法研究分子结构和脱色性能的关系。该方法简单易行,了解了分子结构信息,就可以分析和预测染料的理化性质或环境行为[7]。
本研究分别采用NaClO催化氧化法和NaClO氧化法脱色降解活性黄X-R废水,考察比较两种方法的脱色效果;比较催化氧化法对活性黄X-R和另外两种偶氮染料的脱色效果,在此基础上采用QSPR分析该方法处理不同染料效果存在差异的原因,进而指出其适用范围。本研究选择适当的染料分子结构描述符,通过线性回归法研究上述目标染料分子结构与NaClO催化氧化法对其脱色效果之间的关系。研究结果将为推广应用NaClO催化氧化法提供理论依据。
1. 材料与方法 (Materials and methods)
1.1 实验材料
催化剂载体选用水处理用耐酸碱的γ-Al2O3小球,参数如下:直径为 2−3 mm,Al2O3 > 92%,孔容为0.35 mL·g−1,比表面积大于300 m2·g−1。Na2S2O8 (99%)、NAOH (99%)、Ni(NO3)2·6H2O (99%)、H2SO4 (98%)、呋喃甲醇(99.2%)和叔丁醇(99.9%)均为分析纯,NaClO溶液有效氯含量大于10%。
仪器包括:ZYL便携式余氯分析仪、MIT-3F型COD检测仪、723N扫模型可见光分光光度计、Rigaku Smartlab9 x射线衍射仪(日本理学)、EscaLab 250Xi型X射线光电子能谱仪,Al-Kα射线单色源(美国赛默飞)、扫描电镜SEM(美国FEI Inspect F50)。
1.2 催化剂制备
催化剂制备步骤如下:先将γ-Al2O3小球浸泡在摩尔浓度为0.6 mol·L−1 Na2S2O8和0.5 mol·L−1 NaOH的混合液里,在振荡器上以100 r·min−1的频率振荡2 h,将得到的Na2S2O8-NaOH/Al2O3小球滤出后烘干。然后将Na2S2O8-NaOH/Al2O3小球浸泡在含有0.6 mol·L−1 Ni2+的溶液里发生反应,在γ-Al2O3表面形成一层镍氧化物/镍氢氧化物沉淀,将制得的小球滤出后烘干,得到镍基Al2O3小球。将得到的镍基Al2O3小球再次浸泡在Na2S2O8-NaOH混合液里,在振荡器上以100 r·min−1的频率振荡2 h后将催化剂小球滤出,用蒸馏水清洗。最后将洗净的催化剂置于马弗炉中低温焙烧2 h,制得催化氧化实验所需的催化剂样品。
Ni(OH)2为还原性氢氧化物,能和强氧化剂反应生成羟基氧化镍NiOOH。通过Ni2+在碱性溶液中被Na2S2O8氧化的反应来合成NiOOH(见式(1)和式(2)),从中可以看出,碱性条件促进Ni(OH)2和NiOOH的生成。
Ni2++2OH−⟶Ni(OH)2 (1) 2Ni(OH)2+S2O2−8+2OH−⟶2NiOOH+2SO2−4+2H2O (2) 在NiOOH存在的情况下,NaClO的分解反应2NaClO→2NaCl+O2↑可以看作是反应(3)和反应(4)的总和:
2NiOOH+NaClO⟶NaCl+2NiO2+H2O (3) 2NiO2+NaClO+H2O⟶2NiOOH+NaCl+O2 (4) 产生的氧分子能被物理吸附在镍基催化层上(式5),捕获电子后转化为化学吸附氧
O−2 O2(g)+S↔O2 (5) O2+e−↔O−2+∗ (6) O−2\xLeftrightarrowΔG1O−+O (7) O2\xLeftrightarrowΔG22O (8) 其中,O2(g)为气态氧,S为表面吸附位置,O2为表面物理吸附的氧,*和e−代表导带底部空位和导带电子,ΔG为反应能。反应产生的原子氧O非常活跃,可以快速氧化和分解有机物。羟基氧化镍可以长时间用作催化剂,因为它可以通过反应(3)和(4)进行再生利用。
1.3 活性黄X-R浓度的检测
染料废水在波长为390 nm处有最大特征吸收峰,在390 nm检测不同浓度废水的吸光度,建立质量浓度和吸光度的标准曲线方程y =96.877 x –1.1831,R2 = 0.9987。
1.4 染料脱色率分析
配制一定浓度的活性黄X-R溶液,加入一定量的NaClO溶液,充分搅拌,调节pH至所需值,得到废水/NaClO混合液。取50 mL混合液放入100 mL锥形瓶内,把一定量催化剂样品快速放入溶液中。在振荡器上以100 r·min−1的速度振荡120 min。分别在第10、30、50、70、90、120 min时取3 mL左右上清液,直接测其吸光度,利用标准曲线方程求得染料的浓度,按公式(9)计算其脱色率。测好吸光度后将染料溶液倒回锥形瓶中继续反应。
脱色率=C0−CtC0×100(%) (9) 式中,C0 和Ct 分别为初始染料浓度和t时刻染料浓度,mg·L−1。
1.5 自由基清除剂实验
配制质量浓度为200 mg·L−1的活性黄X-R溶液,加入120 mg·L−1的NaClO溶液,充分搅拌,调节到pH 9,得到废水/NaClO混合液。在两个相同组分的混合液中分别加入20 mmol·L−1的叔丁醇和呋喃甲醇,与催化剂一起放入100 mL锥形瓶内,在振荡器上以100 r·min−1的速度振荡反应,检测染料的脱色率变化,并以此来判断在反应中起主导作用的自由基。叔丁醇是一种良好的OH·和
SO−4⋅ 2. 结果与讨论 (Results and discussion)
2.1 反应条件对活性黄X-R溶液脱色率的影响
2.1.1 染料浓度对脱色率的影响
检测了当pH 为9、有效氯浓度为120 mg·L、催化剂投加量为240 g·L−1、初始染料浓度为100、200、300、400 mg·L−1时的脱色率,结果如图1所示。前期的研究结果表明[11],有催化剂时,弱碱性环境pH 9有利于反应(1)和反应(2)的发生,促进活性氧的产生,增大NaClO的转化率。当催化剂存在时,脱色率随着初始染料浓度的增加而增加:当染料浓度为100、200、300、400 mg·L−1时,脱色率在120 min时分别为41.1%、41.21%、42.47%和50.03%。没有催化剂时,当初始染料浓度为100、200、300、400 mg·L−1时,脱色率在反应120 min时分别为43.7%、42.67%、41.78%和40.17%。加入催化剂后,初始染料浓度为100、200、300 mg·L−1溶液在120 min时的脱色率基本没有发生变化,可能是因为NaClO的直接氧化起了主导作用。当初始染料浓度为400 mg·L−1时,催化剂的加入使脱色率增加到50.03%,催化剂的吸附和活性氧的氧化作用对脱色率的增量做了一定的贡献,吸附量随着染料浓度的增加而增大,进而促进了活性氧与之发生反应。
催化氧化法对活性黄X-R的脱色效果远差于其对活性艳红K-2BP和酸性大红3R的脱色效果,脱色率随浓度变化的趋势也和后面两种染料的相反,活性艳红K-2BP和酸性大红3R的脱色率随着染料初始浓度的增加而减小(图2),因为反应的速率受到活性氧产量的限制,高浓度溶液需要更多的活性氧才能保持同样的降解速率。
 图 2 初始染料浓度对脱色率的影响Figure 2. Effect of initial dye concentration on color removal ratepH为9,催化剂投加量为240 g·L−1和 (a) 活性艳红K-2BP,有效氯为120 mg·L−1 (b) 酸性大红3R,有效氯为60 mg·L−1pH 9, catalyst dosage 240 g·L−1 and (a) reactive brilliant red K-2BP, available chlorine 120 mg·L−1 (b) acid red 3R, available chlorine 60 mg·L−1
图 2 初始染料浓度对脱色率的影响Figure 2. Effect of initial dye concentration on color removal ratepH为9,催化剂投加量为240 g·L−1和 (a) 活性艳红K-2BP,有效氯为120 mg·L−1 (b) 酸性大红3R,有效氯为60 mg·L−1pH 9, catalyst dosage 240 g·L−1 and (a) reactive brilliant red K-2BP, available chlorine 120 mg·L−1 (b) acid red 3R, available chlorine 60 mg·L−1以上实验结果表明,催化氧化体系降解活性黄X-R的机理可能有别于活性艳红K-2BP和酸性大红3R的降解机理,NaClO更倾向于直接氧化活性黄X-R,因此抑制了其本身的催化分解反应,减少了活性氧的产量;活性黄X-R分子也可能不易被具有亲电子性的活性氧攻击,使NaClO的直接氧化作用在脱色反应中占据了主导地位。因此,当NaClO有效氯浓度足够高的时候,染料的分解速率随着染料浓度的增加而增大,从表观上看,脱色率增大。
2.1.2 有效氯浓度对脱色率的影响
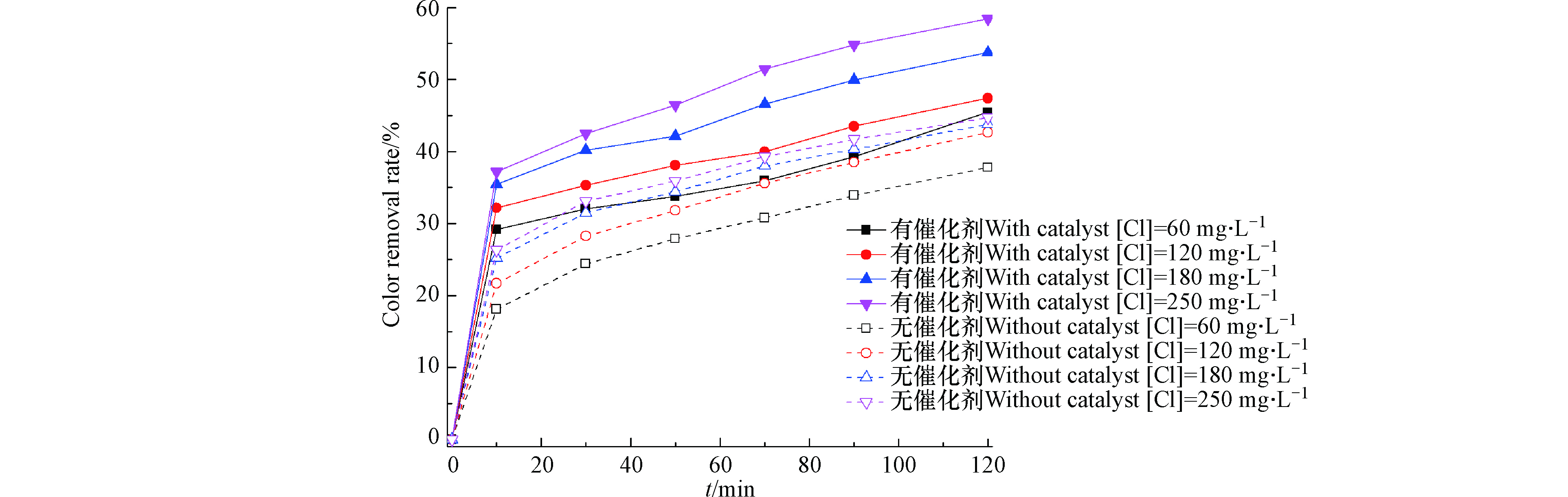
检测了当pH 9、染料浓度为200 mg·L−1、催化剂投加量为240 g·L−1、 有效氯为60、120、180 、250 mg·L−1时的脱色率,结果如图3所示。脱色率随着有效氯浓度的增加而增大。有催化剂存在时,当有效氯浓度从60 mg·L−1增加到250 mg·L−1,120 min时染料的脱色率从45%提升到了58%,增幅有限,主要是因为NaClO的直接氧化起了主导作用。NaClO在pH 9时的氧化性较弱,脱色效果差,单独氧化时NaClO的利用率较低[12]。有效氯浓度的增大也促进了NaClO直接氧化染料反应的进行,改善了活性黄X-R的脱色效果:当初始有效氯浓度从60 mg·L−1增加到250 mg·L−1,染料的脱色率从37.8%提升到了44.7%,比催化剂存在时的脱色率低6.3%–13.3%,增值是由催化剂的吸附和产生的活性氧作用所导致的。
2.1.3 pH对脱色率的影响
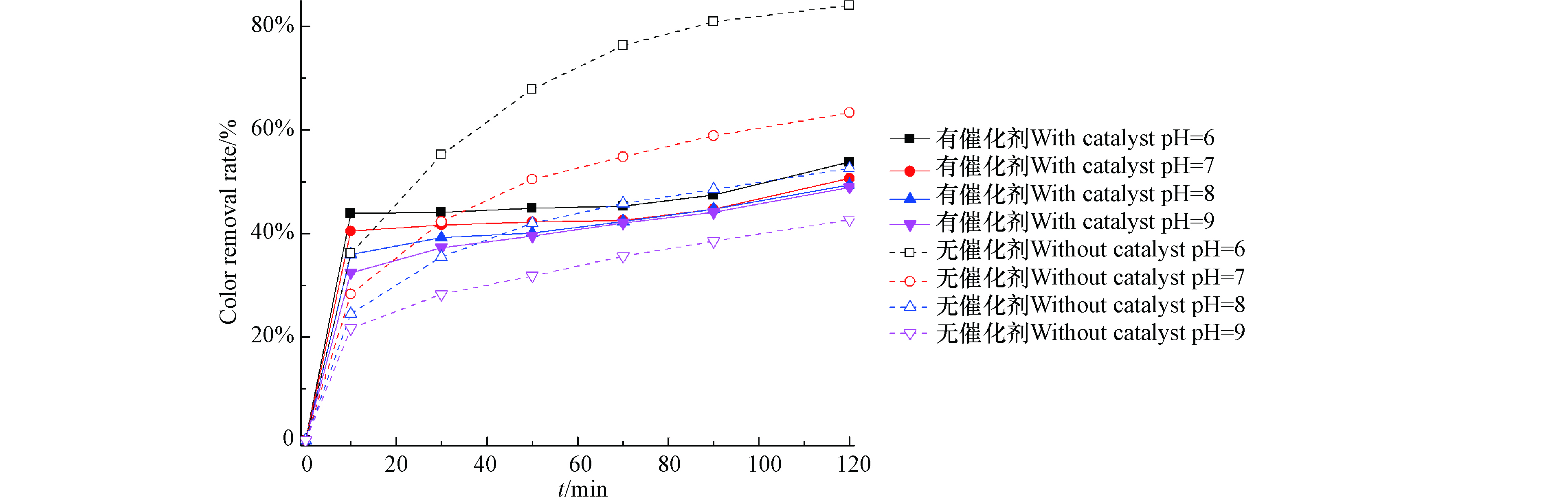
检测了当有效氯为120 mg·L−1、染料浓度为200 mg·L−1、催化剂投加量为240 g·L−1、初始pH值为6、7、8、9时的脱色率,结果如图4所示。NaClO催化氧化法的脱色率随着pH的提升而减小,pH 6、7时的脱色效果略胜于pH 8、9时的脱色效果,初始pH为6时的脱色效果最好,当反应时间为120 min,脱色率达到53.8%,远低于弱碱性条件下NaClO催化氧化降解活性艳红K-2BP和酸性大红3R溶液的脱色率(图5),催化作用明显受到了抑制,这是因为反应机理不同而导致的。原子氧在活性艳红K-2BP和酸性大红3R的脱色中起了主导作用,NaClO的直接氧化在活性黄X-R的脱色中起了主导作用。当初始pH为9,加催化剂反应120 min,活性黄X-R的脱色率达到49%,无催化剂时脱色率为42.7%(图4)。NaClO法降解活性黄X-R的脱色率随着pH的增加明显降低,当pH值从6增加到9,脱色率从84.1%降到42.7%,这是因为NaClO在酸性条件下会以游离氯存在,氧化性能大大提升。
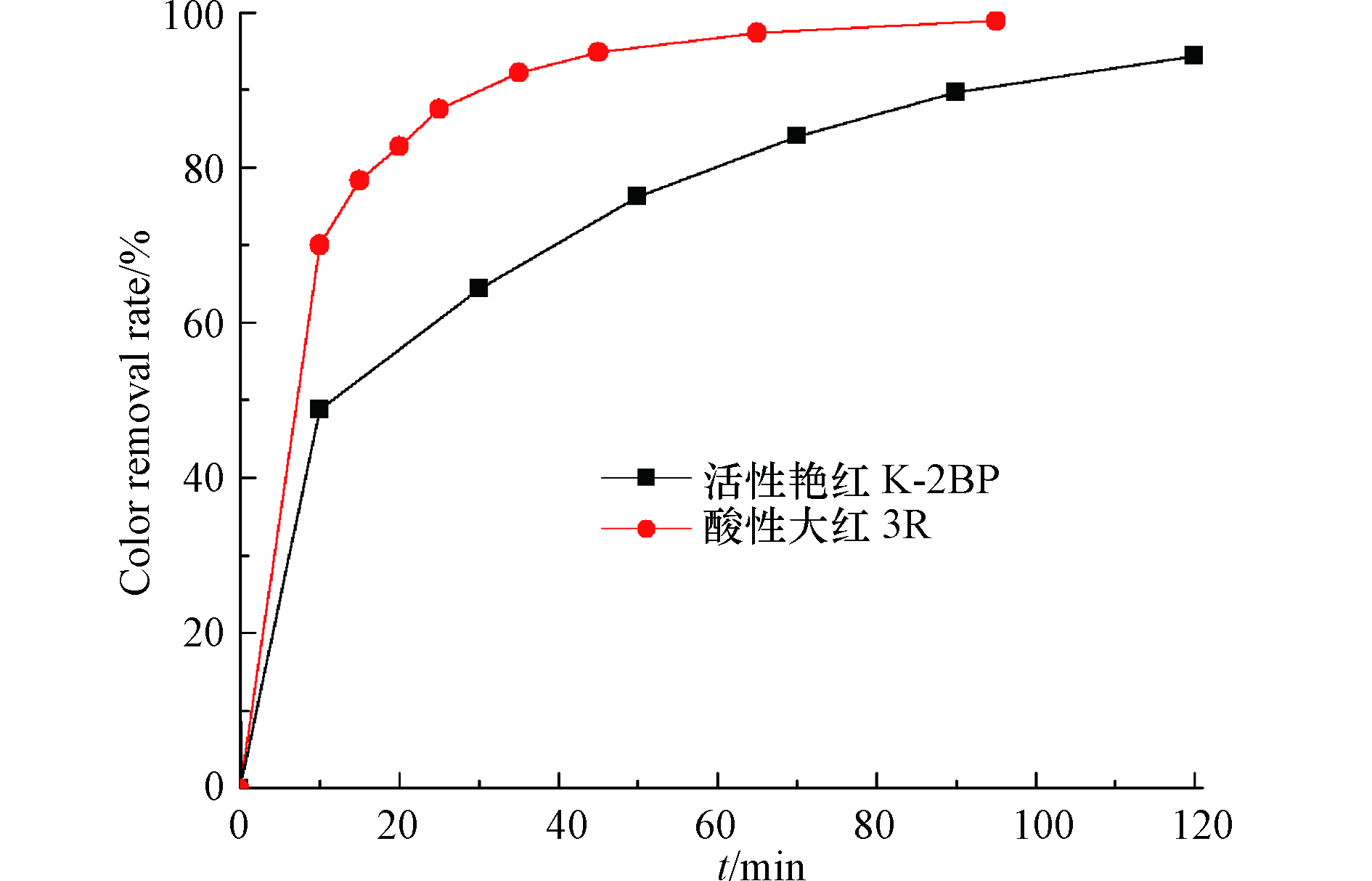 图 5 不同偶氮染料对脱色率的影响Figure 5. Effect of different azo-dyes on color removal rate初始pH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1initial pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant red K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red and available chlorine are 200 mg·L−1 and 60 mg·L−1
图 5 不同偶氮染料对脱色率的影响Figure 5. Effect of different azo-dyes on color removal rate初始pH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1initial pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant red K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red and available chlorine are 200 mg·L−1 and 60 mg·L−1当pH值为6、7、8时,加入催化剂反而导致活性黄X-R的脱色效果变差(图4)。当pH 6时,NaClO主要以HClO的形式存在。随着pH值的提升,ClO−的量增多,pH 9时NaClO主要以ClO−的形式存在。催化剂表面含有大量Ni(OH)2,带有正电荷[13]。当pH 6时,催化剂与次氯酸电荷相斥,不利于其在催化剂表面的有效吸附;当pH值为8、9,催化剂与ClO−存在电荷相吸作用,有利于NaClO在催化剂表面的有效吸附。催化剂表面和含有磺酸根离子的染料分子之间的静电吸引可能有利于染料在其表面的有效吸附。因此,当pH 6时,催化剂的存在降低了HClO与染料分子之间的反应几率,从而降低了脱色率,虽然此时的溶液具有较强的氧化性。当pH值为8、9,NaClO和染料分子在催化剂表面的有效吸附使两者之间的反应几率增大,从而使脱色率和酸性条件下的相差不大。催化剂存在时,弱碱性条件促进了活性氧的产生,但对染料的脱色率基本没有产生影响,可能是活性氧与染料分子之间的反应受到了阻碍。
采用NaClO催化氧化法降解活性艳红K-2BP和酸性大红3R,初始pH 9时的脱色效果最好(图6),弱碱性条件有利于NiOOH的生成和催化层的固定(式(1)和式(2)),进而促进原子氧的产生(式(3)—(8));同时,弱碱性条件还能抵消由于降解过程产生有机酸而导致的pH值的下降,起到平衡pH值的作用。
 图 6 pH对不同偶氮染料脱色率的影响Figure 6. Effect of different azo-dyes on color removal ratepH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red 3R and available chlorine are 200 mg·L−1 and 60 mg·L−1
图 6 pH对不同偶氮染料脱色率的影响Figure 6. Effect of different azo-dyes on color removal ratepH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red 3R and available chlorine are 200 mg·L−1 and 60 mg·L−12.1.4 催化剂对脱色率的影响
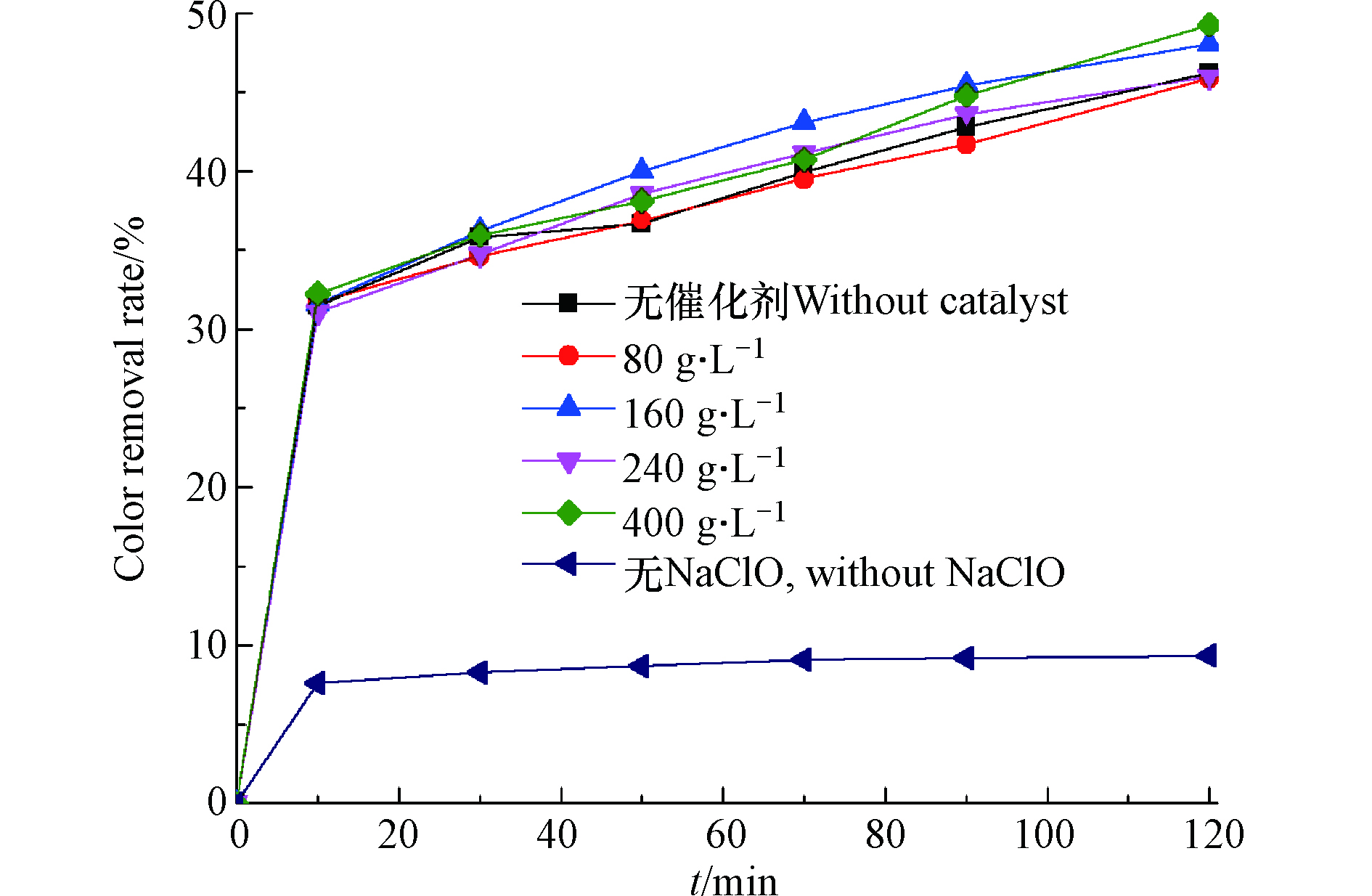
检测了当有效氯浓度为120 mg·L−1、染料浓度为200 mg·L−1、初始pH为9、催化剂投加量为80、160、240、400 g·L−1时的脱色率,结果如图7所示。催化剂投加量的增加对染料脱色率的影响很小,当催化剂投加量从80 g增加到400 g·L−1,脱色率在反应120 min时只提升了3.4%。单独使用NaClO时的脱色率与催化剂存在时的基本相同。单独使用400 g·L−1新制备的催化剂处理废水120 min,仅有7.6%–9.4%的脱色率,随着反应时间的延长,脱色率变化幅度很小,说明这部分脱色率主要是由吸附导致的,其贡献较小。实验结果再次验证了NaClO的氧化在脱色反应中的主导作用,当初始pH为9时,催化剂对脱色反应的影响甚微,催化作用受到了抑制。因此,催化氧化法不太适用于脱色降解活性黄X-R废水。
2.1.3节的研究结果表明,当pH为6,200 mg·L−1活性黄X-R废水中有效氯浓度达到120 mg·L−1,反应 120 min后脱色率达到84.1%。继续调低pH能进一步提升脱色率,但是NaClO氧化法会导致出水中产生毒性较强的氯代有机物。王元刚等[14]采用Mg(OH)2混凝脱色降解浓度为100 mg·L−1的活性黄X-R废水,当pH 值为12、Mg2+投加量为216 mg·L−1时,脱色率达到90%以上。王昶等[15]采用蛭石类芬顿降解活性黄X-R染料,结果表明,把蛭石粉碎到7.5 μm的颗粒,其投加量为1.0 g·L−1、pH 3、H2O2用量 2.94 mmol·L−1时,反应180 min 后,50—300 mg·L−1活性黄X-R 脱色率均能达到95%以上。后面两种方法的运行成本偏高。
2.2 机理研究
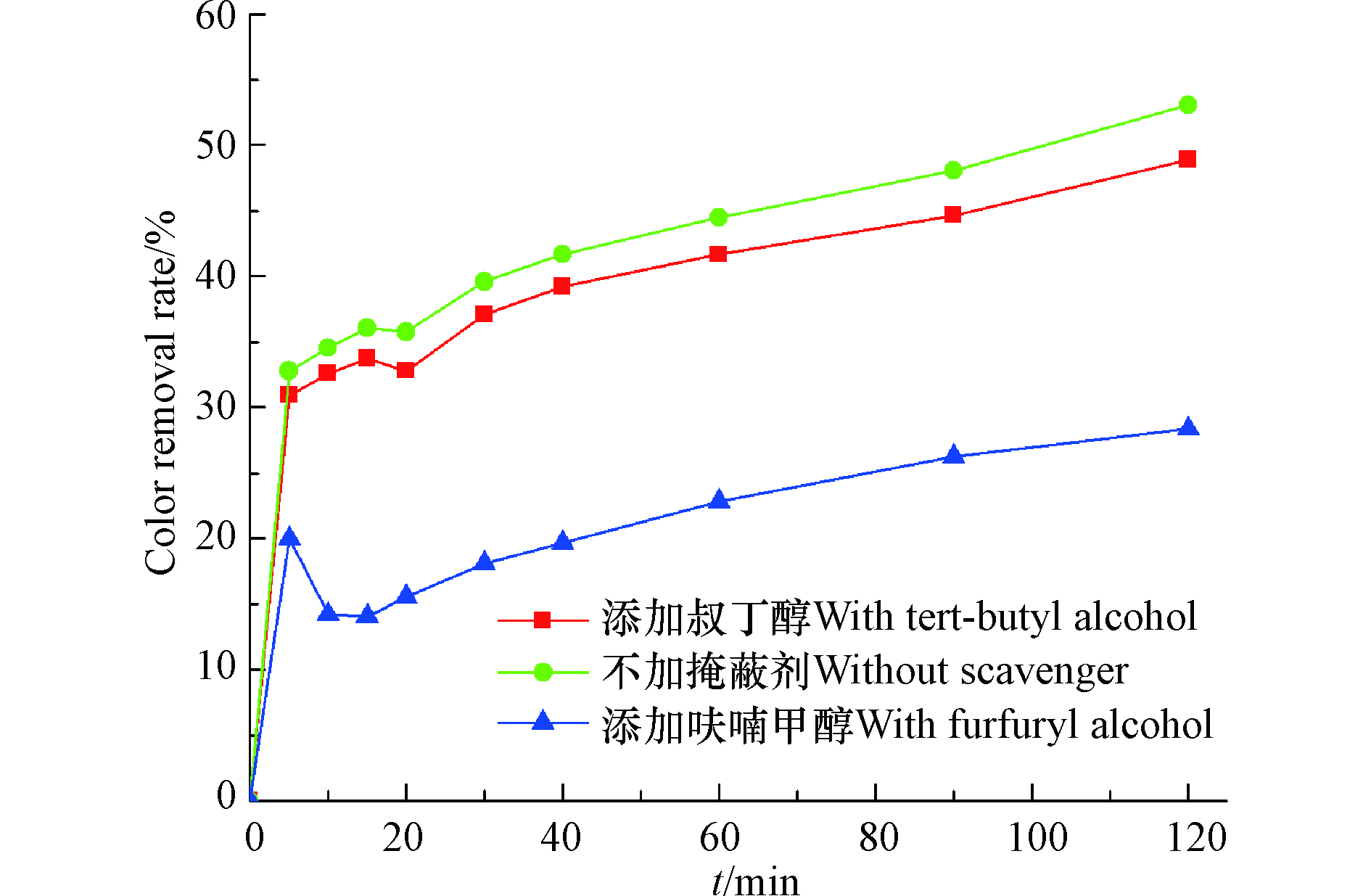
叔丁醇的加入对活性黄X-R的降解过程几乎没有影响,而呋喃甲醇对脱色具有一定的抑制作用,两者之间的脱色率差值在12%―24%之间(图8),因此可以断定原子氧在染料脱色过程中起了一定的作用,OH·和
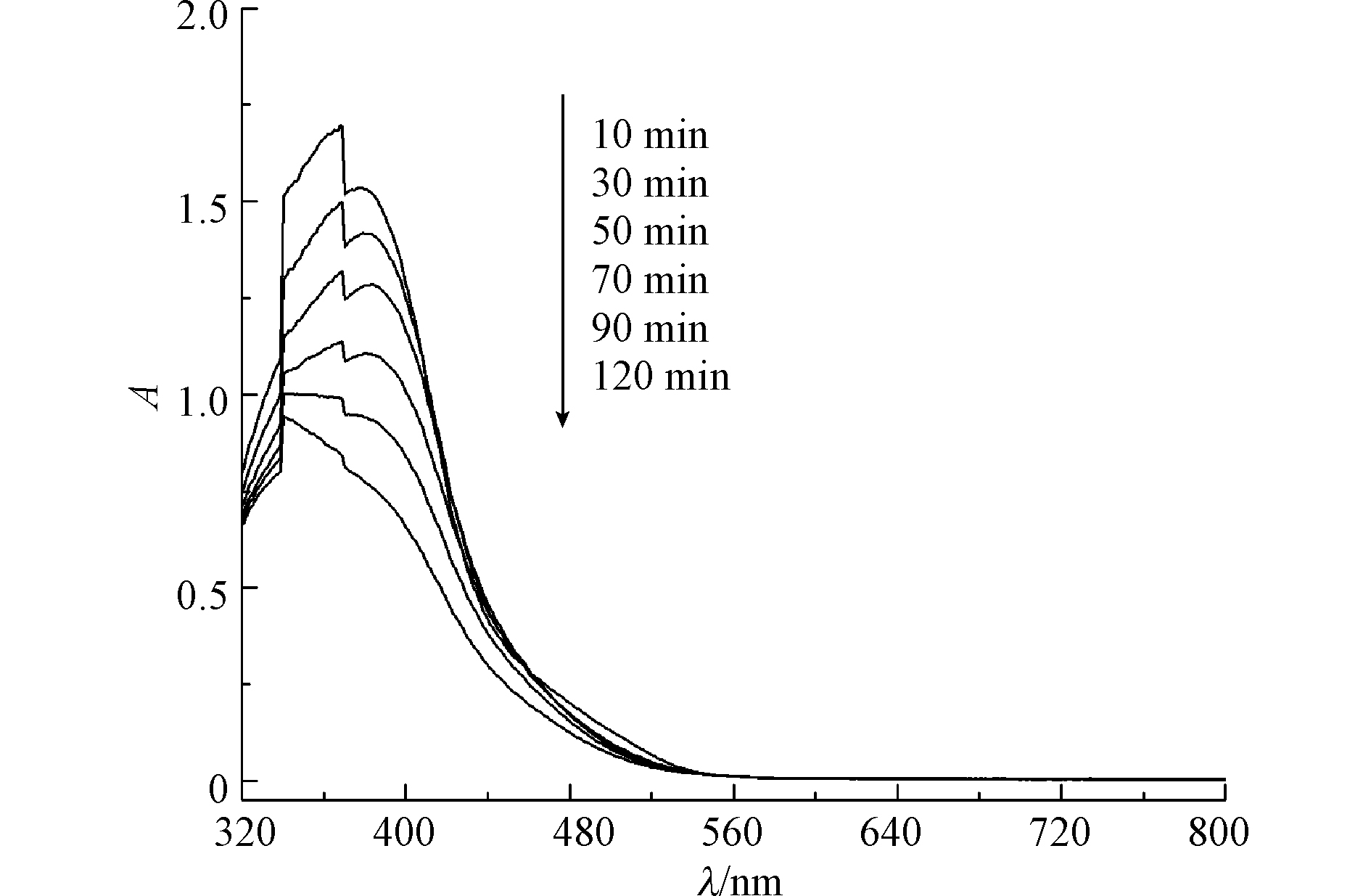
SO−4⋅ 活性黄X-R在390 nm的最大吸收峰对应偶氮键(图9),该峰随着反应的进行逐渐减小,但没有消失,可见偶氮键并未被完全破坏。367―370 nm之间为萘环的吸收峰,峰面积随着反应的进行减小,但反应120 min后该特征吸收峰还在,萘环没有完全打开。
2.3 染料分子结构与脱色率的关系
根据染料的分子结构特征及脱色率,选择磺酸基(
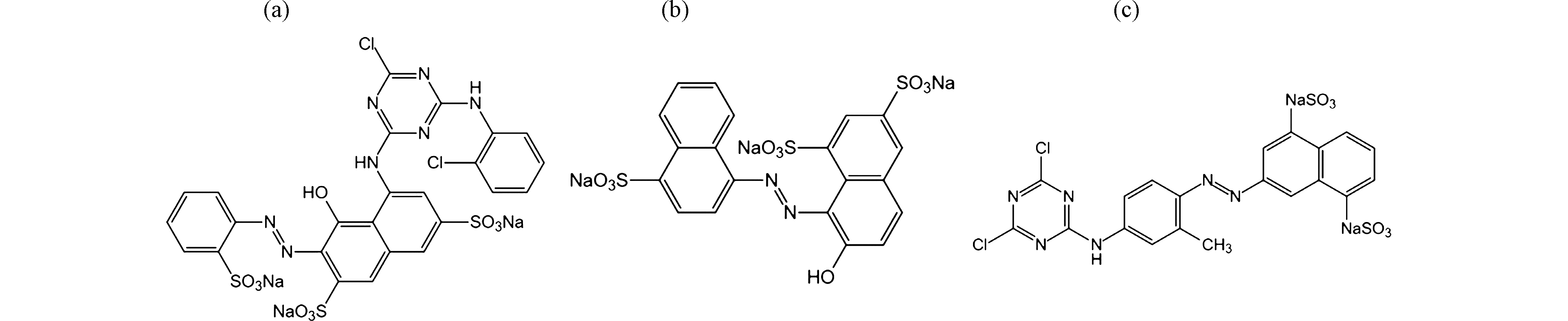
SO−3 分别配制浓度为200 mg·L−1的活性艳红K-2BP、酸性大红3R和活性黄X-R溶液,往里投加NaClO,使混合液中有效氯浓度达到120 mg·L−1,调节废水/NaClO混合液的pH值到9,投加催化剂240 g·L−1,在振荡器上反应90 min后取样,于染料的最大吸收波长下测定溶液的吸光度,换算成浓度,计算其脱色率。3种染料都属于偶氮染料,它们的分子结构见图10,它们的去除率和分子结构描述符见表1.
表 1 偶氮染料的去除率和分子结构描述符Table 1. Removal rate and molecular structure descriptor of the azo dyes染料名称Dye name 分子结构描述符Molecular structure descriptor 脱色率/%Color removal rate A B C 活性艳红K-2BP 3 3.95 5 91.3 酸性大红3R 3 6.25 4 99.69 活性黄 X-R 2 3.14 4 39.3 对表1中的分子结构描述符与脱色率进行线性回归分析,其线性回归方程和参数如表2所示。A、B与脱色率的线性回归数值比较高,说明目标染料的去除率与染料分子结构中磺酸基数目和I/O值之间具有较强的线性相关性,其中磺酸基数目A对去除率的影响尤为突出。染料分子的A值升高,其脱色率增加,这是因为磺酸基数目的增加使染料分子的电子云密度增加,原子氧具有较强的亲电子性,易与偶氮键发生加成反应。染料分子的B值升高,其无机性增强,电离度也随之增大,溶液中磺酸根离子的量增加,原子氧与染料分子之间的反应几率也因此增大,染料的脱色效率提高。C值增大,脱色率也随之增加,但去除率和C值的相关性较差,R2=0.1481,染料分子中C值一般小于10。因此,C值对脱色率的影响很小。
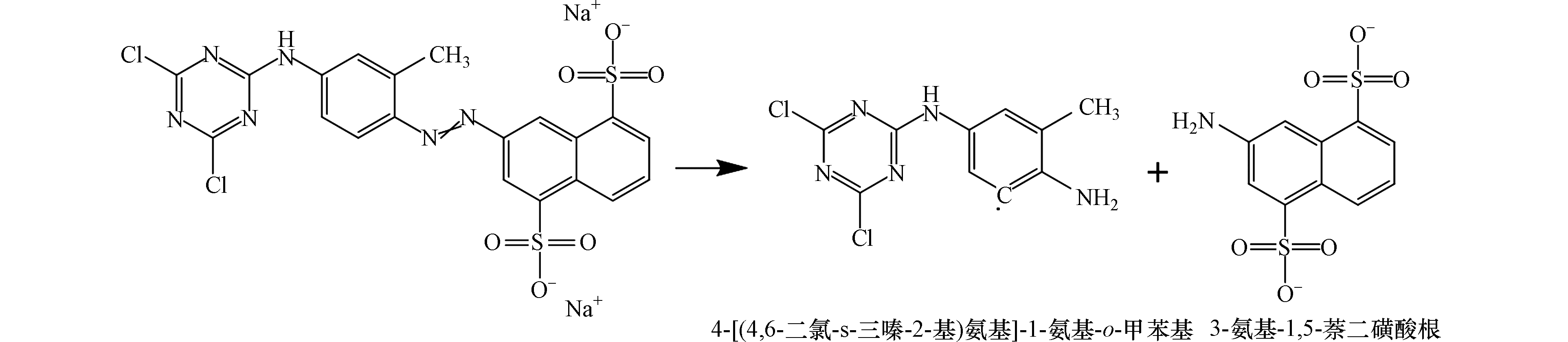
表 2 分子结构描述符与去除率的线性回归方程Table 2. Linear regression equation between molecular structure descriptor and removal rate分子结构描述符Molecular structure descriptor 回归方程Regression equation R2 F A ω 0.9836 59.815 B ω 0.6194 2.627 C ω 0.1481 0.174 偶氮键断开后,活性黄X-R分子被分解成2个芳胺:3-氨基-1,5-萘二磺酸根和4-[(4,6-二氯-s-三嗪-2-基)氨基]-1-氨基-o-甲苯基 (图11)。3-氨基-1,5-萘二磺酸根包含一个萘环,萘环上引入了两个磺酸基,其耐氯牢度大大提高,也就是说OCl−的进攻能力减弱;引入磺酸基的数目越多,耐氯牢度提升也越大[18]。活性黄X-R分子含有二氯均三嗪活性基,由于两个氯原子的吸电子诱导效应,环上的电子云密度较低,故其活性较高,水解率高,固色效果差,容易被浓度高氧化能力弱一些的OCl−进攻。活性艳红K-2BP的分子包含1个偶氮基、一氯均三嗪基、2个苯环和1个萘环(图10)。一氯均三嗪环上的电子云密度高,稳定性强,固色效果好,不易被OCl−进攻[19],却能被氧化性极强的原子氧脱色降解。董亚荣等[20]曾对10种染料的生物降解脱色性能进行了研究,结果表明,X型染料最易降解,K型染料次之。实验结果与该结论吻合。酸性大红3R分子包含1个偶氮基、1个羟基和2个萘环;萘环上有3个磺酸基,其中1个磺酸基位于偶氮基的邻位(图10),其耐氯稳定性好[19],降解过程不易产生有机氯产物。
综上,活性黄X-R分子的耐氯牢度较低,NaClO倾向将其直接氧化,从而抑制了NaClO的催化分解和原子氧的产生,降低了原子氧对脱色降解过程的贡献度。活性艳红K-2BP和酸性大红3R的耐氯稳定性好。NaClO催化氧化法更适合降解耐氯性强的K型活性偶氮染料和含有磺酸钠盐的酸性偶氮染料,不太适合于降解X型活性偶氮染料。苯环染料比萘环染料耐氯性好,这也是吴正雷等[5]用NaClO/镍基催化剂处理甲基橙(对二甲氮基偶苯磺酸钠)废水,没有发现有机氯产物的原因。
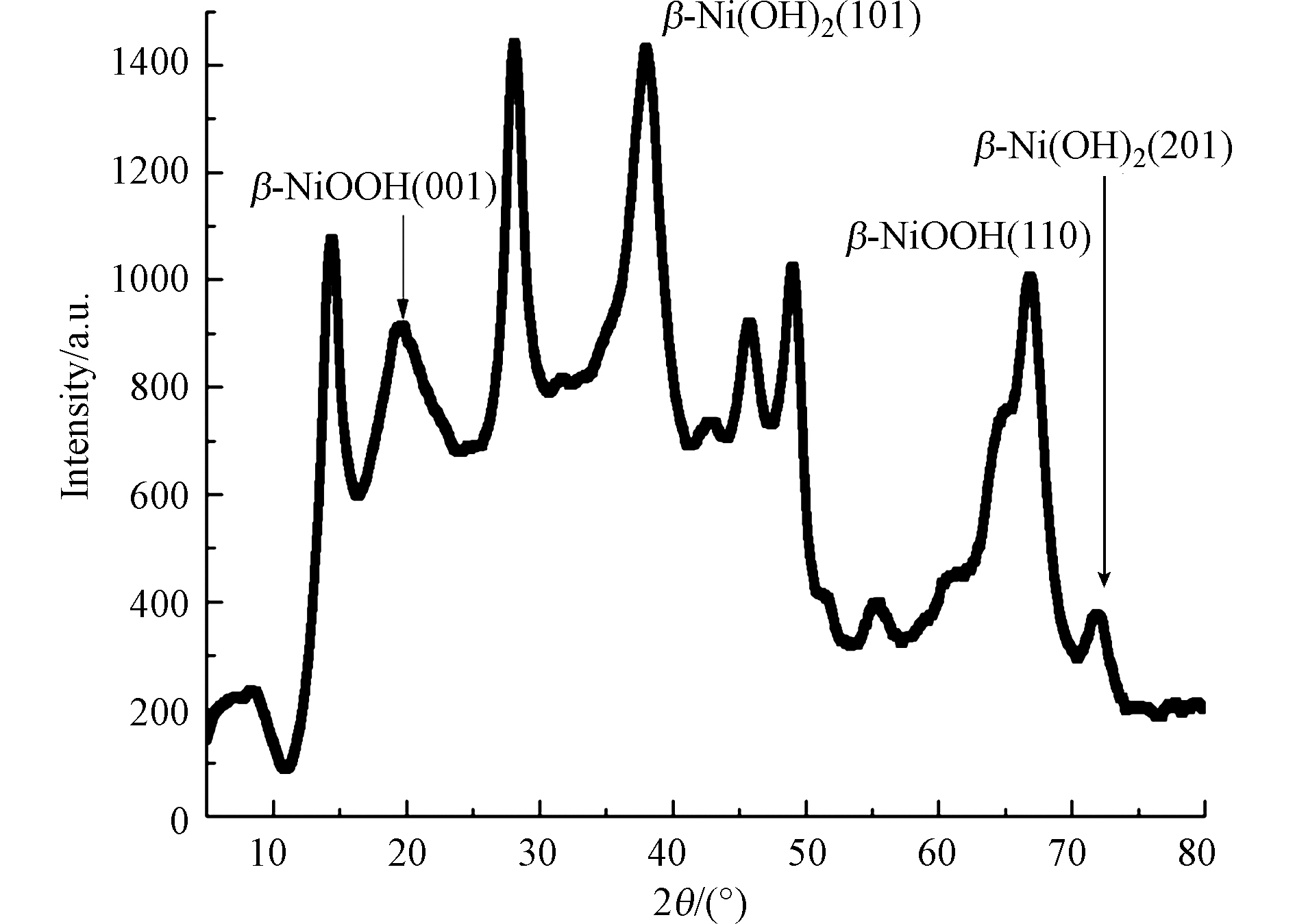
采用XRD对催化剂表层进行物相分析。样品在19.2°和66.7°附近有强的衍射峰(图12),与标准卡(卡号60141)对比可知,样品里含有β-NiOOH,两个衍射峰分别为001和110晶面。样品在38.5°和72.2°处出现两个衍射峰,与标准卡(卡号14117)对比可知,样品里含有β-Ni(OH)2,两个衍射峰分别为101和201晶面。
采用XPS分析法检测催化剂表面的元素及其相对含量。选取新制备的催化剂和分别处理过3000 min不同偶氮染料的三个催化剂小球作为检测样品。样品中氧元素的含量在78%以上(表3)。531.46 eV左右的峰为化学吸附氧引起的[21]。处理过3000 min染料的催化剂样品中氧元素的含量有不同程度的减小,主要是因为产生的原子氧参与降解染料。855.79―856.14 eV的峰是由Ni(Ⅱ)引起的,861.59―861.95 eV的峰是由Ni(Ⅲ)引起的[22]。新制的催化剂样品的Ni(Ⅲ)/Ni(Ⅱ)比值为0.62,处理过3000 min三种不同染料的催化剂样品中Ni(Ⅲ)/Ni(Ⅱ)比值分别为0.46、0.44和0.42,Ni(Ⅲ)的相对含量减少,催化性能略微降低。
表 3 催化剂表面元素的相对占比Table 3. Relative proportion of catalyst surface elements元素Elements 峰位置Position 结合能/eVBinding energy 相对含量/% Relative content 新制备的催化剂New catalyst 处理过3000 min活性艳红K-2BP的催化剂Catalyst of K-2BP treated for 3000 min 处理过3000 min酸性大红3R的催化剂Catalyst of 3R treated for 3000 min 处理过3000 min活性黄X-R的催化剂Catalyst of X-R treated for 3000 min Ni Ni(OH)2,2p3/2 855.98 6.34 10.61 13.46 10.50 Ni Ni(OH)2,2p1/2 873.61 Ni NiOOH,2p3/2 861.86 3.92 4.84 5.95 4.43 Ni NiOOH,2p1/2 879.81 O O1s 531.40 87.67 83.08 78.46 83.83 S S2p 168.67 2.07 1.47 2.13 1.24 图13为新制备的催化剂的SEM照片。由图13可见,催化剂的表面比较平整,镍的沉淀物较为均匀且致密地包裹在氧化铝小球表面,因此,Ni2+不容易渗透到Al2O3小球里。β-NiOOH为球形粒子,β-Ni(OH)2具有六方晶系结构[23],两者紧密缠绕。
3. 结论 (Conclusion)
(1) NaClO催化氧化法对活性黄X-R废水的脱色效果欠佳,催化剂对脱色率的影响甚微。NaClO的直接氧化在脱色过程起了主导作用,原子氧的作用次之。
(2) NaClO催化氧化法更加适合于降解具有较多磺酸基和较高I/O值的偶氮染料。该工艺更加适合于降解稳定性强、耐氯性好的K型活性染料、含有磺酸钠盐的酸性染料和苯环染料。可以采用Mg(OH)2混凝法和Fenton法降解活性黄X-R染料。
(3) XPS分析表明,与用过3000 min的催化剂比较,新制备催化剂表面化学吸附氧占比略高;用过催化剂表面的Ni(Ⅲ)的相对含量减少,催化剂的性能略有降低。化学吸附氧消耗在染料的脱色降解。
-
表 1 采样点情况
Table 1. Sampling sites situation
采样点Sampling site 经纬度坐标Latitude and longitude 土地利用类型Type of land use 主要氨氮污染源Primary pollution sources of ammonium nitrogen 陶岔(TC) 32°40'51.86"N, 111°42'43.88" E 建设用地、耕地、交通用地 采样点位于渠首取水口,其主要污染源为道路交通污染,存在氮肥污染源 宋岗(SG) 32°45'59.28"N, 111°38'07.80" E 湿地、交通用地、耕地、建设用地 采样点位于码头,其主要污染源为交通污染 土门(TM) 32°49'13.92"N, 111°36'24.28" E 耕地、湿地、林地 采样点紧邻耕地,其主要污染源为氮肥污染,存在畜禽粪便污染源 黑鸡嘴(HJZ) 32°49'37.80"N, 111°32'18.01" E 耕地、林地、湿地 采样点位于景区,其主要污染源为交通污染,存在氮肥污染源 党子口(DZK) 32°42'28.78"N, 111°30'28.75" E 耕地、湿地 采样点紧邻园地和耕地,其主要污染源为氮肥污染 表 2 国内部分水库NH4+-N干沉降通量对比
Table 2. Comparison of dry atmospheric ammonia nitrogen deposition fluxes of some reservoirs
表 3 单因素方差分析
Table 3. One-way ANOVA analysis
因素Factor F P NH4+-N浓度Ammonia nitrogen concentration NH4+-N干沉降通量Dry atmospheric ammonia nitrogen deposition fluxes δ15N-NH4+ NH4+-N浓度Ammonia nitrogen concentration NH4+-N干沉降通量Dry atmospheric ammonia nitrogen deposition fluxes δ15N-NH4+ 空间 3.671 0.900 1.334 0.012 0.473 0.274 时间 5.152 2.949 4.546 0.004 0.044 0.008 -
[1] GALLOWAY J N, TOWNSEND A R, ERISMAN J W, et al. Transformation of the nitrogen cycle: Recent trends, questions, and potential solutions [J]. Science, 2008, 320(5878): 889-892. doi: 10.1126/science.1136674 [2] DUAN L, YU Q, ZHANG Q, et al. Acid deposition in Asia: Emissions, deposition, and ecosystem effects [J]. Atmospheric Environment, 2016, 146: 55-69. doi: 10.1016/j.atmosenv.2016.07.018 [3] BOUWMAN A F, van VUUREN D P, DERWENT R G, et al. A global analysis of acidification and eutrophication of terrestrial ecosystems [J]. Water, Air and Soil Pollution, 2002, 141(1/2/3/4): 349-382. [4] NIU D C, YUAN X B, CEASE A J, et al. The impact of nitrogen enrichment on grassland ecosystem stability depends on nitrogen addition level [J]. Science of the Total Environment, 2018, 618: 1529-1538. doi: 10.1016/j.scitotenv.2017.09.318 [5] NIU S L, CLASSEN A T, DUKES J S, et al. Global patterns and substrate-based mechanisms of the terrestrial nitrogen cycle [J]. Ecology Letters, 2016, 19(6): 697-709. doi: 10.1111/ele.12591 [6] LIU X J, DUAN L, MO J M, et al. Nitrogen deposition and its ecological impact in China: An overview [J]. Environmental Pollution, 2011, 159(10): 2251-2264. doi: 10.1016/j.envpol.2010.08.002 [7] SHEN J L, LIU X J, ZHANG Y, et al. Atmospheric ammonia and particulate ammonium from agricultural sources in the North China Plain [J]. Atmospheric Environment, 2011, 45(28): 5033-5041. doi: 10.1016/j.atmosenv.2011.02.031 [8] 许稳, 金鑫, 罗少辉, 等. 西宁近郊大气氮干湿沉降研究 [J]. 环境科学, 2017, 38(4): 1279-1288. doi: 10.13227/j.hjkx.201609237 XU W, JIN X, LUO S H, et al. Dry and bulk nitrogen deposition in suburbs of Xining City [J]. Environmental Science, 2017, 38(4): 1279-1288(in Chinese). doi: 10.13227/j.hjkx.201609237
[9] XU W, LUO X S, PAN Y P, et al. Quantifying atmospheric nitrogen deposition through a nationwide monitoring network across China [J]. Atmospheric Chemistry and Physics, 2015, 15(21): 12345-12360. doi: 10.5194/acp-15-12345-2015 [10] YU G R, JIA Y L, HE N P, et al. Stabilization of atmospheric nitrogen deposition in China over the past decade [J]. Nature Geoscience, 2019, 12(6): 424-429. doi: 10.1038/s41561-019-0352-4 [11] LIU M X, HUANG X, SONG Y, et al. Rapid SO2 emission reductions significantly increase tropospheric ammonia concentrations over the North China Plain [J]. Atmospheric Chemistry and Physics, 2018, 18(24): 17933-17943. doi: 10.5194/acp-18-17933-2018 [12] WARNER J X, DICKERSON R R, WEI Z, et al. Increased atmospheric ammonia over the world's major agricultural areas detected from space [J]. Geophysical Research Letters, 2017, 44(6): 2875-2884. doi: 10.1002/2016GL072305 [13] WEN Z, XU W, LI Q, et al. Changes of nitrogen deposition in China from 1980 to 2018 [J]. Environment International, 2020, 144: 106022. doi: 10.1016/j.envint.2020.106022 [14] SONG W, LIU X Y, HU C C, et al. Important contributions of non-fossil fuel nitrogen oxides emissions [J]. Nature Communications, 2021, 12: 243. doi: 10.1038/s41467-020-20356-0 [15] PAN Y P, GU M N, HE Y X, et al. Revisiting the concentration observations and source apportionment of atmospheric ammonia [J]. Advances in Atmospheric Sciences, 2020, 37(9): 933-938. doi: 10.1007/s00376-020-2111-2 [16] PAN Y P, TIAN S L, LIU D W, et al. Fossil fuel combustion-related emissions dominate atmospheric ammonia sources during severe haze episodes: Evidence from 15N-stable isotope in size-resolved aerosol ammonium [J]. Environmental Science & Technology, 2016, 50(15): 8049-8056. [17] BHATTARAI N, WANG S X, PAN Y P, et al. δ15N-stable isotope analysis of NHx: An overview on analytical measurements, source sampling and its source apportionment [J]. Frontiers of Environmental Science & Engineering, 2021, 15(6): 1-11. [18] FENG S J, XU W, CHENG M M, et al. Overlooked nonagricultural and wintertime agricultural NH3 emissions in Quzhou County, North China plain: Evidence from 15N-stable isotopes [J]. Environmental Science & Technology Letters, 2022, 9(2): 127-133. [19] WU L B, REN H, WANG P, et al. Aerosol ammonium in the urban boundary layer in Beijing: Insights from nitrogen isotope ratios and simulations in summer 2015 [J]. Environmental Science & Technology Letters, 2019, 6(7): 389-395. [20] HUANG S N, ELLIOTT E M, FELIX J D, et al. Seasonal pattern of ammonium 15N natural abundance in precipitation at a rural forested site and implications for NH3 source partitioning [J]. Environmental Pollution, 2019, 247: 541-549. doi: 10.1016/j.envpol.2019.01.023 [21] PAN Y P, TIAN S L, LIU D W, et al. Isotopic evidence for enhanced fossil fuel sources of aerosol ammonium in the urban atmosphere [J]. Environmental Pollution, 2018, 238: 942-947. doi: 10.1016/j.envpol.2018.03.038 [22] 顾梦娜, 潘月鹏, 何月欣, 等. 稳定同位素模型解析大气氨来源的参数敏感性 [J]. 环境科学, 2020, 41(7): 3095-3101. doi: 10.13227/j.hjkx.201911132 GU M N, PAN Y P, HE Y X, et al. Source apportionment of atmospheric ammonia: Sensitivity test based on stable isotope analysis in R language [J]. Environmental Science, 2020, 41(7): 3095-3101(in Chinese). doi: 10.13227/j.hjkx.201911132
[23] 谭静瑶, 王丽涛, 刘振通, 等. 邯郸市NH3污染特征及其在PM2.5形成中的作用 [J]. 环境化学, 2021, 40(7): 2035-2046. TAN J Y, WANG L T, LIU Z T, et al. NH3 pollution and its role in PM2.5 pollution in Handan, China [J]. Environmental Chemistry, 2021, 40(7): 2035-2046(in Chinese).
[24] WANG H B, SHI G M, TIAN M, et al. Wet deposition and sources of inorganic nitrogen in the Three Gorges Reservoir Region, China [J]. Environmental Pollution, 2018, 233: 520-528. doi: 10.1016/j.envpol.2017.10.085 [25] 郭晓明, 金超, 孟红旗, 等. 丹江口水库淅川库区大气氮湿沉降特征 [J]. 生态学报, 2021, 41(10): 3901-3909. GUO X M, JIN C, MENG H Q, et al. Atmospheric wet deposition characteristics of nitrogen in the Xichuan area of Danjiangkou reservoir [J]. Acta Ecologica Sinica, 2021, 41(10): 3901-3909(in Chinese).
[26] 河南省生态环境厅. 河南省生态环境质量年报[EB/OL]. [2021-12-29]. [27] 罗玲. 丹江口水库淅川库区氮沉降特征研究[D]. 焦作: 河南理工大学, 2019. LUO L. Study on the atmospheric nitrogen deposition in Xichuan area of Danjiangkou reservoir[D]. Jiaozuo: Henan Polytechnic University, 2019(in Chinese).
[28] 陈晓舒. 淅川库区农业氨氮释放及其对氮沉降贡献研究[D]. 焦作: 河南理工大学, 2022. CHEN X S. Study on the release of ammonia nitrogen in agriculture and its contribution to nitrogen deposition in Xichuan reservoir area[D]. Jiaozuo: Henan Polytechnic University, 2022 (in Chinese).
[29] 国家环境保护总局, 水和废水监测分析方法编委会. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002. State Environmental Protection Administration, Determination Methods for Examination of Water and Wastewater. Water and waste water monitoring and analysis method [M]. (4th edition)Beijing: China Environment Science Press, 2002(in Chinese).
[30] LIU D W, FANG Y T, TU Y, et al. Chemical method for nitrogen isotopic analysis of ammonium at natural abundance [J]. Analytical Chemistry, 2014, 86(8): 3787-3792. doi: 10.1021/ac403756u [31] CHANG Y H, ZOU Z, DENG C R, et al. The importance of vehicle emissions as a source of atmospheric ammonia in the megacity of Shanghai [J]. Atmospheric Chemistry and Physics, 2016, 16(5): 3577-3594. doi: 10.5194/acp-16-3577-2016 [32] UREY H C. The thermodynamic properties of isotopic substances [J]. Journal of the Chemical Society, 1947: 1947Apr;562-1947Apr;581. [33] HEATON T H E, SPIRO B, ROBERTSON S M C. Potential canopy influences on the isotopic composition of nitrogen and sulphur in atmospheric deposition [J]. Oecologia, 1997, 109(4): 600-607. doi: 10.1007/s004420050122 [34] WILLIAMS J J, LYNCH J A, SAROS J E, et al. Critical loads of atmospheric N deposition for phytoplankton nutrient limitation shifts in western US mountain lakes [J]. Ecosphere, 2017, 8(10): e01955. doi: 10.1002/ecs2.1955 [35] XU W, ZHAO Y H, LIU X J, et al. Atmospheric nitrogen deposition in the Yangtze River Basin: Spatial pattern and source attribution [J]. Environmental Pollution, 2018, 232: 546-555. doi: 10.1016/j.envpol.2017.09.086 [36] 赵宪伟, 李橙, 杨晶, 等. 岗南水库上游流域大气氮干湿沉降研究 [J]. 南水北调与水利科技, 2018, 16(5): 115-121. doi: 10.13476/j.cnki.nsbdqk.2018.0132 ZHAO X W, LI C, YANG J, et al. Dry and wet deposition of nitrogen in the upstream basin of Gangnan Reservoir [J]. South-to-North Water Transfers and Water Science & Technology, 2018, 16(5): 115-121(in Chinese). doi: 10.13476/j.cnki.nsbdqk.2018.0132
[37] 陈海涛, 王晓燕, 黄静宇, 等. 密云水库周边小流域大气氮磷沉降特征研究[J]. 环境科学研究, 2021,35(6): 1419-1431. CHEN H T, WANG X Y, HUANG J Y, et al. Dry and wet atmospheric deposition of nitrogen and phosphorus in small catchment around Miyun Reservoir [J]. Research of Environmental Sciences, 2021, 35(6): 1419-1431(in Chinese).
[38] 王焕晓, 庞树江, 王晓燕, 等. 小流域大气氮干湿沉降特征 [J]. 环境科学, 2018, 39(12): 5365-5374. doi: 10.13227/j.hjkx.201801222 WANG H X, PANG S J, WANG X Y, et al. Dry and wet deposition of atmospheric nitrogen in small catchments [J]. Environmental Science, 2018, 39(12): 5365-5374(in Chinese). doi: 10.13227/j.hjkx.201801222
[39] 张六一. 三峡库区大气氮沉降特征、通量及其对水体氮素的贡献[D]. 重庆: 中国科学院大学(中国科学院重庆绿色智能技术研究院), 2019. ZHANG L Y. Atmospheric nitrogen deposition in the Three Gorges reservoir area: Characteristics, fluxes, and contributions to the aquatic environment[D]. Chongqing: Chongqing Institute of Green and Intelligent Technology, Chinese Academy of Sciences, 2019(in Chinese).
[40] 田光明, 蔡祖聪, 曹金留, 等. 镇江丘陵区稻田化肥氮的氨挥发及其影响因素 [J]. 土壤学报, 2001, 38(3): 324-332. doi: 10.3321/j.issn:0564-3929.2001.03.012 TIAN G M, CAI Z C, CAO J L, et al. Ammonia volatilization from paddy field and its affecting factors in Zhenjiang hilly region [J]. Acta Pedologica Sinica, 2001, 38(3): 324-332(in Chinese). doi: 10.3321/j.issn:0564-3929.2001.03.012
[41] WANG S S, NAN J L, SHI C Z, et al. Atmospheric ammonia and its impacts on regional air quality over the megacity of Shanghai, China [J]. Scientific Reports, 2015, 5: 15842. doi: 10.1038/srep15842 [42] VIATTE C, WANG T Z, van DAMME M, et al. Atmospheric ammonia variability and link with particulate matter formation: A case study over the Paris area [J]. Atmospheric Chemistry and Physics, 2020, 20(1): 577-596. doi: 10.5194/acp-20-577-2020 [43] KUNDU S, KAWAMURA K, LEE M. Seasonal variation of the concentrations of nitrogenous species and their nitrogen isotopic ratios in aerosols at Gosan, Jeju Island: Implications for atmospheric processing and source changes of aerosols [J]. Journal of Geophysical Research:Atmospheres, 2010, 115(D20): D20305. doi: 10.1029/2009JD013323 [44] PARK Y M, PARK K S, KIM H, et al. Characterizing isotopic compositions of TC-C, NO3−-N, and NH4+-N in PM2.5 in South Korea: Impact of China's winter heating [J]. Environmental Pollution, 2018, 233: 735-744. doi: 10.1016/j.envpol.2017.10.072 [45] TI C P, GAO B, LUO Y X, et al. Isotopic characterization of NHx-N in deposition and major emission sources [J]. Biogeochemistry, 2018, 138(1): 85-102. doi: 10.1007/s10533-018-0432-3 [46] KAWASHIMA H, KURAHASHI T. Inorganic ion and nitrogen isotopic compositions of atmospheric aerosols at Yurihonjo, Japan: Implications for nitrogen sources [J]. Atmospheric Environment, 2011, 45(35): 6309-6316. doi: 10.1016/j.atmosenv.2011.08.057 [47] CHANG Y H, DENG C R, DORE A J, et al. Human excreta as a stable and important source of atmospheric ammonia in the megacity of Shanghai [J]. Plos One, 2015, 10(12): e0144661. doi: 10.1371/journal.pone.0144661 [48] FELIX J D, ELLIOTT E M. Isotopic composition of passively collected nitrogen dioxide emissions: Vehicle, soil and livestock source signatures [J]. Atmospheric Environment, 2014, 92: 359-366. doi: 10.1016/j.atmosenv.2014.04.005 [49] 马儒龙, 王章玮, 张晓山. 城市绿化林中大气氨浓度垂直分布观测 [J]. 环境化学, 2021, 40(7): 2028-2034. doi: 10.7524/j.issn.0254-6108.2020032803 MA R L, WANG Z W, ZHANG X S. Observation on the vertical distribution of atmospheric ammonia in urban green vegetation canopy [J]. Environmental Chemistry, 2021, 40(7): 2028-2034(in Chinese). doi: 10.7524/j.issn.0254-6108.2020032803
[50] 尹兴, 张丽娟, 刘学军, 等. 河北平原城市近郊农田大气氮沉降特征 [J]. 中国农业科学, 2017, 50(4): 698-710. doi: 10.3864/j.issn.0578-1752.2017.04.010 YIN X, ZHANG L J, LIU X J, et al. Nitrogen deposition in suburban croplands of Hebei plain [J]. Scientia Agricultura Sinica, 2017, 50(4): 698-710(in Chinese). doi: 10.3864/j.issn.0578-1752.2017.04.010
-









 下载:
下载: