-
全氟化合物(perfluoroalkyl substances,PFASs)是一类碳原子连接的氢原子全部被氟原子取代的有机化合物,因其优良的理化性能,被广泛用于化工、皮革和医药等工业及日常生活领域中[1]. 近年来已在大气、水和土壤等[2-4]环境介质及生物体中[5]被广泛检出. 现有的研究已经充分证明PFASs具有内分泌毒性、致癌性、神经毒性及生殖毒性等毒理效应,对环境和生物均存在潜在风险[6-7],因此2009年和2019年,全氟辛烷磺酸(perfluorooctane sulfonate,PFOS)及其盐类、全氟辛酸(perfluorooctanoic acid,PFOA)先后被列入《斯德哥尔摩公约》并加以限制生产和使用. 然而由于经济和生产需求,PFASs的生产逐步转移到亚洲,尤其是中国[8]. PFASs一旦进入环境后能够随着大气发生长距离迁移,到达海拔较高的地区发生“高山冷凝效应”,从而导致高海拔地区成为污染物的“接收器”[9].
现有的研究证实,树木能够有效截留大气中的有机污染物[10],对有机污染物的全球迁移及分布有重要影响[11-12]. 近年来,树木年轮因其分布广泛、样本易得、连续性强等特点,已经作为环境监测的一种手段[13]. 已有学者利用树木年轮作为指示研究大气环境中的多环芳烃、多溴联苯醚等持久性有机污染物(persistent organic pollutants, POPs)[14-15]的迁移及污染特征. 然而,PFASs不同于传统的持久性有机污染物,具有高表面活性、水溶性强等特点,能否用树木年轮来指示大气中的PFASs,并且对其污染历史进行反演,目前尚不清楚. 因此,有必要展开相关研究,探讨树木年轮对大气中PFASs的指示及污染历史重建,以期为偏远地区PFASs的生态风险评估提供科学依据. 目前公认的PFASs在全球的蓄积库为海洋沉积物,而森林植被占陆地面积的31%[16],若对PFASs有富集,其蓄积量不能忽视. 然而目前鲜有研究报道PFASs在森林中的蓄积能力,因此,本研究以横断山区雅砻江下游的云南松(Pinus yunnanensis)年轮为研究对象,分析其PFASs的污染特征与来源,反演PFASs在该地区的污染历史,并计算PFASs在云南松树干中的积累量,明确森林植被对PFASs迁移蓄积的重要性.
-
横断山区位于青藏高原东南部,覆盖四川、西藏、青海、云南等省区,总面积达50余万km2,由一系列南北走向的高大山脉和深切河谷组成[17]. 研究区域位于横断山区南部,雅砻江下游河谷地带,气候为干湿分明的亚热带气候,垂直方向的变化明显,植被以云南松为主. 该地人口密度小、地区社会经济不发达,因而本地污染源较少,能够反映污染物通过大气长距离迁移对该地区的影响. 云南松属乔木,是我国西南地区的特有树种,平均高达5—20 m,胸径70—150 cm,横断山区云南松常见树龄为30年左右,适用于对PFASs的历史重建分析[18].
-
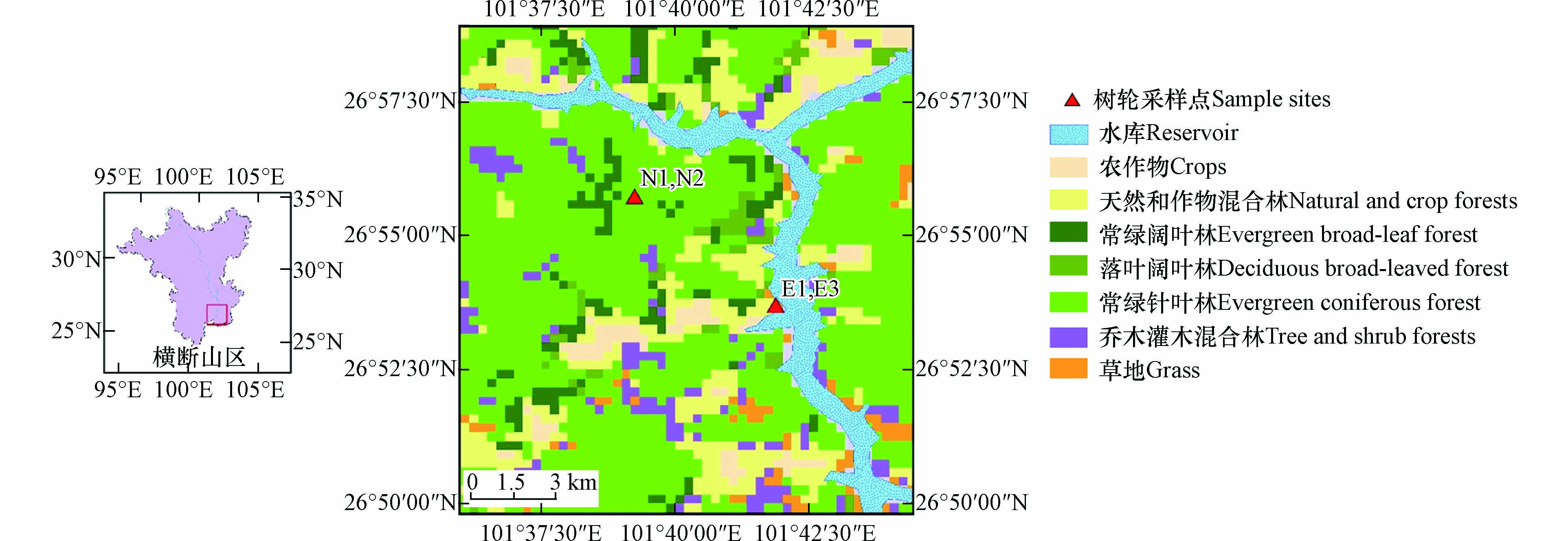
采样地点位于雅砻江河谷二滩水电站库区周边山坡,位于四川省攀枝花境内(101°30′54″E,26°54′7″N). 为避免污染,采样所使用的工具均提前用超纯水和甲醇清洗并干燥,采用内径为5.15 mm的生长锥钻取树芯样,采集位置为距离地面1.3 m处树干位置,分别于2017年8月和2018年1月采集3个(E1、E2、E3)和2个(N1、N2)年轮样品,采样点位置及周边植被情况见图1.
将采集的云南松树芯样品装入聚丙烯采样袋中带回实验室,进行捆绑处理后风干、打磨,通过LINTAB年轮仪测量年轮宽度,利用COFECHA程序辅助交叉定年(排除伪轮、缺轮的影响),实现已知年龄和未知年龄的年轮衔接,最终精确定出每个年轮的生长年份. 树芯基本信息见表1.
-
甲醇(色谱纯/99.8%,成都市科龙化工试剂厂)、氨水(25%,成都市科龙化工试剂厂)、Milli-Q超纯水.
实验所用标准样品为高纯度混合标准品PFAC-MXB(Wellington公司),含有全氟羧酸类和全氟磺酸类化合物. 其中,羧酸类包括:全氟丁酸(perfluorobutanoic acid,PFBA)、全氟戊酸(perfluoropentanoic acid,PFPeA)、全氟己酸(perfluorohexanoic acid,PFHxA)、全氟庚酸(perfluoroheptanoic acid,PFHpA)、全氟辛酸(perfluorooctanoic acid,PFOA)、全氟壬酸(perfluorononanoic acid,PFNA)、全氟癸酸(perfluorodecanoic acid,PFDA)、全氟十一酸(perfluoroundecanoic acid,PFUnDA)和全氟十二酸(perfluorododecanoic acid,PFDoDA). 磺酸类包括:全氟丁烷磺酸(perfluorobutanesulfonic acid,PFBS)、全氟己烷磺酸(perfluorohexanesulfonic acid,PFHxS)和全氟辛烷磺酸(perfluorooctanesulfonic acid,PFOS). PFAC-MXA为高纯度混合碳同位素标记品(Wellington公司),包括:13C4-PFBA、13C2-PFHxA、13C4-PFOA、13C5-PFNA、13C2-PFDA、13C2-PFUnDA、13C2-PFDoDA、13O2-PFHxS和13C4-PFOS.
-
由于一年的年轮生物量较少,处理起来误差较大,因此将年轮样品从1991—2012年以每两年为一个样品进行切割. 样品的萃取及净化方法参照Jin等[19]处理树皮中PFASs的方法,并在此基础上进行优化. 树木年轮经真空冷冻干燥后研磨粉碎,称取0.1 g左右至15 mL聚丙烯离心管中,加入2 ng内标,涡旋混合均匀后静置过夜. 加入5 mL甲醇,涡旋30 s,超声30 min,以250 r·min−1振荡1 h,再以3000 r·min−1离心10 min,提取上清液至新的15 mL PP管中. 重复上述过程2次,将3次上清液合并,温和氮吹至5 mL后用Envi-Carb固相萃取小柱(500 mg/6 mL)净化. 过柱前分别用5 mL 0.1%氨水甲醇溶液、5 mL超纯水、5 mL甲醇对固相萃取柱进行活化,活化完成后将样品溶液以每秒1滴的流速过萃取柱并用新的15 mL PP管收集流出液,然后使用5 mL甲醇洗脱收集残留在固相萃取柱上的PFASs,两部分溶液合并后氮吹至1 mL转移至样品瓶中,于4 ℃保存,待测.
-
实验采用超高效液相色谱串联三重四极杆质谱仪(1290-6470),C18色谱柱(Zorbax SB-C18,2.1 mm×50 mm,1.8 μm). 色谱条件:柱温35 ℃,进样量5 μL,流动相采用5 mmol·L−1乙酸铵溶液(A相)和甲醇(B相),流速0.4 mL·min−1. 流动相梯度洗脱程序:0.00—0.10 min,A相比例为90%;0.10—6.00 min,A相比例由90%降为5%;6.00—8.00 min,A相比例为5%;后运行2 min. 质谱条件:电喷雾离子源;负离子模式(ESI);多反应离子检测(MRM)模式分析;雾化气压力0.24 MPa;电喷雾电压3000 V;干燥气温度250 ℃.
-
本研究采用内标法定量,标准曲线浓度为0、0.5、1、2、5、20、40 ng·mL−1,线性关系r > 0.99. 为降低实验背景及误差,样品在前处理过程中均避免接触和使用玻璃以及聚四氟乙烯容器. 样品前处理过程中每10个样品设置1个方法空白;测定时,每10个样品设置1个溶剂空白. 回收率实验设置两个不同浓度(2 ng·g−1,20 ng·g−1),每个浓度水平3个平行,方法回收率为72.5%—100.7%(表2),满足实验要求.
对于没有在空白样品中检测出的PFASs,其方法检出限(MDLs)为3倍信噪比时对应的浓度;对于在空白样品中检测到的PFASs,其MDLs值为空白样品中浓度的均值加上3倍的标准偏差. 在处理数据时,检测值低于MDLs值时,用MDLs值除以
√2 代替;未检出时,用零代替. 本实验方法的检出限为0.002—0.022 ng·g−1(表2). -
本研究参照王荣芬[20]的方法对单位面积云南松树干中PFASs的积累量进行计算,具体方法如下:采用木材密度法即平均材积与木材密度的乘积计算得到云南松树干的生物量,平均材积根据样方内云南松树干高度和胸径在标准立木材积表[21]中查得后取平均值,木材密度采用树芯重量与树芯体积之比的平均值;然后根据树芯中PFASs的平均含量计算出单株云南松树干中PFASs的平均积累量. 再根据样方大小和样方内云南松密度计算单位平方千米内云南松树干对PFASs的储量,结果可为横断山区森林系统对PFASs的蓄积提供基础数据,计算公式如下:
公式(1)中,M为单位面积云南松树干中PFASs储量(g·km−2),
−w 为树芯中PFASs平均含量(ng·g−1),−N 为单株云南松树干的平均生物量(g),m为树芯干重(g),−V 为单株云南松树干的平均材积(m³),r为树芯横截面半径(m,均为5.15×10−3 m),R为1.3 m取样处树木半径(m),n为单位平方千米内云南松密度(株·km−2). -
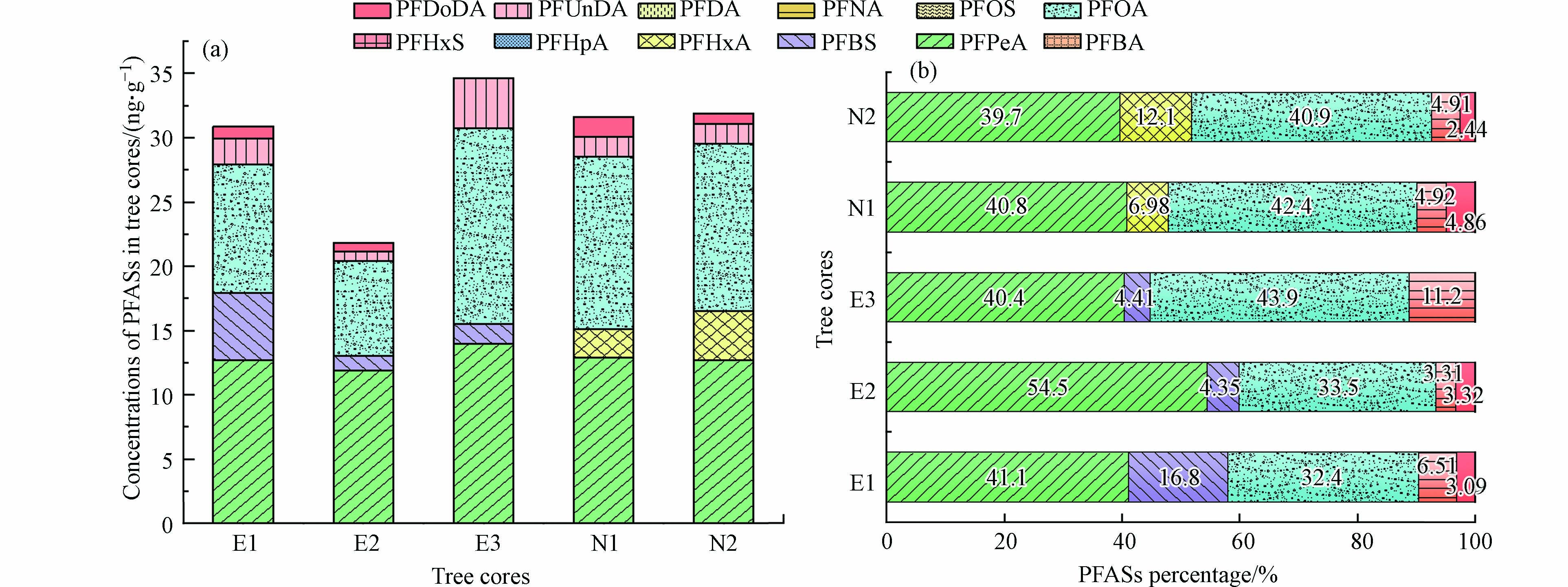
5个树芯样品中检出率最高的单体物质为PFOA和PFPeA,分别为91.8%和89.8%;其次为PFUnDA (22.4%)> PFBS(12.2%)> PFDoDA(10.2%)> PFHxA(6.12%);PFBA、PFHxS、PFHpA、PFOS、PFDA和PFNA均未检出. ΣPFASs浓度范围为nd—75.7 ng·g−1,平均值为30.9 ng·g−1,其中浓度最高的物质是PFPeA,平均值为12.7 ng·g−1;其次为PFOA,平均值为12.5 ng·g−1;然后依次为PFUnDA(1.99 ng·g−1)>PFHxA(1.43 ng·g−1)> PFBS(1.33 ng·g−1)> PFDoDA(0.95 ng·g−1),PFOA和PFPeA的浓度显著高于其余单体浓度. 5个树芯样品中ΣPFASs浓度分别为E1(31.0 ng·g−1)、E2(21.9 ng·g−1)、E3(34.6 ng·g−1)、N1(31.7 ng·g−1)和 N2(31.9 ng·g−1)(图2),平均浓度为(30.2±4.4 )ng·g−1. 魏明翠等[22]研究氟化学工业园周边树叶和树皮样品中的PFASs,得到树叶中ΣPFASs范围为4.90—185 ng·g−1,树皮中∑PFASs范围为0.240—95.4 ng·g−1;Shan等[23]以江苏省受污染地区的樟脑树叶为研究对象,测定树叶中PFASs浓度范围为10—276 ng·g−1. 与受污染地区植物的树叶及树皮中PFASs浓度相比,雅砻江下游云南松年轮样品中PFASs浓度约低1个数量级,此结果与研究地区的人口密度和工业发展程度相吻合. 此外,E为海拔1300 m的树木年轮((28.5±5.4)ng·g−1),N为海拔2045 m的树木年轮((31.8±0.1)ng·g−1),二者ΣPFASs浓度无显著差异. Taniyasu等[24]测定日本偏远山区与周边城市降雪中PFASs的浓度发现其与海拔高度无关;而Wang等[25]测定了山区中不同海拔高度的土壤中PFASs浓度,发现PFOA浓度随海拔高度增加而升高. 说明PFASs浓度的影响因素较复杂,即使是同一研究区域,也可能因样本不同、样本性质、周围环境等因素出现差异.
PFASs各单体在年轮中比例特征如图2所示,总体上PFASs的比例特征较为一致,均以短碳链和PFOA为主,其中PFPeA和PFOA占比分别高达54.5%和43.9%. PFOA作为树木年轮中PFASs的主要贡献者之一,和Jin等[19]及魏明翠等[22]的研究结果一致. E点年轮中均有检出PFBS,占比最高为16.8%;N点年轮中均检出了PFHxA,占比最高为12.1%,说明分别存在PFBS和PFHxA的污染来源. 在所有树芯中,长碳链的PFDoDA和PFUnDA基本上均被检出,占比最高分别为4.86%和11.2%.
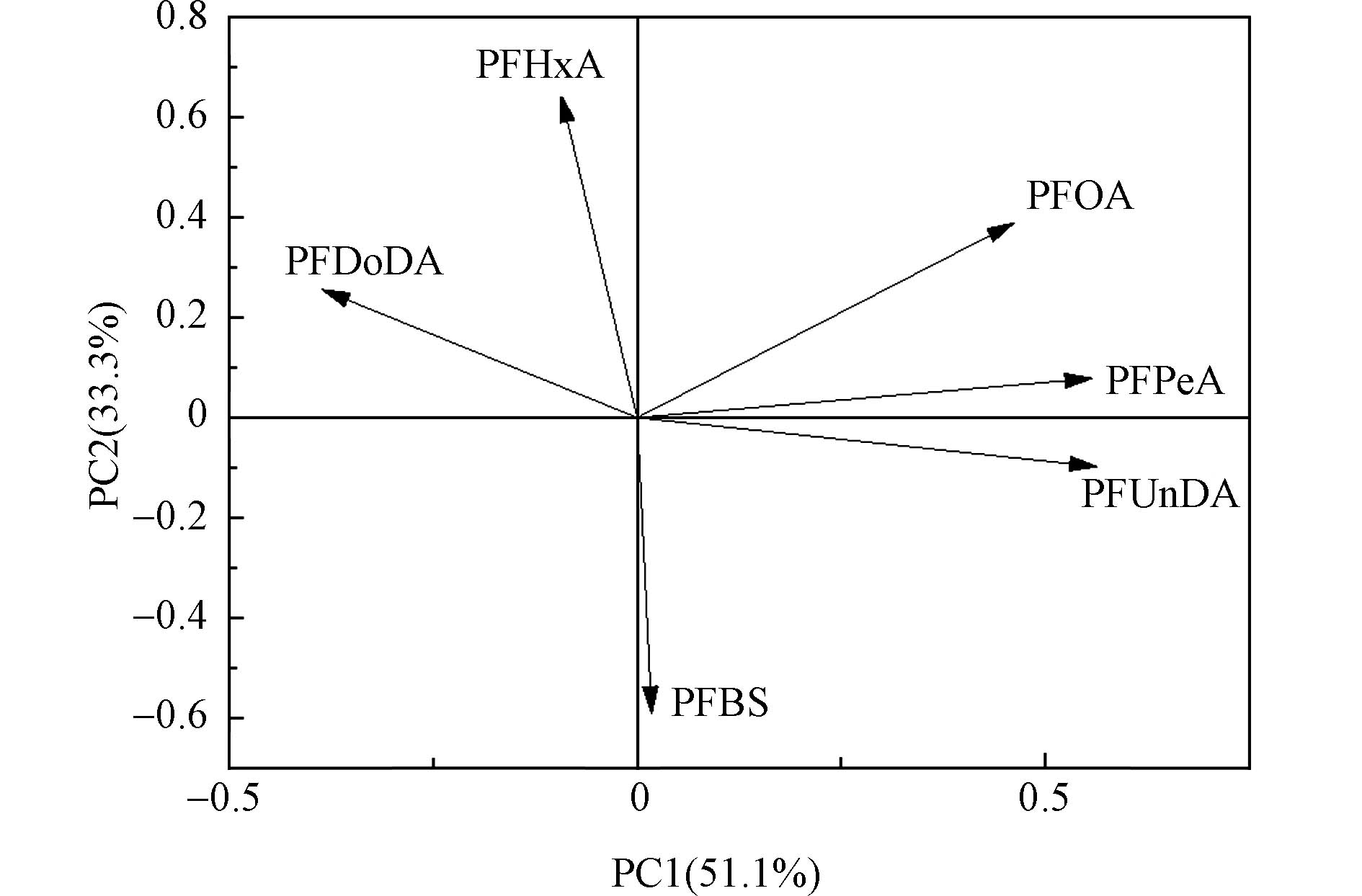
采用主成分分析法对云南松年轮中检出的6种PFASs解析,得到主成分分析图(图3),筛选出2个特征值 > 1的因子,累计方差贡献率达到84.4%. 其中,因子1可以解释年轮中51.1%的PFASs来源,PFUnDA、PFPeA和PFOA具有较高载荷值,分别为0.990、0.973和0.800;因子2可以解释年轮中33.3%的PFASs来源,PFHxA具有较高载荷值(0.911). 由于研究区域远离工业区,周围人类活动较少,说明该区域树木年轮中的PFASs大部分来自于大气远距离传输,PFASs到达偏远地区通常有两个传输途径:第一种为直接路径,PFASs因其较低的挥发性,能随大气和洋流直接在全球范围内进行迁移;第二种为间接途径,PFASs前体物质具有较强的挥发性或半挥发性,可随大气迁移后经过干湿沉降、降解进入偏远地区[26-28]. 研究表明,全氟烷磺酰胺(FASA)和全氟烷磺酰胺乙醇(FASE)可以转化为PFCAs和PFSAs[29],氟调醇(FTOHs)可以通过非生物或生物方式转化为PFCAs[30-31]. 相比于挥发性较强的PFASs前体物的长距离迁移,PFASs吸附到颗粒物上的迁移能力较弱,因此,树木年轮中较高浓度的PFASs可能是其前体物长距离迁移至横断山区河谷发生转化导致的. 横断山区地处川西高原,海拔较高,PFASs及其前体物可通过“蚱蜢跳效应”和“高山冷凝效应”逐步实现从大气到地表的迁移并在高海拔地区累积[32]. 因而森林成为偏远地区PFASs的“蓄积库”,应展开进一步研究,估算横断山区森林系统对PFASs的积累量,为高海拔地区的森林生态安全提供基础数据.
-
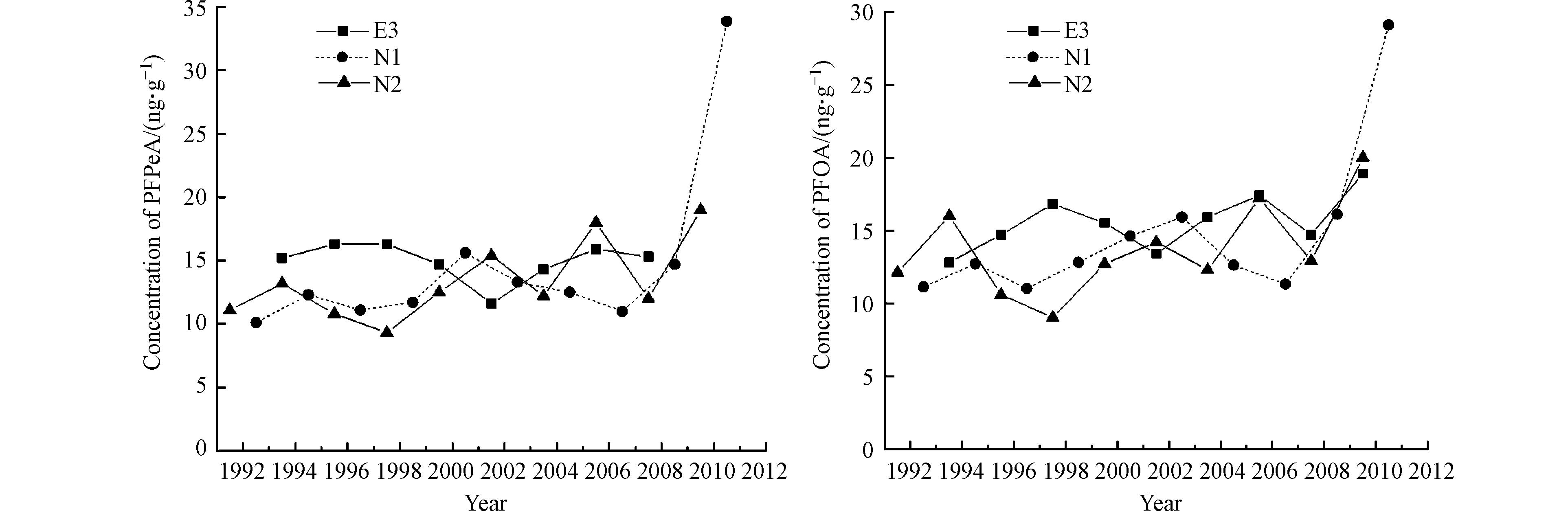
PFPeA与PFOA在E3、N1及N2中的检出率较高,因此,可以通过这3个树芯的年轮探讨PFPeA与PFOA在该区域的污染历史. 如图4所示,PFPeA在E3中1993—2008年的年轮间均有检出,其浓度随时间先降低后升高;在N1和N2中1992—2010年的年轮间均有检出,浓度随时间的变化没有规律性. PFOA在3个树芯年轮的1993—2010年均有检出,整体有升高趋势,尤其是2006年以后上升趋势较为明显,可能是因为全球将氟调聚物作为中间体广泛应用于生产的兴起,而氟调聚物的大气长距离迁移和光化学转化被认为是偏远地区环境中PFCAs主要来源[33].
数据结果显示PFPeA自1991年始就有检出,而PFPeA的生产及使用约从2000年后开始,与其生产使用历史存在明显差异,这可能是前体物的转化导致或者存在横向迁移. 物质的横向迁移表现为在年轮中的含量变化比实际污染历史相位超前或不存在年代变化规律[34],PFASs性质随碳链长度不同存在差异,可能导致不同的物质在年轮中存在不同程度的横向迁移. 另一方面,皮尔逊相关性分析发现PFPeA和PFOA存在显著相关性(r=0.887,P=0.045),PCA分析中也聚为一类,说明两者来源相似,进一步证明云南松年轮中的PFASs来源于大气中前体物的转化. 这也就说明年轮中PFASs的含量变化不符合其生产使用历史且无规律性主要是由于相关前体物的影响. 研究表明,FTOHs可通过生物转化和非生物转化的方式生成PFPeA和PFOA,在微生物接种实验中8:2 FTOH和6:2 FTOH均可以转化为PFPeA和PFOA[35];Ellis等[30]将4:2 FTOH、6:2 FTOH、8:2 FTOH等3种FTOHs在光化学烟雾箱中进行降解反应,结果检测到PFOA及其它代谢产物. 说明FTOHs能够经生物降解和光化学转化生成PFCAs,这些产物以及PFASs颗粒物可通过植物根系和叶片吸收向植物体内传输. 另外PFASs前体物可在植物体内经生物代谢转化为PFASs,如6:2 FTOH和8:2 FTOH能被大豆根吸收向茎和叶传输并逐级代谢生成PFPeA、PFOA及其他代谢产物[36-37]. 因此,在利用树木年轮对PFASs进行历史重建可能会受自身横向迁移以及前体物转化的影响,不能直接用于PFASs的历史反演.
-
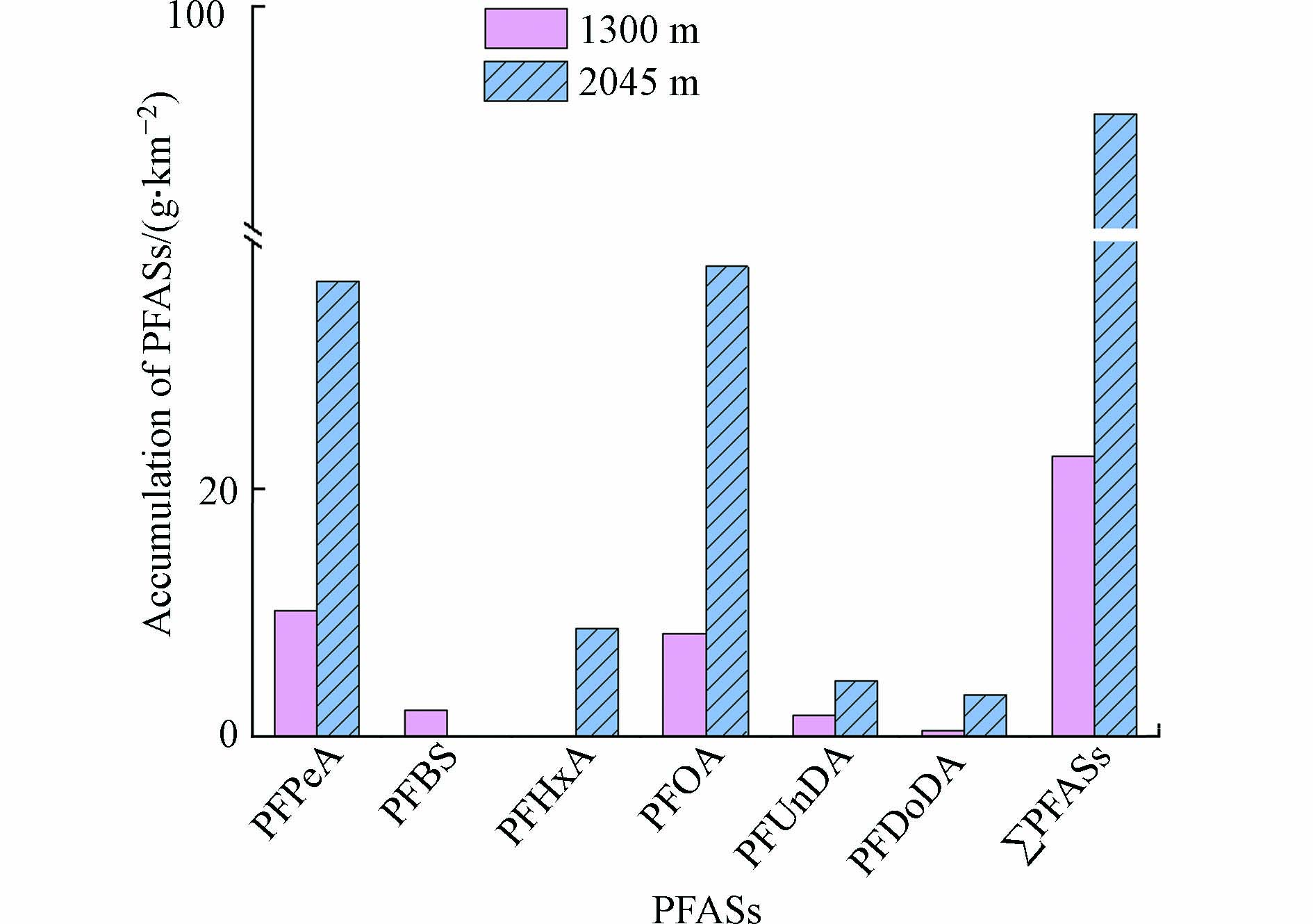
实验数据显示,高低海拔树芯中PFASs平均含量
−w 分别为31.8 ng·g−1和28.5 ng·g−1,据采样调查数据估测(在高低海拔处分别布设35 m×35 m 和 20 m×20 m 样方,样方内云南松密度分别为16株和13株),样方内单株云南松树干的平均生物量−N 分别为71760 g和24397 g. 因此,根据公式(1)可以计算出,单位面积内云南松树干对PFASs的积累量在高低海拔处分别为91.3 g·km−2和22.6 g·km−2(图5),说明高海拔处的云南松树干对PFASs的蓄积量远高于低海拔处. 王褚等[38]发现,随着海拔升高,光照强度也逐渐增强,因此海拔越高处单株植物可生存的空间更多、受光照强度更强,单株植物的生长状况相对更好. 万娟等[39]对三峡库区的植物群落生长特征进行了研究,也发现植被的生长高度随着高程的增加而增加. 说明随着海拔的升高,树干的生物量增大,从而导致全氟化合物在云南松中的积累量增大,因而高海拔地区森林对PFASs的积累更当引起关注. 单位平方千米内云南松树干中ΣPFASs积累量已高达克级别,横断山区森林植被丰富,蓄积的PFASs通量不容小觑,说明森林已经成了继海洋、河流沉积物之后的PFASs的另一个重要蓄积库,一旦随着树木利用再次进入环境,对生态系统和人类健康的风险不可忽视. -
(1)横断山区河谷云南松年轮中共6种PFASs被检出,ΣPFASs浓度范围为nd—75.7 ng·g−1,检出率最高的物质是PFOA(91.8%)和PFPeA(89.8%),二者占比分别高达43.9%和54.5%. 主成分分析结果表明以PFOA、PFPeA、PFUnDA和PFHxA为主要标志物的2个主成分可以解释该地区年轮中84.4%的PFASs来源,主要来源于PFASs及其前体物的大气长距离迁移.
(2)年轮中PFPeA含量随时间变化不符合其生产使用历史,主要是因为前体物发生了生物转化和光化学转化,因此不能直接用于PFASs历史重建,要考虑相关前体物的影响.
(3)单位平方千米内云南松树干对PFASs的积累量已高达克级别,高、低海拔分别为91.3 g·km−2和22.6 g·km−2,说明云南松是PFASs的蓄积库之一,应该引起进一步的关注.
横断山区河谷云南松中全氟化合物的历史反演及赋存特征
Historical inversion and occurrence of perfluoroalkyl substances in Pinus yunnanensis in Valley of Transverse Mountain Area
-
摘要: 为研究森林树木对全氟化合物(PFASs)污染的历史变化及积累,采集了横断山区河谷云南松(Pinus yunnanensis)年轮,采用超高效液相色谱-质谱联用仪分析了树木年轮中12种PFASs的浓度水平. 分析结果表明,年轮中共有6种PFASs检出,ΣPFASs浓度范围为nd—75.7 ng·g-1,其中检出率最高的物质是PFOA(91.8%)和PFPeA(89.8%). 以PFOA、PFPeA、PFUnDA和PFHxA为主要标志物的2个主成分可以解释该地区年轮中84.4%的PFASs来源,主要来源于PFASs及其前体物的大气长距离迁移. 年轮中PFPeA含量随时间变化不符合其生产使用历史,主要受前体物的生物转化和光化学转化影响. 单位面积内云南松树干的积累量在高低海拔分别为91.3 g·km-2和22.6 g·km-2,说明云南松已成为PFASs在环境中的重要蓄积库之一,今后应进一步加强对横断山区和高海拔地区森林树木的研究,为环境中PFASs的管控提供基础数据.
-
关键词:
- 全氟化合物(PFASs) /
- 横断山区河谷 /
- 云南松 /
- 历史反演 /
- 赋存.
Abstract: In order to study the historical change and accumulation of perfluoroalkyl substances in forest trees, twelve PFASs in Pinus yunnanensis’s tree rings collected in Valley of Transverse mountain area were analyzed by ultra-performance liquid chromatography-mass spectrometry (UPLC-MS/MS). The results showed that only six PFASs were detected in the tree rings, and ΣPFASs concentrations ranged in nd— 75.7 ng·g-1, with the greatest detection frequency found in PFOA (91.8%) and PFPeA (89.8%). Two principal components with the main markers of PFOA, PFPeA, PFUnDA and PFHxA could explain 84.4% of the sources of PFASs in the growth rings in this region, which mainly came from the long-distance atmospheric migration of PFASs and their precursors. The temporal distribution of PFPeA concentrations in tree rings was not consistent with its production and use history, which was mainly affected by the biotransformation and photochemical transformation of its precursors. The accumulation of Pinus yunnanensis trunk per unit area were 91.3 g·km-2 and 23.3 g·km-2 at high and low altitudes, respectively, indicating that Pinus yunnanensis has become one of important reservoirs of perfluoroalkyl substances in the environment. Future research on the Transverse mountain area and high altitude areas should be carried out to provide basic data for the control of perfluoroalkyl substances in forest vegetation. -
全氟化合物(perfluoroalkyl substances,PFASs)是一类碳原子连接的氢原子全部被氟原子取代的有机化合物,因其优良的理化性能,被广泛用于化工、皮革和医药等工业及日常生活领域中[1]. 近年来已在大气、水和土壤等[2-4]环境介质及生物体中[5]被广泛检出. 现有的研究已经充分证明PFASs具有内分泌毒性、致癌性、神经毒性及生殖毒性等毒理效应,对环境和生物均存在潜在风险[6-7],因此2009年和2019年,全氟辛烷磺酸(perfluorooctane sulfonate,PFOS)及其盐类、全氟辛酸(perfluorooctanoic acid,PFOA)先后被列入《斯德哥尔摩公约》并加以限制生产和使用. 然而由于经济和生产需求,PFASs的生产逐步转移到亚洲,尤其是中国[8]. PFASs一旦进入环境后能够随着大气发生长距离迁移,到达海拔较高的地区发生“高山冷凝效应”,从而导致高海拔地区成为污染物的“接收器”[9].
现有的研究证实,树木能够有效截留大气中的有机污染物[10],对有机污染物的全球迁移及分布有重要影响[11-12]. 近年来,树木年轮因其分布广泛、样本易得、连续性强等特点,已经作为环境监测的一种手段[13]. 已有学者利用树木年轮作为指示研究大气环境中的多环芳烃、多溴联苯醚等持久性有机污染物(persistent organic pollutants, POPs)[14-15]的迁移及污染特征. 然而,PFASs不同于传统的持久性有机污染物,具有高表面活性、水溶性强等特点,能否用树木年轮来指示大气中的PFASs,并且对其污染历史进行反演,目前尚不清楚. 因此,有必要展开相关研究,探讨树木年轮对大气中PFASs的指示及污染历史重建,以期为偏远地区PFASs的生态风险评估提供科学依据. 目前公认的PFASs在全球的蓄积库为海洋沉积物,而森林植被占陆地面积的31%[16],若对PFASs有富集,其蓄积量不能忽视. 然而目前鲜有研究报道PFASs在森林中的蓄积能力,因此,本研究以横断山区雅砻江下游的云南松(Pinus yunnanensis)年轮为研究对象,分析其PFASs的污染特征与来源,反演PFASs在该地区的污染历史,并计算PFASs在云南松树干中的积累量,明确森林植被对PFASs迁移蓄积的重要性.
1. 材料与方法(Materials and methods)
1.1 研究区域概况
横断山区位于青藏高原东南部,覆盖四川、西藏、青海、云南等省区,总面积达50余万km2,由一系列南北走向的高大山脉和深切河谷组成[17]. 研究区域位于横断山区南部,雅砻江下游河谷地带,气候为干湿分明的亚热带气候,垂直方向的变化明显,植被以云南松为主. 该地人口密度小、地区社会经济不发达,因而本地污染源较少,能够反映污染物通过大气长距离迁移对该地区的影响. 云南松属乔木,是我国西南地区的特有树种,平均高达5—20 m,胸径70—150 cm,横断山区云南松常见树龄为30年左右,适用于对PFASs的历史重建分析[18].
1.2 样品采集
采样地点位于雅砻江河谷二滩水电站库区周边山坡,位于四川省攀枝花境内(101°30′54″E,26°54′7″N). 为避免污染,采样所使用的工具均提前用超纯水和甲醇清洗并干燥,采用内径为5.15 mm的生长锥钻取树芯样,采集位置为距离地面1.3 m处树干位置,分别于2017年8月和2018年1月采集3个(E1、E2、E3)和2个(N1、N2)年轮样品,采样点位置及周边植被情况见图1.
将采集的云南松树芯样品装入聚丙烯采样袋中带回实验室,进行捆绑处理后风干、打磨,通过LINTAB年轮仪测量年轮宽度,利用COFECHA程序辅助交叉定年(排除伪轮、缺轮的影响),实现已知年龄和未知年龄的年轮衔接,最终精确定出每个年轮的生长年份. 树芯基本信息见表1.
表 1 树芯样本信息Table 1. The information of tree core samples树芯Tree cores 位置Location 海拔/mAltitude 胸围/cmDBH 树干高度/mTree height 定年Dating 经度Longitude 纬度Latitude E1 101°41′E 26°53′N 1300 76 12 1993—2012 E2 1300 76 12 1992—2011 E3 1300 73 9 1993—2010 N1 101°39′E 26°55′N 2045 101 16 1992—2011 N2 2045 97 15 1991—2010 1.3 实验材料及试剂
甲醇(色谱纯/99.8%,成都市科龙化工试剂厂)、氨水(25%,成都市科龙化工试剂厂)、Milli-Q超纯水.
实验所用标准样品为高纯度混合标准品PFAC-MXB(Wellington公司),含有全氟羧酸类和全氟磺酸类化合物. 其中,羧酸类包括:全氟丁酸(perfluorobutanoic acid,PFBA)、全氟戊酸(perfluoropentanoic acid,PFPeA)、全氟己酸(perfluorohexanoic acid,PFHxA)、全氟庚酸(perfluoroheptanoic acid,PFHpA)、全氟辛酸(perfluorooctanoic acid,PFOA)、全氟壬酸(perfluorononanoic acid,PFNA)、全氟癸酸(perfluorodecanoic acid,PFDA)、全氟十一酸(perfluoroundecanoic acid,PFUnDA)和全氟十二酸(perfluorododecanoic acid,PFDoDA). 磺酸类包括:全氟丁烷磺酸(perfluorobutanesulfonic acid,PFBS)、全氟己烷磺酸(perfluorohexanesulfonic acid,PFHxS)和全氟辛烷磺酸(perfluorooctanesulfonic acid,PFOS). PFAC-MXA为高纯度混合碳同位素标记品(Wellington公司),包括:13C4-PFBA、13C2-PFHxA、13C4-PFOA、13C5-PFNA、13C2-PFDA、13C2-PFUnDA、13C2-PFDoDA、13O2-PFHxS和13C4-PFOS.
1.4 样品前处理
由于一年的年轮生物量较少,处理起来误差较大,因此将年轮样品从1991—2012年以每两年为一个样品进行切割. 样品的萃取及净化方法参照Jin等[19]处理树皮中PFASs的方法,并在此基础上进行优化. 树木年轮经真空冷冻干燥后研磨粉碎,称取0.1 g左右至15 mL聚丙烯离心管中,加入2 ng内标,涡旋混合均匀后静置过夜. 加入5 mL甲醇,涡旋30 s,超声30 min,以250 r·min−1振荡1 h,再以3000 r·min−1离心10 min,提取上清液至新的15 mL PP管中. 重复上述过程2次,将3次上清液合并,温和氮吹至5 mL后用Envi-Carb固相萃取小柱(500 mg/6 mL)净化. 过柱前分别用5 mL 0.1%氨水甲醇溶液、5 mL超纯水、5 mL甲醇对固相萃取柱进行活化,活化完成后将样品溶液以每秒1滴的流速过萃取柱并用新的15 mL PP管收集流出液,然后使用5 mL甲醇洗脱收集残留在固相萃取柱上的PFASs,两部分溶液合并后氮吹至1 mL转移至样品瓶中,于4 ℃保存,待测.
1.5 仪器分析
实验采用超高效液相色谱串联三重四极杆质谱仪(1290-6470),C18色谱柱(Zorbax SB-C18,2.1 mm×50 mm,1.8 μm). 色谱条件:柱温35 ℃,进样量5 μL,流动相采用5 mmol·L−1乙酸铵溶液(A相)和甲醇(B相),流速0.4 mL·min−1. 流动相梯度洗脱程序:0.00—0.10 min,A相比例为90%;0.10—6.00 min,A相比例由90%降为5%;6.00—8.00 min,A相比例为5%;后运行2 min. 质谱条件:电喷雾离子源;负离子模式(ESI);多反应离子检测(MRM)模式分析;雾化气压力0.24 MPa;电喷雾电压3000 V;干燥气温度250 ℃.
1.6 质量控制与保证
本研究采用内标法定量,标准曲线浓度为0、0.5、1、2、5、20、40 ng·mL−1,线性关系r > 0.99. 为降低实验背景及误差,样品在前处理过程中均避免接触和使用玻璃以及聚四氟乙烯容器. 样品前处理过程中每10个样品设置1个方法空白;测定时,每10个样品设置1个溶剂空白. 回收率实验设置两个不同浓度(2 ng·g−1,20 ng·g−1),每个浓度水平3个平行,方法回收率为72.5%—100.7%(表2),满足实验要求.
表 2 PFASs在年轮中的检出限及回收率Table 2. Detection limits and recoveries of PFASs in tree rings目标物 Objects 检出限/(ng·g−1) MDL 回收率/% Recovery(Avg±SD) 加标2 ng Add standard 2 ng 加标20 ng Add standard 20 ng PFBA 0.003 98.0±1.1 96.1±0.3 PFPeA 0.007 78.9±10.3 74.5±3.0 PFHxA 0.022 100.7±0.6 89.2±1.7 PFHpA 0.002 98.1±4.9 96.5±8.7 PFOA 0.012 98.2±3.2 88.8±1.0 PFNA 0.004 97.0±1.6 86.2±0.5 PFDA 0.011 100.4±1.7 90.1±1.8 PFUnDA 0.006 98.5±5.4 86.2±1.9 PFDoDA 0.006 98.0±1.8 87.5±1.5 PFBS 0.012 76.3±6.8 72.5±8.1 PFHxS 0.008 99.3±5.9 98.9±1.4 PFOS 0.005 97.1±1.8 92.0±1.1 对于没有在空白样品中检测出的PFASs,其方法检出限(MDLs)为3倍信噪比时对应的浓度;对于在空白样品中检测到的PFASs,其MDLs值为空白样品中浓度的均值加上3倍的标准偏差. 在处理数据时,检测值低于MDLs值时,用MDLs值除以
√2 1.7 PFASs积累量
本研究参照王荣芬[20]的方法对单位面积云南松树干中PFASs的积累量进行计算,具体方法如下:采用木材密度法即平均材积与木材密度的乘积计算得到云南松树干的生物量,平均材积根据样方内云南松树干高度和胸径在标准立木材积表[21]中查得后取平均值,木材密度采用树芯重量与树芯体积之比的平均值;然后根据树芯中PFASs的平均含量计算出单株云南松树干中PFASs的平均积累量. 再根据样方大小和样方内云南松密度计算单位平方千米内云南松树干对PFASs的储量,结果可为横断山区森林系统对PFASs的蓄积提供基础数据,计算公式如下:
M=ˉw⋅ˉN⋅n=ˉw⋅[¯(mπ⋅r2⋅R)⋅ˉV]⋅n (1) 公式(1)中,M为单位面积云南松树干中PFASs储量(g·km−2),
−w −N −V 2. 结果与讨论(Results and discussion)
2.1 年轮中PFASs的污染特征及来源解析
5个树芯样品中检出率最高的单体物质为PFOA和PFPeA,分别为91.8%和89.8%;其次为PFUnDA (22.4%)> PFBS(12.2%)> PFDoDA(10.2%)> PFHxA(6.12%);PFBA、PFHxS、PFHpA、PFOS、PFDA和PFNA均未检出. ΣPFASs浓度范围为nd—75.7 ng·g−1,平均值为30.9 ng·g−1,其中浓度最高的物质是PFPeA,平均值为12.7 ng·g−1;其次为PFOA,平均值为12.5 ng·g−1;然后依次为PFUnDA(1.99 ng·g−1)>PFHxA(1.43 ng·g−1)> PFBS(1.33 ng·g−1)> PFDoDA(0.95 ng·g−1),PFOA和PFPeA的浓度显著高于其余单体浓度. 5个树芯样品中ΣPFASs浓度分别为E1(31.0 ng·g−1)、E2(21.9 ng·g−1)、E3(34.6 ng·g−1)、N1(31.7 ng·g−1)和 N2(31.9 ng·g−1)(图2),平均浓度为(30.2±4.4 )ng·g−1. 魏明翠等[22]研究氟化学工业园周边树叶和树皮样品中的PFASs,得到树叶中ΣPFASs范围为4.90—185 ng·g−1,树皮中∑PFASs范围为0.240—95.4 ng·g−1;Shan等[23]以江苏省受污染地区的樟脑树叶为研究对象,测定树叶中PFASs浓度范围为10—276 ng·g−1. 与受污染地区植物的树叶及树皮中PFASs浓度相比,雅砻江下游云南松年轮样品中PFASs浓度约低1个数量级,此结果与研究地区的人口密度和工业发展程度相吻合. 此外,E为海拔1300 m的树木年轮((28.5±5.4)ng·g−1),N为海拔2045 m的树木年轮((31.8±0.1)ng·g−1),二者ΣPFASs浓度无显著差异. Taniyasu等[24]测定日本偏远山区与周边城市降雪中PFASs的浓度发现其与海拔高度无关;而Wang等[25]测定了山区中不同海拔高度的土壤中PFASs浓度,发现PFOA浓度随海拔高度增加而升高. 说明PFASs浓度的影响因素较复杂,即使是同一研究区域,也可能因样本不同、样本性质、周围环境等因素出现差异.
PFASs各单体在年轮中比例特征如图2所示,总体上PFASs的比例特征较为一致,均以短碳链和PFOA为主,其中PFPeA和PFOA占比分别高达54.5%和43.9%. PFOA作为树木年轮中PFASs的主要贡献者之一,和Jin等[19]及魏明翠等[22]的研究结果一致. E点年轮中均有检出PFBS,占比最高为16.8%;N点年轮中均检出了PFHxA,占比最高为12.1%,说明分别存在PFBS和PFHxA的污染来源. 在所有树芯中,长碳链的PFDoDA和PFUnDA基本上均被检出,占比最高分别为4.86%和11.2%.
采用主成分分析法对云南松年轮中检出的6种PFASs解析,得到主成分分析图(图3),筛选出2个特征值 > 1的因子,累计方差贡献率达到84.4%. 其中,因子1可以解释年轮中51.1%的PFASs来源,PFUnDA、PFPeA和PFOA具有较高载荷值,分别为0.990、0.973和0.800;因子2可以解释年轮中33.3%的PFASs来源,PFHxA具有较高载荷值(0.911). 由于研究区域远离工业区,周围人类活动较少,说明该区域树木年轮中的PFASs大部分来自于大气远距离传输,PFASs到达偏远地区通常有两个传输途径:第一种为直接路径,PFASs因其较低的挥发性,能随大气和洋流直接在全球范围内进行迁移;第二种为间接途径,PFASs前体物质具有较强的挥发性或半挥发性,可随大气迁移后经过干湿沉降、降解进入偏远地区[26-28]. 研究表明,全氟烷磺酰胺(FASA)和全氟烷磺酰胺乙醇(FASE)可以转化为PFCAs和PFSAs[29],氟调醇(FTOHs)可以通过非生物或生物方式转化为PFCAs[30-31]. 相比于挥发性较强的PFASs前体物的长距离迁移,PFASs吸附到颗粒物上的迁移能力较弱,因此,树木年轮中较高浓度的PFASs可能是其前体物长距离迁移至横断山区河谷发生转化导致的. 横断山区地处川西高原,海拔较高,PFASs及其前体物可通过“蚱蜢跳效应”和“高山冷凝效应”逐步实现从大气到地表的迁移并在高海拔地区累积[32]. 因而森林成为偏远地区PFASs的“蓄积库”,应展开进一步研究,估算横断山区森林系统对PFASs的积累量,为高海拔地区的森林生态安全提供基础数据.
2.2 PFPeA和PFOA的历史重建
PFPeA与PFOA在E3、N1及N2中的检出率较高,因此,可以通过这3个树芯的年轮探讨PFPeA与PFOA在该区域的污染历史. 如图4所示,PFPeA在E3中1993—2008年的年轮间均有检出,其浓度随时间先降低后升高;在N1和N2中1992—2010年的年轮间均有检出,浓度随时间的变化没有规律性. PFOA在3个树芯年轮的1993—2010年均有检出,整体有升高趋势,尤其是2006年以后上升趋势较为明显,可能是因为全球将氟调聚物作为中间体广泛应用于生产的兴起,而氟调聚物的大气长距离迁移和光化学转化被认为是偏远地区环境中PFCAs主要来源[33].
数据结果显示PFPeA自1991年始就有检出,而PFPeA的生产及使用约从2000年后开始,与其生产使用历史存在明显差异,这可能是前体物的转化导致或者存在横向迁移. 物质的横向迁移表现为在年轮中的含量变化比实际污染历史相位超前或不存在年代变化规律[34],PFASs性质随碳链长度不同存在差异,可能导致不同的物质在年轮中存在不同程度的横向迁移. 另一方面,皮尔逊相关性分析发现PFPeA和PFOA存在显著相关性(r=0.887,P=0.045),PCA分析中也聚为一类,说明两者来源相似,进一步证明云南松年轮中的PFASs来源于大气中前体物的转化. 这也就说明年轮中PFASs的含量变化不符合其生产使用历史且无规律性主要是由于相关前体物的影响. 研究表明,FTOHs可通过生物转化和非生物转化的方式生成PFPeA和PFOA,在微生物接种实验中8:2 FTOH和6:2 FTOH均可以转化为PFPeA和PFOA[35];Ellis等[30]将4:2 FTOH、6:2 FTOH、8:2 FTOH等3种FTOHs在光化学烟雾箱中进行降解反应,结果检测到PFOA及其它代谢产物. 说明FTOHs能够经生物降解和光化学转化生成PFCAs,这些产物以及PFASs颗粒物可通过植物根系和叶片吸收向植物体内传输. 另外PFASs前体物可在植物体内经生物代谢转化为PFASs,如6:2 FTOH和8:2 FTOH能被大豆根吸收向茎和叶传输并逐级代谢生成PFPeA、PFOA及其他代谢产物[36-37]. 因此,在利用树木年轮对PFASs进行历史重建可能会受自身横向迁移以及前体物转化的影响,不能直接用于PFASs的历史反演.
2.3 云南松树干中PFASs积累量
实验数据显示,高低海拔树芯中PFASs平均含量
−w −N 3. 结论(Conclusion)
(1)横断山区河谷云南松年轮中共6种PFASs被检出,ΣPFASs浓度范围为nd—75.7 ng·g−1,检出率最高的物质是PFOA(91.8%)和PFPeA(89.8%),二者占比分别高达43.9%和54.5%. 主成分分析结果表明以PFOA、PFPeA、PFUnDA和PFHxA为主要标志物的2个主成分可以解释该地区年轮中84.4%的PFASs来源,主要来源于PFASs及其前体物的大气长距离迁移.
(2)年轮中PFPeA含量随时间变化不符合其生产使用历史,主要是因为前体物发生了生物转化和光化学转化,因此不能直接用于PFASs历史重建,要考虑相关前体物的影响.
(3)单位平方千米内云南松树干对PFASs的积累量已高达克级别,高、低海拔分别为91.3 g·km−2和22.6 g·km−2,说明云南松是PFASs的蓄积库之一,应该引起进一步的关注.
-
表 1 树芯样本信息
Table 1. The information of tree core samples
树芯Tree cores 位置Location 海拔/mAltitude 胸围/cmDBH 树干高度/mTree height 定年Dating 经度Longitude 纬度Latitude E1 101°41′E 26°53′N 1300 76 12 1993—2012 E2 1300 76 12 1992—2011 E3 1300 73 9 1993—2010 N1 101°39′E 26°55′N 2045 101 16 1992—2011 N2 2045 97 15 1991—2010 表 2 PFASs在年轮中的检出限及回收率
Table 2. Detection limits and recoveries of PFASs in tree rings
目标物 Objects 检出限/(ng·g−1) MDL 回收率/% Recovery(Avg±SD) 加标2 ng Add standard 2 ng 加标20 ng Add standard 20 ng PFBA 0.003 98.0±1.1 96.1±0.3 PFPeA 0.007 78.9±10.3 74.5±3.0 PFHxA 0.022 100.7±0.6 89.2±1.7 PFHpA 0.002 98.1±4.9 96.5±8.7 PFOA 0.012 98.2±3.2 88.8±1.0 PFNA 0.004 97.0±1.6 86.2±0.5 PFDA 0.011 100.4±1.7 90.1±1.8 PFUnDA 0.006 98.5±5.4 86.2±1.9 PFDoDA 0.006 98.0±1.8 87.5±1.5 PFBS 0.012 76.3±6.8 72.5±8.1 PFHxS 0.008 99.3±5.9 98.9±1.4 PFOS 0.005 97.1±1.8 92.0±1.1 -
[1] PREVEDOUROS K, COUSINS I T, BUCK R C, et al. Sources, fate and transport of perfluorocarboxylates [J]. ChemInform, 2006, 37(11): 32-44. [2] SHOEIB M, HARNER T, WILFORD B H, et al. Perfluorinated sulfonamides in indoor and outdoor air and indoor dust: Occurrence, partitioning, and human exposure [J]. Environmental Science & Technology, 2005, 39(17): 6599-6606. [3] 杨洪法, 史斌, 周云桥, 等. 中、韩滨海城市化区域水体全氟化合物的空间特征及生态风险 [J]. 环境科学, 2020, 41(4): 1607-1618. doi: 10.13227/j.hjkx.201910153 YANG H F, SHI B, ZHOU Y Q, et al. Spatial characteristics and ecological risks of perfluoroalkyl substances in coastal urbanized areas of China and south Korea [J]. Environmental Science, 2020, 41(4): 1607-1618(in Chinese). doi: 10.13227/j.hjkx.201910153
[4] 李法松, 倪卉, 黄涵宇, 等. 安徽省部分城市土壤中全氟化合物空间分布及来源解析 [J]. 环境科学, 2017, 38(1): 327-332. doi: 10.13227/j.hjkx.201605019 LI F S, NI H, HUANG H Y, et al. Spatial distribution and source of perfluorinated compounds in urban soil from part of cities in Anhui Province, China [J]. Environmental Science, 2017, 38(1): 327-332(in Chinese). doi: 10.13227/j.hjkx.201605019
[5] SCHUETZE A, HEBERER T, EFFKEMANN S, et al. Occurrence and assessment of perfluorinated chemicals in wild fish from Northern Germany [J]. Chemosphere, 2010, 78(6): 647-652. doi: 10.1016/j.chemosphere.2009.12.015 [6] NEWSTED J L, JONES P D, COADY K, et al. Avian toxicity reference values for perfluorooctane sulfonate [J]. Environmental Science & Technology, 2005, 39(23): 9357-9362. [7] LAU C, ANITOLE K, HODES C, et al. Perfluoroalkyl acids: A review of monitoring and toxicological findings [J]. Toxicological Sciences, 2007, 99(2): 366-394. doi: 10.1093/toxsci/kfm128 [8] WANG Z Y, COUSINS I T, SCHERINGER M, et al. Global emission inventories for C4-C14 perfluoroalkyl carboxylic acid (PFCA) homologues from 1951 to 2030, Part I: Production and emissions from quantifiable sources [J]. Environment International, 2014, 70: 62-75. doi: 10.1016/j.envint.2014.04.013 [9] 潘静, 盖楠. 中国高山及高原边缘过渡区环境中持久性有机污染物研究进展 [J]. 环境化学, 2018, 37(5): 1002-1012. PAN J, GAI N. Research progress on persistent organic pollutants in alpine and plateau edge transitional region environment, China [J]. Environmental Chemistry, 2018, 37(5): 1002-1012(in Chinese).
[10] SIMONICH S L, HITES R A. Vegetation-atmosphere partitioning of polycyclic aromatic hydrocarbons [J]. Environmental Science & Technology, 1994, 28(5): 939-943. [11] MCLACHLAN M S, HORSTMANN M. Forests as filters of airborne organic pollutants: A model [J]. Environmental Science & Technology, 1998, 32(3): 413-420. [12] WANIA F, MCLACHLAN M S. Estimating the influence of forests on the overall fate of semivolatile organic compounds using a multimedia fate model [J]. Environmental Science & Technology, 2001, 35(3): 582-590. [13] 杨银科, 黄强, 王文科, 等. 利用树木年轮资料分析环境污染的研究进展 [J]. 安徽农业科学, 2011, 39(15): 8948-8950. doi: 10.3969/j.issn.0517-6611.2011.15.049 YANG Y K, HUANG Q, WANG W K, et al. Advances in analysis of environmental pollution by using tree-ring data [J]. Journal of Anhui Agricultural Sciences, 2011, 39(15): 8948-8950(in Chinese). doi: 10.3969/j.issn.0517-6611.2011.15.049
[14] 刘波. 乔木树叶、树皮和树木年轮作为大气中PBDEs和重金属污染生物指示物研究[D]. 上海: 华东理工大学, 2017. LIU B. Studies on tree leaves, bark and rings as bionidicators of PBDEs and heavy metals in air[D]. Shanghai: East China University of Science and Technology, 2017(in Chinese).
[15] WANG Q Q, ZHAO Y L, YAN D, et al. Historical records of airborne polycyclic aromatic hydrocarbons by analyzing dated corks of the bark pocket in a Longpetiole Beech tree [J]. Environmental Science & Technology, 2004, 38(18): 4739-4744. [16] Food and Agriculture Organization of the United Nations. Global Forest Resources Assessment 2020-Key findings[R]. Rome: FAO, 2020. [17] DONG D H, TAO W C, LAU W K M, et al. Interdecadal variation of precipitation over the Hengduan mountains during rainy seasons [J]. Journal of Climate, 2019, 32(12): 3743-3760. doi: 10.1175/JCLI-D-18-0670.1 [18] 陈飞, 王健敏, 孙宝刚, 等. 云南松的地理分布与气候关系 [J]. 林业科学研究, 2012, 25(2): 163-168. doi: 10.3969/j.issn.1001-1498.2012.02.009 CHEN F, WANG J M, SUN B G, et al. Relationship between geographical distribution of Pinus yunnanensis and climate [J]. Forest Research, 2012, 25(2): 163-168(in Chinese). doi: 10.3969/j.issn.1001-1498.2012.02.009
[19] JIN H B, SHAN G Q, ZHU L Y, et al. Perfluoroalkyl acids including isomers in tree barks from a Chinese fluorochemical manufacturing park: Implication for airborne transportation [J]. Environmental Science & Technology, 2018, 52(4): 2016-2024. [20] 王荣芬, 邱尔发, 唐丽清. 行道树毛白杨树干中重金属元素分布 [J]. 生态学报, 2014, 34(15): 4212-4222. WANG R F, QIU E F, TANG L Q. Heavy metals distribution in roadside tree trunks under a heavy urban transportation condition [J]. Acta Ecologica Sinica, 2014, 34(15): 4212-4222(in Chinese).
[21] 中华人民共和国农林部. 立木材积表: LY 208—77[S]. 北京: 中国标准出版社, 1978. Ministry of Agriculture and Forestry of the People's Republic of China. Standing timber volume Table: LY 208—77[S]. Beijing: Standards Press of China, 1978 (in Chinese).
[22] 魏明翠, 钟文珏, 赵丽霞, 等. 南方某氟化学工业园周围环境中全氟化合物的分布研究 [J]. 环境科学学报, 2013, 33(7): 1989-1995. doi: 10.13671/j.hjkxxb.2013.07.032 WEI M C, ZHONG W J, ZHAO L X, et al. Distribution and profile of perfluorinated compounds in the environment around a fluorine chemistry industrial park in South China [J]. Acta Scientiae Circumstantiae, 2013, 33(7): 1989-1995(in Chinese). doi: 10.13671/j.hjkxxb.2013.07.032
[23] SHAN G Q, WEI M C, ZHU L Y, et al. Concentration profiles and spatial distribution of perfluoroalkyl substances in an industrial center with condensed fluorochemical facilities [J]. Science of the Total Environment, 2014, 490: 351-359. doi: 10.1016/j.scitotenv.2014.05.005 [24] TANIYASU S, YAMASHITA N, MOON H B, et al. Does wet precipitation represent local and regional atmospheric transportation by perfluorinated alkyl substances? [J]. Environment International, 2013, 55: 25-32. doi: 10.1016/j.envint.2013.02.005 [25] WANG Q, ZHAO Z, RUAN Y F, et al. Occurrence and distribution of perfluorooctanoic acid (PFOA) and perfluorooctanesulfonic acid (PFOS) in natural forest soils: A nationwide study in China [J]. The Science of the Total Environment, 2018, 645: 596-602. doi: 10.1016/j.scitotenv.2018.07.151 [26] STOCK N L, FURDUI V I, MUIR D C G, et al. Perfluoroalkyl contaminants in the Canadian Arctic: Evidence of atmospheric transport and local contamination [J]. Environmental Science & Technology, 2007, 41(10): 3529-3536. [27] WANG Z, XIE Z Y, MI W Y, et al. Neutral poly/per-fluoroalkyl substances in air from the Atlantic to the Southern Ocean and in Antarctic snow [J]. Environmental Science & Technology, 2015, 49(13): 7770-7775. [28] STYLER S A, MYERS A L, DONALDSON D J. Heterogeneous photooxidation of fluorotelomer alcohols: A new source of aerosol-phase perfluorinated carboxylic acids [J]. Environmental Science & Technology, 2013, 47(12): 6358-6367. [29] MARTIN J W, ASHER B J, BEESOON S, et al. PFOS or PreFOS?Are perfluorooctane sulfonate precursors (PreFOS) important determinants of human and environmental perfluorooctane sulfonate (PFOS) exposure? [J]. Journal of Environmental Monitoring, 2010, 12(11): 1979-2004. doi: 10.1039/c0em00295j [30] ELLIS D A, MARTIN J W, de SILVA A O, et al. Degradation of fluorotelomer alcohols: A likely atmospheric source of perfluorinated carboxylic acids [J]. Environmental Science & Technology, 2004, 38(12): 3316-3321. [31] BUTT C M, MUIR D C G, MABURY S A. Biotransformation pathways of fluorotelomer-based polyfluoroalkyl substances: A review [J]. Environmental Toxicology and Chemistry, 2014, 33(2): 243-267. doi: 10.1002/etc.2407 [32] 温祥洁, 陈朝辉, 徐维新, 等. 青藏高原东北部地区表层土壤中全氟化合物的分布特征及来源解析[J]. 环境科学, 2022, 43(6): 3253-3261. WEN X J, CHEN Z H, XU W X, et al. Distribution characteristics and source apportionment of perfluoroalkyl substances in surface soils of the northeast Tibetan Plateau[J]. Environmental Science, 2022, 43(6): 3253-3261 (in Chinese).
[33] 姚义鸣, 赵洋洋, 孙红文. 天津市大气中全氟化合物挥发性前体物的分布和季节变化 [J]. 环境化学, 2016, 35(7): 1329-1336. doi: 10.7524/j.issn.0254-6108.2016.07.2015120903 YAO Y M, ZHAO Y Y, SUN H W. The atmospheric distribution and seasonal variation of volatile perfluoroalkyl substance precursors in Tianjin [J]. Environmental Chemistry, 2016, 35(7): 1329-1336(in Chinese). doi: 10.7524/j.issn.0254-6108.2016.07.2015120903
[34] 陈诗音. 过去170年以来福州重金属含量的树轮记录研究[D]. 福州: 福建师范大学, 2019. CHEN S Y. Heavy metal pollution history in Fuzhou area over the past 170 years inferred from tree rings[D]. Fuzhou: Fujian Normal University, 2019(in Chinese).
[35] 陈红瑞, 张昱, 杨敏. 全氟化合物前体物氟调醇的检测方法、环境分布及转化研究进展 [J]. 环境化学, 2015, 34(12): 2170-2178. doi: 10.7524/j.issn.0254-6108.2015.12.2015052602 CHEN H R, ZHANG Y, YANG M. Research progress on the detection methods, environmental distribution and transformation of perfluorinated compounds' precursors fluorotelomer alcohols [J]. Environmental Chemistry, 2015, 34(12): 2170-2178(in Chinese). doi: 10.7524/j.issn.0254-6108.2015.12.2015052602
[36] ZHANG H N, WEN B, HUANG H L, et al. Biotransformation of 6: 2 fluorotelomer alcohol by the whole soybean (Glycine max L. Merrill) seedlings [J]. Environmental Pollution, 2020, 257: 113513. doi: 10.1016/j.envpol.2019.113513 [37] ZHANG H N, WEN B, HU X Y, et al. Uptake, translocation, and metabolism of 8: 2 fluorotelomer alcohol in soybean (Glycine max L. Merrill) [J]. Environmental Science & Technology, 2016, 50(24): 13309-13317. [38] 王褚, 王世伟, 潘存德, 等. 天山北坡中部天山云杉林植物多样性沿海拔变化特征 [J]. 新疆农业大学学报, 2021, 44(3): 172-178. doi: 10.3969/j.issn.1007-8614.2021.03.003 WANG C, WANG S W, PAN C D, et al. Variation characteristics of plant diversity along altitude in Picea schrenk-iana forestin the central part of the northern slope of Tianshan mountains [J]. Journal of Xinjiang Agricultural University, 2021, 44(3): 172-178(in Chinese). doi: 10.3969/j.issn.1007-8614.2021.03.003
[39] 万娟, 刘佳瑞, 肖衡林, 等. 三峡库区消落带植物群落分布及生长影响因素分析 [J]. 湖北工业大学学报, 2019, 34(5): 83-87. doi: 10.3969/j.issn.1003-4684.2019.05.019 WAN J, LIU J R, XIAO H L, et al. Analysis on the influencing factors of distribution and growth of plant communities in the water-fluctuating zone of the Three Gorges reservoir area [J]. Journal of Hubei University of Technology, 2019, 34(5): 83-87(in Chinese). doi: 10.3969/j.issn.1003-4684.2019.05.019
期刊类型引用(0)
其他类型引用(1)
-






 下载:
下载: