-
随着社会经济的高速发展,人类正面临着能源匮乏和水环境污染的双重危机,亟需开发环境友好、可重复再生的清洁能源。相较于化石能源,生物质能源因具有可再生性、原料丰富和环境友好等优点[1],被认为是环境可持续发展框架下新能源的重要发展方向[2]。在众多生物质原料中,微藻具有生长周期短、光合效率高、适应污水生长以及“不与人争粮和不与粮争地”的优势,被认为是一种极具潜力的生物柴油生产原料[3]。当前,利用微藻制备生物柴油,已成为新型可再生清洁能源开发的研究热点,但高成本问题始终制约着微藻生物柴油的产业化进程[4]。因此,如何提升油脂产率,提高微藻工艺的综合效益已成为促进微藻生物燃料实现低成本、规模化生产的关键。
截止目前,营养盐调控仍是提高微藻产量及油脂含量的可靠方法[5],通常情况下,培养体系中营养成分如碳、氮、硫等的变化会影响微藻生长与内部物质的积累[6]。碳是微藻生长必不可少的营养元素[7],约占藻细胞干质量的50%,是藻细胞的主要组成部分。KHAWAJA等[8]研究表明,不同碳源对促进微藻生长存在较大差异,在异养情况下,小分子碳源更有利于微藻生长。氮是蛋白质合成的重要元素,对促进碳源代谢至关重要。ANAND等[9]研究表明,贫氮条件更利于微藻积累油脂,富氮条件更利于促进微藻生长,存在兼顾微藻生长与油脂积累的氮浓度。碳、氮的耦合作用对微藻生长的促进作用也不容忽视。ZHENG等[10]指出,C/N过低会抑制微藻生长,过高不利于释放微藻生长潜力,存在适宜微藻生长的最适C/N。此外,硫是微藻碳氮代谢的关键偶联元素,调控着微藻生长和细胞代谢过程。LV等[11]研究表明,硫酸盐缺乏会削弱微藻生长与污水净化的能力;王倩雅等[12]也指出,硫限制会导致藻细胞碳氮代谢途径重新调整。当前,针对营养元素影响微藻生长、油脂积累的研究主要集中于单一碳源、单一氮源方面,而对不同C/N条件下硫元素的影响研究较少,而从硫元素出发研究微藻的生长、胞内组分动态变化,对全面了解微藻光合产油机制具有重要意义。
因此,本研究以斜生栅藻为研究对象,探究了微藻生长、碳氮去除、油脂积累与脂肪酸分布对水体C/N变化的响应规律以及硫在其中的调控作用,旨在了解不同C/N条件下硫对微藻光合作用、碳氮利用和油脂积累的影响,以期为探究微藻碳流趋向油脂积累的光合营养机制提供参考。
-
本实验选用由中科院淡水藻种库提供的斜生栅藻(Scenedesmus obliquus,FACHB-12)作为受试藻种。斜生栅藻属于绿藻门,适应污水环境且对营养盐具有较高的吸收转化能力,是生产生物柴油的优势藻种[13]。实验前先将藻种在无菌条件下转接至装有BG11培养基的锥形瓶中,于(25±1) ℃、光照度4800 Lx,光暗比12 h:12 h的恒温培养箱(PGX-350B,宁波赛福实验仪器有限公司)中进行扩大培养,培养期间应每天随机变换锥形瓶位置以保证受光均匀,并按时摇动锥形瓶3次确保藻水混合均匀。实验中所用玻璃制品、培养基等均经高温高压灭菌后使用(温度121 ℃,时间20 min)。
-
乙酸钠、氯化铵是促进微藻生长的优质营养盐[14-15],因此,本实验选用乙酸钠和氯化铵分别作为实验用碳源、氮源,并结合前人已有研究配制实验用水[16],即1 L实验用水中包含385 mg NaAc(300 mg·L−1 COD);115 mg NH4Cl(30 mg·L−1
NH+4 -N);13 mg KH2PO4;0.55 mg FeCl2·4H2O;6 mg CaCl2;66 mg MgCl2·6H2O;1 mL A5溶液 (A5溶液为微量金属的混合液,1 L的A5溶液包括:0.08 g·L−1 CuCl2·2H2O、1.86 g·L−1 MnCl2·4H2O、0.22 g·L−1 ZnCl2、0.39 g·L−1 Na2MoO4·2H2O、0.05 g·L−1 Co(NO3)2·6H2O、2.86 g·L−1 H3BO3)。其中,根据调整配方中NH4Cl的质量配制氮元素浓度分别为0、5、10、20、40 mg·L−1的实验用水。此外,将配方中的FeCl2·4H2O、MgCl2·6H2O替换成等质量的FeSO4·7H2O、MgSO4·7H2O,用于配制含硫实验用水。上述实验用水配制完毕随即置于高压灭菌锅(SN310C,日本雅马拓公司)中灭菌,隔夜冷却后使用。 -
本实验在已有研究基础上设置4种不同C/N水平[17](C/N水平为:7.5,15,30,60)及缺硫、含硫两种条件,对照组中不含NH4+-N,每组设置3个平行实验。首先,将藻液置于BG11培养基中培养10 d至对数生长期,再将对数生长期藻液置于高速冷冻离心机(TGL168,长沙湘智离心机有限公司),在3500 r·min−1、4 ℃条件下离心8 min,舍弃上清液,用15 mg·L−1的NaHCO3溶液冲洗藻体并离心2次,以去除藻细胞表面吸附的营养盐;随后用无菌水冲洗、离心2次再将其转入无氮培养基培养3 d以耗尽藻细胞内营养盐并离心获取藻细胞;最后用无菌水冲洗、离心3次后用无菌水再悬浮,测定藻细胞密度后供实验使用。实验开始时,在已灭菌的锥形瓶里加入500 mL实验用水,再加入一定量上述实验藻液,保证初始接种密度为1×106 cells mL−1,实验周期设置为5 d。每天定时取样。在培养结束后,离心收集各平行实验微藻生物量并富集于50 mL离心管中,经冲洗和真空冷冻干燥(DZF-6020,上海煜南仪器有限公司)用于油脂与脂肪酸测定。
-
取混匀的藻浓液1 mL于15 mL离心管中,用无菌水稀释至10 mL并摇匀,用滴管取适量藻液注入血球计数板(25×16)并利用显微镜(CX33,南京奥力科学仪器有限公司)计数3次,若3次误差大于10%,则重新计数直至符合实验标准。同时,保证每个计数格中的藻细胞数为5—8个,以便精准计数,否则应调整藻液稀释倍数重新计数。
-
取适量藻密度已知的藻浓液按5倍梯度稀释7个样品(每个梯度下的藻密度可根据计算得到),利用紫外可见分光光度计(DR 6000,美国哈希公司)在682 nm波长下进行测定,以得到的吸光度值为横坐标,藻密度为纵坐标绘制藻密度标准曲线(y=197.53x,R2=0.9999)。
-
水质参数:污水pH采用pH计(FE 28,美国梅特勒-托利多公司)测定;水体COD采用COD快速消解仪(DRB 200,美国哈希公司)测定;水体
NH+4 -N浓度采用纳氏试剂分光光度法(HJ535-2009)测定。油脂含量及脂肪酸:取适量真空冷冻干燥后的微藻混合样于试管中,加入10 mL盐酸溶液,在70 —80 ℃下水浴,至试样消解完全;取出试管,加入10 mL乙醇并混匀,将试管中的水解液转移到分液漏斗中,用乙醚石油醚混合液冲洗试管和塞子,冲洗液并入分液漏斗中,加盖振摇后静置,将醚层提取液收集到250 mL烧瓶中,按上述步骤重复提取水解液3次,再用乙醚石油醚混合液冲洗漏斗,并收集到已恒重的烧瓶中,将烧瓶置水浴上蒸干,最后置于 (100 ± 5) ℃干燥至恒重,计算油脂含量。然后对脂肪进行皂化以及脂肪酸甲酯化处理,再利用气相色谱仪(Agilent 7890A,美国安捷伦公司)进行脂肪酸分析,色谱柱为HP-88 (100 m×0.25 mm×0.20 μm),检测器为FID,采用分流方式进样,分流比为0.8。
其中,
Mt 为收获时藻的生物质浓度(mg·L−1),Lt 为收获时总脂含量,t 为培养时间。 -
实验数据采用SPSS 25进行单因素方差分析,采用LSD法进行统计检验,P<0.05表示差异有统计学意义;采用Origin 2017进行绘图。
-
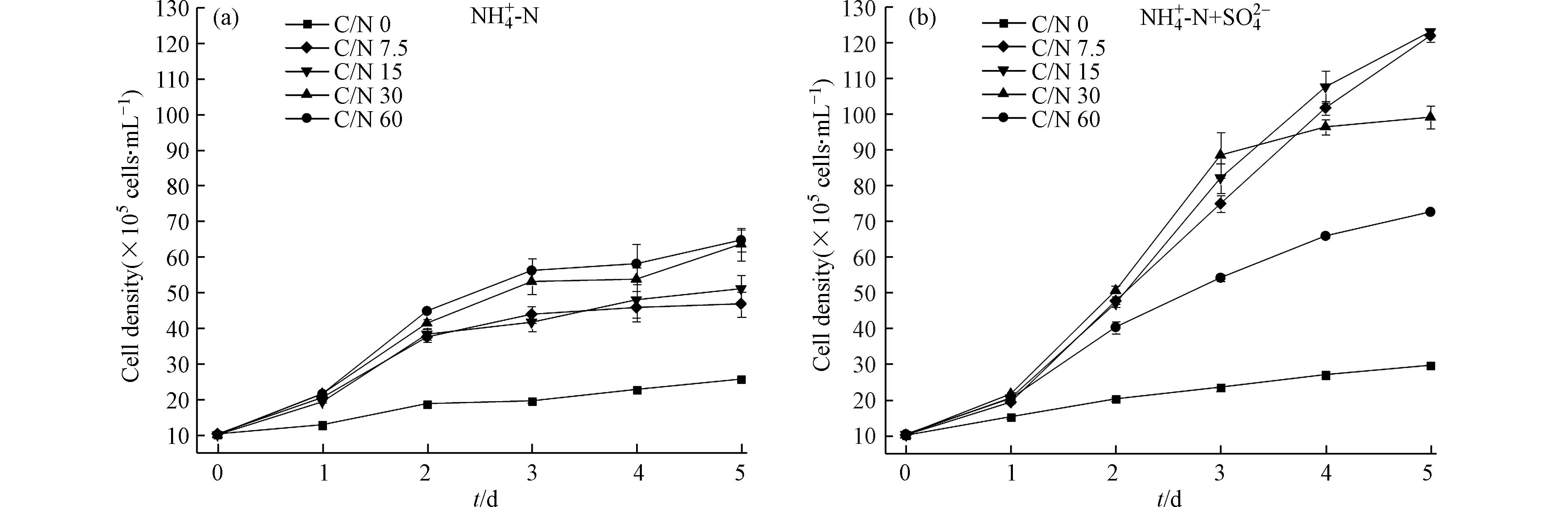
图1为无硫和含硫条件下,水体的C/N对微藻生长的影响情况。培养到第5天,含硫条件下各组别藻细胞密度显著高于无硫组(P<0.05)。
如图1所示,在无硫条件下,斜生栅藻在培养初始阶段经过短暂的适应期后加速生长,藻细胞密度不断升高,随着C/N的增大,藻细胞密度也逐渐上升,培养到第5天,C/N为60的组别藻密度达到最大,为6.46×106 cells·mL−1;而在含硫条件下,藻细胞密度在C/N为15时达到最高,为1.23×107 cells·mL−1,较无硫条件提升了90%。无硫条件下藻细胞密度较低主要是因为藻细胞内加氧酶的酶活性降低,并诱导活性氧的产生,从而抑制了生长[18]。硫作为叶绿素合成的重要因子,加入后可有效促进藻细胞合成叶绿素,进而增强微藻光合作用,促进了藻细胞生长[19],使得含硫条件下藻细胞密度有了较大的提高。MICHAL等[1]通过实验也证实了这一点。此外,在高C/N条件下碳源充足,随着氮素的消耗,氮逐渐成为微藻生长的限制因子[20],而氮元素作为氨基酸的重要组成部分,需要以适当的形式进行合成或外部补充[21],培养环境中氮元素降低反而影响藻细胞利用碳源进行增殖,致使微藻生长受到限制。周涛等[22]通过实验还发现,
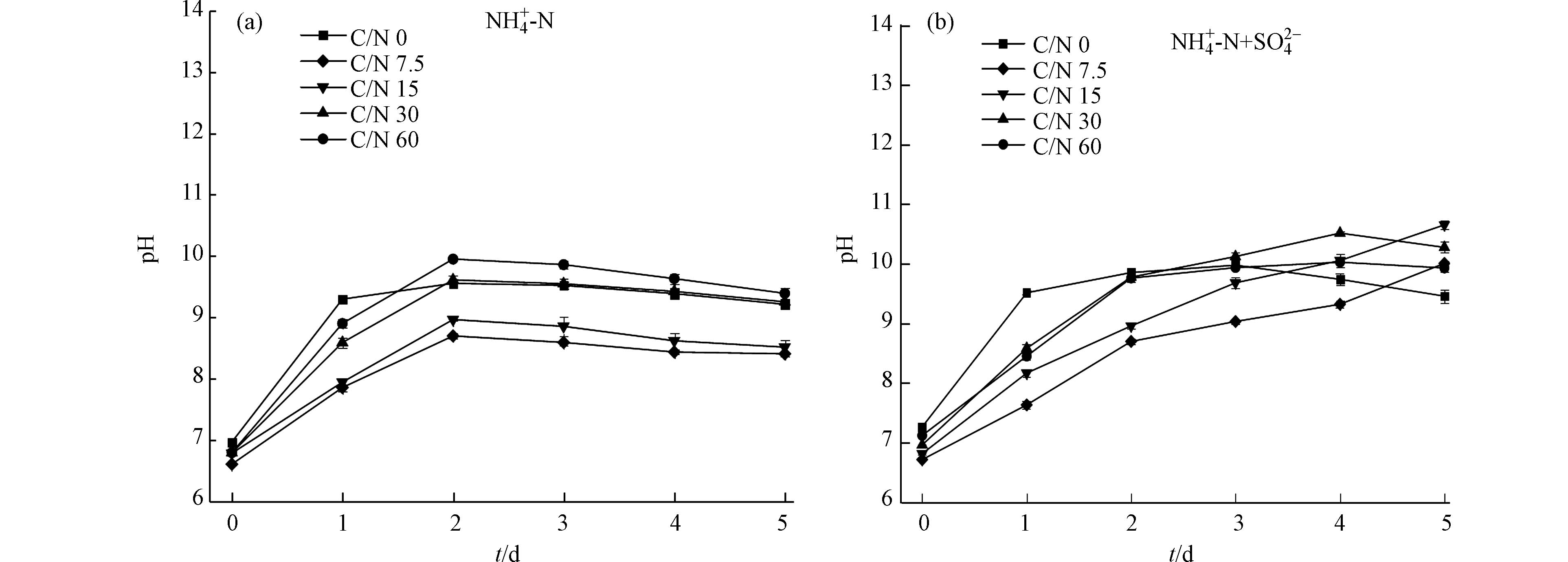
NH+4 -N不宜过高,否则会对藻细胞产生毒害作用,影响其正常生长。因此,在微藻精细化培养过程中应综合考虑碳氮硫等的影响。图2为不同C/N下无硫、含硫条件对微藻生长系统pH变化的影响情况。由图2可以看出,在无硫条件下,各组别pH均呈现先上升后下降的趋势,且均在第2天达到最大,随后趋于稳定。这主要是由于:在无硫条件下藻细胞利用营养物合成生命活动必要的蛋白质、叶绿素等过程受到抑制,生长潜力无法释放,且在低C/N条件下系统中的NH4+-N表现出毒害性,进一步抑制细胞生长,进而导致系统pH下降[3];在含硫条件下,各组别pH变化存在较大差异,C/N为30和60的实验组呈先升后降的趋势,C/N为7.5和15的实验组在培养周期内pH逐渐升高,表明这2组有较大的生长潜力。硫元素加入后,有效驱动藻细胞大量合成叶绿素等光合作用必要前体物,光合作用增强,光合作用产物增多,使得系统pH有一定提高。
-
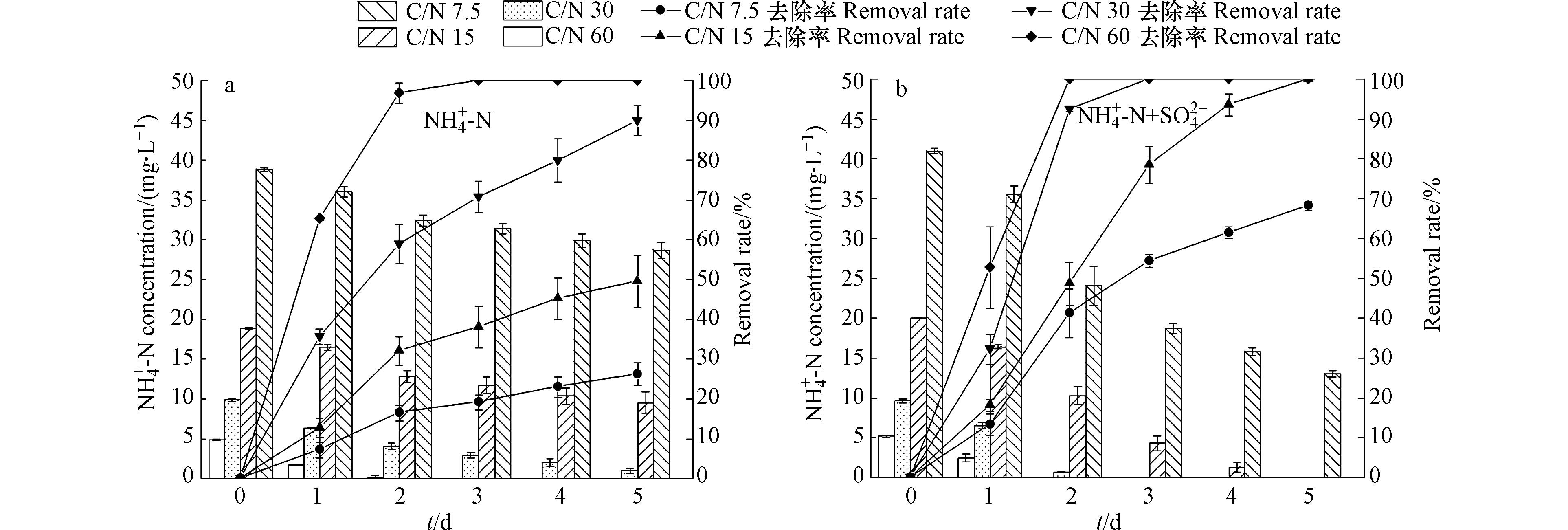
图3为不同C/N下无硫、含硫条件对微藻去除
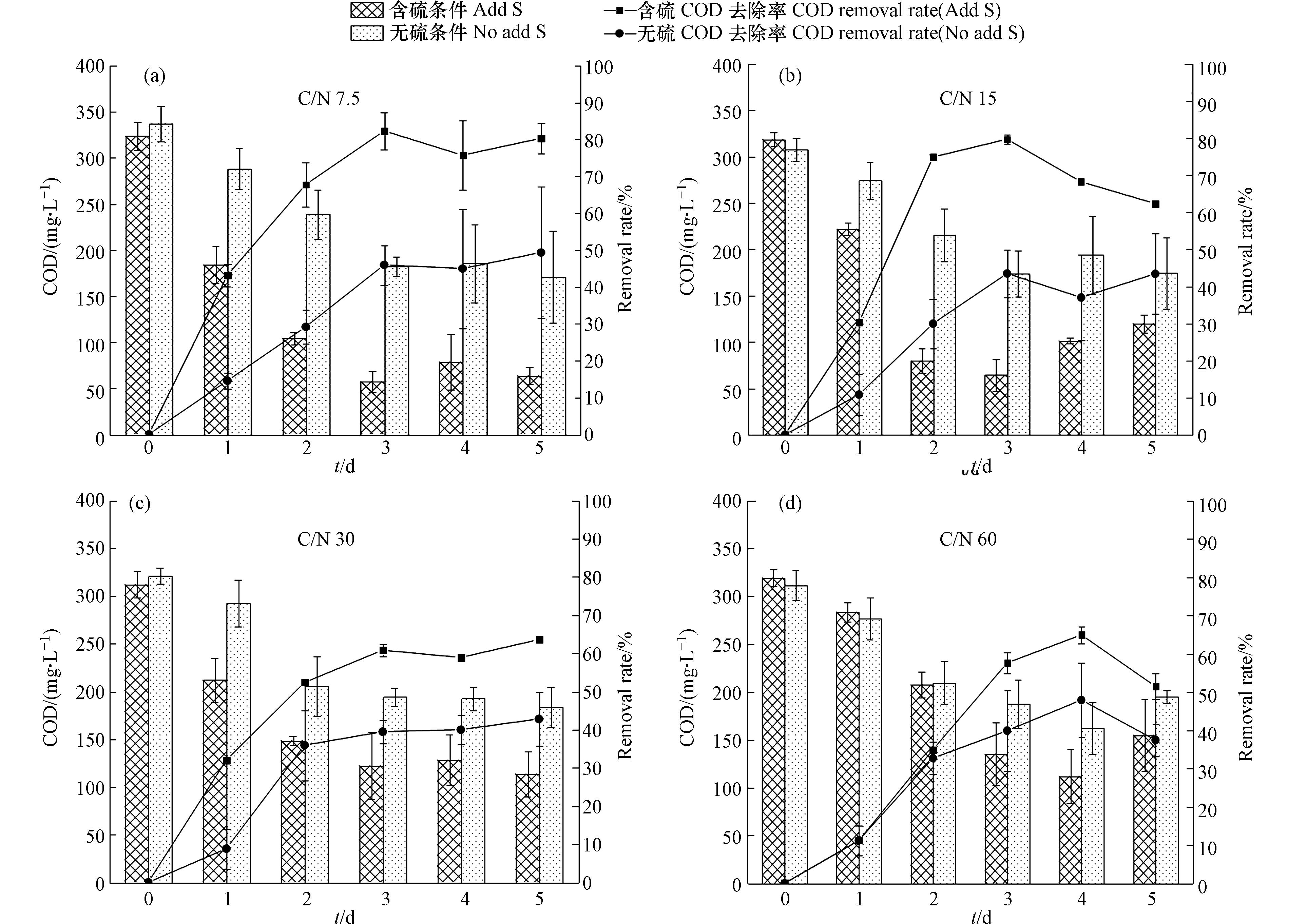
NH+4 -N能力的影响情况。由图3(a)可知,在无硫条件下,微藻对NH+4 -N的去除率随着C/N增大而升高;培养到第3天,C/N为60的实验组中微藻对NH+4 -N的去除率高达100%,高于低C/N组别。而由图3(b)可知,在含硫条件下,当C/N为15、30、60时,微藻对NH+4 -N的去除率均能达到100%,C/N为7.5的实验组微藻对NH+4 -N的去除率为73.6%,较在无硫时提升了1.49倍。对比无硫、含硫条件下,C/N为60的实验组去除率差异不明显,含硫条件下C/N为7.5、15和30的实验组中斜生栅藻对NH+4 -N去除能力显著优于无硫条件(P<0.05)。其原因是,硫元素加入后藻细胞生长加快,吸收利用NH+4 -N的能力增强,相较于无硫条件,能更多的利用NH+4 -N合成有机物质,从而提高NH+4 -N去除效率。图4为不同C/N下无硫、含硫条件对系统COD值的影响。由图4可知,含硫条件下微藻对有机物的去除效率优于无硫条件,且在培养前期微藻对营养物的利用效率更高。整体看来,COD去除率随着C/N降低而升高。培养到第5天,含硫条件下各实验组中微藻对营养物的去除率均高于50%,在C/N为7.5时COD值较初始下降了82.29%,去除效率达到80.33%,较无硫条件提升了63%;而在C/N为15、30、60时,微藻对营养物的利用效率分别是无硫条件的1.43、1.48、1.37倍。硫元素加入有效提升了微藻对碳源的利用效率。这主要是由于微藻从无氮培养基中转入含硫实验污水后大量合成叶了绿素、蛋白质等物质,藻细胞大量吸收营养物质以满足自身生理需求。GALINA等[23]也指出,藻细胞在合成蛋白质、油脂等过程中需要提供能量进行支撑,进一步促进藻细胞吸收有机物。此外,本研究的结果表明,当C/N在7.5—15时,微藻生长与碳氮利用的综合效益较好,但适宜不同种类微藻生长的条件存在差异,兼顾不同微藻碳氮利用与生长的C/N可能会有一定区别[24]。
-
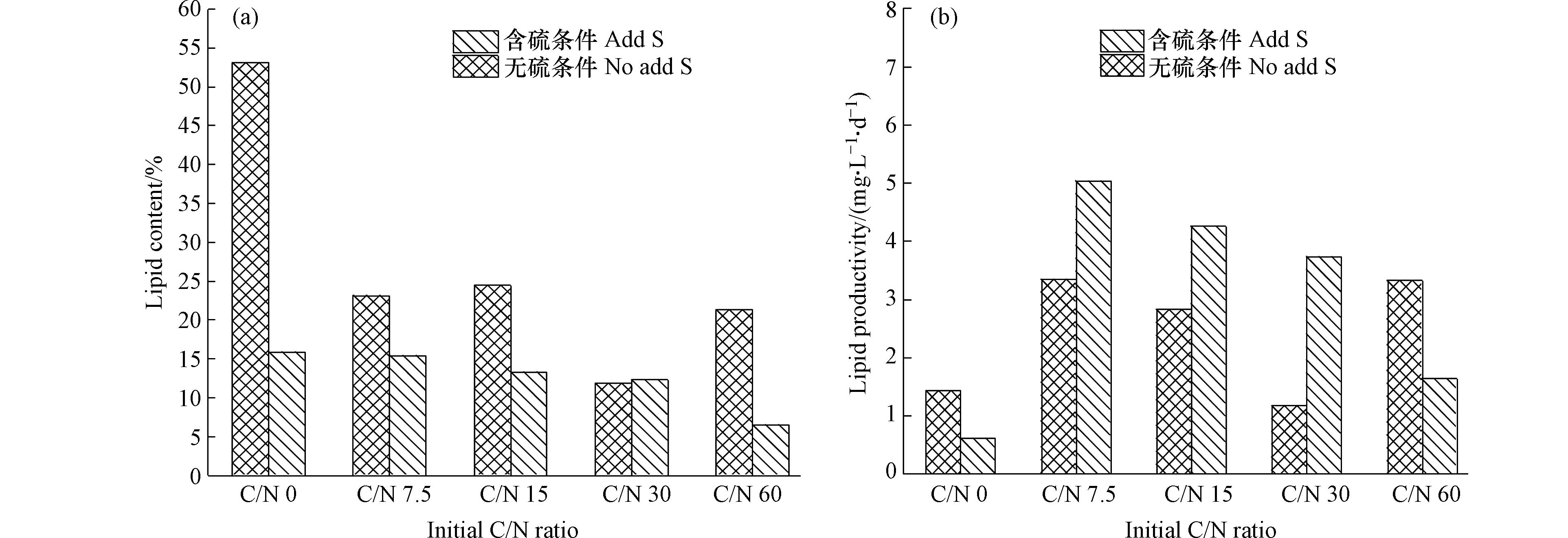
图5(a)为不同C/N下无硫、含硫条件对油脂含量的影响情况。由图5(a)可以看出,无硫条件下,实验组的油脂含量在11.8%—24.4%,且随着C/N的增大先升后降,在C/N为15时达到最大,为24.4%,低于无硫对照组的53.1%,在氮、硫双重限制下的油脂含量是单一硫限制的3.34倍。有研究表明,营养盐限制越多更有利于碳流趋向油脂积累[25]。而在含硫条件下,油脂含量在6.5%—15.4%,且随着C/N增大而减小,在C/N为7.5时最高,占细胞干质量的15.4%,但远低于无硫条件的23.1%。这说明硫元素加入反而不利于微藻积累油脂。其原因在于藻细胞受到营养盐限制等外界环境胁迫时更倾向于积累油脂[26],当硫元素限制或缺乏时影响了藻细胞正常生长,油脂作为一种持久性储能物质,对藻细胞应对营养胁迫和维持正常生命活动具有重要意义[27],因此,藻细胞在硫胁迫时油脂含量更高。此外,氮限制也有利于微藻积累油脂且较低的C/N更利于油脂合成,油脂含量最高可达15.9%。这主要是由于氮素缺乏降低微藻对氮的同化作用,引起藻细胞内部小分子前体物和还原力积累,更利于微藻细胞合成油脂。ANAND等[9]也指出,氮素限制会抑制蛋白质等物质的合成,驱使藻细胞趋向更多的油脂积累。
不同C/N水体中微藻油脂产率对比情况如图5(b)所示。在无硫条件下,油脂产率随着C/N增大先下降后上升,在C/N为60时达到最大,为3.35 mg·(L·d)−1。而在含硫条件下,C/N为7.5、15和30的实验组油脂产率均高于无硫条件,且随着C/N增大产率降低,油脂产率在C/N为7.5时达到最大值,为5.04 mg·(L·d)−1,较无硫条件提升了50.51%。其原因在于硫限制虽然有效提升了油脂含量,但同时加剧了生长和脂质合成的矛盾,外源硫加入后刺激了藻细胞生长,释放了微藻生长潜力,以此来弥补油脂含量降低带来的损失,从而提高了油脂产率;且随着C/N的降低,藻细胞利用营养物质促进生长的效率更高,增殖速率更快,从而能进一步弥补损失。黄怡等[28]通过研究发现,高硫条件更利于提升油脂产率,而本实验结果表明,高硫条件提升油脂产率不仅受硫浓度影响,还与培养体系的C/N息息相关。当C/N较高时,外源硫加入未能有效提升油脂产率,而随着C/N的降低,油脂产率才逐渐升高。因此,在进行微藻精细化培养时,既要关注硫浓度,也应综合考虑不同C/N的影响。
表1为不同C/N下无硫、含硫条件对斜生栅藻脂肪酸组成及相对含量的影响情况。由表1可知,十六烷酸(C16:0)、十八烷酸(C18:0)、十八碳烯酸(C18:1)、十八碳二烯酸(C18:2)、十八碳三烯酸(C18:3)占据脂肪酸的绝大多数。在无硫条件下,各实验组中C18:1相对含量较高,但均小于对照组,且随C/N增大先下降后上升,在C/N为60时最大,为47.11%。对含硫条件而言,C/N为7.5、15、30、60的组别培养5 d后C16—C18的脂肪酸对总脂肪酸的占比分别为97.11%、97.67%、97.63%和97.23%。单不饱和脂肪酸含量随C/N增大先升高后降低,在C/N为15时达到最大,为48.45%。有研究表明,生物柴油的理化性质与脂肪酸组分密切相关[29],C16—C18的脂肪酸更适宜生产生物柴油[30],并且高品位的生物柴油应尽量多地含有单不饱和脂肪酸且尽量减少饱和脂肪酸和多不饱和脂肪酸含量[31],而单不饱和脂肪酸更有利于提升生物柴油的低温流动性、氧化安定性等性能[32]。因此,C/N为15时得到的油脂产物更利于生产高品质柴油。
-
(1)外源硫加入有利于释放微藻生长潜力,且C/N较低时硫促进生长的效果更好。培养到第5天,C/N为15的达到最大,藻密度为1.23×107 cells·mL−1,较无硫条件提升了90%。
(2)外源硫加入可有效提升微藻对碳、氮源的利用效率。C/N为7.5时微藻对有机物的利用效率最高,为80.33%,较无硫条件提升了63%;C/N为7.5时,水体
NH+4 -N的去除率为73.6%,较无硫条件提高了149%,其余各组NH+4 -N均能完全去除。(3)外源硫加入有利于提高油脂产率但不利于油脂积累。油脂产率随着C/N升高而降低且在C/N为7.5时达到最大,为5.04 mg·(L·d)−1,较无硫条件提升了50.51%;低C/N条件下油脂含量更高,C/N为7.5时油脂含量为15.4%,较无硫条件下降了33.3%;C/N为15时单不饱和脂肪酸含量最高,更适宜生产高品质生物柴油。
不同C/N下硫对斜生栅藻生长与油脂积累的调控
Regulation of sulfur on growth and lipid accumulation of Scenedesmus obliquus under different C/N ratio
-
摘要: 为探究不同C/N污水下下硫对微藻生长、水体净化与油脂积累的调控作用,以斜生栅藻为研究对象,通过改变
NH+4 -N浓度配制了4种不同C/N的实验用水,对比研究了斜生栅藻在无硫和含硫条件下经5 d培养后的生长、碳氮利用与油脂合成情况。结果表明,外源硫添加可有效促进微藻的生长,当C/N为15时,藻细胞密度达到最大,为1.23×107 cells·mL−1,较无硫条件提高了90%;同时,外源硫也有助于提升藻细胞对碳氮的利用效率,微藻对有机物的利用效率随着C/N的降低而升高,并在C/N为7.5时最大,为80.33%,较无硫条件提升了63%;当C/N为7.5时NH+4 -N去除率为73.6%,较无硫条件提升了149%,其余实验组别NH+4 -N去除率均达100%;此外,在含硫条件下,油脂产率和油脂含量均随着C/N升高而降低,均在C/N为7.5时达到最大,油脂产率为5.04 mg·(L·d)−1,相较于无硫条件提升了50.51%,油脂含量为15.4%,较无硫条件下降了33.3%,表明硫加入可有效提升油脂产率但不利于油脂积累,在低C/N条件下促进作用更强。综合来看,当C/N在7.5—15时,外源硫加入取得的综合效益最佳。通过探究微藻生长、碳氮利用、油脂积累的适宜条件,可为微藻的精细化培养提供参考。Abstract: To explore the regulating effect of sulfur on the growth and lipid accumulation of Scenedesmus obliquus under different C/N ratio conditions, taked Scenedesmus obliquus as the research object, set 4 kinds of experimental water with different C/N ratios by changing the concentration of ammonia nitrogen, and comparatively studied the growth and lipid synthesis of microalgae after 5 days of culture under both sulfur-free and sulfur-containing conditions. The results showed that the addition of exogenous sulfur can effectively promote the growth of microalgae. When C/N ratio was 15, the density of microalgae reached the maximum, which was 1.23×107 cells·mL−1, it was 90% higher than the sulfur-free condition. Additional sulfur also helped to improve the carbon and nitrogen utilization efficiency of microalgae. The utilization efficiency of organic matter by microalgae increased with the decrease of carbon to nitrogen ratio, when C/N was 7.5, it reached 80.33%, which was 63% higher than that of sulfur-free conditions, while the ammonia nitrogen removal efficiency was 73.6%, which was 149% higher than the sulfur-free condition, and the removal efficiency of the remaining experimental groups reached 100%. In addition, under the sulfur-containing condition, the lipid yield and lipid content both decreased with the increase of carbon to nitrogen ratio. When C/N ratio was 7.5, the lipid yield was highest, which was 5.04 mg·(L·d)−1, it was 50.51% higher than that of sulfur-free conditions. When the C/N ratio was 7.5, the lipid content was 15.4%, which was 33.3% lower than the sulfur-free condition, indicating that sulfur addition can effectively increase the lipid yield but was not conducive to the accumulation of lipid, and exogenous sulfur had a stronger promoting effect under low carbon to nitrogen ratio conditions. In summary, when the C/N ratio was between 7.5 and 15, the overall benefits were relatively best. By exploring the appropriate conditions for microalgae growth, carbon and nitrogen utilization, and lipid accumulation,This research can provide references for the refined cultivation of microalgae.-
Key words:
- Scenedesmus obliquus /
- ammonia nitrogen /
- sulfur /
- growth and metabolism /
- lipid accumulation
-
镉是联合国环境规划署提出的12种全球性的危险化学物质中位于首位的有毒重金属,控制环境中尤其是水体中的镉含量十分重要[1]。当前,去除水体中Cd2+的常用方法包括化学沉淀法、离子交换法、膜处理等,但这些方法受到操作要求高、效率低、成本高等因素的制约,难以大面积推广[2]。吸附法因其具有绿色可行、便捷有效[3]的特点已成为当前研究的一个热点,但选取廉价、高效的吸附材料仍是目前面临的难题。
生物炭是指由富炭生物质经热处理,在限氧条件下不完全燃烧生成的产物[4]。有研究[5]表明,生物炭具有比表面积巨大,表面能高等特性,这些特性决定了生物炭在吸附水体重金属方面具有巨大的潜力。当前,为了强化生物炭的吸附性能,增加其吸附容量,许多研究者通过改性的方法来增加生物炭对重金属的吸附效果。WU等[6]使用化学改性方法对椰子纤维炭进行修饰,增加其表面游离的羧基和羟基,研究结果表明,改性后生物炭的吸附容量较改性前可显著提高。马天行等[7]通过亲电芳香取代和还原反应在生物炭表面实现表面氨基化,再使用液相还原法在制备成功的氨基生物炭表面负载纳米零价铁,研究表明,制得的材料具有优良的吸附性能。王静等[8]利用活性炭与巯基乙酸的酯化反应,将巯基嫁接到活性炭上,改性后活性炭对汞的最大吸附容量为556 mg·L−1,远远优于原材料。陈维芳等[9]使用十六烷基三甲基氯化铵(CTAC)改性活性炭,结果表明,改性后活性炭对As5+的吸附能力显著提高,且在中性pH范围内,吸附效果最佳。在改性材料中,CTAB是一种价格低廉且应用范围较广的阳离子表面活性剂,由于生物炭表面多带负电荷,故CTAB通过静电吸附的作用很容易吸附于生物炭表面,同时插入材料表面的烷基基团在材料表面形成混合胶束,加大了与Cd2+的静电吸引力,从而提升了材料的吸附容量。
本研究采用十六烷基三甲基溴化铵(CTAB)作为改性剂,椰壳炭(CSC)和竹炭(BC)作为改性材料,制备改性椰壳炭(CTAB-CSC)和竹炭(CTAB-BC),运用傅里叶红外变换光谱(FT-IR)、扫描电镜(SEM)、X射线光电子能谱分析(XPS)和热稳定性分析(TGA)对材料进行了表征,研究了其吸附机理,并对其进行了动力学拟合和等温吸附曲线拟合,探究了2种改性材料对溶液中Cd2+的吸附机制。
1. 材料与方法
1.1 试剂与仪器
仪器:磁力搅拌器(MS200型,上海般特仪器制造有限公司)、电子天平(FA1004型,上海舜禹恒平科学仪器有限公司)、超声波清洗机(DTD-6R型,长沙皓嵘仪器设备有限公司)、高速冷冻离心机(ST-16R型,赛默飞世尔科技有限公司)、便携式pH计(PHBJ-260,仪电科学仪器股份有限公司)、恒温培养振荡器(NNY-21113,天津欧诺仪器仪表有限公司)、电感耦合等离子体发射光谱仪(ICP-OES美国PEB00)。
试剂:六偏磷酸钠(Na6O18P6)、氯化镉(CdCl2·2.5H2O)、十六烷基三甲基溴化铵(C19H42BrN)、盐酸(HCl)、氢氧化钠(NaOH)。这些试剂均为分析纯,去离子水为实验室自制。
1.2 材料的制备
材料预处理:椰壳炭购自江苏艾格尼丝环境科技有限公司;竹炭购自浙江省农业科学院。将购买的椰壳炭和竹炭使用研磨机研磨,过0.180 0 mm筛;将过筛后的生物炭使用去离子水清洗3次,于80 ℃条件下,在烘箱中烘干备用,记做CSC(椰壳炭)和BC(竹炭)。
改性材料的制备:称取20.00 g的材料(CSC和BC),置于100 mL烧杯中,在烧杯中按照固液比1∶2.5的比例加入质量分数为6%的六偏磷酸钠溶液50 mL,磁力搅拌30 min,然后超声分散30 min,按照1∶10的质量比(MCTAB∶M材料)在烧杯中加入CTAB(质量为2.000 0 g),于常温下搅拌10 h,静置沉淀,抽滤洗涤至没有泡沫产生,冷冻干燥得改性材料,记作CTAB-CSC和CTAB-BC,密封保存待用。
Cd2+模拟废水配置:准确称取2.032 0 g CdCl2·2.5H2O,置于烧杯中,加500 mL的去离子水溶解,再将其转移至1 000 mL容量瓶中,定容摇匀后,配置Cd2+浓度为1 000 mg·L−1的母液。在后期使用中,所需不同浓度的废水均由母液按照浓度梯度稀释。
1.3 材料的表征
2种材料的形态和外貌采用热场发射扫描电镜显微镜(QUANTA430,美国FEI公司)观测;CTAB-CSC和CTAB-BC吸附前后的能谱图及元素含量由X射线显微分析系统(美国FEI公司)获得;CTAB-CSC和CTAB-BC改性前后的傅里叶红外光谱由NICOLET 570 FTIR Spectrometer(美国热电尼高力仪器公司)获得;材料的热稳定性由热重分析仪(Q500,美国TA公司)测定。
1.4 材料吸附实验
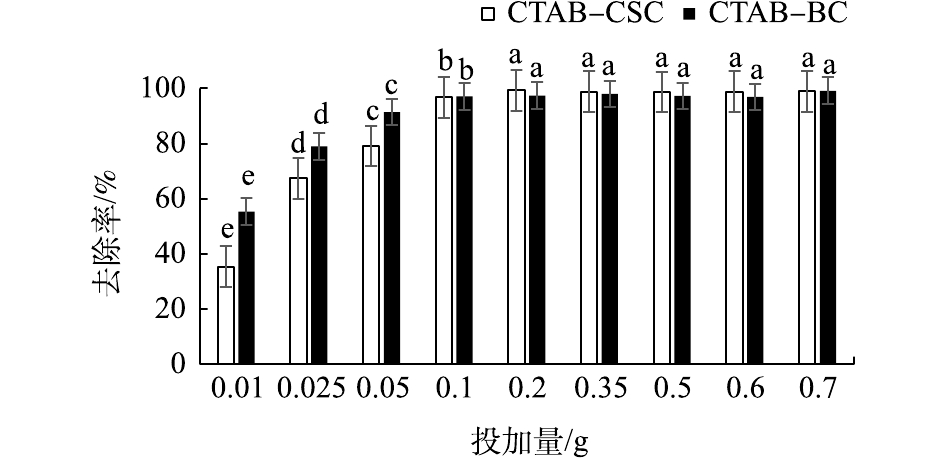
1)吸附剂投加量对吸附效率的影响分析。称量0.050 0、0.100 0、0.200 0、0.350 0、0.500 0、0.600 0、0.700 0 g等7个不同质量梯度(每个梯度设置3个平行样)的CTAB-CSC和CTAB-BC,置于50 mL的离心管中,在离心管中加入25 mL浓度为10 mg·L−1的Cd2+溶液,摇匀放置于气浴恒温振荡箱中振荡,直至吸附平衡,后于3 000 r·min−1离心10 min后取出再过滤,测定滤液中Cd2+浓度。
2)pH对吸附效率的影响分析。准确称量18个0.200 0 g CTAB-CSC和CTAB-BC样品,置于50 mL离心管中,在离心管中加入25 mL浓度为10 mg·L−1的Cd2+溶液,使用0.1 mol·L−1的NaOH和HCl调节溶液的pH,调节pH的梯度至2、3、4、5、6、7(每个梯度设置3个平行样),摇匀后,置于气浴恒温振荡箱振荡至吸附平衡,后于3 000 r·min−1离心10 min后,再取出过滤,测定滤液中Cd2+浓度。
3)吸附动力学实验。准确称量27个0.200 0 g CTAB-CSC和CTAB-BC样品,置于50 mL离心管中,在离心管中加入30 mL浓度为100 mg·L−1的Cd2+溶液,调节溶液pH为7,根据时间梯度5、15、30、60、120、240、320、720、1 440 min(每个梯度设置3个平行样),分批次置于气浴恒温振荡箱中,振荡时间停止后,取出过滤,测定滤液中Cd2+浓度。
4)等温吸附模型实验。准确称量15个0.500 0 g CTAB-CSC和CTAB-BC样品,置于50 mL离心管中,准确设置浓度梯度为30、60、120、250、500 mg·L−1的Cd2+溶液(每个梯度设置3个平行),在离心管中分别加入25 mL不同浓度的溶液,摇匀后,置于气浴恒温振荡箱中振荡至吸附饱和,振荡结束后,在3 000 r·min−1的条件下,离心10 min,离心结束后过滤,滤液稀释待测。
5)材料再生实验。将吸附饱和的材料通过抽滤进行固液分离,将分离出的材料用去离子水充分洗涤3~5次,烘干,分别放入0.01 mol·L−1的HCl溶液中,振荡24 h,振荡结束后,重复进行分离和干燥,将干燥的材料置于10 mol·L−1的Cd2+溶液中进行吸附,待吸附饱和后过滤,测定滤液中Cd2+浓度。重复吸附-脱附步骤3次,测定滤液中Cd2+浓度。
1.5 数据分析
吸附材料的吸附效果分别用去除率和吸附量来衡量,其计算公式分别如式(1)和式(2)所示。
δ=(C0−Ce)C0×100% (1) Qe=(C0−Ce)Vm (2) 式中:δ为去除率;C0为溶液初始浓度,mg·L−1;Ce为溶液吸附平衡时浓度,mg·L−1;V为溶液体积,mL;m为吸附剂质量,g。
动力学模型拟合。为了研究CTAB-CSC和CTAB-BC的吸附动力学,分别用一级动力学方程和二级动力学方程模型进行拟合。一级动力学方程和二级动力学方程[10]如式(3)和式(4)所示。
ln(qe−qt)=lnqe−K1t2.303 (3) tqt=1K2q2e+1qe (4) 式中:qe为吸附剂吸附平衡时吸附容量,mg·g−1;qt为t时刻吸附剂的吸附容量,mg·g−1;K1为一级动力学吸附系数;K2为二级动力学吸附系数。
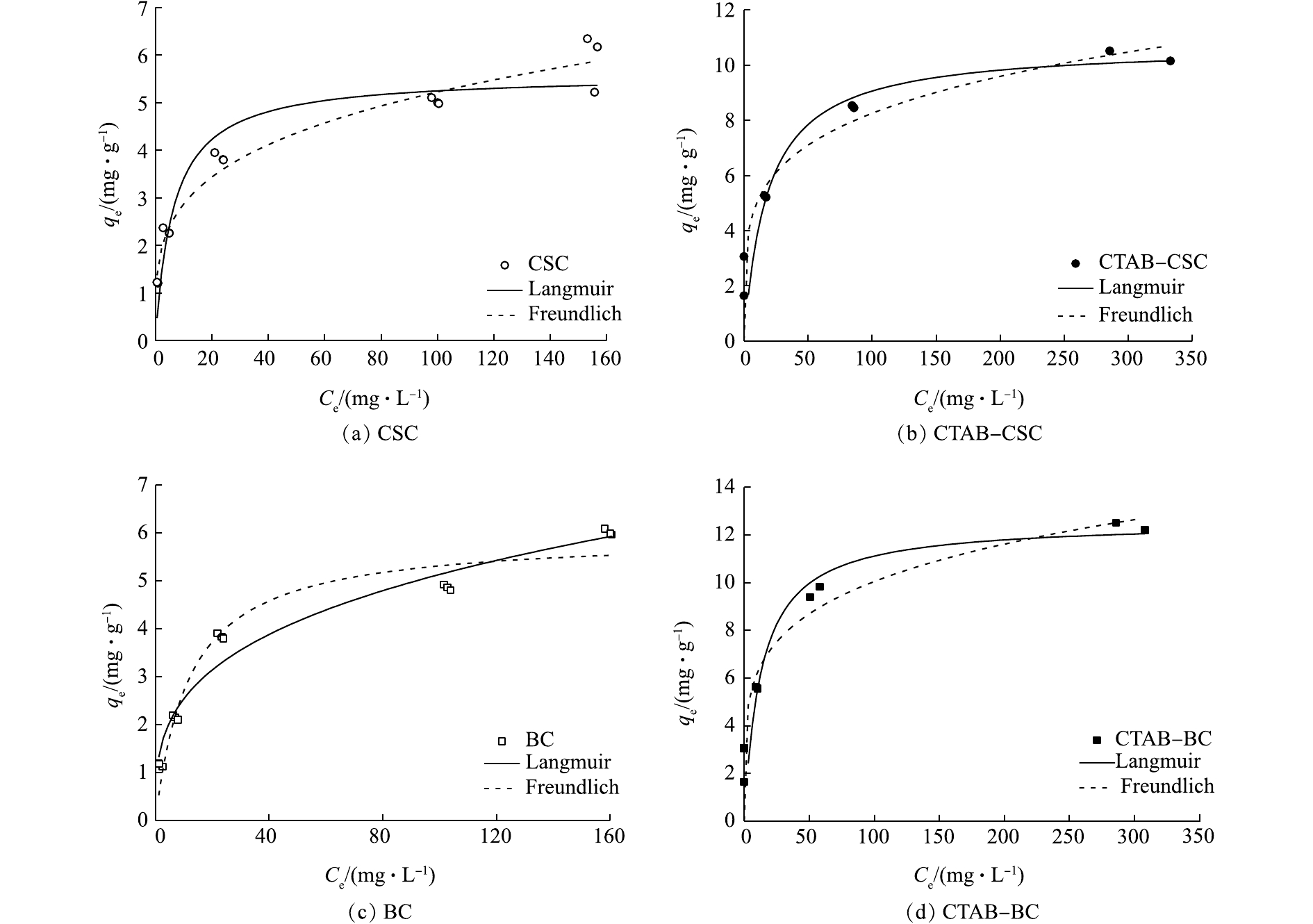
等温吸附模型拟合。本研究使用Langmuir模型和Freundlich模型对CTAB-CSC和CTAB-BC等温吸附实验数据进行分析。其中,Langmuir模型属单分子层吸附,Freundlich模型属多分子层吸附,以参数分离因子来分析CTAB-CSC和CTAB-BC 2种材料的吸附性能,其中Langmuir和Freundlich模型[10]如式(5)和式(6)所示。
qe=qmaxKLCe1+KLCe (5) qe=KFC1ne (6) 式中:qmax为吸附剂的单层饱和最大吸附,mg·g−1;Ce为吸附平衡时溶液浓度,mg·L−1;KL为Langmuir吸附常数,L·mg−1,当0<KL<1,表示有利于吸附;KL>1,表示不利于吸附;KL =1,属于线性分配;KL趋于0,表示不可逆吸附。KF是Freundlich吸附常数;1/n是Freundlich模型中表示吸附强度的参数。
2. 结果与讨论
2.1 材料的表征
2.1.1 傅里叶红外光谱
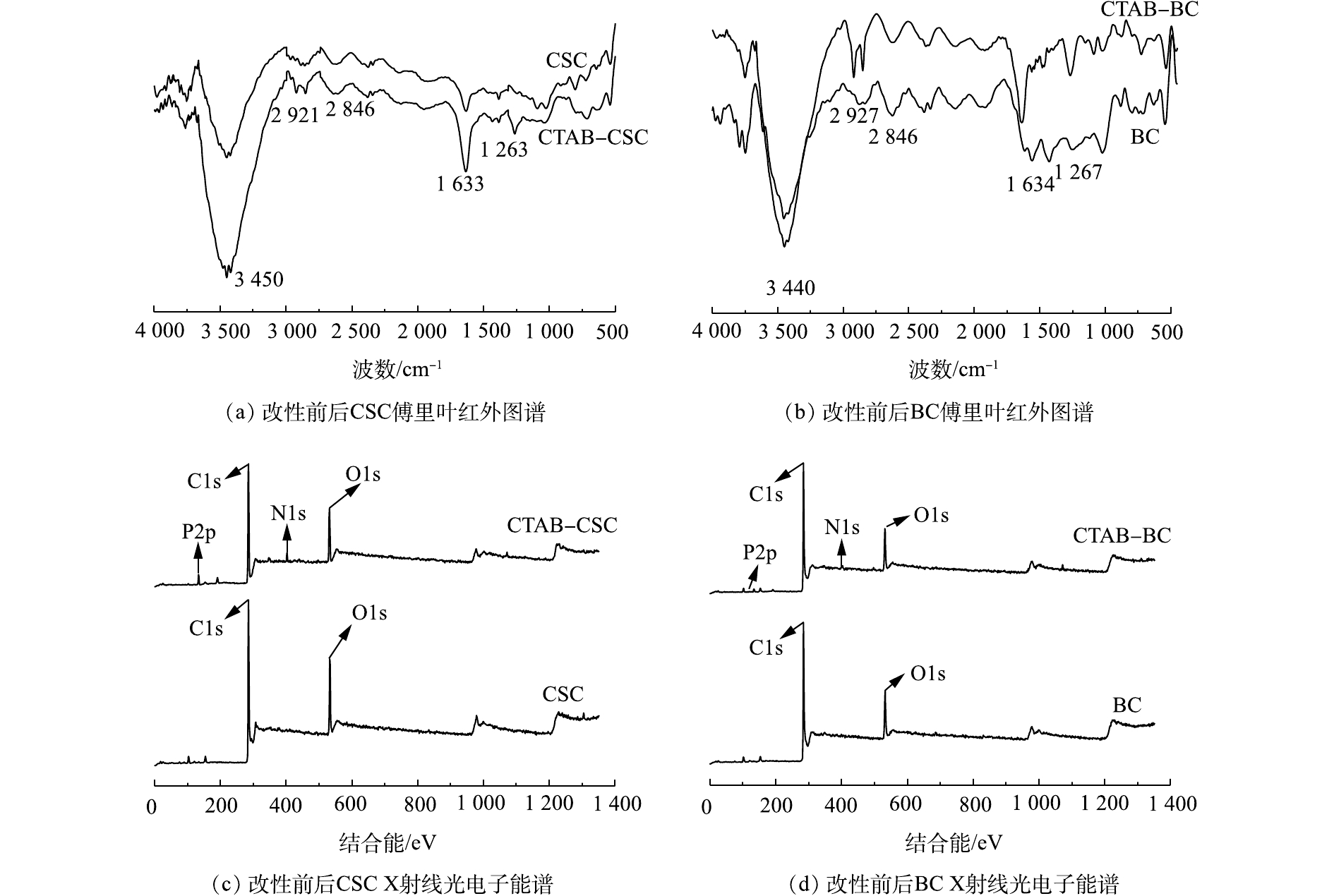
傅里叶红外图谱通过检测材料内部分子的振动和转动,从而可知材料中所含化合物的化学结构,包括各种官能团,如氨基、羧基和羰基等。生物炭改性前后的傅里叶红外图谱如图1(a)和图1(b)所示,从图1中可知,2种改性后的生物炭表面均含有更为丰富的官能团。
由图1(a)可知,CTAB-CSC在3 440 cm−1处对应的是—NH伸缩振动引起的吸收峰[11];在1 634 cm−1处对应的是—NH弯曲振动引起的的吸收峰[12],这充分证明有氨基集团成功嫁接到生物炭表面[13]。氨基基团可以和Cd2+发生配合反应[14]。同时,在2 927 cm−1和2 846 cm−1处的2个峰可以归因于甲基和亚甲基中C—H的伸缩振动,在图1(b)中,也观察到类似的现象,这充分说明CTAB分子已成功嫁接在生物炭表面[15]。图1(c)和图1(d)是改性材料改性前后的XPS总谱,改性后,在400 eV左右出现了N1s的峰,亦可以证明材料改性后,其表面有氨基基团的存在。
2.1.2 扫描电镜
改性前后的2种材料的冷场发射扫描电子显微镜观察结果如图2所示。由图2(a)可知,改性前,CSC表面棱角分明,表面较为平整;而经CTAB改性后,CSC(图2(b))表面有一定凸起,棱角较改性前更加圆滑。由图2(c)和图2(d)可知,改性后的CTAB-BC表面更加平滑,且材料表面还存在一些堆积状的颗粒,且在改性后表面颜色变浅,说明CTAB已经负载在材料的表面。
2.1.3 X射线光电子能谱分析
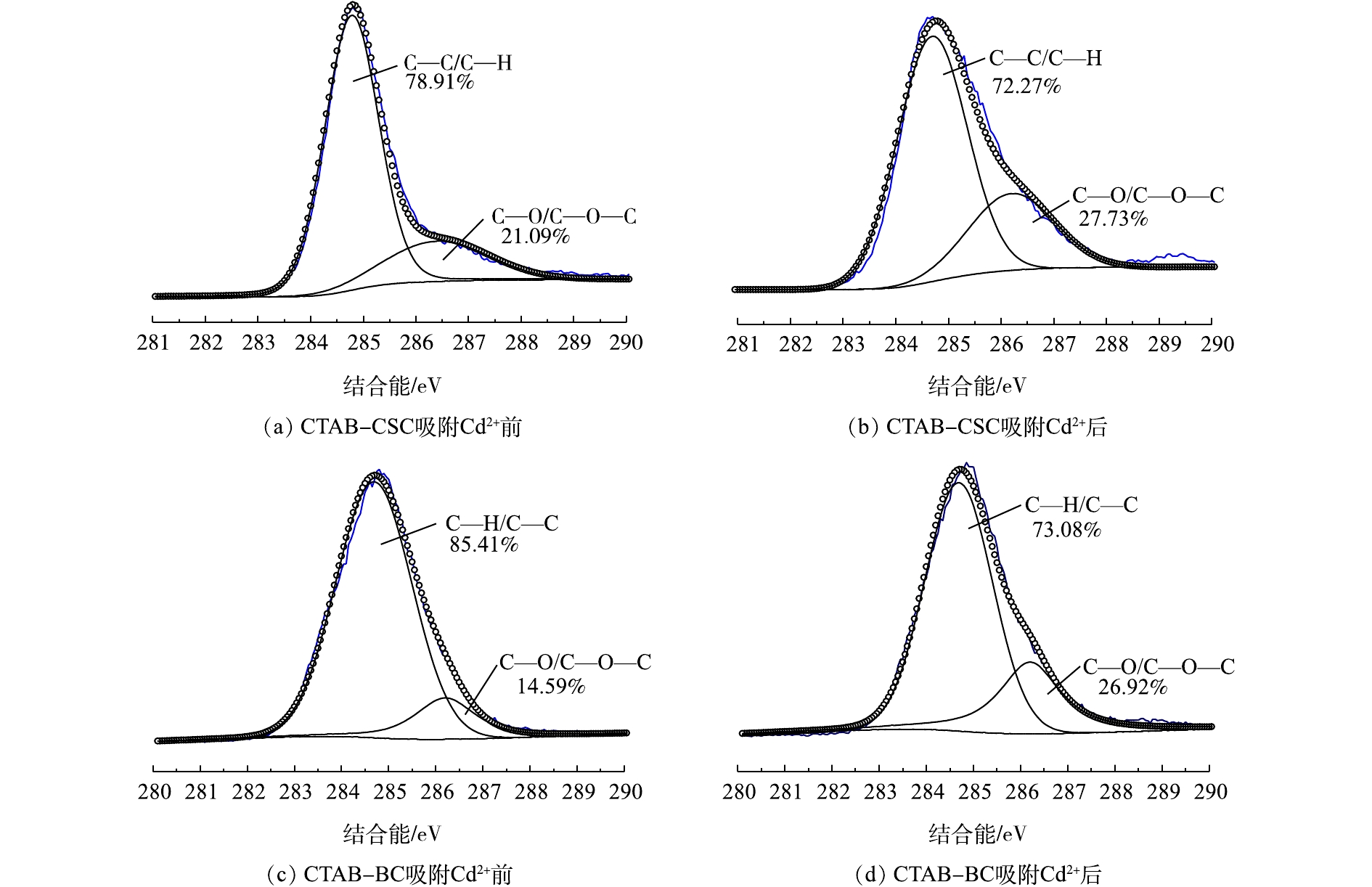
X-射线光电子能谱(XPS)具有比较高的表面灵敏度,通过比较吸附Cd2+前后的生物炭表面元素结合能的变化来进一步研究生物炭对Cd2+的吸附机理。图3(a)和图3(b)分别是CTAB-CSC的吸附Cd2+前后的C1s谱图。通过分峰处理,在284.7 eV和286.4 eV处捕捉到2个可见峰,可以将其归为C—C/C—H(芳香族)和C—O/C—O—C(醇式羟基和醚)[16-18]。利用XPS peak软件对RWA值及峰面积进行分析,发现C—C/C—H的峰未发生显著变化,这说明C—C/C—H形式的碳原子没有直接参与Cd2+的吸附;而C—O/C—O—C的峰面积发生了明显变化,这说明C—O/C—O—C形式的碳原子在一定程度上参与了生物炭对Cd2+的吸附。图3(c)和图3(d)分别是CTAB-BC吸附Cd2+前后的C1s谱图,通过分峰处理,得到了与CTAB-CSC同样的结论。
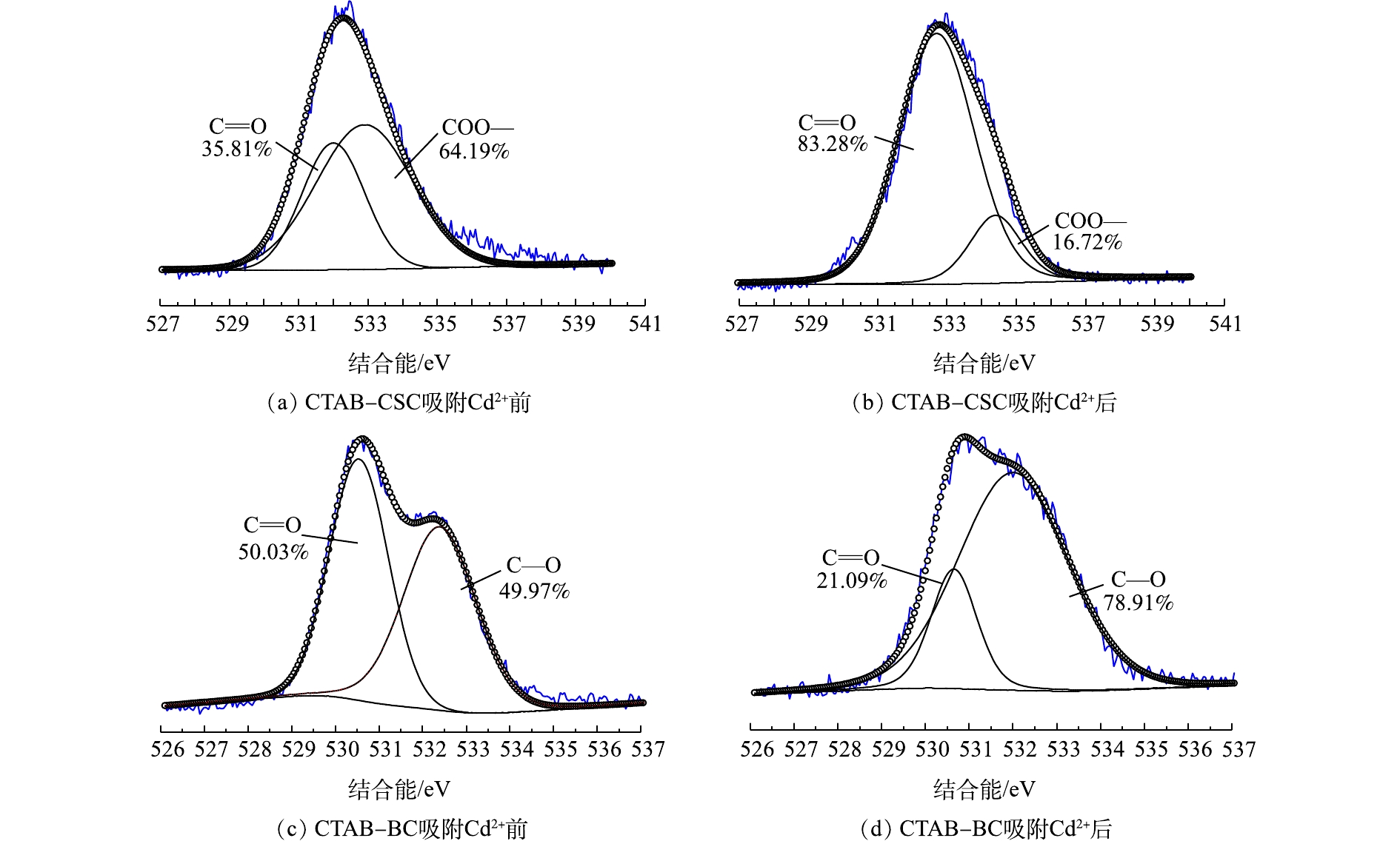
图4(a)和图4(b)是分别是CTAB-CSC吸附Cd2+前后O1s谱图,峰值在532.0 eV和532.7 eV(Cd2+吸附前后)可归类为C=O,峰值在532.9 eV和534.4 eV(Cd2+吸附前后)可归类为COO—[19]。从图4(a)中可以观察到,吸附Cd2+后,C=O的峰面积从35.81%增加到83.28%;COO—的峰面积从64.19%降低到16.72%。图4(c)和图4(d)分别是CTAB-BC吸附Cd2+前后O1s谱图,峰值在530.5 eV和530.7 eV(Cd2+吸附前后)可归类为C=O,峰值在532.4 eV和532.0 eV(Cd2+吸附前后)可归类为C—O/C—O—C(醇羟基和醚)[20]。从图4(b)中可以观察到,吸附后,C=O的峰面积从50.03%减少到21.09%;C—O/C—O—C的峰面积从49.97%增加到78.91%。
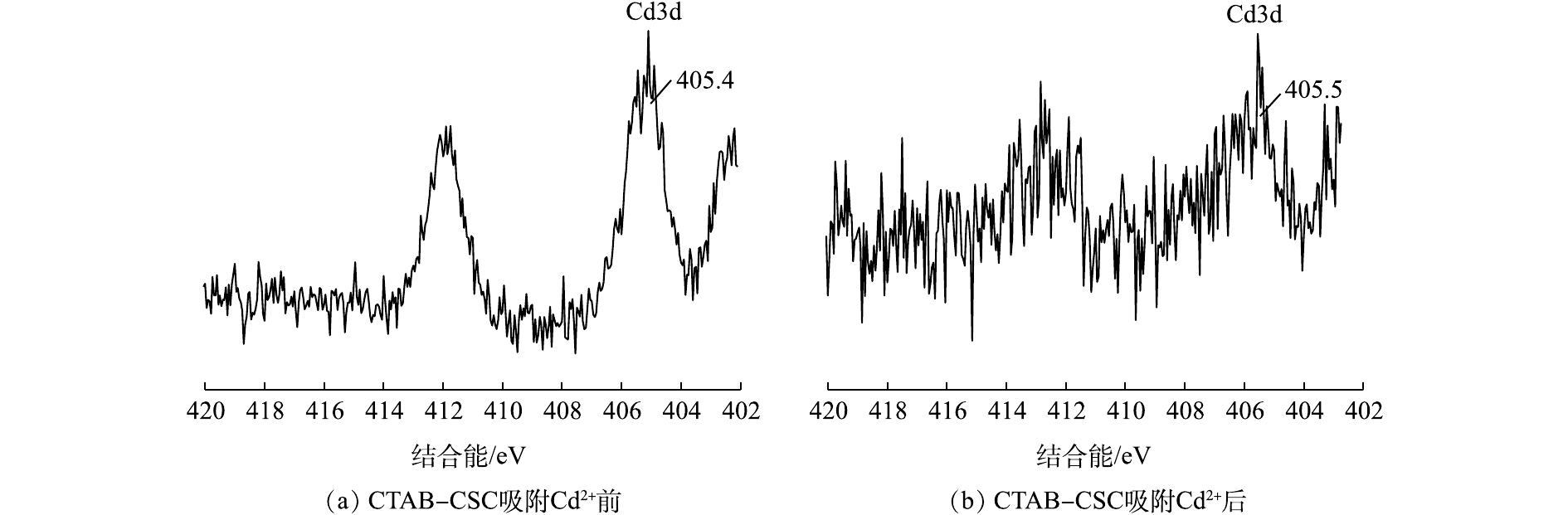
结合能的变化可能是因为Cd2+在吸附过程中与氧元素结合,导致氧元素的电子密度降低[21]。结合峰面积的变化,我们可以推断,氧原子是Cd2+的1个主要吸附点位,氧原子可以和Cd2+形成配位键。图5(a)和图5(b)分别为CTAB-CSC和CTAB-BC吸附Cd2+后Cd3d谱图,经过XPS分析,发现Cd3d的峰出现在405.5 eV的位置,为CdCO3、Cd的氢氧化物以及—OCdOH。这表明生物炭对Cd的吸附机理主要为Cd与生物炭表面的羟基化表面(—OH)或其去质子化(—O—)络合[22],这与O1s谱图的结果一致。
2.1.4 热稳定性分析
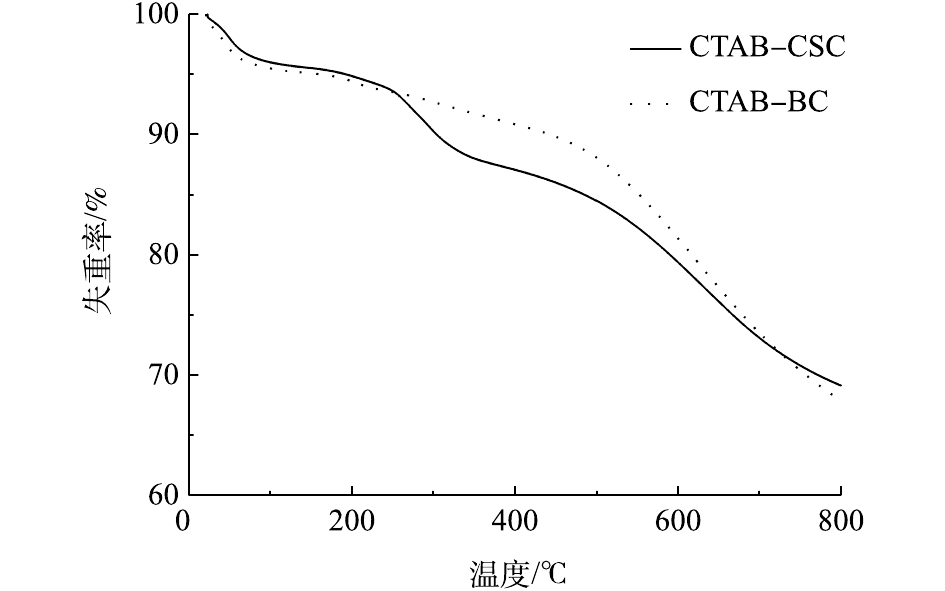
TGA即热重分析,是指在程序控制温度下测量待测样品的质量与温度变化关系的一种热分析技术,用来研究材料的热稳定性和组分。图6是CTAB-CSC和CTAB-BC的热重曲线。由图6可知,CTAB-CSC的热解过程主要分为4个阶段。室温到80 ℃为第1个阶段。此阶段为失水阶段,在此阶段中主要产生水分蒸发以及少量挥发性气体析出现象。80~250 ℃为第2个阶段。本阶段中样品质量变化很小,在此过程中主要产生秸秆的解聚和“玻璃化转变”现象[23],释放出H2O、CO、及CO2等小分子化合物。250~500 ℃为第3个阶段。秸秆类生物炭的3种主要成分为半纤维素、纤维素以及木质素,其热解难易程度为木质素>纤维素>半纤维素[24]。在此阶段中,较易热解的半纤维素和纤维素开始热解;同时,伴随着极少一部分的木质素的分解,主要生成挥发性物质和碳。500 ℃以后为炭化阶段。在本阶段中主要产生木质素缓慢分解现象。图6中CTAB-BC和CTAB-CSC相比,主要差异产生在第3个阶段。这可能是因为CTAB-BC的半纤维素的质量分数低于CTAB-CSC中的半纤维素质量分数,由于半纤维素的质量分数越高的生物质,越容易在该温度范围内出现转折现象[25]。
由图6可知,当温度达到800 ℃时,CTAB-CSC和CTAB-BC的质量损失率分别为30.96%和32.24%。2种材料的热稳定性能均较好,但CTAB-CSC的热稳定性优于CTAB-BC。
2.2 吸附实验分析
2.2.1 吸附剂投加量对吸附效果的影响
由图7可知,设置Cd2+废液初始浓度为10 mg·L−1时,溶液中的Cd2+的去除率随着材料的投加量的增加而升高。当投加量为0.200 0 g时,CTAB-CSC去除率达到98%以上,达到吸附饱和;当投加量为0.100 0 g时,CTAB-BC去除率达到98%以上,同时,由图7可知,CTAB-BC所有投加量的去除率均在90%以上,这可能是由于初始溶液中Cd2+浓度较低所致。综合考虑材料的制备以及原材料的利用率等因素,pH控制及吸附动力学实验的投加量均选为0.200 0 g。
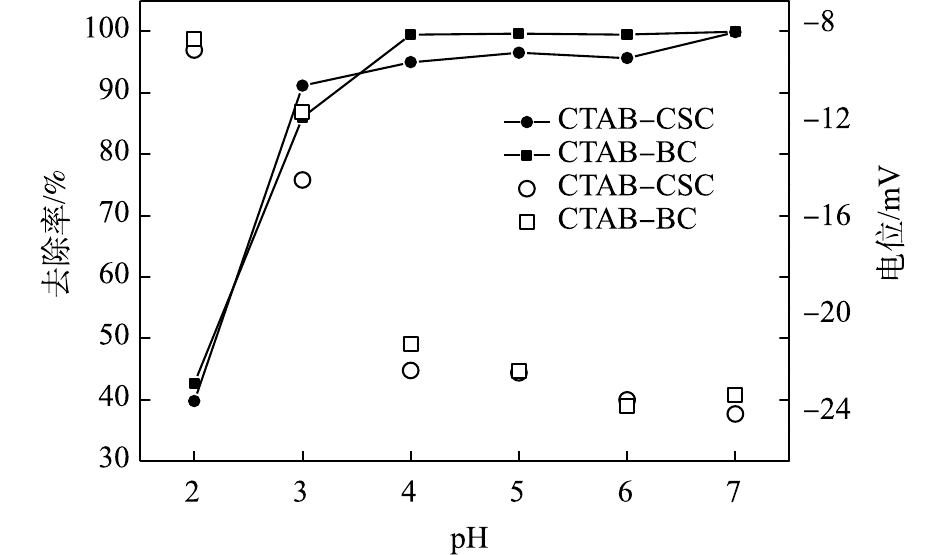
2.2.2 溶液pH对吸附效果的影响
由图8可以看出,当Cd2+废液初始浓度为10 mg·L−1时,溶液中Cd2+的去除率随着溶液pH的增加而升高;在极端的酸环境下,2种材料对溶液中Cd2+的去除率均较低。当pH=2~3时,在CTAB-CSC处理过的溶液中,Cd2+去除率显著上升;当pH=3~7时,去除率缓慢上升;当pH=7时,去除率可达到最高。而CTAB-BC在pH=2~3时,对Cd2+的去除率显著升高;当pH=3~4时,缓慢上升;当pH=4~7时,溶液中Cd2+的去除率均达到98%以上。分析产生上述现象的原因,可能是在pH较低的情况下,溶液中存在大量与Cd2+形成竞争吸附的H+,其会占据有限的结合位点,降低Cd2+去除率[26];同时,这些H+会使材料表面的电荷分布改变,导致一部分有利于重金属吸附的有机官能团发生解离,从而抑制材料对Cd2+的吸附性能[27]。随着pH的升高,H+量减少,会暴露大量吸附剂表面结合位点,负电密度增大,则吸附容量也随之增加[28]。从图8中可以看出,随着pH的升高,体系中Zeta电位在逐渐下降,Zeta电位均处于负电势。这说明材料表面带负电荷,由此推测静电作用是吸附水中Cd2+的原因之一[29]。考虑到2种材料的吸附性能的影响,在后续实验中,设置溶液初始pH为7。
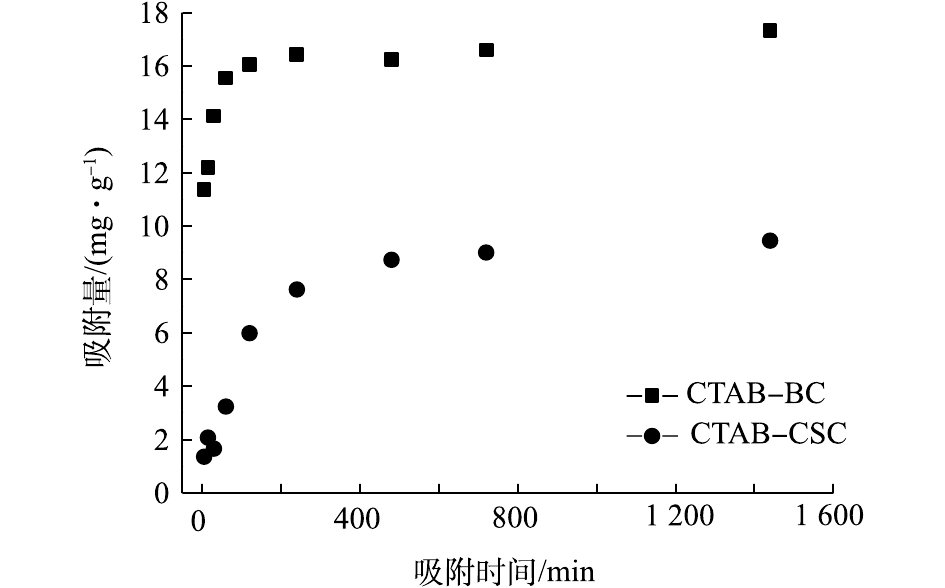
2.2.3 吸附动力学实验
图9为吸附动力学实验结果。可以看出:2种改性材料CTAB-CSC、CTAB-BC对Cd2+的吸附量均随着时间的增加而增加;CTAB-BC在180 min处达到平衡,CTAB-CSC在240 min处达到吸附平衡,CTAB-BC的吸附性能明显优于CTAB-CSC。
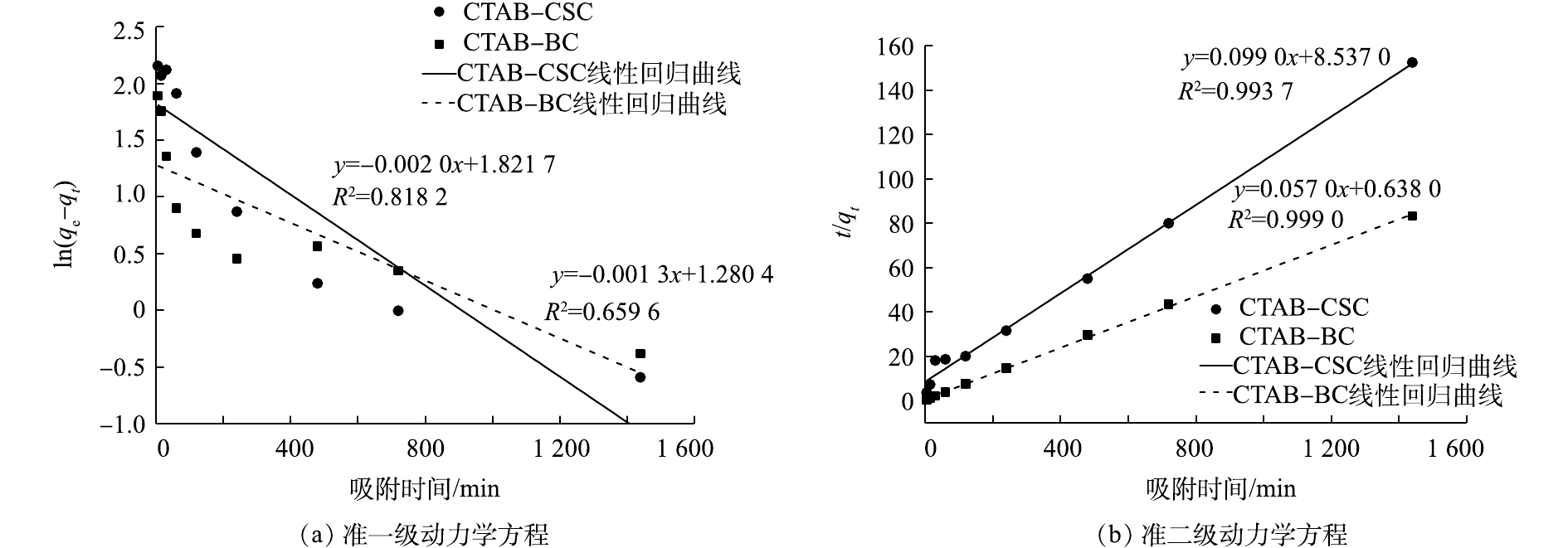
根据式(3)和式(4)拟合ln(qe-qt)-t和t/qt-t的线性关系,结果如图10所示,动力学拟合参数如表1所示。由拟合参数可得,在初始Cd2+浓度为100 mg·L−1时,CTAB-CSC的准二级动力学方程可决系数(0.993 7)大于准一级动力学方程可决系数(0.818 2),CTAB-BC的准二级动力学方程可决系数(0.999 9)大于准一级动力学方程可决系数(0. 659 6),这说明准二级动力学方程能更好地描述CTAB-CSC、CTAB-BC的吸附过程。通过准二级动力学方程拟合计算出CTAB-CSC和CTAB-BC的理论最大吸附量分别为10.10 mg·g−1和17.54 mg·g−1,与等温吸附所得实验值较为接近。这也表明CTAB-CSC和CTAB-BC对Cd2+的吸附主要受化学吸附作用的控制。
表 1 动力学拟合参数Table 1. Kinetic fitting results材料 准一级动力学方程 准二级动力学方程 qe/(mg·g−1) Kl/min−1 R2 qe/(mg·g−1) K2/(g·(mg·min)−1) R2 CTAB-CSC 6.18 0.004 6 0.818 2 10.10 0.001 1 0.993 7 CTAB-BC 3.60 0.003 0 0.659 6 17.54 0.005 1 0.999 9 2.2.4 等温吸附实验
表2是等温吸附模型的拟合参数;根据式(5)和式(6)拟合的Langmuir模型和Freundlich模型,结果如图11所示。通过分析4种材料的拟合度R2可知,改性前的CSC和BC 2种材料的吸附过程更符合Freundlich模型,由此可推测,改性前的CSC和BC这2种材料对溶液中Cd2+的吸附过程是一种非均匀的表面吸附过程,而经过改性后的材料CTAB-CSC和CTAB-BC更符合Langmuir模型,故可推测CTAB-CSC、CTAB-BC 2种材料的表面具有有限的吸附位点,对Cd2+的吸附机制属于单分子层吸附[26]。
表 2 等温吸附模型拟合参数Table 2. Fitness of isotherm models and corresponding parameters材料 Langmuir模型 Freundlich模型 qmax/(mg·L−1) KL/(L·g−1) R2 KF/(L·g−1) n R2 CSC 5.58 0.155 2 0.891 8 1.571 0 3.834 0 0.964 6 CTAB-CSC 10.71 0.054 7 0.976 8 3.037 2 4.608 3 0.731 6 BC 5.95 0.084 0 0.946 8 1.260 0 3.270 0 0,959 0 CTAB-BC 12.56 0.076 9 0.970 3 3.837 0 4.783 0 0.816 3 Freundlich等温吸附方程是一个经验方程。该方程中的n值能反映材料的吸附性能,其中n值越大,表明材料的吸附性能越好。一般认为1/n为0.1~0.5,容易吸附;1/n大于2时,吸附较难进行。通过数据分析,2种材料的1/n均处于0.1~0.5,说明吸附过程是优惠吸附,材料的吸附性能较好。KF值与吸附剂吸附容量正相关,CTAB-BC的KF值大于CTAB-CSC,这表明CTAB-BC对Cd2+的吸附容量大于CTAB-CSC,与本研究结果一致。
CTAB-CSC和CTAB-BC对Cd2+的最大吸附量分别为10.71 mg·g−1和12.56 mg·g−1,较改性前的吸附效果分别提升了92%和111%,改性效果明显提升,且CTAB-BC的吸附效果优于CTAB-CSC。
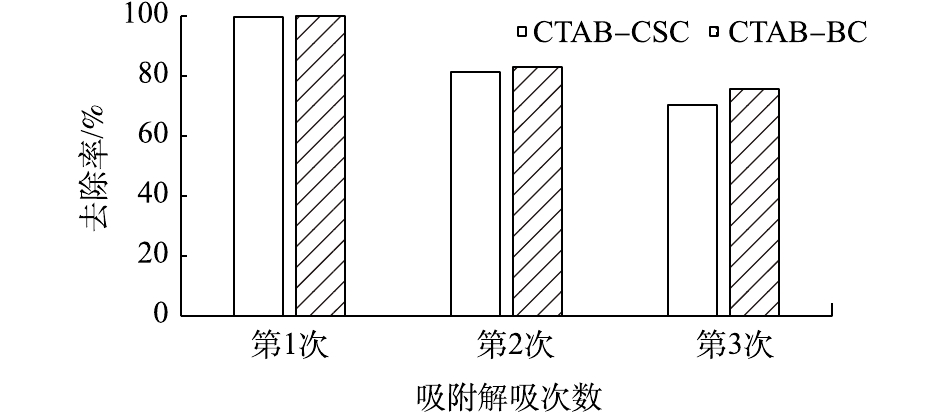
2.2.5 材料再生实验
由图12可以看出,在Cd2+初始浓度为10 mg·g−1时,CTAB-CSC和CTAB-BC首次对Cd2+吸附去除率均在98%以上;经过2次重复的吸附-脱附实验后,CTAB-CSC、CTAB-BC对水中的Cd2+的去除率分别降低为70.33%和75.83%,较原材料对Cd2+的去除率分别减少了29.67%和24.17%。经过连续2次的吸附-脱附实验后,材料对水中Cd2+的去除率还保持在70%左右,且CTAB-BC的再生性能优于CTAB-CSC。以上结果表明2种材料均有较好的再生性。
3. 结论
1)本研究成功制备了CTAB-CSC和CTAB-BC改性吸附材料,通过等温吸附实验证实了改性后的吸附材料对水体中Cd2+的吸附量有明显提升。CTAB-CSC、CTAB-BC对Cd2+的吸附能力较CSC、BC分别提升了92%和111%,吸附性能为CTAB-BC(12.56 mg·g−1)>CTAB-CSC(10.71 mg·g−1)>BC(5.95 mg·g−1)>CSC(5.85 mg·g−1)。
2) 2种改性材料的最佳投加量为0.100 0~0.200 0 g,CTAB-CSC的最适pH范围较窄,为6~7,CTAB-BC的pH范围较广,在4~7时均有较好的吸附效果。
3)通过动力学实验分析,准二级动力学方程能更好地描述CTAB-CSC、CTAB-BC 2种材料的吸附过程,R2均大于0.99,CTAB-BC在180 min时达到平衡,CTAB-CSC在240 min时达到吸附平衡。
-
表 1 不同C/N下无硫、含硫条件对斜生栅藻脂肪酸组成及相对含量的影响(%)
Table 1. Effects of sulfur-free and sulfur-containing conditions on the composition and relative content of fatty acids in Scenedesmus obliquus under different C/N ratio
组别Groups C/N C16:0 C16:1 C18:0 C18:1 C18:2 C18:3 Others 无硫组Sulfur-free group 0 30.40 0.15 5.29 50.82 4.79 3.70 4.85 7.5 32.06 0.34 2.56 41.92 8.44 12.58 2.10 15 38.16 0.22 3.08 39.21 7.18 9.33 2.82 30 29.38 0.20 2.84 45.62 7.93 11.54 2.49 60 29.14 0.18 3.49 47.11 8.24 9.21 2.63 含硫组Sulfur-containing group 0 25.52 0.15 3.99 55.72 5.61 6.02 2.99 7.5 24.70 0.53 0.66 18.48 13.31 39.43 2.89 15 26.78 0.60 3.19 47.14 8.16 11.80 2.33 30 26.15 0.51 2.57 43.06 10.02 15.32 2.37 60 22.86 0.61 0.90 23.90 15.58 33.38 2.77 -
[1] MICHAL B, GRAHAM J E, ANNA K, et al. Transcriptome analysis of the sulfate deficiency response in the marine microalgae Emiliania huxleyi [J]. New Phytologist, 2013, 199(3): 650-662. doi: 10.1111/nph.12303 [2] ABOMOHRA A E F, ELADEL H, EL-ESAWI M, et al. Effect of lipid-free microalgal biomass and waste glycerol on growth and lipid production of Scenedesmus obliquus: Innovative waste recycling for extraordinary lipid production [J]. Bioresource Technology, 2018, 249: 992-999. doi: 10.1016/j.biortech.2017.10.102 [3] YIN Z H, ZHU L D, LI S X, et al. A comprehensive review on cultivation and harvesting of microalgae for biodiesel production: Environmental pollution control and future directions [J]. Bioresource Technology, 2020, 301: 122804. doi: 10.1016/j.biortech.2020.122804 [4] 谢雅清, 郁彬琦, 靳翠丽, 等. 微藻规模化培养与生物能源开发 [J]. 现代化工, 2019, 39(8): 27-32. XIE Y Q, YU B Q, JIN C L, et al. Large-scale cultivation of microalgae for bio-energy utilization [J]. Modern Chemical Industry, 2019, 39(8): 27-32(in Chinese).
[5] RAN W Y, WANG H T, LIU Y H, et al. Storage of starch and lipids in microalgae: Biosynthesis and manipulation by nutrients [J]. Bioresource Technology, 2019, 291: 121894. doi: 10.1016/j.biortech.2019.121894 [6] QIU R H, GAO S, LOPEZ P A, et al. Effects of pH on cell growth, lipid production and CO2 addition of microalgae Chlorella sorokiniana [J]. Algal Research, 2017, 28: 192-199. doi: 10.1016/j.algal.2017.11.004 [7] GAO F, YANG H L, LI C, et al. Effect of organic carbon to nitrogen ratio in wastewater on growth, nutrient uptake and lipid accumulation of a mixotrophic microalgae Chlorella sp. [J]. Bioresource Technology, 2019, 282: 118-124. doi: 10.1016/j.biortech.2019.03.011 [8] BASHIR K M I, MANSOOR S, KIM N R, et al. Effect of organic carbon sources and environmental factors on cell growth and lipid content of Pavlova lutheri [J]. Annals of Microbiology, 2019, 69(4): 353-368. doi: 10.1007/s13213-018-1423-2 [9] ANAND J, ARUMUGAM M. Enhanced lipid accumulation and biomass yield of Scenedesmus quadricauda under nitrogen starved condition [J]. Bioresource Technology, 2015, 188: 190-194. doi: 10.1016/j.biortech.2014.12.097 [10] ZHENG H L, LIU M Z, LU Q, et al. Balancing carbon/nitrogen ratio to improve nutrients removal and algal biomass production in piggery and brewery wastewaters [J]. Bioresource Technology, 2018, 249: 479-486. doi: 10.1016/j.biortech.2017.10.057 [11] LV J, GUO J Y, FENG J, et al. Effect of sulfate ions on growth and pollutants removal of self-flocculating microalga Chlorococcum sp. GD in synthetic municipal wastewater [J]. Bioresource Technology, 2017, 234: 289-296. doi: 10.1016/j.biortech.2017.03.061 [12] 王倩雅, 张莹, 李爱芬, 等. 硫素营养水平对产油尖状栅藻光合生理及生化组成的影响 [J]. 水生生物学报, 2017, 41(4): 904-913. doi: 10.7541/2017.113 WANG Q Y, ZHANG Y, LI A F, et al. Effects of sulfur concentration on the photosynthetic physiology and biochemical composition of Scenedesmus acuminatus [J]. Acta Hydrobiologica Sinica, 2017, 41(4): 904-913(in Chinese). doi: 10.7541/2017.113
[13] ZHANG T Y, WU Y H, ZHU S F, et al. Isolation and heterotrophic cultivation of mixotrophic microalgae strains for domestic wastewater treatment and lipid production under dark condition [J]. Bioresource Technology, 2013, 149: 586-589. doi: 10.1016/j.biortech.2013.09.106 [14] 余亚岑, 钱领, 刘广发, 等. 碳源对巴氏杜氏藻生长及其脂类含量的影响 [J]. 厦门大学学报(自然科学版), 2015, 54(6): 812-818. YU Y C, QIAN L, LIU G F, et al. The influence of carbon resources on the growth and lipid content of Dunaliella bardawil [J]. Journal of Xiamen University (Natural Science), 2015, 54(6): 812-818(in Chinese).
[15] 刘祥, 杨美娟, 散而复, 等. 不同营养模式下固定化斜生栅藻和普通小球藻氨氮去除能力对比分析 [J]. 环境科学研究, 2020, 33(8): 1869-1876. LIU X, YANG M J, SAN E F, et al. Comparative analysis of ammonia nitrogen removal capacity of immobilized Scenedesmus obliquus and Chlorella vulgaris under different trophic modes [J]. Research of Environmental Sciences, 2020, 33(8): 1869-1876(in Chinese).
[16] SHEN Y, GAO J Q, LI L S. Municipal wastewater treatment via co-immobilized microalgal-bacterial symbiosis: Microorganism growth and nutrients removal [J]. Bioresource Technology, 2017, 243: 905-913. doi: 10.1016/j.biortech.2017.07.041 [17] MA C, WEN H Q, XING D F, et al. Molasses wastewater treatment and lipid production at low temperature conditions by a microalgal mutant Scenedesmus sp. Z-4 [J]. Biotechnology for Biofuels, 2017, 10: 111. doi: 10.1186/s13068-017-0797-x [18] ZHANG Y, HUANG Z Z, ZHENG H L, et al. Growth, biochemical composition and photosynthetic performance of Scenedesmus acuminatus under different initial sulfur supplies [J]. Algal Research, 2020, 45: 101728. doi: 10.1016/j.algal.2019.101728 [19] CHENG J, WANG Z Y, LU H X, et al. Hydrogen sulfide improves lipid accumulation in Nannochloropsis oceanica through metabolic regulation of carbon allocation and energy supply [J]. ACS Sustainable Chemistry & Engineering, 2020, 8(6): 2481-2489. [20] 许海, 陈丹, 陈洁, 等. 氮磷形态与浓度对铜绿微囊藻和斜生栅藻生长的影响 [J]. 中国环境科学, 2019, 39(6): 2560-2567. doi: 10.3969/j.issn.1000-6923.2019.06.039 XU H, CHEN D, CHEN J, et al. Effects of nitrogen and phosphorus forms and concentrations on the growth of Microcystis aeruginosa and Scenedesmus obliquus [J]. China Environmental Science, 2019, 39(6): 2560-2567(in Chinese). doi: 10.3969/j.issn.1000-6923.2019.06.039
[21] 尚常花, 王忠铭, 袁振宏, 等. 氮限制对产油杜氏藻转录组的影响 [J]. 中国油料作物学报, 2016, 38(4): 524-528. doi: 10.7505/j.issn.1007-9084.2016.04.018 SHANG C H, WANG Z M, YUAN Z H, et al. Effect of nitrogen limitation on transcriptome of oleaginous Dunaliella parva [J]. Chinese Journal of Oil Crop Sciences, 2016, 38(4): 524-528(in Chinese). doi: 10.7505/j.issn.1007-9084.2016.04.018
[22] 周涛, 李正魁, 冯露露. 氨氮和硝氮在太湖水华自维持中的不同作用 [J]. 中国环境科学, 2013, 33(2): 305-311. doi: 10.3969/j.issn.1000-6923.2013.02.017 ZHOU T, LI Z K, FENG L L. The different roles of ammonium and nitrate in the bloom self-maintenance of Lake Taihu [J]. China Environmental Science, 2013, 33(2): 305-311(in Chinese). doi: 10.3969/j.issn.1000-6923.2013.02.017
[23] 王蒙, 李纯厚, 戴明, 等. C/N对牟氏角毛藻生长速率和总脂含量的影响[J]. 水产学报, 2010, 34(10): 1518-1524. WANG M, LI C H, DAI M, et al. The effect of C/N on the growth and total lipid content of Chaetoceros muelleri[J]. Journal of Fisheries of China, 2010, 34(10): 1518-1524(in Chinese).
[24] ADAMS C, GODFREY V, WAHLEN B, et al. Understanding precision nitrogen stress to optimize the growth and lipid content tradeoff in oleaginous green microalgae [J]. Bioresource Technology, 2013, 131: 188-194. doi: 10.1016/j.biortech.2012.12.143 [25] TAKESHITA T, OTA S, YAMAZAKI T, et al. Starch and lipid accumulation in eight strains of six Chlorella species under comparatively high light intensity and aeration culture conditions [J]. Bioresource Technology, 2014, 158: 127-134. doi: 10.1016/j.biortech.2014.01.135 [26] PAL D, KHOZIN-GOLDBERG I, COHEN Z, et al. The effect of light, salinity, and nitrogen availability on lipid production by Nannochloropsis sp [J]. Applied Microbiology and Biotechnology, 2011, 90(4): 1429-1441. doi: 10.1007/s00253-011-3170-1 [27] 黄怡, 高保燕, 王飞飞, 等. 不同磷、硫及二氧化碳浓度对标志链带藻生长和碳水化合物积累的影响 [J]. 微生物学报, 2019, 59(10): 1915-1926. HUANG Y, GAO B Y, WANG F F, et al. Effects of phosphorus, sulfur and carbon dioxide concentrations on growth and carbohydrate accumulation of Desmodesmus insignis [J]. Acta Microbiologica Sinica, 2019, 59(10): 1915-1926(in Chinese).
[28] THUNYARATCHATANON C, LUENGNARUEMITCHAI A, JITJAMNONG J, et al. Influence of alkaline and alkaline earth metal promoters on the catalytic performance of Pd-M/SiO2 (M = na, ca, or Ba) catalysts in the partial hydrogenation of soybean oil-derived biodiesel for oxidative stability improvement [J]. Energy & Fuels, 2018, 32(9): 9744-9755. [29] MIAO X L, WU Q Y. Biodiesel production from heterotrophic microalgal oil [J]. Bioresource Technology, 2006, 97(6): 841-846. doi: 10.1016/j.biortech.2005.04.008 [30] 韩松芳, 金文标, 涂仁杰, 等. 细菌对城市污水中斜生栅藻生长与产脂的影响 [J]. 中国环境科学, 2017, 37(10): 3867-3872. doi: 10.3969/j.issn.1000-6923.2017.10.031 HAN S F, JIN W B, TU R J, et al. Effects of bacteria on growth and lipid production of Scenedesmus obliquus cultivated in municipal wastewater [J]. China Environmental Science, 2017, 37(10): 3867-3872(in Chinese). doi: 10.3969/j.issn.1000-6923.2017.10.031
[31] HOEKMAN S K, BROCH A, ROBBINS C, et al. Review of biodiesel composition, properties, and specifications [J]. Renewable and Sustainable Energy Reviews, 2012, 16(1): 143-169. doi: 10.1016/j.rser.2011.07.143 [32] HOEKMAN S K, BROCH A, ROBBINS C, et al.Review of biodiesel composition, properties, and specifications[J].Renewable and Sustainable Energy Reviews, 2012, 16(1): 143-169. -









 下载:
下载: