-
石河子市是位于新疆乌昌石区域中部的工业城市,近几年随着经济的快速发展,其大气污染较为严重,冬季以细颗粒物(PM2.5)为首要污染物的污染天时有发生[1-4]. 无机元素作为细颗粒物的主要成分之一,大部分具有容易富集和难以降解的特点,尤其是重金属元素在人体中的富集会危害人体器官健康,造成不可逆的功能性障碍[5-7]. 近年来北京市[8]、上海市[9]、沈阳市[10]、广州市[11]、成都市[12]、乌鲁木齐市[13]、珠三角区域[14]等对PM2.5中无机元素的研究主要针对重金属元素。王琼等[15]研究认为,北京冬季大气PM2.5中元素的致癌风险高于夏季,污染日大气PM2.5中元素的致癌风险高于清洁日,PM2.5中元素的健康风险具有较为明显的季节性变化特征,冬季有针对性地控制大气PM2.5污染,对人体健康意义深远. 任慧清等[16]通过研究石河子市冬季5种重金属元素(Ni、Cu、Zn、Pb、Fe),并选取重金属元素Zn进行大鼠肺部损伤实验发现,供暖季石河子市PM2.5浓度为(109.9±58.8) μg·m−3, PM2.5和Zn浓度的升高能够显著抑制超氧化物歧化酶(SOD)活性,引起对大鼠肺部的损伤.李瑶等[17]通过对石河子市进行PM2.5高精度遥感反演发现,石河子市PM2.5的空间分布呈现北低南高,西低东高的特点. 丁俊男等[18]通过富集因子法研究河南省典型城市采暖季PM2.5中无机元素的来源,发现郑州市、洛阳市和平顶山市的Se、Cd、Br、Pb、Zn、Cu、Co、Sc、Cr、Ni、As、Mn、Ba等元素的富集因子大于10,主要来源于人为源,这13种元素质量浓度在22种元素中占比为18.9%—26.3%,主要来源于燃煤、机动车、扬尘和建筑尘等,Ni、Co、Sr、Ba 还有来自其他排放源的贡献. 张晶晶等[19]通过研究昌吉市采暖季PM2.5的污染特征发现,采暖季PM2.5的浓度高于非采暖季5.6倍,采暖季首要污染物为PM2.5,比例最高占66.3%.
石河子市工业区主要集中在城区北部,紧邻城区. 石河子市冬季以PM2.5为首要污染物的污染天频发,PM2.5中富集的重金属元素会损害人体器官,研究PM2.5中无机元素的变化特征和来源对于评价城市环境质量,制定环境治理对策具有重要意义[20-21]. 本研究在石河子市城区和工业区进行冬季PM2.5样品采集,分析2个功能区无机元素的浓度水平和变化特征,并通过富集因子法(EF)对冬季PM2.5污染来源进行解析[22-23].
-
石河子市工业区主要集中在城区北部,在城区和工业区内共设置2个采样点,采样点信息如表1所示,城区采样点位于环境监测站楼顶,其正东方向1.6 km处为阳光学校国控站点,正南方向1.2 km处为艾青诗歌馆国控站,工业区采样点位于大全新能源股份有限公司(大全)办公楼楼顶,工业区排放源主要以化工、电力、电解铝、硅冶炼、水泥等大型重工业高架点源为主. 2个采样点同时开展为期2个月的全天候PM2.5采样,采样点距地垂直高度均不低于10.0 m,周围无明显污染源,因此能够代表周围区域大气环境特征.
-
在石河子市城区和工业区的2个采样点均使用武汉天虹TH-16A型四通道采样器进行采样(另外两通道平行采样备用),各通道采样流量均为16.7 L·min−1. 采样日期为2020年12月1日—2021年1月31日,共采集62 d,采样时间为每天10:00—翌日09:00,累积采样时长23 h. 每日采样滤膜为一张直径47 mm的石英纤维滤膜(Q膜,Pall,Sweden)和一张直径47 mm的聚丙烯滤膜(P膜,Whatman,Sweden),具体方法按照《环境空气颗粒物(PM2.5)手工监测方法(重量法)技术规范》[24]要求. 利用电感耦合等离子质谱仪(ICP-MS,Agilent 7800,America)对滤膜进行元素分析,取1/4面积滤膜,放置于聚四氟乙烯消解罐中,加入5.0 mL MOS级硝酸,放置2 h后再加入2.0 mL MOS级盐酸,2.0 mL优级纯H2O2,加盖密封后,用微波消解萃取仪消解(在10 min内升温到190 ℃后至少保持30 min). 待消解罐冷却至室温,再利用赶酸器在140 ℃将消解液浓缩至约0.5 mL(约4—5 h),用超纯水转移定容为25.0 mL,然后进行仪器分析. 包括Be、Na、Mg、Al、K、Ca、V、Cr、Mn、Fe、Co、Ni、Cu、Zn、As、Se、Mo、Ag、Cd、Ba、Tl、Pb、Th、U,共24种.
-
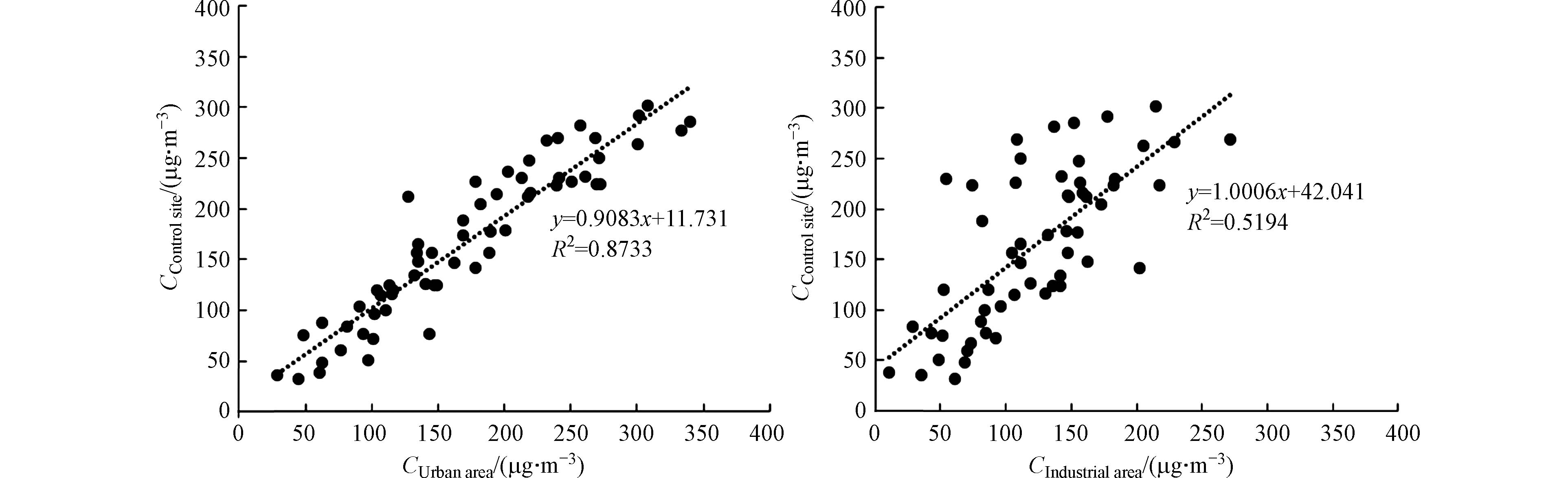
对P膜进行样品称重,根据采集样品量和采样体积计算PM2.5浓度[24],并与石河子市国控站PM2.5值进行对比,如图1所示. 一般认为PM2.5的相关性在80%—120%之间是合理的[25],城区和工业区手工采样PM2.5值与国控站进行比较,可判断手工采样PM2.5的代表性和各点位PM2.5的差异,城区采样点的PM2.5浓度值与国控站的PM2.5浓度值相关系数R2为0.87,线性关系较好,而工业区采样点的PM2.5浓度值与国控站的PM2.5浓度值相关系数R2为0.52,说明工业区PM2.5污染浓度特征与城区有所不同.
-
2020年12月1日—2021年1月31日在石河子市共采样62 d,以PM2.5为首要污染物的污染天占比较高,如表2所示,采样期石河子市空气质量为优的天数为0,重度污染天最多,占整个采样期的38.7%,严重污染天数占整个采样期的14.5%,以PM2.5为首要污染物的污染天数占整个采样期的98.4%,
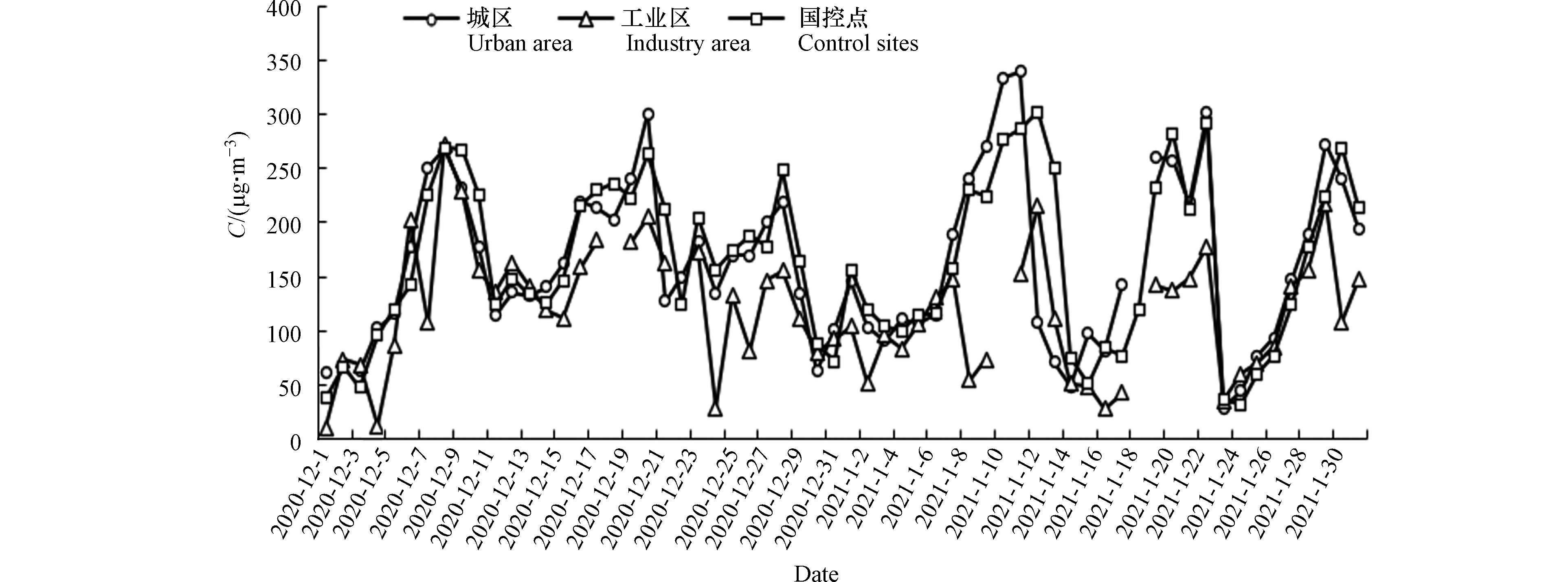
如图2所示,采样期内共发生6次污染过程,其中2020年12月发生3次,2021年1月发生3次,污染过程时间最长的持续8 d,最大PM2.5日均值发生在2021年1月12日,国控站测得日均值为302.0 μg·m−3. 整个采样期国控站PM2.5的日均值为165.0 μg·m−3,以PM2.5为首要污染物的污染天PM2.5日均值为167.2 μg·m−3,两者数据很接近,与《环境空气质量标准》( GB 3095—2012) [26]中规定的PM2.5日均浓度二级标准限值( 75 μg·m−3 )相比,超过75 μg·m−3的天数为54 d,占整个采样期的87.1%,说明石河子市冬季以PM2.5为首要污染物的污染天形势非常严峻. 整个采样期城区手工采样的PM2.5质量浓度日均值为164.7 μg·m−3,工业区手工采样的PM2.5质量浓度日均值为113.6 μg·m−3,表明城区PM2.5污染程度高于工业区. 两采样点直线距离约12.0 km,城区采样点距离国控点较近,由图2可知,城区手工PM2.5与国控点PM2.5的变化趋势较一致,采样期两者PM2.5平均差值为6.7 μg·m−3,说明两者相关性好,误差较小. 工业区主要以化工、火电、电解铝、硅冶炼、水泥等重工业高架点源排放为主,冬季石河子北部区域地面风场以弱偏北风为主,城区位于工业区的下风向,有研究表明一定条件下工业区高架点源对10.0—12.0 km范围区域影响明显[27-28],石河子城区PM2.5浓度高的原因可能与工业区企业高架点源排放和远距离传输到城区有关.
-
石河子市城区和工业区环境PM2.5中元素浓度如表3所示,城区PM2.5中元素浓度由高到低依次为:Na>Ca>K>Fe>Al>Mg>Zn>Pb>Mn>Cu>Ba>As>Cr>V>Ni>Cd>Mo>Co>Se>Tl>Be>U>Ag>Th, 工业区PM2.5中元素浓度由高到低依次为:Na>Ca>K>Al>Fe>Mg>Zn>Pb>Mn>Cr>V>Ba>As>Cu>Ni>Mo>Cd>Co>Tl>Be>U>Se>Th>Ag. 采样期城区PM2.5中元素浓度和为4353.0 ng·m−3,工业区PM2.5中元素浓度和为3556.6 ng·m−3,城区和工业区元素K、Ca、Na、Mg、Al、Fe质量浓度较大,均超过了100.0 ng·m−3,6种元素在城区元素总浓度的占比为97.4%,在工业区元素总浓度的占比为97.5%,说明这6种元素为石河子市无机元素的主要组成部分. 从采样期元素浓度均值来看,工业区的元素浓度值低于城区,说明无机元素在城区PM2.5颗粒物上的富集程度高于工业区. 昌吉市与石河子市同为乌昌石区域城市,赵强等[29]研究发现昌吉市因春、夏、秋季多风,易导致扬尘发生,冬季冰雪覆盖裸土,施工较少,冬季燃煤量大,污染物积累导致元素浓度与PM2.5质量浓度规律不符,元素浓度表现为秋季>夏季>春季>冬季,即冬季元素浓度水平最低,同时与国内南部城市广州市[30]、中部城市南昌市[31]以及北部城市天津市[32]冬季PM2.5中无机元素浓度对比发现,石河子市和昌吉市等区域PM2.5中无机元素浓度水平低于其他城市,原因可能为石河子市冬季大雪覆盖裸土,扬尘较少所致.
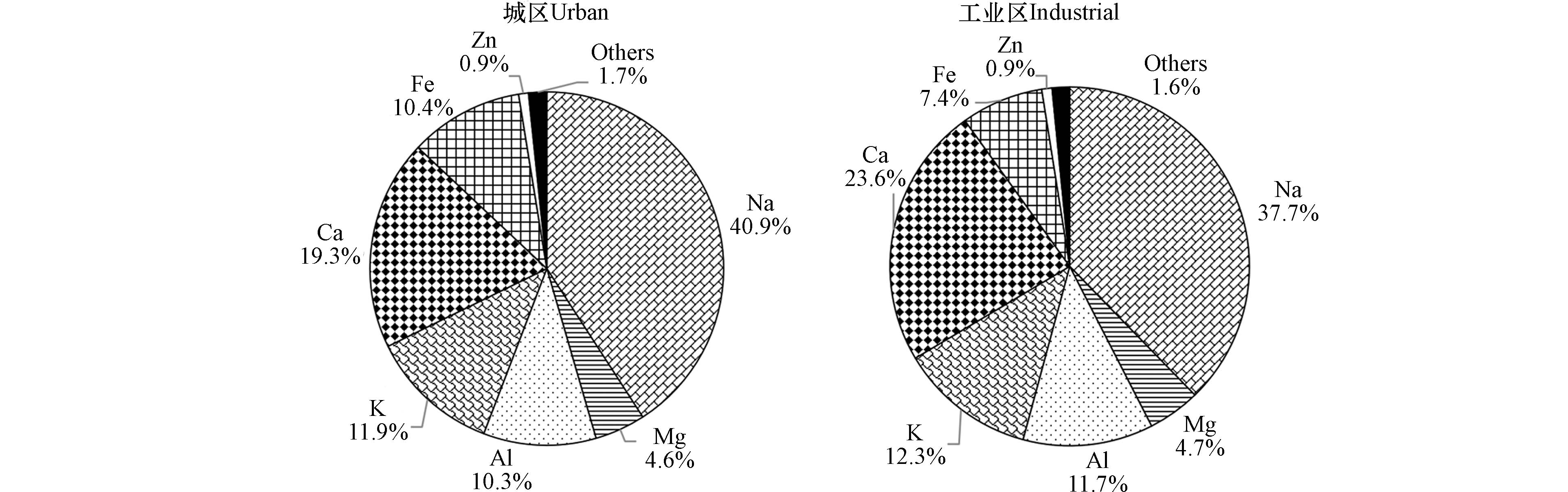
从石河子市城区和工业区元素在无机元素中的占比来看(图3),占比最大的为Na元素,城区Na元素占比40.9%,工业区占比37.7%,其次为Ca元素,城区占比19.3%,低于工业区的23.6%,城区Fe元素占比为10.4%,工业区为7.4%,表明城区的Na、Fe元素相对占比较高,而工业区的Ca元素占比较高,从浓度水平来看,两者元素浓度较为接近.
-
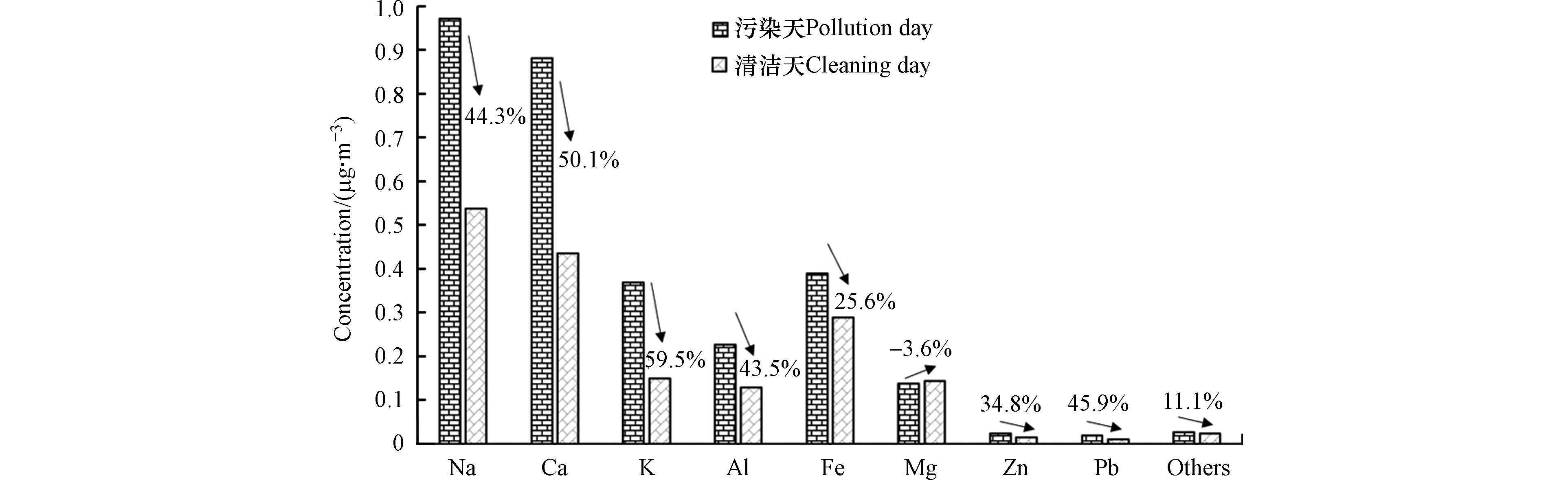
不同的PM2.5污染条件下,元素浓度特征不同,选取非沙尘天的典型污染天2021年1月12日(PM2.5日均值为302.0 μg·m−3)和清洁天2021年1月24日(PM2.5日均值为32.0 μg·m−3)的元素浓度进行对比,如图4所示,与污染天相比,清洁天Na和Ca元素的浓度下降水平较大,下降水平均超过0.4 μg·m−3,其次为K、Al和Fe元素,表明污染天Na和Ca元素的浓度累积量最大. 从下降百分比来看,主要元素浓度下降百分比由高到低依次为:K>Ca>Pb>Na>Al>Zn>Fe,K和Ca元素的浓度百分比下降均超过50%,其中K元素的浓度百分比下降最大,为59.5%,Ca元素为50.1%,表明污染天K和Ca元素的累计速率较快.
-
富集因子法(EF)采用双重归一化的数据处理方法研究人为源和天然源对PM2.5中元素的贡献程度,通过无机元素浓度的富集因子(EF) 来研究大气颗粒物中元素的富集程度,分析PM2.5中污染物的来源,在各类研究中应用较为广泛[33,34]. 元素的富集程度越高,环境PM2.5中相应元素的浓度较地壳物质中相应元素的浓度越高,说明人为因素对环境PM2.5的贡献越大[35].富集因子的计算公式为:
式中:Ci表示为第i种元素的浓度,μg·m−3,Cr表示为选定的表征背景的参比元素的浓度,μg·m−3. 根据富集因子(EF)分级法则,当EFi>100时,表明第i种元素明显受到人为源的影响,当100≥EFi>10时,表明第i种元素受人为扰动,当EFi≤1时,表明第i种元素在环境PM2.5中没有富集. 石河子市土壤主要为灰漠土、潮土和草甸土,本研究中各元素的土壤背景值取自于《中国土壤元素背景值》[36]中以上3种土壤的均值,并选则Al元素作为参比元素[37].
石河子市2020年冬季PM2.5中24种元素的富集因子(EF)如表4所示,由于城市周围土壤不同,石河子市与郴州市[38]、温州市[39]等地级市元素EF值有所不同,城区和工业区的K、Ca、Na、Mg、Fe元素的富集因子均大于1000,表明PM2.5颗粒物中这5种元素主要来自人为源,受周围自然源的影响较小,是典型的人为排放的污染元素,通常Na、K元素多来自生物质燃烧和餐饮油烟,Fe元素多来自于地壳物质或燃煤,Ca元素主要来源是石灰和水泥[40,41],石河子市PM2.5中Ca元素主要来自建筑扬尘以及电石厂原料氧化钙、碳酸钙等,张靳杰[42]研究认为机动车尾气颗粒物中无机元素排放因子最高的是K、Ca、Na、Mg,说明石河子市冬季PM2.5受工业区排放、机动车和地壳物质以及餐饮油烟等的影响,城区Se、Cd、Pb 元素富集因子大于10,工业区Se、Cd、Pb、Ag 元素富集因子大于10,通常Se是燃煤标识物,Cd来自工业粉尘,Pb是机动车排放的标识性元素[43,44],说明环境PM2.5中这些元素受燃煤、工业粉尘和机动车等人为扰动影响. Cu、Zn、As、Cr、Mn、Ba等元素富集因子值较低,受人为扰动影响较小,主要来自天然源.
-
(1) 2020年冬季在石河子市进行为期61d的PM2.5样品采集中,重度及以上污染天数占整个采样期的53.2%,以PM2.5为首要污染物的污染天数占整个采样期的98.4%,采样期城区PM2.5的日均值为164.7 μg·m−3,工业区PM2.5的日均值为113.6 μg·m−3,PM2.5污染较为严重;
(2) 采样期城区PM2.5中元素浓度为4.4 μg·m−3,工业区为3.6 μg·m−3,城区和工业区PM2.5中无机元素的主要成分均为Na、Mg、K、Ca、Al、Fe,6种元素在城区元素中的占比为97.4%,在工业区元素中的占比为97.5%,表明2个功能区PM2.5中元素浓度差异性较小. 污染天K和Ca元素的累积速度最快,Na和Ca元素的累积量最大;
(3) 石河子市2020年冬季PM2.5中主要富集元素为K、Ca、Na、Mg、Fe,富集元素主要来源于工业区、机动车、地壳物质以及餐饮油烟等,城区的元素富集程度和污染程度略高于工业区.
2020年冬季石河子市城区和工业区PM2.5中无机元素污染特征及来源
Characteristics and sources of the inorganic elements of PM2.5 in Shihezi urban and industrial areas in winter, 2020
-
摘要: 石河子市是位于新疆乌昌石区域中部的工业城市,2020年12月和2021年1月在石河子市城区和工业区共布设2个采样点,全天候采集细颗粒物(PM2.5)样品61 d,利用电感耦合等离子质谱仪(ICP-MS)对24种元素含量进行分析,并通过富集因子法(EF)解析PM2.5中无机元素的污染特征及来源. 结果表明,冬季采样期间,石河子市重度及以上污染天数占整个采样期的53.2%,以PM2.5为首要污染物的污染天数占整个采样期的98.4%,采样期城区和工业区的PM2.5日均值分别为164.7 μg·m−3和113.6 μg·m−3,表明石河子市冬季PM2.5污染严重;采样期城区和工业区PM2.5中无机元素浓度分别为4.4 μg·m−3和3.6 μg·m−3,主要成分均为K、Ca、Na、Mg、Al、Fe,6种元素之和在城区和工业区元素中的占比分别为97.4%和97.5%,表明这6种元素为城区和工业区元素的主要组分,城区和工业区主要元素组成差异性较小,污染天K和Ca元素的累积速度最快,Na和Ca元素的累积量最大;石河子市2020年冬季PM2.5中主要富集元素为K、Ca、Na、Mg、Fe,富集元素主要来源于工业区、机动车、地壳物质以及餐饮油烟等,城区元素富集程度和污染程度略高于工业区.Abstract: Shihezi is an industrial city located in the middle of Wu-Chang-Shi region in Xinjiang. 2 sampling sites were set up in Shihezi urban and industrial areas in December 2020 and January 2021, The fine particles (PM2.5) were collected for 61 days in total. 24 kinds of elements were analyzed by ICP-MS, and the characteristics and sources of the inorganic elements of PM2.5 were investigated by using enrichment factor method (EF). The results showed that: During the sampling period in winter, the number of the severe pollution days accounted for 53.2% of the whole sampling days, and the pollution days with PM2.5 as the primary pollutant accounted for 98.4% of the whole sampling period. The daily mean values of PM2.5 in urban and industrial areas were 164.7 μg·m−3 and 113.6 μg·m−3, respectively, demonstrating the heavy air pollution in winter in Shihezi city; The concentrations of the inorganic elements of PM2.5 in urban and industrial areas were 4.4 μg·m−3 and 3.6 μg·m−3, respectively, in the sampling period. The main components of the inorganic elements of PM2.5 in urban and industrial areas were K, Ca, Na, Mg, Al and Fe. These 6 kinds of elements were the primary components of the inorganic elements, and accounted for 97.4% and 97.5% of the whole elements amount in total in urban and industrial areas. The composition structure showed little difference for the inorganic elements of PM2.5 between the urban and industrial areas; The main enriched elements in PM2.5 of Shihezi city in winter were K, Ca, Na, Mg and Fe, and mainly come from industries, motor vehicles, crustal substances and cooking fume, etc. The enrichment and pollution degree of elements in urban areas were slightly higher than those in industrial areas.
-
全氟及多氟烷基化合物(per- and polyfluoroalkyl substances,PFASs),简称全氟化合物,即指化合物分子中与碳原子相连的多个或者全部氢原子被氟原子取代的有机化合物[1]。碳-氟(C—F)键键能较高,导致全氟化合物具有疏油、疏水、耐酸碱、热稳定性和弱分子间相互作用等特性[2]。据不完全统计,过去的几十年中超过4700种全氟化合物被广泛应用于消防、表面活性剂、制冷和催化剂[3-6]等行业,并因为其具有较强的生物富集潜力、生态毒性和长距离迁移能力等,已成为全球性污染物[7-10]。例如目前使用最广的全氟化合物之一的全氟辛酸(perfluorooctanic acid,PFOA),在极地野生动物的血液和器官组织中均有检出[11];毒理学研究表明全氟辛酸具有肝毒性、免疫毒性和神经毒性等[12]。
2014年,PFOA被国际癌症研究所划分为“人类可疑致癌物”[13],2019年正式将PFOA及其衍生品列入《斯德哥尔摩公约》,限制其生产和使用[14]。新型全氟化合物-六氟环氧丙烷二聚体铵盐(ammonium hexafluoropropylene oxide dimer acid,HFPO-DA,商品名Gen X)和六氟环氧丙烷三聚体羧酸(hexafluoropropylene oxide trimer acid,HFPO-TA)(化学结构如图1所示)是目前最主要的PFOA替代物。近年来的环境监测显示,在氟化学工厂附近生活的19—40岁中青年血液中HFPO-TA的检出率为99.2%,其浓度远高于其他新型全氟化合物[15]。在中国南海江豚和海豚的肝脏样品中HFPO-DA的检出率为92%,对样品中总全氟化合物的贡献率为1%。在连续6年的生物监测中,HFPO-DA在海洋哺乳动物体内的浓度呈现出明显的上升趋势[16]。因此新型全氟化合物的生物富集和环境风险值得进一步的关注和研究。
建立一种操作简单且准确度、精密度和灵敏度高的方法,将为后续研究新型全氟化合物的环境行为和生物监测奠定基础。已有的关于传统全氟化合物分析方法多采用阴离子交换液液萃取和WAX固相萃取小柱净化等手段[16-17]。该方法存在操作复杂、耗时长、有机溶剂用量大、经济成本高等不足。对于需要开展大批量样品检测的生物监测类研究,开发一种简便、快捷的方法以提高分析效率尤为重要。基于绿色化学理念的QuEChERs(quick, easy, cheap, effective, rugged, and safe)方法是传统多残留分析方法的简化版[18],于2003年首次被报道应用于食品基质中农药多残留的提取分析[19]。经过研究人员的不断拓展创新,QuEChERs方法已经逐渐被应用于测定环境、食品和生物样品中的多氯联苯、多环芳烃、有机磷阻燃剂和传统全氟化合物[18, 20-21]。已有文献报道将其应用于动物源性食品中传统直链全氟化合物的提取[22-26],对于将QuEChERs方法应用于小鼠器官中新型全氟化合物的提取分析还鲜有报道。
本研究借助QuEChERs和分散固相萃取(dispersive solid-phase extraction,d-SPE)净化方法结合超高效液相色谱串联三重四极杆质谱(UPLC-MS/MS)建立新型全氟化合物(HFPO-TA和HFPO-DA)和与之替代的传统全氟化合物(PFOA)在小鼠器官中的提取净化分析方法。
1. 材料与方法(Materials and methods)
1.1 试剂、材料与仪器
标准样品(HFPO-TA、HFPO-DA和PFOA)均购自梯希爱(上海)化成工业发展有限公司。所用试剂包括:甲醇(色谱纯,默克),乙酸铵(MS级,南试),Milli-Q水(18.25 MΩ·cm,实验室自制),乙腈(分析纯,西陇科学),氯化钠(分析纯,阿拉丁),盐酸(分析纯,南试),甲酸(MS级,阿拉丁)。石墨化炭黑(GCB,120—400目)、十八烷基键合硅胶(C18,40—63 μm)和N-丙基乙二胺(PSA,40—63 μm)购于上海安谱实验科技股份有限公司。
建立方法所需小鼠器官取自未经全氟化合物暴露的Balb/c雌鼠。大脑、心脏、肺、肾脏和肝脏样品收集自江苏生命科技园某医药公司动物房内饲养的小鼠。实验通过实验动物福利与伦理审查。
仪器:QSight® Altus LC-30超高效液相色谱仪(美国Perkin Elmer公司),QSight® 210 三重四极杆质谱仪(美国Perkin Elmer公司),HD-2500多管涡旋混合仪(杭州佑宁仪器有限公司),KH-7000SP超声波清洗器(昆山禾创超声仪器有限公司),Milli-Q超纯水仪( Millipore 公司),SCIENTZ-10ND低温冷冻干燥机(宁波新芝生物科技股份有限公司),Lindberg blue M马弗炉(Thermo Scientific公司),ME204分析天平(Mettler Toledo公司)。
1.2 实验方法
1.2.1 标准溶液配制
标准储备液的配制:十万分之一天平分别称取0.0101 g的HFPO-TA、HFPO-DA和PFOA的标准品于10 mL容量瓶中,用色谱甲醇溶解并定容可得质量浓度为1000 mg·L−1的标准储备液,保存于4 ℃冰箱中。
混合标准储备液以及标准工作溶液的配制:分别准确转移1 mL标准储备液混合于10 mL容量瓶中,用色谱甲醇稀释并定容;再次吸取混合标准溶液1 mL于10 mL容量瓶中,可分别得质量浓度为100 mg·L−1和10 mg·L−1的混合标准储备液。使用混合溶液(甲醇∶水=1∶1,V/V)做逐级梯度稀释,配制质量浓度为0.005、0.01、0.05、0.1、0.5、1 mg·L−1的标准工作溶液。工作溶液保存在4℃冰箱内。
1.2.2 仪器分析条件
液相色谱条件:Perkin Elmer C18色谱柱(2.7 μm,150 mm × 2.1 mm);柱温:40 ℃;流速:0.3 mL·min−1;进样量:10 μL;流动相:A,1 mmol·L−1乙酸铵水溶液;B,甲醇;梯度洗脱顺序:0—2.5 min,40%—10% A;2.5—4.0 min,10% A;4.0—4.1 min,10%—40% A;4.1—6.0 min,40% A。
质谱条件:电喷雾离子源在负离子条件下搭配多重反应监测模式(MRM);毛细管电压:0.41 kV;离子源温度:200 ℃;去溶剂气流:氮气,1000 L·h−1;去溶剂温度:500 ℃。
1.2.3 小鼠器官前处理方法
QuEChERs方法以乙腈做提取溶剂,通过氯化钠等无机盐的盐析作用实现相分离。但是全氟化合物在酸性条件下呈分子态,易于使其进入有机溶剂。已有研究考察了不同浓度(0.05%、0.1%、0.2%和0.3%)盐酸-乙腈溶液对动物源性(猪、牛和羊的肾脏、肝脏和肌肉)食品中13种传统PFASs的提取回收率[26],0.1%、0.2%和0.3%盐酸-乙腈溶液均能满足食品残留分析要求,且0.2%盐酸-乙腈溶液做提取溶剂时基线平稳,在目标峰出峰位置无杂质共流出,因此本研究采用0.2%盐酸的乙腈为提取溶剂。
小鼠器官于-80 ℃冰箱冷冻,放置冷冻干燥机内真空干燥48 h,使用研钵将其粉碎后,盛于聚丙烯(polypropylene,PP)离心管,在-20 ℃冰箱保存备用。准确称取0.10 g 各小鼠器官样品粉末于15 mL PP离 心管,加入2 mL Milli-Q水,在手中剧烈振荡使其浸湿样品。加入2 mL 0.2%盐酸乙腈,涡旋10 min,超声5 min。每只离心管中加入1 g NaCl,再次涡旋10 min,在4000 r·min−1的条件下离心10 min。1.5 mL上清液转移至装有100 mg PSA、80 mg C18和30 mg GCB的15 mL PP离心管中,在手中急速剧烈上下振摇两次后,涡旋30 s。在4000 r·min−1条件下离心10 min,准确吸取1 mL上清液于4 mL离心管中,控制氮气浓缩仪的水温低于40 ℃,气流使液面产生涟漪条件下浓缩至干。准确加入0.1 mL混合溶液(甲醇:水=1:1, V/V)复溶样品,过0.22 μm PP针式滤器,UPLC-MS/MS分析.
1.3 方法学考察
1.3.1 线性范围、检出限、定量限
取小鼠器官样品,按照1.2.3节前处理方法提取净化后,准确量取0.1 mL标准混合工作溶液复溶样品,分别可得质量浓度为0.005、0.01、0.05、0.1、0.5、1 mg L−1的基质匹配标准溶液。分别取混合标准工作溶液和基质匹配标准溶液,按照1.2.2节的仪器条件上机测定。通过Simplicity 3Q软件获取相应数据,提取定量离子对,以定量离子峰面积为纵坐标,质量浓度为横坐标,分别绘制溶剂标准曲线和基质匹配标准曲线。
同时以基质匹配标准曲线最低浓度的信噪比3倍和10倍计算该方法的检出限(Limit of detection, LOD)、定量限(Limit of quantification, LOQ)。具体公式如下:
LOD(μg⋅L−1)=3×噪声峰高×C LOQ(ng)=10×噪声峰高×C×V (ng) 式中,C为基质标样浓度(μg·L−1);V为进样体积(μL)。
1.3.2 基质效应
本研究依据拟合的溶剂和基质匹配标准曲线线性方程的斜率评估所建立前处理方法的基质效应,计算公式如下:
基质效应(matrixeffect,ME)=基质标线斜率−溶剂标线斜率溶剂标线斜率×100% 若|ME| < 20%,无基质干扰效应;若20% ≤ |ME| ≤ 50%,中等基质干扰效应;|ME| > 50%,较强的基质干扰效应[27-28]。
1.3.3 回收率
向小鼠器官样品中添加HFPO-TA、HFPO-DA和PFOA的混合标准液,由于缺乏相应最高残留限量值的支持,参考土壤等环境基质中检出浓度[29],分别取10 μL的50、100、1000 μg·L−1的混合标准溶液注入空白基质中,使目标分析物在基质中的浓度依次为5、10、100 μg·kg−1。根据1.2.3节前处理方法提取净化后测定,分别计算回收率和相对标准偏差(relative standard deviation, RSD)。
1.4 实际样品分析
将HFPO-TA、HFPO-DA和PFOA通过喂食的方式暴露于小鼠,得到富集了目标分析物的小鼠器官样品,进一步验证所建立分析方法的准确性。过程如下:商品化鼠粮冷冻干燥粉碎后,称取50 g,将一定浓度的HFPO-TA、HFPO-DA和PFOA的混合标准工作溶液添加到2 g石英砂中,待溶剂完全挥发后与鼠粮混合,搅拌均匀,加入适量Milli-Q水揉成面团状,人工重新造粒,冷冻干燥后每粒鼠粮的干重为4 g,其中每种目标分析物的浓度为1 mg kg−1。
实验小鼠自由采食饮水驯养一周,饥饿处理12 h后,随机转移至PP塑料笼中。暴露组设置4个重复,每天每只小鼠给予1粒鼠粮,自由饮水;空白组给与商品化鼠粮和自由饮水,连续饲养3 d后收集剩余鼠粮,再次饥饿处理12 h后断颈法处死小鼠,收集目标器官(大脑、肺、心脏、肾脏、肝脏)。
1.5 数据分析
本研究中相关数据均采用Simplicity 3Q色谱工作站采集,OriginPro 2021 (Learning Edition)进行数据处理分析。
2. 结果与讨论(Results and discussion)
2.1 仪器分析条件
2.1.1 液相色谱条件优化
国标[30-31]和一些研究[15-17, 32-34]中以较低硅羟基活性填料的C18做固定相,乙腈-乙酸铵水溶液或者甲醇-乙酸铵水溶液做流动相梯度洗脱可实现全氟化合物的基线分离。本研究探讨了甲醇-乙酸铵水溶液系统中缓冲盐乙酸铵的浓度(0、1、2、5、10 mmol·L−1)对目标化合物的仪器响应值和峰形的影响(图2)。
对比仪器响应值发现(图2 a),对于HFPO-DA和PFOA而言,两者的峰面积随流动相中缓冲盐浓度的增加而逐渐下降,在从0 mmol·L−1到1 mmol·L−1增加过程中,峰面积下降明显,即乙酸铵对目标化合物的响应具有抑制效应[35];对于HFPO-TA,峰面积随流动相中缓冲盐浓度的增加呈现出先上升后下降的变化趋势,且在1 mmol·L−1时达到最大响应。以甲醇-水系统做流动相时,HFPO-TA色谱峰分叉(图2 b),添加乙酸铵缓冲盐后,峰形得到明显改善(图2 c)。综合考虑峰面积和色谱峰形的基础上,本研究选择甲醇-乙酸铵(1 mmol·L−1)水溶液作为流动相。
2.1.2 质谱条件优化
因目标分析物为羧酸及其衍生盐,电喷雾离子源正源模式(electrospray ionization source,ESI)难以将其质子化,因此本研究以ESI−模式扫描定性和定量离子对。借助针泵以30 μL·min−1的流速泵入1000 μg·L−1的标准工作溶液进行m/z 200—1000 ESI一级质谱扫描,结果发现PFOA和HFPO-TA电离后失去羧基上的氢原子,主要以[M-H]−分子离子的相对丰度较高,HFPO-DA生成[M-44-H]−分子离子,推断原因为发生中性丢失CO2[22, 26]。确定分子离子后,进行二级质谱扫描,选取相对丰度较强的碎片离子作为定量离子,次强的作为定性离子。最后,以MRM模式采集数据,进一步优化锥孔电压、碰撞能量等参数,具体参数见表1。
表 1 多重反应监测条件Table 1. Multiple response monitoring conditions化合物Compound 分子量Molecular weight 母离子Parent ion(m/z) 子离子Product ion(m/z) 碰撞能量/eVCollision energy 锥孔电压/VCon voltage PFOA 414.07 412.7 369*,169 13,26 −11,−11 HFPO-DA 347 285 185.1,169* 28,10 −3,−5 HFPO-TA 496.07 495 185*,119 15,76 −29,−34 注:*为定量离子(Quantification ion). 2.2 前处理方法的优化
固相萃取(solid-phase extraction,SPE)技术在食品、环境和生物样品分析中得到广泛应用,选择合适的固定相与流动相可以去除提取液中的绝大数干扰物质并洗脱回收目标分析物,获得较好的回收率并且尽最大可能保护分析仪器,但是SPE法存在操作复杂、耗时长、有机溶剂用量大和成本高等问题。因此d-SPE是一种潜在的替代方法。通过在提取上清液中添加一定质量的吸附材料,能够极大的改善SPE法的缺陷。目前常用的吸附材料有PSA、C18、GCB、碳十八键合锆胶等。PSA可以吸附提取液中碳水化合物、有机酸和少量色素等极性杂质,是一种弱阴离子交换剂[36],C18可降低提取液中脂肪等非极性物质的含量[37],GCB对提取液中色素和甾醇类物质具有较好的去除效果[21]。在已有的文献报道中分别选用PSA、C18和GCB 3种吸附剂单一或不同配比开展动物源性食品中传统直链全氟化合物的净化[20, 22-26, 38]。
基于动物基质提取液外观色泽和潜在杂质,本研究选择100 mg PSA+80 mg C18+30 mg GCB组成的混合物作为吸附剂,结果显示净化效果较好,如图3所示上清液呈无色透明态,氮气浓缩至干后无油脂等析出,且目标分析物的回收率满足试验要求。因此,本研究选用该组合作为吸附剂用于样品的净化。
2.3 方法学考察
2.3.1 线性范围、灵敏度和基质效应
该方法的线性相关性、LODs、LOQs和基质效应结果如表2所示。3种目标分析物在5—500 μg·L−1的线性范围内,质量浓度与对应定量离子峰面积呈现出较好的线性关系,相关性系数均大于0.99。PFOA和HFPO-DA在所选取的5种器官中|ME|为28.9%—80.7%,表现为强基质效应。HFPO-TA在不同器官中基质效应具有较大差异,大脑、肾脏和心脏样品的|ME| < 20%,基质效应可忽略不计;在肺和肝脏样品中表现出中等至较强的基质效应。因此在后续试验中可采用基质匹配标准溶液外标法或者同位素标记内标法定量,进而排除基质效应。3种目标分析物在不同基质中的LODs为0.016—0.077 μg·kg−1与之对应的LOQs为5.35×10−4—2.55×10−3 ng。
表 2 目标分析物的线性关系、基质效应和灵敏度Table 2. The linearity, matrix effect, LOD, and LOQ in different matrices of target analytes化合物Compound 基质Matrix 线性范围/(μg·L−1)Linear range 线性回归方程Linear regression equation 相关系数R2 基质效应Matrix effect 检出限/(μg·kg−1)LOD 定量限/ngLOQ HFPO-TA 溶剂 5—500 y = 1127167.9x−9339.7 0.9985 肺 y = 1513689.3x+64976.9 0.9994 34.3 0.033 1.11×10−3 肝脏 y = 1948167.8x + 4061.1 0.9939 72.8 0.032 1.06 ×10−3 大脑 y = 1141739.2x - 1827.9 0.9983 1.29 0.059 1.95 × 10−3 肾脏 y = 936791.55x - 12930.8 0.9924 −16.9 0.067 2.23 × 10−3 心脏 y = 1176418.9x + 11229.8 0.9981 4.40 0.077 2.55 × 10−3 HFPO-DA 溶剂 5—500 y = 73531199.76x−412121.8 0.9997 肺 y = 14208329.7x+203490.4 0.9959 −80.7 0.070 2.33 × 10−3 肝脏 y = 14903379.9x+103425.3 0.9987 −79.7 0.072 2.41 × 10−3 大脑 y = 26824971.1x - 267020.2 0.9904 −63.5 0.032 1.05 × 10−3 肾脏 y = 18930496.41x + 86476.4 0.9996 −74.3 0.035 1.18 × 10−3 心脏 y = 31251384.1x - 62905.3 0.9997 −57.5 0.037 1.25 × 10−3 PFOA 溶剂 5—500 y = 38001300.6x - 1277.5 0.9998 肺 y = 15354735.3x+131561.6 0.9987 −59.6 0.026 8.79 × 10−4 肝脏 y = 15871133.5x + 148426.0 0.9989 −58.2 0.016 5.35 × 10−4 大脑 y = 20042969.4x + 186424.7 0.9946 −47.3 0.023 7.51 × 10−4 肾脏 y = 21453758.7x + 198,880.2 0.9993 −43.5 0.016 5.49 × 10−4 心脏 y = 27017643.3x - 8176.8 0.9980 −28.9 0.020 6.81 × 10−4 2.3.2 方法的准确度、精密度
通过加标回收率试验验证该方法的准确度和精密度。3种目标分析物在5、10、100 μg·kg−1的3个添加水平下的平均回收率为64.8%—120%,与之对应的RSD分别为:4.1%—20%、0.75%—22.4%、0.6%—14.6%(表3)。该方法的回收率、精密度和灵敏度均能满足GB/T 27417—2017[39]中化学分析方法的要求。
表 3 3种目标分析物在小鼠器官中的回收率和相对标准偏差Table 3. The mean recovery and RSD of 3 target analytes in different matrices基质Matrix 添加浓度/(μg·kg−1) Add Concentration HFPO-TA HFPO-DA PFOA R1 R2 R3 均值% RSD/% R1 R2 R3 均值/% RSD/% R1 R2 R3 均值/% RSD/% 肝脏 5 72.3 73.4 66.8 70.8 5 108.8 95.8 89.5 98 10 98.4 125.6 85.1 103 20 10 84.1 70.3 80.4 78.3 9.1 83 82.1 83.3 82.8 0.75 64.7 63.1 66.5 64.8 2.6 100 87.4 85.4 84.2 85.7 1.9 96.1 72.3 80.5 82.9 14.6 86.2 78 78.6 80.9 5.6 肺 5 112.7 87.9 101.3 100.6 12.3 101.6 84.9 77.8 88.1 13.9 73.5 73.7 83.4 76.9 7.3 10 105 108.9 100.8 104.9 3.86 86 109.1 77 90.7 18.3 84.4 82.4 80.9 82.6 2.1 100 108.7 94.6 91.8 98.4 9.2 95 85.2 83.5 87.9 7.1 98.3 92 80.9 90.4 9.7 脑 5 88.9 80.4 79 82.8 6.5 79.1 76.6 71.3 75.7 5.3 99 84 88 90.3 8.6 10 104.2 75.7 95.9 91.9 15.9 86.2 93.4 86.9 88.8 4.5 87.1 83.8 84.2 85 2.1 100 120.0 120.0 119.4 120.0 0.7 93.2 84.7 85.7 87.9 5.3 100.4 80.6 100.8 93.9 12.3 肾 5 94.3 111.4 82.8 96.2 14.9 105.4 75 78.5 86.3 19.3 103.2 95.4 98 98.9 4.1 10 83.2 84.1 120.9 96.1 22.4 116.2 80.2 81.6 92.7 22 91.3 81.5 85.9 86.2 5.7 100 97.2 104.5 92.2 97.9 6.3 102.2 81.8 88.8 90.9 11.3 92.9 79.9 84.8 85.9 7.6 心脏 5 107.5 91.4 87.7 95.5 11 75.7 80 94.5 83.4 11.8 89.4 88.5 105.3 94.4 10 10 121.6 89.6 85.2 99.8 20 112.6 106 103.2 107.3 4.5 89.3 80.8 80.5 83.5 5.9 100 103.6 79.9 97 93.5 13 90.6 95.8 90.8 92.4 3.2 81.5 82.4 81.5 81.8 0.6 2.4 实际样品分析
经口暴露全氟化合物的小鼠器官样品冷冻干燥粉碎后,经所建立方法检测,各器官中目标全氟化合物浓度结果如图4所示。 3种目标物在不同器官中富集趋势有较大差异,在5种器官中总累积浓度依次为:肝脏((3970.6 ± 645.3) μg·kg−1)>肾脏((2619.2 ± 787.5) μg·kg−1)>肺((2027.1 ± 138.2 )μg·kg−1)>心脏((1070.1 ± 55.6 )μg·kg−1)>大脑((383.7 ± 30.1) μg·kg−1)。3种目标物的生物富集趋势也有明显差异,在各个器官中HFPO-DA的累积浓度显著(P<0.05)低于PFOA和HFPO-TA。例如肝脏中HFPO-TA和PFOA的累积浓度分别为(1726.7 ± 205.7 )μg·kg−1和(1676.1 ± 338.2) μg·kg−1,而HFPO-DA的浓度为 (566.9 ± 101.4) μg·kg−1。据报道在10 μg·mL−1的暴露条件下,人胚胎滋养层细胞模型中,PFOA的细胞内积累浓度是HFPO-DA的5.8倍[40]。此外在小鼠肝脏中HFPO-TA的累积浓度也略高于PFOA,为其浓度的1.1倍。有研究表明,HFPO-TA与人肝脏脂肪酸结合蛋白的结合潜力大于PFOA和HFPO-DA[41]。因此在肝脏中HFPO-TA相比较于PFOA和HFPO-DA具有较强的生物富集潜力。
3. 结论(Conclusion)
本研究通过优化样品前处理方法和仪器分析条件,建立了QuEChERs-UPLC-MS/MS同时测定小鼠器官中新型全氟化合物的方法。该方法操作简单,环境友好,经济适用性高,线性相关性大于0.99,在不同小鼠器官基质中检出限为0.016—0.077 μg·kg−1和定量限为5.35×10−4—2.55×10−3 ng。将建立方法应用于污染暴露的小鼠样品,3种目标分析物在5种器官中具有检出,HFPO-TA在肝脏中的累积浓度与PFOA接近,是HFPO-DA累积浓度的3.4倍。本研究为监测生物体内新型全氟化合物建立了有效的检测方法,有助于新型全氟化合物环境归趋和生物有效性研究。
-
表 1 采样点信息
Table 1. Sample sites information
采样点 Sample sites 环境监测站Environmental monitoring station 大全Daquan 经度 86.0576 E 86.0957 E 纬度 44.3133 N 44.4220 N 高度/m 14.0 13.0 功能区 城区 工业区 有效样品/个 60 61 与国控站距离 阳光学校西1.6 km 阳光学校北12.0 km 表 2 采样期污染天数
Table 2. The number of pollution days in sampling period
优 Excellent 良 Good 轻度 Light 中度 Medium 重度 Heavy 严重 Severe 污染天数/d 0 9 8 12 24 9 PM2.5为首要污染物天数/d 0 8 8 12 24 9 表 3 采样点元素浓度
Table 3. Elements concentration of 2 sample sites
元素Elements 城区/(ng·mc3)Urban 工业区/(ng·m−3)Industrial 比值Ratio 广州市[30]/ (ng·m−3)Guangzhou 天津市[31]/ (ng·m−3)Tianjin 南昌市[32]/ (ng·m−3)Nanchang Be 0.2 0.3 0.6 — — — Na 1779.0 1342.0 1.3 1210.0 1925.0 — Mg 201.7 168.4 1.2 390.0 1188.0 537.0 Al 448.4 416.7 1.1 1190.0 1377.0 740.0 K 520.1 436.2 1.2 2480.0 4081.0 734.0 Ca 838.4 840.9 1.0 1390.0 5278.0 1207.0 V 1.9 4.9 0.4 — 4.9 9.0 Cr 4.3 5.6 0.8 13.5 176.7 20.0 Mn 13.9 7.6 1.8 83.4 190.9 43.0 Fe 453.9 263.4 1.7 1220.0 4357.0 571.0 Co 0.3 0.4 0.8 — 1.2 4.0 Ni 1.3 1.8 0.7 8.6 87.9 150 Cu 10.0 4.3 2.4 112.0 239.1 19.0 Zn 39.3 32.9 1.2 670.0 945.1 279.0 As 5.5 4.3 1.3 35.1 43.4 10.0 Se 0.3 0.3 1.1 — — — Mo 0.4 0.6 0.7 — — — Ag 0.1 0.1 0.4 — — — Cd 0.5 0.5 1.0 6.1 10.2 5.0 Ba 6.1 4.7 1.3 — 51.2 325.0 Tl 0.2 0.3 0.7 — — — Pb 27.2 19.9 1.4 190.0 541.1 106.0 Th 0.1 0.2 0.3 — — — U 0.1 0.3 0.3 — — — 总和 4353.0 3557.0 24.5 8999.0 20498.0 4759.0 备注:“—”表示未检测出. 表 4 石河子市PM2.5中24种元素EF值
Table 4. Enrichment factors of 24 elements in PM2.5 of Shihezi city
序号Serial number 元素Elements PM2.5富集因子Enrichment factors of PM2.5 A层土元素 Element of layer A soil 郴州市[38]EF值Enrichmentfactors of Chenzhou City 温州市[39]EF值Enrichmentfactors ofWenzhou City 城区Urban 工业区Industrial 质量分数(×106)/(g·g−1)Mass percentage 1 Be 1.1 2.1 187.7 — — 2 Na 14765.3 11986.5 151.0 — 22.2 3 Mg 2840.9 2551.4 89.0 — 3.0 4 Al 1.0 1.0 562.0 0.02 — 5 K 3325.4 3001.5 196.0 — 11.6 6 Ca 3704.0 3998.0 283.7 — 20.1 7 V 0.3 0.9 7293.3 45.7 0.4 8 Cr 1.0 1.4 5510.0 106.8 112.5 9 Mn 0.3 0.2 63266.7 14.0 7.7 10 Fe 2078.6 1297.9 273.7 0.6 3.7 11 Co 0.3 0.4 1250.0 — 5.0 12 Ni 0.6 1.0 2496.7 66.8 38.7 13 Cu 5.9 2.7 2136.7 370.0 227.5 14 Zn 7.3 6.6 6753.3 155.8 509.7 15 As 7.6 6.4 910.0 521.1 301.0 16 Se 17.5 16.8 20.0 — — 17 Mo 2.4 3.8 206.7 — — 18 Ag 5.5 15.6 11.7 1599.2 — 19 Cd 61.5 64.7 9.5 10880.9 1691.0 20 Ba 0.2 0.1 50133.3 3.3 — 21 Tl 5.4 8.0 54.7 — — 22 Pb 15.9 12.6 2136.7 262.4 176.8 23 Th 0.1 0.3 1030.7 — — 24 U 0.3 1.3 261.7 — — 备注:“—”表示未检测出. -
[1] 元雪婷, 杨静. 乌昌石区域耗煤行业排放特征及对空气质量的影响 [J]. 工业安全与环保, 2020, 46(9): 60-64. doi: 10.3969/j.issn.1001-425X.2020.09.016 YUAN X T, YANG J. Emission characteristics of the coal-consumption industries in Wuchangshi area and its impact on air quality [J]. Industrial Safety and Environmental Protection, 2020, 46(9): 60-64(in Chinese). doi: 10.3969/j.issn.1001-425X.2020.09.016
[2] 闵月. 天山北坡乌昌石地区污染天气过程的气象特征研究[D]. 兰州: 兰州大学, 2020. MIN Y. The Meteorological characteristics of air pollution in northern slope of Tianshan Mountains[D]. Lanzhou, Lanzhou University, 2020(in Chinese).
[3] 王晴, 王宝庆, 蔡宁宁, 等. 乌昌石区域化石燃料固定燃烧点源大气污染物排放清单及时空分布 [J]. 环境污染与防治, 2020, 42(6): 712-716. WANG Q, WANG B Q, CAI N N, et al. Emission inventory of atmospheric pollutants from fossil fuel fixed combustion point source and its temporal and spatial distribution in Wuchangshi area [J]. Environmental Pollution & Control, 2020, 42(6): 712-716(in Chinese).
[4] 张斌, 吕宝磊, 王馨陆, 等. 利用集合深度学习方法订正空气质量数值预报结果: 以新疆乌昌石城市群为例 [J]. 北京大学学报(自然科学版), 2020, 56(5): 931-938. ZHANG B, LÜ B L, WANG X L, et al. Improving air quality forecast accuracy in Urumqi-Changji-Shihezi region using an ensemble deep learning approach [J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2020, 56(5): 931-938(in Chinese).
[5] HAN X, LIU Y Q, GAO H, et al. Forecasting PM2.5 induced male lung cancer morbidity in China using satellite retrieved PM2.5 and spatial analysis [J]. Science of the Total Environment, 2017, 607/608: 1009-1017. doi: 10.1016/j.scitotenv.2017.07.061 [6] BENMERAD M, SLAMA R, BOTTURI K, et al. Chronic effects of air pollution on lung function after lung transplantation in the Systems prediction of Chronic Lung Allograft Dysfunction (SysCLAD) study [J]. European Respiratory Journal, 2017, 49(1): 1600206. doi: 10.1183/13993003.00206-2016 [7] ZHAI Y B, LIU X T, CHEN H M, et al. Source identification and potential ecological risk assessment of heavy metals in PM2.5 from Changsha [J]. Science of the Total Environment, 2014, 493: 109-115. doi: 10.1016/j.scitotenv.2014.05.106 [8] 王淑兰, 柴发合, 杨天行. 北京市不同尺度大气颗粒物元素组成的特征分析 [J]. 环境科学研究, 2002, 15(4): 10-12. doi: 10.3321/j.issn:1001-6929.2002.04.004 WANG S L, CHAI F H, YANG T X. Characteristics analysis of elements contained in air suspended particles with different sizes in Beijing [J]. Research of Environmental Sciences, 2002, 15(4): 10-12(in Chinese). doi: 10.3321/j.issn:1001-6929.2002.04.004
[9] 胡鸣, 张懿华, 赵倩彪. 上海市冬季PM2.5无机元素污染特征及来源分析 [J]. 环境科学学报, 2015, 35(7): 1993-1999. HU M, ZHANG Y H, ZHAO Q B. Characteristics and sources of inorganic elements in PM2.5 during wintertime in Shanghai [J]. Acta Scientiae Circumstantiae, 2015, 35(7): 1993-1999(in Chinese).
[10] 田莎莎, 张显, 卞思思, 等. 沈阳市PM2.5污染组分特征及其来源解析 [J]. 中国环境科学, 2019, 39(2): 487-496. doi: 10.3969/j.issn.1000-6923.2019.02.006 TIAN S S, ZHANG X, BIAN S S, et al. Characteristics of PM2.5 pollution components and their sources in Shenyang [J]. China Environmental Science, 2019, 39(2): 487-496(in Chinese). doi: 10.3969/j.issn.1000-6923.2019.02.006
[11] 赵金平, 谭吉华, 毕新慧, 等. 广州市灰霾期间大气颗粒物中无机元素的质量浓度 [J]. 环境化学, 2008, 27(3): 322-326. doi: 10.3321/j.issn:0254-6108.2008.03.010 ZHAO J P, TAN J H, BI X H, et al. The mass concentrations of inorganic elements in atmospheric particles during haze period in Guangzhou [J]. Environmental Chemistry, 2008, 27(3): 322-326(in Chinese). doi: 10.3321/j.issn:0254-6108.2008.03.010
[12] 李友平, 刘慧芳, 周洪, 等. 成都市PM2.5中有毒重金属污染特征及健康风险评价 [J]. 中国环境科学, 2015, 35(7): 2225-2232. doi: 10.3969/j.issn.1000-6923.2015.07.052 LI Y P, LIU H F, ZHOU H, et al. Contamination characteristics and health risk assessment of toxic heavy metals in PM2.5 in Chengdu [J]. China Environmental Science, 2015, 35(7): 2225-2232(in Chinese). doi: 10.3969/j.issn.1000-6923.2015.07.052
[13] 纪元, 康宏, 李刚. 乌鲁木齐市冬季重污染天气下PM2.5中重金属污染特征及来源解析 [J]. 干旱环境监测, 2016, 30(3): 127-131. doi: 10.3969/j.issn.1007-1504.2016.03.007 JI Y, KANG H, LI G. The heavy metal pollution characteristics and source apportionment of PM2.5 under the heavy pollution of Urumqi winter weather [J]. Arid Environmental Monitoring, 2016, 30(3): 127-131(in Chinese). doi: 10.3969/j.issn.1007-1504.2016.03.007
[14] 张洛红, 范芳, 蒋炜炜, 等. 珠三角地区大气PM2.5中重金属污染水平及健康风险评价 [J]. 环境科学学报, 2017, 37(1): 370-380. ZHANG L H, FAN F, JIANG W W, et al. Concentrations and health risk assessment of heavy metals in atmospheric PM2.5 in the Pearl River Delta Region [J]. Acta Scientiae Circumstantiae, 2017, 37(1): 370-380(in Chinese).
[15] 王琼, 董小艳, 杨璐璐, 等. 基于北京市大气PM2.5中9种元素的环境健康风险评价 [J]. 环境卫生学杂志, 2018, 8(3): 197-203. WANG Q, DONG X Y, YANG L L, et al. Environment health risk assessment on 9 elements in PM2.5 in Beijing [J]. Journal of Environmental Hygiene, 2018, 8(3): 197-203(in Chinese).
[16] 任慧清, 鲁建江, 宁建英, 等. 石河子市PM2.5中重金属污染及健康风险评价 [J]. 环境化学, 2020, 39(6): 1716-1725. doi: 10.7524/j.issn.0254-6108.2019041004 REN H Q, LU J J, NING J Y, et al. Pollution and health risk assessment of heavy metals in PM2.5 of Shihezi City [J]. Environmental Chemistry, 2020, 39(6): 1716-1725(in Chinese). doi: 10.7524/j.issn.0254-6108.2019041004
[17] 李瑶, 刘琳, 胡潭高, 等. 石河子市PM2.5浓度的遥感反演研究 [J]. 环境科学与管理, 2018, 43(1): 138-142. doi: 10.3969/j.issn.1673-1212.2018.01.031 LI Y, LIU L, HU T G, et al. Remote sensing estimation model of PM2.5 mass concentration in Shihezi city [J]. Environmental Science and Management, 2018, 43(1): 138-142(in Chinese). doi: 10.3969/j.issn.1673-1212.2018.01.031
[18] 丁俊男, 王帅, 王瑞斌, 等. 河南省典型城市PM2.5无机元素污染特征及来源分析 [J]. 中国环境监测, 2017, 33(6): 25-32. DING J N, WANG S, WANG R B, et al. Characteristics and sources analysis of inorganic elements in PM2.5 in typical cities of Henan Province [J]. Environmental Monitoring in China, 2017, 33(6): 25-32(in Chinese).
[19] 张晶晶, 张清花. 昌吉市采暖期和非采暖期PM2.5和PM10污染特征分析 [J]. 干旱环境监测, 2018, 32(1): 24-28. doi: 10.3969/j.issn.1007-1504.2018.01.005 ZHANG J J, ZHANG Q H. Pollution characteristics of PM2.5 and PM10 in heating and non-heating season in Changji city [J]. Arid Environmental Monitoring, 2018, 32(1): 24-28(in Chinese). doi: 10.3969/j.issn.1007-1504.2018.01.005
[20] TAIWO A M, HARRISON R M, SHI Z B. A review of receptor modelling of industrially emitted particulate matter [J]. Atmospheric Environment, 2014, 97: 109-120. doi: 10.1016/j.atmosenv.2014.07.051 [21] XU L L, YU Y K, YU J S, et al. Spatial distribution and sources identification of elements in PM2.5 among the coastal city group in the Western Taiwan Strait region, China [J]. Science of the Total Environment, 2013, 442: 77-85. doi: 10.1016/j.scitotenv.2012.10.045 [22] 乔宝文, 刘子锐, 胡波, 等. 北京冬季PM2.5中金属元素浓度特征和来源分析 [J]. 环境科学, 2017, 38(3): 876-883. QIAO B W, LIU Z R, HU B, et al. Concentration characteristics and sources of trace metals in PM2.5 during wintertime in Beijing [J]. Environmental Science, 2017, 38(3): 876-883(in Chinese).
[23] KYLLÖNEN K, KARLSSON V, RUOHO-AIROLA T. Trace element deposition and trends during a ten year period in Finland [J]. Science of the Total Environment, 2009, 407(7): 2260-2269. doi: 10.1016/j.scitotenv.2008.11.045 [24] 环境保护部. 中华人民共和国环保行业标准: 环境空气颗粒物(PM2.5)手工监测方法 HJ 656—2013[S]. 北京: 中国环境科学出版社, 2013. Ministry of Environmental Protection of the People's Republic of China. Environmental Protection Standard of the People's Republic of China: Technical Specifications for gravimetric measurement methods for PM2.5 in ambient air. HJ 656—2013[S]. Beijing: China Environment Science Press, 2013(in Chinese).
[25] 杨佳美, 戴启立, 刘保双, 等. 关中地区背景点位环境空气PM2.5来源解析与多模型结果对比 [J]. 环境科学研究, 2017, 30(2): 184-192. YANG J M, DAI Q L, LIU B S, et al. Source apportionment of ambient PM2.5 at background sites in Guanzhong area, China: Comparison of results obtained by multiple models [J]. Research of Environmental Sciences, 2017, 30(2): 184-192(in Chinese).
[26] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. 中华人民共和国国家标准: 环境空气质量标准 GB 3095—2012[S]. 北京: 中国环境科学出版社, 2016. General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China, Standardization Administration of the People's Republic of China. National Standard (Mandatory) of the People's Republic of China: Ambient air quality standard. GB 3095—2012[S]. Beijing: China Environment Science Press, 2016(in Chinese).
[27] 王伟平, 苏高利, 杨海鹏. 城北高架点源对西湖风景区影响的研究 [J]. 气象, 2002, 28(1): 13-17. doi: 10.3969/j.issn.1000-0526.2002.01.003 WANG W P, SU G L, YANG H P. A study on influence of high elevation point source of northern Hangzhou on the scenic zone of west lake [J]. Meteorological Monthly, 2002, 28(1): 13-17(in Chinese). doi: 10.3969/j.issn.1000-0526.2002.01.003
[28] 陈瑞. 城市高架点源对空气质量的影响分析 [J]. 浙江树人大学学报, 2003, 3(5): 77-79. doi: 10.3969/j.issn.1671-2714.2003.05.022 CHEN R. Effects of high chimney emission on air quality in the urban area [J]. Journal of Zhejiang Shuren University, 2003, 3(5): 77-79(in Chinese). doi: 10.3969/j.issn.1671-2714.2003.05.022
[29] 赵强. 昌吉市大气颗粒物污染特征及来源解析[D]. 乌鲁木齐: 新疆农业大学, 2018. ZHAO Q. Pollution characteristics and source apportionment of atmospheric particulate matter in Changji City[D]. Urumqi: Xinjiang Agricultural University, 2018(in Chinese).
[30] 符小晴, 彭晓武, 王钰钰, 等. 广州市大气PM2.5中元素特征及重金属健康风险评价 [J]. 环境与健康杂志, 2018, 35(2): 154-158. FU X Q, PENG X W, WANG Y Y, et al. Characteristic of elements in PM2.5 and health risk assessment of heavy metals in Guangzhou [J]. Journal of Environment and Health, 2018, 35(2): 154-158(in Chinese).
[31] 董海燕, 古金霞, 姜伟, 等. 天津市颗粒物中元素化学特征及来源 [J]. 环境监测管理与技术, 2012, 24(1): 25-28. doi: 10.3969/j.issn.1006-2009.2012.01.007 DONG H Y, GU J X, JIANG W, et al. Character and source analysis of chemical element in particulate matters in Tianjin [J]. The Administration and Technique of Environmental Monitoring, 2012, 24(1): 25-28(in Chinese). doi: 10.3969/j.issn.1006-2009.2012.01.007
[32] 樊孝俊, 徐义邦, 赵阳. 南昌市秋季大气PM2.5中金属元素污染及生态风险评价 [J]. 中国环境监测, 2016, 32(2): 26-30. doi: 10.3969/j.issn.1002-6002.2016.02.004 FAN X J, XU Y B, ZHAO Y. The pollution characteristics and potential ecological risk of heavy metals in PM2.5 in autumn in Nanchang [J]. Environmental Monitoring in China, 2016, 32(2): 26-30(in Chinese). doi: 10.3969/j.issn.1002-6002.2016.02.004
[33] 王永慧, 刘芃岩, 于泊蕖, 等. 保定市日间、夜间大气PM2.5中无机组分的特征及来源分析 [J]. 环境化学, 2017, 36(9): 1941-1948. doi: 10.7524/j.issn.0254-6108.2016122201 WANG Y H, LIU P Y, YU B Q, et al. Characteristics and source analysis of inorganic components in PM2.5 samples collected during daytime and night in Baoding City [J]. Environmental Chemistry, 2017, 36(9): 1941-1948(in Chinese). doi: 10.7524/j.issn.0254-6108.2016122201
[34] 滕彦国, 庹先国, 倪师军, 等. 攀枝花工矿区土壤重金属人为污染的富集因子分析 [J]. 土壤与环境, 2002, 11(1): 13-16. TENG Y G, TUO X G, NI S J, et al. Application of an enrichment factor in determining anthropogenical pollution ofheavy metal in topsoil [J]. Soil and Environmental Sciences, 2002, 11(1): 13-16(in Chinese).
[35] 姬亚芹, 朱坦, 冯银厂, 等. 用富集因子法评价我国城市土壤风沙尘元素的污染 [J]. 南开大学学报(自然科学版), 2006, 39(2): 94-99. JI Y Q, ZHU T, FENG Y C, et al. Application of the enrichment factor to analyze the pollution of elements in soil dust in China [J]. Acta Scientiarum Naturalium Universitatis Nankaiensis, 2006, 39(2): 94-99(in Chinese).
[36] 中国土壤环境背景值研究[Z]. 北京市, 中国环境监测总站, 2001.01. 01. Research on the environmental background of soil in China[Z]. Beijing, Environmental Monitoring of China, 2001.01. 01(in Chinese).
[37] 赵晓亮, 岳阳霞, 许端平, 等. 阜新市秋冬季节PM2.5中无机元素污染特征及来源 [J]. 中国环境科学, 2020, 40(10): 4247-4258. doi: 10.3969/j.issn.1000-6923.2020.10.007 ZHAO X L, YUE Y X, XU D P, et al. The pollution characteristics and source analysis of inorganic elements in PM2.5 during autumn and winter in Fuxin [J]. China Environmental Science, 2020, 40(10): 4247-4258(in Chinese). doi: 10.3969/j.issn.1000-6923.2020.10.007
[38] 杨麒, 傅致严, 刘湛, 等. 郴州市大气PM2.5中无机元素污染特征及来源分析 [J]. 湖南大学学报(自然科学版), 2019, 46(6): 133-140. YANG Q, FU Z Y, LIU Z, et al. Characteristics and sources of inorganic elements in atmospheric PM2.5 at Chenzhou city [J]. Journal of Hunan University (Natural Sciences), 2019, 46(6): 133-140(in Chinese).
[39] 郑元铸, 葛琳琳, 郑旭军, 等. 温州市区PM2.5无机元素污染特征及来源分析 [J]. 环境化学, 2017, 36(1): 84-91. doi: 10.7524/j.issn.0254-6108.2017.01.2016051802 ZHENG Y Z, GE L L, ZHENG X J, et al. Characteristics and source apportionment of inorganic elements in PM2.5 in Wenzhou, Zhejiang [J]. Environmental Chemistry, 2017, 36(1): 84-91(in Chinese). doi: 10.7524/j.issn.0254-6108.2017.01.2016051802
[40] TIAN H Z, WANG Y, XUE Z G, et al. Trend and characteristics of atmospheric emissions of Hg, As, and Se from coal combustion in China, 1980–2007 [J]. Atmospheric Chemistry and Physics, 2010, 10(23): 11905-11919. doi: 10.5194/acp-10-11905-2010 [41] ZHANG W J, SUN Y L, ZHUANG G S, et al. Characteristics and seasonal variations of PM2.5, PM10, and TSP aerosol in Beijing [J]. Biomedical and Environmental Sciences, 2006, 19(6): 461-468. [42] 张靳杰. 武汉市机动车尾气VOCs和颗粒物排放特征研究[D]. 武汉: 华中科技大学, 2019. ZHANG J J. Study on the characteristics of volatile organic compounds and particulate matter from on-use vehicles in Wuhan[D]. Wuhan: Huazhong University of Science and Technology, 2019(in Chinese).
[43] 郭海全, 郝俊杰, 李天刚, 等. 河北平原土壤重金属人为污染的富集因子分析 [J]. 生态环境学报, 2010, 19(4): 786-791. doi: 10.3969/j.issn.1674-5906.2010.04.007 GUO H Q, HAO J J, LI T G, et al. Application of an enrichment factor in determining anthropogenic pollution of heavy metal in topsoil in Hebei plain [J]. Ecology and Environmental Sciences, 2010, 19(4): 786-791(in Chinese). doi: 10.3969/j.issn.1674-5906.2010.04.007
[44] 陈翠华, 倪师军, 何彬彬, 等. 江西德兴矿区土壤重金属污染的富集因子分析 [J]. 金属矿山, 2005(12): 57-60. doi: 10.3321/j.issn:1001-1250.2005.12.017 CHEN C H, NI S J, HE B B, et al. Enrichment factor analysis of soil pollution by heavy metals in Dexing mining area, Jiangxi Province [J]. Metal Mine, 2005(12): 57-60(in Chinese). doi: 10.3321/j.issn:1001-1250.2005.12.017
-





 下载:
下载: