-
室内降尘是诸多有毒污染物质的运载体和反应床。其中所携带重金属可以通过手-口摄食、呼吸摄入、皮肤接触等途径进入人体并在脂肪和内脏组织中积累,可能引发癌症、皮肤病、心血管疾病和糖尿病等健康损伤[1-3]。手-口摄食是室内降尘的人体暴露主要途径[4],因此对经胃肠道的降尘中重金属的健康风险评价尤为重要。目前降尘中重金属健康风险评价的研究多基于总量分析,即通过测定降尘中重金属的总暴露剂量以评价其人体健康风险。然而,降尘进入胃肠道环境后,其中的重金属并不能完全溶出,从而被人体吸收并造成危害。仅通过分析重金属的总量,可能会导致降尘中重金属的人体健康风险被高估。因此,需考虑重金属的生物有效性(bioavailability),从而更加真实、准确地评估室内降尘中重金属的人体健康风险[5]。
重金属的生物有效性测定常需开展动物实验,然而动物实验多存在费用高、周期长、重复性差等问题,同时也容易引起伦理方面的争议,限制了其广泛应用[6-7]。因此,目前普遍采用体外提取的方法测定重金属的生物可给性(bioaccessibility)。传统的体外提取方法众多,主要包括单步溶剂提取法、连续提取法和体外胃肠道模拟消化法。单步溶剂提取法的提取剂(如CaCl2和EDTA等)成本较低,操作简便,但试剂用量需要针对不同情况进行调整,提取量与实际生物可给性部分只存在统计学关系[8]。连续提取法(如Tessier法和BCR法等)可分析降尘中重金属的赋存形态,有较好的重现性,在一定程度上能反映大气降尘中重金属的生物有效性。但其缺少统一的操作规范,且提取剂的选择性差,各提取态之间存在交叉影响[9]。体外胃肠道模拟消化法的分析结果通常与动物实验相关性高,是目前优选的生物可给性分析法。然而,不同体外胃肠道模拟消化法所采用的消化液组分、pH值和消化时间等参数各不相同,结果缺乏可比性,并且操作较为复杂[1]。
软饮料是人们日常生活中的常见饮品,具有廉价易得的优势。特别是已有研究表明软饮料可作为提取剂,用于土壤中重金属生物可给性的分析。Schnug等[10]发现,普通可乐作为提取剂可用于分析基于作物生长情况的农田土壤中重金属的生物可给性,其分析结果与EDTA提取法存在着较好的相关性。Lottermoser等[11]进一步以3种可乐作为提取剂,分析铀废矿土壤中铀的生物可给性,发现其分析结果与传统的DTPA和CaCl2提取法均具有较好的相关性。然而,目前尚未有基于软饮料提取法对降尘中重金属生物可给性分析的研究。
综上所述,本文对中国南北方的典型地区室内降尘开展如下研究:(1)采用HNO3-HCl消解法对室内降尘中重金属进行总量测定,并对其污染水平进行评价;(2)采用改进的BCR连续提取法分析室内降尘中重金属的形态;(3)采用一种典型的体外胃肠道模拟法(solubility bioavailability research consortium, SBRC)和磷酸单步提取法分析重金属生物可给性;(4)以软饮料(普通可乐和零度可乐)作为提取剂,构建新型室内降尘中重金属的生物可给性模型。
-
室内降尘样品采集于2019 年10—12 月,来自我国13 个城市的18 个室内环境,编号列为S1至S18。其中S1、S15和S17分别源自吉安、保定和西宁小区居民楼室内降尘,S2和S14分别源自吉安和北京办公区室内降尘,S3和S4源自井冈山不同县城的居民楼室内降尘,S13源自呼和浩特高校画室室内降尘,S5、S6、S9、S12、S16和S18分别源自金华、长沙、泉州、厦门、青岛和天津高校学生宿舍室内降尘,S7和S8源自泉州不同居民楼室内降尘,S10和S11源自昆明不同居民楼室内降尘。样品采用毛刷在天气晴朗干燥至少3 d后,选择无风的天气,在各采样点进行清扫采集。所有样品采集后密封保存,运输至实验室。室内降尘样品于室温条件下干燥,去除毛发、棉絮等大颗粒杂物后,过230 目(63 μm)的尼龙筛后用于后续分析。此外,室内降尘样品的pH和TOC分别采用pH计(美国奥利龙,pHS-29B型)和总有机碳分析仪(日本岛津,TOC-L)测定,其中pH平均值为8.07,TOC平均值为3.47%。
-
室内降尘中重金属总量分析采用HNO3-HCl双酸消解[12]。形态分析采用改进的BCR连续提取法[13],提取态分为F1(酸提取态)、F2(可还原态)、F3(可氧化态)和F4(残渣态)。重金属总量和形态分析样品均采用电感耦合等离子体质谱仪(ICP-MS,7800,美国Agilen公司)测定。总量分析过程中用土壤成分分析标准物质[GBW07407(GSS-7)]和[GBW07405(GSS-5)]进行全程质量监控,回收率在80%—120%之间。
-
室内降尘中重金属生物可给性分别采用SBRC胃相、磷酸、普通可乐和零度可乐等4种提取法进行分析。其中SBRC胃相提取法参考自文献[14]。磷酸单步溶剂法提取步骤为:称取0.1000 g室内降尘样品至15 mL离心管中,加入1 mL 0.3 mol·L−1磷酸溶液,在25 ℃,100 r·min−1条件下振荡2 h,提取液离心过滤后,用2% HNO3稀释至3 mL,保存于4 ℃待测。可乐提取法操作步骤为:称取0.5000 g室内降尘样品至15 mL离心管中,加入5 mL已超声去除气体的可乐(普通可乐和零度可乐),在25 ℃,100 r·min−1条件下振荡1 h,提取液离心后,取2 mL上清液加入40 μL的浓硝酸,消化12 h后,再加入0.2 mL 30% H2O2,放入水浴锅中75 ℃消化1 h,过滤后保存于4 ℃待测。所有提取液中重金属含量均采用ICP-MS(7800,美国Agilent公司)测定。
-
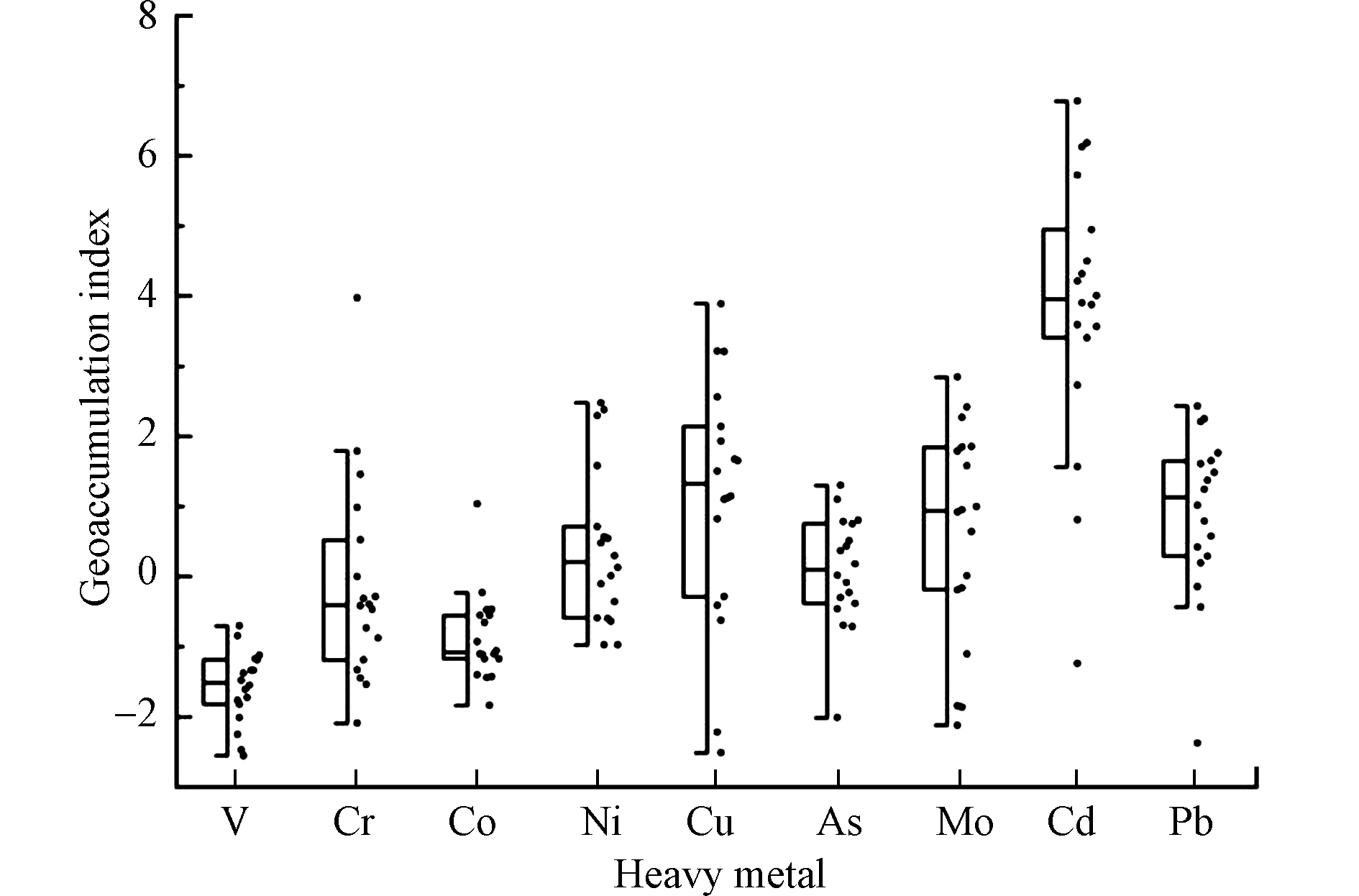
地累积指数(geoaccumulation index,Igeo)被广泛应用于评估降尘重金属污染研究[15]。其计算公式为:Igeo = log2(Ci/1.5Cn)。式中,Ci表示重金属在该样品的实测值,Cn表示重金属在该样品对应省(市)地区的地质背景值[16],1.5是考虑到造岩运动可能引起背景值波动而设定的常数。地累积指数根据指数大小分为7 个等级:Igeo ≤ 0表示无实际污染;0 < Igeo ≤ 1表示轻度污染;1 < Igeo ≤ 2表示中度污染;2 < Igeo ≤ 3表示中度至严重污染;3 < Igeo ≤ 4表示严重污染;4 < Igeo ≤ 5表示严重至极度污染;Igeo > 5表示极度污染。
-
室内降尘中重金属生物可给性计算公式为:BA(%) = (Ce × V) / (C × m) × 100%,式中,BA为重金属的生物可给性;Ce为提取液中某种重金属元素浓度,mg·L−1;V为提取液体积,L;C为室内降尘重金属总量,mg·kg−1;m为提取液中的室内降尘质量,kg。
-
采用SPSS 22.0对数据进行描述性统计和相关性分析,采用Origin 2019b进行作图。
-
室内降尘样品中重金属V、Cr、Co、Ni、Cu、As、Mo、Cd和Pb的总量平均值(表1)分别为44.92、76.06、10.05、51.88、108.73、19.94、5.62、3.49、106.09 mg·kg−1,分别为中国土壤(A层)背景值[16]的0.55、1.25、0.79、1.93、4.81、1.78、2.81、35.97、4.08 倍,表明除V和Co之外的7 种重金属元素均存在不同程度的富集。与此相一致,除V和Co以外,其余重金属的变异系数均超过50.0%,呈强变异性,说明其空间分布不均匀,受人为活动的影响较为强烈,可能存在局部污染源。此外,本研究室内降尘中重金属含量与之前研究中所报道的全国非工业区中重金属含量较为接近[17]。
通过地累积指数进一步对室内降尘污染情况进行分析(图1)。室内降尘各元素污染程度表现为Cd > Cu > Pb > Mo > Ni > As > 0 > Cr > Co > V。除As、Co和V之外,均存在不同程度的污染。其中Cr、Pb、Ni和Mo普遍为轻度污染,Cu为中度污染,Cd为严重污染。值得注意的是,元素Ni和Cr地积累指数较高的采样点多位于南方,这可能与南方城市具有较多的冶金和电镀产业排放有关[18]。此外,As污染程度较严重的降尘样品多来自北方采样点,这可能是由于北方具有更高的燃煤需求[19]。
-
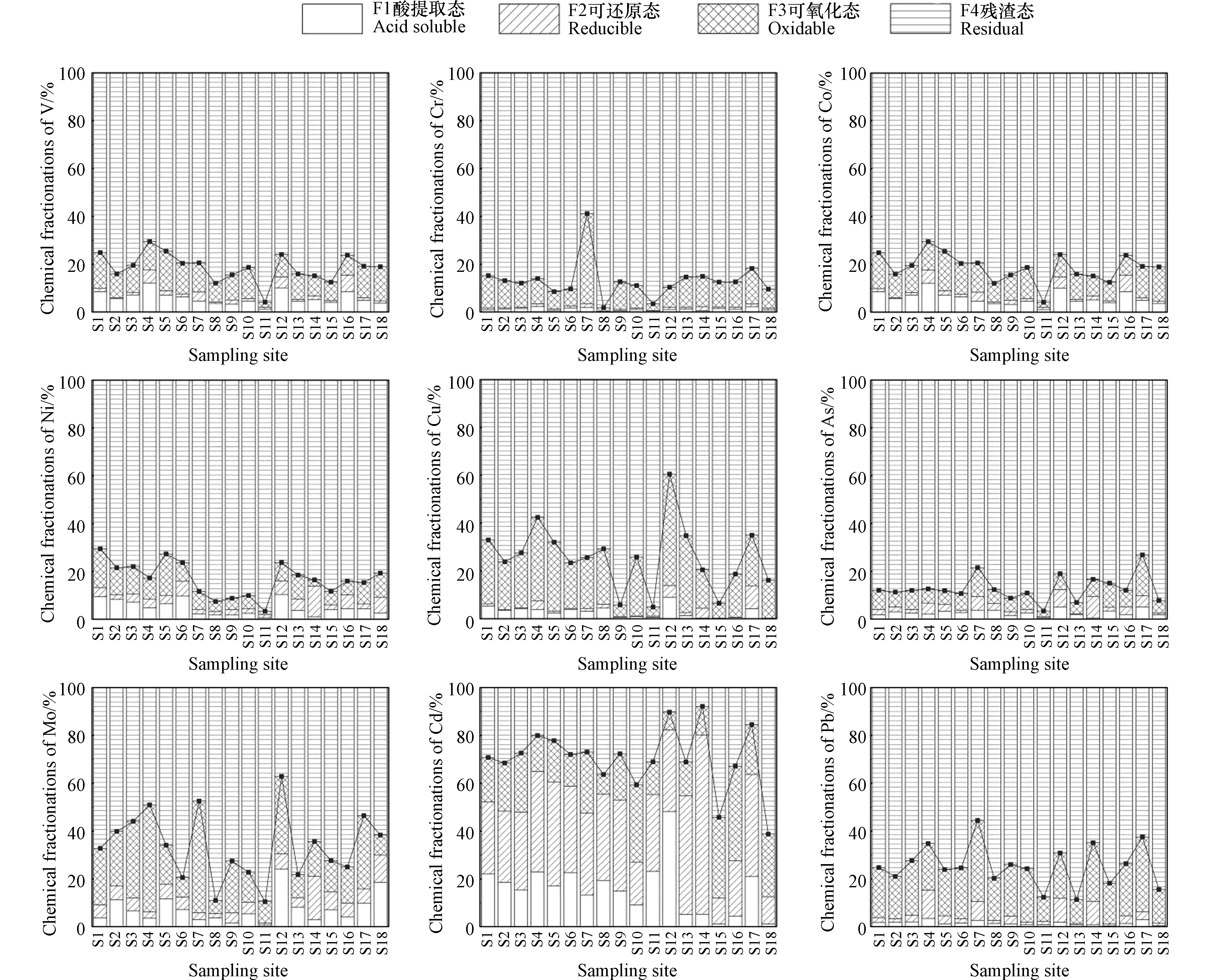
研究区域内不同重金属形态如图2所示。9 种重金属占比最高的形态均为F4(残渣态),平均值依次为:Cr(86.94%) > As(86.88%) > V(85.46%) > Ni(82.29%) > Co(80.48%) > Pb(75.54%) > Cu(73.43%) > Mo(62.36%) > Cd(34.96%)。特别是V、Cr、Co、Ni和As的F4(残渣态)的平均比例高于80%,可能是因为这些元素大部分与铝硅酸盐矿物结合,稳定性较强,其潜在生物可利用性较小[20]。进一步分析发现,Cu和Pb的F3(可氧化态)的比例相对较高(范围分别为3.92%—46.67%和7.67%—33.84%),表明这两种元素可能易与室内降尘中有机质发生吸附作用。Mo在F1(酸提取态)和F3(可氧化态)中的比例相对较高(范围分别为1.47%—24.09%和5.56%—46.71%),表明Mo可能在降尘处于弱酸性和氧化性条件下易释放进入环境。Cd的F1(酸提取态)和F2(可还原态)的比例在上述9 种重金属中最高(范围分别为1.09%—48.08%和10.80%—74.97%)。由于F1(酸提取态)可在中性或弱酸性条件下释放,F2(可还原态)可在还原性条件下释放并造成二次污染,表明Cd可能在环境中容易发生迁移转化,被人体吸收,其环境健康风险特别值得关注。
此外,本研究中南北方室内降尘的形态分布规律较为接近。Zhou等[21]对合肥室内降尘中重金属进行形态分析,结果表明Cd、Pb和Zn的主要存在形态为可迁移态(F1、F2或F3),而V和Cr主要以F4(残渣态)形式存在。Ozcan[22]采用BCR提取法分析Sakarya工业区街道灰尘中重金属的形态,结果显示重金属生物可利用态(F1+F2+F3)占比从大到小顺序为Cd > Mn > Zn > Cu > Ni > Cr,与本研究结果一致。
-
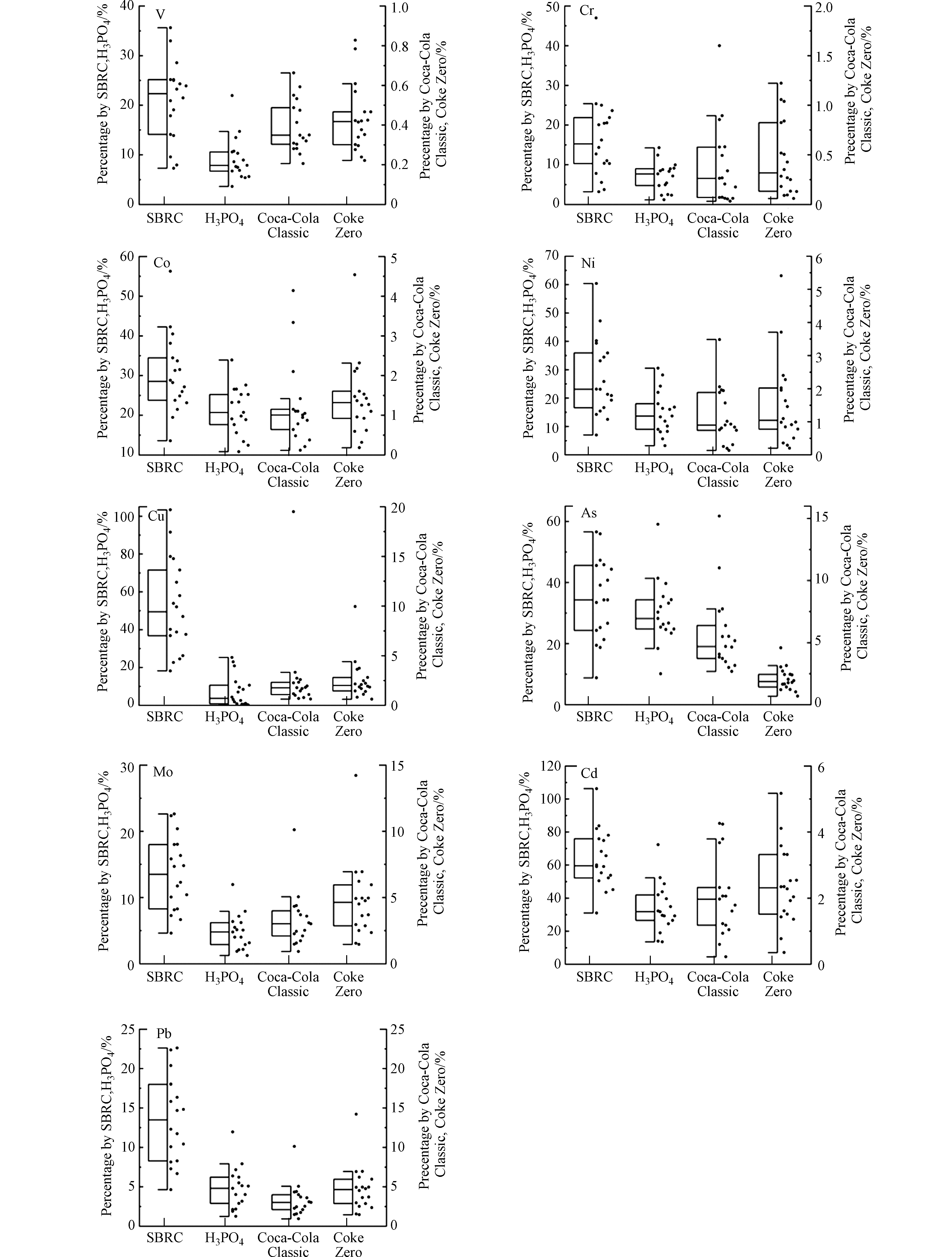
4种不同提取法(SBRC提取法、磷酸提取法、普通可乐提取法和零度可乐提取法)对室内降尘中重金属的生物可给性分析如图3所示。SBRC法生物可给性由大到小为:Pb(70.92%) > Cd(63.57%) > Cu(52.44%) > As(34.54%) > Co(30.26%) > Ni(27.22%) > V(20.89%) > Cr(16.62%) > Mo(13.48%)。Pd、Cd、Cu、As、Co、Ni和V生物可给性介于20%—80%之间,特别是其中Pb、As、Cd属于剧毒型元素,释放到环境后可对人体健康构成潜在威胁。Cr和Mo的生物可给性小于20%,表明其形态较为稳定。与此相一致,Zhao等[23]采用SBRC法分析厦门大气降尘中Cu、Cd及Pb生物可给性分别为18.22%—103.34%、31.00%—106.24%和38.81%—100.46%。此外,Dodd等[24]通过对比改良的EN-71(European Standard Toy Safety protocol)和SBRC两种体外胃肠道模拟法,发现六组研究数据中SBRC法对降尘中重金属Cu、Cd和Pb的提取率均高于60%。
普通可乐提取法和零度可乐提取法的各元素生物可给性结果处于同一数量级(均小于20%),但均远低于SBRC提取法结果。这可能是因为普通可乐和零度可乐均含有磷酸(普通可乐磷含量为172 mg·L−1;零度可乐磷含量为120 mg·L−1)[25],而磷酸根可与铅等重金属阳离子发生沉淀反应,导致其较低的提取率。此外,与普通可乐相较,零度可乐中还添加了柠檬酸。已有研究表明,柠檬酸可从受污染的土壤中溶解更多的重金属[11],导致基于零度可乐的生物可给性略高于普通可乐提取法。与本研究结果数据相似,Lottermoser等[11]采用3种可乐提取铀污染矿区3个分区土壤中的重金属,As和Ni平均提取率分别为0.6%—3.1%和0.2%—1.3%。
-
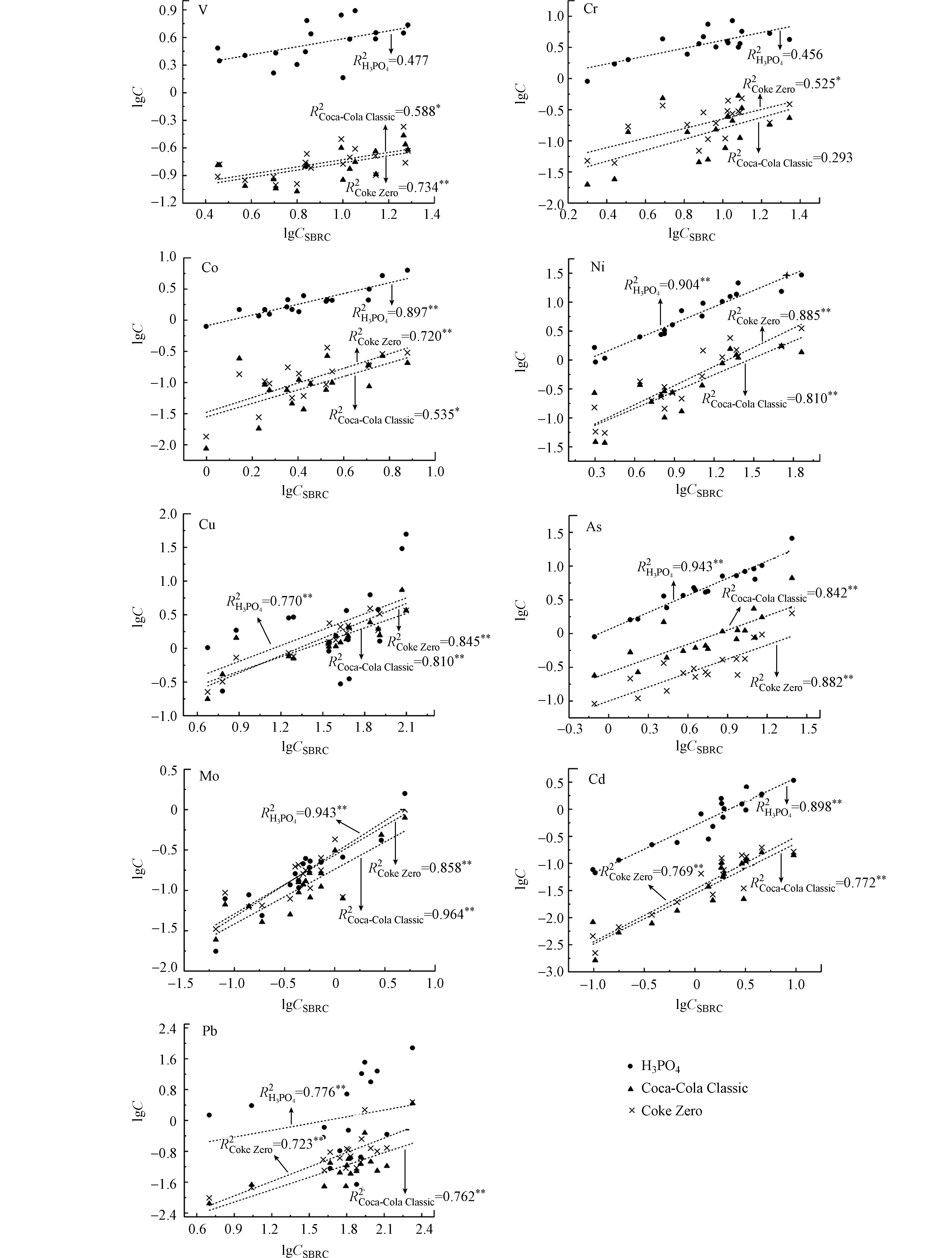
新型可乐提取模型的构建需要与传统生物可给性方法分析数据进行对比,分析两者间是否存在相关性。在本研究中,分别对室内降尘中重金属总量、F1(酸提取态)、生物可利用态(F1+F2+F3)提取量、传统生物可给性分析法(SBRC提取法和磷酸提取法)和软饮料提取法(普通可乐和零度可乐)的提取量之间进行相关性分析,结果如图4和表2所示。
除Cr之外,SBRC提取法分别与生物可利用态(F1+F2+F3)和F1(酸提取态)均呈现极显著相关(P < 0.01)。这可能是因为对于Cr而言,F1、F2和F3三态,特别是F1+F2的含量较低,导致其SBRC与F1+F2+F3的相关性不显著。与此相对应,对于F1+F2+F3含量较高的Cd和Mo,SBRC与F1+F2+F3的相关性系数分别高达0.968**和0.977**。除V之外,磷酸提取法与F1(酸提取态)均呈现显著相关(P < 0.05)。这可能与V和Cr的F1(酸提取态)较低有关。此外,SBRC与磷酸对于除Cr和V的其余7种重金属均呈现极显著相关(P < 0.01)。
普通可乐和零度可乐对所有9 种重金属元素的提取量均呈现极显著相关(P < 0.01)。进一步分析发现,零度可乐与传统生物可给性方法具有更高的相关性。对于所有9 种重金属元素,零度可乐提取法分别与BCR法中的生物可利用态(F1+F2+F3)和SBRC提取法呈现显著相关(P < 0.05)。这表明,尽管两种可乐的提取原理较为相似,但由于零度可乐中去除了普通可乐中糖类的干扰,并加入柠檬酸等酸性物质,增强了零度可乐对于重金属生物可提取态,尤其是F1态的提取效果。特别是针对As和Cd这两种高毒重金属元素,零度可乐提取法具有较大的提取量,并且与SBRC的相关性系数分别高达0.882**(As)和0.769**(Cd)。此外,鉴于软饮料提取法中无需超纯水、优级纯的化学试剂,并且废液环保易于处置,具有方便快捷的特点,使得其在非发达地区和国家中具有较大的实用价值和可行性,可作为提取剂用于室内降尘重金属生物可给性的初步分析。与此同时,仍需注意的是,软饮料提取法尚存在着提取率低等问题,在后续的推广过程中,需进一步扩大样本量,建立体外软饮料生物可给性与动物实验(如小鼠等)生物有效性测试结果间的相关关系,以期用于更精准便捷的健康风险评估。
-
(1)研究区域内室内降尘样品中Cr、Ni、Cu、As、Mo、Cd和Pb均存在不同程度富集,并且Cd污染最为严重。
(2)研究区域内室内降尘中9 种重金属均以F4(残渣态)为主。各分析方法生物可给性平均值由大到小依次为SBRC提取法>磷酸提取法>零度可乐提取法>普通可乐提取法。
(3)软饮料(特别是零度可乐)与传统生物可给性分析方法的提取量显著相关,具有构建新型室内降尘中重金属的生物可给性模型的潜力。
基于软饮料法分析室内降尘重金属生物可给性
Research on bioaccessibility of heavy metals in indoor dusts based on soft drink extraction
-
摘要: 近年来,生物可给性被广泛用于降尘中重金属的健康风险评价,然而传统的生物可给性分析方法存在诸多局限性。鉴于软饮料具有廉价易得的优势,本研究以室内降尘为研究对象,在对其重金属总量、形态和传统生物可给性分析的基础上,进一步通过相关性分析,探讨基于软饮料的新型室内降尘中重金属生物可给性分析方法的可能性。结果表明,室内降尘样品中重金属V、Cr、Co、Ni、Cu、As、Mo、Cd和Pb的总量平均值分别为44.92、76.06、10.05、51.88、108.73、19.94、5.62、3.49、106.09 mg·kg−1。地积累指数法表明室内降尘中Cd为严重污染。9 种重金属形态占比最高的均为F4(残渣态)。各生物可给性分析方法总体提取率由大到小依次为SBRC提取法>磷酸提取法>零度可乐提取法>普通可乐提取法。软饮料提取法(特别是零度可乐法)的重金属提取量分别与BCR法中的生物可利用态(F1+F2+F3)和SBRC提取法的提取量均呈现显著相关(P < 0.05),具有较大的实用价值和可行性。本研究以期为降尘中重金属的健康风险评价提供更为详实的理论基础。Abstract: Recently, bioaccessibility has been widely applied in health risk assessment of dusts, while the traditional analysis methods for bioaccessibility have many limitations. Since the soft drinks have the low-cost advantage, the contents, chemical fractions, and bioaccessibility based on the traditional methods of heavy metals in the indoor dusts were firstly analyzed in this study, and then a new bioaccessibility analysis method based on soft drink extraction was established by correlation analysis. The results showed that the average contents of heavy metals (including V, Cr, Co, Ni, Cu, As, Mo, Cd and Pb) in the indoor dusts were 44.92, 76.06, 10.05, 51.88, 108.73, 19.94, 5.62, 3.49, 106.09 mg·kg−1, respectively. The geoaccumulation index showed that Cd was heavily contaminated in China. Among the chemical fractionations of all the heavy metals, the residual fraction (F4) had the highest concentration. For the extraction rates, the four different methods were ranked in the following order, SBRC > phosphoric acid extraction method > Coke Zero > Coca Cola Classic. The heavy metal concentrations extracted by soft drinks, especially Coke Zero, were well correlated with those extracted by BCR (F1+F2+F3) and SBRC (P < 0.05) methods, which showed that Coke Zero has greater practical value for the determination of bioaccessibility. This research will provide more theoretical basis for the health risk assessment of heavy metals in dusts.
-
Key words:
- indoor dust /
- heavy metal /
- bioaccessibility /
- soft drinks
-
进入河流湖泊的重金属污染物,其中约90%的重金属可通过吸附、絮凝、络合、共沉淀等作用方式沉积于河湖底泥表面并不断积累[1]。底泥中沉积的重金属不仅对水生生物及沿河居民的饮用水安全造成了严重威胁,还容易重新释放至上覆水体,引发“二次污染”,最终危害人类健康[2]。其中,镉(Cd)是一种移动性较强、毒性较大的重金属[3]。
综合处理效率、修复成本及操作难易程度等问题的考虑,稳定化技术逐渐在底泥重金属修复中呈现出较大潜力[4]。对于该修复技术来说,稳定试剂的选择非常关键。目前,利用铁系纳米材料作为稳定试剂来修复底泥重金属污染问题已成为研究的热点[5]。其中,纳米零价铁(nZVI)凭借其独特的结构性质,如吸附还原活性强、粒径小、反应快速等特性,已被广泛应用于废水、地下水、土壤及底泥重金属的稳定修复[6-7]。但nZVI在实际应用中存在易团聚、不稳定、易被氧化等问题,进而限制了其在底泥重金属污染修复领域的进一步发展[8]。生物炭(biochar,BC)是由生物质在低氧条件下通过热解制备得到的碳质材料,在贮存碳汇、土壤肥力改善、污染物固定化和废物处理等诸多方面都发挥着重要作用[9]。BC具有多孔性、碱性、强吸附性、高比表面积、高阳离子交换量及丰富的含氧官能团等特性,对重金属具有较强的吸附和固定能力[10]。因此,将nZVI负载到BC固体载体上构建nZVI/BC复合材料,预计能减少团聚、增强nZVI的稳定性,发挥出两者的优势,实现重金属的有效稳定。基于nZVI/BC能产生多方面的有益效应,目前已有一些关于利用nZVI/BC复合材料去除(或固定)水体或土壤中的重金属和有机污染物的批量实验研究,而将该复合材料体系应用于湖泊底泥重金属修复的研究尚鲜见报道。
与水体、土壤介质不同的是,重金属在水生底栖生物条件下的迁移过程更为复杂,其迁移转化直接涉及到水体环境生态安全[11],研究修复过程中底泥重金属形态的变化是判断nZVI/BC稳定效果的重要指标。此外,重金属的浸出毒性、生物可利用性及上覆水中溶解态重金属质量浓度的变化可作为评价修复底泥中重金属环境效应的综合指标[12-13],对深入理解nZVI/BC修复重金属污染底泥的潜在环境风险具有重要科学意义。基于上述研究,本研究采用液相还原和原位沉积法制备了nZVI/BC复合材料,并对其进行了分析和表征,考察了其对湖泊底泥中Cd的固定效果,并进一步探讨了nZVI/BC对底泥Cd污染的修复机理。
1. 材料与方法
1.1 试剂与仪器
实验所需试剂主要包括:三氯化铁(FeCl3·6H2O)、硼氢化钠(NaBH4)、无水乙醇(CH3CH2OH)、冰醋酸(CH3COOH)、盐酸羟胺(NH2OH·HCl)、乙酸铵(CH3COONH4)、过氧化氢(H2O2)、甘氨酸(C2H5NO2)、硫酸亚铁(FeSO4·7H2O)均为分析纯并采购于国药集团化学试剂有限公司;实验用水均为超纯水(18.25 MΩ·cm)。
实验所需仪器主要包括:真空干燥箱(DZK-6020,上海仪电科学仪器股份有限公司);恒温水浴振荡箱(HH-80,常州市万丰仪器制造有限公司);电感耦合等离子体质谱仪(Optima 7300 DV,美国PerkinElmer公司);便携式pH计(PHS-3D,上海雷磁仪器有限公司);场发射扫描电子显微镜(SEM,S-4800,日本Hitachi公司);透射电子显微镜(TEM,Tecnai 12,荷兰Philips公司);傅里叶红外光谱(FTIR,Nicolet 5700,美国Thermo Nicolet公司);X射线能谱仪(EDS,Quanta 250,美国FEI公司);X射线光电子能谱(XPS,K-Alpha,美国赛默飞世尔科技公司)。
1.2 材料制备
nZVI的制备:将100 mL、4.83 g的FeCl3·6H2O水溶液转移至500 mL的三口烧瓶中,在通氮气的条件下搅拌30 min,然后逐滴加入等体积2.10 g NaBH4溶液,滴加完毕后再搅拌30 min,待反应完全后,用无水乙醇洗涤3次,然后用磁铁收集沉淀物,60 ℃真空干燥8 h,碾磨成粉末,保存备用。
BC的制备:将小麦秸秆放入石英舟内压实,然后置于管式炉,加热前向管内通入氮气5 min以排出管内空气,以5 ℃·min−1的速度升温至600 ℃,保温2 h。然后待管式炉温度降至近50 ℃后取出石英舟,将舟内生物炭碾磨成粉末状,保存备用。
nZVI/BC的制备:将2 g BC和100 mL、2.4156 g的FeCl3·6H2O水溶液转移至500 mL的三口烧瓶中,在通氮气的条件下搅拌30 min,然后逐滴加入等体积1.15 g NaBH4溶液,滴加完毕后再搅拌30 min,待反应完全后,用无水乙醇洗涤3次,然后用磁铁收集沉淀物,60 ℃真空干燥8 h,碾磨成粉末,保存备用。nZVI与BC质量比为1∶4,该质量比是所制备nZVI/BC材料中实际nZVI与BC的质量比。
1.3 底泥样品
采集太湖梅梁湾西北角和东北角入湖河口区域的表层底泥,采样深度约为20 cm。去除其中的石块、树枝、塑料垃圾等杂物后,将底泥样品置于冷冻真空干燥箱中进行干燥,研磨过筛(2 mm)后备用。底泥的pH为7.53,含水率为65.32%,有机质含量为17.72 g·kg−1,阳离子交换量为13.62 cmol·kg−1。底泥样品中Cd、Pb、Zn、Cu、Cr的含量分别为0.46、26.14、53.21、20.81、47.22 mg·kg−1。
1.4 实验设置
实验共设置4组:C(对照组,不添加材料)、2% nZVI(nZVI添加量2%)、2% BC(BC添加量2%)、2% nZVI/BC(nZVI/BC添加量2%),每组设3个平行样。称取一定质量的底泥样品与材料置于50 mL离心管,按照与底泥体积质量比5 mL:1 g的比例添加超纯水,混合均匀后,然后置于恒温培养箱中24 ℃静置培养。分别在第1、7、14、28、42、56 d取样测定修复过程中Cd的形态、浸出毒性、生物可利用性、上覆水中溶解态Cd质量浓度及底泥的pH和有机质。
1.5 分析方法
底泥Cd形态的测定采用改进的三步连续提取法(BCR法)[12],即分为弱酸提取态(以CH3COOH提取)、可还原态(以NH2OH·HCl提取)、可氧化态(以H2O2和CH3COONH4提取)、残渣态(以HNO3-HF-HClO4提取)。Cd的浸出毒性采用醋酸缓冲溶液法测定[12],生物可利用性采用生理提取实验测定[14]。上覆水中溶解态Cd质量浓度采用虹吸法提取,通过电感耦合等离子体质谱仪(Optima 7300 DV,美国PerkinElmer公司)测定Cd的质量浓度。pH采用便携式pH计测定,有机质采用重铬酸钾容量法-稀释热法测定[15]。数据分析采用Excel和SPSS软件,作图采用Origin软件。
2. 结果与讨论
2.1 材料表征
1) SEM分析。由图1(a)可以看出,nZVI为球状并聚集在一起。这主要是由于其自身的磁性引力所致[15]。由图1(b)可以看出,BC具有丰富的孔结构,孔隙结构可为重金属提供更多的吸附位点[16]。图1(c)为nZVI/BC复合材料的SEM图。在图1(c)可以观察到nZVI附着在BC表面,且呈现出较好的分散性。这说明BC作为支撑载体,有效降低了nZVI的团聚。
2) TEM分析。由图2(a)可以看出,nZVI颗粒粒径为50 nm左右,且呈现出链条状,体现了nZVI易团聚的特点。这与SEM的表征结果一致。由图2(b)可以看出,nZVI颗粒被固定在BC表面,nZVI的颗粒粒径分布在50~120 nm,可以看出其分散性明显优于单独的nZVI。
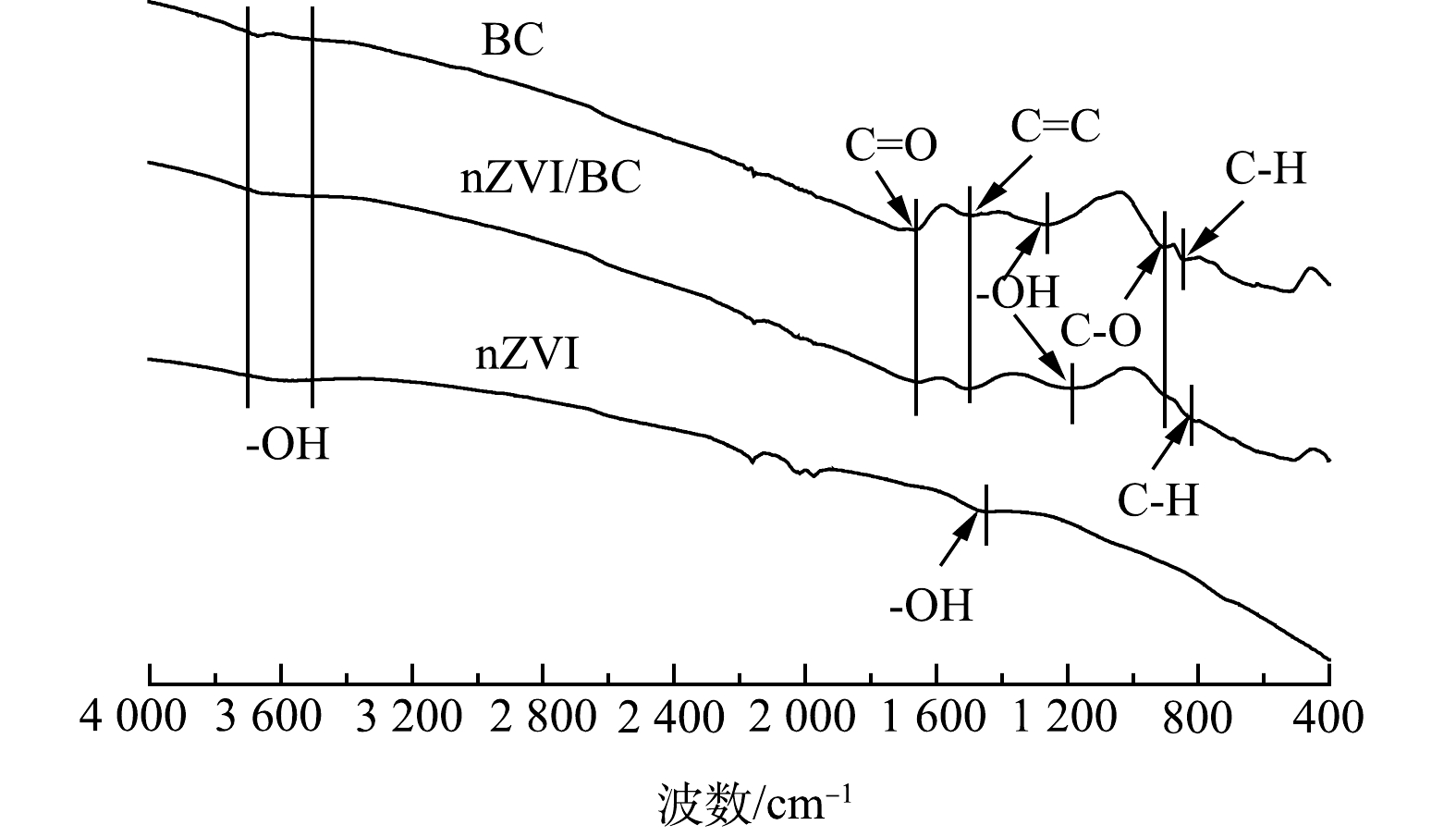
3) FTIR分析。由图3可知,nZVI、BC和nZVI/BC在3 500~3 700 cm−1处均出现了—OH的吸收峰,对nZVI来说是其表面吸附水的O—H基团的弯曲振动[17],对BC来说是其表面存在的羟基形成的[18]。此外,位于1 461 cm−1处的吸收峰为-OH的伸缩振动峰,说明nZVI表面发生了羟基化反应(FeOOH) [18]。由图3可见,波数为1 643、1 500、1 258、910和845 cm−1处分别对应C=O、C=C、—OH、C—O和C—H的伸缩振动峰。这些特征峰是由于BC中存在的羧酸、醇、酚、醚和酯等引起的[19-20],表明BC表面含有丰富的含氧官能团。在nZVI/BC的FTIR图谱中可以看到BC结构中特有的C=O、C=C和C—O键,且观察到—OH和C—H的吸收峰发生偏移。这说明nZVI与BC中的官能团之间发生反应。
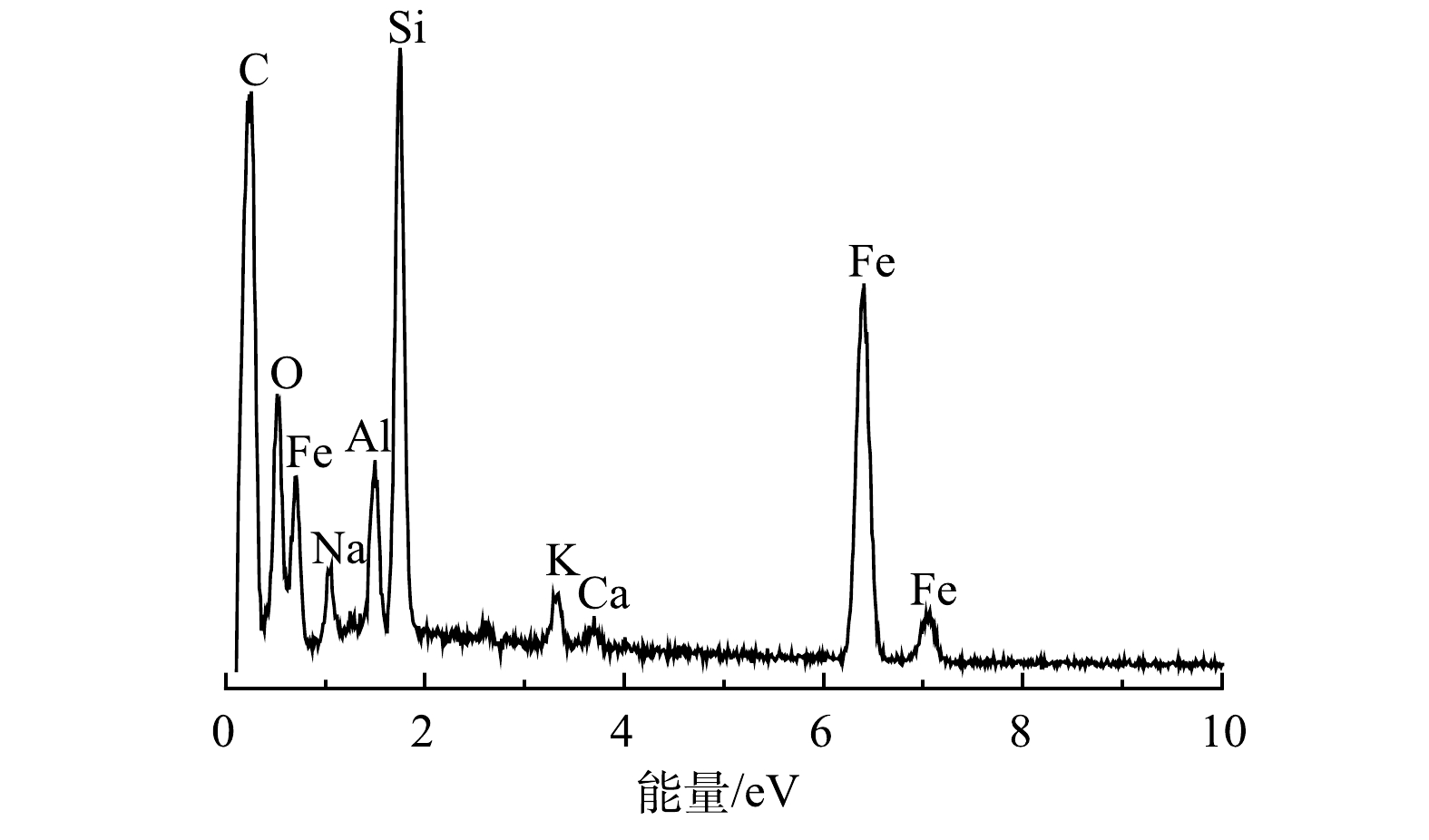
4) EDS分析。由图4可见,nZVI/BC表面除了含有C(54.96%)、O(15.07%)、Fe(18.39%)3种主要元素,还含有Na(1.92%)、Al(1.86%)、Si(6.72%)、K(0.73%)、Ca(0.34%)。这些元素属于生物质中的碱金属离子(灰分),在热解过程中会转化为氧化物、氢氧化物和碳酸盐[21]。
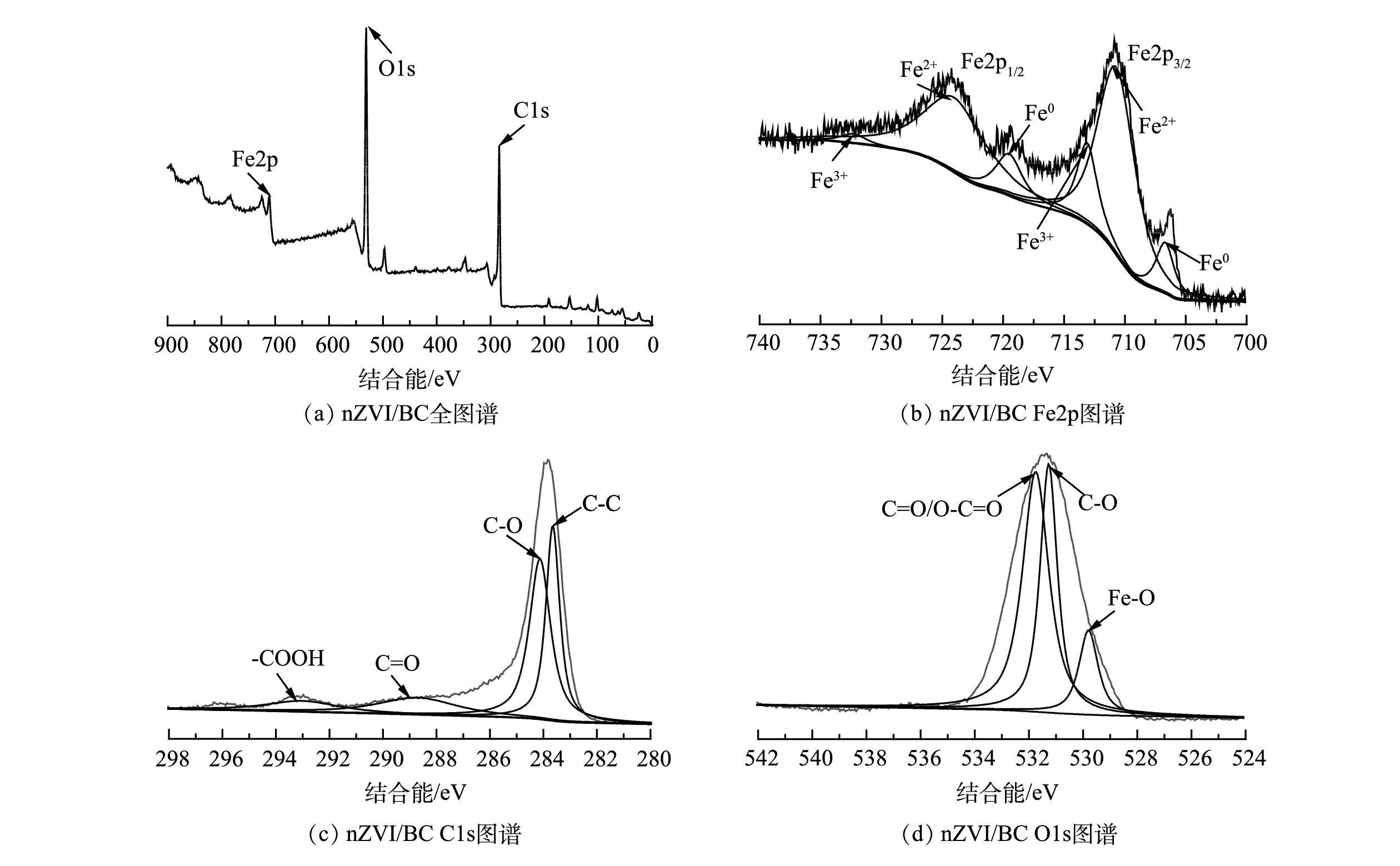
5) XPS分析。由图5(a)可见,nZVI/BC表面含有Fe、C、O 3种元素。为了进一步确定这3种元素的化学状态,分别对其进行分峰。图5(b)中Fe元素主要存在Fe2p3/2和Fe2p1/2轨道特征峰,其中结合能位于706.5 eV和720.0 eV处的特征峰对应Fe0。这说明nZVI的存在[22]。710.1 eV和724.5 eV处为Fe2+特征峰;713.0 eV和731.2 eV处为Fe3+的特征峰。Fe2+和Fe3+的存在说明在制备材料或存储的过程中nZVI不可避免的被氧化,这也与nZVI本身独特的核壳结构有关[23]。由图5(c)可见,结合能位于293.5、288.8、284.4和283.9 eV处的特征峰分别对应BC中的—COOH、C=O、C—O和C—C官能团[23-24]。如图5(d)所示,O1s被分为3个子峰,531.8、531.1和529.4 eV处的特征峰值分别归因于C=O/O—C=O、C—O和Fe—O的存在[15,25]。这表明nZVI/BC复合材料表面含有大量含氧官能团,并存在一些铁氧化物,这与FTIR的结果一致。以上结果表明nZVI/BC复合材料成功合成。
2.2 nZVI/BC对底泥Cd形态的影响
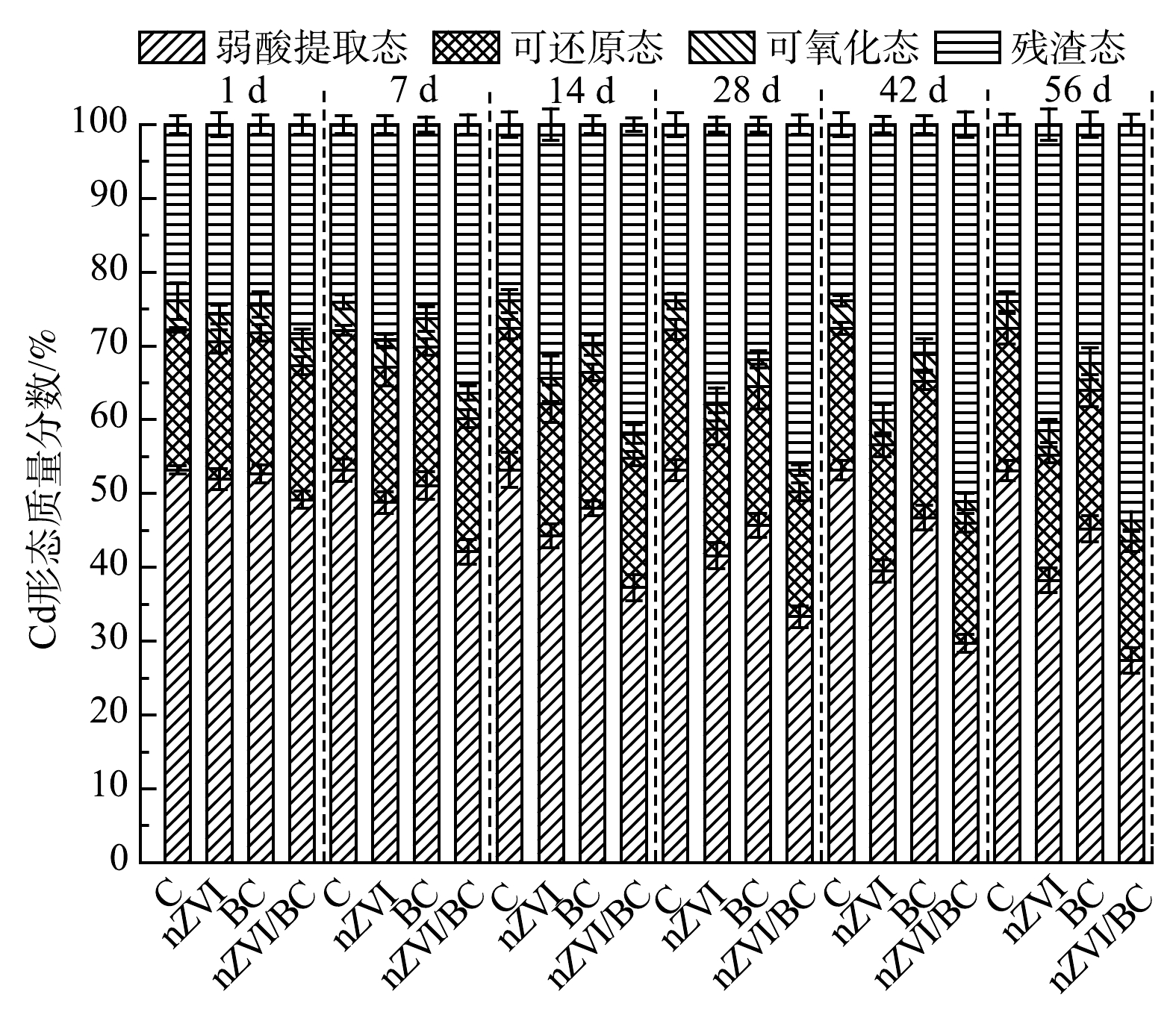
底泥中重金属的毒性和生态风险主要取决于重金属的形态而不是总量,改进的BCR提取法将重金属的形态归为4种,其毒性和移动性大小顺序为弱酸提取态>可还原态>可氧化态>残渣态[12]。由图6可见,原始底泥样品中Cd的弱酸提取态、可还原态、可氧化态和残渣态的质量分数分别为53.19%、19.01%、3.88%和23.92%。根据风险评估准则(RAC),弱酸提取态质量分数高于50%的重金属,属于第5等级,说明底泥中的Cd具有极高风险[26]。对照组中Cd的形态在整个修复过程中仅有轻微波动,侧面说明重金属在自然条件下很难自行稳定。随着修复时间的延长,各处理组中Cd的残渣态质量分数逐渐增加,其余3种形态的质量分数逐渐降低并趋于稳定。56 d后,nZVI、BC和nZVI/BC处理组中Cd的残渣态质量分数与对照组相比分别增加了17.53%、8.44%和29.73%,Cd的弱酸提取态质量分数分别降低了19.41%、7.91%和25.77%。相比于弱酸提取态,Cd的可还原态(Cd与铁锰氧化物结合)和可氧化态(Cd与硫化物和有机物结合)的质量分数的降低程度较小。这主要归因于以下2点:一方面是由于这些结合形态的Cd相对较为稳定;另一方面是可还原态和可氧化态Cd需要先经过强酸的提取,转化为酸溶态,进而才能被材料固定[15]。56 d后,相比于对照组,nZVI/BC处理组中Cd的可还原态和可氧化态质量分数分别降低了3.07%和0.89%。以上结果表明,nZVI、BC和nZVI/BC 3种材料均能使Cd从不稳定的形态逐渐转化成稳定的形态,有效降低了Cd的移动性[14]。其中,nZVI/BC对Cd的稳定效果最好。
目前,有研究采用其他材料修复底泥中的Cd。WEN等[27]采用改性沸石来稳定底泥中的Cd,一定时间后Cd的残渣态质量分数增加了8.3%。LI等[14]利用氧化铁对Cd污染的底泥进行修复56 d后,Cd的最大残渣态质量分数增加了14.94%。ZHANG等[28]发现纳米羟基磷灰石能高效固定底泥中的Cd,且经过14 d的修复,Cd的残渣态质量分数从29.1%(无添加)增加至41.8%(10%添加)。与以上研究相比,本研究所制备的nZVI/BC对底泥中Cd的稳定效果更好。
2.3 nZVI/BC对底泥Cd浸出毒性的影响
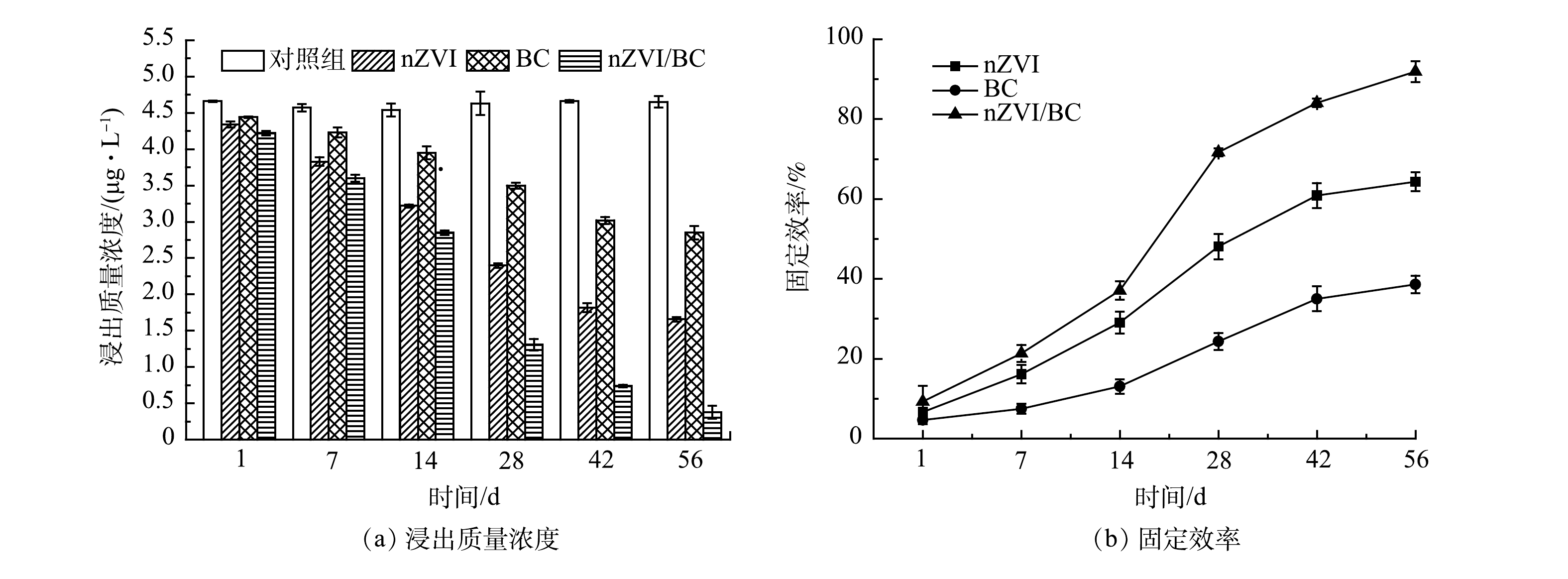
浸出毒性实验(TCLP)可直接反映出底泥Cd的溶出性能[12]。nZVI、BC和nZVI/BC添加后底泥Cd浸出质量浓度的变化及其对Cd的固定效率如图7所示。由图7(a)可以看出,经过材料的修复,底泥样品中Cd浸出质量浓度均呈逐渐降低的趋势。56 d后,nZVI、BC和nZVI/BC处理组中Cd浸出质量浓度分别为1.66、2.85和0.38 μg·L−1,较对照组中Cd浸出质量浓度分别减少了2.99、1.80和4.27 μg·L−1。根据浸出质量浓度,评估了材料对Cd的固定效率。由图7(b)可见,随着时间的延长,3种材料对Cd的固定效率均逐渐增加,其顺序为nZVI/BC>nZVI>BC。56 d后,nZVI、BC和nZVI/BC对Cd的固定效率分别达到了64.31%、38.60%和91.83%。以上结果表明,3种材料均能有效降低Cd的浸出质量浓度并高效固定Cd,进而降低了底泥中Cd的溶出性和环境风险。
2.4 nZVI/BC对底泥Cd生物可利用性的影响
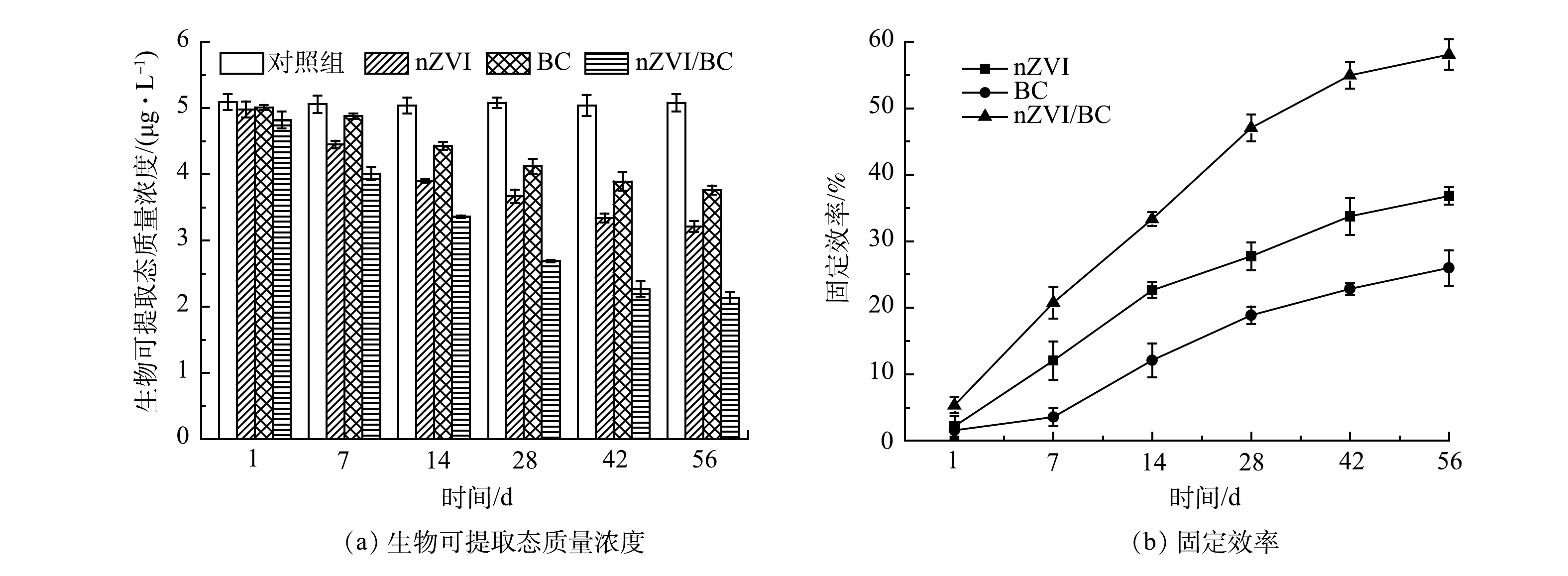
生理提取实验(PBET)主要用于评估重金属的生物可利用性,即指重金属进入生物体内并被利用的难易程度,可反映出重金属对生物体的毒性大小[14]。从图8(a)可以看出,对照组中Cd的生物可提取态质量浓度基本维持在5.06 μg·L−1,各处理组中Cd的生物可提取态质量浓度在整个修复过程中均呈逐渐降低的趋势。由图8可见,56 d后,nZVI、BC和nZVI/BC处理组中Cd的生物可提取态质量浓度由5.08 μg·L−1分别降低到3.21、3.76和2.13 μg·L−1,其固定效率分别为36.81%、25.98%和58.07%。其中nZVI/BC对Cd的固定效果最好,固定效率的大小与TCLP结果一致。以上结果表明,材料的添加有效降低了Cd生物可利用性,有助于减少Cd对底栖生物体的毒害作用。此外,也可以发现Cd的生物可提取态质量浓度要大于浸出质量浓度,这主要是由于PBET所用提取液的pH更低,Cd更容易被提取出来,使得Cd的生物可提取态质量浓度要高一些。这与CHOU等[29]研究结果一致。
2.5 nZVI/BC对上覆水溶解态Cd质量浓度的影响
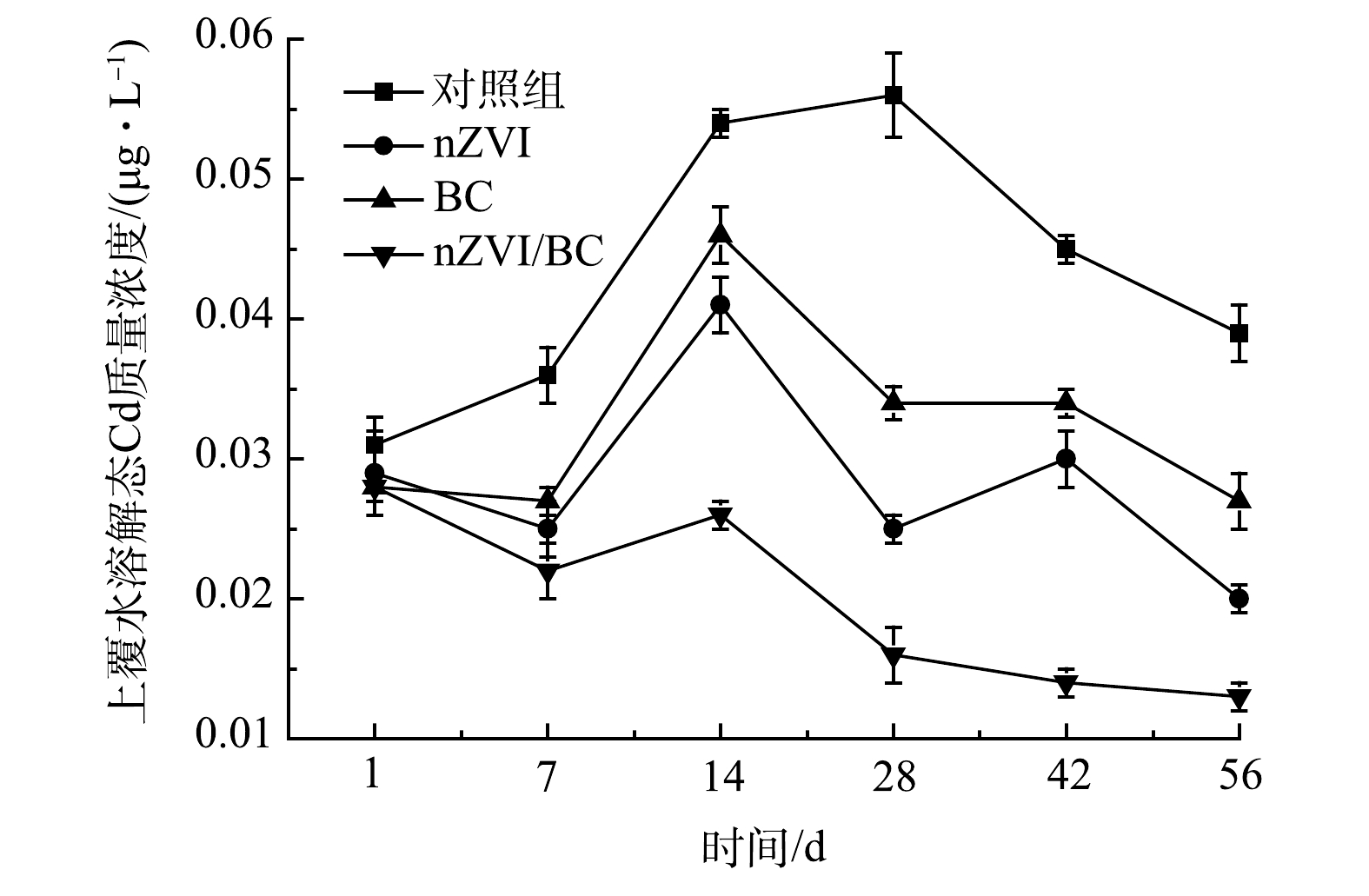
上覆水中溶解态重金属质量浓度的变化直接影响水体生态系统的健康[30]。修复过程中上覆水溶解态Cd质量浓度的变化如图9所示。可以看出,对照组上覆水中溶解态Cd质量浓度在整个修复过程中呈现先上升后降低的趋势。其原因可能是底泥作为主要的内源污染,本身就有向水体释放污染物的趋势。此外,对照组和处理组的底泥样品在实验设置时均进行了摇晃,造成Cd的释放。nZVI、BC和nZVI/BC处理组上覆水中溶解态Cd质量浓度虽在14 d时也有一定上升,但在整个修复过程中其浓度均低于对照组。14 d后各处理组上覆水中溶解态Cd质量浓度逐渐下降,可能是位于泥水界面处的材料对上覆水中溶解态Cd的吸附络合作用[13]。此外,悬浮于上覆水中的溶解态Cd一般与泥沙颗粒吸附在一起,随着修复时间的延长,因其密度大于水,进而会逐渐沉降下来[1]。56 d后,与对照组相比,nZVI、BC和nZVI/BC分别使上覆水中溶解态Cd质量浓度降低48.05%、29.87%和67.53%,说明3种材料均对底泥Cd释放起到抑制作用,其中nZVI/BC对底泥Cd释放抑制效果最好,同时,降低上覆水中溶解态Cd质量浓度也能有效缓解其对水体环境的生态毒性。
2.6 nZVI/BC对底泥pH和有机质的影响
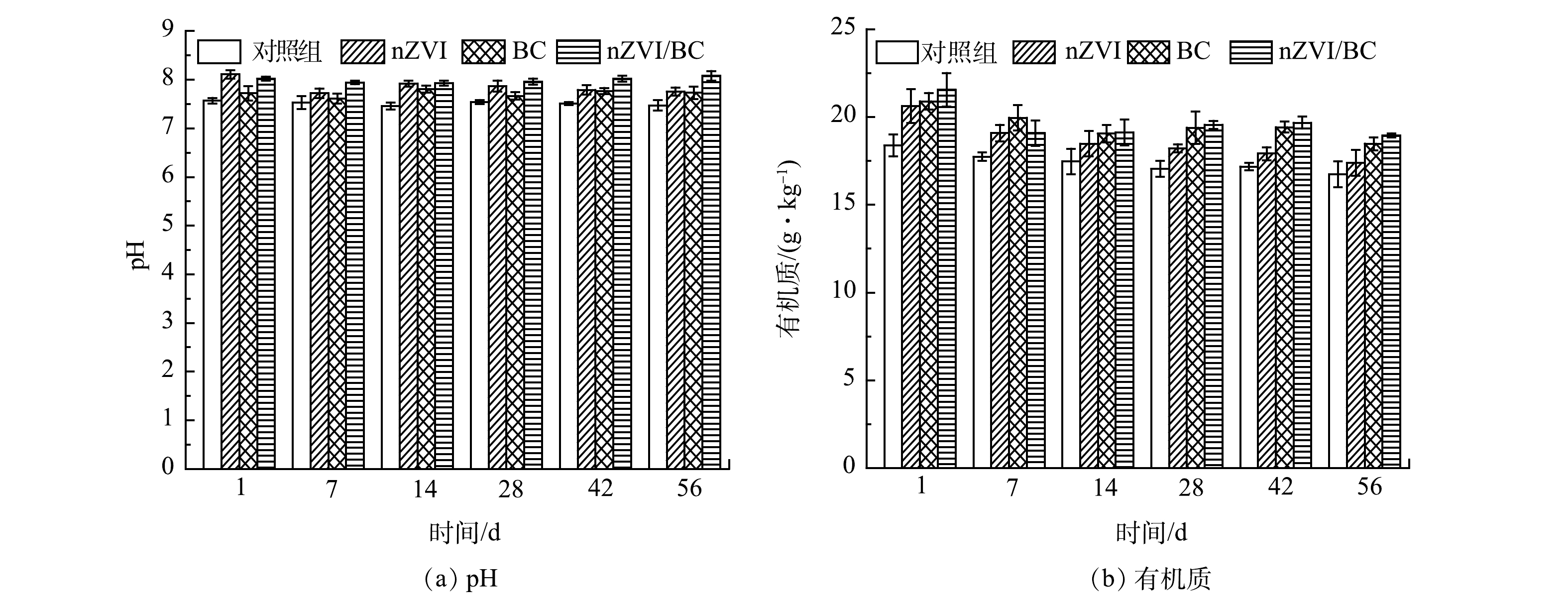
pH对重金属的移动性具有一定影响,如较低的pH会减少底泥颗粒所带的负电荷,从而降低其对Cd的吸附能力,进而增加底泥中Cd的流动性[14]。如图10(a)所示,对照组pH在整个修复过程中有轻微波动,基本维持在7.50左右,且各处理组的pH均高于对照组。56 d后,nZVI、BC和nZVI/BC处理组pH由7.47分别上升至7.76、7.73和8.08。有研究表明,当环境中pH≥8时,Cd的羟基物质开始形成,如CdOH+、Cd2(OH)3+和Cd(OH)2沉淀[31]。此时,nZVI/BC材料表面带有更多的负电荷,Cd羟基物质会被吸附在BC或铁的氧化壳表面,进而降低了Cd的移动性[31]。通过上述结果可以发现,材料的添加均增加了底泥样品pH,其中nZVI/BC在提高底泥pH作用上效果更为明显。nZVI使底泥pH增加的原因在于本身的氧化所致,Fe0可与H2O和O2反应生成Fe2+和OH−[5-6];BC增加底泥pH的原因是由于BC具有丰富的碱性基团和碳酸盐,可以中和底泥酸度,进而导致底泥的pH增加[16,21]。此外,底泥pH的升高与有机质的微生物降解过程也有关,因有机质被微生物分解后会释放出二氧化碳和水,也就是碳酸,这样就会有少量的氢离子流失,进而造成pH上升[36]。pH的升高能增加底泥样品颗粒或矿物表面的电负性,可促进Cd的吸附络合,从而提高对Cd的吸附性能[32]。
有机质可以与重金属形成络合物进而降低重金属的可迁移性,同时,有机质也是微生物生命活动所需的能量和养分来源[15]。从图10(b)可以看出,对照组和各处理组有机质的含量在整个修复过程中逐渐降低并趋于稳定,且各处理组有机质含量均高于对照组。56 d后,对照组、nZVI、BC和nZVI/BC处理组有机质含量分别为16.73、17.38、18.47和18.94 g·kg−1,相比于对照组,nZVI/BC处理组的有机质含量高出1.13倍。相较于对照组,nZVI处理组有机质含量的增加可能是nZVI释放出的Fe离子与底泥固相中的有机质结合形成水溶性化合物所致[33]。BC由小麦秸秆这种有机物质高温裂解制备,本身具有丰富的碳,因而可通过碳封存来增加底泥有机质含量[34]。此外,也有研究表明,BC自身结构中含有部分溶解性有机质[37]。随着修复时间的延长,由于nZVI、BC和nZVI/BC对Cd较好的稳定效果,将可移动态的Cd逐步转化为残渣态,降低了Cd的生物可利用性,促进了某些细菌菌群的增长,进而加大了对有机质的分解利用[15]。以上结果表明,材料的添加均增加了底泥样品中水溶性有机质的含量,有利于重金属的稳定。
2.7 机制分析
nZVI、BC和nZVI/BC的添加促使Cd由不稳定形态转化为稳定形态,均增加了Cd的残渣态质量分数,降低了Cd的迁移性。同时,3种材料的添加均降低了Cd的浸出毒性、生物可利用性和上覆水中溶解态Cd的质量浓度,表明nZVI、BC和nZVI/BC对底泥中Cd具有较好的固定效果。本研究中,3种材料对Cd的固定效率大小均为nZVI/BC>nZVI>BC。材料对Cd的稳定机制可能分为2个方面。一方面,游离的Cd被吸附在材料表面(nZVI、BC或nZVI/BC),并与nZVI表面的铁氢氧化物(FeOOH)发生络合反应(FeOCdOH)进而被固定[17]。FRANCIS等[35]发现Cd与FeOOH的结合力很强,几乎没有Cd能被提取出来。此外,BC的多孔结构和丰富的含氧官能团也对Cd具有较强吸附络合能力,如—OH等基团能增加BC表面的负电荷,增强其对Cd的吸附性能,C=O可与Cd发生络合反应[30]。另一方面,材料的添加增加了底泥样品的pH和有机质,相应的原因已在2.6小节进行了分析,pH和有机质的增加也可促进底泥中Cd的稳定。
3. 结论
1)制备所得的nZVI/BC复合材料与nZVI相比,分散性更好,且BC具有丰富的孔隙结构和大量含氧官能团,对湖泊底泥中重金属Cd具有更好的稳定性能。
2) nZVI、BC和nZVI/BC的添加均可显著降低底泥中Cd的弱酸提取态质量分数及增加残渣态质量分数,Cd的可还原态和可氧化态质量分数降低的程度较小。其中,nZVI/BC处理组中Cd的弱酸提取态质量分数最大降低了25.77%,表明nZVI/BC对Cd具有较好的稳定效果,可促使Cd向稳定形态的转化。
3) nZVI/BC的添加可有效降低底泥中Cd的浸出质量浓度、生物可提取态质量浓度和上覆水中溶解态Cd质量浓度,进而可降低底泥中Cd的环境风险及对底栖生物体和水体环境的生态毒性。
4) nZVI、BC和nZVI/BC的添加均可增加底泥pH和有机质含量,其中nZVI/BC处理组中pH和有机质含量分别增加了0.61和2.21 g·kg−1。材料对Cd的稳定机制包括材料本身对Cd的吸附络合作用及底泥pH和有机质的增加。
-
表 1 室内降尘中重金属总量(mg·kg-1)
Table 1. Heavy metal contents in the indoor dusts (mg·kg-1)
V Cr Co Ni Cu As Mo Cd Pb 室内降尘(n=18) 最小值 21.44 16.13 5.85 13.87 7.33 5.82 0.66 0.14 11.73 最大值 79.16 330.60 18.76 180.59 318.01 43.67 22.09 11.54 282.20 平均值 44.92 76.06 10.05 51.88 108.73 19.94 5.62 3.49 106.09 中位数 42.43 56.32 9.05 37.67 96.66 17.17 3.90 2.43 92.83 标准差 15.24 70.75 3.58 45.35 84.01 11.44 5.80 3.27 70.96 变异系数/% 35.92 125.62 39.55 120.39 86.91 66.61 148.81 134.63 76.44 全国-非工业区[17] — 132.82 — 42.51 116.12 38.16 — 3.31 170.97 全国-工业区[17] — 206.97 — 50.06 332.67 369.39 — 22.02 861.72 中国土壤背景值[16] 82.4 61.0 12.7 26.9 22.6 11.2 2.0 0.097 26.0 表 2 重金属不同提取态间的相关系数(n=16)
Table 2. Correlation coefficients for heavy metal concentrations detected in different extracts (n=16)
V Cr Co Ni Cu As Mo Cd Pb SBRC-F1 0.621** 0.465 0.847** 0.930** 0.879** 0.876** 0.974** 0.901** 0.881** SBRC- (F1+F2+F3) 0.787** 0.395 0.925** 0.956** 0.861** 0.846** 0.977** 0.968** 0.906** 磷酸-F1 0.423 0.616* 0.889** 0.988** 0.967** 0.879** 0.975** 0.953** 0.943** 磷酸- (F1+F2+F3) 0.588* 0.598* 0.923** 0.938** 0.868** 0.843** 0.965** 0.894** 0.740** SBRC-磷酸 0.447 0.456 0.897** 0.904** 0.770** 0.943** 0.943** 0.898** 0.776** 普通可乐-F1 0.641** 0.497 0.464 0.837** 0.802** 0.816** 0.976** 0.843** 0.921** 普通可乐-(F1+F2+F3) 0.778** 0.562* 0.416 0.732** 0.731** 0.812** 0.972** 0.765** 0.666** 普通可乐-SBRC 0.734** 0.293 0.535* 0.810** 0.810** 0.842** 0.964** 0.772** 0.762** 普通可乐-磷酸 0.547* 0.193 0.540* 0.815** 0.730** 0.956** 0.931** 0.877** 0.932** 零度可乐-F1 0.687** 0.807** 0.775** 0.909** 0.749** 0.864** 0.797** 0.838** 0.925** 零度可乐-(F1+F2+F3) 0.717** 0.546* 0.754** 0.909** 0.732** 0.840** 0.805** 0.770** 0.754** 零度可乐-SBRC 0.588* 0.525* 0.720** 0.885** 0.845** 0.882** 0.858** 0.769** 0.723** 零度可乐-磷酸 0.594* 0.342 0.689** 0.888** 0.632** 0.967** 0.677** 0.862** 0.951** 零度可乐-普通可乐 0.922** 0.734** 0.877** 0.875** 0.949** 0.971** 0.888** 0.988** 0.917** **P < 0.01;*P < 0.05. -
[1] KASTURY F, SMITH E, JUHASZ A L. A critical review of approaches and limitations of inhalation bioavailability and bioaccessibility of metal(loid)s from ambient particulate matter or dust [J]. Science of the Total Environment, 2017, 574: 1054-1074. doi: 10.1016/j.scitotenv.2016.09.056 [2] CHEN H, LU X W, LI L Y. Spatial distribution and risk assessment of metals in dust based on samples from nursery and primary schools of Xi'an, China [J]. Atmospheric Environment, 2014, 88: 172-182. doi: 10.1016/j.atmosenv.2014.01.054 [3] HAN Q, WANG M S, CAO J L, et al. Health risk assessment and bioaccessibilities of heavy metals for children in soil and dust from urban Parks and schools of Jiaozuo, China [J]. Ecotoxicology and Environmental Safety, 2020, 191: 110157. doi: 10.1016/j.ecoenv.2019.110157 [4] 田春晖, 杨若杼, 古丽扎尔·依力哈木, 等. 南京市大气降尘重金属污染水平及风险评价 [J]. 环境科学, 2018, 39(7): 3118-3125. doi: 10.13227/j.hjkx.201709120 TIAN C H, YANG R Z, QIAN X, et al. Pollution levels and risk assessment of heavy metals from atmospheric deposition in Nanjing [J]. Environmental Science, 2018, 39(7): 3118-3125(in Chinese). doi: 10.13227/j.hjkx.201709120
[5] IBANEZ Y, le BOT B, GLORENNEC P. House-dust metal content and bioaccessibility: A review [J]. European Journal of Mineralogy, 2010, 22(5): 629-637. doi: 10.1127/0935-1221/2010/0022-2010 [6] LI H B, LI M Y, ZHAO D, et al. Oral bioavailability of as, pb, and Cd in contaminated soils, dust, and foods based on animal bioassays: A review [J]. Environmental Science & Technology, 2019, 53(18): 10545-10559. [7] 陈廷廷, 侯艳伟, 蔡超, 等. 应用四种体外消化方法比较研究场地土壤中重金属的生物可给性及其人体健康风险 [J]. 环境化学, 2018, 37(11): 2342-2350. doi: 10.7524/j.issn.0254-6108.2017110102 CHEN T T, HOU Y W, CAI C, et al. Bioaccessibility and human health risk assessement of heavy metals in soils by using four in vitro digestion methods [J]. Environmental Chemistry, 2018, 37(11): 2342-2350(in Chinese). doi: 10.7524/j.issn.0254-6108.2017110102
[8] MELANIUK-WOLNY E, WIDZIEWICZ K, ADAMCZYK Z, et al. Single-stage extraction to assess metals bioavailability from smelting dust [J]. Journal of Environmental Studies, 2014, 23(6): 2117-2124. [9] 邓晓霞, 米艳华, 黎其万, 等. 利用改进的BCR法和tessier法提取稻田土壤中Pb、Cd的对比研究 [J]. 江西农业学报, 2016, 28(9): 64-68. doi: 10.19386/j.cnki.jxnyxb.2016.09.15 DENG X X, MI Y H, LI Q W, et al. Comparative study on extraction of Pb and Cd from paddy soils by modified BCR method and tessier method [J]. Acta Agriculturae Jiangxi, 2016, 28(9): 64-68(in Chinese). doi: 10.19386/j.cnki.jxnyxb.2016.09.15
[10] SCHNUG E, FLECKENSTEIN J, HANCKLAUS S. Coca cola® is it!the ubiquitous extractant for micronutrients in soil [J]. Communications in Soil Science and Plant Analysis, 1996, 27(5/6/7/8): 1721-1730. [11] LOTTERMOSER B G, SCHNUG E, HANEKLAUS S. Cola soft drinks for evaluating the bioaccessibility of uranium in contaminated mine soils [J]. Science of the Total Environment, 2011, 409(18): 3512-3519. doi: 10.1016/j.scitotenv.2011.05.043 [12] PATTANAMAHAKUL P. Assessments of heavy metal concentration and toxicity of dust from a parking building in bangkok[C]//July 11-12, 2017 Bangkok (Thailand) Back LHHISS-17, FCBHS-17, ASET-17. EAP, 201. [13] PUEYO M, MATEU J, RIGOL A, et al. Use of the modified BCR three-step sequential extraction procedure for the study of trace element dynamics in contaminated soils [J]. Environmental Pollution, 2008, 152(2): 330-341. doi: 10.1016/j.envpol.2007.06.020 [14] XIE J J, YUAN C G, SHEN Y W, et al. Bioavailability/speciation of arsenic in atmospheric PM2.5 and their seasonal variation: A case study in Baoding city, China [J]. Ecotoxicology and Environmental Safety, 2019, 169: 487-495. doi: 10.1016/j.ecoenv.2018.11.026 [15] 杨春, 塔西甫拉提·特依拜, 侯艳军, 等. 新疆准东煤田降尘重金属污染及健康风险评价 [J]. 环境科学, 2016, 37(7): 2453-2461. doi: 10.13227/j.hjkx.2016.07.006 YANG C, TIYIP T, HOU Y, et al. Assessment of heavy metals pollution and its health risk of atmospheric dust fall from east part of Junggar Basin in Xinjiang [J]. Environmental Science, 2016, 37(7): 2453-2461(in Chinese). doi: 10.13227/j.hjkx.2016.07.006
[16] 中国环境监测总站. 中国土壤元素背景值[M]. 北京: 中国环境科学出版社, 1990∶87-493. China Environmental Monitoring Station. Background values of soil elements in China[M]. Beijing: China Environmental Science Press, 1990: 87-493 (in Chinese).
[17] KUMAR M, FURUMAI H, KASUGA I, et al. Metal partitioning and leaching vulnerability in soil, soakaway sediments, and road dust in the urban area of Japan [J]. Chemosphere, 2020, 252: 126605. doi: 10.1016/j.chemosphere.2020.126605 [18] 何予川, 王明娅, 王明仕, 等. 中国降尘重金属的污染及空间分布特征 [J]. 生态环境学报, 2018, 27(12): 2258-2268. doi: 10.16258/j.cnki.1674-5906.2018.12.011 HE Y C, WANG M Y, WANG M S, et al. Pollution and spatial distribution characteristics of heavy metals in dusfall in China [J]. Ecology and Environmental Sciences, 2018, 27(12): 2258-2268(in Chinese). doi: 10.16258/j.cnki.1674-5906.2018.12.011
[19] 苗青青, 姜楠, 张瑞芹, 等. 中原城市群典型城市秋冬季大气PM2.5污染特征及溯源 [J]. 环境科学, 2021, 42(1): 19-29. MIAO Q Q, JIANG N, ZHANG R Q, et al. Characteristics and Sources of PM2.5 pollution in typical cities of the central plains urban agglomeration in autumn and winter [J]. Environmental Science, 2021, 42(1): 19-29(in Chinese).
[20] 伊丹, 王艳, 刘汝海, 等. 青岛市冬季降尘中重金属的形态分析及其环境风险评估 [J]. 环境化学, 2019, 38(9): 1990-1997. doi: 10.7524/j.issn.0254-6108.2018110301 YI D, WANG Y, LIU R H, et al. Speciation analysis and environmental risk assessment of heavy metals in dustfall of Qingdao in winter [J]. Environmental Chemistry, 2019, 38(9): 1990-1997(in Chinese). doi: 10.7524/j.issn.0254-6108.2018110301
[21] ZHOU L, LIU G J, SHEN M C, et al. Characteristics and health risk assessment of heavy metals in indoor dust from different functional areas in Hefei, China [J]. Environmental Pollution, 2019, 251: 839-849. doi: 10.1016/j.envpol.2019.05.058 [22] OZCAN N, ALTUNDAG H. Speciation of heavy metals in street dust samples from Sakarya I. Organized industrial district using the BCR sequential extraction procedure by ICP-OES [J]. Bulletin of the Chemical Society of Ethiopia, 2013, 27(2): 205-212. [23] ZHAO L S, YU R L, YAN Y, et al. Bioaccessibility and provenance of heavy metals in the park dust in a coastal city of southeast China [J]. Applied Geochemistry, 2020, 123: 104798. doi: 10.1016/j.apgeochem.2020.104798 [24] DODD M, RASMUSSEN P E, CHÉNIER M. Comparison of two in vitro extraction protocols for assessing metals’ bioaccessibility using dust and soil reference materials [J]. Human and Ecological Risk Assessment:an International Journal, 2013, 19(4): 1014-1027. doi: 10.1080/10807039.2012.719381 [25] IORIO B D, MICCO L D, TORRACA S, et al. Phosphorus, beverages, and chronic kidney disease [J]. Nutrition and Dietary Supplements, 2012,4: 67-69. doi: 10.2147/NDS.S35290 -






 下载:
下载: