-
水溶性有机物(water-soluble organic matters,WSOM)作为大气颗粒物中可溶于水相的有机组分,占大气有机气溶胶的10%—80%[1-2]. 相关研究表明,WSOM可影响气溶胶作为云凝结核的能力,还有助于吸收太阳辐射,从而影响全球气候变化[2-3]. 并且气溶胶中WSOM与活性氧以及细胞的氧化还原活性有着密切的关联,对人体健康有着重要的影响[4]. 近年来,随着大气灰霾污染问题突出,有关大气中 WSOM光学特性和环境行为的研究已成为大气领域研究的重点之一.
WSOM复杂多样的光学特性与其来源和结构组成信息密切相关. WSOM在大气气溶胶中的来源广泛,研究发现生物质燃烧是其主要的来源[5-6]. Zhang等[5]研究发现,北京、上海、广州和西安城市的气溶胶中WSOM最主要的来源为生物质燃烧排放,占总WSOM的17%—26%. Hecobian等[6]研究确定了生物质燃烧是WSOM中发色团的主要来源之一. 此外,生物质燃烧排放源对大气中WSOM的组成和荧光特性有着重要的影响. 例如,Duarte等[7]在大气气溶胶WSOM中检测到了纤维素类和木质素类物质的存在,证实了生物质燃烧源是大气气溶胶中WSOM化学成分的主要贡献源. 范行军等[8]研究发现,生物质燃烧排放是大气气溶胶中WSOM的类蛋白物质的主要贡献源. Qin等[9]研究发现,由于生物质燃烧排放的贡献,兰州市冬季大气中WSOM的腐殖化程度明显低于夏季. 目前对于不同生物质燃烧产生颗粒物的研究主要集中在化学组成和排放特征(如离子组成和排放因子等), 也有学者对其WSOM光学特性开展了部分工作,表明生物质类型对大气气溶胶中WSOM的发色物质组成和光学特性有着重要的影响[8,10].
尽管已有相关学者关注了生物质燃烧排放WSOM的光学特性,但由于生物质的种类繁多,不同生物质燃烧排放WSOM的组成和光学性质可能存在较大差异. 本文以草本类(包括高粱、玉米、水稻、小麦、花生叶、杂草)和木本类(包括松树、杉树的叶、杆、根部位)两类典型生物质为研究对象,收集模拟野外燃烧试验产生的颗粒物,并分析颗粒物的化学成分特征以及颗粒物中WSOM的紫外-可见光吸收特征和三维荧光光谱特征. 研究结果可以补充生物质燃烧源的光学特性,为大气颗粒物源解析提供基础数据.
-
本研究选取6种草本类生物质(高粱、玉米、水稻、小麦、花生叶、杂草)和2种木本类生物质(松树和杉树)为研究对象. 为避免采样过程中受其他排放源的影响,采样地点远离道路,建筑区和工业区. 燃烧前将生物质样品干燥14 d以上并除去表面灰尘,以减少叶面颗粒污染物沉积引起的误差. 由于木本类生物质(松树和杉树)的根、杆和叶部分的化学组成可能存在较大差异,将根、杆和叶部分分开进行单独燃烧.
生物质燃烧样品采集方法参考文献[11],模拟生物质露天燃烧的方式,将Mini Vol TAS粉尘颗粒采样器(Airmetries,美国)放置于距离生物质燃烧堆水平和垂直分别约1 m的位置采集烟气颗粒(PM2.5),并控制采样流量为6 L·min−1,采样时间为10 min. 将实验室内强制通风后,密闭实验室采集空白对照,并且在每次采集样品前均进行强制通风操作. 每种生物质用量在30 g左右,每种生物质样品燃烧采集2次. 采样过程中每采集好1个样品,用酒精擦拭膜托和采样头,避免不同样品之间发生交叉污染. 采样滤膜采用石英纤维滤膜(Whatman),采样前滤膜用铝膜包裹,放入500 ℃下焙烧5.5 h去除滤膜上的杂质和无机碳,采样后放入−20 ℃冰柜中储存.
-
切割四分之一片膜置于清洗干净的玻璃瓶中,用20 mL超纯水(18.3 MΩ·cm)超声提取15 min,然后用孔径为0.22 μm的针式过滤器过滤,提取过程重复两次,以确保WSOM得以充分提取,将两次提取液混合,过程中以水空白和膜空白作为背景空白. 以同样的方法用超纯水超声提取水溶性离子,使用孔径为0.45 μm的针式过滤器过滤,超声提取时间为10 min,提取过程重复2次.
-
采用总有机碳(TOC)分析仪(Jena AG multi N/C 3100,德国)测定WSOM的浓度,即在680 ℃的高温条件下,水样被Pt催化剂完全氧化成水和二氧化碳,再经非色散红外检测器检测. 使用邻苯二甲酸氢钾标准溶液建立WSOM的校准曲线,所有样品在检测前均用2 mol·L−1盐酸酸化去除无机碳.
-
根据文献[12]中使用DRI热/光碳分析仪测定样品中的有机碳(OC)和元素碳(EC),OC和EC检出限均低于1.0 μg·m−3,每10个样品进行1次重复测定,确保两次误差在5%以内. 采用Dionex ICS 1100和Dionex ICS 900型离子色谱仪测定8种水溶性离子(Cl−、
NO−3 、SO2−4 、NH+4 、Na+、K+、Ca2+、Mg2+),离子回收率在90%—110%之间. -
采用岛津UV-2401PC型号的紫外-可见分光光度计测定提取液的吸光度(Aλ),设定扫描波长范围为200—500 nm,扫描速度为400 nm·min−1.根据扫描数据计算特征吸收指数(SUVA254)、E250/E365和质量吸收指数(MAE365). SUVA254是WSOM浓度标准化后的254 nm处吸光度,通过以下公式计算:
式中,A254为254 nm处的吸光度,C为提取液中WSOM的质量浓度,单位为mg·L−1;L为光程长度,1 cm.
E250/E365为250 nm处吸光度与365 nm处吸光度之比.MAE365是表征发色团吸光能力的重要参数,计算公式如下:
式中,A365为波长365 nm处的吸光度;C为提取液中WSOM的质量浓度,单位为mg·L−1;L为光程长度,1 cm.
-
采用日立的F-7000荧光分光光度计测定样品WSOM的三维荧光光谱. 荧光信号在3-D模式下进行扫描,激发波长(Ex)和发射波长(Em)的范围分别为200—400 nm和250—500 nm,扫描间隔均为5 nm,扫描速度为2400 nm·min−1,光电倍增管检测器的设定电压为700 V. 按照文献[13]中描述的程序,对原始EEM光谱进行了校正和标准化:(1)对EEM光谱进行背景校正即减去超纯水光谱;(2)使用插值法去除一阶和二阶瑞利散射和拉曼散射的干扰信号;(3)利用紫外-可见吸收光谱校正荧光强度的内滤效应;(4)荧光强度通过除以Ex=350 nm处纯水的拉曼峰面积进行标准化,从而去除仪器依赖因子,且结果以拉曼单位(R. U. )表示;(5)标准化后的数据除以WSOM浓度得到比荧光强度(SFI).
主要用以下4个荧光指标描述荧光光谱特征:腐殖化指数(humification index, HIX)、荧光指数(fluorescence index, FI)、自生源指数(freshness index, BIX)和单位TOC平均荧光强度(average fluorescence intensity per unit TOC, AFI/TOC). HIX值为Ex=254 nm时,Em在435—480 nm之间的荧光强度面积除以Em在300—345 nm之间的荧光强度面积的比值[9,14],该值越大表明溶解性有机质的腐殖化程度越高[8-9],HIX值的增加将导致发射光谱红移[15]. BIX值为Em=380 nm处的荧光强度除以Ex=310 nm处Em在420—435 nm之间的最大荧光强度的比值[9,14],该值越高反映溶解性有机质的生物活性越强或生物物质含量越丰富[14-15]. FI值为Ex=370 nm时,Em在450 nm和500 nm处的荧光强度的比值[9,14],FI可以反应溶解性有机质的前体来源[15],该值越大表明芳香氨基酸对溶解性有机质荧光强度的贡献率越大[8]. AFI/TOC可能在很大程度上反应荧光团的密度和分子量,该值的增加反应有机物分子量的减少或荧光团密度的增加[15],计算公式如下[15]:
式中,λEx为激发波长,λEm为发射波长,FI为各激发和发射波长处的荧光强度,avg为平均值函数,TOC的单位为mg·L−1.
-
本研究测定了不同生物质燃烧排放PM2.5的化学组分包括OC、EC和水溶性无机离子. 如表1所示,生物质燃烧排放PM2.5中OC/TC、EC/TC和OC/EC比值范围分别为0.67—0.94、0.06—0.33和2.00—15.40,这与其他研究生物质燃烧烟尘中碳质组分的结果相近[16,17]. 其中草本类与木本类OC/EC值分别为11.89 ± 3.56和5.21 ± 2.34,两者差异性极显著(P<0.01),这可能与两者本身的结构(密度和尺寸)、化学组成差异(如木质素、纤维素、半纤维素等含量的不同)以及燃烧状态有关[17]. 此外,草本类与木本类WSOM/OC的平均值均为0.30,说明WSOM是两类生物质燃烧排放PM2.5中重要的组成部分.
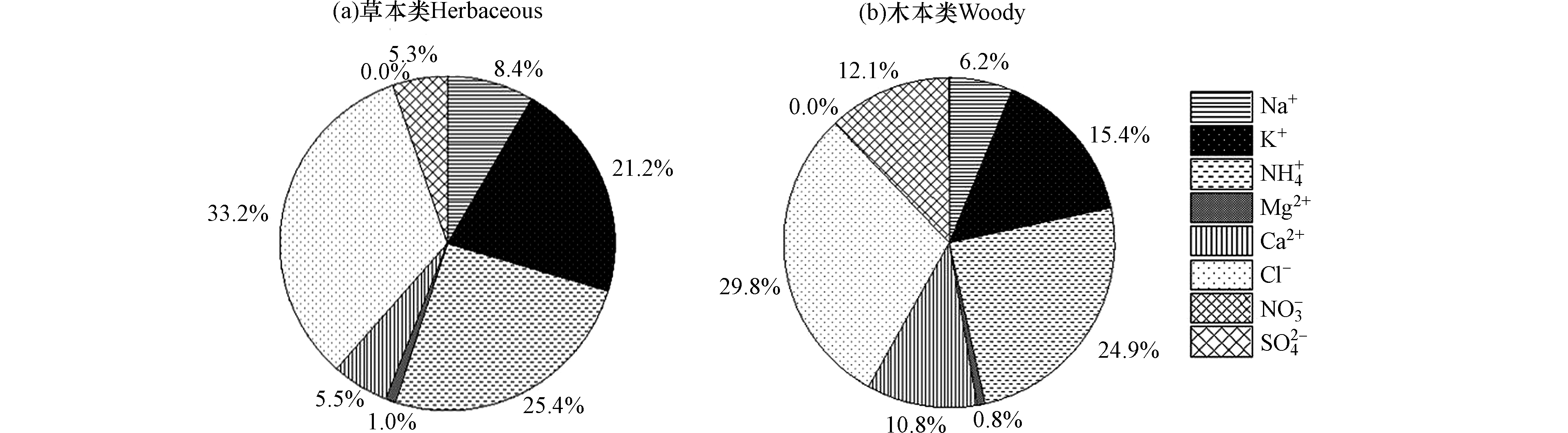
草本类与木本类生物质燃烧排放PM2.5中8种水溶性无机离子占总离子的百分比分布如图1所示. 由图1可知,两者 PM2.5中均以Cl−、
NH+4 和K+占主导地位,三者之和分别为79.8%和70.1%,说明生物质燃烧排放 PM2.5中Cl−、NH+4 和K+是水溶性离子的主要组分. 同样,王真真等[11]研究发现,秸秆燃烧排放烟尘中K+、Na+、NH+4 和Cl−是水溶性离子的主要组成,四者之和的占比为80%—92%. 其他研究也发现,树木和稻草燃烧排放烟尘中以Cl−和K+占主要比例[16,18]. 此外,本研究中所有生物质燃烧排放PM2.5中NO−3 均低于检测限. -
由于254 nm的波长可以代表WSOM样品中存在的芳族结构的最大吸收率[19-20],光谱参数SUVA254可作为生物质燃烧排放PM2.5中WSOM的芳香性和分子量大小的指标;一般SUVA254值越高,表明WSOM的芳香度和分子量越高;与之相反,E250/E365值的大小与有机物的芳香度和分子量呈反比[10,20-21],WSOM中π键高度共轭将导致紫外-可见吸收度向更高波长移动,从而使E250/E365的值降低[15,21]. 表1列出了本研究中生物质燃烧排放PM2.5中WSOM的SUVA254和E250/E365的变化范围分别为1.79—2.60 m2·g−1和4.56—7.65,结果与文献报道杨木和毛竹两种薪柴燃烧排放WSOM的研究结果相近[8];其中SUVA254值均小于燃煤排放的WSOM值(2.6—4.6 m2·g−1)[22]. 表明相比于燃煤源,生物质燃烧排放PM2.5中WSOM的芳香度和分子量较低. 此外,草本类和木本类生物质燃烧排放PM2.5中WSOM的SUVA254值分别为(2.28 ± 0.19) m2·g−1和(2.25 ± 0.27) m2·g−1,E250/E365值分别为5.79 ± 0.63和6.39 ± 0.70,两者之间均无显著性差异.
MAE365可用来表征生物质燃烧排放PM2.5中WSOM的光吸收能力[23-25]. 据文献报道,薪柴和燃煤排放WSOM的MAE365值分别为0.4—0.9 m2·g−1和(0.96 ± 0.71) m2·g−1[8,15];大气气溶胶中WSOM的MAE365值范围为0.51—1.79 m2·g−1[10,23]. 本研究中生物质燃烧排放PM2.5中WSOM的MAE365值范围为0.66—1.17 m2·g−1,说明生物质燃烧排放PM2.5中WSOM具有与燃煤排放的和大气气溶胶中的WSOM类似的吸光能力. 草本类生物质燃烧排放PM2.5中WSOM的MAE365值((0.94 ± 0.14 ) m2·g−1)略大于木本类生物质样品的值((0.84 ± 0.11) m2·g−1),但两者之间亦无显著性差异.
-
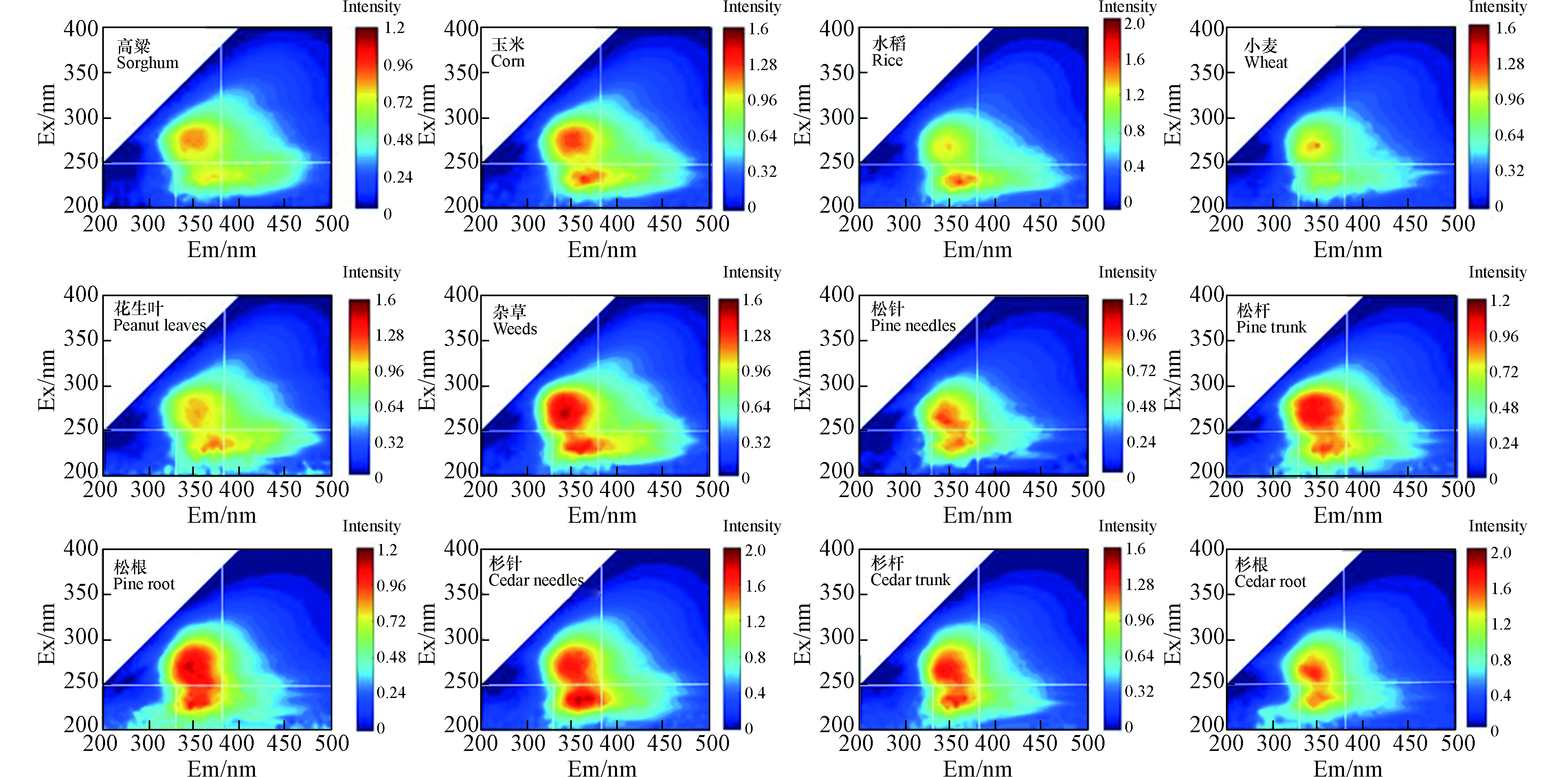
三维荧光光谱(3D-EEM)法是一种快速方便分析有机物类型和结构特征的方法.该方法已被广泛应用于雨水、雾水、大气气溶胶和生物质气溶胶中WSOM的研究[8-10,26-31].本文研究了不同种生物质燃烧排放PM2.5中WSOM的荧光特性,具体谱图见图2.
-
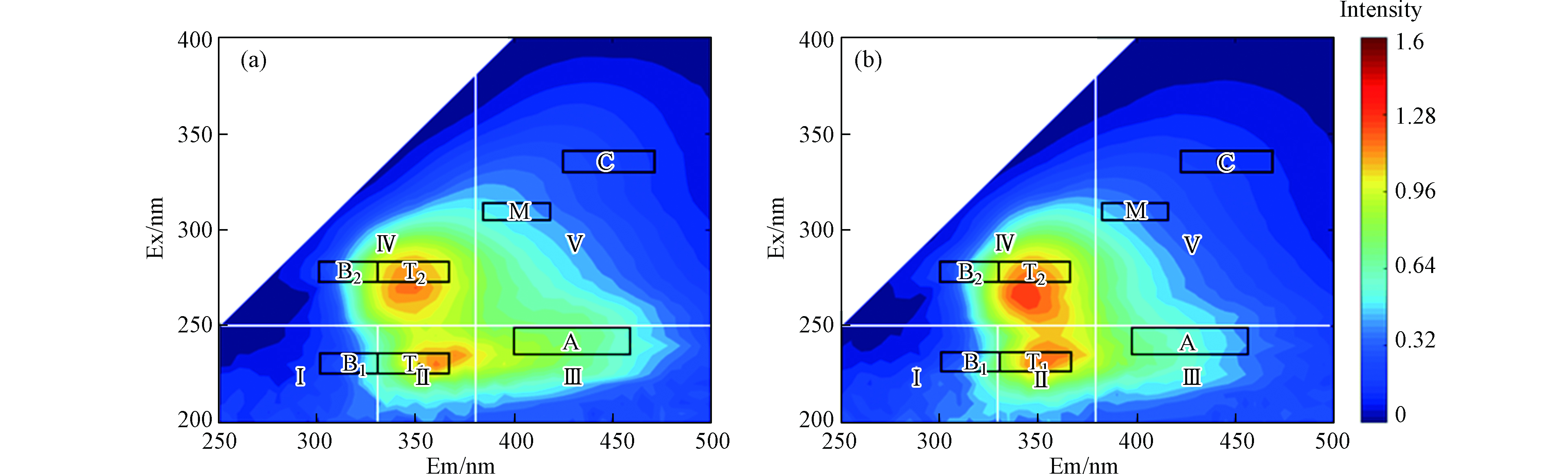
由图2可见,不同种类生物质样品中WSOM的三维荧光谱图具有高度的相似性,有两个主要的强荧光峰,分别为T1 (λEx/λEm≈230—250 nm/335—380 nm)和T2 (λEx/λEm≈260—290 nm/330—360 nm),以及一个弱肩峰A. 根据文献报道,荧光峰T1和T2均可能归属为类色氨酸荧光峰,其中T2峰也有可能是来自芳香类氨基酸和酚类物质的贡献[8,28];荧光峰A归属为紫外光区类腐殖质荧光峰[9,15]. 结果说明生物质燃烧排放PM2.5中WSOM的荧光发色团以类色氨酸、芳香类氨基酸和酚类物质为主,且包含少量的具有紫外吸收的类腐殖质物质. 雨水和大气气溶胶WSOM的EEM中识别出与之类似的荧光峰[26-27, 29,32-33],其中荧光峰T1和T2在本研究中生物质燃烧排放PM2. 5中WSOM的强度显著高于雨水和大气溶胶样品中WSOM的强度,然而荧光峰A却与之相反. 说明生物质燃烧排放PM2. 5中WSOM与雨水和大气气溶胶中的WSOM有着相似的有机组分,但其腐殖化程度相对较低。值得注意的是,草本类生物质燃烧排放PM2. 5中WSOM的荧光谱图中A峰普遍具有较长的发射波长. 为了更好的观察,分别求出了所有草本类和木本类生物质SFI的平均值和标准偏差,并且绘制出3D-EEM谱图(图3),由于标准偏差很小,所以SFI的平均谱图可视为草本类和木本类生物质的典型荧光谱图. 相关研究表明,有机物的荧光范围受分子量大小的影响,分子量较大的有机物会产生波长范围较长的荧光[15, 34]. 从图3可以看出,草本类生物质的A峰具有更长的发射波长. 说明相对于木本类生物质,草本类生物质燃烧排放PM2. 5中WSOM具有较大分子量,这可能跟两者之间化学组成的差异有关.
-
Chen等[35]将荧光光谱范围划分为5个区域,分别对应5种溶解性有机物:区域Ⅰ—Ⅴ分别对应类酪氨酸蛋白质、类色氨酸蛋白质、类富里酸、溶解性微生物产物和类腐殖酸. 由图3可知,生物质燃烧排放PM2.5中WSOM的荧光团主要集中在区域Ⅱ、Ⅲ和Ⅳ. 说明荧光团的主要成分包含色氨酸类、富里酸类物质和微生物代谢产物. 由表2中可以进一步看出,生物质燃烧排放PM2.5中WSOM的荧光强度均在区域Ⅱ中的占比最大,草本类与木本类生物质在区域Ⅱ中积分分别为0.33 ± 0.02和0.36 ± 0.01. 这与前文WSOM的荧光特征峰分析以类色氨酸为主要物质的结论相一致.
Ph/Pp可评价WSOM的稳定性,Ph/Pp值越大表示WSOM越趋于稳定,其中Ph为区域Ⅲ和Ⅴ的占比之和,Pp为区域Ⅰ、Ⅱ和Ⅳ的占比之和,分别代表腐殖质类物质和蛋白类物质的所占比例[36]. 本研究中草本类生物质燃烧排放PM2.5中WSOM的Ph/Pp值(0.57 ± 0.05)大于木本类生物质对应的值(0.42 ± 0.04),说明相对木本类生物质,草本类生物质燃烧排放PM2.5中WSOM的稳定性更高和腐殖质类物质占比更多. 这与前文草本类生物质燃烧排放PM2.5中WSOM具有更大分子量与更高的腐殖化程度的结果一致.
-
荧光指标包括腐殖化指数(HIX)、荧光指数(FI)、自生源指数(BIX)和单位TOC平均荧光强度(AFI/TOC),常用于表征雨水、雾水、大气气溶胶、燃煤和生物质气溶胶中WSOM的浓度、类型和来源等[15,30]. HIX表示有机物的腐殖化程度,较高的HIX(>10)值意味着强腐殖化物质或高度芳香化的有机物,较低的HIX(<5)被认为是新生成的有机物[15,37]. 由表3可知,本研究中生物质燃烧排放PM2.5中WSOM的HIX值变化范围为0.49—1.09,该值略高于杨木和毛竹燃烧样品[8],与燃煤样品结果相当[15],低于大气气溶胶[9,31]、雨水[26-27]以及雾水[30] 中WSOM的HIX值. 说明本研究中生物质燃烧排放PM2.5中WSOM的腐殖化程度较低,这可能与环境中WSOM来源的复杂程度有关[8,9]. 此外,草本类生物质燃烧排放PM2.5中WSOM的HIX值(0.91 ± 0.17)显著高于木本类生物质对应的值(0.59 ± 0.10)(P<0.01),说明相对木本类生物质,草本类生物质燃烧排放PM2.5中WSOM的腐殖化程度更高,这与前文的结果相一致.
FI和BIX可以表征溶解性有机质(DOM)的芳香性强弱与自生源贡献大小[8-9,15,38-39];FI>1.9和BIX>1指示DOM具有较低的芳香性和较高的自生源贡献[38-39]. 由表3可知,生物质燃烧排放的PM2.5中WSOM的FI和BIX值变化范围分别为2.03—2.68和1.32—1.81,普遍高于大气气溶胶[9,31]、雨水[26-27]以及雾水[30]样品中WSOM的FI和BIX值,与杨木和毛竹燃烧[8]以及燃煤[15]样品结果相近,说明生物质燃烧排放PM2.5中WSOM的芳香性较低.值得注意的是,本研究中生物质燃烧排放PM2.5中WSOM具有较高的FI和BIX值并不是由于自生源的贡献. 前期研究表明,大气中WSOM呈现较高的FI 和HIX 值也可归属为生物质燃烧源的贡献[8]. 此外,草本类和木本类生物质燃烧排放PM2.5中WSOM的FI值和BIX值均具有极显著性差异(P<0.01). 这可能说明不同燃料的组成差异对WSOM光谱特性的影响较大.
AFI/TOC值随分子量的减少而增加[13,15],本研究中生物质燃烧排放PM2.5中WSOM的AFI/TOC值变化范围为0.23—0.50,平均值为0.36 ± 0.08;草本类与木本类之间无显著差异(P>0.05);相比于燃煤源[15],生物质燃烧排放PM2.5中WSOM拥有相对较低的分子量.
-
表4为生物质燃烧排放PM2.5中WSOM的吸光特征参数与荧光指标之间的Spearman相关性分析.由表4可知,MAE365与SUVA254(r=0.444,P<0.05)和HIX(r=0.795,P<0.01)显著正相关,与E2/E3(r =−0.914,P<0.01)和BIX(r =−0.698,P<0.01)显著负相关,说明生物质燃烧排放PM2.5中WSOM的光吸收能力与其芳香性和腐殖化程度呈显著正相关.这与范行军等[8]研究发现薪柴燃烧排放棕色炭的光吸收能力与其芳香性和腐殖化程度呈显著正相关的结果一致.
-
(1)生物质燃烧排放PM2.5中WSOM的SUVA254、E250/E365和MAE365值范围分别为1.79—2.60 m2·g−1、4.56—7.65和0.66—1.17 m2·g−1,说明生物质燃烧排放PM2.5中WSOM的芳香度和分子量相对较低,光吸收能力相对较弱.
(2)生物质燃烧排放PM2.5中WSOM产生荧光的主要范围为λEx/λEm≈(230—250) nm/(335—380) nm和λEx/λEm≈(260—290) nm/(330—360) nm,荧光强度均在区域Ⅱ中的占比最大,说明荧光团中以类色氨酸为主要物质;荧光指标(HIX、FI、BIX和AFI/TOC)结果表明生物质燃烧排放PM2.5中WSOM的腐殖化程度、芳香性和分子量均较低;相对于木本类生物质,草本类生物质燃烧排放PM2.5中WSOM具有更高的分子量、稳定性和腐殖化程度.
(3)生物质燃烧排放PM2.5中WSOM的MAE365与SUVA254和HIX显著正相关,与E250/E365和BIX显著负相关,说明生物质燃烧排放PM2.5中WSOM的光吸收能力与其芳香性和腐殖化程度呈显著正相关.
生物质燃烧排放颗粒物中水溶性有机物的光学特性
Optical properties of water-soluble organic matters in particulate matter from biomass burning
-
摘要: 采用紫外-可见光吸收光谱法(UV-vis)和激发-发射矩阵荧光光谱法(EEM)分析了典型生物质燃烧排放颗粒物(PM2.5)中水溶性有机物(WSOM)的光学特性. 结果表明,WSOM的SUVA254、E250/E365和MAE365值分别为1.79—2.60 m2·g−1、4.56—7.65和0.66—1.17 m2·g−1,说明生物质燃烧排放PM2.5中WSOM具有较低的芳香度和分子量以及较弱的吸光能力. 荧光光谱结果显示,WSOM产生荧光峰的主要范围为λEx/λEm≈(230—250)/(335—380) nm和λEx/λEm≈(260—290)/(330—360) nm,说明生物质燃烧排放PM2.5中WSOM主要以类蛋白荧光物质为主;腐殖化指数(HIX)、荧光指数(FI)和自生源指数(BIX)分别为0.49—1.09、2.03—2.68和1.32—1.81,说明生物质燃烧排放PM2.5中WSOM的腐殖化程度、芳香性和分子量均较低.相关性分析结果显示,生物质燃烧排放PM2.5中WSOM的MAE365值与SUVA254和HIX值呈显著正相关关系,与E250/E365和BIX呈显著负相关性,说明生物质燃烧排放PM2.5中WSOM的光吸收特性与芳香性、腐殖化程度和自生源贡献有着紧密的联系.
-
关键词:
- 水溶性有机物 /
- 颗粒物 /
- 生物质燃烧 /
- 激发-发射矩阵荧光光谱
Abstract: The optical properties of water-soluble organic matters (WSOM) in particulate matter (PM2.5) from biomass burning were analyzed by ultraviolet-visible absorption spectroscopy (UV-Vis) and excitation-emission matrix fluorescence spectroscopy (EEM). The results showed that the SUVA254, E250/E365 and MAE365 values of WSOM were 1.79—2.60 m2·g−1, 4.56—7.65 and 0.66—1.17 m2·g−1, respectively, indicating that the WSOM in PM2.5 emitted from biomass burning exhibited low aromaticity and molecular weight as well as weak light absorption capacity. EEM results showed that the main wavelength ranges of fluorescence peaks generated by WSOM were λEx/λEm≈(230—250)/(335—380) nm and λEx/λEm≈(260—290)/(330—360) nm, implying that the protein-like substances were dominant fluorophores for WSOM in PM2.5 emitted from biomass burning. Humification index (HIX), fluorescence index (FI) and freshness index (BIX) were 0.49—1.09, 2.03—2.68 and 1.32—1.81, respectively, suggesting that WSOM in PM2.5 emitted from biomass burning had low humification degree, aromaticity and molecular weight. Correlation analysis showed that MAE365 value of WSOM in PM2.5 emitted from biomass burning was significantly positively correlated with SUVA254 and HIX, but negatively with E250/E365 and BIX, indicating that the light absorption characteristics of WSOM emitted from biomass burning were closely related to their aromaticity, humification degree and autochthonous. -
由于人类活动的影响,大量氮磷等营养元素进入水体,导致水体富营养化[1]。水体富营养化严重破坏水生生态系统,导致蓝藻爆发,鱼类大量死亡,生物多样性丧失[2]。根据2020年《中国生态环境状况公报》,我国主要江河监测的1 614个水质断面中,Ⅴ类水占1.5%,劣Ⅴ类水占0.2%。尽管我国流域水质状况总体变好,但仍需要改善。
目前,富营养水体的治理技术主要分为物理技术、化学技术和生物技术[3-4]。物理技术包括人工曝气、截污、调水冲污和底泥疏浚等措施,而这些措施存在一些缺陷,如底泥疏浚只是将污染物转移,并没有从根本上解决问题。化学技术主要是添加化学药剂和吸附剂改变水体中氧化还原电位、pH、吸附沉淀水体中悬浮物质和有机质,但成本昂贵,不具有可持续性,还可能会造成二次污染。生物技术主要是利用水生生物(植物、动物和微生物)的代谢活动去除富营养水体中氮、磷等营养元素,有利于恢复水生生态系统的健康与稳定,其具有较好的发展前景,但仍需要研究最佳环境因子[5-6]。
水体富营养化的治理是一个系统工程,单一的治理技术效果并不显著,探究综合治理水体富营养化的技术模式十分必要。邓泓等[7]利用截污清淤、调水冲污、异位生物处理、种植水生植物和放养螺、蚌和鱼类等技术对丽娃河进行了综合整治,NH3-N、TN和TP从治理前的劣Ⅴ类达到地表水Ⅴ类标准。闫飞[8]通过引清入河、水下种植沉水植物、混养鲢鳙等水生动物、安装以生物膜为基础的原位修复装置形成综合生态修复系统,使水体水质除TN外,其他指标均达到地表水Ⅲ类标准。四川省广元市王家沟的黑臭水体采用SCEU强化环保生态方法,在不清淤疏浚的条件下,水体黑臭消除,水质由劣Ⅴ类水变为地表水Ⅳ类水[9]。但在实际应用中,根据水体污染情况、水文状况和当地环境条件,选择恰当的技术进行综合匹配,才能快速恢复生态系统、提升水质,同时降低治理成本,从而实现可持续发展。
在我国,因考虑河道的防洪、排涝等问题,目前主要采用的河岸类型是硬质河岸[10]。硬质河岸阻断了河岸土壤与水体之间的物质交换和能量流动,破坏了其原有的生态群落结构,使河岸对水体的净化能力完全消失,降低了河流的水环境容量[11-13]。城市现存硬质驳岸生态化改造的方法主要分为3种:一是利用种植箱,种植攀援植物覆盖原有的硬质护岸;二是采用石笼护岸并覆盖土质护坡,再铺设草皮;三是利用保水剂、粘合剂、抗蒸腾剂、团粒剂、植物纤维、泥炭土、腐殖土、缓释复合肥等材料制成的客土覆盖到很缓的护岸上,并种植水生和湿生植物[14]。例如,英格兰威尔特郡马登河在所有垂直河边挡土墙的地基内,运用石灰岩石板以一致的角度铺设,创造出墙体建在天然岩石上的外观,种植边缘水生植物,并且在铺路砖之间播撒草种,打造整体景观环境[15]。威海某河道原设计采用浆砌石挡墙,对河岸进行生态化改造时,拆除浆砌石挡墙,改为自然原型驳岸,斜坡入水,丛状点缀不同的水生植物,并铺设天然圆石或鹅卵石[16]。目前的硬质驳岸生态改造技术存在成本较高,景观效果较为单一,对水质净化效果有限等缺点。考虑原有河道的排洪能力和护岸的不同倾斜程度,在不破坏原有硬质护岸的基础上,将生态护岸与水体直接连接起来,同时配备适宜的植被,不仅能提升河道景观效果,而且有利于提高水体自净能力。
柴桑河位于四川省眉山市仁寿县,流经天府新区眉山片区后,进入天府新区成都片区并汇入锦江。天府新区成都片区和天府新区眉山片区共同组成天府新区,是四川省的国家级新区,是成渝经济建设的重要部分[17]。天府新区的经济发展需要大量的水资源供给,但天府新区的河流总体水质较差,加之水生态流量不足,水环境容量没有扩容空间,这成为天府新区面临的环境挑战之一[18]。柴桑河的治理对天府新区的水环境状况有着重要意义。由于柴桑河两岸工业的开发以及人口的增加,流域水质逐渐变差,河流的污染问题引发了社会的高度关注。2018年,眉山天府新区投入28.9亿元,对柴桑河进行治理,打造城市公园,构建生态湿地系统,大大提升了当地的环境状况。但是,柴桑河水体水质仍然存在不达标的情况,水体浑浊且泥沙较多,水面有大量油膜覆盖,河道两岸均为浆砌石硬质河岸,无植被生长,河流生态系统破坏严重。因此,眉山天府新区管委会要求对位于天府新区眉山片区中心城区的柴桑河河段进行水质提升和环境改善。
本研究以位于四川省天府新区眉山片区中心城区的柴桑河河段为例,在不破坏原有河岸的基础上,对硬质河岸进行生态重建,改造周围景观环境,实现低成本处理;同时设计了使水质长期稳定在地表水Ⅳ类标准的综合治理技术。以恢复水生生态系统的自净能力为基础,通过各项综合措施,匹配生态系统构成所需的要素,建立强大的生态系统,实现水体长效改善。
1. 研究区域
1.1 治理河段介绍
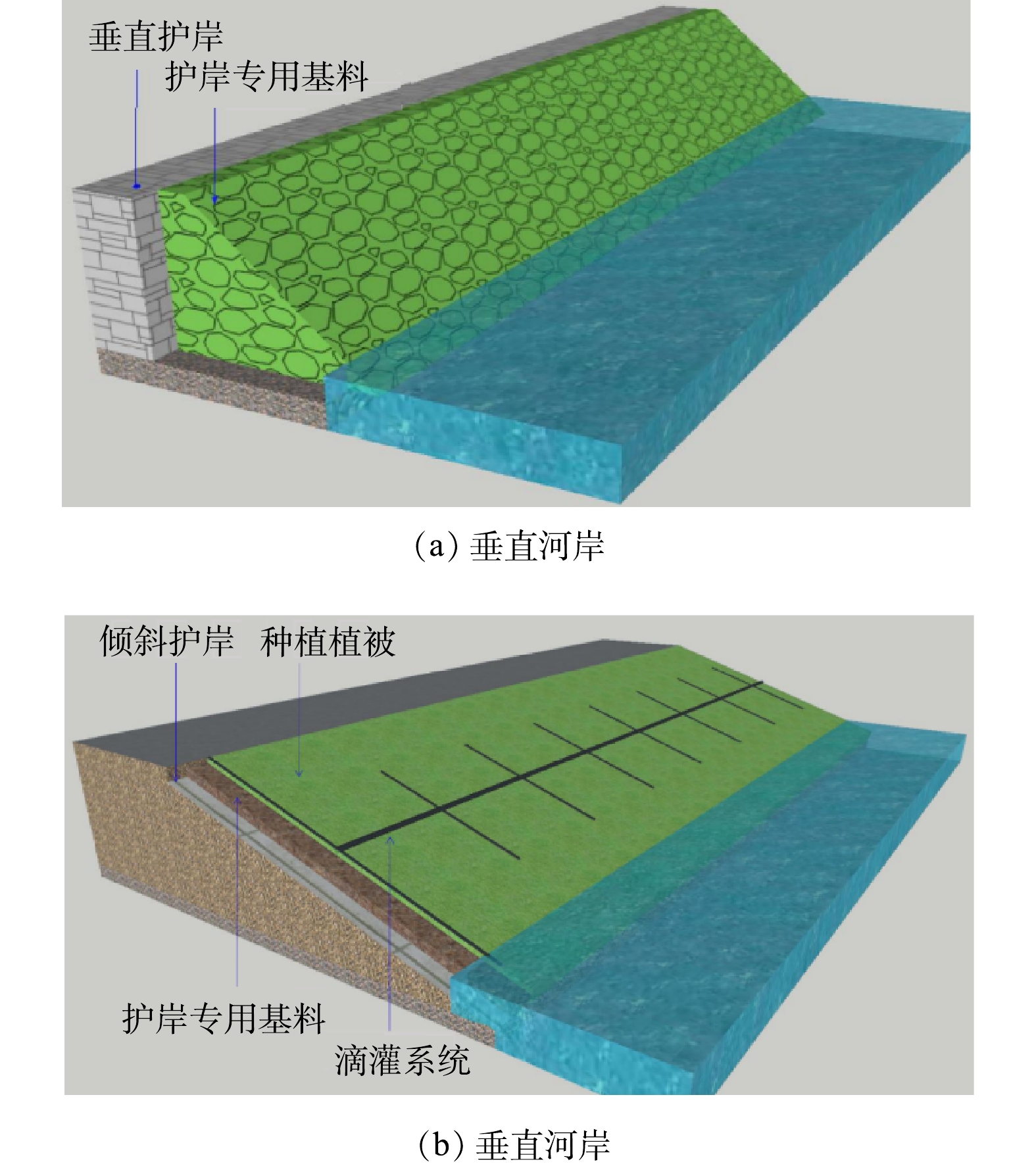
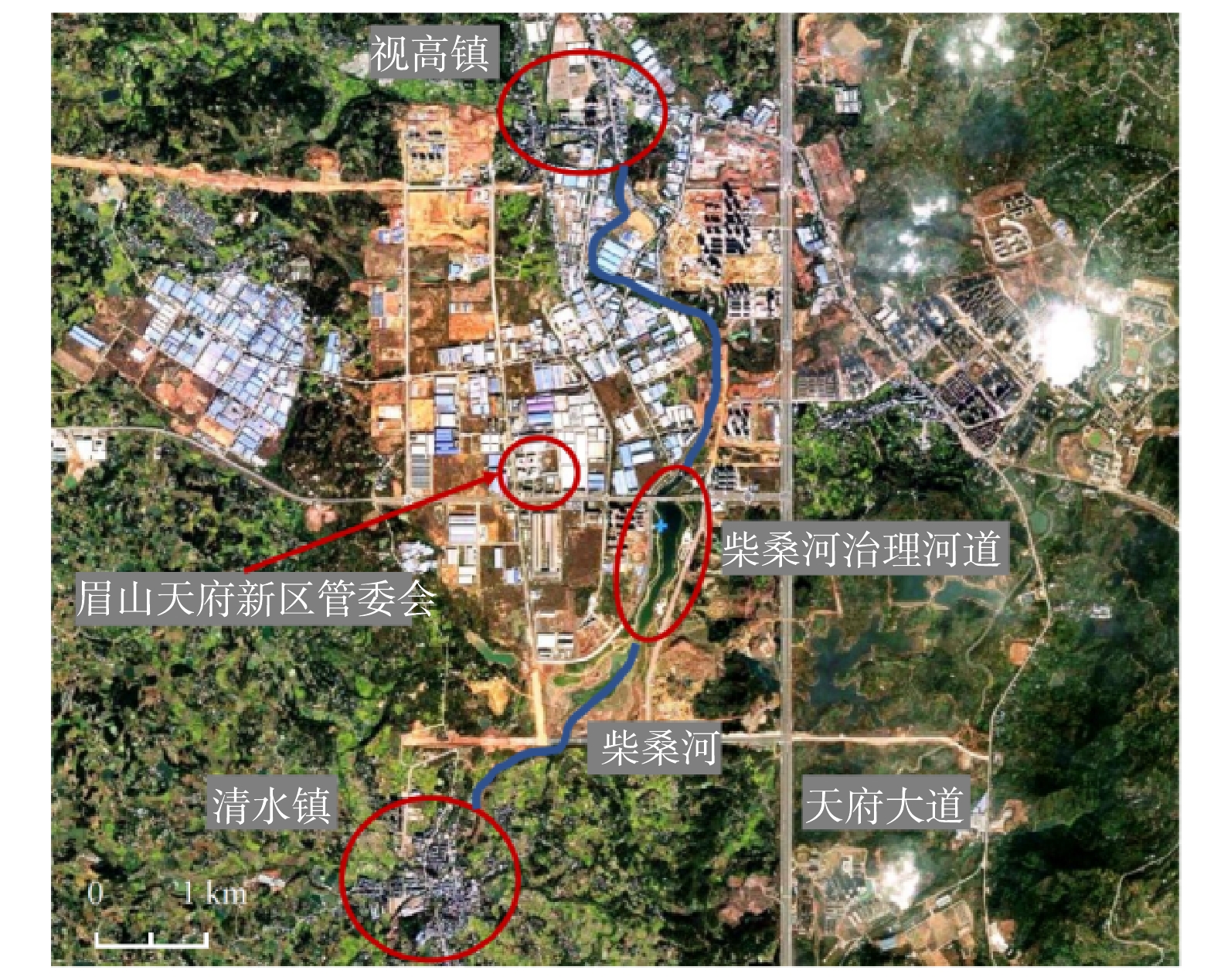
柴桑河治理河段位于四川省天府新区眉山片区,紧邻眉山天府新区管委会和天府大道,是天府新区眉山片区的重要水环境之一(图1)。柴桑河上游流经清水镇后,流入柴桑河治理河道,然后经过天府新区眉山片区,进入视高镇区域。柴桑河治理区域介于2个拦水坝之间,河道长度约为1.5 km,水面宽为80~100 m,平均水深约为1.85 m。柴桑河两岸为浆砌石护岸,无植被生长,水体浑浊,水面漂浮有大量垃圾且有大量油膜,部分排污点发现黑灰色水体并伴有恶臭气味。
1.2 水体污染成因分析
1)上游来水水质较差。前些年柴桑河上游清水镇有近5 万人的居民生活污水和城镇工业生产污水直接排入,致使柴桑河污染严重。
2)治理河段未有效拦截污染物。调查发现,柴桑河治理河段存在排污口,周围建设用水及工人生活用水可能直接排入河中。
3)河流两岸均为浆砌石硬质河岸,阻断了土壤与水体之间的物质交换,水体自净能力差。河段上下游均设置拦水坝,水体流速缓慢,水体长期滞留,污染物无法及时被稀释扩散。
1.3 水体检测及评价
根据当地政府提供的2020年1—4月,清水镇出境和视高镇入境的监测断面水质监测数据(表1),同时参照GB 3838-2002《地表水环境质量标准》进行评价,柴桑河水质为劣Ⅴ类水,水体为重度富营养化状态。
表 1 柴桑河水质状况(2020年1—4月)Table 1. The water quality of Chaisang River (January to April 2020)水质及标准 TP/(mg·L−1) TN/(mg·L−1) NH3-N/(mg·L−1) CODMn/(mg·L−1) GB 3838-2002 V类水标准 ≤0.4 — ≤2.0 ≤15 柴桑河水质 0.16~9.35 10.9~27.6 2.02~25.8 7.3~36 1.4 “一河一策”的治理方案
柴桑河治理河段的主要问题是浆砌石硬质河岸降低了水体自净能力,水体氮磷污染超标,两岸有排污口排入污水,两端有大坝拦截造成水流速度缓慢,不利于污染物的稀释扩散(全年平均风速为1.3 m·s−1)。浆砌石硬质河岸破坏了水体和两岸的物质交换和能量流动,因此,成本低、简单易操作且不破坏原有硬质河岸行洪能力的生态重建方式对水体恢复是至关重要的。本研究选择直接铺设护岸专用基料种植适宜植物,配备滴灌系统为植物提供水分,不仅能够在不破坏原有浆砌石硬质河岸的基础上对河岸进行生态修复,恢复水体自净能力,而且能够改善河岸景观,缓冲岸上氮磷来源对水体的影响。
治理河段在水质方面的主要问题是水体中氮磷等营养物质的浓度超标,因此,去除水体中氮磷的含量是恢复河流生态系统的关键。因除磷剂质地轻,无需外加设备,能够长期悬浮在水体中,故通过施用除磷剂,可以快速高效地去除水体中磷的含量;微生物菌剂是目前水体去除氮磷的常用方法,施用土著微生物菌剂,可以充分利用微生物的生长繁殖消耗水体中的氮磷。另外,治理河段周围为公园环境,水体治理也应考虑与周围景观相契合。设置生态浮床,利用植物生长消耗水体中氮磷,为微生物提供附着的场所,同时还可以改善水面景观环境,与当地公园景观相匹配。
针对治理河段两端设置拦水坝,当地风速小,水流速度缓慢从而导致水体污染物稀释扩散难的问题,本研究在河道中放置水车式增氧机,一方面为水体增氧,使污染物更易稀释扩散,另一方面能够扰动水体表面,使水面油膜等漂浮物沉降下来。同时,为了给滴灌系统和水车式增氧机供能,考虑采用光伏太阳能发电,使系统自运行,降低运行成本,方便后期的运营管理。
2. 材料和方法
2.1 硬质河岸生态重建
选用质量分数为30%的膨润土和70%的腐熟污泥组成的护岸专用基料进行硬质河岸的生态重建[19]。护岸专用基料养分含量丰富,阳离子交换量高,有利于生物生长,同时能有效拦截入河污染物。河道上游段河岸倾角约90°,在水上和水下部分使用装有护岸专用基料并混有植物种子的生态袋堆砌铺设为一个梯形(图2(a));下游段河岸倾角约为25°~30°,在水上和水下部分设置挡板,直接将护岸专用基料铺设在河岸表面,铺设厚度为15~30 cm,同时在铺设好的护岸基料表面播撒狗牙根、三叶草、波斯菊和硫化菊4种植物(图2(b))。为了满足河岸植被生长的水分要求,安装滴灌系统,利用河水对河岸植被进行灌溉。滴灌系统设计总长度750 m,沿河道两岸布置。水泵参数:Q为5 m3·h−1,H为30 m,配合自控系统实现自动运行,同时可根据干旱程度调节滴灌量。
2.2 富营养水体治理
1)除磷剂。除磷剂是根据《一种高效去除富营养水体中磷的方法》专利技术制备而成,具体是利用80%普通硅酸盐水泥与20%膨润土混合均匀[20]。除磷剂为粉末状,难溶于水,可直接加入水体中,加入后可均匀分散于水中并与水反应,无需任何外加设施设备的辅助。根据柴桑河治理河段的总蓄水量,按照5 g·m−3的剂量投加除磷剂,总投入1 250 kg除磷剂。
2)微生物菌剂。本项目使用的微生物菌剂是由水体中能够高效去除氮磷污染物,以硝化菌和反硝化菌为主的土著微生物分离制备而成。土著微生物能够更好地适应当地的水生生态环境,有效地发挥降解污染物的作用。按20 g·m−3的剂量计算微生物菌剂的投加量,柴桑河治理河段一次性投入5 000 kg微生物菌剂。将难溶于水、比表面积大且微生物易附着的特殊材料固定投放在水体中,形成云膜系统,为微生物提供栖息之地,增加微生物的生物量,让微生物菌剂能够长期发挥作用。根据水域面积,每1 000 m2配置1套云膜系统,另外在两岸每个排污口同时放置1套云膜系统,总共145 套。
3)生态浮床。本项目以环保PE材料为浮床框架,同时种植目前在生态浮床方面常用的紫色鸢尾、美人蕉和狐尾藻。在污染严重的入河排口处设置小型生态浮床,在中游和下游河道中间分别设置生态浮床,柴桑河河段共设置生态浮床800 m2(图3(a))。
4)水车式增氧机。柴桑河治理河段选用12个水车式增氧机(图3(a)),利用太阳能供电对水体进行曝气,每小时工作3~5 min。
2.3 太阳能光伏系统
柴桑河治理河段共安装2 套功率为12 kW的太阳能光伏发电系统,配合PLC自动控制程序,为整个柴桑河综合治理系统供电(图3(b))。太阳能光伏系统能够直接利用太阳能为水体中水车式增氧机和滴灌系统提供能源,以降低系统的运行成本。
2.4 水质监测
为了验证富营养水体的综合治理效果,对柴桑河治理河段的治理过程进行了水质监测,频度为每月1次,共进行了为期6个月的跟踪监测。分别在柴桑河治理河段上游、中游和下游设置监测点位,同时在河段中间的明显的排污口处设置1个监测点位,共4个监测点位。2020年12—2021年1月,项目施工阶段,各项综合治理措施已基本设置完毕。2021年2月受新冠疫情影响,无法监测水质状况。在2021年3—6月,连续每月对河段设置的监测点位进行水质监测。
总磷(TP)的测定参照GB 11893-1989《水质 总磷的测定 钼酸铵分光光度法》,总氮(TN)的测定参照HJ 636-2012《水质 总氮的测定 碱性过硫酸钾消解紫外分光光度法》,氨氮(NH3-N)的测定参考HJ 538-2009《水质 氨氮的测定 纳氏试剂分光光度法》,高锰酸盐指数(CODMn)的测定参照GB 11892-1989《水质 高锰酸盐指数的测定》,pH的测定参照GB 6920-1986《水质 pH 值的测定 玻璃电极法》,溶解氧(DO)的测定参考GB 11913-1989《水质溶解氧的测定 电化学探头法》。使用ZEISS Axioskop40立式显微镜对水体中的微生物进行观察。
3. 结果与讨论
3.1 水质提升效果
根据前期当地政府提供的监测数据,治理前柴桑河属于劣Ⅴ类水,治理后TP、TN、NH3-N和CODMn指标下降明显(图4)。2020年12月—2021年1月,河道中水体受项目施工影响,水质状况不稳定。2021年3—6月,水体TP和NH3-N符合地表水Ⅲ类水标准,CODMn符合地表水Ⅳ水标准并接近地表水Ⅲ类水标准,TN符合地表水湖泊、水库Ⅴ类水标。根据GB 3838-2002《地表水环境质量标准》,河流水体不考核TN,因此,项目施工完成后,柴桑河治理河段水体稳定达到地表水Ⅳ水标准。
在2020年12月—2021年6月的连续监测中,排污口间歇性的排入高氮、磷的污水,排入的污水TP最高达1.493 mg·L−1,TN最高达21.952 mg·L−1,NH3-N最高达18.651 mg·L−1(表2)。本研究使用的综合治理技术不仅处理了水体中原有的污染物,同时容纳了一定程度的污水排入,增加了河道水体的环境容量,使河道水体保持稳定。
表 2 排污口处连续监测数据Table 2. Continuous monitoring data at the sewage outlet采样日期 pH DO/(mg·L−1) CODMn/(mg·L−1) TP/(mg·L−1) TN/(mg·L−1) 2020-12 7.93 8.8 8.30 0.057 2.472 2021-01 7.90 6.8 11.80 1.493 21.952 2021-03 8.29 11.3 3.49 0.141 1.712 2021-04 8.05 8.8 6.99 1.033 9.324 2021-05 7.73 6.1 6.00 0.213 2.518 2021-06 7.83 6.1 6.05 0.236 1.860 3.2 生态景观效益
柴桑河治理前水体浑浊,表面有大量油膜覆盖,河岸两侧均为浆砌石硬质河岸,无植被覆盖,整体感官效果较差。治理后水体为浅绿色,河岸两侧全部被植被覆盖,与周围公园景观融为一体。在前期施工过程中,河岸两侧仅播种三叶草、波斯菊和硫化菊4种植物的种子。通过为期6个月的观察发现,河岸通过自然演替生长出大量的空心莲子草、鬼针草、稗草和狗尾草等其他植物,植物种类有数十种。河流经过治理后,观察发现,有大量鸟类觅食,水体中鱼类的数量大大增加,同时发现大量水草。通过光学显微镜观察发现,水体中藻类生物多样性和生物活跃性增加,发现了大量的绿藻、裸藻、甲藻和硅藻。浮游藻类与水生生态环境息息相关,能够从种类和数量上直接反应水质的变化[21-23]。柴桑河河段的藻类生物多样性和活跃性的增加一定程度上也说明了水生生态系统恢复健康和活力。
3.3 经济社会效益
底泥疏浚作为目前富营养水体治理过程中的常用方法,投入产出比及其可能对生态治理的负面影响都是值得重视的问题[24]。疏浚项目通常涉及的投资费用较大,且在消减沉积物中污染物含量的同时可能会导致污染物向水体中释放,对底栖生物造成损害,降低生物多样性,降低生态系统对外界物理干扰的抵抗能力[25-26]。生态环保且成本更低的新型技术是目前社会发展所需要的富营养水体治理技术。
柴桑河治理河段全长为1.5 km,水面宽为80~100 m,平均水深约为1.85 m,利用综合治理技术对其进行水质提升和环境改善,项目总投资约为320 万元。采用硬质河岸生态重建、微生物菌剂、除磷剂、生态浮床、水车式增氧机和太阳能光伏系统等技术综合治理柴桑河河段,匹配生态系统构成所需的要素,可在提升水质的同时打造优美的景观环境,为周围居民提供一个良好的休闲环境。与目前常用的治理技术相比,该项综合治理技术成本更低,无需外加能源,无需大量机械且能够长期维持水质等优点,符合社会发展的需求。
3.4 运营管理建议
河道治理后的运营维护对水体水质长效保持十分重要。后期运营维护可分为以下4点:第一,因柴桑河有较多排口,所以需特别注意突发的大量污水排入破坏整个河流生态系统平衡的情况,应根据情况及时补充微生物菌剂或者除磷剂;第二,雇佣专人巡视,以确保各项综合措施如水车式增氧机和滴灌系统等正常运行;第三,定期监测水质和底泥状况,同时对水体中微生物进行显微镜观察,便于了解水体和水生生物的实际状况,根据监测结果制定相应的治理控制措施;第四,若冬季水温低,应格外注意水体水质状况,根据情况补充适量除磷剂。治理后6个月内的监测频率可为1月1次,待系统稳定后可适当延长监测周期。
4. 结论
1)在浆砌石硬质河岸上铺设护岸专用基料后,播撒植物种子,配合滴灌系统为植物提供水分,对硬质河岸进行生态重建,不仅可改善1河流两岸的景观环境,而且将水体与河流两岸连接起来,增加河流生态系统的生物多样性,增强河道的自净能力。
2)施用除磷剂和微生物菌剂,安装生态浮床、水车式增氧机和太阳能光伏系统对柴桑河水体进行综合治理,能够有效地降低TP、TN、NH3-N和CODMn等指标含量,水体水质由前期劣Ⅴ类水,TP和NH3-N提升至地表水Ⅲ类水标准,CODMn提升至地表水Ⅳ水标准,TN提升至地表水Ⅴ类水标准。
3)本研究采用的综合治理技术不清淤不疏浚,成本低且操作简单,可为我国富营养水体的治理提供参考。
致 谢 感谢项目合作方四川省环境保护治理工程有限公司的大力支持。感谢成都纺织专科高等技术学校税永红教授团队水质监测的技术支持。感谢中国科学院成都山地灾害与环境研究所邱敦莲研究员对文章撰写和修改提出建议。
-
表 1 生物质燃烧排放的PM2.5的化学组成和WSOM的光谱指标
Table 1. Chemical composition in PM2.5 and spectral index of WSOM in PM2.5 emitted from biomass burning
项目Projects 草本类 Herbaceous 木本类 Woody 平均值Mean 最大值Maximum 最小值Minimum 平均值Mean 最大值Maximum 最小值Minimum OC/TC 0.91 ± 0.04* 0.94 0.84 0.81 ± 0.09* 0.89 0.67 EC/TC 0.09 ± 0.04* 0.16 0.06 0.19 ± 0.09* 0.33 0.11 OC/EC 11.89 ± 3.56** 15.40 5.23 5.21 ± 2.34** 7.94 2.00 WSOM/OC 0.30 ± 0.06 0.41 0.25 0.30 ± 0.05 0.39 0.25 SUVA254/ (m2·g−1) 2.28 ± 0.19 2.50 1.92 2.25 ± 0.27 2.60 1.79 E250/E365 5.79 ± 0.63 6.34 4.56 6.39 ± 0.70 7.65 5.57 MAE365/ (m2·g−1) 0.94 ± 0.14 1.17 0.73 0.84 ± 0.11 1.02 0.66 注:用t检验法进行分析.同一行中草本类与木本类相比,**表示差异性极显著(P<0.01),*表示差异性显著(P<0.05),不标注者则为不显著(P>0.05). Note:Analyze with t-test method. In the same row, compared with herbaceous species and woody species, ** means the difference is extremely significant (P<0.01), * means the difference is significant (P<0.05), and those not marked are not (P>0.05). 表 2 不同生物质燃烧排放PM2.5中WSOM的三维荧光光谱区域积分分析
Table 2. Volume integral of different area in 3D-EEM of WSOM in PM2.5 emissions from different biomass burning
样品Sample 区域ⅠRegion Ⅰ 区域ⅡRegion Ⅱ 区域ⅢRegion Ⅲ 区域ⅣRegion Ⅳ 区域ⅤRegion Ⅴ Ph/Pp* 高粱 0.07 0.31 0.23 0.23 0.16 0.64 玉米 0.09 0.33 0.25 0.20 0.13 0.63 水稻 0.08 0.33 0.23 0.22 0.14 0.59 小麦 0.09 0.33 0.23 0.23 0.13 0.55 花生叶 0.10 0.34 0.22 0.22 0.12 0.51 杂草 0.11 0.36 0.23 0.19 0.11 0.53 松树 0.12 ± 0.03 0.36 ± 0.02 0.19 ± 0.02 0.23 ± 0.01 0.11 ± 0.02 0.42 ± 0.05 杉树 0.12 ± 0.03 0.36 ± 0.01 0.20 ± 0.01 0.21 ± 0.01 0.10 ± 0.01 0.43 ± 0.05 草本类 0.09 ± 0.02 0.33 ± 0.02 0.23 ± 0.01 0.21 ± 0.02 0.13 ± 0.02 0.57 ± 0.05 木本类 0.12 ± 0.02 0.36 ± 0.01 0.19 ± 0.02 0.22 ± 0.01 0.10 ± 0.01 0.42 ± 0.04 *: Ph/Pp=∑ (Ⅲ + Ⅴ)/∑ (Ⅰ + Ⅱ + Ⅳ) 表 3 不同来源WSOM荧光特征参数对比
Table 3. Comparison of fluorescence special parameters for WSOM samples from different sources
样品Sample 来源Source HIX FI BIX AFI/TOC 文献References 草本类 湖南 0.91 ± 0.17** 2.57 ± 0.11** 1.38 ± 0.05** 0.37 ± 0.06 本研究 木本类 0.59 ± 0.10** 2.28 ± 0.14** 1.61 ± 0.11** 0.35 ± 0.09 总体 0.49—1.09 2.03—2.68 1.32—1.81 0.23—0.50 杨木 滁州 0.17 ± 0.03 2.10 ± 0.07 2.17 ± 0.06 — [8] 毛竹 池州 0.06 ± 0.01 2.28 ± 0.06 2.40 ± 0.09 — 燃煤 兰州 0.16—0.71 1.84—2.47 0.83—1.29 0.20 ± 0.29 [15] 大气气溶胶 兰州 1.0—2.6 0.2—2.1 1.2—1.6 — [9] 南京 7.07 ± 2.41 1.14—4.22 0.88 ± 0.08 — [31] 雾水 泰山 3.32—6.79 1.42—1.83 0.64—1.02 — [30] 雨水 重庆 0.61—4.79 1.32—1.54 0.64—1.12 — [26] 山东枣庄 1.03—2.07 1.34—1.67 0.78—0.87 — [27] 注:用t检验法进行分析.同一列中木本类与草本类相比,**表示差异性极显著(P<0.01),*表示差异性显著(P<0.05),不标注者则为不显著(P>0.05). Note:Analyze with t-test method. In the same column, compared with herbaceous species and woody species, ** means the difference is extremely significant (P<0.01), * means the difference is significant (e<0.05), and those not marked are not (P>0.05). 表 4 生物质燃烧排放PM2.5中WSOM的吸光特征参数与荧光指标的相关性分析
Table 4. Correlations analysis between light absorption and fluorescence index of WSOM in PM2.5 emitted from biomass burning
MAE365 SUVA254 E250/E365 HIX BIX FI MAE365 1 0.444* −0.914** 0.795** −0.698** −0.318 SUVA254 1 0.090 0.175 −0.287 0.073 E250/E 365 1 −0.753** 0.590** 0.365* HIX 1 −0.883* −0.265 BIX 1 0.074 FI 1 注:**表示在0.01水平(双侧)上显著相关,*表示在0.05水平(双侧)上显著相关. Note:**means significant correlation at 0.01 level (2-tailed), * means significant correlation at 0.05 level (2-tailed). -
[1] DUARTE R M B O, SANTOS E B H, PIO C A, et al. Comparison of structural features of water-soluble organic matter from atmospheric aerosols with those of aquatic humic substances [J]. Atmospheric Environment, 2007, 41(37): 8100-8113. doi: 10.1016/j.atmosenv.2007.06.034 [2] 闫语, 张阳, 张元勋. 大气颗粒物中水溶性有机物的研究进展 [J]. 环境科学研究, 2019, 32(11): 1800-1808. YAN Y, ZHANG Y, ZHANG Y X. The advances of water-soluble organic compounds in atmospheric particles [J]. Research of Environmental Sciences, 2019, 32(11): 1800-1808(in Chinese).
[3] ZONG Z, WANG X P, TIAN C G, et al. Source and formation characteristics of water-soluble organic carbon in the anthropogenic-influenced Yellow River Delta, North China [J]. Atmospheric Environment, 2016, 144: 124-132. doi: 10.1016/j.atmosenv.2016.08.078 [4] BAE M S, SCHAUER J J, LEE T, et al. Relationship between reactive oxygen species and water-soluble organic compounds: Time-resolved benzene carboxylic acids measurement in the coastal area during the KORUS-AQ campaign [J]. Environmental Pollution, 2017, 231: 1-12. doi: 10.1016/j.envpol.2017.07.100 [5] ZHANG Y L, EL-HADDAD I, HUANG R J, et al. Large contribution of fossil fuel derived secondary organic carbon to water soluble organic aerosols in winter haze in China [J]. Atmospheric Chemistry and Physics, 2018, 18(6): 4005-4017. doi: 10.5194/acp-18-4005-2018 [6] HECOBIAN A, ZHANG X, ZHENG M, et al. Water-Soluble Organic Aerosol material and the light-absorption characteristics of aqueous extracts measured over the Southeastern United States [J]. Atmospheric Chemistry and Physics, 2010, 10(13): 5965-5977. doi: 10.5194/acp-10-5965-2010 [7] DUARTE R M B O, DUARTE A C. A critical review of advanced analytical techniques for water-soluble organic matter from atmospheric aerosols [J]. Trends in Analytical Chemistry, 2011, 30(10): 1659-1671. doi: 10.1016/j.trac.2011.04.020 [8] 范行军, 操涛, 余旭芳, 等. 薪柴燃烧溶解性棕色碳排放特征及光学性质 [J]. 中国环境科学, 2019, 39(8): 3215-3224. doi: 10.3969/j.issn.1000-6923.2019.08.011 FAN X J, CAO T, YU X F, et al. Emission characteristics and optical properties of extractable brown carbon from residential wood combustion [J]. China Environmental Science, 2019, 39(8): 3215-3224(in Chinese). doi: 10.3969/j.issn.1000-6923.2019.08.011
[9] QIN J J, ZHANG L M, ZHOU X M, et al. Fluorescence fingerprinting properties for exploring water-soluble organic compounds in PM2.5 in an industrial city of northwest China [J]. Atmospheric Environment, 2018, 184: 203-211. doi: 10.1016/j.atmosenv.2018.04.049 [10] FAN X J, WEI S Y, ZHU M B, et al. Comprehensive characterization of humic-like substances in smoke PM2.5 emitted from the combustion of biomass materials and fossil fuels [J]. Atmospheric Chemistry and Physics, 2016, 16(20): 13321-13340. doi: 10.5194/acp-16-13321-2016 [11] 王真真, 谭吉华, 毕新慧, 等. 秸秆燃烧产生颗粒物化学组分及排放特征 [J]. 环境科学与技术, 2016, 39(11): 150-155. WANG Z Z, TAN J H, BI X H, et al. Emission characteristics and chemical species from agricultural straw burning smoke [J]. Environmental Science & Technology, 2016, 39(11): 150-155(in Chinese).
[12] TAN J H, ZHANG L M, ZHOU X M, et al. Chemical characteristics and source apportionment of PM2.5 in Lanzhou, China [J]. Science of the Total Environment, 2017, 601: 1743-1752. [13] XIAO K, SUN J Y, SHEN Y X, et al. Fluorescence properties of dissolved organic matter as a function of hydrophobicity and molecular weight: Case studies from two membrane bioreactors and an oxidation ditch [J]. RSC Advances, 2016, 6(29): 24050-24059. doi: 10.1039/C5RA23167A [14] COBLE P, LEAD J, BAKER A, et al. Aquatic organic matter fluorescence[M]. Cambridge: Cambridge University Press, 2014: 75-122. [15] YANG Y R, QIN J J, QI T, et al. Fluorescence characteristics of particulate water-soluble organic compounds emitted from coal-fired boilers [J]. Atmospheric Environment, 2020, 223: 117297. doi: 10.1016/j.atmosenv.2020.117297 [16] 洪蕾, 刘刚, 杨孟, 等. 稻草烟尘中有机碳/元素碳及水溶性离子的组成 [J]. 环境科学, 2015, 36(1): 25-33. HONG L, LIU G, YANG M, et al. Composition of organic carbon / elemental carbon and water-soluble ions in rice straw burning [J]. Environmental Science, 2015, 36(1): 25-33(in Chinese).
[17] 朱恒, 戴璐泓, 魏雅, 等. 生物质燃烧排放PM2.5中无机离子及有机组分的分布特征 [J]. 环境科学学报, 2017, 37(12): 4483-4491. ZHU H, DAI L H, WEI Y, et al. Characteristics of inorganic ions and organic components in PM2.5 from biomass burning [J]. Acta Scientiae Circumstantiae, 2017, 37(12): 4483-4491(in Chinese).
[18] 刘刚, 黄柯, 李久海, 等. 树木模拟燃烧排放烟尘中水溶性离子的组成 [J]. 环境科学, 2016, 37(10): 3737-3742. LIU G, HUANG K, LI J H, et al. Chemical composition of water-soluble ions in smoke emitted from tree branch combustion [J]. Environmental Science, 2016, 37(10): 3737-3742(in Chinese).
[19] PEURAVUORI J, PIHLAJA K. Molecular size distribution and spectroscopic properties of aquatic humic substances [J]. Analytica Chimica Acta, 1997, 337(2): 133-149. doi: 10.1016/S0003-2670(96)00412-6 [20] BADUEL C, VOISIN D, JAFFREZO J L. Seasonal variations of concentrations and optical properties of water soluble HULIS collected in urban environments [J]. Atmospheric Chemistry and Physics, 2010, 10(9): 4085-4095. doi: 10.5194/acp-10-4085-2010 [21] DUARTE R M B O, DUARTE A C. Application of non-ionic solid sorbents (XAD resins) for the isolation and fractionation of water-soluble organic compounds from atmospheric aerosols [J]. Journal of Atmospheric Chemistry, 2005, 51(1): 79-93. doi: 10.1007/s10874-005-8091-x [22] LI M J, FAN X J, ZHU M B, et al. Abundance and light absorption properties of brown carbon emitted from residential coal combustion in China [J]. Environmental Science & Technology, 2019, 53(2): 595-603. [23] CHENG Y, HE K B, ZHENG M, et al. Mass absorption efficiency of elemental carbon and water-soluble organic carbon in Beijing, China [J]. Atmospheric Chemistry and Physics, 2011, 11(22): 11497-11510. doi: 10.5194/acp-11-11497-2011 [24] DU Z Y, HE K B, CHENG Y, et al. A yearlong study of water-soluble organic carbon in Beijing II: Light absorption properties [J]. Atmospheric Environment, 2014, 89: 235-241. doi: 10.1016/j.atmosenv.2014.02.022 [25] YAN C Q, ZHENG M, SULLIVAN A P, et al. Chemical characteristics and light-absorbing property of water-soluble organic carbon in Beijing: Biomass burning contributions [J]. Atmospheric Environment, 2015, 121: 4-12. doi: 10.1016/j.atmosenv.2015.05.005 [26] 梁俭, 江韬, 魏世强, 等. 夏、冬季降雨中溶解性有机质(DOM)光谱特征及来源辨析 [J]. 环境科学, 2015, 36(3): 888-897. LIANG J, JIANG T, WEI S Q, et al. Absorption and fluorescence characteristics of dissolved organic matter(DOM) in rainwater and sources analysis in summer and winter season [J]. Environmental Science, 2015, 36(3): 888-897(in Chinese).
[27] 周石磊, 孙悦, 张艺冉, 等. 基于UV-vis和EEMs解析白洋淀冬季冰封期间隙水DOM的光谱特征及来源 [J]. 环境科学学报, 2020, 40(2): 604-614. ZHOU S L, SUN Y, ZHANG Y R, et al. Spectral characteristics and sources of DOM in sediment interstitial water from Baiyangdian Lake in Xiong’an new area during the winter freezing period based on UV-Vis and EEMs [J]. Acta Scientiae Circumstantiae, 2020, 40(2): 604-614(in Chinese).
[28] SANTOS P S M, OTERO M, DUARTE R M B O, et al. Spectroscopic characterization of dissolved organic matter isolated from rainwater [J]. Chemosphere, 2009, 74(8): 1053-1061. doi: 10.1016/j.chemosphere.2008.10.061 [29] SANTOS P S M, SANTOS E B H, DUARTE A C. First spectroscopic study on the structural features of dissolved organic matter isolated from rainwater in different seasons [J]. Science of the Total Environment, 2012, 426: 172-179. doi: 10.1016/j.scitotenv.2012.03.023 [30] BIRDWELL J E, VALSARAJ K T. Characterization of dissolved organic matter in fogwater by excitation-emission matrix fluorescence spectroscopy [J]. Atmospheric Environment, 2010, 44(27): 3246-3253. doi: 10.1016/j.atmosenv.2010.05.055 [31] XIE X C, CHEN Y F, NIE D Y, et al. Light-absorbing and fluorescent properties of atmospheric brown carbon: A case study in Nanjing, China [J]. Chemosphere, 2020, 251: 126350. doi: 10.1016/j.chemosphere.2020.126350 [32] DUARTE R M B O, PIO C A, DUARTE A C. Synchronous scan and excitation-emission matrix fluorescence spectroscopy of water-soluble organic compounds in atmospheric aerosols [J]. Journal of Atmospheric Chemistry, 2004, 48(2): 157-171. doi: 10.1023/B:JOCH.0000036845.82039.8c [33] 范行军, 余旭芳, 操涛, 等. 广州冬季气溶胶中水溶性有机物和类腐殖质的吸光性和荧光光谱特性 [J]. 环境科学, 2019, 40(2): 532-539. FAN X J, YU X F, CAO T, et al. Light absorption and fluorescence characteristics of atmospheric water-soluble organic compounds and humic-like substances during the winter season in Guangzhou [J]. Environmental Science, 2019, 40(2): 532-539(in Chinese).
[34] XIAO K, SHEN Y X, SUN J Y, et al. Correlating fluorescence spectral properties with DOM molecular weight and size distribution in wastewater treatment systems [J]. Environmental Science:Water Research & Technology, 2018, 4(12): 1933-1943. [35] CHEN W, WESTERHOFF P, LEENHEER J A, et al. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter [J]. Environmental Science & Technology, 2003, 37(24): 5701-5710. [36] 吕晶晶, 龚为进, 窦艳艳, 等. PARAFAC和FRI解析ISI中DOM分布 [J]. 中国环境科学, 2019, 39(5): 2039-2047. doi: 10.3969/j.issn.1000-6923.2019.05.031 LÜ J J, GONG W J, DOU Y Y, et al. The distribution of DOM in aeration pretreatment improved soil infiltration system based on FRI and PARAFAC [J]. China Environmental Science, 2019, 39(5): 2039-2047(in Chinese). doi: 10.3969/j.issn.1000-6923.2019.05.031
[37] OHNO T, CHOROVER J, OMOIKE A, et al. Molecular weight and humification index as predictors of adsorption for plant- and manure-derived dissolved organic matter to goethite [J]. European Journal of Soil Science, 2007, 58(1): 125-132. doi: 10.1111/j.1365-2389.2006.00817.x [38] MCKNIGHT D M, BOYER E W, WESTERHOFF P K, et al. Spectrofluorometric characterization of dissolved organic matter for indication of precursor organic material and aromaticity [J]. Limnology and Oceanography, 2001, 46(1): 38-48. doi: 10.4319/lo.2001.46.1.0038 [39] FU P Q, KAWAMURA K, CHEN J, et al. Fluorescent water-soluble organic aerosols in the high arctic atmosphere [J]. Scientific Reports, 2015, 5: 9845. doi: 10.1038/srep09845 -




 下载:
下载: