-
地下水是维持人类生存和发展的一种最重要资源和生态环境因子[1]。近年来,我国经历了快速城市化和工业化,然而,污水的处理能力未能保持同步增长(尤其在农村地区)、农业化肥和农药过量使用、地下水超采严重等问题,已经引起地下水水化学特征发生改变[2-4]。众所周知,地下水水化学改变不仅能够干扰多种生态过程,同时也降低了地下水的使用价值[5]。因此,掌握地下水水化学的演化规律对于可持续利用地下水尤为重要[6-8]。
地下水水化学演化主要受控于自然因素和人类活动的综合影响。地下水水化学特征与自然因素(水文地质条件、包气带岩性、水岩交互作用和海水入侵)密切相关[9-10]。安乐生等研究发现,黄河三角洲浅层地下水化学特点形成的关键驱动因素是黄河入海流路变迁和海水入侵[11]。人类活动(如污水排放、农业施肥、地下水超采等)也严重影响了地下水水化学演化规律。Zhang等研究发现,地下水水化学特征受到了生活污水、工业污水和水岩交互作用的混合影响, 因此,为防止该地区地下水水质恶化,首先要控制污水的排放 [12]。郭高轩等研究表明,潮白河冲洪积扇不同深度地下水水化学具有分层分带特征,且在人类活动强烈区域,浅层地下水水质略差[13]。
中牟县位于郑州市东部新城区,地下水资源是该地区工农业生产的主要供水水源。近年来,随着人口的迅速增长和工业的高速发展、农业灌溉面积极速扩大,地下水的开采量日益增加。基于 2019 年对该地区地下水位统调工作发现,中牟县城一带已经形成一个较大的浅层地下水降落漏斗,并且研究区内人类活动强烈,存在农业面源污染、固体废弃物堆放场和工业污染等3类潜在污染来源,可能对地下水水化学特点构成一定影响。目前,针对该地区地下水水化学演化规律尚未开展深入研究工作,对该地区居民的健康饮水和社会经济可持续发展构成潜在威胁。
本研究针对郑州市中牟县地下水水化学演化机理开展研究,联合应用piper三线图、Gibbs图、离子比例系数法和多元统计技术等手段,识别研究区水化学特征,揭示该地区地下水水化学形成演化机制,探讨控制地下水水化学特征的主控因素,以期为快速城市化地区地下水的可持续开发利用提供科学依据。
-
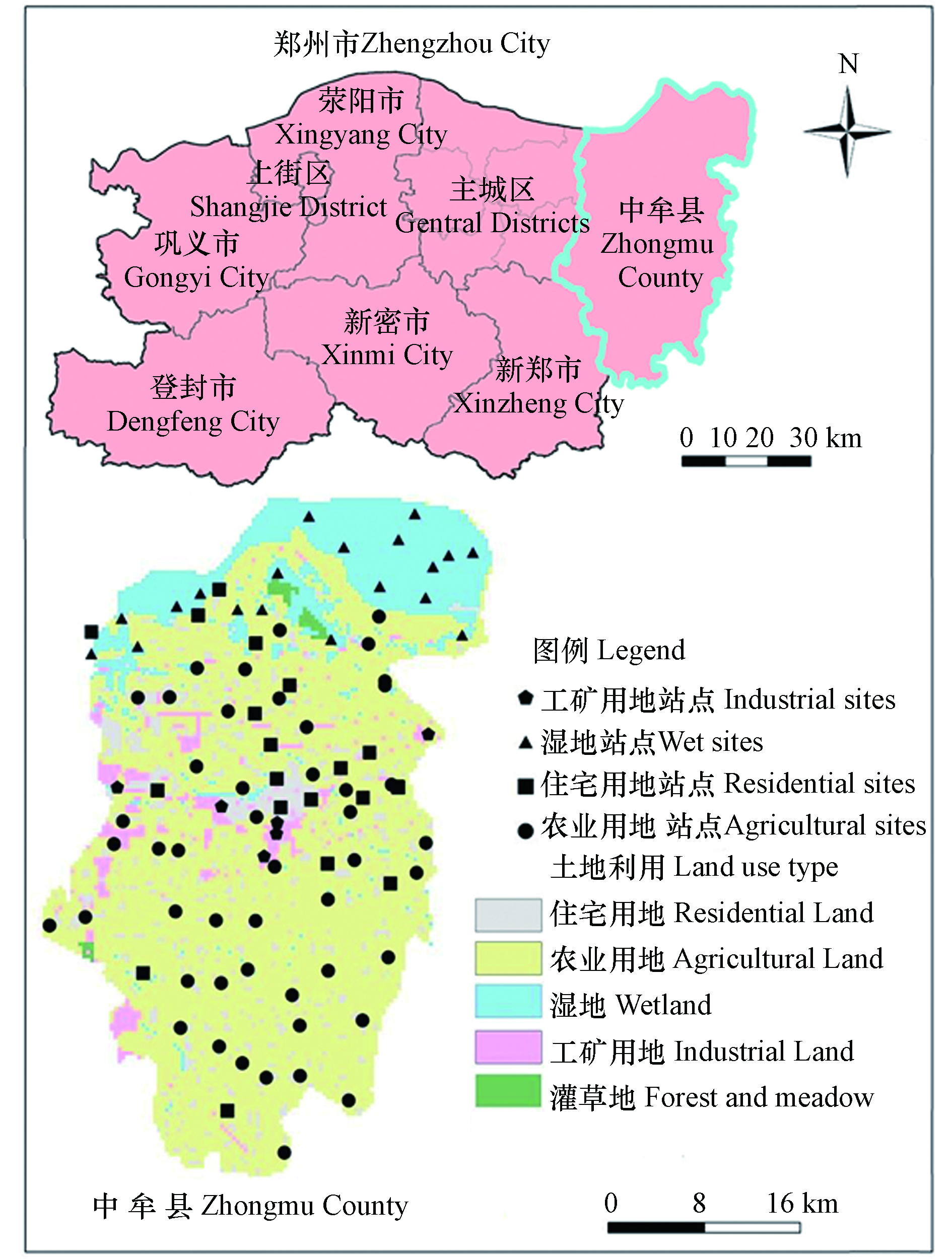
中牟县位于北纬34°26′—34°56′、东经113°46′—114°12′之间,地处中原腹地、河南省中部偏东,隶属郑州市。研究区属暖温带半干旱气候,具明显的大陆季风气候特征,四季分明。多年平均气温14.25℃,多年平均降雨量约为616 mm,年内降水多集中在7—9月,占全年降雨量的40%—48%. 多年平均蒸发量1769.8 mm,平均相对湿度66.3%。研究区总面积为917 km2,主要的土地利用类型为农业用地(68.7%)、居民区(9.2%)、工矿用地(4.3%)、水域(16.2%)(包括湿地和水体)和裸地(1.6%)(图1)。
-
研究区地貌类型为黄河冲积平原,地下水类型主要为松散岩类孔隙水,其含水层分布广,厚度大,水量丰富,可分为浅层水(<80 m)和中深层水(80—400 m)。浅层含水层主要由山前冲洪积与黄河冲积的细砂层组成,深度主要为 40—60 m,该含水层组埋藏浅,其下为一组粉质粘土或粉土弱透水层,与下伏中深层含水层组相隔,厚25—45 m。浅层水易于开采,为农业用水主要开采层,井深25—55 m。中深层含水层组底板埋深310—350 m,其下为厚层粘土夹薄层砂或砂的透镜体,粘土层厚度一般15—40 m,具有很好的隔水性,属承压水类型。中深层水是目前城乡小型集中供水的主要开采层,井深一般在100—300 m 左右。其含水层岩性为中砂、细砂、粗砂等,厚30—80 m,导水系数125—390 m2·d−1,贮水系数4×10−3,单位涌水量3—5 m3·h−1·m−1。地下水主要的补给来源为大气降水、河道侧漏和灌溉回水,主要的排泄方式为人工开采。
-
2020年6—8月采集郑州市中牟县地下水样品93组(图1),包括农业用地站点48个,湿地站点19个,住宅用地站点20个和工矿用地站点6个。采样点布设的原则主要依据不同的土地利用类型平均布设采样点,如果预布设站点区域内无地下水井,可以适当调整,但要保证2个采样点之间的距离大于1 km。地下水主要取自民井和农业灌溉井,采样井的深度范围是25—150 m。采样前抽水洗井10 min,用原水样清洗采样瓶3次,分别采集 1.5 L 和 0.5 L 水样各1瓶,用于分析阴阳离子。分析阳离子的水样加1∶1的
HNO−3 调节水样 pH<2。样品采集后,密封瓶口放入冷藏箱运回实验室,在48 h 内完成样品测试. -
样品测试的指标包括pH、TDS、K+、Na +、Ca2+、Mg2+、
NH+4 、NO−3 、NO−2 、SO2−4 、Cl−、CO2−3 、HCO−3 和总硬度(TH)。其中pH采用多参数水质分析仪—美国哈希HQ40D现场测定。其余指标参照国家饮用天然矿泉水检验方法标准(GB/T 8538-2008)测试。 -
(1)水化学类型判定。本研究按照舒克列夫分类法,即阴阳离子毫克当量百分比大于25%时参与命名。对研究区采样点地下水化学类型定名,并绘制出了地下水化学类型Piper三线图。
(2)地下水化学控制因素识别。选用Gibbs图识别地下水化学控制作用。通常情况下,水样位于 Gibbs 图右下角,表明其受大气降水作用影响较大,水样位于Gibbs 图左中部,表明岩石风化作用是该地区水化学的主要控制作用,而受蒸发结晶作用控制的水样将落于Gibbs 图右上角。
(3)离子来源识别。联合应用Ca2+/Na+ VS
HCO−3 /Na+和Mg2+/Na+ VSHCO−3 /Na+比值端元图识别地下水中离子来源。当水样点离子比值为HCO−3 /Na+=120,Ca2+/Na+= 50,Mg2+/Na+ =10时,表明地下水受碳酸盐岩风化作用控制为主;当水样点离子比值为HCO−3 /Na+=2±1,Ca2+/Na+= 0.35±0.15,Mg2+/Na+=0.24±0.12时,表明地下水主要受硅酸盐岩风化作用控制;而蒸发盐风化作用控制的水样通常位于比值图的左下角。(4)衬度系数方差。方差(Variance)用于刻画一个随机变量对其数学期望(均值)的离散程度。由于地下水各化学组分的绝对数值范围可能相差很大,无法进行方差的对比,为此,先求出每个样本每个变量(Xi)与该变量均值(
¯X )的比值,这里定义为衬度系数V,即Vi=Xi¯X ,由于衬度系数V的平均值为1,因此各变量就转化为均值相等的另一个变量(其衬度系数),然后对各变量的衬度系数求方差,即可进行方差对比。衬度系数方差(Vσi2)的计算公式如下:
式中,Vi是地下水第i个化学组分的衬度系数;
¯Vi 是地下水第i个化学组分的衬度系数的平均值。当Vσi2> 1时,说明该化学组分受人类活动影响强烈;当0.5<Vσi2<1时,说明该组分受中等强度的人类活动影响;当Vσi2<0.5时,说明该组分受人类活动影响较小。
此外,运用Spearman’s 秩相关系数分析了不同土地利用类型地下水水化学组分之间的相关关系。数据分析使用 R 语言(4.0.3)、Origin(2019b)和Arcgis 10.5。
-
研究区pH值的范围介于6.71—8.51之间,均值为7.62,地下水为中性到弱碱性水,样品的超标率为1.1%(表1)。TDS 变化范围为200—1408 mg·L−1,均值为612 mg·L−1。地下水样品中
CO2−3 的浓度均低于检出限,因此未参与统计。地下水中阳离子的大小排序为Ca2+ > Na+ > Mg2+ >K+ >NH+4 ,而阴离子的大小排序是HCO−3 >SO2−4 > Cl− >NO−3 >NO−2 。其中,超标率最高的阳离子是NH+4 ,超标率为6.5%,超标率最高的阴离子为NO−3 ,超标率为19.4%,反映出研究区地下水受到了人类活动的强烈影响,如化肥,污水等 [14]。TH反映了水中多价金属离子含量的总和,是地下水中一个重要的化学指标。在本研究区内,地下水TH的浓度范围介于28.3—978 mg·L−1之间,均值为414 mg·L−1,超标率高达39.8%,是研究区地下水中最主要的污染因子。饮用水中TH的浓度较高,可能诱发多种疾病,如血管疾病急性心肌梗塞和湿疹[15,16]。因此,当地环境管理者应当高度关注。 -
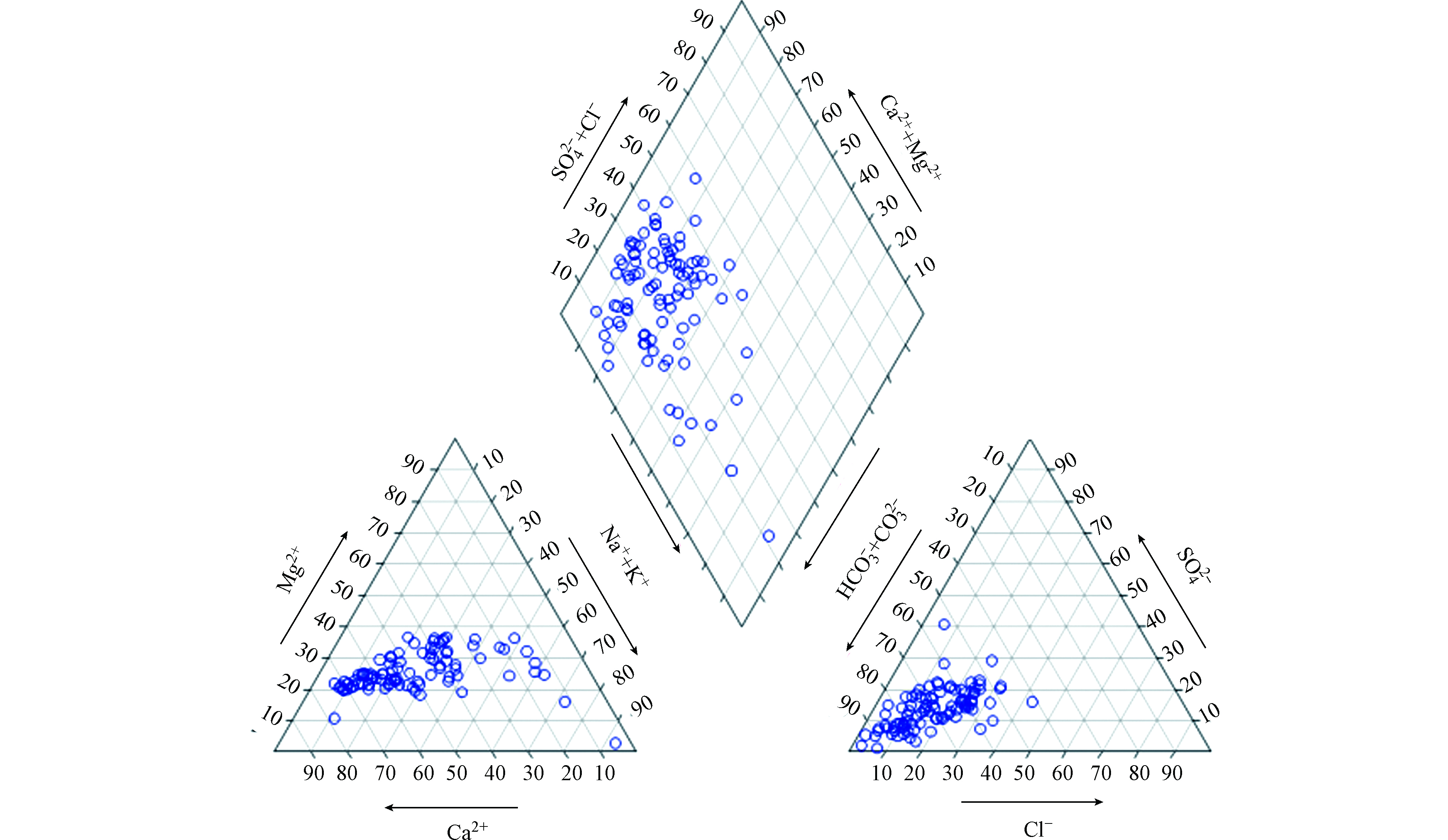
Piper三线图常用来表征地下水化学成分的演化规律[18]。由图2 可以看出,研究区地下水主要的水化学类型为HCO3-Ca(Mg)型,占总水样的46.2%。近年来,由于人类活动的干扰,地下水水化学类型趋于复杂化,出现了Cl型水(18.3%),Na型水(39.8%)和SO4型水(3.2%)。不同土地利用类型下地下水水化学类型有明显的区别。正如表2显示,在农业用地和工矿用地中,地下水主要的水化学类型是HCO3-Ca(Mg)型,但是,农业用地受到施肥的影响,水化学类型出现了Cl型水(20.8%)和SO4型水(6.25%)。住宅用地地下水主要的水化学类型是HCO3-Ca(Mg)型水(40.0%),并且Na型水出现的比例高达55.0%。此外,在湿地(郑州黄河湿地自然保护区)内,Na型水是地下水主要的水化学类型,占比高达89.5%,这主要与湿地地下水受到黄河水和污水处理厂回水混合影响有关。
-
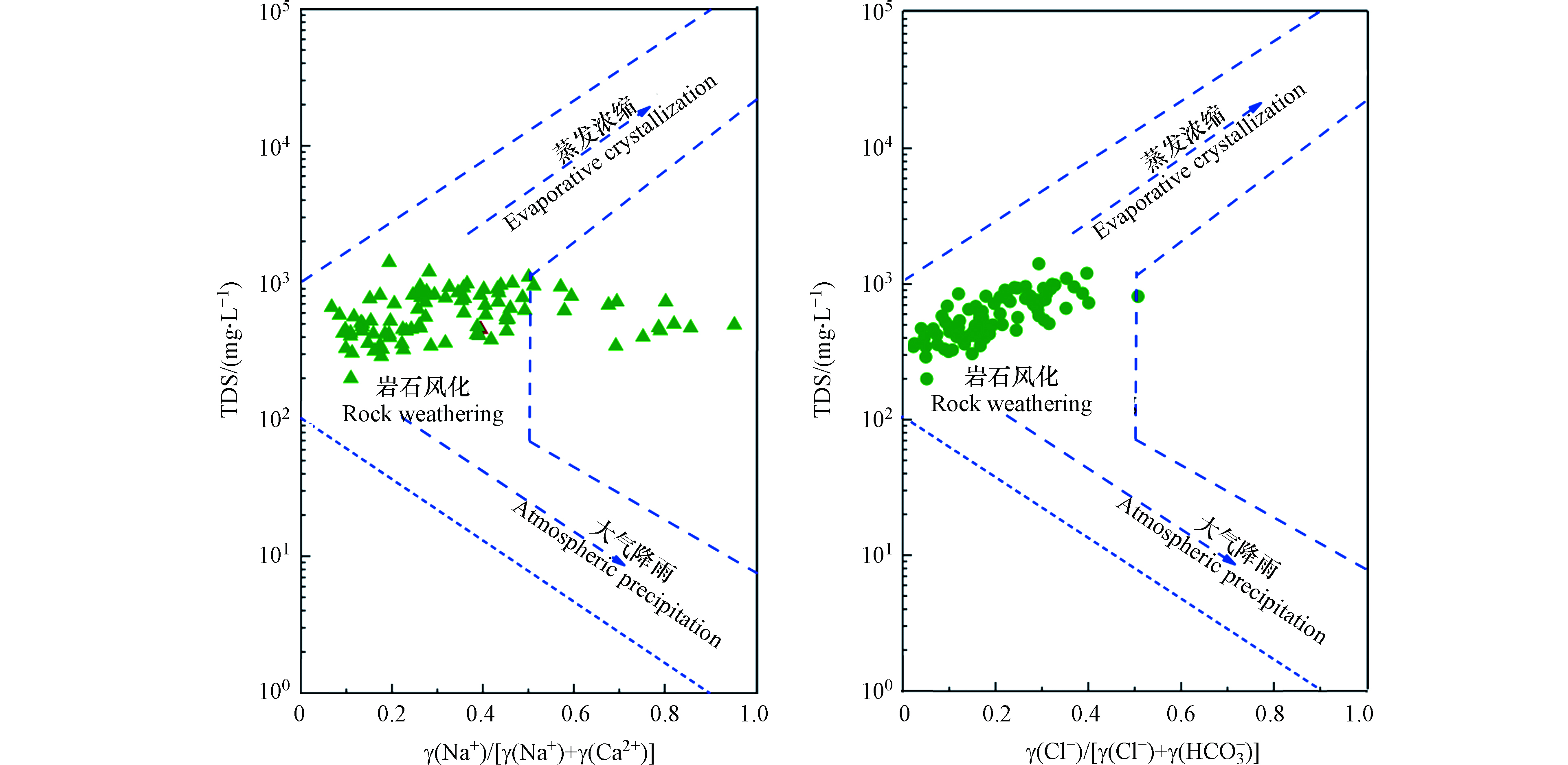
地下水化学组分的形成机制主要受控于大气降雨、岩石风化、蒸发浓缩和混合作用等[19]。正如图3显示,地下水采样点的离子含量投点绝大部分落于Gibbs图中间位置,表明岩石风化是研究区地下水水化学离子组分的主要控制因素。但是,研究区部分采样点,有向右上方区域偏移的趋势,说明蒸发-浓缩作用对研究区地下水的水化学组分也有一定的影响。此外,部分点位超出了岩石分化的控制边界,说明这些采样点的水化学组分受到人类活动的影响。
-
衬度系数方差可用于区分地下水化学组分的形成以天然条件演化作用为主,还是受人类活动影响较大。地下水化学组分的衬度系数方差越大,表明该组分受人类活动影响就越强烈[20]。由表3可见,整体上看,在不同土地利用类型中地下水中的Ca2+、Mg2+和
HCO−3 均受人类活动影响较小。然而,农业用地、居住用地和工矿用地地下水三氮(NH+4 、NO−3 和NO−2 )的衬度系数方差值均大于1,表明三者均受到人类活动的强烈的影响。值得注意的是,在农业用地地下水中,K+的衬度系数方差值大于1, Cl−、SO2−4 和K+的衬度系数方差值介于0.5—1之间,说明农业的活动对它们存在强烈和中等强度的影响。此外,在住宅用地地下水中,人类活动对Cl−和K+有中等强度的影响,而人类活动对工矿用地地下水中Cl−和SO2−4 也存在强烈和中等强度的影响。 -
为了进一步探讨地下水化学组分的来源,联合应用Ca2+/Na+ VS
HCO−3 /Na+和Mg2+/Na+ VSHCO−3 /Na+比值端元图来进一步区分地下水水化学组分是来自碳酸盐岩风化、硅酸盐岩风化还是蒸发盐岩风化[21]。由图4可以看出,研究区内水样主要集中于硅酸盐岩与碳酸盐岩控制端元之间,表明研究区地下水化学组分主要受控于硅酸盐岩与碳酸盐风化溶解,并且以硅酸盐岩风化为主。 -
地下水化学组分之间的相互关系可以反映各离子的物质来源[22]。在本研究中,对农业用地、住宅用地和湿地地下水水化学组分分别做了相关性分析(表4),结果表明,农业用地地下水水化学组分,除三氮(NH4+、NO3−和NO2−)外,其余水化学组分之间均表现出极显著的正相关关系,表征它们来自于共同的来源。地下水中TDS、K+、Na +、Ca2+、Mg2+和HCO3− 主要来自于地层岩石风化[23-24]。在该研究区,这些离子主要受控于硅酸盐岩风化作用控制。NH4+与Cl−、TDS、SO42-、K+、Na +、Mg2+和HCO3−之间表现出显著或极显著的正相关关系。众所周知,NH4+主要来自于生活污水和化肥[25-26],并且污水和化肥中也含有一定量的Cl−、SO42-、K+和Na+。由于这些地下水样品在农业地区,因此,地下水中NH4+主要来自于化肥。水环境中NO3−的来源包括生活污水、化肥、粪肥、大气降雨等[27-28]。值得注意的是NO3−和NH4+表现出极显著的负相关关系,首先说明二者来自于共同的污染源-化肥。其次,由于NH4+在氧化环境下极易发生硝化反应转化为NO3−[29],从而降低水环境中NH4+的浓度。在这个地区,地下水处于氧化环境(DO的均值约为5.02 mg·L−1),并且NO3−的平均浓度高达61.7 mg·L−1,而NH4+的平均浓度仅为0.085 mg·L−1,表明地下水中发生了强烈硝化作用,所以二者表现出极显著的负相关关系。
在住宅用地,地下水中TDS、Cl−、SO42-、K+、Ca2+、Mg2+和HCO3−均表现出极显著的正相关关系,表征它们主要来自于地层岩石风化。值得关注的是Na+与NH4+表现出显著的正相关关系,表明二者有共同的来源。正如前面分析,水环境中的Na+与NH4+可能来自于生活污水和化肥[26]。由于采样站点位于住宅用地,并且村庄四周密布农田,且存在垃圾填埋场。因此,污水管网的破损,垃圾填埋场的渗漏,以及农业的施肥都会对其造成影响。与农业用地相似,NO3−和NH4+表现出显著的负相关关系,表明二者主要来自于生活污水和化肥,且地下水中发生了硝化作用。
在湿地,水化学指标TDS、Cl−、
SO2−4 、Na+、Ca2+和Mg2+均表现出极显著或显著的正相关关系,表征它自于共同的源-地层岩石风化。在湿地地下水中NH+4 的平均浓度(0.458 mg·L−1)要显著高于农业用地(0.085 mg·L−1)和住宅用地(0.087 mg·L−1)。但是,NO−3 的平均浓度(0.511 mg·L−1)要显著小于农业用地(61.7 mg·L−1)和住宅用地(43.8 mg·L−1),这主要是由于湿地地下水受到了黄河的补给以及污水处理厂回水的影响。NO−3 和NH+4 表现出显著的负相关关系。但是,NO−3 的浓度是非常低的,这可能是由于地下水与黄河河水交换强烈,受到了黄河河水稀释的影响。此外,湿地由于长期处于水饱和状态,地下水可能发生反硝化作用,进而降低地下水中NO−3 的浓度[30-31]。 -
(1)郑州市中牟县地下水pH的变化范围介于6.71—8.51之间,处于中性到弱碱性。地下水中阳离子的大小排序为Ca2+> Na+> Mg2+>K+>
NH+4 ,而阴离子的大小排序是HCO−3 >SO2−4 >Cl−>NO−3 >NO−2 。TH和NO−3 是该地区地下水中最主要的污染因子。(2)地下水水化学类型主要为HCO3-Ca(Mg)型,占总水样的46.2%。农业用地受到施肥的影响,水化学类型出现了Cl型水和SO4型水。而湿地受黄河水和污水处理厂回水补给的混合影响,导致主要的水化学类型改变为HCO3-Ca·Mg·Na型水。
(3)基于Gibbs模型分析表明,中牟县地下水水化学组分主要控制因素是岩石风化作用。人类活动对水化学组分也存在一定的影响。其中,三氮受人类活动影响强烈,而Na+、K+、
SO2−4 和Cl−也受到不同程度人类活动的影响。(4)基于相关性分析,在不同土地利用类型下,地下水水化学组分除三氮(NH4+、NO3−和NO2−)外,均表现出极显著或显著的正相关关系,表征它们来自于地层岩石风化。而NH4+和NO3−表现出显著的负相关关系,二者主要来自于化肥和生活污水。在农业用地和住宅用地中地下水可能发生强烈的硝化作用,但在湿地,地下水受到黄河河水的稀释,且地下水可能发生了反硝化作用。
(5)上述研究结果表明,生活污水和化肥是该地区地下水主要的污染源。因此,建议当地政府和环保部门要严格立法和监管,禁止生活污水的不达标排放。此外,农业管理者应该推广科学施肥策略(如测土配方施肥,因时和因作物施肥,施用缓释肥等)来提高肥料的利用率,防止过量施肥对地下水的污染。
郑州市中牟县地下水水化学特征及控制因素
Research of groundwater chemical characteristics and controlling factors in Zhongmu County, Zhengzhou City
-
摘要: 地下水是维持人类生存和发展的重要资源。近年来,由于人类活动的强烈干扰,导致地下水的水化学特征发生改变,严重影响了其使用价值和生态功能。本研究以郑州市中牟县作为研究地区,联合应用Piper三线图、Gibbs图、离子比例系数法和多元统计技术,探究该地区地下水化学演变特征及形成机制,结果表明,中牟县地下水主要的阳离子是Ca2+ 和Na+,主要的阴离子是
HCO−3 和 Cl−。地下水主要的水化学类型为HCO3-Ca(Mg)型,占总水样的46.2%。农业用地受到施肥的影响,水化学类型出现了Cl型水(20.8%)和SO4型水(6.25%),住宅用地由于受到生活污水的影响,出现了高比例的Na型水(55.0%)。而在湿地,地下水受到黄河水和污水处理厂回水混合影响,导致其主要的水化学类型转变为HCO3-Ca(Mg)·Na型。中牟县地下水水化学组分主要控制因素是岩石风化作用,并且主要受控于硅酸盐岩风化,而人类活动对水化学组分也存在一定的影响。相关性分析表明,在不同土地利用类型下,除NH+4 、NO−3 和NO−2 外,其余水化学组分之间表现出显著的正相关关系,表征它们主要来自地层岩石风化。NH+4 和NO−3 表现出显著的负相关关系,说明二者主要来自于化肥和生活污水。在农业用地和住宅用地中地下水可能发生强烈的硝化作用,但是,湿地地下水可能发生了反硝化作用。研究结果可为中牟县地下水可持续开发利用提供理论依据和数据支撑。Abstract: Groundwater is an important resource for human survival and development. In recent years, due to the strong interference of human activities, the hydrochemical characteristics of groundwater have changed, which has seriously affected its use value and ecological function. In this study, the evolution characteristics and formation mechanism of groundwater chemistry in Zhongmu County, Zhengzhou City, were analyzed by using Piper trilinear diagram, Gibbs diagram, ion proportion coefficient and multivariate statistical techniques. The results showed that the main cations of groundwater in the study area were Ca2+ and Na+, and the anions were dominated byHCO−3 and Cl−. The main hydrochemical type of groundwater was HCO3-Ca(Mg), which accounts for 46.2% of the total water samples. Affected by agricultural activities, Cl type water (20.8%) and SO4 type water (6.25%) were found in agricultural land. Residential land was affected by domestic sewage, Na type water (55.0%) accounted for a high proportion. However, in wetlands, groundwater was affected by the mixed action of Yellow River and sewage treatment water, resulting in the major hydrochemical type changed to HCO3-Ca (Mg)-Na. The main controlling factor for the chemical composition of groundwater in Zhongmu County was rock weathering (silicate rock weathering). Human activities also have an effect on the chemical composition of groundwater. Correlation analysis showed that the main groundwater hydrochemical components (exceptNH+4 ,NO−3 andNO−2 ) in different land use type have a significant positive correlation, which indicated that they came from rock weathering.NH+4 andNO−3 showed a significant negative correlation, indicating that they mainly came from fertilizer and domestic sewage. Strong nitrification may occur in groundwater in agricultural and residential lands, while in wetlands, denitrification may occur in aquifers. The results can provide theoretical basis and data support for sustainable development and utilization of groundwater in Zhongmu County.-
Key words:
- Hydrochemistry /
- evolution law /
- controlling factor /
- ion source
-
地下水是维持人类生存和发展的一种最重要资源和生态环境因子[1]。近年来,我国经历了快速城市化和工业化,然而,污水的处理能力未能保持同步增长(尤其在农村地区)、农业化肥和农药过量使用、地下水超采严重等问题,已经引起地下水水化学特征发生改变[2-4]。众所周知,地下水水化学改变不仅能够干扰多种生态过程,同时也降低了地下水的使用价值[5]。因此,掌握地下水水化学的演化规律对于可持续利用地下水尤为重要[6-8]。
地下水水化学演化主要受控于自然因素和人类活动的综合影响。地下水水化学特征与自然因素(水文地质条件、包气带岩性、水岩交互作用和海水入侵)密切相关[9-10]。安乐生等研究发现,黄河三角洲浅层地下水化学特点形成的关键驱动因素是黄河入海流路变迁和海水入侵[11]。人类活动(如污水排放、农业施肥、地下水超采等)也严重影响了地下水水化学演化规律。Zhang等研究发现,地下水水化学特征受到了生活污水、工业污水和水岩交互作用的混合影响, 因此,为防止该地区地下水水质恶化,首先要控制污水的排放 [12]。郭高轩等研究表明,潮白河冲洪积扇不同深度地下水水化学具有分层分带特征,且在人类活动强烈区域,浅层地下水水质略差[13]。
中牟县位于郑州市东部新城区,地下水资源是该地区工农业生产的主要供水水源。近年来,随着人口的迅速增长和工业的高速发展、农业灌溉面积极速扩大,地下水的开采量日益增加。基于 2019 年对该地区地下水位统调工作发现,中牟县城一带已经形成一个较大的浅层地下水降落漏斗,并且研究区内人类活动强烈,存在农业面源污染、固体废弃物堆放场和工业污染等3类潜在污染来源,可能对地下水水化学特点构成一定影响。目前,针对该地区地下水水化学演化规律尚未开展深入研究工作,对该地区居民的健康饮水和社会经济可持续发展构成潜在威胁。
本研究针对郑州市中牟县地下水水化学演化机理开展研究,联合应用piper三线图、Gibbs图、离子比例系数法和多元统计技术等手段,识别研究区水化学特征,揭示该地区地下水水化学形成演化机制,探讨控制地下水水化学特征的主控因素,以期为快速城市化地区地下水的可持续开发利用提供科学依据。
1. 材料与方法(Materials and methods)
1.1 研究区概况
中牟县位于北纬34°26′—34°56′、东经113°46′—114°12′之间,地处中原腹地、河南省中部偏东,隶属郑州市。研究区属暖温带半干旱气候,具明显的大陆季风气候特征,四季分明。多年平均气温14.25℃,多年平均降雨量约为616 mm,年内降水多集中在7—9月,占全年降雨量的40%—48%. 多年平均蒸发量1769.8 mm,平均相对湿度66.3%。研究区总面积为917 km2,主要的土地利用类型为农业用地(68.7%)、居民区(9.2%)、工矿用地(4.3%)、水域(16.2%)(包括湿地和水体)和裸地(1.6%)(图1)。
1.2 水文地质条件
研究区地貌类型为黄河冲积平原,地下水类型主要为松散岩类孔隙水,其含水层分布广,厚度大,水量丰富,可分为浅层水(<80 m)和中深层水(80—400 m)。浅层含水层主要由山前冲洪积与黄河冲积的细砂层组成,深度主要为 40—60 m,该含水层组埋藏浅,其下为一组粉质粘土或粉土弱透水层,与下伏中深层含水层组相隔,厚25—45 m。浅层水易于开采,为农业用水主要开采层,井深25—55 m。中深层含水层组底板埋深310—350 m,其下为厚层粘土夹薄层砂或砂的透镜体,粘土层厚度一般15—40 m,具有很好的隔水性,属承压水类型。中深层水是目前城乡小型集中供水的主要开采层,井深一般在100—300 m 左右。其含水层岩性为中砂、细砂、粗砂等,厚30—80 m,导水系数125—390 m2·d−1,贮水系数4×10−3,单位涌水量3—5 m3·h−1·m−1。地下水主要的补给来源为大气降水、河道侧漏和灌溉回水,主要的排泄方式为人工开采。
1.3 样品采集
2020年6—8月采集郑州市中牟县地下水样品93组(图1),包括农业用地站点48个,湿地站点19个,住宅用地站点20个和工矿用地站点6个。采样点布设的原则主要依据不同的土地利用类型平均布设采样点,如果预布设站点区域内无地下水井,可以适当调整,但要保证2个采样点之间的距离大于1 km。地下水主要取自民井和农业灌溉井,采样井的深度范围是25—150 m。采样前抽水洗井10 min,用原水样清洗采样瓶3次,分别采集 1.5 L 和 0.5 L 水样各1瓶,用于分析阴阳离子。分析阳离子的水样加1∶1的
HNO−3 1.4 样品的测试
样品测试的指标包括pH、TDS、K+、Na +、Ca2+、Mg2+、
NH+4 NO−3 NO−2 SO2−4 CO2−3 HCO−3 1.5 研究方法
(1)水化学类型判定。本研究按照舒克列夫分类法,即阴阳离子毫克当量百分比大于25%时参与命名。对研究区采样点地下水化学类型定名,并绘制出了地下水化学类型Piper三线图。
(2)地下水化学控制因素识别。选用Gibbs图识别地下水化学控制作用。通常情况下,水样位于 Gibbs 图右下角,表明其受大气降水作用影响较大,水样位于Gibbs 图左中部,表明岩石风化作用是该地区水化学的主要控制作用,而受蒸发结晶作用控制的水样将落于Gibbs 图右上角。
(3)离子来源识别。联合应用Ca2+/Na+ VS
HCO−3 HCO−3 HCO−3 HCO−3 (4)衬度系数方差。方差(Variance)用于刻画一个随机变量对其数学期望(均值)的离散程度。由于地下水各化学组分的绝对数值范围可能相差很大,无法进行方差的对比,为此,先求出每个样本每个变量(Xi)与该变量均值(
¯X Xi¯X 衬度系数方差(Vσi2)的计算公式如下:
Vσ2i=1n∑ni=1(Vi−¯Vi)2 (1) 式中,Vi是地下水第i个化学组分的衬度系数;
¯Vi 当Vσi2> 1时,说明该化学组分受人类活动影响强烈;当0.5<Vσi2<1时,说明该组分受中等强度的人类活动影响;当Vσi2<0.5时,说明该组分受人类活动影响较小。
此外,运用Spearman’s 秩相关系数分析了不同土地利用类型地下水水化学组分之间的相关关系。数据分析使用 R 语言(4.0.3)、Origin(2019b)和Arcgis 10.5。
2. 结果与讨论(Results and discussion)
2.1 地下水水化学特点
研究区pH值的范围介于6.71—8.51之间,均值为7.62,地下水为中性到弱碱性水,样品的超标率为1.1%(表1)。TDS 变化范围为200—1408 mg·L−1,均值为612 mg·L−1。地下水样品中
CO2−3 NH+4 HCO−3 SO2−4 NO−3 NO−2 NH+4 NO−3 表 1 研究区地下水水化学参数统计表Table 1. Descriptive statistics of groundwater hydrochemical parameters in the study area.均值Mean value 最小值Minimum value 最大值Maximum value 标准差Standard deviation 超标率/%Exceed standard rate 国标Ⅲ类Standard(Ⅲ) pH 7.62 6.71 8.51 0.26 1.1 6.5—8.5 TDS/(mg·L−1) 612 200 1408 231 3.2 1000 K+/(mg·L−1) 2.10 0.27 10.6 2.00 — — Na+/(mg·L−1) 69.5 6.72 208 48.5 1.1 200 Ca2+/(mg·L−1) 107 7.86 281 47.5 — — Mg2+/(mg·L−1) 36.1 2.90 87.0 16.6 — — HCO3−/(mg·L−1) 418 165 792 137 — — Cl−/(mg·L−1) 67.3 5.21 190 49.6 0 250 SO42-/(mg·L−1) 71.8 4.03 248 47.9 0 250 NO3−/(mg·L−1) 42.4 0.20 338 66.3 19.4 88.6 NH4+/(mg·L−1) 0.159 0.002 1.106 0.237 6.5 0.64 NO2−/(mg·L−1) 0.160 0.002 1.960 0.307 0 3.29 TH/(mg·L−1) 414 28.3 978 159 39.8 450 注:国标Ⅲ类指地下水质量标准Ⅲ类(GB/T14848-2017)[17]. Note: Standard is grade Ⅲ standard for groundwater quality in China (GB/T14848-2017)[17]. 2.2 地下水水化学类型
Piper三线图常用来表征地下水化学成分的演化规律[18]。由图2 可以看出,研究区地下水主要的水化学类型为HCO3-Ca(Mg)型,占总水样的46.2%。近年来,由于人类活动的干扰,地下水水化学类型趋于复杂化,出现了Cl型水(18.3%),Na型水(39.8%)和SO4型水(3.2%)。不同土地利用类型下地下水水化学类型有明显的区别。正如表2显示,在农业用地和工矿用地中,地下水主要的水化学类型是HCO3-Ca(Mg)型,但是,农业用地受到施肥的影响,水化学类型出现了Cl型水(20.8%)和SO4型水(6.25%)。住宅用地地下水主要的水化学类型是HCO3-Ca(Mg)型水(40.0%),并且Na型水出现的比例高达55.0%。此外,在湿地(郑州黄河湿地自然保护区)内,Na型水是地下水主要的水化学类型,占比高达89.5%,这主要与湿地地下水受到黄河水和污水处理厂回水混合影响有关。
表 2 研究区不同土地利用类型地下水水化学类型统计表Table 2. Statistic table of groundwater hydrochemistry type of different land use in the study area水化学类型Hydrochemical type 水化学类型出现比例/%Proportions of hydrochemical type 农业用地Agricultural land 住宅用地Residential Land 湿地Wetland 工矿用地Industrial land HCO3-Ca(Mg) 58.3 40.0 10.5 83.3 Cl型水 20.8 20.0 10.5 16.7 Na型水 20.8 55.0 89.5 0 SO4型水 6.25 0 0 0 2.3 地下水化学的控制因素及离子来源
2.3.1 地下水化学的控制因素
地下水化学组分的形成机制主要受控于大气降雨、岩石风化、蒸发浓缩和混合作用等[19]。正如图3显示,地下水采样点的离子含量投点绝大部分落于Gibbs图中间位置,表明岩石风化是研究区地下水水化学离子组分的主要控制因素。但是,研究区部分采样点,有向右上方区域偏移的趋势,说明蒸发-浓缩作用对研究区地下水的水化学组分也有一定的影响。此外,部分点位超出了岩石分化的控制边界,说明这些采样点的水化学组分受到人类活动的影响。
2.3.2 人类活动的影响
衬度系数方差可用于区分地下水化学组分的形成以天然条件演化作用为主,还是受人类活动影响较大。地下水化学组分的衬度系数方差越大,表明该组分受人类活动影响就越强烈[20]。由表3可见,整体上看,在不同土地利用类型中地下水中的Ca2+、Mg2+和
HCO−3 NH+4 NO−3 NO−2 SO2−4 SO2−4 2.3.3 地下水化学的离子来源
为了进一步探讨地下水化学组分的来源,联合应用Ca2+/Na+ VS
HCO−3 HCO−3 表 3 中牟县地下水化学成分衬度系数方差表Table 3. variance analysis of contrast coefficient of groundwater hydrochemical compositions in the Zhongmu County水化学组分Hydrochemical compositions 农业用地Agricultural land 住宅用地Residential land 湿地Wetland 工矿用地Industrial land SO42− 0.513 0.267 0.283 0.796 Cl− 0.644 0.517 0.189 1.798 NH4+ 2.855 4.751 0.353 1.359 NO2− 4.938 3.168 1.297 1.949 NO3− 1.520 1.980 0.428 3.789 HCO3− 0.151 0.045 0.065 0.049 Na+ 0.725 0.279 0.183 0.443 K+ 1.232 0.933 0.380 0.156 Ca2+ 0.161 0.418 0.067 0.167 Mg2+ 0.256 0.140 0.092 0.100 2.4 水化学指标相关性分析
地下水化学组分之间的相互关系可以反映各离子的物质来源[22]。在本研究中,对农业用地、住宅用地和湿地地下水水化学组分分别做了相关性分析(表4),结果表明,农业用地地下水水化学组分,除三氮(NH4+、NO3−和NO2−)外,其余水化学组分之间均表现出极显著的正相关关系,表征它们来自于共同的来源。地下水中TDS、K+、Na +、Ca2+、Mg2+和HCO3− 主要来自于地层岩石风化[23-24]。在该研究区,这些离子主要受控于硅酸盐岩风化作用控制。NH4+与Cl−、TDS、SO42-、K+、Na +、Mg2+和HCO3−之间表现出显著或极显著的正相关关系。众所周知,NH4+主要来自于生活污水和化肥[25-26],并且污水和化肥中也含有一定量的Cl−、SO42-、K+和Na+。由于这些地下水样品在农业地区,因此,地下水中NH4+主要来自于化肥。水环境中NO3−的来源包括生活污水、化肥、粪肥、大气降雨等[27-28]。值得注意的是NO3−和NH4+表现出极显著的负相关关系,首先说明二者来自于共同的污染源-化肥。其次,由于NH4+在氧化环境下极易发生硝化反应转化为NO3−[29],从而降低水环境中NH4+的浓度。在这个地区,地下水处于氧化环境(DO的均值约为5.02 mg·L−1),并且NO3−的平均浓度高达61.7 mg·L−1,而NH4+的平均浓度仅为0.085 mg·L−1,表明地下水中发生了强烈硝化作用,所以二者表现出极显著的负相关关系。
在住宅用地,地下水中TDS、Cl−、SO42-、K+、Ca2+、Mg2+和HCO3−均表现出极显著的正相关关系,表征它们主要来自于地层岩石风化。值得关注的是Na+与NH4+表现出显著的正相关关系,表明二者有共同的来源。正如前面分析,水环境中的Na+与NH4+可能来自于生活污水和化肥[26]。由于采样站点位于住宅用地,并且村庄四周密布农田,且存在垃圾填埋场。因此,污水管网的破损,垃圾填埋场的渗漏,以及农业的施肥都会对其造成影响。与农业用地相似,NO3−和NH4+表现出显著的负相关关系,表明二者主要来自于生活污水和化肥,且地下水中发生了硝化作用。
表 4 研究区农业用地地下水水化学组分的相关性分析Table 4. Correlation analysis of groundwater hydrochemistry component of agricultural land in the study areaTH TDS SO42− Cl− NH4+ NO2− NO3− HCO3− Na+ K+ Ca2+ Mg2+ 农业用地 TH 1 0.950** 0.713** 0.877** 0.267 0.347* 0.132 0.778** 0.699** 0.663** 0.928** 0.916** TDS 1 0.801 0.922** 0.320* 0.337* 0.186 0.776** 0.796** 0.666** 0.850** 0.939** SO42− 1 0.750** 0.325* 0.093 −0.029 0.606** 0.709** 0.630** 0.624** 0.719** Cl− 1 0.396** 0.262 0.102 0.710** 0.764** 0.616** 0.815** 0.853** NH4+ 1 0.168 −0.496** 0.506** 0.532** 0.393** 0.188 0.402** NO2− 1 0.321* 0.170 0.176 0.030 0.356* 0.303* NO3− 1 −0.292* −0.222 −0.125 0.253 −0.003 HCO3− 1 0.879** 0.668** 0.587** 0.895** Na+ 1 0.642** 0.496** 0.880** K+ 1 0.619** 0.646** Ca2+ 1 0.732** Mg2+ 1 住宅 TH 1 0.767** 0.674** 0.734** −0.363 0.139 0.438 0.465* −0.344 0.513* 0.958** 0.681** TDS 1 0.893** 0.890** −0.122 0.159 0.283 0.626** 0.241 0.598** 0.684** 0.624** SO42− 1 0.832** −0.111 0.197 0.314 0.448* 0.266 0.352 0.593** 0.653** Cl− 1 −0.158 0.158 0.229 0.472* 0.111 0.543* 0.695** 0.614** NH4+ 1 0.272 −0.543* 0.19 0.480* −0.133 −0.436 −0.016 NO2− 1 0.193 0.002 0.06 0.252 0.257 0.207 NO3− 1 −0.373 −0.441 0.065 0.487* 0.099 HCO3− 1 0.424 0.564** 0.333 0.43 Na+ 1 0.089 −0.445* 0.032 K+ 1 0.471* 0.460* Ca2+ 1 0.531* Mg2+ 1 湿地 TH 1 0.946** 0.639** 0.722** −0.031 0.217 0.421 0.786** 0.789** 0.298 0.883** 0.818** TDS 1 0.611** 0.736** 0.109 0.098 0.333 0.830** 0.918** 0.291 0.787** 0.823** SO42− 1 0.756** 0.053 0.14 0.379 0.16 0.416 0.077 0.685** 0.391 Cl− 1 0.213 0.225 0.235 0.302 0.600** −0.057 0.705** 0.505* NH4+ 1 0.2 −0.552* 0.055 0.176 −0.301 −0.175 0.048 NO2− 1 0.265 0.043 −0.021 0.108 0.157 0.219 NO3− 1 0.168 0.213 0.169 0.315 0.463* HCO3− 1 0.844* 0.396 0.565* 0.821* Na+ 1 0.281 0.591** 0.825* K+ 1 0.296 0.261 Ca2+ 1 0.556* Mg2+ 1 注:** 表示在 0.01 水平上线性相关,* 表示在 0.05 水平上线性相关. Note:** P<0.01; * P<0.05. 在湿地,水化学指标TDS、Cl−、
SO2−4 NH+4 NO−3 NO−3 NH+4 NO−3 NO−3 3. 结论(Conclusion)
(1)郑州市中牟县地下水pH的变化范围介于6.71—8.51之间,处于中性到弱碱性。地下水中阳离子的大小排序为Ca2+> Na+> Mg2+>K+>
NH+4 HCO−3 SO2−4 NO−3 NO−2 NO−3 (2)地下水水化学类型主要为HCO3-Ca(Mg)型,占总水样的46.2%。农业用地受到施肥的影响,水化学类型出现了Cl型水和SO4型水。而湿地受黄河水和污水处理厂回水补给的混合影响,导致主要的水化学类型改变为HCO3-Ca·Mg·Na型水。
(3)基于Gibbs模型分析表明,中牟县地下水水化学组分主要控制因素是岩石风化作用。人类活动对水化学组分也存在一定的影响。其中,三氮受人类活动影响强烈,而Na+、K+、
SO2−4 (4)基于相关性分析,在不同土地利用类型下,地下水水化学组分除三氮(NH4+、NO3−和NO2−)外,均表现出极显著或显著的正相关关系,表征它们来自于地层岩石风化。而NH4+和NO3−表现出显著的负相关关系,二者主要来自于化肥和生活污水。在农业用地和住宅用地中地下水可能发生强烈的硝化作用,但在湿地,地下水受到黄河河水的稀释,且地下水可能发生了反硝化作用。
(5)上述研究结果表明,生活污水和化肥是该地区地下水主要的污染源。因此,建议当地政府和环保部门要严格立法和监管,禁止生活污水的不达标排放。此外,农业管理者应该推广科学施肥策略(如测土配方施肥,因时和因作物施肥,施用缓释肥等)来提高肥料的利用率,防止过量施肥对地下水的污染。
-
表 1 研究区地下水水化学参数统计表
Table 1. Descriptive statistics of groundwater hydrochemical parameters in the study area.
均值Mean value 最小值Minimum value 最大值Maximum value 标准差Standard deviation 超标率/%Exceed standard rate 国标Ⅲ类Standard(Ⅲ) pH 7.62 6.71 8.51 0.26 1.1 6.5—8.5 TDS/(mg·L−1) 612 200 1408 231 3.2 1000 K+/(mg·L−1) 2.10 0.27 10.6 2.00 — — Na+/(mg·L−1) 69.5 6.72 208 48.5 1.1 200 Ca2+/(mg·L−1) 107 7.86 281 47.5 — — Mg2+/(mg·L−1) 36.1 2.90 87.0 16.6 — — HCO3−/(mg·L−1) 418 165 792 137 — — Cl−/(mg·L−1) 67.3 5.21 190 49.6 0 250 SO42-/(mg·L−1) 71.8 4.03 248 47.9 0 250 NO3−/(mg·L−1) 42.4 0.20 338 66.3 19.4 88.6 NH4+/(mg·L−1) 0.159 0.002 1.106 0.237 6.5 0.64 NO2−/(mg·L−1) 0.160 0.002 1.960 0.307 0 3.29 TH/(mg·L−1) 414 28.3 978 159 39.8 450 注:国标Ⅲ类指地下水质量标准Ⅲ类(GB/T14848-2017)[17]. Note: Standard is grade Ⅲ standard for groundwater quality in China (GB/T14848-2017)[17]. 表 2 研究区不同土地利用类型地下水水化学类型统计表
Table 2. Statistic table of groundwater hydrochemistry type of different land use in the study area
水化学类型Hydrochemical type 水化学类型出现比例/%Proportions of hydrochemical type 农业用地Agricultural land 住宅用地Residential Land 湿地Wetland 工矿用地Industrial land HCO3-Ca(Mg) 58.3 40.0 10.5 83.3 Cl型水 20.8 20.0 10.5 16.7 Na型水 20.8 55.0 89.5 0 SO4型水 6.25 0 0 0 表 3 中牟县地下水化学成分衬度系数方差表
Table 3. variance analysis of contrast coefficient of groundwater hydrochemical compositions in the Zhongmu County
水化学组分Hydrochemical compositions 农业用地Agricultural land 住宅用地Residential land 湿地Wetland 工矿用地Industrial land SO42− 0.513 0.267 0.283 0.796 Cl− 0.644 0.517 0.189 1.798 NH4+ 2.855 4.751 0.353 1.359 NO2− 4.938 3.168 1.297 1.949 NO3− 1.520 1.980 0.428 3.789 HCO3− 0.151 0.045 0.065 0.049 Na+ 0.725 0.279 0.183 0.443 K+ 1.232 0.933 0.380 0.156 Ca2+ 0.161 0.418 0.067 0.167 Mg2+ 0.256 0.140 0.092 0.100 表 4 研究区农业用地地下水水化学组分的相关性分析
Table 4. Correlation analysis of groundwater hydrochemistry component of agricultural land in the study area
TH TDS SO42− Cl− NH4+ NO2− NO3− HCO3− Na+ K+ Ca2+ Mg2+ 农业用地 TH 1 0.950** 0.713** 0.877** 0.267 0.347* 0.132 0.778** 0.699** 0.663** 0.928** 0.916** TDS 1 0.801 0.922** 0.320* 0.337* 0.186 0.776** 0.796** 0.666** 0.850** 0.939** SO42− 1 0.750** 0.325* 0.093 −0.029 0.606** 0.709** 0.630** 0.624** 0.719** Cl− 1 0.396** 0.262 0.102 0.710** 0.764** 0.616** 0.815** 0.853** NH4+ 1 0.168 −0.496** 0.506** 0.532** 0.393** 0.188 0.402** NO2− 1 0.321* 0.170 0.176 0.030 0.356* 0.303* NO3− 1 −0.292* −0.222 −0.125 0.253 −0.003 HCO3− 1 0.879** 0.668** 0.587** 0.895** Na+ 1 0.642** 0.496** 0.880** K+ 1 0.619** 0.646** Ca2+ 1 0.732** Mg2+ 1 住宅 TH 1 0.767** 0.674** 0.734** −0.363 0.139 0.438 0.465* −0.344 0.513* 0.958** 0.681** TDS 1 0.893** 0.890** −0.122 0.159 0.283 0.626** 0.241 0.598** 0.684** 0.624** SO42− 1 0.832** −0.111 0.197 0.314 0.448* 0.266 0.352 0.593** 0.653** Cl− 1 −0.158 0.158 0.229 0.472* 0.111 0.543* 0.695** 0.614** NH4+ 1 0.272 −0.543* 0.19 0.480* −0.133 −0.436 −0.016 NO2− 1 0.193 0.002 0.06 0.252 0.257 0.207 NO3− 1 −0.373 −0.441 0.065 0.487* 0.099 HCO3− 1 0.424 0.564** 0.333 0.43 Na+ 1 0.089 −0.445* 0.032 K+ 1 0.471* 0.460* Ca2+ 1 0.531* Mg2+ 1 湿地 TH 1 0.946** 0.639** 0.722** −0.031 0.217 0.421 0.786** 0.789** 0.298 0.883** 0.818** TDS 1 0.611** 0.736** 0.109 0.098 0.333 0.830** 0.918** 0.291 0.787** 0.823** SO42− 1 0.756** 0.053 0.14 0.379 0.16 0.416 0.077 0.685** 0.391 Cl− 1 0.213 0.225 0.235 0.302 0.600** −0.057 0.705** 0.505* NH4+ 1 0.2 −0.552* 0.055 0.176 −0.301 −0.175 0.048 NO2− 1 0.265 0.043 −0.021 0.108 0.157 0.219 NO3− 1 0.168 0.213 0.169 0.315 0.463* HCO3− 1 0.844* 0.396 0.565* 0.821* Na+ 1 0.281 0.591** 0.825* K+ 1 0.296 0.261 Ca2+ 1 0.556* Mg2+ 1 注:** 表示在 0.01 水平上线性相关,* 表示在 0.05 水平上线性相关. Note:** P<0.01; * P<0.05. -
[1] MA B, JIN M G, LIANG X, et al. Groundwater mixing and mineralization processes in a mountain–oasis–desert basin, northwest China: Hydrogeochemistry and environmental tracer indicators [J]. Hydrogeology Journal, 2018, 26(D22): 233-250. [2] JIANG Y, WU Y, GROVES C, et al. Natural and anthropogenic factors affecting the groundwater quality in the Nandong karst underground river system in Yunan, China [J]. Journal of Contaminant Hydrology, 2009, 109(1-4): 49-61. doi: 10.1016/j.jconhyd.2009.08.001 [3] QIN R, WU Y, XU Z, et al. Assessing the impact of natural and anthropogenic activities on groundwater quality in coastal alluvial aquifers of the lower Liaohe River Plain, NE China [J]. Applied Geochemistry, 2013, 31(2): 142-158. [4] XUE D, BOTTE J, BAETS B D, et al. Present limitations and future prospects of stable isotope methods for nitrate source identification in surface-and groundwater [J]. Water Research, 2009, 43(5): 1159-1170. doi: 10.1016/j.watres.2008.12.048 [5] REN C B , ZHANG Q Q. Groundwater chemical characteristics and controlling factors in a region of Northern China with intensive human activity [J]. International Journal of Environmental Research and Public Health, 2020, 17: 9126. doi: 10.3390/ijerph17239126 [6] PAZAND K, KHOSRAVI D, GHADERI M R, et al. Identification of the hydrogeochemical processes and assessment of groundwater in a semi-arid region using major ion chemistry: A case study of Ardestan basin in Central Iran [J]. Groundwater for Sustainable Development, 2018, 6: 245-254. doi: 10.1016/j.gsd.2018.01.008 [7] HUANG G, SUN J, ZHANG Y, et al. Impact of anthropogenic and natural processes on the evolution of groundwater chemistry in a rapidly urbanized coastal area, South China [J]. Science of the Total Environment, 2013, 463–464(5): 209-221. [8] 孙厚云, 毛启贵, 卫晓锋, 等. 哈密盆地地下水系统水化学特征及形成演化 [J]. 中国地质, 2018, 45(6): 1128-1141. SUN H Y, MAO Q G, WEI X F, et al. Hydrogeochemical characteristics and formation evolutionary mechanism of the groundwater system in the Hami basin [J]. Geology in China, 2018, 45(6): 1128-1141(in Chinese).
[9] 崔佳琪, 李仙岳, 史海滨, 等. 河套灌区地下水化学演变特征及形成机制 [J]. 环境科学, 2020, 41(9): 135-144. CUI J Q, LI X Y, SHI H B, et al. Chemical evolution and formation mechanism of groundwater in Hetao Irrigation Area [J]. Environmental Science, 2020, 41(9): 135-144(in Chinese).
[10] 刘江涛, 蔡五田, 曹月婷, 等. 沁河冲洪积扇地下水水化学特征及成因分析 [J]. 环境科学, 2018, 39(12): 142-153. LIU J T, CAI W T, CAO Y T, et al. Hydrochemical characteristics of groundwater and the origin in alluvial-proluvial fan of Qinhe River [J]. Environmental Science, 2018, 39(12): 142-153(in Chinese).
[11] 安乐生, 赵全升, 叶思源, 等. 黄河三角洲浅层地下水化学特征及形成作用 [J]. 环境科学, 2012, 33(2): 370-378. AN L S, ZHAO Q S, YE S Y, et al. Hydrochemical characteristics and formation mechanism of shallow groundwater in the Yellow River delta [J]. Environmental Science, 2012, 33(2): 370-378(in Chinese).
[12] ZHANG Q Q, WANG L, WANG H W, et al. Spatio-temporal variation of groundwater quality and source apportionment using multivariate statistical techniques for the Hutuo River alluvial-pluvial fan, China [J]. International Journal of Environmental Research and Public Health, 2020, 17: 1055. doi: 10.3390/ijerph17031055 [13] 郭高轩, 侯泉林, 许亮, 等. 北京潮白河冲洪积扇地下水水化学的分层分带特征 [J]. 地球学报, 2014, 35(2): 204-210. doi: 10.3975/cagsb.2014.02.12 GUO G X, HOU Q L, XU L, et al. Delamination and zoning characteristics of quaternary groundwater in Chaobai alluvial-proluvial fan, Beijing, based on hydrochemical analysis [J]. Acta Geoscientica Sinica, 2014, 35(2): 204-210(in Chinese). doi: 10.3975/cagsb.2014.02.12
[14] ZHANG Q Q, WANG H W. Assessment of sources and transformation of nitrate in the alluvial-pluvial fan region of north China using a multi-isotope approach [J]. Journal of Environmental Sciences, 2020, 89: 9-22. doi: 10.1016/j.jes.2019.09.021 [15] KNEZOVIC N J, MEMIC M, MABIC M, et al. Correlation between water hardness and cardiovascular diseases in Mostar city, Bosnia and Herzegovina [J]. Journal of Water and Health, 2014, 12(4): 817-823. doi: 10.2166/wh.2014.129 [16] KOUSA A, HAVULINNA A, MOLTCHANOVA E, et al. Calcium magnesium ratio in local ground-water and incidence of acute myocardial in faction among males in rural Finland [J]. Environmental Health Perspect, 2006, 114(1): 730-734. [17] 中华人民共和国自然资源部. 地下水质量标准(GB/T 14848-2017). 中华人民共和国国家质量监督检验检疫局, 2017. Ministry of natural resources of the People's Republic of China. Standard for Groundwater quality. (GB/T 14848-2017). General Administration of Quality Supervision, Inspection and Quarantine of the People's Republic of China, 2017(in Chinese).
[18] 冯建国, 赫明浩, 李贵恒, 等. 泰莱盆地孔隙水水化学特征及其控制因素分析 [J]. 环境化学, 2019, 38(11): 2594-2600. FENG J G, HE M H, LI G H, et al. Analysis of hydrochemical characteristics and controlling factors of porewater in the Tailai Basin [J]. Environmental Chemistry, 2019, 38(11): 2594-2600(in Chinese).
[19] 唐金平, 张强, 胡漾, 等. 湔江冲洪积扇地下水化学特征及控制因素分析 [J]. 环境科学, 2019, 40(7): 3089-3098. TANG J P, ZHANG Q, HU Y, et al. Groundwater chemical characteristics and analysis of their controlling factors in an Alluvial Fan of Jianjiang River [J]. Environmental Science, 2019, 40(7): 3089-3098(in Chinese).
[20] 张千千, 王慧玮, 王龙, 等. 滹沱河冲洪积扇地区地下水硬度升高的机理研究 [J]. 环境科学与技术, 2018, 41(S2): 62-68. ZHANG Q Q, WANG H W, WANG L, et al. Increasing mechanism of groundwater total hardness (TH) in the Hutuo River alluvial-pluvial fan [J]. Environmental Science & Technology, 2018, 41(S2): 62-68(in Chinese).
[21] GAILLARDET J, DUPRE B, LOUVAT P, et al. Global silicate weathering and CO2 consumption rates deduced from the chemistry of large rivers [J]. Chemical Geology, 1999, 159(1-4): 3-30. doi: 10.1016/S0009-2541(99)00031-5 [22] GUO G, WU F, XIE F, et al. Spatial distribution and pollution assessment of heavy metals in urban soils from southwest China [J]. Journal of Environmental Sciences, 2012(3): 410-418. [23] LIU C Q, LI S L, LANG Y C, et al. Using delta15N- and delta18O-values to identify nitrate sources in karst ground water, Guiyang, southwest China[J]. Environmental Science & Technology, 2006, 40(22): 6928. [24] ZHANG Q, WANG H, WANG Y, et al. Groundwater quality assessment and pollution source apportionment in an intensely exploited region of northern China [J]. Environmental Science & Pollution Research, 2017, 24(20): 16639. [25] ZHANG Q, WANG X, WAN W, et al. The spatial-temporal pattern and source apportionment of water pollution in a trans-urban river [J]. Polish Journal of Environmental Studies, 2015, 24(2): 841-851. [26] SU S, ZHI J, LOU L, et al. Spatio-temporal patterns and source apportionment of pollution in Qiantang River (China) using neural-based modeling and multivariate statistical techniques [J]. Physics & Chemistry of the Earth, 2011, 36(9-11): 379-386. [27] NESTLER A, BERGLUND M, ACCOE F, et al. Isotopes for improved management of nitrate pollution in aqueous resources: review of surface water field studies [J]. Environmental Science Pollution Research, 2011, 18(4): 519-533. doi: 10.1007/s11356-010-0422-z [28] PASTEN –ZAPATA E, LEDESMA-RUIZ R, HARTER T, et al. Assessment of sources and fate of nitrate in shallow groundwater of an agricultural area by using a multi-tracer approach [J]. Science of Total Environment, 2014, 470/471(2): 855-864. [29] JIN Z, XUE Q, CHEN L, et al. Using dual isotopes to evaluate sources and transformations of nitrate in the West Lake watershed, eastern China [J]. Journal of Contaminant Hydrology, 2015, 177/178: 64-75. doi: 10.1016/j.jconhyd.2015.02.008 [30] KUMAZAWA K. Nitrogen fertilization and nitrate pollution in groundwater in Japan: present status and measures for sustainable agriculture [J]. Nutr Cycl Agroecosyst, 2002, 63(2/3): 129-137. doi: 10.1023/A:1021198721003 [31] ZHANG Q, SUN J, LIU J, et al. Driving mechanism and sources of groundwater nitrate contamination in the rapidly urbanized region of south china [J]. Journal of Contaminant Hydrology, 2015, 182: 221-230. doi: 10.1016/j.jconhyd.2015.09.009 -
















 下载:
下载: