-
硫在自然界中广泛分布,但地壳中含量仅为0.048%,并且主要存在于岩石矿物、化石燃料和海洋中。硫有多种存在形态,可分为无机硫和有机硫,其中无机硫包括硫酸盐、硫化物以及单质硫等,有机硫主要包括酯键硫和碳键硫[1]。沉积物和岩石中储存约7.80×1018 kg的硫,且主要以金属硫化物和石膏的形式存在。金属硫化物(如黄铁矿、磁黄铁矿、方铅矿、闪锌矿、黄铜矿和砷黄铁矿等)尾矿在空气、水和微生物作用下氧化、酸化,形成含大量重金属离子的酸性矿山废水(acid mine drainage, AMD)[2-3]。AMD随地表径流进入河流后,其携带的硫化物也会进入到沉积物中并迁移转化。自然界有32S、33S、34S和36S 的4种稳定同位素,地球化学研究中一般考虑丰度最大的34S和32S,其组成一般用δ34S表示[4]。不同源区的硫一般具有不同的同位素组成特征,且不同形态硫的来源和迁移过程也不尽相同,因此,硫同位素组成可用来指示硫的来源以及迁移转化过程[5-6]。
沉积物是水生态系统的重要组成部分,是众多污染物在环境中迁移转化的载体、归宿和蓄积库,是研究污染物环境地球化学循环的重要载体[7-9]。在硫的迁移、转化过程中,地表径流携带的硫素被输送到河流与海洋,这些硫一部分被浮游动植物及鱼类利用,其余部分在水-沉积物界面发生复杂的生物地球化学迁移转化,最终埋藏于河流或海洋底部[10]。沉积物中的无机硫主要包括硫酸盐、酸可挥发性硫(AVS)、黄铁矿硫(CRS)和单质硫(ES)等。AVS是指在酸性条件下能够分解生成硫化氢的那部分硫化物,化学性质相对活跃,主要包括结晶型马基诺矿、游离硫化物、无定型FeS等以及其它二价金属硫化物[11],可进一步与铁反应生成更为稳定的黄铁矿。CRS(FeS2)化学性质较为稳定,不溶于盐酸,是硫铁化物成岩后的最终产物[12]。
庐江县是安徽省矿产资源富集区之一,有“地下聚宝盆”之称,也是安徽省确定的第五大工矿区和重点开发建设的工矿基地。全县共有以龙桥、矾山、泥河和罗河为代表的大小矿区(床)77个,保有资源储量居全省前五位的有6种矿产,其中铅、锌、硫铁矿、明矾石等4种居首位,铜矿居第二位,铁矿居第三位[13]。钟山铁矿床位于庐枞火山岩盆地北部,规模为中型铁矿,主要矿石类型为赤铁矿和磁铁矿,并共生黄铁矿[14]。庐江县钟山铁矿于1967年开始建设矿山,1979年投产开采[14]。采选矿形成的尾矿中硫化物经氧化、酸化形成AMD,随雨水径流排入河流,给局地的水生态环境带来潜在危害。
本文以安徽省庐江县钟山铁矿尾矿库周边失曹河与黄屯河为研究对象,采集河流水和沉积物样品,分析了水和沉积物硫形态含量、硫酸根硫同位素组成及其分布特征,为尾矿区酸性矿山废水环境影响及其排放控制提供基础参考。
-
如图1所示,庐江县失曹河与黄屯河上游均发源于钟山尾矿库周边,受到酸性矿山废水的影响,两条河流从尾矿库周边分别经西、东方向,从上游往下游向北流入庐江县天河,并最终汇入长江。本文研究样品采集于2017年7月,采样点分布见图1,失曹河点位为S1—S4,黄屯河点位为H1—H7,其中S1和H1靠近尾矿区,H5处有化工污染的复合酸性水排入,S4和H7靠近县河道,C1、C2是未受AMD污染的河流对照点位。分别采集各点位水和沉积物样品并置于冰袋冷藏箱中,带回实验室待分析.
-
河流水体pH在现场由便携式pH计(HQ11D)测定。采集的河流水样经0.45 μm膜过滤后用离子色谱仪(型号: AQUION INTER,检测器型号: AS-DV)测定
SO2−4 的含量。取部分沉积物样品冷冻干燥,研磨过200目,总硫(TS)使用高频红外碳硫分析仪(型号: HCS-218)测定;硫酸根(SO2−4 )用氢氧化钠提取[15],提取液稀释后用离子色谱(型号: AQUION INTER, 检测器型号: AS-DV)测定。取部分SO2−4 提取液加入HCl调节溶液pH值小于2,缓缓加入过量BaCl2 (2 mol·L−1),室温下静置12 h,将溶液过滤(两层慢速无尘滤纸),BaSO4沉淀被保留在无尘滤纸上面,反复用去离子水清洗滤纸上的沉淀,用1% AgNO3溶液检测滤液氯离子残留,直到无氯离子存在为止。再将BaSO4连同滤纸放置到坩埚中,在马弗炉中850 ℃保持3 h。关闭马弗炉,收集白色BaSO4沉淀,用称量纸包裹好放置于密封袋中。BaSO4硫同位素分析采用气体稳定同位素比值质谱仪MAT253、Flash EA 2000型元素分析仪以及Conflo Ⅳ连续流装置完成(中国科学院地球化学研究所)。将含有不超过100 μg硫的制成样品和3倍于样品的V2O5包裹于锡杯中,由自动进样器送入填充氧化剂WO3及还原剂Cu的反应器中,样品落入反应管的同时送入氧气,此时反应管中富集纯氧,样品与锡迅速熔化燃烧,生成SO2及SO3,SO3在Cu的还原下生成SO2,之后被氦气流载入质谱分析。所用标样为IAEA-SO-5 (+0.5‰), IAEA-SO-6 (−34.1‰)和NBS 127 (+20.3‰),其分析结果用相对于国际标准CDT的δ34S表示,测试精度优于0.2‰ (1σ)。
沉积物中还原态无机硫含量采用改进的“冷扩散法”测定[15]。具体步骤如下:取解冻新鲜沉积物样品2—4 g迅速置于反应瓶中,先后加入盐酸(6 mol·L−1)、还原态氯化铬和DMF (N-N二甲基甲酰胺)分别将沉积物中的AVS、CRS和ES转化为硫化氢气体,并用氮气将其吹入装有碱式醋酸锌的吸收瓶中固定为硫化锌沉淀,实验过程中通过90 ℃水浴加热将反应时间分别缩短为1.5、2、2 h,再通过亚甲基蓝分光光度法测定其含量,本研究ES因含量太低而未检出。实验中采用加入固体ZnS的方式进行AVS的回收实验,回收率为82.01%—108.71%,加标回收率为82.34%—114.71%。
-
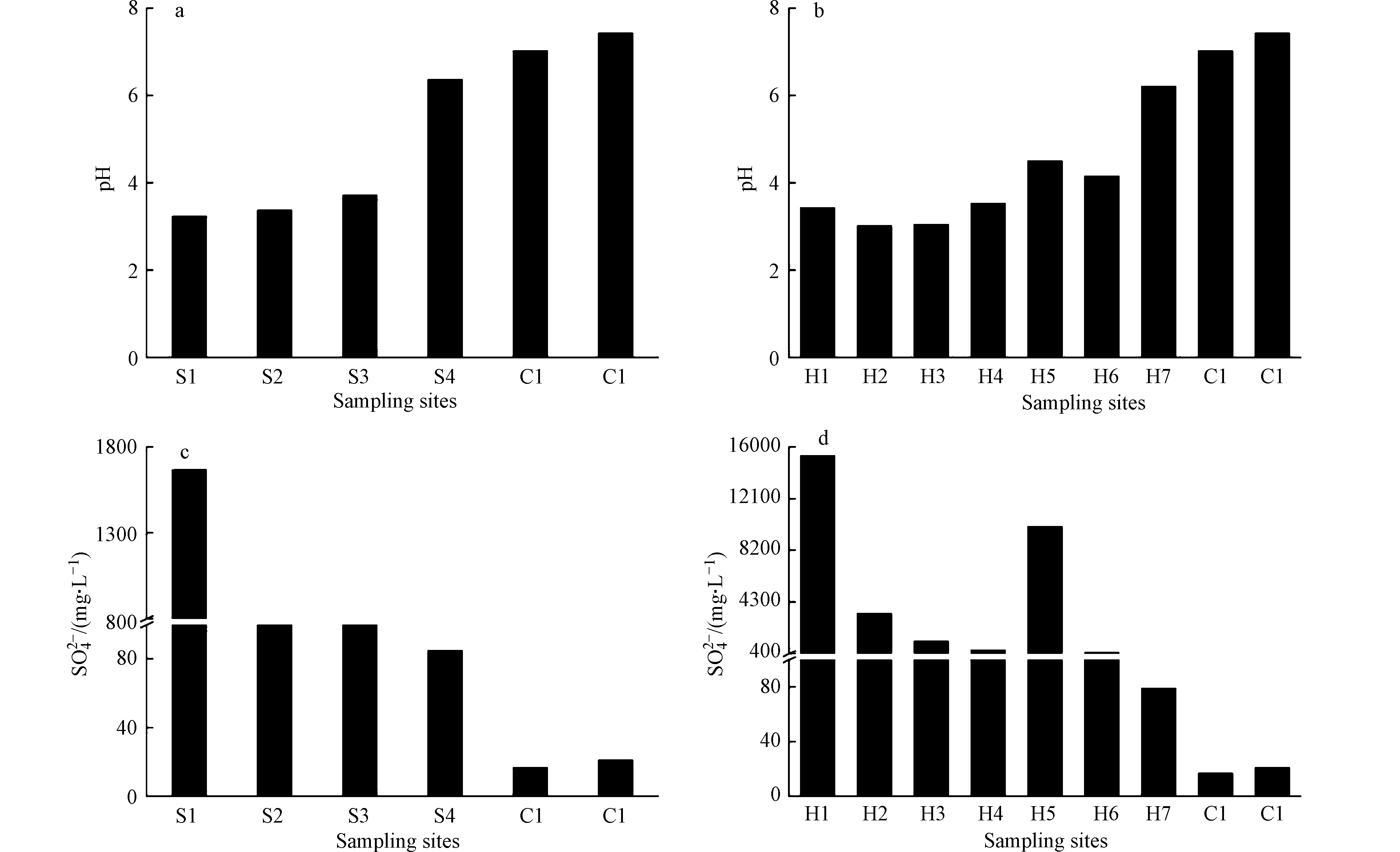
溶解性硫酸盐在河流中广泛存在,其来源主要包括大气沉降、岩石矿物风化、硫化物氧化以及人类活动所产生的含硫污染物[16]。失曹河与黄屯河水样中
SO2−4 含量及pH如图2所示。失曹河中水的pH值在3.24—6.37之间,黄屯河中水的pH值在3.02—6.21之间,均呈酸性,说明受AMD的影响显著;对照点位C1和C2水的pH值分别为7.03和7.43。两条河流水中SO2−4 含量变化波动非常大,失曹河SO2−4 含量平均值为347.10 mg·L−1,范围在85.06—1669.04 mg·L−1;而黄屯河平均值为673.42 mg·L−1,范围在79.05 mg·L−1—15348.10 mg·L−1;两条河流SO2−4 含量均远高于对照点位C1和C2的含量。如图2所示,失曹河水样中的
SO2−4 含量从上游到下游(S1—S4)逐渐降低。黄屯河H1点位SO2−4 含量很高,这是因为H1点位距离尾矿库最近,接受尾矿库AMD输入较多。黄屯河水样SO2−4 含量沿河流方向总体上呈现下降趋势,但是在H5点位明显增高,野外调查时发现H5点位附近有其他点源酸性废水排入,导致SO2−4 升高。研究表明,硫酸盐进入河流后通过稀释扩散、吸附与解吸、沉淀与溶解以及氧化还原等过程发生迁移转化,硫酸根在AMD污染河流中河水稀释作用明显[17]。除河流稀释作用外,SO2−4 的迁移、转化对其浓度也具有重要的影响。硫酸根在金属硫化物矿区AMD污染河流中的迁移过程及其作用机制的研究[18-19]表明,河流中SO2−4 浓度的降低还与含铁次生矿物生成及其吸附密切相关,如形成的施氏矿物可进一步吸附硫酸根;另外,在酸性水体中,以天然粘土矿物为主的悬浮物和沉积物的表面带正电荷,具有较强的吸附SO2−4 能力。SO42-的迁移呈保守元素特征,河水中SO2−4 的迁移行为与水体的pH值紧密相关[20]。如图2所示,本研究中两条河流水中SO2−4 浓度与pH整体上呈负相关。 -
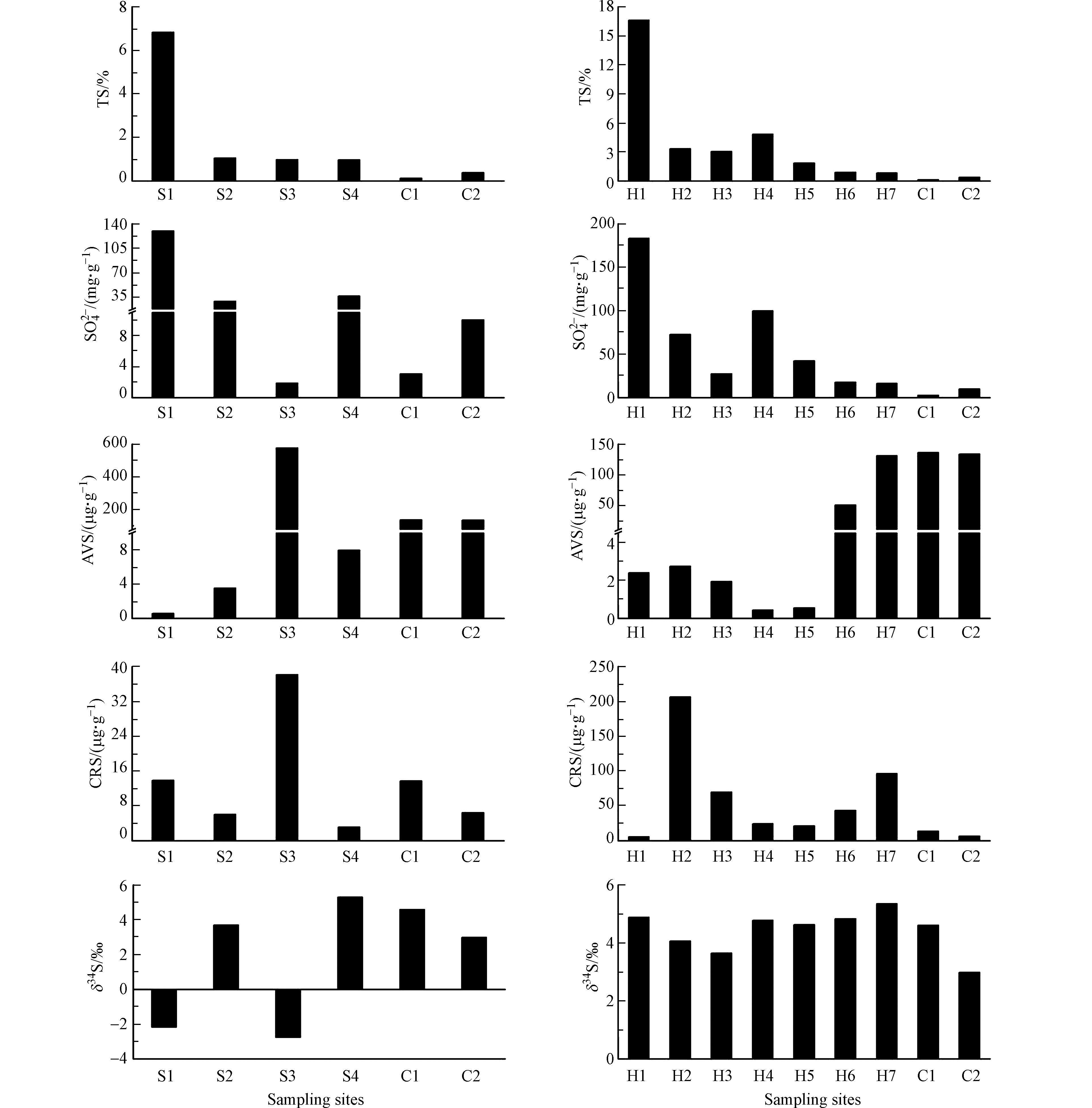
失曹河沉积物中TS平均含量为2.46%,变化范围为0.97%—6.84%;
SO2−4 平均含量为42.34 mg·g−1,变化范围为1.90—129.79 mg·g−1。黄屯河沉积物中TS平均含量为3.03%,变化范围为0.83%—16.62%;SO2−4 平均含量为65.75 mg·g−1,变化范围为16.42—183.31 mg·g−1。如图3所示,两条河流沉积物中TS与SO2−4 的变化趋势高度一致,SO2−4 占TS比例均值在60%以上,表明SO2−4 是沉积物中硫的主要存在形式。如图3所示,失曹河沉积物中AVS的平均含量为5.80 μg·g−1,变化范围为0.58—577.10 μg·g−1,CRS的平均含量为9.97 μg·g−1,变化范围为3.09—38.14 μg·g−1。黄屯河沉积物中AVS的平均含量为2.40 μg·g−1,变化范围为0.43—131.51 μg·g−1,CRS的平均含量为43.54 μg·g−1,变化范围为5.76—206.33 μg·g−1。两条河流沉积物中还原态无机硫均以CRS为主,而在受AMD影响较弱的点位则AVS较高。还原态无机硫是硫转化、循环过程中的重要中间产物,一般易被化学或生物氧化[21]。硫酸盐还原一般是厌氧条件下硫酸盐还原菌介导的耦合有机质降解过程,产生的H2S可与沉积物中的活性铁反应生成FeS[22]。FeS可通过与沉积物中的H2S、元素硫或者聚硫化物反应生成稳定的黄铁矿[23]。黄屯河在H6、H7点位水位变深,还原条件加强,这些点位AVS含量显著高于其他点位,指示了这些点位沉积物中
SO2−4 发生了还原转化,生成了AVS;失曹河在S3点位AVS含量显著增加,达到577.10 μg·g−1,指示在该点位也发生了SO2−4 的还原转化。两条河流多个点位沉积物中的CRS含量高于对照组,而AVS的含量除了S3点位明显高于对照组外,其他均低于对照组。总体上,对照点位沉积物AVS>CRS,而河流沉积物中AVS<CRS,这很可能是由于对照点位沉积物有机质含量高,水位深,易于形成AVS,而大部分河流点位受AMD影响显著,水位较浅,与大气连通性好,不利于AVS的形成。沉积物中还原形态硫的转化受到氧化还原条件、硫酸盐还原菌、有机质、活性铁等多种因素影响,与一系列环境生物地球化学过程耦合,因而具有多种生态环境效应[24-26]。例如沉积物中硫酸盐异化还原形成的S2−可有效结合二价重金属离子,使其难以再次释放到水环境中,显著影响金属的生物有效性[27]。本研究中沉积物硫形态分布与转化分析可为今后开展AMD输入对河流产生的重金属污染环境效应研究奠定基础。
-
自然界中不同来源的硫通常具有不同的同位素组成,并且在硫的迁移、转化过程中会发生分馏,因此硫同位素可用来示踪硫的来源及其迁移、转化过程[28-30]。研究表明,在自然条件下硫酸盐被还原成无机硫化物的过程中硫同位素分馏明显[31-32],形成的硫化物硫同位素组成显著亏损34S,剩余的硫酸盐则更集34S,而硫化物的氧化过程不产生硫同位素分馏[33-34]。本研究两条河流沉积物的δ34
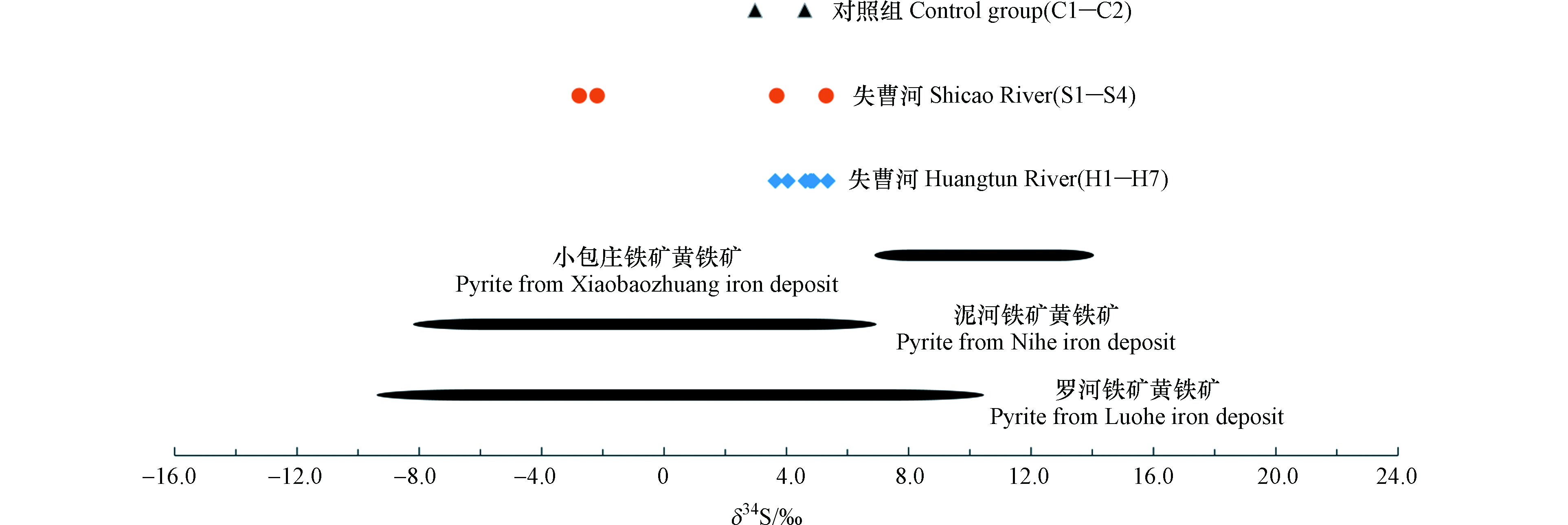
SSO4 沿程变化如图3所示,失曹河δ34SSO4 范围为−2.8‰—5.3‰;黄屯河δ34SSO4 范围为3.7‰—5.4‰。失曹河沉积物δ34SSO4 变化幅度比黄屯河稍大,S1和S3点位δ34SSO4 明显偏负。对照组两个点位δ34SSO4 为3.0‰和4.6‰,其反映的是区域大气降水和风化产物混合的自然背景信号。整体上,两条河流沉积物硫酸根硫同位素组成变化范围很窄,表明硫酸根来源相对单一。相关分析表明硫酸根硫同位素组成与各形态硫含量均无相关关系,指示本研究中有限的硫形态转化作用未对硫酸根硫同位素组成产生实质影响。由于未能采集到研究区黄铁矿样本,本文选取了研究区附近其它铁矿中黄铁矿硫同位素组成以做比较。如图4所示,泥河铁矿中黄铁矿的δ34S范围为−8.2‰—7.0‰[35],罗河铁矿中黄铁矿的δ34S范围为−9.3‰—10.4‰[36],小包庄黄铁矿的δ34S范围为6.9‰—14.2‰[37]。钟山、泥河和罗河铁矿地质成因一致[38],它们的黄铁矿很可能具有相似的硫同位素组成。本研究中两条河流沉积物中硫酸根硫同位素组成均落在泥河、罗河铁矿黄铁矿硫同位素组成区间内,指示失曹河和黄屯河沉积物中SO42-很可能主要来源于当地铁尾矿中黄铁矿的氧化。
值得注意的是,沉积物硫酸根硫同位素组成除失曹河S1和S3点位明显偏负外,两条河流其它点位与对照组基本重叠(图4),表明受酸性矿山废水影响显著的两条河流河沉积物硫酸盐来源也不能排除当地降水和自然风化背景,不过基于两条河流非常高的硫酸根含量水平,其来源主要应是钟山尾矿区酸性矿山废水,也即尾矿中黄铁矿的氧化。在利用硫同位素示踪硫酸盐来源时,有时会遇到物源同位素信号重叠以及生物地球化学转化导致的硫同位素分馏等而难以分辨其来源,在今后的研究中可尝试同时分析硫酸盐硫和氧双同位素组成以做更有效的示踪。
-
庐江失曹河与黄屯河河水呈酸性,受钟山尾矿区AMD影响显著,需进一步加强AMD漏排管理与控制。河水
SO2−4 受稀释和迁移转化作用,从上游至下游呈递减趋势。沉积物中SO2−4 是硫的主要存在形态,而CRS是还原无机硫的主要形态;部分点位沉积物SO2−4 发生还原转化并形成AVS。河流沉积物中非常高的硫酸根含量及其变化幅度很窄的硫同位素组成,指示其来源主要是钟山尾矿区酸性矿山废水,也即尾矿中黄铁矿的氧化。
安徽庐江钟山尾矿区河流水体硫形态及硫同位素分布特征
Distribution characteristics of sulfur species and isotopes in sediments of rivers around Zhongshan tailing at Lujiang County, Anhui Province
-
摘要: 分析了安徽省庐江县钟山尾矿区周边受酸性矿山废水影响的失曹河和黄屯河水体硫形态及硫酸根(
SO2−4 )硫同位素组成与分布特征。结果表明,两条河流河水整体呈酸性;失曹河河水SO2−4 含量为85.06—1669.04 mg·L−1(均值347.10 mg·L−1),黄屯河河水SO2−4 含量为79.05—15348.10 mg·L−1(均值673.42 mg·L−1);两条河流河水SO2−4 含量沿流向呈下降趋势。河流沉积物SO2−4 占总硫比值超过60%,是硫的主要存在形态。失曹河沉积物中酸可挥发性硫(AVS)含量为0.58—577.10 μg·g−1(均值5.80 μg·g−1);黄铁矿硫(CRS)含量为3.09—38.14 μg·g−1(均值9.97 μg·g−1);SO42-含量为1.90—129.79 mg·g−1(均值33.20 mg·g−1)。黄屯河沉积物中AVS含量为0.43—131.51 μg·g−1(均值2.40 μg·g−1);CRS含量为5.76—206.33 μg·g−1(均值43.54 μg·g−1);SO2−4 含量为16.42—183.31 mg·g−1(均值42.34 mg·g−1)。失曹河沉积物δ34SSO4 范围为−2.8‰—5.3‰;黄屯河沉积物δ34SSO4 范围为3.7‰—5.4‰,指示河流中的SO2−4 主要来源于尾矿中黄铁矿的氧化。失曹河S3点位及黄屯河H6、H7点位沉积物的AVS含量高于上游点位,指示了随着河流下游水位增加、还原环境增强,沉积物中部分SO2−4 发生了还原并生成AVS,但δ34SSO4 未有明显变化。本研究表明,失曹河和黄屯河受酸性矿山废水影响明显,庐江钟山尾矿区需进一步加强酸矿水漏排控制。Abstract: In this study, sulfur species and sulfur isotope of sulfate in sediments from Shicao and Huangtun rivers which affected by Acid Mine Drainage (AMD) near Zhongshan tailing, Lujiang County were analyzed and discussed. Overall, the waters in these two rivers were acidic. The concentration of sulfate (SO2−4 ) in waters of Shicao river ranged from 85.06 mg·L−1 to 1669.04 mg·L−1, with a mean of 347.10 mg·L−1, while that of Huangtun river ranged from 79.05 mg·L−1 to 15348.10 mg·L−1, with a mean of 673.42 mg·L−1; All of them showed a decline trend from upstream to downstream.SO2−4 in sediments was very high, and it was the main species of sulfur in these two rivers. The ranges ofSO2−4 , acid volatile sulfur (AVS) and pyrite sulfur (CRS) in Shicao river sediments were 1.90—129.79 mg·g−1, 0.58—577.10 μg·g−1 and 3.09—38.14 μg·g−1, respectively; While those in Huangtun river were 16.42—183.31 mg·g−1, 0.43—131.51 μg·g−1 and 5.76—206.33 μg·g−1, respectively. The stable sulfur isotope ratios of sulfate (δ34SSO4 ) in Shicao and Huangtun river sediments were −2.8‰—5.3‰ and 3.7‰—5.4‰, indicating a source from the oxidation of local pyrites. High values of AVS in S3, H6 and H7 suggested a possible sulfate reduction in these sediments. The study indicated that more efforts should be made to control the AMD discharge in Zhongshan tailing.-
Key words:
- acid mine drainage /
- tailing /
- river sediments /
- sulfur species /
- sulfur isotope
-
硫在自然界中广泛分布,但地壳中含量仅为0.048%,并且主要存在于岩石矿物、化石燃料和海洋中。硫有多种存在形态,可分为无机硫和有机硫,其中无机硫包括硫酸盐、硫化物以及单质硫等,有机硫主要包括酯键硫和碳键硫[1]。沉积物和岩石中储存约7.80×1018 kg的硫,且主要以金属硫化物和石膏的形式存在。金属硫化物(如黄铁矿、磁黄铁矿、方铅矿、闪锌矿、黄铜矿和砷黄铁矿等)尾矿在空气、水和微生物作用下氧化、酸化,形成含大量重金属离子的酸性矿山废水(acid mine drainage, AMD)[2-3]。AMD随地表径流进入河流后,其携带的硫化物也会进入到沉积物中并迁移转化。自然界有32S、33S、34S和36S 的4种稳定同位素,地球化学研究中一般考虑丰度最大的34S和32S,其组成一般用δ34S表示[4]。不同源区的硫一般具有不同的同位素组成特征,且不同形态硫的来源和迁移过程也不尽相同,因此,硫同位素组成可用来指示硫的来源以及迁移转化过程[5-6]。
沉积物是水生态系统的重要组成部分,是众多污染物在环境中迁移转化的载体、归宿和蓄积库,是研究污染物环境地球化学循环的重要载体[7-9]。在硫的迁移、转化过程中,地表径流携带的硫素被输送到河流与海洋,这些硫一部分被浮游动植物及鱼类利用,其余部分在水-沉积物界面发生复杂的生物地球化学迁移转化,最终埋藏于河流或海洋底部[10]。沉积物中的无机硫主要包括硫酸盐、酸可挥发性硫(AVS)、黄铁矿硫(CRS)和单质硫(ES)等。AVS是指在酸性条件下能够分解生成硫化氢的那部分硫化物,化学性质相对活跃,主要包括结晶型马基诺矿、游离硫化物、无定型FeS等以及其它二价金属硫化物[11],可进一步与铁反应生成更为稳定的黄铁矿。CRS(FeS2)化学性质较为稳定,不溶于盐酸,是硫铁化物成岩后的最终产物[12]。
庐江县是安徽省矿产资源富集区之一,有“地下聚宝盆”之称,也是安徽省确定的第五大工矿区和重点开发建设的工矿基地。全县共有以龙桥、矾山、泥河和罗河为代表的大小矿区(床)77个,保有资源储量居全省前五位的有6种矿产,其中铅、锌、硫铁矿、明矾石等4种居首位,铜矿居第二位,铁矿居第三位[13]。钟山铁矿床位于庐枞火山岩盆地北部,规模为中型铁矿,主要矿石类型为赤铁矿和磁铁矿,并共生黄铁矿[14]。庐江县钟山铁矿于1967年开始建设矿山,1979年投产开采[14]。采选矿形成的尾矿中硫化物经氧化、酸化形成AMD,随雨水径流排入河流,给局地的水生态环境带来潜在危害。
本文以安徽省庐江县钟山铁矿尾矿库周边失曹河与黄屯河为研究对象,采集河流水和沉积物样品,分析了水和沉积物硫形态含量、硫酸根硫同位素组成及其分布特征,为尾矿区酸性矿山废水环境影响及其排放控制提供基础参考。
1. 材料与方法 (Materials and methods)
1.1 样品采集与处理
如图1所示,庐江县失曹河与黄屯河上游均发源于钟山尾矿库周边,受到酸性矿山废水的影响,两条河流从尾矿库周边分别经西、东方向,从上游往下游向北流入庐江县天河,并最终汇入长江。本文研究样品采集于2017年7月,采样点分布见图1,失曹河点位为S1—S4,黄屯河点位为H1—H7,其中S1和H1靠近尾矿区,H5处有化工污染的复合酸性水排入,S4和H7靠近县河道,C1、C2是未受AMD污染的河流对照点位。分别采集各点位水和沉积物样品并置于冰袋冷藏箱中,带回实验室待分析.
1.2 样品分析
河流水体pH在现场由便携式pH计(HQ11D)测定。采集的河流水样经0.45 μm膜过滤后用离子色谱仪(型号: AQUION INTER,检测器型号: AS-DV)测定
SO2−4 SO2−4 SO2−4 BaSO4硫同位素分析采用气体稳定同位素比值质谱仪MAT253、Flash EA 2000型元素分析仪以及Conflo Ⅳ连续流装置完成(中国科学院地球化学研究所)。将含有不超过100 μg硫的制成样品和3倍于样品的V2O5包裹于锡杯中,由自动进样器送入填充氧化剂WO3及还原剂Cu的反应器中,样品落入反应管的同时送入氧气,此时反应管中富集纯氧,样品与锡迅速熔化燃烧,生成SO2及SO3,SO3在Cu的还原下生成SO2,之后被氦气流载入质谱分析。所用标样为IAEA-SO-5 (+0.5‰), IAEA-SO-6 (−34.1‰)和NBS 127 (+20.3‰),其分析结果用相对于国际标准CDT的δ34S表示,测试精度优于0.2‰ (1σ)。
沉积物中还原态无机硫含量采用改进的“冷扩散法”测定[15]。具体步骤如下:取解冻新鲜沉积物样品2—4 g迅速置于反应瓶中,先后加入盐酸(6 mol·L−1)、还原态氯化铬和DMF (N-N二甲基甲酰胺)分别将沉积物中的AVS、CRS和ES转化为硫化氢气体,并用氮气将其吹入装有碱式醋酸锌的吸收瓶中固定为硫化锌沉淀,实验过程中通过90 ℃水浴加热将反应时间分别缩短为1.5、2、2 h,再通过亚甲基蓝分光光度法测定其含量,本研究ES因含量太低而未检出。实验中采用加入固体ZnS的方式进行AVS的回收实验,回收率为82.01%—108.71%,加标回收率为82.34%—114.71%。
2. 结果与讨论 (Results and discussion)
2.1 河水
SO2−4 溶解性硫酸盐在河流中广泛存在,其来源主要包括大气沉降、岩石矿物风化、硫化物氧化以及人类活动所产生的含硫污染物[16]。失曹河与黄屯河水样中
SO2−4 SO2−4 SO2−4 SO2−4 如图2所示,失曹河水样中的
SO2−4 SO2−4 SO2−4 SO2−4 SO2−4 SO2−4 SO2−4 SO2−4 SO2−4 2.2 河流沉积物中硫形态分布
失曹河沉积物中TS平均含量为2.46%,变化范围为0.97%—6.84%;
SO2−4 SO2−4 SO2−4 SO2−4 SO2−4 如图3所示,失曹河沉积物中AVS的平均含量为5.80 μg·g−1,变化范围为0.58—577.10 μg·g−1,CRS的平均含量为9.97 μg·g−1,变化范围为3.09—38.14 μg·g−1。黄屯河沉积物中AVS的平均含量为2.40 μg·g−1,变化范围为0.43—131.51 μg·g−1,CRS的平均含量为43.54 μg·g−1,变化范围为5.76—206.33 μg·g−1。两条河流沉积物中还原态无机硫均以CRS为主,而在受AMD影响较弱的点位则AVS较高。还原态无机硫是硫转化、循环过程中的重要中间产物,一般易被化学或生物氧化[21]。硫酸盐还原一般是厌氧条件下硫酸盐还原菌介导的耦合有机质降解过程,产生的H2S可与沉积物中的活性铁反应生成FeS[22]。FeS可通过与沉积物中的H2S、元素硫或者聚硫化物反应生成稳定的黄铁矿[23]。黄屯河在H6、H7点位水位变深,还原条件加强,这些点位AVS含量显著高于其他点位,指示了这些点位沉积物中
SO2−4 SO2−4 两条河流多个点位沉积物中的CRS含量高于对照组,而AVS的含量除了S3点位明显高于对照组外,其他均低于对照组。总体上,对照点位沉积物AVS>CRS,而河流沉积物中AVS<CRS,这很可能是由于对照点位沉积物有机质含量高,水位深,易于形成AVS,而大部分河流点位受AMD影响显著,水位较浅,与大气连通性好,不利于AVS的形成。沉积物中还原形态硫的转化受到氧化还原条件、硫酸盐还原菌、有机质、活性铁等多种因素影响,与一系列环境生物地球化学过程耦合,因而具有多种生态环境效应[24-26]。例如沉积物中硫酸盐异化还原形成的S2−可有效结合二价重金属离子,使其难以再次释放到水环境中,显著影响金属的生物有效性[27]。本研究中沉积物硫形态分布与转化分析可为今后开展AMD输入对河流产生的重金属污染环境效应研究奠定基础。
2.3 河流沉积物中硫酸根硫同位素特征及其潜在来源
自然界中不同来源的硫通常具有不同的同位素组成,并且在硫的迁移、转化过程中会发生分馏,因此硫同位素可用来示踪硫的来源及其迁移、转化过程[28-30]。研究表明,在自然条件下硫酸盐被还原成无机硫化物的过程中硫同位素分馏明显[31-32],形成的硫化物硫同位素组成显著亏损34S,剩余的硫酸盐则更集34S,而硫化物的氧化过程不产生硫同位素分馏[33-34]。本研究两条河流沉积物的δ34
SSO4 SSO4 SSO4 SSO4 SSO4 SSO4 整体上,两条河流沉积物硫酸根硫同位素组成变化范围很窄,表明硫酸根来源相对单一。相关分析表明硫酸根硫同位素组成与各形态硫含量均无相关关系,指示本研究中有限的硫形态转化作用未对硫酸根硫同位素组成产生实质影响。由于未能采集到研究区黄铁矿样本,本文选取了研究区附近其它铁矿中黄铁矿硫同位素组成以做比较。如图4所示,泥河铁矿中黄铁矿的δ34S范围为−8.2‰—7.0‰[35],罗河铁矿中黄铁矿的δ34S范围为−9.3‰—10.4‰[36],小包庄黄铁矿的δ34S范围为6.9‰—14.2‰[37]。钟山、泥河和罗河铁矿地质成因一致[38],它们的黄铁矿很可能具有相似的硫同位素组成。本研究中两条河流沉积物中硫酸根硫同位素组成均落在泥河、罗河铁矿黄铁矿硫同位素组成区间内,指示失曹河和黄屯河沉积物中SO42-很可能主要来源于当地铁尾矿中黄铁矿的氧化。
值得注意的是,沉积物硫酸根硫同位素组成除失曹河S1和S3点位明显偏负外,两条河流其它点位与对照组基本重叠(图4),表明受酸性矿山废水影响显著的两条河流河沉积物硫酸盐来源也不能排除当地降水和自然风化背景,不过基于两条河流非常高的硫酸根含量水平,其来源主要应是钟山尾矿区酸性矿山废水,也即尾矿中黄铁矿的氧化。在利用硫同位素示踪硫酸盐来源时,有时会遇到物源同位素信号重叠以及生物地球化学转化导致的硫同位素分馏等而难以分辨其来源,在今后的研究中可尝试同时分析硫酸盐硫和氧双同位素组成以做更有效的示踪。
3. 结论 (Conclusion)
庐江失曹河与黄屯河河水呈酸性,受钟山尾矿区AMD影响显著,需进一步加强AMD漏排管理与控制。河水
SO2−4 SO2−4 SO2−4 -
-
[1] 单孝全, 陈斌. 土壤和河流沉积物中硫的形态分析 [J]. 环境科学学报, 1991, 11(2): 172-177. doi: 10.3321/j.issn:0253-2468.1991.02.007 SHAN X Q, CHEN B. Fractionation of sulfur in soil and river sediment [J]. Acta Scientiae Circumstantiae, 1991, 11(2): 172-177(in Chinese). doi: 10.3321/j.issn:0253-2468.1991.02.007
[2] YANG C, LU G, CHEN M, et al. Spatial and temporal distributions of sulfur species in paddy soils affected by acid mine drainage in Dabaoshan sulfide mining area, South China [J]. Geoderma, 2016, 281: 21-29. doi: 10.1016/j.geoderma.2016.06.032 [3] 吴惠明, 李晓, 李锦文, 等. 模拟风化过程硫铁矿尾矿的产酸性及污染物的释放行为 [J]. 环境化学, 2014, 33(3): 447-451. doi: 10.7524/j.issn.0254-6108.2014.03.002 WU H M, LI X, LI J W, et al. Acid generation behavior of pyrite tailing and characteristic of pollutant release during simulated weathering process [J]. Environmental Chemistry, 2014, 33(3): 447-451(in Chinese). doi: 10.7524/j.issn.0254-6108.2014.03.002
[4] 陕亮, 郑有业, 许荣科, 等. 硫同位素示踪与热液成矿作用研究 [J]. 地质与资源, 2009, 18(3): 197-203. doi: 10.3969/j.issn.1671-1947.2009.03.007 SHAN L, ZHENG Y Y, XU R K, et al. Review on sulfur isotopic tracing and hydrothermal metallogenesis [J]. Geology and Resources, 2009, 18(3): 197-203(in Chinese). doi: 10.3969/j.issn.1671-1947.2009.03.007
[5] 吴攀, 刘丛强, 张国平, 等. 矿山环境地表水系的硫同位素研究—以贵州赫章后河为例 [J]. 矿物岩石地球化学通报, 2007, 26(3): 224-227. doi: 10.3969/j.issn.1007-2802.2007.03.005 WU P, LIU C Q, ZHANG G P, et al. Sulfur Isotopic geochemistry of the water system in mine area a case study of the Hou River in Hezhang County, Guizhou, China [J]. Bulletin of Mineralogy, Petrology and Geochemistry, 2007, 26(3): 224-227(in Chinese). doi: 10.3969/j.issn.1007-2802.2007.03.005
[6] KILLINGSWORTH B A, BAO H M. Significant human impact on the flux and δ34S of sulfate from the largest river in North America [J]. Environmental Science & Technology, 2015, 49(8): 4851-60. [7] 黄飞, 王泽煌, 蔡昆争, 等. 大宝山尾矿库区水体重金属污染特征及生态风险评价 [J]. 环境科学研究, 2016, 29(11): 1701-1708. HUANG F, WANG Z H, CAI K Z, et al. Pollution characteristics and potential ecological risks of heavy metals in water of tailing zone in Dabaoshan Mine, Guangdong Province, China [J]. Research of Environmental Science, 2016, 29(11): 1701-1708(in Chinese).
[8] 陈明, 李凤果, 陶美霞, 等. 赣南典型矿区河流上覆水与表层沉积物重金属分布特征及风险评价 [J]. 环境化学, 2019, 38(7): 1461-1469. doi: 10.7524/j.issn.0254-6108.2018120706 CHEN M, LI F G, TAO M X, et al. Distribution characteristics and risk assessment of heavy metals in overlying water and surface sediments in rivers in typical mining areas of southern Jiangxi Province [J]. Environmental Chemistry, 2019, 38(7): 1461-1469(in Chinese). doi: 10.7524/j.issn.0254-6108.2018120706
[9] 贺梦醒, 高毅, 孙庆业. 尾矿废水对河流沉积物和稻田土壤细菌多样性的影响 [J]. 环境科学, 2011, 32(6): 1778-1785. HE M X, GAO Y, SUN Q Y. Influence of mine tailings drainage on microbial diversity in the river sediments and paddy soil [J]. Environmental Science, 2011, 32(6): 1778-1785(in Chinese).
[10] 曹爱丽, 周桂平, 胡姝, 等. 崇明东滩湿地沉积物中还原无机硫的形态特征 [J]. 复旦学报(自然科学版), 2010, 49(5): 612-617. CAO A L, ZHOU G P, HU S, et al. The chemical characteristic of reduced inorganic sulfur in the wetland sediments of Chongming Dongtan [J]. Journal of Fudan University (Natural Science), 2010, 49(5): 612-617(in Chinese).
[11] RICKARD D, MORSE J W. Acid volatile sulfide (AVS) [J]. Marine Chemistry, 2005, 97(3): 141-197. [12] WILKIN R T, BAMES H L. Pyrite formation by reactions of iron monosulfides with dissolved inorganic and organic sulfur species [J]. Geochimica et Cosmochimica Acta, 1996, 60(21): 4167-4179. doi: 10.1016/S0016-7037(97)81466-4 [13] 谢自信, 胡长友, 高一军, 等. 庐江县矿产资源总体规划[R]. 庐江县人民政府, 2010. XIE Z X, HU C Y, GAO Y J, et al. General planning of Lujiang county's mineral resources[R]. Lujiang County People's Government, 2010(in Chinese).
[14] 吴旭升. 安徽省庐江县钟山铁矿床地质特征及找矿方向 [J]. 华东地质, 2016, 37(3): 214-220. WU X S. Geological feature and exploration direction of the Zhongshan iron ore deposit in Lujiang County, Anhui Province [J]. East China Geology, 2016, 37(3): 214-220(in Chinese).
[15] 王小芳, 李方晓, 黄涛, 等. 安徽铜陵铜尾矿硫形态及硫同位素分布特征 [J]. 中国环境科学, 2019, 39(4): 1664-1671. doi: 10.3969/j.issn.1000-6923.2019.04.039 WANG X F, LI F X, HUANG T, et al. Distribution characteristics of sulfur species and isotopes in a copper tailing at Tongling, Anhui Province [J]. China Environmental Science, 2019, 39(4): 1664-1671(in Chinese). doi: 10.3969/j.issn.1000-6923.2019.04.039
[16] 郭照冰, 董琼元, 陈天, 等. 硫稳定同位素对环境污染物的示踪 [J]. 南京信息工程大学学报(自然科学版), 2010, 2(5): 426-430. GUO Z B, DONG Q Y, CHEN T, et al. Identification of pollutants using sulfur isotope [J]. Journal of Nanjing University of Information Science and Technology (Natural Science), 2010, 2(5): 426-430(in Chinese).
[17] CHEN M, LU G, GUO C, et al. Sulfate migration in a river affected by acid mine drainage from the Dabaoshan mining area, South China [J]. Chemosphere, 2015, 119: 734-743. doi: 10.1016/j.chemosphere.2014.07.094 [18] 杨成方. 金属硫化物矿区稻田土壤中硫素的迁移转化及次生硫酸盐矿物中重金属的溶出机制[D]. 广州: 华南理工大学, 2016. YANG C F. Migration and transformation of sulfur in paddy soil and dissolution of mechanism of heavy metal in secondary iron sulfate mineral in metal sulfide mine area[D]. Guangzhou: South China University of Technology, 2016(in Chinese).
[19] 陈梅芹. 硫酸根在金属硫化物矿区AMD污染河流中的迁移过程及其作用机制[D]. 广州: 华南理工大学, 2015. CHEN M Q. Sulfate migration and its mechanism in a river affected by acid mine drainage in metal sulfide mining area[D]. Guangzhou: South China University of Technology, 2015(in Chinese).
[20] 张国平. 贵州典型矿山的水环境地球化学特征[D]. 北京: 中国科学院研究生院, 2005. ZHANG G P. Case studies of the water envrionmental geochemistry of mines in Guizhou Province[D]. Graduate University of Chinese Academay of Science, 2005(in Chinese).
[21] GLOVER F, WHITWORTH K L, KAPPEN P, et al. Acidification and buffering mechanisms in acid sulfate soil wetlands of the Murray-Darling Basin, Australia [J]. Environmental Science & Technology, 2011, 45(7): 2591-2597. [22] JANAAEN G M, TEMMINGHOFF E J. In situ metal precipitation in a zinc-contaminated, aerobic sandy aquifer by means of biological sulfate reduction [J]. Environmental Science Technology, 2004, 38(14): 4002-4011. [23] 叶焰焰. 罗源湾滨海湿地沉积物中还原性无机硫的分布特征及影响研究[D]. 北京: 中国地质大学, 2017. YE Y Y. Study on the distribution and the effects of reduced inorganic sulfur in the sediment of Luoyuan Bay coastal wetland[D]. Beijing: China University of Geosciences, 2017(in Chinese).
[24] PESTER M, KNORR K H, FRIEDRICH M W, et al. Sulfate-reducing microorganisms in wetlands–fameless actors in carbon cycling and climate change [J]. Frontiers in Microbiology, 2012, 3: 1-19. [25] EGGER M, KRAAL P, JILBERT T, et al. Anaerobic oxidation of methane alters sediment records of sulfur, iron and phosphorus in the Black Sea [J]. Biogeosciences, 2016, 13(18): 5333-5355. doi: 10.5194/bg-13-5333-2016 [26] CHEN Y, SHEN L, HUANG T, et al. Transformation of sulfur species in lake sediments at Ardley Island and Fildes Peninsula, King George Island, Antarctic Peninsula [J]. Science of the Total Environment, 2020, 703: 135591. doi: 10.1016/j.scitotenv.2019.135591 [27] CHEN Y, GE J, HUANG T, et al. Restriction of sulfate reduction on the bioavailability and toxicity of trace metals in Antarctic lake sediments [J]. Marine Pollution Bulletin, 2020, 151: 110807. doi: 10.1016/j.marpolbul.2019.110807 [28] 韩珣, 任杰, 陈善莉, 等. 基于硫氧同位素研究南京北郊夏季大气中硫酸盐来源及氧化途径 [J]. 环境科学, 2010, 39(5): 2010-2014. HAN X, REN J, CHEN S L, et al. Sulfur sources and oxidation pathways in summer Aerosol from Nanjing Northern suburb using S and O isotopes [J]. Environmental Science, 2010, 39(5): 2010-2014(in Chinese).
[29] 夏迪. 基于硫氧双同位素的矿区河流中硫酸根来源识别及微生物转化研究[D]. 广州: 华南理工大学, 2018. XIA D. Minning river sulfate source identification and microbial transformation-Based on sulfur and oxygen isotopes[D]. Guangzhou: South China University of Technology, 2018(in Chinese).
[30] 蒋颖魁, 刘丛强, 陶发祥. 贵州乌江水系河水硫同位素组成特征研究 [J]. 水科学进展, 2007, 18(4): 558-565. doi: 10.3321/j.issn:1001-6791.2007.04.013 JANG Z K. Sulfur isotope composition characters of Wujiang river water in Guizhou province [J]. Advances in Water Science, 2007, 18(4): 558-565(in Chinese). doi: 10.3321/j.issn:1001-6791.2007.04.013
[31] 张伟, 刘丛强, 梁小兵. 硫同位素分馏中的生物作用及其环境效应 [J]. 地球与环境, 2007, 35(3): 223-227. ZHANG W, LIU C Q, LIANG X B. Biological function in sulfur isotope fractionation and environmental effect [J]. Earth and Environment, 2007, 35(3): 223-227(in Chinese).
[32] FRY B, COX J, GEST H, et al. Discrimination between 34S and 32S during bacterial metabolism of inorganic sulfur compounds [J]. Journal of Bacteriology, 1986, 165(1): 328-330. doi: 10.1128/JB.165.1.328-330.1986 [33] JUTTA K, MARTIN H S, STEFANO M B, et al. Sulfur isotope fractionation during growth of sulfate-reducing bacteria on various carbon sources [J]. Geochimica et Cosmochimica Acta, 2004, 68(23): 4891-4904. doi: 10.1016/j.gca.2004.05.034 [34] KAPLAN I R, RITTENBERG S C. Microbiological fractionation of sulfur isotopes [J]. Journal of General Microbiology, 1964, 34(2): 195-212. doi: 10.1099/00221287-34-2-195 [35] 张舒, 吴明安, 赵文广, 等. 安徽庐江泥河铁矿矿床地球化学特征及其对成因的制约 [J]. 岩石学报, 2014, 30(5): 1382-1396. ZHANG S, WU M A, ZHAO G W, et al. Geochemistry characteristics of Nihe iron deposit in Lujiang, Anhui Province and their constrains to ore genesis [J]. Acta Petrologica Sinica, 2014, 30(5): 1382-1396(in Chinese).
[36] 储雪蕾, 陈锦石, 王守信. 安徽罗河铁矿的硫同位素温度及意义 [J]. 地球化学, 1984(4): 350-356. doi: 10.3321/j.issn:0379-1726.1984.04.007 CHU X L, CHEN J S, WANG S X. Sulfur isotopic temperatures and their significance of Luohe iron deposit in Anhui Province [J]. Geochemistry, 1984(4): 350-356(in Chinese). doi: 10.3321/j.issn:0379-1726.1984.04.007
[37] 温冰冰, 张招崇, 谢秋红, 等. 安徽庐枞盆地小包庄铁矿的矿床地质特征和成矿机制以及与罗河铁矿的关系 [J]. 地质学报, 2018, 92(7): 1474-1492. doi: 10.3969/j.issn.0001-5717.2018.07.010 WEN B B, ZHANG Z C, XIE Q H, et al. Geological characteristics and metallogenic mechanism of the Xiaobaozhuang iron deposit and their genetic relationship with the Luohe iron deposit in the Lujiang-Zongyang basin, Anhui Province [J]. Acta Geologica Sinica, 2018, 92(7): 1474-1492(in Chinese). doi: 10.3969/j.issn.0001-5717.2018.07.010
[38] 吴明安, 汪青松, 郑光文, 等. 安徽庐江泥河铁矿的发现及意义 [J]. 地质学报, 2011, 85(5): 802-809. WU M A, WANG Q S, ZHEN G W, et al. Discovery of the nihe iron deposit in Lujiang, Anhui, and its exploration significance [J]. Acta Geologica Sinica, 2011, 85(5): 802-809(in Chinese).
-






















 下载:
下载: