-
自然土地处理系统因其成本低且运行管理简单的优点而被广泛应用于小规模分散式污水处理,其中人工湿地(constructed wetlands,CWs)在分散式污水处理应用方面最为常见,在世界范围内都有大量建造[1–3]。但诸多实践结果表明,CWs易受土地面积、气候条件、自身基质和操作参数等因素制约,且经常出现内部溶解氧不足的问题,导致在营养物质去除效果方面不尽如人意[4-5]。人工湿地有机负荷较低,也限制了其使用范围。
人工快速渗滤系统(constructed rapid infiltration system,CRIS)也属于土地渗滤处理类型,是在传统快速渗滤系统的基础上开发的,常以河砂代替天然土壤充当填料基质[6]。CRI系统运行具备经济和生态上的优势,且无需额外曝气,能综合物理、化学和生物反应机理有效处理污水[7]。目前关于CRIS的研究多集中于垂直流,垂直流CRIS应用研究的相关报道已较为丰富。
为了更好地满足分散式污水处理的要求,本研究设计构建了一个水平流人工渗滤系统(horizontal flow constructed infiltration system,HFCIS)(简称水平渗滤系统)。该系统结合了CRIS和水平潜流人工湿地(horizontal subsurface flow constructed wetlands,HSSFCWs)的特点,运行时无需种植植物。目前对HFCIS的研究报道极少,对于该技术的滤层结构、进水工艺参数、污染物处理影响因素和规律等,尚无深入的研究。本研究优化了水平渗滤系统的滤层结构和填料组成,并研究该系统在不同污染物质量浓度和水力负荷条件下的沿程去除效果,粗略分析系统内部污染物垂向分布情况,以此建立水平渗滤过程污染物去除的一级反应动力学方程,得出一阶去除速率常数,并与CRIS和HSSFCWs的速率常数做对比,为水平渗滤技术在小型分散式污水处理方面的实际应用化提供参考。
-
查询相关研究[8]可知,应用HSSFCWs处理废水的耗氧有机物(以COD计)和NH4+-N质量浓度通常分别约200 mg·L−1和20 mg·L−1。但废水所含污染物也可能达到较高质量浓度,如COD值在600 mg·L−1以上、NH4+-N质量浓度在40 mg·L−1以上[9-10]。为了更好地考察HFCI系统的处理性能,将实验分为4个阶段进行,编号为S1~S4,相关水质参数如表1所示。进水的营养物质由糖蜜或葡萄糖和氯化铵提供。
-
实验装置如图1所示。该水平流人工渗滤系统为自制,室外构建,采用厚度不低于10 mm的PVC板制作,槽体长宽高为2 m×0.2 m×0.4 m,沿长度方向设置有4个出水口,每个出水口之间相距0.4 m,分别编号为1#、2#、3#和4#,4#出水口为最终出水口。槽以一定角度倾斜放置,进水一端抬高约5 cm,使槽的另一端顺利出水。
槽所用填料为天然砂、碎石和木炭粉。天然砂尺寸为0.25~2 mm;碎石为石灰石,主要成分是碳酸钙,尺寸为2~5 cm;木炭粉是一种常见的用于CRIS的基质,廉价易得,对NH4+-N有较好的吸附效果[11],适量添加进系统也有利于提高有机物的去除效率[12],此处将其过50目筛。填充天然砂和木炭粉的两段区域是废水处理的主要区域,前一段长75 cm,后一段长50 cm。底下一层(20 cm)是以5∶1体积比混合的天然砂与木炭粉的混合填料,上面一层(10 cm)为纯天然砂。孔隙率较大的碎石在槽体前面、中间和后面部分都有填充,每一段长25 cm。
-
4个运行阶段皆采用间歇进水方式,直接将配制好的废水迅速倾倒于前面碎石段,每次进水量为5 L。S1和S2阶段进水COD值均为300 mg·L−1左右,S3和S4阶段分别提至约550 mg·L−1和650 mg·L−1;S1阶段进水NH4+-N质量浓度在20 mg·L−1左右,S2~S4阶段在40 mg·L−1左右。前3阶段的进水频率为1次·d−1,进水量为5 L·d−1,水力负荷皆为0.083 m·d−1,湿干比为1:5。S4阶段的进水频率增加到3次·d−1,进水量为15 L·d−1,间隔约8 h,水力负荷变为0.25 m·d−1,湿干比为3:5。每天取系统进水及4个出水口出水,水质检测指标为COD和NH4+-N。待系统运行稳定后,检测4个出水口的溶解氧(DO)质量浓度和pH。分别采用快速消解分光光度法和纳氏试剂分光光度法测定水样的COD和NH4+-N。使用便携式pH计和溶氧仪测定水中pH和DO。
污染物垂向分布实验方法:在系统运行稳定的情况下,某次进水后,出水基本完全时,分别在第1段填料区域L=15、30、45 cm处取上中下层填料,沿程取样点编号A、B、C,上层(5~10 cm)取样为纯天然砂,中(15~20 cm)、下层(25~30 cm)取样为混合填料。之后,取一定体积填料于50 mL锥形瓶中,加入一定量pH=1的硫酸溶液,填料与加入溶液体积比为1:3,保鲜膜密封瓶口后,放入恒温水浴振荡器,25 ℃、160 r·min−1振荡24 h,离心后0.45 μm滤膜过滤,取滤液进行COD和NH4+-N指标的检测分析。对照为不加填料的相应体积溶液。做3次平行,结果取平均值。
-
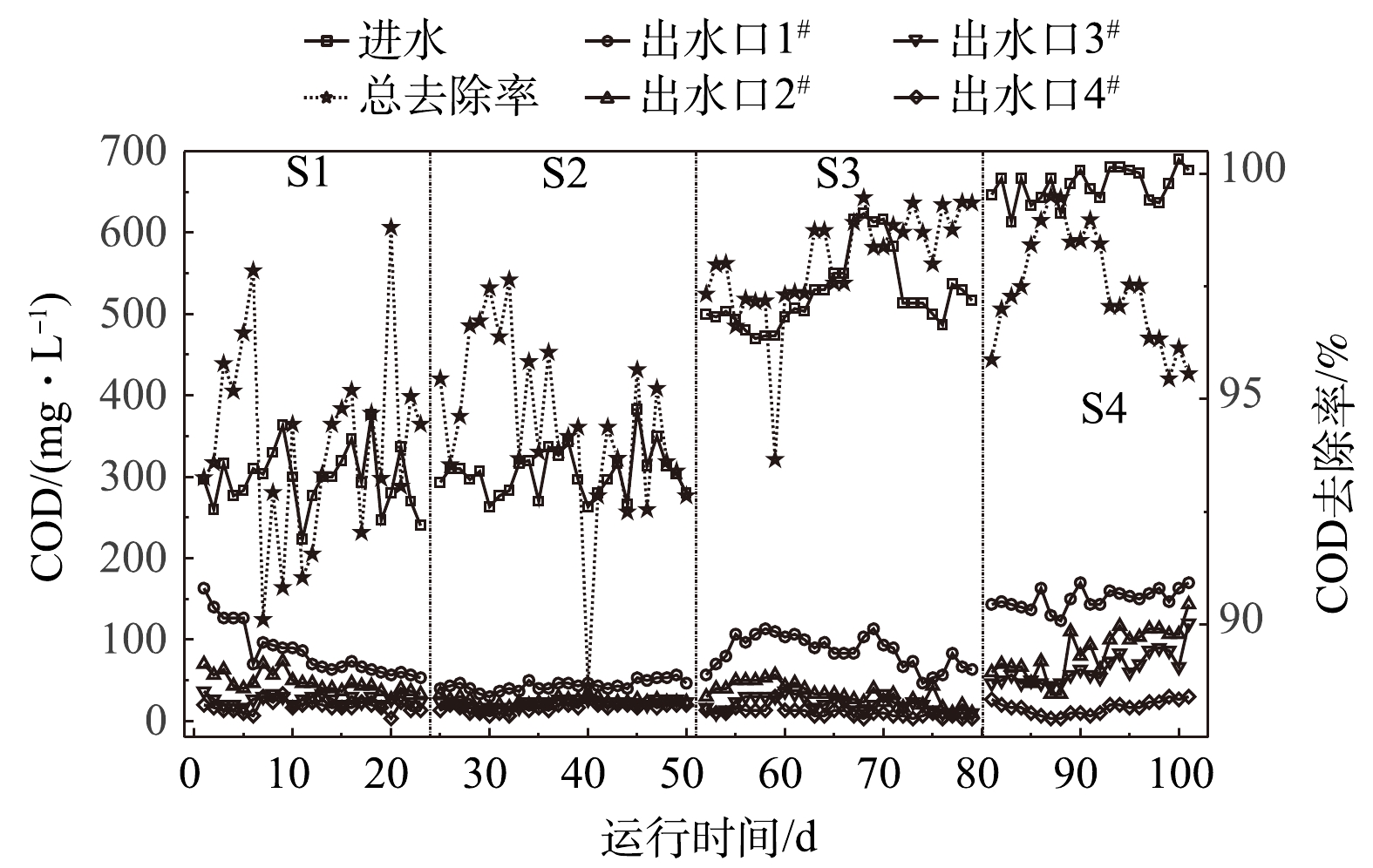
1)耗氧有机物(以COD计)的沿程去除效果。4个阶段的进出水COD值及去除率变化如图2所示。4个阶段的进水COD值分别为(300.00±76.67)、(323.33±60.00)、(546.67±76.66)和(651.67±38.34) mg·L−1。出水COD值分别为(18.33±15)、(18.34±11.66)、(16.67±13.33)和(16.67±13.34) mg·L−1。系统运行稳定后平均去除率分别达到94.48%、93.69%、98.98%和96.42%。S1阶段为微生物群落培养阶段,系统刚开始运行时,出水口1#、2#的出水COD值不断下降,且沿程4个出水口出水COD值有非常明显的递减关系。此时系统内部的微生物群落在不断生长富集,生物降解已开始发挥作用,还伴有一定的吸附作用。运行约13 d后,随着系统的生化降解性不断提高,截至出水口1#的COD去除率增加,后面填料区域的降解差异缩小,各出水口耗氧有机物(以COD计)浓度的递减关系逐渐弱化,表明有机物去除开始主要发生在系统的前半部分区域。
在系统稳定状态下,4个阶段中,截至出水口1#的长度分别能去除约80%、84%、87%和76%的耗氧有机物(以COD计);截至出水口2#的长度分别能去除约87%、92%、96%和83%的耗氧有机物(以COD计),后续耗氧有机物(以COD计)去除率平缓增长。该结果与AKRATOS等[13]在HSSFCWs得到的结果相似,即三分之二的有机物会在系统前三分之一的区域被去除。结果表明,尽管S3和S4阶段中进水COD值和水力负荷有明显提高,但最终COD去除率仍保持在95%以上,表明水平渗滤系统能承受较高有机负荷。
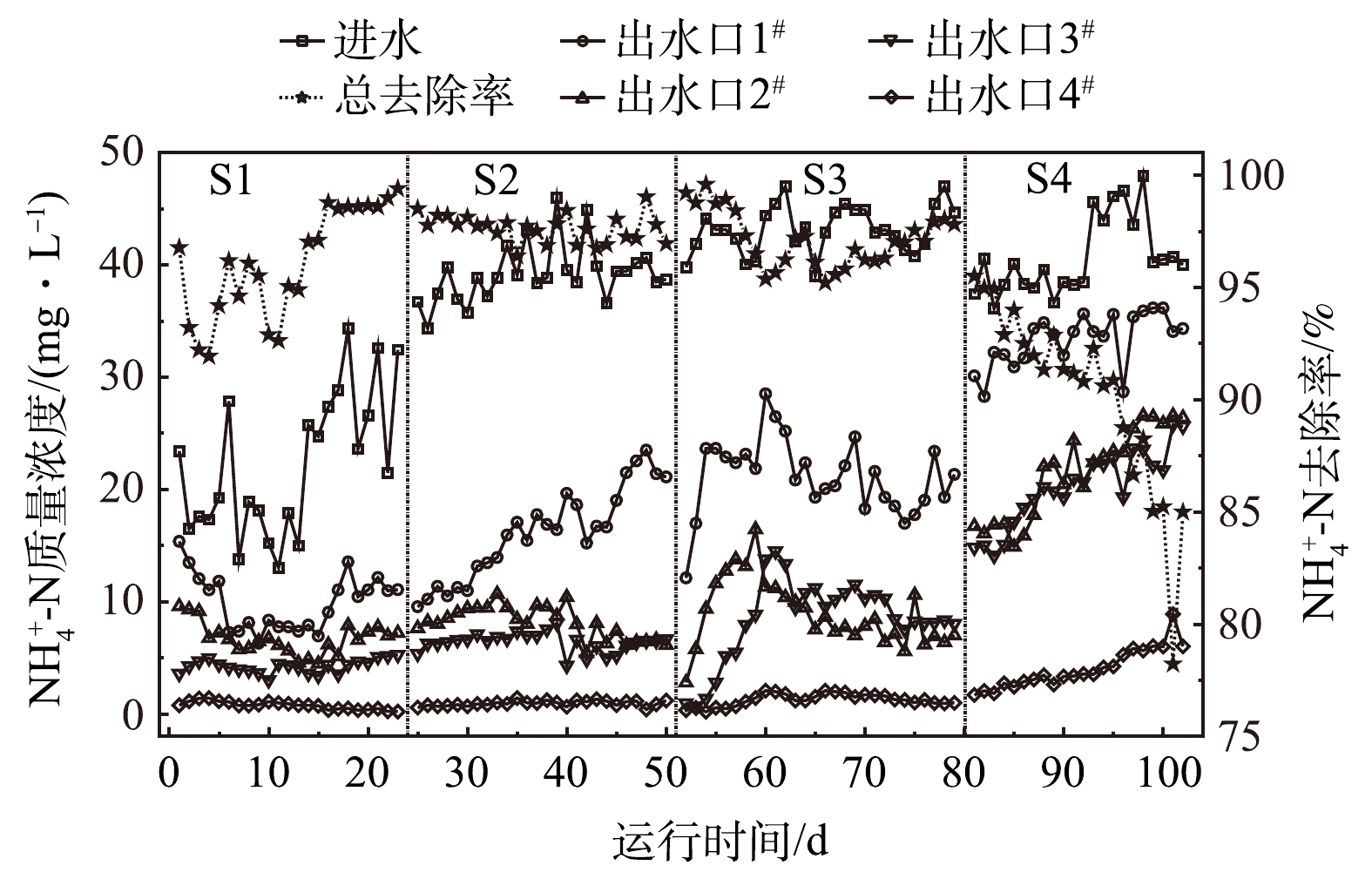
2) NH4+-N的沿程去除效果。4个阶段的NH4+-N进出水质量浓度及去除率变化如图3所示。4个阶段的NH4+-N进水质量浓度分别为(23.70±10.65)、(40.17±5.83)、(43.00±3.97)和(42.03±5.92) mg·L−1。出水质量浓度分别为(0.80±0.60)、(0.90±0.50)、(1.13±0.93)和(5.28±3.59) mg·L−1,系统运行稳定后平均去除率达到98.75%、97.59%、97.48%和85.30%。在S1阶段,系统内部的NH4+-N质量浓度为沿程降低。期间前3个出水口的出水NH4+-N质量浓度在不断变化,但总去除率在运行15 d后稳定下来。S2和S3阶段加大进水污染物质量浓度后,出水口1#的出水质量浓度逐渐增加,之后保持在一定范围内波动,而出水口2#和3#出水质量浓度都表现为先增加后下降。与耗氧有机物(以COD计)降解规律相同。前3个阶段的NH4+-N降解也主要发生在系统的前段填料区域,截至出水口2#分别能去除约76%、83%和83%的NH4+-N。在水力负荷明显提升的S4阶段中,除了各出水口出水NH4+-N质量浓度都有明显增加,NH4+-N的主要去除区域也有所改变,其中出水口3#、4#间填料区域能去除约40%的NH4+-N,与前3个阶段(14%~17%)相比有明显提高。
在整个系统运行期间,出水口2#、3#的NH4+-N出水质量浓度总是比较接近,甚至S3阶段稳定期的出水口3#出水质量浓度更高。推测是因为出水口2#、3#之间填料区域对NH4+-N的吸附已经到达极限,有部分NH4+-N解吸返回溶液中。有研究[14]表明,在渗滤过程中,NH4+-N会先被渗滤介质所吸附,之后在硝化菌的作用下被氧化去除,渗滤介质又恢复对NH4+-N的吸附能力,依此循环。S3阶段中,因为流入后段填料区域的溶液中NH4+-N质量浓度较小,培养繁殖起来的硝化菌较少,无法满足快速转化NH4+-N恢复填料吸附能力的要求,就会有部分NH4+-N解吸回到质量浓度较小的溶液中。而S4阶段后期未出现此类情况,此时流入后段填料区域的溶液中NH4+-N质量浓度翻了一倍,利于硝化菌生长。
综上所述,在较低水力负荷条件下,进水COD值为220~630 mg·L−1时,总去除率为88.6%~99.5%;进水NH4+-N质量浓度为13~47 mg·L−1时,总去除率为91.9%~99.6%。此时系统的最终出水污染物质量浓度能一直保持在较低水平,尽管进水污染物质量浓度有所变动,系统内部也能进行调节,最终达到稳定有效的污染物去除效果。加大水力负荷到0.25 m·d−1后,进水COD值和NH4+-N质量浓度分别为613~690 mg·L−1和36~48 mg·L−1的条件下,总去除率也能分别保持在95.5%~99.5%和78.2%~95.5%。在相似的耗氧有机物(以COD计)进水质量浓度为211~652 mg·L−1、NH4+-N为38.9 mg·L−1和水力负荷为0.042~0.16 m·d−1的条件下,比常规水平潜流湿地系统(COD去除率47%~89%;NH4+-N去除率48.3%)[9,15–17]对污染物的处理效果要好。
有研究[18]表明,CRI系统比CWs系统的处理能力高,其原因在于CRI系统的复氧能力强。因此,该系统运行稳定后,检测各出水口的DO出水质量浓度,结果如表2所示。
由表2可知,S1~S3阶段中系统内部的DO质量浓度为3.36~7.31 mg·L−1;S4阶段的DO质量浓度有所下降,为1.67~5.75 mg·L−1,整个系统内部基本处于好氧环境中。其中,各出水口DO质量浓度呈逐渐增加的趋势。系统运行期间内部DO质量浓度普遍高,可以猜测系统的复氧效率非常好,利于降解有机物的好氧微生物和硝化细菌生长,从而实现优异的耗氧有机物(以COD计)和NH4+-N去除性能。
-
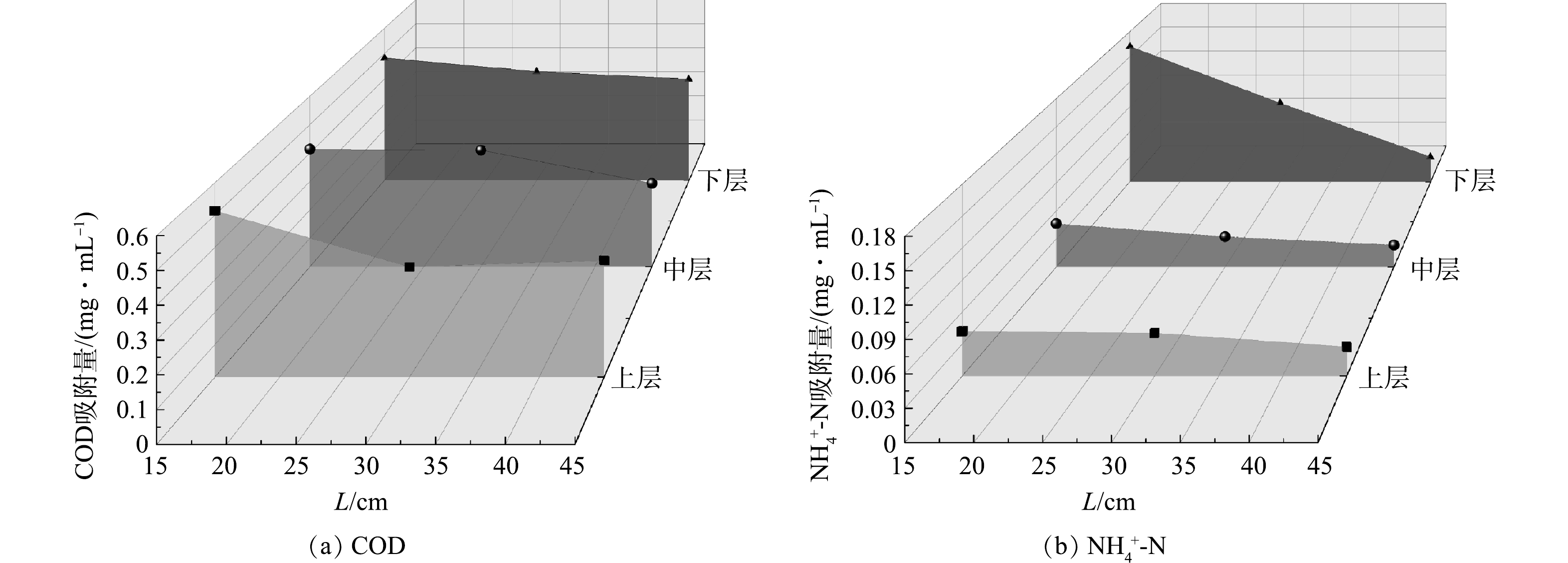
以出水基本完全、落干期刚刚开始时所取不同高度填料对各污染物的吸附量粗略判断污染物在系统内部的垂向分布情况,并使用origin软件进行单因素方差分析,对沿程各污染物吸附量的垂向变化进行差异性分析。P为显著性系数(0.01≤P<0.05表示显著,P<0.01表示极显著,P≥0.05表示不显著),结果如图4所示。
由图4可知,各层填料对各污染物的吸附量基本满足沿程减小的规律,其中下层的变化趋势最为明显。耗氧有机物(以COD计)的垂向分布最为均匀,A、B、C 3个取样点的上中下层吸附量之间均没有显著性差异。NH4+-N的垂向分布不均匀,各取样点的NH4+-N下层吸附量皆为最高,A、B取样点的各层吸附量间存在显著性差异。越靠近进水端的NH4+-N垂向吸附量差异越明显,随着污染物沿程逐渐降解,各高度层吸附量越接近,垂向分布越均匀。
因为污水主要在系统下层流动,所以通常下层填料的污染物吸附截留量最大。另一方面,由于自然环境土壤中普遍存在的毛细作用和蒸发作用,溶于溶液中的污染物质会被向上的水流带到土壤上、中层,水被蒸发后,一定量的污染物质就会附着在填料表面[19]。耗氧有机物(以COD计)和NH4+-N的垂向分布不同的原因可能在于,充当有机碳源的葡萄糖在水中溶解度较高,所以极易随着水流进行快速迁移。而大多数带正电荷的铵离子很容易首先被底部带负电荷的填料介质和微生物吸附截留下来[14]。
-
HFCIS内污染物质量浓度的沿程变化呈现一种逐渐衰减的趋势,假设系统稳定后在水平流向(X轴向)上为理想推流,污染物只在X轴向发生质量浓度变化,反应期间系统内部每个微小单元是混合均匀的。对于理想推流式生物反应器,可采用一级反应动力学方程(式(1))[20]来描述系统内部的污染物降解。
式中:ρL为系统沿程长度为L处污染物出水质量浓度,mg·L−1;ρ*为进水污染物质量浓度,mg·L−1;m为污染物去除速率常数,反映系统中污染物降解效率。m值与进水质量浓度ρ*和水力负荷q密切相关。
根据每天系统进水质量浓度ρ*及各出水口出水质量浓度ρL,计算ρL/ρ*。取每个阶段最后稳定期的7 d数据,分别编号为FT1~FT7、ST1~ST7、TT1~TT7和HT1~HT7,以L为横坐标,ρL/ρ*为纵坐标,设定经过约束点(0,1),进行指数拟合。其中,L为两段填充天然砂和木炭粉区域的长度。
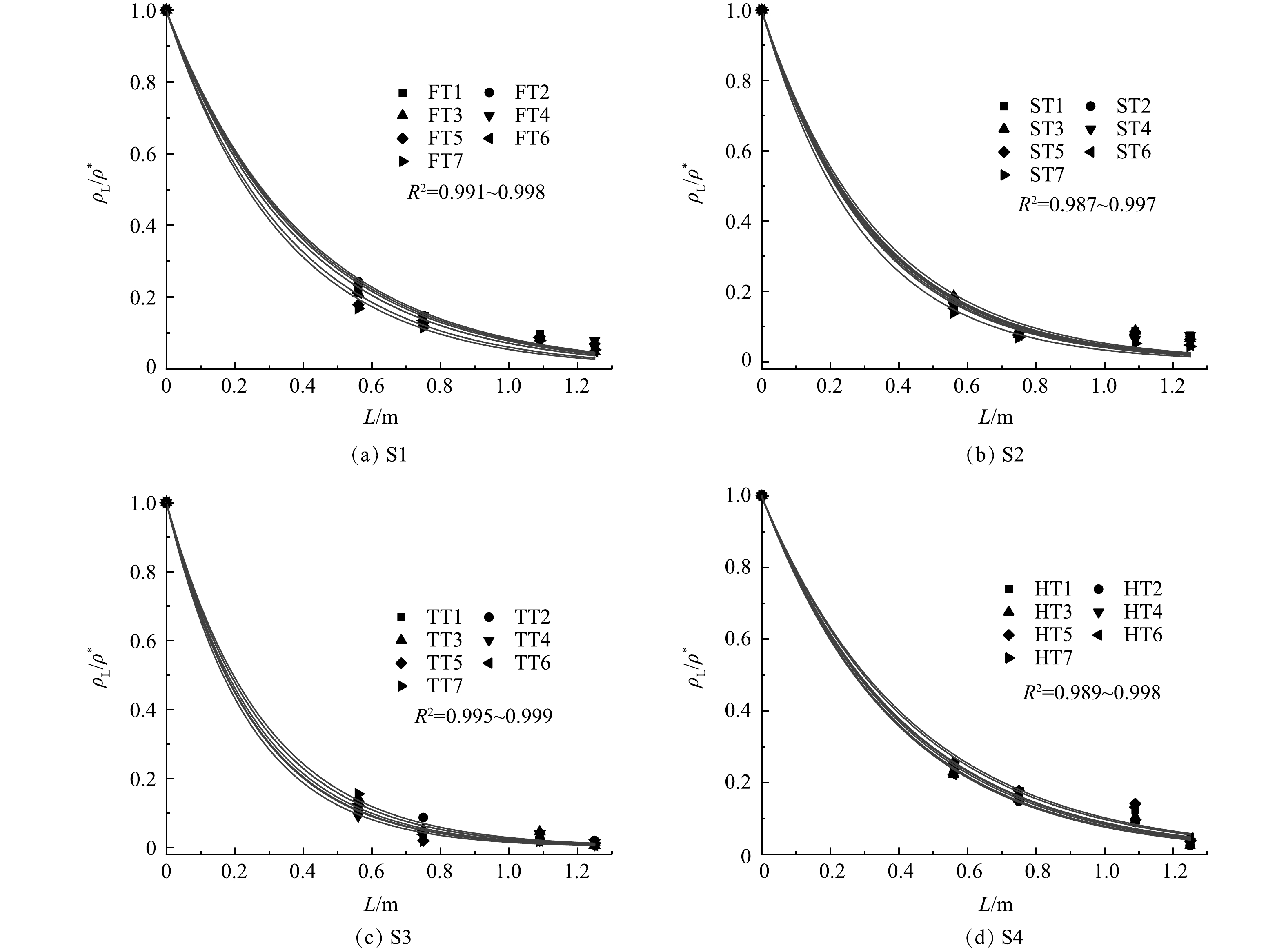
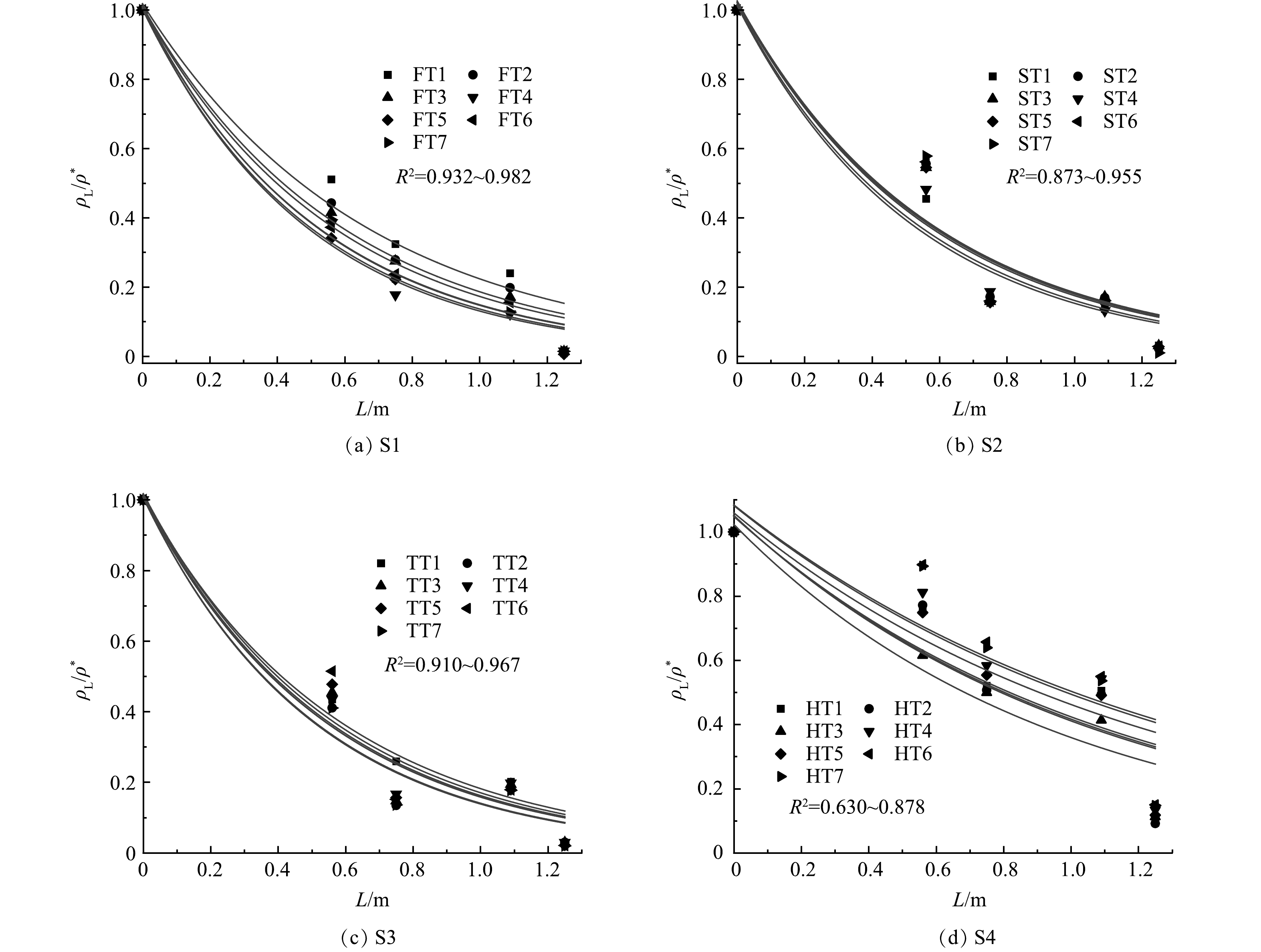
1)动力学拟合情况。根据沿程COD值和NH4+-N质量浓度数据对式(1)进行指数拟合如图5、图6所示。
耗氧有机物(以COD计)和NH4+-N指数拟合所得A值和m值如表3所示。实际拟合方程如式(2)所示。
式中:A为系数,修正实际拟合模型与理论模型之间的差距[21]。由图5、图6拟合曲线经过数据点情况和表3数据可知,使用式(2)表示有机物和NH4+-N降解动力学有较好的准确性。其中,4个阶段耗氧有机物(以COD计)拟合曲线R2值为0.987~0.999;前3个阶段的NH4+-N拟合曲线R2值为0.873~0.982,S4阶段R2值较低,最高仅0.878。由表3可知,耗氧有机物(以COD计)和NH4+-N拟合所得m值在已报道的垂直流CRIS的m值(mCOD=0.81~3.36;m氨氮=0.01~2.72),甚至处于较高的水平[22–26]。整体上看,相同水力负荷条件下,随着进水质量浓度的增加,耗氧有机物(以COD计)去除率及m值呈上升趋势;而NH4+-N去除率随着进水质量浓度增加呈下降趋势,m值却有所升高。水力负荷的增加使耗氧有机物(以COD计)、NH4+-N的去除率和m值都有所降低。
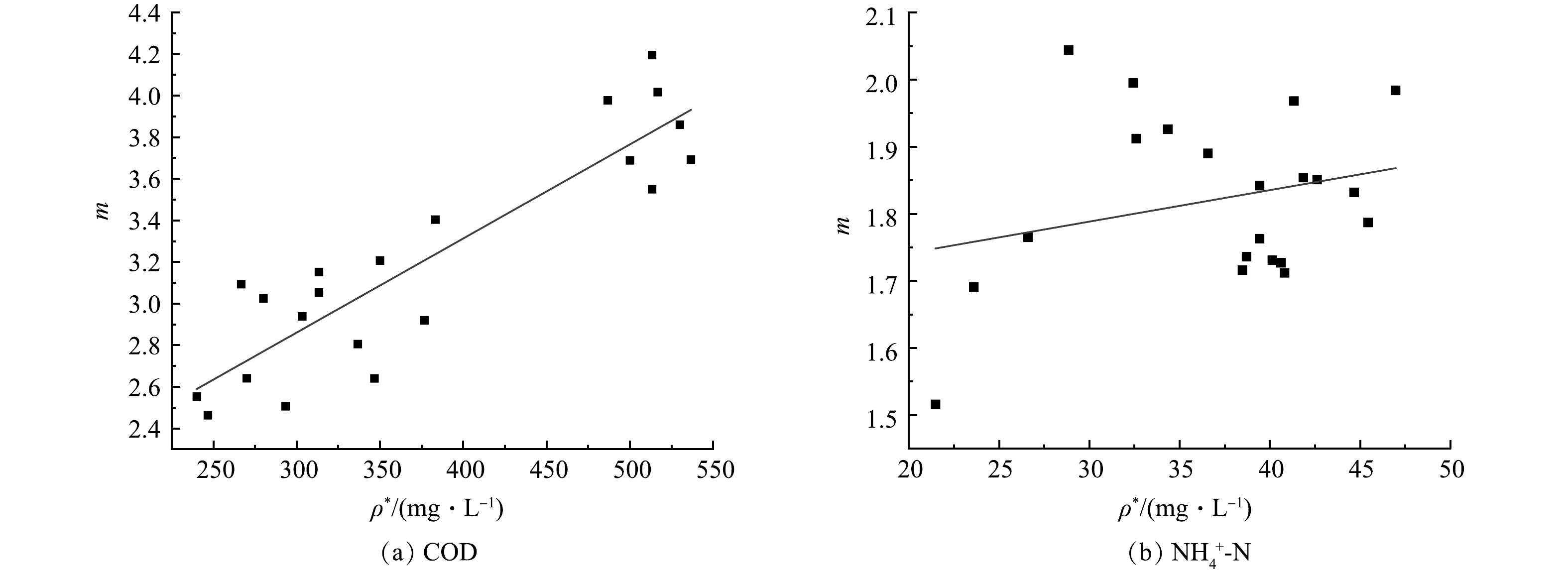
为了更直观表示进水质量浓度ρ*与m值之间的关系,将前3个阶段稳定期的ρ*与m值分别为横纵坐标进行线性拟合,结果如图7所示。由图7可知,耗氧有机物(以COD计)进水浓度与m值拟合得到一条明显为上升趋势的直线,ρ*与m为显著正相关,相关方程为m=(0.004 5±5.22×10−4)ρ*+(1.503 1±0.20)(R2=0.798)。当水力负荷固定时,系统m值随着进水有机物浓度的增加而增加,输入有机负荷的增加或者减小会带动系统有机物去除速率的上升或者降低,这是系统在不同进水质量浓度下能保持稳定良好出水质量浓度的原因,表明该系统有较高的有机负荷承受能力。这也说明,该系统的耗氧有机物(以COD计)去除速率常数并不是固定的,而是取决于进水质量浓度、水力负荷、填料结构等一系列影响因素。另一方面,NH4+-N进水质量浓度的增加没有明显提高m值,且m值与NH4+-N进水质量浓度间相关性不显著,表明NH4+-N去除还明显受到除进水质量浓度因素之外的限制,可能是因为氧交换速率、硝化菌总量无法在短期内迅速增加,所以导致硝化能力没有随着进水质量浓度增加而明显提高。
2)动力学常数比较。湿地系统也常采用一级动力学模型来反映污染物去除规律,但与本研究不同的是,HSSFCWs的一阶建模多集中于水力负荷变化的影响,主要考虑水力负荷或水力停留时间与处理效率之间的关系。水平潜流人工湿地的一阶动力学方程(式(3)、式(4))[27]有2种表现形式,可相互转化(式(5)、式(6)和式(7))[28]。
式中:t为水力停留时间,d;Q为流量,m3·d−1;n与填料特性有关,此处为填料有效孔隙率,%。kA和kV分别为基于面积和体积的一阶速率常数,分别用于确定湿地所需的面积和体积,可分别转化表示为式(8)和式(9)[29]。
kA和kV同样反映系统处理效率,该值越大,达到相同去除效果所需湿地面积或体积越小。将HFCI系统所得动力学系数与HSSFCWs的作对比评价,则换算m=(kvn)/q,kV=mq/n。将求得各m值及q=0.083/0.25 m·d−1、n=36%代入关系式求得kA和kV值如表4所示。由表4可知,随着水力负荷增加,耗氧有机物(以COD计)和NH4+-N的kA和kV值也有所增加。
目前已报道的一些HSSFCWs的kA和kV值如表5所示。由表4、表5可知,在相似的水力负荷率下,HFCIS的速率常数值在报道的HSSFCWs速率常数范围内,与近年来文献报道的潜流湿地速率常数值相比,也处于较高的水平。表明HFCI系统内耗氧有机物(以COD计)和氨氮的反应速率普遍高于HSSFCWs,能在实现污染物高效率去除的基础上大大缩小占地面积。
生物膜系统中,基质反应速率通常与物质在液相和生物膜相的传质过程密切相关[34]。另一方面,本研究所得污染物降解模型与曝气生物滤池遵循的一级动力学模型相似,即Eckenfelder方程(式(10))[35]。
式中:K和n分别是与微生物量、生物膜活性和填料特性相关的常数[36]。
上述由式(1)、式(2)所求得的m值可近似于式(7)的K/qn。另有研究者从微生物作用出发,推导土地渗滤系统的一级反应速率常数kV近似于vmax/Ks,而vmax和Ks均与微生物活性有关[18]。因此,考虑到HFCIS所用天然砂表面较为光滑,系统内部实际微生物量非常少,推测HFCRI系统污染物去除效果更好的原因在于该系统内部基质和氧的传质速率高、微生物活性强。因为填料间空隙很小,导致附着在填料表面的水膜和微生物膜很薄,基质和氧气都能更快速的传质进入微生物细胞,使微生物活性增强。
本研究计算所得去除速率常数主要用于与水平潜流湿地的去除速率常数作对比,在系统设计方面能在一定程度上预测污染物在系统内部的预期去除效果,从而优化HFCI系统的尺寸设计,以节约成本和占地面积。另一方面,因为湿地传统的一阶模型基于理想推流流态,通常无法完美反映系统内部的流体和污染物行为,且估计的去除速率常数取决于进水质量浓度和水力负荷等因素[37]。根据TRANG等[33]的研究结果,本文以系统从入口到出口的沿程污染物浓度分布为基础估算去除速率常数,或许能更准确地反映系统内部污染物去除的动力学过程。
-
1)水平渗滤系统有优异的耗氧有机物(以COD计)和NH4+-N去除性能,系统内部的高溶解氧质量浓度利于好氧微生物生存。整个运行期间的耗氧有机物(以COD计)和NH4+-N最终去除率分别为88.61%~99.47%和78.22%~99.58%,最终出水质量浓度满足《城镇污水处理厂污染物排放标准(GB 18918-2002)》一级A类标准。
2)耗氧有机物(以COD计)的垂向分布均匀,各取样点的上中下层吸附量之间没有显著性差异;NH4+-N主要分布在系统下层进行去除,前段区域不同高度间吸附量存在显著性差异。
3)沿程污染物出水质量浓度基本呈现逐渐衰减的趋势,以耗氧有机物(以COD计)和NH4+-N相关数据进行动力学拟合,有机物拟合效果更好,其速率常数m与进水质量浓度ρ*为显著正相关,而NH4+-N的m与进水质量浓度之间不存在显著相关关系。水力负荷的增加导致两指标的m值降低,但kA和kV值却有所增加。两指标的去除速率常数的变化在CRIS和HSSFCWs的速率常数范围内,甚至处于较高水平。
4)构建的水平渗滤系统结合了人工快渗和人工湿地的优点,构建、运行和管理简单,具备优异的污染物去除性能和污染负荷承受能力,在污水处理方面可大大改善水质,明显提高了土地利用效率,能很好地满足分散式污水处理的要求。
水平渗滤系统的污染物去除效果及动力学分析
Analysis of performance and kinetics of pollutant removal by a horizontal flow infiltration system
-
摘要: 基于人工快渗(CRIS)和水平潜流人工湿地(HSSFCWs)构建了水平流人工渗滤系统(HFCIS),研究了该系统对耗氧有机物(以COD计)、氨氮(NH4+-N)的沿程去除情况和污染物在系统内的垂向分布情况,并进行了动力学分析。结果表明,在水力负荷为0.083 m·d−1、进水耗氧有机物(以COD计)浓度为220~630 mg·L−1、NH4+-N质量浓度为13~47 mg·L−1时,COD、NH4+-N的去除率分别为88.6%和91.9%以上。在水力负荷为0.25 m·d−1的条件下,进水耗氧有机物(以COD计)和NH4+-N质量浓度分别为613~690 mg·L−1和36~48 mg·L−1时,总去除率分别为95.5%和78.2%以上。水平方向沿程污染物质量浓度呈现逐渐衰减的趋势,污染物降解符合一阶动力学模型,去除速率常数在CRIS和HSSFCWs的速率常数范围内并处于较高水平。该HFCI系统填料简单,复氧效果好,污染物去除性能优异,提高了土地利用率,建造位置选择较为灵活,在分散式污水处理中有独特的优势。Abstract: In this study, a horizontal flow constructed infiltration system (HFCIS) was constructed based on the artificial rapid infiltration (CRIS) and the horizontal subsurface flow constructed wetland (HSSFCWs). The removal of oxygen consuming organic matter (COD) and ammonia nitrogen (NH4+-N) along HFCIS and the vertical distribution of pollutants in HFCIS were studied, as well as the kinetic analysis. The results showed that at the hydraulic load of 0.083 m·d−1, the influent oxygen consuming organic matter (COD) concentration of 220~630 mg·L−1, and the influent NH4+-N mass concentration of 13~47 mg·L−1, the removal rates of COD and NH4+-N were higher than 88.6% and 91.9%, respectively. When the hydraulic loading was 0.25 m·d−1, the mass concentrations of influent oxygen consuming organic matter (COD) and NH4+-N were 613-690 mg·L−1 and 36-48 mg·L−1, the total removal rates were over 95.5% and 78.2%, respectively. The pollutant mass concentration along the horizontal direction showed a gradually decreasing trend. The pollutant degradation accorded with the first-order kinetic model, and the removal rate constant was at a high level in the range of CRIS and HSSFCWs rate constants. HFCI system had a simple filling, a good reoxygenation effect, an excellent pollutant removal performance, improved the land utilization rate with a flexible construction location selection. It has unique advantages in decentralized sewage treatment.
-
我国是抗生素生产大国,每年产生的抗生素菌渣量达到1.3×106 t以上[1]。菌渣在自然环境下易腐败变质,任意堆放极易造成环境污染。此外,菌渣不合理处置会导致其中的残留抗生素在环境介质中扩散和传播,从而对人群健康和生态环境造成巨大威胁。而另一方面,菌渣中含有大量的微生物菌丝体及未代谢利用完的有机物,营养物质含量丰富,可对其进行资源化利用。因此,如何将抗生素菌渣无害化处理及资源化利用已成为当今急需解决的难题。
好氧堆肥被广泛应用于固体有机废物处理,研究表明畜禽粪便或抗生素菌渣中的残留抗生素可以通过好氧堆肥降解[2-3]。菌渣经好氧堆肥后可被制成有机肥料,其不仅可提高土壤肥力,还保证了农产品品质安全[4]。堆肥中的微生物除了参与有机物料的分解外,其也对抗生素降解有重要作用。赵军超[5]发现,红霉素菌渣经好氧堆肥处理后降解率可达99%以上。这表明,好氧堆肥可实现抗生素菌渣无害化处理。
由于传统好氧堆肥温度不够高,限制了其对抗生素的降解[6]。因此,目前关于应用好氧堆肥法处理抗生素菌渣的研究都是在外源添加物的条件下进行的。一般外源添加物主要分为生物炭、氯化铁、天然沸石和生物菌剂等,而在好氧堆肥处理中添加生物菌剂效果显著[7]。研究发现,在堆肥中添加微生物菌剂,可提高堆肥温度,增加堆肥中微生物的种类和活性,延长高温分解周期,加快堆肥腐殖化进程,提高其中抗生素去除率,降低其环境风险,使堆肥成品达到无害化要求[8-12]。
本研究选取土霉素菌渣为研究对象,探究添加复合菌剂后土霉素菌渣和玉米秸秆混合堆肥的基本理化参数、堆肥中土霉素降解和微生物群落结构变化情况,并优化好氧堆肥对土霉素菌渣中残留土霉素的处理,为抗生素菌渣的无害化处理和资源化利用提供参考。
1. 材料与方法
1.1 堆肥原料
土霉素菌渣取自石家庄市某制药厂。玉米秸秆取自石家庄周边农户农田中,将其在105 ℃条件下烘干处理后破碎,长度约为1~2 cm。堆肥原料初始基本理化性质如表1所示。
表 1 堆肥原料基本理化性质Table 1. Basic physical and chemical property of compost raw materials供试样品 含水率/% pH 电导率EC/(mS·cm−1) C/N 玉米秸秆 9.89 5.32 2.67 50.89 土霉素菌渣 78.04 4.47 — 5.73 1.2 实验装置和设计
堆肥试验在河北科技大学堆肥实验场进行。堆肥容器容积70 L,底部连接曝气泵以调节气量,并装有气体流量计。装置中连有3个温度探头,对其上、中、下温度进行实时监控。本实验设计分为2组,一组添加自制菌剂A(制备方法见专利:申请号CN 202111337864.9,编号C);另一组不添加菌剂(编号CK)作为对照组。C组为15 kg菌渣+15 kg玉米秸秆+菌剂A(0.3%);CK组为15 kg菌渣+15 kg玉米秸秆。
通过调节气体流量计,控制曝气速度为7 L·min−1。采样天数设定为第0、4、8、15、22、28、34、38 d,每次取样前进行翻堆,每次取样在罐体的上、中、下3个平面取样,遵循5点取样原则。每次取200 g样品,分为2份保存,一份用真空冷冻干燥机(FD-1A 50,博医康(北京)仪器有限公司)冷冻干燥,然后在20 ℃下保存,用于土霉素质量浓度的测定,另一份在4 ℃下保存用于理化性质分析。
1.3 实验测定指标及分析方法
堆肥温度采用自制堆肥装置内PT100温度探头对温度进行实时监测,每天选取0、4、8、12、16、20 h进行数据记录;含水率的测定运用失重法,参照GB/T 1931-2009中检测方法[13];堆肥样品中pH采用雷磁ZD-2自动电位滴定仪测定(PHS-2F,上海仪电科学仪器股份有限公司);EC采用多参数在线测定仪(哈纳HI993302,上海耀壮检测仪器设备有限公司);全碳、全氮、全磷和全钾含量采用流动分析仪测定(AA3,英国希尔公司)。
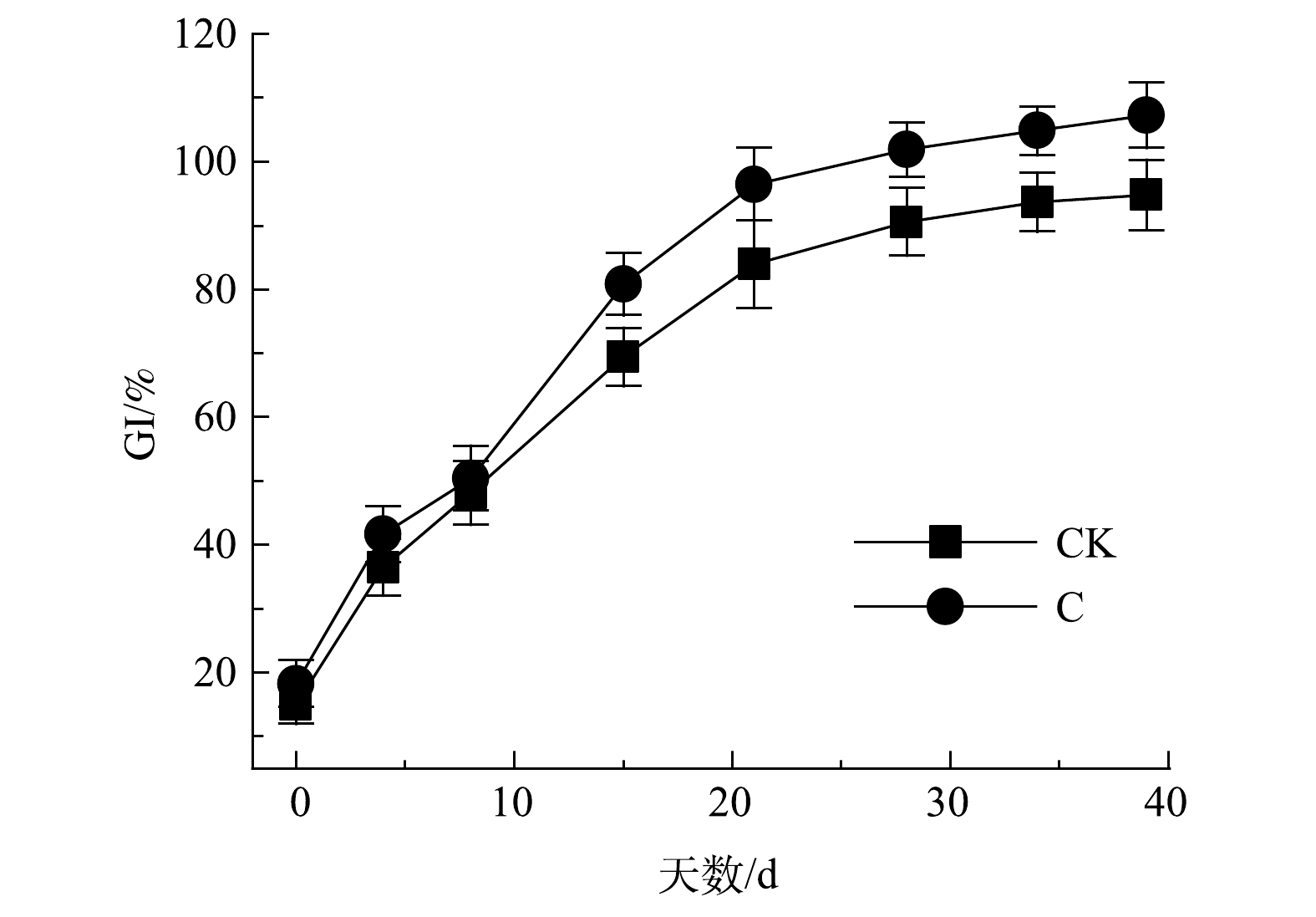
种子发芽指数(GI)测定:首先取10 g样品与蒸馏水按比例1∶10放入250 mL锥形瓶中,然后置于150 r·min−1摇床振荡30 min;再取其上清液过滤后吸取5 mL滤液于铺有滤纸的培养皿中,在其中放置20颗白菜种子,置于25 ℃下避光培养48 h后;最后,测定种子的根长,同时用去离子水做空白对照。
细菌群落结构通过宏全基因组法进行测定。残留土霉素采用高效液相色谱法测定(岛津LCM S8050,色谱柱为C18,1.9 μm×2.1 mm×50 mm;初始流动相为20%乙腈:80%甲酸水),土霉素降解率(D)如式(1)。
stringUtils.convertMath(!{formula.content}) (1) 式中:D为土霉素降解率;C0为第0 d堆肥中土霉素质量分数,mg·g−1;Cn为第n 天堆肥中土霉素质量分数,mg·g−1。
2. 结果与讨论
2.1 堆肥过程的理化性质
图1为堆肥过程中理化性质变化。含水率是堆肥过程中重要影响因素之一,其变化如图1(a)。C组和CK组的初始含水率分别为66.42%和64.05%。在堆肥初期,2组反应的含水率均小幅上升,然后开始下降。这可能是因为,微生物大量繁殖生长,产生了水分,后由于微生物分解有机质并散发较多热量,使堆体保持较长时间的高温,水分随热量挥发,故经翻堆后堆体含水率明显下降。堆肥结束后C组和CK组的含水率分别下降至41.08%和43.04%,由此表明,添加菌剂有利于堆体水分挥发。
由图1(b)可看出,2组堆体pH变化趋势相似。投加菌剂对堆体pH的影响不大,均出现先上升,再降低,翻堆后又升高的趋势。pH上升可能是由于堆肥前期大量排放的氨气的累积。随后氨气的产生速率小于其随曝气带出堆肥体系中的速率,pH开始下降[14]。堆肥第21 d后进入降温期,堆肥过程中的营养消耗减少,大量N元素以NH3的形式释放,并且在该阶段硝化细菌增多,其进行硝化反应产生大量H+,从而导致堆体的pH有轻微下降[15]。
堆体中铵态氮(NH4+-N)的转化过程如图1(c)所示。C组和CK组在堆肥第2 d后NH4+-N均呈上升状态,第21 d分别达到284.14和347.68 mg·kg−1。这可能是因为,堆体的C/N较低,物料中有机氮源被微生物矿化分解,使硝化反应在高温环境下受阻,导致NH4+-N大量积累[16-17]。此趋势与红霉素和青霉素菌渣堆肥研究中NH4+-N的转化过程相似[5,18]。NH4+-N的浓度达到峰值后开始下降,且C组下降速率大于CK组,最终C组NH4+-N质量浓度略低于CK组。这表明,添加菌剂有利于保留堆体中的氮源。
EC是反映堆肥中的可溶性盐含量的指标。一般情况下,堆体的EC>4 mS·cm−1,对植物种子发芽有强烈的抑制作用。因此,对堆肥过程中EC的变化过程进行了研究,结果如图1(d)所示。堆体的EC变化趋势为先上升后下降,可能是前期随着物料的消耗,释放出矿物盐和铵根离子而上升。高温期后,有机质降解速率下降,由于CO2和NH3的挥发,导致EC下降,这与以往的研究结果相似[19]。2组堆肥中的EC峰值达到3.0和2.85 mS·cm−1,均未超过其应用限值,故不会对植物种子发芽产生较强的抑制。C组初始EC值高于CK组,但最终EC值分别为2.57和2.21 ms·cm−1,低于CK组,处于安全水平。这表明,添加菌剂有利于降低堆肥中的可溶性盐的含量。
2.2 堆肥毒性
堆肥过程中种子发芽率指数(GI)可在一定程度上代表堆肥产品对植物毒性的强弱。其变化如图2所示,2组堆肥初期GI均低于20%。这表明,土霉素菌渣有较强的植物毒性,在农田应用中可能会存在较大的环境风险[20]。由于堆肥初期物料中的有机酸和铵根离子浓度较高,故导致了堆体初期的GI偏低。随着堆肥的进行,在微生物的作用下,物料GI逐渐升高,逐步实现脱毒。当GI>80%时,认定堆肥产品对植物基本无毒,2组堆肥产品均达到安全水平。添加菌剂使C组比CK组处理时间提前了7 d。这表明,复合菌剂在一定程度上加强了堆肥对植物毒性的削减。最终产品的GI分别为94.8%和107.3%。添加菌剂后,在提高微生物的种类和活性的作用下,缩减了堆肥周期,加快了堆肥物料的脱毒。马骏[21]研究表明,牛粪堆肥产品的GI高达124%,远高于本研究结果。由此可推测,土霉素残留不仅对GI有抑制作用,且质量浓度越高其抑制效应越强。
2.3 堆肥肥效
随着堆肥的进行,微生物的生长发育消耗了一定的碳源,导致有机质质量分数下降。堆肥结束后C组中有机物质的降解率为14.80%,而CK组仅为9.24%。因此,投加复合菌剂可增加堆体中微生物的数量和活性,加快了对碳源的消耗,提高了堆肥过程的最高温度,可间接增强对有机质的降解。
对堆肥成品进行检测,检测指标参照《有机肥料标准》(NY/T525-2021)[22]中对肥料的要求,将检测结果同标准中要求值进行对比,其结果见表2。堆肥成品指标除水分的质量分数偏高外,其余指标均满足《有机肥料标准》(NY/T 525-2021)[22]中标准,在后续晾干过程中可降低其水分的质量分数。本研究结果可为抗生素菌渣及其衍生物的工程化好氧堆肥资源化利用提供数据支持和技术参考。
表 2 堆肥成品指标Table 2. Composting product index对照指标 本实验检测值 NY/T 525-2021指标值[22] 有机质的质量分数(以烘干基计) 57.3%~58.1% ≥30% 总养分(N+P2O5+K2O)的质量分数(以烘干基计) 5.7%~6.7% ≥4.0% 水分(鲜样)的质量分数 41.08%~43.04% ≤30% 种子发芽率指数(GI) 99.8%~107.3% ≥70% 机械杂质的质量分数 <0.3% ≤0.5% 2.4 菌剂对堆肥中土霉素降解及微生物群落结构变化影响
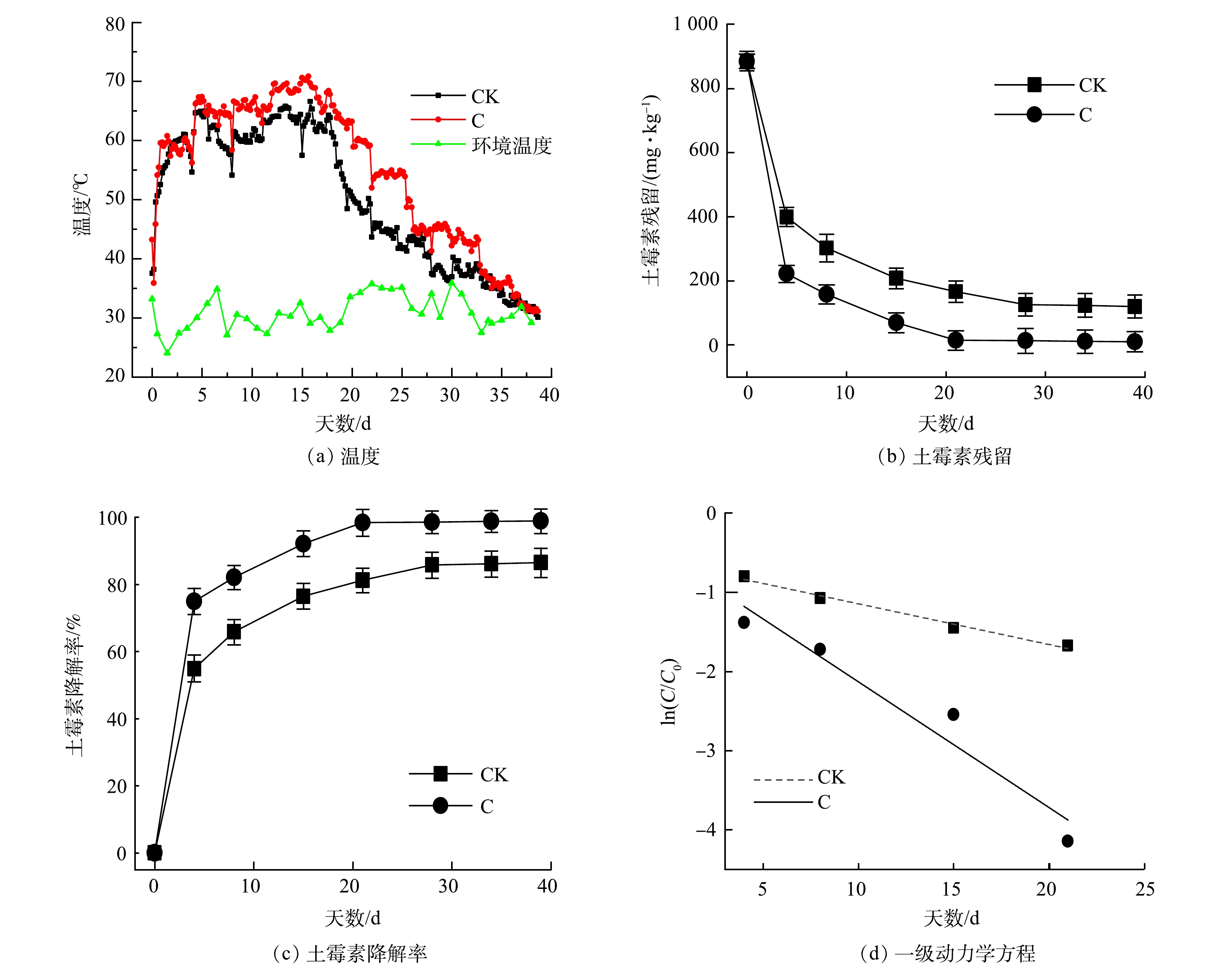
1)菌剂对堆肥中土霉素降解影响。堆体温度是堆肥过程中最重要的参数之一,与有机物降解程度和堆肥产物的腐熟程度密切相关。堆肥温度变化和土霉素降解变化间的关系如图3所示。堆肥期间,温度变化经历了升温期、高温期和降温腐熟期3个阶段。在堆肥第2天,2组温度分别达到54.56和52.66 ℃。其中,C组比CK组提前1 d达到最高温度,最高温度分别为70.55和66.57 ℃,且高温期延长了5 d。这可能是因为,堆肥初期CK组含有的土著微生物较少,微生物活性较差,难以迅速降解堆体中的有机物。堆肥38 d时,堆体温度与环境温度接近,堆肥发酵结束,有机质降解完全,实现了土霉素菌渣的无害化和资源化。马骏[21]研究发现,菌剂能提高堆肥温度,使最高温度达到80 ℃以上,高于本次堆肥温度。这可能是因为,制药菌渣中高浓度的重金属对高温期优势微生物菌群的抑制作用。ZHANG等[23]在泰乐菌素菌渣与污泥堆肥的研究中也表明,高浓度Cu能致使高温期温度不高,与本研究结果一致。
由图3(b)可知,土霉素降解趋势为先迅速下降,最后趋于稳定。CK组在堆肥21 d降解率为81.23%。这表明,堆肥处理可以降低土霉素残留。堆肥结束时,CK组土霉素质量分数为119.67 mg·kg−1,降解率达86.47%;C组土霉素质量分数为10 mg·kg−1,降解率高达98.87%(图3(c))。C组优于CK组,这与REN等[24]、ZHU等[25]、EZZARIAI等[26]、SARDAR等[27]和SARDAR等[28]的研究结果结果相似。土霉素降解主要发生在升温期及高温期。这一方面可能是,升温中键能较弱的四环素类分子中的C—N易断裂,导致羧基及哌嗪环断裂并脱去;另一方面可能是,温度升高增强了嗜温菌和嗜热菌的生物活性,进而提高了土霉素的降解。因此,高温是抗生素降解的重要影响因素,有利于将抗生素菌渣无害化和资源化[29]。
图3(d)是对2组降解曲线的一级动力学模拟图,CK组和C组R2分别为0.986和0.941。表3列出了堆肥过程中几种抗生素的半衰期,C组和CK组的半衰期分别为13.59和4.38。对比发现,CK组的半衰期最大。这表明,土霉素为难降解抗生素[30-31]。但是,C组的半衰期小于CK组。这说明,复合菌剂的添加有利于土霉素的降解。
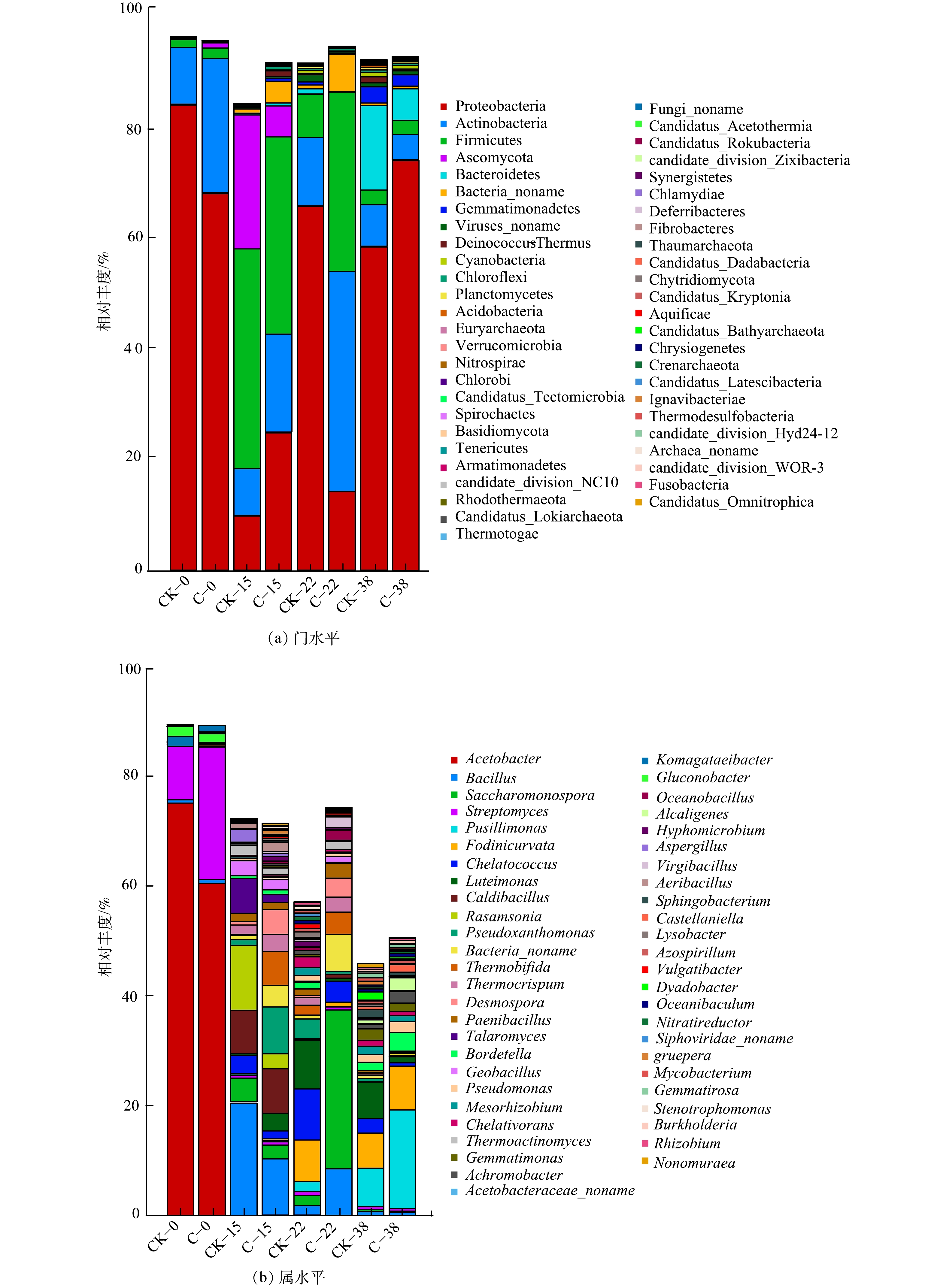
表 3 土霉素降解的线性拟合方程、半衰期和R2Table 3. Linear fitting equation for oxytetracycline degradation, half-life, and R2组别 方程 斜率 R2 半衰期 数据来源 CK ln(C/C0)=−0.051x−0.632 −0.051 0.986 13.59 本研究 C ln(C/C0)=−0.158x−0.544 −0.158 0.941 4.38 本研究 红霉素 ln(C/C0)=−0.500x−0.604 −0.500 0.801 1.40 [26] 多环西素 ln(C/C0)=−0.183x−0.638 −0.183 0.765 3.80 [26] 诺氟沙星 ln(C/C0)=−0.328x−0.689 −0.328 0.894 2.10 [26] 青霉素 ln(C/C0)=−0.798x−0.697 −0.798 0.962 1.72 [30] 庆大霉素 ln(C/C0)=−0.116x−0.087 −0.116 0.985 6.70 [31] 2)菌剂对堆肥中微生物群落结构影响。2组堆肥处理中细菌群落组成在门水平和属水平的相对丰度见图4。C组堆肥样品细菌、真菌和病毒所占的比例分别为94.86%、0.21%和0.97%。细菌主要由放线菌门Actinobacteria、变形菌门Proteobacteria、厚壁菌门Firmicutes和拟杆菌门Bacteroidetes组成。细菌群落在高温期变化较大,而土霉素降解也主要发生在高温期。这表明,土霉素降解可能与其微生物群落变化有密切关系。在堆肥初期,C组中Firmicutes增加到40.03%,Proteobacteria从68.45%降低到9.55%。此时优势菌群为Firmicutes和Actinobacteria,其耐受力强,释放热量促使堆体升温。在升温期,C组中Firmicutes和Bacteroidetes相对丰度分别增加了10.1%和2.5%,Actinobacteria减少了15%。在高温期后,Firmicutes和Bacteroidetes相对丰度分别增加了12.27%和5.7%。堆肥结束时,细菌中Actinobacteria数量下降到4.49%,真菌数量下降到0.16%,病毒降低到0.72%。这说明,土霉素菌渣对细菌、放线菌和真菌生长均有不同程度的抑制。此外,在堆肥过程中,子囊菌门Ascomycota只出现在高温期,随堆肥的进行其相对丰度降低,Ascomycota可能为致病菌,故堆肥有利于致病菌的去除。此结果与PENG等[32]的研究结果相似。
从属水平上分析细菌相对丰度,堆肥升温期,以Acetobacter为代表的1类好氧或兼性厌氧的杆状菌群能够分解堆料,提高堆体温度。在堆肥第22 d,堆体中优势菌群以Saccharomonospora和Bacillus为代表,Saccharomonospora具有较强的蛋白酶、淀粉酶和脂肪酶活性,有较强的有机质分解能力;Bacillus为木质纤维素降解菌。因此,C组堆肥产物中纤维素和半纤维素含量的下降可能与Bacillus菌群数量的增加有关。堆肥高温期,C组的优势菌属无论在功能还是数量上都比CK组能更好的加速堆肥进程。而且,CK组中反硝化细菌存在较多,降低了堆体中氮的含量,导致氮元素缺少,不利于菌渣堆肥产品向有机肥方向发展。在堆肥第38 d,由于复合菌剂中存在Geobacillusthermodenitrificans,因此堆体中优势菌群以Geobacillus为代表,其可分解菌渣中的蛋白质,进而提高抗生素降解率。
3)环境因子和细菌群落之间的相关性分析。环境因素(pH、残留土霉素、温度、C/N)与细菌群落(基于门的丰度)的RDA分析结果如图5所示。RDA1和RDA2分别解释了细菌群落和环境因子总变异的72.85%和42.09%。这表明,残留土霉素的变化主要受细菌群落变化的影响。随着堆肥的进行,Firmicutes减少,而其他菌群在升温期和高温期增加,促进了土霉素的降解。这表明,Firmicutes和Actinobacteria是降解土霉素的优势菌群。在堆肥初期,残留土霉素和C/N是影响堆肥进程的主要因素。然而,在高温和降温阶段,pH和温度成为影响堆肥效果的主要因素。且RAMASWAMY等[33]和BAO等[34]的研究也表明,pH、温度以及微生物的活性在降解抗生素过程中起重要作用。因此,在堆肥过程中,土霉素残留的变化和温度、微生物群落的变化有着密不可分的关系。堆肥结束时,C组土霉素质量浓度小于CK组。这表明,添加菌剂可提高微生物种类和活性以及堆体温度,促进了土霉素的降解。
综上所述,细菌群落的演替和环境因素的变化都会影响土霉素的降解。因温度变化而引起的不同细菌丰度在不同堆肥阶段的差异,可能是残留抗生素随堆肥过程变化的内在机制。接种菌剂既改变了堆肥土著细菌群落的互作模式,降低了细菌群落的复杂度,又为优化建立新的和更健康的堆肥细菌群落奠定了基础。
3. 结论
1) C组的NH4+-N浓度比CK组提前7 d降至腐熟堆肥的安全浓度范围内。堆肥后的成品基本可以满足《有机肥料标准》(NY/T525-2021),复合菌剂在促进堆肥腐熟和氮磷保留中具有良好的效果。
2)复合菌剂增加了堆体中微生物活性,延长了高温期5 d;C组的土霉素降解率高达98.41%,比CK组高12.39 %。这表明,菌剂堆肥化处理在提高堆体温度的同时提高了土霉素降解率。
3)在堆肥中,优势门为Firmicutes和Actinobacteria,土霉素残留的变化与其密切相关。因温度变化而造成的不同细菌丰度在不同堆肥阶段的差异可能是引起残留抗生素随堆肥过程变化的原因。
-
表 1 合成废水水质参数
Table 1. Water quality parameters of the synthetic wastewater
运行阶段 COD/(mg·L−1) NH4+-N/(mg·L−1) DO/(mg·L−1) pH S1 220~380 13~35 7.50~7.84 7.06~7.47 S2 260~390 34~46 7.25~7.68 7.08~7.44 S3 470~630 39~47 7.17~7.30 7.10~7.33 S4 613~690 36~48 7.36~7.62 7.01~7.06 表 2 4阶段各出水口出水DO质量浓度
Table 2. DO concentration of each outlet at four stages mg·L−1
运行阶段 出水口1# 出水口2# 出水口3# 出水口4# S1 3.49~4.04 5.91~6.27 6.50~6.89 7.20~7.31 S2 3.50~3.95 5.83~6.21 6.66~6.78 7.21~7.28 S3 3.36~3.61 5.81~6.00 6.47~6.77 7.19~7.30 S4 1.67~2.93 3.60~4.34 3.79~5.59 5.51~5.75 表 3 4阶段耗氧有机物(以COD计)和NH4+-N指数拟合的相关参数
Table 3. Relevant parameters for the index fitting of oxygen consuming organic matter (COD) and ammonia nitrogen at four stages
水质指标 实验编号 ρ*/(mg·L−1) 去除率/% A m COD FT1~FT7 308.34±68.34 93.62±1.57 0.997~0.998 2.691±0.228 ST1~ST7 325.00±58.33 94.08±1.58 0.997~0.999 3.171±0.233 TT1~TT7 511.67±25.00 98.69±0.69 0.999~1.001 3.873±0.322 HT1~HT7 663.34±26.67 96.50±1.05 0.996~0.999 2.425±0.146 NH4+-N FT1~FT7 27.92±6.44 98.95±0.46 1.003~1.019 1.780±0.264 ST1~ST7 38.60±2.03 97.97±1.07 1.013~1.026 1.803±0.087 TT1~TT7 43.90±3.08 97.52±0.51 1.006~1.017 1.848±0.136 HT1~HT7 44.11±3.85 87.94±2.93 1.023~1.084 0.907±0.140 表 4 4阶段耗氧有机物(以COD计)和NH4+-N的kA和kV值
Table 4. The kA and kV values of oxygen consuming organic matter (COD) and ammonia nitrogen at four stages
指标 实验编号 m kV/d−1 kA/(m·d−1) COD FT1~FT7 2.691±0.228 0.621±0.053 0.280±0.024 ST1~ST7 3.171±0.233 0.731±0.054 0.329±0.024 TT1~TT7 3.873±0.322 0.893±0.075 0.402±0.034 HT1~HT7 2.425±0.146 1.677±0.101 0.755±0.045 NH4+-N FT1~FT7 1.780±0.264 0.405±0.055 0.185±0.028 ST1~ST7 1.803±0.087 0.416±0.020 0.187±0.009 TT1~TT7 1.848±0.136 0.426±0.031 0.192±0.014 HT1~HT7 0.907±0.140 0.627±0.097 0.283±0.043 表 5 已报道的一些HSSFCWs的kA和kV值
Table 5. The reported kA and kV values of some HSSFCWs
指标 q/(m·d−1) kV/d−1 kA/(m·d−1) 文献 NH4+-N 0.047 — 0.027 [3] COD 0.042 — 0.113~0.135 [17] BOD 0.002~0.300 0.170~6.110 0.060~1.000 [28] BOD — — 0.080~0.310 [29] COD 0.08 — 0.136 [30] COD 0.055~0.440 — 0.283、0.271 [31] BOD — — 0.018~0.092 [32] NH4+-N — — 0.013~0.086 [32] COD 0.031~0.146 — 0.060~0.082 [33] -
[1] ZHONG L, DING J, WU T, et al. Bibliometric overview of research progress, challenges, and prospects of rural domestic sewage: Treatment techniques, resource recovery, and ecological risk[J]. Journal of Water Process Engineering, 2023, 51: 103389. doi: 10.1016/j.jwpe.2022.103389 [2] ROUSSEAU D P L, VANROLLEGHEM P A, PAUW N D. Constructed wetlands in Flanders: A performance analysis[J]. Ecological Engineering, 2004, 23(3): 151-163. doi: 10.1016/j.ecoleng.2004.08.001 [3] KNIGHT R L, JR V W E P, BORER R E, et al. Constructed wetlands for livestock wastewater management[J]. Ecological Engineering, 2000, 15(1/2): 41-55. [4] PENG X X, YANG W, JIN Q, et al. Biofilter-constructed wetland-trophic pond system: A new strategy for effective sewage treatment and agricultural irrigation in rural area[J]. Journal of Environmental Management, 2023, 332: 117436. doi: 10.1016/j.jenvman.2023.117436 [5] WU H, ZHANG J, NGO H H, et al. A review on the sustainability of constructed wetlands for wastewater treatment: Design and operation[J]. Bioresource Technology, 2015, 175: 594-601. doi: 10.1016/j.biortech.2014.10.068 [6] YANG L, KONG F L, XI M, et al. Environmental economic value calculation and sustainability assessment for constructed rapid infiltration system based on emergy analysis[J]. Journal of Cleaner Production, 2017, 167: 582-588. doi: 10.1016/j.jclepro.2017.08.172 [7] WANG M C, ZHANG H Z. Chemical oxygen demand and ammonia nitrogen removal in a non-saturated layer of a strengthened constructed rapid infiltration system[J]. Water, Air, & Soil Pollution, 2017, 228(11): 440. [8] LI X Y, DING A Z, ZHENG L, et al. Relationship between design parameters and removal efficiency for constructed wetlands in China[J]. Ecological Engineering, 2018, 123: 135-140. doi: 10.1016/j.ecoleng.2018.08.005 [9] VYMAZAL J. Removal of nutrients in various types of constructed wetlands[J]. Science of the Total Environment, 2007, 380(1/2/3): 48-65. [10] ANDREO-MARTÍNEZ P, GARCÍA-MARTÍNEZ N, QUESADA-MEDINA J, et al. Domestic wastewaters reuse reclaimed by an improved horizontal subsurface-flow constructed wetland: A case study in the southeast of Spain[J]. Bioresource Technology, 2017, 233: 236-246. doi: 10.1016/j.biortech.2017.02.123 [11] 庞俊玲. 多级土壤渗滤系统处理模拟生活污水研究[D]. 沈阳: 沈阳师范大学, 2022. [12] 姚琪. CRI系统COD降解试验及滤池有效高度模型构建[D]. 成都: 西南交通大学, 2012. [13] AKRATOS C S, TSIHRINTZIS V A. Effect of temperature, HRT, vegetation and porous media on removal efficiency of pilot-scale horizontal subsurface flow constructed wetlands[J]. Ecological Engineering, 2007, 29(2): 173-191. doi: 10.1016/j.ecoleng.2006.06.013 [14] 刘家宝. 人工快速渗滤系统污染物去除机理及其处理效果研究[D]. 北京: 中国地质大学, 2006. [15] ÇAKIR R, GIDIRISLIOGLU A, ÇEBI U. A study on the effects of different hydraulic loading rates (HLR) on pollutant removal efficiency of subsurface horizontal-flow constructed wetlands used for treatment of domestic wastewaters[J]. Journal of Environmental Management, 2015, 164: 121-128. [16] LI J Y, WANG J J, ZHANG Q, et al. Efficient carbon removal and excellent anti-clogging performance have been achieved in multilayer quartz sand horizontal subsurface flow constructed wetland for domestic sewage treatment[J]. Journal of Environmental Management, 2023, 335: 117516. doi: 10.1016/j.jenvman.2023.117516 [17] VYMAZAL J. Is removal of organics and suspended solids in horizontal sub-surface flow constructed wetlands sustainable for twenty and more years?[J]. Chemical Engineering Journal, 2019, 378: 122117. doi: 10.1016/j.cej.2019.122117 [18] 何江涛, 段光杰, 张金炳, 等. 污水渗滤土地处理系统中水力停留时间与出水效果的讨论[J]. 地球科学, 2002(2): 203-208. doi: 10.3321/j.issn:1000-2383.2002.02.016 [19] ZHANG Z, CHEN Y Z, CHEN H H, et al. Novel efficient capture of Cr(VI) from soil driven by capillarity and evaporation coupling[J]. Chemosphere, 2022, 288: 132593. doi: 10.1016/j.chemosphere.2021.132593 [20] XU W L, ZHANG J Q, LIU Y. NH3-N degradation dynamics and calculating model of filtration bed height in Constructed Soil Rapid Infiltration[J]. Chinese Geographical Science, 2011, 21(6): 637-645. doi: 10.1007/s11769-011-0476-y [21] 肖璐. 水平潜流人工湿地净化府河水的试验研究[D]. 保定: 河北农业大学, 2019. [22] 曹帆. 人工快渗生物滤池中污染物归趋机制及滤料界面反应动力学研究[D]. 合肥: 合肥工业大学, 2010. [23] 石国玉. 人工快渗系统处理工业园区污水厂尾水研究[D]. 合肥: 合肥工业大学, 2011. [24] 陈佼. 人工快渗系统PN-ANAMMOX耦合脱氮性能及机理研究[D]. 成都: 西南交通大学, 2018. [25] 许文来. 人工快速渗滤系统污染物去除机理及动力学研究[D]. 成都: 西南交通大学, 2011. [26] 陈佼, 李晓媛, 刘欢, 等. 生物炭对人工快渗系统氨氮去除的影响研究[J]. 成都工业学院学报, 2022, 25(3): 35-41. [27] 史云鹏, 周琪. 人工湿地污染物去除动力学模型研究进展[J]. 工业用水与废水, 2002(6): 12-15. doi: 10.3969/j.issn.1009-2455.2002.06.004 [28] ROUSSEAU D P L, VANROLLEGHEM P A, PAUW N D. Model-based design of horizontal subsurface flow constructed treatment wetlands: a review[J]. Water Research, 2004, 38(6): 1484-1493. doi: 10.1016/j.watres.2003.12.013 [29] AGUADO R, PARRA O, GARCÍA L, et al. Modelling and simulation of subsurface horizontal flow constructed wetlands[J]. Journal of Water Process Engineering, 2022, 47: 102676. doi: 10.1016/j.jwpe.2022.102676 [30] KANTAWANICHKUL S, KLADPRASERT S, BRIX H. Treatment of high-strength wastewater in tropical vertical flow constructed wetlands planted with Typha angustifolia and Cyperus involucratus[J]. Ecological Engineering, 2009, 35(2): 238-247. doi: 10.1016/j.ecoleng.2008.06.002 [31] KONNERUP D, KOOTTATEP T, BRIX H. Treatment of domestic wastewater in tropical, subsurface flow constructed wetlands planted with Canna and Heliconia[J]. Ecological Engineering, 2009, 35(2): 248-257. doi: 10.1016/j.ecoleng.2008.04.018 [32] ÖÖVEL M, TOOMING A, MAURING T, et al. Schoolhouse wastewater purification in a LWA-filled hybrid constructed wetland in Estonia[J]. Ecological Engineering, 2007, 29(1): 17-26. doi: 10.1016/j.ecoleng.2006.07.010 [33] TRANG N T D, KONNERUP D, SCHIERUP H H, et al. Kinetics of pollutant removal from domestic wastewater in a tropical horizontal subsurface flow constructed wetland system: Effects of hydraulic loading rate[J]. Ecological Engineering, 2010, 36(4): 527-535. doi: 10.1016/j.ecoleng.2009.11.022 [34] 侯云霞. 人工快速渗滤系统有机物质量浓度随机模型研究[D]. 成都: 西南交通大学, 2014. [35] YAN G, XU X, YAO L R, et al. Process of inorganic nitrogen transformation and design of kinetics model in the biological aerated filter reactor[J]. Bioresource Technology, 2011, 102(7): 4628-4632. doi: 10.1016/j.biortech.2011.01.009 [36] 王春荣, 李军, 王宝贞, 等. 2种不同填料曝气生物滤池处理生活污水的经验模型[J]. 环境污染治理技术与设备, 2005(12): 56-60. [37] FERREIRA A G, BORGES A C, ROSA A P. Comparison of first-order kinetic models for sewage treatment in horizontal subsurface-flow constructed wetlands[J]. Environmental Technology, 2020(12): 1-17. -





 DownLoad:
DownLoad: