-
饮用水安全关系着人们的身体健康,生命安全。随着社会发展、科技进步,以地表水为代表的各类水源中发现了多种的新型污染物,如内分泌干扰物、药品、甜味剂、个人护理产品等[1-2]。这些新型污染物的存在不仅会对人体产生危害并且降低消费者对饮用水的信心。由于常规给水处理工艺(混凝、沉淀、过滤和消毒)的主要功能是去除细菌和降低浊度等,对有机物尤其是溶解性有机物(dissolved organic carbon, DOC)的去除能力很低,而深度处理,例如活性炭吸附、高级氧化等可以实现更好的去除效果[3-4]。综合国内外研究,在新型污染物暴露的情况下,具备深度处理工艺的水厂比常规工艺的水厂的抗风险能力更强,受新型污染物威胁的风险更小[5]。因此,饮用水深度处理工艺已经成为给水工艺中不可或缺的一环,尤其是集吸附与生物降解于一体的生物活性炭(biological activated carbon, BAC)工艺,无论是对传统水处理指标还是对新型污染物去除均有较好的效果[6-7];由于BAC工艺具有应用范围广、水源水质针对性强、水质保障能力强、出水稳定性高、技术成熟等优点,已经成为我国给水深度处理的主推广技术[8]。截至2020年底,全国已有近130余座水厂采用BAC工艺进行深度处理,处理能力已达3 580万m3·d−1,占日供水能力的35%以上[9],如苏州市的供水水厂已经全面实现了BAC深度工艺,出厂水水质达到了高品质饮用水的标准[10],这表明BAC工艺在我国给水工艺中的优势地位与普适性。
然而由于资源的有限性、可持续发展的紧迫性,作为BAC工艺中关键净水材料的活性炭,其应用效率有待进一步研究[11-15]。基于此,本研究以新疆煤基压块活性炭为例,探究2种不同指标活性炭的小试BAC工艺应用效果,以期为BAC工艺中活性炭的靶向选择提供借鉴和指导。
-
实验所用2种不同指标新疆煤基压块活性炭,LBC(碘吸附值为968 mg·g−1,亚甲基蓝吸附值为199 mg·g−1)和HBC(碘吸附值为1 162 mg·g−1,亚甲基蓝吸附值为220 mg·g−1)均由国家能源集团新疆能源公司提供,其孔隙结构表征数据如表1所示。
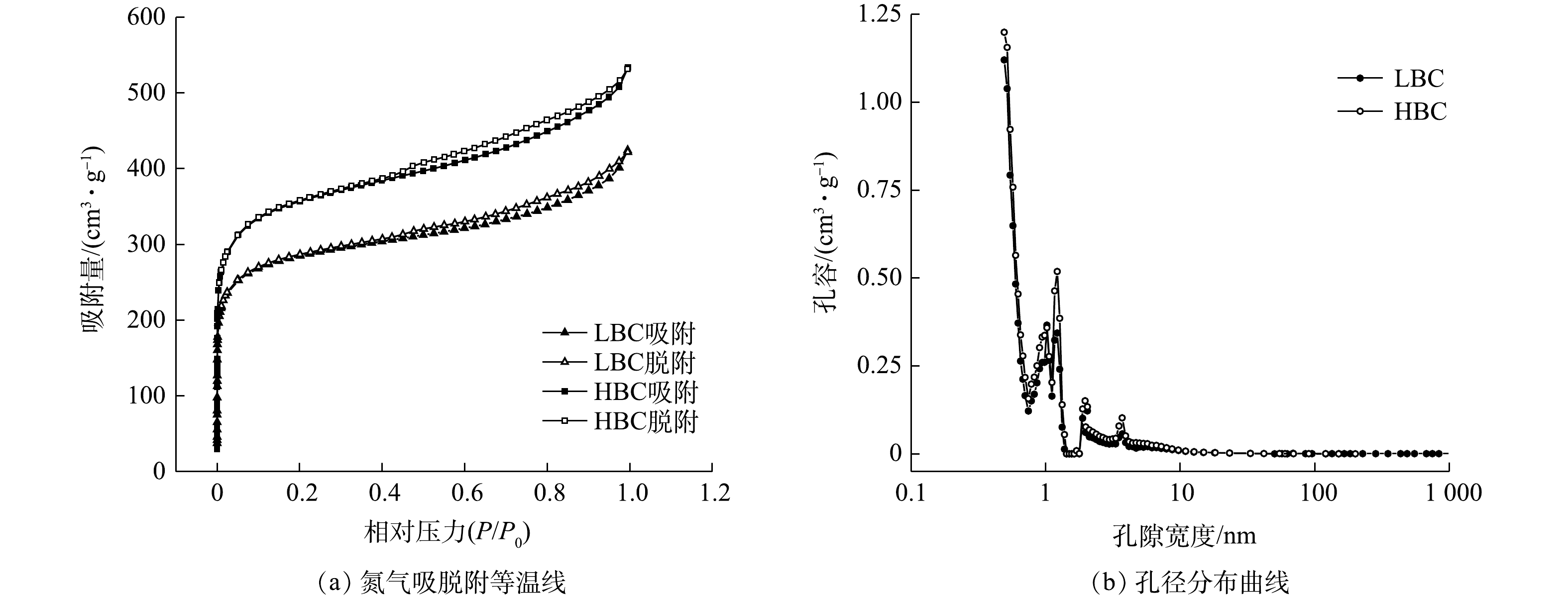
LBC与HBC的氮气吸脱附等温线和孔径分布曲线如图1所示。如图1(a)所示,在相对压力<0.4时,吸附等温线展现出狭窄的通道,属于Ⅰ型等温线,LBC和HBC含有微孔结构。随着相对压力的增大,LBC与HBC出现吸附滞后环,LBC和HBC含有中孔结构[16]。由图1(b)可知,LBC与HBC孔径主要分布在0.3~10.0 nm。
-
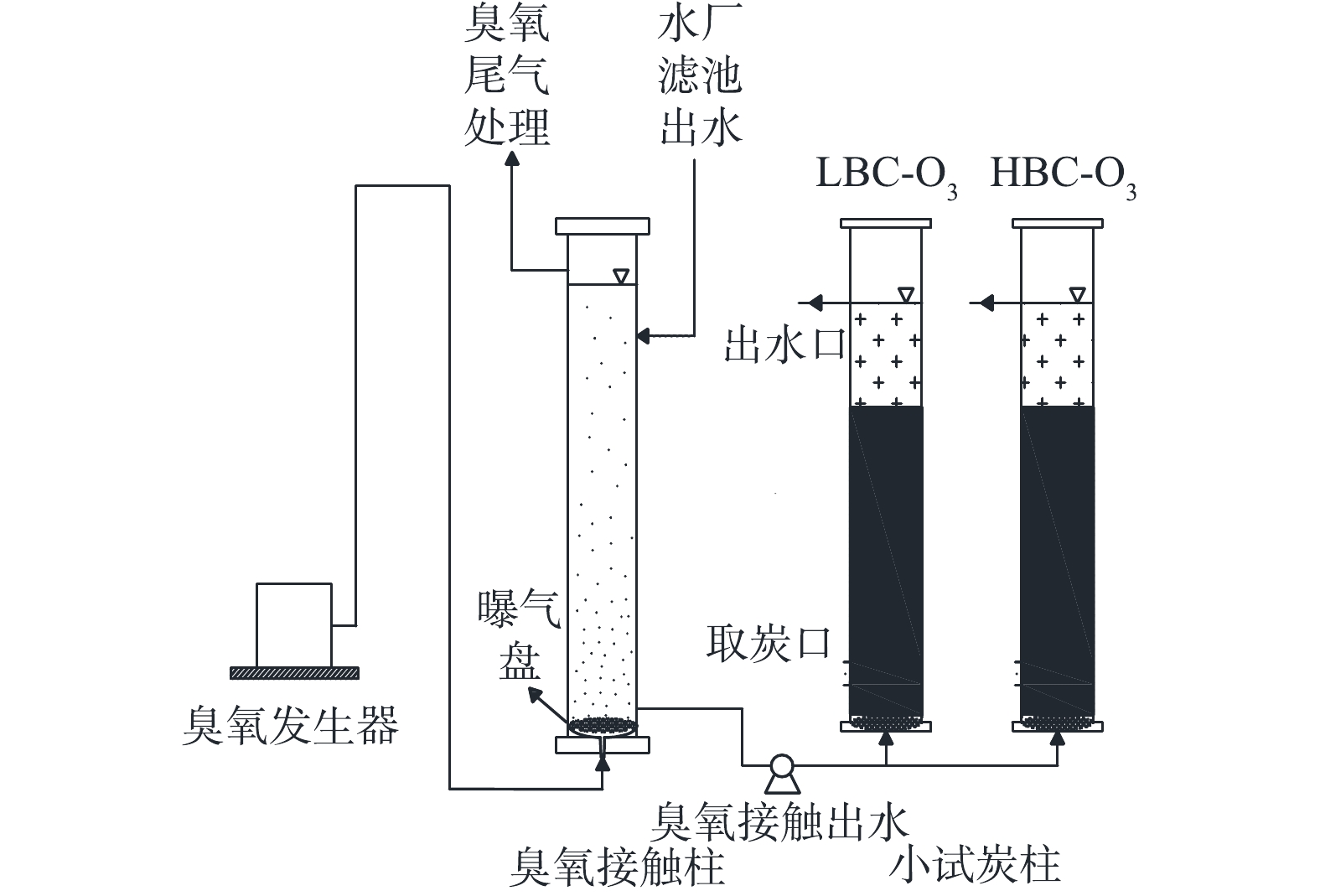
1)小试BAC工艺装置。如图2所示,上向流小试装置由1根120 L的臭氧接触柱和2根内径为6 cm的活性炭柱(LBC-O3和HBC-O3)组成。炭柱内分别装填LBC和HBC,炭层高为1 m,出水口设在顶部,取炭口设在距底部10 cm处[17-18]。运行参数如下:炭柱进水为上向流,滤速为2 m·h−1,空床接触时间(EBCT)为30 min,流量为0.09 L·min−1,臭氧投加量为2 mg·L−1,每天运行8 h,单根炭柱处理水量为43.2 L·d−1。
该小试BAC工艺从2019年9月开始运行,直至2020年12月结束。运行期间,由于2020年2月开始的疫情导致实验暂停运行约4个月,疫情结束后,对炭柱进行反冲洗后重新运行,共运行约300 d。为考察不同指标压块活性炭在BAC工艺中的作用,以每周1次的取样频次,对小试BAC工艺进出水的常规水质指标,如溶解氧(dissolved oxygen, DO)、浊度、pH、UV254、高锰酸钾指数(CODMn)等进行了检测;以每月1次的取样频次,对活性炭上负载的微生物-细菌总数进行了检测。通过比较臭氧接触前后的水质状况,分析臭氧对原水产生的影响;通过对LBC-O3和HBC-O3出水水质及炭上细菌总数进行分析,评估不同指标压块活性炭对小试BAC工艺运行情况的影响,以期为水厂处理不同水质时的用炭选择提供指导。
2)水质指标分析测试方法。分别使用便捷式溶解氧仪(Hach HQ30D)、便捷式浊度计(Hach2011)、便捷式酸度计(HACH PHC101)测定水的DO、浊度和pH。水样经0.45微米滤膜过滤后,以纯水(Elix Advantage 10, Millipore)作参比,采用紫外可见分光光度计(TU-1810,北京普析通用)测试水样于254 nm处的吸光度(UV254)。根据高锰酸盐指数法(GB 11892-89)[19]测定CODMn。将活性炭放于振荡器内振荡以分离炭上吸附的细菌[17],按照生活饮用水标准检验方法微生物指标(GB/T 5750.12-2006)[20]规定的方法测定活性炭上细菌总数。
-
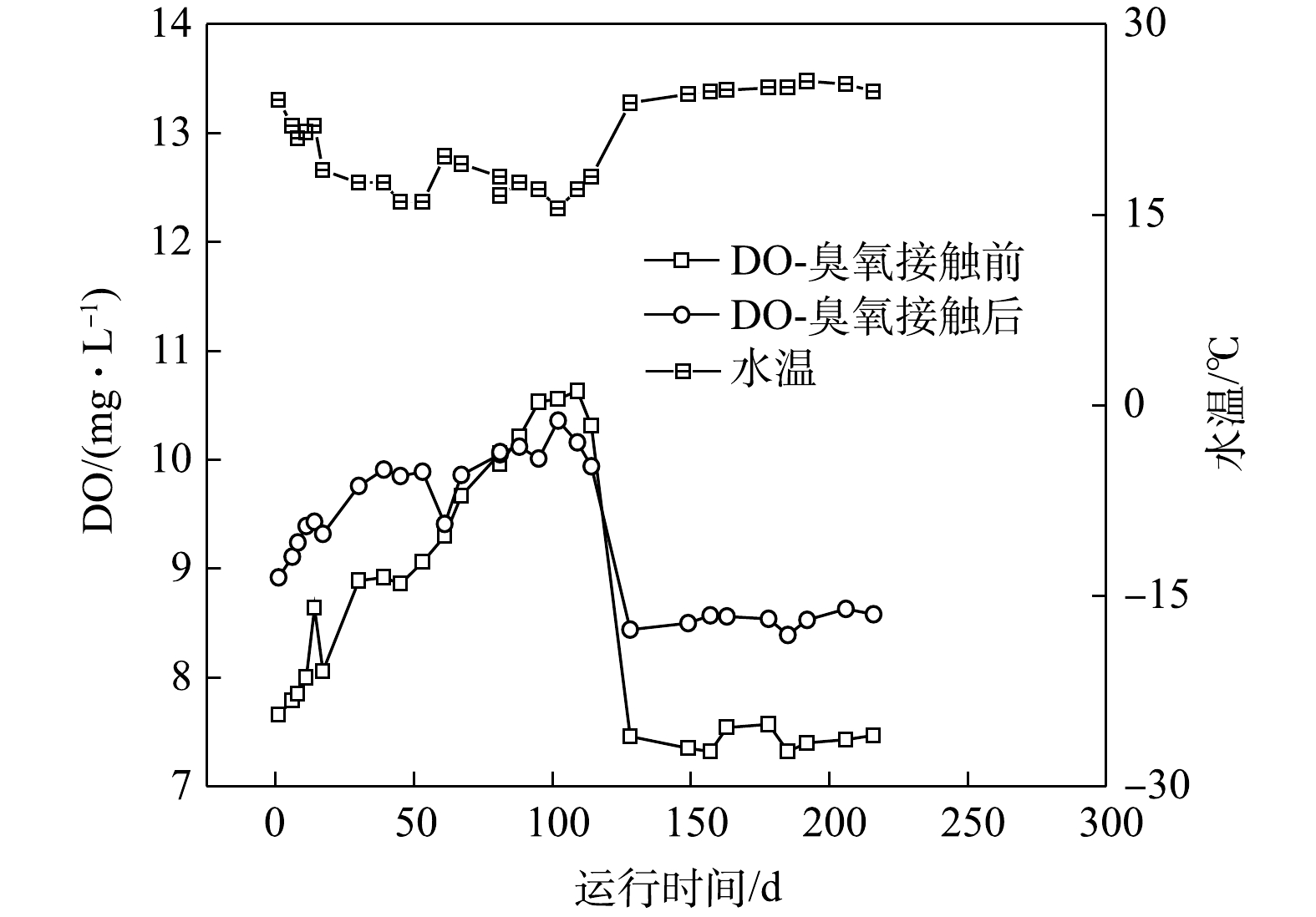
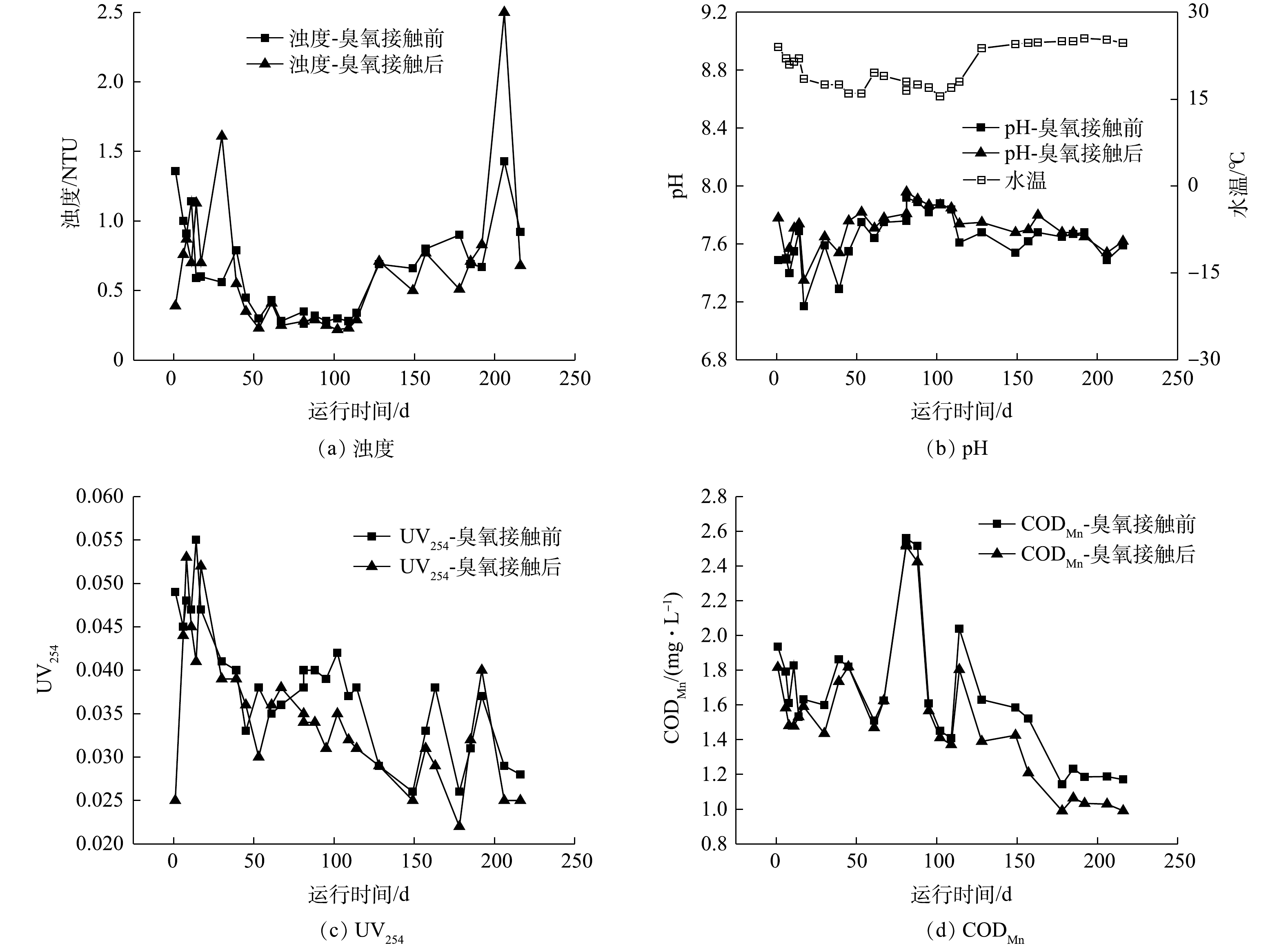
1)臭氧接触前后的水质比较。为观察臭氧氧化前后的水质变化情况,对臭氧接触前后水质进行检测,其中臭氧接触前后水中DO变化情况如图3所示,浊度、pH、UV254、CODMn变化情况如图4所示。由图3可知,臭氧接触后出水中DO在8.5~10.5 mg·L−1,与臭氧接触前相比,其提升了大约10%~20%。在水温较高的阶段(20~26 ℃),臭氧接触前后的DO增加值基本维持在1.0 mg·L−1左右,这表明臭氧氧化可使DO值升高。在水温较低的阶段(14~20 ℃),即运行至50~125 d,此时所体现的臭氧接触导致DO升高的作用并不明显甚至相反。这是由于室外温度过低,输水压强作用导致臭氧接触前的原水已经达到DO过饱和状态,相同的现象在水厂中也会出现。
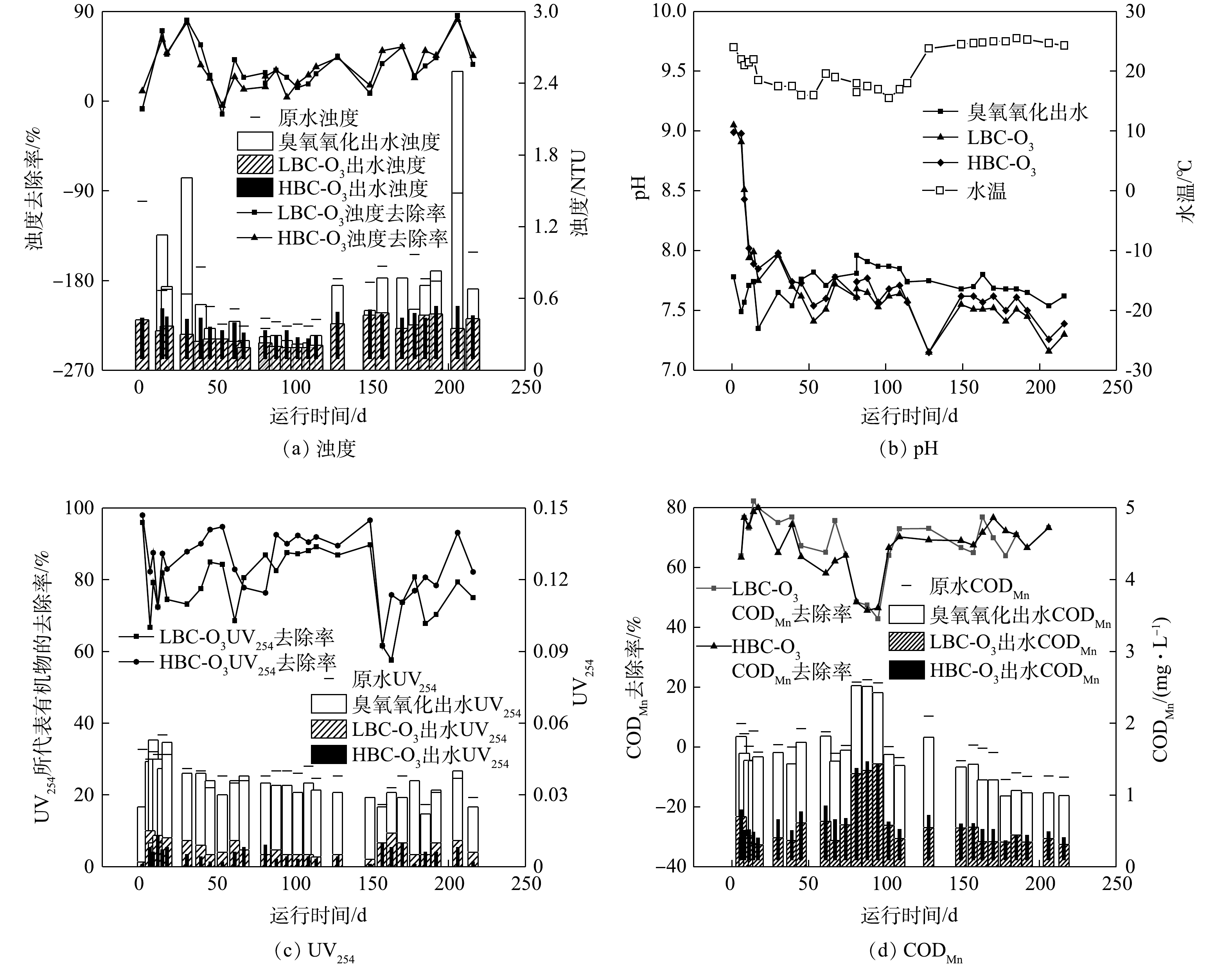
由图4(a)可知,原水浊度保持在0.25~1.50 NTU,除局部几个测试点出现升高外,臭氧接触出水的浊度出现了微弱的降低。其原因可能是臭氧接触作用于一部分浊度,使其分解或转化;而局部几点升高的现象可能是当天原水中存在氧化后能增加浊度的物质所致。
如图4(b)所示,臭氧接触后的pH升高。这是接触过程中水温的变化以及复杂的臭氧反应过程导致的,基于臭氧的NFG模型分解机理可知[21],其分解过程中有OH−产生,导致pH升高。如图4(c)所示,与臭氧接触前相比,臭氧接触后出水的UV254总体上存在一定程度的降低,其原因是UV254代表的较大分子质量有机物被臭氧氧化分解成更小分子质量的有机物。由图4(d)可知,在小试BAC工艺运行期间原水的CODMn稳定在1.1~2.6 mg·L−1,经过臭氧接触后,CODMn降低。这是因为臭氧氧化了原水中部分可以被高锰酸钾氧化的物质。
综上所述,臭氧接触后原水DO出现10%~20%的升高(冬季低温水除外),浊度轻微降低,pH升高,UV254和CODMn降低,即臭氧能够氧化分解部分有机物,并在一定程度上使出水的DO升高。
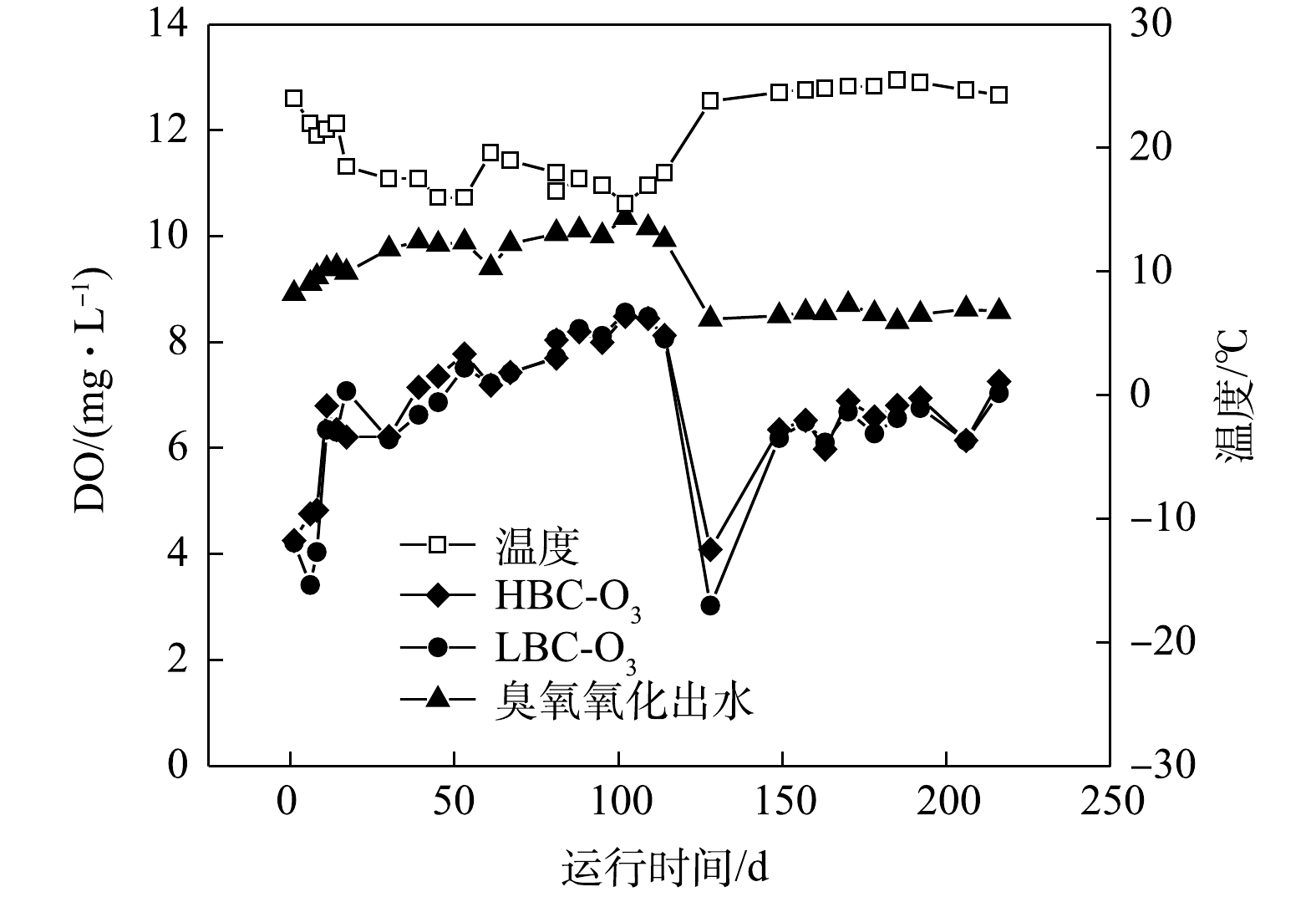
2) LBC-O3与HBC-O3体系的出水水质比较。小试BAC工艺LBC-O3和HBC-O3进、出水的DO如图5所示,出水浊度、pH变化如图6(a)和图6(b)所示,出水UV254、CODMn及其所代表有机物的去除率分别如图6(c)和图6(d)所示。
由图5可知,运行前期(约0~14 d),炭柱出水DO在3.0~5.0 mg·L−1,随后维持在6.0 mg·L−1以上,与进水DO的差值维持在2.0~4.0 mg·L−1,即运行初期DO的消耗量最大。在疫情后的运行前期(约128~150 d)也出现了相同的现象,这是运行前期活性炭对DO的强吸附作用所致[22],在吸附达到饱和后DO消耗量稳定,这表明活性炭表面的氧气充足,利于好氧微生物的生长繁殖。
如图6(a)所示,HBC-O3和LBC-O3对于浊度的去除无明显差异。如图6(b)所示, LBC-O3和HBC-O3出水pH随时间的变化表现出相同的变化趋势:在0~60 d内,出水pH由最初的9.0左右(高于进水)快速下降并稳定在7.5左右且低于进水。与LBC-O3相比,在0~17 d,HBC-O3出水pH低,这与新活性炭LBC的pH大于HBC有关(LBC、HBC的pH分别为9.0和8.0);约17 d后,HBC-O3出水pH高,差值维持在0~0.2左右,以上趋势应该是由压块活性炭本身的表面特性及BAC工艺的综合作用(臭氧氧化、吸附、生物降解等)所导致[23]。由图6(c)可知,对于UV254所代表的有机物,HBC-O3和LBC-O3的去除率主要集中在70%~90%,其平均去除率分别为84.2%和77.3%,即HBC-O3的去除效果更好。有研究表明,UV254代表水中腐殖质类和各种芳香族等大分子有机化合物[24],HBC-O3效果较好的原因是其孔隙结构特点更适宜去除水中UV254所代表的有机物[25]。由图1和表1可知,LBC和HBC的孔径均主要分布在0.3~10.0 nm,以微孔和中孔为主;与LBC相比,HBC具有更大的比表面积、更高的孔隙容积,且其中微孔容积较LBC高出19.9%,中孔容积高出28.5%;即HBC更丰富的次微孔及中孔结构为吸附大分子有机物创造了有利条件[23]。基于课题组前期的研究结果可知,就宏观技术指标而言,去除UV254所代表的大分子有机物应选择亚甲基蓝吸附值更高的活性炭[26]。由图6(d)可知,对于CODMn,LBC-O3和HBC-O3的去除率均在30%~90%,主要集中在60%~75%,其平均去除率分别为65.7%和64.3%,即LBC-O3的去除效果略好于HBC-O3。在运行0~60 d,LBC-O3和HBC-O3的去除效果较好,去除率可达55%~80%,这是因为炭在投加初期具有较强的吸附能力;在60~100 d,由于进水中CODMn值增加导致去除率降低;100 d后去除率稳定在60%~70%,这是由于该阶段中微生物(详见2.2节)对有机物的生物降解作用,使活性炭吸附位点在被释放与被占据中平衡[22],从而使出水的CODMn值稳定在一定范围;与HBC-O3相比,LBC-O3对CODMn的去除率略高,表明该活性炭的孔隙结构适宜吸附水体中该类有机污染物;即由于LBC-O3与HBC-O3对CODMn表现出较佳的吸附性能,而被吸附的有机污染物又为微生物的生长繁殖提供了饵料,从而促成了活性炭表面微生物的生长,进而构成了吸附、生物降解的良性循环[26]。
综上所述,虽然经LBC-O3和HBC-O3处理后,出水水质均达到了要求,但其分别对以CODMn、UV254为代表的两类目标污染物的不同净化效果与BAC工艺的核心材料——活性炭的孔隙结构密切相关。对于UV254代表的有机污染物而言,HBC-O3的平均去除率比LBC-O3高6.9%;对于CODMn而言,LBC-O3的平均去除率比HBC-O3高1.4%。这是由活性炭的孔隙结构及原水中污染物的特性共同决定的,即针对原水水质进行分析,靶向选择活性炭将有助于提高污染物去除率、节约资源,符合双碳目标。
-
1)细菌总数的变化。小试BAC工艺LBC-O3和HBC-O3内活性炭上附着的细菌总数随运行时间的变化如图7所示,小试BAC工艺中LBC-O3和HBC-O3活性炭上附着的细菌总数在2 500~12 500 CFU·g−1,其中LBC-O3细菌总数稍高,这与其对CODMn的去除效果(2.1节)较好相互印证。在小试装置运行80 d时,活性炭上细菌总数已接近稳定状态,微生物的稳定状态与CODMn的去除阶段基本一致;小试装置运行第128 d,反冲洗再次运行后,活性炭上的细菌开始增长,并于190 d后再次稳定。
2)微生物扫描电镜表征。小试BAC工艺运行280 d的活性炭样的表面微生物电镜照片如图8所示,细菌主要生长在活性炭表面和孔隙处,主要为杆状菌、丝状菌和球状菌。这进一步验证了细菌总数的测定结果。
-
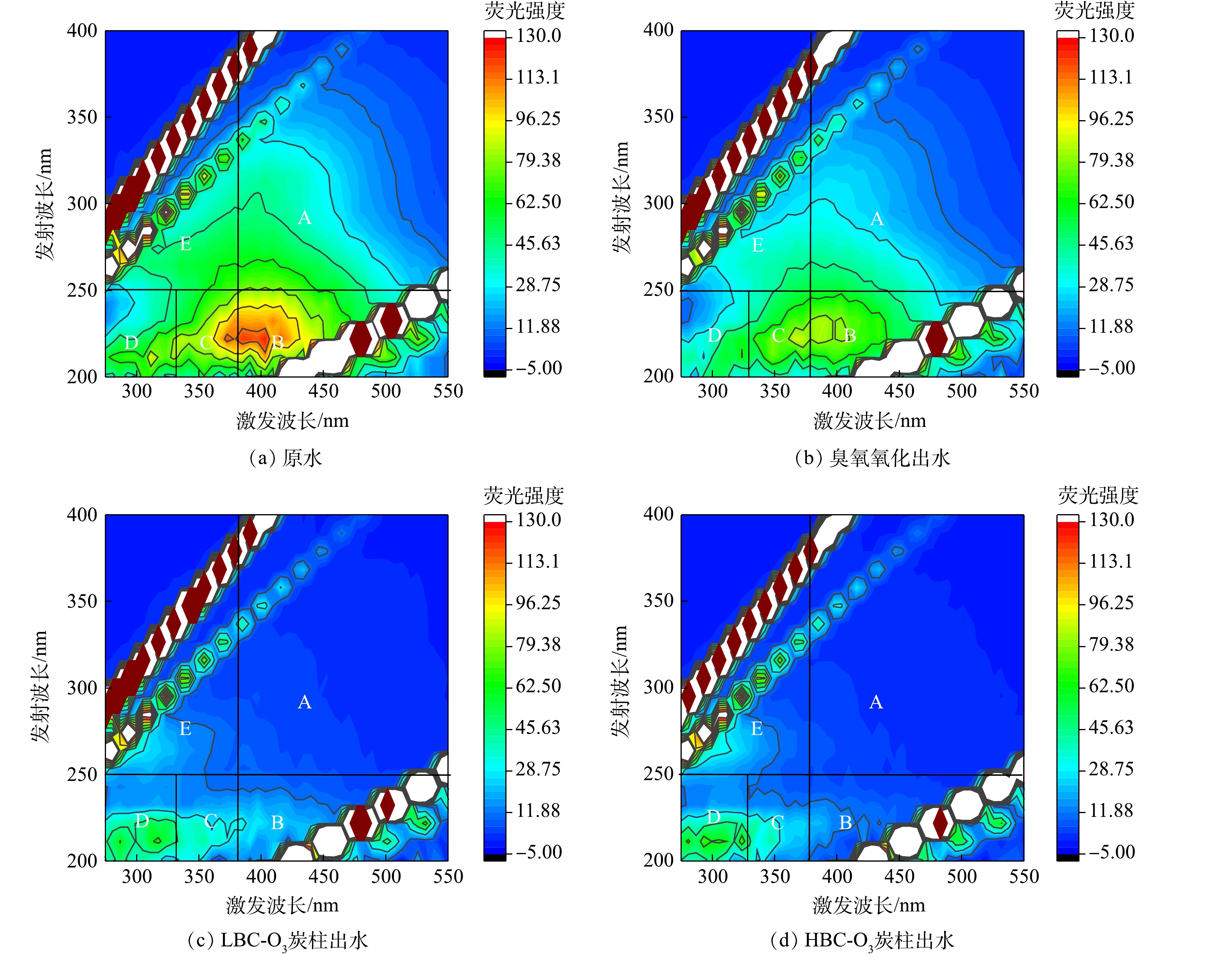
利用三维荧光光谱对小试BAC工艺进出水中溶解性有机物的光谱特性等进行表征,结果如图9所示。三维荧光光谱图按激发波长(Em)和发射波长(Ex)可分为5个区域:A区(Em>380 nm,Ex>250 nm)代表类腐植酸类有机物;B区(Em>380 nm,Ex<250 nm)代表类富里酸类物质;C区(330 nm<Em<380 nm,Ex<250 nm)和D区(Em<330 nm,Ex<250 nm)代表简单的芳香族蛋白质(C区主要代表色氨酸类芳香族蛋白质,D区主要代表酪氨酸类芳香族蛋白质);E区(Em<380 nm,Ex>250 nm)代表溶解性微生物代谢物[27-28]。
由图9(a)可知,实验原水在B、C、D区有明显荧光峰,A、E区没有明显的荧光峰,以肩峰形式呈现,说明原水中溶解性有机物以类富里酸和芳香族蛋白质为主。
对比图9(a)和图9(b)可知,臭氧氧化出水中上述区域的强度均明显降低,说明臭氧对原水中存在的物质均存在分解作用,此处与2.1节臭氧接触后水中CODMn和UV254的降低呼应:CODMn在一定程度上表示水中有机物的多少,所以其降低与臭氧导致的溶解性有机物的减少有关,UV254的降低是臭氧导致的A、C、D区所代表的类腐殖酸类有机物,芳香族蛋白质的减少所致。由图9(c)和图9(d)可知,LBC-O3和HBC-O3出水中A、B、C、E区的物质强度明显降低,说明小试BAC工艺中的炭柱对类腐殖酸类、类富里酸类、色氨酸类芳香族蛋白质和溶解性微生物代谢物有很好的去除效果。D区荧光强度的降低程度较弱,表明小试BAC工艺中的炭柱对D区代表的酪氨酸类芳香族蛋白质去除效果相对较差。
对比图9(c)和图9(d)可知,两者对A区物质的去除效果相当,HBC-O3对B、C、D区物质的去除效果略好于LBC-O3。表明HBC-O3对水中类富里酸类有机物、芳香族蛋白质的去除效果更好,该结果与上述HBC-O3对UV254代表的有机污染物的去除效果优于LBC-O3的结论一致。
如图9(c)和图9(d)所示,对于E区代表的溶解性微生物代谢物,二者均有荧光峰,荧光峰强度不大且两者无明显差异,可能是炭柱对进水中E区物质具有去除作用,同时炭上微生物又产生了E区物质,最终体现在出水的结果。
-
1)HBC-O3对于UV254所代表有机物的平均去除率比LBC-O3高6.9%;而LBC-O3对于CODMn的平均去除率比HBC-O3略高1.4%。这是由活性炭的孔隙结构及原水中污染物的特性共同决定的,即针对原水水质进行分析,靶向选择活性炭将有助于提高污染物去除率、节约资源,符合双碳目标。
2)细菌生长在LBC-O3和HBC-O3活性炭表面和孔隙中,主要为杆状菌、丝状菌和球状菌;细菌总数在2 500~12 500 CFU·g−1,且LBC-O3的细菌总数比HBC-O3略高,与CODMn的去除效果一致。即BAC工艺中活性炭良好的吸附性能与微生物的降解效果的良性循环,不仅能够提高出水水质,还可延长活性炭的工作周期(减少再生次数),从而降低水处理费用。
3)炭柱出水中溶解性有机物的三维荧光光谱特性分析结果表明:HBC-O3对水中B、C、D区物质去除效果更好,验证了前文HBC-O3对UV254所代表有机物的去除效果优于LBC-O3的结论。即原水中类富里酸类有机物、芳香族蛋白质含量高时,应选择亚甲基蓝吸附值更高的活性炭。
新疆煤基压块活性炭在BAC工艺中的应用
Application of Xinjiang coal-based briquetted activated carbon in BAC process
-
摘要: 鉴于新疆丰富的煤炭资源,本研究对由2种不同指标新疆煤基压块活性炭(LBC和HBC)组成的上向流活性炭柱构成的小试生物活性炭(biological activated carbon, BAC)工艺进行了为期约300 d的实验研究。考察了2种不同指标的压块活性炭柱(LBC-O3与HBC-O3)的运行情况。结果表明,LBC-O3对于CODMn的去除效果优于HBC-O3(进水平均值为1.56 mg·L−1,出水平均值为0.55 mg·L−1);而HBC-O3对于UV254所代表有机物去除效果优于LBC-O3(进水平均值为0.053 cm−1,出水平均值为0.005 cm−1)。LBC-O3对CODMn的较佳去除性能,促成了活性炭表面微生物量的生长,进而构成了吸附和生物降解的良性循环;而兼具发达次微孔和中孔结构的HBC-O3对UV254代表的有机物表现出了靶向吸附性;微生物检测结果和炭柱出水中溶解性有机物的光谱特性分析验证了该结论。因此,结合目标水体中污染物的特性靶向选择相应指标(孔隙结构)的压块活性炭可取得更佳的BAC工艺处理效果:提高污染物去除率、节约资源,符合双碳目标。Abstract: In view of the rich coal resources in Xinjiang, a lab-scale biological activated carbon (BAC) process consisting of two up-flow columns was conducted for about 300 days and its running status was investigated, in which two kinds of Xinjiang coal-based briquetted activated carbon (LBC and HBC) with different indicators were packed, denoted as LBC-O3 and HBC-O3 columns, respectively. The results showed that the CODMn removal effect by LBC-O3 was better than that of HBC-O3 (the average value of influent was 1.56 mg·L−1, and the average value of effluent was 0.55 mg·L−1). The removal effect of organic compounds represented with UV254 by HBC-O3 was better than that of LBC-O3 (the average value of influent was 0.053 cm−1, and the average value of effluent was 0.005 cm−1). The better adsorption performance of LBC-O3 on organic compounds represented by CODMn promoted the growth of microbial biomass on the surface of activated carbon, thus forming a good cycle of adsorption and biodegradation. HBC-O3 with developed sub-microporous and mesoporous structures showed targeted adsorption to organic compounds represented by UV254. The results of microbial detection during BAC process and three dimensional fluorescence spectra of influent and effluent of BAC columns confirmed the conclusion. Therefore, combining with the characteristics of pollutants in the target water, the targeted selection of the briquetted activated carbon was made and could achieve better BAC process treatment effect, which can improve pollutant removal rate and save resources, being in line with the goal of carbon emission peak and carbon neutrality.
-
由于锂离子电池具有安全环保,电池容量大,输出功率大,自放电小等诸多优点,被广泛用于便携式电子产品,航空航天,医疗器械等领域[1~2]。据报道,2022年中国锂电池正极材料和负极材料产量分别有1.85×106 t和1.4×106 t,而2022年锂电池回收量仅有4.15×105 t,只有15%不到的锂电池得到有效回收,因锂电池使用寿命只有1~3年,如果回收率不变,到2025年可能会有2.835×106 t废电池不能得到有效回收。这些废旧锂电池中含有钴、镍等有毒重金属,直接丢弃会对土壤、河流等造成严重污染,而锂离子电池中锂、镍、钴、锰等金属的含量远高于一般矿物,具有极高的资源性和价值,随着科技不断发展和资源的不断开发,对资源的可循环利用和环境保护的要求被日益重视[3],因此废旧锂离子电池的回收显得尤为重要并已经迫在眉睫[4-5]。
溶剂萃取法[6]因其具有高提取率、选择分离性高、流程简单和操作连续化等优点,已经成为处理废旧锂电池中金属离子分离回收的主要方法。目前废旧三元锂电池中有价金属提取主要是在无机酸 (硫酸、盐酸等)体系中进行,因此,萃取分离的研究重点主要在硫酸、盐酸等无机酸体系中开展。如:代梦雅等[7]对电极材料使用硫酸浸出,浸出液经过P204除锰,在pH=5.2条件下,分别以0.5 mol·L−1 P507和0.6 mol·L−1 Cyanex272为萃取剂,经过两级错流萃取,钴萃取率分别为98.21%和99.44%, 镍共萃取率分别为24.42%和4.26%, 锂共萃取率分别为15.84%和5.11%;鲁桃等[8]在硫酸体系中使用Cyanex272,初始pH为4,萃取剂体积分数为50%,皂化率75%左右,O/A=1∶1,振荡时间为2 min,钴的一级萃取率为98.38%,而镍的损失率为2.28%。但在无机酸体系提取过程中易产生Cl2、SO2等有害气体、设备易腐蚀、铜、铝等杂质浸出率高等缺点,近年来,更多研究选用酸性较为温和、更为环保、杂质浸出率低的有机酸对正极材料中有价金属进行浸出被越来越多的研究者所关注[9]。如孟飞[10]使用柠檬酸对废旧三元电池浸出,镍钴锂锰的浸出率均大于90%,而铜、铝的浸出率均小于30%;高桂兰[11]对正极材料在柠檬酸浓度1.2 mol·L−1、硫代硫酸钠浓度0.3 mol·L−1、固液比20 g·L−1、浸出温度70 ℃、浸出时间30 min,钴的浸出率可达96%左右,锂的浸出率可达99%左右;但目前,关于在有机酸体系萃取分离废旧三元锂电池中的有价金属的文献较少。
本研究选用的是有机酸中较为便宜的D, L-苹果酸浸出废旧锂电池正极材料,经过前期一定的探索实验探究有机酸体系各种萃取剂对有价金属元素的萃取率;对浸出液选用一种或几种萃取剂来对其中的锰和钴进行分步萃取,研究不同影响因素下萃取剂对苹果酸浸出液中金属元素的萃取效果,为有机酸体系高效萃取锰、钴提供一定的参考。
1. 材料与方法
1.1 实验原料
本实验采用模拟的废旧三元电池正极材料LiNi0.6Co0.2Mn0.2O2的苹果酸浸出液。浸出液Ⅰ的成分为:Mn 2.26 g·L−1、Ni 5.7 g·L−1、Co 2.5 g·L−1、Li 1.24 g·L−1,苹果酸质量浓度为100 g·L−1。浸出液Ⅱ的成分为:Mn 4.51 g·L−1,苹果酸质量浓度为100 g·L−1。浸出液Ⅲ的成分为:Co 5.31 g·L−1,苹果酸质量浓度为100 g·L−1。浸出液IV的成分为:Co 2.50 g·L−1、Ni 4.94 g·L−1、Li 1.28 g·L−1,苹果酸质量浓度为100 g·L−1。萃取剂P204和萃取剂Cyanex272由重庆康普化学工业股份有限公司生产、萃取剂溶剂为煤油 (航空煤油)、NaOH为天津市风船化学试剂科技有限公司生产,苹果酸为湖县利乐生物科技实业有限公司生产。
1.2 实验方案
实验时,首先使用30%NaOH溶液对浸出液pH值进行调节,然后按设定相比将浸出液与有机相混于分液漏斗中,在震荡器上震荡一段时间,取出分液漏斗静置分相,随后对负载有机相使用极低质量浓度的被萃金属苹果酸溶液进行洗涤,静置分相并分离,随后用一定质量浓度苹果酸溶液与洗涤后的负载有机相进行反萃处理,静置分相并分离得到反萃液。方程式如式(1)~式(3)所示,其中Men+代表被萃金属离子,Mn+代表其它金属离子,HR表示萃取剂。
stringUtils.convertMath(!{formula.content}) (1) stringUtils.convertMath(!{formula.content}) (2) stringUtils.convertMath(!{formula.content}) (3) 式(1)是萃取剂将浸出液中的金属元素萃取到有机相中,式(2)是通过低质量浓度的苹果酸溶液将其它金属离子洗涤到溶液中,式(3)是使用低质量浓度苹果酸溶液将负载有机相中的金属离子反萃到苹果酸溶液中。
2. 结果与讨论
2.1 P204萃取Mn2+的研究
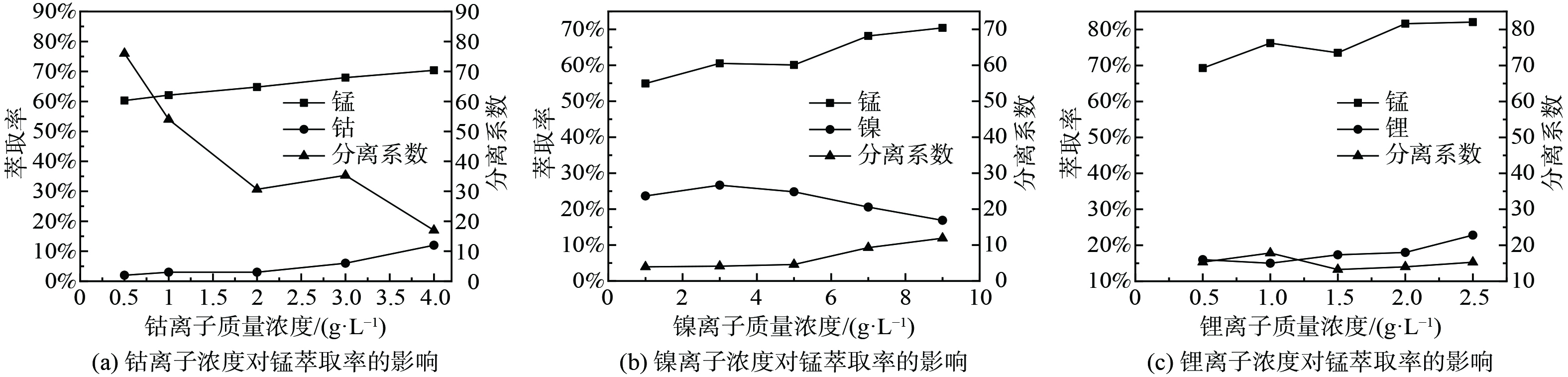
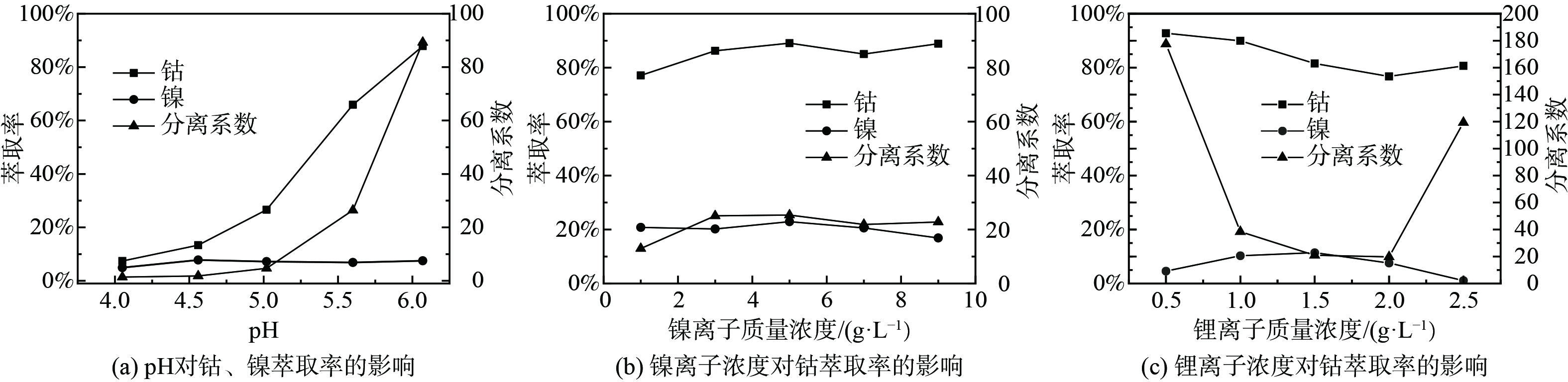
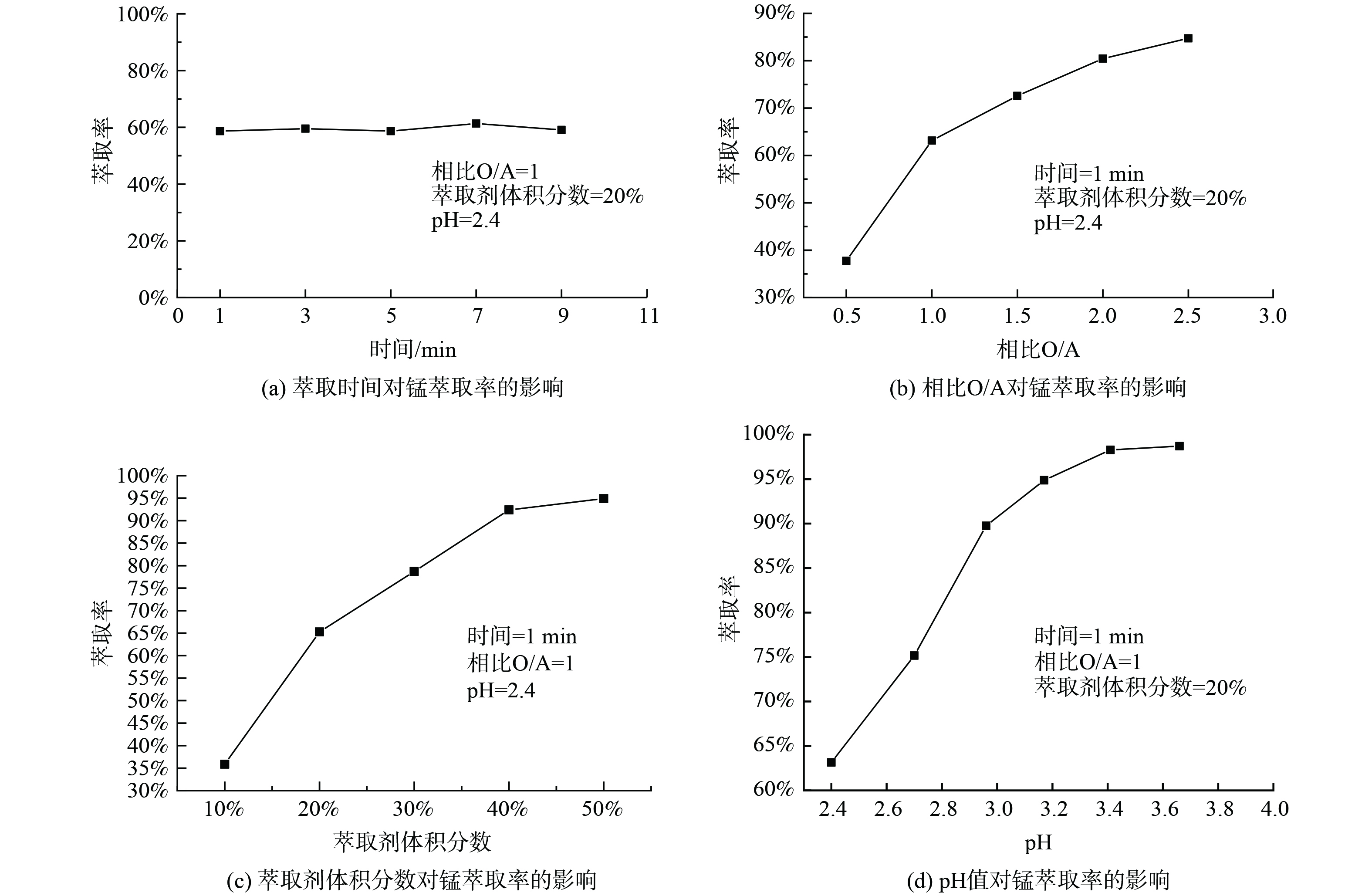
1)萃取条件对P204萃取Mn2+的影响。取浸出液Ⅱ20 mL,进行温度为25 ℃,萃取时间为1~9 min,相比O/A为1∶2至5∶2,萃取剂体积分数为10%~50%,浸出液pH为2.40~3.70系列条件下的萃取实验,实验结果如图1所示。如图1(a)所示,随着时间的增加,萃取率有轻微变化,但起伏不大,说明反应进行较快。当萃取时间为1 min时,反应已达到平衡,萃取率在60.00%左右;如图1(b)所示,随着相比O/A增加,锰的萃取率先迅速增加后趋于稳定,这是因为在溶液中其他离子质量浓度确定的情况下,锰的萃取率取决于萃取剂P204量的多少,增大相比O/A就等于增加萃取剂的量,当相比O/A较小时,萃取剂P204基本与锰完全反应,因溶液中锰的含量是一定的,所以最终锰的萃取率是趋于稳定的。考虑到原料利用率,相比过大导致体系粘度增加,影响分相效率及分相速率等问题,选择最佳相比O/A为1∶1,其萃取率为63.15%。由图1(c)可知,当萃取剂体积分数分别为10%、20%、30%时,萃取率分别为35.87%、65.25%、78.70%,随着萃取剂体积分数的增加,锰的萃取率也迅速增加,最后趋于平衡,这是因为随着P204含量的增加,萃取剂与锰的接触几率增加,形成萃合物的几率增加,从而萃取率增加,因锰的含量是固定的,所以最后萃取率趋于平衡。考虑到成本及萃取率增加速率,选择最佳萃取剂体积分数为20%。由图1(d)可知,随着初始pH的增加,萃取率迅速增加,然后趋于平缓,这是因为在萃取反应过程中金属离子会与萃取剂反应产生H+离子,pH值的增加有利于反应向生成萃合物的方向进行,当pH=2.96时,萃取率为89.75%,再继续增加pH,萃取率增加相对较小,因此选择最佳pH为2.96。取浸出液Ⅰ在最佳实验条件下进行三级逆流萃取实验,锰的萃取率可达到99.99%,镍、钴、锂的共萃率分别为12.11%、9.20%、3.23%。
2)其他金属离子对P204萃取Mn2+的影响。取浸出液Ⅱ20 ml,分别加入一定量碳酸钴、碳酸镍、碳酸锂,进行温度为 25 ℃,萃取时间为1 min,相比O/A=1∶1,萃取剂体积分数为20%的萃取实验,实验结果如图2所示。随着钴离子质量浓度的增加,锰离子萃取率在缓慢增加。由于添加碳酸钴导致初始pH发生变化,初始pH变为2.44~2.65,在无钴离子存在的情况下,P204对锰的萃取率从63%左右升至73%左右,而添加钴离子后,锰的萃取率从60.30%增加到70.40%,说明锰离子萃取率的增加主要是由于添加碳酸钴导致的初始pH值变化引起的。由于钴的萃取率在在逐渐增加,从而使锰、钴的分离系数在不断降低。由图2(b)可知,随着镍离子质量浓度的增加,锰离子的萃取率不断增加。由于加入了碳酸镍,导致初始pH值变为2.48~2.78,在无镍离子存在的情况下,锰的萃取率从64.00%左右升至78.00%左右,而添加镍离子后,锰的萃取率从54.93%升到70.40%,说明锰离子萃取率的增加主要是由于添加碳酸镍导致的pH值变化引起的。而镍离子的萃取率先增加后降低,这是因为P204对镍的萃取容量达到了最大值,继续增加镍离子质量浓度,萃取率降低。由图2(c)可知,随着锂离子质量浓度的增加,锰离子的萃取率不断增加,由于加入了碳酸锂,初始pH值变为2.70~3.28,在无锂离子存在的情况下,P204对锰的萃取率从75.00%左右上升到95.00%左右,添加锂离子后,萃取率由69.28%上升至82.06%,说明锰离子萃取率的增加主要是由于添加碳酸锂导致的pH值变化引起的。由图2的(a)、(b)、(c)可知,3种离子与锰的分离系数均较差,为了保证纯度,需要在后续对负载有机相进行水洗以除去其中大部分的其他金属离子。
3) P204负载有机相反萃锰的研究。为了抑制有机相中锰被洗出,使用含1 g·L−1锰的100 g·L−1苹果酸溶液以相比O/A=1∶1对浸出液Ⅰ使用P204进行三级逆流萃取后的负载锰有机相洗涤,洗涤前有机相中Mn为2.255 g·L−1,Ni为0.69 g·L−1,Co为0.23g·L−1,洗涤后有机相中Mn为2.51 g·L−1,Ni为0.04 g·L−1,Co仅含0.03 g·L−1,锂离子质量浓度太低未检测到,表明洗涤效果较良好。对洗涤后的负载有机相进行反萃,固定条件为:反萃介质为苹果酸,相比O/A=1∶1、反萃时间20 min、温度25 ℃,实验结果如图3。由图3可知,在此反萃条件下,Mn的单级反萃率可达55.00%左右。在同样反萃条件下对Mn负载有机相进行三级逆流反萃,反萃率可达88.80%,由此可见,苹果酸溶液能将大部分的锰反萃。
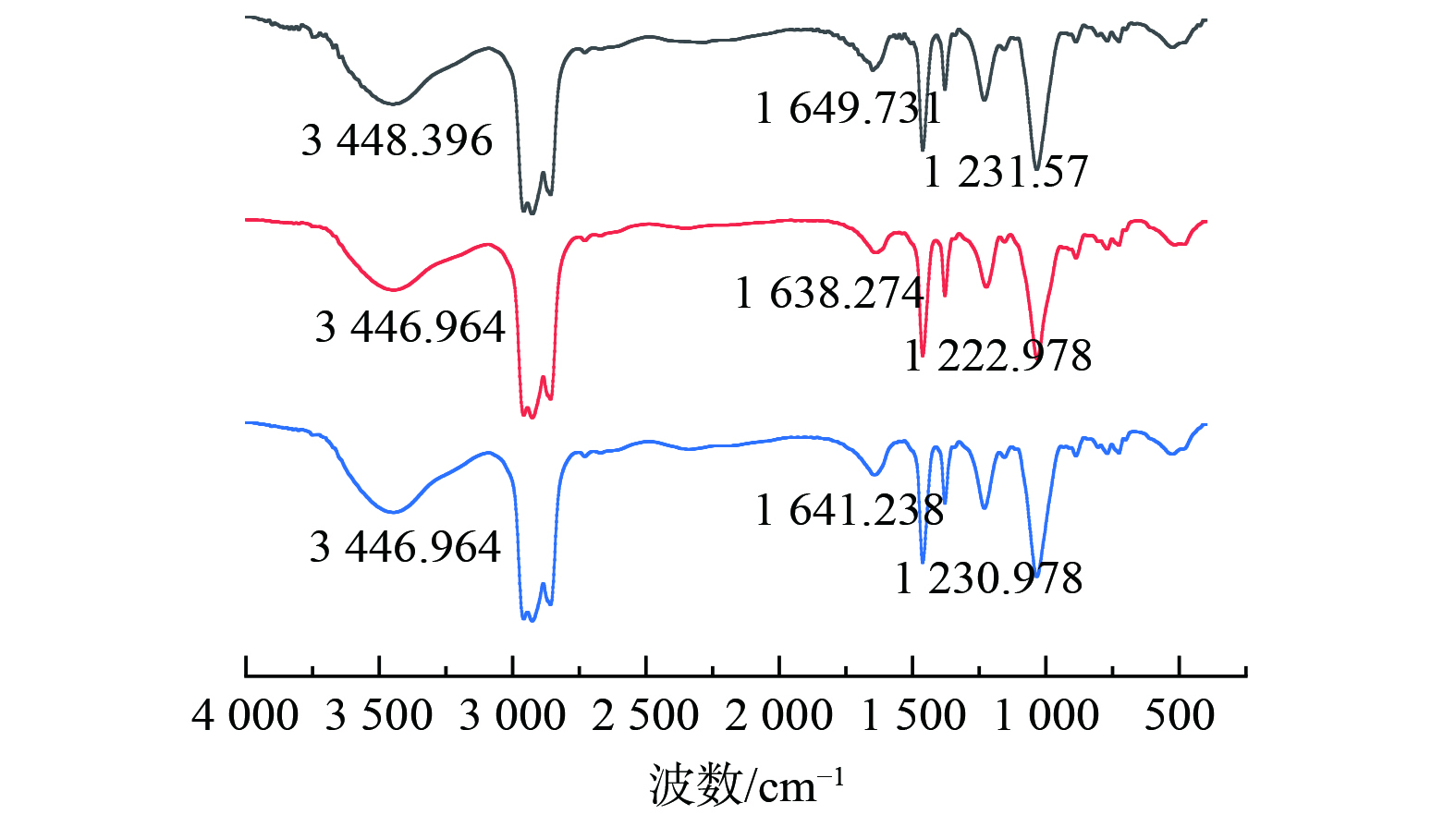
4)红外光谱测试分析P204萃取锰对P204有机相萃取前后及反萃后进行了红外光谱分析,如图由图4可知,在3 448.396 cm−1出现二聚体分子间氢键伸缩振动峰,在1 649.731 cm−1出现二聚体的O-H面内弯曲振动峰。在萃取后,3 448.396 cm−1振动峰强度降低但是仍能观察到二聚体峰,说明分子间形成的-OH键中的H被锰取代,但是P204过量,未能完全消除二聚体的影响。而1 649.731 cm−1的峰向低波数1 638.274移动,且峰强度有所降低,这是因为P-O→Mn的生成的同时使氢键电子云降低。在反萃后,振动峰强度有一定恢复且向高波数偏移至1 641.238 cm−1,这是因为反萃后锰被氢离子置换出去,但是仍未置换完全。在1 231.570 cm−1处出现P=O的伸缩振动峰,在萃取后,由高波数的1 231.570 cm−1位移到1 222.978 cm−1说明P=O键与Mn离子发生配位,波数变化是由于P=O键与Mn形成P=O→Mn配位键,使P=O双键的电子云密度降低,键的强度减弱,从而导致其震动频率下降。同时因为Mn与P=O的配位,使P204的对称性发生变化,P=O键的偶极矩发生变化,导致峰强度减弱[12-14]。即P204萃取锰的反应的实质是Mn与P-O-H中的氢发生置换反应,且与P=O形成配位键进而被萃取。
2.2 Cyanex272萃取钴的研究
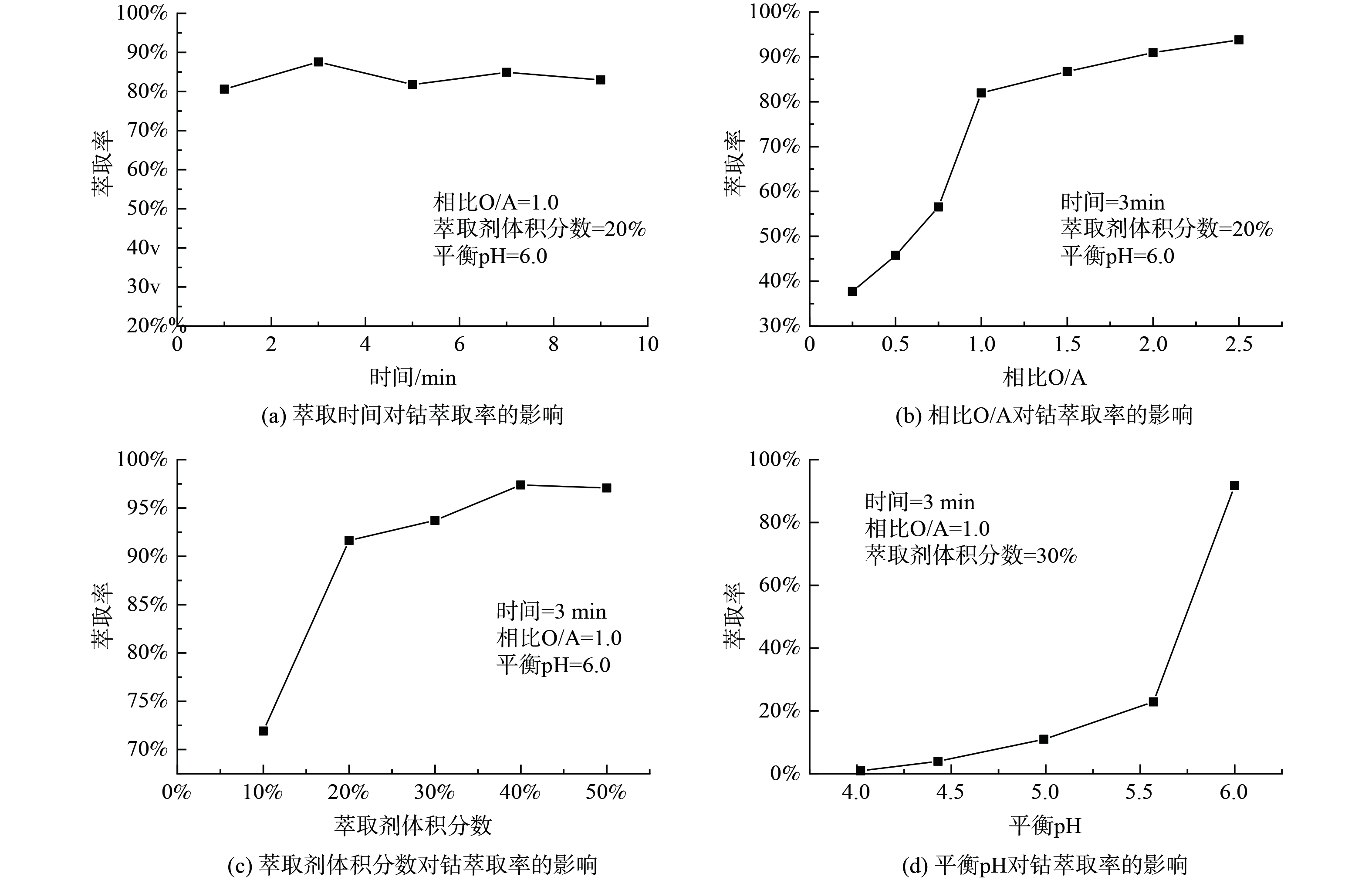
1)萃取条件对Cyanex272萃取Co2+的影响。取浸出液Ⅲ 20ml,进行温度为25 ℃,萃取时间为1~9 min,相比O/A为1∶4至5∶2,萃取剂体积分数为10%~50%,平衡pH为4~6的萃取实验,实验结果如图5所示。如图5(a)所示,整个反应进行较快,萃取率整体变化不大。当萃取时间为3min时,萃取率为87.56%,达到最大值,因此,3 min为最佳萃取时间。由图5(b)可知,随着相比O/A的不断增加,萃取率也在不断增加。因溶液中钴离子的含量是一定的,相比O/A的不断增加,最终钴的萃取率时趋于稳定的。考虑到成本,原料利用率,以及相比过大时导致影响分相效率及分相速率低,选择最佳相比O/A为1∶1,钴的最佳萃取率为81.97%。由图5(c)可知,随着萃取剂体积分数的不断增加,萃取率也是在不断增加的。这是因为Cyanex272的增加,萃取剂与钴的接触几率也在不断增加,形成萃合物的几率增加,最终萃取率增加。当萃取剂体积分数分别10%、20%、30%,萃取率分别为71.92%、91.65%、93.72%,因萃取剂体积分数为20%时,萃取率上升幅度较大,所以最佳萃取剂体积分数为20%。由图5(d)可知,随着pH的增加,萃取率不断增加,当pH为5~6时,萃取率有较大幅度增加。当平衡pH=6,钴的萃取率为91.75%。随着萃取反应的进行,溶液的pH在不断降低,增加水相的平衡pH有利于萃取反应发生,进而增大钴的萃取率,最终选择最佳平衡pH为6。取浸出液IV在最佳实验条件下进行三级逆流萃取钴实验,钴的萃取率为94.01%,锂、镍的共萃率分别为11.21%和0.02%。
2)其他金属离子对Cyanex272萃取Co2+的影响。取浸出液Ⅲ20ml,分别加入一定量碳酸镍、碳酸锂,并重新定容,进行温度为25 ℃,萃取时间为3min,相比O/A=1∶1,萃取剂体积分数为20%,平衡pH=6的萃取实验,实验结果如图6所示。因Cyanex272对钴、镍均具有良好的萃取效果,所以测试在添加一定量镍离子后,在萃取剂体积分数为20%,相比O/A=1∶1,萃取时间3 min,镍离子质量浓度为10.4 g·L−1条件下,不同平衡pH下Cyanex272对镍、钴的萃取效果,结果如图6(a)所示,随着平衡pH的增加,钴离子的萃取率在不断增加,镍离子的萃取率基本保持不变。当pH=6时,钴的萃取率为89.62%,镍的萃取率未超过10%,说明不同pH下,镍离子对Cyanex272萃钴过程基本无影响。由图6(b)可知,随着镍离子质量浓度的增加,钴离子萃取率先增后趋于平衡,与未添加镍离子时相比,钴的的萃取率有一定的下降,即镍离子对Cyanex272萃钴有抑制作用,但是随着镍离子质量浓度的增加,这种抑制作用在不断降低。镍离子萃取率基本维持在20.00%左右,当镍离子质量浓度为3 g·L−1时,钴的萃取率为86.24%,此时镍钴的分离系数为20.2,两者较易进行分离。由图6(c)可知,随着锂离子质量浓度增加,钴离子萃取率整体呈下降趋势,说明锂离子对钴离子的萃取有一定抑制作用,且这种抑制作用在不断增强。
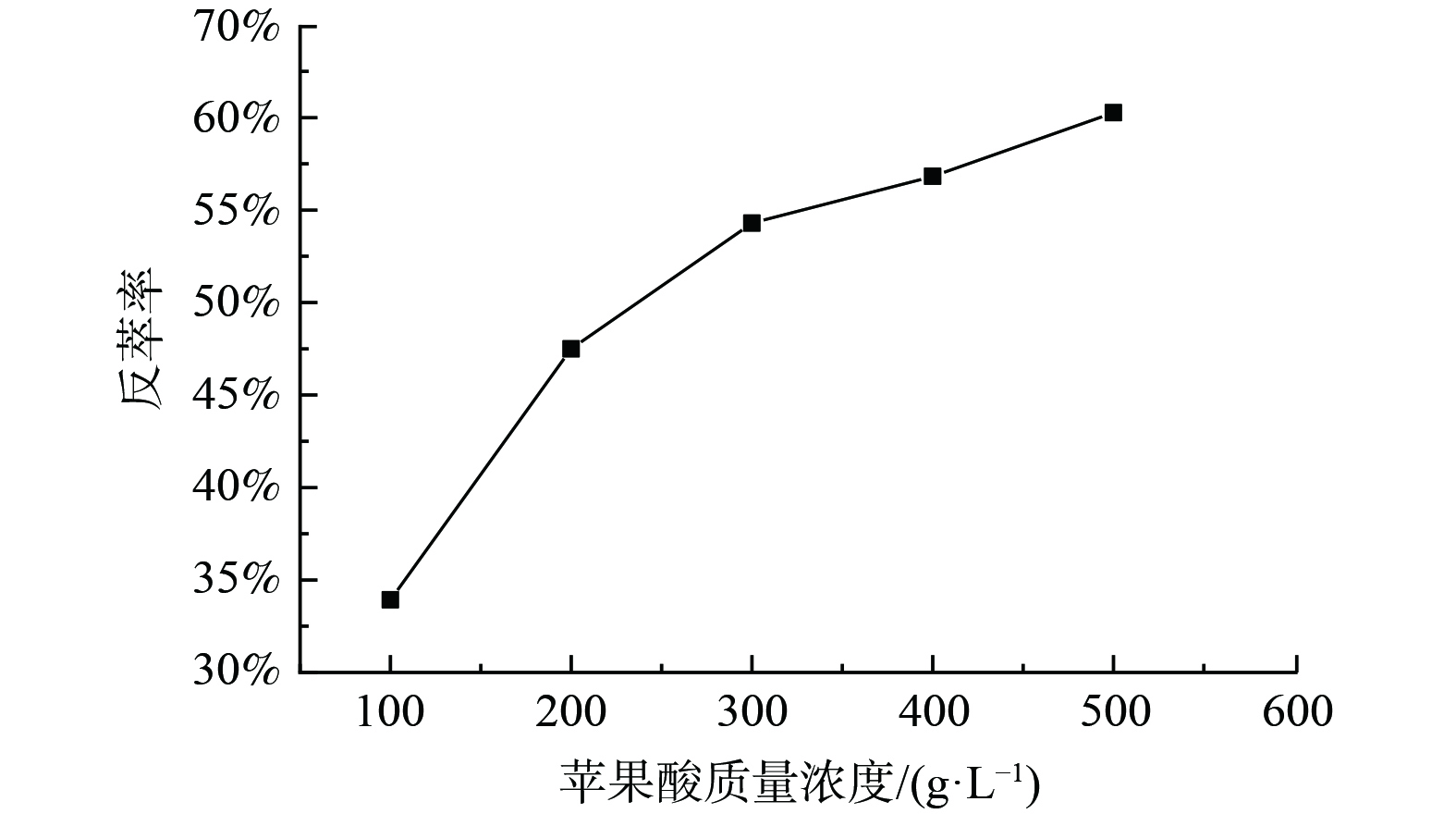
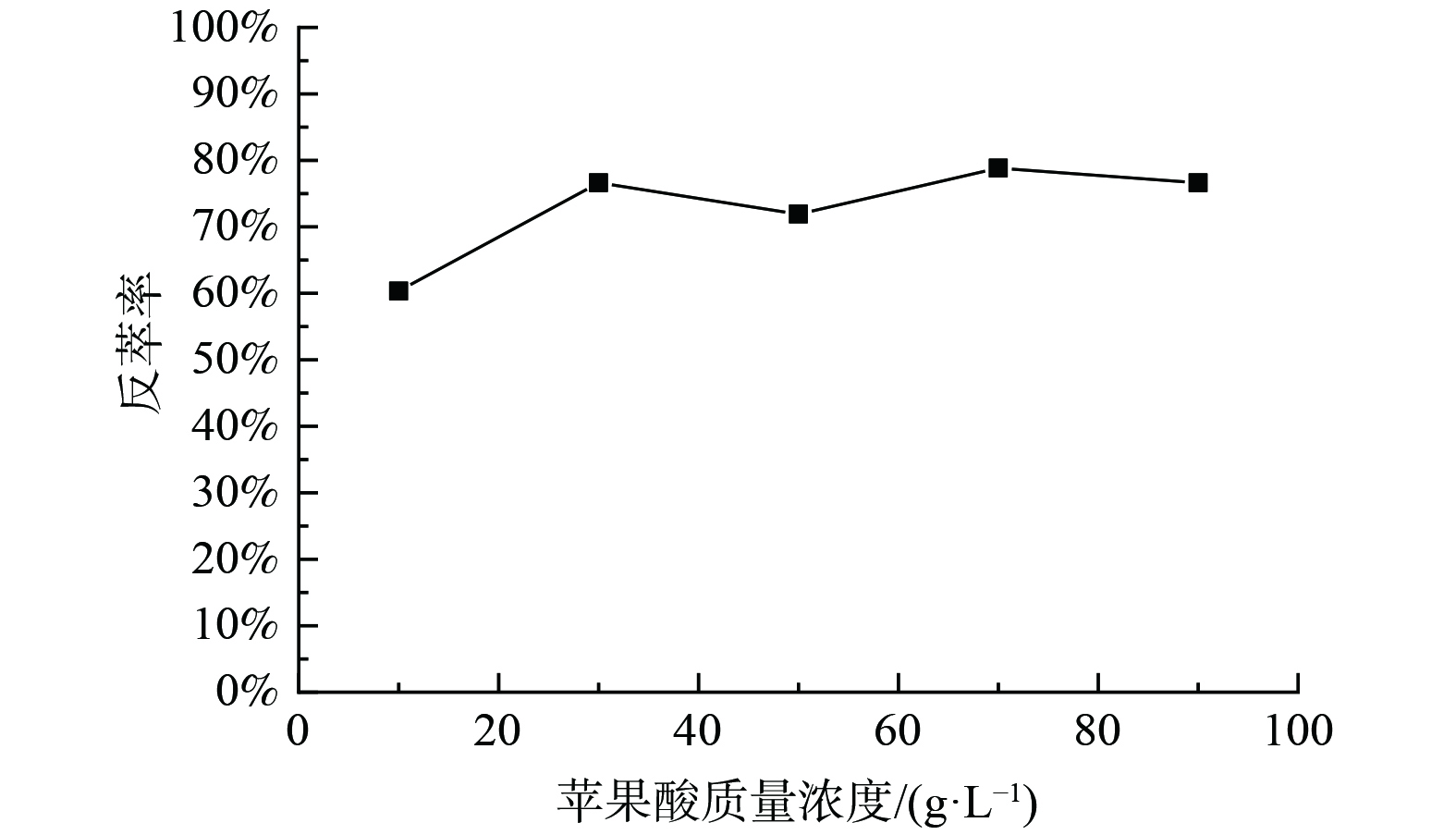
3) Cyanex272负载有机相反萃钴的研究。为了抑制有机相中的钴被洗出,使用含1 g·L−1钴的10 g·L−1苹果酸溶液以相比O/A=1∶1对浸出液IV使用Cyanex272进行三级逆流萃取后的负载钴有机相洗涤,洗涤前有机相中Co 2.31 g·L−1,Ni 0.01 g·L−1,Li 0.14 g·L−1,洗涤后有机相中Co为2.81 g·L−1,镍未检测出,锂仅含5.47 mg·L−1,洗涤效果良好。对洗涤后的负载有机相进行反萃,固定条件为:反萃介质为苹果酸、相比O/A=1∶1、反萃时间10min、温度25 ℃。实验结果如图7。由图7可知,当反萃介质苹果酸质量浓度为30 g·L−1时,Co的单级反萃率可达76.61%。在同样条件下进行三级逆流反萃Co后,Co反萃率为99.98%。
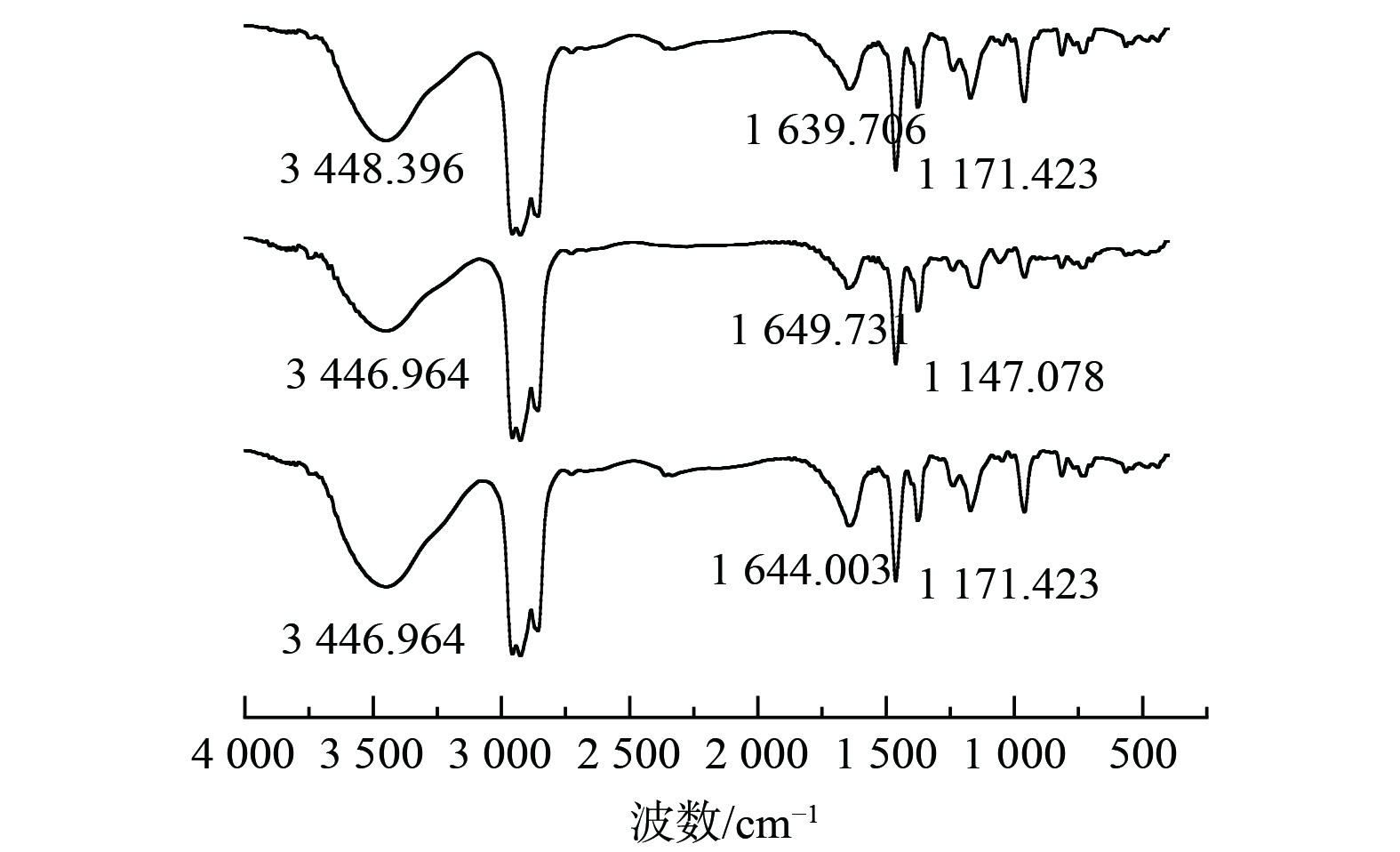
4)红外光谱测试分析Cyanex272萃取钴对Cyanex272有机相萃取前后及反萃后进行了红外光谱分析, 如图8所示。在3 448.396 cm−1附近和1 639.706 cm−1附近出现了二聚体分子间氢键伸缩振动峰, 和二聚体的O-H面内弯曲振动峰,在1 171.423 cm−1附近出现了P=O的伸缩振动峰。萃取后,位于3 448.396 cm−1的吸收峰的强度变低和位于1 639.706cm−1的峰向高波位1 649.731 cm−1移动,且峰强度有所降低,在反萃后有所恢复,说明-OH中的氢与锰发生了置换反应,而在萃取后,由高波位的1 171.423 cm−1的P=O的伸缩振动峰位移到低波位的1 147.078 cm−1,且峰强度变弱,这说明P=O键与钴离子发生配位反应,使P=O的电子云密度降低,减弱了P=O键的强度,使其振动频率减弱。因为P=O与Co的配位,使得Cyanex272的对称性改变,P=O键的偶极矩发生变化,导致峰强度减弱。即Cyanex272萃取钴的反应的实质是钴与P-O-H中的氢发生置换反应,且与P=O形成配位键进而被萃取。
3. 结论
1)在苹果酸体系中, P204做萃取剂通过三级逆流萃取可使锰的萃取率达99.99%,其中除萃取时间外,相比O/A、萃取剂体积分数、pH这3个因素对P204萃锰的萃取率有显著影响;通过三级逆流反萃,锰的反萃率可达88.88%。
2)在苹果酸体系中,Cyanex272做萃取剂通过三级逆流萃取可使钴的萃取率达94.01%,其中平衡pH对Cyanex272萃取钴的萃取率影响最为显著,其次分别是相比O/A和萃取剂体积分数。通过三级逆流萃取,钴的反萃率可达99.98%。
3)根据红外光谱结果表明,P204萃锰、Cyanex272萃钴的原理为金属离子与P-O-H中的氢发生置换反应,且与P=O形成配位键进而被萃取。
-
表 1 LBC与HBC的孔隙结构表征
Table 1. Characterization of pore structure of LBC and HBC
编号 比表面积/ (cm2·g−1) 总孔容/ (cm3·g−1) 微孔容积/ (cm3·g−1) LBC/HBC 微孔含量比 中孔容积/ (cm3·g−1) LBC/HBC 中孔含量比 平均孔径/ nm LBC 1 069 0.656 4 0.366 0 1.0 0.237 9 1.0 2.457 HBC 1 331 0.825 5 0.438 9 1.2 0.305 8 1.29 2.481 -
[1] HOEK J P, BERTELKAMP C, VERLIEFDE A, et al. Drinking water treatment technologies in Europe: State of the art challenges-research needs[J]. Journal of Water Supply Research and Technology-Aqua, 2014, 63(2): 124-130. doi: 10.2166/aqua.2013.007 [2] HOUTMAN C J. Emerging contaminants in surface waters and their relevance for the production of drinking water in Europe[J]. Journal of Integrative Environmental Sciences, 2010, 7(4): 271-295. doi: 10.1080/1943815X.2010.511648 [3] 刘淑彦, 王秀蘅. 饮用水深度净化技术的现状与发展方向[J]. 哈尔滨工业大学学报, 2003, 35(6): 711-714. [4] 文湘华, 申博. 新兴污染物水环境保护标准及其实用型去除技术[J]. 环境科学学报, 2018, 38(3): 847-857. [5] 王占生, 刘文君. 我国给水深度处理应用状况与发展趋势[J]. 中国给水排水, 2005, 21(9): 29-33. [6] 兰亚琼, 刘锐, 马正杰, 等. 臭氧-生物活性炭对微污染原水中典型持久性有机物的去除效果[J]. 环境科学, 2018, 39(12): 5541-5549. [7] 王占生, 刘文君, 董丽华. 饮用水深度处理的必要性与发展趋势[J]. 给水排水, 2014, 50(2): 1-5. [8] 黄美心, 邹苏红, 张金松. 臭氧-生物活性炭技术在我国饮用水深度处理的研究进展[J]. 城镇供水, 2021(3): 46-50. [9] LU Z D, LI C, JING Z B, et al. Implication on selection and replacement of granular activated carbon used in biologically activated carbon filters through meta-omics analysis[J]. Water Research, 2021, 198: 117152. doi: 10.1016/j.watres.2021.117152 [10] 董秉直, 肖健, 华建良, 等. 高品质饮用水的思考以及苏州实践[J]. 给水排水, 2021, 57(8): 19-27. [11] 李景乐, 解炜. 水深度净化用活性炭的指标及选择[J]. 煤炭加工与综合利用, 2021(8): 85-88. [12] 陶辉, 韩锦辉, 徐春蕾. 给水厂生物活性炭更换方式评价[J]. 华中科技大学学报(自然科学版), 2020, 48(8): 121-126. [13] 顾向明, 徐庶伟. 一种新型评价模型在庙港水厂活性炭选型中的应用[J]. 净水技术, 2020, 39(S2): 21-27. doi: 10.15890/j.cnki.jsjs.2020.s2.005 [14] 万超然, 解强, 刘德钱, 等. 饮用水深度处理用煤基活性炭吸附性能表征[J]. 矿业科学学报, 2021, 6(4): 487-496. [15] 梁大明. 用于饮用水深度净化的煤基生物活性炭[J]. 洁净煤技术, 2008, 14(6): 25-28. doi: 10.3969/j.issn.1006-6772.2008.06.007 [16] 侯立安, 董丽华. 活性炭与水净化[M]. 天津: 天津大学出版社, 2021. [17] 陈默. 上向流微膨胀生物活性炭工艺微生物特性研究[D]. 北京: 清华大学, 2012. [18] 韩立能. 微膨胀上向流生物活性炭工艺特性及应用研究[D]. 北京: 清华大学, 2013. [19] 中华人民共和国环境保护部. 水质 高锰酸盐指数的测定: GB/T 11892-1989[S]. 北京: 中国标准出版社, 1989. [20] 中华人民共和国卫生部, 中国国家标准化管理委员会. 生活饮用水标准检验方法 微生物指标: GB/T 5750. 12-2006[S]. 北京: 中国标准出版社, 2007. [21] NEMES A, FABIAN I, VAN ELDIK R. Kinetics and mechanism of the carbonate ion inhibited aqueous ozone decomposition[J]. Journal of Physical Chemistry A, 2000, 104(34): 7995-8000. doi: 10.1021/jp000972t [22] 刘红, 李安婕, 全向春, 等. 生物活性炭降解2, 4-二氯酚的特性[J]. 环境科学, 2004, 25(6): 80-84. [23] 董丽华, 杨晓红, 陈志颖, 等. BAC工艺中活性炭去除重金属机理研究——以Pb(II)为例[J]. 中国环境科学, 2023, 43(5): 2228-2238. [24] 蒋绍阶, 刘宗源. UV254作为水处理中有机物控制指标的意义[J]. 重庆建筑大学学报, 2002, 24(2): 61-65. [25] [日]立本英机, 安部郁夫. 活性炭的应用技术[M]. 高尚愚, 译. 南京: 东南大学出版社, 2002. [26] 董丽华, 刘文君, 蒋仁甫, 等. 给水深度处理活性炭的孔隙结构特征探讨[J]. 给水排水, 2014, 50(1): 91-94. [27] 赵蓓, 曹新垲, 王敏, 等. 样品前处理对三维荧光检测的影响[J]. 净水技术, 2017, 36(S2): 44-50. [28] CHEN W, WESTERHOFF P, LEENHEER J A, et al. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(24): 5701-5710. 期刊类型引用(1)
1. 刘豹,孙谦,李鑫,王行通,徐康,郑兴. 典型含氮有机物氯化消毒过程中碘代三卤甲烷生成特征. 环境化学. 2023(09): 3221-3224 .  本站查看
本站查看
其他类型引用(1)
-






 下载:
下载: