-
根据第21届联合气候变化大会通过的《巴黎气候协定》,我国提出到2030年实现“碳达峰”、2060年实现“碳中和”的“双碳”目标。在污水处理过程中,由于大量药剂,以及曝气、污泥脱水设备、水泵等的电耗非常大,因此,污水处理行业在保护水环境的同时,实际为高耗能产业。同时,一些污水处理过程还伴有CH4、N2O等温室气体排放。据估算,全球污水处理行业的整体温室气体贡献率约为1%~3%[1-2]。因此,污水处理过程的碳排放问题不可小觑。
以实现碳中和 (Carbon neutrality) 或能量自给自足(Energy self-sufficiency)为目标,多个国家对污水处理碳中和运行制定了相关政策。荷兰提出NEWs概念,将未来污水处理厂描述为“营养物 (Nutrient) ”、“能源 (Energy) ”、“再生水 (Water) ”三厂 (Factories) 合一运行的模式;新加坡国家水务局推行“NEWater”计划,并制定水行业能源自给自足的三阶段目标,其远期目标为完全实现能源自给自足,甚至向外提供能量;美国以“Carbon-free Water”为目标,期望实现对水的取用、分配、处理、排放全过程以实现碳中和;日本发布“Sewerage Vision 2100”,宣布本世纪末将完全实现污水处理过程中能源的自给自足。
而已有国家通过不同手段已实现了污水处理厂的“能量中和”或“碳中和”运行[3-8]。奥地利Strass污水处理厂利用初沉池可截留进水悬浮物 (SS) 中近60%的COD,并以A/B工艺最大化富积剩余污泥,将初沉与剩余污泥共厌氧消化并热电联产 (CHP) 后可实现108%的能源自给率[3]。美国Sheboygan污水处理厂利用厂外高浓度食品废弃物与剩余污泥厌氧共消化并热电联产实现产电量与耗电量比值达90%~115%、产热量与耗热量比值达85%~90%[4]。德国Bochum-Ölbachtal污水处理厂通过节能降耗与热电联产实现能源中和率96.9%、碳中和率63.2%[9]。德国Köhlbrandhöft/Dradenau污水处理厂通过厌氧消化与污泥干化焚烧实现能源中和率>100%,并实现42.3%的碳中和率[10]。希腊Chania污水处理厂通过厌氧消化实现70%的能源中和率,碳中和率达到58.5%[11]。德国布伦瑞克市Steinhof污水处理厂通过剩余污泥单独厌氧消化并热电联产获得79%的能源中和率,再通过补充出水农灌、污泥回田等手段额外实现了35%的碳减排量,使碳中和率高达114%[2]。芬兰Kakolanmäki污水处理厂通过热电联产与余温热能回收最终实现高达640%能源中和率与332.7%碳中和率[12-13]。
以上案例表明,为实现碳中和目标,国外污水处理厂大都采取超量有机物厌氧消化并热电联产的方案。然而,我国市政污水处理厂普遍存在碳源低下的情况,故该思路可能无法实现。这就需要全方位分析污水自身潜能及利用方式来制定适宜于我国污水处理领域的碳中和规划。在国内,基于碳中和的污水处理运行机制研究才刚起步。在技术层面,各种节能降耗、能量回收方式直接或间接补偿污水处理碳排放量似乎是实现污水处理碳中和的重要方式[4-6,9,13]。基于此,本文从能量中和与碳中和基本概念入手,梳理污水处理行业的碳减排策略,同时探讨其能量潜力、技术路径及可操作性等,以期为我国污水处理领域选择适宜的碳中和路径提供参考。
-
1) 通过技术升级实现节能减排。污水处理过程碳排放分直接碳排放与间接碳排放[14]。其中,按联合国政府间气候变化专门委员会 (Intergovernmental Panel on Climate Change, IPCC) 规定由污水中生源性COD产生的CO2 (直接排放) [15]不应纳入污水处理碳排放清单,而甲烷 (CH4) 、氧化亚氮 (N2O) 及污水COD中化石成分[14]产生的CO2则应纳入污水处理直接碳排放清单。因此,间接碳排放包括:电耗 (化石燃料) 碳排放,即污水、污泥处理全过程涉及的能耗;以及药耗碳排放,指污水处理所用碳源、除磷药剂等在生产与运输过程中形成的碳排放。
在污水、污泥处理过程中,直接产生的CH4、N2O是节能减排中应重点关注的物质。控制污水处理过程中产生的CH4有2种方式:一是严防其从污泥厌氧消化池中逃逸,二是在污水处理其他单元及管道中避免沉积物聚积的死角,也要注意沉砂池 (需选用曝气沉砂池或旋流沉砂池) 去除沙粒表面有机物是否被撇除干净。对N2O的控制则比CH4显得难度要大,N2O主要产生于硝化和反硝化过程。目前,有关N2O形成的机理研究已渐清晰,硝化过程是N2O形成的主因,反硝化过程对N2O形成的作用为次因[16-17]。根据N2O产生机理,提高硝化过程溶解氧 (DO) 浓度,增加反硝化过程有效碳源量有助于抑制N2O的形成[18-20],然而这势必会增加碳排放量。
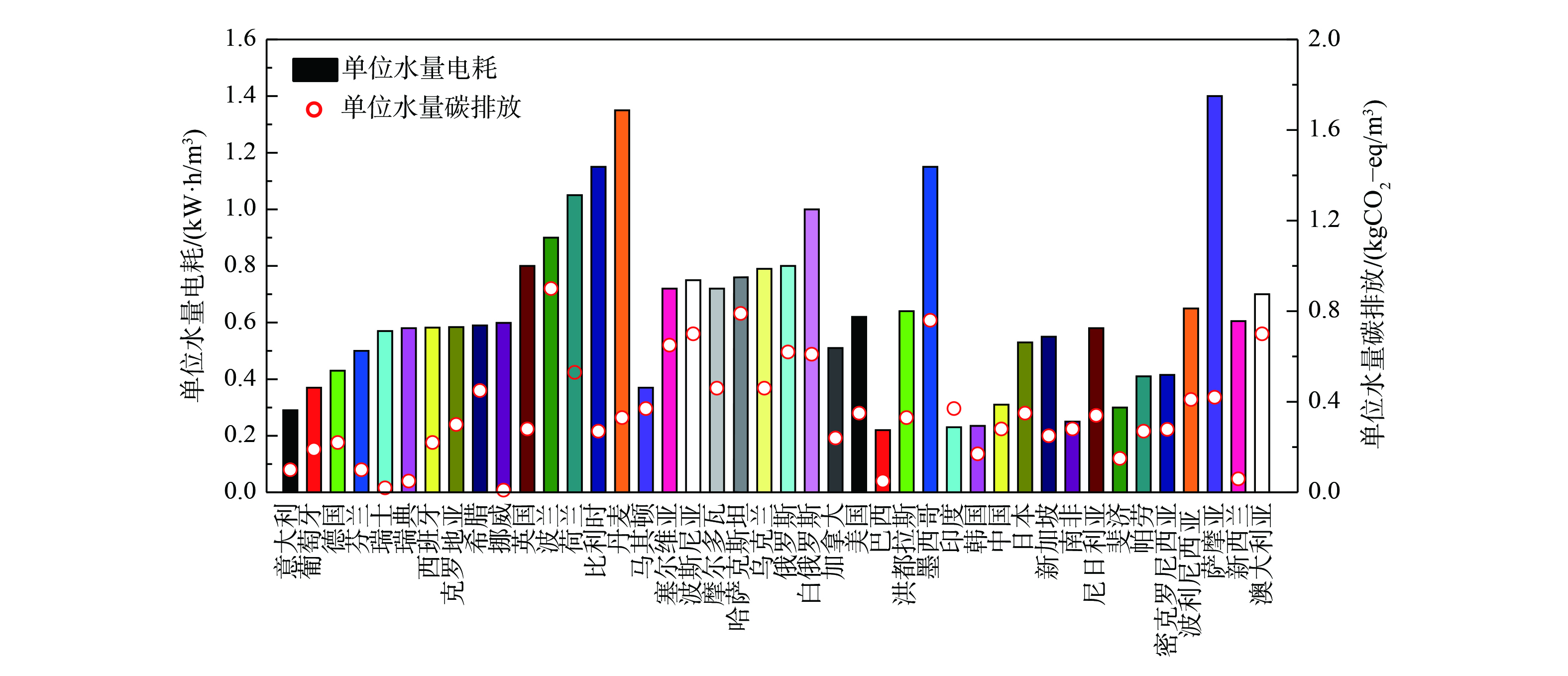
间接排放主要是能耗和药耗。由于在污水处理厂运行种最直接反映的是能耗,而药耗形成的碳排放一般在污水处理以外的行业 (化工、运输等) 产生 (但应计入污水处理碳排放清单) ,故污水处理厂并不关心。图1为不同国家污水处理能耗以及所对应的碳排放量[21]。不同地区能耗差异较为明显,但大数国家的处理能耗为0.5~0.6 kW·h·m−3;我国平均处理能耗为0.31 kW·h·m−3,巴西和印度处理能耗仅有0.22 kW·h·m−3,而丹麦、比利时、萨摩亚 (1.4 kW·h·m−3) 等国家污水处理平均能耗超过1.0 kW·h·m−3。然而,碳排放量结果显示,瑞士、巴西单位水处理碳排量最低,仅为0.05 kg CO2-eq·m−3,墨西哥最高,达0.76 kg CO2-eq·m−3,我国则处于中等水平 (平均值约0.28 kg CO2-eq·m−3)。高能耗一般伴随着那里有着严格的出水排放标准。图1表明,上述高能耗国家碳排放量水平却处于与我国一样的中等水平 (≤0.4 kg CO2-eq·m−3) 。这说明以上国家的污水处理大都利用了污泥厌氧消化与热电联产、甚至余温热能等清洁能源利用方式,从而抵消了一部分碳排放量。
药耗碳排放因工艺本身使用的药剂所产生,因此,应考虑减少碳源与化学除磷药剂投加量,以减少此类间接碳排放。因此,强化生物脱氮除磷技术以减少对碳源和药剂的依赖,将是今后污水处理的主流。如德国Bochum-Ölbachtal污水处理厂通过对原有前置反硝化工艺进行改造,不仅出水可满足严格排放标准,而且能耗也从原来的0.47 kW·h·m−3降至0.33 kW·h·m−3[9]。
另外,通过模型软件对工艺流程进行优化,或基于在线数据实现实时的参数调整也可实现污水处理工艺的节能降耗。欧盟开发“ENEWATER”项目,用于污水处理厂能量在线平衡分配。该项目可采用模糊逻辑、人工神经网络及随机森林等机器学习技术,对实际污水处理厂的水泵、鼓风机等设备进行优化,可不同程度降低污水处理厂运行能耗,最高节能可达80%[22]。然而,“零能耗”的污水处理工艺是很难实现的,除非采用基于自然的处理系统 (nature-based solutions,NBS) 。因此,仅仅靠节能降耗这种间接碳减排方式,尚不能完全实现碳中和运行的目标。
2) 污泥厌氧消化产CH4以实现能源转化。在碳中和目标提出后,剩余污泥的厌氧消化重获关注。上述从污水中获取有机 (COD) 能源来弥补污水处理中的能耗,成为实现碳中和目标的有效思路。然而,污泥厌氧消化所能回收的有机能量取决于进水中有机物浓度 (BOD/COD) 的多寡及厌氧消化有机物能源转化效率[23],尚不能完全照搬。
因生活水平、食物结构、无化粪池设置等原因,欧美等国家地区污水处理厂的进水COD普遍高于我国,COD大于600 mg·L−1的情况非常普遍。因此,通过初沉池以悬浮固体 (suspended solid,SS) 形式截留大部分COD,以及剩余污泥厌氧共消化并热电联产可获得较高的有机能源转化率。另外,以上通过污泥厌氧消化并热电联产实现碳中和案例大多还通过外源有机物添加 (厨余垃圾或食品废物) 以保证入水有机物的浓度,从而保证其实现碳中和运行目标[3,24]。然而,我国市政污水的进水COD普遍偏低,COD一般为100~300 mg·L−1,甚至难以满足基本脱氮除磷对碳源的需求,以至于为保留碳源而不设初沉池已成为主流工艺设计思路。这也使得仅依靠剩余污泥厌氧消化转化有机能源无法实现碳中和运行目标,即使存在热水解等手段强化污泥厌氧消化,在最佳运行状况下也难突破50%CH4的增产量[25]。
表1为几个污水处理厂污泥有机能源回收过程中COD平衡数据,展示了污泥厌氧消化有机能源转率。数据表明,进水COD中有机能最终只有不到15%可通过厌氧消化与热电联产转化为电或热。如进水COD为400 mg·L−1 (理论电当量1.54 kW·h·m−3) 的市政污水在完成脱氮除磷目的后所产生的剩余污泥经中温厌氧消化产CH4并热电联产,转化率仅13%,即实际转化电当量仅为0.20 kW·h·m−3[23,26]。
3) 与污水处理相关的清洁能源工艺。既然仅靠节能降耗和污泥厌氧消化并热电联产很难实现碳中和目标,那可考虑通过吸收/捕捉CO2 (如植树造林) 或在污水处理工艺或厂区使用清洁能源来达到碳减排目的。因此,传统意义上的可再生能源成为首要选择。近年来,微型发电机、光伏能、风能等新型能源用于英国、土耳其和澳大利亚等国的污水处理厂,产生的新能源大约可弥补7%~60%的污水处理厂能耗。POWER等[30]将微型发电机技术成功用于英国和爱尔兰等国的污水处理厂,产生约50%的电能,用于弥补厂区能耗。澳大利亚的污水处理厂充分利用太阳能、风能和污水水力发电技术,最终产生能源可满足该水厂69%的运行能耗[6]。希腊的克里特岛某污水处理厂利用光伏发电项目减排25%、风力发电环节减排25%、人工种植林固碳减排至少30%,并辅以污泥厌氧消化能源回收方来实现碳中和目标[5]。
具有可行性清洁能源还有太阳能。然而,受限于污水处理厂的地理位置、自然环境 (光照、风速) 等条件,经详细测算,即使将太阳能光伏发电板铺满整个污水处理厂最多也只能弥补约10%的污水处理能耗[26],距离碳中和目标仍有差距。
4) 通过余温热能利用回收能源的相关技术。污水中被忽视的另外一种潜能——水热 (余温热能) 实际上潜力巨大,可通过热交换 (水源热泵) 方式回收并加以利用[23,26]。污水余热 (<30 ℃) 排放约占城市总废热排放量的40%,且其流量稳定,具有冬暖夏凉的特点[31-32]。
热能衡算表明,若提取处理后出水4 ℃温差,实际可产生1.77 kW·h·m−3电当量(热)和1.18 kW·h·m−3电当量(冷)[23]。这是上述实际可转化有机能 (0.20 kW·h·m−3) 的9倍,亦表明有机能与热能分别为污水总潜能的10%和90% [23,29,33]。因此,污水余温热能蕴含量巨大,不仅能完全满足污水处理自身碳中和运行 (案例污水处理平均能耗约0.37 kW·h·m−3) 需要,而且还有更多余热 (约85%) 可外输供热或自身使用 (如用以进行污泥的低温干化) ,能形成大量可进行碳交易的碳汇。
污水热能的有效利用可使污水处理厂转变成“能源工厂”。芬兰Kakolanmäki污水处理厂的案例[12]表明,该厂2020年的总耗能为21.0 GWh·a−1,通过热能回收等主要手段使能源回收总量高达211.4 GWh·a−1,产能几乎为运行能耗的10倍。其污泥厌氧消化产能仅占3.7%,只能满足36.8%的运行能耗 (0.31 kW·h·m−3) ,而余温热能回收占比达95%。
-
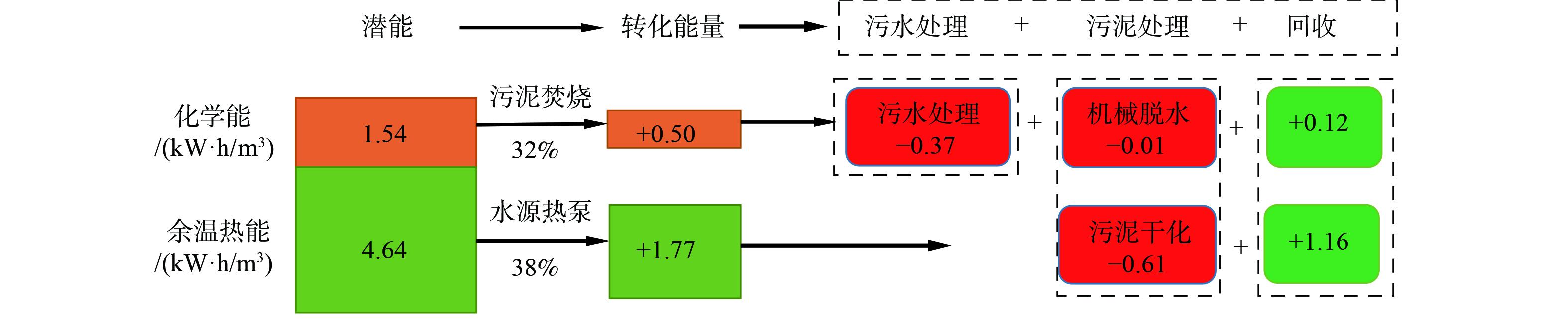
现有研究表明,污泥厌氧消化有机能源转化率普遍不高,仅靠此路径很难实现碳中和目标,且厌氧消化至少还有50%有机质需进行进一步的稳定处理[23-24,27],因此,在污泥处理中跳过厌氧消化,而直接干化、焚烧污泥应该是污泥处置与能源回收的上策[34],也成为国内外普遍采用的方法。前文提及的进水COD为400 mg·L−1的案例[23,26],若采用直接干化焚烧工艺来处理污泥,其有机能转化率可升至0.50 kW·h·m−3 (电当量) ,远远高于厌氧消化的0.20 kW·h·m−3,扣除污水处理厂运行能耗 (0.37 kW·h·m−3) 后,可盈余电当量0.12 kW·h·m−3。若再进一步考虑出水的热能利用,按上述热能实际转化计算,水源热泵提取4 ℃温差后,可获得热能1.77 kW·h·m−3 (电当量) ,再扣除污泥干化能耗0.61 kW·h·m−3,可盈余热能1.16 kW·h·m−3 (电当量) (见图2) 。因此,污泥焚烧热能与余温热能回收可实现污水处理自身能源中和、甚至碳中和运行,还可使其变成能源工厂,向社会输电、供热。
以上案例表明,污水处理仅靠节能降耗难以实现碳中和,还应通过开源来达到目标。利用光伏发电、剩余污泥化学能厌氧消化回收与水源热泵余温热能回收方式,分别核算3种能量回收方式对运行能耗的贡献率。结果表明,若进水COD为400 mg·L−1,污水化学能通过厌氧消化产CH4并热电联产 (combined heat and power,CHP) 最多仅可弥补约一半的污水处理运行能耗,剩余一半能量赤字仍需靠其他途径来补充。若利用出水余温热能,仅需要<10%热能或<15%冷能交换 (通过碳交易) 便可弥补能量赤字,间接实现碳中和目标。剩余约90%热能或85%冷能则可用于周边建筑物空调、温室供暖等,以减少外部的化石能源 (煤电、油电) 消耗。相比之下,光伏发电可获得的能量则显得有些“微不足道”,最多也就能提供<10%的运行能耗。因此,污水处理厂若考虑余温热能回收不仅可实现碳中和运行目标,亦可向厂外供热/冷,从而实现向能源工厂的转变。这种认知在颠覆传统能量利用观念的同时,也揭示了污水化学能的利用局限,表明可将COD的利用向高附加值产品 (如藻酸盐、PHA等) 资源化方向转变,而无需再去刻意强调污泥厌氧消化产CH4[23]。
余温热能的回收与应用并无障碍,唯一的设备水源热泵已较成熟。热能利用的最大问题是这是一种低品位热能 (60~80 ℃) ,只适合热量的直接利用,尚不能用于发电。在作为热源外输冬季供暖时,较低的水温又决定了热量的有效输送半径不能太大,仅适用于3~5 km的输送半径。而且在余温热能的实际利用中,政府部门的决策与规划最为重要。个别北欧国家的作法值得借鉴,其热能利用已涵盖建筑供暖、温室加温、人工养鱼等多个方面。如瑞典首都斯德哥尔摩建筑物中有40%采用水源热泵技术供热,其中10%热源来自污水处理厂出水[35];芬兰Kakolanmäki污水处理厂对出水余温热能予以回收利用,并向图尔库市居民供热、制冷,形成了大量碳汇[12-13];荷兰于2021年在乌特勒支De Stichtse Rijnlanden污水处理厂建成25 MW水源热泵系统,为周边10 000户家庭提供供热服务[36]。奥地利学者通过全生命周期影响评价 (life cycle impact assessment, LCIA) 方法得出,该国总共173个污水处理厂中约3/4的出水潜热可被利用,并在厂区周围有稳定的热源用户[37]。
尽管对污水处理厂余温热能的近距离外输利用可大大提高工艺的能耗利用,然而在现状难以调整的已规划区域,若外部无法利用这部分热能,则只能在污水处理厂内部进行利用。如将余温热能可原位用于低温干化污泥,随后将污泥集中运送至具有邻避效应的焚烧厂集中焚烧利用。这样便可将不能发电的低品位热能间接转化为可高温发电的高品位热能[34,38-40]。另外,在冬季寒冷的北方城市,还可考虑用出水余温热能加热前端进水,以确保在冬季维持生物处理效率。
-
“碳中和”已成为的热词。污水处理厂固然可通过节能降耗、污泥厌氧消化、太阳能源等方式很大程度上减少碳排放量。然而,由于我国污水存在有机质含量低的特点,要通过这些常规手段实现真正的碳中和目标差距较大。尽管污水余温热能的利用是使污水处理厂转型为“能源工厂”的有效手段,但在我国污水余温热能尚未被视为清洁能源,更未被列入碳交易清单。因此,除了在常规“降碳”技术上下功夫,还应在管理层面,从整个污水处理领域的整体规划、污水处理厂的设计布局,以及碳汇政策等多方面着手,来选择适合我国国情的污水处理厂碳中和路径。
污水处理行业实现碳中和的路径及其适用条件分析
Analysis on the path and applciable conditions of carbon neutrality in wastewater treatment industry
-
摘要: 节能降耗、厌氧消化产甲烷、工艺相关的能源利用等策略可有助于碳减排,但这些常规方法的潜力距碳中和目标仍有相当距离。国外诸多案例表明,污水余温热能利用技术是污水处理领域实现碳中和运行的可行方案。在总结污水处理领域碳减排策略的基础上,评价分析其对碳中和的贡献。通过对国内案例计算分析余温热能潜力并与有机 (COD) 能转化率进行比较发现,污水中蕴含的余温热能潜力为有机能的9倍。余温热能利用可使污水处理厂达到碳中和目标,还可将剩余热能 (约75%~85%) 向外以供热/制冷形式输出,或用于原位低温干化污泥,实现污水处理厂向“能源工厂”的转型。Abstract: Strategies such as energy conservation, anaerobic digestion and methanogenesis, and process-related energy use can contribute to carbon emission, but the potential of these conventional approaches is still far from carbon neutrality. Many cases abroad indicated that waste water heat energy utilization technology was a feasible scheme to achieve carbon neutrality in wastewater treatment. Based on the summary of carbon reduction strategies in the field of wastewater treatment, the contribution to carbon neutrality was evaluated and analyzed. By calculating and analyzing the waste heat energy potential of domestic cases and comparing with the conversion rate of organic energy (COD), it was found that the waste heat energy potential contained in sewage was 9 times that of organic energy. The use of residual heat energy can make the waste water treatment plants (WWTP) achieve carbon neutrality, and also export the residual heat energy (about 75% ~85%) outward for outside heating/cooling, or for in situ low temperature desiccating sludge to realize the transformation of WWTP into “energy plants”.
-
湖泊、水库是我国重要的饮用水源,且不少水体都存在不同程度的富营养化问题。当富营养水体发生“水华”时,造成水质恶化[1]。水源水中有害藻华(HABs)因其对水生态系统安全和人类健康产生了负面影响,引起了全世界的关注[2-3]。作为淡水中最普遍的蓝藻之一,铜绿微囊藻(Microcystis aeruginosa)具有生长繁殖的生态优势,在富营养化水体中成为优势藻种影响水质[4]。藻类种群密度在藻华季节的急剧增加严重影响了水处理过程的效率[5]。混凝作为一种常规处理方式,也常用于处理含藻水体工艺中[6]。原水水质是影响混凝效果的最主要因素之一,不同的原水水质,水中污染物含量、成分、pH、碱度等差异将直接影响混凝剂种类的选择和投加量[7-8]。藻华暴发将导致水体pH、碱度等异常升高,水体中的pH甚至可达到9~10,碱度会高于120 mg·L−1。而原水的碱度过高会对混凝过程产生不利影响,尤其是对于铝盐混凝剂,可能会产生出水余铝含量超标的问题[9-10]。
因此,本研究以氯化铝作为混凝剂,以铜绿微囊藻为研究对象,通过投加不同浓度的碳酸氢钠溶液来调节水样的碱度,考察了碱度对混凝去除藻细胞的性能影响,以期为处理富营养化水体和保证饮用水水质提供参考。
1. 实验材料和方法
1.1 实验试剂
氯化铝(AlCl3·6H2O)、碳酸氢钠(NaHCO3)、硝酸钠(NaNO3)、氢氧化钠(NaOH)、盐酸(HCl)均购自国药集团化学试剂有限公司。
1.2 藻种培养
铜绿微囊藻(PCC7820),购自中国科学院水生生物研究所,采用BG11培养基进行培养,无菌条件下接种至锥形瓶中,放在人工气候培养箱中培养,培养条件为温度(25±1) ℃、光照强度2 000 lx、光暗比(L∶D)=12 h∶12 h。定期进行细胞计数,绘制生长曲线,待藻种达到稳定期后用于实验。
1.3 水样配制
为了模拟蓝藻暴发时水体中的藻细胞浓度,控制水样藻细胞密度为1×106个·mL−1[11],并加入5. 0 mmol·L−1NaNO3提供离子强度。由于饮用水中只含有碳酸氢根碱度,故在此实验中只考虑调节碳酸氢根碱度[12-14]。配制0. 5 mol·L−1NaHCO3溶液,在500 mL稀释好的藻液中分别加入0、1.0、2.0、2.5、3.5、4.5 mL溶液,制成总碱度(以CaCO3计)分别为50、95、175、245、330、415 mg·L−1的水样,使用盐酸(0. 1 mol·L−1) 和氢氧化钠(0. 1 mol·L−1)溶液调节水样pH。
1.4 实验方法
使用MY3000-6G智能型混凝搅拌仪(武汉梅宇有限公司)进行混凝实验,在200 r·min−1下快搅60 s,加混凝剂后,在200 r·min−1下快搅90 s,再在40 r·min−1下,慢搅10 min,静置沉淀30 min。在液面以下2.0 cm处取上清液,测定藻的吸光度及浊度。
利用马尔文激光粒度分析仪(Laser Particle Analyzer,Mastersizer2000,Malvern,UK)对混凝实验中絮体的形成过程进行在线监测,以D50代表絮体的平均粒径,并对已经形成的絮体进行破碎实验(5 min,200 r·min−1),随后进行絮体恢复实验(10 min,40 r·min−1),考察絮体的强度因子、恢复因子以及分形维数。
1.5 分析方法
藻细胞密度采用UV-8500紫外/可见分光光度计(上海天美公司)测定;浊度采用浊度仪(2100N,Turbidimeter,HACH,USA)测定;将水样经0.45 μm水相滤头过滤后,采用总有机碳分析仪(Shimadzu,Japan)测定DOC;pH采用pH计(MP220,pH Meter,Mettler-Toledo,Switzerland)测定;出水余铝采用电感耦合等离子-原子发射光谱仪(ICP-OES OPTIMA-2000,PerknELMER,US)测定;于混凝快搅结束后取样,采用Zeta电位仪(zetasizer2000,Malvern,UK)测定Zeta电位;混凝静沉后的底部絮体经高速冷冻离心机(Aantij26XP,Beckman Coulter.Inc.USA)冷冻干燥后采用扫描电子显微镜(HITACHI SU8020 FE-SEM,Japan)测定。
2. 结果与讨论
2.1 混凝剂投加量对混凝性能的影响
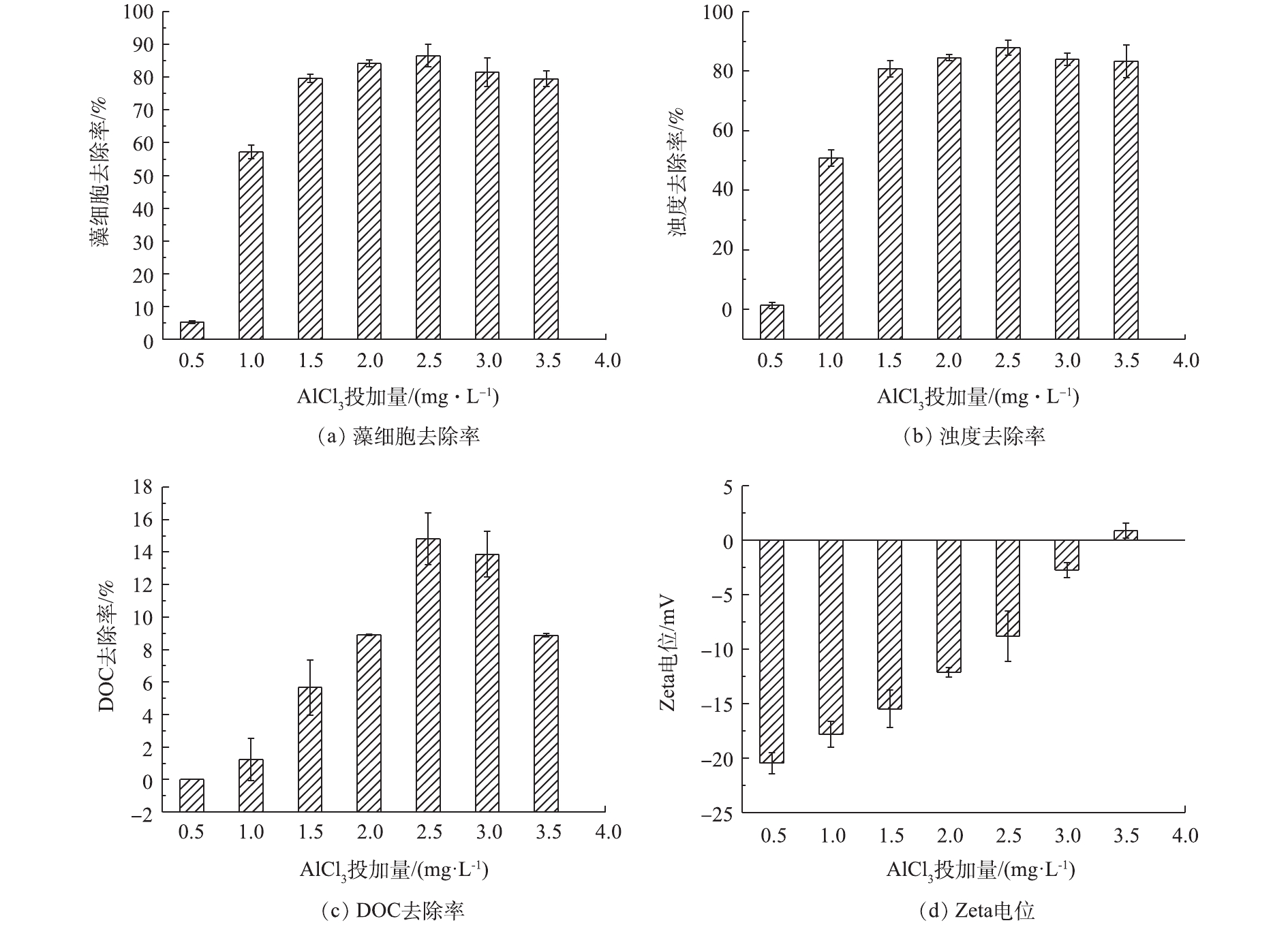
为探究混凝剂投加量对混凝效果的影响,考察了AlCl3(以Al计)投加量为0.5~3.5 mg·L−1、水样pH=7.5条件下藻细胞、浊度和DOC的去除率,结果见图1。由图1可见:当混凝剂投加量为0.5~2.0 mg·L−1时,藻细胞、浊度和DOC的去除率随着混凝剂投加量的增加而增加;当AlCl3投加量为2.5 mg·L−1时,藻细胞、浊度和DOC的去除率分别达到了86.52%、87.95%和14.80%;当投加量增大至3.5 mg·L−1时,藻细胞、浊度和DOC的去除率均有所降低。这主要是因为:当混凝剂投加量为0.5~2.0 mg·L−1时,投加量不足,导致电中和能力受到抑制,因此,藻细胞、浊度和DOC的去除率均不高;当混凝剂投加量过大时,体系中的胶体颗粒由于带有过高的正电荷而出现复稳现象,部分颗粒物难以聚集形成絮体而被去除,导致混凝效果下降。
2.2 不同碱度对混凝性能的影响
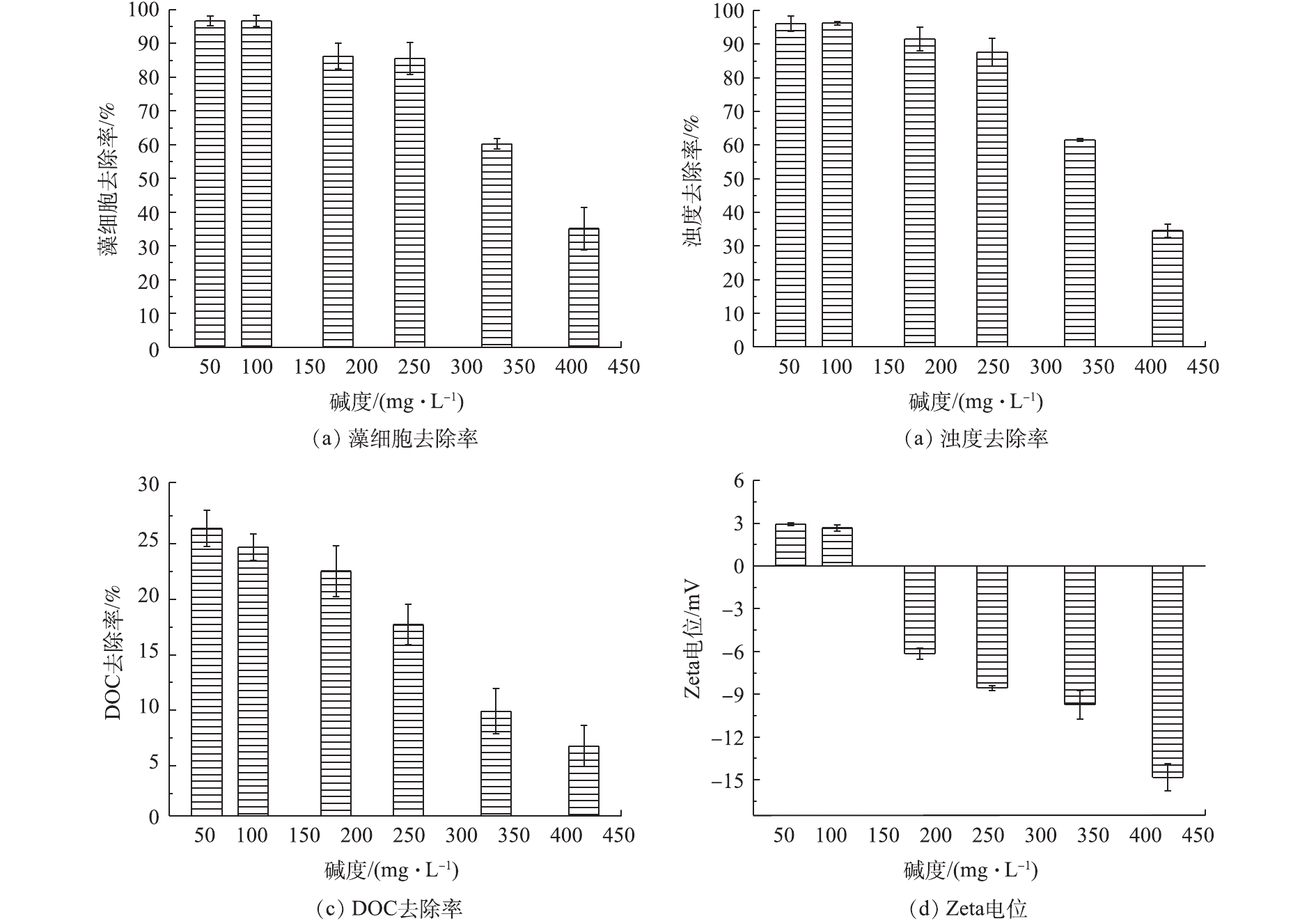
为探究碱度对混凝性能的影响,考察了各碱度含藻水样在AlCl3投加量为2.5 mg·L−1、pH=7.5条件下的藻细胞、浊度和DOC的去除率,结果见图2。由图2可知,随着碱度的增加,藻细胞、浊度、DOC的去除率以及Zeta电位值均呈下降趋势。藻细胞的去除率由96.65%降低至35.12%,浊度的去除率由96.12%降低至34.55%,有机物的去除率由24.61%降低至15.26%。同时也可以看到,随着碱度的增加,Zeta电位由2.67 mV降低至-14.83 mV。分析其原因在于,当水样pH=7.5、碱度为50~245 mg·L−1时,水样中主要存在Al(OH)3活性溶胶和一些具有较高聚合度的带正电水解产物,其可通过黏附架桥、网捕卷扫等作用达到较好的混凝效果[15],导致藻细胞、浊度和DOC的去除率较高。随着碱度的增加,负离子形态的
Al(OH)−4 占据优势,与带负电荷的铜绿微囊藻细胞之间产生了静电排斥,导致混凝效率下降[16],Zeta电位值也逐渐减小。2.3 pH对不同碱度含藻水混凝性能的影响
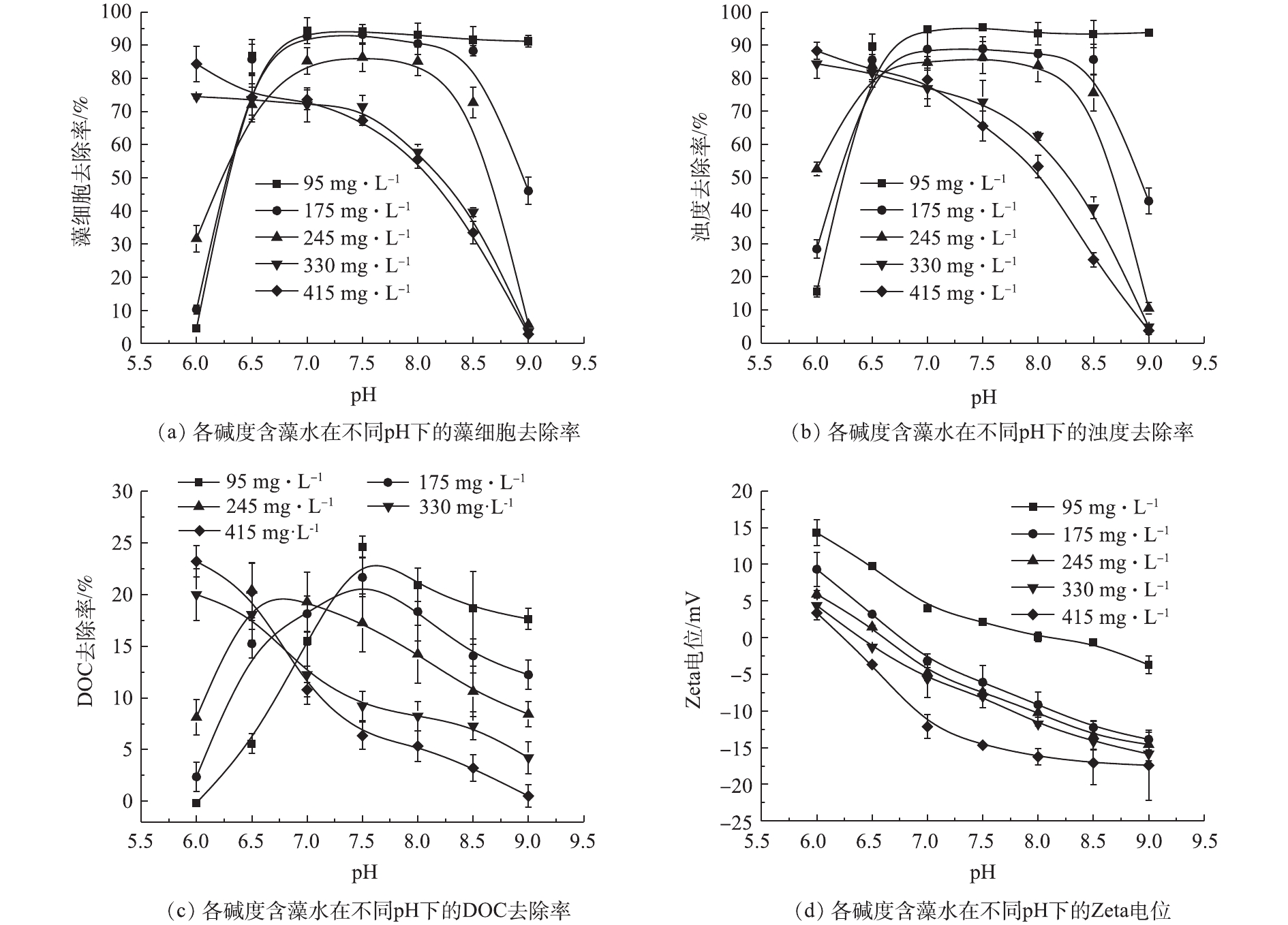
碱度和pH共同决定铝盐投加后的水解形态,进而影响混凝性能[17]。因此,可通过调整pH缓解碱度对混凝性能的影响,结果如图3所示。由图3可知:当碱度为95 mg·L−1和175 mg·L−1、pH=6.0时,藻细胞的去除率分别为4.59%和10.27%,在相同碱度条件下,当pH=6.5~8.5时,藻细胞的去除率在88.30%以上;当碱度为245 mg·L−1、pH=7.0~8.0时,藻细胞的去除率达到86.31%,当pH=6.0、9.0时,藻细胞的去除率均在31.64%以下;在碱度为330 mg·L−1和415 mg·L−1时,随着pH的增大,藻细胞的去除率呈下降的趋势,分别由74.45%和84.32%降低至3.56%和2.81%。浊度的去除率和藻细胞的去除效果一致。DOC的去除率虽然不高,在25%以下,但与藻细胞和浊度的去除率趋势一致。
分析原因在于,当水样的pH=6.0时,随着碱度的增加,Zeta电位绝对值逐渐减小,趋于等电点状态,体系的稳定性逐渐减弱,电荷排斥力逐渐下降,有助于絮体形成,有利于混凝过程进行,因此,导致藻细胞、浊度以及有机物的去除率增加。当水样的pH=6.5、碱度为95、175、245 mg·L−1时,混凝过程主要依靠吸附架桥和网捕卷扫协同作用,形成较大絮体,絮体沉降性好,去除率增加。当水样的pH=7~9、碱度为95 mg·L−1时,Zeta电位值趋近于0,体系趋于失稳状态,颗粒间的排斥力降低,藻细胞和浊度的去除率趋于稳定。而在其他各碱度下,随着pH的增大,铝盐混凝剂发生过度水解反应,生成的
Al(OH)−4 负离子增多,网捕卷扫作用减弱,且系统脱稳困难,不利于混凝过程的进行[18-20],所以藻细胞、浊度和DOC的去除率逐渐下降。在各碱度下,体系Zeta电位值均随pH的增大而降低,这是因为藻细胞本身的Zeta电位值会随着pH的增大而降低;水样pH对铝盐的水解形态分布也会影响体系的Zeta电位值;在相同pH下,碱度越高,带正电荷的铝盐水解产物越少,从而也会降低体系的Zeta电位值。综上所述,通过调节水样的pH,可以达到减缓碱度影响混凝过程的目的。当体系碱度较低时,可将pH调整至中性范围,以提高藻细胞的去除率;当体系碱度过高时,可以调节水样pH,从而使体系Zeta电位的绝对值趋近于0,打破体系稳定状态,进而有利于混凝过程的进行。
2.4 絮体特性
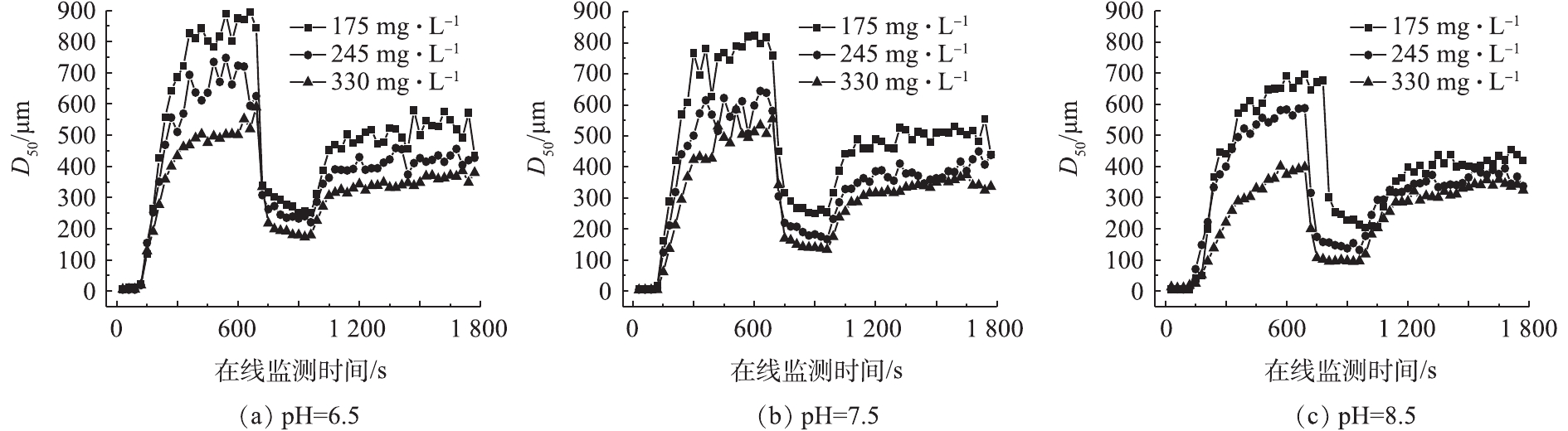
由于絮体的大小和强度对于分离过程有重要影响,因此,在大多数水处理过程中,絮体特性被当作是一个重要的操作参数[21],混凝过程絮体粒径变化情况如图4所示。
由图4可以看出,在相同pH条件下,随着碱度的增加,平衡时的絮体粒径逐渐减小。当pH=7.5、碱度为175、245和330 mg·L−1时,平衡时絮体粒径分别为811.02、633.28和540.62 μm。分析原因在于,在水样pH一定的条件下,碱度较低时,混凝过程依靠吸附架桥和网捕卷扫协同作用,形成粒径较大的絮体。随着碱度的增加,铝盐的水解产物Al(OH)3胶体更多转变为
Al(OH)−4 ,絮体间排斥能力增强,不利于颗粒聚集生成,故导致平衡时的絮体粒径减小。为了更好地了解不同条件下混凝形成絮体的特性,对强度因子(Sf)和恢复因子(Rf) (表1)以及分形维数(Df)[22](表2)进行了计算。
表 1 各碱度含藻水样在不同pH条件下形成絮体的强度因子和恢复因子Table 1. Strength factors and recovery factors of flocs formed in algae-laden water sample with different alkalinity at different pHspH 碱度为175 mg·L−1 碱度为245 mg·L−1 碱度为330 mg·L−1 强度因子/% 恢复因子/% 强度因子/% 恢复因子/% 强度因子/% 恢复因子/% 6.5 37.41 30.12 32.98 38.97 25.95 39.20 7.5 35.97 35.31 32.29 44.42 24.79 47.88 8.5 34.19 47.68 27.39 45.86 21.17 73.99 表 2 各碱度含藻水样在不同pH条件下形成絮体的分形维数Table 2. Fractal dimension of flocs formed in algae-laden water sample with different alkalinity at different pHspH 碱度为175 mg·L−1 碱度为245 mg·L−1 碱度为330 mg·L−1 平衡时 破碎后 再生长后 平衡时 破碎后 再生长后 平衡时 破碎后 再生长后 6.5 1.744 1.916 1.908 1.591 1.756 1.734 1.584 1.748 1.704 7.5 1.586 1.733 1.718 1.516 1.694 1.63 1.372 1.554 1.503 8.5 1.550 1.704 1.677 1.432 1.615 1.551 1.25 1.434 1.395 由表1可知,在相同pH条件下,随着碱度的增加,絮体的强度因子逐渐减小,恢复因子逐渐增大。当水样pH=7.5时,随着碱度的增加,絮体强度因子由35.97%降低至24.79%,恢复因子由35.31%增加至47.88%。强度因子逐渐减小的原因为:在相同pH条件下,碱度较低时,网捕卷扫在混凝机理上占主导地位,体系中有足够的Al(OH)3胶状沉淀,会促使形成比较密实的絮状结构[23],相应的强度因子就大;随着碱度的升高,铝盐水解生成的无定型Al(OH)3胶状沉淀逐渐转变为
Al(OH)−4 ,Al(OH)3胶状沉淀减少,导致网捕卷扫作用减弱,形成的絮体变得疏松,相应的强度因子就减小。恢复因子逐渐增大的原因在于,当网捕卷扫在混凝机理上占主导地位,破碎的絮体颗粒带正电荷[24],这些破碎的絮体颗粒可以继续吸附水样中的残余颗粒物。在水样pH一定的条件下,碱度较低时,藻细胞和有机物的去除率高,水样中残余颗粒物就少,在一定时间内与破碎的颗粒物碰撞概率小,因此,絮体恢复因子小;而碱度较高时,平衡时絮体粒径小,而且由于藻细胞去除率低,水样中还有大量的颗粒物,这就增大了与破碎絮体的碰撞概率,一定时间内破碎絮体吸附中和这些颗粒物使粒径再次增大,因此恢复因子也增大。由表2可以看出:在相同pH条件下,随着碱度的增加,平衡时絮体的分形维数逐渐减小;同一碱度下,随着pH的增加,平衡时絮体的分形维数也逐渐减小。当水样pH=7.5时,随着碱度的增加,平衡时絮体的分形维数由1.586减小到1.372;当碱度为245 mg·L−1时,随着pH的增加,平衡时絮体的分形维数由1.591降低至1.432。分析原因在于:当pH和碱度较低时,网捕卷扫占主导地位,形成的絮体结构更为致密,相应的分形维数就较高[25];随着碱度的增加,铝盐水解生成的Al(OH)3胶状沉淀逐渐转变为
Al(OH)−4 ,网捕卷扫作用减弱,胶体颗粒间的静电斥力增加,因此,形成的絮体结构变得疏松,相应的分形维数较低[26]。2.5 扫描电镜分析
由图5可知,水样pH和碱度的不同导致混凝过程的作用机理不同,而不同混凝机理形成的絮体结构是有差异的。当水样pH和碱度较低时,形成的絮体更为致密,而当水样pH和碱度较高时,形成的絮体相对疏松。这主要是因为,在水样pH和碱度不同的情况下,形成的絮体粒径和分形维数不同。水样pH和碱度较低时,混凝过程依靠吸附架桥和网捕卷扫协同作用,形成絮体的分形维数大,絮体结构更为密实,絮体沉降性好,所以混凝效果较好;随着水样pH和碱度的增加,
Al(OH)−4 逐渐增多,致使网捕卷扫作用减弱,絮体间排斥能力增强,因此,分形维数逐渐减小,絮体结构越来越疏松,形成的絮体表面粗糙且多孔,而且絮体粒径小,沉降性差,导致混凝效果减弱。2.6 出水余铝
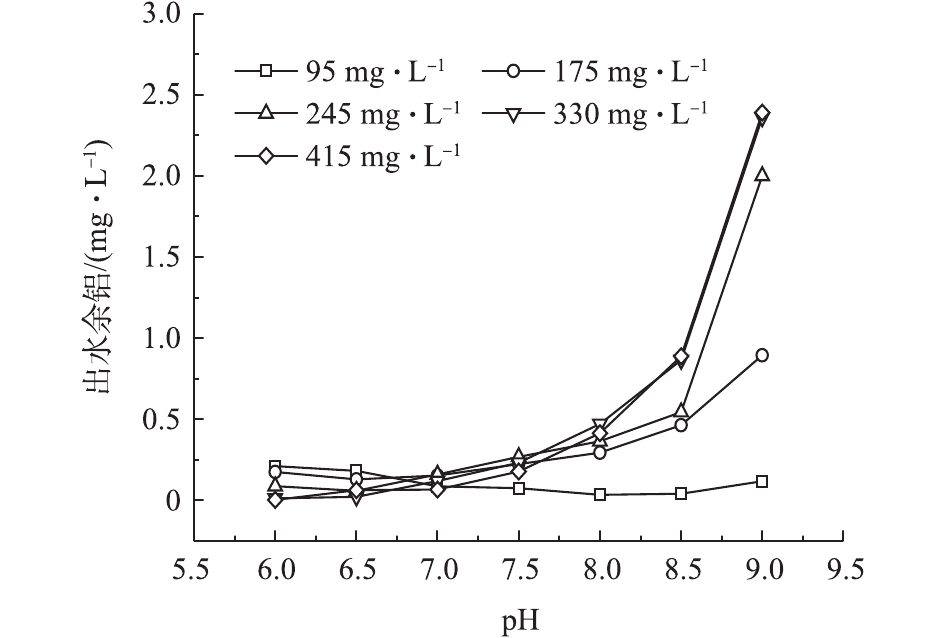
水样的碱度过高会导致使用铝盐混凝剂的残留铝含量增加,因此,实验对比了各碱度含藻水在不同pH条件下的出水余铝,结果如图6所示。可以看出:当碱度为95 mg·L−1、pH为6.0~8.0时,出水余铝从0.212 0 mg·L−1降低至0.035 3 mg·L−1。这是因为混凝效果逐渐增强,沉后出水中的溶解态铝含量降低,所以出水余铝减少。在其他碱度下,随着pH的增大,出水余铝均有所增加,且在相同pH下,随着碱度的增加,出水余铝也呈升高的趋势,当pH=9.0时,碱度为245、330和415 mg·L−1对应的出水余铝分别为2.030、2.360和2.390 mg·L−1。这是因为随着pH和碱度的升高,铝离子水解形成的 Al(OH)3胶状沉淀会溶解为负离子
Al(OH)−4 ,导致出水余铝含量升高。2.7 反应体系出水pH
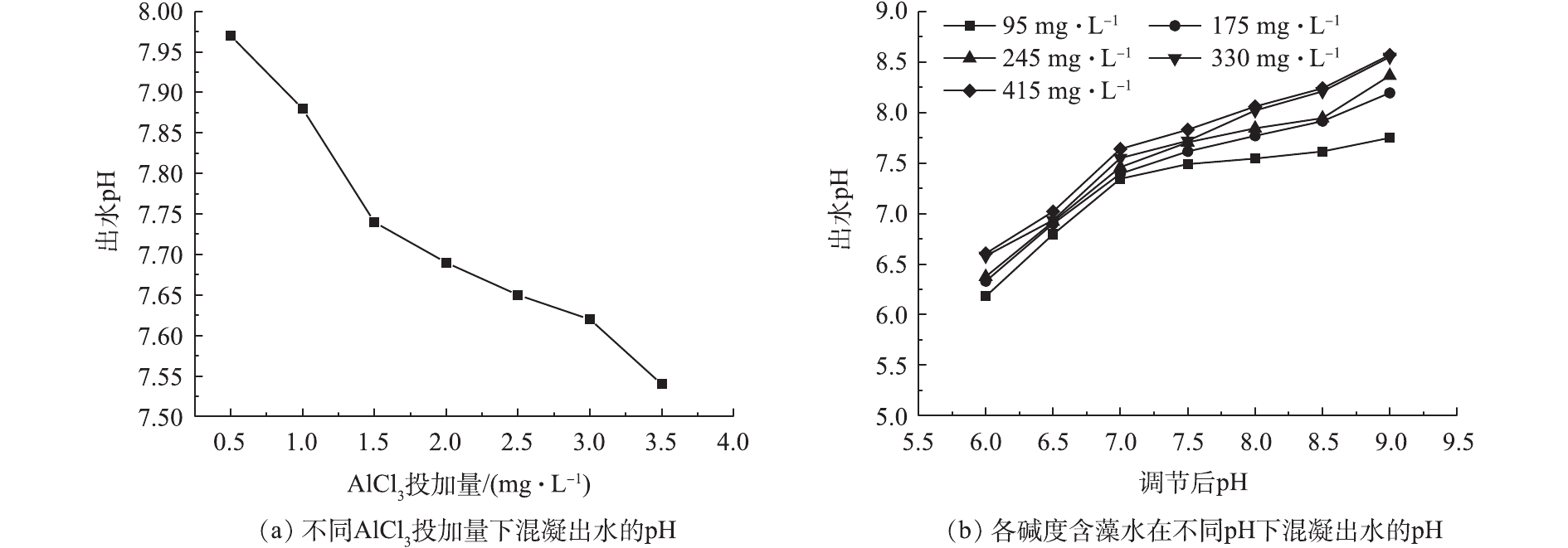
本研究对不同AlCl3投加量和各碱度含藻水在不同pH条件下混凝出水的pH进行测定,结果如图7所示。如图7(a)所示,当pH=7.5、碱度为245 mg·L−1时,随混凝剂投加量增大,出水pH由7.97降低至7.54。这是因为铝盐水解过程中会产生H+,H+的积聚会使体系的pH有所降低,虽然
HCO−3 能吸收H+,使体系pH波动减小,但是因为体系中HCO−3 的量是有限的,因此,无法中和过多的H+,所以随着混凝剂投加量的增加,体系出水pH有所降低。如图7(b)所示,在调节后的pH相同条件下,出水pH随着碱度的增大而增大,这是因为在体系中投加的铝离子的量是有限的,铝盐水解产生的H+也就有限,而HCO−3 浓度是增加的,其水解产生的OH−逐渐增多,但是没有足够的H+来中和,因此,反应后的出水pH随着碱度的增大而升高。3. 结论
1)当水样pH=7.5、氯化铝投加量为2.5 mg·L−1、碱度为50、95 mg·L−1时,对于藻细胞和浊度的去除率均在96.50%左右,随着碱度的升高,对于藻细胞,浊度以及有机物的去除率均呈下降趋势,并且水样的Zeta电位值也逐渐降低。
2)通过调整水样pH,可有效缓解碱度对混凝过程的影响。当体系碱度较低时,可将pH调整至中性范围,提高藻细胞的去除效率,出水余铝含量也会降低;当体系碱度过高时,可通过调节pH使体系Zeta电位的绝对值趋近于0,打破体系稳定状态,从而有利于混凝过程的进行,出水残留铝含量也会有相应减少。
3)当水样pH≥6.5,碱度较低时,混凝过程依靠吸附架桥和网捕卷扫协同作用,形成的絮体粒径较大,而且絮体的结构较为致密,分形维数较大;随着pH和碱度的增加,絮体间排斥能力增强,不利于颗粒物的聚集生成,导致形成的絮体粒径较小,而且絮体结构比较疏松,分形维数逐渐减小。
-
-
[1] LARSEN T A. CO2-neutral wastewater treatment plants or robust, climate-friendly wastewater management? A systems perspective[J]. Water Research, 2015, 87: 513-521. doi: 10.1016/j.watres.2015.06.006 [2] JIM F. Encouraging energy efficiency in US wastewater treatment[J]. Water 21, 2011, 11(3): 32-34. [3] 郝晓地, 金铭, 胡沅胜. 荷兰未来污水处理新框架——NEWs及其实践[J]. 中国给水排水, 2014, 30(20): 7-15. doi: 10.19853/j.zgjsps.1000-4602.2014.20.002 [4] 郝晓地, 任冰倩, 曹亚莉. 德国可持续污水处理工程典范——Steinhof厂[J]. 中国给水排水, 2014, 30(22): 6-11. [5] 郝晓地, 程慧芹, 胡沅胜. 碳中和运行的国际先驱——奥地利Strass 污水厂案例剖析[J]. 中国给水排水, 2014, 30(22): 1-5. [6] 郝晓地, 魏静, 曹亚莉. 美国碳中和运行成功案例——Sheboygan污水处理厂[J]. 中国给水排水, 2014, 30(24): 1-6. [7] VOURDOUBAS J. Irrigation of tree plantations with treated sewage effluents and use of the produced biomass for pellets production—A case study in Crete-Greece[J]. Journal of Chemical Engineering and Chemistry Research, 2015, 2: 824-831. [8] ALI S M H, LENZEN M, SACK F, et al. Electricity generation and demand flexibility in wastewater treatment plants: benefits for 100% renewable electricity grids[J]. Applied Energy, 2020, 268: 114960. doi: 10.1016/j.apenergy.2020.114960 [9] MARNER S T, SCHRÖTER D, JARDIN N. Towards energy neutrality by optimising the activated sludge process of the WWTP Bochum-Ölbachtal[J]. Water Science and Technology, 2016, 73(12): 3057-3063. doi: 10.2166/wst.2016.142 [10] BEHÖRDE F U , Klima, energie und agrarwirtschaft. Abwasserreinigung des klärwerkverbundes köhlbrandhöft/dradenau in hamburg - welcome to the geoss information exchange datahub [EB/OL] (2019–06–20) [2021–07–12]. https://cloud.csiss.gmu.edu/uddi/en/dataset/abwasserreinigung-des-klarwerkverbundes-kohlbrandhoft-dradenau-in-hamburg. [11] VOURDOUBAS J. Creation of zero carbon emissions wastewater treatment plants-a case study in Crete, Greece[J]. Energy and Environment Research, 2018, 8(1): 64-72. doi: 10.5539/eer.v8n1p64 [12] Turun seudun puhdistamo Oy, Kakolanmäen jätevedenpuhdistamon Tarkkailututkimus Vuosiraportti 2020[EB/OL][2021-2-25]. https://www.turunseudunpuhdistamo.fi/. [13] 郝晓地, 赵梓丞, 李季等. 污水处理厂的能源与资源回收方式及其碳排放核算: 以芬兰Kakolanmäen污水处理厂为例[J]. 环境工程学报, 2021, 15(9): 2849-2857. doi: 10.12030/j.cjee.202106073 [14] 王向阳. 污水处理碳足迹核算及环境综合影响评价研究[D]. . 北京: 北京建筑大学, 2019. [15] IPCC. 2006 IPCC Guidelines for National Greenhouse Gas Inventories[M]. Japan: IGES, 2006. [16] KIM S W, MIYAHARA M, FUSHINOBU S, et al. Nitrous oxide emission from nitrifying activated sludge dependent on denitrification by ammonia-oxidizing bacteria[J]. Bioresource Technology, 2010, 101: 3958-3963. doi: 10.1016/j.biortech.2010.01.030 [17] TALLEC G, GARNIER J, BILLEN G, et al. Nitrous oxide emissions from secondary activated sludge in nitrifying conditions of urban wastewater treatment plants: Effect of oxygenation level[J]. Water Research, 2006, 40: 2972-2980. doi: 10.1016/j.watres.2006.05.037 [18] YU R, KAMPSCHREUR M J, VAN LOOSDRECHT M C M, et al. Mechanisms and specific directionality of autotrophic nitrous oxide and nitric oxide generation during transient anoxia[J]. Environmental Science & Technology, 2010, 44: 1313-1319. [19] 王淑莹, 委燕, 马斌, 等. 控制污水生物处理过程中N2O的释放[J]. 环境科学与技术, 2014, 37(7): 78-84. [20] 付昆明, 张晓航, 刘凡奇, 等. 葡萄糖碳源条件下C/N对反硝化和N2O释放性能的影响[J]. 环境工程学报, 2021, 15(4): 1279-1288. doi: 10.12030/j.cjee.202010137 [21] WANG H, YANG Y, KELLER A A, et al. Comparative analysis of energy intensity and carbon emissions in wastewater treatment in USA, Germany, China and South Africa[J]. Applied Energy, 2016, 184: 873-881. doi: 10.1016/j.apenergy.2016.07.061 [22] NAKKASUNCHI S, HEWITT N J, ZOPPI C, et al. A review of energy optimization modelling tools for the decarbonisation of wastewater treatment plants[J]. Journal of Cleaner Production, 2021, 279: 123811. doi: 10.1016/j.jclepro.2020.123811 [23] HAO X, LI J, VAN LOOSDRECHT M C M, et al. Energy recovery from wastewater: Heat over organics[J]. Water Research, 2019, 161: 74-77. doi: 10.1016/j.watres.2019.05.106 [24] 郝晓地, 李季, 曹达啟. 污水处理碳中和运行需要污泥增量[J]. 中国给水排水, 2016, 32(12): 1-6. doi: 10.19853/j.zgjsps.1000-4602.2016.12.001 [25] 郝晓地, 张璇蕾, 刘然彬, 等. 剩余污泥转化能源的瓶颈与突破技术[J]. 中国给水排水, 2014, 30(18): 1-7. doi: 10.19853/j.zgjsps.1000-4602.2014.18.001 [26] HAO X D, LIU R B, HUANG X. Evaluation of the potential for operating carbon neutral WWTPs in China[J]. Water Research, 2015, 87: 424-431. doi: 10.1016/j.watres.2015.05.050 [27] FERNÁNDEZ-ARÉVALO T, LIZARRALDE I, FDZ-POLANCO F, et al. Quantitative assessment of energy and resource recovery in wastewater treatment plants based on plant-wide simulations[J]. Water Research, 2017, 118: 272-288. doi: 10.1016/j.watres.2017.04.001 [28] SCHAUM C, LENSCH D, BOLLE P Y, et al. Sewage sludge treatment: evaluation of the energy potential and methane emissions with COD balancing[J]. Journal Water Reuse Desalination, 2015, 5: 437-445. doi: 10.2166/wrd.2015.129 [29] FRIJNS J, HOFMAN J, NEDERLOF M. The potential of (waste)water as energy carrier[J]. Energy Conversion Management, 2013, 65: 357-363. doi: 10.1016/j.enconman.2012.08.023 [30] POWER C, MCNABOLA A, COUGHLAN P. Development of an evaluation method for hydropower energy recovery in wastewater treatment plants: case studies in Ireland and the UK[J]. Sustain Energy and Technology, 2014, 7: 166-177. [31] CIPOLLA S S, MAGLIONICO M. Heat recovery from urban wastewater: Analysis of the variability of flow rate and temperature in the sewer of Bologna, Italy[J]. Energy Procedia 2014, 45, 288–297. https://doi.org/10.1016/j.egypro.2014.01.031 [32] ARIF H, EMRAH B, ORHAN E, et al. A key review of wastewater source heat pump (WWSHP) systems[J]. Energy Conversion and Management 2014, 88, 700–722. https://doi.org/10.1016/j.enconman.2014.08.065. [33] MCCARTY P L, JAEHO B, JEONGHWAN K. Domestic wastewater treatment as a net energy producer-can this be achieved?[J]. Environmental Science & Technology, 2011, 45(17): 7100-7106. [34] HAO X D, CHEN Q, VAN LOOSDRECHT M C M, et al. Sustainable disposal of excess sludge: Incineration without anaerobic digestion[J]. Water Research, 2020, 170: 115298. doi: 10.1016/j.watres.2019.115298 [35] AVERFALK H, INGVARSSON P, PERSSON U. Large heat pumps in Swedish district heating systems[J]. Renewable and Sustainable Energy Reviews, 2017, 79: 1275-1284. doi: 10.1016/j.rser.2017.05.135 [36] Heat pump at Utrecht sewage treatment plant. https://www.eneco.com/what-we-do/sustainable-sources/heat-pump-at-utrecht-sewage-treatment-plant/[EB/OL], 2020. [37] NEUGEBAUER G, STGLEHNER G. Realising energy potentials from wastewater by integrating spatial and energy planning[J]. Sustainable Sanitation Practice, 2015, 22: 15-21. [38] GROSS T S C. Thermal drying of sewage sludge[J]. Water Environment Journal, 2010, 7: 255-261. doi: 10.1111/j.1747-6593.1993.tb00843.x [39] MURAKAMI T, SUZUKI Y, NAGASAWA H, et al. Combustion characteristics of sewage sludge in an incineration plant for energy recovery[J]. Fuel Processing Technology, 2009, 90: 778-783. doi: 10.1016/j.fuproc.2009.03.003 [40] 郝晓地, 张益宁, 李季, 等. 污水处理能源中和与碳中和案例分析[J]. 中国给水排水, 2021, 37(20): 1-8. doi: 10.19853/j.zgjsps.1000-4602.2021.20.001 -






 下载:
下载: