-
长链二元酸是指碳链中含有10个以上碳原子的直链二元酸,结构通式为HOOC-(CH2)n-COOH(n=8~16),是一类有着重要和广泛工业用途的精细化工品。生物发酵法是长链二元酸的主要生产工艺,以正构烷烃(C10~C18)为原料,利用专性微生物进行生产。发酵液过滤设备的反冲洗过程和二元酸晶体的压滤过程会排放高浓度废水;二元酸滤饼的洗涤过程会排放低浓度废水。二元酸废水中残留二元酸盐及培养基成分,故其水质指标中总磷和COD非常高。总磷过高会导致石油化工企业综合污水处理厂(简称“污水处理厂”)无法将污水直接处理至达标;COD虽易被降解,但其负荷较大,会大幅增加污水处理厂生化处理单元的运行负荷。目前,二元酸废水处理多采用复杂组合工艺且多数未解决总磷超标问题。杨建等[1]采用“中和沉淀+SBR”工艺处理二元酸废水,COD去除率可达到90%,但未考虑总磷去除。汤贵兰[2]采用“中和沉淀+UASB+MBR”工艺处理二元酸废水可降解97%的COD,但未提及总磷超标问题。许莉等[3]采用“电解+纳滤”工艺能去除99%的COD,但总磷未满足达标排放要求。因此,亟需开发简单、经济、高效的预处理除磷技术以降低二元酸废水的总磷和COD,保障污水处理厂的稳定运行。
除磷方法主要有生物法、吸附法和化学沉淀法。生物除磷成本低,但耗时长、能耗高、除磷效率低且效果易受环境影响,通常适用于低含磷的城市污水处理工艺[4-5]。吸附法虽工艺简单,但其除磷效率不高。常用吸附剂有粉煤灰、沸石、凹凸棒石、海泡石等。吸附剂存在再生困难和再生后吸附性能下降等问题,使得该方法成本高且无法有效处理高浓度含磷废水[6-9]。化学沉淀法操作简单、反应迅速、除磷效率高,常被用于处理高含磷废水。常用除磷剂有铝盐、铁盐和钙盐3类。铝盐在水中可电离出Al3+并与PO43-反应生成AlPO4沉淀,反应如式(1)所示。PARK等[10]将氢氧化钠涂层包覆的铝渣用于去除真实废水中的磷酸盐并探究pH对除磷效果的影响时发现,在pH大于8的碱性条件下该方法的除磷效率稳定在60%。铁盐通过电离出的Fe3+与PO43-生成难溶盐[11-15],反应如式(2)所示。HANG等[16]发现铁盐作为除磷剂时还可刺激反硝化菌的活性,强化反硝化作用。另外,钙盐除磷剂主要利用Ca2+与PO43-生成一系列难溶性磷酸钙盐,包括磷酸氢钙、磷酸八钙、无定形磷酸钙、多羟基磷灰石、磷酸三钙等[17-18],相关反应如式(3)
~ 式(5)所示。本研究以真实二元酸废水为对象,结合化学沉淀、混凝与吸附等多种方法,先进行预处理实验,即在实验室对除磷药剂进行筛选,再探究优化絮体沉降性能的方法及实验室最优处理条件,确定降低总磷和COD的预处理方案,最终在此基础上设计并构建二元酸废水预处理的现场装置,考察实际工程运行条件及处理效果,以期为实现石油炼化企业或化工园区综合污水处理厂的稳定达标运行提供参考。
-
1)实验水样。预处理实验采用取自某石油化工企业新建二元酸生产流程集水池的真实长链二元酸发酵废水。该废水的pH为3~4,总磷为250~300 mg·L−1,COD为6 000~7 000 mg·L−1,总有机碳(TOC)为2 200~2 500 mg·L−1,BOD5为3 000~3 500 mg·L−1。
2)实验药剂。氢氧化钠、聚合氯化铝(PAC)、氯化铁(FeCl3)、氯化钙(CaCl2)、氢氧化钙(Ca(OH)2)、聚丙烯酰胺(PAM)等药剂均为工业级。
-
1)预处理药剂筛选及投加量优化。取100 mL水样于200 mL烧杯中进行烧杯实验。分别向烧杯中投加相同质量浓度(2 g·L−1)的PAC、CaCl2、FeCl3和Ca(OH)2,用氢氧化钠溶液调节水样pH。将烧杯置于六联搅拌器下以300 r·min−1快速搅拌180 s,之后加入25 mg·L−1 PAM以促进絮体分离(PAM的投加量由预实验确定);在进行快速搅拌(转速为300 r·min−1)20 s后,再慢速搅拌(转速为100 r·min−1)300 s;静置20 min后取上清液过滤,测定总磷和COD。根据测定结果,筛选出最优预处理药剂及最佳pH条件,并通过测定不同投加剂量下总磷和COD变化,确定最优药剂投加量。
2)预处理副产物固渣产率和元素组成分析。副产物固渣经定量滤纸过滤后置于洁净蒸发皿中,放入105 ℃的烘箱烘烤4~5 h,随后放入干燥器中冷却至室温后称重。反复烘干称重,直至恒重,即2次称重数值相差不超过0.000 5 g,得到结果为固渣干重并以此计算预处理单位废水的绝干固渣产率。采用X射线荧光光谱法(X Ray Fluorescence, XRF)分析固渣的元素组成,并判断其可利用性,。
3)沉淀粒径分析。取沉淀反应及絮凝阶段的沉淀物,为保证数据准确性,整个取样过程控制在10 s内。采用激光粒度仪(Mastersizer 3000,英国马尔文) 对沉淀物平均粒径进行分析测量;采用光学显微镜(BK1201,重庆光电)观察沉淀反应阶段及絮凝阶段沉淀物的形貌特征。
4)水质指标分析。pH的测定参照《水质pH值的测定 玻璃电极法》(GB 6920-1986),采用梅特勒-托利多FE28型pH仪测定;总磷(TP)的测定参照《水质 总磷的测定 钼酸铵分光光度法》(GB 11893-1989),采用美国哈希DR1900型便携式分光光度计测定;总有机碳(TOC)的测定参照《总有机碳水质自动分析仪技术要求》(HJ/T 104-2003),采用日本岛津TOC-L CPH CN 200 TOC分析仪测定;化学需氧量(COD)的测定参照《水质 化学需氧量的测定 重铬酸钾法》(HJ 828-2017),使用CTL-12型化学需氧量速测仪;五日生化需氧量(BOD5)的测定参照《水质 五日需氧量的测定 稀释与接种法》(HJ 505-2009),使用美国哈希BODTrakII型BOD测定仪;总溶解固体(TDS)的测定参照《水质 总溶解性固体测定 重量法》(GB 5749-2006)。
5)有机组成分析。利用气相色谱-质谱法(GC-MS)分析预处理前后水样中有机组成的变化。样品预处理步骤如下:取100 mL水样于250 mL分液漏斗,用NaOH溶液调节pH至12以下,加入30 mL二氯甲烷,置于振荡器中振荡10 min,取下静置20 min后,分离出有机相,再加入30 mL二氯甲烷,重复上述步骤;在分离后的水相中加入一定量的10%硫酸溶液调节水样 pH至2以下,加入30 mL二氯甲烷,置于振荡器中振荡10 min,取下静置20 min后,分离出油相,再向水相中加入30 mL二氯甲烷,重复上述步骤;最后,将有机相集中在同一锥形瓶中,氮吹浓缩至1~2 mL后转移至色谱瓶中,于-18 ℃下暗处保存直至检测。仪器分析条件:采用安捷伦7890B GC/5977B MSD联用仪以及DB-35毛细管色谱柱(30 m×0.25 mm×0.25 μm),进样温度50 ℃,接口温度300 ℃。色谱柱升温程序:50 ℃恒温,2 min;10 ℃·min−1升至100 ℃,恒温2 min;10 ℃·min−1升至200 ℃,恒温2 min;10 ℃·min−1升至280 ℃。
-
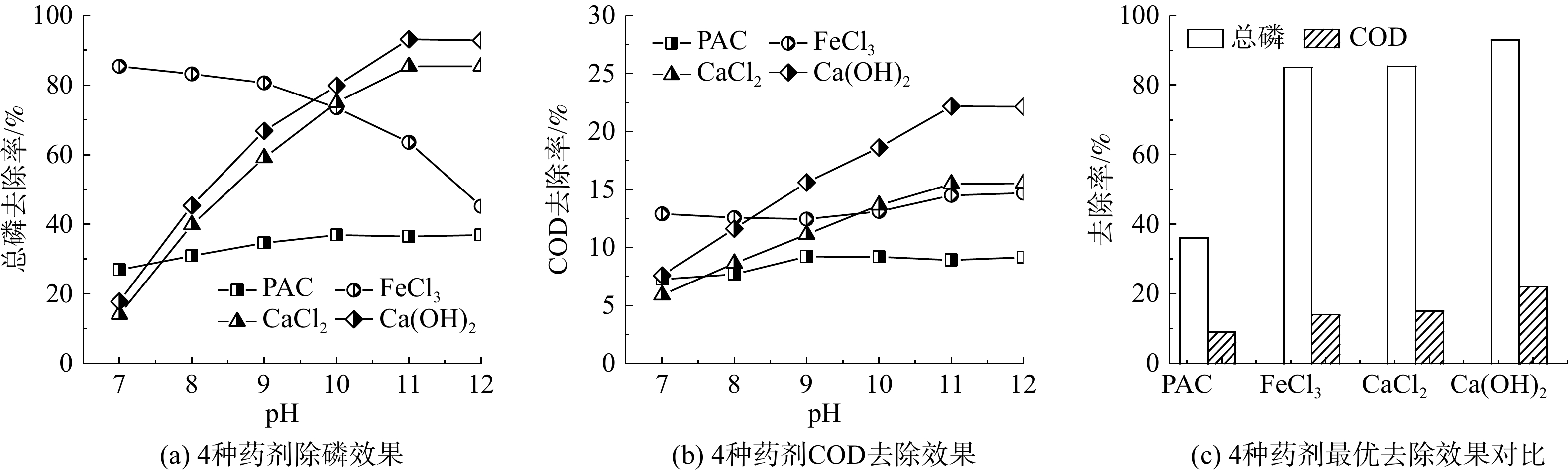
在实验室进行4种预处理药剂的筛选,结果如图1(a)和1(b)所示。在较宽的pH范围内,PAC的除磷效果均不佳是由磷酸铝沉淀易发生再溶解所致。当pH为7时,FeCl3除磷率达到最高的82.1%,但随着pH的升高又迅速下降。这是由于在中性条件下,Fe3+与
PO3−4 生成磷酸铁沉淀;而在碱性条件下,Fe3+会优先与OH−生成Fe(OH)3沉淀,与PO3−4 生成磷酸铁沉淀的几率降低,故在碱性条件下铁盐的除磷效果不理想。而在碱性条件下,Ca2+能与
PO3−4 形成更为稳固的羟基磷酸钙沉淀。在铝盐、铁盐和钙盐和PO3−4 形成的沉淀中,以羟基磷灰石的平衡常数最大,是最易形成且最稳定的固态磷酸盐沉淀,故钙基药剂对总磷的去除率优于铁基和铝基。CaCl2和Ca(OH)2的除磷率随pH的升高而增大,而Ca(OH)2的除磷率要优于CaCl2,在pH为11时达到93%。4种预处理药剂对COD都表现出一定去除效果。随着pH升高,Ca(OH)2对COD的去除率明显增大。在pH达到11时,COD去除率达到22.5%,明显优于其他3种。Ca(OH)2相比于CaCl2而言性能更加稳定,无论是去除水体中总磷还是COD,都具有明显优势。这是由于投加Ca(OH)2后会直接生成沉淀物絮体,而CaCl2在碱度驱动下生成絮体的速度较慢,而且Ca(OH)2生成絮体更加密实,对水中游离磷酸钙沉淀微粒及有机物具有更强的卷扫捕集和吸附作用[19]。对比了在相同投加质量浓度(2 g·L−1)条件下,4类预处理药剂对二元酸废水总磷和COD的去除效果,结果如图1(c)所示。PAC的综合去除效果最差。FeCl3仅表现出对总磷的去除效果较好。而Ca(OH)2对总磷和COD的去除率均大于其他3种,故优选出Ca(OH)2继续开展预处理实验。
-
通过实验继续确定预处理药剂的投加量并对预处理前后水质指标变化进行综合分析,以判断预处理后废水对污水处理厂的影响。如图2所示,随着药剂投加质量浓度增至3.0 g·L−1,对总磷和COD的去除率分别达到97.9%和41.5%,再继续增大投加量对去除效果无明显改善,故确定最佳药剂投加质量浓度为3.0 g·L−1。
-
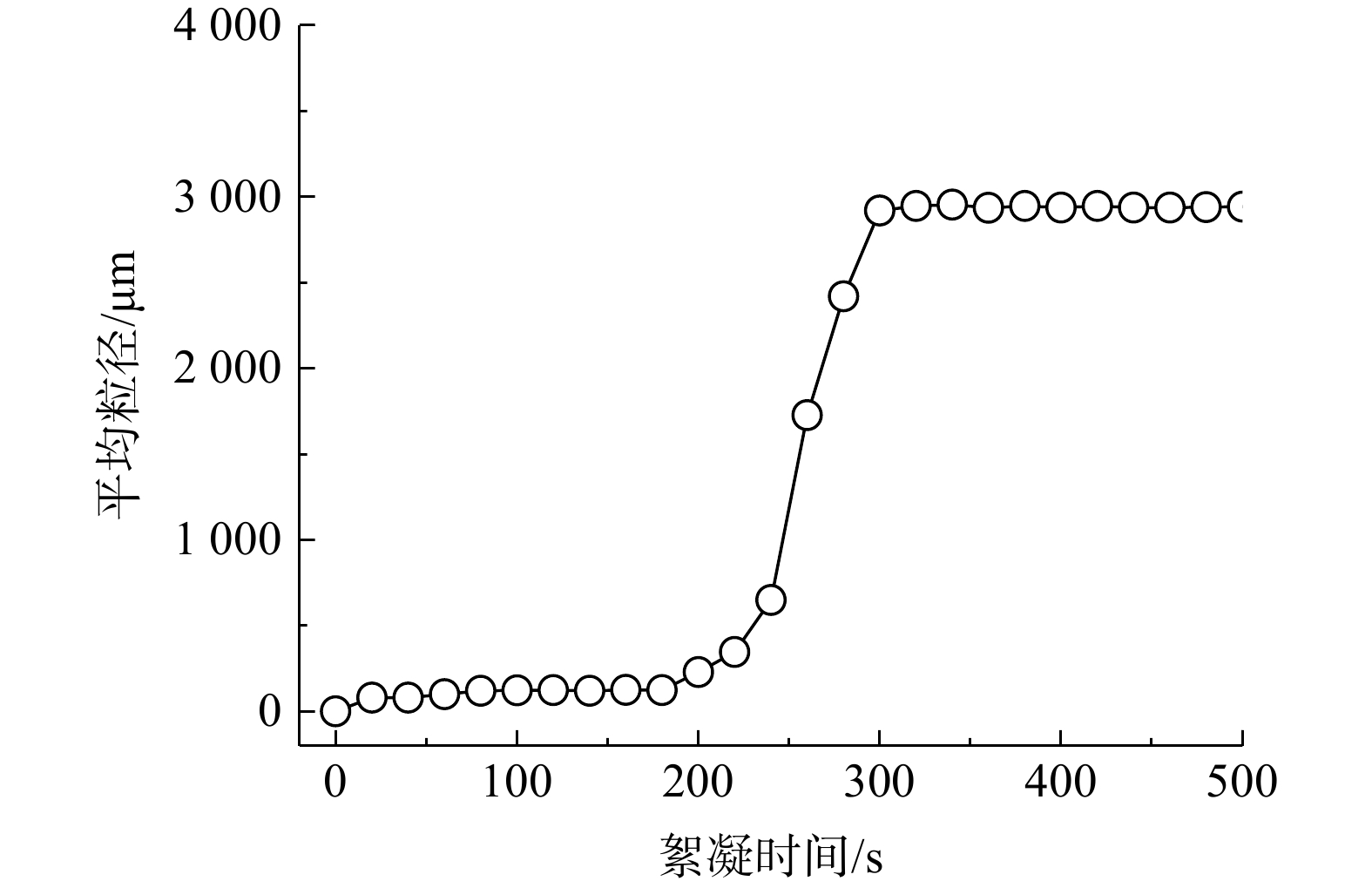
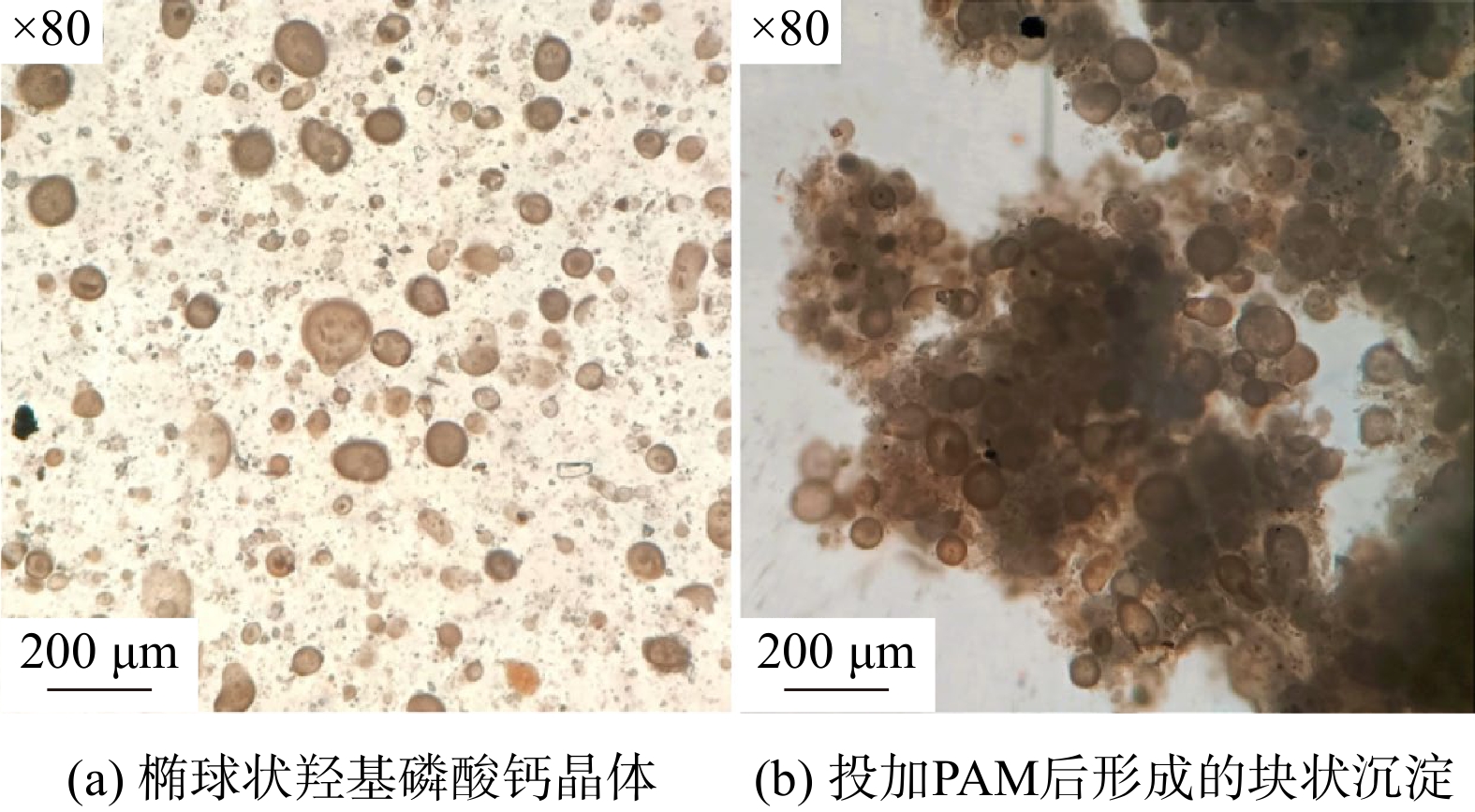
为考察Ca(OH)2最佳药剂投加质量浓度为3.0 g·L−1时,除磷过程中沉淀物平均粒径的变化,将除磷过程分为沉淀反应(0~180 s)和絮凝(180~500 s)2个阶段。在絮凝阶段,投加质量浓度25 mg·L−1的PAM至水样中以促进沉淀物的沉降。此时沉淀物的平均粒径开始缓慢上升,如图3所示。在除磷过程的沉淀反应阶段,Ca2+与PO43-逐渐形成椭球状羟基磷酸钙晶体,如图4(a)所示。当反应进行至80 s时,沉淀物的平均粒径为121 μm。随着反应继续进行,受到晶体饱和度及离子质量浓度的影响,沉淀物的粒径没有进一步增大。在投加PAM后,为确保PAM能均匀分散至水样中,在絮凝的初始阶段(180~200 s)需要快速搅拌,此时分散的晶体颗粒无法有效聚结,平均粒径增长较为缓慢;在慢速搅拌阶段(200~500 s),沉淀物平均粒径骤增,分散的椭球状晶体和悬浮颗粒在PAM吸附桥联的作用下聚结,形成不规则的块状沉淀,如图4(b)所示。当反应进行至320 s时,沉淀物的平均粒径为2 946 μm,且随着反应的进行平均粒径不再增加。因此,投加25 mg·L−1 PAM可提高沉淀物的沉降性,并促进反应在短时间内完成固液分离。
-
在最优药剂投加量下,二元酸废水预处理前后水质指标变化如表1所示。预处理对TOC和COD的去除率均达到40%以上。该结果表明,化学沉淀法、混凝作用以及其他物理化学反应的共同作用才使得该方法的有机负荷去除率能达到此水平。这是由于二元酸废水以有机酸类为主,在酸性条件下,有机酸类的电离程度较低,通常以分子态的形式存在。然而,在碱性条件下,有机酸易电离,以带负电荷的有机酸阴离子状态存在。本研究优选的预处理药剂为水体提供了适宜的pH,二元酸废水进水pH为3.5,而当投加量为3.0 g·L−1时,pH为11.0,故有机酸类污染物一直以阴离子状态存在。另外,Ca(OH)2絮体在水中带正电荷,通过静电引力吸附作用可对这些有机酸阴离子进行去除,从而大幅降低了二元酸废水中的有机负荷。
有机污染组成的变化情况如表2所示。二元酸废水的有机污染组成以有机酸类为主,相对丰度达到92.9%。此外,还含有少量酯类、醇类、胺类及长链正构烷烃类。这些有机污染物均为发酵产物、副产物和原料在水体中的残留,故此类废水的可生化性较好(BOD5/COD达到0.56)。经过预处理后,有机污染物数量减少,烷烃和醇类被彻底去除,且部分易生化有机酸类亦被去除,使得BOD5/COD微降至0.46,但仍为易生化降解废水。
预处理后废水的TDS由19 197 mg·L−1微降至17 183 mg·L−1。高浓度絮体沉淀的吸附和卷扫捕集作用能去除部分电离的有机物,但预处理药剂又会带入无机盐,故预处理对TDS去除率仅有10.5%。
预处理的绝干固渣产率为每吨废水3.4 kg。固渣主要由磷酸钙、羟基磷酸钙、硫酸钙及氢氧化钙沉淀构成,Ca、P和S元素含量分别为65 %、20.3%和4.2%。固渣呈碱性且含有大量Ca元素,其中Ca(OH)2和羟基磷酸钙占比较大。
-
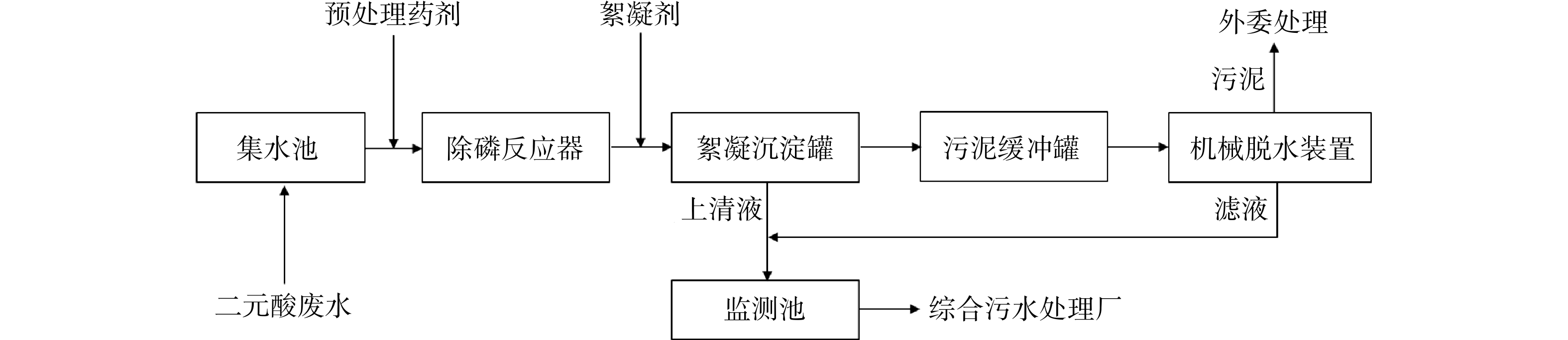
根据预处理实验结果,为某石油化工企业新建的二元酸生产流程配套设计了6 t·h−1规模的废水预处理工程装置。装置主体由药剂投加系统、除磷全混流反应器、絮凝沉降罐、污泥缓冲罐和板框压滤机等设备构成。主体工艺流程如图5所示。二元酸生产排放的点源废水在集水池内进行混合,均质均量后进入预处理装置。二元酸废水经水泵提升后在管道内通过静态混合器与预处理药剂(投加量3 kg·t−1)充分混合,再进入除磷全混流反应器内。在反应器内通过沉淀、混凝与吸附综合作用去除总磷和COD;全混流反应器出料与絮凝剂PAM(投加量25 g·t−1)混合后,自流进入絮凝沉降罐,凝聚形成大颗粒絮体沉淀;上层清液溢流至监测池,下层沉淀送入污泥缓冲罐;污泥缓冲罐内污泥经气动隔膜泵送入板框压滤机实现固液分离,脱水后污泥(60%含水率)作为一般固废外委处置,滤液排放至监测池。监测池总磷满足小于30 mg·L−1的要求后,再排往污水处理厂。
-
1)药剂投加系统。药剂投加系统由除磷药剂投加单元和絮凝剂投加单元构成。除磷药剂制备箱外形尺寸:3 000 mm×1 500 mm×2 250 mm,数量1台。搅拌机型号:BLD2-29-2.2KW,数量2台。预处理药剂投加泵:G25-1,Q=2 m3·h−1,H=60 m,N=2.2 kW,数量2台。絮凝剂制备箱外形尺寸:2 000 mm×1 000 mm×2 250 mm,数量1台。搅拌机型号:BLD2-29-1.5KW,数量2台。絮凝剂投加泵:JXM-A-315/0.5,Q=0.315 m3·h−1,H=50 m,N=0.55 kW,数量2台。絮凝剂制备箱内有隔断,2个絮凝剂配制罐一用一备,分为制备和投加两个环节。
2)除磷罐全混流反应器。除磷罐反应器外形尺寸:Φ1 800 mm×2 250 mm,数量1台。搅拌机型号:BLD2-17-4KW,数量1台。反应器设计水力停留时间为0.95 h。二元酸含磷污水废水通过泵打入全混流反应器除磷罐,当液位淹没搅拌机桨叶时开启搅拌机,同时开启除磷预处理药剂投加泵。根据全混流反应器除磷罐pH及出水总磷调整除磷剂的投加量,pH应控制在11~12。
3)沉淀罐。沉淀罐外形尺寸:Φ1 800 mm×5 400 mm,数量2台。污泥提升泵:QBY-40,Q=8 m3·h−1,H=40 m,数量2台。全混流反应器除磷罐出水和絮凝剂混合后自流进入沉淀罐中心筒,在沉淀罐内完成初步泥水分离。沉淀罐上清液溢流至清水箱,罐底含磷污泥通过污泥提升泵排入污泥缓冲罐内。2台沉降罐交替使用,每台沉降罐进水6 h(时间可根据进水量调节)。当一台罐进水时,另一台罐沉淀3 h,通过排泥2.5 h静置0.5 h后再进水。
4)固液分离系统。固液分离系统主要由污泥缓冲罐和板框压滤机2部分构成,主要功能为实现预处理后二元酸废水的固液分离。污泥缓冲罐外形尺寸:Φ3 000 mm×5 400 mm,数量1台。系统设计水力停留时间为6.4 h。污泥提升泵为2台,Q=8 m3·h−1,H=40 m)。板框压滤机:XMZ150/1250-30U。过滤面积为150 m2。滤室容积为2 200 L。额定过滤压力为0.55 MPa。
-
1)投加絮凝剂的操作要点。高分子絮凝剂PAM溶解缓慢且易结块,配置时应缓慢投加,避免絮凝剂成坨无法溶解,会影响絮凝剂投加泵的稳定运行。若絮凝剂溶解充分,则溶液呈透明状并有一定粘度;若絮凝剂未充分溶解,罐中会形成结团的白色漂浮物。以上现象可用来判断絮凝剂是否充分溶解。当絮凝剂投加量不足时易导致絮体松散、沉降性能差,进而影响除磷效果。另外,还应通过二元酸废水的水量和沉淀罐内絮体的絮凝效果来控制絮凝剂溶液的投加量。若沉淀罐中絮体上浮松散,则需要增大絮凝剂的投加量。
2)固液分离系统操作要点。污泥缓冲罐中污泥的质量浓度会直接影响固液分离效率。若缓冲罐中污泥浓度过低,则固液分离效率差。当污泥缓冲罐内污泥液位至溢流口时,可打开污泥沉降罐中的污泥提升泵。若开泵后污泥缓冲罐中的污泥上浮明显,则表明污泥缓冲罐中的污泥已达到一定浓度,可进行压滤。压滤机进泥泵为气动隔膜泵,开启气源阀门,泵开始工作。在气泵隔膜泵开启前,需对气路管道进行检查,若气路管道含水将会影响隔膜泵的使用。
-
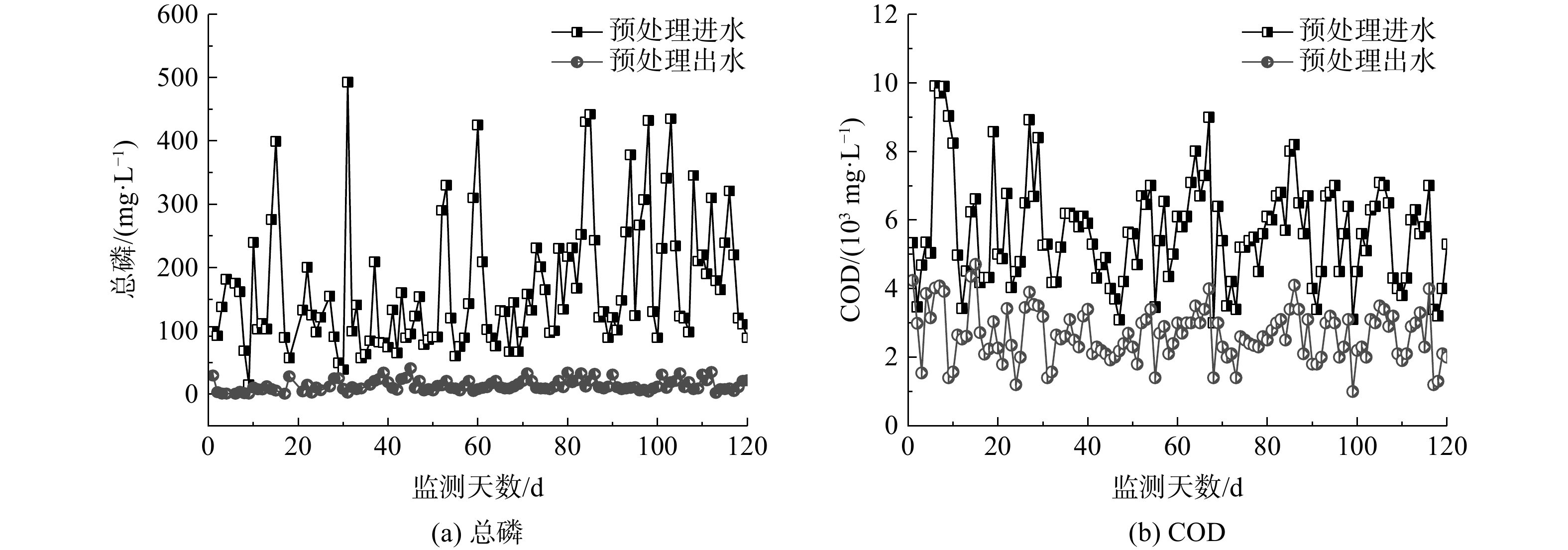
二元酸废水预处理现场装置于2020年初建成,在完成调试后进行了3个月的试运行,运行效果如见图6所示。进水总磷平均值为160.3 mg·L−1,出水总磷平均值为12.3 mg·L−1,去除率高达93.3%,远优于出水30 mg·L−1的设计指标。进水COD平均值为5 641 mg·L−1,出水COD平均值为2 651 mg·L−1,远优于设计进水5 000 mg·L−1的去除指标,去除率达53.0%,且预处理出水的可生化性良好。预处理现场装置投入运行后,有效保障了污水处理厂出水的稳定达标,出水的总磷远低于0.5 mg·L−1的排放限值。
-
对预处理现场装置的直接运行成本进行了评估,处理每吨废水会消耗3 kg预处理药剂和25 g PAM,以及52 kg新鲜水(用于药剂配制),其中预处理药剂约2 000元·t−1、PAM约60 000元·t−1、新鲜水4.1元·t−1,故药剂使用及用水成本约合7.71元·t−1。此外,提升、搅拌、注剂及压滤等动力过程的电耗约2.12元·t−1。因此,合计每吨二元酸废水预处理的直接成本约为9.83元。如果考虑到冬季采用保温伴热等措施,运行成本会略有增加,但总体保持在较低水平。
-
1)为缓解发酵法长链二元酸生产流程排放的高总磷、高COD废水对石油化工企业综合污水处理厂的冲击,基于源头控制开展了预处理方法研究。在实验室优选出钙基预处理药剂Ca(OH)2,在最佳投加量下,二元酸废水的总磷和COD去除率达到97.9%和41.5%,副产物固渣产量约每吨废水3.4 kg。
2) Ca(OH)2电离出的Ca2+与废水中游离的磷酸根生成磷酸钙、羟基磷酸钙等沉淀。Ca(OH)2向水体提供足量的OH−,使得有机酸类污染物以阴离子状态存在,有利于带正电Ca(OH)2絮体的静电吸附。Ca(OH)2絮体紧实,通过沉淀、混凝与吸附等综合效应,可共同促进对总磷和COD的去除。在投加PAM后,沉淀物平均粒径为2 946 μm,沉降性能良好。
3)在预处理实验基础上,设计并建成处理量6 t·h−1的二元酸废水预处理现场装置,其总磷和COD去除率为93.3%和53.0%,可综合污水处理厂的总磷达标和稳定运行。该现场装置的直接运行成本仅为9.83元·t−1。
某石化企业长链二元酸生产废水的预处理工艺及现场应用
Industrial application and study for pretreatment of long chain dicarboxylic acid fermentation wastewater
-
摘要: 某石油化工企业的发酵法长链二元酸生产装置会排放高浓度废水。废水中的二元酸盐及培养基成分使下游综合污水处理厂的进水总磷和有机负荷偏高,可能造成出水总磷严重超标的风险。通过实验优选出钙基预处理药剂并确定最优处理条件。即在pH为11、药剂投加量为3 g·L−1的最优条件下,对总磷和COD的去除率分别达到97.9%和41.5%,且出水可生化性较好(BOD5/COD约0.46),副产物绝干固渣产量仅有3.4 g·L−1。以此为基础,开发了二元酸废水预处理工艺,并建成处理量6 t·h−1的现场工程化装置。在长周期运行过程中,装置对总磷和COD的平均去除率为93.3%和53.0%。该工艺可有效保障了石化企业综合污水处理厂的总磷达标和稳定运行。Abstract: The wastewater discharged from the fermentation long-chain dicarboxylic acid unit of a petrochemical company greatly increased the total phosphorus (TP) and COD load of the downstream wastewater treatment plant (WWTP), and TP of the effluent was at a serious risk of exceeding the standard. In this study, calcium-based pretreatment agent was selected through experiments, and 97.9% of TP and 41.5% of COD can be removed at a laboratory scale. The production rate of dry residue is low (3.4 g·L−1) and treated wastewater kept good biodegradability (BOD5/COD=0.46). Based on experimental results, the pretreatment processes for fermentation wastewater was designed and a 6 t·h−1 unit was built. During operation, TP and COD removal rates reached 93.3% and 53.0%, respectively. The efficiencies of the petrochemical WWTP are fully guaranteed.
-
六六六,学名六氯环己烷 (Hexachlorocyclohexane, HCH) ,是典型有机氯农药,在我国的产量占全世界生产总量的33%[1-2]。HCH作为持久性有机污染物 (persistent organic pollutants,POPs) 可通过多种环境介质传播,危害人类健康。目前,我国存在环境中HCH残留量过高的问题,特别是曾经作为农药大量使用的林丹 (γ-HCH) ,在农田、湖泊等环境中存在残留[3-5]。因此,亟需探索HCH在环境中的迁移转化过程的有效解析方法,以制定污染防治策略。
林丹在环境介质中的浓度可能受到吸附、挥发等物理过程的影响,单一的检测数据易造成污染物减少的假象,并不能准确地反映其在环境中的迁移转化过程[6-8]。单体稳定同位素分析技术 (compound-specific isotope analysis,CSIA) 能避免因产物浓度变化和复杂实地环境产生的干扰,弥补传统测试方法的不足,近年来在环境领域的应用中发展较快[9-10]。在有机物降解过程中,一般含轻同位素12C化学键的断键速度快于含重同位素13C的化学键,从而导致底物中13C的富集[11]。重同位素的丰度与轻同位素的丰度值之比为同位素比值。CSIA技术可通过测定并对照反应前后污染物中某元素的同位素比值变化来追踪污染物的来源并解析其在环境中的迁移转化过程[12],为解析有机污染物在环境中的迁移转化过程提供了新思路[9, 13]。
好氧微生物降解是HCH在环境中转化的重要途径。目前,有多达30多种好氧微生物被证实具有降解HCH的能力[14]。然而,这类微生物在降解HCH过程中的同位素分馏特性不明,极大限制了应用稳定同位素技术解析HCH在环境中的迁移转化行为。BASHIR等[15]利用碳同位素分馏特性表征了Sphingobium indicum strain B90A 和Sphingobium japonicum strain UT26对α-HCH和γ-HCH的降解过程,并计算了同位素富集系数ε值。这两种微生物降解α-HCH过程中的ε值分别为−(1.0±0.2) ‰和−(1.6±0.3) ‰,降解γ-HCH过程中的ε值分别为−(1.5±0.1) ‰和−(1.7±0.2) ‰。
基于已经报道的ε值,用式 (1) 计算了地下水中HCH的降解程度 (B%) ,与实测结果进行对照,发现部分采样点的计算结果与实际测试值并不相符[10, 16]。
B%=[1−(δt+1δ0+1)1/ε]×100 (1) 式 (1) 表明,污染物降解程度评估的准确性取决于ε值,然而,已见报道的ε值还很有限,限制了技术在解析环境中林丹降解程度以及污染场地修复效果评估中的应用。此外,实际环境中林丹的降解可能由多个微生物共同参与完成,而同一污染场地中不同微生物降解林丹过程中的同位素分馏特性是否相同亦为制约CSIA技术应用的关键,故尚需开展进一步研究。
以3种从同一污染场地分离纯化获取的好氧微生物S. quisquiliarum P25、S. ummariense RL-3和Sphingobium sp. F2为研究对象[17-19],对比分析其降解林丹过程中的降解动力学特性、单体稳定同位素分馏效应、二维稳定同位素分馏及表观动力学同位素特性。拟揭示不同好氧微生物在降解HCH过程中的同位素分馏特性,并基于二维同位素分析,解析不同微生物降解林丹过程中同位素分馏特性的差异。以期为建立模型解析实际环境中HCH的迁移转化过程提供重要参考值,为应用CSIA评估林丹污染场地修复效果的实际应用提供数据基础。
1. 材料与方法
1.1 实验材料
实验所用林丹 (γ-HCH,分析纯) 、六氯苯 (HCB,分析纯) 、正己烷 (分析纯) ,均由Sigma-Aldrich公司提供。
1.2 实验方法
1) 降解实验:将S. quisquiliarum P25、S. ummariense RL-3和Sphingobium sp. F2在LB培养基中进行预培养。当A600达到0.5~0.6时,取100 µL菌液 (基于前期预实验结果确定) 到50 mL无机盐培养基中 (120 mL血清瓶) ,每瓶添加5.5 µLγ-HCH储备液 (0.1 mol·L−1) 并添加葡萄糖作为碳源,开展序批实验。每组实验设置15个平行培养体系,其中包括2个非生物对照组,在微生物最适温度30 ℃下进行恒温培养。在达到不同降解程度时 (基于前期预实验结果确定) 分别向培养瓶中添加l mL硫酸和硫酸钠混合饱和溶液 (pH=2) 以终止反应。将终止反应后的培养瓶置于4 ℃的冰箱内冷藏保存,至实验结束后统一萃取HCH。
2) 萃取实验:以正己烷为萃取液,HCB为内标,通过液液萃取提取HCH。内标浓度约为HCH初始浓度的一半 (2.5 µmol·L−1) 。具体方法详见文献[8]。
1.3 测试方法
1) 浓度测试:HCH的浓度采用气相色谱 (GC,安捷伦6890) 连接火焰离子化检测器 (FID,安捷伦7820A,美国) 由安捷伦HP-5毛细管柱 (30 m×0.32 mm ID×0.25 µm FD) 测定,载气流速为2.0 mL·min−1。升温程序设置为初始温度35 ℃保持5 min, 然后以8 ℃·min−1的升温速率升至180 ℃,接着以2 ℃·min−1的速度升高至195 ℃,最后以8 ℃·min−1的速度升高至220 ℃并保持2 min[8]。在建立计算曲线的基础上计算HCH浓度。
2) 稳定同位素测试:碳稳定同位素值 (δt13C) 采用GC (安捷伦6890) 连接同位素质谱仪 (IRMS, 赛默飞MAT253) 测定,色谱柱为ZB1 (60 m×0.32 mm×1 µm,Phenomenex) ,载气流速为2.0 mL·min−1。升温程序设置为40 ℃的初始温度保持5 min, 然后以6 ℃·min−1的速度升高至200 ℃,再以3 ℃·min−1的速度升温至260 ℃,最后以20 ℃·min−1的速度升高至300 ℃并保持5 min [7]。氯稳定同位素值 (δt37Cl) 采用GC耦合多集电极电感耦合等离子体质谱仪 (GC-MC-ICPMS) 测定,GC (安捷伦6890) 所用色谱柱及参数设置与碳同位素设置一致[20-22]。
1.4 数据分析方法
1) 酶促反应动力学。用Michaelis−Menten动力学方程[23]来表征酶促反应,计算式如式 (2) 。
v=kcat×[E]0[S]KM+[S] (2) 式中:v为反应速率,mol∙L−1∙s−1;kcat为催化常数,s−1;KM为米氏常数;[E]0为酶的初始浓度。
2) 同位素分馏的定量分析。γ-HCH降解过程中的碳同位素值变化的快慢可以通过碳同位素分馏系数 (εC) 来定量,εC利用瑞利方程计算,如式 (3) 所示。
ln(δ13Ct+1δ13C0+1)=εC×ln(CtC0) (3) 式中:
εC 3) 二维同位素定量分析。通过同位素分馏实验获取的δ13C和δ37Cl,计算二维同位素分馏系数 (Λ) 来表征C—Cl的断键机理,表观动力学同位素分馏常数(apparent kinetic isotope effect,AKIE),计算如式 (4) 。
ΛC-Cl=(δ13Ct−δ13C0)/(δ37Clt−δ37Cl0) (4) 表观动力学同位素分馏常数 (AKIE) 可在考虑物质结构的基础上表征不同物质降解过程中同位素变化的速度,从而实现不同物质在相同降解作用下的对比分析。AKIE根据式 (5) 计算[24]。
AKIEC=11+nzx×εC/1000 (5) 式中:n为底物分子中所有碳原子数量;x为反应点位上的碳原子数量;z为不可区分的反应点位数量。
2. 结果与讨论
2.1 降解动力学分析
微生物降解反应的核心是酶促反应,这些酶均由跟HCH降解酶相关的基因 (lin 基因) 表达而来,如LinA、LinB、LinC等[25]。当底物浓度远远小于Michaelis常数,即[S]
≪ v=−k×[S] (6) 式中:
k=−kcat×[E]0KM 因此,当[S]
≪ ≪ ≪ 2.2 降解速率分析
如图1所示,Sphingobium sp. F2,S. ummariense RL-3和S. quisquiliarum P25均可降解γ-HCH。空白对照组γ-HCH浓度稳定,可排除非生物降解对污染物浓度的影响。在对HCH持续降解25 h后,Sphingobium sp. F2组中γ-HCH从5.5 µmol·L−1降至0.8 µmol·L−1,降解率达到86%,降解速率为0.08 h−1;S. ummariense RL-3组在培养10 h后,降解率达到97%,降解速率为0.36 h−1;而S. quisquiliarum P25组5 h内降解率达到94%,降解速率为0.52 h−1。在相同培养条件下3种微生物降解γ-HCH速率差异较大,原因是微生物降解HCH的关键酶是水解脱氢酶的变异体[17-19],3种微生物的不同的水解脱氢酶对γ-HCH的降解速率有较大影响。BASHIR等 [15]也报道过Sphingobium indicum strain B90A 和 Sphingobium japonicum strain UT26在同等条件下降解γ-HCH的降解速率不同。
2.3 稳定同位素分馏效应分析
如图2 (a) 所示,3组实验γ-HCH降解过程中均发生了明显的碳稳定同位素分馏现象。其中,在Sphingobium sp. F2的降解过程中,当γ-HCH降解率达到86%时,δ13C由−(27.2±0.2) ‰富集为−(16.5±0.3) ‰;在S. ummariense RL-3的降解过程中,当γ-HCH降解率达到97%时,δ13C由−(27.2±0.2) ‰富集为−(21.7±0.4) ‰;当S. quisquiliarum P25降解γ-HCH达到94%时,δ13C由−(27.2±0.2) ‰富集为−(15.7±0.3) ‰。3组降解实验中δ13C的富集差值 (△δ13C=δ13Ct-δ13C0) 分别达到了 (10.7±0.49) ‰(γ-HCH降解速率为0.08 h−1,降解率为86%)、 (5.5±3.24) ‰ (γ-HCH降解速率为0.36 h−1,降解率为97%) 、 (11.5±0.73) ‰ (γ-HCH降解速率为0.52 h−1,降解率为94%) 。对于同一物质的同一降解反应,降解率越高,同位素富集效应越明显。值得注意的是,Sphingobium sp. F2的降解率只有86%,而△δ13C值却明显比降解率更高 (97%) 的S. ummariense RL-3的更大。这表明Sphingobium sp. F2 和S. ummariense RL-3降解γ-HCH过程中有明显不同的同位素分馏特性。同时,S. ummariense RL-3和S. quisquiliarum P25降解率相近,但△δ13C值差别同样较为明显。因此,根据降解率和碳稳定同位素分馏效应分析,这3种菌降解γ-HCH的过程存在明显差异。这一结果与BASHIR等[15]研究Sphingobium indicum strain B90A和Sphingobium japonicum strain UT26降解γ-HCH过程所产生的同位素分馏效应的结果类似。
如图2 (b) 所示,3种微生物在降解γ-HCH过程中,氯稳定同位素分馏也较为明显。在Sphingobium sp. F2降解γ-HCH过程中,当降解率为65%时,底物中γ-HCH的δ37Cl值为 (3±0.2) ‰;在S. ummariense RL-3的降解过程中,当降解率达到75%时,底物中γ-HCH的δ37Cl值为 (3.2±0.1) ‰;在S. quisquiliarum P25的降解γ-HCH达到82%时,γ-HCH的δ37Cl值为 (3.7±0.1) ‰。氯元素的稳定同位素分馏相对于碳稳定同位素分馏较小,故3种微生物在降解γ-HCH过程中氯稳定同位素分馏的差异也较小。
2.4 同位素富集过程的定量分析
为消除降解率不同的干扰,进行了基于瑞利方程的同位素富集过程的定量分析。如图3 (a) 所示,Sphingobium sp. F2,S. ummariense RL-3和S. quisquiliarum P25在降解γ-HCH过程中的εC分别为−(5.7±0.5) ‰,−(1.6±0.1) ‰和−(4.3±0.4) ‰。协方差分析结果显示,这3组εC值具有显著性差异 (p<0.005) ,且任意两组εC值之间同样具有显著性差异。与△δ13C值的排序对比可知,εC值的计算有效的排除了降解率的干扰,更准确的反应了γ-HCH降解过程中的同位素分馏特性。基于同位素分馏形成的机制,由于遮蔽效应的存在,过高的降解速率可能会降低同位素富集效果[7]。在本实验中,S. ummariense RL-3降解γ-HCH的速率 (0.36 h−1) 比S. quisquiliarum P25的降解速率 (0.52 h−1) 低,但后者的εC值明显高于前者,故同位素遮蔽效应不是导致同位素分馏系数差异的原因。导致εC不同的原因是不同微生物酶降解γ-HCH时的同位素分馏特性不同。这与BASHIR等[15]对Sphingobium indicum strain B90A和Sphingobium japonicum strain UT26在相同培养条件下降解γ-HCH过程中的同位素分馏系数类似的结果存在一定差异。此外,与报道的土壤实验结果对比发现,在土壤环境中S. quisquiliarum P25降解γ-HCH所产生的εC值 (−3.2‰) [27],较本实验结果εC值偏低。这是由于土壤相对于液体环境来说是非均质环境,HCH在非均质环境中不均匀的分散是导致局部降解过程中出现同位素遮蔽效应的主要原因。
如图3 (b) 所示,Sphingobium sp. F2,S. ummariense RL-3和S. quisquiliarum P25在降解γ-HCH过程中均发生明显的氯同位素分馏,经瑞利方程拟合得到的εCl值分别为− (1.1±0.6) ‰,− (1.5±0.2) ‰和− (1.5±0.4) ‰。基于协方差分析结果,Sphingobium sp. F2的εCl值与其他2组具有显著性差异 (p<0.05) ;S. ummariense RL-3和S. quisquiliarum P25的εCl值不具有显著性差异 (p>0.05) ,这与3组实验碳同位素分馏过程中的εC值都具有显著性差异的结果不同,表明单一元素的同位素分馏对断键过程的表征具有一定的局限性。有报道显示纯化后的水解脱氢酶LinA1和LinA2降解γ-HCH过程中εCl值分别为− (2.7±0.3) ‰和− (2.5±0.4) ‰,明显高于微生物降解过程中的εCl值,这与跨膜传质过程可能会导致同位素分馏遮蔽效应的结论一致[7]。
2.5 二维稳定同位素分析
如图4所示,Sphingobium sp. F2,S. ummariense RL-3和S. quisquiliarum P25在降解γ-HCH过程中的碳/氯二维同位素分馏系数 (ΛC-Cl) 分别为 (3.0±0.3) , (1.1±0.1) 和 (2.7±0.2) 。基于协方差分析结果,S. ummariense RL-3与其他2种微生物的ΛC-Cl值具有显著性差异 (p<0.05) ,然而Sphingobium sp. F2和S. quisquiliarum P25的ΛC-Cl值不具有显著性差异 (p>0.05) 。由于传质过程对反应点位的C和H的影响是同步的,因此二维同位素可以有效消除传质过程中同位素的遮蔽效应[21]。基于二维同位素分析结果,认定Sphingobium sp. F2和S. quisquiliarum P25在降解γ-HCH过程中具有相同的降解机理,且与S. ummariense RL-3的降解机理不同。这可能是由于Sphingobium sp. F2和S. quisquiliarum P25与S. ummariense RL-3的lin基因表达了不同的HCH降解酶。例如,前者是LinB酶,而后者是LinA酶等。LIU等[28]的研究结果为纯化后得水解脱氢酶LinA1和LinA2降解γ-HCH过程中的ΛC-Cl值分别为 (2.7±0.2) 和 (2.9±0.2) ,与本研究中Sphingobium sp. F2和S. quisquiliarum P25的值一致,无显著性差异 (p>0.05) 。这一结果与分析微生物降解与纯酶降解单一同位素富集系数存在差异的结果形成对照,进一步表明二维同位素分析可消除同位素分馏的遮蔽效应,并表征污染物的断键机理。
2.6 表观动力学同位素分馏常数解析
HCH的降解是一个脱氯化氢的过程,利用公式 (5) 分别计算了3种微生物降解γ-HCH过程中的AKIEC值。由于在HCH的6个C—Cl键中,处于轴向的C—Cl键比处于横向的C—Cl键更容易断键,因此,γ-HCH处于轴向的3个C—Cl键都是可能的反应点位,而不可区分的反应点位有2个。在计算AKIEC的时候,总碳原子数、反应点位数和不可区分反应点位数分别为n=6,x=3,z=2。经计算,Sphingobium sp. F2,S. ummariense RL-3和S. quisquiliarum P25降解实验中的AKIEC值分别为 (1.023±0.002) , (1.006±0.001) 和 (1.018±0.002) 。3种菌降解γ-HCH所获得的AKIEC值均低于Streitwieser-半经典极限中C—Cl断键产生的AKIEC值1.057[24]。SCHILLING等[26]的研究中水解脱氢酶LinA酶降解γ-HCH过程中获得的AKIEC值分别为 (1.024±0.001) 和 (1.023±0.001) 。文献[15]的结果表明,Sphingobium indicum strain B90A和Sphingobium japonicum strain UT26降解α-HCH过程中所产生的AKIEC值分别为 (1.003±0.001) 和 (1.005±0.001) ,均与Sphingobium sp. F2降解γ-HCH所获得的AKIEC值 (1.023±0.002) 接近。AKIEC的计算中已考虑物质结构差异的影响,故不同物质相似的AKIEC表明反应机理一致。此外,不同的微生物在降解不同物质过程中可能产生类似的同位素分馏效应。如Sphingobium japonicum strain UT26和S. ummariense RL-3在分别降解α-HCH和γ-HCH过程中碳同位素分馏特性类似。这表明这2种微生物在脱氯化氢过程中机理相同。有报道称Sphingobium japonicum strain UT26的lin基因所表达的HCH降解酶为LinA酶[25],故推断S. ummariense RL-3的lin基因所表达的酶为LinA酶。
3. 结论
本研究中所涉及的3种微生物降解林丹的过程均符合一级反应动力学,并且降解过程中林丹均发生了明显的碳/氯同位素分馏效应。基于组内对照及前期研究对比,不同好氧微生物降解林丹过程中同位素分馏效应差异较大。Sphingobium quisquiliarum P25、Sphingobium ummariense RL-3和Sphingobium sp. F2降解林丹过程中εC值分别为−(4.3±0.4) ‰,−(1.6±0.1) ‰和−(5.7±0.5) ‰;εCl值分别为−(1.1±0.6) ‰,−(1.5±0.2) ‰和−(1.5±0.4) ‰;ΛC-Cl值分别为 (3.0±0.3) , (1.1±0.1) 和 (2.7±0.2) ;AKIEC值分别为: (1.023±0.002) , (1.006±0.001) 和 (1.018±0.002) 。基于二维同位素分析和AKIEC分析,这种同位素分馏效应的差异是由不同微生物的HCH降解酶不同引起的,并推测S. ummariense RL-3的lin基因所表达的酶为LinA酶。以上结论可为应用CSIA技术解析林丹在自然条件下的迁移转化过程,以及分析在微生物修复过程中不同微生物的贡献提供数据支撑。
-
表 1 预处理前后二元酸废水主要水质指标的变化
Table 1. Changes of main pollution indicators before and after pretreatment
水质指标 预处理前/(mg·L−1) 预处理后/(mg·L−1) 去除率/% 总磷 270 5.72 97.9 COD 6 200 3 627 41.5 BOD5 3 486 1 673 53.3 BOD5/COD 0.56 0.46 - TOC 2 441 1 342 45.0 TDS 19 197 17 182 10.5 表 2 预处理前后有机污染组成变化
Table 2. Changes of organic pollution composition before and after pretreatment
水样 有机物类型 碳数范围 分子量范围 相对丰度/% 预处理前 有机酸类 C6~C12 116~230 92.93 酯类 C6~C10 296~390 3.42 醇类 C8 122.16 0.44 烷烃类 C11 156.31 1.03 胺类 C8 135.16 2.18 预处理后 有机酸类 C6~C12 122~230 95.32 酯类 C6~C10 142~234 2.31 胺类 C8 135.16 2.36 -
[1] 杨健, 黄伟星, 王士芬. 十三碳二元酸发酵有机废水处理研究[J]. 环境污染与防治, 1999, 21(1): 15-18. [2] 汤贵兰, 蓝伟光, 严滨. 二元酸废水处理工艺改造的中试研究[J]. 水处理技术, 2007(6): 91-94. doi: 10.3969/j.issn.1000-3770.2007.06.026 [3] 许莉, 王明毓, 王伟. 电解与纳滤工艺联合处理十三碳二元酸生产中的废水[J]. 化学工程, 2008, 33(9): 43-46. doi: 10.3969/j.issn.1005-9954.2008.09.012 [4] 孙 梦, 张培玉, 张 晨. 城市污水的除磷技术分析[J]. 水处理技术, 2010, 36(8): 16-20. [5] 徐庆国, 吴贵明, 满春生. 工业含磷废水处理的研究与应用[J]. 工业水处理, 2003, 23(12): 76-78. doi: 10.3969/j.issn.1005-829X.2003.12.025 [6] 白卯娟, 褚衍洋. 硫酸亚铁改性粉煤灰处理含磷废水[J]. 青岛科技大学学报(自然科学版), 2008, 29(3): 213-216. [7] 唐代瑶, 刘文辉, 王东燕. 粉煤灰改性造粒及对含磷污水处理的研究[J]. 环境与发展, 2020, 32(11): 101-102. [8] 姚俊琪, 商卫纯, 李梦洁. 改性凹凸棒土吸附剂的制备及其在含磷废水处理中的应用[J]. 环境科技, 2018, 31(5): 35-40. doi: 10.3969/j.issn.1674-4829.2018.05.008 [9] 蒙浩焱, 杨名帆, 罗国芝. 载铁牡蛎壳粉对水中磷的吸附性能及机理[J]. 环境工程学报, 2021, 15(2): 446-456. doi: 10.12030/j.cjee.202004076 [10] PARK T, AMPUNAN V, MAENG S. Application of steel slag coated with sodium hydroxide to enhance precipitation-coagulation for phosphorus removal[J]. Chemosphere, 2017, 167(5): 91-97. [11] 谢经良, 刘娥清, 赵新. 不同形态铁盐的除磷效果[J]. 环境工程学报, 2012, 6(10): 3429-3432. [12] 赵艳梅, 刘起峰, 李涛. 混凝强化除磷的模拟实验研究[J]. 环境工程学报, 2007, 1(5): 11-14. doi: 10.3969/j.issn.1673-9108.2007.05.003 [13] ZHANG Z B, LI Y, WEI L L. Effect of ferric chloride on the properties of biological sludge in co-precipitation phosphorus removal process[J]. Chinese Journal of Chemical Engineering, 2013, 21(5): 564-568. doi: 10.1016/S1004-9541(13)60511-X [14] 郁娜, 袁林江, 吕景花. 某城市污水处理厂废水化学除磷沉淀特性及影响因素[J]. 环境工程学报, 2015, 9(12): 5813-5817. doi: 10.12030/j.cjee.20151227 [15] BARCA C, GERENTE C, MEYER D. Phosphate removal from synthetic and real wastewater using steel slags produced in Europe[J]. Water Research, 2012, 46(7): 2376-2384. doi: 10.1016/j.watres.2012.02.012 [16] MA H, GAO X L, CHEN Y H. Fe(II)enhances simultaneous phosphorus removal and denitrification in heterotrophic denitrification by chemical precipitation and stimulating denitrifiers activity[J]. Environmental Pollution, 2021, 287(5): 117668. [17] 杨珍珠, 范瑞江. 两级石灰沉淀法在高浓度含氟含磷污水处理中的应用[J]. 化肥设计, 2015, 53(6): 34-37. doi: 10.3969/j.issn.1004-8901.2015.06.009 [18] 周瑾, 宋同林, 李鹏涛. 加碱混凝沉淀工艺在处理含磷废水中的应用[J]. 新疆环境保护, 2006, 28(4): 19-21. doi: 10.3969/j.issn.1008-2301.2006.04.005 [19] PETZOLDT C S, LEZCANO J P, MOREDA I L. Removal of orthophosphate and dissolved organic phosphorus from synthetic wastewater in a combined struvite precipitation-adsorption system[J]. Journal of Environmental Chemical Engineering, 2020, 8(4): 4634. -











 下载:
下载: