-
炼化企业的污水集输系统和污水处理厂很难做到完全密闭。管渠、构筑物和设备等均有挥发性污染物从水体逸出并形成废气排放,成为炼化企业重要的恶臭污染物排放源。为此,污水处理厂的恶臭污染治理已成为炼化企业污染防治体系中的重要组成部分[1-2]。污水处理厂排放的恶臭气体有2类:一是物化设施和污油罐、浮渣池等处散发的高浓度臭气,在组成上以非甲烷总烃为主,硫化氢、氨和有机硫化物等恶臭物质浓度也比较高;二是生化设施和污泥池(间)等处散发的低浓度臭气。高浓度臭气适合采用燃烧法(催化氧化燃烧、蓄热氧化燃烧等)处理。低浓度臭气多采用碱液洗涤、吸附和生物除臭等方法处理[3]。
国内外对恶臭污染的源头控制和减排都有严格的要求[4]。炼化企业已全面执行《石油炼制工业污染物排放标准》(GB 31570-2015),对废水处理有机废气收集处理装置的苯(4 mg·m−3)、甲苯(15 mg·m−3)、二甲苯(20 mg·m−3)和非甲烷总烃(120 mg·m−3)都提出了具体要求和更高标准。相对于《恶臭污染物排放标准》(GB 14554-1993),《恶臭污染物排放标准(征求意见稿)》(2018版)对8项恶臭污染物指标的排放限值作出了更加严格的规定。
以往的研究多关注污水处理设施所释放恶臭气体的组成特性,主要目的是为恶臭治理工艺设计提供依据[3, 5-6],而对恶臭治理设施所排放气体的组成及健康风险评估,则研究较少。本研究以北方某炼化企业污水处理厂为研究对象,对其3套恶臭治理设施的外排气体组成特征进行了综合分析,确定了关键的致臭化合物种类,评估了恶臭污染物的综合健康风险,并有针对性地提出相应污染控制策略,以期为新标准下炼化企业恶臭污染管理与防控工作的进一步完善提供参考。
全文HTML
-
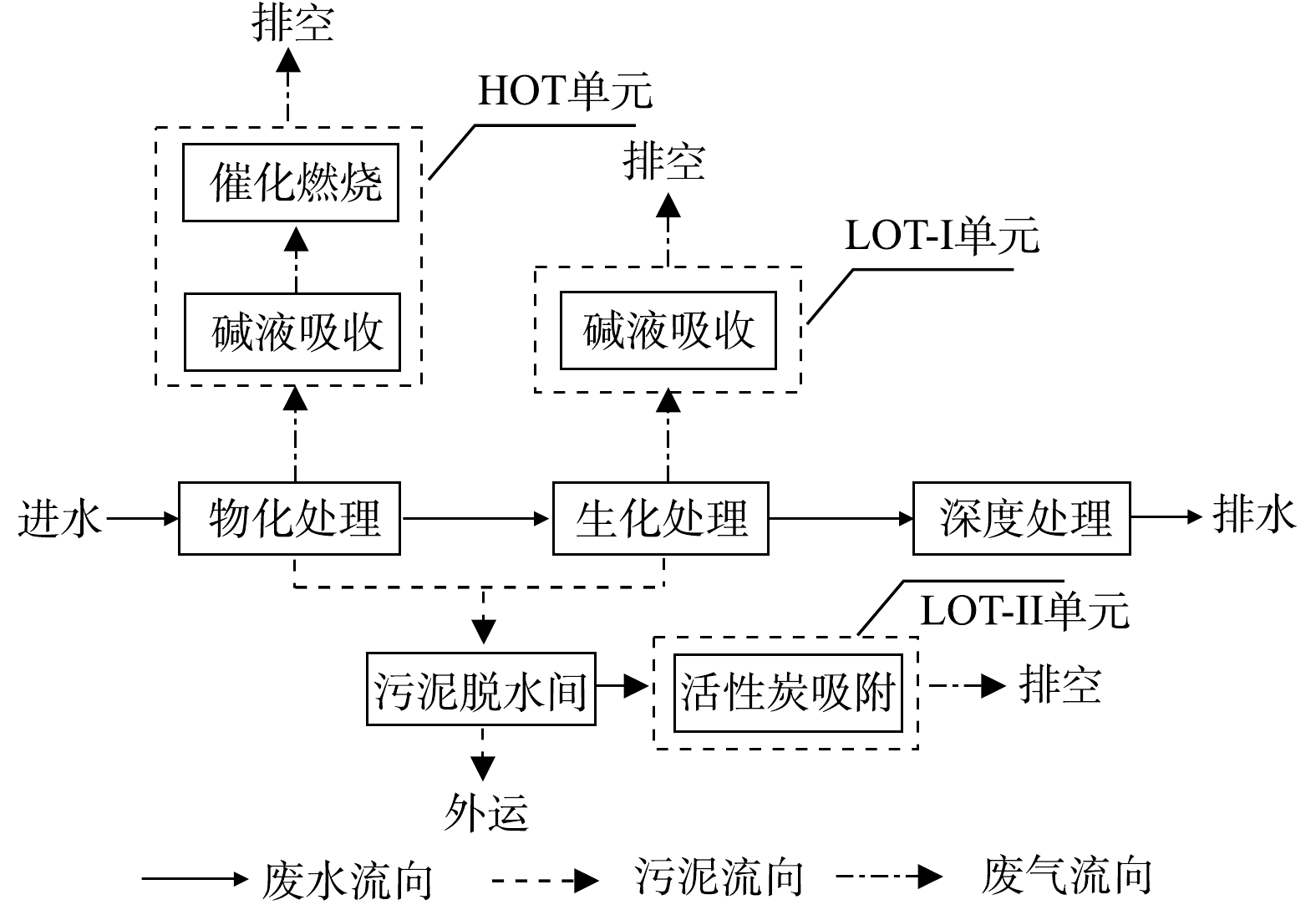
以某炼化企业污水处理厂恶臭治理设施排放气为研究对象。如图1所示,物化设施产生的高浓度臭气采用“碱液吸收+催化燃烧”工艺进行治理,标记为高浓度臭气治理(high-concentration odor treatment, HOT)单元。生化设施产生的低浓度废气采用“碱液吸收”工艺处理,标记为低浓度臭气处理单元I(low-concentration odor treatment, LOT-Ⅰ)。污泥脱水间产生的低浓度废气采用“活性炭吸附”工艺处理,标记为低浓度臭气处理单元II(LOT-Ⅱ)。臭气采样点位于3套臭气治理单元的排气筒出口,连续采样3次,每次间隔8 h。采样方法按照《固定污染源排气中颗粒物测定与气态污染物采样方法》(GB/T 16157-1996),采用1.5 L Tedlar气袋真空采样。
-
恶臭污染物指标及其检测方法见表1。这些指标包括:《恶臭污染物排放标准(征求意见稿)》中的氨、三甲胺、硫化氢、甲硫醇、甲硫醚、二甲二硫、二硫化碳、苯乙烯和臭气浓度9项指标;《石油炼制工业污染物排放标准》(GB 31570-2015)中的苯、甲苯、二甲苯和非甲烷总烃4项指标;《固定污染源废气挥发性有机物的测定固相吸附-热脱附/气相色谱质谱法》(HJ 734-2014)中的51种挥发性化合物。恶臭污染物浓度值取3次采样检测结果的平均值。
-
单一组分占总检出物质的比例并不能代表其对恶臭的贡献度,因此引入理论臭气浓度(theoretical odor concentration, Cod)以筛选关键致臭物质[7-9]。Cod是恶臭气体中各恶臭污染物组分的质量浓度与嗅觉阈值的比值。根据臭气中各恶臭污染物组分的嗅觉阈值及质量浓度计算Cod, i及该污染源总Cod,并通过各组分Cod, i在总Cod的占比得到其恶臭贡献值Pi,计算公式见式(1)~(5)。
式中: Cod, i为各组分的Cod;Ci为各组分的质量浓度,mg·m−3;COT为各恶臭污染物的嗅觉阈值,mg·m−3;Cod为所有组分的总Cod, i;Pi为各污染物组分恶臭贡献值;Cod, n为区域内各污染源的Cod总和;Pn为区域内各污染源恶臭贡献值。
-
利用非致癌健康风险指数(health risk index, HI)和终生致癌风险(lifetime cancer risk, LCR)评估其非致癌风险和致癌风险。气体主要通过呼吸影响人群健康,因此,根据US EPA环境毒物非致癌物的呼吸吸入参考浓度(inhalation reference concentration, RfC)和致癌物的呼吸吸入单位致癌风险(inhalation unit risk, IUR)计算HI和LCR,计算公式见式(6)~(7)[10]。
式中:Ci为空气中某污染物的质量浓度,mg·m−3;ET为每日暴露时间,取8 h;EF为一年持续暴露频率,取250 d·a−1;ED为暴露持续时间,取25 a;AT为人群平均寿命(LCR取70 a,HI取25 a);IUR为污染物单位致癌风险,m3·mg−1;RfC为污染物的非致癌参考基准浓度,mg·m−3[11-15]。
混合源的健康风险值为各污染物危害指数之和,评价过程中不考虑各物质之间的协同和拮抗作用。对于致癌风险,LCR>10−4时,表明有较大的潜在致癌风险;LCR范围为10−6~10−4时,表明存在潜在的致癌风险;LCR<10−6时,表明致癌风险在可以接受的范围内。对于非致癌风险,HI>1时,表明会对人体造成非致癌健康风险;而当HI≤1时,可视为不会对人体造成伤害。
1.1. 样品采集
1.2. 分析指标与方法
1.3. 恶臭贡献分析
1.4. 健康风险评估
-
该炼化污水处理厂3个臭气治理单元外排气体中共检出42项恶臭物质,包括氨、硫化氢、三甲胺以及其他39种恶臭物质(2种烷烃、1种烯烃、11种芳香烃、4种有机硫化物、13种含氧化合物和8种卤代烃)。其中,LOT-Ⅰ单元检出的恶臭物质种类最多,HOT单元检出的种类最少(见表2)。
HOT单元排放的主要恶臭污染物为氨、硫化氢、烷烃、芳香烃、甲硫醇、甲硫醚、二硫化碳和非甲烷总烃。其中,非甲烷总烃含量最高,接近GB 31570-2015中规定的质量浓度限值。烷烃和芳香烃的质量浓度也较高,这主要是因为HOT单元的臭气来源为隔油池、气浮池等物化设施,这些设施中油类物质产生大量的非甲烷总烃和芳香烃等恶臭污染物。吕秀荣等[16]对某稠油炼制污水隔油和气浮处理系统进行恶臭物质筛查的结果与本研究一致。LOT-Ⅰ单元排放的主要恶臭污染物是氨、甲硫醇、硫化氢、二硫化碳和非甲烷总烃。其中,甲硫醇含量比HOT和 LOT-Ⅱ单元要高,这主要因为LOT-Ⅰ单元的臭气来源是生物处理设施,有较多的甲硫醇等生物降解产物[17]。污泥脱水间是炼化污水厂重要的恶臭污染源[18-20]。LOT-Ⅱ单元排放的主要恶臭污染物是氨、硫化氢、烷烃、二硫化碳和非甲烷总烃,氨、硫化氢含量与LOT-Ⅰ单元基本一致,但臭气浓度低。
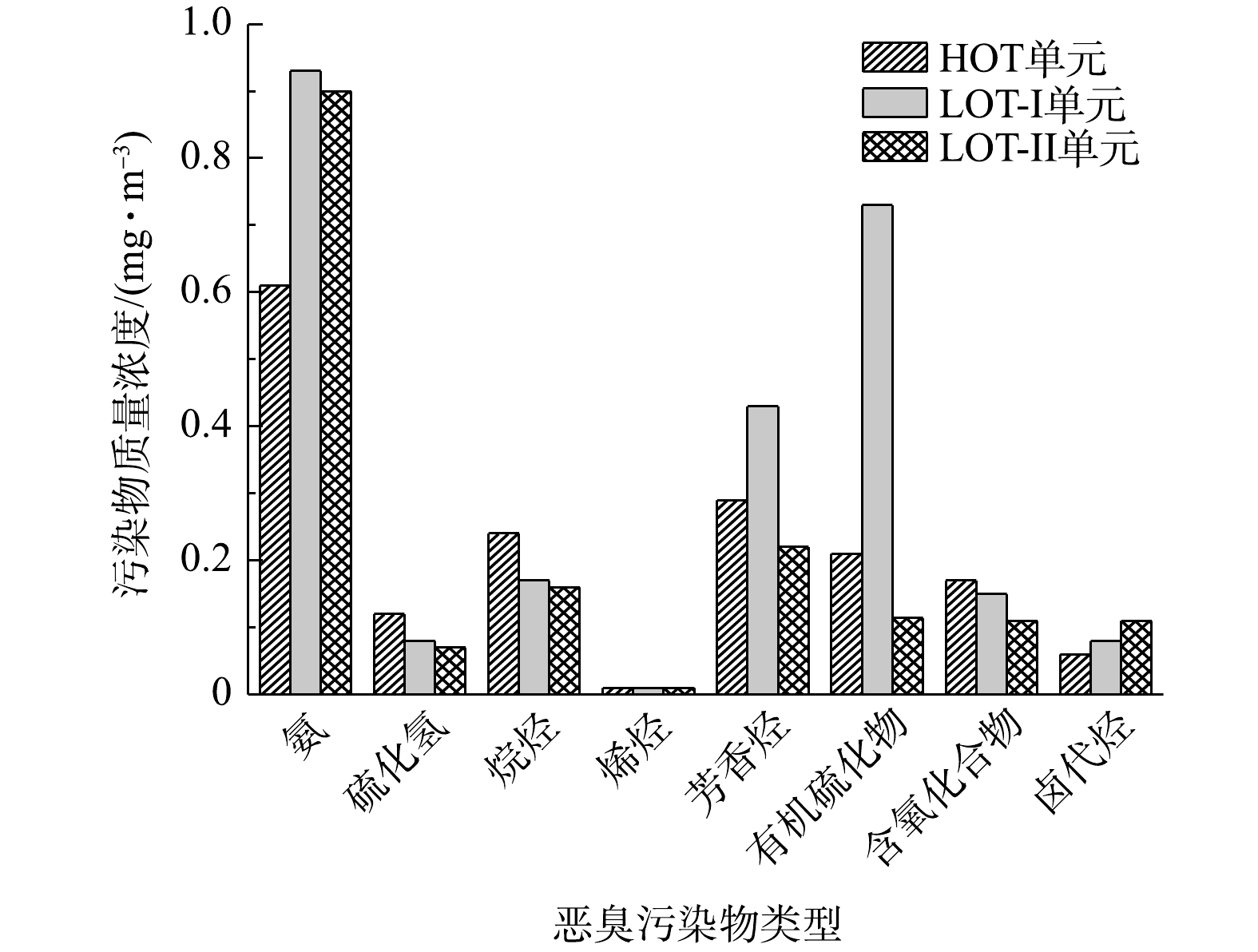
将恶臭污染物分为氨、硫化氢、烷烃、烯烃、芳香烃、含氧化合物、卤代烃及有机硫化物8种类型。各类型恶臭污染物排放浓度见图2。其中,氨的浓度最高,分别占HOT、LOT-Ⅰ和LOT-Ⅱ单元外排恶臭总浓度的35.7%、36.0%和53.1%。烷烃和芳香烃是炼化企业的特征恶臭污染物[21],经过恶臭治理设施处理后其浓度仍较高。二者排放总浓度分别占HOT、LOT-Ⅰ和LOT-Ⅱ单元外排恶臭总质量浓度的30.6%、23.0%和22.0%。排放的有机硫化物质量浓度分别占HOT、LOT-Ⅰ和LOT-Ⅱ单元外排恶臭总质量浓度的12.3%、28.3%和6.7%。HOT和LOT-Ⅰ单元外排有机硫化物主要是甲硫醇,LOT-Ⅱ单元主要是二硫化碳和甲硫醇。含氧化合物和卤代物种类较多,但3个臭气单元的排放质量浓度水平均较低。硫化氢质量浓度较低,3个臭气单元的排放质量浓度分别为0.12 mg·m−3、0.08 mg·m−3和0.07 mg·m−3,分别占HOT、LOT-Ⅰ和LOT-Ⅱ单元外排恶臭总质量浓度的7.0%、3.1%和4.1%。烯烃类仅含有1,3-丁二烯,在3个单元外排气中的浓度均很低。以往对炼化企业污水处理厂各处理工艺段臭气组成的调研发现,主要污染物类型包括非甲烷总烃、有机含硫化合物、苯系物、烷烃和环烷烃等[6, 21-22]。由此可见,HOT、LOT-Ⅰ和LOT-Ⅱ单元处理前后,恶臭污染物的主要类型基本不变,只是污染物浓度变化较大。
-
根据中国化学物质性质信息及日本环境卫生中心对恶臭物质嗅阈值的研究[23-24],3个臭气治理单元外排气中检测出的恶臭污染物嗅阈值见表2。硫化氢、甲硫醇、甲硫醚和二甲二硫等恶臭污染物排放浓度虽然没有超过GB 14554-1993的要求,但其质量浓度大于其嗅阈值。另外,4-乙基甲苯虽未列入控制标准,但其质量浓度大于嗅阈值。这些恶臭污染物可能对炼化企业污水厂外排气体臭气浓度贡献较大。
臭气治理单元外排气中有明确嗅阈值的32项恶臭污染物的Cod和恶臭贡献值Pi见表3。甲硫醇在3个臭气治理单元外排气中的Cod均为最大,其中以LOT-Ⅰ单元的甲硫醇Cod最大,数值超过3 500,并且甲硫醇在3个臭气治理单元外排气中的Pi均超过了0.7;硫化氢的Cod均超过100,为所有恶臭污染物中Pi第二高的物质。因此,甲硫醇和硫化氢是该炼化污水处理厂外排气体中的关键致臭物质。另外,甲硫醚、二甲二硫和4-乙基甲苯的Cod为1~10。以上恶臭污染物对该污水厂的恶臭贡献最大。实际排放的氨质量浓度最高,但因其嗅阈值较高,故其恶臭贡献度相对较小。虽然芳香烃、烷烃、卤代烃和含氧化合物的质量浓度也较高,但由于其嗅阈值较高,故其恶臭贡献度较小。垃圾处理厂与本研究中污水处理厂的主要恶臭贡献物质具有一定相似度[25]。然而,不同类型污水处理厂主要恶臭贡献物质并不相同:城市污水处理厂的主要恶臭贡献物质为硫化氢、氨和甲硫醚[26- 27];发酵类制药企业污水处理厂的恶臭主要由硫化氢、丁硫醇和异丙硫醇贡献[28]。
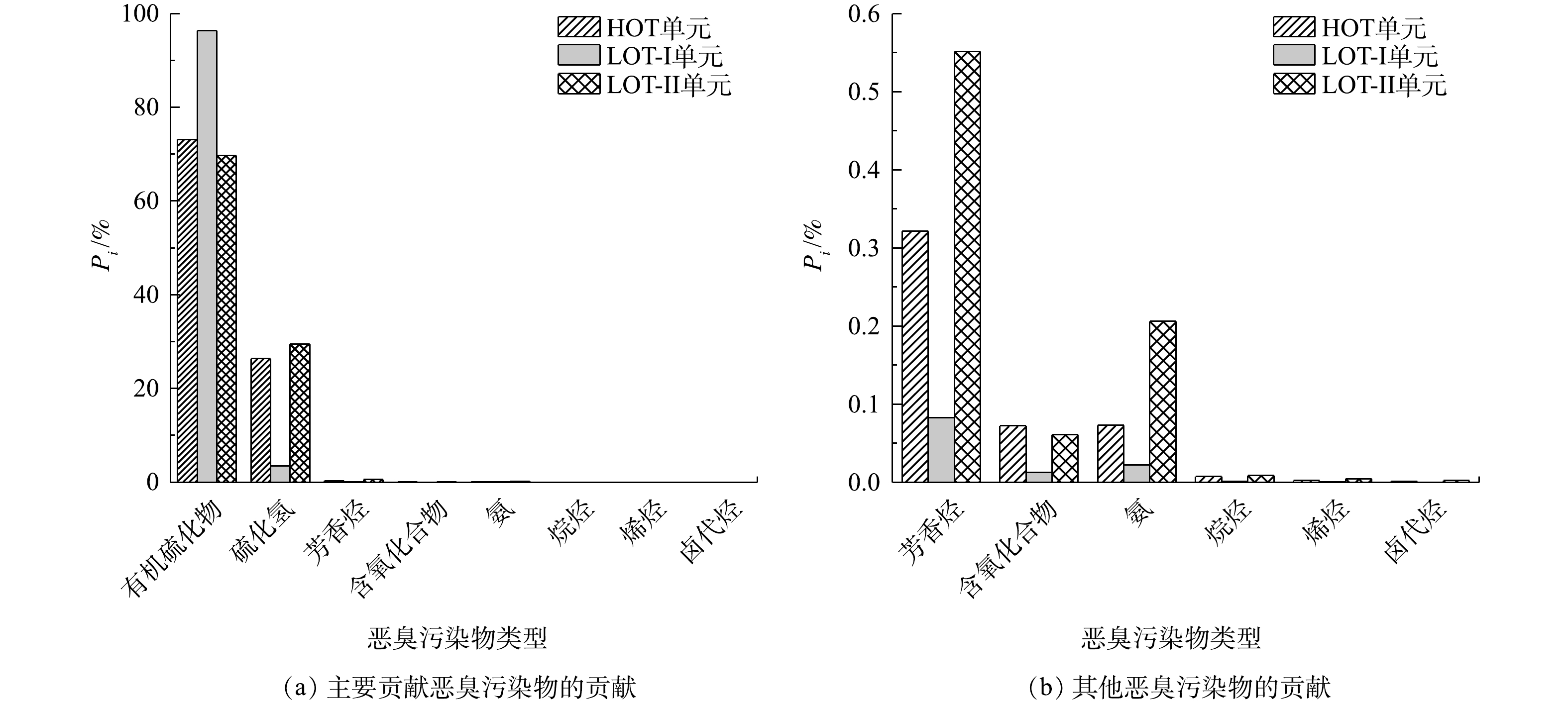
各污染物类型对恶臭污染程度的贡献度见图3。其中,有机硫化物对恶臭污染的贡献度最高,3个臭气治理单元外排气中Pi均超过70%,HOT和LOT-Ⅱ单元外排气的硫化氢Pi超过25%。因此,炼化污水处理厂的关键致臭污染物为有机硫化物和硫化氢。另外,芳香烃、含氧化合物和氨亦是主要致臭污染物。杜亚峰等[29]将炼油污水处理厂恶臭污染物分为苯系物、卤代烃、有机硫化物和含氮有机物4类,其中苯系物与有机硫化物为主要致臭污染物,这与本研究结果基本相同。不同类型污水处理厂的主要致臭污染物也不相同,如生活垃圾堆肥产生的主要致臭污染物类型是含氧有机物,其次是芳香烃类[8];汽车制造业的致臭污染物主要是卤代烃类和芳香烃类,1,3-丁二烯是其典型致臭物质[30]。
表3中,3个恶臭治理设施外排气对炼化污水处理厂区域总恶臭污染贡献值Pn数据表明,LOT-Ⅰ单元外排气体对恶臭污染的贡献值占76.69%,为关键致臭污染源。甲硫醇在LOT-Ⅰ单元外排气中的Pi占96.37%,故应控制生物处理设施臭气治理单元排放的甲硫醇。
-
对恶臭治理设施外排气体中的部分恶臭污染物进行了健康风险评估。鉴于化学物质的IUR和RfC信息不全,故本研究仅对检出的20种恶臭污染物进行健康风险评估。根据3个臭气治理单元排气筒高度、排气量、气体温度等数据,计算了各恶臭污染物的最大地面浓度,并以其为依据计算出各恶臭污染物的HI和LCR(见表4)。3个臭气治理单元外排气的非致癌和致癌健康风险由高到低均为LOT-Ⅰ单元>LOT-Ⅱ单元>HOT单元。20种恶臭污染物的HI均远小于1.0,其中,1,3-丁二烯是非致癌风险最高的恶臭污染物,苯和四氯乙烯次之。3个臭气治理单元外排气中恶臭污染物的HItotal相差不大,均处于10−4数量级,非致癌健康风险极低。所有单元排放的恶臭污染物LCR远小于10−6,二溴一氯甲烷和LOT-Ⅰ单元排放的1,1,2,2-四氯乙烷为致癌风险最高的恶臭污染物,1,3-丁二烯和苯次之。3个臭气治理单元外排气中恶臭污染物的LCRtotal相差较小,总致癌风险在10−8数量级。由上述可见,炼化企业污水处理厂此前通过对臭气进行治理,有效控制了恶臭污染物对人群的致癌和非致癌健康风险,降低了其对炼厂职工和附近居民的危害[31]。
-
炼化企业污水处理厂恶臭污染经过治理后,外排气中仍含有一定浓度的特征恶臭污染物,主要为致臭物质甲硫醇、硫化氢、甲硫醚、二甲二硫、4-乙基甲苯,及污染物浓度高的非甲烷总烃和氨。为控制炼厂区域内恶臭污染,保障人群身体健康,应优化和升级恶臭污染治理设施以提高对上述恶臭污染物的控制能力。
HOT单元需主要控制的恶臭污染物为非甲烷总烃、硫化氢、甲硫醇、甲硫醚、二甲二硫、4-乙基甲苯。HOT单元采用的工艺为碱液吸收+催化燃烧,可通过优化碱液吸收工艺方案(如增加碱液浓度、强化传质等)提高硫化氢、甲硫醇、甲硫醚、二甲二硫等含硫物质的吸收效能,减少臭气排放浓度。另外,需要优化催化燃烧工艺,提高非甲烷总烃和有机硫化物等恶臭物质的去除率[6]。若催化燃烧不能达到较好的去除效能,可考虑采用适用性更好、更节能、净化效率更高的蓄热式氧化炉(regenerative thermal oxidizer, RTO)工艺[22, 32-33],以减少恶臭污染物逸出对人群健康的危害。对LOT-Ⅰ单元,需主要控制的恶臭污染物是氨、甲硫醇、硫化氢、甲硫醚、二甲二硫、4-乙基甲苯。其中,甲硫醇是LOT-Ⅰ恶臭污染治理单元主要的恶臭气体物质。LOT-Ⅰ单元采用的碱液吸收工艺,碱液吸收对氨、甲硫醇、甲硫醚、二甲二硫等恶臭物质的去除效能有限,而且不适用于4-乙基甲苯等恶臭物质的去除。因此,需要在保障碱液吸收工艺运行效能的基础上对LOT-Ⅰ单元进行相应改造,如增加活性炭吸附或催化燃烧等工艺[34-35]。LOT-Ⅱ单元外排气中恶臭污染物浓度较低,但仍需控制氨、硫化氢、4-乙基甲苯等恶臭物质排放。LOT-Ⅱ单元采用的工艺为活性炭吸附。为进一步减少氨及硫化氢排放浓度,可有针对性地增加碱液吸收工艺,也可通过优化活性炭吸附塔运行参数以提高4-乙基甲苯等的去除率[36]。
2.1. 外排气体恶臭污染物组成特征分析
2.2. 恶臭污染物贡献分析
2.3. 健康风险评估
2.4. 污染控制策略
-
1)在炼化企业污水处理厂恶臭污染治理设施的外排气体中,共检出42种恶臭物质,主要污染物为氨、有机硫化物、芳香烃和硫化氢;甲硫醇和硫化氢为关键致臭物质,且有机硫化物对臭气总浓度的贡献度最高;在该污水处理厂中,污水生化处理设施臭气治理单元对恶臭的贡献值最高。
2)该污水处理厂所有外排气中恶臭污染物的非致癌和致癌风险极低,其中污水生化处理设施臭气治理单元外排气中恶臭污染物的非致癌健康风险指数和终生致癌风险最高。
3)建议优化物化处理设施臭气治理单元“碱液吸收+催化燃烧”工艺,或采用“碱液吸收+蓄热式氧化炉”处理工艺;生化处理设施臭气治理单元增加“活性炭吸附”或“催化燃烧”工艺;污泥脱水间臭气治理单元增加“碱液吸收”工艺。



 下载:
下载: