-
纳米FeS作为一种非常有前景的工程修复材料,已经广泛应用于环境修复和危险废物处理中[1-2]。FeS是一种高效还原剂,由于Fe2+和S2−可以作为电子供体,FeS对土壤和地下水中常见污染物有很好的处理效果,例如氯乙烯、六氯乙烷、三氯乙烯、四氯化碳、Cr(Ⅵ)和As等[3-6]。然而传统利用共沉淀的方法合成的FeS纳米颗粒,由于范德华力大、表面能高以及密度大等因素,裸露FeS易于团聚失活,使其在迁移过程中沉积截留在多孔介质当中,导致其迁移受阻[7]。化学反应活性较低的裸露FeS纳米颗粒难以在污染土壤和含水层介质中分散,限制了其在环境修复中的作用[8]。因此,必须将FeS纳米颗粒进行改性,从而增加其稳定性、迁移能力和反应活性。
针对上述现象,一些学者在裸露FeS表面涂覆稳定剂(聚合物或表面活性剂),通过提供空间位阻和静电斥力来限制其聚集[9]。鉴于大分子链上存在大量的羧基和羟基,聚合物稳定剂羧甲基纤维素钠被广泛应用于纳米颗粒(NZVI、FeS)的改性,其可以在纳米粒子的表面形成负电荷,从而提供粒子间的静电排斥力,以提高纳米材料的稳定性和迁移能力[7, 10-11]。海藻酸钠(SA)是多糖类生物大分子,由于其独特的结构性能、安全性和可生物降解性,被广泛用于食品和环境中。从理论上讲,SA可以类似于CMC用作稳定剂,但关于其利用的研究很少[12]。淀粉(ST)也被认为是抑制纳米颗粒(Fe/Pd、Fe3O4和ZVI)聚集的稳定剂[13-14]。GG是从一种豆科植物(瓜尔豆)中提取的高纯化天然多糖,作为剪切稀化流体,在多孔介质中迁移时由于剪切力的作用,可以有效地提高纳米颗粒的迁移能力[15]。FeS纳米材料经过这些高分子聚合物改性之后,不仅能阻碍纳米颗粒团聚,减小粒径,还能提高稳定性,增强纳米材料的反应性及迁移性能[16-18]。
本文利用无毒、低成本、环境友好的4种聚合物作为FeS纳米材料的稳定剂,制备出稳定的CMC-FeS、ST-FeS、GG-FeS和SA-FeS纳米材料,综合研究了改性FeS纳米颗粒的抗沉降性能,在饱和多孔介质中的迁移特性及其稳定化FeS纳米颗粒对地下水中Cr(Ⅵ)去除效率的影响,以期为FeS纳米材料在土壤和地下水的修复提供参考。
全文HTML
-
七水合硫酸亚铁(FeSO4·7H2O)、九水硫化钠(Na2S·9H2O)和铬酸钾(K2Cr2O7)购于阿拉丁试剂(上海)有限公司;氢氧化钠(NaOH)、盐酸(HCl)、氯化钠(NaCl)和过氧化氢(H2O2)购于天津福晨化学试剂有限公司,以上试剂均为分析纯;羧甲基纤维素钠 (CMC)、淀粉(ST)、瓜尔胶(GG)和海藻酸钠(SA),购自国药集团化学试剂有限公司,均为化学纯。实验用水均为无氧去离子水(用N2吹脱至少1 h)。石英砂用标准筛进行筛分,分别得到粗砂(0.50~1.00 mm)、中砂(0.25~0.50 mm)和细砂(0.10~0.25 mm)。石英砂在使用之前,需按照MATTISON 等[19]所采用的方法将石英砂进行清洗以去除其表面包含的金属氧化物和有机物。
-
裸露 FeS的制备:在手套箱(95%N2+5%H2)中,先将0.316 g FeSO4·7H2O溶于50 mL无氧去离子水中,得到0.023 mol·L−1的FeSO4·7H2O溶液,将0.273 g Na2S·9H2O溶于50 mL无氧去离子水中,得到0.023 mol·L−1的Na2S·9H2O溶液,将配制的0.023 mol·L−1的FeSO4·7H2O溶液加入100 mL去离子水中,然后逐滴将配制的Na2S·9H2O溶液加入上述体系,静置24 h得到500 mg·L−1的裸露 FeS储备液。待静置结束后,将溶液在离心机上分离,分离出的物质多次水洗,即得到未改性FeS纳米材料。
改性FeS(CMC-FeS、ST-FeS、GG-FeS和SA-FeS)的制备:在手套箱(95%N2+5%H2)中,将0.023 mol·L−1的FeSO4·7H2O溶液分别加入到100 mL CMC、100 mL ST、100 mL GG和100 mL SA(均为1%)溶液中,再将0.023 mol·L−1的Na2S·9H2O溶液加入上述体系,静置24 h得到500 mg·L−1的改性 FeS储备液。待静置结束后,将溶液在离心机上分离,分离出的物质多次水洗,即得到改性FeS纳米材料。
使用JSM-7800F型超高分辨率场发射扫描电子显微镜(SEM)来对纳米材料的形貌特征、颗粒大小、分散性及元素组成进行表征;使用D/Max-2500型X射线粉末衍射仪(XRD)对所制备的材料进行表征以确定其物相和晶型;使用红外光谱(FTIR)分析纳米材料化学结构;使用Litesizer™ 500动态光散射纳米粒度测量仪测定纳米材料的水动力学直径和Zeta电位。
-
将新鲜制备的500 mg·L−1的纳米材料超声处理30 min,然后将40 mL的纳米颗粒悬浮液从烧瓶反应器中转移到50 mL的玻璃瓶中。通过观测沉降距离和溶液颜色变化分析抗沉降性能,并用照片记录。同时,每隔一段时间(1、3、5、10、20、30、60、720、1 440 min)在上层溶液中取样,采用邻菲罗啉比色法测量其中的总铁浓度。
-
将已经清洗过的干燥的砂均匀地填充在内径为1 cm,长度为10 cm的玻璃柱内。待填充完毕,首先将砂柱用CO2气体(纯度>99%)进行冲气,用来排除砂柱内残余的空气。然后采用100 mL的去离子水以3 mL·h−1的速率冲洗砂柱。由于土壤柱内空气已经被CO2气体置换,而CO2气体能够溶于水,因此采用这方法可以比较容易地使土壤柱达到饱和含水状态。最后采用大约180 mL的背景电解质溶液(背景溶液为5 mmol·L−1 NaCl)冲洗砂柱,使砂柱内达到平衡状态。实验过程中,使用蠕动泵采用自下而上的方式来对砂柱进行注射。
在开始砂柱实验之前,首先配置好FeS纳米材料的注射液,将FeS储备液与适量的背景溶液混合,然后用磁力搅拌器充分搅拌1 h;将搅拌均匀的注射液转移到100 mL的注射器中,然后用注射泵以6.6 mL·h−1的速度注入到砂柱内;待纳米材料在砂柱中的迁移达到平衡后,用相应的背景电解质溶液(不含FeS)来冲洗砂柱,直到流出液不能再检测出Fe浓度。在砂柱的终端每间隔5 min收集流出的溶液,在24 h内完成测样,Fe质量浓度采用邻菲罗啉比色法测量。
-
所有实验均在40 mL玻璃瓶中进行,在12.5 mL无氧去离子水中加入10 mL 50 mg·L−1的K2Cr2O7 溶液,用HCl和NaOH调节溶液pH到7±0.1,然后再向该体系中加入2.5 mL 500 mg·L−1的裸露 FeS或改性FeS纳米材料,将玻璃瓶置于恒温振荡箱(25 ℃)中以200 r·min−1振荡180 min,采用二苯碳酰二肼分光光度法测定其中Cr(Ⅵ)的质量浓度。
1.1. 实验试剂与介质
1.2. 材料制备及表征
1.3. 抗沉降实验
1.4. 在饱和多孔介质中的迁移实验
1.5. 反应性实验
-
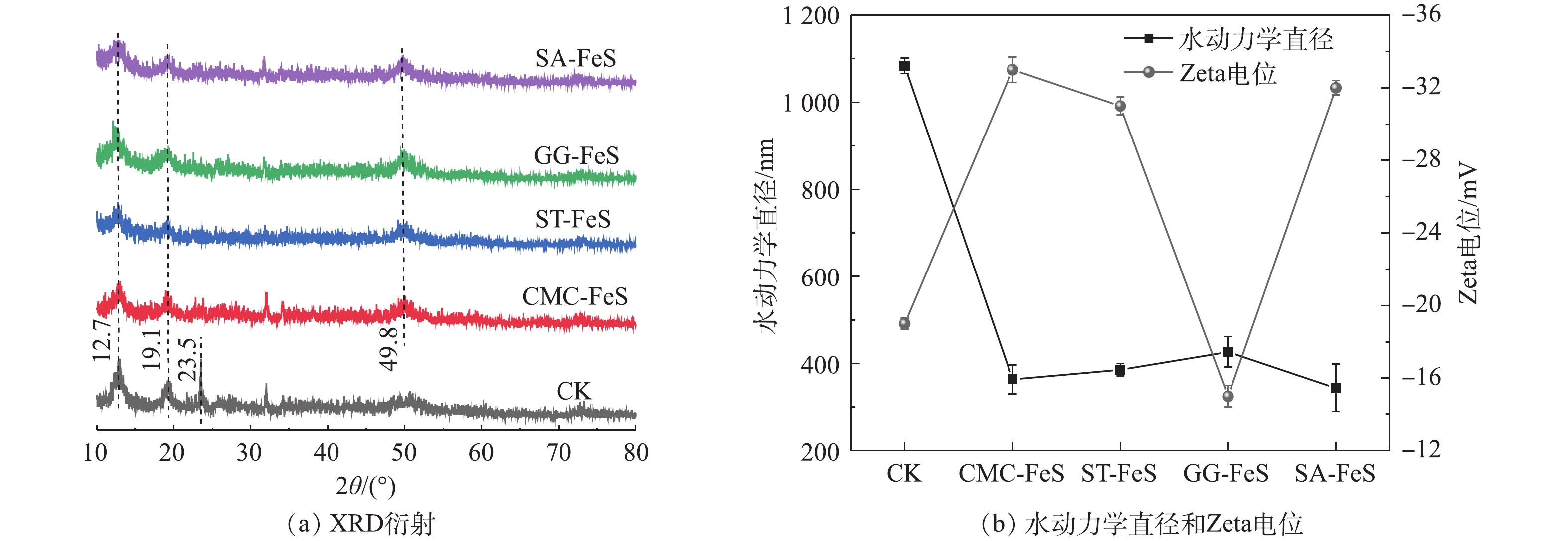
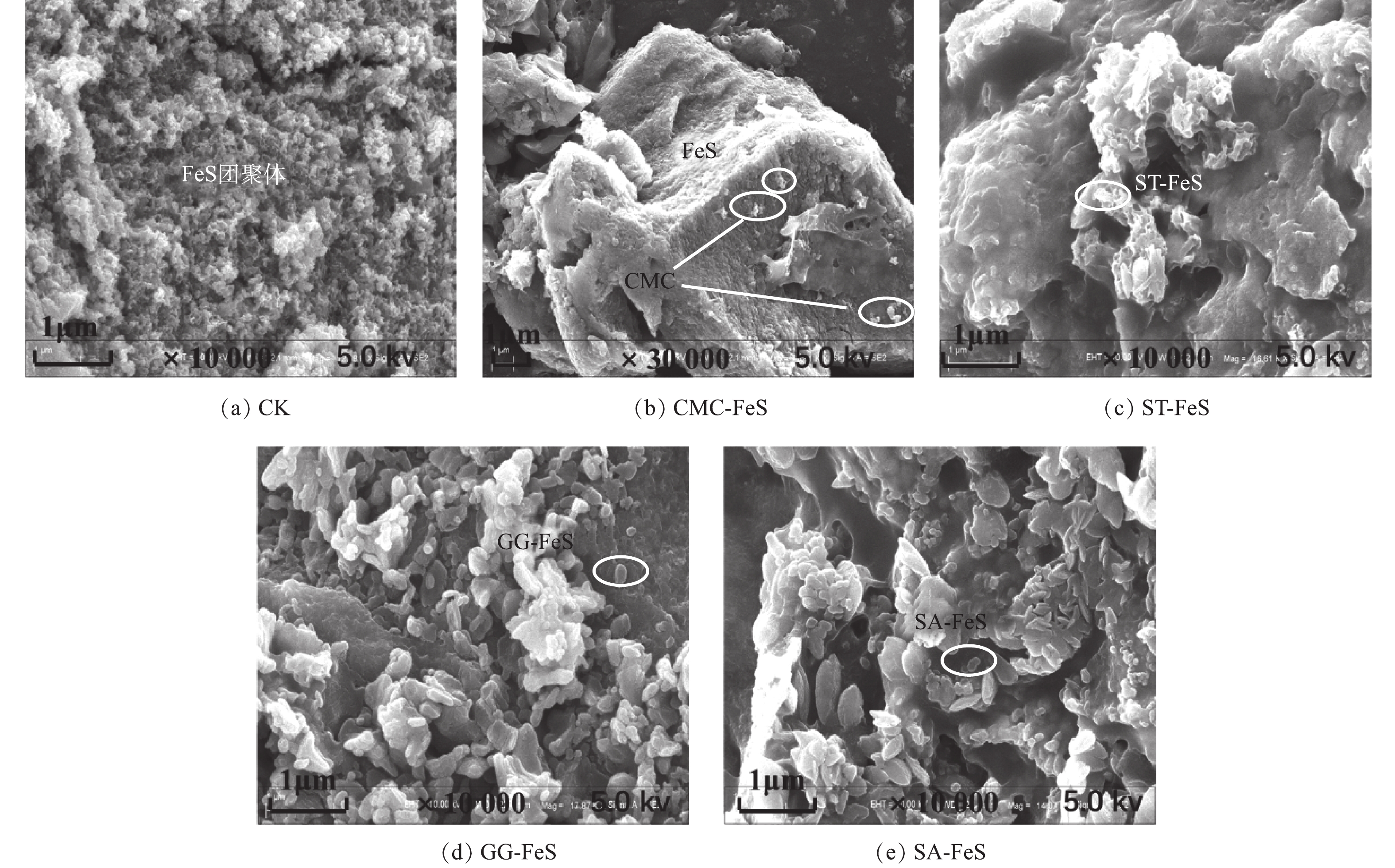
未改性和4种改性FeS纳米材料的SEM表征结果如图1所示,裸露FeS纳米颗粒呈丝状,但由于范德华作用力,其已经凝聚成较大的链状团聚体。经过羧甲基纤维素钠、淀粉、瓜尔胶和海藻酸钠改性以后,改性FeS纳米颗粒比裸露FeS的分布更加分散和均匀,只有少量发生团聚。XRD衍射能够提供纳米材料的晶体组成。由图2(a)可知,未改性和改性FeS纳米颗粒都在2θ为12.7°和19.1°出现明显的衍射峰,裸露FeS在2θ为23.5°的衍射峰消失,但改性FeS却在2θ为49.8°出现新的衍射峰,2θ为12.7°和23.5°为无定型FeS特征峰,而2θ为19.1°和49.8°分别对应于(001)和(112)晶型[20]。这说明稳定剂的加入可能抑制了制备过程中FeS的成核和晶体生长,FeS经过改性以后,晶型可能会发生一定程度的改变。未改性和改性FeS纳米颗粒的水动力学直径和Zeta电位如图2(b)所示,相比裸露FeS (1 084±21) nm,经过CMC、ST、GG和SA改性后FeS纳米颗粒的水动力学直径明显减小,分别为 (316±27)、(341±18)、(434±12)和(320±19) nm。此外,相应的Zeta电位由(−19±0.3) mV变化为(−34±0.9)、(−31±0.6)、(−15±1.1)和(−32±1.1) mV,这主要是由于CMC、ST和SA属于阴离子型稳定剂,GG属于阳离子型稳定剂[21]所示。
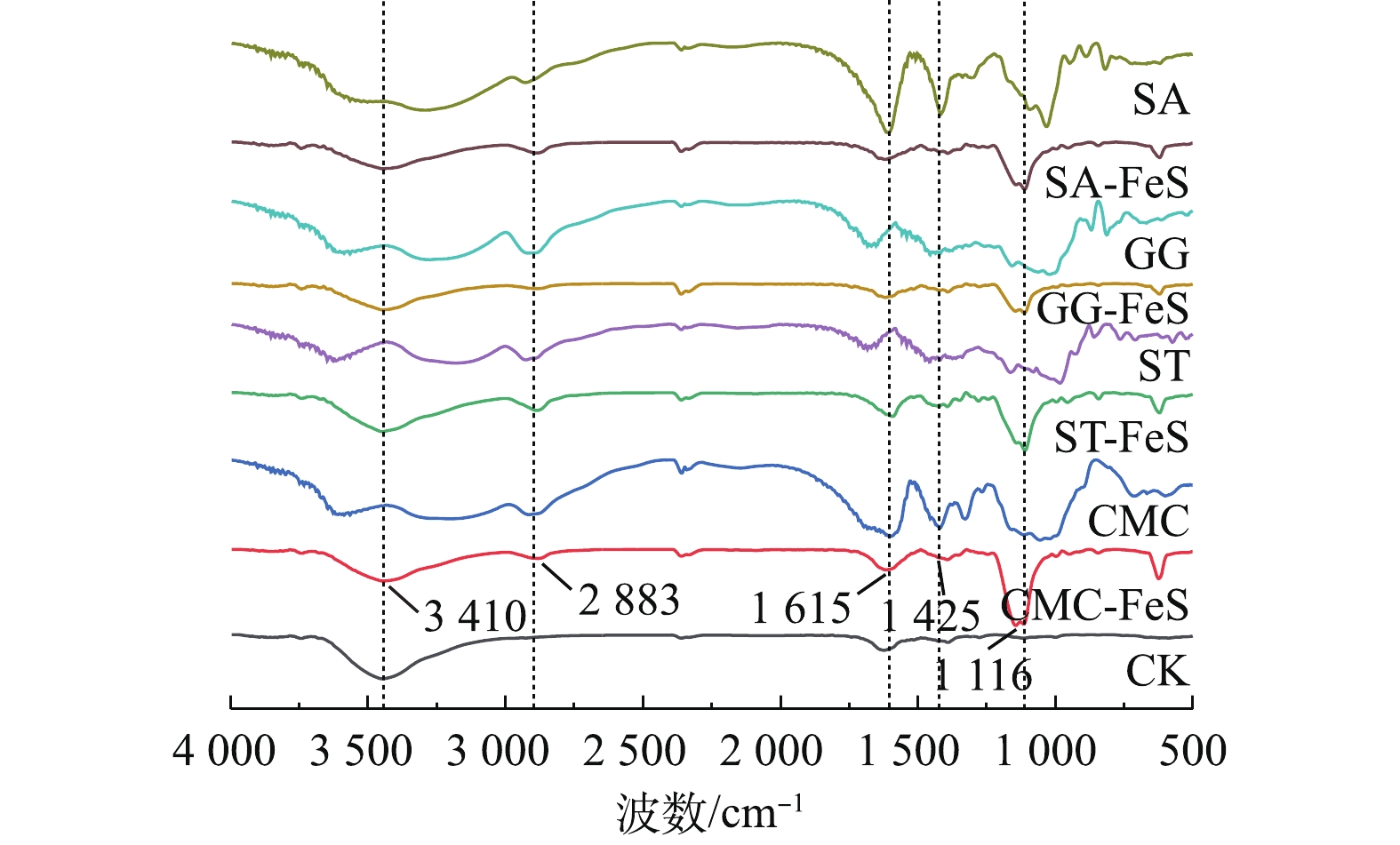
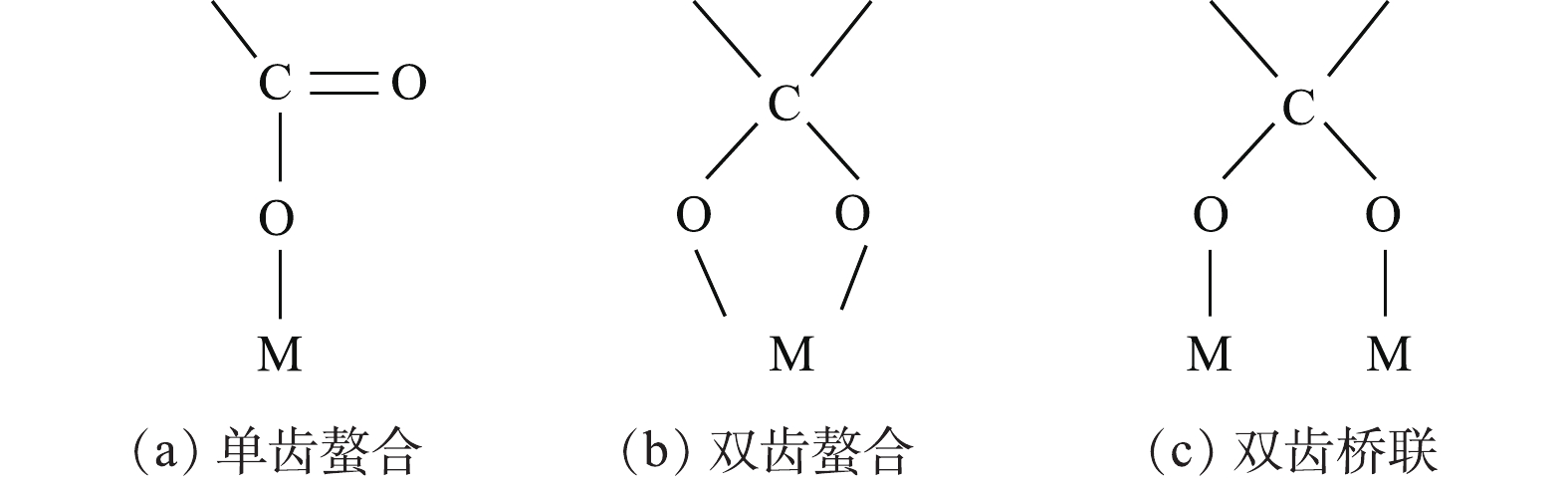
为了阐明CMC-FeS、ST-FeS、GG-FeS和SA-FeS的稳定机理,并进一步了解稳定剂与FeS之间的相互作用,可以使用红外光谱数据来识别他们的吸附构型。由图3可知,裸露FeS的红外光谱图中没有观察到明显的透射峰(3 410 cm−1为水中的O—H),对于4种改性FeS纳米材料,在波数为3 410(O—H)、2 883(非对称CH2)、2 361(C—H)、1 615(不对称COO−)、1 393(对称COO−)和1 116 cm−1(C—O—C)出现明显的透射峰[22-23],表明4种稳定剂(CMC、ST、GG和SA)改性材料成功负载到FeS颗粒上。根据4种稳定剂和改性FeS纳米材料在红外光谱图中正反羧基波数差(Δν),可以判定稳定剂和FeS之间的吸附构型[24-25]:如果红外光谱图中有C—O特征峰,且Δν改性FeS>Δν稳定剂,则吸附构型属于单原子螯合;如果红外光谱图中没有C—O特征峰,且Δν改性FeS<Δν稳定剂,则吸附构型属于双齿螯合;如果红外光谱图中没有C—O特征峰,且Δν改性FeS ≈Δν稳定剂,则吸附构型属于双齿桥接。由图3可知,无C—O特征峰(1 720 cm−1),Δν改性FeS (183、226、214、190 cm−1) ≈ Δν稳定剂 (190、225、219、194 cm−1),4种稳定剂以羧基通过双齿桥接(图4)的形式结合到FeS颗粒表面[25]。
-
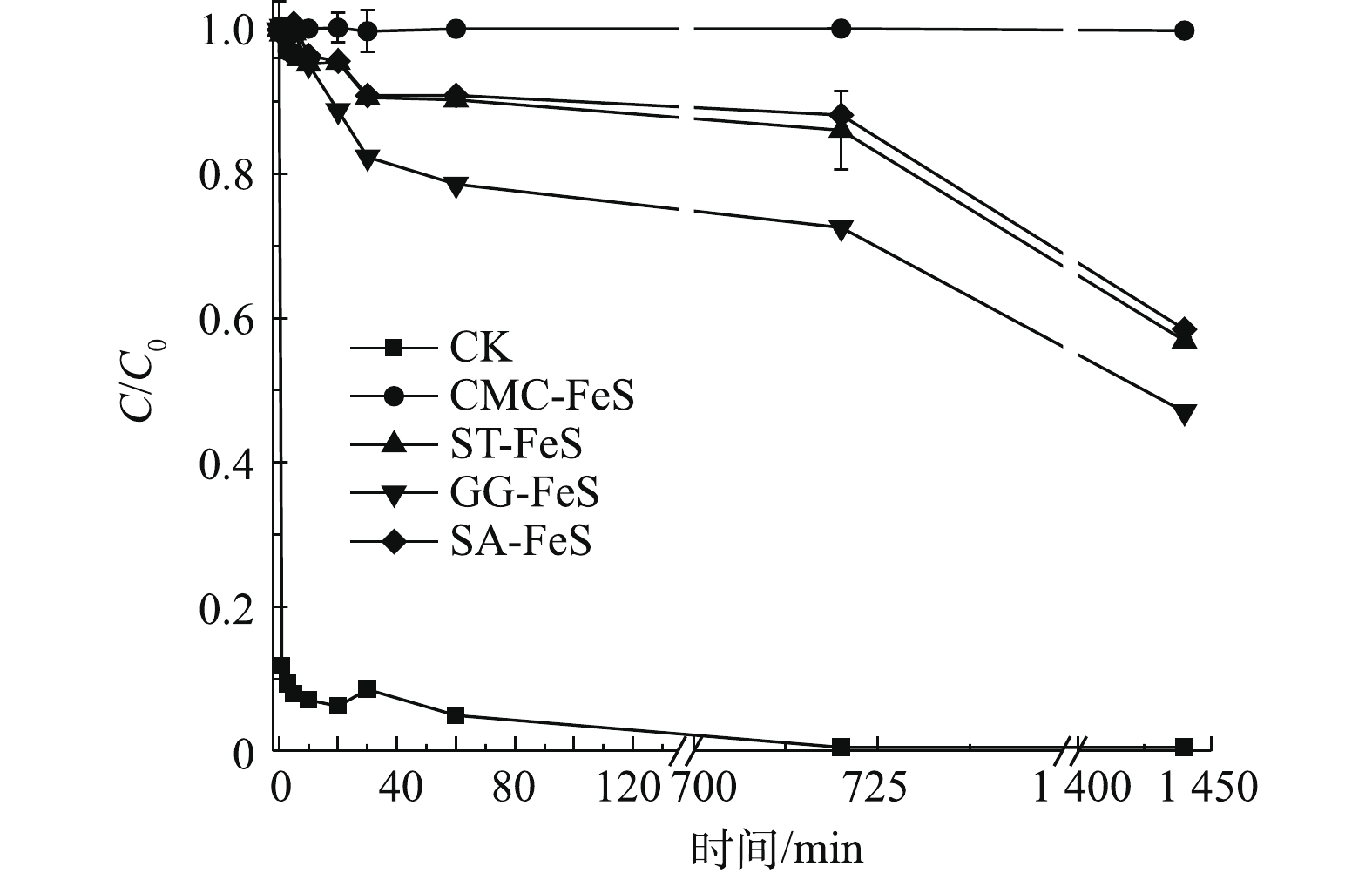
FeS纳米颗粒的反应活性和潜在的现场应用潜能与他们的沉积或聚集状态有关[26],FeS易团聚的特性极大地限制了其工程应用。根据裸露FeS和4种改性FeS纳米材料在24 h内的沉降实验结果(图5)可知,裸露FeS在3 min内基本完全沉降,ST-FeS、GG-FeS和SA-FeS在12 h内也发生完全沉降,但SA-FeS的沉降性能优于ST-FeS和GG-FeS。CMC-FeS在24 h内仍然保持良好的稳定状态,这表明其抗沉降性能最好。由上层溶液中相对铁含量随沉降时间的变化规律(图6)可见,4种稳定剂对FeS抗沉降性能最优为CMC-FeS,其他顺序为SA-FeS> ST-FeS >GG-FeS。值得注意的是,经过24 h沉降,在上层溶液中仍然能检测出一定含量的铁 (2FeS(s)+O2+4H+→2Fe2++2S0(s)+2H2O)[27]。以上结果表明,4种改性FeS的抗沉降性能均高于裸露FeS,说明改性后的FeS纳米材料分散性能较好,能够保持一定稳定性。
有研究[18]表明,石英砂表面的Zeta电位大约为−22 mV。由图3可知,CMC-FeS、ST-FeS、GG-FeS和SA-FeS的Zeta电位分别为−34、−31、−15和−32 mV,说明加入阴离子型稳定剂后,使得FeS颗粒表面的Zeta电位变得更低,增加了颗粒之间的静电斥力,从而增加了FeS纳米材料的抗沉降性能和稳定性。但值得注意的是,虽然阳离子型稳定剂GG增加了FeS颗粒表面Zeta电位,但GG-FeS却仍然能够保持很好的稳定性和抗沉降性能,这主要是因为瓜尔胶大分子结构使FeS表面空间位阻效应增大,使得其能量势垒变大,所以增加了其稳定性和抗沉降性能[18]。因此,4种聚合物能够稳定FeS的主要原因在于静电斥力和空间位阻效应增大,这也有利于增加FeS纳米颗粒在饱和多孔介质中的迁移性能。
-
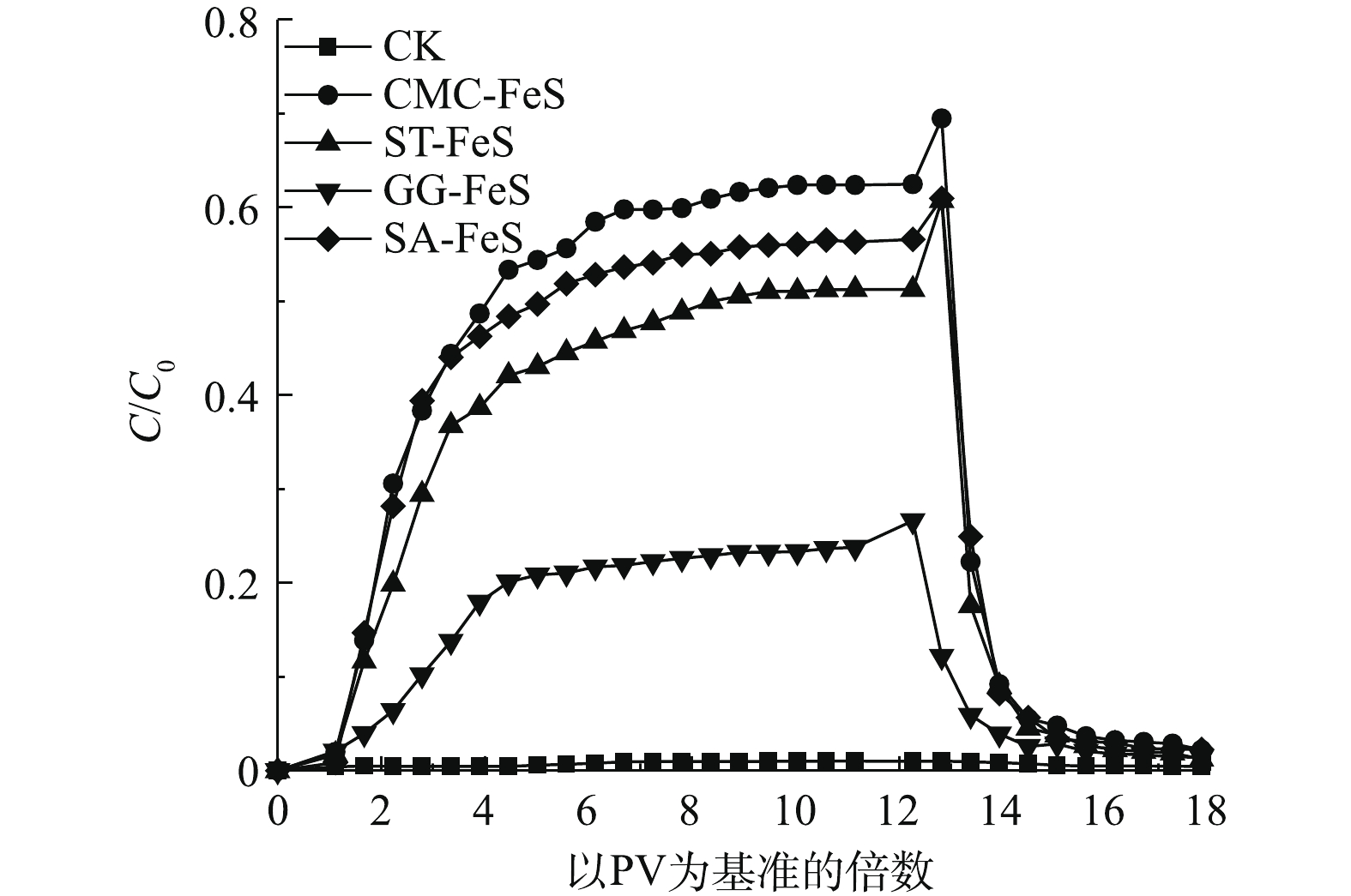
从原位修复的角度来看,要使纳米颗粒到达目标污染区,就必须有较高的迁移率[28]。因此,我们通过柱实验以比较裸露 FeS和改性FeS纳米材料在饱和多孔介质中的穿透曲线(图7)。当FeS纳米材料注射浓度为500 mg·L−1,背景溶液NaCl浓度为5 mmol·L−1、pH=7和流速为6.6 mL·h−1时,裸露FeS迁出率非常小,C/C0仅为0.01。CMC-FeS、ST-FeS、GG-FeS和SA-FeS在11PV (pore volume)时,迁出浓度达到最高,此时C/C0最大,分别为0.62、0.59、0.50和0.25,迁移能力表现为CMC-FeS>SA-FeS>ST-FeS>GG-FeS。如上文所述,阴离子型稳定剂(CMC、SA、ST)使FeS表面Zeta电位更负,增大了颗粒之间的静电斥力,阻碍了颗粒之间的团聚,并且减小了在石英砂上的附着,从而增加了在饱和石英砂介质中的迁出性能。对于阳离子型稳定剂(GG),一方面GG聚合物大分子结构增大了颗粒间的空间位阻效应,阻碍了颗粒间的团聚;另一方面,瓜尔胶属于剪切稀化流体,是非牛顿流体,当在流动时黏性变小时,受到流层之间的剪应力作用,收缩成团发生滚动旋转,从而提高了GG-FeS在饱和多孔介质中的迁移能力。ALBERTO等[29]利用柱实验发现纳米NZVI几乎全部截留在柱子顶端,而GG-NZVI的迁出率C/C0可达0.8。
在饱和稳定流条件下,胶体颗粒在饱和多孔介质中的沉积速率可以通过沉积动力学和滤床模型计算[30-31]。同时根据胶体过滤理论,可以通过计算其最大迁移距离(指胶体颗粒在迁移过程中,99%的颗粒被截留在含水层介质时所迁移过的距离)来判断其迁移能力[32-33]。沉积速率k和最大迁移距离Lmax与C/C0关系如式(1)和式(2)所示。
式中:v为纳米材料注射速率,cm·s−1;φ为多孔介质的孔隙度;l为多孔介质长度,cm。裸露FeS和4种改性FeS纳米材料的沉积速率和最大迁移距离如表1所示。沉积速率k遵循CMC-FeS<SA-FeS<ST-FeS<GG-FeS<裸露FeS的顺序;相反地,最大迁移距离Lmax为CMC-FeS>SA-FeS>ST-FeS>GG-FeS>裸露FeS。相比裸露FeS,CMC-FeS、SA-FeS、ST-FeS和GG-FeS的k值分别减小了76.9%、72.3%、69.2%和29.2%,Lmax值分别增加了296%、254%、233%和114%。因此,在实际污染场地修复中,为提高污染物的去除率,可以选用迁移性能比较好的CMC-FeS和SA-FeS。XIONG等[26]利用CMC-FeS纳米颗粒固定沉积物中的汞,发现CMC-FeS能够在黏土介质中保持很好的流动性,当注射量为18 PV时,迁移率C/C0最大,并且能够明显抑制沉积物中汞的淋出率。ZHANG等[34]的研究表明,零价铁(NZVI)经过SA改性以后,在饱和多孔石英砂介质中的迁移性能明显提高,并且负载SA浓度越高,迁出率越大。
-
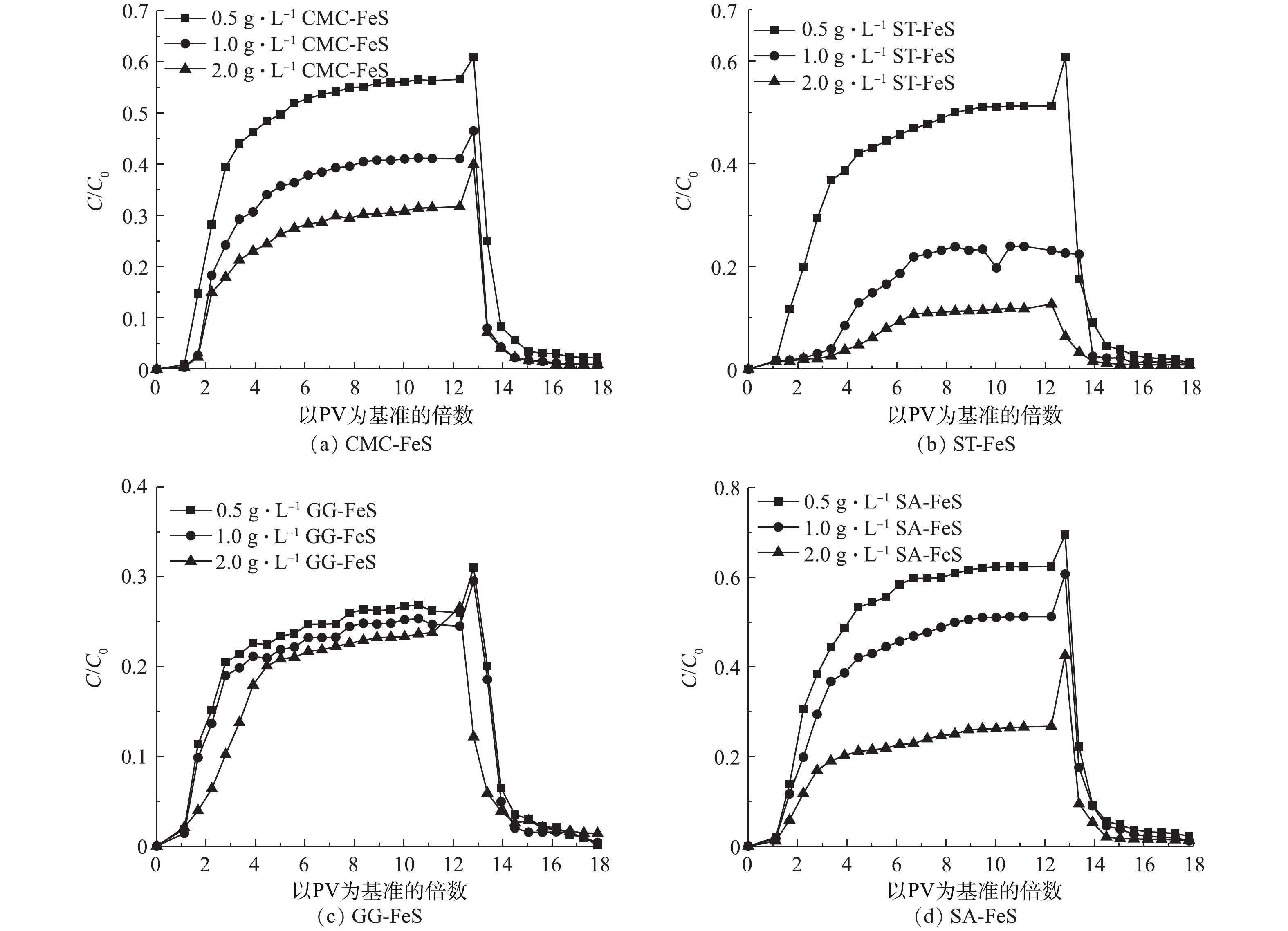
4种改性FeS纳米材料在不同注入质量浓度(0.5、1.0和2.0 g·L−1)下在饱和石英砂介质中的穿透曲线如图8所示。4种改性FeS纳米材料的迁移能力随着注入质量浓度增大而减小。这主要是因为:当一次性注入大量的FeS纳米材料,颗粒不能够及时迁移扩散,填充于含水层介质孔隙中造成孔堵塞,从而阻碍迁移;另一方面,一次性注入较高质量浓度会增加FeS颗粒之间,或FeS和石英砂介质间的碰撞机会,增加了团聚沉积概率,使FeS的分散性能变差,从而在饱和多孔介质上的迁移性能降低[35-36]。
当注入质量浓度从0.5 g·L−1提高到1.0 g·L−1时,CMC-FeS、ST-FeS和SA-FeS的迁出率C/C0分别减小了31.0%、55.8%和19.4%;当继续增大至2.0 g·L−1时,迁出率分别减小了30.0%、47.8%和35.1%。当GG-FeS注入浓度从0.5 g·L−1增加到1.0 g·L−1时,迁出率C/C0变化不大,仅减小了0.04%;当注入质量浓度从1.0 g·L−1增加至2.0 g·L−1时,C/C0减小了0.08%。综合以上结果,可以看出,注入质量浓度对GG-FeS在饱和多孔介质中的迁移能力影响要弱于其他3种改性FeS材料,这可能是由于瓜尔胶作为一种剪切稀化流体,在多孔介质中迁移时由于受到剪切力的作用,可以有效地改善纳米颗粒的迁移能力。
-
4种改性FeS纳米材料在不同粒径介质(粗砂、中砂和细砂)条件下在饱和石英砂介质中的穿透曲线如图9所示。4种改性FeS纳米材料的迁移能力随着注入介质粒径增大而增大。CMC-FeS和SA-FeS在粗砂、中砂和细砂3种介质中的迁移率C/C0分别为0.80、0.52、0.40和0.79、0.52、0.28,可以看出,介质粒径的减小对CMC-FeS和SA-FeS在饱和多孔介质中的迁移性能影响较大。ST-FeS和GG-FeS在粗、中、细砂3种介质中的最大迁出率C/C0值分别为0.62、0.49、0.45和0.58、0.22、0.21,可以看出,由粗砂到中砂,粒径减小对ST-FeS和GG-FeS的迁移能力影响较大。而在细砂中,即使介质粒径继续减小,这两者迁移能力下降却不明显。
-
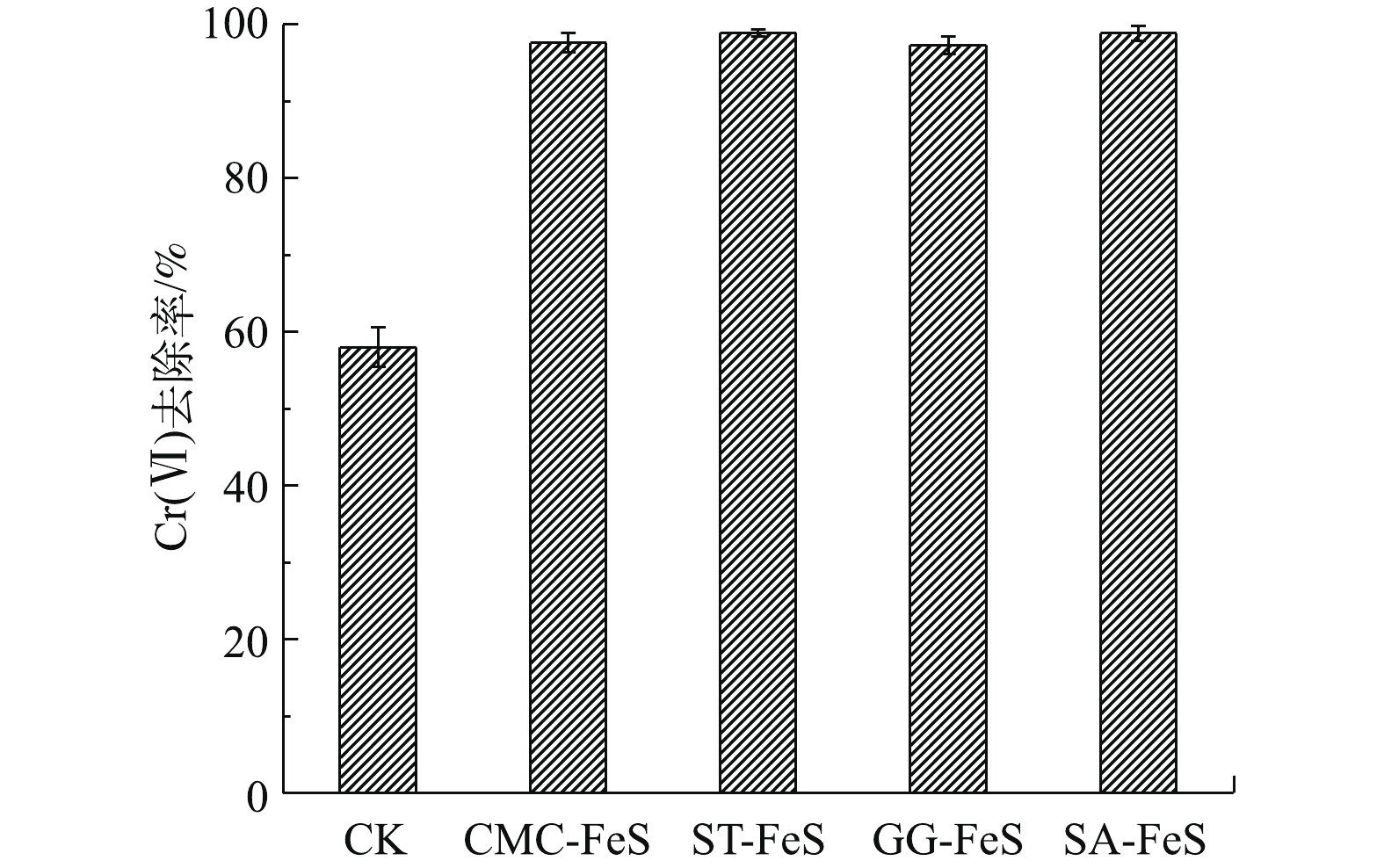
在Cr(Ⅵ)初始浓度为20 mg·L−1、FeS纳米颗粒添加量为50 mg·L−1、pH=7反应时,经过180 min后,不同改性材料对Cr(Ⅵ)的处理效果如图10所示。由图10可知,裸露FeS对Cr(Ⅵ)的去除率仅为58%。相比裸露FeS,4种改性纳米材料对Cr(Ⅵ)的去除效果均明显提高,分别提高了67.2%,66.8%,58.4%和67.0%。洪梅等[37]在pH=7、FeS与
Cr2O2−7 摩尔比为0.66∶1时研究了裸露FeS和CMC-FeS对Cr(Ⅵ)的去除,发现在该反应体系下,裸露和CMC-FeS对Cr(Ⅵ)的去除效果相当,分别为84.90%和82.78%。这可能是由于在FeS表面负载的CMC过量,阻碍了Cr(Ⅵ)与FeS的接触反应。此外,WU等[12]研究表明,相比裸露FeS,SA-FeS可将Cr(Ⅵ)的去除率由65%提高到100%。在本研究中,由于FeS为足量,理论上能够完全还原Cr(Ⅵ),但可能由于FeS已经发生氧化,或者在Cr(Ⅵ)的还原过程中,在FeS颗粒表面形成了(CrxFe1−x)(OH)3沉淀,从而阻碍了FeS和Cr(Ⅵ)之间的电子传递,从而导致Cr(Ⅵ)的去除率达不到100%。
2.1. 不同改性FeS纳米材料的表征
2.2. 不同改性材料对FeS纳米颗粒稳定性的影响
2.3. 不同改性材料对FeS纳米颗粒在饱和多孔介质中迁移性能的影响
2.4. 质量浓度对改性FeS纳米颗粒迁移性能的影响
2.5. 不同粒径介质对改性FeS纳米颗粒迁移性能的影响
2.6. 不同改性材料对FeS反应活性的影响
-
1) 4种高聚物稳定剂主要以羧基通过双齿桥接的形式结合到FeS颗粒表面,从而抑制了颗粒间的团聚。改性后的FeS纳米颗粒具有更强的稳定性和分散能力。
2)相比裸露FeS,4种改性FeS纳米材料在饱和多孔石英砂介质中的迁移能力明显有所提高;提高注入质量浓度可以明显降低CMC-FeS、ST-FeS和SA-FeS的迁移能力,但对GG-FeS的迁移影响较小;介质粒径对4种改性FeS纳米材料的迁移能力产生明显的影响,总体表现迁移能力为随着介质粒径的减小而降低。
3) CMC-FeS、ST-FeS和SA-FeS较强的抗沉降性能和迁移能力主要与静电斥力和空间位阻效应的增加有关。对于GG-FeS,空间位阻和剪切稀化特性使其具有一定的稳定性且在多孔介质中具有良好的迁移能力。
4) 4种改性纳米材料对Cr(Ⅵ)的去除效果均明显高于未改性的FeS,但均未达到100%,这可能是由于FeS已经发生氧化,或者在Cr(Ⅵ)的还原过程中,在FeS颗粒表面形成了(CrxFe1−x)(OH)3沉淀,从而阻碍了FeS和Cr(Ⅵ)之间的电子传递。





 下载:
下载: