-
在石油开采、加工、运输及使用过程中,原油以及各种石油制品的泄漏和排放事故时有发生,不可避免地会造成土壤的石油污染[1]。而土壤石油污染普遍是多种污染物复合污染,而不是单一污染。石油污染物中除了含有大量有机物外,还含有重金属等,他们会进入土壤并对生态环境造成复合污染[2-3]。近年来,我国部分油气田地区遭受了不同程度的石油-重金属复合污染。例如,长宁某页岩气井场土壤中含有原油和重金属镍2种污染物[4];黄河三角洲石油污染土壤中重金属元素多达10余种[5]。土壤中多种污染物之间的相互作用使得修复过程变得更加复杂。重金属与有机污染物之间的相互作用可能会改变污染物的形态、溶解度和生物可利用度,从而相互抑制或促进彼此的修复效率[6]。重金属及石油中多环芳烃等具有致癌性和诱变性[7-8],会对人体健康和自然生态系统造成极大威胁[9-10],因此,有机-重金属复合污染问题在全球范围内引起了极大的关注[11]。目前,针对石油-重金属复合污染土壤修复的研究已迫在眉睫。
微生物修复是去除或降解土壤污染物的最常见和最可靠的技术之一,该技术主要是利用微生物的新陈代谢及生物吸附等作用修复污染土壤。但是,将游离菌加入土壤中易受不良环境影响,导致修复效果不佳。固定化微生物技术(IMT)可为外源微生物提供保护屏障,避免微生物受环境的不利影响,包括与土著微生物竞争、污染物浓度过高、pH和温度不适宜等[12-13]。WANG等[14]发现,固定化微生物可以促进盐碱地中多环芳烃的降解,效果优于游离菌。张秀霞等[15-16]研究了固定化微生物修复石油污染土壤过程中对土壤生物学特性及理化性质的影响,结果表明,固定化微生物处理方式对石油烃降解效果最好,能增加土壤酶活性,对pH具有缓冲作用。IMT不仅可用于修复有机污染土壤,还可应用于重金属污染土壤。有研究表明,生物炭吸附固定化微生物对土壤中U、Cd钝化效果显著[17]。
目前,关于固定化微生物技术的研究多聚焦于单一污染土壤,针对有机-重金属复合污染土壤的研究鲜见报道[18]。外源微生物的加入可能会影响土壤微生物生态平衡[19],故在修复过程中不仅要考察固定化微生物对有机-重金属复合污染土壤修复效果,还要考察其对土壤环境的影响[20]。土壤酶活性和土壤细菌数量作为土壤生物学特性相关指标,可作为评价修复状况和污染对土壤性质影响的指标[15, 21]。
本研究从四川长宁-威远地区页岩气开发井场重度污染区的含油土壤中筛选出1株具有镉抗性和石油烃降解能力的菌株,以玉米芯生物炭作为固定化材料负载该菌株,研究固定化微生物对镉-石油烃污染土壤的修复效果,以期为复合污染土壤的生物修复提供参考。
全文HTML
-
本研究使用的未受污染土壤取自四川长宁某页岩气井场附近未污染区域。从土壤表层(0~20 cm)处取样,将采集的土壤密封在聚乙烯袋中。自然风干后,将大块土壤破碎研磨并过2 mm的筛网备用。分别将溶于四氯化碳(CCl4)中的原油和硝酸镉(Cd(NO3)·4H2O)溶液喷洒于1/4的土壤中,混合均匀置于通风橱内,待CCl4完全挥发后,与剩下3/4的土壤混合均匀得到石油-镉复合污染模拟土壤。模拟污染土壤物理化学性质如表1所示。
-
1)石油烃重金属液体培养基:石油烃10 g·L−1、酵母膏3 g·L−1、NaCl 5 g·L−1、MgSO4·7H2O 0.25 g·L−1、(NH4)2SO4 1 g·L−1、K2HPO4·3H2O 13 g·L−1、KH2PO4 4 g·L−1、Cd(NO3)2·4H2O 0.82 g·L−1。
2)石油烃重金属固体培养基:在上述石油烃重金属液体培养基中加入质量分数为2%的琼脂。
富集培养基、基础扩大培养基和固定化培养基见参考文献[22]。上述培养基pH均调整为7.0~7.5,在121 ℃、1×105 Pa下高压蒸汽灭菌20 min。
-
1)具有镉抗性的石油烃降解菌的筛选。称取10 g新鲜土壤样品(采自长宁某长期遭受石油烃和重金属镉复合污染的地区)进行具有镉抗性的石油烃降解菌筛选,具体筛选方法见文献[23]。最终得到具有镉抗性且能高效降解石油烃的菌株共计7株(记为W3~W9),冷冻保存于丙三醇中。
2)菌株的吸附特性及降解特性研究。将筛选出的7株菌株的菌液分别接种1 mL于100 mL含300 mg·L−1 Cd2+的基础扩大培养基中,在30 ℃、130 r·min−1下培养72 h,取0.5 g上清液消解,采用原子吸收分光光度法测定培养基中镉的含量,培养基中减少的镉含量被认为全部是菌体吸附的镉含量。镉的吸附率按式(1)计算。
式中:η为菌株对Cd的吸附率;CCd0为处理前Cd浓度,mg·L−1;CCdt为处理后Cd浓度,mg·L−1。
分别将1 mL菌液接入100 mL以10 g·L−1石油烃为唯一碳源的无机盐培养基中,在30 ℃、130 r·min−1下培养7 d,采用重量法测定培养基中的石油烃含量,计算石油烃降解率。石油烃的降解率按式(2)计算。
式中:R为石油烃 (TPH) 降解率;C0为处理前石油烃含量,mg·L−1;Ct为处理后石油烃含量,mg·L−1。
对7株菌株进行重金属镉吸附特性和石油烃降解特性的研究,筛选出1株对镉具有耐受性且石油烃去除能力较高的菌株作为鉴定和生理生化实验的供试菌株。
3)菌株菌落及细胞形态的观察采用稀释涂布平板法。在石油烃重金属固体培养基上培养1~2 d,观察菌落的形状、透明度、颜色等指标,并用扫描电子显微镜(SEM)观察菌株的细胞大小和形状。甲基红实验、硝酸盐还原实验、柠檬酸盐实验、吲哚实验、动力实验、接触酶实验、糖发酵实验、V-P实验、硫化氢产生实验、明胶液化实验、酪蛋白水解实验、革兰氏染色实验方法参照参考文献[24]。参照《常见细菌系统鉴定手册》[25]和《医学细菌名称及分类鉴定》[26]对菌株形态及生理生化实验结果初步鉴定菌株的属。核酸提取及PCR扩增方法见文献[23]。本研究的菌株16S rDNA测序结果提交数据库进行BLAST比对,并构建系统发育树,分析菌株种属。
-
选用玉米芯制备生物炭,马弗炉500 ℃高温热解3 h,热解得到生物炭作为固定化载体[27]。无菌条件下,将1 μL存于丙三醇中的筛选菌株接入基础扩大培养基中,置于30 ℃、130 r·min−1恒温摇床中活化8 h以上,作为储备菌液。将2 g制备好的生物炭置于100 mL固定化培养基中,在121 ℃、1×105 Pa下高压蒸汽灭菌20 min,接入1 mL储备菌液,置于130 r·min−1、30 ℃的摇床中固定18 h后,以3 500 r·min−1离心5 min后弃上清液,所得固体即为固定化微生物。生物炭和固定化微生物的形貌表征参照文献[22]。
-
固定化微生物修复石油–重金属混合污染土壤在高15 cm、直径10 cm的塑料盆中进行。本研究共设4组对照:对照组(CK),生物炭和游离菌均不添加;游离降解菌组(FC),采用平板计数法添加与固定化微生物组等量的游离菌;固定化微生物组(IM),1 g干土添加3%的固定化微生物;生物炭组(BC),1 g干土添加3%的生物炭。每组3个重复,每盆400 g土壤。分别以硝酸铵和磷酸氢二钾作为氮源和磷源,以土壤中有机碳为基准,将土壤中的C、N、P调至C∶N∶P=100∶10∶1。定时给土壤翻土保持充分的氧气供给,并定期添加去离子水,使土壤含水率维持在20%。实验周期为60 d,每5 d分别测定土壤pH、土壤脱氢酶(DHA)、多酚氧化酶(S-PPO)和过氧化氢酶(CAT)活性、石油烃残留量的变化;每10 d分别测定重金属形态及土壤细菌数量的变化。其中,含水率采用105 ℃烘干法[28]测定;土壤pH采用1∶2.5(W/V)的水提取液玻璃电极法[29]测定;有机质、总氮和总磷分别采用重铬酸钾容量法、碱性过硫酸钾消解紫外分光光度法和氢氧化钠熔融-钼锑抗分光光度法[30-32]测定;重金属形态采用Tessier五步浸提法[33]测定;石油烃含量采用重量法[34]测定;脱氢酶、多酚氧化酶和过氧化氢酶活性分别氯化三苯基四氮唑(TTC)分光光度法、邻苯三酚比色法和高锰酸钾滴定法[30, 35]测定;细菌数量采用稀释涂布平板法[36]测定。
1.1. 供试土壤
1.2. 培养基
1.3. 具有镉抗性的石油烃降解菌的筛选及鉴定
1.4. 固定化微生物的制备及表征
1.5. 土壤修复实验
-
1)菌株吸附特性及降解特性。菌株对镉吸附率和石油烃降解率如图1所示。由图1(a)可知,筛出的菌株W3、W4和W8均对Cd2+有较好的吸附作用,吸附率均在28%以上。3株菌均能在含Cd的培养基中存活并吸附一定量的Cd,但整体来说菌株对Cd的吸附率相差不大。菌株主要通过吸附沉淀对Cd2+产生生物钝化,利用自身代谢产物与Cd2+络合等,对Cd进行吸附[37]。由图1(b)可知,菌株W8对石油烃的降解率最高,达39.15%,而吸附Cd效果较好的W3和W4对石油烃的降解不佳。菌株主要是通过将石油烃作为碳源来维持自身的新陈代谢从而达到去除的目的。将微生物应用于修复石油烃-镉复合污染土壤中,所需的菌株势必对重金属镉具有较好的抗性,同时对石油烃具有较好的降解能力才能在污染土壤中更好地存活,才能使修复效率更佳[23]。综上所述,W8是吸附和降解效果最佳的菌株,故确定W8为本研究筛选出的目的菌株,用作后续生物学特性研究的供试菌株。
2)菌株形态观察及生理生化指标。菌株W8的SEM图及菌株W8和柠檬酸杆菌的生理生化特性对照分别如图2和表2所示。该菌株的菌落形态为圆形,颜色为淡黄色,边缘平滑,透明度较差。由图2可得出,细菌细胞为杆状,菌体长1~2 μm。生理生化实验中除动力实验、接触酶实验、V-P实验、明胶液化实验、酪蛋白水解实验和革兰氏染色结果呈阴性(−)外,其余生理生化反应均呈阳性(+)。菌株W8的形态和生理生化特性同柠檬酸杆菌属的细菌特征相似,初步判定为柠檬酸杆菌。
3)菌株16S rDNA的序列分析。将测序得到的W8菌株16S rDNA序列提交至数据库进行比对,构建出如图3所示的系统发育树。分析结果表明,菌株W8与柠檬酸杆菌属的同源性相近(97%),2者在系统发育树上聚为1簇。综合细菌形态、生理生化实验结果和16S rRNA分析,可确定W8属柠檬酸杆菌,将其命名为Citrobacter sp.W8。
-
生物炭和固定化微生物的形貌表征如图4所示。从图4(a)可以看到,生物炭骨架结构清晰,形成松散、孔隙发达的结构。生物炭的多孔结构可以给微生物提供较大的附着空间,同时也有利于其对污染物的吸附,缩短污染物与微生物的距离[38]。由图4(b)中可以观察到,生物炭孔径中附着大量目标菌株,这说明生物炭表面已成功负载Citrobacter sp.W8。
-
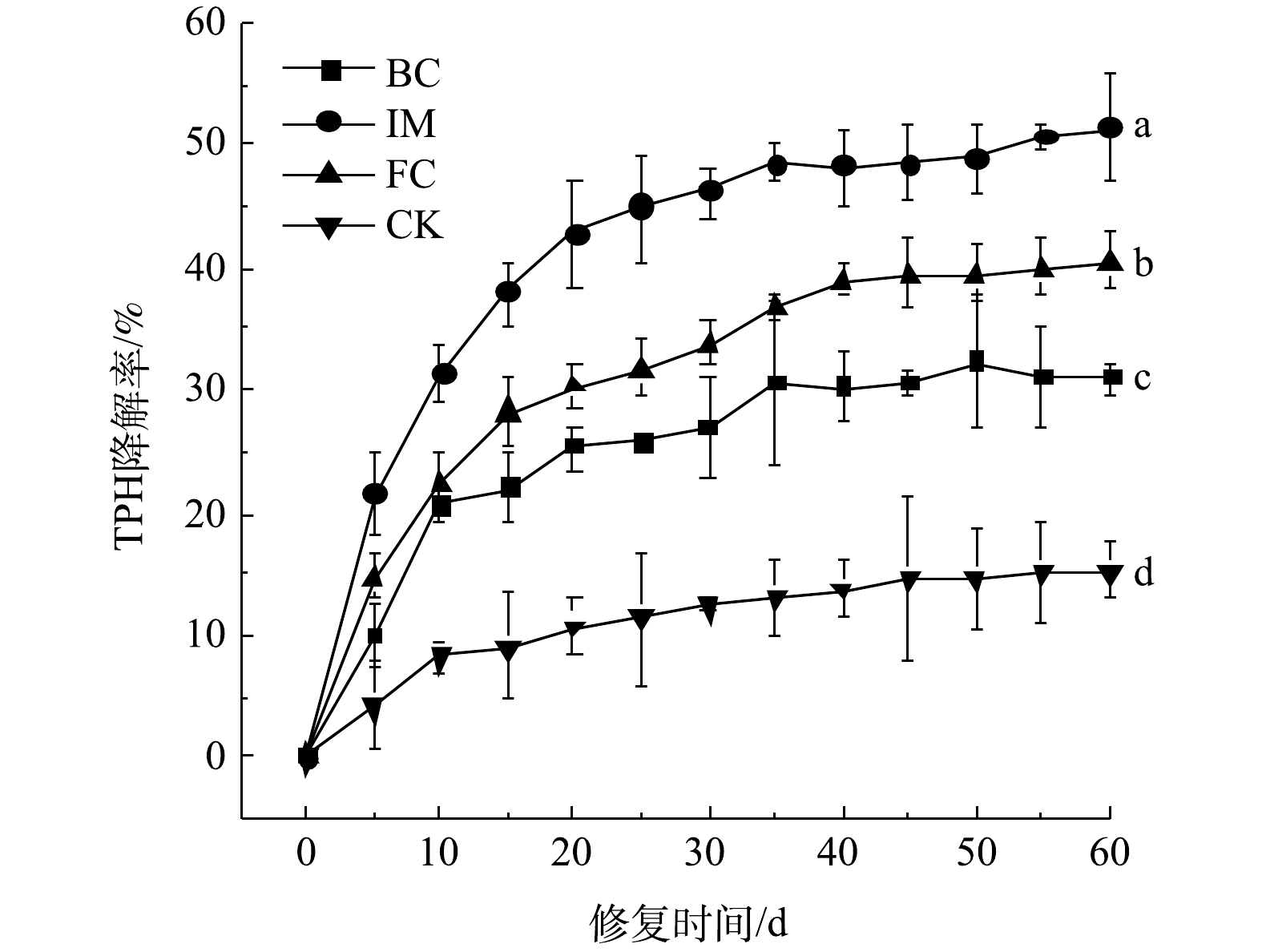
采用不同修复方式对石油烃-Cd复合污染土壤进行为期60 d的修复,修复过程中石油烃(TPH)降解率变化如图5所示。在60 d的修复周期内,各组TPH降解率均呈上升趋势,固定化微生物组(IM)、游离菌组(FC)、生物炭组(BC)、空白组(CK)的TPH降解率分别为51.25%、40.44%、31.11%、15.18%。在0~30 d内,IM组TPH降解率迅速上升,这主要是因为生物炭的孔隙结构为微生物提供了适宜的生存空间[39],有效避免了外源微生物与土著微生物的竞争,减轻了污染物对微生物的直接毒害作用。同时,生物炭的加入能够提供N、P、K等营养元素[40],促使细菌数量迅速增加,进而增强微生物对TPH的代谢能力。生物炭能够吸附部分污染物并缩短微生物与污染物的距离,提高降解效率[38]。30 d后的降解速率逐渐趋于平稳,这可能与TPH降解过程中产生的有毒代谢产物积累过量以及土壤中营养物质的逐渐缺乏有关。而FC缺乏生物炭的保护作用,TPH降解率明显低于IM(P<0.05)。BC的TPH降解率明显高于CK,这证明生物炭对TPH的降解有促进作用。CK也有较低的TPH降解率,这主要是由于土著微生物的降解以及TPH的自然挥发[15]。
-
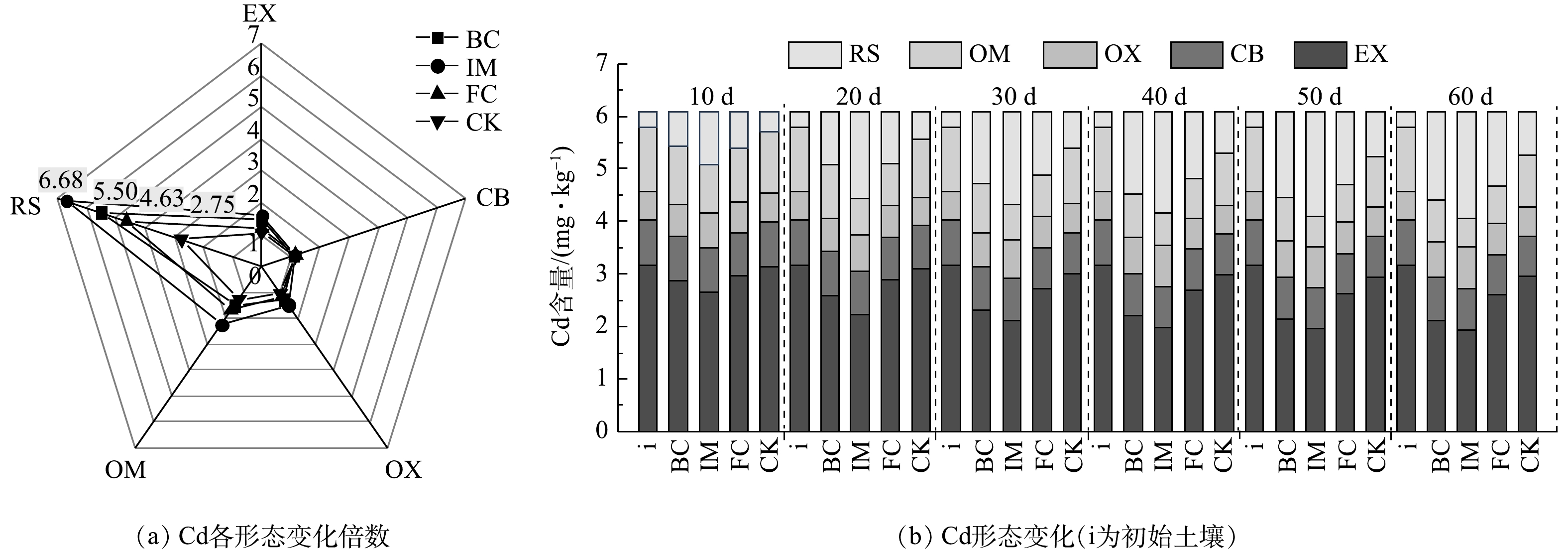
图6(a)为各组第60天 Cd形态含量与初始土壤中Cd形态含量的比值,表示各形态变化的倍数。可以看出,IM组中RS与初始土壤相比增加了6.68倍,相较于其他组而言,IM在降低Cd迁移性方面作用更为明显,这是因为生物炭对重金属的固定起着至关重要的作用。生物炭表面丰富的含氧官能团(羟基和羧基)可以与重金属结合,通过络合或共沉淀降低重金属的可利用态含量[40]。DAS等[41]发现,生物炭表面含氧官能团越多,其与金属离子的离子交换作用越强。同时,Citrobacter sp.可以通过生物吸附的方式降低部分可利用态重金属[42]。因此,IM中EX含量的降低是生物炭络合、共沉淀与微生物吸附联合作用。Cd的形态变化表明,添加固定化微生物可减轻Cd的直接毒性,降低Cd的流动性和生物利用度[17]。
采用不同修复方式对石油烃-Cd复合污染土壤进行为期60 d的修复,修复过程中土壤中Cd形态含量变化如图6(b)所示。土壤中重金属形态可以分为可交换态(EX)、碳酸盐结合态(CB)、铁锰氧化物结合态(OX)、有机结合态(OM)和残渣态(RS)。5种形态的重金属的生物可利用性为:EX > CB > OM > OX > RS[43]。从图6(b)中可以看出,初始土壤(i)中Cd的EX含量较高,占重金属总量的51.78%,RS含量低,土壤中重金属迁移性强,生物有效性高,土壤环境风险高。修复60 d后,BC、IM、FC、CK各组土壤中EX含量分别从初始3.150 3 mg·kg−1降至2.124、1.942 9、2.601 1 mg·kg−1和2.957 0 mg·kg−1。土壤中石油烃被微生物降解导致有机质含量降低,OM含量下降,其中IM下降最多,减少了0.6653 mg·kg−1。IM组Cd的OX和RS含量增加最多,分别增加了0.251 8和1.725 7 mg·kg−1。此外,培养时间也有利于Cd从非残留组分向残留组分的转移。
-
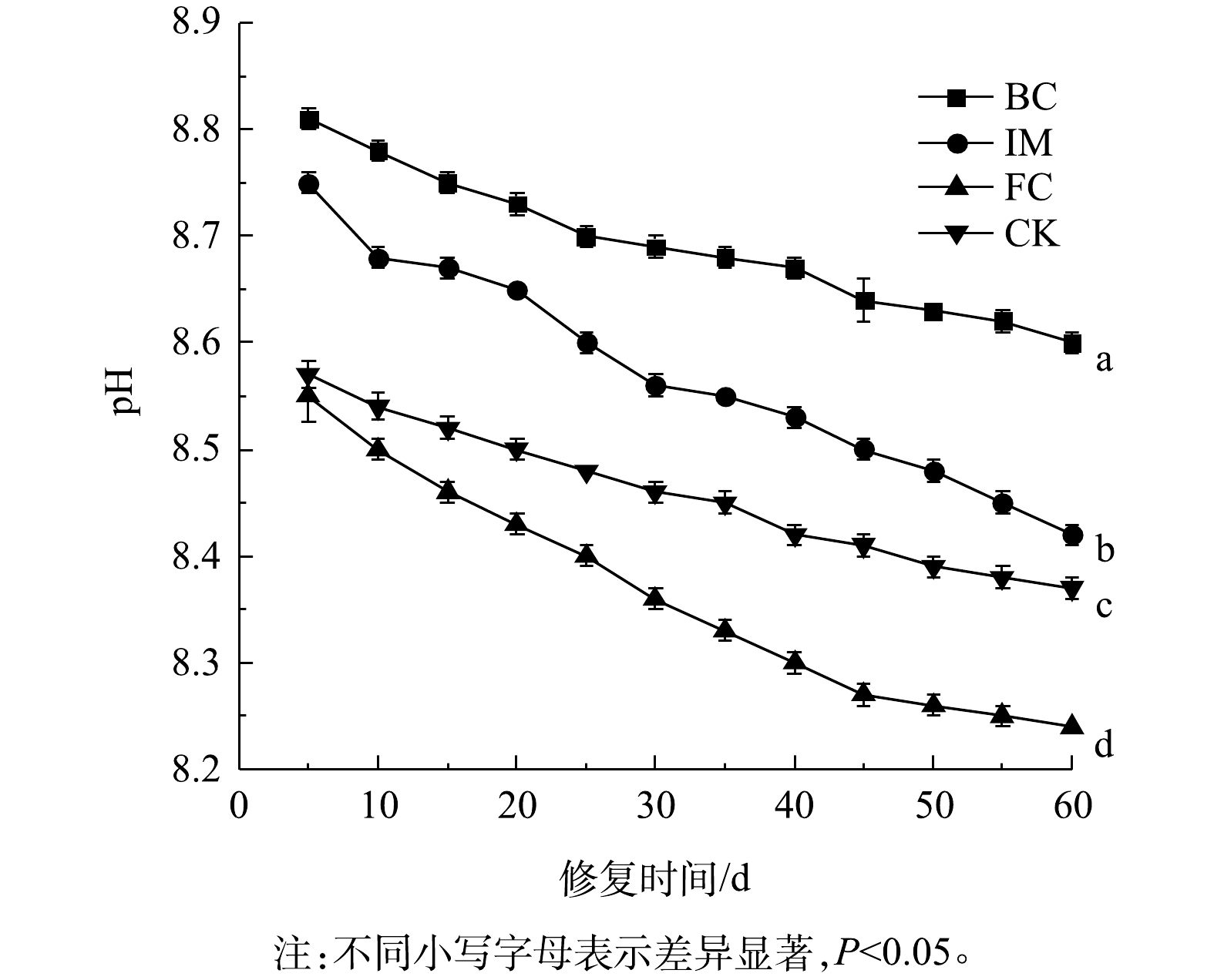
由于生物炭呈碱性,故生物炭的加入轻微提升了IM和BC组的土壤pH,分别为8.75和8.81。Citrobacter sp.W8在pH为5~9时均能较好生长,因此,菌株的生长不会受到生物炭导致土壤pH变化的影响。采用不同修复方式对石油烃-Cd复合污染土壤进行修复,在60 d的修复过程中土壤pH的变化如图7所示。修复周期内各组土壤pH均呈下降趋势,这是因为微生物在代谢石油烃的过程中产生了脂肪酸等有机酸[44]。在土壤中添加生物炭(BC和IM)后,土壤pH明显高于不添加生物炭(CK和FC)的处理组(P<0.05)。与FC相比,BC和IM对土壤pH的影响相对较小,维持在原土pH(8.65)附近,具有一定的缓冲作用。这是因为,在热解过程中生物炭中灰分含量的增加,以及生物炭中表面官能团和可溶性碳酸盐的作用,可以中和土壤的酸性[45]。pH突然改变会对微生物造成损害,抑制相关酶活性[46],而pH的缓冲作用可减轻微生物损伤。同时,生物炭的加入相对提高了土壤pH,这会促进重金属沉淀,增强重金属的固定,从而减轻重金属对微生物的毒性[47]。
-
生物修复效果的关键在于微生物活性及酶促反应速率的高低[48]。土壤酶在微生物新陈代谢过程中起着催化作用,可以作为评价石油污染土壤修复效果的指标[49]。采用不同修复方式对石油烃-镉复合污染土壤进行修复,在60 d的修复过程中土壤CAT、DHA、S-PPO活性变化如图8所示。60 d内,IM组对土壤DHA、CAT、S-PPO活性均有促进作用,最大值分别为0.549 7 μg·(mL·h·g)−1、9.063 7 mL·(g·30 min)−1和9.809 3 mg·(h·g)−1。修复过程中酶活性均呈先增大后缓慢减小的趋势。添加游离菌、生物炭和固定化微生物都能增加土壤酶活性,但IM组3种酶活性均高于其他3组。这是因为,IM组中的生物炭能够降低土壤不良环境对固定化菌株的负面影响,使微生物具有较高的活性,因而促进微生物分泌更多的酶。修复前期土壤中的营养物质充足,微生物数量增加,酶活性也随之提高。但随着微生物数量的大量增加,土壤中营养物质缺乏,并且在生长繁殖过程中产生了许多有害的代谢产物,导致后期土壤酶活性缓慢下降[49]。同时,Cd化学形态的改变对土壤酶活性也有不同程度的影响[50]。结合图6(a)可知,IM组中Cd的可交换态含量降低最多,残渣态含量增加亦最多,导致该组Cd的生物毒性较小,所以土壤酶活性高。目前,针对土壤酶活性受抑制的机理主要有2种解释:一是土壤微生物数量和活性决定土壤酶的合成与分泌,污染物会抑制土壤微生物的生长繁殖,减少微生物分泌土壤酶,降低酶活性;二是污染物直接与酶的活性位点结合,使酶失活[51]。固定化微生物的加入使得石油烃含量降低,减少了污染物与酶的结合位点;同时,Cd的生物可利用性和石油烃含量的降低也减轻了污染物对微生物的抑制作用,使微生物分泌酶的能力增强。因此,IM组脱氢酶、过氧化氢酶和多酚氧化酶的活性表现为最强。
-
采用不同修复方式对石油烃-Cd复合污染土壤进行修复,在60 d的修复过程中土壤细菌数量变化如图9所示。在修复过程中,固定化微生物、游离菌及生物炭的添加都能促进土壤微生物的生长,细菌呈先增大后平缓的趋势。但是,各实验组的上升幅度不同:IM组最高,从6.18×107增加到2.48×108 cfu·g−1;其次为FC组,从6.09×107增加至1.70×108 cfu·g−1。IM和FC组细菌数量均高于BC和CK组,这说明固定化微生物和游离菌的加入提高了土壤细菌量,使细菌数量处在较高的水平,能够提高细菌对石油烃的降解。在修复初期,IM组细菌数量迅速增加,其原因主要有4个方面:1)生物炭的多孔特性可以将微生物吸附在内孔,提高细菌数量,减少外界不良环境对微生物的影响[52];2)生物炭利用其强吸附能力将TPH吸附在表面,供生物炭上的降解菌降解[53];3)重金属形态对微生物毒害作用存在明显差异[54],IM组Cd的化学形态最大程度地从可交换态和有机结合态转换成了残渣态,降低了Cd对微生物的直接毒害作用;4)外源微生物Citrobacter sp.W8的加入可能对土著微生物的生长起促进作用,土壤中细菌总量增多,细菌对石油烃的降解也随之提高。而游离菌直接加入土壤中,因其不适应土壤环境,故其细菌数量增加缓慢;随着修复时间的延长,细菌以石油烃为碳源,不断繁殖,细菌量增多。在40~60 d内,细菌数量变化不大,这是因为在石油烃降解过程中产生并积累了一些有毒中间产物,这些有毒中间产物对细胞有毒害作用,因而对细菌数量有一定的抑制作用[49]。
2.1. 降解菌及其性能分析
2.2. 生物炭及固定化微生物表征
2.3. 土壤中石油烃降解率的变化
2.4. 土壤中重金属形态的变化
2.5. 土壤pH的变化
2.6. 土壤酶活性的变化
2.7. 土壤细菌数量的变化
-
1)筛选出1株具有镉抗性的石油烃降解菌,该菌株为柠檬酸杆菌,命名为Citrobacter sp.W8,该菌株可有效用于固定化微生物技术修复石油烃-镉复合污染土壤。
2)固定化微生物技术可利用微生物新陈代谢显著降低土壤石油烃含量,并通过生物炭吸附、络合和共沉淀作用及生物吸附作用将重金属Cd由可交换态和有机结合态转化为残渣态,从而达到固定土壤重金属的效果。
3)生物炭固定化微生物对土壤pH具有缓冲作用,从而减轻pH突变对微生物造成的损害。此外,该技术通过促进HDA、CAT、SPPO的分泌,以及土壤细菌数的增加,达到提高土壤微生物活性的目的。



 DownLoad:
DownLoad: