洗涤方式对电解锰渣中锰回收效率及无害化处理的影响
Effects of washing methods on recovery efficiency of manganese from manganese residue and harmless treatment
-
摘要: 以化浆-滤饼洗涤代替传统化浆洗涤回收锰渣中的硫酸锰及对洗涤后的锰渣进行无害化处置,对比洗涤方式对电解锰渣中锰回收效率及无害化处理的影响。结果表明,在同等6倍渣重用水量的情况下,化浆-滤饼洗涤比传统化浆洗涤硫酸锰回收率提高10%以上,可达到95.82%。同时回收锰后的锰渣用氢氧化钠无害化处置,在保证锰渣浸出液中锰、氨氮离子满足污水综合排放标准(GB 8978-1996)要求的前提下,药剂用量相比未水洗的节省70%以上,大幅度节约药剂成本。洗涤液以碳酸钠为沉锰药剂回收碳酸锰产品,可产生一定的经济价值,进一步降低锰渣无害化处理成本。Abstract: Slurrying-cake washing was used instead of the slurrying washing to investigate the recovery efficiency of manganese sulfate from manganese residues and to examine the effect on the subsequent harmless treatment of manganese residues. The recovery rate of manganese sulfate reached 95.82% when slurrying-cake washing was used, 10% higher than the rate achieved when slurrying washing was used. The recovered manganese residue was disposed harmlessly using sodium hydroxide, meeting the requirement of Integrated Wastewater Discharge Standard (GB 8978-1996) on manganese residue leaching solution of manganese and ammonia ion. Compared with the treatment of the manganese residues without washing, reagent dosage was reduced by 70% in the harmless treatment of manganese residue.
-
Key words:
- cake washing /
- slurrying washing /
- rate of recovery /
- harmless treatment
-
地下水是维持人类生存和发展的一种最重要资源和生态环境因子[1]。近年来,我国经历了快速城市化和工业化,然而,污水的处理能力未能保持同步增长(尤其在农村地区)、农业化肥和农药过量使用、地下水超采严重等问题,已经引起地下水水化学特征发生改变[2-4]。众所周知,地下水水化学改变不仅能够干扰多种生态过程,同时也降低了地下水的使用价值[5]。因此,掌握地下水水化学的演化规律对于可持续利用地下水尤为重要[6-8]。
地下水水化学演化主要受控于自然因素和人类活动的综合影响。地下水水化学特征与自然因素(水文地质条件、包气带岩性、水岩交互作用和海水入侵)密切相关[9-10]。安乐生等研究发现,黄河三角洲浅层地下水化学特点形成的关键驱动因素是黄河入海流路变迁和海水入侵[11]。人类活动(如污水排放、农业施肥、地下水超采等)也严重影响了地下水水化学演化规律。Zhang等研究发现,地下水水化学特征受到了生活污水、工业污水和水岩交互作用的混合影响, 因此,为防止该地区地下水水质恶化,首先要控制污水的排放 [12]。郭高轩等研究表明,潮白河冲洪积扇不同深度地下水水化学具有分层分带特征,且在人类活动强烈区域,浅层地下水水质略差[13]。
中牟县位于郑州市东部新城区,地下水资源是该地区工农业生产的主要供水水源。近年来,随着人口的迅速增长和工业的高速发展、农业灌溉面积极速扩大,地下水的开采量日益增加。基于 2019 年对该地区地下水位统调工作发现,中牟县城一带已经形成一个较大的浅层地下水降落漏斗,并且研究区内人类活动强烈,存在农业面源污染、固体废弃物堆放场和工业污染等3类潜在污染来源,可能对地下水水化学特点构成一定影响。目前,针对该地区地下水水化学演化规律尚未开展深入研究工作,对该地区居民的健康饮水和社会经济可持续发展构成潜在威胁。
本研究针对郑州市中牟县地下水水化学演化机理开展研究,联合应用piper三线图、Gibbs图、离子比例系数法和多元统计技术等手段,识别研究区水化学特征,揭示该地区地下水水化学形成演化机制,探讨控制地下水水化学特征的主控因素,以期为快速城市化地区地下水的可持续开发利用提供科学依据。
1. 材料与方法(Materials and methods)
1.1 研究区概况
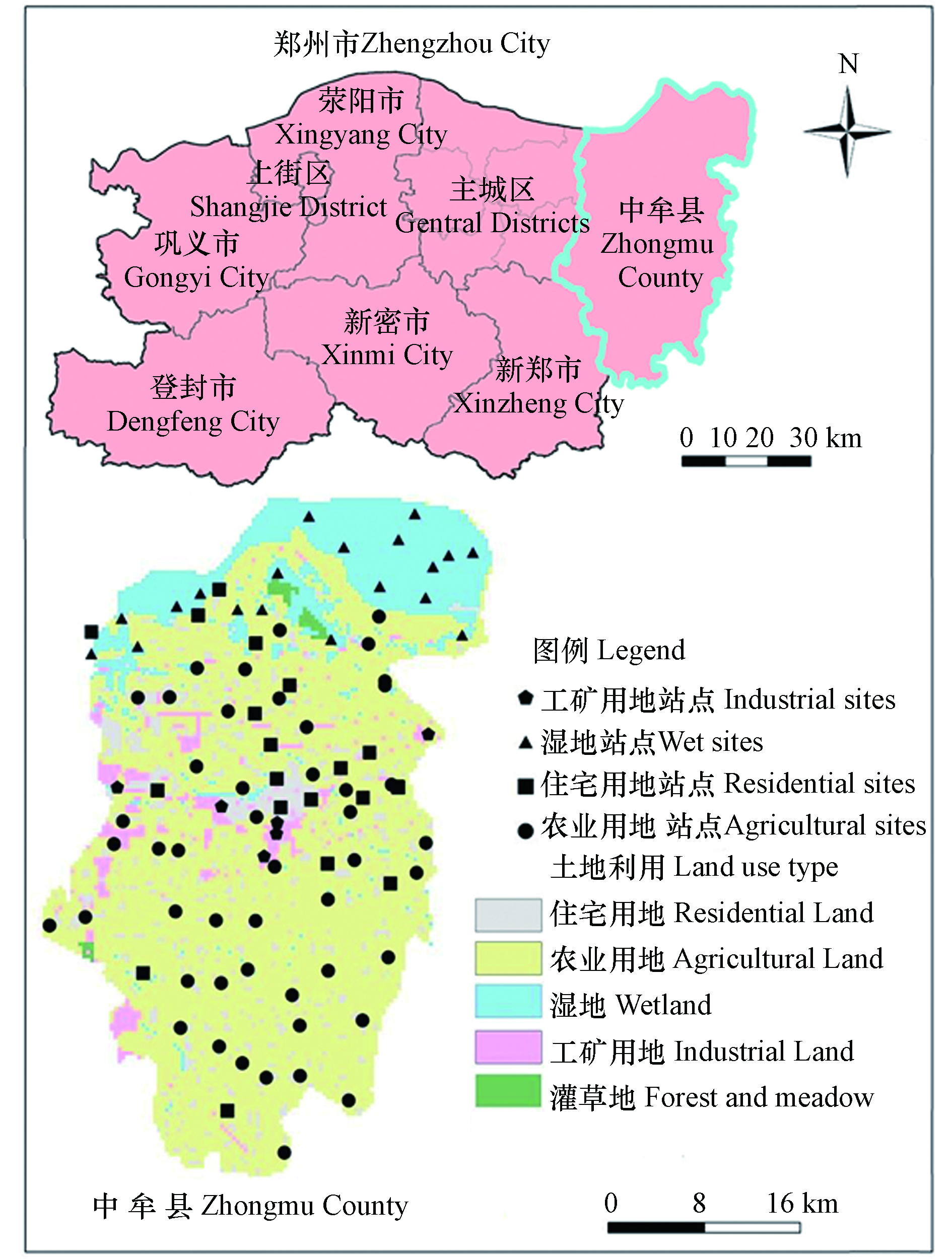
中牟县位于北纬34°26′—34°56′、东经113°46′—114°12′之间,地处中原腹地、河南省中部偏东,隶属郑州市。研究区属暖温带半干旱气候,具明显的大陆季风气候特征,四季分明。多年平均气温14.25℃,多年平均降雨量约为616 mm,年内降水多集中在7—9月,占全年降雨量的40%—48%. 多年平均蒸发量1769.8 mm,平均相对湿度66.3%。研究区总面积为917 km2,主要的土地利用类型为农业用地(68.7%)、居民区(9.2%)、工矿用地(4.3%)、水域(16.2%)(包括湿地和水体)和裸地(1.6%)(图1)。
1.2 水文地质条件
研究区地貌类型为黄河冲积平原,地下水类型主要为松散岩类孔隙水,其含水层分布广,厚度大,水量丰富,可分为浅层水(<80 m)和中深层水(80—400 m)。浅层含水层主要由山前冲洪积与黄河冲积的细砂层组成,深度主要为 40—60 m,该含水层组埋藏浅,其下为一组粉质粘土或粉土弱透水层,与下伏中深层含水层组相隔,厚25—45 m。浅层水易于开采,为农业用水主要开采层,井深25—55 m。中深层含水层组底板埋深310—350 m,其下为厚层粘土夹薄层砂或砂的透镜体,粘土层厚度一般15—40 m,具有很好的隔水性,属承压水类型。中深层水是目前城乡小型集中供水的主要开采层,井深一般在100—300 m 左右。其含水层岩性为中砂、细砂、粗砂等,厚30—80 m,导水系数125—390 m2·d−1,贮水系数4×10−3,单位涌水量3—5 m3·h−1·m−1。地下水主要的补给来源为大气降水、河道侧漏和灌溉回水,主要的排泄方式为人工开采。
1.3 样品采集
2020年6—8月采集郑州市中牟县地下水样品93组(图1),包括农业用地站点48个,湿地站点19个,住宅用地站点20个和工矿用地站点6个。采样点布设的原则主要依据不同的土地利用类型平均布设采样点,如果预布设站点区域内无地下水井,可以适当调整,但要保证2个采样点之间的距离大于1 km。地下水主要取自民井和农业灌溉井,采样井的深度范围是25—150 m。采样前抽水洗井10 min,用原水样清洗采样瓶3次,分别采集 1.5 L 和 0.5 L 水样各1瓶,用于分析阴阳离子。分析阳离子的水样加1∶1的
HNO−3 1.4 样品的测试
样品测试的指标包括pH、TDS、K+、Na +、Ca2+、Mg2+、
NH+4 NO−3 NO−2 SO2−4 CO2−3 HCO−3 1.5 研究方法
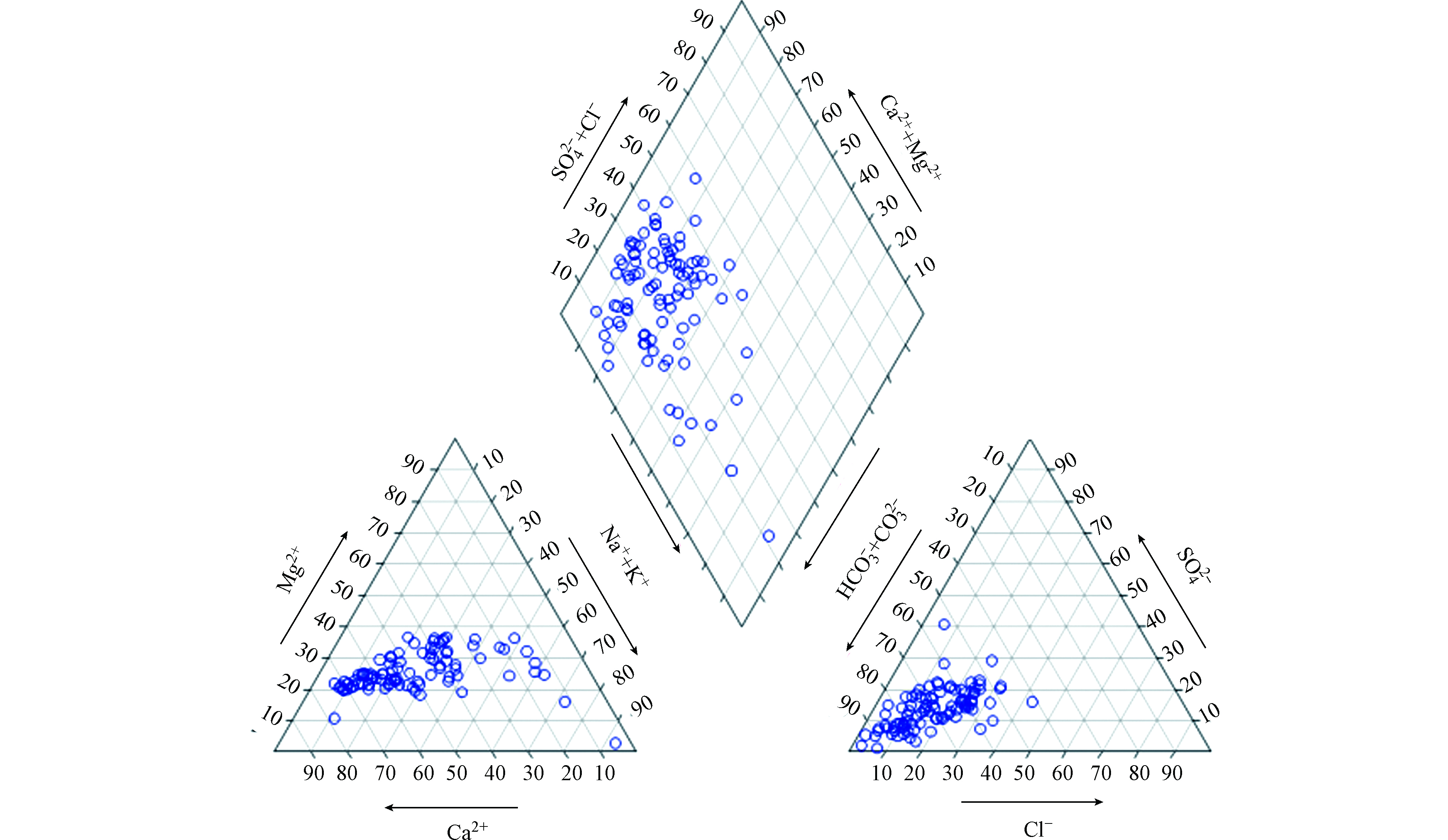
(1)水化学类型判定。本研究按照舒克列夫分类法,即阴阳离子毫克当量百分比大于25%时参与命名。对研究区采样点地下水化学类型定名,并绘制出了地下水化学类型Piper三线图。
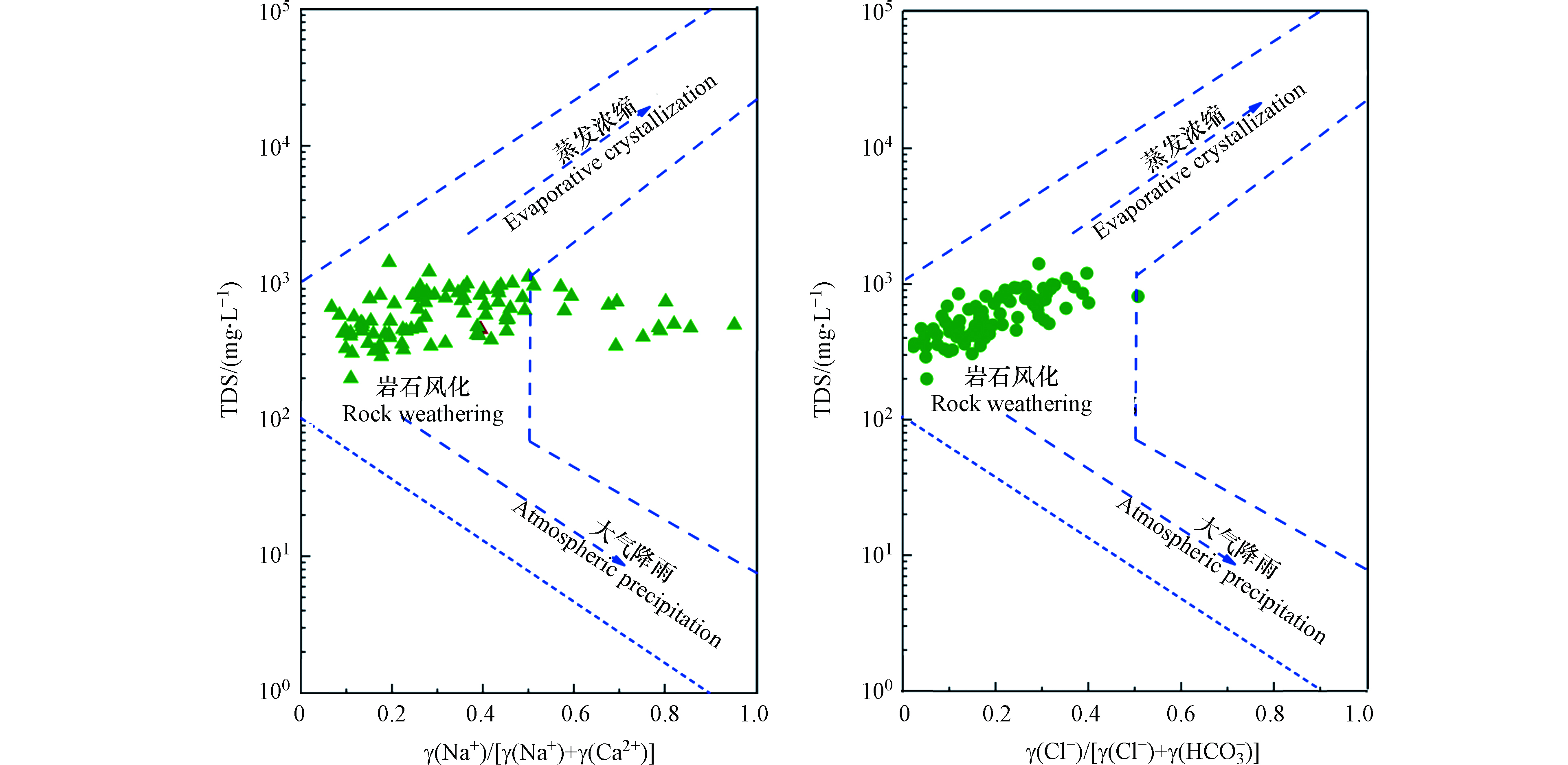
(2)地下水化学控制因素识别。选用Gibbs图识别地下水化学控制作用。通常情况下,水样位于 Gibbs 图右下角,表明其受大气降水作用影响较大,水样位于Gibbs 图左中部,表明岩石风化作用是该地区水化学的主要控制作用,而受蒸发结晶作用控制的水样将落于Gibbs 图右上角。
(3)离子来源识别。联合应用Ca2+/Na+ VS
HCO−3 HCO−3 HCO−3 HCO−3 (4)衬度系数方差。方差(Variance)用于刻画一个随机变量对其数学期望(均值)的离散程度。由于地下水各化学组分的绝对数值范围可能相差很大,无法进行方差的对比,为此,先求出每个样本每个变量(Xi)与该变量均值(
¯X Xi¯X 衬度系数方差(Vσi2)的计算公式如下:
Vσ2i=1n∑ni=1(Vi−¯Vi)2 (1) 式中,Vi是地下水第i个化学组分的衬度系数;
¯Vi 当Vσi2> 1时,说明该化学组分受人类活动影响强烈;当0.5<Vσi2<1时,说明该组分受中等强度的人类活动影响;当Vσi2<0.5时,说明该组分受人类活动影响较小。
此外,运用Spearman’s 秩相关系数分析了不同土地利用类型地下水水化学组分之间的相关关系。数据分析使用 R 语言(4.0.3)、Origin(2019b)和Arcgis 10.5。
2. 结果与讨论(Results and discussion)
2.1 地下水水化学特点
研究区pH值的范围介于6.71—8.51之间,均值为7.62,地下水为中性到弱碱性水,样品的超标率为1.1%(表1)。TDS 变化范围为200—1408 mg·L−1,均值为612 mg·L−1。地下水样品中
CO2−3 NH+4 HCO−3 SO2−4 NO−3 NO−2 NH+4 NO−3 表 1 研究区地下水水化学参数统计表Table 1. Descriptive statistics of groundwater hydrochemical parameters in the study area.均值Mean value 最小值Minimum value 最大值Maximum value 标准差Standard deviation 超标率/%Exceed standard rate 国标Ⅲ类Standard(Ⅲ) pH 7.62 6.71 8.51 0.26 1.1 6.5—8.5 TDS/(mg·L−1) 612 200 1408 231 3.2 1000 K+/(mg·L−1) 2.10 0.27 10.6 2.00 — — Na+/(mg·L−1) 69.5 6.72 208 48.5 1.1 200 Ca2+/(mg·L−1) 107 7.86 281 47.5 — — Mg2+/(mg·L−1) 36.1 2.90 87.0 16.6 — — HCO3−/(mg·L−1) 418 165 792 137 — — Cl−/(mg·L−1) 67.3 5.21 190 49.6 0 250 SO42-/(mg·L−1) 71.8 4.03 248 47.9 0 250 NO3−/(mg·L−1) 42.4 0.20 338 66.3 19.4 88.6 NH4+/(mg·L−1) 0.159 0.002 1.106 0.237 6.5 0.64 NO2−/(mg·L−1) 0.160 0.002 1.960 0.307 0 3.29 TH/(mg·L−1) 414 28.3 978 159 39.8 450 注:国标Ⅲ类指地下水质量标准Ⅲ类(GB/T14848-2017)[17]. Note: Standard is grade Ⅲ standard for groundwater quality in China (GB/T14848-2017)[17]. 2.2 地下水水化学类型
Piper三线图常用来表征地下水化学成分的演化规律[18]。由图2 可以看出,研究区地下水主要的水化学类型为HCO3-Ca(Mg)型,占总水样的46.2%。近年来,由于人类活动的干扰,地下水水化学类型趋于复杂化,出现了Cl型水(18.3%),Na型水(39.8%)和SO4型水(3.2%)。不同土地利用类型下地下水水化学类型有明显的区别。正如表2显示,在农业用地和工矿用地中,地下水主要的水化学类型是HCO3-Ca(Mg)型,但是,农业用地受到施肥的影响,水化学类型出现了Cl型水(20.8%)和SO4型水(6.25%)。住宅用地地下水主要的水化学类型是HCO3-Ca(Mg)型水(40.0%),并且Na型水出现的比例高达55.0%。此外,在湿地(郑州黄河湿地自然保护区)内,Na型水是地下水主要的水化学类型,占比高达89.5%,这主要与湿地地下水受到黄河水和污水处理厂回水混合影响有关。
表 2 研究区不同土地利用类型地下水水化学类型统计表Table 2. Statistic table of groundwater hydrochemistry type of different land use in the study area水化学类型Hydrochemical type 水化学类型出现比例/%Proportions of hydrochemical type 农业用地Agricultural land 住宅用地Residential Land 湿地Wetland 工矿用地Industrial land HCO3-Ca(Mg) 58.3 40.0 10.5 83.3 Cl型水 20.8 20.0 10.5 16.7 Na型水 20.8 55.0 89.5 0 SO4型水 6.25 0 0 0 2.3 地下水化学的控制因素及离子来源
2.3.1 地下水化学的控制因素
地下水化学组分的形成机制主要受控于大气降雨、岩石风化、蒸发浓缩和混合作用等[19]。正如图3显示,地下水采样点的离子含量投点绝大部分落于Gibbs图中间位置,表明岩石风化是研究区地下水水化学离子组分的主要控制因素。但是,研究区部分采样点,有向右上方区域偏移的趋势,说明蒸发-浓缩作用对研究区地下水的水化学组分也有一定的影响。此外,部分点位超出了岩石分化的控制边界,说明这些采样点的水化学组分受到人类活动的影响。
2.3.2 人类活动的影响
衬度系数方差可用于区分地下水化学组分的形成以天然条件演化作用为主,还是受人类活动影响较大。地下水化学组分的衬度系数方差越大,表明该组分受人类活动影响就越强烈[20]。由表3可见,整体上看,在不同土地利用类型中地下水中的Ca2+、Mg2+和
HCO−3 NH+4 NO−3 NO−2 SO2−4 SO2−4 2.3.3 地下水化学的离子来源
为了进一步探讨地下水化学组分的来源,联合应用Ca2+/Na+ VS
HCO−3 HCO−3 表 3 中牟县地下水化学成分衬度系数方差表Table 3. variance analysis of contrast coefficient of groundwater hydrochemical compositions in the Zhongmu County水化学组分Hydrochemical compositions 农业用地Agricultural land 住宅用地Residential land 湿地Wetland 工矿用地Industrial land SO42− 0.513 0.267 0.283 0.796 Cl− 0.644 0.517 0.189 1.798 NH4+ 2.855 4.751 0.353 1.359 NO2− 4.938 3.168 1.297 1.949 NO3− 1.520 1.980 0.428 3.789 HCO3− 0.151 0.045 0.065 0.049 Na+ 0.725 0.279 0.183 0.443 K+ 1.232 0.933 0.380 0.156 Ca2+ 0.161 0.418 0.067 0.167 Mg2+ 0.256 0.140 0.092 0.100 2.4 水化学指标相关性分析
地下水化学组分之间的相互关系可以反映各离子的物质来源[22]。在本研究中,对农业用地、住宅用地和湿地地下水水化学组分分别做了相关性分析(表4),结果表明,农业用地地下水水化学组分,除三氮(NH4+、NO3−和NO2−)外,其余水化学组分之间均表现出极显著的正相关关系,表征它们来自于共同的来源。地下水中TDS、K+、Na +、Ca2+、Mg2+和HCO3− 主要来自于地层岩石风化[23-24]。在该研究区,这些离子主要受控于硅酸盐岩风化作用控制。NH4+与Cl−、TDS、SO42-、K+、Na +、Mg2+和HCO3−之间表现出显著或极显著的正相关关系。众所周知,NH4+主要来自于生活污水和化肥[25-26],并且污水和化肥中也含有一定量的Cl−、SO42-、K+和Na+。由于这些地下水样品在农业地区,因此,地下水中NH4+主要来自于化肥。水环境中NO3−的来源包括生活污水、化肥、粪肥、大气降雨等[27-28]。值得注意的是NO3−和NH4+表现出极显著的负相关关系,首先说明二者来自于共同的污染源-化肥。其次,由于NH4+在氧化环境下极易发生硝化反应转化为NO3−[29],从而降低水环境中NH4+的浓度。在这个地区,地下水处于氧化环境(DO的均值约为5.02 mg·L−1),并且NO3−的平均浓度高达61.7 mg·L−1,而NH4+的平均浓度仅为0.085 mg·L−1,表明地下水中发生了强烈硝化作用,所以二者表现出极显著的负相关关系。
在住宅用地,地下水中TDS、Cl−、SO42-、K+、Ca2+、Mg2+和HCO3−均表现出极显著的正相关关系,表征它们主要来自于地层岩石风化。值得关注的是Na+与NH4+表现出显著的正相关关系,表明二者有共同的来源。正如前面分析,水环境中的Na+与NH4+可能来自于生活污水和化肥[26]。由于采样站点位于住宅用地,并且村庄四周密布农田,且存在垃圾填埋场。因此,污水管网的破损,垃圾填埋场的渗漏,以及农业的施肥都会对其造成影响。与农业用地相似,NO3−和NH4+表现出显著的负相关关系,表明二者主要来自于生活污水和化肥,且地下水中发生了硝化作用。
表 4 研究区农业用地地下水水化学组分的相关性分析Table 4. Correlation analysis of groundwater hydrochemistry component of agricultural land in the study areaTH TDS SO42− Cl− NH4+ NO2− NO3− HCO3− Na+ K+ Ca2+ Mg2+ 农业用地 TH 1 0.950** 0.713** 0.877** 0.267 0.347* 0.132 0.778** 0.699** 0.663** 0.928** 0.916** TDS 1 0.801 0.922** 0.320* 0.337* 0.186 0.776** 0.796** 0.666** 0.850** 0.939** SO42− 1 0.750** 0.325* 0.093 −0.029 0.606** 0.709** 0.630** 0.624** 0.719** Cl− 1 0.396** 0.262 0.102 0.710** 0.764** 0.616** 0.815** 0.853** NH4+ 1 0.168 −0.496** 0.506** 0.532** 0.393** 0.188 0.402** NO2− 1 0.321* 0.170 0.176 0.030 0.356* 0.303* NO3− 1 −0.292* −0.222 −0.125 0.253 −0.003 HCO3− 1 0.879** 0.668** 0.587** 0.895** Na+ 1 0.642** 0.496** 0.880** K+ 1 0.619** 0.646** Ca2+ 1 0.732** Mg2+ 1 住宅 TH 1 0.767** 0.674** 0.734** −0.363 0.139 0.438 0.465* −0.344 0.513* 0.958** 0.681** TDS 1 0.893** 0.890** −0.122 0.159 0.283 0.626** 0.241 0.598** 0.684** 0.624** SO42− 1 0.832** −0.111 0.197 0.314 0.448* 0.266 0.352 0.593** 0.653** Cl− 1 −0.158 0.158 0.229 0.472* 0.111 0.543* 0.695** 0.614** NH4+ 1 0.272 −0.543* 0.19 0.480* −0.133 −0.436 −0.016 NO2− 1 0.193 0.002 0.06 0.252 0.257 0.207 NO3− 1 −0.373 −0.441 0.065 0.487* 0.099 HCO3− 1 0.424 0.564** 0.333 0.43 Na+ 1 0.089 −0.445* 0.032 K+ 1 0.471* 0.460* Ca2+ 1 0.531* Mg2+ 1 湿地 TH 1 0.946** 0.639** 0.722** −0.031 0.217 0.421 0.786** 0.789** 0.298 0.883** 0.818** TDS 1 0.611** 0.736** 0.109 0.098 0.333 0.830** 0.918** 0.291 0.787** 0.823** SO42− 1 0.756** 0.053 0.14 0.379 0.16 0.416 0.077 0.685** 0.391 Cl− 1 0.213 0.225 0.235 0.302 0.600** −0.057 0.705** 0.505* NH4+ 1 0.2 −0.552* 0.055 0.176 −0.301 −0.175 0.048 NO2− 1 0.265 0.043 −0.021 0.108 0.157 0.219 NO3− 1 0.168 0.213 0.169 0.315 0.463* HCO3− 1 0.844* 0.396 0.565* 0.821* Na+ 1 0.281 0.591** 0.825* K+ 1 0.296 0.261 Ca2+ 1 0.556* Mg2+ 1 注:** 表示在 0.01 水平上线性相关,* 表示在 0.05 水平上线性相关. Note:** P<0.01; * P<0.05. 在湿地,水化学指标TDS、Cl−、
SO2−4 NH+4 NO−3 NO−3 NH+4 NO−3 NO−3 3. 结论(Conclusion)
(1)郑州市中牟县地下水pH的变化范围介于6.71—8.51之间,处于中性到弱碱性。地下水中阳离子的大小排序为Ca2+> Na+> Mg2+>K+>
NH+4 HCO−3 SO2−4 NO−3 NO−2 NO−3 (2)地下水水化学类型主要为HCO3-Ca(Mg)型,占总水样的46.2%。农业用地受到施肥的影响,水化学类型出现了Cl型水和SO4型水。而湿地受黄河水和污水处理厂回水补给的混合影响,导致主要的水化学类型改变为HCO3-Ca·Mg·Na型水。
(3)基于Gibbs模型分析表明,中牟县地下水水化学组分主要控制因素是岩石风化作用。人类活动对水化学组分也存在一定的影响。其中,三氮受人类活动影响强烈,而Na+、K+、
SO2−4 (4)基于相关性分析,在不同土地利用类型下,地下水水化学组分除三氮(NH4+、NO3−和NO2−)外,均表现出极显著或显著的正相关关系,表征它们来自于地层岩石风化。而NH4+和NO3−表现出显著的负相关关系,二者主要来自于化肥和生活污水。在农业用地和住宅用地中地下水可能发生强烈的硝化作用,但在湿地,地下水受到黄河河水的稀释,且地下水可能发生了反硝化作用。
(5)上述研究结果表明,生活污水和化肥是该地区地下水主要的污染源。因此,建议当地政府和环保部门要严格立法和监管,禁止生活污水的不达标排放。此外,农业管理者应该推广科学施肥策略(如测土配方施肥,因时和因作物施肥,施用缓释肥等)来提高肥料的利用率,防止过量施肥对地下水的污染。
-
[1] 吴霜, 王家伟, 刘利, 等. 电解锰渣综合利用评述[J]. 无机盐工业, 2016, 48(4):22-25 [2] 吴建锋, 宋谋胜, 徐晓虹, 等. 电解锰渣的综合利用进展与研究展望[J]. 环境工程学报, 2014, 8(7):2645-2652 [3] XIN B, CHEN B, DUAN N, et al. Extraction of manganese from electrolytic manganese residue by bioleaching[J]. Bioresource Technology, 2011, 102(2):1683-1687 [4] 范丹, 邓倩, 熊利芝, 等. 从电解锰渣中提取金属锰[J]. 吉首大学学报(自然科学版), 2012, 33(1):94-97 [5] OUYANG Y, LI Y, LI H, et al. Recovery of manganese from electrolytic manganese residue by different leaching techniques in the presence of accessory ingredients[J]. Rare Metal Materials & Engineering, 2008, 37(3):603-608 [6] 王勇. 电解锰渣作水泥混合材的研究[J]. 新型建筑材料, 2016, 43(5):78-80 [7] 高松林, 冯云, 宋利峰, 等. 电解锰渣替代石膏作水涨调凝剂的试验[J]. 水泥技术, 2001(6):75-76 [8] 陈平, 刘荣进, 安庆锋. 锰渣矿物掺合料水泥混凝土耐久性试验研究[J]. 混凝土, 2008(10):77-79 [9] 张金龙, 彭兵, 柴立元, 等. 电解锰渣-页岩-粉煤灰烧结砖的研制[J]. 环境科学与技术, 2011, 34(1):144-147 [10] 兰家泉. 玉米生产施用锰渣混配肥的肥效试验[J]. 中国锰业, 2006, 24(2):43-44 [11] 田定科, 罗来和. 烤烟生产施用锰渣混配肥的肥效试验[J]. 中国锰业, 2007, 25(2):25-26 [12] 蒋明磊, 杜亚光, 杜冬云, 等. 利用电解金属锰渣制备硅锰肥的试验研究[J]. 中国锰业, 2014, 32(2):16-19 [13] 胡南, 周军媚, 刘运莲, 等. 硫酸锰废渣的浸出毒性及无害化处理的研究[J]. 中国环境监测, 2007, 23(2):49-52 [14] 王积伟, 周长波, 杜兵, 等. 电解锰渣无害化处理技术[J]. 环境工程学报, 2014, 8(1):329-333 [15] 陈红亮. 新鲜电解锰渣和长期堆存渣的矿物成分和毒性特征的差异分析[J]. 贵州师范大学学报(自然科学版), 2016, 34(2):32-36 期刊类型引用(10)
1. 陆红雨,程红光,Gratien Twagirayezu,房鑫,黄鉎岚,邓林波,吉波. 生物炭辅助湿法球磨锰渣增效吸附Sb(V). 中国环境科学. 2024(07): 3741-3748 .  百度学术
百度学术
2. 田祎,赵虎,赵博超,矫云阳,蒋文博,叶旌. 《锰渣污染控制技术规范》(HJ 1241-2022)解读及实施建议. 世界有色金属. 2024(10): 188-192 .  百度学术
百度学术
3. 叶其樊,杨勇,李美娴,陈发明,陆展升,魏汉可,黄敏峰,张丽云. 新型压滤洗涤设备在电解金属锰制液过程的工程应用. 中国锰业. 2024(04): 121-125 .  百度学术
百度学术
4. 赵博超,聂一凡,王雪婷,田向勤,田祎,潘涔轩. 不同制液工艺对锰矿锰浸出回收及钙镁铁迁移影响. 化工学报. 2024(S1): 292-299 .  百度学术
百度学术
5. 康志鹏,林晔,岳波,闫敏婕,孟棒棒,梁宇廷. 水洗联合固化处理电解锰渣. 环境工程学报. 2023(01): 235-241 .  本站查看
本站查看
6. 刘士朋,张欢欢,程金科. 电解锰渣中氨氮的草酸浸取工艺及机理研究. 硅酸盐通报. 2022(02): 715-724 .  百度学术
百度学术
7. 王鹏星,祝楚微,汪玉碧,刘兵兵,韩桂洪,黄艳芳. 电解锰渣有价元素回收及有害物质处理技术研究进展. 化工矿物与加工. 2022(07): 1-9 .  百度学术
百度学术
8. 赵侣璇,刘凯,覃楠钧,樊勇吉,宋晓薇. 电解锰渣锰和硫酸铵资源回收及无害化试验研究. 工业安全与环保. 2019(01): 103-106 .  百度学术
百度学术
9. 刘谊兵,赵钺,杨高天,张星本. 新型过滤洗涤一体技术在电解锰废渣脱水洗涤中的应用研究. 矿冶工程. 2019(04): 72-74+78 .  百度学术
百度学术
10. 蓝际荣,孙燕,潘滢,李卓蔓,杜冬云. 球磨与助剂强化选择性回收电解锰渣中的锰. 中国有色金属学报. 2019(08): 1749-1755 .  百度学术
百度学术
其他类型引用(18)
-

 点击查看大图
点击查看大图
计量
- 文章访问数: 2025
- HTML全文浏览数: 1773
- PDF下载数: 233
- 施引文献: 28





 下载:
下载: