-
我国不发达的偏远农村地区由于水资源缺乏不得不使用重金属超标的水体作为饮用水水源[1],一些地区存在锰含量超标的现象[2-3],对饮用水安全造成威胁。当人体摄入过量重金属后,可能导致胃溃疡、脑损伤、心力衰竭、糖尿病以及神经系统疾病[4-5]。由于农村饮用水源较分散,常规用于城市集约化饮用水处理的工艺在农村较难实现,重力驱动膜过滤系统(gravity-driven membrane filtration system,GDM)作为一种分散性强、操作简单、低能耗和低成本的水处理技术,在农村地区饮用水处理方面具有较高的应用前景[6]。GDM在4~10 kPa条件下运行,无需任何物理或化学清洗,能够稳定运行数月甚至数年[6-8],适用于农村水处理场景。在GDM系统中,原水中的大分子污染物被膜截留,随着时间的增长,在膜表面形成一层不均匀的污垢层,进一步截留和吸附污染物以实现水质净化[9-11]。
传统的GDM系统很难去除重金属[12],对此,研究者们尝试对GDM系统进行改进以增强处理效能。一些研究将各种预处理方式与GDM系统相结合,以提高重金属的去除率。这包括在膜表面预涂锰氧化物增加生物膜的孔隙率,提高微生物群落的多样性,利用微生物去除锰和铁[13]。此外,DU等[14]通过在膜表面的粉末活性炭上沉积一层锰氧化物,使锰氧化细菌在膜上富集,从而促进锰的去除。SHI等[12]还通过在膜表面添加零价铁从而增加生物膜的多孔结构,极大地提高了重金属的去除率。但是,在膜表面添加锰和零价铁等重金属,易造成锰和铁的流失,导致二次污染。因此,开发一种绿色环保的方法提高GDM系统对重金属的去除,以及对促进GDM系统在饮用水处理中的应用具有重大意义。
木质膜(wood membrane,WM)是一种具有几至几十微米孔道结构的天然绿色微滤膜,在水处理领域具有巨大的应用潜力[15]。VITAS等[16]将其羧基化后,提高了对铜的去除率。YANG等[17]将木质膜巯基功能化,以快速去除重金属。考虑到经济性和材料可得性,运用木质膜改进GDM系统在农村易于实现。当前关于木质膜运用于GDM系统的报道较为缺乏,其对GDM系统运行的影响仍不清楚。因此,本研究利用典型乔木(白杨木)为原材料作为木质膜,探究基于聚合物微滤(microfiltration,MF)膜和木质膜的GDM系统对重金属的去除效能及潜在机理,以期为解决农村饮水安全问题提供绿色且成本低廉的处理方案。
-
实验用水取自北京市饮用水水源之一的京密引水渠,其水中Fe、Mn和Cu的质量浓度分别为(111.3±0.2)、(4.2±0.2)和(31.69±0.1) μg·L−1。为了模拟某些地区Mn含量超标而Fe和Cu含量不超标的情况,在京密水中加入FeCl3、MnCl2和CuCl2,控制Fe、Mn和Cu质量浓度均为200 μg·L−1。最终进水的其他化学性质为:pH为7.8~8.1;电导率为353.5~376.1 μS·cm−1;总有机碳为9.4~13.7 mg·L−1,出水以期达到我国《生活饮用水卫生标准》(GB 5749-2022)。
-
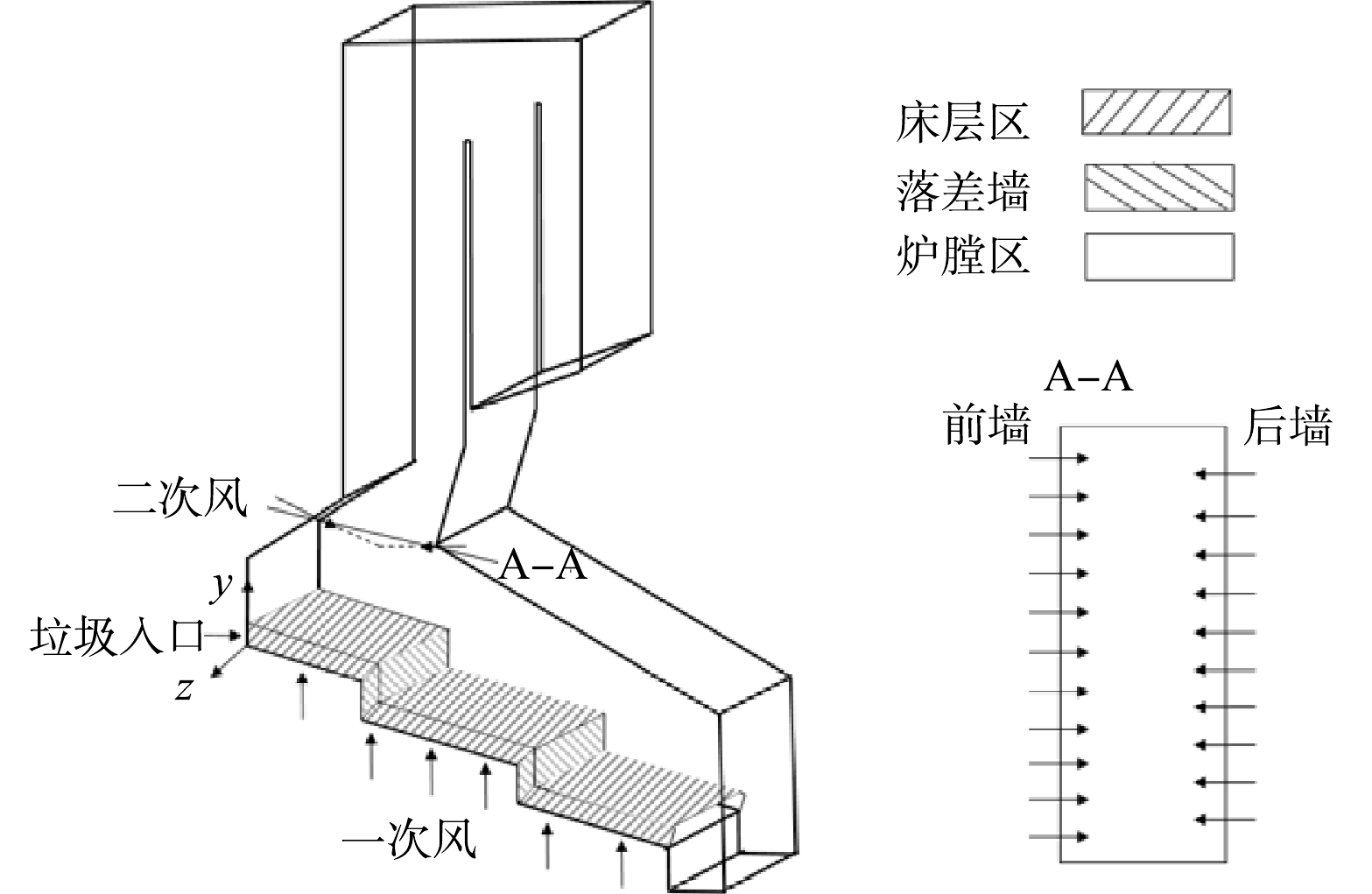
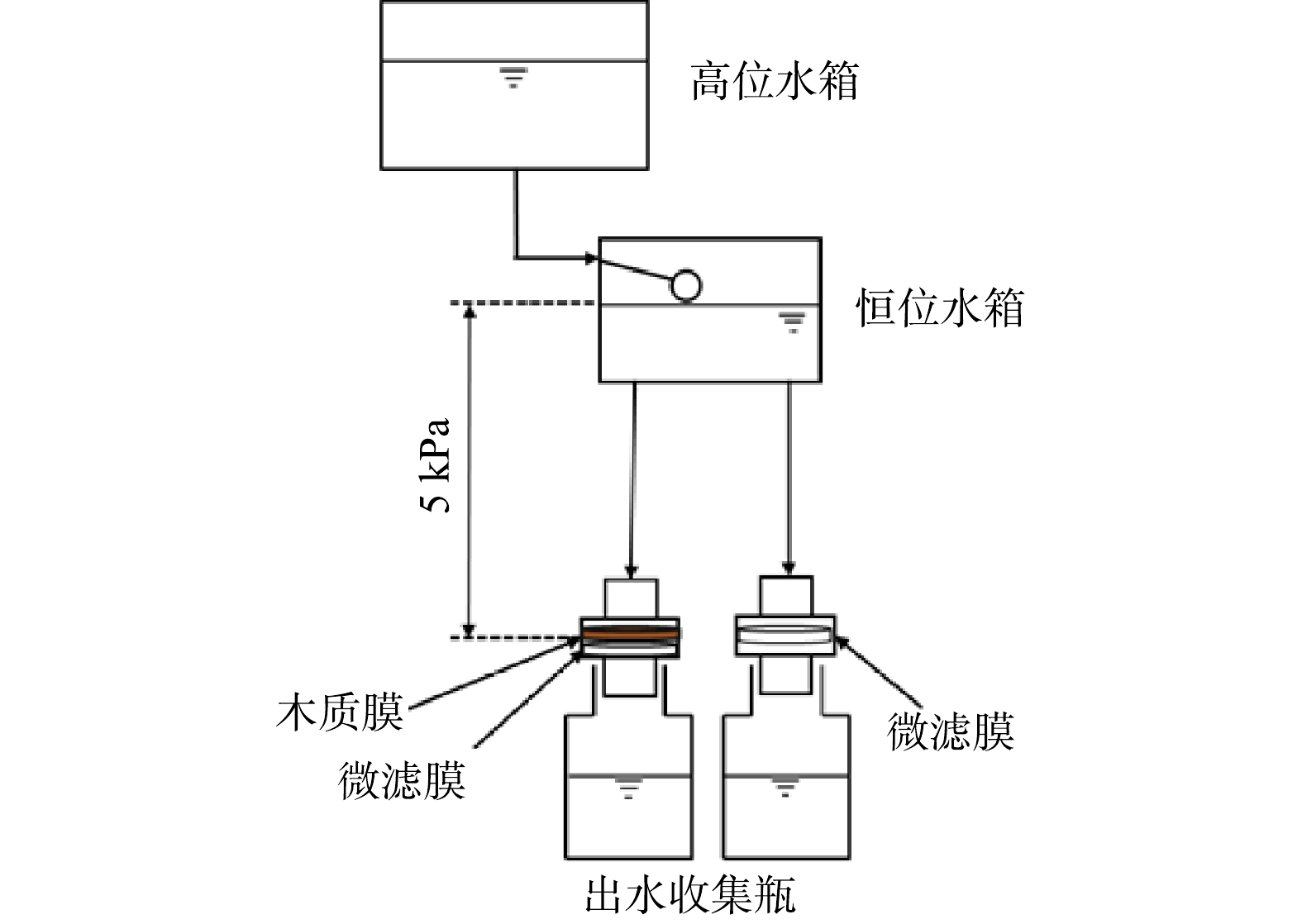
本实验的GDM系统装置图如图1所示,采用圆形白杨木和醋酸纤维素膜分别作为木质膜(WM)和聚合物微滤(MF)膜。木质膜从福建省森林人木材公司购买,孔径为10~70 μm,密度为0.39 g·cm−3,厚度为5 mm,容积为0.25 mL,比表面积为2.13 m2·g−1,膜面积为7.07 cm2,木质膜对Cu的吸附量为0.06 mg,对Fe和Mn的吸附量约为0,其清水通量为24 442.5 L·(m2·h)−1。聚合物微滤膜的孔径为0.45 μm,对Fe、Mn和Cu的吸附量约为0,清水通量为1 151.8 L·(m2·h)−1。木质膜和聚合物微滤膜的表面形貌如图3(a)~(b)所示,木质膜表面粗糙且存在较大孔洞,而聚合物微滤膜表面致密均匀。实验设置2组GDM系统,第1组为木质膜耦合聚合物微滤膜系统(GDM1),其中木质膜为GDM1-WM,微滤膜为GDM1-MF;第2组为聚合物微滤膜系统(GDM2),其微滤膜为GDM2-MF。实验前,将木质膜依次通过乙醇、1% NaOH和热超纯水进行抽滤冲洗,直至通过木质膜的出水在紫外254 nm处的吸光度(UV254)小于0.001。同样地,用超纯水将微滤膜冲洗至UV254小于0.001。2组GDM系统以死端过滤模式并联运行,膜有效过滤直径为3 cm,驱动压力为恒压5 kPa(50 cm水头)。为了尽可能减少其他因素的影响,2组过滤系统共用1个恒位水箱。运行过程中,每天记录渗透通量,定期收集出水并对水质进行检测。
-
进出水样品的紫外吸光度采用紫外-可见分光光度计(UV-2600,岛津公司,日本)测定,利用680 nm处吸光度检测水样颗粒物浓度的变化。采用荧光分光光度计(F-4600,日立,日本)识别胞外聚合物(extracellular polymeric substances,EPS)中的蛋白和腐殖类物质。水样中Fe、Mn和Cu的含量经过微波消解之后用电感耦合等离子体质谱仪(inductively coupled plasma-mass spectrometry,ICP-MS,Agilent 7800,美国)检测。
-
1)生物膜表征。在实验结束后将生物膜样品切割成数份。取1块生物膜进行冷冻,经过提取脱氧核糖核酸(deoxyribonucleic acid,DNA)、聚合酶链反应(polymerase chain reaction,PCR)扩增等流程,在Illumina MiSeq平台对16S rRNA进行测序,在美吉生物云平台(上海美吉生物医药科技有限公司)进行数据处理,分析生物膜中微生物群落组成的信息。生物膜样品经冷冻干燥后,用溅射法对样品进行镀铂,在扫描电子显微镜(scanning electron microscopy,SEM,SU8020,日本)下观察生物膜的表面和横截面形貌。此外,生物膜经自然风干后进行如下表征:用X射线光电子能谱(X-ray photoelectron spectroscopy,XPS,ESCALAB 250Xi,美国)揭示生物膜中的元素组成及其化学键信息;通过傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR,Spectrum 400,美国)对生物膜的官能团进行表征;采用接触角仪(Dataphysics,OCA15EC,德国)测定生物膜的亲疏水性。
2) EPS的提取与测定。取部分生物膜,将其剪碎并置于磷酸盐缓冲溶液(phosphate buffer solution,PBS)中,再进行涡旋振荡和离心,取上清液即为EPS提取液[18]。EPS中的蛋白含量用Bradford法测定[19]。多糖含量采用苯酚-硫酸法测定[20]。
3)数据分析方法。数据处理在Microsoft Office 2019中进行,并使用Origin 2021作图。2组GDM系统的组间差异通过配对t检验方法进行检验,在IBM SPSS Statistics 26中进行。
-
如图2(a)所示,GDM系统共运行67 d,根据通量的变化可分为0~10、11~40和41~67 d 3个阶段,这与FENG等[21]发现GDM系统通量呈现阶段性变化的现象一致。在第I阶段(0~10 d),2组GDM系统通量较高,但迅速降低,这与进水中的污染物堵塞膜孔以及生物膜的形成有关[22];在第II阶段(11~40 d),通量缓慢下降;第III阶段(41~67 d)中,2组GDM系统通量均维持在一个相对稳定的状态。最终,在第III阶段,GDM1系统的平均通量为1.1 L·(m2·h)−1,GDM2系统的平均通量为0.9 L·(m2·h)−1,GDM1系统的通量显著高于GDM2(P<0.05)。与此同时,由图2(b)可见,生物膜的水力阻力与通量呈现出完全相反的趋势,并且GDM1系统的阻力显著低于GDM2(P<0.05)。这表明在GDM1系统中,木质膜的存在降低了系统的水力阻力,因此,GDM1系统具有较高的稳定通量。
在GDM系统不同运行阶段共选取5个时间点测定重金属离子质量浓度。如图2(c)~(e)所示,GDM1和GDM2系统在运行后期对3种重金属的去除率均表现出Fe>Cu>Mn的规律。其中,GDM1在稳定运行阶段(第III阶段)的Fe、Mn、Cu的平均去除率分别为67%、43%和59%,GDM2 中Fe、Mn、Cu的平均去除率分别为64%、15%和36%。2组重力流系统Fe和Cu的去除率均高于Mn,这是由于Fe和Cu在中性或弱碱性体系中易形成氢氧化物胶体而更易被系统截留,同时,也通过吸附于膜表面、微生物细胞壁或蛋白质衣壳等去除,而Mn的去除更多依赖于与生物膜以及特定微生物群落的直接相互作用[23-24]。在运行初始阶段,生物量不断增长,使得生物吸附位点增多,Fe的去除率增加,随着吸附位点逐渐饱和,Fe的去除率有所降低。此外,由于GDM1的通量高于GDM2,使得GDM1截留的生物量更多,从而具有较多的吸附位点,因此,GDM1的Fe去除率高于GDM2。GDM1对Mn的去除率随着时间的增长而逐渐增加,而GDM2的去除率却降低,去除规律的差异主要与微生物和Mn之间的相互作用有关[25],这将在后续进一步讨论。GDM1和GDM2对Cu的去除原理与Fe类似,主要通过生物吸附去除Cu[26],GDM1的吸附位点多于GDM2,因此,GDM1对于Cu的去除率相对较高。鉴于Fe和Mn去除率在49 d后呈现出相对降低的趋势,这可能是由于可溶性微生物产物与重金属结合从膜表面流失进入出水导致的[27],建议在67 d对膜进行冲洗,并可以在膜表面接种锰氧化细菌,进而缩短启动时间和提高去除率。
根据图2(f)所示,即使进水浊度有一定程度的波动,GDM1和GDM2系统均能显著降低浊度(P<0.001)。表明GDM1和GDM2系统有着良好的颗粒或胶体截留能力。与此同时,GDM1系统还可显著降低出水中DOM的芳香性(SUVA254)(P<0.05),而GDM2系统的作用不显著(P>0.05)。
-
PETER-VARBANETS等[8]认为生物膜的结构特性是影响GDM通量的主导因素,因此本研究对生物膜的形态结构进行了表征,3种生物膜的表面和横截面结构在SEM下呈现出较大差别。由图3(c)~(e)可知,GDM1-WM的生物膜表面存在较多孔洞,且GDM1-MF生物膜表面为疏松多孔的结构,而GDM2-MF生物膜比GDM1-WM和GDM1-MF均更加致密。有研究[28]表明,生物膜的多孔结构和GDM的稳定通量之间存在正相关关系,较大的孔径有助于水流穿过。另一方面,如图3(f)~(h)所示,GDM2-MF生物膜的厚度远大于GDM1中WM和MF生物膜的厚度,不利于水流的通过。因此,木质膜的存在改变了GDM生物膜的表面和横截面结构,造成2种GDM系统的通量和水力阻力差异,这部分解释了图2(a)~(b)中GDM2系统比GDM1系统的水力阻力更大且稳定通量更低的原因。
如图3(i)所示,2个GDM系统生物膜的接触角显示其亲疏水性存在明显差异。GDM1-WM、GDM1-MF和GDM2-MF中生物膜的初始接触角分别为141.6°、93.6°和87.7°,因此GDM1-WM生物膜表现出强疏水性,GDM1-MF为弱疏水性,而GDM2-MF为弱亲水性。GDM1-WM生物膜的动态接触角下降缓慢,而GDM1-MF和GDM2-MF的生物膜动态接触角下降更快且下降速度近似。GDM1系统中2种生物膜均表现为疏水性,而疏水性物质如具有双键或芳环的物质与金属离子存在阳离子-π键作用,这种作用可能加强GDM1系统中重金属与生物膜的相互作用,使得重金属更易被截留[29]。此外,值得注意的是,相比GDM2系统,GDM1系统中生物膜更加疏水但其稳定通量更高,这表明生物膜结构对稳定通量的主导作用强于亲疏水性的作用。
图3(j)反映了3种生物膜的红外光谱结果。3种生物膜中1 634、1 545和1 457 cm−1处的峰分别为—NH2/C=O、C—N/N—H以及C—OH。这些基团与微生物分泌的蛋白类物质有关[30]。而1 244/1 257 cm−1和1 024 cm−1分别为C—O—C和C—O,主要来自于多糖类物质[30]。GDM1-MF生物膜中的—NH2/C=O、C—N/N—H、C—OH、C—O—C和C—O峰的强度最强,其次是GDM2-MF和GDM1-WM生物膜,这表明GDM1-MF可能含有更多蛋白和多糖类物质。3 274 cm−1和1 727 cm−1处的峰来自于—OH和—COOH中的C=O的拉伸振动[16, 30-31],这些峰在GDM2-MF中均显示出较低的强度。同时,与GDM1-MF和GDM2-MF相比,GDM1-WM生物膜中—OH强度更强。CHOIŃSKA-PULIT等[32]认为—OH和—COOH等可以作为活性金属结合位点,可将其从溶液中去除。因此,GDM1系统中的生物膜具有更好的重金属去除能力。生物膜内化学键特性的XPS表征结果如图3(k)~(l)所示。O1s图谱中532.5 eV处的峰为C—O—C或C—O—H键,常见于醇、半缩醛、糖[33];N1s图谱中399.2 eV处的峰被解析为胺中的N—H,与蛋白的存在有关[34]。GDM1-MF生物膜的C—O—C和N—H的信号最强,其次是GDM2-MF和GDM1-WM。因此,FTIR和XPS的结果均表明木质膜的存在可能增加了GDM系统的蛋白和多糖含量。
-
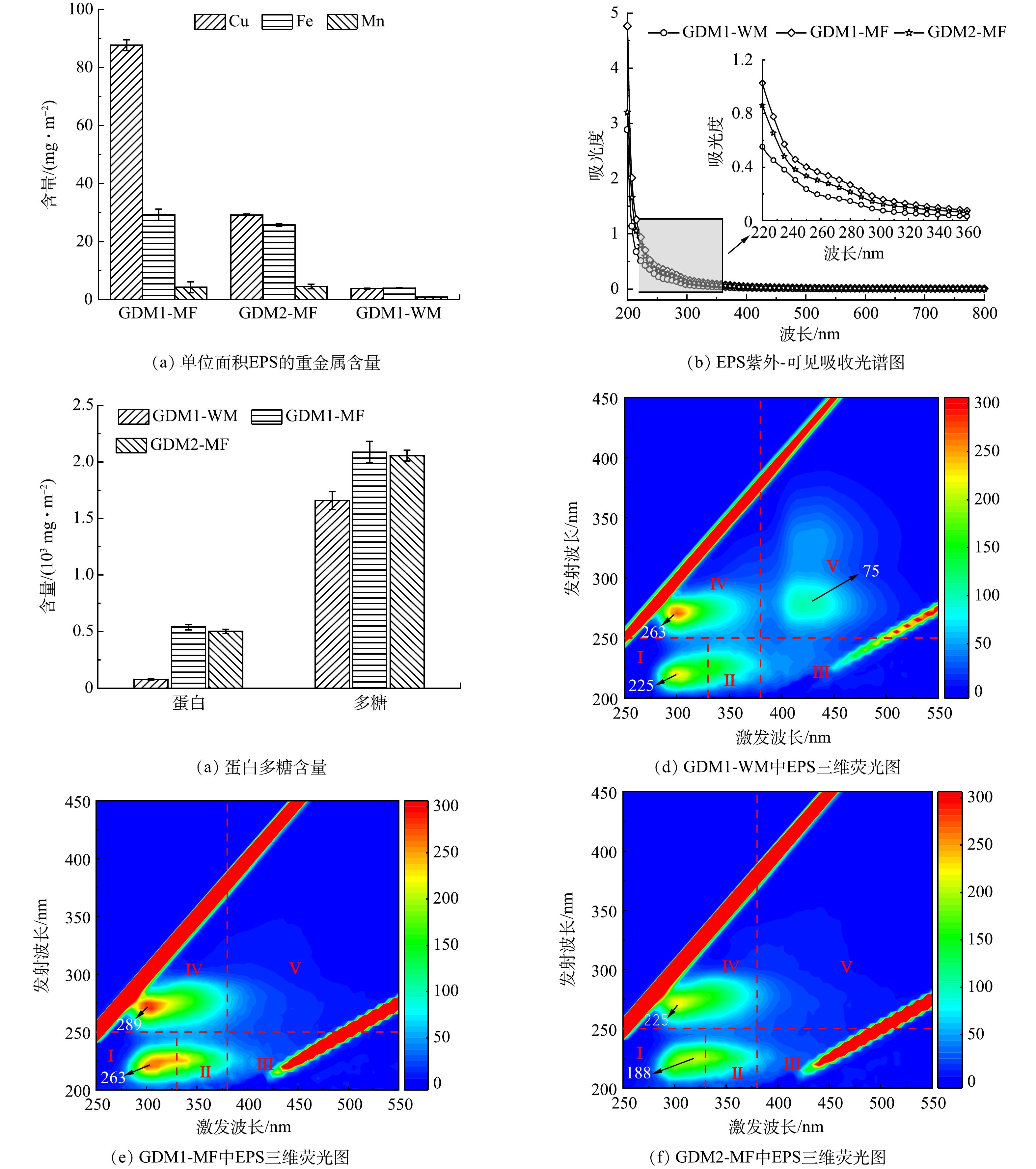
为确定生物膜对重金属去除的作用,测定了实验结束时EPS中单位面积生物膜内的重金属含量。如图4(a)所示,单位膜面积上Fe、Mn和Cu的含量在2组GDM系统生物膜中均表现出相同规律,即GDM1-WM+GDM1-MF>GDM2-MF,并且2组GDM系统中微滤膜单位膜面积生物膜中Fe和Cu的含量均为GDM1-MF>GDM2-MF。上述结果表明GDM1的生物膜对Fe、Mn和Cu的去除作用优于GDM2,木质膜促进了GDM1-MF对Fe和Cu的去除。
为进一步探究生物膜的化学组成对重金属的去除作用,对生物膜中蛋白和多糖的含量进行了分析。图4(b)中UV254吸光度大小表现为:GDM1-WM<GDM2-MF<GDM1-MF,与图4(c)中生物膜中的蛋白和多糖含量规律一致。以上结果表明3种膜表面EPS的含量为:GDM1-WM<GDM2-MF<GDM1-MF。此外,图4(d)~(f)展示了生物膜内荧光有机物的组成和含量。GDM1-WM和GDM1-MF生物膜中EPS的荧光强度均强于GDM2-MF,表明在GDM1系统中,木质膜的存在使得系统生物膜中酪氨酸(荧光区域I)和色氨酸(荧光区域II)类物质以及溶解性微生物副产物的含量(荧光区域IV)增加。GDM1系统生物膜中的蛋白和多糖含量高于GDM2,与FTIR和XPS结果一致。这可能是因为增加的木质膜能够为微生物生长繁殖提供适宜的条件,从而促进EPS的分泌,致使GDM1中EPS的浓度更高,从而对重金属的吸附作用更强[35]。ZHAO等[29]还发现蛋白类物质与金属离子存在阳离子-π键作用,故GDM1系统EPS中更高的蛋白含量促进了重金属的去除。与此同时,EPS在通量稳定中发挥着重要作用,本研究中GDM1系统同时具有更高含量的EPS和更高的稳定通量,这符合TANG等[36]发现的以蛋白和多糖为特征的EPS含量越高,相对应的稳定通量也越高的结果。此外,在GDM1-WM生物膜中存在明显的腐殖酸类物质的荧光峰信号(荧光区域V),这可能是由于木质膜中的木质纤维素吸附了水中的腐殖酸[37],这与GDM1出水中有机物芳香性(SUVA254)(图2(f))显著降低相一致。另一方面,这些在木质膜表面或内部的腐殖类物质可与金属络合形成胶体[38],对GDM1系统出水重金属质量浓度的降低有一定贡献。
-
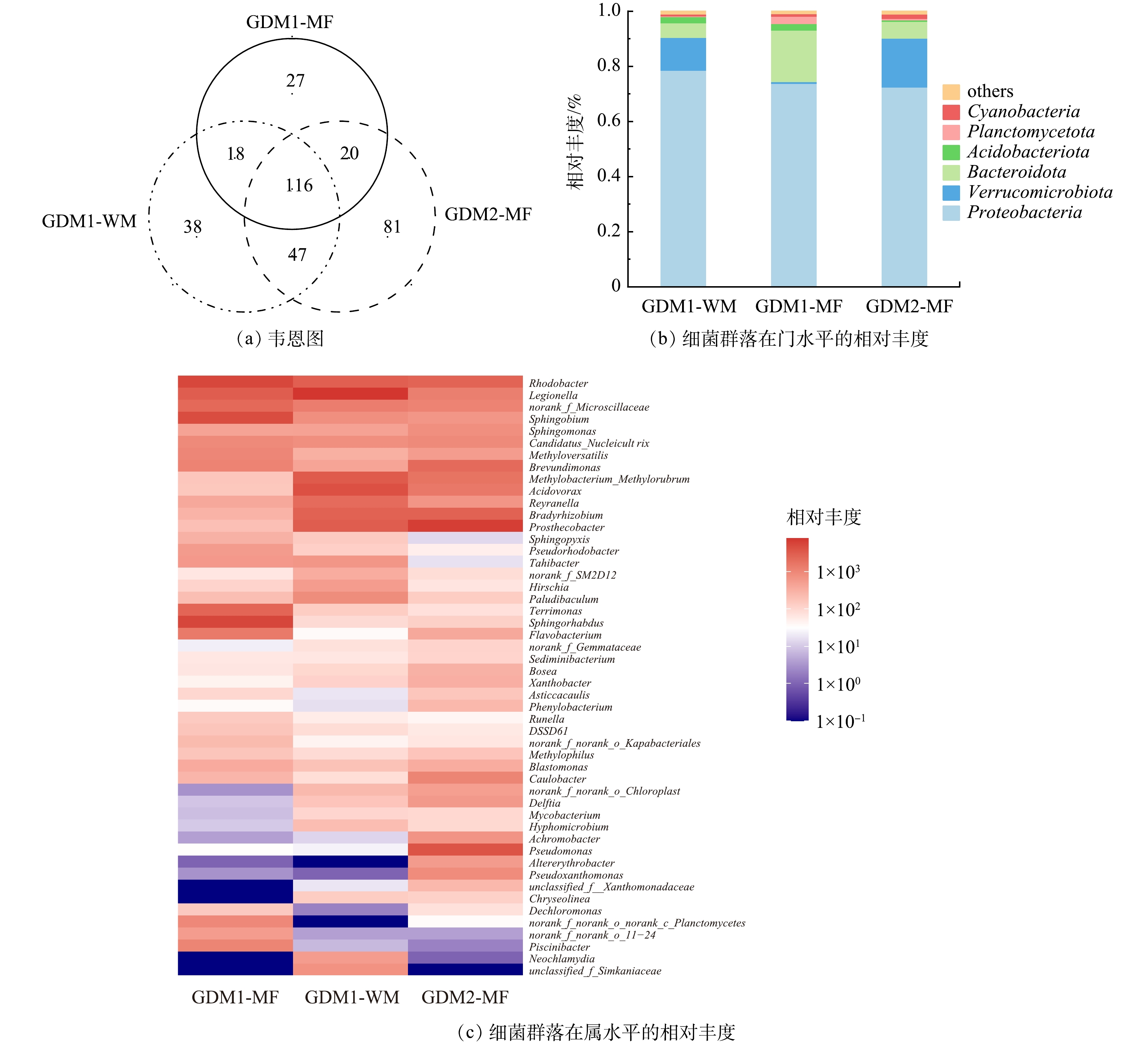
如图5(a)所示,GDM1-WM、GDM1-MF和GDM2-MF生物膜中微生物的OTU数分别为219、181和264个。其中,3种生物膜中有116个OTU是共有的,对于单独拥有的OTU数量,GDM2-MF最多(81个),其次是GDM1-WM(38个)和GDM1-MF(27个),并且GDM2-MF中Chao(270.4)和Shannon指数(3.6)均高于GDM1-MF(分别为202.4和3.2)。这表明木质膜的存在能降低GDM系统细菌群落的丰富度和多样性。由图5(b)可见,3种生物膜内变形菌门Proteobacteria的相对丰度均最高(70%~80%),疣微菌门Verrucomicrobiota和拟杆菌门Bacteroidota为次优势菌门。GDM1-WM和GDM1-MF中酸杆菌门Acidobacteriota的相对丰度均高于GDM2-MF,而Acidobacteriota具有去除Cu的作用[39],因此,GDM1系统对Cu的去除效果较好。
图5(c)反映了属水平微生物群落的差异。GDM1-MF中的norank_f__Microscillaceae、甲基异黄酮Methyloversatilis和脱氯单胞菌Dechloromonas的相对丰度均高于GDM2-MF,而此3种菌可产生大量EPS[40-42],最终导致GDM1-MF中的EPS含量更高,进一步解释了图4(c)的结果。同时,EPS中的蛋白对重金属有较强的相互作用[29, 35],因此,GDM1系统对重金属的去除效果更好。黄杆菌属Flavobacterium、红细菌属Rhodobacter、鞘氨醇单胞菌属Sphingopyxis、军团菌Legionella以及生丝微菌属Hyphomicrobium属于锰氧化细菌,它们能将Mn2+氧化为Mn3+或者Mn4+,形成大量的锰氧化物并通过锰氧化物的吸附作用和化学自催化氧化去除Mn,从而实现重金属的去除[13, 25, 43]。尽管GDM2-MF中Hyphomicrobium的相对丰度高于GDM1-MF,但低于GDM1-WM。总之,稳定运行阶段GDM1系统中的Flavobacterium、Rhodobacter、Sphingopyxis、Legionella和Hyphomicrobium相对丰度较高,对Mn的去除效果较好。GDM2系统在第II阶段对Mn的去除优于GDM1系统,这可能是因为锰氧化细菌还未在GDM1系统上稳定生长,但随着时间的增加而逐渐增长,最后可能由于GDM2膜表面的锰氧化物的吸附容量达到饱和而导致去除率下降。此外,Flavobacterium可以通过吸附作用去除Cu[44],而GDM1-MF中Flavobacterium的相对丰度远高于GDM2-MF,因而GDM1系统对Cu的去除效果更好。综上,尽管木质膜降低了系统微生物群落的丰富度和多样性,但其促进了去除重金属的细菌群落的生长,提升了微生物群落去除重金属的专一性,使得GDM1系统具有更好的重金属去除能力。
-
1)在稳定运行阶段,木质膜耦合聚合物微滤膜(GDM1S)和聚合物微滤膜(GDM2)的重力驱动膜过滤系统的稳定通量分别为1.1 L·(m2·h)−1和0.9 L·(m2·h)−1,且GDM1对Mn和Cu的去除率达43%和59%,比GDM2分别高出28%和23%。
2)与GDM2系统相比,GDM1-WM和GDM1-MF表面生物膜结构更加疏松多孔,因此,具有更高的稳定通量。同时,GDM1系统整体胞外聚合物(EPS)含量更高,从而可强化对重金属的去除。
3) GDM1系统中微生物群落的多样性和丰富度低于GDM2系统,但与重金属直接去除有关的微生物菌群(如锰氧化细菌、Flavobacterium和Acidobacteriota)以及通过分泌EPS间接促进重金属去除的微生物菌群丰度更高。




 下载:
下载: