-
铅(Pb)是一种普遍存在且具有生理毒性和生物蓄积性的重金属[1],低浓度暴露也会对人体和生活环境造成永久性损害[2-3],被公认为最具毒性的金属之一[4]。铅离子主要来源于铅冶炼、电池制造、印刷和采矿等行业。根据地表水环境质量标准,Ⅴ类水中Pb2+的含量为不高于0.1 mg·L−1[5]。目前,重金属检测方法包括原子光谱法、色谱法、电化学法、表面增强拉曼光谱法等[6-8]。这些方法灵敏度高、重现性好,但存在预处理复杂、耗时、设备昂贵等缺点[9]。与之相比,荧光检测法具有速度快、操作简单、价格低廉等优点[10],适用于偏远分散水源的检测以及突发环境事件的应急检测。因此,开发一种便捷原位检测铅离子的方法势在必行。
金属-有机框架(MOFs)是一种新型的微孔材料,它通过金属离子或金属簇与有机配体之间的配位进行组装,在吸附和分离[11-12]、催化[13]、光电及电化学[14]等方面被广泛使用。MOFs不仅具有表面积大、可结合位点多、设计性强等特点[15],而且具有良好的荧光性能。已有研究[15-16]表明,基于MOFs的荧光传感器可以与重金属离子选择性结合,与Fe3+、Cu2+、Pb2+、Cr2O72+和CrO42+等结合后具有敏感的荧光淬灭响应。近年来,有研究者利用这种效应,开展了铅离子荧光法检测相关研究。LIU等[17]通过合成碱土金属有机框架[Ca2(µ10-L)(EtOH)]n,利用荧光淬灭机制检测Pb2+,检测限达69.4 µmol·L−1。LI等[18]合成的基于氟烯基的镧系元素金属-有机框架([Eu2(FDC)3DMA(H2O)3]·DMA·4.5H2O),作为荧光探针可以快速选择性检测水相中的铅离子,检测限为8.22 µmol·L−1。现已报道的荧光探针存在灵敏度较低的问题,故制备灵敏高效的荧光探针具有十分重要的现实意义。
碳点(CDs)是一种新型的量子点,大量研究[19-21]表明,CDs@MOFs复合材料是可调可设计的荧光探针,对各种目标分析物具有高灵敏度和选择性,是一种很有前途的荧光材料。HAO等[19]通过合成花球状CDs@Eu-DPA MOFs,开发了一种检测Cu2+的荧光探针,CDs发射的荧光可以降低激发源不稳定性等系统误差,从而提高荧光探针的精度。XU等[20]设计了一种CD@Eu3+-MOF-253复合材料用于检测Hg2+,并发现Hg2+通过与CDs的表面官能团协调,可以显著淬灭CDs的荧光,而不影响Eu-MOF的荧光强度。到目前为止,已有许多关于MOFs的荧光探针研究[19-21],然而,CDs@MOFs荧光材料用于重金属铅离子检测的研究鲜有报道。
本研究通过碳点(N,S,I-CDs)修饰MIL-101-NH2, 制备了CDs@MIL-101-NH2复合材料,通过TEM、XRD、FT-IR、XPS等对材料进行表征,研究碳点修饰对MOFs结构的影响以及材料浓度、pH值、时间对CDs@MOFs复合材料荧光强度的影响,在将复合材料作为荧光探针用于水中Pb2+的荧光检测过程中,考察其检测范围、检出限以及离子选择性等,探讨CDs@MIL-101-NH2复合材料发生荧光淬灭的可能机理,以期为荧光法检测重金属离子的MOF材料设计提供参考。
-
实验所用试剂均为分析纯。六水合氯化铁(FeCl3·6H2O)和乙二胺购自国药集团;N,N-二甲基甲酰胺和无水乙醇购自麦克林有限公司;2-氨基对苯二甲酸购自毕得医药有限公司;三聚硫氰酸(C3H3N3S3)购自贤鼎生物有限公司;碘酸钾(KIO3)购自迈瑞尔有限公司;实验用水为去离子水,电阻率为18.2 MΩ·cm−1。
-
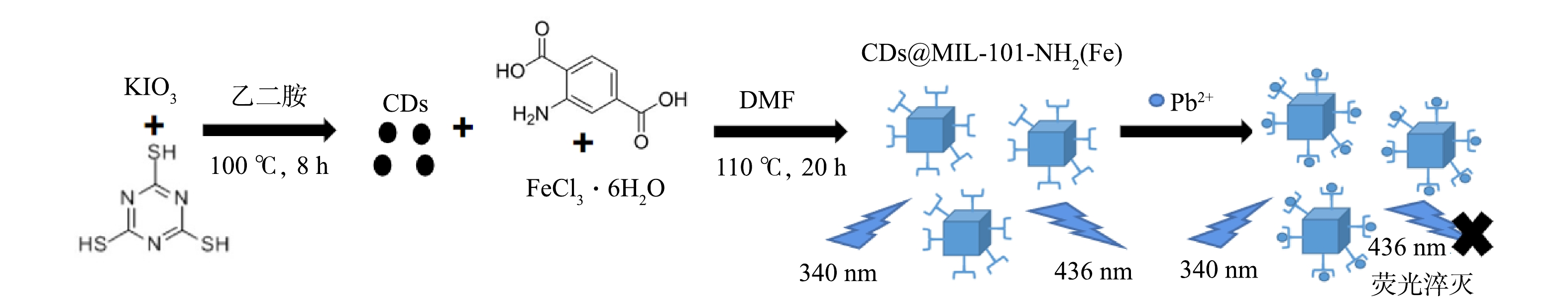
在碳点(N,S,I-CDs)制备过程中,室温下,将250 mg碘酸钾和25 mg三聚硫氰酸混合于25 mL去离子水中,加入1.5 mL乙二胺,超声振荡至完全溶解。将混合液置于50 mL聚四氟乙烯反应釜中,设定温度为180 °C,反应8 h,反应结束后,取出,自然冷却至室温。反应后的混合液经0.22 μm亲水PTFE滤膜过滤,取澄清溶液于4 °C保存待用。
采用水热法,在室温下,将0.67 g FeCl3·6H2O(5 mmol)和0.45 g NH2-H2BDC(2.5 mmol)分散于30 mL于DMF中,超声10 min,待完全溶解后,再加入体积为200 μL的CDs溶液。将混合液转移至50 mL的聚四氟乙烯反应釜,置于110 °C的烘箱中,反应20 h。反应结束后,自然冷至室温,离心出产物,用乙醇反复离心洗涤3次以上去除多余的杂质,于80 °C真空条件下烘干,得到CDs@MIL-101-NH2(Fe)复合材料。
-
针对实验室制备的CDs@MIL-101-NH2(Fe)材料,采用材料型场发射透射电镜(Talos F200X G2,USA)表征样品的形貌;采用MAXima 7000型X射线衍射分析仪(Shimadzu,Japan)表征材料的晶体结构;采用Nicolet 670光谱仪(Thermo Fisher,USA)记录傅里叶变换红外光谱并分析有机配体官能团的存在形态;采用X射线光电子能谱仪(Kratos,Japan)分析材料的元素及价态;采用Autosorb IQ3分析仪(Quantachrome,USA)测定材料的比表面积、介孔孔径分布;通过Brunauer-Emmett-Teller (BET)法和Barrett-Joyner-Halenda (BJH)法分别计算比表面积和孔径。
-
在室温下,采用荧光光谱仪FLS1000 (Edinburgh,UK)进行测量;使用450 W的氙灯和光电倍增管(PMT900)作为测试光源。待测液的容器为石英比色皿(1 cm×1 cm),激发波长和狭缝宽度的选取须同时考虑样品特征与仪器最大接受荧光强度。将1.0 g的CDs@MIL-101-NH2(Fe)粉末溶于1 000 mL的去离子水中,超声10 min,使其完全分散均匀,得到初始质量浓度为1 000 mg·L−1的悬浮液荧光探针。然后将其质量浓度分别稀释至5、10、25、50、100、200、300、500 mg·L−1,测量上述质量浓度材料的荧光强度。制备最佳质量浓度的CDs@MOFs溶液,然后利用1 mol ·L−1的硫酸和氢氧化钠溶液将其pH分别调至5~13,测量上述pH下的CDs@MIL-101-NH2荧光探针的荧光强度。在最佳浓度和最佳pH值下,将响应时间设置为1、20、60、90、120、150、180、240和300 min,检测各个响应时间下溶液的荧光强度。
检测不同Pb2+浓度(0、10、20、40、60、80、100、120、150、180、200、240、280、320、360、400、450、500 μmol·L−1) CDs@MIL-101-NH2(Fe)溶液的荧光强度。CDs@MOFs荧光探针效率的定量计算采用Stern-Volmer计算方法[21] (式(1))。
式中:I0和I分别为CDs@MOFs加入被分析物前后的荧光强度;c为被分析物的浓度;Ksv为Stern-Volmer常数,Ksv值越高,说明荧光探针的效率越高。
在CDs@MIL-101-NH2(Fe)溶液溶液中,加入阴离子Cl−、CO32−、PO43−、SO42−以及阳离子K+、Mg2+、Ba2+、Fe3+、Co2+、Ni2+、Cu2+、Cd2+、Cr3+(离子浓度= 0.5 mmol·L−1),混合均匀并检测CDs@MOFs溶液的荧光强度。
-
利用自来水和湖水来验证CDs@MIL-101-NH2(Fe)荧光探针在水基质中检测铅离子的实用性。湖水水样取自思源湖(上海交通大学),自来水水样取自实验室(上海交通大学)。水样均通过0.45 μm孔径的滤膜过滤,去除悬浮颗粒物,分别加入Pb2+标准溶液,制备出不同浓度的加标水样。将1 mg CDs@MIL-101-NH2分散于100 mL加标水样中,孵育90 min后,测其荧光强度。
-
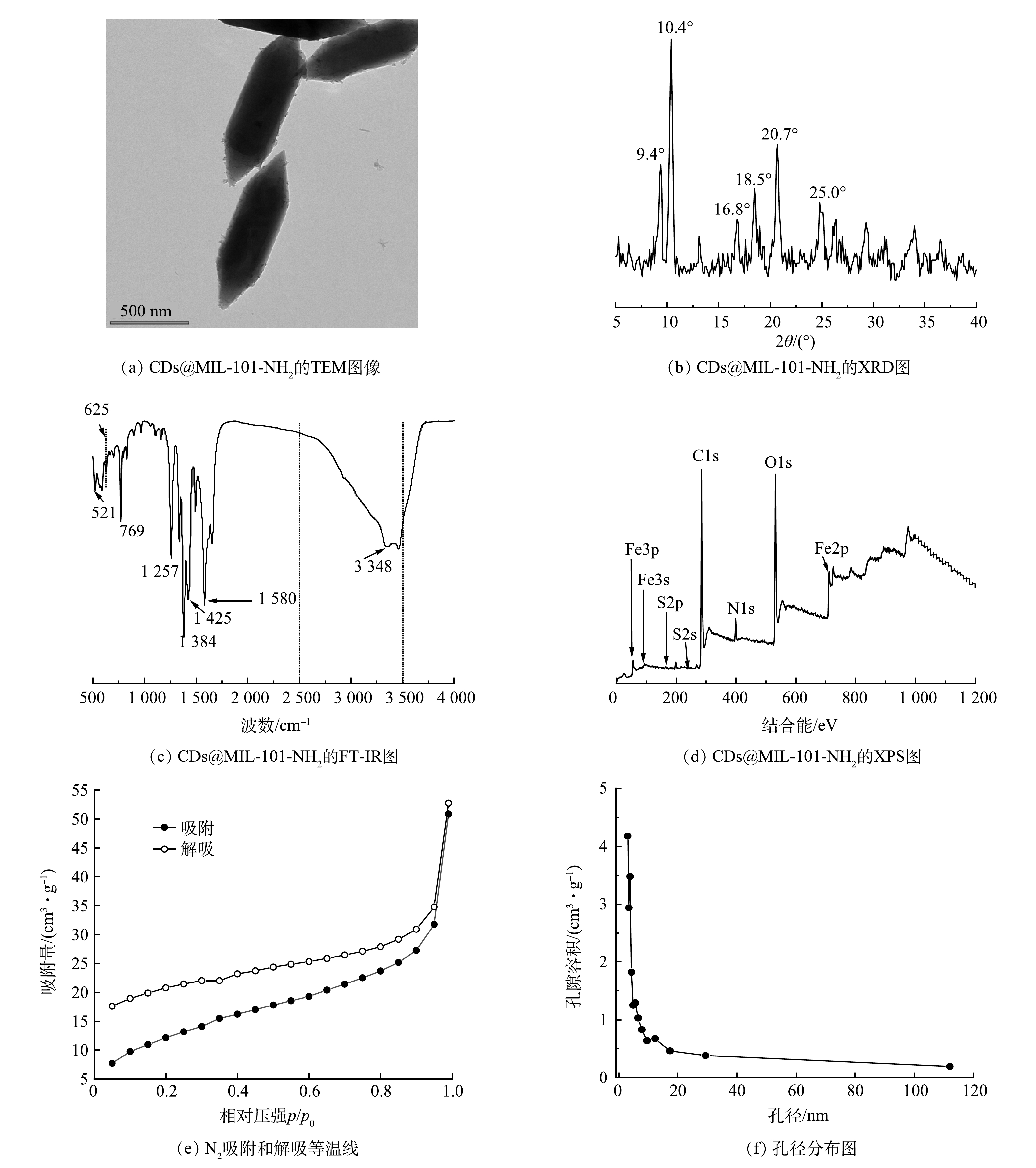
通过场发射透镜研究CDs@MIL-101-NH2(Fe)的微观形貌。如图1(a)所示,材料为纺锤形晶体,与已有研究[22]中的MIL-101-NH2晶体形状一致。显然,MIL-101-NH2在引入碳点后,晶体形貌仍呈纺锤形,说明碳点修饰不改变晶体形貌。XRD对样品的组成和晶体形态表征结果如图1(b)所示。可以看出:CDs@MIL-101-NH2的XRD谱图在9.4°、10.4°、16.8°、18.5°、20.7°和25.0°处有明显的特征峰;10.4°和16.8°处的特征峰与MIL-101-NH2(Fe)的特征峰[22-23]符合,在25.0°处的特征峰与碳点(N,S,I-CDs)的特征峰[24]相符。这说明CDs@MIL-101-NH2复合材料的构建是成功的,且碳点(N,S,I-CDs)的引入未对晶体MIL-101-NH2结构造成很大影响。
为研究CDs@MIL-101-NH2(Fe)的结构,采用傅里叶变换红外光谱仪分析有机配体官能团的存在形态,红外光谱如图1(c)所示。吸附谱带在625 cm−1处分配给Fe—O键[23],1 400~1 600 cm−1处对应芳香环上的C=C伸缩振动吸收峰,1 384 cm−1处的强波段对应C—C键、—COO—的反对称伸缩振动峰和对称伸缩振动峰,说明CDs@MIL-101-NH2中存在二羧酸结构[25]。769 cm−1和3 348 cm−1处的吸收峰分别是N—H键的摇摆带和C—N键的拉伸带[24],说明氨基已成功修饰于框架上。这些吸收振动峰与已有研究[24]中报道的MIL-101-NH2的特征峰相似。复合材料CDs@MIL-101-NH2中还出现了一些新的峰,其中包括在2 500~3 500 cm−1处属于O—H键的伸缩振动峰[26],在1 656 cm−1处对应于C=O键的伸缩振动吸收峰以及1 257 cm−1、521 cm−1对应的C—S键、C—I键的伸缩振动峰[27]。这些新的特征峰进一步证实了碳点(N,S,I-CDs)在复合材料中的存在。本研究针对CDs@MIL-101-NH2进行了XPS分析,结果如图1(d)所示。CDs@MIL-101-NH2探测到的元素有C、N、O、Fe、S,碳点修饰的材料探测到的S元素进一步说明碳点(N,S,I-CDs)修饰过程的成功。I元素由于含量少而未被检测到,表明碳点在复合材料CDs@MIL-101-NH2中的占比较少。
CDs@MIL-101-NH2(Fe)的N2吸附-解吸等温线如图1(e)所示。可以看出,曲线形状符合IV型等温线。CDs@MIL-101-NH2材料的孔径分布如图1(f)所示,其比表面积为45.374 m2·g−1,孔径为3.054 nm,这表明CDs@MIL-101-NH2具有介孔结构。
-
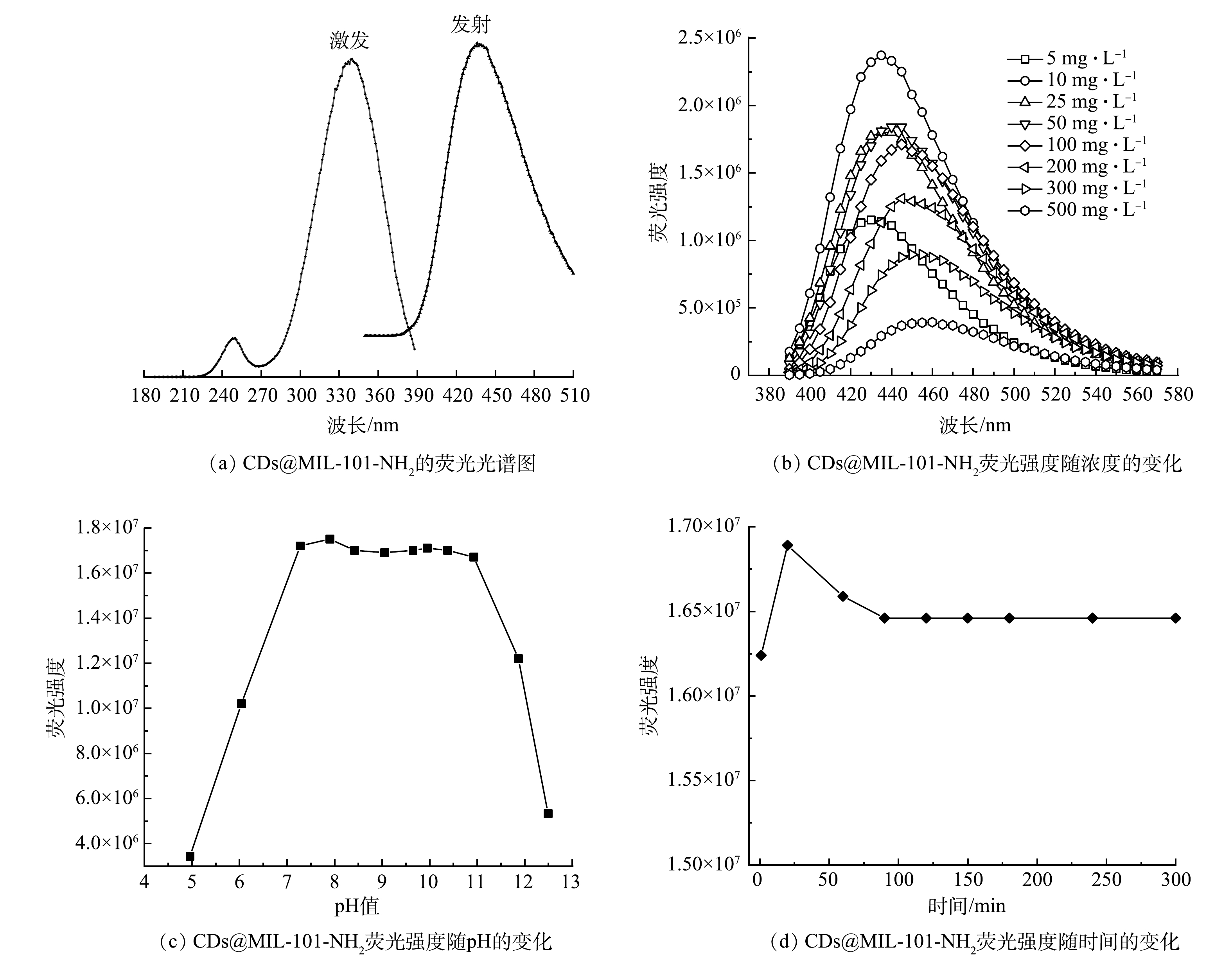
图2(a)为CDs@MIL-101-NH2(Fe)的荧光激发和发射光谱图。在检测过程中,使用荧光光谱仪FLS1000在室温下进行测量,使用 450 W的氙灯和光电倍增管(PMT900)作为测试光源,激发狭缝宽度和发射狭缝宽度均为1.5 nm。确定CDs@MIL-101-NH2材料的最佳激发波长为340 nm,最佳发射波长为436 nm。
发光CDs@MOFs的质量浓度和pH对荧光性质有重要影响[26,28]。如图2(b)所示,随着CDs@MIL-101-NH2(Fe)质量浓度的降低,荧光强度逐渐增大。当质量浓度达到10 mg·L−1时,荧光强度达到最大值。随着材料质量浓度的升高,荧光强度也呈现下降趋势,这可能与CDs@MIL-101-NH2的自淬灭行为有关。为达到最佳的荧光强度,以上实验确定材料的最佳质量浓度为10 mg·L−1。如图2(c)所示,MOFs材料荧光强度会受到pH的影响。pH值在5~7时,复合材料的荧光强度显著增大;pH为7~11时,荧光强度的变化不大;pH>11时,荧光强度锐减。由此可见,材料对酸性环境的变化十分敏感,在碱性环境中则相对稳定。这可能是由于CDs@MIL-101-NH2表面的氨基在酸性环境中容易质子化,从而对荧光信号产生了不良影响,在碱性环境中则不受影响。为获得最佳荧光强度,材料溶液的pH需要控制为7。
响应时间会影响荧光强度的变化。如图2(d)所示,CDs@MIL-101-NH2(Fe)的响应时间大于90 min时,其荧光强度没有显著变化,趋于稳定状态。因此,90 min为CDs@MIL-101-NH2材料的最佳响应时间。
-
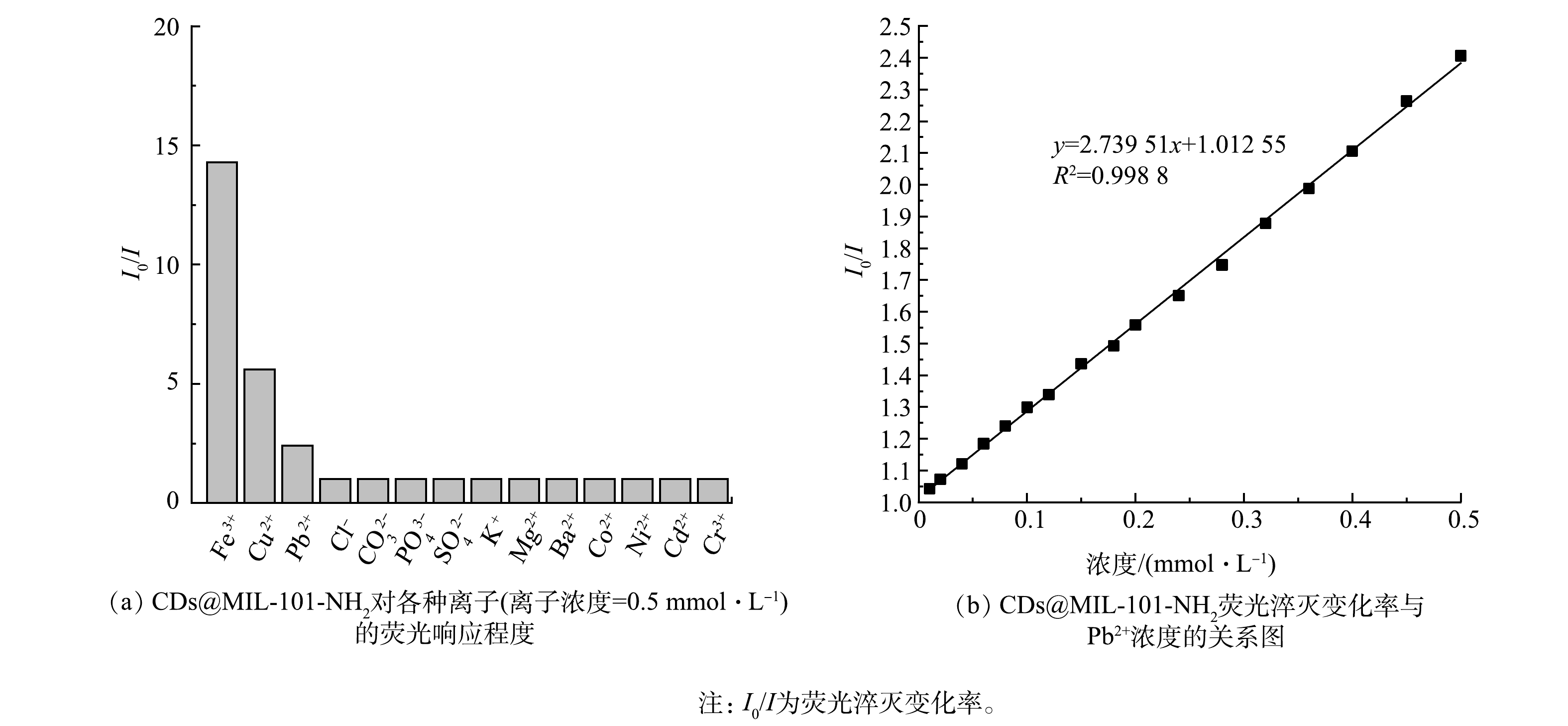
为探讨CDs@MIL-101-NH2(Fe)作为荧光探针对金属离子的荧光响应的应用前景,研究了不同阴阳离子对CDs@MIL-101-NH2荧光强度的影响。由图3(a)可以看出,阴离子Cl−、CO32−、PO43−、SO42−加入前后对复合材料荧光强度几乎没有影响(I0/I=1),而不同的金属离子对复合材料的荧光强度变化有不同的影响,如Fe3+、Cu2+和Pb2+与CDs@MIL-101-NH2(Fe)的相互作用可以显著淬灭荧光。上述结果表明,CDs@MIL-101-NH2在水介质中具有较高的选择性和灵敏度,用来检测水体中Pb2+的荧光探针会受到Fe3+和Cu2+的干扰。实验结果表明,过量的Na+和F−对CDs@MIL-101-NH2溶液的荧光强度没有影响,故可采用NaF溶液消除Fe3+和Cu2+的干扰。对照实验表明,含100 μmol·L−1 Pb2+的CDs@MIL-101-NH2溶液在加入过量NaF后,荧光强度没有显著变化,变化率为2%~3%。同时,含100 μmol·L−1 Fe3+、100 μmol·L−1 Cu2+、100 μmol·L−1 Pb2+和过量NaF的CDs@MIL-101-NH2溶液产生的荧光淬灭,是含100 μmol·L−1 Pb2+和过量NaF的CDs@MIL-101-NH2溶液产生的荧光淬灭的98%~102%。实验结果证明,当NaF消除了Fe3+和Cu2+的干扰后,Pb2+的检测不受影响。因此,CDs@MIL-101-NH2对水中的Pb(Ⅱ)有较好的选择性,对实际水体中Pb(Ⅱ) 的检测具有较高的可行性。
本研究进一步探讨了0~500 µmol·L−1的Pb2+浓度对CDs@MIL-101-NH2(Fe)荧光强度的影响,结果如图3(b)所示。采用上述方法制备的复合材料溶液,荧光淬灭效率由式(1)计算得出。CDs@MIL-101-NH2溶液I0/I与Pb2+质量浓度之间可决系数R2为0.998 8,Ksv为2 739.5 mol·L−1。这表明复合材料作为荧光探针检测水中的铅离子有较好的灵敏度。Pb2+的检出限为1.22 µmol·L−1 (3σ水平),检测区间为1.22~500 µmol·L−1。
-
为探究碳点修饰对MOF材料检测Pb2+的性能影响,比较了未经碳点修饰和碳点修饰的2种材料检测重金属Pb2+的效果差异。碳点(N,S,I-CDs)修饰获得的CDs@MIL-101-NH2(Fe)复合材料与未经碳点修饰的材料相比,检测区间由5.72~100 µmol·L−1变为1.22~500 µmol·L−1。可决系数R2从0.974 2提高至0.998 8,Pb2+的检出限从5.72 µmol·L−1降至1.22 µmol·L−1,Ksv从831.2 mol·L−1增至2 739.5 mol·L−1。由此可证明碳点的修饰明显地提高了MIL-101-NH2对Pb2+的荧光淬灭传感效率。与其他报道结果(表1)相比,本研究所制备的复合材料用于荧光法检测铅离子具有更大的检测区间(1.22~500 µmol·L−1)和优异的荧光传感效率(Ksv)。这是因为,与传统的MOFs材料比较,碳点修饰可以弥补MOFs材料自身存在的一些缺陷,增强复合材料的光学性能。
本研究通过CDs@MIL-101-NH2(Fe)的表征分析,探讨了CDs@MIL-101-NH2荧光淬灭的可能机制。如图2(c)所示,随着pH的升高,复合材料的荧光强度先增大后减小,pH为7~11时,荧光强度的变化不大,且氨基为MIL-101-NH2荧光产生的关键[24],可推测氨基在CDs@MIL-101-NH2荧光探针检测铅离子的荧光淬灭现象中起着重要作用。WU等[29]在制备NH2-UiO-66荧光探针用于铜离子的荧光检测研究中,发现铜离子具有顺磁性,d轨道对氨基有较高的亲和力,荧光淬灭的发生可能与Cu2+-NH2配合物的形成有关。已有研究者[24]在基于MIL-101-NH2材料荧光检测金属离子的研究中,提出氨基与金属离子的之间的螯合作用可以诱导主-客体电子转移,从而导致荧光淬灭的发生。由此可以看出,碳点的引入没有改变MIL-101-NH2的晶相,且CDs@MIL-101-NH2复合材料发生荧光淬灭的主要原因为氨基与铅离子的作用(图4)。
已有研究[19,30]表明,荧光碳点的修饰增强了铅离子与激发态π电子的接触。荧光碳点的尺寸通常远小于MOFs材料,本研究所制备的MIL-101-NH2晶体粒径为800 nm~1 µm,制备的荧光碳点的粒径为4~5 nm。样品形貌与结构表征结果表明,荧光碳点的加入并未改变配位网络的结构。因此,推测荧光碳点的存在形式是分布于配位网络之间的极富电子的纳米结构。在铅离子荧光响应过程中,碳点的富电子基团具有远强于氨基的供电子能力,能够有效吸引铅离子的空轨道,使铅离子能够为附近的π*电子供弛豫途径[31],因此,荧光碳点的加入未改变MOFs配位网络本身的结构,但有效提高了铅离子的荧光响应效率。
根据靶受体的不同,CDs@MOFs复合材料的传感途径一般可分为3类:1) CDs为受体; 2) MOFs为受体;3)CDs和MOFs为共同受体[32]。在本研究中,MIL-101-NH2作为受体,Pb2+可以通过与配体官能团氨基的相互作用改变荧光探针的荧光强度。因此,CDs和MOFs的荧光可以相互对照,从而提高了荧光检测的精确度。
-
在实验过程中,配置不同浓度梯度的铅离子浓度标准液(0、10、20、40、60、80、100、120、150、180、200 μmol·L−1),获得了CDs@MIL-101-NH2(Fe)荧光探针结合后混合液的荧光强度。以铅离子的质量浓度为横坐标,荧光淬灭变化率为纵坐标,绘制标准曲线。基于标准曲线,根据实际样品中的荧光淬灭率,计算得出实际样品的铅离子质量浓度。实际样品主要为自来水和思源湖湖水,在进行实验前,对实际样品进行预处理过滤并对添加铅离子的自来水和思源湖湖水进行加标回收实验,结果如表2所示。由表2可以看出,加标回收率分别为98.74%~106.16%和97.24%~103.63%,相对标准偏差RSD<4%(n=3),检测可靠性和准确性较高。这说明基于CDs@MIL-101-NH2复合材料的荧光检测法应用于水体中的铅离子检测具有可行性。
-
1) CDs@MIL-101-NH2(Fe)复合材料在质量浓度为10 mg·L−1,pH为7,反应时间为90 min的条件下,荧光强度最佳。
2)碳点(N,S,I-CDs)修饰提高了MIL-101-NH2(Fe)检测Pb2+的性能,检测区间由5.72~100 µmol·L−1变为1.22~500 µmol·L−1,可决系数R2从0.974 2提至0.998 8,Pb2+的检出限从5.72 µmol·L−1降至1.22 µmol·L−1,Ksv从831.2 mol·L−1增至2 739.5 mol·L−1。
3) Pb2+的荧光淬灭效应可归因于CDs@MIL-101-NH2(Fe)复合材料上的氨基与铅离子的相互作用。荧光碳点(N,S,I-CDs)的加入不改变MIL-101-NH2(Fe)配位网络本身的结构,但有效提高了铅离子的荧光响应效率(Ksv)。





 下载:
下载: