-
城市快速发展产生的各类污染物,如抗生素、微生物、重金属、化妆品和染料等,不可避免地释放到水体环境中[1 − 2]. 这些污染物在水环境中不断累积,通过食物链最终进入人体,危害人体健康. 1817年以来,全球至少发生过7次霍乱流行病,罪魁祸首便是水体中的致病微生物—霍乱弧菌. 经世卫组织统计,欧洲每年约有450万人感染水体传染病[3]. 因此,开发有效去除废水中污染物的方法对环境保护和人类健康都至关重要. 目前对废水污染物的去除方法主要包括吸附、沉淀、离子交换、膜分离、电化学、光催化降解、还原固化以及高级氧化等工艺[4 − 6]. 其中电化学、光催化和高级氧化等工艺因经济、高效、安全而广受学者关注. 然而,这些方法对于抗生素等低浓度、难降解有机物的去除仍有较大挑战,如催化剂利用效率低、污染物降解不彻底等.
单原子催化剂,指载体上的金属以单原子形式分散且作为活性中心的一类催化剂[7]. SACs兼具多相和均相催化的特性,既保持了多相催化剂的稳定性和可回收性,又有均相催化中配体的可调性和活性位点的均匀性. 因为金属之间不会成键、存在不饱和配位的电子结构和具有明确的配位环境等特性,所以SACs表现出100%理论原子效率、高催化活性、高选择性和不对称自旋等特点. 在环境催化领域中,材料的催化效率、稳定性及经济性是应用竞争的关键问题. SACs具有的高原子利用率、高选择性、可调控性等特点可以使其以小投加量达到高催化效果,在污染物的降解中,更有望突破污染物降解不彻底等瓶颈.
SACs可经光催化、电催化、过硫酸盐(PS)和类芬顿反应等方式驱动,通过还原氧气或活化氧化剂,产生活性物质,如羟基自由基(·OH)、硫酸根自由基(·SO4−)等,实现对水环境多种污染物的降解. 虽然SACs在环境污染物降解中表现出优异催化效果,但SACs与污染物降解的构效关系尚缺少系统性研究,SACs对污染物降解机理同样缺少系统性总结. 因此,有必要从结构层面对SACs进行分类,对水体污染物降解应用等研究进行归纳,以阐明SACs对水环境污染物的催化降解机制.
文章系统地综述了SACs分类、合成方法及水环境污染物的降解应用. 介绍了SACs可被驱动方式及机理,包括光催化、电催化、过硫酸盐活化和类芬顿反应. 最后,重点讲明了SACs对不同水环境污染物的降解机理.
-
SACs的起源可以追溯到20世纪60年代,Boudart利用化学测定方法确定了某些低负载量催化剂的金属分散程度几乎一致,这也就表明了原子分散的活性中心的存在[8]. 1999年,Iwasawa 及其同事发现,用浸渍法制备出的MgO在催化丙烷燃烧时,MgO上的Pt原子表现出了与纳米Pt相同的活性,通过扩展X射线吸收精细结构谱图证实了并不存在Pt—Pt键[9]. 2011年,中国科学院大连化学物理研究所张涛院士团队正式提出了“单原子催化剂”的概念,他们合成了负载在FeO上的单个Pt原子催化剂,通过一系列的表征手段证实了Pt是以单个原子的形式孤立负载在载体上[10].
在过去的十几年里,SACs的研究主要集中在设计合成、表征手段、能量转换、储存方式及有机化学领域,包括CO氧化、氨合成、加氢反应和脱氢反应等[11 − 13]. 近年来,SACs开始被作为非均相催化剂被应用于环境催化的各种高级氧化系统中,包括光催化、电催化、光/H2O2(O3或PMS)耦合系统及类芬顿反应对有机污染物的去除中[14 − 15]. 相比之下,SACs在环境领域的应用仍处于起步阶段.
SACs在环境催化中表现出高活性、高选择性和稳定性,主要源于以下几个因素[16]:(1)相互作用:金属单原子会与载体的相邻原子(如C、N和O)形成配位环境,优化二者之间的电子转移途径和整体吸附性能,改变电子结构进而调节催化活性;(2)配位结构:不同配位结构的中心金属单原子在化学反应中会呈现出不同的自由能;(3)共价键:金属单原子与载体之间的强共价键能够固定单个金属原子,即使在高温或大氧化电位环境下也能防止其发生聚集. 因此,通过组合不同载体和金属单原子,能够有针对性地设计和制备高效的SACs,以应对不同类型的环境催化需求.
以不同载体和单原子为主体对SACs进行分类,如图1所示.
-
SACs载体可以分为以下几类:(1)金属载体:包括Cu、Ag、Au等;(2)金属氧化物载体:包括FeOx、CeO2、TiO2、MnO2等;(3)碳基载体:包括石墨烯、活性碳、碳纳米管、碳纳米纤维和C3N4等;(4)有机骨架载体;(5)沸石载体.
-
以金属作为载体的SACs又称单原子合金(SAAs)是一种独特的SACs,孤立的金属原子被锚定在金属主体表层,单原子和金属载体之间相互作用使SAAs产生显著催化性能. 这类SACs研究主要集中在将微量的8、9、10族过渡金属(Pd、Pt、Rh、Ni、Ru)负载在11族金属(Cu、Ag、Au)上[17 − 18]. SAAs独特的几何和电子特性使反应物易于解离,中间产物会在其表面形成弱吸附环境,这两点代表了SAAs具有高效和选择性催化两个非常理想的特征[19].
SAAs合成方法主要包括[20]:(1)浸渍法:通过浸渍、干燥,使金属和金属氧化物盐均匀分布在载体的细孔中;(2)顺序还原法:制备核壳结构双金属粒子常用方法,一种金属在另一种金属之后被还原. 如Zhao等[21]通过在5 mol·L−1 NaBH4中还原CuCl2和SnCl2水相混合物,制备了Cu97Sn3催化剂,由于Sn2+具有比Cu2+更负的标准电极电位,因此首先发生Cu2+还原,然后在Cu表面沉积原子Sn位;(3)电替换法:利用两种金属前驱体之间标准电极电位差异来合成具有特殊成分和结构的表面合金,Duan等[22]用该方将Cu NWAs浸入RuCl3溶液中,通过改变RuCl3的浓度和更换时间,得到了不同含量Ru负载的Ru1Cu SAAs.
与其他SACs相比,SAAs形成的金属—金属键在热力学上更加稳定,表现出更佳的催化活性. SAAs上分散的高活性位点能轻易的激活化学键,改变与目标物质的结合能使其更易吸附到表面,实现选择性催化. 如在低温情况下,SACs可以快速激活C—H键,并选择性的使不饱和烃加氢,对药物污染废水有很好的去除效果.
-
金属化合物载体SACs包括碳化物、氮化物、硫化物和氧化物,其中含有过渡金属氧化物的SACs在调节催化过程中起着重要作用. 在各类型负载的单原子催化剂中,金属氧化物载体的研究最为广泛,包括FeOx、CeO2、TiO2、MnO2等.
金属氧化物载体SACs的合成方法主要包括[23]:(1)共沉淀法:金属氧化物载体SACs最常用的合成方法,共沉淀成核过程中,可溶的单金属与氧化物载体前驱体紧密混合,使单原子分布均匀;(2)浸渍法:该方法可以把活性金属位点都暴露在SACs的表面,应用最多的为CeO2和TiO2载体的SACs;(3)强静电吸附法:氧化物表面与金属阳离子之间存在静电作用,不利于SACs合成,该法可以去除电荷影响,为构建更多种类SACs提供机会.
金属氧化物拥有高比表面积、丰富的金属或非金属空位、表面官能团等特点,可以表现出特定或可变性质,如表面酸性、碱性及氧化还原特征,从而导致其产生特定的催化性能. FeOx和CeO2是使用最多的两类金属氧化物载体,二者表面富含氧空位可以与单原子形成金属—氧—金属键,在催化反应中保持高稳定性,可用于特殊条件下的环境催化反应. TiO2是典型的半导体材料,其带隙约为3.0—3.2 eV,表面丰富的Ti和O空位可以锚定金属原子,多应用于光催化反应的环境催化中. MnO2是一种还原型载体,其最大特点为表面具有丰富的缺陷空位,研究多集中在通过缺陷策略合成SACs,在电催化反应的环境催化中有较好的应用前景.
-
碳基载体利用自身缺陷结构来锚定金属单原子,如微孔结构或掺杂被N、S等原子修饰过的官能团. 碳基载体成本低,制备方便,在碱性和酸性介质中具有优异的耐受性. 该类催化剂一般拥有高孔隙率和丰富的活性位点,在电催化领域应用广泛. 包括石墨烯、活性碳、碳纳米管、碳纳米纤维和C3N4等.
碳基载体SACs合成方法包括[24]:(1)热解法:金属有机框架热解、有机小分子热解、聚合物热解等;(2)液相合成法:通过液相合成的各种相互作用如静电吸引和共价键等将金属单原子锚定在碳基载体上形成SACs;(3)球磨法:球磨过程中会产生强大的剪切力和高达
1000 ℃的局部高温,重建有机分子化学键,从而形成理想的金属原子配位结构.碳基载体SACs通常以稳定的金属—C、O、N、S键来稳定金属单原子,同时材料中存在的金属— π的相互作用使得该类SACs具有高稳定性. 低维sp2杂化的碳具有大比表面积、电导率高等特点,金属单原子与碳基载体之间具有优异的电子传递环境. 因此,该类SACs在电催化反应的环境催化中具有很好的应用前景.
-
金属有机骨架(MOF)是一种新型多孔晶体,由一组有机连接体和金属节点组成,可以作为支撑材料. MOF具有优异功能配体、孔径可调、高孔隙率等特性,在催化领域特别是电催化领域应用较多. MOF中金属原子和非金属原子之间形成的配位键,在水环境中表现出极好的稳定性[25]. 因此,该类SACs在电催化反应的水环境污染物去除领域极具稳定性,可通过合理设计表现出高活性的SACs扩大其可应用性.
SA@MOF大多数是通过热解法制得,热解过程中,MOF材料的内外压力差促进了衍生碳氮结构出现,从而扩大了MOF空腔[26]. 同时,SA@MOF中丰富的孔隙结构有助于暴露更多活性位点,同时还可以促进物质迁移,活性物质能够长时间与活性位点接触,从而提高催化效率[27].
-
沸石是一种天然或合成的多孔性矿物,具有优异的微孔通道和热稳定性,是单原子的优良载体. 沸石包覆金属催化剂相对于其他SACs具有特殊而优异的选形催化性能,大多数活性中心都限制在孔结构内,只有能进入孔内的分子才可以与活性中心发生反应. 这使其在特定的环境催化领域非常有吸引力,目前多应用于有机废气的处理. 表1总结了不同结构的SACs对水环境污染物的降解应用.
-
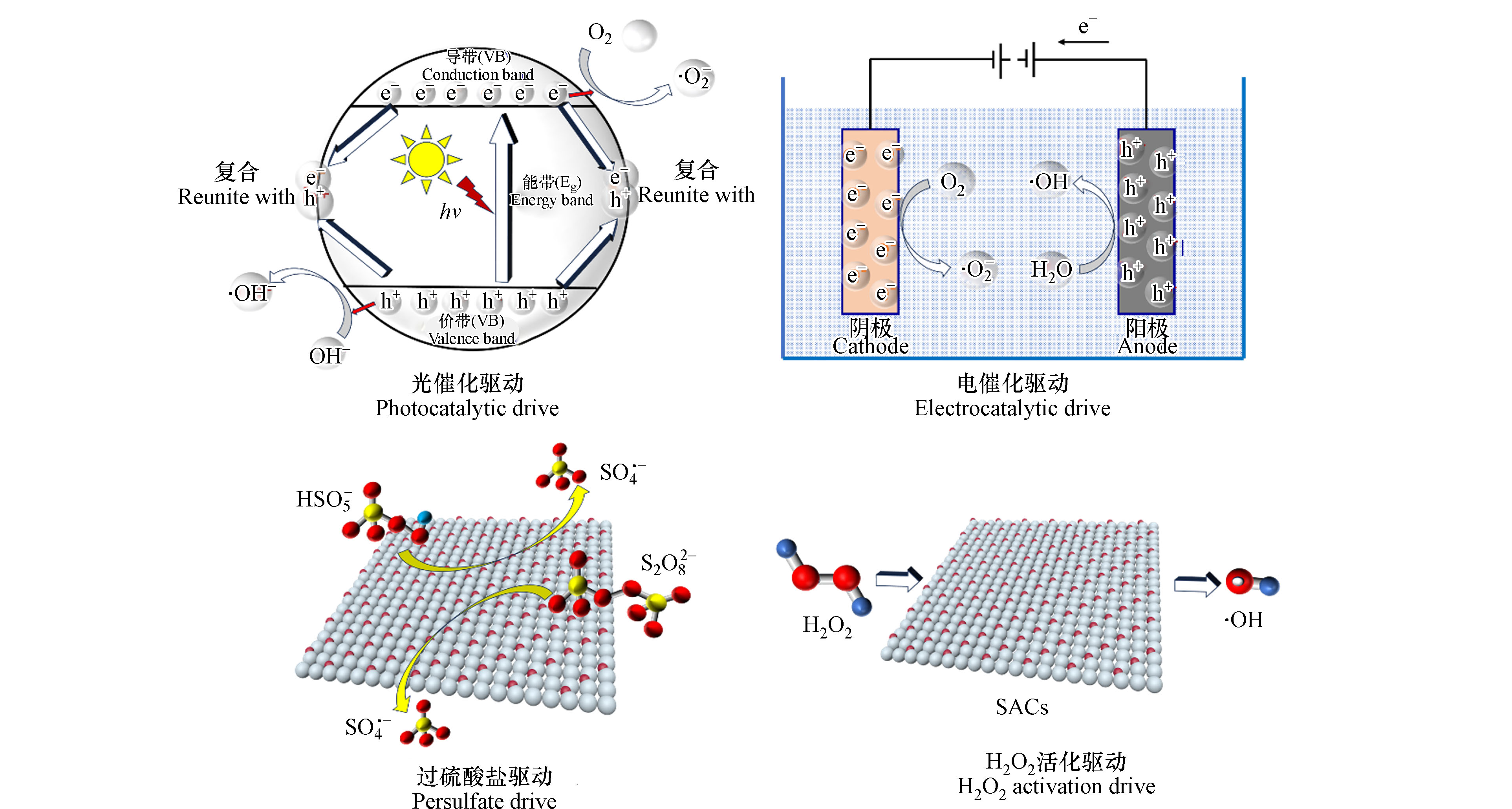
SACs可通过光催化、电催化、过硫酸盐活化及H2O2活化等方式驱动,原子分散的催化位点和最高的原子效率使其在这些催化过程中展现了突出的性能. 然而,不同的激发方式下催化性能却有所差别. 如图2所示,系统地介绍了SACs的驱动方式、驱动机理以及其对水环境污染物的降解机理.
-
光催化是一种将光作为能源的方法,SACs光催化剂从光中吸收光子来驱动和加快催化反应的速度[40]. 典型的光催化反应有三个步骤[41]:(1)催化剂在光照射下被活化产生光生载流子;(2)光生载流子在电场作用下迁移,产生电子(e−)—空穴(h+)对;(3)催化剂表面的光生电子和空穴与周围物质反应,生成多种自由基.
因此,光催化性能会随着光响应范围、光生载流子分离和转移及材料表面非饱和活性位点的改变而增强. 金属本身具有优良的电子性能,光生载流子转移和电子—空穴对分离能力极强. SACs中金属负载使得其电子性能增强,具有优异的光催化效果. 驱动机理如下式(1-3)所示:
-
SACs被用作各种电催化反应的工作电极. 与传统电极相比,SACs电极可以最大限度地分散活性位点,从而提高电催化活性. SACs通常作为阴极,通过还原O2产生自由基降解污染物或直接还原重金属.
电催化体系中,SACs对催化性能提升的原因主要归于以下四点[42]:(1)大量高反应活性的单原子位点可以有效提高电催化激活效率;(2)单原子和载体之间的强相互作用形成可调谐的电子结构,改善电催化过程中电荷传输和分离,并增强活性;(3)不饱和配位环境对SACs上反应物的吸附和活化起到重要作用,如形成的吸附环境有利于降低电化学反应的能垒;(4)小分子在单原子位点的精确吸附排列可以控制催化反应的选择性.
-
过硫酸盐(PS)主要包括过氧单硫酸盐(PMS)和过氧二硫酸盐(PDS),PS介导的高级氧化可以氧化复杂水系中难降解污染物. PMS是一种具有代表性的不对称过硫酸盐结构,PDS具有对称结构,PMS的整体性能优于PDS[43].
PMS不对称结构使其更容易被金属氧化物活化,同时可通过氧化还原循环再生,一般具有较长寿命. PMS活化过程中自由基和非自由基途径共存对复杂污染物的降解具有一定优势. SACs激活PMS产生活性物质,主要为硫酸盐自由基(·SO4−)和羟基自由基(·OH). 驱动机理如式(4—5)(其中M代表金属离子):
PDS具有对称分子结构,相同的单原子催化剂对PMS和PDS具有不同的活化机制. 以Fe、Cu、Co和Ag为单原子中心的SACs被认为是活化PDS的优选催化剂,该类SACs具有活性高、稳定性好、水溶性好等特点,在污染物降解领域具有良好的应用前景[44]. 驱动机理如下式(6—7)(其中M代表金属离子):
-
过氧化氢(H2O2)活化主要包括传统芬顿反应溶解的Fe2+和Fe3+对及类芬顿反应中过渡金属氧化物等参与的氧化循环,被活化的H2O2可以产生·OH,用于降解各种污染物. 然而,均相体系中H2O2的活性和适用性对pH非常敏感,主要因为过渡金属如Fe离子的存在形态会随pH变化,同时可能会和氢氧根离子生成沉淀,需要持续添加催化剂维持反应进行. 在非均相反应中,催化剂可以在更宽的pH范围内活化H2O2,但是除·OH外会额外产生·O2−和高价Fe(Ⅳ),这些活性物质的氧化性较弱. 因此,如何更稳定的实现H2O2到·OH是其活化的关键.
SACs可以以溶解的金属、表面结合等形式参与H2O2的活化反应. SACs有更多均匀分散的活性中心,既可以避免单一金属位点对·OH的淬灭作用,又可以降低吸附能,加速与H2O2的电子传递过程,兼具均相和非均相的优点. 驱动机理如下式(8—9)(其中M代表金属离子):
-
水环境污染物可分为抗生素、病原微生物、有机污染物和重金属离子等. 抗生素作为一种新兴污染物广泛存在于水环境中,各类水中抗生素浓度从ng·L−1到mg·L−1不等,常见的主要包含β-内酰胺类、磺胺类、四环素类、喹诺酮类抗生素. 随着各类废水的排放,大量的细菌、真菌和寄生虫等致病微生物开始在水环境中富集,在中国,这些致病微生物主要包括大肠杆菌、志贺氏菌、变形杆菌和轮状病毒等. 除此之外,有机物主要包括酚类污染物、染料、药物等,常见的重金属离子包括汞、铅、镉和铬等.
-
SACs对抗生素的降解机制可分为[43,45,46]:(1)自由基机制:SACs经多种催化方式驱动产生活性物质(如·OH、·O2−、·SO4−等),SACs提供反应环境,活性物质与抗生素直接接触发生反应破坏其分子结构从而彻底降解抗生素,如·OH会发生原子萃取和加成反应,·SO4−发生氢捕获反应等;(2)非自由基机制:包括单线态氧(1O2)和M=O(M代表金属)活性物质,如经SACs催化产生的1O2可以通过亲电加成和电子萃取与抗生素中的不饱和键发生反应,从而将其转化为较小的中间体,最终转化为CO2和H2O;(3)电子转移机制:SACs的原子分散结构会加速电荷激发和转移,增强电子密度及吸附能力,为电子在化学反应的转移提供优异的环境,如PMS和抗生素同时参与反应时,会发生介导的电子转移过程,污染物结构被改变而降解.
Yang等报道了一种Fe单原子催化剂(Fe-TNFs),通过光芬顿驱动产生·OH,实现了5 h降解95%的诺氟沙星(20 mg·L−1)[47]. ·OH通过攻击诺氟沙星的苯环和哌嗪环,产生各种中间体,最终转化为H2O和CO2. 铁单原子催化剂(SAFe@CN)是一种高活性且稳定的类芬顿催化剂,可以在25 ℃左右激活H2O2降解磺胺嘧啶(SDZ),SDZ(2 mg·L−1)在60 min内脱除96%[48]. Fe—N的存在为反应体系提供了电子转移环境,加速了H2O2向·OH的转化,同时加速了Fe(Ⅱ)Fe(III)的氧化还原循环,产生的·OH有效降解了SDZ. 铜单原子催化剂(SAS-Cu)活化过硫酸盐可以有效降解四环素(TC),在只有0.1 mmol·L−1过硫酸钠(PS)和0.1 g·L−1催化剂的条件下,LED照射30 min后,20 mg·L−1的TC去除率达到83%[49]. 密度泛函理论表明,SAS-Cu可以优化PS的吸附和活化,产生自由基(·O2−、·SO4−、·OH)降解TC.
Xiao等通过两步煅烧法合成了Co单原子催化剂(Co-SA),通过PMS驱动实现60 min内对50 mmol·L−1布洛芬、磺胺嘧啶等95%以上的降解[50]. Co-SA /PMS体系中自由基和非自由基(1O2)都未起到降解作用,Co=O是主要活性物质,通过界面氧化实现了对污染物的降解[50]. Nb单原子催化剂(SANb@C3N4)通过光催化驱动可以有有效降解阿莫西林(AMX),实现40 min降解69%的AMX(5 mg·L−1),同时将产生的CO2有效还原为CO和CH4[51]. 通过光电子性质和DFT计算表明,SANb@C3N4形成的Nb-C有类似“高速铁路”的电子转移环境,电子密度的增加和吸附能力的增强提高了SANb@C3N4体系生成活性氧和还原CO2的能力.
-
SACs的杀菌机制可分为[52 − 54]:(1)释放金属离子,使酶蛋白失活;(2)通过催化驱动产生活性氧自由基或非自由基含氧分子(包括·OH、H2O2、1O2、·O2−等),通过这些活性物质攻击细胞内的蛋白质、细胞膜、核酸或细胞壁起到杀菌效果;(3)SACs和微生物表面吸附接触,通过阻断细胞膜上的电子传递,影响细胞膜结构从而杀菌. Yang等[55]在氮掺杂的多孔碳上负载Fe制成SAFe@CN,通过活化PMS实现5 min内完全杀灭108(CFU)的大肠杆菌. 引入NaN3(1O2的猝灭剂)后,大肠杆菌的杀菌活性明显受损,1O2是提供抗菌功能的关键活性物质. Wang等[56]制备了一种Ag单原子催化剂(Ag1/ZIF),在太阳光驱动下5 min内快速灭活了99 %的大肠杆菌、99%的金黄色葡萄杆菌和99%以上的MS2病毒,浓度均为106(CFU),通过转录组学揭示了·OH和e−是细胞损伤和消毒的主要原因.
Liu等以革兰氏阴性大肠杆菌(E.coli)和革兰氏阳性枯草芽孢杆菌(B. subtilis)为例,用负载在炭黑纳米材料上的Cu单原子催化剂在808 nm的激光照射下几乎杀死了所有的大肠杆菌和枯草芽孢杆菌[57]. 通过自由基捕获实验验证氧化应激在系统中的贡献,消除所有活性物质后,细胞活力几乎没有变化,产生的活性物质并没有灭活该类细菌. 在扫描电镜下发现,催化剂周围吸附了大量的大肠杆菌,其细胞膜结构发生改变从而被灭活. 脂多糖(LPS)是革兰氏阴性菌细胞壁的特征成分,LPS吸附测试发现,LPS被大量吸附从而导致革兰氏阴性菌细胞壁结构改变而致死.
表2为不同水环境污染物的降解情况.
-
SACs对酚类污染物、染料、药物等有机污染物的去除机理同抗生素类. 酚类化合物作为最常见的有机化合物之一,其可导致内分泌紊乱和癌症. Wang等合成了一种Fe-Nx构型的单原子催化剂(FeSAC),用于降解4,4-磺酰基二酚(BPS),并研究了催化剂耐久性、稳定性和适用性[58]. 加入FeSAC和PDS后,20 μmol·L−1的 BPS在40 min内被完全降解,并且发现FeSAC /PDS系统对自来水和地表水中的BPS去除率可达90%以上.
甲基橙(MO)、罗丹明B(RhB)、亚甲基蓝(MB)等有机染料受到越来越多的关注,这些有机污染物在水体中难以降解,长期富集会对水体系统造成严重危害. Guo等[59]将铁单原子嵌入g-C3N4中合成了一种复合材料,用于光芬顿去除水环境中有机染料,对典型有机染料(包括MB、MO和RhB)有很好的去除效果,高效的·OH转化使其在60 min内完全降解200 mg·L−1的MB、MO、RhB.
-
SACs对于重金属的去除机理概括为[64]:(1)吸附:重金属在水环境中主要以离子的形式存在,会与带电荷基团产生吸附效果,碳基等载体SACs具有多孔结构,自身具有优异的重金属吸附效果;(2)氧化还原:被吸附后的重金属离子与功能基团或活性物质等发生氧化还原、络合反应变成完全的游离态,再以沉淀方法去除.
如Ma等[60]报道了一种Fe单原子催化剂(Fe-CN),通过光催化驱动探究了其对U(Ⅵ)的去除效果,实验表明240 min内50 mg·L−1 U(VI)被降解96%. Fe-CN复合材料会对U(VI)产生静电吸附,U(VI)在SACs的表面与e−、·O2−发生还原反应,大部分U(VI)被还原为U(IV),以UO2(s)、(UO2)O2·H2O的形式被去除. Xu等[61]报道了一种Ag单原子催化剂(Ag@PDA/M-ATP/PCN),在光催化驱动下探究了其对铬Cr的去除效果,实验表明90 min内10 mg·L−1 Cr(VI)被降解98%. 该单原子材料表面具有优异的电子环境,Cr(VI)的还原过程主要以e−参与实现.
Ma等[62]制备了氮碳负载铁的SACs,该材料具有优异的铀吸附—电萃取能力,通过对天然海水中的铀进行萃取性能测试,萃取24 h后,海水中检出的铀从3.5 μg·L−1降到小于0.5 μg·L−1(24 h吸附容量相当于1.2 mg·g−1). 该吸附剂表面的Fe单位点和偕胺肟基团是萃取铀的关键,这种表面功能基团使其具有亲水性和对铀离子的高亲和力,而Fe位点为最终生成铀化合物沉淀提供了可逆的电子转移平台. Wang等[63]报道了一种Fe、N掺杂的层状多孔生物炭SACs(Fe-N@BC),对重金属铬表现出了优异的还原性,通过光驱动在甲酸体系下实现150 min内还原98%的10 mg·L−1-Cr(CrVI→CrⅢ). Fe-N@BC中多孔结构提高了金属负载,其优异的导电性加速催化过程中的电子传递,通过活化甲酸从而实现对高价铬的还原去除.
-
SACs作为多相和均相催化剂之间的桥梁,具有较高的活性、选择性和稳定性,在新一代催化剂中有很大的发展潜力. 本文从环境应用方面梳理了SACs分类、水体污染物去除、不同的催化方式、催化机理及污染物降解机理. SACs有接近100%的原子利用率和特殊的电子结构,经过光催化、电催化、过硫酸盐活化和类芬顿反应驱动均表现出优异催化性能. 不同金属—载体组合的SACs对水环境污染物包括抗生素、病原微生物、有机物和重金属,具有较高的去除效果.
SACs在实际的应用当中仍存在不少机遇和挑战:
1)SACs的设计仍是理想催化体系,实际的工业应用中仍存在许多风险. 因此,必须深入了解结构和活性之间的关系,理解其催化过程中的关键步骤、催化机理和影响因素,为优化催化性能提供理论指导.
2)工业上通常需要高负载比的催化剂,探索新的载体设计和制备新方法,以增加活性物质的负载量,并实现规模化制备,在工业应用中具有重要意义.
3)SACs的稳定性和再生能力在工业应用中同样重要,其稳定性依赖于金属与载体之间的强相互作用或者强化学键,合理设计金属单原子和周围原子之间的配位结构.
4)优化载体和原子的适应关系,通过深入研究不同载体和原子之间的适应关系,寻找出更适合的载体-原子组合,以提高SACs的催化性能和稳定性.
单原子催化剂对水环境中污染物的降解
Degradation of pollutants in water environment using single atom catalysts
-
摘要: 抗生素、微生物、染料和重金属等污染物以各种途径进入水环境中,不可避免地危害人类健康. 单原子催化剂(Single-atom catalysts,SACs)以其优异催化性能在环境催化领域应用广泛,然而迄今尚未见到有关SACs对水环境污染物降解方面的相关报道. 基于此,综述了SACs的详细分类、合成方法及其降解应用,SACs经光、电、过硫酸盐和类芬顿反应的驱动机理,并重点介绍了SACs对抗生素、微生物、有机物和重金属的降解机制. 以期为评估单原子催化剂及其活化技术在水环境中的应用提供理论依据.Abstract: Antibiotics, microorganisms, dyes, and heavy metals, among other pollutants, enter the water environment through various pathways and inevitably pose a threat to human health. Single atom catalysts (Single-atom catalysts, SACs) are widely used in the field of environmental catalysis due to their excellent catalytic performance. However, there have been no reports on the degradation of water pollutants by SACs so far. This article provides a detailed overview of the classification, synthesis methods, and degradation applications of SACs. SACs are driven by light, electricity, persulfate, and Fenton like reactions, with a focus on their application and mechanism in the degradation of antibiotics, microorganisms, organic matter, and heavy metals. By analyzing the structure-activity relationship of SACs and their efficiency and mechanism in pollutant degradation, operational guidelines and theoretical basis are provided for evaluating the potential application of single atom catalysts and their activation technologies in water environments.
-
城市快速发展产生的各类污染物,如抗生素、微生物、重金属、化妆品和染料等,不可避免地释放到水体环境中[1 − 2]. 这些污染物在水环境中不断累积,通过食物链最终进入人体,危害人体健康. 1817年以来,全球至少发生过7次霍乱流行病,罪魁祸首便是水体中的致病微生物—霍乱弧菌. 经世卫组织统计,欧洲每年约有450万人感染水体传染病[3]. 因此,开发有效去除废水中污染物的方法对环境保护和人类健康都至关重要. 目前对废水污染物的去除方法主要包括吸附、沉淀、离子交换、膜分离、电化学、光催化降解、还原固化以及高级氧化等工艺[4 − 6]. 其中电化学、光催化和高级氧化等工艺因经济、高效、安全而广受学者关注. 然而,这些方法对于抗生素等低浓度、难降解有机物的去除仍有较大挑战,如催化剂利用效率低、污染物降解不彻底等.
单原子催化剂,指载体上的金属以单原子形式分散且作为活性中心的一类催化剂[7]. SACs兼具多相和均相催化的特性,既保持了多相催化剂的稳定性和可回收性,又有均相催化中配体的可调性和活性位点的均匀性. 因为金属之间不会成键、存在不饱和配位的电子结构和具有明确的配位环境等特性,所以SACs表现出100%理论原子效率、高催化活性、高选择性和不对称自旋等特点. 在环境催化领域中,材料的催化效率、稳定性及经济性是应用竞争的关键问题. SACs具有的高原子利用率、高选择性、可调控性等特点可以使其以小投加量达到高催化效果,在污染物的降解中,更有望突破污染物降解不彻底等瓶颈.
SACs可经光催化、电催化、过硫酸盐(PS)和类芬顿反应等方式驱动,通过还原氧气或活化氧化剂,产生活性物质,如羟基自由基(·OH)、硫酸根自由基(·SO4−)等,实现对水环境多种污染物的降解. 虽然SACs在环境污染物降解中表现出优异催化效果,但SACs与污染物降解的构效关系尚缺少系统性研究,SACs对污染物降解机理同样缺少系统性总结. 因此,有必要从结构层面对SACs进行分类,对水体污染物降解应用等研究进行归纳,以阐明SACs对水环境污染物的催化降解机制.
文章系统地综述了SACs分类、合成方法及水环境污染物的降解应用. 介绍了SACs可被驱动方式及机理,包括光催化、电催化、过硫酸盐活化和类芬顿反应. 最后,重点讲明了SACs对不同水环境污染物的降解机理.
1. 单原子催化剂常见的分类(Common classifications of single atom catalysts)
1.1 SACs的发展和研究现状
SACs的起源可以追溯到20世纪60年代,Boudart利用化学测定方法确定了某些低负载量催化剂的金属分散程度几乎一致,这也就表明了原子分散的活性中心的存在[8]. 1999年,Iwasawa 及其同事发现,用浸渍法制备出的MgO在催化丙烷燃烧时,MgO上的Pt原子表现出了与纳米Pt相同的活性,通过扩展X射线吸收精细结构谱图证实了并不存在Pt—Pt键[9]. 2011年,中国科学院大连化学物理研究所张涛院士团队正式提出了“单原子催化剂”的概念,他们合成了负载在FeO上的单个Pt原子催化剂,通过一系列的表征手段证实了Pt是以单个原子的形式孤立负载在载体上[10].
在过去的十几年里,SACs的研究主要集中在设计合成、表征手段、能量转换、储存方式及有机化学领域,包括CO氧化、氨合成、加氢反应和脱氢反应等[11 − 13]. 近年来,SACs开始被作为非均相催化剂被应用于环境催化的各种高级氧化系统中,包括光催化、电催化、光/H2O2(O3或PMS)耦合系统及类芬顿反应对有机污染物的去除中[14 − 15]. 相比之下,SACs在环境领域的应用仍处于起步阶段.
SACs在环境催化中表现出高活性、高选择性和稳定性,主要源于以下几个因素[16]:(1)相互作用:金属单原子会与载体的相邻原子(如C、N和O)形成配位环境,优化二者之间的电子转移途径和整体吸附性能,改变电子结构进而调节催化活性;(2)配位结构:不同配位结构的中心金属单原子在化学反应中会呈现出不同的自由能;(3)共价键:金属单原子与载体之间的强共价键能够固定单个金属原子,即使在高温或大氧化电位环境下也能防止其发生聚集. 因此,通过组合不同载体和金属单原子,能够有针对性地设计和制备高效的SACs,以应对不同类型的环境催化需求.
以不同载体和单原子为主体对SACs进行分类,如图1所示.
1.2 载体分类
SACs载体可以分为以下几类:(1)金属载体:包括Cu、Ag、Au等;(2)金属氧化物载体:包括FeOx、CeO2、TiO2、MnO2等;(3)碳基载体:包括石墨烯、活性碳、碳纳米管、碳纳米纤维和C3N4等;(4)有机骨架载体;(5)沸石载体.
1.2.1 金属载体(SA@M)
以金属作为载体的SACs又称单原子合金(SAAs)是一种独特的SACs,孤立的金属原子被锚定在金属主体表层,单原子和金属载体之间相互作用使SAAs产生显著催化性能. 这类SACs研究主要集中在将微量的8、9、10族过渡金属(Pd、Pt、Rh、Ni、Ru)负载在11族金属(Cu、Ag、Au)上[17 − 18]. SAAs独特的几何和电子特性使反应物易于解离,中间产物会在其表面形成弱吸附环境,这两点代表了SAAs具有高效和选择性催化两个非常理想的特征[19].
SAAs合成方法主要包括[20]:(1)浸渍法:通过浸渍、干燥,使金属和金属氧化物盐均匀分布在载体的细孔中;(2)顺序还原法:制备核壳结构双金属粒子常用方法,一种金属在另一种金属之后被还原. 如Zhao等[21]通过在5 mol·L−1 NaBH4中还原CuCl2和SnCl2水相混合物,制备了Cu97Sn3催化剂,由于Sn2+具有比Cu2+更负的标准电极电位,因此首先发生Cu2+还原,然后在Cu表面沉积原子Sn位;(3)电替换法:利用两种金属前驱体之间标准电极电位差异来合成具有特殊成分和结构的表面合金,Duan等[22]用该方将Cu NWAs浸入RuCl3溶液中,通过改变RuCl3的浓度和更换时间,得到了不同含量Ru负载的Ru1Cu SAAs.
与其他SACs相比,SAAs形成的金属—金属键在热力学上更加稳定,表现出更佳的催化活性. SAAs上分散的高活性位点能轻易的激活化学键,改变与目标物质的结合能使其更易吸附到表面,实现选择性催化. 如在低温情况下,SACs可以快速激活C—H键,并选择性的使不饱和烃加氢,对药物污染废水有很好的去除效果.
1.2.2 金属氧化物载体(SA@MX)
金属化合物载体SACs包括碳化物、氮化物、硫化物和氧化物,其中含有过渡金属氧化物的SACs在调节催化过程中起着重要作用. 在各类型负载的单原子催化剂中,金属氧化物载体的研究最为广泛,包括FeOx、CeO2、TiO2、MnO2等.
金属氧化物载体SACs的合成方法主要包括[23]:(1)共沉淀法:金属氧化物载体SACs最常用的合成方法,共沉淀成核过程中,可溶的单金属与氧化物载体前驱体紧密混合,使单原子分布均匀;(2)浸渍法:该方法可以把活性金属位点都暴露在SACs的表面,应用最多的为CeO2和TiO2载体的SACs;(3)强静电吸附法:氧化物表面与金属阳离子之间存在静电作用,不利于SACs合成,该法可以去除电荷影响,为构建更多种类SACs提供机会.
金属氧化物拥有高比表面积、丰富的金属或非金属空位、表面官能团等特点,可以表现出特定或可变性质,如表面酸性、碱性及氧化还原特征,从而导致其产生特定的催化性能. FeOx和CeO2是使用最多的两类金属氧化物载体,二者表面富含氧空位可以与单原子形成金属—氧—金属键,在催化反应中保持高稳定性,可用于特殊条件下的环境催化反应. TiO2是典型的半导体材料,其带隙约为3.0—3.2 eV,表面丰富的Ti和O空位可以锚定金属原子,多应用于光催化反应的环境催化中. MnO2是一种还原型载体,其最大特点为表面具有丰富的缺陷空位,研究多集中在通过缺陷策略合成SACs,在电催化反应的环境催化中有较好的应用前景.
1.2.3 碳基载体(SA@C)
碳基载体利用自身缺陷结构来锚定金属单原子,如微孔结构或掺杂被N、S等原子修饰过的官能团. 碳基载体成本低,制备方便,在碱性和酸性介质中具有优异的耐受性. 该类催化剂一般拥有高孔隙率和丰富的活性位点,在电催化领域应用广泛. 包括石墨烯、活性碳、碳纳米管、碳纳米纤维和C3N4等.
碳基载体SACs合成方法包括[24]:(1)热解法:金属有机框架热解、有机小分子热解、聚合物热解等;(2)液相合成法:通过液相合成的各种相互作用如静电吸引和共价键等将金属单原子锚定在碳基载体上形成SACs;(3)球磨法:球磨过程中会产生强大的剪切力和高达
1000 ℃的局部高温,重建有机分子化学键,从而形成理想的金属原子配位结构.碳基载体SACs通常以稳定的金属—C、O、N、S键来稳定金属单原子,同时材料中存在的金属— π的相互作用使得该类SACs具有高稳定性. 低维sp2杂化的碳具有大比表面积、电导率高等特点,金属单原子与碳基载体之间具有优异的电子传递环境. 因此,该类SACs在电催化反应的环境催化中具有很好的应用前景.
1.2.4 金属有机骨架载体(SA@MOF)
金属有机骨架(MOF)是一种新型多孔晶体,由一组有机连接体和金属节点组成,可以作为支撑材料. MOF具有优异功能配体、孔径可调、高孔隙率等特性,在催化领域特别是电催化领域应用较多. MOF中金属原子和非金属原子之间形成的配位键,在水环境中表现出极好的稳定性[25]. 因此,该类SACs在电催化反应的水环境污染物去除领域极具稳定性,可通过合理设计表现出高活性的SACs扩大其可应用性.
SA@MOF大多数是通过热解法制得,热解过程中,MOF材料的内外压力差促进了衍生碳氮结构出现,从而扩大了MOF空腔[26]. 同时,SA@MOF中丰富的孔隙结构有助于暴露更多活性位点,同时还可以促进物质迁移,活性物质能够长时间与活性位点接触,从而提高催化效率[27].
1.2.5 沸石载体(SA@ZIF)
沸石是一种天然或合成的多孔性矿物,具有优异的微孔通道和热稳定性,是单原子的优良载体. 沸石包覆金属催化剂相对于其他SACs具有特殊而优异的选形催化性能,大多数活性中心都限制在孔结构内,只有能进入孔内的分子才可以与活性中心发生反应. 这使其在特定的环境催化领域非常有吸引力,目前多应用于有机废气的处理. 表1总结了不同结构的SACs对水环境污染物的降解应用.
表 1 SACs催化降解水环境污染物(以不同SACs分类)Table 1. Degradation of water environmental pollutants by SACs catalysts (classified by different SACs)SACs类别SACs category SACs 污染物Contaminants 浓度/(mg·L−1)Concentration 驱动方式Drive mode 时间/minTime 降解效果Degradation effect 机理Mechanism 参考文献Reference SA@M Pt1-FeOX/G 磺胺嘧啶 50 电芬顿 30 90% ·OH [28] SA@MX Fe1/TiO2-OV 苯酚 10 光芬顿 80 91% ·OH [29] Fe/MnO2 溶解氧激活 — — — — — [30] MnO2/SAC 溶解氧激活 — — — — — [31] SA@C FeP/Fe1 四环素 10 光芬顿 30 100% ·OH [32] SA@C Co/SAC 1,4-二恶烷 50 PMS 120 100% ·SO4-、·OH [33] rGO/Fe1/C3N4 四环素 20 光电催化 60 88% ·OH [34] SA@MOF Fe2-N/C 双酚A 20 PMS 6 100% 电子转移 [35] SA@ZIF Co- SACs 卡马西平 5 PMS 5 99% 1O2、 ·SO4- [36] NMSACs PtSA/g-C3N4 对氯酚 10 光催化 240 70% 电子转移 [37] MSACs Fe-PANI ARG 100 芬顿 120 76% 吸附、·OH [38] TiZrO4@Cu 腐殖酸 1000 热催化 10 91% ·O2− [39] 注: —表示未查找到. 2. SACs的驱动方式及对水环境污染物的去除机理(The driving mode of SACs and their removal mechanism for water environmental pollutants)
SACs可通过光催化、电催化、过硫酸盐活化及H2O2活化等方式驱动,原子分散的催化位点和最高的原子效率使其在这些催化过程中展现了突出的性能. 然而,不同的激发方式下催化性能却有所差别. 如图2所示,系统地介绍了SACs的驱动方式、驱动机理以及其对水环境污染物的降解机理.
2.1 SACs的驱动方式
2.1.1 光催化驱动
光催化是一种将光作为能源的方法,SACs光催化剂从光中吸收光子来驱动和加快催化反应的速度[40]. 典型的光催化反应有三个步骤[41]:(1)催化剂在光照射下被活化产生光生载流子;(2)光生载流子在电场作用下迁移,产生电子(e−)—空穴(h+)对;(3)催化剂表面的光生电子和空穴与周围物质反应,生成多种自由基.
因此,光催化性能会随着光响应范围、光生载流子分离和转移及材料表面非饱和活性位点的改变而增强. 金属本身具有优良的电子性能,光生载流子转移和电子—空穴对分离能力极强. SACs中金属负载使得其电子性能增强,具有优异的光催化效果. 驱动机理如下式(1-3)所示:
stringUtils.convertMath(!{formula.content}) (1) stringUtils.convertMath(!{formula.content}) (2) stringUtils.convertMath(!{formula.content}) (3) 2.1.2 电催化驱动
SACs被用作各种电催化反应的工作电极. 与传统电极相比,SACs电极可以最大限度地分散活性位点,从而提高电催化活性. SACs通常作为阴极,通过还原O2产生自由基降解污染物或直接还原重金属.
电催化体系中,SACs对催化性能提升的原因主要归于以下四点[42]:(1)大量高反应活性的单原子位点可以有效提高电催化激活效率;(2)单原子和载体之间的强相互作用形成可调谐的电子结构,改善电催化过程中电荷传输和分离,并增强活性;(3)不饱和配位环境对SACs上反应物的吸附和活化起到重要作用,如形成的吸附环境有利于降低电化学反应的能垒;(4)小分子在单原子位点的精确吸附排列可以控制催化反应的选择性.
2.1.3 过硫酸盐驱动
过硫酸盐(PS)主要包括过氧单硫酸盐(PMS)和过氧二硫酸盐(PDS),PS介导的高级氧化可以氧化复杂水系中难降解污染物. PMS是一种具有代表性的不对称过硫酸盐结构,PDS具有对称结构,PMS的整体性能优于PDS[43].
PMS不对称结构使其更容易被金属氧化物活化,同时可通过氧化还原循环再生,一般具有较长寿命. PMS活化过程中自由基和非自由基途径共存对复杂污染物的降解具有一定优势. SACs激活PMS产生活性物质,主要为硫酸盐自由基(·SO4−)和羟基自由基(·OH). 驱动机理如式(4—5)(其中M代表金属离子):
stringUtils.convertMath(!{formula.content}) (4) stringUtils.convertMath(!{formula.content}) (5) PDS具有对称分子结构,相同的单原子催化剂对PMS和PDS具有不同的活化机制. 以Fe、Cu、Co和Ag为单原子中心的SACs被认为是活化PDS的优选催化剂,该类SACs具有活性高、稳定性好、水溶性好等特点,在污染物降解领域具有良好的应用前景[44]. 驱动机理如下式(6—7)(其中M代表金属离子):
stringUtils.convertMath(!{formula.content}) (6) stringUtils.convertMath(!{formula.content}) (7) 2.1.4 H2O2活化驱动
过氧化氢(H2O2)活化主要包括传统芬顿反应溶解的Fe2+和Fe3+对及类芬顿反应中过渡金属氧化物等参与的氧化循环,被活化的H2O2可以产生·OH,用于降解各种污染物. 然而,均相体系中H2O2的活性和适用性对pH非常敏感,主要因为过渡金属如Fe离子的存在形态会随pH变化,同时可能会和氢氧根离子生成沉淀,需要持续添加催化剂维持反应进行. 在非均相反应中,催化剂可以在更宽的pH范围内活化H2O2,但是除·OH外会额外产生·O2−和高价Fe(Ⅳ),这些活性物质的氧化性较弱. 因此,如何更稳定的实现H2O2到·OH是其活化的关键.
SACs可以以溶解的金属、表面结合等形式参与H2O2的活化反应. SACs有更多均匀分散的活性中心,既可以避免单一金属位点对·OH的淬灭作用,又可以降低吸附能,加速与H2O2的电子传递过程,兼具均相和非均相的优点. 驱动机理如下式(8—9)(其中M代表金属离子):
stringUtils.convertMath(!{formula.content}) (8) stringUtils.convertMath(!{formula.content}) (9) 2.2 SACs降解水环境污染物机理
水环境污染物可分为抗生素、病原微生物、有机污染物和重金属离子等. 抗生素作为一种新兴污染物广泛存在于水环境中,各类水中抗生素浓度从ng·L−1到mg·L−1不等,常见的主要包含β-内酰胺类、磺胺类、四环素类、喹诺酮类抗生素. 随着各类废水的排放,大量的细菌、真菌和寄生虫等致病微生物开始在水环境中富集,在中国,这些致病微生物主要包括大肠杆菌、志贺氏菌、变形杆菌和轮状病毒等. 除此之外,有机物主要包括酚类污染物、染料、药物等,常见的重金属离子包括汞、铅、镉和铬等.
2.2.1 SACs对抗生素的去除机理
SACs对抗生素的降解机制可分为[43,45,46]:(1)自由基机制:SACs经多种催化方式驱动产生活性物质(如·OH、·O2−、·SO4−等),SACs提供反应环境,活性物质与抗生素直接接触发生反应破坏其分子结构从而彻底降解抗生素,如·OH会发生原子萃取和加成反应,·SO4−发生氢捕获反应等;(2)非自由基机制:包括单线态氧(1O2)和M=O(M代表金属)活性物质,如经SACs催化产生的1O2可以通过亲电加成和电子萃取与抗生素中的不饱和键发生反应,从而将其转化为较小的中间体,最终转化为CO2和H2O;(3)电子转移机制:SACs的原子分散结构会加速电荷激发和转移,增强电子密度及吸附能力,为电子在化学反应的转移提供优异的环境,如PMS和抗生素同时参与反应时,会发生介导的电子转移过程,污染物结构被改变而降解.
Yang等报道了一种Fe单原子催化剂(Fe-TNFs),通过光芬顿驱动产生·OH,实现了5 h降解95%的诺氟沙星(20 mg·L−1)[47]. ·OH通过攻击诺氟沙星的苯环和哌嗪环,产生各种中间体,最终转化为H2O和CO2. 铁单原子催化剂(SAFe@CN)是一种高活性且稳定的类芬顿催化剂,可以在25 ℃左右激活H2O2降解磺胺嘧啶(SDZ),SDZ(2 mg·L−1)在60 min内脱除96%[48]. Fe—N的存在为反应体系提供了电子转移环境,加速了H2O2向·OH的转化,同时加速了Fe(Ⅱ)Fe(III)的氧化还原循环,产生的·OH有效降解了SDZ. 铜单原子催化剂(SAS-Cu)活化过硫酸盐可以有效降解四环素(TC),在只有0.1 mmol·L−1过硫酸钠(PS)和0.1 g·L−1催化剂的条件下,LED照射30 min后,20 mg·L−1的TC去除率达到83%[49]. 密度泛函理论表明,SAS-Cu可以优化PS的吸附和活化,产生自由基(·O2−、·SO4−、·OH)降解TC.
Xiao等通过两步煅烧法合成了Co单原子催化剂(Co-SA),通过PMS驱动实现60 min内对50 mmol·L−1布洛芬、磺胺嘧啶等95%以上的降解[50]. Co-SA /PMS体系中自由基和非自由基(1O2)都未起到降解作用,Co=O是主要活性物质,通过界面氧化实现了对污染物的降解[50]. Nb单原子催化剂(SANb@C3N4)通过光催化驱动可以有有效降解阿莫西林(AMX),实现40 min降解69%的AMX(5 mg·L−1),同时将产生的CO2有效还原为CO和CH4[51]. 通过光电子性质和DFT计算表明,SANb@C3N4形成的Nb-C有类似“高速铁路”的电子转移环境,电子密度的增加和吸附能力的增强提高了SANb@C3N4体系生成活性氧和还原CO2的能力.
2.2.2 SACs对微生物的去除机理
SACs的杀菌机制可分为[52 − 54]:(1)释放金属离子,使酶蛋白失活;(2)通过催化驱动产生活性氧自由基或非自由基含氧分子(包括·OH、H2O2、1O2、·O2−等),通过这些活性物质攻击细胞内的蛋白质、细胞膜、核酸或细胞壁起到杀菌效果;(3)SACs和微生物表面吸附接触,通过阻断细胞膜上的电子传递,影响细胞膜结构从而杀菌. Yang等[55]在氮掺杂的多孔碳上负载Fe制成SAFe@CN,通过活化PMS实现5 min内完全杀灭108(CFU)的大肠杆菌. 引入NaN3(1O2的猝灭剂)后,大肠杆菌的杀菌活性明显受损,1O2是提供抗菌功能的关键活性物质. Wang等[56]制备了一种Ag单原子催化剂(Ag1/ZIF),在太阳光驱动下5 min内快速灭活了99 %的大肠杆菌、99%的金黄色葡萄杆菌和99%以上的MS2病毒,浓度均为106(CFU),通过转录组学揭示了·OH和e−是细胞损伤和消毒的主要原因.
Liu等以革兰氏阴性大肠杆菌(E.coli)和革兰氏阳性枯草芽孢杆菌(B. subtilis)为例,用负载在炭黑纳米材料上的Cu单原子催化剂在808 nm的激光照射下几乎杀死了所有的大肠杆菌和枯草芽孢杆菌[57]. 通过自由基捕获实验验证氧化应激在系统中的贡献,消除所有活性物质后,细胞活力几乎没有变化,产生的活性物质并没有灭活该类细菌. 在扫描电镜下发现,催化剂周围吸附了大量的大肠杆菌,其细胞膜结构发生改变从而被灭活. 脂多糖(LPS)是革兰氏阴性菌细胞壁的特征成分,LPS吸附测试发现,LPS被大量吸附从而导致革兰氏阴性菌细胞壁结构改变而致死.
表2为不同水环境污染物的降解情况.
表 2 SACs催化剂降解水环境污染物(以不同污染物分类)Table 2. Degradation of water environmental pollutants by SACs catalysts (classified by different pollutants)污染物类别Types of pollutants 名称Name 浓度/(mg·L−1)Concentration SACs 驱动方式Driving method 时间/minTime 降解效果Degradation effect 机理Mechanism 参考文献Reference 抗生素 诺氟沙星 20 Fe-TNFs 光芬顿 300 95% ·OH [47] 磺胺嘧啶 2 SAFe@CN 芬顿 60 96% ·OH [48] 四环素 20 SAS-Cu PMS 30 83% ·O2−、·SO4− [49] 磺胺嘧啶 50 Co-SA PMS 60 95% Co=O [50] 阿莫西林 5 SANb@C3N4 光催化 40 69% 电子转移 [51] 微生物 大肠杆菌 108(CFU) SAFe@CN PMS 5 100% 1O2 [55] 金黄色葡萄杆菌 106(CFU) Ag1/ZIF 光催化 5 99% ·OH、 e− [56] 大肠杆菌 — Cu-SA 光催化 10 100% 吸附接触 [57] 枯草芽孢杆菌 — Cu-SA 光催化 10 100% 吸附接触 [57] 酚类化合物 4,4-磺酰基二酚 5.6 FeSAC PDS 40 100% 电子转移 [58] 有机染料 甲基橙 200 FeSAC 光芬顿 60 100% ·OH [59] 重金属 铀 50 Fe-CN 光催化 240 96% e−、·O2− [60] 铬 10 Ag-SA 光催化 90 98% e− [61] 铀 0.0035 SA-Fe/N 电催化 1440 85% 吸附、萃取 [62] 铬 10 Fe-N@BC 光催化 150 97% 吸附、还原 [63] 注: —表示未查找到. 2.2.3 SACs对酚类、染料等有机污染物的去除机理
SACs对酚类污染物、染料、药物等有机污染物的去除机理同抗生素类. 酚类化合物作为最常见的有机化合物之一,其可导致内分泌紊乱和癌症. Wang等合成了一种Fe-Nx构型的单原子催化剂(FeSAC),用于降解4,4-磺酰基二酚(BPS),并研究了催化剂耐久性、稳定性和适用性[58]. 加入FeSAC和PDS后,20 μmol·L−1的 BPS在40 min内被完全降解,并且发现FeSAC /PDS系统对自来水和地表水中的BPS去除率可达90%以上.
甲基橙(MO)、罗丹明B(RhB)、亚甲基蓝(MB)等有机染料受到越来越多的关注,这些有机污染物在水体中难以降解,长期富集会对水体系统造成严重危害. Guo等[59]将铁单原子嵌入g-C3N4中合成了一种复合材料,用于光芬顿去除水环境中有机染料,对典型有机染料(包括MB、MO和RhB)有很好的去除效果,高效的·OH转化使其在60 min内完全降解200 mg·L−1的MB、MO、RhB.
2.2.4 SACs对重金属的去除机理
SACs对于重金属的去除机理概括为[64]:(1)吸附:重金属在水环境中主要以离子的形式存在,会与带电荷基团产生吸附效果,碳基等载体SACs具有多孔结构,自身具有优异的重金属吸附效果;(2)氧化还原:被吸附后的重金属离子与功能基团或活性物质等发生氧化还原、络合反应变成完全的游离态,再以沉淀方法去除.
如Ma等[60]报道了一种Fe单原子催化剂(Fe-CN),通过光催化驱动探究了其对U(Ⅵ)的去除效果,实验表明240 min内50 mg·L−1 U(VI)被降解96%. Fe-CN复合材料会对U(VI)产生静电吸附,U(VI)在SACs的表面与e−、·O2−发生还原反应,大部分U(VI)被还原为U(IV),以UO2(s)、(UO2)O2·H2O的形式被去除. Xu等[61]报道了一种Ag单原子催化剂(Ag@PDA/M-ATP/PCN),在光催化驱动下探究了其对铬Cr的去除效果,实验表明90 min内10 mg·L−1 Cr(VI)被降解98%. 该单原子材料表面具有优异的电子环境,Cr(VI)的还原过程主要以e−参与实现.
Ma等[62]制备了氮碳负载铁的SACs,该材料具有优异的铀吸附—电萃取能力,通过对天然海水中的铀进行萃取性能测试,萃取24 h后,海水中检出的铀从3.5 μg·L−1降到小于0.5 μg·L−1(24 h吸附容量相当于1.2 mg·g−1). 该吸附剂表面的Fe单位点和偕胺肟基团是萃取铀的关键,这种表面功能基团使其具有亲水性和对铀离子的高亲和力,而Fe位点为最终生成铀化合物沉淀提供了可逆的电子转移平台. Wang等[63]报道了一种Fe、N掺杂的层状多孔生物炭SACs(Fe-N@BC),对重金属铬表现出了优异的还原性,通过光驱动在甲酸体系下实现150 min内还原98%的10 mg·L−1-Cr(CrVI→CrⅢ). Fe-N@BC中多孔结构提高了金属负载,其优异的导电性加速催化过程中的电子传递,通过活化甲酸从而实现对高价铬的还原去除.
3. 结论与展望(Conclusion and perspectives)
SACs作为多相和均相催化剂之间的桥梁,具有较高的活性、选择性和稳定性,在新一代催化剂中有很大的发展潜力. 本文从环境应用方面梳理了SACs分类、水体污染物去除、不同的催化方式、催化机理及污染物降解机理. SACs有接近100%的原子利用率和特殊的电子结构,经过光催化、电催化、过硫酸盐活化和类芬顿反应驱动均表现出优异催化性能. 不同金属—载体组合的SACs对水环境污染物包括抗生素、病原微生物、有机物和重金属,具有较高的去除效果.
SACs在实际的应用当中仍存在不少机遇和挑战:
1)SACs的设计仍是理想催化体系,实际的工业应用中仍存在许多风险. 因此,必须深入了解结构和活性之间的关系,理解其催化过程中的关键步骤、催化机理和影响因素,为优化催化性能提供理论指导.
2)工业上通常需要高负载比的催化剂,探索新的载体设计和制备新方法,以增加活性物质的负载量,并实现规模化制备,在工业应用中具有重要意义.
3)SACs的稳定性和再生能力在工业应用中同样重要,其稳定性依赖于金属与载体之间的强相互作用或者强化学键,合理设计金属单原子和周围原子之间的配位结构.
4)优化载体和原子的适应关系,通过深入研究不同载体和原子之间的适应关系,寻找出更适合的载体-原子组合,以提高SACs的催化性能和稳定性.
-
表 1 SACs催化降解水环境污染物(以不同SACs分类)
Table 1. Degradation of water environmental pollutants by SACs catalysts (classified by different SACs)
SACs类别SACs category SACs 污染物Contaminants 浓度/(mg·L−1)Concentration 驱动方式Drive mode 时间/minTime 降解效果Degradation effect 机理Mechanism 参考文献Reference SA@M Pt1-FeOX/G 磺胺嘧啶 50 电芬顿 30 90% ·OH [28] SA@MX Fe1/TiO2-OV 苯酚 10 光芬顿 80 91% ·OH [29] Fe/MnO2 溶解氧激活 — — — — — [30] MnO2/SAC 溶解氧激活 — — — — — [31] SA@C FeP/Fe1 四环素 10 光芬顿 30 100% ·OH [32] SA@C Co/SAC 1,4-二恶烷 50 PMS 120 100% ·SO4-、·OH [33] rGO/Fe1/C3N4 四环素 20 光电催化 60 88% ·OH [34] SA@MOF Fe2-N/C 双酚A 20 PMS 6 100% 电子转移 [35] SA@ZIF Co- SACs 卡马西平 5 PMS 5 99% 1O2、 ·SO4- [36] NMSACs PtSA/g-C3N4 对氯酚 10 光催化 240 70% 电子转移 [37] MSACs Fe-PANI ARG 100 芬顿 120 76% 吸附、·OH [38] TiZrO4@Cu 腐殖酸 1000 热催化 10 91% ·O2− [39] 注: —表示未查找到. 表 2 SACs催化剂降解水环境污染物(以不同污染物分类)
Table 2. Degradation of water environmental pollutants by SACs catalysts (classified by different pollutants)
污染物类别Types of pollutants 名称Name 浓度/(mg·L−1)Concentration SACs 驱动方式Driving method 时间/minTime 降解效果Degradation effect 机理Mechanism 参考文献Reference 抗生素 诺氟沙星 20 Fe-TNFs 光芬顿 300 95% ·OH [47] 磺胺嘧啶 2 SAFe@CN 芬顿 60 96% ·OH [48] 四环素 20 SAS-Cu PMS 30 83% ·O2−、·SO4− [49] 磺胺嘧啶 50 Co-SA PMS 60 95% Co=O [50] 阿莫西林 5 SANb@C3N4 光催化 40 69% 电子转移 [51] 微生物 大肠杆菌 108(CFU) SAFe@CN PMS 5 100% 1O2 [55] 金黄色葡萄杆菌 106(CFU) Ag1/ZIF 光催化 5 99% ·OH、 e− [56] 大肠杆菌 — Cu-SA 光催化 10 100% 吸附接触 [57] 枯草芽孢杆菌 — Cu-SA 光催化 10 100% 吸附接触 [57] 酚类化合物 4,4-磺酰基二酚 5.6 FeSAC PDS 40 100% 电子转移 [58] 有机染料 甲基橙 200 FeSAC 光芬顿 60 100% ·OH [59] 重金属 铀 50 Fe-CN 光催化 240 96% e−、·O2− [60] 铬 10 Ag-SA 光催化 90 98% e− [61] 铀 0.0035 SA-Fe/N 电催化 1440 85% 吸附、萃取 [62] 铬 10 Fe-N@BC 光催化 150 97% 吸附、还原 [63] 注: —表示未查找到. -
[1] LI Q, CHEN Z, WANG H, et al. Removal of organic compounds by nanoscale zero-valent iron and its composites[J]. Science of The Total Environment, 2021, 792: 148546. doi: 10.1016/j.scitotenv.2021.148546 [2] LIU X, MA R, ZHUANG L, et al. Recent developments of doped g-C3N4 photocatalysts for the degradation of organic pollutants[J]. Critical Reviews in Environmental Science and Technology, 2021, 51(8): 751-790. doi: 10.1080/10643389.2020.1734433 [3] ZHANG Q, MA R, TIAN Y, et al. Sterilization Efficiency of a Novel Electrochemical Disinfectant against Staphylococcus aureus[J]. Environmental Science & Technology, 2016, 50(6): 3184-3192. [4] LU Y, CAI Y, ZHANG S, et al. Application of biochar-based photocatalysts for adsorption-(photo)degradation/reduction of environmental contaminants: mechanism, challenges and perspective[J]. Biochar, 2022, 4(1): 45. doi: 10.1007/s42773-022-00173-y [5] CAI Y, LING Q, YI Y, et al. Application of covalent organic frameworks in environmental pollution management[J]. Applied Catalysis A: General, 2022, 643: 118733. doi: 10.1016/j.apcata.2022.118733 [6] ZHANG Y, LIU H, GAO F, et al. Application of MOFs and COFs for photocatalysis in CO2 reduction, H2 generation, and environmental treatment[J]. EnergyChem, 2022, 4(4): 100078. doi: 10.1016/j.enchem.2022.100078 [7] RACHNA DEVI H, BISEN O Y, CAO X, et al. Design of hierarchical Oxide‐Carbon Nanostructures for Trifunctional Electrocatalytic Applications[J]. Advanced Materials Interfaces, 2022, 9(14): 2200071. doi: 10.1002/admi.202200071 [8] SPENADEL L, BOUDART M. Dispersion of platinum on supported catalysts[J]. The Journal of Physical Chemistry, 1960, 64(2): 204-207. doi: 10.1021/j100831a004 [9] ASAKURA K, NAGAHIRO H, ICHIKUNI N, et al. Structure and catalytic combustion activity of atomically dispersed Pt species at MgO surface[J]. Applied Catalysis A: General, 1999, 188(1/2): 313-324. [10] QIAO B, WANG A, YANG X, et al. Single-atom catalysis of CO oxidation using Pt1/FeOx[J]. Nature Chemistry, 2011, 3(8): 634-641. doi: 10.1038/nchem.1095 [11] HU H, XI J. Single-atom catalysis for organic reactions[J]. Chinese Chemical Letters, 2023, 34(6): 107959. doi: 10.1016/j.cclet.2022.107959 [12] SHANG Y, XU X, GAO B, et al. Single-atom catalysis in advanced oxidation processes for environmental remediation[J]. Chemical Society Reviews, 2021, 50(8): 5281-5322. doi: 10.1039/D0CS01032D [13] XI J B, JUNG H S, XU Y, et al. Synthesis strategies, catalytic applications, and performance regulation of single-atom catalysts[J]. Advanced Functional Materials, 2021, 31(12): 2008318. doi: 10.1002/adfm.202008318 [14] CUI T, LI L, YE C, et al. Heterogeneous Single Atom Environmental Catalysis: Fundamentals, Applications, and Opportunities[J]. Advanced Functional Materials, 2022, 32(9): 2108381. doi: 10.1002/adfm.202108381 [15] HU H Y, ZHAO Y Y, ZHANG Y, et al. Performance regulation of single-atom catalyst by modulating the microenvironment of metal sites[J]. Topics in Current Chemistry (Cham), 2023, 381(5): 24. doi: 10.1007/s41061-023-00434-9 [16] SU J, ZHUANG L, ZHANG S, et al. Single atom catalyst for electrocatalysis[J]. Chinese Chemical Letters, 2021, 32(10): 2947-2962. doi: 10.1016/j.cclet.2021.03.082 [17] DARBY M T, STAMATAKIS M, MICHAELIDES A, et al. Lonely Atoms with Special Gifts: Breaking Linear Scaling Relationships in Heterogeneous Catalysis with Single-Atom Alloys[J]. The Journal of Physical Chemistry Letters, 2018, 9(18): 5636-5646. doi: 10.1021/acs.jpclett.8b01888 [18] GIANNAKAKIS G, FLYTZANI-STEPHANOPOULOS M, SYKES E C H. Single-Atom Alloys as a Reductionist Approach to the Rational Design of Heterogeneous Catalysts[J]. Accounts of Chemical Research, 2019, 52(1): 237-247. doi: 10.1021/acs.accounts.8b00490 [19] XU Z L, AO Z M, YANG M, et al. Recent progress in single-atom alloys: Synthesis, properties, and applications in environmental catalysis[J]. Journal of Hazardous Materials, 2022, 424(Pt B): 127427. [20] SUN X, SONG Y, JIANG G, et al. Fundamentals and catalytic applications of single-atom alloys[J]. Science China Materials, 2024, 67(1): 1-17. doi: 10.1007/s40843-023-2713-6 [21] REN W, TAN X, QU J, et al. Isolated copper–tin atomic interfaces tuning electrocatalytic CO2 conversion[J]. Nature Communications, 2021, 12(1): 1449. doi: 10.1038/s41467-021-21750-y [22] JI K Y, XU M, XU S M, et al. Electrocatalytic hydrogenation of 5-hydroxymethylfurfural promoted by a Ru1Cu single-atom alloy catalyst[J]. Angewandte Chemie International Edition, 2022, 61(37): e202209849. [LinkOut] [23] LANG R, DU X, HUANG Y, et al. Single-Atom Catalysts Based on the Metal–Oxide Interaction[J]. Chemical Reviews, 2020, 120(21): 11986-12043. doi: 10.1021/acs.chemrev.0c00797 [24] SHANG Y, DUAN X, WANG S, et al. Carbon-based single atom catalyst: Synthesis, characterization, DFT calculations[J]. Chinese Chemical Letters, 2022, 33(2): 663-673. doi: 10.1016/j.cclet.2021.07.050 [25] LI X, WANG B. Atomic regulations of single atom from metal-organic framework derived carbon for advanced water treatment[J]. Nano Research, 2023, 16(7): 10326-10341. doi: 10.1007/s12274-023-5616-z [26] ZHOU H, YANG T, KOU Z, et al. Negative Pressure Pyrolysis Induced Highly Accessible Single Sites Dispersed on 3D Graphene Frameworks for Enhanced Oxygen Reduction[J]. Angewandte Chemie International Edition, 2020, 59(46): 20465-20469. doi: 10.1002/anie.202009700 [27] LI Y, CHEN J, CAI P, et al. An electrochemically neutralized energy-assisted low-cost acid-alkaline electrolyzer for energy-saving electrolysis hydrogen generation[J]. Journal of Materials Chemistry A, 2018, 6(12): 4948-4954. doi: 10.1039/C7TA10374C [28] SONG X, ZHANG M, XIU X, et al. Accelerated removal of sulfadiazine by heterogeneous electro-Fenton system with Pt-FeOX/graphene single-atom alloy cathodes[J]. Journal of Environmental Management, 2024, 349: 119541. doi: 10.1016/j.jenvman.2023.119541 [29] YANG M, LI H, LIU F, et al. Mechanism insight into oxygen vacancy-dependent effect in Fe1/TiO2 single-atom catalyst for highly enhanced photo-Fenton mineralization of phenol[J]. Applied Catalysis B: Environment and Energy, 2024, 354: 124071. doi: 10.1016/j.apcatb.2024.124071 [30] GU H, LIU X, LIU X, et al. Adjacent single-atom irons boosting molecular oxygen activation on MnO2[J]. Nature Communications, 2021, 12(1): 5422. doi: 10.1038/s41467-021-25726-w [31] LIAO X, GUO M, TANG W, et al. Bimetallic single atom promoted α-MnO2 for enhanced catalytic oxidation of 5-hydroxymethylfurfural[J]. Green Chemistry, 2022, 24(21): 8424-8433. doi: 10.1039/D2GC01769E [32] LI X, HU J, DENG Y, et al. High stable photo-Fenton-like catalyst of FeP/Fe single atom-graphene oxide for long-term antibiotic tetracycline removal[J]. Applied Catalysis B: Environmental, 2023, 324: 122243. doi: 10.1016/j.apcatb.2022.122243 [33] WU X, RIGBY K, HUANG D, et al. Single-Atom Cobalt Incorporated in a 2D Graphene Oxide Membrane for Catalytic Pollutant Degradation[J]. Environmental Science & Technology, 2022, 56(2): 1341-1351. [34] ZHANG X, WANG H, GUO Y, et al. Enhanced tetracycline degradation by a confinement structure rGO/Fe1/C3N4 photocathode during the sequential oxygen reduction process[J]. Separation and Purification Technology, 2024, 330: 125473. doi: 10.1016/j.seppur.2023.125473 [35] YANG X, QIN J, DAI Z, et al. MOF-derived Fe based catalysts for efficiently Advanced Oxidation Processes: From single atoms to diatomic and nanoparticles[J]. Progress in Natural Science: Materials International, 2023, 33(4): 534-543. doi: 10.1016/j.pnsc.2023.10.002 [36] ZHANG W, LI M, LUO J, et al. Modulating the coordination environment of Co single-atom catalysts through sulphur doping to efficiently enhance peroxymonosulfate activation for degradation of carbamazepine[J]. Chemical Engineering Journal, 2023, 474: 145377. doi: 10.1016/j.cej.2023.145377 [37] ZENG Z, YE F, DENG S, et al. Accelerated organic pollutants mineralization in interlayer confined single Pt atom photocatalyst for hydrogen recovery[J]. Chemical Engineering Journal, 2022, 444: 136561. doi: 10.1016/j.cej.2022.136561 [38] SHI B, LI H, FU X, et al. Fe Single-Atom Catalyst for Cost-Effective yet Highly Efficient Heterogeneous Fenton Catalysis[J]. ACS Applied Materials & Interfaces, 2022, 14(48): 53767-53776. [39] CAI J, LI H, FENG K, et al. Low-temperature degradation of humic acid via titanium zirconium oxide@copper single-atom activating oxygen: Mechanism and pathways[J]. Chemical Engineering Journal, 2022, 450: 138239. doi: 10.1016/j.cej.2022.138239 [40] LIU X, GAO Z, HUANG H, et al. Simultaneous catalytic oxidation of nitric oxide and elemental mercury by single-atom Pd/g-C3N4 catalyst: A DFT study[J]. Molecular Catalysis, 2020, 488: 110901. doi: 10.1016/j.mcat.2020.110901 [41] SUN H, TANG R, HUANG J. Considering single-atom catalysts as photocatalysts from synthesis to application[J]. iScience, 2022, 25(5): 104232. doi: 10.1016/j.isci.2022.104232 [42] ZHANG Q, GUAN J. Single‐Atom Catalysts for Electrocatalytic Applications[J]. Advanced Functional Materials, 2020, 30(31): 2000768. doi: 10.1002/adfm.202000768 [43] LI D, ZHANG S, LI S, et al. Mechanism of the application of single-atom catalyst-activated PMS/PDS to the degradation of organic pollutants in water environment: A review[J]. Journal of Cleaner Production, 2023, 397: 136468. doi: 10.1016/j.jclepro.2023.136468 [44] ZHOU Q, WANG S, LIU J, et al. Geological evolution of offshore pollution and its long-term potential impacts on marine ecosystems[J]. Geoscience Frontiers, 2022, 13(5): 101427. doi: 10.1016/j.gsf.2022.101427 [45] LIAN L, YAO B, HOU S, et al. Kinetic Study of Hydroxyl and Sulfate Radical-Mediated Oxidation of Pharmaceuticals in Wastewater Effluents[J]. Environmental Science & Technology, 2017, 51(5): 2954-2962. [46] LI H, SHAN C, PAN B. Fe(III)-Doped g-C3N4 Mediated Peroxymonosulfate Activation for Selective Degradation of Phenolic Compounds via High-Valent Iron-Oxo Species[J]. Environmental Science & Technology, 2018, 52(4): 2197-2205. [47] JI Z, CAI R, YE W, et al. Confined Fe single atomic sites on (100) plane of anatase TiO2 nanofibers boost white LED driven Fenton-like norfloxacin degradation[J]. Journal of Cleaner Production, 2023, 382: 135161. doi: 10.1016/j.jclepro.2022.135161 [48] YANG W, HONG P, YANG D, et al. Enhanced Fenton-like degradation of sulfadiazine by single atom iron materials fixed on nitrogen-doped porous carbon[J]. Journal of Colloid and Interface Science, 2021, 597: 56-65. doi: 10.1016/j.jcis.2021.03.168 [49] LIU J, HE H, SHEN Z, et al. Photoassisted highly efficient activation of persulfate over a single-atom Cu catalyst for tetracycline degradation: Process and mechanism[J]. Journal of Hazardous Materials, 2022, 429: 128398. doi: 10.1016/j.jhazmat.2022.128398 [50] XIAO Z J, ZHOU B Q, FENG X C, et al. Anchored Co–oxo generated by cobalt single atoms outperformed aqueous species from the counterparts in peroxymonosulfate treatment[J]. Applied Catalysis B: Environmental, 2023, 328: 122483. doi: 10.1016/j.apcatb.2023.122483 [51] LUO J, HAN H, WANG X, et al. Single-atom Nb anchored on graphitic carbon nitride for boosting electron transfer towards improved photocatalytic performance[J]. Applied Catalysis B: Environmental, 2023, 328: 122495. doi: 10.1016/j.apcatb.2023.122495 [52] LI Z M, ZHAO Z Q, CHEN S T, et al. Chemically tailored single atoms for targeted and light-controlled bactericidal activity[J]. Advanced Healthcare Materials, 2024, 13(5): e2302480. [PubMed] [53] ZHENG J, FAN C, LI X, et al. Intelligent multifunctional ruthenium monoatomic/ZnAl-LDH photocatalysts for simultaneous detection and rapid degradation of antibiotics[J]. Journal of Environmental Management, 2024, 353: 120156. doi: 10.1016/j.jenvman.2024.120156 [54] OU H H, QIAN Y P, YUAN L T, et al. Spatial position regulation of Cu single atom site realizes efficient nanozyme photocatalytic bactericidal activity[J]. Advanced Materials, 2023, 35(46): e2305077. doi: 10.1002/adma.202305077 [55] YANG L X, YANG H Q, YIN S Y, et al. Fe single-atom catalyst for efficient and rapid Fenton-like degradation of organics and disinfection against bacteria[J]. Small, 2022, 18(9): e2104941. doi: 10.1002/smll.202104941 [56] WANG J, LI Y, HUANG D, et al. Rapid inactivation of droplet-transmitted microorganisms using silver-single-atom photocatalysts impregnated masks under weak solar irradiation[J]. Chemical Engineering Journal, 2024, 483: 149309. doi: 10.1016/j.cej.2024.149309 [57] YANG Y, SUN J, WEN J, et al. Single-atom doping in carbon black nanomaterials for photothermal antibacterial applications[J]. Cell Reports Physical Science, 2021, 2(8): 100535. doi: 10.1016/j.xcrp.2021.100535 [58] WANG Z, BAO J, HE H, et al. Single-Atom iron catalyst activating peroxydisulfate for efficient organic contaminant degradation relying on electron transfer[J]. Chemical Engineering Journal, 2023, 458: 141513. doi: 10.1016/j.cej.2023.141513 [59] AN S, ZHANG G, WANG T, et al. High-Density Ultra-small Clusters and Single-Atom Fe Sites Embedded in Graphitic Carbon Nitride (g-C3 N4 ) for Highly Efficient Catalytic Advanced Oxidation Processes[J]. ACS Nano, 2018, 12(9): 9441-9450. doi: 10.1021/acsnano.8b04693 [60] WEI W, LUO J, LIU S, et al. Enhancing the photocatalytic performance of g-C3N4 by using iron single-atom doping for the reduction of U(VI) in aqueous solutions[J]. Journal of Solid State Chemistry, 2022, 312: 123160. doi: 10.1016/j.jssc.2022.123160 [61] ZHANG Z, ZHANG N, LIU Y, et al. Efficient degradation of organic dyes and reduced Cr(VI) in environmental water purification by in-situ deposition of silver nanoparticles on polydopamine-modified M-ATP/PCN[J]. Catalysis Communications, 2022, 172: 106528. doi: 10.1016/j.catcom.2022.106528 [62] YANG H, LIU X L, HAO M J, et al. Functionalized iron-nitrogen-carbon electrocatalyst provides a reversible electron transfer platform for efficient uranium extraction from seawater[J]. Advanced Materials, 2021, 33(51): e2106621. [PubMed] [63] YAO Y, LIU X, HU H, et al. Synthesis and characterization of iron-nitrogen-doped biochar catalysts for organic pollutant removal and hexavalent chromium reduction[J]. Journal of Colloid and Interface Science, 2022, 610: 334-346. doi: 10.1016/j.jcis.2021.11.187 [64] HOU H, FANG L, LIU L, et al. Efficient iron single-atom materials for environmental pollutants removal from aqueous solutions: A review[J]. Journal of Cleaner Production, 2023, 426: 139150. doi: 10.1016/j.jclepro.2023.139150 -





 下载:
下载: